Дисфункция малых дыхательных путей и состояние легочной функции при легкой бронхиальной астме | Минеева
1. Моисеев С.В. Поражение малых дыхательных путей при бронхиальной астме // Клиническая фармакология и терапия. 2012; Т.21, №5. С.5‒10.
2. Ненашева Н.М. Роль мелких дыхательных путей при бронхиальной астме // Атмосфера. Пульмонология и аллергология. 2010. №4. С.27‒33.
3. Ненашева Н.М. Современное представление о фенотипах бронхиальной астмы // Фарматека. 2013. №4. С.41‒46.
4. Usmani OS., Singh D., Spinola M., Bizzi A., Barnes P.J. The prevalence of small airways disease in adult asthma: a systematic literature review // Respir. Med. 2016. Vol.116. P.19‒27. doi: 10.1016/j.rmed.2016.05.006
5. Фассахов Р.С. Большая роль малых дыхательных путей: новые возможности циклесонида в терапии бронхиальной астмы // Медицинский Совет. 2017. №18. С.56‒60. https://doi.org/10.21518/2079-701X-2017-18-56-60
6. Минеева Е.Е., Антонюк М.В., Юренко А.В., Гвозденко Т. А. Функциональное состояние малых дыхательных путей у пациентов с бронхиальной астмой, ассоциированной с ожирением // Терапевтический архив. 2019. Т.91, №1. С.60–63. https://doi.org/ 10.26442/00403660.2019.01.000031
А. Функциональное состояние малых дыхательных путей у пациентов с бронхиальной астмой, ассоциированной с ожирением // Терапевтический архив. 2019. Т.91, №1. С.60–63. https://doi.org/ 10.26442/00403660.2019.01.000031
7. van der Wiel E., ten Hacken N.H., Postma D.S., van den Berge M. Small-airways dysfunction associates with respiratory symptoms and clinical features of asthma: a systematic review // J. Allergy Clin. Immunol. 2013. Vol.131, №3. Р.646‒657. doi: 10.1016/j.jaci.2012.12.1567
8. Singhania A., Rupani H., Jayasekera N., Lumb S., Hales P., Gozzard N., Davies D.E,. Woelk C.H., Howarth P.H. Altered Epithelial Gene Expression in Peripheral Airways of Severe Asthma // PLoS One 2017. Vol.12, №1. e0168680. doi: 10.1371/journal.pone.0168680
9. Синопальников А.И., Белоцерковская Ю.Г., Романовских А.Г. Возможности оптимизации контроля бронхиальной астмы: малые дыхательные пути и экстрамелкодисперсные формы ингаляционных препаратов // Фарматека. 2018. №8. С.49–57. https://dx. doi.org/10.18565/pharmateca.2018.8.49-57
doi.org/10.18565/pharmateca.2018.8.49-57
10. Global Initiative for Asthma (GINA). Global strategy for asthma management and prevention (Update 2019). URL: http://www.ginasthma.com
11. Савушкина О.И., Черняк А.В. Теоретические и методические аспекты бодиплетизмографии и ее клиническое применение // Бюллетень физиологии и патологии дыхания. 2016. Вып.60. С.117‒124. https://doi.org/10.12737/20131
12. Pellegrino R., Viegi G., Brusasco V., Crapo R.O., Burgos F., Casaburi R., Coates A., van der Grinten C.P.M., Gustafsson P., Hankinson J., Jensen R., Johnson D.C., MacIntyre N., McKay R., Miller M.R., Navajas D., Pedersen O.F., Wanger J. Interpretative strategies for lung function tests // Eur. Respir. J. 2005. Vol.26, №5. Р.948–968. https://doi.org/10.1183/09031936.05.00035205
13. Айсанов З.Р., Калманова Е.Н. Поражение малых дыхательных путей при бронхиальной астме: новые данные, новая парадигма // Практическая пульмонология. 2019. №1. С.1‒8.
14. Lipworth B., Manoharan A. , Anderson W. Unlocking the quiet zone: the small airway asthma phenotype // Lancet Respir. Med. 2014. Vol.2, №6. P.497‒506. doi: 10.1016/S2213-2600(14)70103-1
, Anderson W. Unlocking the quiet zone: the small airway asthma phenotype // Lancet Respir. Med. 2014. Vol.2, №6. P.497‒506. doi: 10.1016/S2213-2600(14)70103-1
15. Wagner E.M., Bleecker E.R., Permutt S., Liu M.C. Direct assessment of small airways reactivity in human subjects // Am. J. Respir. Crit. Care Med. 1998. Vol.157, №2. Р.447‒452. https://doi.org/10.1164/ajrccm.157.2.9611043
16. Rao D.R., Gaffin J.M., Baxi S.N., Sheehan W.J., Hoffman E.B., Phipatanakul W. The utility of forced expiratory flow between 25% and 75% of vital capacity in predicting childhood asthma morbidity and severity // J. Asthma. 2012. Vol.49, №6. Р.586‒592. doi: 10.3109/02770903.2012.690481
17. Jarjour N.N., Erzurum S.C., Bleecker E.R., Calhoun W.J., Castro M., Comhair S.A., Chung K.F., Curran-Everett D., Dweik R.A., Fain S.B., Fitzpatrick A.M., Gaston B.M., Israel E., Hastie A., Hoffman E.A., Holguin F., Levy B.D., Meyers D.A., Moore W.C., Peters S.P., Sorkness R.L., Teague W.G., Wenzel S.E., Busse W.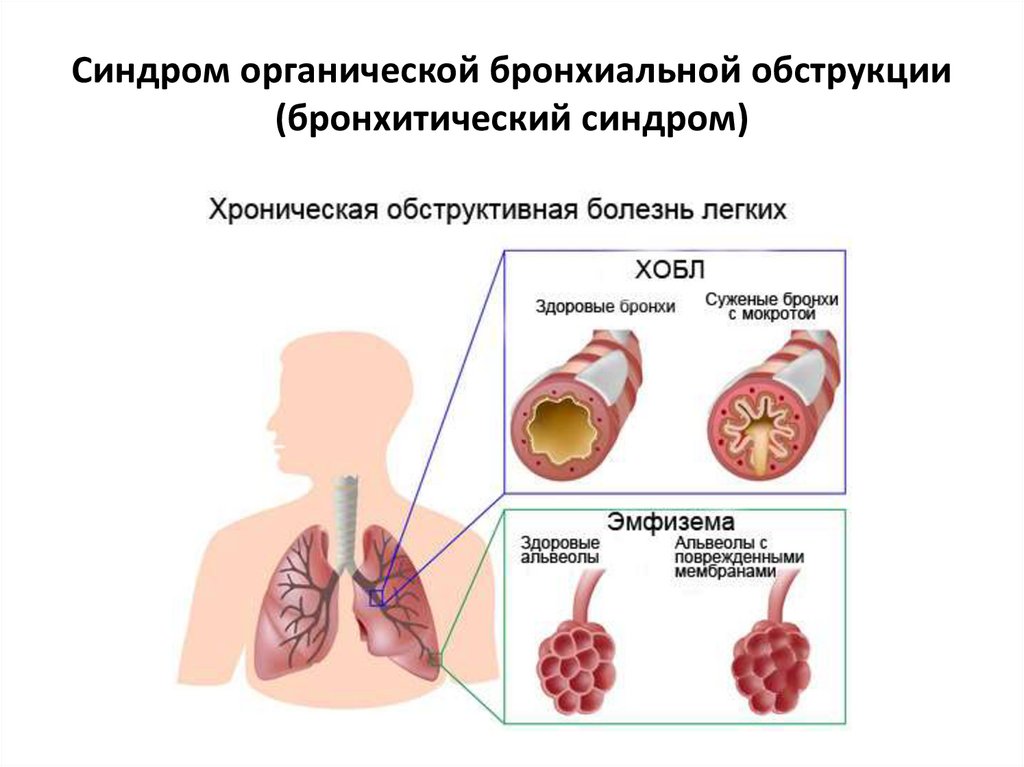 W. Severe asthma: lessons learned from the National Heart, Lung, and Blood Institute Severe Asthma Research Program // Am. J. Respir .Crit. Care Med. 2012. Vol.185, №4. Р.356‒362. https://doi.org/10.1164/rccm.201107-1317PP
W. Severe asthma: lessons learned from the National Heart, Lung, and Blood Institute Severe Asthma Research Program // Am. J. Respir .Crit. Care Med. 2012. Vol.185, №4. Р.356‒362. https://doi.org/10.1164/rccm.201107-1317PP
18. Авдеев С.Н., Айсанов З.Р., Архипов В.В., Белевский А.С., Геппе Н.А., Илькович М.М., Княжеская Н.П., Ненашева Н.М., Овчаренко С.И., Степанян И.Э., Фассахов Р.С., Шмелев Е.И. Согласованные рекомендации по обоснованию выбора терапии бронхиальной астмы и хронической обструктивной болезни легких с учетом фенотипа заболевания и роли малых дыхательных путей // Атмосфера. Пульмонология и аллергология. 2013. №2. С.15‒26.
19. Yuan H., Liu X., Li L., Wang G., Liu C., Zeng Y., Mao R., Du C., Chen Z. Clinical and pulmonary function changes in cough variant asthma with small airway disease // Allergy Asthma Clin. Immunol. 2019. Vol.15: Article number: 41. doi: 10.1186/s13223-019-0354-1
20. Sorkness R.L., Bleecker E.R., Busse W.W., Calhoun W.J., Castro M., Chung K. F., Curran-Everett D., Erzurum S.C., Gaston B.M., Israel E., Jarjour N.N., Moore W.C., Peters S.P., Teague W.G., Wenzel S.E. Lung function in adults with stable but severe asthma: air trapping and incomplete reversal of obstruction with bronchodilation // J. Appl. Physiol. 2008. Vol.104, №2. Р.394‒403. https://doi.org/10.1152/japplphysiol.00329.2007
F., Curran-Everett D., Erzurum S.C., Gaston B.M., Israel E., Jarjour N.N., Moore W.C., Peters S.P., Teague W.G., Wenzel S.E. Lung function in adults with stable but severe asthma: air trapping and incomplete reversal of obstruction with bronchodilation // J. Appl. Physiol. 2008. Vol.104, №2. Р.394‒403. https://doi.org/10.1152/japplphysiol.00329.2007
21. Савушкина О.И., Черняк А.В. Клиническое применение метода бодиплетизмографии // Атмосфера. Пульмонология и аллергология. 2013. №2. С.38‒41.
Современные методы исследования функции легких у детей | #03/03
Оценке функционального состояния легких практические врачи в последнее время уделяют большое внимание. Показатели функции внешнего дыхания (ФВД) важны как для установления диагноза и определения степени тяжести заболевания, так и для выбора лечебных программ. Динамические наблюдения за больными с повторными исследованиями ФВД позволяют вносить изменения в лечение, прогнозировать течение и даже исход заболеваний органов дыхания у детей.
Основной задачей исследования ФВД у большинства пациентов является установление нарушений вентиляционной способности легких, среди которых доминируют обструктивные, то есть вызванные изменениями прохождения воздуха по трахеобронхиальному дереву. Реже диагностируются рестриктивные, или ограничительные, нарушения, происходящие вследствие изменения растяжимости легочной ткани. В отличие от взрослых у детей продолжается рост и развитие бронхолегочных структур. Этим объясняется тот факт, что даже при наличии хронических заболеваний органов дыхания благодаря высоким компенсаторным возможностям нарушения функции легких нередко отсутствуют. Дети, страдающие бронхиальной астмой, часто имеют нормальные функциональные показатели не только в период ремиссии, но даже в стадии обострения заболевания.
Наиболее полная характеристика вентиляционной способности легких возможна при исследовании структуры общей емкости легких. Метод бодиплетизмографии одновременно с исследованием общей емкости легких позволяет оценить бронхиальное сопротивление, чего достаточно для диагностики характера и степени нарушений.
Оценка полученных показателей проводится по отклонению от должной величины, то есть теоретически наиболее вероятной величины показателя, установленной у здоровых детей, которая рассчитывается по регрессионному уравнению. Для оценки границ нормальных значений применяют персентильное распределение, поскольку в группах здоровых детей, как правило, распределение отличается от нормального [1].
Анализ показателей кривой поток—объем (КПО) выдоха форсированной жизненной емкости легких позволяет выявить нарушения бронхиальной проводимости, степень тяжести этих нарушений, а также уровень поражения: нарушения проходимости мелких (или периферических) бронхов, крупных (или центральных) бронхов или генерализованные нарушения.
Проведение тестов с ингаляционными бронходилататорами решает вопрос об обратимости выявленной обструкции дыхательных путей. Эти тесты широко используются как у детей с бронхиальной астмой, так и при хронической неспецифической патологии легких.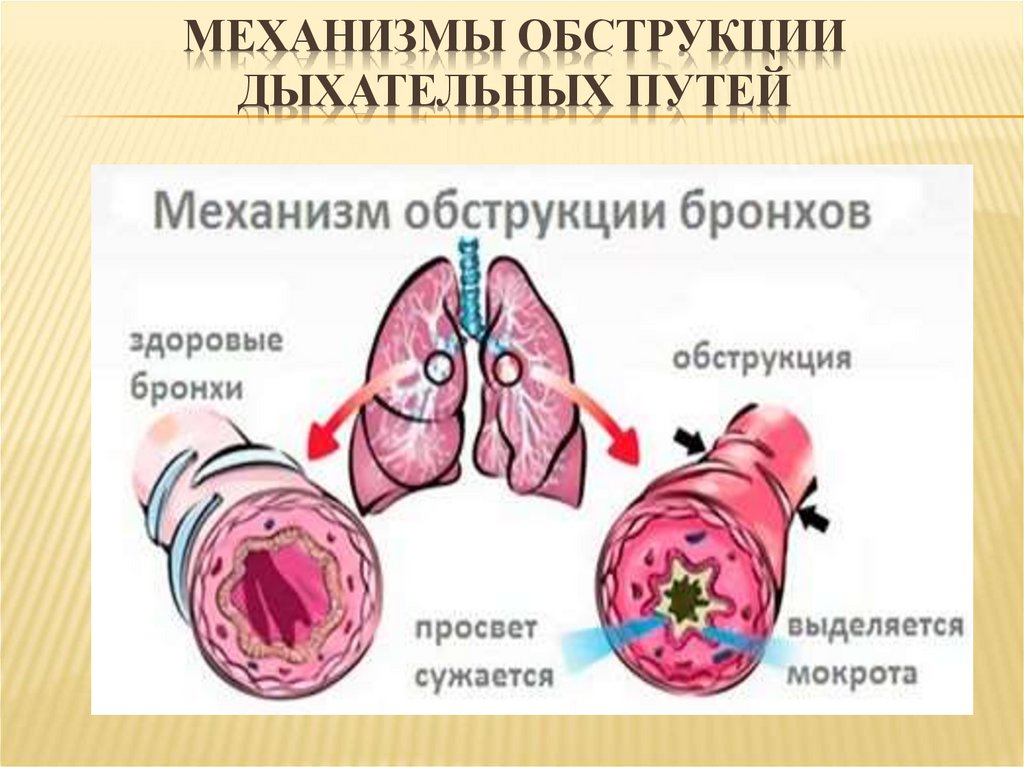 По нашим данным, более половины детей с хронической пневмонией и клиническим синдромом бронхиальной обструкции дают достоверный прирост величины ОФВ1 на ингаляцию бронхолитика. Для правильного выполнения и оценки теста необходимо до начала исследования отменить проводимую терапию: β
По нашим данным, более половины детей с хронической пневмонией и клиническим синдромом бронхиальной обструкции дают достоверный прирост величины ОФВ1 на ингаляцию бронхолитика. Для правильного выполнения и оценки теста необходимо до начала исследования отменить проводимую терапию: β
Воспаление дыхательных путей сопровождается гиперреактивностью бронхов, для диагностики которой применяются провокационные пробы с гистамином и метахолином. Для исследования гиперреактивности бронхов (ГРБ) существует несколько методов, выбор которых зависит от используемой аппаратуры: корректировка постепенно повышающейся дозы метахолина (гистамина) происходит при вдыхании постоянного объема воздуха и различной концентрации аэрозоля либо дозу увеличивают путем повышения вдыхаемого объема при неизменной концентрации.

Не следует назначать бронхопровокационные тесты с целью дифференциальной диагностики: на сегодня нет провокационных агентов, позволяющих четко дифференцировать бронхиальную астму и другие хронические болезни легких, протекающие с бронхообструктивным синдромом. Проведение провокационных проб с метахолином (гистамином) обычно показано у детей с длительной ремиссией бронхиальной астмы, в некоторых случаях (при нормальных показателях ФВД) — для установления степени тяжести болезни, поскольку имеется связь степени гиперреактивности бронхов с тяжестью течения болезни. Смена положительного ответа на ингаляцию провокационного агента на отрицательный после проведенного лечения, или снижение степени гиперреактивности бронхов, несомненно, свидетельствует об эффективности назначенной терапии. При хронических неспецифических воспалительных заболеваниях легких, как показали наши исследования, почти у половины больных определяется гиперреактивность бронхов, однако степень ее обычно бывает низкой, гораздо реже — средней, высокой степени ГРБ мы не наблюдали ни разу.
Тест с дозированной физической нагрузкой широко применяется у детей при заболеваниях бронхолегочной системы. Тестирование проводится на велоэргометре из расчета 1 Вт на 1 кг массы тела при частоте педалирования 60—70 в 1 минуту, можно также использовать беговую дорожку, в этом случае нагрузка устанавливается в зависимости от возраста ребенка [1]. Большинство исследователей оценивают тест как положительный при снижении величины ОФВ1 на 10% после физической нагрузки. Как показали исследования, имеется прямая корреляционная зависимость между частотой возникновения посленагрузочного бронхоспазма и тяжестью течения бронхиальной астмой. Кроме того, посленагрузочный бронхоспазм чаще диагностируется у пациентов, предъявляющих жалобы на одышку при физической активности [4]. Достоверной связи между выявлением посленагрузочного спазма и подтверждением имеющейся гиперреактивности бронхов не существует [5]. В связи с этим выбор комплекса функциональных исследований определяется не только оснащенностью соответствующей аппаратурой, но и кругом проблем, которые приходится решать практическому врачу.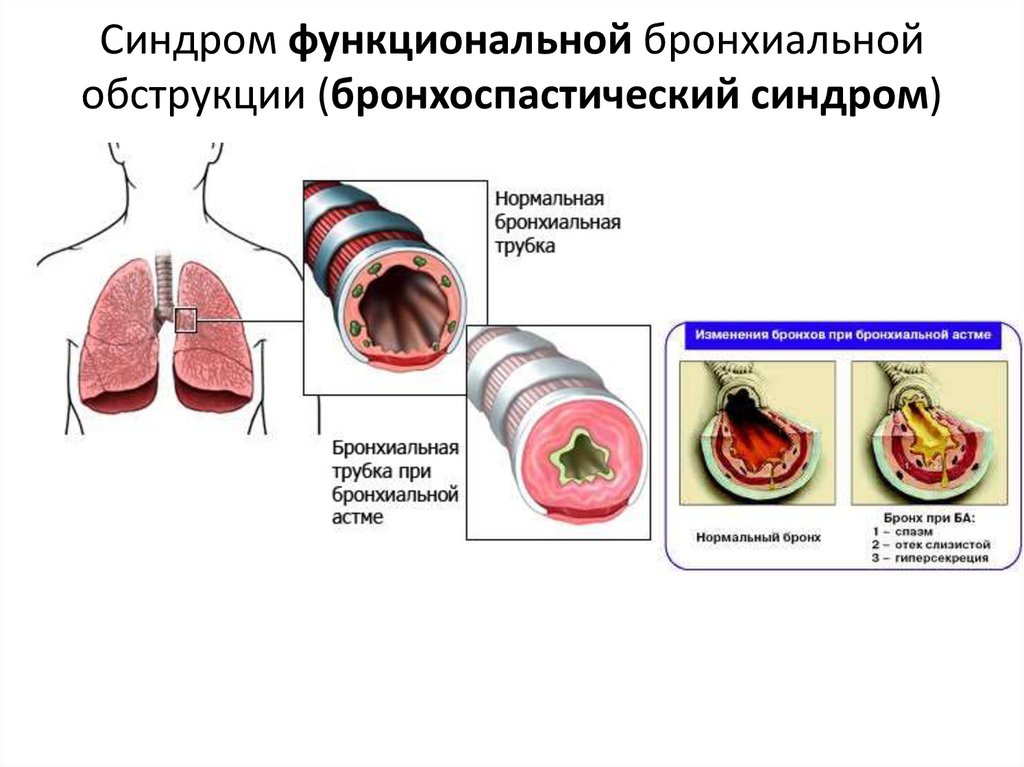
О. Ф. Лукина, доктор медицинских наук, профессор
Научный центр здоровья детей РАМН
Литература
- Савельев Б. П., Ширяева И. С. Функциональные параметры системы дыхания у детей и подростков. М.: Медицина, 2001. 232 с.
- Переверзева Н. Ю. Флоуметрические изменения при бронхиальной астме у детей по данным кривой поток-объем: Автореф. дис. … канд. мед. наук. М., 1990. 20 с.
- Лукина О. Ф., Куличенко Т. В., Гончарова Н. В., Середа Е. В. Проведение и оценка бронхопровокационного теста с метахолином у детей (методические рекомендации). М., 2001. 14 с.
- Гончарова Н. В. Эффективность современных технологий при бронхиальной астме у детей: Автореф. дис. …канд. мед. наук. М., 2001. 25 с.
- Лукина О. Ф., Куличенко Т. В., Гончарова Н. В. Провокационные тесты у детей с бронхиальной астмой (БА)//Пульмонология. 2002. Приложение.
 С. 96.
С. 96.
Обструкция мелких дыхательных путей при ХОБЛ
1. Rabe KF, Hurd S, Anzueto A, et al.; Глобальная инициатива по хронической обструктивной болезни легких. Глобальная стратегия диагностики, лечения и профилактики хронической обструктивной болезни легких: краткое изложение GOLD. Am J Respir Crit Care Med. 2007;176(6):532-555. [PubMed] [Google Scholar]
2. Hogg JC, Chu F, Utokaparch S, et al. Характер обструкции мелких дыхательных путей при хронической обструктивной болезни легких. N Engl J Med. 2004;350(26):2645-2653. [PubMed] [Академия Google]
3. Кумар В., Аббас А., Фаусто Н. Обновление и восстановление тканей: регенерация, заживление и фиброз. В: Роббинс и Котран Патологические основы болезни. 7-е изд. Эльзевир Сондерс; 2005:87-118. [Google Scholar]
4. Рид Л. Измерение слоя слизистых желез бронхов: диагностический критерий при хроническом бронхите. грудная клетка. 1960; 15:132-141. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Mullen JB, Wright JL, Wiggs BR, Pare PD, Hogg JC.
Переоценка воспаления дыхательных путей при хроническом бронхите. Br Med J (Clin Res Ed). 1985;291(6504):1235-1239. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Mullen JB, Wright JL, Wiggs BR, Pare PD, Hogg JC.
Переоценка воспаления дыхательных путей при хроническом бронхите. Br Med J (Clin Res Ed). 1985;291(6504):1235-1239. [Бесплатная статья PMC] [PubMed] [Google Scholar]
6. Saetta M, Di Stefano A, Maestrelli P, et al. Активированные Т-лимфоциты и макрофаги в слизистой оболочке бронхов у лиц с хроническим бронхитом. Ам преподобный Респир Дис. 1993;147(2):301-306. [PubMed] [Google Scholar]
7. Hogg JC, Macklem PT, Thurlbeck WM. Локализация и характер обструкции дыхательных путей при хронической обструктивной болезни легких. N Engl J Med. 1968;278(25):1355-1360. [PubMed] [Google Scholar]
8. Миллер В.С. Легкие. Спрингфилд, Иллинойс: CC Thomas; 1947:222. [Google Scholar]
9. McDonough JE, Yuan R, Suzuki M, et al. Обструкция мелких дыхательных путей и эмфизема при хронической обструктивной болезни легких. N Engl J Med. 2011;365(17):1567-1575. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Reid L.
Вторичная долька в легком взрослого человека с особым акцентом на ее внешний вид на бронхограммах. грудная клетка. 1958;13(2):110-115. [Бесплатная статья PMC] [PubMed] [Google Scholar]
грудная клетка. 1958;13(2):110-115. [Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Weibel ER. Морфометрия легких человека. Нью-Йорк, штат Нью-Йорк: Academic Press Inc; 1963. [Google Scholar]
12. Хорсфилд К., Камминг Г. Морфология бронхиального дерева у человека. J Appl Physiol. 1968;24(3):373-383. [PubMed] [Google Scholar]
13. Macklem PT, Mead J. Сопротивление центральных и периферических дыхательных путей измеряется ретроградным катетером. J Appl Physiol. 1967; 22(3):395-401. [PubMed] [Google Scholar]
14. Янаи М., Секидзава К., Оруи Т., Сасаки Х., Такисима Т. Место обструкции дыхательных путей при заболеваниях легких: прямое измерение внутрибронхиального давления. J Appl Physiol. 1992;72(3):1016-1023. [PubMed] [Google Scholar]
15. Альтшулер Б., Пальмес Э.Д., Ярмус Л., Нельсон Н. Внутрилегочное смешение исследуемых газов с аэрозолями. J Appl Physiol. 1959;14(3):321-327. [PubMed] [Google Scholar]
16. Рорер Ф.
Der Stromungswiderstand in der menschlichen Atemwegen und der Einfluss derundegelmässigen Verzweigung es Бронхиальные системы auf der Atmungsverlauf in vershiedenen Lungenbezinken. Arch Ges Physiol. 1915;162:225-229. [Google Scholar]
Arch Ges Physiol. 1915;162:225-229. [Google Scholar]
17. Рорер Ф. Physiologie der Atembewegung. В: Бете А., фон Бергманн Г., Эмбден Г. и др., Ред. Справочник по нормальной и патологической физиологии. Берлин, Германия: Springer; 1925:70-127. [Google Scholar]
18. Грин М. Насколько велики бронхиолы? Сент-Томас Хосп Газ. 1965; 63:136-139. [Google Scholar]
19. Мид Дж. «Тихая зона» легких. N Engl J Med. 1970;282(23):1318-1319. [PubMed] [Google Scholar]
20. Macklem PT, Permutt S, ред. Легкие в переходный период между здоровьем и болезнью. Нью-Йорк, штат Нью-Йорк: Marcel Dekker Inc.; 1979. [Google Scholar]
21. Флетчер С., Пето Р. Естественная история хронической обструкции дыхательных путей. БМЖ. 1977;1(6077):1645-1648. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Cosio M, Ghezzo H, Hogg JC, et al.
Взаимосвязь между структурными изменениями мелких дыхательных путей и легочно-функциональными тестами. N Engl J Med. 1978;298(23):1277-1281.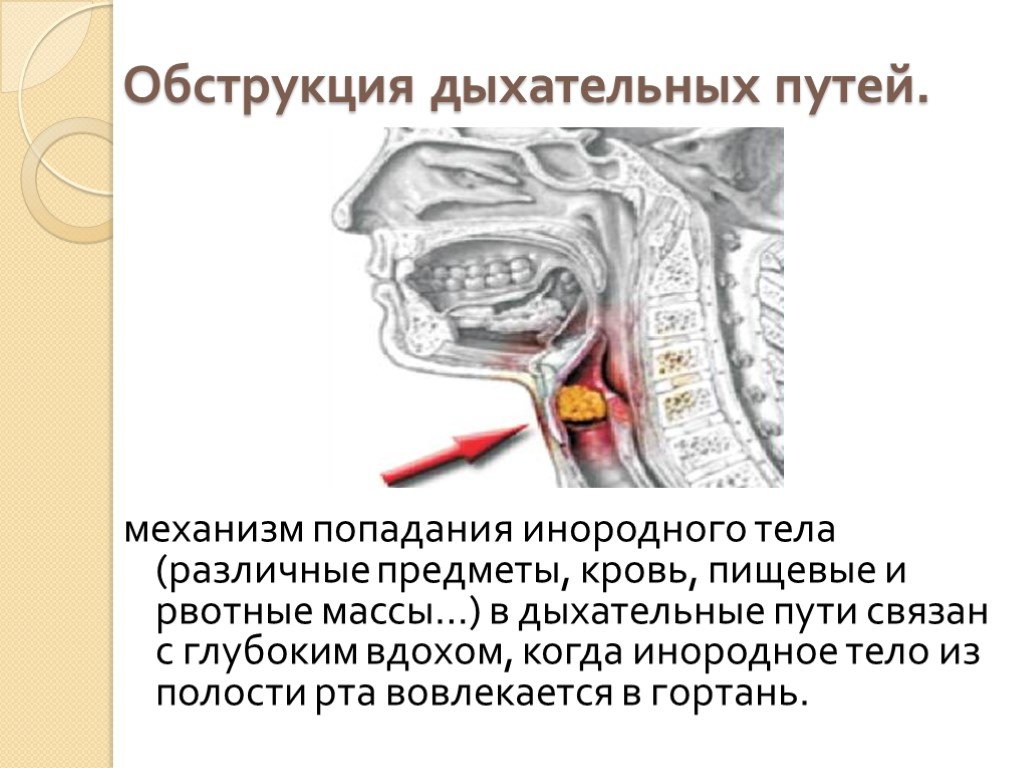 [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
23. Van Brabandt H, Cauberghs M, Verbeken E, Moerman P, Lauweryns JM, Van de Woestijne KP. Разделение легочного импеданса в иссеченных легких человека и собаки. J Appl Physiol. 1983;55(6):1733-1742. [PubMed] [Академия Google]
24. Вагнер Э.М., Лю М.С., Вайнманн Г.Г., Пермутт С., Бликер Э.Р. Периферическое сопротивление легких у нормальных и больных астмой. Ам преподобный Респир Дис. 1990;141(3):584-588. [PubMed] [Google Scholar]
25. Вагнер Э.М., Бликер Э.Р., Пермутт С., Лю М.С. Прямая оценка реактивности малых дыхательных путей у человека. Am J Respir Crit Care Med. 1998;157(2):447-452. [PubMed] [Google Scholar]
26. Bignon J, Khoury F, Even P, Andre J, Brouet G. Морфометрическое исследование при хронической обструктивной бронхолегочной болезни. Патологические, клинические и физиологические корреляции. Ам преподобный Респир Дис. 1969;99(5):669-695. [PubMed] [Google Scholar]
27. Мацуба К., Терлбек В.М.
Количество и размеры мелких дыхательных путей в эмфизематозных легких. Ам Джей Патол. 1972;67(2):265-275. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Ам Джей Патол. 1972;67(2):265-275. [Бесплатная статья PMC] [PubMed] [Google Scholar]
28. Hsia CC, Hyde DM, Ochs M, Weibel ER; Совместная рабочая группа ATS/ERS по количественной оценке структуры легких. Официальное заявление о политике исследований Американского торакального общества/Европейского респираторного общества: стандарты количественной оценки структуры легких. Am J Respir Crit Care Med. 2010;181(4):394-418. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Findeisen W. Uber das Absetzen kleiner, in dur Luft suspendierter Teilchen in der menschlichen Lunge bei der Atmung. Arch Ges Physiol. 1935; 236:367-379. [Google Scholar]
30. Леопольд Дж. Г., Гоф Дж. Центрилобулярная форма гипертрофической эмфиземы и ее связь с хроническим бронхитом. грудная клетка. 1957;12(3):219-235. [Бесплатная статья PMC] [PubMed] [Google Scholar]
31. McLean KH.
Гистология генерализованной эмфиземы легких. I. Генез раннего центролобулярного поражения: очаговая эмфизема. Австралас Энн Мед. 1957;6(2):124-140. [PubMed] [Google Scholar]
Австралас Энн Мед. 1957;6(2):124-140. [PubMed] [Google Scholar]
32. Hogg JC, Nepszy SJ, Macklem PT, Thurlbeck WM. Эластические свойства центролобулярного эмфизематозного пространства. Джей Клин Инвест. 1969;48(7):1306-1312. [Бесплатная статья PMC] [PubMed] [Google Scholar]
33. Otis AB, McKerrow CB, Bartlett RA, et al. Механические факторы в распределении легочной вентиляции. J Appl Physiol. 1956;8(4):427-443. [PubMed] [Google Scholar]
34. Hogg JC, Macklem PT, Thurlbeck WM. Сопротивление коллатеральных каналов в иссеченных легких человека. Джей Клин Инвест. 1969;48(3):421-431. [Бесплатная статья PMC] [PubMed] [Google Scholar]
35. Терри П.Б., Трейстман Р.Дж., Ньюболл Х.Х., Батра Г., Менкес Х.А. Коллатеральная вентиляция у человека. N Engl J Med. 1978;298(1):10-15. [PubMed] [Google Scholar]
36. Кирби М., Мэтью Л., Уитли А., Сантир Г.Э., Маккормак Д.Г., Паррага Г.
Хроническая обструктивная болезнь легких: продольная гиперполяризованная (3) He МРТ. Радиология. 2010;256(1):280-289. [PubMed] [Google Scholar]
Радиология. 2010;256(1):280-289. [PubMed] [Google Scholar]
37. Marshall H, Deppe MH, Parra-Robles J, et al. Прямая визуализация коллатеральной вентиляции при ХОБЛ с помощью МРТ с гиперполяризованным газом. грудная клетка. 2012;67(7):613-617. [PubMed] [Академия Google]
38. Yuan R, Hogg JC, Paré PD, et al. Прогноз скорости снижения ОФВ(1) у курильщиков с помощью количественной компьютерной томографии. грудная клетка. 2009;64(11):944-949. [Бесплатная статья PMC] [PubMed] [Google Scholar]
39. Mohamed Hoesein FA, de Hoop B, Zanen P, et al. КТ-количественная эмфизема у заядлых курильщиков: связь со снижением функции легких. грудная клетка. 2011;66(9):782-787. [PubMed] [Google Scholar]
40. Vestbo J, Edwards LD, Scanlon PD, et al.; Эклипс Исследователи. Изменение объема форсированного выдоха за 1 секунду во времени при ХОБЛ. N Engl J Med. 2011;365(13):1184-1192. [PubMed] [Google Scholar]
41. Нисимура М., Макита Х., Нагаи К. и др.; Исследователи когортного исследования ХОБЛ на Хоккайдо. Ежегодное изменение легочной функции и клинического фенотипа при хронической обструктивной болезни легких. Am J Respir Crit Care Med. 2012;185(1):44-52. [PubMed] [Google Scholar]
Ежегодное изменение легочной функции и клинического фенотипа при хронической обструктивной болезни легких. Am J Respir Crit Care Med. 2012;185(1):44-52. [PubMed] [Google Scholar]
Что вызывает это, как это лечится и многое другое
Написано авторами редакционных статей WebMD
Медицинский обзор Дэна Бреннана, доктора медицинских наук, 25 октября 2021 г.
В этой статье
- Какие существуют типы обструкции дыхательных путей?
- Что может вызвать обструкцию верхних дыхательных путей?
- Что может вызвать обструкцию нижних дыхательных путей?
- Каковы симптомы обструкции дыхательных путей?
- Как лечится обструкция дыхательных путей?
Обструкция дыхательных путей возникает, когда вы не можете протолкнуть воздух в легкие или вывести их из них. Это может быть потому, что вы вдохнули что-то, что блокирует ваши дыхательные пути. Или это может быть вызвано болезнью, аллергической реакцией или травмой. Обструкции дыхательных путей могут блокировать часть ваших дыхательных путей или все это.
Какие существуют типы обструкции дыхательных путей?
Обструкция дыхательных путей может возникнуть в любом месте вдоль дыхательных путей, включая:
Верхние дыхательные пути. Верхние дыхательные пути состоят из следующих частей:
- Нос
- Рот
- Глотка
- Гортань
Нижние дыхательные пути. Нижние дыхательные пути включают:
- Трахею
- Бронхи
- Бронхиолы
- Альвеолы
Что может вызвать обструкцию верхних дыхательных путей?
Посторонние предметы. Вдыхание предметов, блокирующих дыхательные пути, является четвертой по значимости причиной непреднамеренной смерти. Это чаще случается у детей, у которых узкие дыхательные пути, и у людей, у которых есть проблемы с нервами и мышцами. Объекты, которые с наибольшей вероятностью могут вызвать смерть от удушья у детей, включают:
- Хот-доги
- Конфеты
- Орехи
- Виноград
- Воздушные шары
У взрослых предметы, которые с наибольшей вероятностью могут вызвать смерть от удушья, включают: 095
Анафилаксия . Аллергия может привести к тяжелой, опасной для жизни реакции. Это почти всегда неожиданно и может привести к смерти. Анафилаксия вызывает отек дыхательных путей и остановку дыхания, если ее не лечить сразу. Наиболее распространенные причины анафилаксии включают:
Аллергия может привести к тяжелой, опасной для жизни реакции. Это почти всегда неожиданно и может привести к смерти. Анафилаксия вызывает отек дыхательных путей и остановку дыхания, если ее не лечить сразу. Наиболее распространенные причины анафилаксии включают:
- Арахис
- Орехи
- Семена
- Молоко
- Лекарства
- Яд насекомых
Ожоги. Когда температура воздуха становится достаточно высокой, например, при пожаре, это может привести к повреждению верхних дыхательных путей. Эти травмы вызывают отек надгортанника, который представляет собой лоскут хряща у корня языка, и слизистых оболочек вокруг гортани. Этот отек может блокировать ваши дыхательные пути.
Инфекции. Наиболее частой причиной инфекционной обструкции дыхательных путей у детей является круп, вызываемый вирусом. Инфекции, вызванные бактериями, также могут привести к обструкции дыхательных путей, хотя и не так часто. К ним относятся:
К ним относятся:
- Эпиглоттит
- Бактериальный трахеит, инфекция трахеи
- Дифтерия
- Заглоточный абсцесс
- Паратонзиллярный абсцесс
Обструкция нижних дыхательных путей может быть вызвана множеством различных состояний. Некоторые из наиболее распространенных включают в себя:
Астма. Астма — это пожизненное заболевание, которое влияет на дыхательные пути. Симптомы включают отек дыхательных путей, гиперреактивность и выделение большего количества слизи. Они могут вызывать кашель, свистящее дыхание, одышку и стеснение в груди. Астма может быть вызвана многими различными факторами, в том числе: Бронхиолит чаще всего поражает детей раннего возраста и обычно вызывается вирусом. Это заставляет ваши дыхательные пути набухать, блокируя поток воздуха. Симптомы бронхиолита могут включать:
- Затрудненное дыхание
- Кашель
- Насморк
- Лихорадка
- Свистящее дыхание
- У маленьких детей может периодически прекращаться дыхание
13 Хроническая обструктивная болезнь легких Это воспалительное заболевание легких, которое блокирует поток воздуха в легкие. ХОБЛ может вызвать воспаление слизистой оболочки трубок, по которым воздух поступает в легкие. Это называется хроническим бронхитом. Эмфизема также способствует ХОБЛ, разрушая воздушные мешочки в конце мельчайших дыхательных путей. Симптомы ХОБЛ включают:
ХОБЛ может вызвать воспаление слизистой оболочки трубок, по которым воздух поступает в легкие. Это называется хроническим бронхитом. Эмфизема также способствует ХОБЛ, разрушая воздушные мешочки в конце мельчайших дыхательных путей. Симптомы ХОБЛ включают:
- Свистящее дыхание
- Стеснение в груди
- Хронический кашель
- Одышка
- Отек ног, лодыжек или стоп
- Частые инфекции дыхательных путей
Симптомы обструкции дыхательных путей могут варьироваться в зависимости от степени закупорки, в том числе:
- Сильный кашель
- Затрудненное дыхание
- Посинение
- Удушье
- Рвота
- Рвота
- Свистящее дыхание
Как лечится обструкция дыхательных путей?
Лечение обструкции дыхательных путей зависит от причины и степени тяжести.
Вдыхание предмета требует неотложной медицинской помощи и требует немедленного лечения. Если вдыхаемый предмет вызывает удушье, следует позвонить по номеру 911 и оказать первую помощь.

