как правильно принимать, самые распространенные ошибки
Антибиотики – лекарственные препараты, которые официально используются в медицине менее века. Их открытие датируется 1928 годом, когда Александр Флеминг обнаружил пенициллин. С тех пор началась эра антибиотиков, которая коренным образом изменила ход медицины и повлияла на все человечество.
Теги:
Здоровье
Коронавирус
Лекарства
бактерии
Антибиотики, или, как их сейчас принято называть, антимикробные препараты, способны уничтожить бактерии и подавить развитие воспалительного процесса в организме. После того как врачи начали использовать антибиотики, смертность от инфекций серьезно сократилась – многие болезни и травмы перестали быть смертельными.
Сейчас в арсенале врачей десятки разных антибиотиков, которые помогают бороться с инфекциями.
Как работают антибиотики
Начнем с самого главного – антибиотики способны бороться только с бактериальными инфекциями. Это значит, что при вирусных инфекциях, например при гриппе или коронавирусе, они совершенно точно не помогут.
РЕКЛАМА – ПРОДОЛЖЕНИЕ НИЖЕ
Но, погодите, скажешь ты, ведь антибиотики назначают и при вирусных заболеваниях. Да, такое действительно бывает. В некоторых случаях такое назначение связано с некомпетентностью врача, но в большинстве случаев прием антибиотиков при вирусной инфекции нужен для подавления присоединившейся бактериальной инфекции, чтобы не развивались осложнения.
Антибиотики действуют на бактериальные клетки разными способами – одни полностью уничтожают бактерии, а другие оставляют их целыми, но мешают делиться. Независимо от того, как именно работает антибиотик, его вмешательство приводит к тому, что распространение инфекции замедляется или совсем останавливается.
Существуют антибиотики, которые действуют против бактерий одного вида, а есть и те, которые могут уничтожать разные виды бактерий – такие препараты называют антибиотиками широкого спектра действия.
Почему антибиотики перестают работать
Выписывать антибиотик должен врач, а продавать их в аптеке должны по рецепту – к сожалению, это не всегда так, и мы с легкостью покупаем препарат без рецепта, самостоятельно перед этим его себе назначив.
Просто взять и начать принимать таблетки, которые ты или кто-то из членов семьи когда-то принимал, в корне неправильно – антибиотик может оказаться совершенно бесполезен. Так, например, бактерии, вызвавшие инфекцию, могут совсем не реагировать на антимикробный препарат, а для борьбы с ними потребуется лекарство посильнее. Часто для подбора нужного лекарства проводится посев на чувствительность к антибиотикам, при котором и выясняется, убивает ли тот или иной препарат бактерии – возбудители инфекции или же они совершенно на него не реагируют.
Часто для подбора нужного лекарства проводится посев на чувствительность к антибиотикам, при котором и выясняется, убивает ли тот или иной препарат бактерии – возбудители инфекции или же они совершенно на него не реагируют.
Не работать они могут из-за того, что у бактерий сформировалась резистентность к антибиотикам. Это серьезная проблема, которой сейчас озабочены эксперты Всемирной организации здравоохранения. Из-за того, что многие пациенты сами решают, какую дозу им пить, при малейших улучшениях прекращают прием антибиотиков, пьют один и тот же препарат в течение долгих лет, бактерии могут быть устойчивыми к антибиотикам.
У них появляются мутации, которые позволяют бактериям выживать, несмотря на действие антимикробных препаратов. Бесконтрольное использование антибиотиков приводит к появлению супербактерий – микроорганизмов, на которые не действует ни один антибиотик. Такие бактерии уже существуют и вызвали не один летальный исход. Пациентов просто не удалось вылечить, так как ни один антибиотик не помогал.
ВОЗ считает, что антибиотиков в мире разрабатывается недостаточно и опасается, что бактерии меняются быстрее, чем появляются новые антимикробные лекарства. Это значит, что недалек тот день, когда лечить бактериальную инфекцию будет просто нечем.
Как правильно принимать антибиотики: 8 правил
Антибиотики выпускают в разных формах – врач может выписать таблетки или уколы антибиотиков. В домашних условиях пить таблетки гораздо удобнее, чем делать уколы. Инъекции – в основном способ для лечения в больничных условиях, и их редко прописывают для домашнего использования. В уколах выпускают обычно более «сильные» препараты, чем в таблетках – их назначают, когда нужно справиться с особо тяжелой инфекцией.
Чтобы лечение было эффективным, а антибиотики все же использовались для лечения как можно дольше, нужно пить эти препараты по правилам.
- Антибиотики используются для лечения бактериальных инфекций и совершенно бесполезны при гриппе, ковиде и других вирусных болезнях.
 Но в случае развития бактериальных осложнений антимикробные препараты могут быть назначены.
Но в случае развития бактериальных осложнений антимикробные препараты могут быть назначены. - Сам антибиотик, его дозировку, режим и продолжительность приема назначает врач. Нельзя самостоятельно начинать и отменять прием лекарства, менять дозировку в меньшую или большую сторону.
- Прекращать прием антибиотиков до завершения курса нельзя: даже если улучшения наступили на второй день из семи, пить препараты нужно неделю, если так велел врач.
- В том случае, если спустя 72 часа после начала приема состояние не изменилось, надо сообщить об этом врачу – антибиотик не работает и его нужно заменить.
- Принимай лекарство четко по инструкции – там будет написано нужно его пить до еды, после или во время. Запивать таблетки лучше всего негазированной водой, а вот молоко и фруктовые соки для этого категорически не подходят.
- Следи за диетой: пей больше жидкости, ешь меньше жирной пищи, ограничь острое.
- Откажись от алкоголя: на фоне одновременного курса антибиотиков и употребления спиртного антимикробные препараты могут просто не сработать.
 В худшем случае разовьется побочная реакция или аллергия на препарат.
В худшем случае разовьется побочная реакция или аллергия на препарат. - Антибиотики могут уничтожить не только вредные, но и полезные бактерии – те, которые присутствуют в нашем кишечнике и нужны для пищеварения. Часто на фоне приема антибиотиков развивается диарея – снизить шансы на ее возникновение поможет прием пробиотиков. Впрочем, эта рекомендация не является обязательной.
Фото: Shutterstock
Почему нельзя принимать антибиотики бесконтрольно
Свежий номер
РГ-Неделя
Родина
Тематические приложения
Союз
Свежий номер
Общество
11.04.2021 08:00
Поделиться
Бесконтрольный прием антибиотиков приводит к появлению «супербактерий»
Ирина Невинная
Почему нельзя принимать антибиотики бесконтрольно, угрожают ли нам «супербактерии» и как снизить этот риск? На вопросы «РГ-Недели» ответил главный внештатный специалист Минздрава России по клинической микробиологии и антимикробной резистентности, руководитель Сотрудничающего центра ВОЗ по укреплению потенциала в сфере надзора и исследований антимикробной резистентности, ректор СГМУ Минздрава России, член-корреспондент РАН Роман Козлов.
Донат Сорокин / ТАСС
Сейчас, в ковидные времена, нас изо дня в день предупреждают: нельзя лечить COVID-19 антибиотиками, нельзя заниматься самолечением. Почему эта тема стала сейчас так актуальна?
Роман Козлов: Не только COVID-19, но и все вирусные инфекции антибиотиками лечить не нужно, бесполезно и даже вредно, и специалисты об этом говорят уже давно. В последний год проблема обострилась, потому что большой процент больных COVID-19 начинает принимать антибиотики даже на ранней стадии заболевания, причем большинство самостоятельно, без назначения врача. Понимая, к чему это может привести, какими могут быть последствия, специалисты, естественно, бьют тревогу.
А какими могут быть последствия?
Роман Козлов: Сейчас на планете от инфекций, устойчивых к антибиотикам, умирают примерно 700 тысяч человек в год. Если ничего не делать, это число будет нарастать. По прогнозам, к 2050 году жертвами антибиотикорезистентности могут стать уже 10 млн человек ежегодно — это больше, чем даже прогнозируемая смертность от онкозаболеваний. Избыточное применение этих лекарств — это проблема не только нашей страны, это одна из основных движущих сил развития устойчивости к антибиотикам в мире.
Избыточное применение этих лекарств — это проблема не только нашей страны, это одна из основных движущих сил развития устойчивости к антибиотикам в мире.
Во время пандемии COVID-19 положение усугубилось. Понятно, что инфекция новая, сначала было абсолютно непонятно, чем и как лечить. Но сейчас уже есть достоверные данные, что только у 8-20 процентов заразившихся развиваются осложнения, требующие лечения антибиотиками. А по факту их получают девять из десяти пациентов. Конечно, это может привести к еще более быстрому росту устойчивости к таким препаратам.
Поясните, пожалуйста, что, собственно, это такое — антибиотикорезистентность?
Роман Козлов: Давайте разберемся с азов. Антибиотики — это препараты, которые создавались для того, чтобы бороться с бактериями, вызывающими различные инфекционные заболевания. Уничтожить болезнетворные бактерии — значит убрать причину заболевания. Казалось бы, все просто. Но нет. Микроорганизмы сравнительно простые по строению живые существа, но у них, как у всяких живых существ, две цели — выжить и произвести как можно больше себе подобных. Поэтому у них есть определенные защитные механизмы, которые они используют при встрече с антибиотиком. Например, бактерия вырабатывает особый фермент, который нарушает структуру антибиотика, делает его неактивным. Другой вариант — бактерия изменяет проницаемость своей клеточной стенки, чтобы антибиотик не мог попасть внутрь. Третий механизм — это такая мутация, при которой микроорганизм изменяет ферменты, обеспечивающие его жизненный цикл — функции дыхания, питания, деления. Антибиотик не может с новым ферментом связаться и, соответственно, не может повлиять на бактерию. Еще один механизм — очень элегантный. Это «эффлюкс» — механизм «активного выброса». В любом организме есть система выделения — чтобы избавляться от ненужных продуктов жизнедеятельности. Некоторые микробы умеют адаптировать эти механизмы и начинают выбрасывать не только собственные «отработанные» токсические вещества, но заодно и антибиотики. Еще один хитрый способ стать неуязвимым — это так называемый механизм «обходного пути», когда микроб блокирует свою мишень, на которую действует антибиотик, а вместо нее формирует другую, резервную мишень.
Поэтому у них есть определенные защитные механизмы, которые они используют при встрече с антибиотиком. Например, бактерия вырабатывает особый фермент, который нарушает структуру антибиотика, делает его неактивным. Другой вариант — бактерия изменяет проницаемость своей клеточной стенки, чтобы антибиотик не мог попасть внутрь. Третий механизм — это такая мутация, при которой микроорганизм изменяет ферменты, обеспечивающие его жизненный цикл — функции дыхания, питания, деления. Антибиотик не может с новым ферментом связаться и, соответственно, не может повлиять на бактерию. Еще один механизм — очень элегантный. Это «эффлюкс» — механизм «активного выброса». В любом организме есть система выделения — чтобы избавляться от ненужных продуктов жизнедеятельности. Некоторые микробы умеют адаптировать эти механизмы и начинают выбрасывать не только собственные «отработанные» токсические вещества, но заодно и антибиотики. Еще один хитрый способ стать неуязвимым — это так называемый механизм «обходного пути», когда микроб блокирует свою мишень, на которую действует антибиотик, а вместо нее формирует другую, резервную мишень. Одним словом, эта «война» на выживание продолжается постоянно и «военные действия» разнообразны и сложны.
Одним словом, эта «война» на выживание продолжается постоянно и «военные действия» разнообразны и сложны.
Что происходит, если мы злоупотребляем приемом антибиотиков?
Роман Козлов: Внутри нас живет великое множество микроорганизмов. Пока они существуют в балансе — мы остаемся здоровыми. Но когда мы принимаем антибиотик необоснованно, то есть когда нет бактериальной инфекции, этот баланс нарушается. Ведь антибиотик не выбирает — убивает он болезнетворную бактерию или вполне себе мирную и безвредную. В результате с каждым таким курсом лечения погибает часть чувствительных к этому антибиотику бактерий, но остаются устойчивые, в том числе и патогенные. И со временем риск, что в следующий раз инфекционное заболевание будет вызвано такой вот устойчивой бактерией, становится все больше.
Значит ли это, что антибиотики, которые были открыты первыми, уже устарели и ими нельзя лечить?
Роман Козлов: Нет, в клинической практике используют все препараты, поэтому говорить «устаревший» применительно к антибиотику неправильно. Тот же пенициллин, который был открыт первым и во время Второй мировой войны спас миллионы жизней, применяют до сих пор. Для лечения сифилиса, например. Другое дело, что один и тот же антибиотик у двух пациентов с одинаковой инфекцией может и давать хороший результат, и быть неэффективным. Например, один больной редко лечился антибиотиками и принимал их правильно. Другой, как поступают многие, считал, что любой «чих» можно по-быстрому задавить таблетками. Он мог перепробовать несколько препаратов, толком не долечиваясь. В итоге, когда он снова заболеет, найти эффективное лекарство будет значительно труднее — именно из-за высокого риска резистентности.
Тот же пенициллин, который был открыт первым и во время Второй мировой войны спас миллионы жизней, применяют до сих пор. Для лечения сифилиса, например. Другое дело, что один и тот же антибиотик у двух пациентов с одинаковой инфекцией может и давать хороший результат, и быть неэффективным. Например, один больной редко лечился антибиотиками и принимал их правильно. Другой, как поступают многие, считал, что любой «чих» можно по-быстрому задавить таблетками. Он мог перепробовать несколько препаратов, толком не долечиваясь. В итоге, когда он снова заболеет, найти эффективное лекарство будет значительно труднее — именно из-за высокого риска резистентности.
Почему если назначен курс лечения антибиотиком, обязательно нужно завершить его полностью, не бросать прием препарата на полдороги?
Роман Козлов: Ответ простой: мертвый микроб не мутирует. Во время лечения в первую очередь погибают патогены, наиболее чувствительные к антибиотику. Количество микробов, вызывающих инфекцию, снижается, больному становится лучше. Если прием прекратить преждевременно — какая-то часть микробов, наиболее устойчивая к данному препарату, останется и начнет размножаться — возникнет рецидив инфекции либо она перейдет в хроническую форму.
Если прием прекратить преждевременно — какая-то часть микробов, наиболее устойчивая к данному препарату, останется и начнет размножаться — возникнет рецидив инфекции либо она перейдет в хроническую форму.
Вообще-то самолечение — это не только наша безграмотность. Во многих случаях до врача просто сложно дойти. К тому же при амбулаторном лечении COVID-19 врачи очень многим буквально сразу назначали антибиотики, иногда и по два препарата сразу…
Роман Козлов: Я должен встать на защиту медработников. Мы все год назад столкнулись с совершенно новой, неизвестной ранее инфекцией, которая стремительно распространялась по всему миру, а осложнения были очень тяжелыми. Мы понимали, что это инфекционное заболевание, но не было от него ни вакцины, ни специфических лекарств. Поэтому врачи действительно сначала пробовали применять различные препараты — против гриппа, против малярии, не говоря уже о симптоматической терапии. Но по мере накопления практики и опыта ситуация поменялась. Я уже сказал, что осложнения, связанные с присоединением бактериальной инфекции, возникают у 8-20 процентов больных COVID-19. И им назначение антибиотиков, конечно, необходимо.
Я уже сказал, что осложнения, связанные с присоединением бактериальной инфекции, возникают у 8-20 процентов больных COVID-19. И им назначение антибиотиков, конечно, необходимо.
Все это четко прописано в клинических рекомендациях Минздрава. Основная масса врачей это понимают и выполняют. А вот сами люди — далеко не всегда. Самолечение по-прежнему остается большой проблемой.
Как врач выбирает конкретный антибиотик, их ведь много?
Роман Козлов: В помощь врачу есть клинические рекомендации, которые пишут лучшие специалисты в конкретной области. Это не диктат врачу, это та база, на которую он опирается, выбирая терапию для конкретного пациента, исходя из его особенностей и с учетом своего собственного опыта.
Современный врач, если он серьезно относится к своей профессии, учится постоянно, он следит за современными тенденциями, анализирует их и применяет в своей практике. Собственно, этого требует и внедренная минздравом система непрерывного медицинского образования.
Насколько я знаю, чтобы выбрать самый эффективный антибиотик, врач должен назначить пациенту специальный анализ на чувствительность микрофлоры. Но на практике это делается нечасто. В результате иногда приходится менять препарат в ходе лечения.
Роман Козлов: Вы правы, для выбора тактики лечения это важно. Но тут нужно учитывать и специфику заболевания, и анамнез у конкретного больного. Покажу на примере. Самая частая инфекция мочевых путей у женщин — это цистит. Многие лечат его сами, в том числе и антибиотиками. Это заболевание вызывает очень ограниченный спектр микроорганизмов, и врач знает, какой антибиотик против них наиболее эффективен. Обычно, если до этого пациентка не принимала антибиотики, может хватить всего одной дозы. Зачем тут делать посев, ждать три дня результата? Правильнее начать лечение немедленно. А в идеале — все-таки направить больную сдать анализ и, получив результат, если нужно, скорректировать схему лечения.
Заодно, если врач такие исследования выполняет регулярно, он видит, что, например, у 70 процентов его пациенток с таким диагнозом причиной заболевания стала кишечная палочка. То есть у него накапливаются знания, какие виды патогенов, устойчивых к антибактериальным препаратам, встречаются чаще всего. И это позволяет выбирать оптимальную схему лечения.
То есть у него накапливаются знания, какие виды патогенов, устойчивых к антибактериальным препаратам, встречаются чаще всего. И это позволяет выбирать оптимальную схему лечения.
В нашем Методическом верификационном центре по вопросам антимикробной резистентности мы проводим масштабное исследование — получаем изо всех регионов возбудителей инфекционных заболеваний, примерно 10 тысяч в год, тестируем их на чувствительность к имеющимся в клинической практике и перспективным антибиотикам. В результате мы создали интерактивную «Карту антибиотикорезистентности России» (map.antibiotic.ru), которая постоянно обновляется и пополняется новыми данными. Аналогов этому проекту в мире нет.
Любой врач, к которому пришел пациент с инфекционным заболеванием, может зайти в нашу базу данных и посмотреть, что происходит в его регионе, и назначать лечение с учетом этой информации.
Еще практический вопрос. При лечении антибиотиками иногда возникают нежелательные явления — например, диарея. Нужно ли параллельно принимать препараты для восстановления микрофлоры или правильнее пропить их, когда лечение антибиотиком уже закончится?
Нужно ли параллельно принимать препараты для восстановления микрофлоры или правильнее пропить их, когда лечение антибиотиком уже закончится?
Роман Козлов: Давайте определимся жестко: назначение антибиотиков — это эксклюзивная прерогатива врача. Ни фармацевта, ни провизора, ни советчиков из интернета, а лечащего врача. Только он знает своего пациента и может учесть его индивидуальные особенности. Например, возникновение аллергической реакции при предыдущем назначении.
В большинстве случаев побочные реакции, в том числе и нарушения перистальтики кишечника, проходят после завершения курса приема антибиотика и не требуют дополнительного лечения.
Но поймите: антибиотики — это серьезные лекарства. Ни у кого же не вызывает сомнения, что онкопрепараты больной не может назначить себе сам? Почему же тогда мы так легко начинаем глотать антибиотики даже при легком недомогании? Это для меня очень больной вопрос.
Ну сейчас по сравнению с тем, что было несколько лет назад, ситуация изменилась: в большинстве аптек антибиотики без рецепта купить уже сложно…
Роман Козлов: Я рад, мы за это долго боролись. Это не излишние строгости, как многие считают и выражают недовольство, а нормальная практика. Нигде — ни в Европе, ни в США, ни в других странах без рецепта врача в аптеке с вами и разговаривать не будут.
Это не излишние строгости, как многие считают и выражают недовольство, а нормальная практика. Нигде — ни в Европе, ни в США, ни в других странах без рецепта врача в аптеке с вами и разговаривать не будут.
Насколько велика угроза появления «супербактерий», против которых вообще не будет эффективных лекарств?
Роман Козлов: Скажу сразу, профессионалам этот придуманный кем-то термин не очень нравится. Он, конечно, привлекает внимание, но с точки зрения микробиологии неправильный.
Да, есть микроорганизмы, устойчивые к большинству антибиотиков. Это большая проблема стационаров, например, отделений реанимации, где у пациентов а часто применяют антибиотики и, соответственно, появляются устойчивые к ним штаммы.
ВОЗ на основе опроса экспертов из разных стран в 2017 году опубликовала список критически значимых патогенов, для борьбы с которыми нужны новые антибиотики, поскольку те, что сегодня имеются, неэффективны. По сути, это и есть список «супербактерий». Я тоже принимал участие в этой работе — от России. Эксперты были единодушны — возбудители, которые были включены в этот перечень (он разбит на несколько групп — по степени опасности), одинаковы для всех стран. И это понятно — бактерии границ не знают.
Я тоже принимал участие в этой работе — от России. Эксперты были единодушны — возбудители, которые были включены в этот перечень (он разбит на несколько групп — по степени опасности), одинаковы для всех стран. И это понятно — бактерии границ не знают.
Фото: Photoexpress
Насколько критична ситуация? Правда ли, что фармакологи исчерпали возможности в разработке новых препаратов и армия бактериальных инфекций вот-вот человечество обыграет?
Роман Козлов: Нет. Я настроен оптимистично. Думаю, «Армагеддон» не наступит. За последние годы и в мире, и в нашей стране этой проблемой стали заниматься всерьез. Сокращается применение антибиотиков в сельском хозяйстве. Государства стимулируют фармкомпании разрабатывать новые препараты. Дело не в том, что исчерпаны возможности в проведении таких изысканий, а в том, что экономически фармкомпаниям это не очень интересно. Чтобы успешный антибиотик вернул вложенные в его разработку средства, требуется в среднем 28 лет. Эти лекарства, как правило, назначают коротким курсом, и в целом уровень их потребления намного ниже, чем, допустим, популярного антидепрессанта, который пациент будет принимать пожизненно.
Эти лекарства, как правило, назначают коротким курсом, и в целом уровень их потребления намного ниже, чем, допустим, популярного антидепрессанта, который пациент будет принимать пожизненно.
Хорошо, что правительства разных стран это понимают и сейчас в мире отрабатывают разнообразные экономические модели, которые позволят обеспечить наши потребности в таких препаратах. Наша страна тоже в тренде: в рамках программы «Фарма-2030» создание новых антибиотиков — в приоритете.
Российская газета — Неделя — Федеральный выпуск: №74(8425)
Поделиться
Здоровье
Как избежать устойчивости к антибиотикам — когда мне нужен антибиотик?
Семейный врач. 2001;63(6):1097-1098
Что такое антибиотики?
Антибиотики — это лекарства, которые борются (или предотвращают) инфекции, вызванные бактериями. Бактерии также называют микробами. Если инфекция вызвана вирусом, антибиотики не могут бороться с вирусом.
Бактерии также называют микробами. Если инфекция вызвана вирусом, антибиотики не могут бороться с вирусом.
Что такое устойчивость к антибиотикам?
Когда бактерии подвергаются воздействию тех же антибиотиков, через некоторое время антибиотик уже не может бороться с микробами. Воздействие одного и того же антибиотика в течение длительного времени может привести к изменению некоторых микробов. Иногда микробы просто меняются сами по себе. Некоторые изменения делают микробы настолько сильными, что они могут дать отпор антибиотикам и победить в этой битве. Эти сильные микробы могут жить и размножаться, даже когда вы принимаете антибиотики. Говорят, что эти микробы «резистентны» к этому антибиотику. Микробы могут даже стать устойчивыми ко многим антибиотикам. Устойчивость к антибиотикам становится распространенной проблемой во многих частях Соединенных Штатов.
Нужно ли опасаться устойчивости к антибиотикам?
Если ваша инфекция устойчива к антибиотику, который вы принимаете, инфекция может длиться дольше.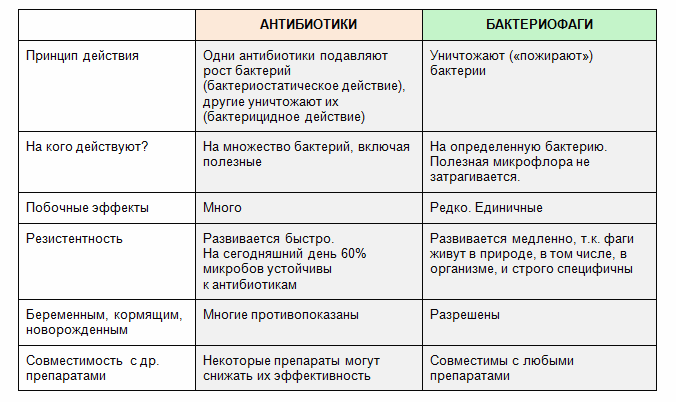 Вместо улучшения ваша инфекция может ухудшиться. Возможно, вам придется несколько раз посетить кабинет врача. Возможно, вам придется принимать различные лекарства или обратиться в больницу за антибиотиками, введенными в ваши вены.
Вместо улучшения ваша инфекция может ухудшиться. Возможно, вам придется несколько раз посетить кабинет врача. Возможно, вам придется принимать различные лекарства или обратиться в больницу за антибиотиками, введенными в ваши вены.
В то же время члены вашей семьи или другие люди, с которыми вы контактируете, могут заразиться имеющимися у вас резистентными микробами. Тогда эти люди также могут заболеть инфекциями, которые трудно вылечить.
Итак, когда мне можно принимать антибиотики?
Ваш врач может назначить антибиотики только при заболеваниях, вызванных микробами. Эти заболевания включают такие инфекции, как ангина, инфекции мочевыводящих путей и ушные инфекции. Люди иногда просят у своего врача антибиотики, когда у них есть вирусное заболевание, такое как простуда, грипп (грипп) или мононуклеоз (моно). Антибиотики не могут вылечить эти болезни.
Вы не должны настаивать на том, чтобы ваш врач давал вам или вашим детям антибиотики для лечения вирусного заболевания. Вместо этого спросите у своего врача, что вы можете сделать, чтобы почувствовать себя лучше. Каждый раз, когда вы принимаете антибиотики, когда они вам на самом деле не нужны, вы увеличиваете вероятность того, что когда-нибудь заболеете болезнью, вызванной микробами, устойчивыми к антибиотикам.
Вместо этого спросите у своего врача, что вы можете сделать, чтобы почувствовать себя лучше. Каждый раз, когда вы принимаете антибиотики, когда они вам на самом деле не нужны, вы увеличиваете вероятность того, что когда-нибудь заболеете болезнью, вызванной микробами, устойчивыми к антибиотикам.
Как мне принимать антибиотики, прописанные врачом?
Внимательно следуйте указаниям врача. Ваш врач скажет вам принять все антибиотики. Не прекращайте прием антибиотика только потому, что вам стало лучше. Прием меньшего количества антибиотика, когда он вам нужен, не поможет предотвратить устойчивость к антибиотикам.
Что еще я могу сделать, чтобы снизить риск устойчивости к антибиотикам?
Мойте руки водой с мылом перед едой и после посещения туалета. Регулярное мытье рук поможет сохранить здоровье и предотвратить распространение микробов.
Спросите своего врача, есть ли у вас все прививки (прививки), необходимые для защиты от болезни.
Где я могу получить дополнительную информацию об устойчивости к антибиотикам?
Центры по контролю и профилактике заболеваний
Альянс за разумное использование антибиотиков
Лечение длительных и повторных назначений антибиотиков в учреждениях первичной медико-санитарной помощи: соображения поведенческого подхода
Текст статьи
Меню статьи
- Статья
Текст - Артикул
Информация - Цитата
Инструменты - Поделиться
- Быстрое реагирование
- Артикул
Метрика - Оповещения
Редакция
Лечение длительных и повторных назначений антибиотиков в учреждениях первичной медико-санитарной помощи: соображения поведенческого подхода
- Ева М Кроков1,
- Элеонора Дж.
 Харви2,
Харви2, - http://orcid.org/0000-0001-9579-2028Дайан Аширу-Оредоп2
- 2 1 Кафедра неврологии, психологии и поведения, Лестерский университет, Лестер, Великобритания
- 2 HCAI, Fungal, AMR, AMU & Отдел сепсиса, UK Health Security Agency, Лондон, Великобритания
- Соответствие Д-р Diane Ashiru-Oredope, Агентство по охране здоровья Великобритании, Лондон, Северо-Западная 95EQ, Лондон, Великобритания; Diane.Ashiru-Oredope{at}ukhsa.gov.uk
http://dx.doi.org/10.1136/bmjqs-2022-014821
Статистика с сайта Altmetric.com
Запросить разрешения
приведет вас к службе RightsLink Центра защиты авторских прав. Вы сможете получить быструю цену и мгновенное разрешение на повторное использование контента различными способами.
- Лечение антибиотиками
- Общая врачебная практика
- Фармацевты
- Первичная медико-санитарная помощь
- Совместное принятие решений
Чрезмерное назначение антибиотиков в учреждениях первичной медико-санитарной помощи является одной из важных причин устойчивости к противомикробным препаратам (УПП) во всем мире.

Авторы подчеркивают значительную изменчивость в структуре случаев, при этом некоторые клиницисты сталкиваются с более серьезными проблемами из-за высокого исходного риска микробной инфекции среди своих пациентов. Используя обобщенные аддитивные модели смешанных эффектов Пуассона, предполагается, что наибольшее потенциальное сокращение назначения антибиотиков может быть достигнуто за счет назначения на основе риска, особенно для пациентов, получающих повторные назначения. Также предполагается, что сокращение количества повторных курсов антибиотикотерапии до уровня среднего врача позволит сэкономить 21 813 назначений антибиотиков на 1000 клиницистов в год. Если еще больше сократить этот показатель до самого низкого 25-го процентиля, это приведет к сокращению на 38 871 назначений антибиотиков на 1000 клиницистов в год.
van Staa et al.3 Показатели повторных назначений антибиотиков выше, чем в когортном исследовании 2002–2017 гг. в Великобритании4, в котором сообщалось, что средний процент повторных назначений антибиотиков составляет 10%. Тем не менее, средний показатель в 23,2% все еще ниже, чем результаты исследования выписывания рецептов на дому в Великобритании5, которые показали, что 30% назначений антибиотиков соответствовали определению повторных назначений. В исследовании, проведенном в Великобритании на дому престарелых, антибиотиками, которые чаще всего повторяли в течение длительного времени, были азитромицин, цефалексин, нитрофурантоин и триметоприм. Эти препараты обычно рекомендовали для профилактики хронической обструктивной болезни легких и инфекций мочевыводящих путей. Другое британское исследование показало, что большинство повторных назначений антибиотиков имело место при отсутствии определенного закодированного клинического состояния, что позволяет предположить, что повторные назначения потенциально использовались в качестве лечения в случаях клинической неопределенности.
Определение повторных назначений
Одной из проблем при обсуждении роли повторных назначений в контексте чрезмерного использования антибиотиков является трудность определения повторных назначений. van Staa et al.3 определение включает любой антибиотик, назначенный в течение 30 дней после предыдущего назначения того же препарата. В других исследованиях использовалась другая продолжительность (например, 35 дней5) или вообще разные определения (например, любое назначение антибиотика, кроме первого, которое имело место в последовательности назначений одного и того же препарата4, 6). Различные определения могут объяснять некоторые различия, наблюдаемые в статистике повторных назначений. Кроме того, существующие определения, по-видимому, смешивают два разных типа повторного назначения лекарств. Первый тип относится к долгосрочным повторным назначениям при хронических состояниях, принимаемым непрерывно с небольшим перерывом или без перерыва. Второй тип относится к краткосрочным повторным назначениям по поводу острых проблем, которые не разрешились после однократного курса антибиотиков или вызваны дополнительными инфекциями, возникшими в течение установленного периода.
В Великобритании долгосрочные повторные рецепты — это предварительно утвержденные рецепты на лекарства, которые пациенты могут запрашивать без необходимости каждый раз консультироваться. Обычно их предлагают пациентам, которым требуются лекарства для длительного применения в рамках лечения хронических заболеваний. Длительное использование антибиотиков может происходить как часть профилактики инфекции. Краткосрочные повторные назначения, с другой стороны, относятся к повторным курсам антибиотиков, которые назначаются после повторных консультаций пациентов по поводу одной и той же или разных инфекций в течение определенного периода времени, например, 6 месяцев.
Большинство врачей общей практики следуют рекомендациям 28-дневных курсов рецептов, а это означает, что долгосрочные повторные рецепты выписываются каждый месяц7. Следовательно, определения предыдущих исследований вряд ли позволят провести более детальный анализ и сравнение чрезмерного использования антибиотиков на основе длительного -срочные по сравнению с краткосрочными повторными рецептами. Поэтому для целей этой редакционной статьи мы рассмотрим оба типа, совместно назвав их «повторными» рецептами.
Поэтому для целей этой редакционной статьи мы рассмотрим оба типа, совместно назвав их «повторными» рецептами.
Врачи общей практики в Великобритании используют электронные системы для управления повторными рецептами, но предыдущие исследования выявили проблемы с электронными рецептами, которые могут увеличить риск ненадлежащего постоянного использования лекарств.8 Эти проблемы, связанные с автоматизацией утверждения рецептов, могут привести к недостаткам в надлежащем процедуры авторизации и проверки. Недавние исследования показывают, что долгосрочное применение антибиотиков малоэффективно для большинства пациентов.9Фактически, повторное назначение антибиотиков, по-видимому, предсказывает более высокий долгосрочный риск госпитализации, связанной с инфекцией,9 и это может быть связано с биологическими механизмами дисбактериоза (т. е. с нарушением микробиоты кишечника). Кроме того, сообщалось о негативном влиянии пандемии COVID-19 на разумное назначение противомикробных препаратов. Например, врачи общей практики сообщили о более низких порогах использования антибиотиков при респираторных симптомах, особенно в начале пандемии.10
Например, врачи общей практики сообщили о более низких порогах использования антибиотиков при респираторных симптомах, особенно в начале пандемии.10
В контексте ранее выявленных проблем, связанных с повторным назначением антибиотиков, которые, возможно, еще более усугубились недавней пандемией, «выводы, сделанные van Staa et al.3, подчеркивают необходимость сокращения повторного назначения антибиотиков как части меню вариантов борьбы с УПП. .
Психология повторных назначений
Чтобы изменить поведение, связанное с назначением лекарств, важно учитывать возможные психосоциальные факторы текущей лечебной практики. Несколько взаимозависимых психологических факторов, вероятно, играют определенную роль.
Предубеждения при принятии решений
Исследования в области поведенческих наук неоднократно демонстрировали силу когнитивных искажений, которые систематически влияют на процесс принятия решений. Действительно, в недавней редакционной статье были отмечены специфические предубеждения, возникающие в результате диагностической неопределенности в контексте назначения антибиотиков пациентам с острыми состояниями в условиях вторичной медицинской помощи. 11 В контексте повторных назначений врачами общей практики, вероятно, играют роль несколько иные когнитивные механизмы. Это включает в себя «предвзятость статус-кво», которая описывает человеческую тенденцию поддерживать статус-кво по умолчанию, даже если изменение стратегии может иметь предпочтительные результаты. Это тесно связано с «предвзятостью упущения», которая относится к иррациональному предпочтению ошибок, основанных на упущении, а не на активном выборе. Предыдущие исследования показали, что и пациенты, и врачи подвержены этим предубеждениям.12 Качественные данные вторичной медицинской помощи указывают на нерешительность в отношении деэскалации или прекращения курсов антибиотиков, даже когда состояние пациентов улучшалось, по общим причинам, включая нежелание «сменить команду-победительницу». .13 Вполне вероятно, что подобные мотивы лежат в основе нерешительности в отношении прекращения повторных назначений в первичном звене, особенно если назначение антибиотика было начато в вторичном звене.
11 В контексте повторных назначений врачами общей практики, вероятно, играют роль несколько иные когнитивные механизмы. Это включает в себя «предвзятость статус-кво», которая описывает человеческую тенденцию поддерживать статус-кво по умолчанию, даже если изменение стратегии может иметь предпочтительные результаты. Это тесно связано с «предвзятостью упущения», которая относится к иррациональному предпочтению ошибок, основанных на упущении, а не на активном выборе. Предыдущие исследования показали, что и пациенты, и врачи подвержены этим предубеждениям.12 Качественные данные вторичной медицинской помощи указывают на нерешительность в отношении деэскалации или прекращения курсов антибиотиков, даже когда состояние пациентов улучшалось, по общим причинам, включая нежелание «сменить команду-победительницу». .13 Вполне вероятно, что подобные мотивы лежат в основе нерешительности в отношении прекращения повторных назначений в первичном звене, особенно если назначение антибиотика было начато в вторичном звене.
Инерция решений
Предвзятость статус-кво также связана с «инерцией решений», которая относится к тенденции отдавать предпочтение решениям, связанным с меньшими когнитивными усилиями. Критические обзоры повторных рецептов могут считаться трудоемкими и требуют больше усилий, чем сохранение статус-кво. Учитывая нехватку времени в общей практике, существует давление, направленное на минимизацию рабочей нагрузки, и это может способствовать тому, что рецепты пациентов не пересматриваются.8 Предыдущие исследования показали, что ограниченное время и когнитивные ресурсы могут влиять на выбор лечения антибиотиками, а врачи больниц описывали назначение антибиотиков как «легкий». вариант, особенно в нерабочее время.14 Когнитивные усилия, вероятно, будут еще больше снижены при выборе продолжения предыдущего курса лечения в общей практике.
Социальные нормы
Общепризнано, что культура медицинской среды влияет на привычки местных врачей выписывать рецепты. Действительно, в предыдущих исследованиях были выявлены доминирующие правила этикета назначения антибиотиков, часто формируемые социальными и профессиональными иерархиями, которые влияют на выбор назначения антибиотиков. быть старшим или, возможно, специалистом, либо с точки зрения профессионального опыта, либо уровня подготовки или образования. Кроме того, противоречие коллеге и предоставление непоследовательных советов пациентам может считаться плохой практикой, которая может способствовать подрыву позиций других коллег-медиков.16
быть старшим или, возможно, специалистом, либо с точки зрения профессионального опыта, либо уровня подготовки или образования. Кроме того, противоречие коллеге и предоставление непоследовательных советов пациентам может считаться плохой практикой, которая может способствовать подрыву позиций других коллег-медиков.16
Распределение ответственности
Другим психологическим фактором, способствующим чрезмерному использованию повторных назначений, может быть рассеяние ответственности. Пассивное решение продолжить лечение, начатое предыдущим врачом, скорее всего, снизит предполагаемую ответственность текущего врача за любые связанные с ним результаты. В случае неблагоприятного исхода бремя последующих жалоб или расследований, скорее всего, будет нести первоначальный врач. Действительно, предыдущие исследования подчеркивали, что боязнь судебных разбирательств является важной движущей силой принятия решений об антибиотиках во вторичной медицинской помощи,17 и аналогичные факторы могут играть роль в повторном выборе назначения в общей практике.
Стратегии по сокращению/избежанию необоснованных повторных назначений антибиотиков
Для решения проблемы повторного назначения противомикробных препаратов и содействия изменению поведения мы предлагаем учитывать психосоциальные факторы повторного назначения при разработке механизмов контроля или вмешательств (рис. 1). Для уменьшения последствий статус-кво и предубеждений, связанных с пропусками, может потребоваться адаптация электронной среды существующих систем выписывания рецептов. Необходимо соблюдать осторожность, чтобы не выделить продолжение повторного назначения по умолчанию. Этого можно достичь путем введения системных барьеров, которые побуждают к более тщательным проверкам и увеличивают когнитивные ресурсы, вкладываемые в процесс выдачи разрешений на повторные курсы антибиотиков. Некоторый значительный успех был отмечен австралийским исследованием, которое показало, что устранение системных настроек по умолчанию привело к резким изменениям в назначении противомикробных препаратов. или структурированный обзор лекарств,20 который требует изучения опыта повторного назначения пациентами противомикробных препаратов, предлагает возможности для улучшения.
или структурированный обзор лекарств,20 который требует изучения опыта повторного назначения пациентами противомикробных препаратов, предлагает возможности для улучшения.
Рисунок 1
Стратегии по сокращению необоснованного долгосрочного и краткосрочного повторного назначения антибиотиков.
Решение проблем нехватки времени и связанных с ними проблем инерции решений может потребовать пересмотра и расширения традиционных ролей назначающих врачей. В этом отношении были достигнуты первые успехи. В глобальном масштабе наблюдается изменение кадровых ресурсов первичной медико-санитарной помощи, особенно в Канаде, США, Австралии и Великобритании. Поскольку роль фармацевтов быстро развивается в общей практике, у них есть значительные возможности для их участия. Важное значение имеет повышение уверенности фармацевтов общей практики и внебольничных фармацевтов в необходимости наблюдения за пациентами, получающими повторное лечение антибиотиками, путем непрерывного обучения и наличия специализированных наборов инструментов. Благодаря более длительному времени приема и специализированным наборам инструментов для помощи в клиническом анализе фармацевты могут считаться хорошо подготовленными для устранения некоторых барьеров.21
Благодаря более длительному времени приема и специализированным наборам инструментов для помощи в клиническом анализе фармацевты могут считаться хорошо подготовленными для устранения некоторых барьеров.21
Изменение существующих социальных норм и создание критической, но конструктивной культуры обратной связи в различных медицинских профессиях — это долгосрочные задачи, которые можно решить, внедрив более групповые подходы к принятию решений11 и выработав привычку к коллегиальному анализу. Повторное назначение антибиотиков в общей практике может происходить различными путями, и важно определить, как социальные нормы могут влиять на эти разные пути и способствовать тому, что неотложные назначения становятся долгосрочными. Одним из вариантов может быть введение рутинных обзоров выписных справок от врачей второго звена через бригаду первичного звена (фармацевтов, медсестер и врачей). Это может предотвратить добавление несоответствующих больничных рецептов в список повторных лекарств пациента.
Психологическое стремление к размыванию ответственности путем продолжения назначения противомикробных препаратов другими врачами часто связано со страхом перед жалобами пациентов и судебными разбирательствами. Исследования показали, что общая практика с частотой назначений антибиотиков ниже среднего показателя по стране имела более низкие оценки удовлетворенности пациентов. общий контекст УПП.23 Таким образом, бесполезные стратегии защитной медицины и чрезмерного назначения лекарств можно было бы заменить более активными усилиями по улучшению общения между врачом и пациентом и улучшению знаний пациентов. Их необходимо будет реализовать наряду с постоянным поощрением «сетевого обеспечения безопасности» для лиц, назначающих препараты11, и постоянными усилиями по увеличению числа медицинских работников и информированности населения. Национальные и международные кампании, такие как Keep Antibiotics Work (Великобритания), Be Antibiotics Aware (США) и Всемирная неделя осведомленности о противомикробных препаратах (WHO/Global), были направлены на повышение осведомленности об антимикробных препаратах. Текущая международная кампания Antibiotic Guardian, направленная на принятие обязательств, может способствовать изменению поведения и повлиять на действия людей по борьбе с распространением УПП.24
Текущая международная кампания Antibiotic Guardian, направленная на принятие обязательств, может способствовать изменению поведения и повлиять на действия людей по борьбе с распространением УПП.24
Следует отметить, что в некоторых случаях повторные курсы антибиотиков или антибиотикопрофилактика клинически оправданы, например, для лечения хронической инфекции. Длительная профилактика антибиотиками также имеет решающее значение для некоторых людей, например, для людей, перенесших спленэктомию или страдающих серповидно-клеточной анемией. Клинические обзоры пациентов, получающих повторные назначения антибиотиков, должны использовать целостный подход, чтобы понять перспективы и цели пациентов. Следует поощрять совместное принятие решений, и пациенты должны быть проинформированы об альтернативах антибиотикам (при их наличии) и потенциальном вреде антибиотиков, как с точки зрения побочных эффектов (например, нитрофурантоин-индуцированный гепатит), так и воздействия на микробиоту, а также риска. возможное инфицирование устойчивыми к антибиотикам возбудителями.
возможное инфицирование устойчивыми к антибиотикам возбудителями.
Наконец, какие бы вмешательства ни были разработаны, важно учитывать неравенство в отношении здоровья, чтобы избежать риска того, что определенные группы не получат одинаковый доступ к медицинскому обслуживанию. Текущие примеры включают недостаточное использование антибиотиков в зависимости от контекста (например, среди сельского населения маори в Новой Зеландии25).
Выводы
Борьба с необоснованным повторным назначением антибиотиков может иметь большой потенциал для снижения чрезмерного назначения антибиотиков в первичной медико-санитарной помощи. Мы выделяем психосоциальные факторы повторного назначения антибиотиков и предлагаем механизмы учета этих факторов при разработке вмешательств. Основываясь на нашем обзоре теории и соответствующих международных исследованиях, мы даем действенные рекомендации по внедрению новых моделей поведения и осуществлению позитивных изменений.
Необходима дальнейшая работа, чтобы понять соответствующие масштабы долгосрочного и краткосрочного повторного назначения антибиотиков в различных секторах здравоохранения и разработать конкретные меры для поддержки пересмотра повторного назначения антибиотиков при наиболее распространенных инфекциях и часто назначаемых антибиотиков.
Благодарности
Рэйчел Фрэнсис-Нвеке, клинический фармацевт общей практики и службы скорой помощи выражает благодарность за комментарии к статье перед ее отправкой.
Ссылки
- ↵
- Ллор С ,
- Бьеррум Л.
. Устойчивость к противомикробным препаратам: риск, связанный с чрезмерным использованием антибиотиков, и инициативы по уменьшению этой проблемы. Ther Adv Drug Saf 2014; 5:229–41.doi:10.1177/2042098614554919 пмид: http://www.ncbi.nlm.nih.gov/pubmed/25436105
- ↵
- Смешек Т ,
- Пауэлс КБ ,
- Долк FCK , и другие
. Потенциал для сокращения необоснованного назначения антибиотиков в первичной медико-санитарной помощи на английском языке. J Antimicrob Chemother 2018;73:ii36–43.doi:10.1093/jac/dkx500 пмид: http://www.ncbi.nlm.nih.
 gov/pubmed/294
gov/pubmed/294
- ↵
- Ван Стаа Т ,
- Ли Ю ,
- Золото Н
. Сравнение назначений антибиотиков клиницистами первичной медико-санитарной помощи в Великобритании: анализ в когортном исследовании восьми различных показателей назначения антибиотиков. BMJ Qual Saf 2022;31:831–8.doi:10.1136/bmjqs-2020-012108 пмид: http://www.ncbi.nlm.nih.gov/pubmed/35241573
- ↵
- Гуллифорд МЦ ,
- Солнце Х ,
- Чарльтон Дж. , и другие
. Серьезные бактериальные инфекции и назначение антибиотиков в учреждениях первичной медико-санитарной помощи: когортное исследование с использованием электронных медицинских карт в Великобритании. BMJ Open 2020;10:e036975.doi:10.1136/bmjopen-2020-036975 пмид: http://www.ncbi.nlm.nih.gov/pubmed/32114481
- ↵
- Смит см ,
- Уильямс Х ,
- Джасс А , и другие
.
 Назначение антибиотиков в домах престарелых в Великобритании, 2016–2017 гг.: ретроспективное когортное исследование связанных данных. BMC Health Serv Res 2020;20.doi:10.1186/s12913-020-05422-z
Назначение антибиотиков в домах престарелых в Великобритании, 2016–2017 гг.: ретроспективное когортное исследование связанных данных. BMC Health Serv Res 2020;20.doi:10.1186/s12913-020-05422-z - ↵
- Солнце Х ,
- Гуллифорд МЦ
. Сокращение назначения антибиотиков в учреждениях первичной медико-санитарной помощи в Англии с 2014 по 2017 год: популяционное когортное исследование. BMJ Open 2019;9:e023989.doi:10.1136/bmjopen-2018-023989 пмид: http://www.ncbi.nlm.nih.gov/pubmed/31289049
- ↵
- Дэвис Дж. Э. ,
- Тейлор Д.Г.
. Индивидуализация или стандартизация: тенденции в продолжительности рецептов национальных служб здравоохранения в Англии, 1998–2009 гг. Prim Health Care Res Dev 2013;14:164–74.doi:10.1017/S146342361200045X пмид: http://www.
 ncbi.nlm.nih.gov/pubmed/23031628
ncbi.nlm.nih.gov/pubmed/23031628 - ↵
- Петти ДР ,
- Зерманский А.Г. ,
- Олдред ДП
. Масштаб повторного назначения – время обновления. BMC Health Serv Res 2014; 14:1–4.doi:10.1186/1472-6963-14-76
- ↵
- ван Стаа ТП ,
- Палин В. ,
- Ли Ю , и другие
. Эффективность частого использования антибиотиков в снижении риска госпитализаций в связи с инфекцией: результаты двух крупных популяционных когорт. BMC Med 2020;18:40.doi:10.1186/s12916-020-1504-5 пмид: http://www.ncbi.nlm.nih.gov/pubmed/32114981
- ↵
- Борек А.Дж. ,
- Мейтленд К. ,
- Маклеод М , и другие
. Влияние пандемии COVID-19 на назначение антибиотиков и управление ими в сообществе: качественное интервью с врачами общей практики в Англии.
 Антибиотики 2021;10:1531.doi:10.3390/антибиотики10121531
пмид: http://www.ncbi.nlm.nih.gov/pubmed/34943743
Антибиотики 2021;10:1531.doi:10.3390/антибиотики10121531
пмид: http://www.ncbi.nlm.nih.gov/pubmed/34943743 - ↵
- Таррант С ,
- Кроков Э.М.
. Злоупотребление антибиотиками: управление неопределенностью и смягчение последствий чрезмерного лечения. BMJ Qual Saf 2022;31:163–7.doi:10.1136/bmjqs-2021-013615 пмид: http://www.ncbi.nlm.nih.gov/pubmed/34285113
- ↵
- Сури Джи ,
- Шеппес Г. ,
- Шварц С , и другие
. Инерция пациента и предвзятость статус-кво: когда предпочтение отдается худшему варианту. Psychol Sci 2013;24:1763–9.doi:10.1177/0956797613479976 пмид: http://www.ncbi.nlm.nih.gov/pubmed/23873580
- ↵
- Кроков Э.М. ,
- Колман AM ,
- Чатто-Браун E , и другие
.
 Уравновешивание рисков для человека и общества: систематический обзор и обобщение качественных исследований поведения при назначении антибиотиков в больницах. J Hosp Infect 2019;101:428–39.doi:10.1016/j.jhin.2018.08.007
пмид: http://www.ncbi.nlm.nih.gov/pubmed/30099092
Уравновешивание рисков для человека и общества: систематический обзор и обобщение качественных исследований поведения при назначении антибиотиков в больницах. J Hosp Infect 2019;101:428–39.doi:10.1016/j.jhin.2018.08.007
пмид: http://www.ncbi.nlm.nih.gov/pubmed/30099092 - ↵
- Таррант С ,
- Колман AM ,
- Дженкинс Д.Р. , и другие
. Причины чрезмерного использования антибиотиков широкого спектра действия в различных больницах. Качественное исследование врачей, назначающих лекарства, в Великобритании, Шри-Ланке и Южной Африке. Антибиотики 2021;10:94.doi:10.3390/антибиотики10010094 пмид: http://www.ncbi.nlm.nih.gov/pubmed/33477994
- ↵
- Чарани Э. ,
- Кастро-Санчес Э. ,
- Севдалис Н , и другие
. Понимание детерминант назначения противомикробных препаратов в больницах: роль «этикета назначения».
 Clin Infect Dis 2013;57:188–96.doi:10.1093/cid/cit212
пмид: http://www.ncbi.nlm.nih.gov/pubmed/23572483
Clin Infect Dis 2013;57:188–96.doi:10.1093/cid/cit212
пмид: http://www.ncbi.nlm.nih.gov/pubmed/23572483 - ↵
- Март А
. Перспектива: последовательность, преемственность и координация — 3C непрерывного ухода за пациентами. качество имеет значение. Архив 2006 г. Доступно: https://www.commonwealthfund.org/publications/newsletter-article/perspective-consistency-continuity-and-coordinate-3cs-seamless [Доступ 2922 марта].
- ↵
- Ливорси Д ,
- Угол А ,
- Матиас М.С. , и другие
. Факторы, влияющие на решения о назначении антибиотиков врачами стационара: качественное исследование. Infect Control Hosp Epidemiol 2015;36:1065–72.doi:10.1017/ice.2015.136 пмид: http://www.ncbi.nlm.nih.gov/pubmed/26078017
- ↵
- Ньюби Д.А.
 ,
, - Робертсон Дж.
. Компьютеризированное назначение: оценка влияния на повторные назначения и замену некоторых широко используемых антибиотиков. Med J Aust 2010;192:192–5.doi:10.5694/j.1326-5377.2010.tb03477.x пмид: http://www.ncbi.nlm.nih.gov/pubmed/20170455
- Ньюби Д.А.
- ↵
Обучение в RCGP. Центр набора инструментов для целевых антибиотиков. Доступно: https://elearning.rcgp.org.uk/course/view.php?id=553?gclid=CjwKCAjwuYWSBhByEiwAKd_n_uRLVj2ByLk7qtuK0w_3FhsiVvs5WDJFcOr8AhJ9dD9YuUHvGoTxvBoCfAgQAvD_BwE [Проверено 28 марта 22].
- ↵
- NHS
. Сетевой контракт направлен на расширенное обслуживание – структурированные обзоры лекарств и оптимизация лекарств: руководство. Национальная служба здравоохранения, 2020 г. Доступно: https://www.england.nhs.uk/wp-content/uploads/2020/09/SMR-Spec-Guidance-2020-21-FINAL-.pdf [Проверено 29 марта 22] .

- ↵
- Хейхо Б. ,
- Сеспедес Дж.А. ,
- Фоли К. , и другие
. Влияние интеграции фармацевтов в бригады первичной медико-санитарной помощи на показатели систем здравоохранения: систематический обзор. Br J Gen Pract 2019;69:e665–74.doi:10.3399/bjgp19X705461 пмид: http://www.ncbi.nlm.nih.gov/pubmed/31455642
- ↵
- Эшворт М ,
- Белый П ,
- Йонгсма Х , и другие
. Назначение антибиотиков и удовлетворенность пациентов в первичной медико-санитарной помощи в Англии: перекрестный анализ данных национального опроса пациентов и данных о назначении. Br J Gen Pract 2016;66:e40–6.doi:10.3399/bjgp15X688105 пмид: http://www.ncbi.nlm.nih.gov/pubmed/26639947
- ↵
- Ху Дж ,
- Ван З
.
 Использование антибиотиков без рецепта и использование услуг врачей общей практики среди китайских мигрантов в Австралии. Aust J Prim Health 2016; 22:434–9.doi:10.1071/PY15076
пмид: http://www.ncbi.nlm.nih.gov/pubmed/26328599
Использование антибиотиков без рецепта и использование услуг врачей общей практики среди китайских мигрантов в Австралии. Aust J Prim Health 2016; 22:434–9.doi:10.1071/PY15076
пмид: http://www.ncbi.nlm.nih.gov/pubmed/26328599 - ↵
- УХСА
. Хранитель антибиотиков: станьте хранителем антибиотиков. Агентство по безопасности здравоохранения Великобритании, 2022 г. Доступно: https://antibioticguardian.com/, по состоянию на 05.04.22.
- ↵
- Норрис П. ,
- Хорсбург С ,
- Киоун С , и другие
. Слишком много и слишком мало? распространенность и степень использования антибиотиков в регионе Новой Зеландии. J Antimicrob Chemother 2011;66:1921–6.doi:10.1093/jac/dkr194 пмид: http://www.ncbi.nlm.nih.gov/pubmed/21622675
Сноски
Твиттер @EM_Krockow, @E_J_Harvey, @DrDianeAshiru
Авторы DA-O и EMK разработали документ.

