Обструкция у детей | Чайка
Бронхиальная обструкция — это затруднение дыхания с удлиненным выдохом и свистящими хрипами. Бронхообструкция — это не самостоятельное заболевание, а симптом, который может возникать при разных состояниях. Наиболее частые причины обструкции — обструктивный бронхит, бронхиальная астма, реже обструкция возникает при гастроэзофагеальном рефлюксе, инородном теле бронхов, муковисцидозе и других заболеваниях.
Исследования показывают, что к возрасту трех лет каждый третий ребенок перенес хотя бы одну бронхообструкцию. Чаще всего, к возрасту 13–14 лет, дети перерастают это состояние.
В основе развития бронхообструктивного синдрома лежит несколько механизмов:
- спазм гладких мышц в стенке бронха;
- отек стенки бронха;
- выделение вязкой слизи в просвет бронха (мокроты).
В результате происходит сужение просвета дыхательных путей, что проявляется затруднением дыхания, одышкой, тяжелым малопродуктивным кашлем, иногда свистящими хрипами.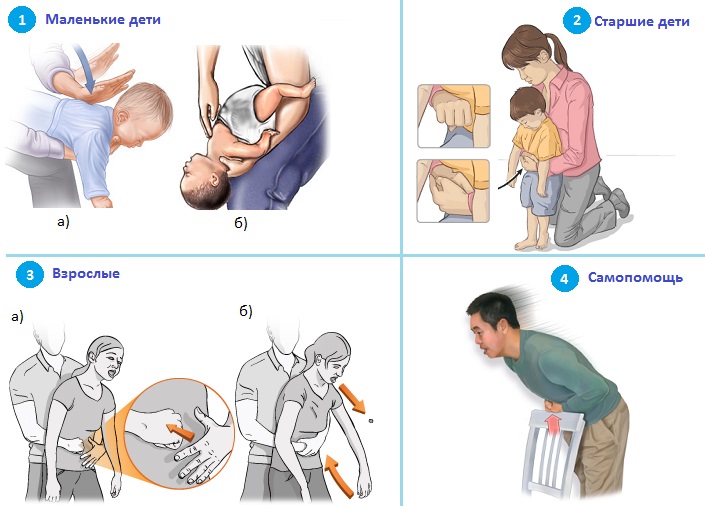
Триггеры для развития бронхообструкции можно разделить на две основные группы:
- Вирусные инфекции. Обострения случаются на фоне ОРВИ, у ребенка могут также присутствовать такие симптомы — насморк, кашель, повышение температуры.
- Мультитриггерные обструкции. Факторами провокации может быть вдыхание табачного дыма, резких запахов, физическая нагрузка. Симптомов ОРВИ при этом может не быть.
Необходимо обратиться к врачу, если при очередной вирусной инфекции у ребенка появились такие симптомы:
- упорный навязчивый кашель;
- затруднение дыхания;
- увеличение частоты дыхания;
- свистящие хрипы.
На приеме доктор сможет оценить степень выраженности бронхиальной обструкции и предложить соответствующую терапию. Как правило, она включает ингаляции специальными лекарственными препаратами — бронхолитиками.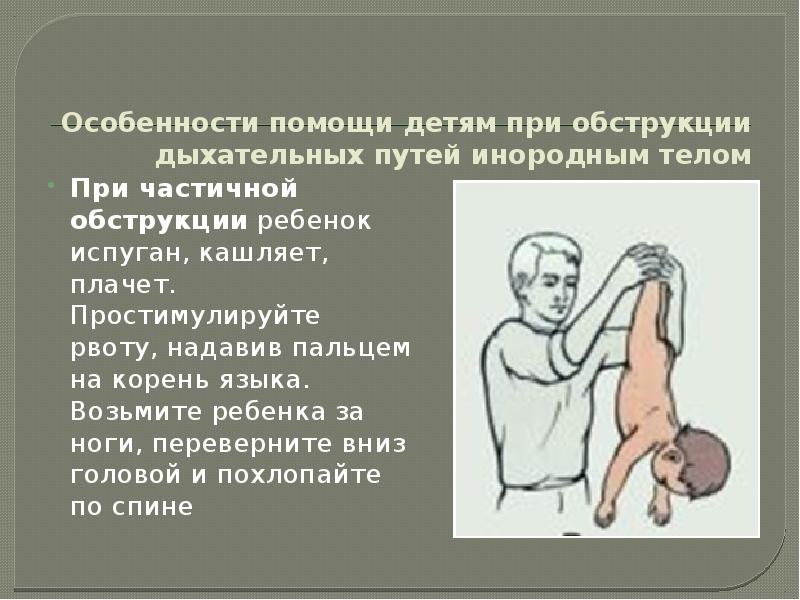
Большинство бронхообструкций можно лечить дома — для этого нужен компрессорный небулайзер. Однако в случае тяжелых форм может потребоваться госпитализация и более серьезная терапия — введение глюкокортикостероидов (гормонов) и подача кислорода.
Распространенные заблуждения о бронхообструкции
1. Это астма?
Вовсе не обязательно. Действительно, рецидивирующие бронхообструкции — сигнал о возможном развитии бронхиальной астмы, и доктор обязательно обратит на это внимание, чтобы не пропустить момент для назначения дополнительных тестов. Однако частота вирус-индуцированных обструкций снижается с возрастом, и у большинства детей проходит по достижении 13–14 лет.
2. Может, не долечили и пора принимать антибиотики?
Нет. Антибиотик действует лишь на бактериальную инфекцию. Если ее нет, то нет смысла в применении антибиотика. Не нужно впустую давать ребенку серьезное лекарство.
3. Может, проблемы с иммунитетом и нужны иммуномодуляторы?
Нет. Доказательной медицине неизвестны никакие полезные эффекты этой группы препаратов. Это потраченное впустую время и деньги, и к тому же — риск развития аллергических реакций.
Это потраченное впустую время и деньги, и к тому же — риск развития аллергических реакций.
4. Помогут ли антигистаминные препараты?
Нет. Использование противоаллергических препаратов не помогает справиться с обструктивным бронхитом.
5. Может ли помочь физиотерапия?
Нет данных об эффективности физиопроцедур при лечении обструктивного бронхита.
Следует понимать, что те побочные эффекты от приема глюкокортикостероидов, которых обычно опасаются родители (синдром Кушинга или ожирение, привыкание, хрупкость костей, раннее половое созревание), связаны с длительным приемом системных глюкокортикостероидов, которые тем или иным образом (при приеме внутрь, уколах в мышцу или вену) попадают в кровеносную систему организма. Ингаляционные препараты, которые могут назначить при определенном течении и частоте возникновения бронхообструкций, действуют местно. Они попадают в легкие, а процент попадания препаратов в кровеносную систему ничтожно мал и не может вызвать этих побочных эффектов.
7. Что делать, если бронхообструкции продолжают возникать?
При определенной частоте возникновения обструктивных бронхитов доктор может направить пациента к пульмонологу (врачу, занимающемуся заболеваниями дыхательной системы). Пульмонолог может предложить дополнительное исследование – функции внешнего дыхания. На основании его вместе с оценкой частоты и степени выраженности эпизодов бронхообструкции врач может проверить диагноз бронхиальная астма и принять решение о назначении ингаляционных кортикостероидов на длительный срок. Иногда, если пациент в силу возраста или индивидуальных особенностей не может выполнить это исследование правильно, эти препараты назначаются эмпирически — пробно, с оценкой эффективности на срок от одного до трех месяцев.
Своевременное обращение к врачу позволит правильно поставить диагноз и подобрать подходящую терапию.
Терапия острого обструктивного синдрома у детей с острыми респираторными заболеваниями | #11/13
Несмотря на современные достижения медицины, в ХХI веке распространенность инфекций не только не снижается, а все больше возрастает. Длительное время первое место в структуре инфекционной заболеваемости у детей занимают острые респираторные заболевания (ОРЗ) [1, 2]. Согласно данным государственного отчета Роспотребнадзора, в России заболеваемость ОРЗ у детей за 2012 год составила более 28 млн (28 423 135), или 19 896,3 случая на 100 тыс. детей [3]. Такая высокая распространенность ОРЗ в детском возрасте обусловлена как контагиозностью инфекционного фактора, так и анатомо-физиологическими особенностями детского организма. Значительное место в этиологической структуре ОРЗ отводится вирусным инфекциям. За последние десятилетия идентифицированы новые вирусы, определяющие тяжелое течение ОРЗ с обструкцией дыхательных путей, особенно у детей первых лет жизни. Особое внимание уделяется роли метапневмовируса, короновируса, бокавируса, риновируса, реассортантам вируса гриппа, респираторно-синцитиальному вирусу в развитии обструктивного синдрома дыхательных путей. Их роль в развитии острого обструктивного синдрома дыхательных путей (ООСДП) у детей неоспорима, вместе с этим существуют данные, свидетельствующие о возможной их роли в развитии бронхиальной астмы (БА) у генетически предрасположенных лиц [1, 4].
Длительное время первое место в структуре инфекционной заболеваемости у детей занимают острые респираторные заболевания (ОРЗ) [1, 2]. Согласно данным государственного отчета Роспотребнадзора, в России заболеваемость ОРЗ у детей за 2012 год составила более 28 млн (28 423 135), или 19 896,3 случая на 100 тыс. детей [3]. Такая высокая распространенность ОРЗ в детском возрасте обусловлена как контагиозностью инфекционного фактора, так и анатомо-физиологическими особенностями детского организма. Значительное место в этиологической структуре ОРЗ отводится вирусным инфекциям. За последние десятилетия идентифицированы новые вирусы, определяющие тяжелое течение ОРЗ с обструкцией дыхательных путей, особенно у детей первых лет жизни. Особое внимание уделяется роли метапневмовируса, короновируса, бокавируса, риновируса, реассортантам вируса гриппа, респираторно-синцитиальному вирусу в развитии обструктивного синдрома дыхательных путей. Их роль в развитии острого обструктивного синдрома дыхательных путей (ООСДП) у детей неоспорима, вместе с этим существуют данные, свидетельствующие о возможной их роли в развитии бронхиальной астмы (БА) у генетически предрасположенных лиц [1, 4].
Острые обструктивные состояния дыхательных путей у детей встречаются достаточно часто и иногда протекают тяжело, сопровождаясь признаками дыхательной недостаточности. Самыми распространенными из них является острый стенозирующий ларинготрахеит (круп), обусловленный воспалением слизистой и подслизистого пространства гортани и трахеи, с вовлечением в процесс тканей и структур подсвязочного пространства и развитием стеноза гортани. Также достаточно часто причиной острых обструктивных состояний дыхательных путей на фоне острой респираторной вирусной инфекции (ОРВИ) у детей являются острый обструктивный бронхит, бронхиолит и БА [5].
Под термином «круп» понимают клинический синдром, сопровождающийся хриплым или сиплым голосом, грубым «лающим» кашлем и затрудненным (стенотическим) дыханием. В отечественной литературе это заболевание описывается под названием «стенозирующий ларинготрахеит», в Международной классификации болезней 10-го пересмотра (МКБ-10) — «острый обструктивный ларингит».
Бронхообструктивный синдром — это симптомокомплекс функционального или органического происхождения, клинические проявления которого складываются из удлиненного выдоха, свистящего, шумного дыхания, приступов удушья, кашля и др. Термины «бронхообструктивный синдром» и «круп» не могут быть использованы как самостоятельный диагноз.
Распространенность обструктивных состояний дыхательных путей на фоне ОРВИ достаточно высока, особенно у детей первых 6 лет жизни. Это связано с анатомо-физиологическими особенностями респираторного тракта у детей раннего возраста. Так, частота развития бронхиальной обструкции на фоне острых респираторных заболеваний у детей первых лет жизни составляет, по данным разных авторов, от 5% до 50%. Наиболее часто обструктивные состояния отмечаются у детей с отягощенным семейным анамнезом по аллергии.
Проведенный нами анализ распространенности обструктивного синдрома у детей с ОРЗ, являющегося причиной госпитализации в отделение респираторных инфекций детской городской клинической больницы Святого Владимира г. Москвы, свидетельствует об увеличении в последние годы пациентов с обструктивным синдромом дыхательных путей. Согласно нашим данным, в 2011 г. в респираторное отделение поступило 1348, из них 408 детей — с достаточно тяжелым течением ООСДП на фоне ОРЗ. В последующие годы мы наблюдаем увеличение роли ООСДП, определяющего тяжесть ОРЗ, так, в 2012 г. количество госпитализаций достигло 1636, а детей с ООСДП увеличилось до 669. Следует отметить, что в 90% случаев возраст детей с ООСДП был менее 5 лет. Был проведен анализ причин недостаточной эффективности терапии обструктивных состояний у детей на догоспитальном этапе. Установлено, что основными среди них являются неадекватная оценка тяжести ООСДП и соответственно отсутствие своевременной и рациональной терапии ООСДП, позднее назначение противовоспалительной терапии, отсутствие контроля за техникой выполнения ингаляции.
количество госпитализаций достигло 1636, а детей с ООСДП увеличилось до 669. Следует отметить, что в 90% случаев возраст детей с ООСДП был менее 5 лет. Был проведен анализ причин недостаточной эффективности терапии обструктивных состояний у детей на догоспитальном этапе. Установлено, что основными среди них являются неадекватная оценка тяжести ООСДП и соответственно отсутствие своевременной и рациональной терапии ООСДП, позднее назначение противовоспалительной терапии, отсутствие контроля за техникой выполнения ингаляции.
Высокая частота возникновения ООСДП у детей обусловлена как особенностями инфекционного фактора в современном мире, так и анатомо-физиологическими особенности детского организма. Известно, что иммунная система детей первых лет жизни отличается незрелостью и недостаточными резервными возможностями. Так, ответ врожденной иммунной системы детей первых лет жизни отличается ограниченной секрецией интерферонов (ИФН), недостаточной активностью комплемента, снижением клеточной цитотоксичности. Особенности адаптивного иммунитета в этой возрастной группе пациентов обусловлены Th3-направленностью иммунного ответа, что нередко способствует развитию аллергических реакций, незрелостью гуморального звена иммунного ответа со снижением уровня секреторного иммуноглобулина (Ig) А на слизистых, преимущественной выработкой IgМ на инфекционные патогены. Незрелость иммунного ответа способствует частым ОРЗ и нередко определяет тяжесть их течения [1].
Особенности адаптивного иммунитета в этой возрастной группе пациентов обусловлены Th3-направленностью иммунного ответа, что нередко способствует развитию аллергических реакций, незрелостью гуморального звена иммунного ответа со снижением уровня секреторного иммуноглобулина (Ig) А на слизистых, преимущественной выработкой IgМ на инфекционные патогены. Незрелость иммунного ответа способствует частым ОРЗ и нередко определяет тяжесть их течения [1].
Часто развитие ООСДП у детей первых лет жизни обусловлено анатомо-физиологическими особенностями строения дыхательных путей этой возрастной группы пациентов. Среди них особенно важными являются наличие гиперплазии железистой ткани, секреция преимущественно вязкой мокроты, относительная узость дыхательных путей, меньший объем гладких мышц, низкая коллатеральная вентиляция, особенности строения гортани. Развитие крупа у детей с ОРВИ обусловлено малыми абсолютными размерами гортани, мягкостью хрящевого скелета, рыхлым и вытянутым надгортанником. Все это создает особые предпосылки для компонентов стеноза: спазма и отека. Кроме того, в связи с тем, что пластинки щитовидного хряща у детей сходятся под прямым углом (у взрослых он острый), голосовые связки (складки) становятся непропорционально короткими, и до 7 лет глубина гортани превышает ее ширину. Чем меньше ребенок, тем больше относительная площадь, занимаемая рыхлой соединительной тканью в подскладочном пространстве, что увеличивает объем отека слизистой гортани. У детей первых трех лет жизни гортань, трахея и бронхи имеют относительно меньший диаметр, чем у взрослых. Узость всех отделов дыхательного аппарата значительно увеличивает аэродинамическое сопротивление. Для детей раннего возраста характерны недостаточная ригидность костной структуры грудной клетки, свободно реагирующей втяжением уступчивых мест на повышение сопротивления в воздухоносных путях, а также особенности положения и строения диафрагмы. Недостаточна и дифференцировка нервного аппарата вследствие того, что слиты 1-я и 2-я рефлексогенные зоны на всем их протяжении и не оформлена 3-я рефлексогенная зона, рецепторы которой обильно разветвляются на всей слизистой подскладочного пространства, что способствует возникновению длительного спазма голосовой щели и стенозу гортани.
Все это создает особые предпосылки для компонентов стеноза: спазма и отека. Кроме того, в связи с тем, что пластинки щитовидного хряща у детей сходятся под прямым углом (у взрослых он острый), голосовые связки (складки) становятся непропорционально короткими, и до 7 лет глубина гортани превышает ее ширину. Чем меньше ребенок, тем больше относительная площадь, занимаемая рыхлой соединительной тканью в подскладочном пространстве, что увеличивает объем отека слизистой гортани. У детей первых трех лет жизни гортань, трахея и бронхи имеют относительно меньший диаметр, чем у взрослых. Узость всех отделов дыхательного аппарата значительно увеличивает аэродинамическое сопротивление. Для детей раннего возраста характерны недостаточная ригидность костной структуры грудной клетки, свободно реагирующей втяжением уступчивых мест на повышение сопротивления в воздухоносных путях, а также особенности положения и строения диафрагмы. Недостаточна и дифференцировка нервного аппарата вследствие того, что слиты 1-я и 2-я рефлексогенные зоны на всем их протяжении и не оформлена 3-я рефлексогенная зона, рецепторы которой обильно разветвляются на всей слизистой подскладочного пространства, что способствует возникновению длительного спазма голосовой щели и стенозу гортани. Именно эти особенности способствуют частому развитию и рецидивам обструкции дыхательных путей у детей первых лет жизни, особенно на фоне ОРЗ [1, 5, 8].
Именно эти особенности способствуют частому развитию и рецидивам обструкции дыхательных путей у детей первых лет жизни, особенно на фоне ОРЗ [1, 5, 8].
Прогноз течения ООСДП может быть довольно серьезен и зависит от формы заболевания, ставшего причиной развития обструкции, и своевременного проведения патогенетически обусловленных схем терапии и профилактики.
Основными направлениями терапии ООСДП у детей являются собственно лечение респираторной инфекции и лечение обструкции дыхательных путей.
Согласно современным данным в механизме развития ООСДП основное место отводят воспалению. Развитие воспаления слизистой оболочки верхних и нижних дыхательных путей способствует гиперсекреции вязкой слизи, формированию отека слизистой оболочки респираторного тракта, нарушению мукоцилиарного транспорта и развитию обструкции. Соответственно, основным направлениям терапии ООСДП является противовоспалительная терапия [9–11].
Воспаление является важным фактором бронхиальной обструкции детей раннего возраста и может быть вызвано различными факторами. В результате их воздействия запускается каскад иммунологических реакций, способствующих выходу в периферический кровоток медиаторов 1-го и 2-го типов. Именно с этими медиаторами (гистамином, лейкотриенами, простагландинами) связаны основные патогенетические механизмы обструктивного синдрома — усиление проницаемости сосудов, появление отека слизистой оболочки бронхов, гиперсекреции вязкой слизи, развитие бронхоспазма.
В результате их воздействия запускается каскад иммунологических реакций, способствующих выходу в периферический кровоток медиаторов 1-го и 2-го типов. Именно с этими медиаторами (гистамином, лейкотриенами, простагландинами) связаны основные патогенетические механизмы обструктивного синдрома — усиление проницаемости сосудов, появление отека слизистой оболочки бронхов, гиперсекреции вязкой слизи, развитие бронхоспазма.
У детей первых лет жизни именно отек и гиперплазия слизистой оболочки дыхательных путей являются основной причиной обструкции дыхательных путей на разном уровне. Развитые лимфатическая и кровеносная системы респираторного тракта ребенка обеспечивают ему многие физиологические функции. Однако в условиях патологии характерным для отека является утолщение всех слоев бронхиальной стенки (подслизистого и слизистого слоя, базальной мембраны), что ведет к нарушению проходимости дыхательных путей. При рецидивирующих бронхолегочных заболеваниях нарушается структура эпителия, отмечается его гиперплазия и плоскоклеточная метаплазия.
Другим не менее важным механизмом ООСДП у детей первых лет жизни является нарушение бронхиальной секреции, которое развивается при любом неблагоприятном воздействии на органы дыхания и в большинстве случаев сопровождается увеличением количества секрета и повышением его вязкости. Функция слизистых и серозных желез регулируется парасимпатической нервной системой, ацетилхолин стимулирует их деятельность. Такая реакция изначально носит защитный характер. Однако застой бронхиального содержимого приводит к нарушению вентиляционно-респираторной функции легких. Продуцируемый густой и вязкий секрет, помимо угнетения цилиарной активности, может вызвать бронхиальную обструкцию вследствие скопления слизи в дыхательных путях. В тяжелых случаях вентиляционные нарушения сопровождаются развитием ателектазов.
Немалая роль в развитии бронхообструктивного синдрома (БОС) отводится гиперреактивности бронхов. Гиперреактивность бронхов — это повышение чувствительности и реактивности бронхов к специфическим и неспецифическим раздражителям.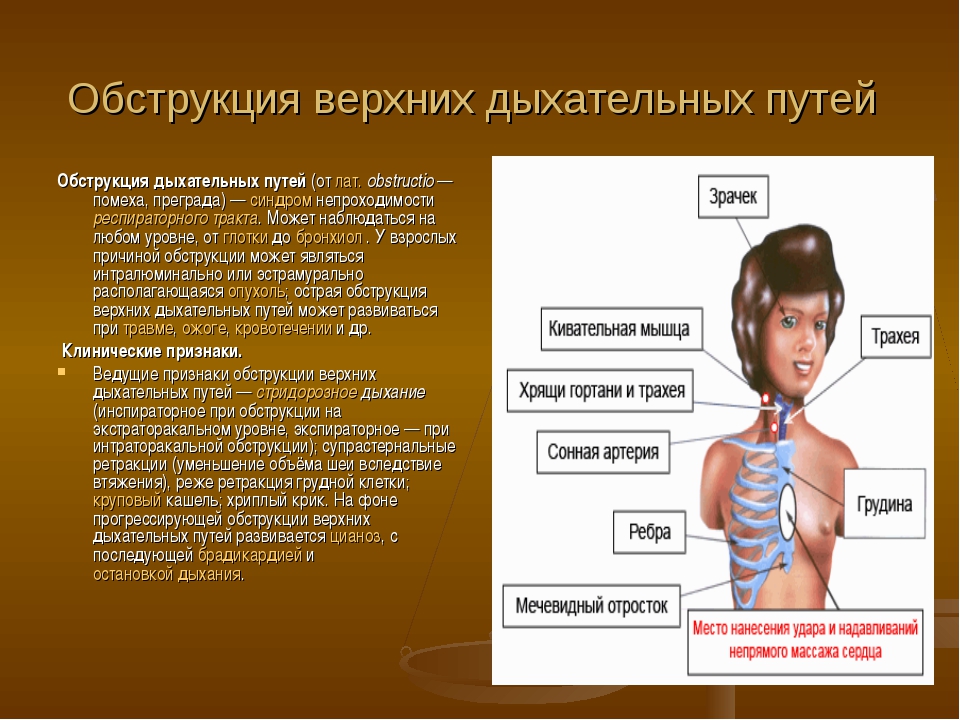 Причиной гиперреактивности бронхов является нарушение равновесия между возбуждающими (холинергическая, нехолинергическая и α-адренергическая системы) и ингибирующими (β-адренергическая система) влияниями на тонус бронхов. Известно, что стимуляция β2-адренорецепторов катехоламинами, также как повышение концентрации цАМФ и простагландинов Е2, уменьшает проявления бронхоспазма. Согласно классической теории A. Szentivanyi (1968 г.) у больных с гиперреактивностью бронхов имеется дефект в биохимической структуре β2-рецепторов, сводящийся к недостаточности аденилатциклазы. У этих пациентов снижено число β-рецепторов на лимфоцитах, имеется дисбаланс адренорецепторов в сторону гиперчувствительности α-адренорецепторов, что предрасполагает к спазму гладких мышц, отеку слизистой оболочки, инфильтрации и гиперсекреции. Наследственно обусловленная блокада аденилатциклазы снижает чувствительность β2-адренорецепторов к адреномиметикам, что достаточно часто встречается у больных БА.
Причиной гиперреактивности бронхов является нарушение равновесия между возбуждающими (холинергическая, нехолинергическая и α-адренергическая системы) и ингибирующими (β-адренергическая система) влияниями на тонус бронхов. Известно, что стимуляция β2-адренорецепторов катехоламинами, также как повышение концентрации цАМФ и простагландинов Е2, уменьшает проявления бронхоспазма. Согласно классической теории A. Szentivanyi (1968 г.) у больных с гиперреактивностью бронхов имеется дефект в биохимической структуре β2-рецепторов, сводящийся к недостаточности аденилатциклазы. У этих пациентов снижено число β-рецепторов на лимфоцитах, имеется дисбаланс адренорецепторов в сторону гиперчувствительности α-адренорецепторов, что предрасполагает к спазму гладких мышц, отеку слизистой оболочки, инфильтрации и гиперсекреции. Наследственно обусловленная блокада аденилатциклазы снижает чувствительность β2-адренорецепторов к адреномиметикам, что достаточно часто встречается у больных БА. В то же время некоторые исследователи указывают на функциональную незрелость β2-адренорецепторов у детей первых месяцев жизни.
В то же время некоторые исследователи указывают на функциональную незрелость β2-адренорецепторов у детей первых месяцев жизни.
Установлено, что у детей раннего возраста достаточно хорошо развиты М-холинорецепторы, что, с одной стороны, определяет особенности течения бронхообструктивных заболеваний у этой группы пациентов (склонность к развитию обструкции, продукция очень вязкого бронхиального секрета), с другой стороны, объясняет выраженный бронхолитический эффект М-холинолитиков у них.
Таким образом, анатомо-физиологические особенности детей раннего возраста определяет как высокую распространенность ООСДП у детей первых лет жизни, так и механизмы его развития с соответствующей клинической картиной «влажной астмы».
Терапия ООСДП должна быть начата непосредственно после выявления симптомов у постели больного. Необходимо безотлагательно начинать неотложную терапию и одновременно выяснять причины бронхообструкции.
Основные направления неотложной терапии ООСДП включают в себя мероприятия по бронхолитической, противовоспалительной терапии, улучшению дренажной функции бронхов и восстановлению адекватного мукоцилиарного клиренса. Тяжелое течение приступа бронхообструкции требует проведения оксигенации вдыхаемого воздуха, а иногда искусственной вентиляции легких.
Тяжелое течение приступа бронхообструкции требует проведения оксигенации вдыхаемого воздуха, а иногда искусственной вентиляции легких.
Проведение неотложной терапии ООСДП у детей должно проводиться с учетом патогенеза формирования обструкции в различные возрастные периоды. В генезе БОС у детей раннего возраста преобладают воспалительный отек и гиперсекреция вязкой слизи, а бронхоспазм выражен незначительно. С возрастом увеличивается гиперреактивность бронхов и вместе с этим возрастает роль бронхоспазма.
Основными направлениями терапии острых обструктивных состояний верхних и нижних дыхательных путей у детей с ОРЗ являются лечение самой респираторной инфекции и лечение обструкции дыхательных путей [12]. Безусловно, лечение ОРЗ должно быть комплексным и индивидуальным в каждом конкретном случае.
Этиотропная терапия наиболее частых вирусных инфекций в настоящее время является затруднительной в силу узости спектра действия противовирусных препаратов, возрастного ограничения их применения у детей в первые годы жизни, недостаточности доказательной базы эффективности данной группы препаратов. В настоящее время активно используются в терапии ОРЗ вирусной этиологии препараты рекомбинантного интерферона и препараты, стимулирующие синтез эндогенного интерферона. Назначение антибактериальных препаратов показано в случае длительной лихорадки (более 3–4 суток), и/или наличии признаков дыхательной недостаточности при отсутствии БОС, и/или при подозрении на пневмонию, и/или выраженных изменений в клиническом анализе крови.
В настоящее время активно используются в терапии ОРЗ вирусной этиологии препараты рекомбинантного интерферона и препараты, стимулирующие синтез эндогенного интерферона. Назначение антибактериальных препаратов показано в случае длительной лихорадки (более 3–4 суток), и/или наличии признаков дыхательной недостаточности при отсутствии БОС, и/или при подозрении на пневмонию, и/или выраженных изменений в клиническом анализе крови.
Современные стандарты терапии обструктивных состояний респираторного тракта определены в международных и национальных программных документах [5, 9, 13], согласно которым основными препаратами в терапии ООСДП являются бронхолитические препараты и препараты с противовоспалительным действием. В качестве эффективной противовоспалительной терапии рекомендуют широкое использование ингаляционных глюкокортикостероидов (ИГКС). ИГКС являются наиболее эффективным средством лечения острого стенозирующего ларинготрахеита, бронхиальной астмы и острого обструктивного бронхита. Механизм их лечебного действия связан с мощным противовоспалительным эффектом. Противовоспалительный эффект ИГКС связан с ингибирующим действием на клетки воспаления и их медиаторы, включая продукцию цитокинов (интерлейкинов), провоспалительных медиаторов и их взаимодействия с клетками-мишенями. ИГКС оказывают влияние на все фазы воспаления, независимо от его природы, при этом ключевой клеточной мишенью могут являться эпителиальные клетки дыхательных путей. ИГКС прямо или косвенно регулируют транскрипцию генов клеток-мишеней. Они увеличивают синтез противовоспалительных белков (липокортина-1) или снижают синтез провоспалительных цитокинов — интерлейкинов, фактора некроза опухолей и др. При длительной терапии ИГКС у больных с бронхиальной астмой значительно снижается количество тучных клеток и эозинофилов на слизистых дыхательных путей, происходит стабилизация клеточных мембран, мембран лизосом и уменьшается проницаемость сосудов.
Механизм их лечебного действия связан с мощным противовоспалительным эффектом. Противовоспалительный эффект ИГКС связан с ингибирующим действием на клетки воспаления и их медиаторы, включая продукцию цитокинов (интерлейкинов), провоспалительных медиаторов и их взаимодействия с клетками-мишенями. ИГКС оказывают влияние на все фазы воспаления, независимо от его природы, при этом ключевой клеточной мишенью могут являться эпителиальные клетки дыхательных путей. ИГКС прямо или косвенно регулируют транскрипцию генов клеток-мишеней. Они увеличивают синтез противовоспалительных белков (липокортина-1) или снижают синтез провоспалительных цитокинов — интерлейкинов, фактора некроза опухолей и др. При длительной терапии ИГКС у больных с бронхиальной астмой значительно снижается количество тучных клеток и эозинофилов на слизистых дыхательных путей, происходит стабилизация клеточных мембран, мембран лизосом и уменьшается проницаемость сосудов.
Помимо уменьшения воспалительного отека слизистой оболочки и гиперреактивности бронхов ИГКС улучшают функцию β2-адренорецепторов как путем синтеза новых рецепторов, так и повышая их чувствительность. Поэтому ИГКС потенцируют эффекты β2-агонистов.
Поэтому ИГКС потенцируют эффекты β2-агонистов.
Ингаляционное применение ГКС создает высокие концентрации препаратов в дыхательных путях, что обеспечивает максимально выраженный местный противовоспалительный эффект и минимальные проявления системных (нежелательных) эффектов.
Однако эффективность и безопасность ИГКС в терапии ООСДП у детей во многом определяется способом доставки их непосредственно в дыхательные пути и техникой выполнения ингаляции [14, 16]. В качестве средств доставки в настоящее время имеются дозирующие аэрозольные ингаляторы (ДАИ), ДАИ со спейсером и лицевой маской (аэрочэмбер, бебихалер), ДАИ, активируемые вдохом пациента, порошковые ингаляторы и небулайзеры. В настоящее время признано, что оптимальной системой доставки лекарственных препаратов в дыхательные пути при ООСДП у детей раннего возраста является небулайзер. Его использование способствует наилучшей положительной динамике клинических данных, достаточному бронхорасширяющему эффекту периферических отделов бронхов, и техника его использования практически безошибочна. Основной целью небулайзерной терапии является доставка терапевтической дозы требуемого препарата в аэрозольной форме за короткий период времени, обычно за 5–10 мин. К ее преимуществам относятся: легко выполнимая техника ингаляции, возможность доставки более высокой дозы ингалируемого вещества и обеспечение проникновения его в плохо вентилируемые участки бронхов. У детей раннего возраста необходимо использовать маску соответствующего размера, с 3–4 лет лучше использовать мундштук, чем маску, т. к. применение маски снижает дозу ингалируемого вещества за счет его оседания в носоглотке.
Основной целью небулайзерной терапии является доставка терапевтической дозы требуемого препарата в аэрозольной форме за короткий период времени, обычно за 5–10 мин. К ее преимуществам относятся: легко выполнимая техника ингаляции, возможность доставки более высокой дозы ингалируемого вещества и обеспечение проникновения его в плохо вентилируемые участки бронхов. У детей раннего возраста необходимо использовать маску соответствующего размера, с 3–4 лет лучше использовать мундштук, чем маску, т. к. применение маски снижает дозу ингалируемого вещества за счет его оседания в носоглотке.
В настоящее время в практической деятельности врача могут быть использованы следующие ИГКС: беклометазон, будесонид, флутиказона пропионат, мометазона фуроат и циклесонид. Необходимо отметить возрастные аспекты назначения ИГКС у детей. Так, у детей с 6-месячного возраста разрешен к применению в ингаляциях через компрессорный небулайзер препарат суспензия будесонида, с 12 месяцев — флутиказона пропионат через спейсер, беклометазона пропионат разрешен для использования в детской практике с 4 лет, циклесонид с 6 лет, а мометазона фуроат с 12-летнего возраста.
Для проведения небулайзерной терапии используются только специально предназначенные для этих целей растворы лекарственных средств, разрешенные Фармакологическим комитетом РФ для небулайзеров. При этом даже маленькая частица раствора в аэрозоле сохраняет все лекарственные свойства вещества, сами растворы для небулайзерной терапии не вызывают повреждения слизистой бронха и альвеол, а упаковка в виде флаконов или небул позволяет удобно дозировать препараты как в стационарных, так и в домашних условиях.
Совсем недавно в нашей стране была зарегистрирована целая линейка препаратов, предназначенных для небулайзерной терапии, включающая ИГКС — будесонид (Буденит Стери-Неб) и 3 бронхолитика: сальбутамол (Саламол Стери-Неб), ипратропия бромид (Ипратропиум Стери-Неб) и комбинацию сальбутамол/ипратропия бромид (Ипрамол Стери-Неб).
Препарат Буденит Стери-Неб (будесонид) является генериком оригинального препарата будесонида Пульмикорт суспензия. Согласно определению Управления по надзору за качеством пищевых продуктов и лекарственных средств США (Food and Drugs Administration of the United States, FDA), генерик (дженерик) — это лекарственный препарат, сравнимый с оригинальным лекарственным препаратом по лекарственной форме, силе действия, способу назначения, качеству, фармакологическим свойствам и показаниям к назначению. Для препаратов-генериков, соответствующих этому определению, характерно: соответствие фармакопейным требованиям, производство в условиях GMP (Good Manufacturing Practice — надлежащая производственная практика), почти полное соответствие оригинальному продукту по составу (вспомогательные вещества могут быть иными) и производимым эффектам, отсутствие патентной защиты, более доступная цена, чем у оригинального препарата.
Для препаратов-генериков, соответствующих этому определению, характерно: соответствие фармакопейным требованиям, производство в условиях GMP (Good Manufacturing Practice — надлежащая производственная практика), почти полное соответствие оригинальному продукту по составу (вспомогательные вещества могут быть иными) и производимым эффектам, отсутствие патентной защиты, более доступная цена, чем у оригинального препарата.
Все вышеперечисленные характеристики можно отнести к Стери-Небам. Препараты в небулах созданы по передовой технологии 3-ступенчатого «горячего запечатывания, что позволяет достигать максимальной стерильности. В каждом Стери-Небе содержится одна доза лекарственного вещества, и препарат полностью готов к применению (не требует разведения), что исключает ошибки дозирования [15]. Пластиковые ампулы Стери-Неба легко открываются. Лекарственные препараты, находящиеся в Стери-Небах, не содержат бензалкония хлорида и прочих консервантов, что делает их более безопасными, а это очень важно при использовании, особенно в педиатрической практике.
Таким образом, основные принципы терапии бронхообструкции — противовоспалительное лечение и применение бронхолитиков. Именно ИГКС являются важной составляющей противовоспалительной терапии БОС. В настоящее время небулизированный будесонид при обострении БА рассматривается в качестве альтернативы системным глюкокортикостероидам [13]. Преимуществом будесонида при ингаляционном назначении является более быстрое действие ГКС (в течение 1–3 ч), максимальное улучшение бронхиальной проходимости через 3–6 часов, снижение гиперреактивности бронхов и гораздо более высокий профиль безопасности.
С учетом того факта, что в большинстве клинических исследований небулайзерной терапии будесонидом использовался оригинальный препарат Пульмикорт (суспензия), для оценки сопоставимости результатов этих исследований в отношении Буденита Стери-Неб было выполнено сравнение фармацевтической эквивалентности данных препаратов.
Прямое сравнение терапевтической эффективности и безопасности Буденита Стери-Неб (ТEVA, Израиль) и Пульмикорта (суспензии) (AstraZeneca, Великобритания) было проведено в многоцентровом рандомизированном плацебо-контролируемом исследовании в когорте детей (от 5 лет до 11 лет 8 мес), доставленных в отделения неотложной помощи в связи с обострением бронхиальной астмы (исследование III фазы в параллельных группах; 23 исследовательских центра набирали пациентов в 6 странах — Эстонии, Израиле, Латвии, Польше, Колумбии и Мексике). В исследование было включено 302 ребенка. Буденит Стери-Неб (0,5 мг/2 мл и 1 мг/2 мл) и Пульмикорт суспензия (0,5 мг/2 мл и 1 мг/2 мл) значимо не различались по компонентному составу, размеру частиц суспензии, распределению частиц генерируемого аэрозоля по размерам, количеству будесонида во вдыхаемой смеси. Таким образом, химико-фармакологические исследования Буденита Стери-Неб и оригинального препарата Пульмикорт выявили эквивалентность суспензии будесонида двух производителей по основным показателям, влияющим на терапевтический эффект ИГКС. Была продемонстрирована терапевтическая эквивалентность и схожий профиль безопасности Буденита Стери-Неб и оригинального препарата Пульмикорт (суспензия), что позволяет экстраполировать данные, полученные в исследованиях небулизированного будесонида [16].
В исследование было включено 302 ребенка. Буденит Стери-Неб (0,5 мг/2 мл и 1 мг/2 мл) и Пульмикорт суспензия (0,5 мг/2 мл и 1 мг/2 мл) значимо не различались по компонентному составу, размеру частиц суспензии, распределению частиц генерируемого аэрозоля по размерам, количеству будесонида во вдыхаемой смеси. Таким образом, химико-фармакологические исследования Буденита Стери-Неб и оригинального препарата Пульмикорт выявили эквивалентность суспензии будесонида двух производителей по основным показателям, влияющим на терапевтический эффект ИГКС. Была продемонстрирована терапевтическая эквивалентность и схожий профиль безопасности Буденита Стери-Неб и оригинального препарата Пульмикорт (суспензия), что позволяет экстраполировать данные, полученные в исследованиях небулизированного будесонида [16].
Таким образом, согласно международным и национальным рекомендациям, наиболее оптимальным, доступным и эффективным препаратом противовоспалительной терапии острого стенозирующего ларинготрахеита, бронхообструктивного синдрома у детей с 6 месяцев жизни является суспензия будесонида с ингаляционным использованием через небулайзер. Появление на фармацевтическом рынке качественных генериков в форме Стери-Небов, в том числе и будесонида (Буденит Стери-Неб), расширяет выбор врача-педиатра при терапии острого стенозирующего ларинготрахеита и бронхообструктивного синдрома у детей. Раннее назначение данного препарата при ООСДП является залогом благоприятного прогноза и предупреждения осложнений.
Появление на фармацевтическом рынке качественных генериков в форме Стери-Небов, в том числе и будесонида (Буденит Стери-Неб), расширяет выбор врача-педиатра при терапии острого стенозирующего ларинготрахеита и бронхообструктивного синдрома у детей. Раннее назначение данного препарата при ООСДП является залогом благоприятного прогноза и предупреждения осложнений.
Данные регламентирующих документов [5, 9, 13] и результаты собственных клинических наблюдений свидетельствуют, что назначение современных ИКС является высокоэффективным и безопасным методом терапии ООСДП тяжелого течения. У детей с 6-месячного возраста и старше наилучшим является ингаляционное введение будесонида через небулайзер в суточной дозе 0,25–1 мг/сутки (объем ингалируемого раствора доводят до 2–4 мл, добавляя физиологический раствор). Препарат можно назначать 1 раз в сутки, однако, как свидетельствует наш опыт, на высоте тяжелого приступа бронхообструкции или стенозе гортани 2–3 степени у детей первых лет жизни более эффективны ингаляции препарата 2 раза в сутки. У больных, ранее не получавших ИКС, целесообразно начать с дозы 0,5 мг через каждые 12 часов, а на 2–3 день, при хорошем терапевтическом эффекте, переходят на 0,25–0,50 мг 1 раз в сутки. Целесообразно назначать ИГС через 15–20 минут после ингаляции бронхолитика, однако возможно и одновременное использование обоих препаратов в одной камере небулайзера. Продолжительность терапии ингаляционными кортикостероидами определяется характером заболевания, длительностью и тяжестью течения обструкции, а также эффектом от проводимой терапии. У детей при остром обструктивном бронхите с тяжелой бронхиальной обструкцией необходимость в терапии ИКС обычно составляет 5–7 дней, а у детей с крупом — 2–3 дня.
У больных, ранее не получавших ИКС, целесообразно начать с дозы 0,5 мг через каждые 12 часов, а на 2–3 день, при хорошем терапевтическом эффекте, переходят на 0,25–0,50 мг 1 раз в сутки. Целесообразно назначать ИГС через 15–20 минут после ингаляции бронхолитика, однако возможно и одновременное использование обоих препаратов в одной камере небулайзера. Продолжительность терапии ингаляционными кортикостероидами определяется характером заболевания, длительностью и тяжестью течения обструкции, а также эффектом от проводимой терапии. У детей при остром обструктивном бронхите с тяжелой бронхиальной обструкцией необходимость в терапии ИКС обычно составляет 5–7 дней, а у детей с крупом — 2–3 дня.
Брнхолитическая терапия
В качестве препаратов бронхолитической терапии при БОС могут быть использованы β2-адреномиметики, антихолинергические препараты и их сочетание, а также теофиллины короткого действия.
Согласно национальным рекомендациям препаратами первого выбора являются β2-адреномиметики короткого действия (сальбутамол, тербуталин, фенотерол). Действие данной группы препаратов начинается через 5–10 минут после ингаляции и продолжаются 4–6 часов. Разовая доза сальбутамола, ингалируемого через ДАИ, составляет 100–200 мкг (1–2 дозы), при использовании небулайзера разовая доза может быть значительно увеличена и составляет 2,5 мг (небулы по 2,5 мл 0,1% раствора). Алгоритм неотложной терапии тяжелого БОС предполагает проведение трех ингаляций β2-агониста короткого действия в течение 1 часа с интервалом в 20 минут. Препараты этой группы высокоселективны, следовательно, имеют минимальные побочные эффекты. Однако при длительном бесконтрольном применении β2-агонистов короткого действия возможно усиление бронхиальной гиперреактивности и снижение чувствительности β2-адренорецепторов к препарату.
Действие данной группы препаратов начинается через 5–10 минут после ингаляции и продолжаются 4–6 часов. Разовая доза сальбутамола, ингалируемого через ДАИ, составляет 100–200 мкг (1–2 дозы), при использовании небулайзера разовая доза может быть значительно увеличена и составляет 2,5 мг (небулы по 2,5 мл 0,1% раствора). Алгоритм неотложной терапии тяжелого БОС предполагает проведение трех ингаляций β2-агониста короткого действия в течение 1 часа с интервалом в 20 минут. Препараты этой группы высокоселективны, следовательно, имеют минимальные побочные эффекты. Однако при длительном бесконтрольном применении β2-агонистов короткого действия возможно усиление бронхиальной гиперреактивности и снижение чувствительности β2-адренорецепторов к препарату.
В качестве бронхолитической терапии с учетом патогенетических механизмов БОС могут быть использованы антихолинергические препараты (ипратропиума бромид). Эта группа препаратов блокируют мускариновые М3-рецепторы для ацетилхолина. Бронходилатирующий эффект ингаляционной формы ипратропиума бромида развивается через 15–20 минут после ингаляции. Через ДАИ со спейсером однократно ингалируют 2 дозы (40 мкг) препарата, через небулайзер — 8–20 капель (100–250 мкг) 3–4 раза в сутки. Антихолинэргические препараты в случаях БОС, возникших на фоне респираторной инфекции, несколько более эффективны, чем α2-агонисты короткого действия.
Бронходилатирующий эффект ингаляционной формы ипратропиума бромида развивается через 15–20 минут после ингаляции. Через ДАИ со спейсером однократно ингалируют 2 дозы (40 мкг) препарата, через небулайзер — 8–20 капель (100–250 мкг) 3–4 раза в сутки. Антихолинэргические препараты в случаях БОС, возникших на фоне респираторной инфекции, несколько более эффективны, чем α2-агонисты короткого действия.
В настоящее время установлено, что физиологической особенностью детей раннего возраста является наличие относительно небольшого количества адренорецепторов, с возрастом отмечается увеличение их числа и повышение чувствительности к действию медиаторов. Чувствительность М-холинорецепторов, как правило, достаточно высока с первых месяцев жизни. Эти наблюдения послужили предпосылкой для создания комбинированных препаратов. Наиболее часто в комплексной терапии БОС у детей раннего возраста в настоящее время используется комбинированный препарат, сочетающий 2 механизма действия: стимуляцию адренорецепторов и блокаду М-холинорецепторов. При совместном применении ипратропия бромида и фенотерола бронхорасширяющий эффект достигается путем воздействия на различные фармакологические мишени [9, 11, 13].
При совместном применении ипратропия бромида и фенотерола бронхорасширяющий эффект достигается путем воздействия на различные фармакологические мишени [9, 11, 13].
Муколитическая и отхаркивающая терапия
Муколитическая и отхаркивающая терапия детям с ООСДП инфекционного генеза проводится с учетом возраста ребенка, тяжести течения респираторной инфекции, количества продуцируемой мокроты и ее реологических свойств. Основной целью является разжижение мокроты, снижение ее адгезивности и увеличение эффективности кашля.
При наличии у детей малопродуктивного кашля с вязкой мокротой целесообразно сочетать ингаляционный (через небулайзер) и пероральный путь введения муколитиков, наилучшими из которых являются препараты амброксола (Лазолван, Амбробене, Амброгексал и др.). Эти препараты хорошо зарекомендовали себя в комплексной терапии бронхообструктивного синдрома у детей. Они обладают выраженным муколитическим и мукокинетическим эффектом, умеренным противовоспалительным действием, увеличивают синтез сурфактанта, не усиливают бронхообструкцию, практически не вызывают аллергических реакций.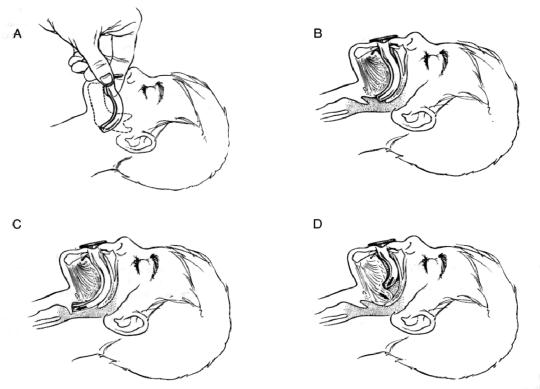 Препараты амброксола при респираторной инфекции детям назначают по 7,5–15 мг 2–3 раза в сутки в виде сиропа, раствора и/или ингаляционно.
Препараты амброксола при респираторной инфекции детям назначают по 7,5–15 мг 2–3 раза в сутки в виде сиропа, раствора и/или ингаляционно.
Детям с навязчивым малопродуктивным кашлем, отсутствием мокроты целесообразно назначение отхаркивающих лекарственных средств: щелочного питья, фитопрепаратов и др. Фитопрепараты детям с аллергией надо назначать с осторожностью. Можно рекомендовать препараты, созданные из натурального растительного сырья с использованием современных технологий (экстракт листьев плюща — Проспан, Бронхипрет и др.). Возможно сочетание отхаркивающих и муколитических лекарственных средств.
Таким образом, особенностью течения ОРЗ у детей первых лет жизни является частое развитие острых обструктивных состояний дыхательных путей. Основные причины острых обструктивных состояний дыхательных путей у детей с ОРВИ — острый стенозирующий ларинготрахеит, острый обструктивный бронхит, бронхиолит и бронхиальная астма. Эти состояния требуют неотложного проведения терапии. Основным способом доставки препаратов в период обострения заболевания является ингаляционный с использованием небулайзеров. Основными направлениями терапии при ООСДП являются назначение противовоспалительных препаратов, бронхолитических и муколитических препаратов. Препаратами выбора противовоспалительной терапии при ООСДП являются ИГКС. Своевременно назначенная рациональная терапия ООСДП — залог быстрого купирования ООСДП и предупреждения жизнеугрожающих состояний.
Основным способом доставки препаратов в период обострения заболевания является ингаляционный с использованием небулайзеров. Основными направлениями терапии при ООСДП являются назначение противовоспалительных препаратов, бронхолитических и муколитических препаратов. Препаратами выбора противовоспалительной терапии при ООСДП являются ИГКС. Своевременно назначенная рациональная терапия ООСДП — залог быстрого купирования ООСДП и предупреждения жизнеугрожающих состояний.
При информационной поддержке ООО «ТЕВА»
Литература
- Инфекции респираторного тракта у детей раннего возраста / Под ред. Г. А. Самсыгиной. М., 2006. 280 с.
- Ключников С. О., Зайцева О. В., Османов И. М., Крапивкин А. И. и др. Острые респираторные заболевания у детей. Пособие для врачей. М., 2009. 35 с.
- Государственный отчет Роспотребнадзора «Инфекционная заболеваемость в Российской федерации за 2012 год». Опубликовано 05.02.2013 на сайте http://75.
 rospotrebnadzor.ru/content/infektsionnaya-zabolevaemost-v-rossiiskoi-federatsii-za-2012-god.
rospotrebnadzor.ru/content/infektsionnaya-zabolevaemost-v-rossiiskoi-federatsii-za-2012-god. - Global Atlas oF Asthma. Cezmi A. Akdis, Ioana Agache. Published by the European Academy of Allergy and Clinical Immunology, 2013, с. 42–44.
- Острые респираторные заболевания у детей: лечение и профилактика. Научно-практическая программа Союза педиатров России. М.: Международный фонд охраны здоровья матери и ребенка, 2002.
- Зайцева О. В. Бронхообструктивный синдром у детей // Педиатрия. 2005, № 4, с. 94–104.
- Педанова Е. А., Троякова М. А., Чернышова Н. И. Особенности рецидивирующего обструктивного бронхита у детей раннего возраста. В кн.: Пульмонология. Прил. 2003. Тринадцатый нац. конгр. по бол. орг. дых., СПб, 10–14 ноября 2003 г. С. 188.
- Котлуков В. К., Блохин Б. М., Румянцев А. Г., Делягин В. М., Мельникова М. А. Синдром бронхиальной обструкции у детей раннего возраста с респираторными инфекциями различной этиологии: особенности клинических проявлений и иммунного ответа // Педиатрия.
 2006, № 3, с. 14–21.
2006, № 3, с. 14–21. - Национальная программа «Бронхиальная астма у детей. Стратегия лечения и профилактика». 4-е изд., перераб. и доп. М.: Оригинал-макет, 2012. 184 с.
- Фисенко В. П., Чичкова Н. В. Современная лекарственная терапия бронхиальной астмы // Врач. 2006; 1: 56–60.
- Iramain R., López-Herce J., Coronel J. Inhaled salbutamol plus ipratropium in moderate and severe asthma crises in children // J Asthma. 2011 Apr; 48 (3): 298–303.
- Рачинский С. В., Таточенко В. К. Болезни органов дыхания у детей: Рук-во для врачей. М. 1987. 495 с.
- Global Initiative for Asthma. Global Strategy for Asthma Management and Prevention. 2009 // http://www.ginasthma.org.
- Жестков А. В., Светлова Г. Н., Косов А. И. Короткодействующие b2-агонисты: механизмы действия и фармакотерапия бронхиальной астмы и хронической обструктивной болезни легких // Consilium Medicum. 2008, т. 10, № 3, с.
 99–103.
99–103. - Авдеев С. Н., Бродская О. Н. Стеринебы — новые возможности небулайзерной терапии обструктивных заболеваний легких // Научное обозрение респираторной медицины. 2011; 3: 18–24.
- Авдеев С. Н. Небулайзерная терапия обструктивных заболеваний легких // Consilium Medicum. 2011. Т. 13. № 3. С. 36–42.
С. В. Зайцева, кандидат медицинских наук
С. Ю. Снитко
О. В. Зайцева, доктор медицинских наук, профессор
Э. Э. Локшина, кандидат медицинских наук
ГБОУ ВПО МГМСУ им А. И. Евдокимова МЗ РФ, Москва
1 Контактная информация: [email protected]
Маневр обструкции дыхательных путей у детей при рвоте или жидкости: да или нет?
Молоко или рвота могут вызвать затруднение дыхания и удушье у маленького ребенка. Тем не менее, является ли обязательной процедура удаления обструкции дыхательных путей? Некоторые утверждают, что «никогда не пытаются приступить к процедурам удаления обструкции дыхательных путей в случае жидкостей или полужидкостей», и те, кто заявляют, что «следуют рекомендациям, выполняют процедуру даже в случае жидкостей или полужидкостей». ».
».
Как все мы знаем, устранение обструкции дыхательных путей — это медицинская практика, которая позволила спасти жизнь десяткам, если не сотням детей, чьи дыхательные пути были заблокированы инородными телами на протяжении многих лет.
Но когда нужно удалять обструкцию дыхательных путей у детей?
Ответ на этот вопрос кажется безошибочно простым, потому что так оно и должно быть: понятно каждому. Независимо от того, являетесь ли вы домохозяйками, фермерами, юристами или дипломатами, рекомендации написаны для понимания, изучали ли вы медицину или вас не беспокоило чтение справочника на страницах 360 по устранению обструкции дыхательных путей и сердечно-легочная реанимация, Ответ на этот вопрос: устранение обструкции дыхательных путей должно выполняться, когда дыхательные пути закрыты.
Но когда кто-то может сказать, что дыхательные пути действительно заблокированы?
Когда я решаю, что дыхательные пути закрыты? Когда я должен начать думать о маневры обструкции дыхательных путей? С одной стороны, есть те, кто считает, что дыхательные пути быть заблокированным только в случае проглатывания или вдыхания инородного тела. Следовательно, регургитация не может препятствовать дыхательным путям, потому что это не инородное тело и это не твердый, а полужидкий. С другой стороны, есть те, кто утверждает, что полужидкие тела могут также смертельно затруднять дыхательные пути и что вам следует действовать тем не менее. Высший научный орган в сердечно-легочная реанимация и поле беспрепятственного, ILCOR, заявлял что-то немного другое и намного, гораздо более эффективное, это вращается вокруг совершенно другого параметра: кашель.
Следовательно, регургитация не может препятствовать дыхательным путям, потому что это не инородное тело и это не твердый, а полужидкий. С другой стороны, есть те, кто утверждает, что полужидкие тела могут также смертельно затруднять дыхательные пути и что вам следует действовать тем не менее. Высший научный орган в сердечно-легочная реанимация и поле беспрепятственного, ILCOR, заявлял что-то немного другое и намного, гораздо более эффективное, это вращается вокруг совершенно другого параметра: кашель.
И это потому, что кашель автоматический рефлекс нашего тела, когда посторонний объект блокирует наши дыхательные пути. И что? Тебе просто нужно кашлять? Иногда да, и в этих случаях речь идет об эффективном кашле. В других случаях, к сожалению, этого недостаточно. Есть научные исследования тот пытался понять, почему кашель — иногда — не эффективен. Именно по этой причине, когда курсы устранения обструкции дыхательных путей проводятся там много разговоров о МОРС, a синдром, связанный с регургитацией молока и это может привести к удушье. Не вдаваясь в технические аспекты, чтобы сосредоточиться на теме «устранение обструкции дыхательных путей, да / нет», давайте посмотрим, что написано в Европейский совет реанимации принципы:
Не вдаваясь в технические аспекты, чтобы сосредоточиться на теме «устранение обструкции дыхательных путей, да / нет», давайте посмотрим, что написано в Европейский совет реанимации принципы:
- Оцените серьезность ситуации (как долго ребенку мешали? Как долго он кашлял? Стал ли он синюшным / голубым?)
- Если кашель неэффективен, а ребенок в сознании, нанесите спинной удар 5 и компрессию грудной клетки 5.
- Если кашель неэффективен, а ребенок без сознания и не дышит, откройте дыхательные пути, приступите к вентиляции 5 и запустите СЛР.
- Если ребенок продолжает кашлять, и вы замечаете, что он все еще может дышать между кашлями, побудите его продолжать кашлять и продолжайте оценивать, появляются ли какие-либо признаки сенсорной обнибуляции, становится ли кашель неэффективным или устраняется ли препятствие.
Итак, есть ли ясность?
Да, процедуры должны выполняться в полных препятствиях когда ребенок не может кашлятьплакать или говорить, но все еще в сознании.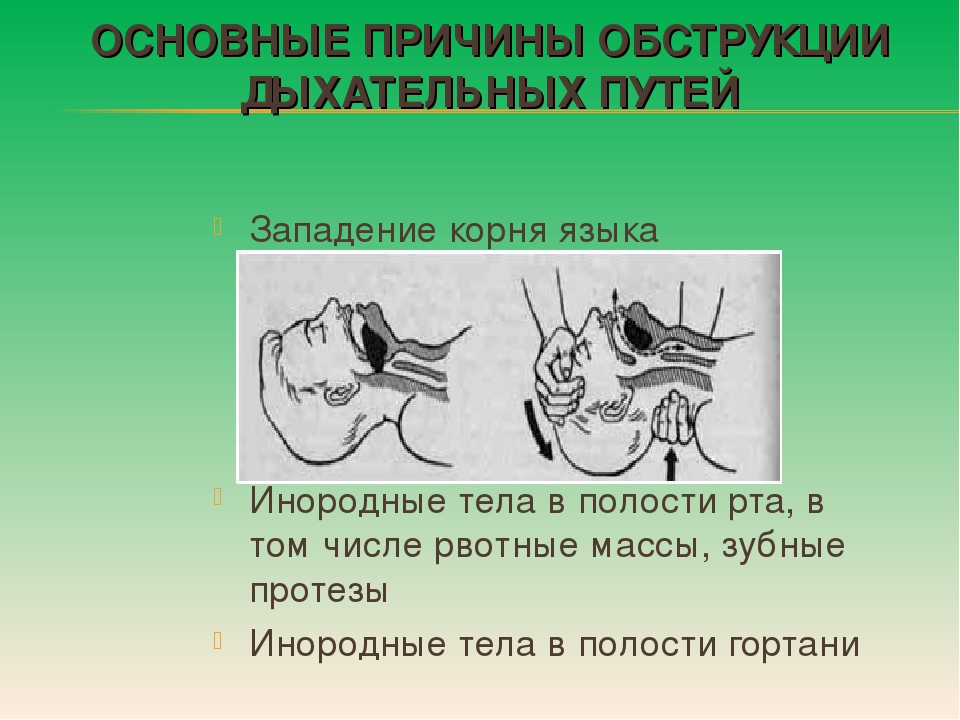 Если он потерял сознание, приступайте к сердечно-легочная реанимация. Нет никаких доказательств, чтобы сделать иначе.
Если он потерял сознание, приступайте к сердечно-легочная реанимация. Нет никаких доказательств, чтобы сделать иначе.
Настоящая проблема — паника у свидетелей, будь то первый ответчик или спасатель. Зачем?
Чтобы лучше разрешить спор, мы попросили многих anaesthesists, поэтому мы могли бы предоставить более полную и более правдивую картину ситуации. На сегодняшний день это правда, что сенсибилизация к спасательные маневры стало возможным избежать множественных трагедий, но в некоторых случаях — когда методика плохо преподается или способ предотвращения паники не объясняется — возникали эксцессы, которые приводили к реальному клиническая проблематика, Фактически, данные, предоставленные министерством, добавляют к смертельным случаям, вызванным обструкцией дыхательных путей, а также смерти от удушья, мекония прием пищи or вдыхание пищеварительных соков. Это преувеличило пропорцию проблемы, создавая — помимо правильного и должного внимания — также панику, в большинстве случаев из-за неверной информации. Единственные данные о реальных препятствиях для инородных тел — в Италии — это данные, предоставленные ISTAT, и они представлены в таблицах ниже.
Единственные данные о реальных препятствиях для инородных тел — в Италии — это данные, предоставленные ISTAT, и они представлены в таблицах ниже.
Кто тогда прав?
Следуя рекомендациям ILCOR, невозможно отличить, кто прав, а кто нет, в разнице между жидкостью и твердым веществом, потому что В руководящих принципах проводится различие между препятствием и отсутствием препятствий, Любой врач (и мы проконсультировались с 5 из них перед написанием этой статьи) скажет вам, чтоПрежде чем приступить к процедуре устранения препятствий, необходимо хорошо оценить ситуацию.потому что процент жидкости или регургитации вызвал препятствия, которые устраняются благодаря автоматическим рефлексам, которые приводят в движение наши тела, очень высоки. С другой стороны, он отличается от посторонних предметов (батарейки для часов, оливки и т. Д.). В любом случае, на странице 117 указывается, что причинами обструкции дыхательных путей являются:
«Обструкция дыхательных путей может быть частичной или полной.
Это может произойти на любом уровне, от носа до рта, до трахеи. У пациента без сознания наиболее частыми местами обструкции дыхательных путей являются мягкое небо и надгортанник. Обструкция также может быть вызвана рвотой или кровью (желудочная регургитация или травма) или инородными телами. Обструкция гортани может быть вторичной по отношению к отеку ожога, воспалению или анафилаксии. Стимуляция верхних дыхательных путей может вызвать спазм гортани. Обструкция дыхательных путей, уступающая гортани, встречается реже, но может возникнуть в случае чрезмерной секреции бронхов, отека слизистой оболочки, бронхоспазма, отека легких или всасывания содержимого желудка ».
Итак, я должен попробовать любой маневр обструкции дыхательных путей или нет?
Да, обструкция дыхательных путей маневры должны быть выполнены, когда вы уверены, что ребенок не дышит и не кашляет эффективным способом, чтобы избавиться от обструкции самостоятельно, давая явные признаки удушья. И они должны быть сделаны, не поддаваясь паника, который является настоящим настоящим врагом каждого первого ответчика. Когда вы имеете дело с ребенком с частичной или полной обструкцией, самое важное — сохранять спокойствие, ждать явных признаков обструкции, которые позволяют начать официальные процедуры разблокировки, и в то же время побуждать жертву кашлять. Паника и тревога вмешательства являются виновниками ненужных маневров по устранению препятствий. И они могут заставить нас наносить ненужные сильные удары по спине, которые могут помешать кашлю или причинить ребенку травмы, вызывая еще одно очень, очень опасное состояние; так называемый синдром тряски младенца. Всегда будьте осторожны и не смущайтесь: следуйте инструкциям и никогда не выходите из себя.
И они должны быть сделаны, не поддаваясь паника, который является настоящим настоящим врагом каждого первого ответчика. Когда вы имеете дело с ребенком с частичной или полной обструкцией, самое важное — сохранять спокойствие, ждать явных признаков обструкции, которые позволяют начать официальные процедуры разблокировки, и в то же время побуждать жертву кашлять. Паника и тревога вмешательства являются виновниками ненужных маневров по устранению препятствий. И они могут заставить нас наносить ненужные сильные удары по спине, которые могут помешать кашлю или причинить ребенку травмы, вызывая еще одно очень, очень опасное состояние; так называемый синдром тряски младенца. Всегда будьте осторожны и не смущайтесь: следуйте инструкциям и никогда не выходите из себя.
Инородные тела дыхательных путей у детей
Чаще всего (примерно в 95-98% всех случаев) инородные тела дыхательных путей встречаются у детей в возрасте от 1,5 до 3 лет. Именно в этом возрасте ребенок активно сознательно начинает познавать окружающий мир. И именно в этом возрасте ребенок тянет в рот все, что попало. Этот возраст еще характерен тем, что ребенок самостоятельно, на основе собственных ощущений учится правильно жевать и глотать твердую пищу. И разумеется, не сразу у него все получается. Поэтому именно в этом возрасте максимальна опасность попадания мелких предметов в дыхательные пути. Плохо еще и то, что ребенок не всегда может сказать, что именно с ним произошло. И иногда инородные тела в дыхательных путях выявляются слишком поздно. Инородные тела дыхательных путей могут находиться где угодно — в носовых ходах, гортани, трахее, бронхах, в ткани самого легкого, в плевральной полости. По локализации самое опасное место — гортань и трахея. Инородные тела в этой области могут полностью перекрыть доступ воздуха. Если не оказать немедленную помощь, то смерть наступает за 1-2 минуты. Инородные тела в главных и долевых бронхах так же очень опасны.
Именно в этом возрасте ребенок активно сознательно начинает познавать окружающий мир. И именно в этом возрасте ребенок тянет в рот все, что попало. Этот возраст еще характерен тем, что ребенок самостоятельно, на основе собственных ощущений учится правильно жевать и глотать твердую пищу. И разумеется, не сразу у него все получается. Поэтому именно в этом возрасте максимальна опасность попадания мелких предметов в дыхательные пути. Плохо еще и то, что ребенок не всегда может сказать, что именно с ним произошло. И иногда инородные тела в дыхательных путях выявляются слишком поздно. Инородные тела дыхательных путей могут находиться где угодно — в носовых ходах, гортани, трахее, бронхах, в ткани самого легкого, в плевральной полости. По локализации самое опасное место — гортань и трахея. Инородные тела в этой области могут полностью перекрыть доступ воздуха. Если не оказать немедленную помощь, то смерть наступает за 1-2 минуты. Инородные тела в главных и долевых бронхах так же очень опасны.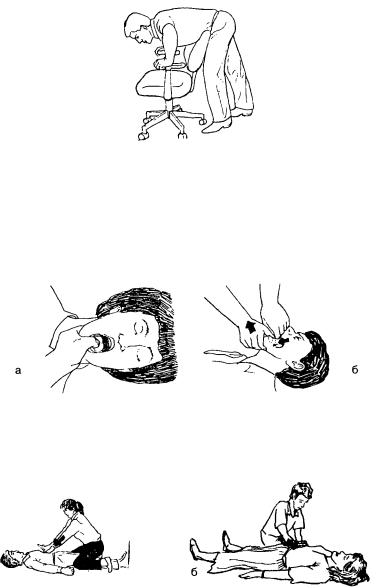 Если они закрывают просвет бронха по типу «клапана», то развивается синдром внутригрудного напряжения, приводящий к очень опасным нарушениям дыхания и кровообращения. Инородные тела мелких бронхов могут вообще никак себя не проявлять в первое время. Они не вызывают выраженных дыхательных расстройств, и никак не влияют на самочуствие ребенка. Hо спустя некоторое время (дни, недели, а иногда — и месяцы и годы) в этом месте развивается гнойный процесс, ведущий к образованию бронхоэктазов или развитию легочного кровотечения.
Если они закрывают просвет бронха по типу «клапана», то развивается синдром внутригрудного напряжения, приводящий к очень опасным нарушениям дыхания и кровообращения. Инородные тела мелких бронхов могут вообще никак себя не проявлять в первое время. Они не вызывают выраженных дыхательных расстройств, и никак не влияют на самочуствие ребенка. Hо спустя некоторое время (дни, недели, а иногда — и месяцы и годы) в этом месте развивается гнойный процесс, ведущий к образованию бронхоэктазов или развитию легочного кровотечения.
Баллотирующие инородные тела трахеи опасны еще и тем, что при ударе ими снизу по голосовым связкам возникает стойкий ларингоспазм, приводящий сам по себе к практически полному закрытию просвета гортани. Длительно стоящие инородные тела дыхательных путей вызывают хроническое воспаление, приводящее к развитию бронхоэктазов, или фиброза, или к возникновению легочного кровотечения. Все эти осложнения лечатся только оперативно. Иногда происходит миграция инородных тел в плевральную полость (чаще всего это колоски злаковых растений), в следствие чего может возникнуть пиоторакс и/или пиопневмоторакс.
Основными признаками попадания инородных тел являются: кашель во время еды или игры, свистящее дыхание, цианоз кожных покровов, одышка, и т.д. Могут присутствовать как и все эти признаки, так и каждый из них в отдельности. Обычно родители четко связывают появление этих симптомов с едой или с игрой с мелкими игрушками. Hо иногда, особенно когда ребенок остается без присмотра, этой связи можно и не установить. Тогда диагностика особенно затруднительна. Иногда инородные тела дыхательных путей могут вообще никак себя не проявлять. Заподозрить наличие инородного тела можно при аускультации, рентгенографии и рентгеноскопии грудной клетки. Характер аускультативных и рентгенологических изменений зависит от типа обструкции дыхательных путей. Hе все инородные тела рентгеноконтрастны. Hо полностью исключить или подтвердить наличие инородного тела дыхательных путей можно только при трахеобронхоскопии. И при любом, даже малейшем подозрении на аспирацию инородного тела есть прямые показания для проведения трахеобронхоскопии.
Лечение должно проводиться в специализированном отделении где есть врачи, владеющие трахеобронхоскопией. Инородные тела трахеи и бронхов удаляются при помощи эндоскопических щипцов. Дальнейшая терапия (антибиотики, ФЗТ, массаж) зависит от характера и выраженности воспалительного процесса в бронхах. Иногда при длительностоящих инородных телах с развитием осложнений (бронхоэктазы, фиброз, кровотечение и т.д.) приходится прибегать к оперативному лечению.
Еще раз повторяю: для практически 100-процентной диагностики инородного тела дыхательных путей трахеобронхоскопия необходима! Pазумеется, я не имею ввиду инородные тела носовых ходов и глотки. В этих случаях необходима консультация ЛОP-врача.
Проанализирован опыт работы хирургического отделения «Центра матери и ребенка» г. Усть- Каменогорска по инородным телам дыхательных путей в период с 2009г по 2014г, изучены истории болезней, протокола из журналов бронхоскопий.
Всего за данный период произведено манипуляций с результатом удаления инородного тела — бронхоскопия- 51. Возраст больных составил: от 11мес-3 лет — 26; от 4-6лет — 14; от 7-14 лет — 11. Диагностика включала как клинические, так и инструментально-лабораторные методы исследования.
Возраст больных составил: от 11мес-3 лет — 26; от 4-6лет — 14; от 7-14 лет — 11. Диагностика включала как клинические, так и инструментально-лабораторные методы исследования.
Врачами «ЦМиР» г. Усть-Каменогорска осуществляется экстренная бронхологическая помощь в отдаленных районах Восточно-Казахстанской области по линии санавиации. В состав бронхологической бригады входят: детский хирург, анестезиолог, эндоскопическая мед. сестра. В подобных случаях за последние 5 лет помощь оказана 8 пациентам.
В заключение: инородные тела дыхательных путей — страшная и очень опасная патология. Много детей стали инвалидами, многие перенесли тяжелейшие манипуляции и операции из-за оплошности и невнимательности их родителей. Бывали и смертельные исходы.
Уважаемые родители! Запомните одно правило:
Hельзя давать детям младше 3-4 лет мелкие игpушки и пpодукты питания (оpехи, гоpох и т.п.), Котоpые они могли бы вдохнуть.
Поверьте, ваш ребенок прекрасно проживет без них. И избежит таким образом многих неприятностей.
И избежит таким образом многих неприятностей.
Будьте осторожны! Hе рискуйте жизнью и здоровьем собственных детей!
Врач хирург «Центр Матери и Ребенка»: Пушкарев Михаил Анатольевич
ОСТРЫЕ СОСТОЯНИЯ ПРИ ЗАБОЛЕВАНИЯХ ОРГАНОВ ДЫХАНИЯ У ДЕТЕЙ. ОБЗОР ЛИТЕРАТУРЫ
Аннотация
Острые нарушения дыхания у детей являются актуальной проблемой современной неотложной педиатрии. Их доля в структуре первичной заболеваемости детей составляет около 60%. Обструктивные нарушения дыхания у детей могут зависеть от разных причин и иметь разноуровневую локализацию препятствия. Независимо от причины и характера препятствия, острая и подострая обструкция дыхательных путей представляет собой драматическую клиническую ситуацию с быстро нарастающей гипоксией, требующую оказания экстренных лечебных мероприятий. В статье показаны особенности клинических проявлений, методы диагностики и тактика лечения заболеваний, сопровождающихся обструкцией верхних или нижних дыхательных путей у детей. Неотложная терапия острых нарушений дыхания у детей является комплексной. Рациональное использование современных фармакологических препаратов обеспечивает эффективность проводимого лечения.
Неотложная терапия острых нарушений дыхания у детей является комплексной. Рациональное использование современных фармакологических препаратов обеспечивает эффективность проводимого лечения.
Литература
1. Неотложная педиатрия: национальное руководство. Под ред. Блохина Б.М. М.: ГЭОТАР-Медиа, 2017. с. 832.
2. Заболевания органов дыхания у детей. Практическое руководство по детским болезням. Том 9. Под редакцией Блохина Б.М. М.: Медпрактика – М; 2007. с. 616.
3. Полякова А.С. Бакрадзе М.Д. Таточенко В.К. Синдром крупа у детей: предрассудки и доказательная медицина. Фарматека. 2018; 1: 15-22.
4. Darras K, Roston A, Yewchuk L. Imaging Acute Airway Obstruction in Infants and Children. Radiographics. 2015; 35(7): 2064-2079.
5. Pawelczyk M., Kowalski M. The Role of Human Parainfluenza Virus Infections in the Immunopathology of the Respiratory Tract. Curr Allergy Asthma Rep. 2017; 17(3):16. doi: 10.1007/s11882-017-0685-2.
2017; 17(3):16. doi: 10.1007/s11882-017-0685-2.
6. Овсянников Д.Ю., Кузьменко Л.Г., Алексеева О.В. Вирусный и рецидивирующий круп у детей. Медицинский совет. 2019; 2: 100-105.
7. Круп у детей (острый обструктивный ларингит). Клинические рекомендации. Клиническая и неотложная педиатрия. 2015; 1: 103-110.
8. Russell K, Liang Y, O’Gorman K, Johnson D, Klassen T. Glucocorticoids for croup. Cochrane Database Syst. Rev. 2011; (1):CD001955. doi: 10.1002/14651858.CD001955.pub3.
9. Cutrera R, Baraldi E, Indinnimeo L, Miraglia Del Giudice M, Piacentini G5, Scaglione F at al. Management of acute respiratory diseases in the pediatric population: the role of oral corticosteroids. Ital J Pediatr. 2017; 43(1):31. doi: 10.1186/s13052-017-0348-x.
10. Савенкова М.С., Балясинская Г.Л., Бычков В.А., Воротнюк Г.М.., Коробко Л.М., Анин А.Н. Острый эпиглоттит у детей (этиопатогенез, диагностика, лечение) Вопросы современной педиатрии. 2008; 7(5): 91-97.
11. Tibballs J., Watson T. Symptoms and signs differentiating croup and epiglottitis. J Paediatr Child Health. 2011; 47(3): 77–82.
12. Reena K.A., Singh S.K., Agrawal V. Unsuspected subglottic web in a child managed for severe respiratory obstruction. Saudi J Anaesth. 2017; 11(1): 99-101. doi: 10.4103/1658-354X.197336.
13. Бриткова Т.А., Лекомцева О.И., Кравцова Н.А., Пчелина Е.В., Иванов И.В. Острый эпиглоттит у мальчика 3 лет (клиническое наблюдение). Детские инфекции. 2016; 3: 69-70.
14. Таточенко В.К. Болезни органов дыхания у детей: практическое руководство. М.: «Педиатръ», 2012. с. 480.
15. Сиренко Н.В., Алексеенко С.И., Цурикова Г.П., Волкова М.О. Паратонзиллярные абсцессы у детей. Клинико-микробиологические методы исследования. Антибиотики и химиотерапия 2017; 62(1): 35-39
16. Свистушкин В.М. Мустафаев Д.М. Гнойные осложнения воспалительных заболеваний глотки. РМЖ. 2015; 6: 332-335.
17. Ibrahimov M., Yollu U. , Akil F, Aydin F, Yener M. Laryngeal foreign body mimicking croup. J Craniofac Surg. 2013; 24(1): 7-8. doi: 10.1097/SCS.0b013e31826465e5.
, Akil F, Aydin F, Yener M. Laryngeal foreign body mimicking croup. J Craniofac Surg. 2013; 24(1): 7-8. doi: 10.1097/SCS.0b013e31826465e5.
18. Зайцева О.В. Дифференциальный диагноз бронхообструктивного синдрома у детей. Клиническая и неотложная педиатрия. 2015;1: 66-75.
19. Блохин Б.М, Лобушкова И.П., Рощина А.К., Кузнецов А.Ю., Мирзоев Т.Х. Диагностика, тактика и методы лечения кашля у детей. РМЖ Педиатрия. 2015; 3: 3-7.
20. Schulte‑Michels J, Keksel C, Häberlein H, Franken S. Anti‑inflammatory effects of ivy leaves dry extract: influence on transcriptional activity of NFκB. Inflammopharmacology. 2019; 27(2): 339-347 doi: 10.1007/s10787-018-0494-9/.
21. Schulte-Michels J, Runkel F, Gokorsch S, Häberlein H. Ivy leaves dry extract EA 575® decreases LPS-induced IL-6 release from murine macrophages. Pharmazie. 2016; 71: 158–161.
22. Мизерницкий Ю.Л.. Эффективность и безопасность сухого экстракта плюща (Проспан®) в терапии бронхитов у детей (по результатам наблюдательного исследования ProSpiro) Педиатрия. 2019; 98(2): 18-27.
2019; 98(2): 18-27.
23. Cwientzek U, Ottillinger B, Arenberger P. Acute bronchitis therapy with ivy leaves extracts in a two-arm study. A double-blind, randomised study vs. an other ivy leaves extract. Phytomedicine. 2011; 18(13): 1105-1109. doi: 10.1016/j.phymed.2011.06.014.
24. Beigelman A, Chipps B, Bacharier LB. Update on the utility of corticosteroids in acute pediatric respiratory disorders. Allergy Asthma Proc. 2015; 5(36): 332-338. doi: 10.2500/aap.2015.36.3865.
25. Barclay L. AAP Update Guidelines on Bronchiolitis in Young Children. [Internet] Medscape Medical News; 2014. http://www.medscape.com/viewarticle/833884/.
26. Ralston SL, Lieberthal AS, Meissner HC, Alverson BK, Baley JE, Gadomski AM at al. American Academy of Pediatrics. Clinical Practice Guideline: The Diagnosis, Management, and Prevention of Bronchiolitis Pediatrics. 2014; 134(5): 1474-1502. doi: 10.1542/peds.2014-2742.
27. Национальная программа «Бронхиальная астма у детей. Стратегия лечения и профилактика». М.: Оригиналмакет, 2017. с. 160.
Стратегия лечения и профилактика». М.: Оригиналмакет, 2017. с. 160.
28. Global Initiative for asthma. [Internet] Global Strategy for Asthma Management and Prevention; 2018. http://www.ginasthma.org/.
29. Суровенко Т.Н., Глушкова Е.Ф. Новые возможности терапии бронхиальной астмы у детей. Медицинский совет. 2018; 17: 192-198.
30. Green CE, Turner AM. The role of the endothelium in asthma and chronic obstructive pulmonary disease (COPD). Respir Res. 2017; 18(1): 20. doi: 10.1186/s12931-017-0505-1.
Фиксированная обструкция дыхательных путей у больных бронхиальной астмой | Сергеева
1. Global Initiative for Asthma. Global Strategy for Asthma Management and Prevention. 2020 GINA Report. Available at: www.ginasthma.org
2. Contoli M., Baraldo S., Marku B. et al. Fixed airflow obstruction due to asthma or chronic obstructive pulmonary disease: 5-year follow-up.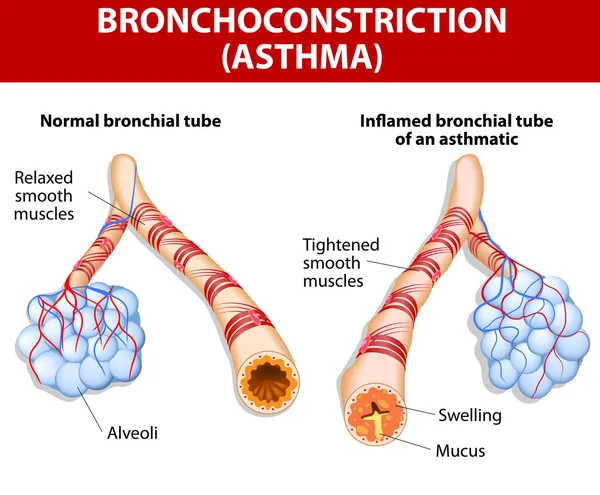 J. Allergy Clin. Immunol. 2010; 125 (4): 830–837. DOI: 10.1016/j.jaci.2010.01.003.
J. Allergy Clin. Immunol. 2010; 125 (4): 830–837. DOI: 10.1016/j.jaci.2010.01.003.
3. Lee T., Lee Y.S., Bae Y.J. et al. Smoking, longer disease duration and absence of rhinosinusitis are related to fixed airway obstruction in Koreans with severe asthma: findings from the COREA study. Respir. Res. 2011; 12: 1. DOI: 10.1186/1465-9921-12-1.
4. Lee J.H., Haselkorn T., Borish L. et al. Risk factors associated with persistent airflow limitation in severe or difficult-to-treat asthma: insights from the TENOR study. Chest. 2007; 132 (6): 1882–1889. DOI: 10.1378/chest.07-0713.
5. Емельянов А.В., Сергеева Г.Р., Коровина О.В. и др. Современная терапия бронхиальной астмы. Российский семейный врач. 2012; 16 (2): 9–15. DOI: 10.17816/RFD201229-15.
6. Федеральные клинические рекомендации по диагностике и лечению бронхиальной астмы. Российское респираторное общество; 2016. Доступно на: https://spulmo.ru/
Федеральные клинические рекомендации по диагностике и лечению бронхиальной астмы. Российское респираторное общество; 2016. Доступно на: https://spulmo.ru/
7. Zhang L., He L., Gong J., Liu C. Risk factors associated with irreversible airway obstruction in asthma: a systematic review and meta-analysis. Biomed. Res. Int. 2016; 2016: 9868704. DOI: 10.1155/2016/9868704.
8. Konstantellou E., Papaioannou A.I., Loukides S. et al. Persistent airflow obstruction in patients with asthma: Characteristics of a distinct clinical phenotype. Respir. Med. 2015; 109 (11): 1404–1409. DOI: 10.1016/j.rmed.2015.09.009.
9. Bumbacea D., Campbell D., Nguyen L. et al. Parameters associated with persistent airflow obstruction in chronic severe asthma. Eur. Respir. J. 2004; 24 (1): 122–128. DOI: 10.1183/09031936.04.00077803.
DOI: 10.1183/09031936.04.00077803.
10. ten Brinke A., Zwinderman A.H., Sterk P.J. et al. Factors associated with persistent airflow limitation in severe asthma. Am. J. Respir. Crit. Care Med. 2001; 164 (5): 744–748. DOI: 10.1164/ajrccm.164.5.2011026.
11. Boulet L.P. Irreversible airway obstruction in asthma. Curr. Allergy Asthma Rep. 2009; 9 (2): 168–173. DOI: 10.1007/s11882-009-0025-2.
12. Vonk J.M., Jongepier H., Panhuysen C.I. et al. Risk factors associated with the presence of irreversible airflow limitation and reduced transfer coefficient in patients with asthma after 26 years of follow up. Thorax. 2003; 58 (4): 322–327. DOI: 10.1136/thorax.58.4.322.
13. Mogensen I. , Alving K., Bjerg A. et al. Simultaneously elevated exhaled nitric oxide and serum-eosinophil cationic protein relate to recent asthma events in asthmatics in a cross-sectional population-based study. Clin. Exp. Allergy. 2016; 46 (12): 1540–1548. DOI: 10.1111/cea.12792.
, Alving K., Bjerg A. et al. Simultaneously elevated exhaled nitric oxide and serum-eosinophil cationic protein relate to recent asthma events in asthmatics in a cross-sectional population-based study. Clin. Exp. Allergy. 2016; 46 (12): 1540–1548. DOI: 10.1111/cea.12792.
14. Oishi K.., Hirano T., Suetake R. et al. A trial of oral corticosteroids for persistent systemic and airway inflammation in severe asthma. Immun. Inflamm. Dis. 2017; 5 (3): 261–264. DOI: 10.1002/iid3.166.
15. Mogensen I., Alving K., Dahlen S.E. et al. Fixed airflow obstruction relates to eosinophil activation in asthmatics. Clin. Exp. Allergy. 2019; 49 (2): 155–162. DOI: 10.1111/cea.13302.
16. Ненашева Н.М., Белевский А.С., Фассахов Р.С., Емельянов А.В. Фенотипы трудной для терапии бронхиальной астмы: возможности достижения контроля. Российский аллергологический журнал. 2016; (4-5): 43–54.
Российский аллергологический журнал. 2016; (4-5): 43–54.
17. Ulrik C.S., Backer V. Nonreversible airflow obstruction in life-long nonsmokers with moderate to severe asthma. Eur. Respir. J. 1999; 14 (4): 892–896. DOI: 10.1034/j.1399-3003.1999.14d27.x.
18. Boulet L.P., Boulay M.È., Dérival J.L. et al. Asthma-COPD overlap phenotypes and smoking: Comparative features of asthma in smoking or non-smoking patients with an incomplete reversibility of airway obstruction. COPD. 2018; 15 (2): 130–138. DOI: 10.1080/15412555.2017.1395834.
19. Сергеева Г.Р., Емельянов А.В., Лешенкова Е.В. и др. Стабильность фиксированной обструкции дыхательных путей у больных бронхиальной астмой. Российский аллергологический журнал. 2017; 14 (1): 129–131.
20. Сергеева Г.Р., Емельянов А.В., Лешенкова Е.В. и др. Стабильность фиксированной обструкции дыхательных путей у больных бронхиальной астмой по данным ретроспективного исследования. Российский аллергологический журнал. 2018; 15 (1, ч. 2): 87–90.
Сергеева Г.Р., Емельянов А.В., Лешенкова Е.В. и др. Стабильность фиксированной обструкции дыхательных путей у больных бронхиальной астмой по данным ретроспективного исследования. Российский аллергологический журнал. 2018; 15 (1, ч. 2): 87–90.
Алгоритм оказания помощи «Обструкция дыхательных путей инородным телом»
При попадании инородного тела в дыхательные пути, сразу же появляется кашель, который является эффективным и безопасным средством удаления инородного тела и попыткой его стимулирования – средством первой помощи.
При отсутствии кашля и его неэффективности при полной обструкции дыхательных путей быстро развивается асфиксия и требуются срочные меры для эвакуации инородного тела.
Основные симптомы ИТДП:
- Внезапная асфиксия.
- “Беспричинный”, внезапный кашель, часто приступообразный.
- Кашель, возникший на фоне приема пищи.
- При инородном теле в верхних дыхательных путях одышка инспираторная, при инородном теле в бронхах — экспираторная.
- Свистящее дыхание.
- Возможно кровохарканье из-за повреждения инородным телом слизистой оболочки дыхательных путей.
- При аускультации легких — ослабление дыхательных шумов с одной или обеих сторон.
Попытки извлечения инородных тел из дыхательных путей предпринимаются только у пациентов с прогрессирующей ОДН, представляющей угрозу для их жизни.
Необходимо осмотреть глотку пациента, далее следовать алгоритму:
- Инородное тело в глотке — выполните манипуляцию пальцем или корнцангом по извлечению инородного тела из глотки. При отсутствии положительного эффекта выполните поддиафрагмально-абдоминальные толчки.
- Инородное тело в гортани, трахее, бронхах — выполните поддиафрагмально-абдоминальные толчки.
2. 1. Пострадавший в сознании.
1. Пострадавший в сознании.
- Пострадавший в положении сидя или стоя: встаньте позади пострадавшего и поставьте свою стопу между его стоп. Обхватите его руками за талию. Сожмите кисть одной руки в кулак, прижмите ее большим пальцем к животу пострадавшего на средней линии чуть выше пупочной ямки и значительно ниже конца мечевидного отростка. Обхватите сжатую в кулак руку кистью другой руки и быстрым толчкообразным движением, направленным кверху, нажмите на живот пострадавшего. Толчки нужно выполнять раздельно и отчетливо до тех пор, пока инородное тело не будет удалено, или пока пострадавший не сможет дышать и говорить, или пока пострадавший не потеряет сознание.
- Хлопки по спине младенца: поддерживайте младенца лицом вниз горизонтально или с несколько опущенным головным концом на левой руке, положенной на твердую поверхность, например, на бедро, причем средним и большим пальцами поддерживайте рот младенца приоткрытым. Проведите до пяти достаточно сильных хлопков по спине младенца открытой ладонью между лопатками.
 Хлопки должны быть достаточной силы. Чем меньше времени прошло с момента аспирации инородного тела – тем легче его удалить.
Хлопки должны быть достаточной силы. Чем меньше времени прошло с момента аспирации инородного тела – тем легче его удалить.
- Толчки в грудь. Если пять хлопков по спине не привели к удалению инородного тела, попробуйте толчки в грудь, которые выполняются так: переверните младенца лицом вверх. Поддерживайте младенца или его спину на своей левой руке. Определите точку выполнения компрессий грудной клетки при ЗМС, то есть приблизительно на ширину пальца выше основания мечевидного отростка. Сделайте до пяти резких толчков в эту точку.
- Толчки в эпигастральную область – прием Геймлиха – можно проводить ребенку старше 2-3 лет, когда паренхиматозные органы (печень, селезенка) надежно скрыты реберным каркасом. Поместите основание ладони в подреберье между мечевидным отростком и пупком и надавите внутрь и вверх.
О выходе инородного тела будет свидетельствовать свистящий/шипящий звук выходящего из легких воздуха и появление кашля.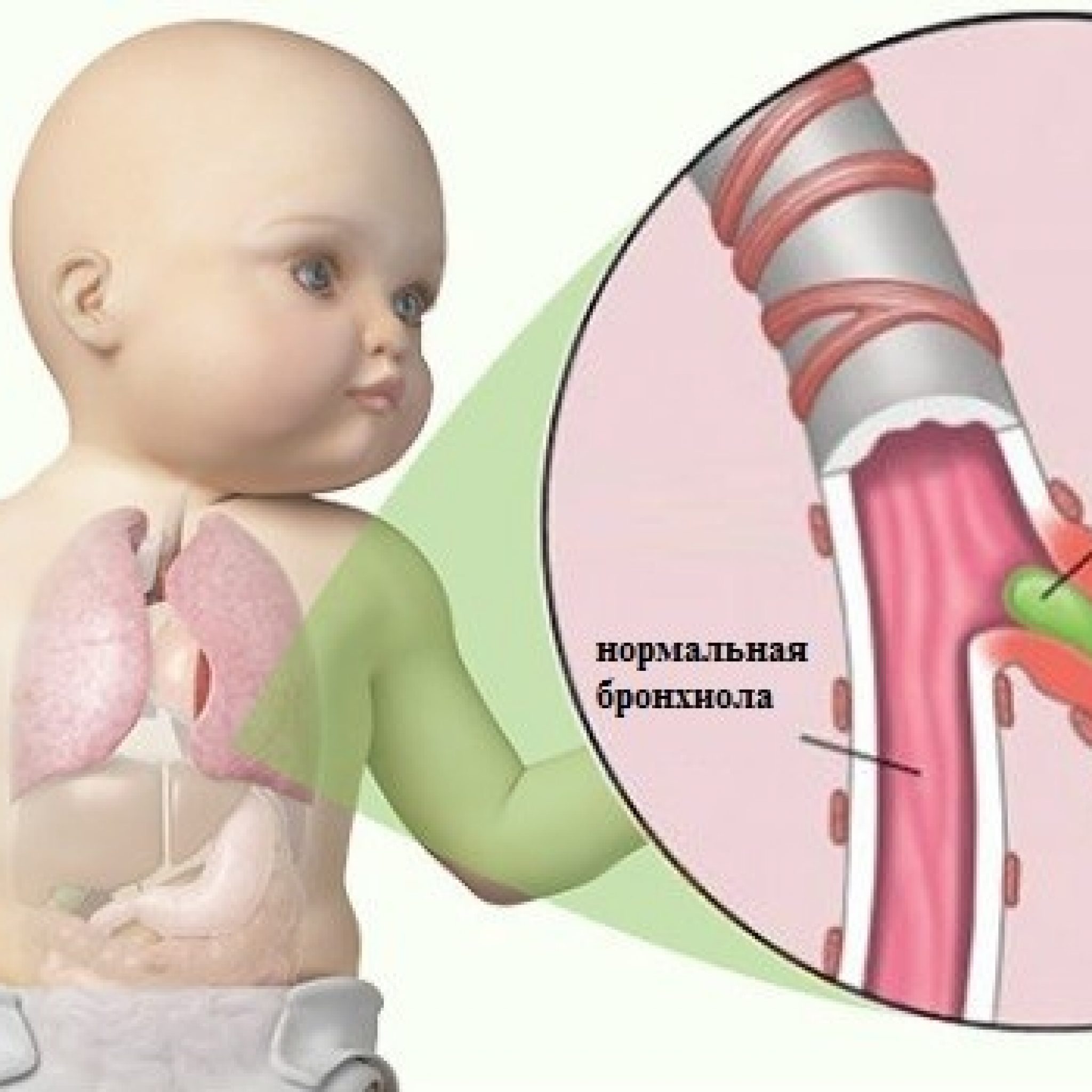
Если пострадавший потерял сознание, выполняйте следующую манипуляцию.
2.2. Пострадавший без сознания.
Уложите пострадавшего на спину, положите одну руку основанием ладони на его живот вдоль средней линии, чуть выше пупочной ямки, достаточно далеко от конца мечевидного отростка. Сверху положите кисть другой руки и надавливайте на живот резкими толчкообразными движениями, направленными к голове, 5 раз с интервалом 1-2 с. Проверьте ABC (проходимость дыхательных путей, дыхание, кровообращение). При отсутствии эффекта от поддиафрагмально-абдоминальных толчков приступайте к коникотомии.
Коникотомия: нащупайте щитовидный хрящ и соскользните пальцем вниз вдоль срединной линии. Следующий выступ – перстневидный хрящ, имеющий форму обручального кольца. Углубление между этими хрящами и будет являться конической связкой. Обработайте шею йодом или спиртом. Зафиксируйте щитовидный хрящ пальцами левой руки (для левшей – наоборот).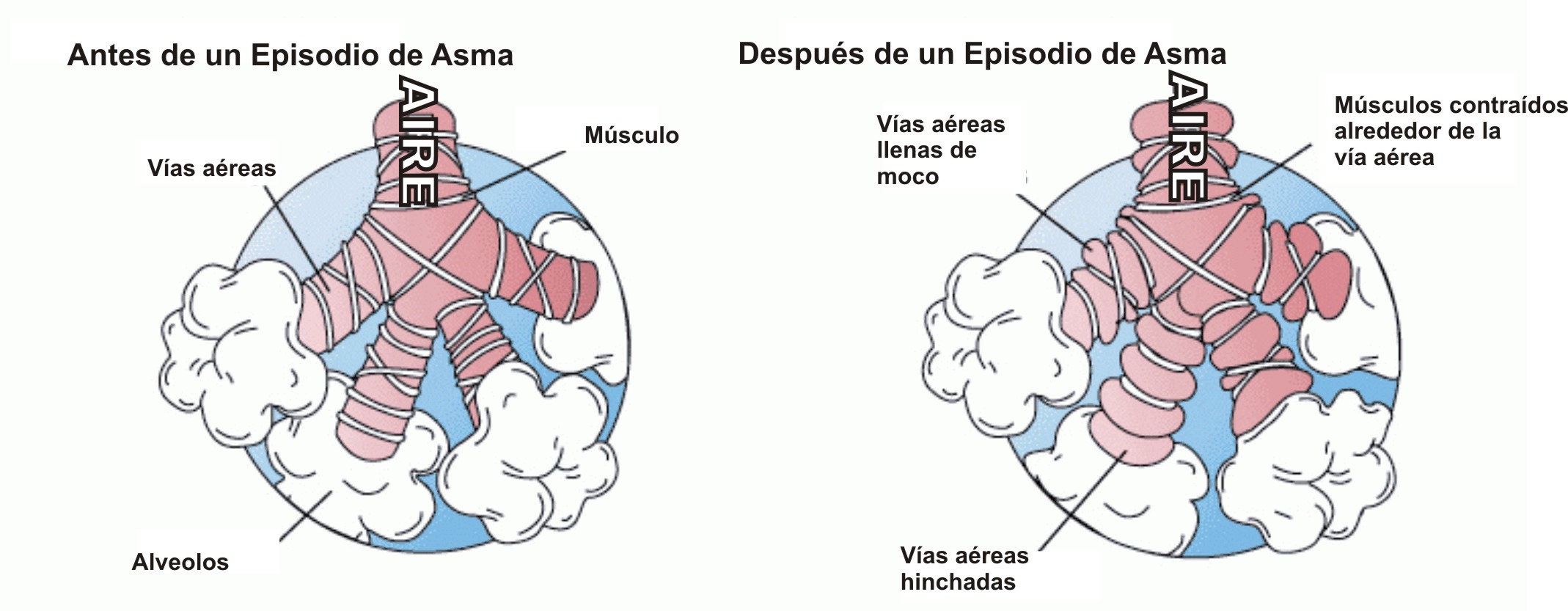 Правой рукой введите коникотом через кожу и коническую связку в просвет трахеи. Выньте проводник.
Правой рукой введите коникотом через кожу и коническую связку в просвет трахеи. Выньте проводник.
У детей до 8 лет, если размер коникотома больше диаметра трахеи, то применяется пункционная коникотомия. Зафиксируйте щитовидный хрящ пальцами левой руки (для левшей – наоборот). Правой рукой введите иглу через кожу и коническую связку в просвет трахеи. Для увеличения дыхательного потока можно последовательно вставить несколько игл.
Всех детей с ИТДП обязательно госпитализируют в стационар, где есть реанимационное отделение и отделение торакальной хирургии или пульмонологическое отделение и где можно выполнить бронхоскопию.
Обструкция дыхательных путей | Бостонская детская больница
Что такое обструкция дыхательных путей?
Если вашему ребенку трудно дышать, он синеет или батарея застряла в ухе, носу или горле, немедленно обратитесь за неотложной медицинской помощью.
Обструкция дыхательных путей, также известная как обструкция дыхательных путей инородным телом, возникает, когда маленький предмет застревает в горле или верхних дыхательных путях ребенка, и ребенку становится трудно дышать. Из-за своего небольшого размера дыхательные пути ребенка могут быть заблокированы, когда кусок пищи или маленький круглый предмет, например, монета или мрамор, застревают в его горле.Другие обычные предметы домашнего обихода, такие как драпированные шнуры или пластиковые пакеты, могут задушить или задушить ребенка.
Из-за своего небольшого размера дыхательные пути ребенка могут быть заблокированы, когда кусок пищи или маленький круглый предмет, например, монета или мрамор, застревают в его горле.Другие обычные предметы домашнего обихода, такие как драпированные шнуры или пластиковые пакеты, могут задушить или задушить ребенка.
В среднем 5000 детей в возрасте 14 лет и младше ежегодно проходят лечение в больничных отделениях неотложной помощи по поводу обструкции дыхательных путей. Большинство этих детей в возрасте 4 лет и младше.
Более 650 детей умирают в течение года от удушения, удушения, удушения или попадания в ловушку с бытовым прибором или сундуком с игрушками.
Как снизить риск обструкции дыхательных путей
Нарезать пищу на мелкие кусочки
Американская академия педиатрии (AAP) рекомендует, чтобы дети младше 4 лет не получали круглую твердую пищу, если пища не нарезана на небольшие некруглые кусочки.Маленькие дети могут неправильно пережевывать пищу, глотать ее целиком и задыхаться. Продукты, которых следует избегать или нарезать небольшими кусочками для детей до 4 лет, включают:
Продукты, которых следует избегать или нарезать небольшими кусочками для детей до 4 лет, включают:
- хот-доги целиком или нарезанные кружками
- куски мяса
- виноград цельный
- попкорн
- арахис и прочие цельные орехи
- семена тыквы и прочие семена
- изюм
- морковь сырая
Детям младше 4 лет нельзя давать леденцы или жевательную резинку.
Маленькие дети могут есть хот-доги и виноград при условии снятия кожуры и нарезания пищи на небольшие некруглые кусочки.
Следите за тем, как ребенок ест
Всегда следите за маленькими детьми, пока они едят. Иногда удушье может возникнуть, когда старший ребенок кормит младшего брата или сестры небезопасной пищей. Убедитесь, что ваши маленькие дети сидят прямо во время еды, и никогда не позволяйте им ходить, играть или бегать с едой во рту.
Держите подальше от удушья
Маленькие, круглые или подходящие непродовольственные товары могут стать причиной удушья для вашего маленького ребенка.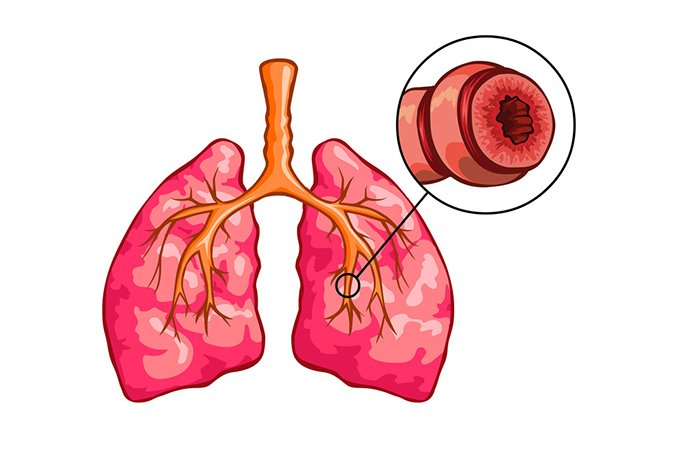 Вы можете приобрести тестер мелких деталей, чтобы определить, какие предметы представляют опасность удушья. Убедитесь, что ваш ребенок играет с игрушками, подходящими для его возраста, держите подальше от мелких предметов, которые могут подавиться. Проверьте под мебелью и между подушками сиденья на предмет опасности удушья, например:
Вы можете приобрести тестер мелких деталей, чтобы определить, какие предметы представляют опасность удушья. Убедитесь, что ваш ребенок играет с игрушками, подходящими для его возраста, держите подальше от мелких предметов, которые могут подавиться. Проверьте под мебелью и между подушками сиденья на предмет опасности удушья, например:
- монет
- маленькие шары
- Воздушные шары (надутые и спущенные)
- мрамора
- мелкие детали игры
- мелкие детали игрушек
- английские булавки
- ювелирные изделия
- пуговицы
- колпачки для ручек
- круглые батарейки в форме монет (как для часов)
Устранение опасности удушения и удушения
Дети могут задушить себя потребительскими товарами, которые оборачиваются вокруг шеи, такими как оконные шторы и шнуры для драпировки, ленты, ожерелья, завязки для пустышек и завязки на одежде.Несколько советов, которые нужно иметь в виду, чтобы обезопасить своего ребенка:
- Свяжите или перережьте все оконные шторы и шнуры драпировки и снимите завязки с капюшона и шеи с верхней одежды ваших детей.
- Не позволяйте ребенку носить ожерелья, кошельки, шарфы или одежду с завязками на игровом оборудовании.
- Не позволяйте вашему ребенку играть на креслах-мешках, содержащих небольшие поролоновые гранулы — если кресло-мешок порвется, ваш ребенок может вдохнуть и подавиться гранулами.
- Не позволяйте маленькому ребенку играть со стрелковыми игрушками. Стрела, дротик или дробина могут стать причиной удушья, если выстрелить ребенку в рот.
- Убедитесь, что расстояние между ограждениями кровати, рамой и всеми пространствами в изголовье и подножках не превышает 3,5 дюйма. Небольшие проходы, через которые проходит тело ребенка, но не голова, могут задушить ребенка. Сюда входят места на двухъярусных кроватях, детских кроватках, игровых площадках, детских колясках, колясках и стульчиках для кормления.
Устранение опасности удушья
Младенцы могут задохнуться в мягкой постели или когда человек перевернется на них в постели для взрослых.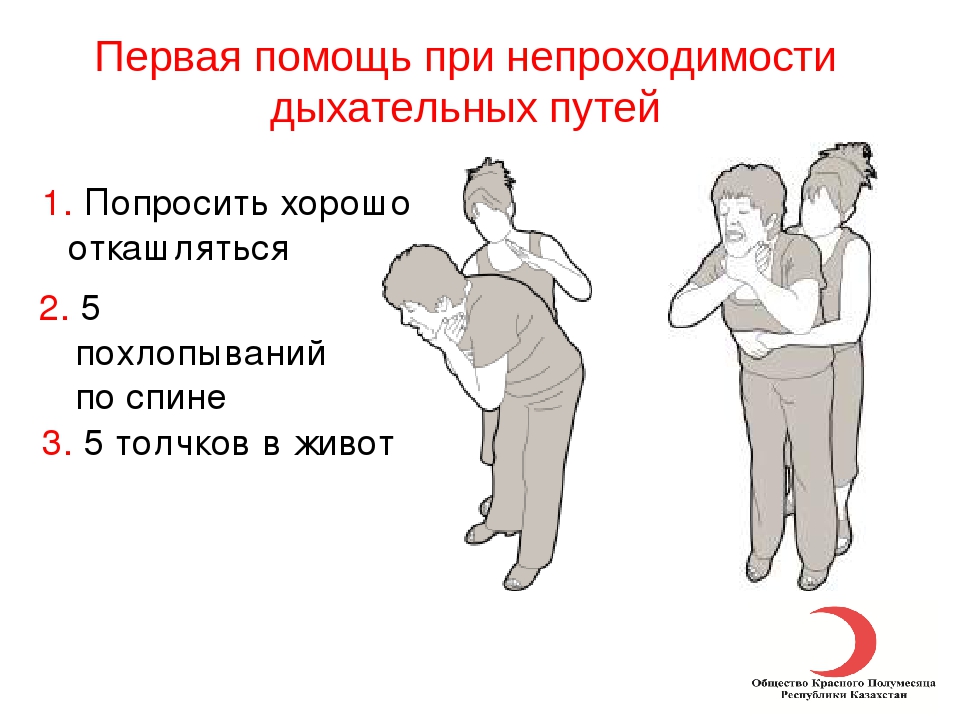 Вот еще несколько советов, которые помогут предотвратить удушье:
Вот еще несколько советов, которые помогут предотвратить удушье:
- Выбросьте пластиковые пакеты и полиэтиленовую пленку, которые могут закрыть нос и рот и задушить маленького ребенка.
- Снимите дверцы неиспользуемых бытовых приборов и крышки с игрушечных сундуков, чтобы дети не застряли внутри и не задохнулись.
- Не позволяйте детям младше 6 лет спать на верхней койке двухъярусной кровати, так как они могут задохнуться или задохнуться в случае падения.
Уложить спящих младенцев на спину
Медицинское сообщество рекомендует помещать младенцев на спину в их кроватки, чтобы снизить риск синдрома внезапной детской смерти (СВДС).Размещение младенцев на спине также может снизить вероятность удушья. Младенцам может быть трудно поднимать голову, если они лежат лицом вниз. Детская кроватка должна соответствовать национальным стандартам безопасности и иметь жесткий плоский матрас. Не кладите мягкое постельное белье, игрушки и другие мягкие предметы, подушки и одеяла в кроватку вместе с младенцем.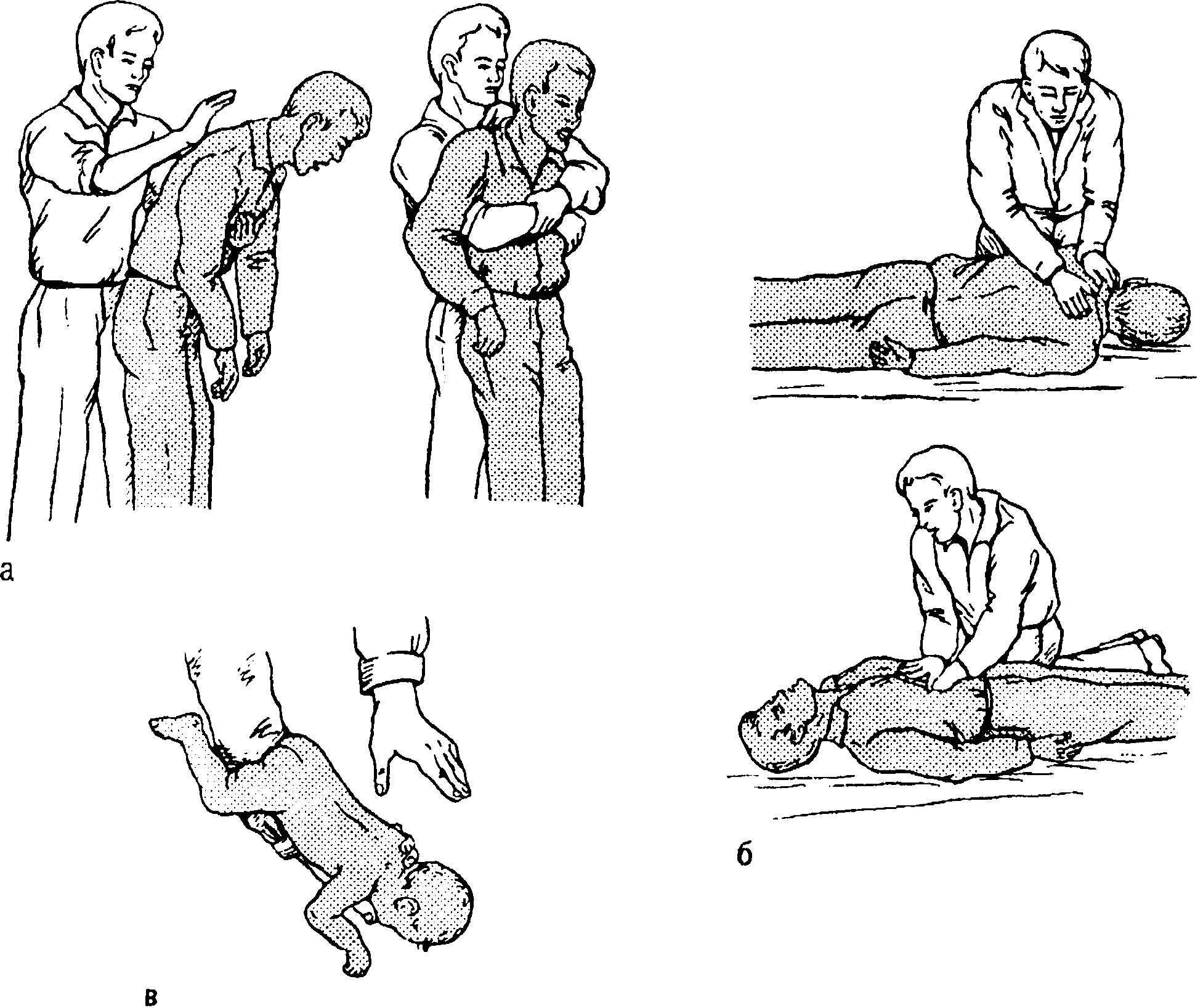
Как мы лечим обструкцию дыхательных путей
Бостонская детская больница имеет одну из крупнейших педиатрических бригад отоларингологов (ушей, носа и горла) в стране.Наш отдел отоларингологии и улучшения коммуникации ежегодно обслуживает более 60 000 младенцев, детей, подростков и молодых людей в Бостоне и в пяти дополнительных пунктах в Уолтеме, Пибоди, Уэймуте, Лексингтоне и Северном Дартмуте.
Обструкция верхних дыхательных путей в педиатрии | 2012-01-01
Обструкция верхних дыхательных путей в педиатрии
Авторы:
Мэтью Р. Леду, доктор медицинских наук , доцент, педиатрическая реанимация, Университет Восточной Каролины, Медицинская школа Броди, Гринвилл, NC.
Рональд М. Перкин, доктор медицины, MA , профессор и заведующий кафедрой педиатрии Медицинской школы Броуди, Университет Восточной Каролины, Гринвилл, Северная Каролина.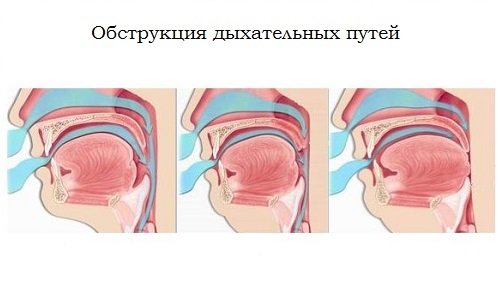
Рецензент:
Газала К. Шарифф, доктор медицинских наук, FACEP, FAAEM , директор педиатрической неотложной медицины, Система здравоохранения Паломар Померадо / Врачи скорой помощи Калифорнии; Медицинский директор Центра неотложной помощи детской больницы Рэди, доцент Калифорнийского университета в Сан-Диего.
Полная обструкция верхних дыхательных путей является редким осложнением заболеваний у педиатрических пациентов; однако он должен оставаться в центре внимания дифференциального диагноза, потому что он может внезапно стать сценарием жизни или смерти. Давно известно, что респираторная недостаточность является основной причиной остановки сердца у детей. 1
Этиология варьируется от инфекционных причин до неинфекционных причин или наследственного ангионевротического отека. Авторы рассматривают общие презентации, соответствующую диагностическую оценку и стратегии лечения болезненных процессов, которые могут вызывать обструкцию верхних дыхательных путей.
— Редактор
Введение
Определение обструкции верхних дыхательных путей — это сужение нормальных дыхательных путей над уровнем входного отверстия грудной клетки, включая верхнюю трахею над манубрием. Педиатрические пациенты подвержены более высокому риску полной обструкции и могут проявлять симптомы даже при небольшом сужении их дыхательных путей. Поскольку сопротивление пропорционально длине трубы, но обратно пропорционально радиусу трубы в четвертой степени, препятствие, которое сокращает радиус вдвое, потребует изменения давления в 16 раз для поддержания того же ламинарного потока воздуха, и потенциально 32 раза (r5) для турбулентного потока.У очень маленького младенца даже при малейшем сужении может возникнуть сильное недомогание и затрудненное дыхание. Поскольку обструкция возникает ближе к связкам и подсвязочной области, часто слышен классический стридор. Закупорка трахеи на уровне входного отверстия грудной клетки будет слышна как стридор или пронзительный свист.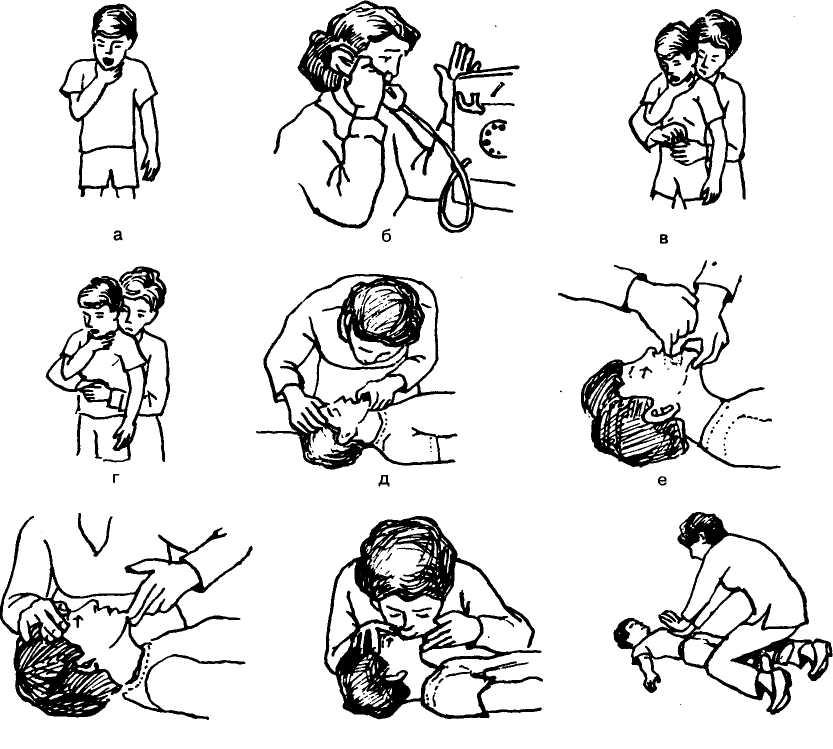
Пациент, поступающий в отделение неотложной помощи с респираторной недостаточностью, должен быть обследован быстро. Эта быстрая оценка должна включать оценку серьезности дистресса и быструю оценку наиболее вероятной этиологии.В случае наличия у пациента стридора или других симптомов, связанных с обструкцией верхних дыхательных путей, различия часто делятся на острые и хронические, а также инфекционные и неинфекционные причины. Инфекционные причины, обсуждаемые в этой статье, включают круп, перитонзиллярные и заглоточные абсцессы, эпиглоттит и бактериальный трахеит. Неинфекционные причины включают инородное тело, проглатывание / ожоги, травмы и наследственный ангионевротический отек.
Инфекционные причины
Инфекции, бактериальные или вирусные, как правило, являются наиболее частой причиной острой обструкции верхних дыхательных путей.Бактериальные причины включают дифтерию (редко и не обсуждаемую в этой статье), бактериальный трахеит и эпиглоттит. Однако наиболее частыми инфекционными причинами острой обструкции верхних дыхательных путей являются вирусы. На парагрипп приходится примерно 75% случаев вирусных инфекций, вызывающих некоторую степень обструкции дыхательных путей, при этом на другие вирусы, включая грипп A и B, аденовирус, респираторно-синцитиальный вирус (RSV) и корь, приходится еще 25%. 2
Однако наиболее частыми инфекционными причинами острой обструкции верхних дыхательных путей являются вирусы. На парагрипп приходится примерно 75% случаев вирусных инфекций, вызывающих некоторую степень обструкции дыхательных путей, при этом на другие вирусы, включая грипп A и B, аденовирус, респираторно-синцитиальный вирус (RSV) и корь, приходится еще 25%. 2
Круп. Эпидемиология. Также известный как ларинготрахеит, он чаще всего поражает детей в возрасте от 6 месяцев до 3 лет. Согласно многочисленным исследованиям, заболеваемость крупом в этой возрастной группе колеблется в пределах 1,5-6%. Это чаще встречается у мальчиков, и впоследствии их госпитализируют чаще, чем девочек. Кроме того, было обнаружено, что госпитализация более вероятна в возрастной группе младше 1 года, чем в возрастной группе 1–4 года. 3
Этиология. Круп чаще всего вызывается вирусной инфекцией гортани и трахеи.Вирусные инфекции были обнаружены методом ПЦР у 80% пациентов с диагнозом круп. 4 Вирусная инфекция вызывает отек и припухлость подсвязочной области трахеи, вызывая сужение и, таким образом, характерный стридор. Хотя замешаны многие вирусы, наиболее частой причиной является парагрипп 1 типа; однако также были задействованы типы 2 и 3. 4 Другие вирусные причины включают риновирус, энтеровирусы, грипп A и B, коронавирус, а также метапневмовирус человека.
4 Вирусная инфекция вызывает отек и припухлость подсвязочной области трахеи, вызывая сужение и, таким образом, характерный стридор. Хотя замешаны многие вирусы, наиболее частой причиной является парагрипп 1 типа; однако также были задействованы типы 2 и 3. 4 Другие вирусные причины включают риновирус, энтеровирусы, грипп A и B, коронавирус, а также метапневмовирус человека.
Презентация. Круп имеет типичное проявление, вызванное ограниченным или турбулентным потоком воздуха, проходящим мимо уровня подсвязочного канала, на котором происходит воспалительный процесс. Произведенная турбулентность вызывает классическое физическое обнаружение инспираторного стридора. Помимо стридора при физикальном обследовании, у пациента часто наблюдается лающий кашель. Может присутствовать субфебрильная температура и насморк.
Пациенты с крупом и значительным стридором часто обращаются в отделение неотложной помощи с респираторной недостаточностью.Westley et al. В 1978 г. опубликовали клиническую систему баллов для определения уровня респираторного дистресса. Он использовал уровень сознания, цианоз, стридор, аускулятивные данные и ретракцию, чтобы оценить уровень дистресса. 5 Это часто цитируется и используется при исследованиях и публикациях; однако это не имеет большого значения в клинической практике. Более уместно, рекомендации по клинической практике Альберты включают полезную классификацию, основанную на физических данных, и делят круп на легкий, средний и тяжелый. 6,7 ( См. Таблицу 1. ) Этот инструмент можно использовать для первоначальной оценки, а также для оценки прогрессирования заболевания. Диагноз круп обычно ставится клинически, и рентген обычно не показан. Однако, если это сделано для исключения другой патологии (ФБ, эпиглоттит), сужение верхних дыхательных путей, называемое «ступенчатым признаком», является классическим для крупа.
В 1978 г. опубликовали клиническую систему баллов для определения уровня респираторного дистресса. Он использовал уровень сознания, цианоз, стридор, аускулятивные данные и ретракцию, чтобы оценить уровень дистресса. 5 Это часто цитируется и используется при исследованиях и публикациях; однако это не имеет большого значения в клинической практике. Более уместно, рекомендации по клинической практике Альберты включают полезную классификацию, основанную на физических данных, и делят круп на легкий, средний и тяжелый. 6,7 ( См. Таблицу 1. ) Этот инструмент можно использовать для первоначальной оценки, а также для оценки прогрессирования заболевания. Диагноз круп обычно ставится клинически, и рентген обычно не показан. Однако, если это сделано для исключения другой патологии (ФБ, эпиглоттит), сужение верхних дыхательных путей, называемое «ступенчатым признаком», является классическим для крупа.
Таблица 1. Клиническая оценка крупа в Альберте
Оценка степени тяжести крупа | |
Мягкая | Периодически лающий кашель Нет стридора в состоянии покоя Слабые ретракции или их отсутствие |
Умеренная | Частый лающий кашель Звуковой стридор в состоянии покоя Надгрудинная ретракция в покое Без волнения или беспокойства |
Тяжелая | Частый лающий кашель Выдающийся инспираторный стридор Случайный стридор выдоха Отмеченные опровержения Волнение и бедствие |
Лечение. Как и в случае любой причины респираторного дистресса, врач должен быстро оценить ABC и действовать соответствующим образом. Сначала ребенку можно дать немного увлажненного кислорода, чтобы обеспечить надлежащую оксигенацию. Нет никаких доказательств того, что использование увлажненного воздуха (теплого или прохладного тумана) играет какую-либо роль в улучшении симптомов. 8-10 Тем не менее, есть некоторые мнения, что это может помочь с выделениями и увлажнить слизистую дыхательных путей и сделать ребенка более комфортным.Рекомендуется свести к минимуму ненужные вмешательства, поскольку расстроенный, сердитый ребенок может значительно усугубить степень обструкции.
Как и в случае любой причины респираторного дистресса, врач должен быстро оценить ABC и действовать соответствующим образом. Сначала ребенку можно дать немного увлажненного кислорода, чтобы обеспечить надлежащую оксигенацию. Нет никаких доказательств того, что использование увлажненного воздуха (теплого или прохладного тумана) играет какую-либо роль в улучшении симптомов. 8-10 Тем не менее, есть некоторые мнения, что это может помочь с выделениями и увлажнить слизистую дыхательных путей и сделать ребенка более комфортным.Рекомендуется свести к минимуму ненужные вмешательства, поскольку расстроенный, сердитый ребенок может значительно усугубить степень обструкции.
Испытания показали, что адреналин улучшает тяжесть крупа у пациентов со значительными симптомами. Обзор Кокрановской базы данных показывает убедительные доказательства того, что аэрозоли адреналина имеют хороший эффект в течение 30 минут после введения и могут потребовать повторного введения. 11 Необходимо тщательно контролировать основные побочные эффекты тахикардии, особенно у младенцев, у которых может развиться наджелудочковая тахикардия.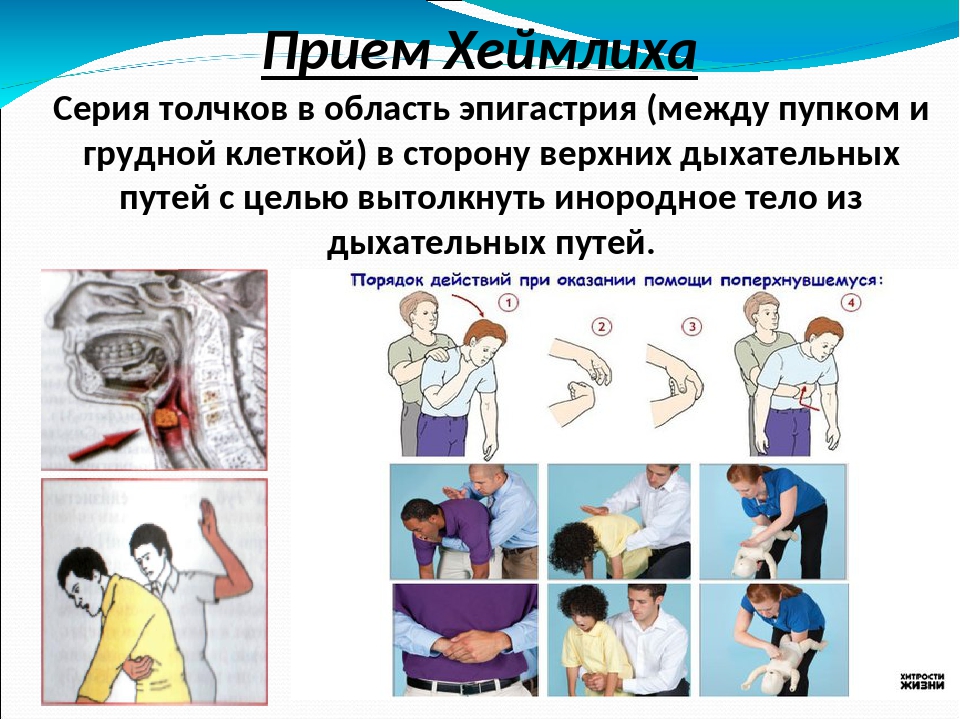 Если вводится рацемический адреналин, следует также назначить дозу стероидов.
Если вводится рацемический адреналин, следует также назначить дозу стероидов.
Лечение кортикостероидами повсеместно признано стандартом лечения даже легкого крупа, оцениваемого в медицинских учреждениях. Однократная доза, вводимая перорально или внутримышечно / внутривенно, составляющая 0,6 мг / кг дексаметазона, показала свою эффективность. Результаты рандомизированных контролируемых исследований убедительно свидетельствуют о том, что глюкокортикоиды полезны; однако есть также некоторые свидетельства того, что даже более низкие дозы перорального дексаметазона могут быть столь же эффективными.Двойное слепое исследование не показало различий в приеме перорального дексаметазона в разовой дозе 0,15, 0,3 и 0,6 мг в зависимости от продолжительности госпитализации и облегчения симптомов. 12 Кортикостероиды не только снижают оценку тяжести через 6 часов, но и уменьшают количество повторных посещений, госпитализаций и обращений в отделения неотложной помощи. 13 Существует мнение экспертов, что многократные дозы не требуются и могут увеличить риск побочных эффектов. Будесонид традиционно используется в виде небулайзерной формы, а доза составляет 2 мг на 4 мл распыляемой формы.
Будесонид традиционно используется в виде небулайзерной формы, а доза составляет 2 мг на 4 мл распыляемой формы.
Heliox (смесь гелия и кислорода) — еще один метод лечения крупа. Однако Кокрановский обзор гелиокса для крупа (два рандомизированных контролируемых испытания), в котором сравнивали гелиокс с 30% увлажненным кислородом и 100% кислород с рацемическим распылением адреналина, не обнаружил значительных изменений в баллах по крупу среди пациентов, получавших гелиокс, по сравнению с контрольной группой. Эти исследования не показывают реальной пользы от использования гелиокса. 14 Следует отметить, что более мелкие исследования показали некоторое улучшение показателей крупа при применении гелиокса, но по сравнению с рацемическим адреналином не было никакой разницы в улучшении показателей крупа между двумя методами лечения. 15
В отделении неотложной помощи часто применяется пошаговый подход в зависимости от степени тяжести симптомов.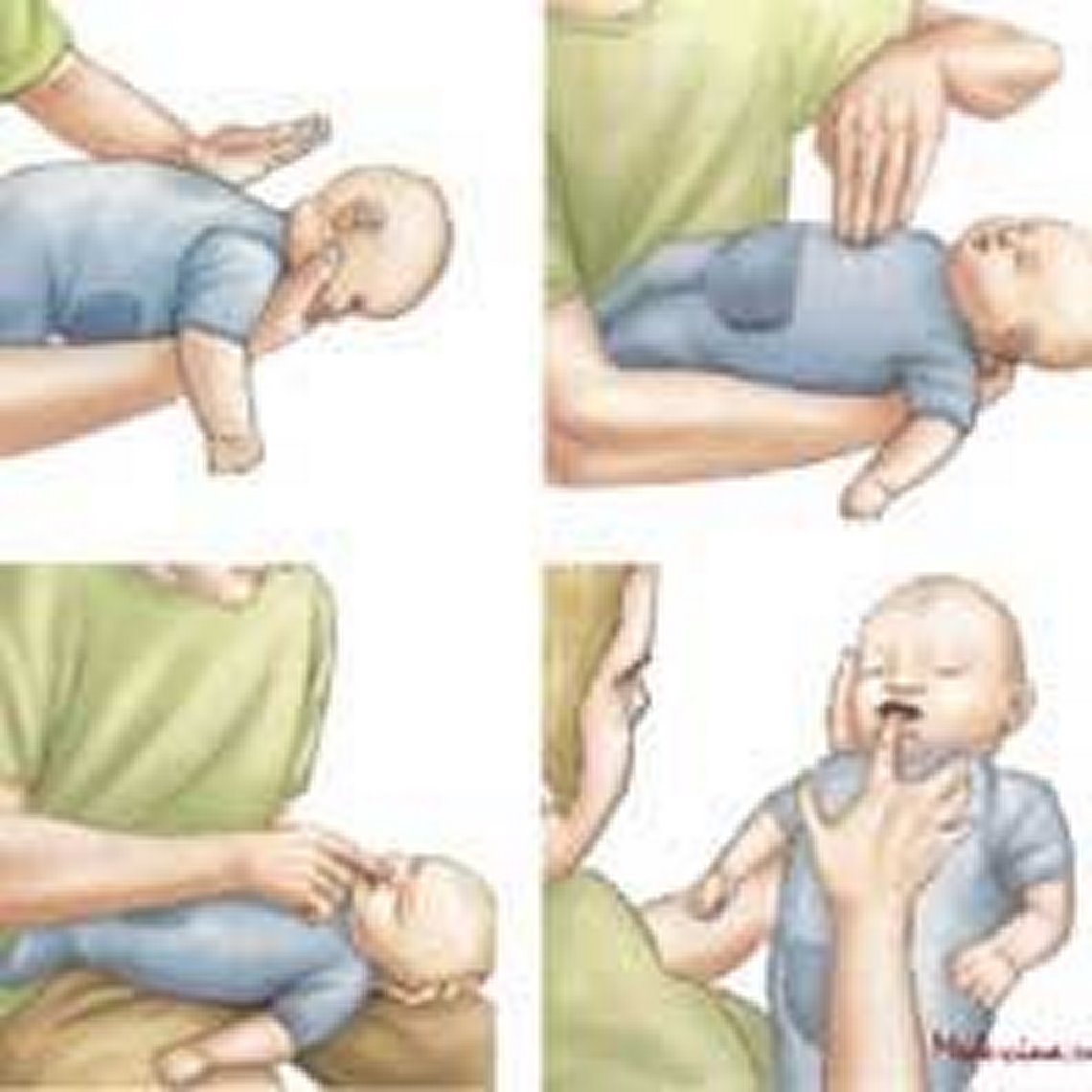 Используя Практические рекомендации Альберты для определения степени тяжести, указанной в таблице 1, врач может разделить степень тяжести крупа на легкую, среднюю или тяжелую. При легких симптомах доза стероидов может быть адекватным лечением с последующей выпиской из дома и семейным обучением. Однако при умеренных симптомах могут потребоваться стероиды с более длительным периодом наблюдения до 4 часов с госпитализацией, если улучшение симптомов не наступает.Что касается тяжелых симптомов, вначале обычно требуются стероиды, а также небулайзерный адреналин. Пациенты, которые изначально были тяжелыми, могут быть выписаны, если их симптомы не вернутся, и они находятся под наблюдением в течение определенного периода времени. Если у пациентов наблюдаются повторяющиеся тяжелые симптомы или изменение психического статуса, скорее всего, будет показана госпитализация в педиатрическое отделение интенсивной терапии (PICU). Алгоритмы, подобные Руководству по клинической практике Альберты, помогают составить план терапии и выписки.
Используя Практические рекомендации Альберты для определения степени тяжести, указанной в таблице 1, врач может разделить степень тяжести крупа на легкую, среднюю или тяжелую. При легких симптомах доза стероидов может быть адекватным лечением с последующей выпиской из дома и семейным обучением. Однако при умеренных симптомах могут потребоваться стероиды с более длительным периодом наблюдения до 4 часов с госпитализацией, если улучшение симптомов не наступает.Что касается тяжелых симптомов, вначале обычно требуются стероиды, а также небулайзерный адреналин. Пациенты, которые изначально были тяжелыми, могут быть выписаны, если их симптомы не вернутся, и они находятся под наблюдением в течение определенного периода времени. Если у пациентов наблюдаются повторяющиеся тяжелые симптомы или изменение психического статуса, скорее всего, будет показана госпитализация в педиатрическое отделение интенсивной терапии (PICU). Алгоритмы, подобные Руководству по клинической практике Альберты, помогают составить план терапии и выписки.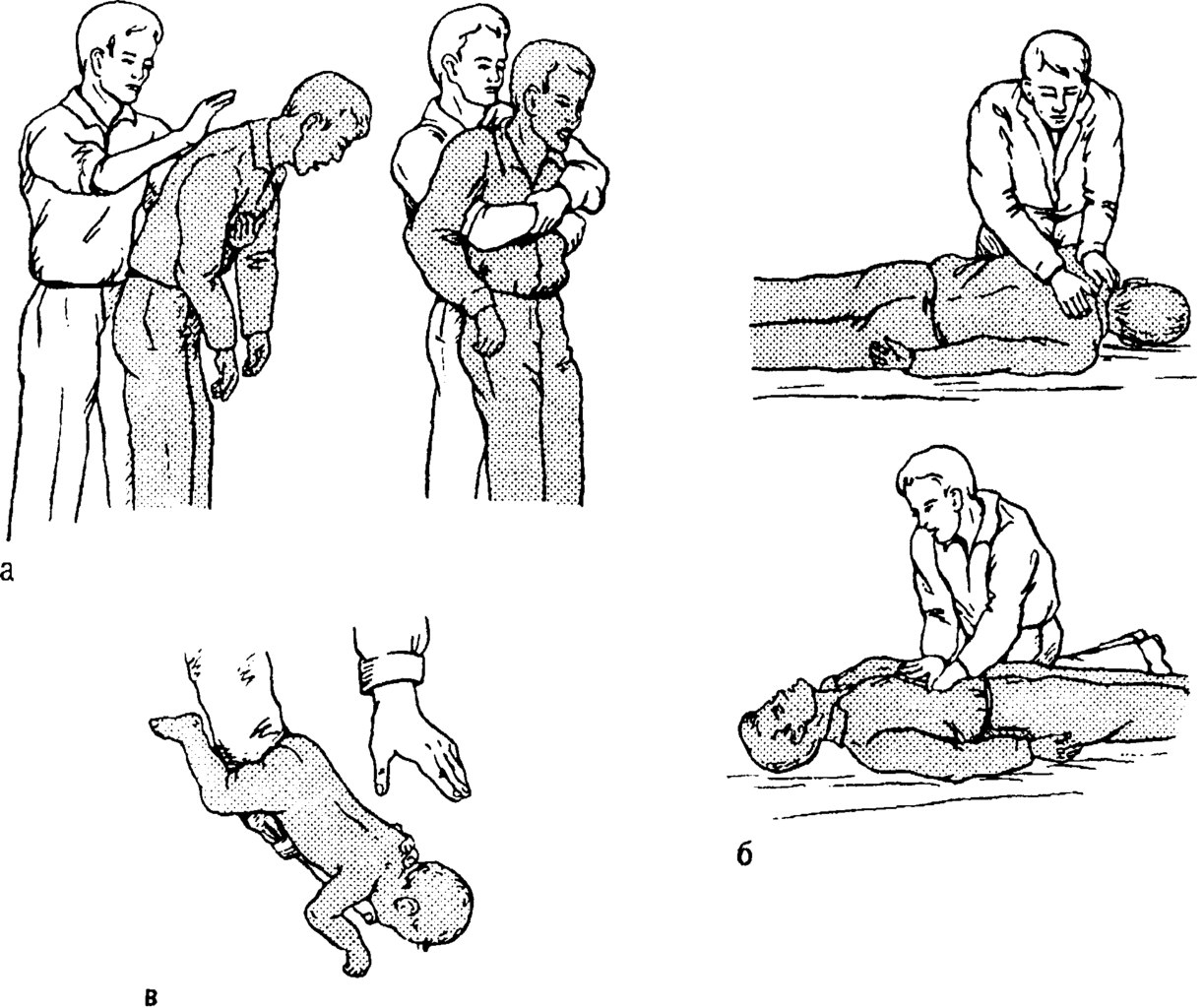 6 Все пациенты, которым требуется несколько доз рацемического адреналина или у которых сохраняется стридор в состоянии покоя, должны быть госпитализированы. 6 ( См. Таблицу 2. )
6 Все пациенты, которым требуется несколько доз рацемического адреналина или у которых сохраняется стридор в состоянии покоя, должны быть госпитализированы. 6 ( См. Таблицу 2. )
Таблица 2. Доказательное управление крупом
Уровень серьезности | Симптомы | Лечение | Распоряжение |
* Альтернативой дексаметазону, особенно у детей, не переносящих пероральный прием, может быть распыленный будесонид 2 мг. ** Подробнее об основанном на доказательствах управлении см. В тексте. | |||
Мягкая | Без стридора Барки кашель Отзывов нет | Дексаметазон перорально / внутримышечно 0,6 мг / кг * | Выписка из дома |
Умеренная | Частый кашель Стридор в состоянии покоя Отзывов Не терпит бедствия | Дексаметазон PO / IM 0. | Отсутствие или минимальное улучшение, рассмотреть вопрос о госпитализации после периода наблюдения В случае улучшения выписать домой |
Тяжелая | Частый кашель Выступающий стридор Отмеченные опровержения Возбуждение или беспокойство | Дексаметазон PO / IM 0.6 мг / кг Распыленный рацемический эпинефрин 2,25% 0,5 мл в 2,5 мл физиологического раствора; при необходимости повторить; мониторинг HR Продувка кислородом по необходимости | Если состояние не улучшилось или не возобновилось, рассмотрите возможность госпитализации в ОИТ Если симптомы исчезнут или после наблюдения они станут легкими, можно выписать домой |
Глубокие инфекции шеи
Перитонзиллярный абсцесс и заглоточный абсцесс — это инфекции глубоких тканей шеи.Они часто вызывают серьезное беспокойство и могут вызвать осложнение в виде непроходимости и аспирации, если абсцесс разрывается.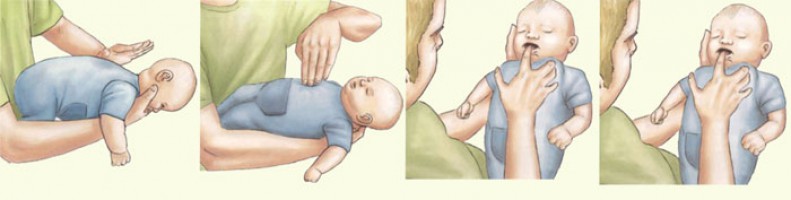
Перитонзиллярный абсцесс. Клиническая презентация. Как правило, у пациента в анамнезе имеется боль в горле, а также боль при глотании. В анамнезе может быть предыдущий перитонзиллярный абсцесс, и родители могут обнаружить, что ребенок храпит и страдает апноэ во сне. При осмотре рта и глотки обнаруживается чрезвычайно болезненная задняя часть глотки с эритемой и припухлостью.Обычно перитонзиллярный абсцесс представляет собой одностороннюю инфекцию с характерным отклонением язычка в противоположную сторону. Также отмечается флюктуация миндалин, но необходимо соблюдать осторожность, чтобы не допустить разрыва абсцесса при пальпации. Двусторонний перитонзиллярный абсцесс описан в литературе, но встречается редко. 16 Двусторонние абсцессы могут не проявляться с отклонением язычка. Еще одна классическая находка при перитонзиллярном абсцессе — тризм внутренней крыловидной мышцы лица.Об этом сообщалось примерно у двух третей пациентов. 17 Кроме того, при осмотре часто обнаруживаются увеличенные подчелюстные лимфатические узлы.
Хотя в большинстве случаев визуализация не требуется, при необходимости предпочтительным режимом визуализации является КТ с контрастированием. Перитонзиллярный абсцесс следует рассматривать как скопление жидкости с кольцевым расширением перитонзиллярного пространства. Если компьютерная томография или клиническое обследование подтверждают перитонзиллярный абсцесс, следует обратиться за консультацией к ЛОРу.Седация не должна использоваться во время визуализации, если присутствует какая-либо степень обструкции верхних дыхательных путей, поскольку седация может усугубить респираторный дистресс.
Менеджмент. Необходимо дренировать перитонзиллярный абсцесс и получить консультацию ЛОР после того, как диагноз будет поставлен с помощью осмотра или КТ. Доступны три различных метода дренирования (пункционная аспирация, разрез и дренирование или тонзиллэктомия).
Некоторых пожилых пациентов можно лечить амбулаторно, если они хорошо гидратированы, могут поддерживать гидратацию, могут пройти либо пункционную аспирацию, либо разрез и дренирование, а также принимать антимикробную терапию через рот. Однако это может быть невозможно, если пациент моложе 10 лет и / или уже имеет обезвоживание и боль в такой степени, с которой невозможно справиться дома. В этом случае пациент должен быть госпитализирован для внутривенного введения жидкости, обезболивания и парентерального введения антибиотиков.
Однако это может быть невозможно, если пациент моложе 10 лет и / или уже имеет обезвоживание и боль в такой степени, с которой невозможно справиться дома. В этом случае пациент должен быть госпитализирован для внутривенного введения жидкости, обезболивания и парентерального введения антибиотиков.
Парентеральные антибиотики следует выбирать с осторожностью, чтобы избежать полимикробной природы этих инфекций. Прикрываться должны не только стафилококки и стрептококки, но и анаэробы. Выбор антибиотиков можно будет скорректировать после получения результатов посева.Выбор антибиотика может включать ампициллин-сульбактам, клиндамицин и / или ванкомицин. 18 ( См. Таблицу 3. )
Таблица 3. Лечение глубоких инфекций шеи
Парентерально | ||
Лекарство | Доза | Частота |
Ампициллин-сульбактам | 50-100 мг / кг / доза | Каждые 6 часов |
Клиндамицин | 25-40 мг / кг / сут | Каждые 6-8 часов |
+/- Ванкомицин | 40 мг / кг / день | Делится каждые 6-8 часов |
или линезолид | 10 мг / кг / доза 600 мг / доза (дети> 12 лет) | Каждые 8 часов Каждые 12 часов |
Некоторые врачи отдают предпочтение глюкокортикоидам. Однако доказательства, лежащие в основе таких рекомендаций, ограничены. Есть одно испытание с использованием глюкокортикоидов у пациентов старше 16 лет, и, по-видимому, в группе стероидов наблюдалось более быстрое улучшение симптомов. Однако в настоящее время имеется ограниченное количество доказательств универсальной рекомендации по применению стероидов. 18
Однако доказательства, лежащие в основе таких рекомендаций, ограничены. Есть одно испытание с использованием глюкокортикоидов у пациентов старше 16 лет, и, по-видимому, в группе стероидов наблюдалось более быстрое улучшение симптомов. Однако в настоящее время имеется ограниченное количество доказательств универсальной рекомендации по применению стероидов. 18
Заглоточный абсцесс. Заглоточный абсцесс — это инфекция пространства между претрахеальной фасцией и крыловидной фасцией шеи.Это потенциальное пространство проходит от основания черепа до средостения и содержит лимфатические узлы (узлы Рувье) у маленьких детей. Эти лимфатические узлы обычно атрофируются в период полового созревания, что объясняет, почему подростки и молодые люди редко болеют этим типом инфекции, которая чаще всего встречается у детей в возрасте 2-4 лет.
Презентация. Как и при многих других инфекциях шеи, пациенты могут обращаться с болью в горле, лихорадкой и дискомфортом. Однако степень тяжести заглоточного абсцесса прогрессирует по мере того, как инфекция отслеживает фасциальную плоскость.У пациентов часто наблюдаются дисфазия и одинофагия. У них может быть жар и отек шеи с множественным увеличением лимфатических узлов на шее. Эти пациенты также могут иметь респираторный дистресс в зависимости от поражения дыхательных путей. При появлении симптомов обследующий должен проявлять осторожность, чтобы не усугубить респираторный дистресс из-за выполнения ненужных процедур. Пациенты с заглоточным абсцессом также могут быть похожи на пациентов с перитонзиллярным абсцессом или эпиглоттитом с изменениями качества голоса, а также слюнотечением и позой для поддержания проходимости дыхательных путей.При осмотре иногда может визуализироваться односторонний отек задней части глотки или одностороннее образование на шее, если абсцесс распространился латерально. Независимо от причины их симптомов, этих пациентов следует наблюдать на предмет острого ухудшения состояния и, возможно, их нужно будет доставить в операционную для защиты дыхательных путей.
Однако степень тяжести заглоточного абсцесса прогрессирует по мере того, как инфекция отслеживает фасциальную плоскость.У пациентов часто наблюдаются дисфазия и одинофагия. У них может быть жар и отек шеи с множественным увеличением лимфатических узлов на шее. Эти пациенты также могут иметь респираторный дистресс в зависимости от поражения дыхательных путей. При появлении симптомов обследующий должен проявлять осторожность, чтобы не усугубить респираторный дистресс из-за выполнения ненужных процедур. Пациенты с заглоточным абсцессом также могут быть похожи на пациентов с перитонзиллярным абсцессом или эпиглоттитом с изменениями качества голоса, а также слюнотечением и позой для поддержания проходимости дыхательных путей.При осмотре иногда может визуализироваться односторонний отек задней части глотки или одностороннее образование на шее, если абсцесс распространился латерально. Независимо от причины их симптомов, этих пациентов следует наблюдать на предмет острого ухудшения состояния и, возможно, их нужно будет доставить в операционную для защиты дыхательных путей.
Возможны боковые рентгенограммы шеи; однако правильное положение пациента важно . Когда голова пациента полностью вытянута, можно оценить расширение превертебрального пространства.Расширение более 7 мм на уровне C2 и 14 мм на уровне C6 обычно считается значительным. 19 Может потребоваться визуализация шеи, и золотым стандартом диагностики является компьютерная томография с внутривенным контрастированием. ( См. Рисунки 1 и 2. ) Базовые лабораторные исследования не требуются, но могут быть получены, и пациенты с заглоточным абсцессом часто имеют повышенное содержание лейкоцитов. Однако наличие бактериемии не является обычным явлением.
Рис. 1. Заглоточный абсцесс
Рисунок 2.Заглоточный абсцесс
10-месячный ребенок обратился с жалобой на слюнотечение и отек шеи. Компьютерная томография выявила большой заглоточный абсцесс размером 1,8 см в передне-заднем отделе, 6,8 см в боковом направлении и 7,5 см в вертикальном направлении (рис. 1 и 2).
Лечение. Как и другие инфекции глубокого отдела шеи, заглоточный абсцесс обычно является полимикробной инфекцией, преобладающими видами которой являются стафилококк, стрептококк и анаэробы глотки.Первоначально лечение должно быть парентеральными антибиотиками широкого спектра действия. ( См. Таблицу 3. ) Если заглоточный абсцесс подозревается или подтверждается компьютерной томографией, пациенты должны быть госпитализированы для внутривенного введения антибиотиков и консультации от ЛОР по поводу хирургического дренирования. Две основные характеристики, которые, по-видимому, предсказывают осложненное течение, — это пациенты с обструктивными симптомами, требующими госпитализации и вмешательства на дыхательных путях, и пациенты с множественными абсцессами. 20 Пациенты с обструктивными симптомами, по-видимому, обращались в более молодом возрасте.Поэтому за более молодыми пациентами следует внимательно наблюдать на предмет ухудшения симптомов.
В обсервационных исследованиях есть несколько историй успеха лечения только антибиотиками. 21,22 Однако другие исследования сообщают о более низких показателях успеха, особенно при более крупных абсцессах. Пациентам с тяжелым заболеванием, пациентам, поступающим в отделения интенсивной терапии или пациентам, проживающим в районах с высокой долей резистентности к метициллину, следует начинать прием ванкомицина.
Эпиглоттит. Эпиглоттит — это припухлость надгортанника и надгортанной области дыхательных путей.
Эпидемиология. Заболеваемость эпиглоттитом резко изменилась с момента введения вакцины HiB. Современные этиологические агенты включают Haemophilus типа B, нетипируемые, культивированные типа A и F., а также S. aureus и виды стрептококка . 23,24
Этиология. Воспаление чаще всего вызывается бактериальной инфекцией слизистой оболочки надгортанника, но также может быть вторичным по отношению к травме или повреждению поверхности в результате ожога, проглатывания или даже от трансплантата vs.болезнь хозяина у пациентов после трансплантации. 25 Это тяжелая инфекция, которая сопряжена со значительным риском смерти, особенно при отсутствии лечения. Когда происходит инфекция и поражается слизистая оболочка, надгортанник набухает и скручивается в нижнем и заднем отделах, вызывая определенную обструкцию дыхательных путей в зависимости от степени опухания. Припухлость обычно распространяется на подсвязочную область, но может быть затронута надгортанная область. Это включает отек надгортанника, аретиноидов и язычка, а также надгортанника.
Презентация. Крайне важно, чтобы пациенты с эпиглоттитом были быстро распознаны и вылечены. Это осложняется тем фактом, что из-за успеха программы иммунизации в Соединенных Штатах и во всем мире некоторые клиницисты, прошедшие обучение с начала 1990-х годов, не видели и не лечили пациентов с эпиглоттитом.
У педиатрических пациентов симптомы развиваются остро, и они довольно быстро прогрессируют. Пациенты обычно обращаются за медицинской помощью в течение 12-48 часов с момента появления симптомов с высокой температурой (40 ° C) и жалуются на боль в горле и респираторный дистресс.Кроме того, у пациентов часто возникают проблемы с выделениями, и они чаще пускают слюни, чем глотают. Педиатрические пациенты часто сидят в очень специфической позе, наклоняя руки вперед с вытянутой шеей. Это называется триподированием и используется для поддержания проходимости дыхательных путей и может быть зловещим признаком. Практики часто описывают пациентов как имеющих «токсичный» вид. ( См. Таблицу 4. )
Таблица 4. Распространенность симптомов эпиглоттита у детей 32
Признак | Процент больных |
Затрудненное дыхание | 80 |
История лихорадки | 57 |
Боль в горле | 50 |
Слюни | 38 |
Кашель | 30 |
Затруднения при глотании | 26 |
При проведении медицинского осмотра практикующий должен приложить усилия, чтобы не причинять пациенту какой-либо дискомфорт, который может усугубить респираторный дистресс, который затем может прогрессировать до отказа.У пациентов с тяжелым дистрессом и в анамнезе, совместимым с эпиглоттитом, разумно отложить обследование до тех пор, пока пациент не окажется в соответствующих условиях, чтобы обезопасить дыхательные пути, если это необходимо. Скорее всего, это произойдет в операционной. Оборудование и персонал должны быть доступны в любое время для устранения полного препятствия.
Дополнительное обследование может включать лабораторные исследования; однако у педиатрических пациентов это может явно усугубить обструкцию и взволновать и без того ослабленного пациента, и этого следует отложить до тех пор, пока дыхательные пути не станут безопасными.После того, как проходимость дыхательных путей будет обеспечена, можно получить обычные лабораторные анализы, которые должны включать общий анализ крови и посев крови. Возможные культуры слизистой оболочки надгортанника должны быть получены при обеспечении проходимости дыхательных путей.
Радиологические боковые изображения шеи могут быть полезны при диагностике стабильного пациента с легким дистрессом. Они не всегда чувствительны, но могут помочь в диагностике. Одно исследование показало, что боковые рентгенограммы шеи предполагают или являются диагностическими в 247 из 287 подтвержденных случаев эпиглоттита, что дает 86% чувствительность. 26 Классическая находка, описанная радиологами, — это «отпечаток большого пальца». ( См. Рисунок 3. )
Рисунок 3. Эпиглоттит
Обратите внимание на знак отпечатка большого пальца (стрелка)
Лечение. Пациентам с клиническими проявлениями, указывающими на эпиглоттит, которые страдают респираторной недостаточностью, требуется немедленное вмешательство в дыхательные пути. Это должно выполняться наиболее квалифицированным и опытным оператором при поддержке хирурга, способного выполнить экстренную трахеостомию или крикотироидотомию.Для интубации следует использовать трубку меньшего размера, чем рассчитано. Важно отметить, что часто вентиляция с помощью маски клапана мешка эффективна, даже если голосовые связки трудно визуализировать. После того, как проходимость дыхательных путей обеспечена, за пациентом следует наблюдать в отделении интенсивной терапии до тех пор, пока опухоль не уменьшится и у пациента не появится лихорадка. 27,28
После того, как дыхательные пути обеспечены, следует ввести антибиотики. Следует начать эмпирический охват, который будет охватывать Haemophilus influenzae , Staphylococcus и Streptococcus, обычно это цефалоспорины второго или третьего поколения, такие как цефуроксим или цефтриаксон. 29 Кроме того, во многих сообществах наблюдается повышенное присутствие метициллин-резистентных Staphylococcus aureus , требующих добавления ванкомицина для покрытия метициллин-устойчивых изолятов. 30
Было высказано предположение, что глюкокортикоиды обладают некоторой пользой для уменьшения воспаления дыхательных путей. Однако не было окончательного исследования, показывающего пользу от использования стероидов. 31,32 Одно исследование действительно показало длительный курс лечения в стационаре у пациентов, получавших стероиды.Некоторые утверждали, что это могло быть связано с тем, что пациенты, получавшие стероиды, были клинически хуже. 31 Исследования носили ретроспективный характер, что не позволяло обеспечить единообразие в сравнении двух групп. Их использование может иметь теоретическую ценность, но, вероятно, их следует использовать непосредственно перед экстубацией и в течение ограниченного времени, учитывая долгосрочные побочные эффекты стероидов, включая риск желудочно-кишечного кровотечения и гипергликемии. 23,26,32
Бактериальный трахеит. Бактериальный трахеит — это инфекция мягких тканей трахеи, вызванная бактериальной инвазией слизистой оболочки. Это острый процесс, который может быстро прогрессировать и быть опасным для жизни. Другие названия бактериального трахеита включают ларинготрахеобронхит, псевдомембранозный круп или перепончатый круп.
Эпидемиология / этиология. Бактериальный трахеит — редкое заболевание, по оценкам одного исследования частота встречаемости 0,4 на 1000 педиатрических госпитализаций, 33 , которая обычно возникает после вирусной инфекции верхних дыхательных путей. 34 Это чаще всего происходит в зимние месяцы, когда наиболее распространены вирусные инфекции верхних дыхательных путей (URI). Это, по-видимому, встречается в основном у здоровых детей и часто встречается у маленьких детей в возрасте 5-6 лет, но также может наблюдаться у подростков и взрослых. Также, кажется, есть небольшое преобладание мужчин. 35,36 Было задействовано несколько вирусов, включая парагрипп, грипп A и B и RSV. 34,37 Считается, что предшествующая вирусная инфекция приводит к микроповреждениям слизистой оболочки, что предрасполагает ее к инфекции, вызванной бактериями.Самый распространенный бактериальный изолят трахеита — это Staphylococcus aureus; , однако, во многих отчетах о случаях заболевания Moraxella catarrhalis указывается как все более распространенный патоген. 35,37 Другие изоляты включали Streptococcus pneumoniae и пиогенез, а также устойчивый к метициллину Staphylococcus aureus . 38
Презентация. Пациенты часто обращаются с симптомами со стороны верхних дыхательных путей до появления лихорадки, кашля и респираторной недостаточности.Дополнительные симптомы, которые были описаны, включают боль в горле, одышку и охриплость голоса. 33,35,36
При осмотре пациенты выглядят плохо и могут быть описаны как токсичные. У них часто бывает респираторный дистресс с обструкцией дыхательных путей, такой как стридор на вдохе и выдохе, а также втягивание. Часто пациенты с трахеитом не реагируют на лечение других причин респираторного дистресса, таких как круп.
Хотя рентгенограммы не требуются, визуализация может помочь в постановке диагноза.На боковой рентгенограмме шеи обычно видно сужение подсвязочной области и, возможно, неровность стенки трахеи. 35 Однако рентгенограммы могут быть отложены, если они усугубят респираторный дистресс у пациента или у тяжелобольного пациента, до тех пор, пока не удастся защитить дыхательные пути. Рентгенограммы должны быть портативными, так как пациента нельзя оставлять без присмотра, поскольку может произойти внезапное угнетение дыхания.
Лечение. Тщательный мониторинг дыхательной недостаточности является обязательным.Большей части пациентов с трахеитом потребуется интубация. Хотя в некоторых исследованиях сообщается о 100% интубации, в других исследованиях сообщается о 83-92% пациентов. 33,35 Интубация может быть осложнена тем фактом, что у пациентов часто наблюдаются густые гнойные выделения с неприлипающими мембранами, которые затрудняют прохождение дыхательных путей и затрудняют оксигенацию и вентиляцию легких. Часто интубация требуется только в среднем на 3 дня, пока выполняется лечение и легочный туалет. 36 Пациентам может потребоваться повторное промывание и отсасывание дыхательных путей для обеспечения проходимости. В некоторых случаях может потребоваться замена окклюзированной эндотрахеальной трубки. Кроме того, жесткая или гибкая бронхоскопия может быть полезной не только для взятия образцов на посевы, но также для диагностики, а также по терапевтическим показаниям.
Антибиотики должны быть начаты немедленно, и они должны иметь широкий спектр действия до тех пор, пока культура и чувствительность не смогут идентифицировать организм. Наиболее распространенные изоляты включают S.aureus; , однако, микроорганизмы, включая метициллин-резистентный стафилококк, а также стрептококк группы А и пневмонию и Haemophilus influenzae , могут способствовать развитию бактериального трахеита. Схемы лечения могут включать цефалоспорин третьего поколения в сочетании с ванкомицином или ампициллин-сульбактам в сочетании с ванкомицином. Учитывая возрастающую распространенность резистентного стафилококка, ванкомицин рекомендуется в качестве эмпирического покрытия. 35
Стероиды использовались во множестве ретроспективных обзоров для предполагаемой пользы при воспалении дыхательных путей.Однако следует отметить, что ретроспективный анализ еще не показал, что их использование уменьшает продолжительность интубации или пребывания в больнице. 36 Один многоцентровый ретроспективный обзор показал, что дексаметазон используется у 26 из 30 пациентов, получавших стероиды; однако также использовались гидрокортизон, солумедрол и преднизолон. 36 На сегодняшний день нет рандомизированных исследований, показывающих пользу какого-либо конкретного стероида или продолжительность лечения стероидами. 36
Неинфекционные причины обструкции
Хотя инфекции являются частой причиной острой обструкции дыхательных путей у педиатрических пациентов, существуют и другие неинфекционные причины, которые могут вызывать значительную заболеваемость и смертность.Распространенные неинфекционные причины включают проглатывание инородного тела, травмы и случайные проглатывания, вызывающие химические ожоги и возможность обструкции дыхательных путей.
Инородное тело. Инородные тела могут вызвать обструкцию дыхательных путей в значительной степени, что приводит к смертности и заболеваемости среди педиатрических пациентов. Они могут быть относительно стабильными, не требующими неотложного вмешательства, или могут проявляться полной обструкцией дыхательных путей и полной остановкой дыхания и сердца. Многие организации, включая AAP и Центры по контролю и профилактике заболеваний, приложили усилия для повышения уровня информированности о предотвращении этих несчастных случаев, что способствовало снижению общей заболеваемости.
Эпидемиология. По оценкам, в 2000 году приблизительно 160 детей в возрасте до 14 лет умерли от закупорки дыхательных путей инородными телами, которые были проглочены или вдыхались. 39 По оценкам, на каждого ребенка, умершего от удушья, 110 детей обращаются в отделения неотложной помощи для лечения эпизода удушья.
В 2001 году было отмечено, что 17 537 детей в возрасте до 14 лет лечились в отделениях неотложной помощи от эпизодов удушья, что соответствует уровню заболеваемости 30 на 100 000 человек.Показатели были самыми высокими среди младенцев младше 1 года, причем в равной степени затрагивались мальчики и девочки. Семьдесят семь процентов этих пациентов были моложе 3 лет. Следует отметить, что 59% этих случаев удушья происходили с едой, включая конфеты и жевательную резинку, но чаще всего орехи или семена. 40 Тридцать один процент эпизодов включали непищевые вещества, такие как монеты, которые составляли 12% непищевых веществ, вызывающих удушье. Остальные 18% включали такие вещи, как игрушки, шарики, воздушные шары, бумагу, кусочки пазлов, колпачки для ручек, скотч, винты и другое оборудование, ключи, пластик, целлофан, растения, камни, украшения, аксессуары для волос, баночки из-под газировки и т. Д. указанные непродовольственные товары.Десять процентов случаев удушья произошли с неизвестным веществом или предметом. 39
Из пациентов, проходивших лечение в отделениях неотложной помощи, примерно 10,5% или 1844 из 17 537 детей нуждались в госпитализации или переводе на более высокий уровень помощи в связи с эпизодом удушья. 39
Презентация. Пациенты могут обратиться сразу или, во многих случаях, через несколько дней или недель после события. У пациентов, которые обращаются немедленно, часто наблюдаются серьезные симптомы, связанные с закупоркой трахеи или гортани продуктом.Однако это случается довольно редко. У этих пациентов наблюдаются симптомы обструкции дыхательных путей при остром респираторном дистресс-синдроме с одышкой, стридором и / или хрипом. Другая группа пациентов, которые обращаются в течение первых 72 часов, — это пациенты, у которых был очевидный эпизод удушья и аспирация, независимо от их текущих симптомов. 41
Еще одна группа пациентов обращается через некоторое время после появления стойких, часто легких симптомов, таких как постоянный кашель, лихорадка, хрипы или стридор.Было обнаружено, что у пациентов, поступивших через 4-7 дней после аспирации, частота осложнений составляет 64%, а у пациентов, поступивших через 30 дней после события, частота осложнений составляет 95%. 42 Осложнения включают рецидивирующую пневмонию, воспаление дыхательных путей и развитие ателектазов. Считается, что у любого педиатрического пациента, у которого наблюдаются повторяющиеся симптомы, которые, кажется, не улучшаются, есть инородное тело. Эти инородные тела почти всегда находятся в дистальных отделах дыхательных путей бронхов.Пациенты, у которых развиваются обструктивные симптомы в верхних дыхательных путях, обычно поступают с острой аспирацией и испытывают значительный стресс.
Лечение. Основным методом лечения пациента, у которого возникла обструкция после аспирации инородного тела, является стабилизация состояния пациента. Рентгенограммы могут быть полезны для подтверждения аспирации рентгеноконтрастного объекта; однако у пациента, у которого было очевидное событие и который страдает респираторной недостаточностью, рентгенограммы не должны откладывать лечение с помощью ригидной бронхоскопии.В одном исследовании сообщалось, что только 11% инородных тел были рентгеноконтрастными. 43 Другие находки на AP-пленках, которые указывают на инородное тело, включают гиперинфляцию, инфильтрат дистальнее инородного тела или ателектаз, если аспирируемый предмет застревает в нижних дыхательных путях. Если подозрение на аспирацию находится в верхних дыхательных путях, могут быть полезны рентгенограммы передней и задней части шеи для выявления отека или припухлости. Другие рентгенографические изображения, которые могут быть полезны, включают двусторонние виды пролежня, виды принудительного выдоха и, возможно, рентгеноскопию или компьютерную томографию.Может потребоваться дополнительный кислород и даже интубация, если пациент находится в тяжелом состоянии или задерживается. Интубацию следует проводить в тяжелых случаях обструкции дыхательных путей, и по возможности ее следует проводить в операционной. Это позволяет при необходимости проводить хирургическое вмешательство, включая крикотироидотомию. Даже в операционной существует риск индукции анестезии и жесткой бронхоскопии. В одной серии примерно у 1% пациентов были осложнения во время извлечения, включая отек гортани, бронхоспазм, пневмоторакс или средостение, остановку сердца, разрыв дыхательных путей или гипоксическое повреждение мозга. 43
Хотя это не обсуждается здесь подробно, инородные тела в пищеводе также могут проявляться респираторными симптомами, что затрудняет определение местонахождения инородного тела в некоторых случаях. Одно одноцентровое исследование сообщило о 33% пациентов с респираторными симптомами из-за инородных тел пищевода. Наиболее частым зарегистрированным респираторным симптомом был кашель у 21% пациентов. Дополнительные респираторные симптомы включали стридор, заложенность носа, хрипы и даже апноэ у 2% пациентов. 44 Хотя респираторные симптомы не были наиболее частым симптомом, было отмечено, что чем дольше сохранялось инородное тело, тем более вероятно развитие респираторных симптомов. Предполагается, что это вызвано длительным сдавливанием мягких тканей прилегающей трахеи инородным телом. Иногда эти симптомы даже напоминали инфекционные причины, такие как круп с инспираторным стридором.
Наследственный ангионевротический отек. Наследственный ангионевротический отек (НАО) — редкая причина ангионевротического отека и обычно не сопровождается характерным зудом и крапивницей, которые наблюдаются при аллергических причинах ангионевротического отека, таких как анафилаксия.Его важность при обсуждении острой обструкции верхних дыхательных путей состоит в том, что в прошлом от этого заболевания, который мог произойти, смертность от него доходила до 80%. 45
HAE встречается редко, вызывается мутациями в гене ингибитора C1 и является аутосомно-доминантным по наследству. По оценкам, это происходит у 1 из 10 000–50 000 человек. 46 HAE обычно проявляется у педиатрических пациентов в подростковом или раннем взрослом возрасте. У пациентов с НАО наблюдаются повторяющиеся эпизоды отека слизистых оболочек и кожи.У большинства пациентов наблюдаются не опасные для жизни симптомы НАО, такие как ангионевротический отек желудочно-кишечного тракта или кожи; однако отек гортани был описан как первоначальная жалоба.
Хотя кожные и желудочно-кишечные симптомы встречаются чаще, приступы гортани могут быть представлены в отделении неотложной помощи как острый эпиглоттит. 47 С уменьшением количества бактериальных причин эпиглоттита следует учитывать такую этиологию, как HAE, тем более, что традиционные методы лечения отека дыхательных путей, такие как глюкокортикоиды, антигистаминные препараты и адреналин, не кажутся эффективными. 47
Пациенты с приступами гортани составляют около 1% всех приступов НАО. 48 Большинство приступов происходит в возрасте от 11 до 45 лет. 46 Однако важность этих атак состоит в том, что они могут прогрессировать до полной обструкции дыхательных путей и смерти. Отек верхних дыхательных путей может включать, помимо прочего, язычок, мягкое небо и гортань. Симптомы, о которых сообщалось во время приступа гортани, включают дисфагию, ощущение комка в горле или стеснения, изменения голоса, в том числе охриплость, и одышку. 46 Следует также отметить, что большинство эпизодов отека гортани, вызванного НАО, не прогрессировали до обструкции. Похоже, что приступы развиваются в течение нескольких часов и, как сообщается, происходят через 8–12 часов после появления симптомов. Эти симптомы могут прогрессировать до почти полной непроходимости. В то время пациенты часто сообщали о чувстве удушья и афонии. 46
Лечение. Первоначальной основой приступа гортани из-за НАО является обеспечение проходимости дыхательных путей пациента.У любого пациента, страдающего респираторным дистресс-синдромом, обязательно осознавать, что симптомы пациента могут прогрессировать и может возникнуть полная обструкция. Под рукой должен быть постоянный мониторинг дыхательных путей и соответствующий персонал для интубации и защиты дыхательных путей. После того, как будет установлено, что у пациента сохраняются проходимость дыхательных путей или проходимость дыхательных путей установлена, можно приступить к лечению и лечению отека Квинке. Дальнейшее лечение включает гидратацию, обезболивание и начало лечения, специфичного для HAE.Существуют согласованные рекомендации по ведению НАО. 45
Лечение включает использование протеина, замещающего ингибитор C1-эстеразы (C1INHRP), продукта, доступного в Соединенных Штатах с 2008 года. Многочисленные исследования показали эффективность этого продукта при желудочно-кишечных, а также кожных эпизодах. Также было показано, что при эпизодах гортани устраняются симптомы, обычно в течение 30-60 минут после приема дозы, а также уменьшается продолжительность отека гортани с 103 часов до 15 часов. 46 Вводится внутривенно в течение 10 минут.
Еще одно лекарство, доступное в США, — это экалантид. Экаллантид одобрен с 2009 года для пациентов старше 16 лет. Это рекомбинантный ингибитор калликреина, который, в свою очередь, блокирует выработку брадикинина. Брадикинин активируется при HAE и отвечает за утечку капилляров, наблюдаемую при HAE и последующий отек. Следовательно, экаллантид подавляет выработку брадикинина. Он вводится в виде трех подкожных инъекций по 10 мг в разные места, общая доза для взрослых составляет 30 мг подкожно. 49 Экаллантид действительно безопасен, пациенты сообщают о побочных эффектах, таких как головная боль, тошнота, диарея и лихорадка (4-8%). Однако существует небольшой риск, примерно 3%, тяжелой анафилаксии. Пациенты, получающие экаллантид, должны находиться под тщательным наблюдением на предмет признаков анафилаксии во время лечения. 49,50
Клиницисты должны знать, что свежезамороженная плазма также использовалась для лечения отека гортани у пациентов с НАО. Его следует использовать только в том случае, если лечение первой линии C1INHRP или экалантидом недоступно.Свежезамороженная плазма использовалась до утверждения этих препаратов FDA с некоторой предполагаемой пользой. Теоретически плазма содержит ингибитор С1, который может улучшить симптомы и обратить вспять прогрессирование отека гортани. 51 У взрослых две единицы СЗП и у детей 10-15 мл / кг, которые можно повторять каждые 2-4 часа до улучшения симптомов. Следует отметить, что были только отчеты о случаях использования СЗП, а не о каких-либо рандомизированных контролируемых исследованиях. 52
HAE следует рассматривать у пациентов с отеком гортани, которые не отвечают на стандартное лечение.Этим пациентам следует вести агрессивное лечение, чтобы обеспечить надлежащее управление дыхательными путями и предотвратить внезапную смерть. После стабилизации эти пациенты должны пройти полное обследование на HAE, включая сывороточные уровни белка ингибитора C1 и консультацию со специалистом. В семейном анамнезе также может присутствовать ангионевротический отек у детей с НАО.
Разные причины обструкции дыхательных путей
Острая обструкция верхних дыхательных путей также может быть вызвана другими состояниями, такими как травма шеи или лица в результате дорожно-транспортных происшествий или другого травматического механизма, прием внутрь химических веществ, вызывающих локальный ожог слизистой оболочки, или локализованные опухоли дыхательных путей.
Одной из таких опухолей дыхательных путей, которая встречается редко, но часто встречается у младенцев, являются гемангиомы подсвязочного и надгортанного отделов. Пациенты с этими доброкачественными опухолями обращаются в отделение неотложной помощи, часто имея в анамнезе несколько эпизодов респираторной недостаточности, и эти опухоли могут вызывать обструкцию дыхательных путей. 53,54 Подсвязочная гемангиома, хотя и встречается редко, является наиболее частым новообразованием дыхательных путей младенца. 55 Наиболее частым обнаружением при физикальном осмотре является двухфазный стридор, и примерно у 50% пациентов наблюдаются кожные гемангиомы. 55 Подробный анамнез может указывать на несколько эпизодов крупа, диагностированных в прошлом, без наличия симптомов URI. Диагноз ставится с помощью прямой ларингоскопии, может помочь МРТ. Эти опухоли необходимо тщательно контролировать, так как сообщаемый уровень смертности среди недиагностированных или пролиферирующих опухолей составляет 30-70%. 56,57 Лечение варьируется от консервативного лечения до использования стероидов, лазерной терапии и даже открытой резекции и использования трахеостомии. 55
Заключение
Пациент, поступающий в отделение неотложной помощи с респираторным дистресс-синдромом, должен быть быстро обследован.В случае наличия у пациента стридора или других симптомов, связанных с обструкцией верхних дыхательных путей, различия часто делятся на острые и хронические, а также инфекционные и неинфекционные причины. Инфекционные причины, рассматриваемые в этой статье, включают круп, перитонзиллярные и заглоточные абсцессы, эпиглоттит и бактериальный трахеит. Неинфекционные причины включают инородное тело, проглатывание / ожоги, травмы и наследственный ангионевротический отек. Своевременное распознавание и агрессивное лечение могут снизить заболеваемость и смертность детей с этими состояниями.
Ссылки
1. Людвиг С., Кеттрик Р.Г., Паркер М. Педиатрическая сердечно-легочная реанимация. Обзор 130 дел. Clin Pediatr (Phila). 1984; 23 (2): 71-75.
2. Рузвельт Г. Острая воспалительная обструкция верхних дыхательных путей. В: Behrman RE, Kliegman RM, Jenson HB, редакторы. Нельсон Учебник педиатрии , 17-е изд. Сондерс; 2004: 1405-1409.
3. Сигал А.О., Крайтон Э.Дж., Моинеддин Р. и др. Крупные госпитализации в Онтарио: анализ временных рядов за 14 лет. Педиатрия 2005; 116: 51-55.
4. Рихканен Х., Ронкко Э., Ниеминен Т. и др. Респираторные вирусы при крупе гортани у детей раннего возраста. J Pediatr 2008; 152: 661-665.
5. Уэстли К.Р., Коттон Е.К., Брукс Дж. Распыленный рацемический адреналин от IPPB для лечения крупа. Am J Dis Child 1978; 132: 484-487.
6. Руководства по диагностике и лечению крупа [Интернет] .; 2008 г. Доступно по адресу: www.albertadoctors.org.
7.Cherry JD. Клиническая практика. Круп. N Engl J Med 2008; 358: 384-391.
8. Colletti JE. Миф: Холодный туман — эффективное средство от крупа. CJEM 2004; 6: 357-358.
9. Нето Г. М., Кентаб О., Классен Т. П. и др. Рандомизированное контролируемое испытание тумана в лечении острого крупа средней степени тяжести. Acad Emerg Med 2002; 9: 873-879.
10. Мур М., Литтл П. Ингаляции увлажненного воздуха для лечения крупа. Кокрановская база данных Syst Rev 2006; 3: CD002870.
11. Бьёрнсон С., Рассел К.Ф., Вандермейр Б. и др. Распыленный адреналин при крупе у детей. Кокрановская база данных Syst Rev 2011; (2) (2): CD006619.
12. Джилхоед ГК, Макдональд ВБ. Пероральный дексаметазон при лечении крупа: 0,15 мг / кг по сравнению с 0,3 мг / кг по сравнению с 0,6 мг / кг. Pediatr Pulmonol 1995; 20: 362-368.
13. Рассел К.Ф., Лян Й., О’Горман К. и др. Глюкокортикоиды при крупе. Кокрановская база данных Syst Rev 2011; (1) (1): CD001955.
14. Vorwerk C, Coats T. Heliox при крупе у детей. Кокрановская база данных Syst Rev , 17 февраля 2010 г .; (2) (2): CD006822.
15. Weber JE, Chudnofsky CR, Younger JG, et al. Рандомизированное сравнение гелий-кислородной смеси (гелиокс) и рацемического адреналина для лечения умеренного и тяжелого крупа. Педиатрия Июнь 2001; 107 (6): E96.
16. Simons JP, Branstetter BF, 4th, Mandell DL. Двусторонние перитонзиллярные абсцессы: история болезни и обзор литературы.Am J Otolaryngol. 2006 ноябрь-декабрь; 27 (6): 443-5.
17. Szuhay G, Tewfik TL. Перитонзиллярный абсцесс или целлюлит? Клиническое сравнительное педиатрическое исследование. J Отоларингол 1998; 27: 206-212.
18. Озбек Ч., Айгенч Э., Тунец ЕС и др. Использование стероидов при лечении перитонзиллярного абсцесса. Дж. Ларингол Отол 2004; 118: 439-442.
19. Ли С.С., Шварц Р.Х., Бахадори Р.С. Заглоточный абсцесс: эпиглоттит нового тысячелетия. J Pediatr 2001; 138: 435-437.
20. Эльшериф А.М., Парк А.Х., Альдер С.К. и др. Показатели более сложного клинического течения педиатрических больных с заглоточным абсцессом. Int J Pediatr Otorhinolaryngol 2010; 74: 198-201.
21. Craig FW, Schunk JE. Заглоточный абсцесс у детей: клиническая картина, применение изображений и текущее лечение. Педиатрия 2003; 111 (6 Pt 1): 1394-1398.
22. МакКлей Дж. Э., Мюррей А. Д., Бут Т. Внутривенная антибиотикотерапия глубоких абсцессов шеи, определяемых компьютерной томографией. Хирургия головы и шеи Arch Otolaryngol 2003; 129: 1207-1212.
23. Sivakumar S, Latifi SQ. Ветряная оспа со стридором: вспомните стрептококковый эпиглоттит группы А. J Paediatr Child Health 2008; 44: 149-151.
24. Somenek M, Le M, Walner DL. Мембранозный ларингит у ребенка. Int J Pediatr Otorhinolaryngol 2010; 74: 704-706.
25. de Diego JI, Prim MP, Hardisson D, et al. Болезнь трансплантат против хозяина как причина увеличения надгортанника у ребенка с ослабленным иммунитетом. Arch Otolaryngol Head Neck Surg 2 001; 127: 439-441.
26. Мэйо-Смит М.Ф., Спинале Дж. Термический эпиглоттит у взрослых: новое осложнение употребления запрещенных наркотиков. J Emerg Med 1997; 15: 483-485.
27. Страуд Р.Х., Фридман Н.Р. Обновленная информация о воспалительных заболеваниях дыхательных путей у детей: эпиглоттит, круп и трахеит. Am J Otolaryngol 2001; 22: 268-275.
28. Дамм М., Экель Х. Э., Юнгехулсинг М. и др. Эндоскопия дыхательных путей в междисциплинарном лечении острого эпиглоттита. Int J Pediatr Otorhinolaryngol 1996; 38: 41-51.
29. Глинн Ф, Фентон Дж. Диагностика и лечение супраглоттита (эпиглоттита). Curr Infect Dis Rep 2008; 10: 200-204.
30. Американская академия педиатрии. Haemphilus influenzae инфекций. В: Пикеринг Л.К., Бейкер С.Дж., Лонг СС, Макмиллан Дж. А., ред. Красная книга: Отчет Комитета по инфекционным болезням за 2006 г. , 27-е изд. Деревня Элк Гроув, Иллинойс: Американская академия педиатрии; 2006: 310-318.
31. Гульдфред Л.А., Лайн Д., Беккер BC. Острый эпиглоттит: эпидемиология, клинические проявления, лечение и исход. Дж. Ларингол Отол 2008; 122: 818-823.
32. Mayo-Smith MF, Spinale JW, Donskey CJ, et al. Острый эпиглоттит. 18-летний опыт работы на Род-Айленде. Сундук 1995; 108: 1640-1647.
33. Галлахер П.Г., Майер К.М., 3-й. Подход к диагностике и лечению перепончатого ларинготрахеобронхита у младенцев и детей. Педиатр скорой помощи 1991; 7: 337-342.
34. Liston SL, Gehrz RC, Siegel LG и др. Бактериальный трахеит. Am J Dis Child 1983; 137: 764-767.
35. Аль-Мутаири Б., Кирк В. Бактериальный трахеит у детей: подход к диагностике и лечению. Детский педиатр 2004; 9: 25-30.
36. Тебрюгге М., Пантазиду А., Торбурн К. и др. Бактериальный трахеит: многоцентровая перспектива. Scand J Infect Dis 2009; 41: 548-557.
37. Миранда А.Д., Вальдес Т.А., Перейра К.Д.Бактериальный трахеит: разнообразное заболевание. Педиатр неотложной помощи 2011; 27: 950-953.
38. Ямазаки Ю., Хираи К., Хонда Т. Псевдомембранозный трахеобронхит, вызванный устойчивостью к метициллину Staphylococcus aureus . Scand J Infect Dis 2002; 34: 211-213.
39. Центры по контролю и профилактике заболеваний. Несмертельные эпизоды удушья среди детей. Morb Mortal Wkly Rep MMWR 2002; 51: 945-948.
40. Эзер С.С., Огузкурт П., Инс Э. и др.Аспирация инородного тела у детей: анализ диагностических критериев и точное время для бронхоскопии. Педиатр скорой помощи 2011; 27: 723-726.
41. Orji FT, Akpeh JO. Аспирация трахеобронхиального инородного тела у детей: насколько надежны клинические и рентгенологические признаки при диагностике? Клин Отоларингол 2010; 35: 479-485.
42. Mu L, He P, Sun D. Причины и осложнения поздней диагностики аспирации инородного тела у детей. отчет о 210 случаях. Arch Otolaryngol Head Neck Surg 1991; 117: 876-879.
43. Фидковски К.В., Чжэн Х., Ферт PG. Анестезиологические аспекты трахеобронхиальных инородных тел у детей: обзор литературы 12 979 случаев. Anesth Analg 2010; 111: 1016-1025.
44. Macpherson RI, Hill JG, Othersen HB, et al. Инородное тело пищевода у детей: диагностика, лечение и осложнения. AJR Am J Roentgenol 1996; 166: 919-924.
45. Bowen T, Cicardi M, Farkas H, et al.Алгоритм международного консенсуса 2010 г. по диагностике, терапии и лечению наследственного ангионевротического отека. Allergy Asthma Clin Immunol 2010; 6:24.
46. Bork K, Hardt J, Schicketanz KH, et al. Клинические исследования внезапной обструкции верхних дыхательных путей у пациентов с наследственным ангионевротическим отеком из-за дефицита ингибитора эстеразы C1. Arch Intern Med 2003; 163: 1229-1235.
47. О’Бир А., Мунис А.Е., Фостер Р.Л. Наследственный ангионевротический отек, проявляющийся в виде эпиглоттита. Педиатр скорой помощи 2005; 21: 27-30.
48. Farkas H, Varga L, Szeplaki G, et al. Лечение наследственного ангионевротического отека у детей. Педиатрия 2007; 120: e713-e722.
49. Lunn M, Banta E. Ecallantide для лечения наследственного ангиодема у взрослых. Clin Med Insights Cardiol 2011; 5: 49-54.
50. Шеффер А.Л., Кэмпион М., Леви Р.Дж. и др. Экаллантид (DX-88) для лечения острых наследственных приступов ангионевротического отека: интегрированный анализ 2 двойных слепых исследований фазы 3. J Allergy Clin Immunol. 2011; 128: 153,159.e4.
51. Prematta M, Gibbs JG, Pratt EL, et al. Свежезамороженная плазма для лечения наследственного ангионевротического отека. Ann Allergy Asthma Immunol. 2007; 98: 383-388.
52. Пекдемир М., Эрсель М., Аксай Э. и др. Эффективное лечение наследственного ангионевротического отека свежезамороженной плазмой в отделении неотложной помощи. J Emerg Med 2007; 33: 137-139.
53. Киер С., Баллуз Р., Моди В. и др. Визуальный диагноз: респираторный дистресс: отличный маскарад. Pediatr Ред. 2011; 32: e95-101.
54. Ада М., Гувенц М.Г., Йилмаз С. Инфантильная надгортанная гемангиома: отчет о клиническом случае. Ухо-носовое горло J 2006; 85: 388-391.
55. Рахбар Р., Николлас Р., Роджер Г. и др. Биология и лечение подсвязочной гемангиомы: прошлое, настоящее, будущее. Ларингоскоп 2004; 114: 1880-1891.
56. Малликен Дж. Б., Фишман С. Дж., Берроуз ЧП. Сосудистые аномалии. Curr Probl Surg 2000; 37: 517-584.
57.Бродский Л, Йошпе Н, Рубен Р.Дж. Клинико-патологические корреляты врожденных гемангиом подсвязочного канала. Ann Otol Rhinol Laryngol Suppl 1983; 105: 4-18.
Обструкция дыхательных путей: типы, причины и диагностика
Что такое обструкция дыхательных путей?
Обструкция дыхательных путей — это закупорка любой части дыхательных путей. Дыхательные пути — это сложная система трубок, по которым вдыхаемый воздух из носа и рта поступает в легкие. Препятствие может частично или полностью препятствовать попаданию воздуха в легкие.
Некоторые обструкции дыхательных путей незначительны, в то время как другие представляют опасность для жизни, требующую немедленной медицинской помощи.
Типы обструкции дыхательных путей классифицируются в зависимости от того, где возникает обструкция и насколько она блокирует:
- Обструкция верхних дыхательных путей возникает в области от носа и губ до гортани (голосовой аппарат).
- Обструкция нижних дыхательных путей возникает между гортани и узкими проходами в легких.
- Частичная закупорка дыхательных путей позволяет воздуху проходить. Вы все еще можете дышать с частичной обструкцией дыхательных путей, но это трудно.
- Полная обструкция дыхательных путей не позволяет воздуху проходить. Вы не можете дышать, если у вас полная обструкция дыхательных путей.
- Острая обструкция дыхательных путей — это быстро возникающая закупорка. Удушье посторонним предметом является примером острой непроходимости дыхательных путей.
- Хроническая обструкция дыхательных путей возникает двумя способами: из-за длительной закупорки или длительной закупорки.
Классический образ обструкции дыхательных путей — это когда кто-то подавился куском пищи. Но это только одна из многих причин, которые могут вызвать обструкцию дыхательных путей. Другие причины включают:
Дети имеют более высокий риск закупорки посторонними предметами, чем взрослые. Они чаще засовывают игрушки и другие мелкие предметы в нос и рот. Они также могут плохо пережевывать пищу перед проглатыванием.
К другим факторам риска обструкции дыхательных путей относятся:
- тяжелая аллергия на укусы насекомых, например от пчел, или на такие продукты, как арахис
- врожденные дефекты или наследственные заболевания, которые могут вызвать проблемы с дыхательными путями
- курение
- нервно-мышечные расстройства и другие состояния, из-за которых людям трудно правильно глотать пищу
Симптомы обструкции дыхательных путей зависят от причины.Они также зависят от расположения препятствия. Симптомы, которые могут возникнуть у вас, включают:
- возбуждение
- цианоз (кожа голубоватого цвета)
- спутанность сознания
- затрудненное дыхание
- затрудненное дыхание
- паника
- высокие звуки дыхания, такие как хрипы
- потеря сознания
Обструкцию дыхательных путей диагностируют, оценивая ваши признаки и симптомы. Врачи ищут признаки, которые включают:
- изменения в вашем обычном дыхании, будь то частое или поверхностное дыхание
- снижение шума дыхания в легких
- звуки высокого дыхания в верхних дыхательных путях или во рту
- отсутствие дыхания
- синеватый цвет кожи
- потеря сознания
Некоторые тесты также могут быть использованы для определения причины обструкции дыхательных путей.В экстренных случаях ваш врач, скорее всего, сначала назначит рентген, чтобы определить причину ваших симптомов.
Если рентген не может определить причину непроходимости, ваш врач может назначить более расширенное обследование. Это может включать бронхоскопию.
Во время этой процедуры ваш врач вводит через рот или нос инструмент, называемый бронхоскопом, чтобы проверить ваши легкие на наличие инородных тел.
Бронхоскопия также может помочь вашему врачу оценить различные причины непроходимости.Это включает трахеомаляцию (слабость и коллапс трахеи).
Он также включает инфекционные причины, такие как закупорка слизистой у пациентов с хроническими заболеваниями легких, такими как эмфизема и кистозный фиброз.
Ваш врач может также назначить ларингоскопию. Во время этой процедуры ваш врач осмотрит вашу гортань с помощью ларингоскопа.
Дополнительные тесты могут включать компьютерную томографию головы, шеи или грудной клетки для определения других источников непроходимости, таких как эпиглоттит (инфекция и воспаление надгортанника).
Надгортанник — это лоскут ткани, который защищает и покрывает трахею, предотвращая попадание пищи и инородных тел.
Обструкция дыхательных путей обычно является неотложной ситуацией. Если вы заметили, что у кого-то возникла обструкция дыхательных путей, позвоните 911.
Есть несколько вещей, которые вы можете сделать, ожидая прибытия экстренных служб, в том числе следующие.
Маневр Геймлиха
Это экстренная техника, которая может помочь человеку, который задыхается от постороннего предмета:
- В маневре один человек стоит позади задыхающегося человека и обнимает его за талию.
- Человек, выполняющий маневр, затем сжимает кулак одной рукой и помещает его немного выше пупка.
- Затем они должны схватить этот кулак другой рукой и надавить на живот человека пятью быстрыми толчками.
- Они должны повторять эти пять толчков в живот, пока объект не смещается или пока не прибудут службы экстренной помощи.
Примечание: Красный Крест также рекомендует включить пять ударов в спину, хотя некоторые институты, такие как Американская кардиологическая ассоциация, не обучают этой технике.
Если вы следуете технике Красного Креста, повторите цикл из пяти ударов в спину и пяти толчков в живот, пока объект не смещается или не прибудут службы экстренной помощи.
Адреналин
Адреналин можно использовать для лечения отека дыхательных путей из-за аллергической реакции.
У людей с тяжелой аллергией, например, с аллергией на пищу или укусы пчел, может возникнуть внезапный и быстрый отек горла и языка. Это может привести к почти полной или почти полной обструкции дыхательных путей в течение нескольких минут.
Люди с тяжелой аллергией обычно носят EpiPens. Это простые инъекторы, содержащие адреналин. Людям, которые носят EpiPens, рекомендуется вводить одну инъекцию в наружную поверхность бедра, как только они испытывают симптомы тяжелой аллергической реакции.
Инъектор адреналина может помочь человеку, испытывающему анафилактический шок, пока он ожидает прибытия медицинской помощи. Медицинские работники всегда должны как можно раньше оценивать людей, получающих инъекции адреналина.
Сердечно-легочная реанимация (СЛР)
СЛР используется, когда человек не может дышать и потерял сознание. Он поддерживает приток насыщенной кислородом крови к мозгу до прибытия службы экстренной помощи.
Чтобы выполнить СЛР:
- Поместите пятку руки в центр груди.
- Вторую руку положите сверху и надавите на грудь, используя вес верхней части тела.
- Делайте это примерно 100 раз в минуту, пока не приедет скорая помощь.
Когда приехала скорая помощь, существует несколько различных способов лечения обструкции дыхательных путей в зависимости от того, чем она вызвана.
В дыхательные пути можно ввести эндотрахеальную или назотрахеальную трубку. Это может помочь получить кислород через опухшие дыхательные пути. Трахеостомия и крикотиротомия — это хирургические отверстия, которые делают в дыхательных путях для обхода препятствия.
Эти процедуры должны выполняться высококвалифицированными медицинскими специалистами и обычно требуются, когда все вышеперечисленные вмешательства оказались безуспешными.
При своевременном лечении часто можно успешно вылечить обструкцию дыхательных путей. Однако обструкция дыхательных путей чрезвычайно опасна. Они могут быть смертельными даже после лечения.
Если у вас или вашего знакомого может быть обструкция дыхательных путей, немедленно обратитесь за помощью .
Можно предотвратить многие виды обструкции дыхательных путей. Снизьте свой риск, сделав следующее:
- Избегайте употребления большого количества алкоголя перед едой.
- Ешьте небольшими порциями.
- Ешьте медленно.
- Следите за маленькими детьми во время еды.
- Тщательно разжевать перед проглатыванием.
- Убедитесь, что протезы подходят правильно.
- Храните мелкие предметы в недоступном для детей месте.
- Не курите.
- Посещайте врача регулярно, если у вас есть состояние, которое может вызвать хроническую обструкцию дыхательных путей.
Лечение обструкции дыхательных путей Birmingham, AL
Обструкция дыхательных путей представляет опасность для маленьких детей, потому что их дыхательные пути еще не полностью сформировались, и поэтому они меньше и более склонны к обструкции.Важно не подпускать маленьких детей к маленьким игрушкам, которые могут стать причиной удушья, а также кормить их только небольшими кусками пищи. Поскольку маленькие дети часто кладут что-нибудь в рот, необходим постоянный присмотр.
Дополнительными причинами обструкции дыхательных путей у детей могут быть, среди прочего, осложнения от астмы, эпиглоттита, воспаления или увеличения миндалин или аденоидов, аллергии или гастроэзофагеального рефлекса. Известные врачи Pediatric ENT Associates в Бирмингеме, штат Алабама, являются специалистами по лечению обструкции дыхательных путей и являются участниками программы Aerodigestive Program at Children of Alabama.Клиника Aerodigestive Clinic работает вместе с другими педиатрическими отделениями, чтобы создать полную картину лечения обструкции дыхательных путей, чтобы обеспечить наилучший уход за вашим ребенком.
Экстренное лечение обструкции дыхательных путей у детей
Если ваш ребенок подавился игрушкой или другим предметом, это требует неотложной медицинской помощи, и вам следует немедленно позвонить в службу 911. Существуют способы быстрого и эффективного удаления посторонних предметов из дыхательного горла, однако требуется хирург, специально обученный лечению дыхательных путей у детей.Все хирурги PENTA имеют подготовку и опыт, необходимые для выполнения этих процедур. Главное — действовать быстро, чтобы вашего ребенка можно было спасти достаточно быстро и предотвратить долгосрочные осложнения.
Тяжелые аллергические реакции и все, что полностью закрывает трахею вашего ребенка, следует рассматривать как неотложную помощь и немедленно обращаться за помощью. Если ваш ребенок испытывает тяжелую аллергическую реакцию, рекомендуется после неотложной помощи отвести его или ее к детскому ЛОР-специалисту, чтобы можно было принять меры для предотвращения таких тяжелых аллергических реакций в будущем.
Проблемы с дыханием и храпом
Если ваш ребенок шумно дышит , храпит и, кажется, не может нормально дышать, возможно, он страдает от увеличенных аденоидов или миндалин. Они могут быть вызваны инфекцией или иметь большие размеры. Если вы заметили эти признаки у своего ребенка, отнесите их педиатрическим экспертам в Pediatric ENT Associates в Бирмингеме, Алабама, для получения полной оценки и плана лечения. Увеличенные аденоиды и миндалины могут вызывать ряд симптомов, в том числе затрудненное дыхание, потерю концентрации во время бодрствования из-за отсутствия полноценного ночного сна, шумное дыхание (также называемое стридором) и храп.Голос вашего ребенка также может быть нарушен, если воспаленные миндалины не лечить своевременно.
Для получения дополнительной информации о лечении обструкции дыхательных путей посетите medlineplus.gov.
Запишитесь на прием в Pediatric ENT Associates
Если вы заметили, что у вашего ребенка проблемы с дыханием, не стесняйтесь отвезти его в Pediatric ENT Associates в Бирмингеме, Алабама, для обследования. Чтобы узнать больше о лечении обструкции дыхательных путей и записаться на прием, позвоните сегодня по телефону (205) 831-0101.
Далее прочтите о трахеостомии.
Обструкция дыхательных путей у детей: знайте о рисках
Обструкция дыхательных путей у детей может быть редким явлением для респондентов службы неотложной медицинской помощи, но она является частой причиной детской смерти во всем мире. По данным клиники Мэйо, удушение — частая причина травм и смерти среди детей. И это может быть просто вопросом времени, когда вас попросят освободить дыхательные пути или вылечить ребенка, который задыхается.
Давайте рассмотрим некоторые из причин, по которым дети часто задыхаются.
Поведенческие факторы при удушье в детстве
Прежде чем мы обсудим анатомические различия, которые делают детей уязвимыми для обструкции дыхательных путей, давайте коснемся некоторых поведенческих факторов, которые подвергают детей риску.
- Изучение окружающей среды: Маленькие дети, как правило, кладут вещи в рот, исследуя окружающий мир.Мелкие предметы легко попадают в дыхательные пути.
- Отсутствие ловкости: Дети все еще осваивают контроль над своими конечностями и пальцами, из-за чего им сложно выбить предмет из собственного горла.
- Неспособность общаться: В случае частичных препятствий дети могут быть не в состоянии передать непосредственность и / или серьезность своей ситуации.
- Переход на твердую пищу: Дети, которые все еще учатся правильно кусать и жевать твердую пищу, особенно уязвимы для пищевых препятствий из-за таких продуктов, как хот-доги, виноград и леденцы.
- Неспособность распознавать опасности: Маленькие дети не способны распознавать опасности и предвидеть потенциальные риски, связанные с попаданием предметов в рот.
По мере того, как дети растут, развиваются и учатся, они могут лучше избегать рискованного поведения, которое может привести к обструкции дыхательных путей.
Анатомические и физиологические различия, предрасполагающие детей к удушью
Есть много анатомических и физиологических различий у детей, которые делают их склонными к удушью.Их меньший размер — один из них. Вот некоторые из других уникальных качеств детей, которые делают их уязвимыми:
- Язык: У детей размер языка больше по отношению к ротовой полости, чем у взрослых.
- Трахея: Трахея ребенка не только меньше в диаметре, но и незрелые кольца трахеи делают ее более гибкой, что может привести к гиперфлексии или гиперэкстензии, которые затем могут перекрыть дыхательные пути. Меньший диаметр также проблематичен, когда дело доходит до отека, потому что минимальное количество может привести к закупорке дыхательных путей.
- Надгортанник: Надгортанник у ребенка больше, и его сложнее поднять во время интубации, поэтому прямое лезвие — лучший выбор для педиатрических пациентов.
- Гортань: Гортань у ребенка выше и ближе к передней части — это следует учитывать, особенно при хирургическом вмешательстве в дыхательные пути.
- Сердце: Сердце ребенка не может увеличивать ударный объем, потому что оно не может увеличивать силу сокращений, а только частоту.Используйте брадикардию как индикатор гипоксии у младенцев и детей.
- Легкие: Легкие ребенка менее способны увеличивать емкость, потому что сердце занимает большую часть грудной полости.
- Живот: Живот ребенка меньше и скучен, что затрудняет движение диафрагмы вниз, чтобы увеличить объем легких.
- Регулировка температуры: Это сложнее, потому что у детей большая площадь поверхности, но меньше возможностей выделять тепло.Остерегайтесь переохлаждения.
При всех этих вариациях неудивительно, что дети страдают от обструкции дыхательных путей или испытывают трудности с компенсацией во время респираторной неотложной помощи.
Знай знаки опасности
Распознавать респираторный дистресс у детей так же важно, как и лечить его, особенно если он связан с обструкцией. Вот некоторые признаки того, что ребенок в беде:
- Тахипноэ (> 60 / мин)
- Брадикардия (<60 / мин)
- Расширение носа
- Использование дополнительных мышц
- Позиционирование (штатив)
- Измененный уровень сознания
- Бледность или цианоз
- Аномальные звуки / паттерны дыхания
- Лихорадка
- Изъятия
- Потеря сознания
Знание уникальных характеристик младенцев и детей — поведенческих, анатомических и физиологических — и распознавание признаков и симптомов у ребенка, находящегося в бедственном положении, — важные первые шаги в понимании рисков обструкции дыхательных путей у детей.Будьте внимательны при возникновении проблем и немедленно устраняйте респираторные заболевания, чтобы снизить риск смерти младенцев и детей.
¹ «Детское удушье: как обезопасить своего ребенка», Mayo Clinic, 2016,
www.mayoclinic.org/healthy-lifestyle/infant-and-toddler-health/in-depth/infant-choking/art-20044661
«Помимо основ: педиатрическая оценка», EMS World, 2006,
https://www.emsworld.com/article/10322897/beyond-basics-pediatric-assessment
Рекомендации по клинической практике: острая обструкция верхних дыхательных путей
Экстренные лекарства и жидкости калькулятор
Признаки частичной острой обструкции верхних дыхательных путей:
Стридор.
- Повышенная работа дыхания, о чем свидетельствует надгрудинная, межреберная и субкостальная ретракция наряду с повышенным использованием вспомогательных мышц дыхания.
Признаки ухудшения состояния и показания к неотложной помощи интервенции:
- Гипоксия — беспокойство, беспокойство, беспокойство.
- Усталость или снижение сознания.
- Повышение работы дыхания.
Обсудить всех детей с тяжелой или ухудшающейся обструкцией верхних дыхательных путей с консультант срочно
- позвоните в ICU x5211
- Или позвоните в педиатрическую службу перинатальной неотложной помощи (PIPER): 1300 137 650.
Оценка
- Сильный лающий кашель при лихорадке, жалкий, но в остальном хорошо, ребенок предлагает Круп.
- Отсутствующий кашель с низким стридором на выдохе (часто храп) и слюнотечение свидетельствует об эпиглоттите.
- Внезапное начало у здорового ребенка с кашлем и удушьем. афония предполагает вдыхание инородного тела.
- Отек лица и языка, хрипы или крапивница предполагают Анафилаксия.
Другие возможные диагнозы
| Симптомы | Возможный диагноз |
| Высокая температура Гиперэкстензия шеи Дисфагия, скопление секрета в горле | эпиглоттит заглоточный / перитонзиллярный абсцесс |
| «Токсичный» ребенок Заметно болезненная трахея | трахеит бактериальный |
| Существующий ранее стридор (младенец) | врожденная аномалия, напр.гибкая гортань, гемангиома / стеноз подсвязочного канала |
Примечание: клинические проявления во многом совпадают. между эпиглоттитом, бактериальным трахеитом и верхними дыхательными путями абсцесс.
Менеджмент
Банкноты
- Внутривенный доступ следует отложить — расстроить ребенка можно. вызвать увеличивающееся препятствие.
- Рентгенография мягких тканей шейного отдела позвоночника не помогает при
управление.
При тяжелой обструкции дыхательных путей рентген вызывает чрезмерную задержку окончательное лечение и может быть опасным (позиционирование может вызвать остановку дыхания).
| Размер трубки ЭТ в верхних дыхательных путях препятствие | |
| Новорожденные | 2,5 — 3 мм |
| <6 месяцев | 3,0 мм |
| 6 месяцев — 2 года | 3,5 мм |
| 2–5 лет | 4,0 мм |
| > 5 лет | От 1/2 до 1 размера меньше обычного |
| (обычный размер (мм) = 4 + возраст / 4) | |
(PDF) Обструкция верхних дыхательных путей у детей
Подсвязочный стеноз
Вторичная форма является наиболее частой и возникает после интубации трахеи en-
или травмы гортани.Принимая во внимание, что генитальная форма con-
возникает из-за аномалии перстневидного хряща
и проявляется рецидивирующими эпизодами крупоподобного заболевания [42].
Варианты лечения включают микроларингоскопию /
бронхоскопию с расширением бужей, разрезом перстневидного хряща,
резекцию трахеи и гортани [43].
Выводы
Обструкция верхних дыхательных путей — обычная экстренная ситуация у детей
, требующая быстрого и эффективного ведения острых случаев для
предотвращения тяжелых осложнений и даже летального исхода.Диагноз
почти всегда клинический. В развивающихся странах по-прежнему преобладают острые инфекционные причины
.
Круп является наиболее частой причиной обструкции верхних дыхательных путей, встречающейся в клинической практике
, и лечится с помощью кортикостероидов и распыления адреналина
. Другие инфекционные этиологии требуют внутривенного введения антибиотиков
отиков в сочетании с надлежащим контролем проходимости дыхательных путей, частой механической вентиляцией легких.Жесткая бронхоскопия остается предпочтительной процедурой
для диагностики и лечения чужеродной аспирации тела
.
За последние десятилетия благодаря усовершенствованным хирургическим методам и поддерживающему уходу прогноз хронических случаев
значительно улучшился.
Конфликт интересов Нет.
Источник финансирования Нет.
Ссылки
1. Чан П.В., Го А., Лум Л. Тяжелая обструкция верхних дыхательных путей в тропиках
, требующая интенсивной терапии.Pediatr Int. 2001; 43: 53–7.
2. Богадана А., Избицкий Г., Краман С.С. Основы аускультации легких
тации. N Engl J Med. 2014; 370: 744–51.
3. Холингер Л.Д. Оценка стридора и хрипов. В: Holinger LD,
редактор. Детская ларингология и бронхоэзофагология. Нью-Йорк:
Липпинкотт Рэйвен; 1997. стр. 41–8.
4. Уэстли К.Р., Коттон Е.К., Брукс Дж. Распыленный рацемический эпинеф-
от IPPB для лечения крупа: двойное слепое исследование.Am J
Dis Child. 1978; 132: 484–7.
5. Рассел К.Ф., Лян Й., О’Горман К., Джонсон Д.В., Классен Т.П.
Глюкокортикоиды при крупе. Кокрановская база данных Syst Rev.2011; 1:
CD001955.
6. Мур М., Литтл П. Ингаляции увлажненного воздуха для лечения крупа.
Кокрановская база данных Syst Rev.2006; 3: CD002870.
7. Бьёрнсон С., Рассел К., Вандермейер Б., Классен Т.П., Джонсон Д.В.
Распыленный адреналин при крупе у детей. Кокрановская база данных
Syst Rev.2013; 10: CD006619.
8. Vorwerk C, Coats T. Heliox при крупе у детей. Cochrane
Database Syst Rev.2010; 2: CD006822.
9. Блэксток Д., Эддерли Р. Дж., Стюард Д. Эпиглоттит у детей раннего возраста —
детей. Анестезиология. 1987. 67: 97–100.
10. Mayo-Smith MF, Spinale JW, Donskey CJ, et al. Острый эпиглоттит.
18-летний опыт работы в Род-Айленде. Грудь. 1995; 108: 1640–7.
11. Hammer J. Приобретенная обструкция верхних дыхательных путей. Педиатр Респир
Ред.2004. 5: 25–33.
12. Галлахер П.Г., Майер 3-й руководитель. Подход к диагностике и лечению
перепончатого ларинготрахеобронхита у младенцев и
детей. Педиатр Emerg Care. 1991; 7: 337–42.
13. Eckel HE, Wideman B, Damm M, et al. Эндоскопия дыхательных путей в
Диагностика и лечение бактериального трахеита у детей. Int J
Оториноларингол. 1993. 27: 147–57.
14. Аль-Мутаири Б., Кирк В. Бактериальный трахеит у детей: подход к диагностике и лечению
.Педиатр детского здоровья. 2004; 9: 25–30.
15. Американская академия педиатрии. Дифтерия. В: Пикеринг Л.К.,
редактор. Отчет Комитета по инфекционным болезням за 2012 год. 29-е
изд. Деревня Элк Гроув: Американская академия педиатрии; 2012. с.
302.
16. Craig FW, Schunk JE. Заглоточный абсцесс у детей: клинические проявления
, применение визуализации и текущее лечение.
Педиатрия. 2003; 111: 1394–8.
17.Тебрюгге М., Кертис Н. Инфекции, связанные с верхними и средними
дыхательных путей. В: Лонг С.С., Пикеринг Л.К., Пробер К.Г., редакторы. Принципы
и Практика детских инфекционных болезней. 3-е изд. Нью-Йорк:
Elsevier Saunders; 2012. с. 205.
18. Schraff S, McGinn JD, Derkay CS. Перитонзиллярный абсцесс у детей:
10-летний обзор диагностики и лечения. Int J Pediatr
Оториноларингол. 2001; 57: 213–8.
19. Herzon FS, Никлаус П.Детский перитонзиллярный абсцесс: ведение
рекомендаций. Curr Probl Pediatr. 1996; 26: 270–8.
20. Балдассари С, Шах РК. Детский перитонзиллярный абсцесс: обзор.
Целевые препараты для лечения инфекционных расстройств. 2012; 12: 277–80.
21. Пассали Д., Лауриелло М., Беллусси Л. и др. Вдыхание инородных тел у
детей: обновленная информация. Acta Otorhinolaryngol Ital. 2010; 30: 27–32.
22. Ruiz FE. Инородные тела дыхательных путей у детей. Доступно по адресу http: //
www.uptodate.com/contents/airway-foreign-bodies-in-children.
Доступ 17 марта 2015 г.
23. Rovin JD, Rodgers BM. Аспирация инородных тел у детей. Педиатр
Ред. 2000; 21: 86–90.
24. Чаттерджи С., Чаттерджи П. Обращение с инородными телами в воздухе
прохода. Анестезия. 1972; 27: 390–5.
25. Cevizci N, Dokucu AI, Baskin D, et al. Виртуальная бронхоскопия как динамический метод
в диагностике и лечении предполагаемой аспирации тела.Eur J Pediatr Surg. 2008; 18: 398–401.
26. Рамирес-Фигероа JL, Gochicoa-Rangel LG, Ramirez-San Juan
DH, et al. Удаление инородного тела гибким фиброоптическим бронхоскопом-
рун у младенцев и детей. Педиатр Пульмонол. 2005; 40: 392–7.
27. Грин К.Г., Айзенберг Дж., Леонг А. и др. Гибкая эндоскопия дыхательных путей у детей
. Am Rev Respir Dis. 1992; 145: 233–5.
28. Bork K, Barnstedt SE. Лечение 193 эпизодов отека гортани —
мА с концентратом ингибитора С1 у пациентов с наследственным отеком ангио —
.Arch Intern Med. 2001; 161: 714–8.
29. Ван В., Аберер В., Эберл В. и др. Наследственный ангиоотек у
детей и подростков — консенсус в отношении терапевтических стратегий.
Eur J Pediatr. 2012; 171: 1339–48.
30. Мураро А., Робертс Дж., Кларк А. и др. Позиционный документ Европейской академии аллергологии и клинической иммунологии
: лечение
анафилаксии в детстве. Аллергия. 2007. 62: 857–71.
31. Дайя Х., Хосни А., Беджар-Солар I и др.Детский паралич голосовых складок.
Arch Otolaryngol Head Neck Surg. 2000; 126: 21–5.
32. Дедо Д. Д., Дедо Х. Х. Нейрогенные заболевания гортани. В: Stool
E, Alper CM, Arjinand EM, Casselbrant ML, Dohar JE, Yellon E,
редакторы. Детская отоларингология. Филадельфия: Сондерс; 2003. с.
1505–10.
33. Worley G, Bajaj Y, Cavalli L, et al. Лазерная аритеноидэктомия у
детей с двусторонней неподвижностью голосовых складок. J Laryngol Otol.
2007; 121: 25–7.

 6 мг / кг
6 мг / кг