Когда грудное вскармливание невозможно — «Клиники Чайка»
Инфекции у матери
Самые частые инфекционные заболевания – простуды (ОРВИ) и кишечные инфекции – не являются противопоказанием для грудного вскармливания. Мама, находясь в близком контакте с ребенком, конечно, может заразить его, но возбудители этих заболеваний не передаются через молоко, и заразной мама обычно становится за несколько часов (а то и за сутки) до появления у нее первых симптомов. Поэтому единственной мерой профилактики является соблюдение личной гигиены (см. рекомендации в статьях, посвященных ОРВИ и кишечным инфекциям).
Инфекционные заболевания, при которых необходимы некоторые ограничения
- Женщина, болеющая гриппом h2N1 должна быть разделена с ребенком до тех пор, пока у нее не нормализуется температура. Сцеженное ею молоко можно давать ребенку.
- При ВИЧ-инфекции женщине не следует кормить ребенка грудью.
 Исключение составляют ситуации, когда другого питания для ребенка нет.
Исключение составляют ситуации, когда другого питания для ребенка нет. - Женщина, у которой кровь положительна на Т-лимфотропный вирус человека типов I и II, и которая не получает лечения по поводу имеющегося у нее бруцеллеза, не должна кормить грудью или сцеженным грудным молоком.
- Женщина, у которой есть на груди герпетические высыпания, не должна кормить ребенка этой грудью (другой можно, т.к. вирус передается только при непосредственном контакте). Матери следует соблюдать тщательную гигиену, прикрывать высыпания на груди, чтобы ребенок не мог их коснуться. Женщина может аккуратно сцеживать молоко и давать ее ребенку.
- Женщина, которая заболела ветряной оспой в течение 5-ти дней до и 2-х дней после родов должна быть разделена с ребенком, но сцеженное ею молоко можно давать ребенку. В отношении непривитой и неболевшей женщины, которая была в контакте с больным ветряной оспой, следует рассмотреть вопрос экстренной специфической профилактики – вакцинации или введения иммуноглобулина.

- Женщина с активной формой туберкулеза не должна кормить ребенка грудью, пока она будет заразна (обычно в течение 2-х недель после начала противотуберкулезного лечения). Поскольку инфекция передается с выдыхаемым воздухом, а не через молоко, то сцеженное ею молоко можно давать ребенку. Прием противотуберкулезных препаратов не является противопоказанием для грудного вскармливания.
- Если у женщины гепатит, то она может кормить ребенка грудью после проведения иммунопрофилактики.
- Риск передачи цитомегаловирусной инфекции через грудное молоко крайне низкий, за исключением детей, рожденных с очень низким весом, у которых высока вероятность проявления симптомов этой инфекции. Таким детям можно давать грудное молоко после пастеризации (30 минут при т-ре 62,5 градусов С или 5 минут при 72 градуса С).
Заметьте: о стафилококке в молоке у мамы ни слова!
Употребление мамой различных веществ
Совместимость грудного вскармливания с приемом алкоголя, наркотиков, лекарственных препаратов, а также с курением следует обсуждать лично с педиатром, поскольку все зависит от того, какие конкретно препараты мама принимает и как часто она это делает. В целом:
В целом:
Злоупотребление матерью алкоголем или наркотиками, а также курение – не жесткое противопоказание.
Прием мамой лекарственных средств чаще всего не является показанием для прекращения грудного вскармливания (см. статью об этом).
Заболевания ребенка
Ребенок может плохо себя чувствовать и быть очень слабым вследствие того, что он, например, недоношенный, очень мало весит или серьезно болен. Если из-за этого ему будет тяжело сосать грудь, его могут начать кормить из бутылочки. Если и это у него будут плохо получаться, то ему могут вводить молоко через зонд в желудок или поставить капельницу с питательными веществами. В медицинских учреждениях маме могут отказать в приеме ее молока и перевести ребенка на смесь, но связано это в первую очередь с тем, что медицинский персонал не может быть уверен, что мама соблюдает личную гигиену и правильно хранит молоко, а для больного ребенка это особенно важно.
В остальных случаях противопоказаниями для естественного вскармливания могут быть только некоторые нарушения обмена веществ:
- Галактоземия у ребенка – абсолютное противопоказание к грудному вскармливанию. Дети с этим заболеванием не могут перерабатывать один из компонентов грудного молока – галактозу, накопление которой в организме ребенка ведет к необратимым изменениям. Если скрининг на это заболевание пришел положительный, но у ребенка нет его проявлений, то мама все равно должна срочно прекратить грудное вскармливание, но до подтверждения диагноза ей следует сцеживать и замораживать молоко.
- При других нарушениях метаболизма, таких как фенилкетонурия, можно частично сохранить грудное вскармливание, но надо будет регулярно контролировать в крови ребенка уровень некоторых веществ.
Обратите внимание: лейкоциты в кале, сыпь, лактазная недостаточность и т.п. не рассматриваются как поводы перевода ребенка на искусственное вскармливание!
Некоторые особенности груди у женщины могут мешать наладить грудное вскармливание
- Гипоплазия ткани молочной железы (т.

- Плоские и втянуты соски могут мешать ребенку находить место для присасывания и удерживать грудь во рту. В такой ситуации требуется больше терпения и стараний для налаживания грудного вскармливания, но со временем ребенок привыкает к особенностям груди его матери. Во время беременности соски не надо никак готовить.
- Предыдущие операции на груди могут приводить к тому, что у женщины будет образовываться меньше молока. Кроме того у нее выше вероятность застоя молока (лактостаза). Однако совсем необязательно, что у конкретной женщины после операции на груди будут какие-то проблемы с грудным вскармливанием.
Диета матери, в том числе гипокалорийная
- Количество образовываемого молока зависит не от того, сколько женщина ест, а от того, сколько она пьет.
 Качество, то есть насыщенность молока питательными веществами, слабо связано с тем, что женщина ест. Однако следует обсудить с педиатром, необходимо ли женщине, исключившей из своего питания те или иные продукты (например, при вегетарианстве), принимать добавки витаминов и микроэлементов.
Качество, то есть насыщенность молока питательными веществами, слабо связано с тем, что женщина ест. Однако следует обсудить с педиатром, необходимо ли женщине, исключившей из своего питания те или иные продукты (например, при вегетарианстве), принимать добавки витаминов и микроэлементов.
Лучше, чтобы женщина получала витамины и минералы из пищи, а не из специальных витаминно-минеральных комплексов. Если женщина разнообразно питается, то ей не нужны специальные добавки. Исключение составляют женщины, которым была проведена операция на желудке.
Следующая беременность – не противопоказание для кормления грудью
- Однако одновременная беременная и кормящая женщина должна пить много жидкости и получать достаточное количество калорий.
- Сосание груди стимулирует сокращения матки. Поэтому в связи с отсутствием данных относительно влияния грудного вскармливания на осложненные беременности, беременности с высоким риском преждевременных родов или маточно-плацентарной недостаточностью (например, при преэклампсии, задержке роста плода), в таких случаях, вероятно, следует прекратить грудное вскармливание на сроке около 24 недель – это решается индивидуально на приеме у гинеколога.

С использованием UpToDate.
Кормление грудью при кишечных инфекциях
Все кишечные инфекции делятся на бактериальные (сальмонеллез, дизентерия и т.д.) и вирусные (энтеровирус, ротавирус, норовирус и т.д.). Энтеровирусные кишечные инфекции – это лето и начало осени; ротавирус и норовирус гуляют, преимущественно, зимой.
Основные положения:
1. Все вирусные кишечные инфекции передаются не только через грязные руки, но еще и воздушно-капельным путем. Поэтому, как правило, болеет вся семья, по очереди.
2. Клиника острых вирусных кишечных инфекций может быть разной. Ротавирус – это, как правило, высокая температура+частая рвота+многократный понос. Норовирус – это, как правило, сильнейшая тошнота и интоксикация+боли в животе+не очень сильно выраженный понос и рвота.
3. Иммунитет разный – к ротавирусу пожизненный, к норовирусу и к энтеровирусам на несколько месяцев. Поэтому норовирусной инфекцией болеть можно каждый год, а от ротавирусной инфекции существуют прививки
4. Основа лечения острых кишечных вирусных инфекций – борьба с обезвоживанием и интоксикацией, т.е. выпаивание. Отдельно и большими буквами – ЭНТЕРОФУРИЛ (он же ЭРСЕФУРИЛ) НЕ НУЖЕН при острых кишечных вирусных инфекциях! Можно использовать смекту (неосмектин и т.д.) и пробиотики на основе L rhamnosus GG и S boulardii, хотя однозначного мнения на эту тему нет. Мотилиум, церукал, имодиум и прочие препараты от рвоты или поноса – только по очной рекомендации врача! Ферментные препараты (мезим, креон и т.д.) не нужны.
5. Выпаивание – основа помощи для ребенка. Вначале о технике, потом о выборе продуктов для выпаивания.
a. Техника очень проста. Представьте себя капельницей. Берете жидкость, берете чайную ложку, ставите перед собой часы – и начинаете давать каждые 3-4 минуты по 1 ложечке жидкости. Кап.Кап.Кап.Кап.Кап.Кап – и так, пока не выпоите хотя бы стакан жидкости. Если вы хотите дать смекту или какой-то другой жидкий препарат – включаете его в выпаивание. Ложечка жидкости – 4 минуты – ложечка препарата – 4 минуты – ложечка жидкости и т.д. Через 40-60 минут выпаивания интервалы можно чуть-чуть сократить, до 2-3 минут. Больших объемов питья одномоментно не давать – опять начнет тошнить.
Техника очень проста. Представьте себя капельницей. Берете жидкость, берете чайную ложку, ставите перед собой часы – и начинаете давать каждые 3-4 минуты по 1 ложечке жидкости. Кап.Кап.Кап.Кап.Кап.Кап – и так, пока не выпоите хотя бы стакан жидкости. Если вы хотите дать смекту или какой-то другой жидкий препарат – включаете его в выпаивание. Ложечка жидкости – 4 минуты – ложечка препарата – 4 минуты – ложечка жидкости и т.д. Через 40-60 минут выпаивания интервалы можно чуть-чуть сократить, до 2-3 минут. Больших объемов питья одномоментно не давать – опять начнет тошнить.
b. Выбор жидкости для выпаивания. ТОЛЬКО НЕ РЕГИДРОН!! Нет, его тоже можно и он прекрасен. Но только после того, как ребенка посмотрел врач и рекомендовал именно регидрон. Самостоятельно его использовать не надо. Там много солей, при неправильном использовании Регидрон может провоцировать дополнительное разжижение стула – и добавочную потерю жидкости. Из готовых препаратов для выпаивания лучше выбирать Гастролит или Хумана электролит. Также можно использовать морковно-рисовый отвар (есть готовый от Хипп, есть рецепты в интернете). До консультации врача, и если под рукой ничего другого нет, лучше возьмите для начала обычный некрепкий подслащенный чай. Или разведенный компот из сухофруктов (изюм, курага). Или разведенный яблочный сок, или разведенную кока-колу, из которой выпустили газ.
Также можно использовать морковно-рисовый отвар (есть готовый от Хипп, есть рецепты в интернете). До консультации врача, и если под рукой ничего другого нет, лучше возьмите для начала обычный некрепкий подслащенный чай. Или разведенный компот из сухофруктов (изюм, курага). Или разведенный яблочный сок, или разведенную кока-колу, из которой выпустили газ.
c. Через несколько часов выпаивания, когда состояние ребенка немного стабилизировалось, обязательно предложите ему еду! Голод на фоне кишечной инфекции может сам по себе провоцировать развитие рвоты. Поэтому ставьте под нос маленькие порции еды – соленые сухие крекеры, изюм, курага, нарезанные кусочки банана, самодельные сухарики из белого или черного хлеба с солью или сахаром и т.д., пусть берет по аппетиту и продолжает пить-пить-пить. Если ребенок сам попросил что-то съесть – дайте! Только все небольшими порциями, на блюдечке. Лучше поесть три раза по чуть-чуть, чем один раз полную порцию.
6. На что обращать внимание. На мочу. В первую очередь, на мочу. Ребенок должен писать. Часто. И моча должна быть светлой, прозрачной, без сильного запаха. Если моча концентрированная – жидкости в организме не хватает, надо поить. Если ребенок писает редко и у него понос – нужна срочная консультация врача.
На мочу. В первую очередь, на мочу. Ребенок должен писать. Часто. И моча должна быть светлой, прозрачной, без сильного запаха. Если моча концентрированная – жидкости в организме не хватает, надо поить. Если ребенок писает редко и у него понос – нужна срочная консультация врача.
7. Питание ребенка – после выпаивания и прекращения частой рвоты, т.е. на 2-5 день болезни – может быть практически таким же, как и до болезни. Да, без фаст-фуда и без консервов, но основной набор – мясо-овощи-крупы-рыба и т.д. – остается прежним, специфических ограничивающих диет не надо. Супы-каша-салаты и прочее. Исключение – молоко и молочные продукты (сыр, творог, каши на молоке и т.д.). Вирусные кишечные инфекции поражают тонкий кишечник, в котором вырабатывается лактаза, фермент, необходимый для переваривания молочного сахара лактозы. Соответственно, для восстановления слизистой и выработки фермента в полном объеме требуется время, от 7 до 14 дней. Если в этот период – без фермента – будет поступать с питанием лактоза, начнется пенистый понос и боли в животе. Поэтому либо исключаем продукты с лактозой (молоко, сыр, творог, в тяжелых случаях – и кисломолочные напитки), либо предлагаем безлактозные варианты, либо добавляем к молочным продуктам фермент лактазу (Лактазар, Лактаза-беби). Также про питание напоминаю известные факты:
Поэтому либо исключаем продукты с лактозой (молоко, сыр, творог, в тяжелых случаях – и кисломолочные напитки), либо предлагаем безлактозные варианты, либо добавляем к молочным продуктам фермент лактазу (Лактазар, Лактаза-беби). Также про питание напоминаю известные факты:
i. Закреплению стула способствуют рис, черничный кисель (делайте сами! Крахмал+замороженная или сушеная черника), груша
ii. Кефир влияет на стул! Свежий кефир послабляет, а трехдневный – наоборот, крепит. К йогуртам это, кстати, не относится, по-моему…
Список литературы:
1.http://www.espghan.org/fileadmin/user_upload/guidelines_pdf/Guidelines_2404/European_Society_for_Pediatric_Gastroenterology_.26.pdf — европейский гайдлайн по лечению кишечных инфекций у детей
2. http://medspecial.ru/for_doctors/29/27940/ — про выбор напитков для регидратации
3. http://www.euro.who.int/__data/assets/pdf_file/0007/130696/9244593181R.pdf — ВОЗ-овский гайдлайн по лечению диареи у детей
Грудное вскармливание и острые кишечные инфекции
Документов на эту тему столько, что не знаешь, за что хвататься и на что ссылки давать. Даже в российские государственные рекомендации уже давно вошло, как определение – при острых кишечных инфекциях прерывать грудное вскармливание не надо!
Даже в российские государственные рекомендации уже давно вошло, как определение – при острых кишечных инфекциях прерывать грудное вскармливание не надо!
Поэтому кратко и по пунктам:
1. Грудное молоко играет важную роль в борьбе с кишечными инфекциями. Оно богато защитными веществами и, благодаря оптимальному солевому и углеводному составу, является наилучшим средством для выпаивания детей.
2. Дети на грудном вскармливании легче болеют и быстрее выздоравливают, чем дети без грудного молока.
3. Рвота и понос на фоне острой кишечной инфекции – ПОКАЗАНИЕ к грудному вскармливанию, а не противопоказание.
4. Ограничивать ребенка в количестве грудного молока не надо. Но, поскольку, на фоне кишечной инфекции рвота может провоцироваться, в том числе, быстрым поступлением большого объема пищи, иногда лучше сцедить грудное молоко и давать его из ложечки – выпаивать ребенка. Через 1-2 часа рвота, как правило, прекращается – и ребенка можно снова прикладывать к груди. Еще раз:
Еще раз:
a. Если у ребенка рвота-температура-понос, его надо кормить грудью. При этом все продукты прикорма даются только по желанию и аппетиту ребенка, а грудное молоко становится основным продуктом питания и питья, которое поступает малышу. Кормим по требованию, многие дети просто «повисают» на груди – это нормально и хорошо. Никаких искусственных ограничений – 5 минут раз в 2 часа и т.д. – не надо! Наоборот, жидкость должна поступать постоянно, для борьбы с обезвоживанием
b. Если малыш прикладывается, жадно сосет, его тошнит, он снова прикладывается и его опять тут же начинает тошнить – и так по кругу – можно сцедить 100-200 мл грудного молока и давать их из ложечки, по 1 ложечке в 3-4 минуты (время засекать по часам!). После того, как рвота прекратилась (как правило, через 1-2 часа) – ребенка можно снова прикладывать к груди
c. Если рвота у ребенка возникает независимо от активного сосания – никакого специального выпаивания грудным молоком не надо, можно просто прикладывать и прикладывать к груди. Да, это инфекция, ребенка будет тошнить, увы.
Да, это инфекция, ребенка будет тошнить, увы.
5. Одним из основных углеводов грудного молока является лактоза. На фоне острых кишечных инфекций организм часто теряет способность переваривать этот углевод. Это называется вторичная лактазная недостаточность. Для лечения вторичной лактазной недостаточности достаточно давать ребенку препараты фермента лактазы. Дозировку, начало и длительность приема определяется врач, обычно хватает 7-14 дневного курса лечения, после чего можно возвращаться к обычной практике грудного вскармливания
Ссылки (их миллионы, привожу русскоязычные, с подтверждением того, что при кишечной инфекции можно и нужно кормить грудным молоком):
1. КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ (ПРОТОКОЛ ЛЕЧЕНИЯ) ОКАЗАНИЯ МЕДИЦИНСКОЙ ПОМОЩИ ДЕТЯМ БОЛЬНЫМ РОТАВИРУСНОЙ ИНФЕКЦИЕЙ — «Дети с ротавирусным гастроэнтеритом, находящиеся на естественном вскармливании, продолжают получать грудное молоко, при необходимости проводится коррекция диеты матери, при выраженной клинике лактазной недостаточности возможно использование фермента лактазы (из расчета: 700 единиц на 100 мл грудного молока)»
2. Национальная программа оптимизации вскармливания детей первого года жизни в РФ – «Сохраняется грудное молоко», «при грудном вскармливании – лактаза»
Национальная программа оптимизации вскармливания детей первого года жизни в РФ – «Сохраняется грудное молоко», «при грудном вскармливании – лактаза»
3. Лечебное питание при острых кишечных инфекциях у детей — «Оптимальным видом питания грудных детей является материнское молоко, которое назначают дробно до 10 раз в день (каждые 2 часа по 50,0 мл). Возможно применение принципа «свободного вскармливания».
4. Англоязычный метаанализ, подтверждающий, в том числе, что грудное вскармливание полезно и необходимо при острых кишечных инфекциях у детей
5. Все тоже самое, только подробнее + ссылки на украинские источники
Суламифь Вольфсон, врач-педиатр. Оригинал публикации
Перейти к другим интересным статьям по ГВ для мам
Наши полезные и интересные вебинары для кормящих мам
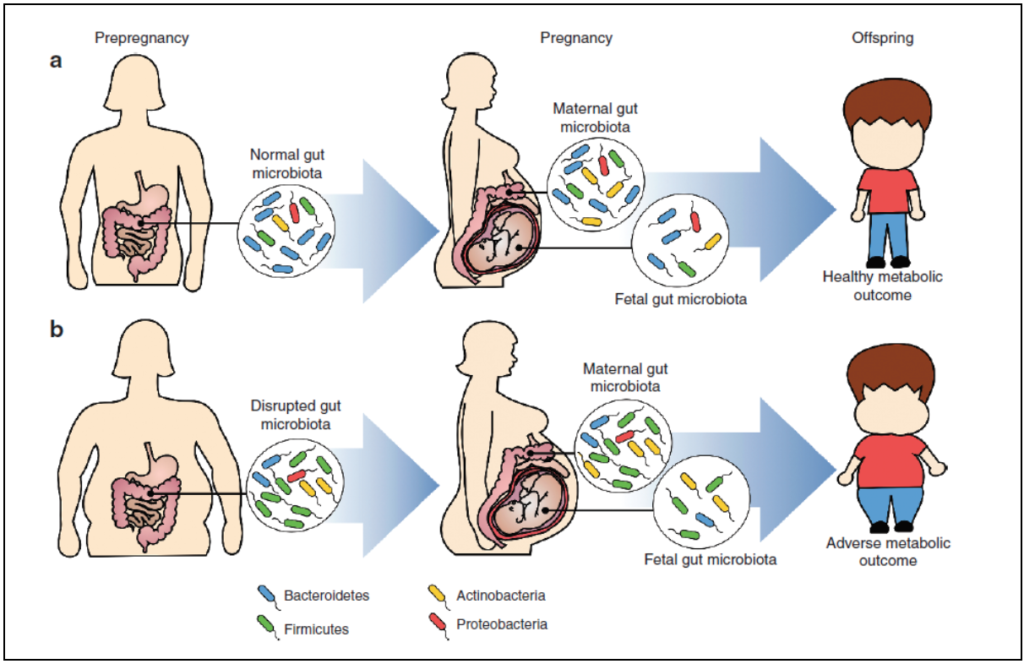
Человеческое грудное молоко и врожденная иммунная система желудочно-кишечного тракта
1. Gill N, Wlodarska M, Finlay BB. Будущее иммунологии слизистых оболочек: изучение интегрированного общесистемного органа. Нат Иммунол. 2010;11(7):558–60. [PubMed] [Google Scholar]
Gill N, Wlodarska M, Finlay BB. Будущее иммунологии слизистых оболочек: изучение интегрированного общесистемного органа. Нат Иммунол. 2010;11(7):558–60. [PubMed] [Google Scholar]
2. Берг Р.Д. Аборигенная микрофлора желудочно-кишечного тракта. Тенденции микробиол. 1996;4(11):430–5. [PubMed] [Google Scholar]
3. Раздел о грудном вскармливании. Грудное вскармливание и использование грудного молока. Педиатрия. 2012;129(3):e827–41. [PubMed] [Академия Google]
4. Лоннердал Б. Грудное молоко: действительно функциональная пища. Питание. 2000;16(7–8):509–11. [PubMed] [Google Scholar]
5. Ньюбург Д.С. Врожденный иммунитет и грудное молоко. Дж Нутр. 2005;135(5):1308–12. [PubMed] [Google Scholar]
6. Grulee CG, Sanford HN, Herron PH. Грудное и искусственное вскармливание. J Am Med Assoc. 1934; 103: 735–8. [Google Scholar]
7. Лукас А., Коул Т.Дж. Грудное молоко и неонатальный некротизирующий энтероколит. Ланцет. 1990;336(8730):1519–23. [PubMed] [Академия Google]
8. Strand TA, Sharma PR, Gjessing HK, et al. Факторы риска длительной острой диареи у детей раннего возраста. ПЛОС Один. 2012;7(5):e36436. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Strand TA, Sharma PR, Gjessing HK, et al. Факторы риска длительной острой диареи у детей раннего возраста. ПЛОС Один. 2012;7(5):e36436. [Бесплатная статья PMC] [PubMed] [Google Scholar]
9. Bachrach VR, Schwarz E, Bachrach LR. Грудное вскармливание и риск госпитализации по поводу респираторных заболеваний в младенчестве: метаанализ. Arch Pediatr Adolesc Med. 2003;157(3):237–43. [PubMed] [Google Scholar]
10. Duncan B, Ey J, Holberg CJ, et al. Исключительно грудное вскармливание в течение как минимум 4 месяцев защищает от среднего отита. Педиатрия. 1993;91(5):867–72. [PubMed] [Google Scholar]
11. Dewey KG, Heinig MJ, Nommsen-Rivers LA. Различия в заболеваемости детей, находящихся на грудном и искусственном вскармливании. J Педиатр. 1995; 126 (5 часть 1): 696–702. [PubMed] [Google Scholar]
12. Бодри М., Дюфур Р., Марку С. Связь между вскармливанием младенцев и инфекциями в течение первых шести месяцев жизни. J Педиатр. 1995;126(2):191–7. [PubMed] [Google Scholar]
13. Скариати П.Д., Груммер-Страун Л.М., Фейн С.Б. Продольный анализ младенческой заболеваемости и степени грудного вскармливания в Соединенных Штатах. Педиатрия. 1997;99(6):Е5. [PubMed] [Google Scholar]
Скариати П.Д., Груммер-Страун Л.М., Фейн С.Б. Продольный анализ младенческой заболеваемости и степени грудного вскармливания в Соединенных Штатах. Педиатрия. 1997;99(6):Е5. [PubMed] [Google Scholar]
14. Duffy LC, Faden H, Wasielewski R, et al. Исключительно грудное вскармливание защищает от бактериальной колонизации и воздействия дневного ухода за средним отитом. Педиатрия. 1997;100(4):E7. [PubMed] [Google Scholar]
15. Marild S, Hansson S, Jodal U, et al. Защитный эффект грудного вскармливания от инфекций мочевыводящих путей. Акта Педиатр. 2004;93(2):164–8. [PubMed] [Google Scholar]
16. Баллард О., Морроу А.Л. Состав грудного молока: питательные вещества и биологически активные факторы. Педиатр Клин Норт Ам. 2013;60(1):49–74. [Бесплатная статья PMC] [PubMed] [Google Scholar]
17. Laboisse C, Jarry A, Branka JE, et al. Регуляция экзоцитоза муцина из бокаловидных клеток кишечника. Биохим Сок Транс. 1995;23(4):810–3. [PubMed] [Google Scholar]
18. Lievin-Le Moal V, Servin AL. Передняя линия кишечной защиты хозяина от нежелательного проникновения вредоносных микроорганизмов: муцинов, антимикробных пептидов и микробиоты. Clin Microbiol Rev. 2006;19(2):315–37. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Lievin-Le Moal V, Servin AL. Передняя линия кишечной защиты хозяина от нежелательного проникновения вредоносных микроорганизмов: муцинов, антимикробных пептидов и микробиоты. Clin Microbiol Rev. 2006;19(2):315–37. [Бесплатная статья PMC] [PubMed] [Google Scholar]
19. Йоханссон М.Е., Шовалл Х., Ханссон Г.К. Слизистая система желудочно-кишечного тракта в норме и при патологии. Нат Рев Гастроэнтерол Гепатол. 2013;10(6):352–61. [Бесплатная статья PMC] [PubMed] [Google Scholar]
20. Johansson ME, Ambort D, Pelaseyed T, et al. Состав и функциональная роль слизистых оболочек кишечника. Cell Mol Life Sci. 2011;68(22):3635–41. [PubMed] [Google Scholar]
21. Johansson ME, Larsson JM, Hansson GC. Два слизистых слоя толстой кишки организованы муцином MUC2, тогда как внешний слой является законодателем взаимодействий между хозяином и микробами. Proc Natl Acad Sci U S A. 2011; 108 (Suppl 1): 4659.–65. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Johansson ME, Phillipson M, Petersson J, et al. Внутренняя часть двух муцин-зависимых слоев слизи Muc2 в толстой кишке лишена бактерий. Proc Natl Acad Sci U S A. 2008;105(39):15064–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Внутренняя часть двух муцин-зависимых слоев слизи Muc2 в толстой кишке лишена бактерий. Proc Natl Acad Sci U S A. 2008;105(39):15064–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
23. McElroy SJ, Weitkamp JH. Врожденный иммунитет в тонкой кишке недоношенного ребенка. Необзоры. 2011;12(9):e517–26. [Бесплатная статья PMC] [PubMed] [Google Scholar]
24. Heazlewood CK, Cook MC, Eri R, et al. Аберрантная сборка муцина у мышей вызывает стресс эндоплазматического ретикулума и спонтанное воспаление, напоминающее язвенный колит. ПЛОС Мед. 2008;5(3):e54. [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Sherman MP, Bennett SH, Hwang FF, et al. Клетки Панета и антибактериальная защита хозяина в тонком кишечнике новорожденных. Заразить иммун. 2005;73(9):6143–6. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Rakoff-Nahoum S, Paglino J, Eslami-Varzaneh F, et al. Распознавание комменсальной микрофлоры толл-подобными рецепторами необходимо для гомеостаза кишечника. Клетка. 2004;118(2):229–41. [PubMed] [Google Scholar]
Клетка. 2004;118(2):229–41. [PubMed] [Google Scholar]
27. Андерсон Дж.М., Ван Итали К.М. Плотные соединения. Карр Биол. 2008;18(20):R941–3. [PubMed] [Google Scholar]
28. Balda MS, Fallon MB, Van Itallie CM, et al. Структура, регуляция и патофизиология плотных контактов в желудочно-кишечном тракте. Йель Дж Биол Мед. 1992;65(6):725–35. [обсуждение: 737–40] [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Clayburgh DR, Shen L, Turner JR. Пористая защита: негерметичный эпителиальный барьер при кишечных заболеваниях. Лаборатория Инвест. 2004;84(3):282–91. [PubMed] [Google Scholar]
30. Сартор Р.Б. Влияние микробов при воспалительных заболеваниях кишечника. Гастроэнтерология. 2008; 134(2):577–9.4. [PubMed] [Google Scholar]
31. Henry MC, Moss RL. Некротизирующий энтероколит новорожденных. Семин Педиатр Хирург. 2008;17(2):98–109. [PubMed] [Google Scholar]
32. Исмаил А.С., Берендт К.Л., Хупер Л.В. Реципрокные взаимодействия между комменсальными бактериями и внутриэпителиальными гамма-дельта-лимфоцитами при повреждении слизистой оболочки. Дж Иммунол. 2009;182(5):3047–54. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Дж Иммунол. 2009;182(5):3047–54. [Бесплатная статья PMC] [PubMed] [Google Scholar]
33. Varol C, Zigmond E, Jung S. Защита иммунного каната: мононуклеарные фагоциты в собственной пластинке кишечника. Нат Рев Иммунол. 2010;10(6):415–26. [PubMed] [Академия Google]
34. Спитс Х., Ди Санто Дж.П. Растущее семейство врожденных лимфоидных клеток: регуляторы и эффекторы иммунитета и ремоделирования тканей. Нат Иммунол. 2011;12(1):21–7. [PubMed] [Google Scholar]
35. Подробнее K, Athalye-Jape G, Rao S, et al. Ассоциация ингибиторов секреции желудочного сока и более высокой частоты некротизирующего энтероколита у недоношенных детей с очень низкой массой тела при рождении. Ам Дж. Перинатол. 2013;30(10):849–56. [PubMed] [Google Scholar]
36. Terrin G, Passariello A, De Curtis M, et al. Ранитидин связан с инфекциями, некротизирующим энтероколитом и летальным исходом у новорожденных. Педиатрия. 2012;129(1): e40–5. [PubMed] [Google Scholar]
37. Bianconi S, Gudavalli M, Sutija VG, et al. Ранитидин и поздний сепсис в отделении интенсивной терапии новорожденных. J Перинат Мед. 2007;35(2):147–50. [PubMed] [Google Scholar]
Ранитидин и поздний сепсис в отделении интенсивной терапии новорожденных. J Перинат Мед. 2007;35(2):147–50. [PubMed] [Google Scholar]
38. Graham PL, 3rd, Begg MD, Larson E, et al. Факторы риска позднего грамотрицательного сепсиса у новорожденных с низкой массой тела при рождении, госпитализированных в отделение реанимации новорожденных. Pediatr Infect Dis J. 2006;25(2):113–7. [PubMed] [Google Scholar]
39. Лоуренс Р.М., Pane CA. Грудное молоко человека: современные представления об иммунологии и инфекционных заболеваниях. Curr Probl Pediatr Adolesc Health Care. 2007;37(1):7–36. [PubMed] [Академия Google]
40. Гольдман А.С. Иммунная система женского молока: антимикробные, противовоспалительные и иммуномодулирующие свойства. Pediatr Infect Dis J. 1993;12(8):664–71. [PubMed] [Google Scholar]
41. Gross SJ, Buckley RH, Wakil SS, et al. Повышенная концентрация IgA в молоке матерей, родивших недоношенных детей. J Педиатр. 1981; 99(3):389–93. [PubMed] [Google Scholar]
42. Schlesinger L, Munoz C, Arevalo M, et al. Функциональная способность колостральных лейкоцитов у женщин, родивших преждевременно. J Pediatr Gastroenterol Nutr. 1989;8(1):89–94. [PubMed] [Google Scholar]
Schlesinger L, Munoz C, Arevalo M, et al. Функциональная способность колостральных лейкоцитов у женщин, родивших преждевременно. J Pediatr Gastroenterol Nutr. 1989;8(1):89–94. [PubMed] [Google Scholar]
43. Мехта Р., Петрова А. Биологически активные белки грудного молока в связи с очень преждевременными родами и периодом лактации. Дж. Перинатол. 2011;31(1):58–62. [PubMed] [Google Scholar]
44. Гарофало Р. Цитокины в грудном молоке. J Педиатр. 2010; 156 (Приложение 2): S36–40. [PubMed] [Google Scholar]
45. Saarinen UM, Kajosaari M. Грудное вскармливание как профилактика атопического заболевания: проспективное наблюдение до 17 лет. Ланцет. 1995;346(8982):1065–9. [PubMed] [Google Scholar]
46. Koletzko S, Sherman P, Corey M, et al. Роль практики вскармливания младенцев в развитии болезни Крона в детском возрасте. БМЖ. 1989; 298 (6688): 1617–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
47. Mayer EJ, Hamman RF, Gay EC, et al. Снижение риска ИЗСД среди детей, находящихся на грудном вскармливании. Диабет реестра IDDM штата Колорадо. 1988;37(12):1625–32. [PubMed] [Google Scholar]
Диабет реестра IDDM штата Колорадо. 1988;37(12):1625–32. [PubMed] [Google Scholar]
48. Уокер А. Грудное молоко как золотой стандарт защитных питательных веществ. J Педиатр. 2010; 156 (Приложение 2): S3–7. [PubMed] [Академия Google]
49. Маккракен В.Дж., Лоренц Р.Г. Экосистема желудочно-кишечного тракта: шаткий союз эпителия, иммунитета и микробиоты. Клеточная микробиология. 2001;3(1):1–11. [PubMed] [Google Scholar]
50. Уокер, Вашингтон. Начальная кишечная колонизация у младенцев и иммунный гомеостаз. Энн Нутр Метаб. 2013; 63 (Приложение 2): 8–15. [PubMed] [Google Scholar]
51. Collier-Hyams LS, Sloane V, Batten BC, et al. Передний край: бактериальная модуляция эпителиальной передачи сигналов посредством изменений в неддиляции куллина-1. Дж Иммунол. 2005;175(7):4194–8. [PubMed] [Google Scholar]
52. Hooper LV, Wong MH, Thelin A, et al. Молекулярный анализ комменсальных отношений хозяин-микроб в кишечнике. Наука. 2001;291(5505):881–4. [PubMed] [Google Scholar]
53. Kelly D, Campbell JI, King TP, et al. Комменсальные анаэробные кишечные бактерии ослабляют воспаление, регулируя ядерно-цитоплазматический перенос PPAR-гамма и RelA. Нат Иммунол. 2004;5(1):104–12. [PubMed] [Google Scholar]
Kelly D, Campbell JI, King TP, et al. Комменсальные анаэробные кишечные бактерии ослабляют воспаление, регулируя ядерно-цитоплазматический перенос PPAR-гамма и RelA. Нат Иммунол. 2004;5(1):104–12. [PubMed] [Google Scholar]
54. Tao Y, Drabik KA, Waypa TS, et al. Растворимые факторы от Lactobacillus GG активируют МАРК и индуцируют цитопротекторные белки теплового шока в эпителиальных клетках кишечника. Am J Physiol Cell Physiol. 2006; 290(4):C1018–30. [PubMed] [Google Scholar]
55. Yan F, Polk DB. Пробиотическая бактерия предотвращает индуцированный цитокинами апоптоз в эпителиальных клетках кишечника. Дж. Биол. Хим. 2002;277(52):50959–65. [Бесплатная статья PMC] [PubMed] [Google Scholar]
56. Mirpuri J, Brazil JC, Berardinelli AJ, et al. Комменсал Escherichia coli снижает апоптоз эпителия за счет опосредованной IFN-альфаА индукции гуанилат-связывающего белка-1 в моделях развивающегося кишечника человека и мыши. Дж Иммунол. 2010; 184(12):7186–9. 5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
57. Rimoldi M, Chieppa M, Salucci V, et al. Кишечный иммунный гомеостаз регулируется перекрестными помехами между эпителиальными клетками и дендритными клетками. Нат Иммунол. 2005;6(5):507–14. [PubMed] [Google Scholar]
58. Yoshioka H, Iseki K, Fujita K. Развитие и различия кишечной флоры в неонатальном периоде у детей, находящихся на грудном и искусственном вскармливании. Педиатрия. 1983;72(3):317–21. [PubMed] [Google Scholar]
59. Ньюбург Д.С. Неонатальная защита врожденной иммунной системой грудного молока, состоящей из олигосахаридов и гликанов. J Anim Sci. 2009 г.; 87 (Приложение 13): 26–34. [PubMed] [Google Scholar]
60. McVeagh P, Miller JB. Олигосахариды грудного молока: только грудное. J Педиатр Здоровье ребенка. 1997;33(4):281–6. [PubMed] [Google Scholar]
61. Insoft RM, Sanderson IR, Walker WA. Развитие иммунной функции в кишечнике и ее роль в заболеваниях новорожденных. Педиатр Клин Норт Ам. 1996;43(2):551–71. [PubMed] [Google Scholar]
1996;43(2):551–71. [PubMed] [Google Scholar]
62. Ньюбург Д.С. Олигосахариды и гликоконъюгаты в грудном молоке: их роль в защите хозяина. J Биол. неоплазия молочной железы. 1996;1(3):271–83. [PubMed] [Google Scholar]
63. Brandtzaeg P. Иммунная система слизистых оболочек и ее интеграция с молочными железами. J Педиатр. 2010; 156 (Приложение 2): S8–15. [PubMed] [Google Scholar]
64. Xanthou M, Bines J, Walker WA. Грудное молоко и защита кишечника у новорожденных: обновленная информация. Adv Педиатр. 1995; 42: 171–208. [PubMed] [Google Scholar]
65. Хэнсон Л.А. Сравнительные иммунологические исследования иммуноглобулинов грудного молока и сыворотки крови. Int Arch Allergy Appl Immunol. 1961;18:241–67. [PubMed] [Google Scholar]
66. Newburg DS, Walker WA. Защита новорожденного врожденной иммунной системой развивающегося кишечника и грудного молока. Педиатр Рез. 2007;61(1):2–8. [PubMed] [Google Scholar]
67. Адамкин Д.Х. Материнское молоко, стратегии кормления и лактоферрин для профилактики некротизирующего энтероколита. JPEN J Parenter Enteral Nutr. 2012; 36 (Приложение 1): 25S–9S. [PubMed] [Google Scholar]
JPEN J Parenter Enteral Nutr. 2012; 36 (Приложение 1): 25S–9S. [PubMed] [Google Scholar]
68. Manzoni P, Rinaldi M, Cattani S, et al. Добавление коровьего лактоферрина для профилактики позднего сепсиса у новорожденных с очень низкой массой тела при рождении: рандомизированное исследование. ДЖАМА. 2009 г.;302(13):1421–1428. [PubMed] [Google Scholar]
69. Manzoni P, Stolfi I, Messner H, et al. Бычий лактоферрин предотвращает инвазивные грибковые инфекции у младенцев с очень низкой массой тела при рождении: рандомизированное контролируемое исследование. Педиатрия. 2012;129(1):116–23. [PubMed] [Google Scholar]
70. Валенти П., Антонини Г. Лактоферрин: важная защита хозяина от микробной и вирусной атаки. Cell Mol Life Sci. 2005;62(22):2576–87. [PubMed] [Google Scholar]
71. Kuwata H, Yip TT, Tomita M, et al. Прямые доказательства образования в желудке человека антимикробного пептидного домена (лактоферрицина) из проглоченного лактоферрина. Биохим Биофиз Акта. 1998;1429(1):129–41. [PubMed] [Google Scholar]
1998;1429(1):129–41. [PubMed] [Google Scholar]
72. Эллисон Р.Т., 3-й, Гил Т.Дж. Уничтожение грамотрицательных бактерий лактоферрином и лизоцимом. Джей Клин Инвест. 1991;88(4):1080–91. [Бесплатная статья PMC] [PubMed] [Google Scholar]
73. Sherman MP. Лактоферрин и некротизирующий энтероколит. Клин Перинатол. 2013;40(1):79–91. [Бесплатная статья PMC] [PubMed] [Google Scholar]
74. Mulligan P, White NR, Monteleone G, et al. Лактоферрин грудного молока регулирует экспрессию генов, связывая CpG-мотивы бактериальной ДНК, но не промоторы геномной ДНК в модельных клетках кишечника. Педиатр Рез. 2006; 59(5): 656–61. [Бесплатная статья PMC] [PubMed] [Google Scholar]
75. Manzoni P, Mostert M, Stronati M. Лактоферрин для профилактики неонатальных инфекций. Curr Opin Infect Dis. 2011;24(3):177–82. [PubMed] [Google Scholar]
76. Buccigrossi V, de Marco G, Bruzzese E, et al. Лактоферрин индуцирует зависимую от концентрации функциональную модуляцию кишечной пролиферации и дифференцировки. Педиатр Рез. 2007;61(4):410–4. [PubMed] [Google Scholar]
Педиатр Рез. 2007;61(4):410–4. [PubMed] [Google Scholar]
77. Haversen L, Ohlsson BG, Hahn-Zoric M, et al. Лактоферрин подавляет индуцированную ЛПС продукцию цитокинов в моноцитарных клетках через NF-каппа B. Cell Immunol. 2002; 220(2):83–9.5. [PubMed] [Google Scholar]
78. Лоннердал Б. Биоактивные белки грудного молока. J Педиатр Здоровье ребенка. 2013; 49 (Приложение 1): 1–7. [PubMed] [Google Scholar]
79. Plaisancie P, Claustre J, Estienne M, et al. Новый биоактивный пептид из йогуртов модулирует экспрессию гелеобразующего муцина MUC2, а также популяцию бокаловидных клеток и клеток Панета вдоль тонкой кишки. Дж. Нутр Биохим. 2013;24(1):213–21. [PubMed] [Google Scholar]
80. Лоннердал Б. Биоактивные белки в грудном молоке: механизмы действия. J Педиатр. 2010; 156 (Приложение 2): S26–30. [PubMed] [Академия Google]
81. Ньюбург Д.С. Защищают ли связывающие свойства олигосахаридов в молоке младенцев от желудочно-кишечных бактерий? Дж Нутр. 1997; 127 (Приложение 5): 980S–4S. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
82. Stromqvist M, Falk P, Bergstrom S, et al. Каппа-казеин грудного молока и ингибирование адгезии Helicobacter pylori к слизистой оболочке желудка человека. J Педиатр Гастро-энтерол Нутр. 1995;21(3):288–96. [PubMed] [Google Scholar]
83. Claud EC, Savidge T, Walker WA. Модуляция секреции IL-8 эпителиальными клетками кишечника человека факторами грудного молока. Педиатр Рез. 2003;53(3):419–25. [PubMed] [Google Scholar]
84. Neu J, Mihatsch WA, Zegarra J, et al. Система защиты слизистой оболочки кишечника, Часть 1. Согласованные рекомендации по иммунонутриентам. J Педиатр. 2013; 162 (Приложение 3): S56–63. [PubMed] [Google Scholar]
85. Garofalo R, Chheda S, Mei F, et al. Интерлейкин-10 в грудном молоке. Педиатр Рез. 1995; 37 (4 часть 1): 444–9. [PubMed] [Google Scholar]
86. Kuhn R, Lohler J, Rennick D, et al. У мышей с дефицитом интерлейкина-10 развивается хронический энтероколит. Клетка. 1993;75(2):263–74. [PubMed] [Google Scholar]
87. Glocker EO, Kotlarz D, Boztug K, et al. Воспалительные заболевания кишечника и мутации, влияющие на рецептор интерлейкина-10. N Engl J Med. 2009;361(21):2033–45. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Glocker EO, Kotlarz D, Boztug K, et al. Воспалительные заболевания кишечника и мутации, влияющие на рецептор интерлейкина-10. N Engl J Med. 2009;361(21):2033–45. [Бесплатная статья PMC] [PubMed] [Google Scholar]
88. Emami CN, Chokshi N, Wang J, et al. Роль интерлейкина-10 в патогенезе некротического энтероколита. Am J Surg. 2012;203(4):428–35. [Бесплатная статья PMC] [PubMed] [Google Scholar]
89. Dvorak B, Halpern MD, Holubec H, et al. Материнское молоко снижает тяжесть некротизирующего энтероколита и повышает интестинальный ИЛ-10 в модели новорожденных крыс. Педиатр Рез. 2003;53(3):426–33. [PubMed] [Академия Google]
90. Пенттила И.А. Молочный трансформирующий фактор роста-бета и иммунный ответ младенцев. J Педиатр. 2010; 156 (Приложение 2): S21–5. [PubMed] [Google Scholar]
91. Chang M, Suen Y, Lee SM, et al. Экспрессия трансформирующего фактора роста-бета-1, макрофагального воспалительного белка-1-альфа и интерлейкина-8 ниже в стимулированных неонатальных клетках человека по сравнению со взрослыми мононуклеарными клетками. Кровь. 1994;84(1):118–24. [PubMed] [Google Scholar]
Кровь. 1994;84(1):118–24. [PubMed] [Google Scholar]
92. Hawkes JS, Bryan DL, James MJ, et al. Цитокины (ИЛ-1бета, ИЛ-6, ФНО-альфа, ТФР-бета1 и ТФР-бета2) и простагландин Е2 в материнском молоке в течение первых трех месяцев после родов. Педиатр Рез. 1999;46(2):194–9. [PubMed] [Google Scholar]
93. Kalliomaki M, Ouwehand A, Arvilommi H, et al. Трансформирующий фактор роста-бета в грудном молоке: потенциальный регулятор атопического заболевания в раннем возрасте. J Аллергия Клин Иммунол. 1999;104(6):1251–7. [PubMed] [Google Scholar]
94. Oddy WH, Halonen M, Martinez FD, et al. TGF-бета в человеческом молоке связан с хрипами в младенчестве. J Аллергия Клин Иммунол. 2003;112(4):723–8. [PubMed] [Google Scholar]
95. Ogawa J, Sasahara A, Yoshida T, et al. Роль трансформирующего фактора роста-бета в грудном молоке для инициации продукции IgA у новорожденных. Ранний Хам Дев. 2004;77(1–2):67–75. [PubMed] [Академия Google]
96. Дворжак Б. Эпидермальный фактор роста молока и защита кишечника. J Педиатр. 2010; 156 (Приложение 2): S31–5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
J Педиатр. 2010; 156 (Приложение 2): S31–5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
97. Dvorak B, Fituch CC, Williams CS, et al. Повышение уровня эпидермального фактора роста в грудном молоке матерей с глубоко недоношенными детьми. Педиатр Рез. 2003;54(1):15–9. [PubMed] [Google Scholar]
98. Coursodon CF, Dvorak B. Эпидермальный фактор роста и некротизирующий энтероколит. Curr Opin Педиатр. 2012;24(2):160–4. [PubMed] [Академия Google]
99. Dvorak B, Halpern MD, Holubec H, et al. Эпидермальный фактор роста уменьшает развитие некротизирующего энтероколита в модели новорожденных крыс. Am J Physiol Gastrointest Liver Physiol. 2002; 282(1):G156–64. [PubMed] [Google Scholar]
100. Clark JA, Doelle SM, Halpern MD, et al. Нарушение кишечного барьера при экспериментальном некротизирующем энтероколите: защитный эффект лечения EGF. Am J Physiol Gastrointest Liver Physiol. 2006; 291(5):G938–49. [PubMed] [Академия Google]
101. Итикава М., Сугита М. , Такахаши М. и др. Макрофаги грудного молока спонтанно продуцируют гранулоцитарно-макрофагальный колониестимулирующий фактор и дифференцируются в дендритные клетки только в присутствии экзогенного интерлейкина-4. Иммунология. 2003;108(2):189–95. [Бесплатная статья PMC] [PubMed] [Google Scholar]
, Такахаши М. и др. Макрофаги грудного молока спонтанно продуцируют гранулоцитарно-макрофагальный колониестимулирующий фактор и дифференцируются в дендритные клетки только в присутствии экзогенного интерлейкина-4. Иммунология. 2003;108(2):189–95. [Бесплатная статья PMC] [PubMed] [Google Scholar]
102. Thormar H, Isaacs CE, Brown HR, et al. Инактивация оболочечных вирусов и уничтожение клеток жирными кислотами и моноглицеридами. Противомикробные агенты Chemother. 1987;31(1):27–31. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Антитела в грудном молоке помогают формировать кишечные бактерии и иммунитет младенцев
Исследователям уже давно известно, что материнское грудное молоко обеспечивает жизненно важные питательные вещества для новорожденных, а антитела от матерей, вакцинированных против определенных болезнетворных бактерий или вирусов, могут передаваться через грудное молоко детям. Теперь новое доклиническое исследование, проведенное исследователями Weill Cornell Medicine, показывает, что один конкретный набор антител, который естественным образом индуцируется полезными бактериями кишечника, может передаваться от матерей к младенцам через грудное молоко и помогает младенцам защищаться от диареи, вызванной инфекцией.
Исследование предполагает, что усиление этих «естественно вырабатываемых» антител у матерей может повысить иммунитет младенцев против бактериальных патогенов, вызывающих инфекционные желудочно-кишечные заболевания.
В исследовании, опубликованном 10 июня в журнале Science Immunology, команда исследователей сосредоточилась на классе антител, называемых IgG, которые помогают избавить организм от инфекционных бактерий и вирусов. Мало что было известно о том, как антитела IgG, которые естественным образом индуцируются кишечными бактериями, влияют на иммунитет кишечника младенцев. Поэтому исследователи использовали мышиную модель, чтобы определить, как эти IgG-антитела переносятся из крови матери в ее грудное молоко и как они защищают молодых мышей от Citrobacter rodentium (эквивалент патогенной кишечной палочки у людей), вызывающей потенциально опасные кишечные инфекции.
«Мы обнаружили, что эти IgG-антитела защищают от кишечной инфекции у младенцев, и что мы можем усилить эту защиту», — сказала старший автор Мелоди Цзэн, доцент кафедры иммунологии педиатрии на кафедре педиатрии и член Центра Гейла. и Институт детских исследований Иры Друкьер в Weill Cornell Medicine.
и Институт детских исследований Иры Друкьер в Weill Cornell Medicine.
Подобно тому, как антитела к вирусу SARS-CoV-2 обнаруживаются в грудном молоке женщин, привитых мРНК-вакциной от COVID-19, исследователи стремились обеспечить дополнительную защиту от кишечных инфекций у младенцев, индуцируя антитела IgG, которые могли бы передаваться таким образом. Они разработали вакцину с использованием компонента, обнаруженного в кишечных бактериях, а затем иммунизировали ею самок мышей, прежде чем они забеременели.
«Та же концепция, согласно которой вакцинация повышает уровень антител IgG у матерей и передает этот иммунитет ее детям, может защитить младенцев», — сказал Цзэн. «Эта стратегия может особенно принести пользу недоношенным детям, поскольку они, как правило, подвергаются гораздо более высокому риску диарейных заболеваний».
Такие инфекции представляют значительную опасность для детей младшего возраста в целом. По данным Всемирной организации здравоохранения, диарейные заболевания являются второй по значимости причиной смерти детей в возрасте до пяти лет.
В своих экспериментах исследователи, в том числе соавторы Кэтрин Санидад и Мохаммед Амир, оба постдокторские сотрудники в лаборатории Цзэна, впервые продемонстрировали, что при попадании к новорожденным мышам через грудное молоко IgG предотвращал прикрепление болезнетворных бактерий к слизистая оболочка кишечника младенцев, ранняя стадия инфекции.
Они также изучили, как IgG взаимодействует с другим набором микробов — полезными бактериями, живущими в кишечнике, — чтобы способствовать здоровому развитию кишечных бактерий у младенцев. Ученые обнаружили, что эти микробы способствуют развитию и функционированию иммунной системы. Например, полезные бактерии обучают иммунную систему распознавать своих патогенных родственников.
Это исследование также выявило долгосрочные эффекты этих защитных антител IgG. У мышей, которые никогда не получали IgG от своих матерей, в кишечнике развились аномальные микробные сообщества, что привело к изменениям в их иммунной системе. В частности, исследователи обнаружили увеличение количества иммунных клеток кишечника, которые продуцируют IL-17, провоспалительный цитокин, связанный с воспалительными заболеваниями.

 Исключение составляют ситуации, когда другого питания для ребенка нет.
Исключение составляют ситуации, когда другого питания для ребенка нет.