Какие признаки могут указать на неврологические проблемы ребенка при осмотре перед прививкой?
У маленьких детей — напряжение, выбухание большого родничка в вертикальном положении, расширение подкожных вен головы, частые срыгивания, излишние движения языка, повышение мышечного тонуса рук и ног, тремор (мелкое дрожание) подбородка и рук в спокойном состоянии, нарушение сна и пр. Перечисленные признаки могут свидетельствовать о повышенном внутричерепном давлении. Чрезмерно быстрый рост головы, увеличение размеров большого родничка, вместо его сокращения и другие признаки могут свидетельствовать о гидроцефальном синдроме — избыточном накоплении мозговой жидкости в желудочках мозга и других внутричерепных пространствах. Эти и другие заболевания нервной системы выявляет и описывает при плановом осмотре детей до 3-х месяцев невролог. Для подтверждения или исключения патологии проводят дополнительные исследования, например, ультразвуковое исследование головного мозга — нейросонографию. Многие педиатры, неврологи склонны настороженно относиться к вакцинации детей с неврологическими проблемами из-за боязни усугубить течение патологии в поствакцинальном периоде. Это не правильно, так как инфекция, от которой проводится прививка, гораздо более опасна для ребенка с поражением нервной системы. Например, коклюш у таких детей, особенно в возрасте до года может вызывать тяжелые поражения мозга, судороги и прочее. К сожалению, иногда о поражении нервной системы начинают думать уже после прививки, которая спровоцировала временные ухудшения в работе этой системы. Поэтому основным средством предупреждения поствакцинальных осложнений со стороны нервной системы является своевременное выявление неврологической патологии у новорожденного, ее лечение и проведение прививок на фоне медикаментозной терапии или по ее окончании. Какие медикаментозные средства обычно применяют при подготовке к иммунизации детей с неврологическими проблемами?
Многие педиатры, неврологи склонны настороженно относиться к вакцинации детей с неврологическими проблемами из-за боязни усугубить течение патологии в поствакцинальном периоде. Это не правильно, так как инфекция, от которой проводится прививка, гораздо более опасна для ребенка с поражением нервной системы. Например, коклюш у таких детей, особенно в возрасте до года может вызывать тяжелые поражения мозга, судороги и прочее. К сожалению, иногда о поражении нервной системы начинают думать уже после прививки, которая спровоцировала временные ухудшения в работе этой системы. Поэтому основным средством предупреждения поствакцинальных осложнений со стороны нервной системы является своевременное выявление неврологической патологии у новорожденного, ее лечение и проведение прививок на фоне медикаментозной терапии или по ее окончании. Какие медикаментозные средства обычно применяют при подготовке к иммунизации детей с неврологическими проблемами?
Детям с повышенным внутричерепным давлением и гидроцефальным синдромом, назначают мочегонные средства (в том числе травы), препараты, улучшающие кровоток и обмен веществ в мозговой ткани. Курсы терапии повторяют 2-3 раза в год, в эти же периоды может быть проведена иммунизация ребенка. Если прививку делают после завершения лечения, то желательно в момент иммунизации снова провести короткий курс ранее применявшихся средств (мочегонных, успокоительных и т.п.). Если у ребенка были судороги, вызванные повышенной температурой, прививки можно проводить не ранее, чем через 1 месяц после приступа. До и после прививки назначают противосудорожные, и иногда мочегонные лекарства. Детям, перенесшим судороги, причиной которых являлась температура выше 38,0 градусов С, в дальнейшем можно делать все прививки. Если судороги были на фоне температуры менее 38,0 градусов С, то не вводят коклюшную вакцину, входящую в состав комплексной вакцины против коклюша, дифтерии, столбняка (АКДС). Остальные вакцины могут быть использованы. Всем детям, ранее имевшим судороги или предрасположенным к ним, после прививки назначают и жаропонижающие препараты, так как вакцины могут вызвать высокую температуру и снова провоцировать судороги.
Курсы терапии повторяют 2-3 раза в год, в эти же периоды может быть проведена иммунизация ребенка. Если прививку делают после завершения лечения, то желательно в момент иммунизации снова провести короткий курс ранее применявшихся средств (мочегонных, успокоительных и т.п.). Если у ребенка были судороги, вызванные повышенной температурой, прививки можно проводить не ранее, чем через 1 месяц после приступа. До и после прививки назначают противосудорожные, и иногда мочегонные лекарства. Детям, перенесшим судороги, причиной которых являлась температура выше 38,0 градусов С, в дальнейшем можно делать все прививки. Если судороги были на фоне температуры менее 38,0 градусов С, то не вводят коклюшную вакцину, входящую в состав комплексной вакцины против коклюша, дифтерии, столбняка (АКДС). Остальные вакцины могут быть использованы. Всем детям, ранее имевшим судороги или предрасположенным к ним, после прививки назначают и жаропонижающие препараты, так как вакцины могут вызвать высокую температуру и снова провоцировать судороги.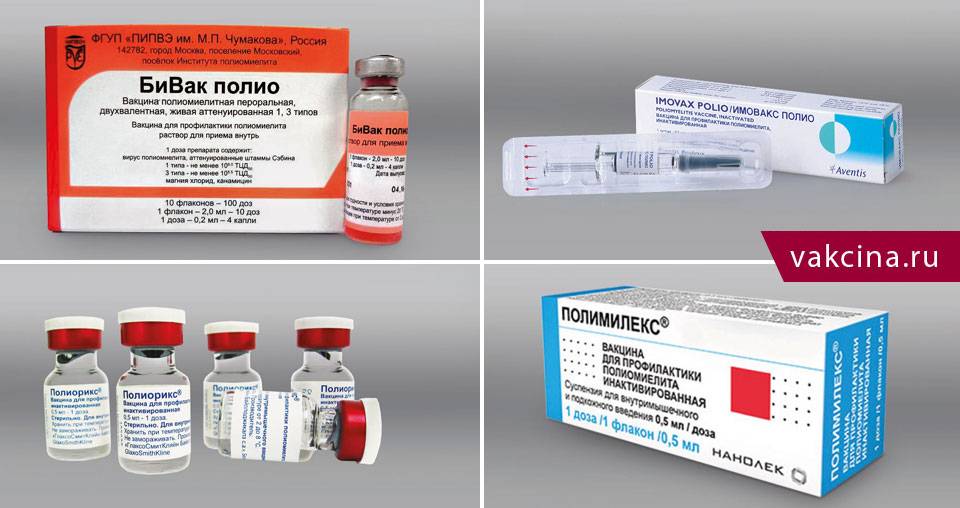 При наличии у ребенка эпилепсии, вакцинация также осуществляется не ранее, чем через 1 месяц после приступа, без коклюшной вакцины, на фоне противосудорожной терапии. При тяжелых формах эпилепсии вопрос о прививках решается индивидуально с врачом невропатологом. Дети с непрогрессирующими поражениями нервной системы (хромосомные, генетические заболевания, врожденные аномалии развития, детский церебральный паралич и т.п.), психическими заболеваниями вне острого периода, с умственной отсталостью и перенесшие воспалительные заболевания нервной системы не имеют противопоказаний к прививкам. Их вакцинируют с использованием симптоматической (применяемой при лечении конкретного заболевания) терапии или не назначают лекарств совсем.
При наличии у ребенка эпилепсии, вакцинация также осуществляется не ранее, чем через 1 месяц после приступа, без коклюшной вакцины, на фоне противосудорожной терапии. При тяжелых формах эпилепсии вопрос о прививках решается индивидуально с врачом невропатологом. Дети с непрогрессирующими поражениями нервной системы (хромосомные, генетические заболевания, врожденные аномалии развития, детский церебральный паралич и т.п.), психическими заболеваниями вне острого периода, с умственной отсталостью и перенесшие воспалительные заболевания нервной системы не имеют противопоказаний к прививкам. Их вакцинируют с использованием симптоматической (применяемой при лечении конкретного заболевания) терапии или не назначают лекарств совсем.
Возможные причины и меры по минимизации рисков развития абсцессов после прививки АКДС-вакциной | Терешкина
1. Таточенко ВК, Намазова ЛС, Харит СМ, Аликова ОА, Богидаев СВ. Реактогенность и безопасность адсорбированных вакцин против коклюша, дифтерии и столбняка: результаты наблюдательного многоцентрового исследования. Вопросы современной педиатрии. 2006;5(4):32–8.
Вопросы современной педиатрии. 2006;5(4):32–8.
2. Чупринина РП, Перелыгина ОВ, Алексеева ИА, Озерецковский НА. Сравнительная характеристика отечественных и зарубежных вакцин для профилактики коклюша, дифтерии и столбняка. БИОпрепараты. Профилактика, диагностика, лечение. 2006;4(24):27–30.
3. Харит СМ, Воронина ОЛ, Лакоткина ЕА, Черняева ТВ. Специфическая профилактика коклюша: проблемы и перспективы. Вопросы современной педиатрии. 2007;6(2):71–7.
4. Алексеева ИА, Чупринина РП, Борисова ВН. Сравнительный анализ безопасности и эффективности отечественных и зарубежных комплексных вакцин, содержащих цельноклеточную коклюшную вакцину. Эпидемиология и вакцинопрофилактика. 2012;(3):48–54.
5. Брико НИ, Лобзин ЮВ, Баранов АА, Намазова-Баранова ЛС, Ильина СВ, Королёва ИС и др. Оценка эффективности вакцинации: основные подходы и спорные вопросы. Педиатрическая фармакология. 2014;11(4):8–15.
6. Фельдблюм ИВ. Эпидемиологический надзор за вакцинопрофилактикой. Журнал МедиАль. 2014;3(13):37–55.
2014;3(13):37–55.
7. Чупринина РП, Алексеева ИА, Обухов ЮИ, Соловьев ЕА. Эффективность иммунопрофилактики коклюша комбинированными вакцинами, содержащими цельноклеточную или бесклеточную коклюшную вакцину. БИОпрепараты. Профилактика, диагностика, лечение. 2014;(4):4–13.
8. Пруцкова ЕВ, Черданцев АП, Андреева НП. Вакцины и вакцинация против коклюша детей и взрослых. Инфекционные болезни: новости, мнения, обучение. 2018;7(2):71–7. https://doi.org/10.24411/2305-3496-2018-12008
9. Алексеева ИА, Перелыгина ОВ, Никитюк НФ, Обухов ЮИ, Гаврилова НА, Колышкина ЕД, Тутукова ВИ. Заболеваемость коклюшем в России, ее причины и пути снижения. Медицинский альманах. 2019;(3–4):24–32.
10. Torch WC. Diphtheria — pertussis — tetanus (DPT) immunization: a potential cause of the sudden infant death syndrome (SIDS) (abstract). American Academy of Neurology, 34th Annual Meeting, April 25 — May 1, 1982. Neurology. 1982;32(4, part 2):A169–70.
11. Griffin MR, Ray WA, Livengood JR, Schaffner W. Risk of sudden infant death syndrome after immunization with the diphtheria-tetanus-pertussis vaccine. N Engl J Med. 1988;319(10):618– 23. https://doi.org/10.1056/NEJM198809083191006
Risk of sudden infant death syndrome after immunization with the diphtheria-tetanus-pertussis vaccine. N Engl J Med. 1988;319(10):618– 23. https://doi.org/10.1056/NEJM198809083191006
12. Griffin MR, Ray WA, Mortimer EA, Fenichel GM, Schaffner W. Risk of seizures and encephalopathy after immunization with the diphtheria-tetanus-pertussis vaccine. JAMA. 1990;263(12):1641–5. https://doi.org/10.1001/jama.1990.03440120063038
13. Ray P, Hayward J, Michelson D, Lewis E, Schwalbe J, Black S, et al. Encephalopathy after whole-cell pertussis or measles vaccination: lack of evidence for a causal association in a retrospective case-control study. Pediatr Infect Dis J. 2006;25(9):768–73. https://doi.org/10.1097/01.inf.0000234067.84848.e1
14. Таточенко ВК. Безопасность вакцинации: современные данные. Педиатрическая фармакология. 2007;4(3):73–9.
15. Харит СМ, Черняева ТВ, Лакоткина ЕА. Структура заболеваний поствакцинального периода (анализ наблюдений за 40 лет). Эпидемиология и вакцинопрофилактика. 2010;(2):64–9.
2010;(2):64–9.
16. Strathdee SA, Loughlin AM. Vaccines: past, present, and future. In: Infectious Disease Epidemiology. Gaithersburg, MD: Aspen Publishers, Inc.; 2001. P. 255–80.
17. Chen RT, Moro PL, Bauwens J, Bonhoeffer J. Obstetrical and neonatal case definitions for immunization safety data. Vaccine. 2016;34(49):5991–2. https://doi.org/10.1016/j.vaccine.2016.08.026
18. Яковлева ТВ. Вакцинопрофилактика: достижения и проблемы. Эпидемиология и вакцинопрофилактика. 2009;(6):36–9.
19. Мац АН. Врачам об антипрививочном движении и его вымыслах в СМИ. Педиатрическая фармакология. 2009;6(6):12–35.
20. Федосеенко МВ, Галицкая МГ, Ивардава МИ, Гайворонская АГ, Маянский НА, Ботвиньева ВВ, Родионова ТВ. Коклюш возвращается? Усовершенствование борьбы с забытой детской инфекцией. Педиатрическая фармакология. 2012;9(2):28–36. https://doi.org/10.15690/pf.v9i2.242
21. Белов АБ. Дифтерия: уроки прошлых эпидемий и перспективы контроля эпидемического процесса. Эпидемиология и вакцинопрофилактика. 2012;(5):12–9.
2012;(5):12–9.
22. Паньков АС, Денисюк НБ, Кайкова ОВ. Эволюция коклюшной инфекции: вопросы профилактики. Медицинский альманах. 2015;(5):129–32.
23. Костинов АМ, Костинов МП. Заболеваемость коклюшем и эффект от ревакцинации детей дошкольного и школьного возраста. Инфекция и иммунитет. 2018;8(3):284–94. https://doi.org/10.15789/2220-7619-2018-3-284-294
24. Галицкая МГ, Намазова ЛС, Федосеенко МВ, Гайворонская АГ, Алексина СГ. Реактогенность ацеллюлярной коклюшной вакцины и возможность ее использования у детей старшего возраста. Педиатрическая фармакология. 2008;5(1):14–9.
25. Чупринина РП, Озерецковский НА, Алексеева ИА. Иммунопрофилактика и заболеваемость коклюшем. Настоящее и будущее. Эпидемиология и вакцинопрофилактика. 2014;(6):89–99.
26. Антонова НА, Ерицян КЮ, Дубровский РГ, Спирина ВЛ. Отказ от вакцинации: качественный анализ биографических интервью. Теория и практика общественного развития. 2014;(20):208–11.
27. Байбусинова АЖ, Мусаханова АК, Шалгумбаева ГМ. Отношение, барьеры и проблемы вакцинопрофилактики в современном мире: обзор литературы. Наука и здравоохранение. 2016;(3):123–34.
Отношение, барьеры и проблемы вакцинопрофилактики в современном мире: обзор литературы. Наука и здравоохранение. 2016;(3):123–34.
28. Брико НИ, Намазова-Баранова ЛС, Лобзин ЮВ, Харит СМ, Начарова ЕП, Фельдблюм ИВ. Совершенствование мониторинга неблагоприятных событий поствакцинального периода (в порядке дискуссии). Эпидемиология и вакцинопрофилактика. 2016;15(6):95–101. https://doi.org/10.31631/2073-3046-2016-15-6-95-101
29. Николаева ИВ, Шайхиева ГС. Коклюш на современном этапе. Вестник современной клинической медицины. 2016;9(2):25–9. https://doi.org/10.20969/VSKM.2016.9(2).25-29
30. Степенко АВ, Миндлина АЯ. Управление рисками развития эпидемического процесса коклюша: упущенные возможности и новые перспективы. Медицинский альманах. 2017;(4):83–6.
31. Антонова НА, Ерицян КЮ. Систематический обзор эмпирических исследований факторов отказа от вакцинации. Гигиена и санитария. 2018;97(7):664–70. https://doi.org/10.18821/0016-9900-2018-97-7-664-670
32. Самодова ОВ, Кригер ЕА, Шишко ЛА. Вакцинопрофилактика коклюша: проблемы и возможности. Инфекционные болезни. 2019;17(4):18–21. https://doi.org/10.20953/1729-9225-2019-4-18-21
Вакцинопрофилактика коклюша: проблемы и возможности. Инфекционные болезни. 2019;17(4):18–21. https://doi.org/10.20953/1729-9225-2019-4-18-21
33. Начарова ЕП, Харит СМ, Лобзин ЮВ, Брико НИ. Принципы мониторинга неблагоприятных событий после вакцинации в России и в мире. Журнал микробиологии, эпидемиологии и иммунобиологии. 2017;(1):86–96. https://doi.org/10.36233/0372-9311-2017-1-86-96
34. Лопушов ДВ, Фазулзянова ИМ, Трифонов ВА. Организация и результаты мониторинга нежелательных поствакцинальных явлений в Республике Татарстан. Эпидемиология и вакцинопрофилактика. 2017;16(5):98–103. https://doi.org/10.31631/2073-3046-2017-16-5-98-103
35. Лопушов ДВ, Шайхразиева НД, Фазулзянова ИМ. Совершенствование мониторинга нежелательных явлений в поствакцинальном периоде в республике Татарстан. Журнал научных статей «Здоровье и образование в XXI веке». 2017;19(9):158–62.
36. Коновалова ЕП, Соколова МО, Сердюк СВ. Значение агрессивности фармакологических препаратов в развитии постинъекционных осложнений. В кн.: Молодежный научный форум: Естественные и медицинские науки: электронный сборник статей по материалам ХХХII студенческой международной заочной научно-практической конференции. 2016;3(31):40–7.
В кн.: Молодежный научный форум: Естественные и медицинские науки: электронный сборник статей по материалам ХХХII студенческой международной заочной научно-практической конференции. 2016;3(31):40–7.
37. Hervé C, Laupèze B, Del Giudice G, Didierlaurent AM, Da Silva FT. The how’s and what’s of vaccine reactogenicity. NPJ Vaccines. 2019;4:39. https://doi.org/10.1038/s41541-019-0132-6
38. Ураков АЛ, Уракова НА, Козлова ТС. Локальная токсичность лекарств как показатель их вероятной агрессивности при местном применении. Вестник Уральской медицинской академической науки. 2011;(1):105–8.
39. Стрелков НС, Уракова НА. Фармацевтическая агрессия лекарств при инъекциях. Медицинский вестник Башкортостана. 2013;8(3):96–100.
40. Авдеева ЖИ, Алпатова НА, Бондарев ВП, Волкова РА, Лонская НИ, Лебединская ЕВ и др. Вакцины с адъювантами. Доклинические исследования. БИОпрепараты. Профилактика, диагностика, лечение. 2015;(1):15–20.
41. Ураков АЛ, Уракова НА, Альес МЮ, Никитюк ДБ, Гуревич КГ, Ловцова ЛВ и др. Физико-химическая активность растворов как составная часть механизма местного действия лекарств. Фармация. 2019;68(6):42–9. https://doi.org/10.29296/25419218-2019-06-08
Физико-химическая активность растворов как составная часть механизма местного действия лекарств. Фармация. 2019;68(6):42–9. https://doi.org/10.29296/25419218-2019-06-08
42. Vargas KM, Koil A, Dehority W. Recurrent sterile abscesses after immunization with aluminum-adjuvant based vaccines. Clin Pediatr (Phila). 2018;57(6):733–7. https://doi.org/10.1177/0009922817728702
43. Klein NP, Edwards KM, Sparks RC, Dekker CL, Clinical Immunization Safety Assessment (CISA) Network. Recurrent sterile abscesses following aluminium adjuvant-containing vaccines. BMJ Case Rep. 2009;2009:bcr09.2008.0951. https://doi.org/10.1136/bcr.09.2008.0951
44. Keith LS, Jones DE, Chou CH. Aluminum toxicokinetics regarding infant diet and vaccinations. Vaccine. 2002;20 Suppl 3:S13–7. https://doi.org/10.1016/s0264-410x(02)00165-2
45. Caubet JC, Ponvert C. Vaccine allergy. Immunol Allergy Clin North Am. 2014;34(3):597–613. https://doi.org/10.1016/j.iac.2014.04.004
46. Lauren CT, Belsito DV, Morel KD, LaRussa P. Case report of subcutaneous nodules and sterile abscesses due to delayed type hypersensitivity to aluminum-containing vaccines. Pediatrics. 2016;138(4):e20141690. https://doi.org/10.1542/peds.2014-1690
Case report of subcutaneous nodules and sterile abscesses due to delayed type hypersensitivity to aluminum-containing vaccines. Pediatrics. 2016;138(4):e20141690. https://doi.org/10.1542/peds.2014-1690
47. McFarland G, La Joie E, Thomas P, Lyons-Weiler J. Acute exposure and chronic retention of aluminum in three vaccine schedules and effects of genetic and environmental variation. J Trace Elem Med Biol. 2020;58:126444. https://doi.org/10.1016/j.jtemb.2019.126444
48. Igbokwe IO, Igwenagu E, Igbokwe NA. Aluminium toxicosis: a review of toxic actions and effects. Interdiscip Toxicol. 2019;12(2):45–70. https://doi.org/10.2478/intox-2019-0007
49. Lyons-Weiler J, Ricketson R. Reconsideration of the immunotherapeutic pediatric safe dose levels of aluminum. J Trace Elem Med Biol. 2018;48:67–73. https://doi.org/10.1016/j.jtemb.2018.02.025
50. Lehman HK, Faden HS, Fang YV, Ballow M. A case of recurrent sterile abscesses following vaccination: delayed hypersensitivity to aluminum. J Pediatr. 2008;152(1):133–5. https://doi.org/10.1016/j.jpeds.2007.08.039
J Pediatr. 2008;152(1):133–5. https://doi.org/10.1016/j.jpeds.2007.08.039
51. Tan NWH, Pan WJ, Yunos HHBM, Tan WC, Lim KBL. Post-vaccination abscesses requiring surgical drainage in a tertiary children’s hospital in Singapore. J Pediatr Infect Dis. 2010;5(2):139–47. https://doi.org/10.3233/JPI-2010-0239
52. Lauren CT, Belsito DV, Morel KD, LaRussa P. Case report of subcutaneous nodules and sterile abscesses due to delayed type hypersensitivity to aluminum-containing vaccines. Pediatrics. 2016;138(4):e20141690. https://doi.org/10.1542/peds.2014-1690
53. Bergfors E, Trollfors B, Inerot A, Gente Lidholm A. Contact allergy to aluminium induced by commonly used pediatric vaccines. Clin Transl Med. 2017;6(1):4. https://doi.org/10.1186/s40169-016-0129-y
54. Антипов ОН, Михеева ИВ, Мельникова АА, Чекалина КИ. Проблемы организации непрерывного контроля температурного режима при хранении и транспортировании вакцин. Эпидемиология и вакцинопрофилактика. 2009;(4):70–3.
55. Акимкин ВГ, Чернова ОЭ. Гнойно-воспалительные постинъекционные осложнения, связанные с введением медицинских иммунобиологических препаратов. В кн.: Актуальные вопросы инфекционной патологии у детей (диагностика и лечение). Четверный конгресс педиаторов-инфекционистов России. Москва, 14–16 декабря 2005 года. Специальная литература; 2005. C. 192–3.
Акимкин ВГ, Чернова ОЭ. Гнойно-воспалительные постинъекционные осложнения, связанные с введением медицинских иммунобиологических препаратов. В кн.: Актуальные вопросы инфекционной патологии у детей (диагностика и лечение). Четверный конгресс педиаторов-инфекционистов России. Москва, 14–16 декабря 2005 года. Специальная литература; 2005. C. 192–3.
56. Мовсесянц АА. Безопасность иммунизации: риски, связанные с вакциной. БИОпрепараты. Профилактика, диагностика, лечение. 2009;19(5):33–6.
57. Гилмуллина ФС, Загидуллина АИ, Гайфуллина ГР, Родыгина ЖА. Организация прививочного дела: потенциальные риски. Практическая медицина. 2019;17(8):8–10. https://doi.org/10.32000/2072-1757-2019-8-8-10
58. Алексеева ИА, Перелыгина ОВ, Колышкина ЕД. Оценка стабильности производства коклюшного компонента АКДС-вакцины по показателям иммуногенной активности и специфической безопасности с использованием карт Шухарта. БИОпрепараты. Профилактика, диагностика, лечение. 2018;18(4):243–8. https://doi. org/10.30895/2221-996X-2018-18-4-243-248
org/10.30895/2221-996X-2018-18-4-243-248
59. Перелыгина ОВ, Алексеева ИА. Безопасность комбинированных вакцин с цельноклеточным коклюшным компонентом. Эпидемиология и вакцинопрофилактика. 2016;15(6):62–9. https://doi.org/10.31631/2073-3046-2016-15-6-62-69
60. Kohl KS, Walop W, Gidudu J, Ball L, Halperin S, Hammer SJ, et al. Induration at or near injection site: case definition and guidelines for collection, analysis, and presentation of immunization safety data. Vaccine. 2007;25(31):5839–57. https://doi.org/10.1016/j.vaccine.2007.04.062
61. Чернова ОЭ, Жукова ЭВ, Мартьянова НМ. Постинъекционные осложнения. Микробиологический пейзаж. Эпидемиология и вакцинопрофилактика. 2005;(6):44–8.
62. Ураков АЛ, Стрелков НС, Уракова НА, Бендерская ЕЮ. Физико-химические и биофизические факторы постинъекционной агрессивности растворов лекарственных средств в инфильтрированных тканях и способы предотвращения некрозов. Патологическая физиология и экспериментальная терапия. 2010;(1):20–4.
63. Козлова ТС, Кононова СА. Локальные постинъекционные осложнения: причины возникновения, их тепловизорная оценка. Проблемы экспертизы в медицине. 2013;13(4):21–5.
64. Витер ВИ, Козлова ТС, Поздеев АР. Ранняя диагностика постинъекционных осложнений после внутримышечных введений лекарственных препаратов. Проблемы экспертизы в медицине. 2012;12(3–4):29–31.
65. Poland GA, Borrud A, Jacobson RM, McDermott K, Wollan PC, Brakke D, Charboneau JW. Determination of deltoid fat pad thickness. Implications for needle length in adult immunization. JAMA. 1997;277(21):1709–11.
66. Рами А. Анатомические вариации седалищного нерва. Актуальные проблемы медицины и биологии. 2018;3(3):16–9.
67. Харит СМ, Лакоткина ЕА, Черняева ТВ, Воронина ОЛ, Начарова ЕП. Дифференциальный диагноз поствакцинальных осложнений. Трудный пациент. 2006;4(2-1):17–22.
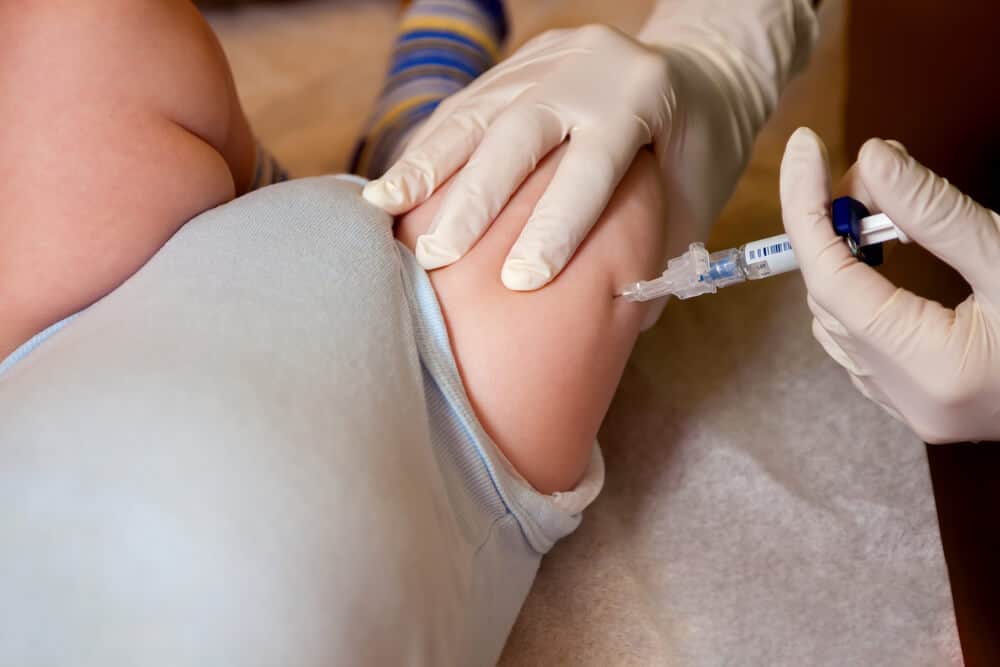
Характер и частота побочных реакций, связанных с иммунизацией АКДС и АКДС у младенцев и детей
Клинические испытания
. 1981 ноябрь; 68 (5): 650-60.
1981 ноябрь; 68 (5): 650-60.
К. Л. Коди, Л. Дж. Барафф, Дж. Д. Черри, С. М. Марси, С. Р. Манкларк
- PMID: 7031583
Клинические испытания
C L Cody et al. Педиатрия. 1981 ноября
. 1981 ноябрь; 68 (5): 650-60.
Авторы
К. Л. Коди, Л. Дж. Барафф, Дж. Д. Черри, С. М. Марси, С. Р. Манкларк
- PMID: 7031583
Абстрактный
 Соотношение скоростей реакций, связанных с иммунизацией DTP и DT (АКДС/ДТ) для выбранных местных и системных реакций, было следующим: локальное покраснение 37,4%/7,6%; местный отек, 40,7%/7,6%; боль, 50,9%/9,9%; лихорадка, 31,5%/14,9%; сонливость 31,5%/14,9%; раздражительность — 53,4%/22,6%; рвота, 6,2%/2,6%; анорексия, 20,9%/7,0% и постоянный плач, 3,1%/0,7%. После иммунизации АКДС у девяти детей развились судороги, а у девяти развились гипотонические гипореактивные эпизоды. Никаких последствий после этих реакций обнаружено не было.
Соотношение скоростей реакций, связанных с иммунизацией DTP и DT (АКДС/ДТ) для выбранных местных и системных реакций, было следующим: локальное покраснение 37,4%/7,6%; местный отек, 40,7%/7,6%; боль, 50,9%/9,9%; лихорадка, 31,5%/14,9%; сонливость 31,5%/14,9%; раздражительность — 53,4%/22,6%; рвота, 6,2%/2,6%; анорексия, 20,9%/7,0% и постоянный плач, 3,1%/0,7%. После иммунизации АКДС у девяти детей развились судороги, а у девяти развились гипотонические гипореактивные эпизоды. Никаких последствий после этих реакций обнаружено не было.Похожие статьи
Реакции на вакцину АКДС: влияние предшествующих реакций на частоту последующих реакций.
Барафф Л.Дж., Черри Д.Д., Коди К.Л., Марси С.М., Манкларк К.Р. Барафф Л.Дж. и соавт. Стенд Дев Биол. 1985;61:423-8. Стенд Дев Биол. 1985. PMID: 3879687
Младенцы и дети с судорогами и эпизодами гипотонии-гипореактивности после иммунизации против дифтерии-столбняка-коклюша: последующая оценка.
Барафф Л.Дж., Шилдс В.Д., Беквит Л., Строум Г., Марси С.М., Черри Д.Д., Манкларк К.Р. Барафф Л.Дж. и соавт. Педиатрия. 1988 июня; 81 (6): 789-94. Педиатрия. 1988 год. PMID: 3259305
Незначительные нежелательные явления в сравнительном испытании эффективности в Германии у детей грудного возраста, получавших бесклеточную вакцину против коклюша АКДС (АКДС) Ледерле/Такеда, цельноклеточную компонентную вакцину АКДС (АКДС) Ледерле или вакцину АКДС Ледерле. Группа по изучению коклюшной вакцины.
Шмитт-Гроэ С., Штер К., Черри Д.Д., Хайнингер У., Убералл М.А., Лауссук С., Экхардт Т. Шмитт-Гроэ С. и др. Стенд Дев Биол. 1997;89:113-8. Стенд Дев Биол. 1997. PMID: 9272341 Клиническое испытание.
Иммунологические основы введения АКДС-полиовакцины.
Коэн Х. Коэн Х. Верх К Академ Генескд Белг. 2000;62(4):245-67. Верх К Академ Генескд Белг. 2000. PMID: 11004905 Обзор. Голландский.
Ацетаминофен и ибупрофен для предотвращения побочных реакций, связанных с иммунизацией детей.
Мэнли Дж., Таддио А. Мэнли Дж. и др. Энн Фармакотер. 2007 г., июль; 41 (7): 1227-32. doi: 10.1345/аф.1Н647. Epub 2007 22 мая. Энн Фармакотер. 2007. PMID: 17519301 Обзор.
Посмотреть все похожие статьи
Цитируется
Неврологические последствия вакцин.
McAlpine LS, Zubair AS. McAlpine LS и др. Неврология наук. 2023 янв.
 9:1-9. doi: 10.1007/s10072-022-06581-z. Онлайн перед печатью.
Неврология наук. 2023.
PMID: 36622478
Бесплатная статья ЧВК.
Обзор.
9:1-9. doi: 10.1007/s10072-022-06581-z. Онлайн перед печатью.
Неврология наук. 2023.
PMID: 36622478
Бесплатная статья ЧВК.
Обзор.Условный дефект роста мутантов Bordetella pertussis и Bordetella bronchiseptica, регулирующих поглощение железа (мех).
де Йонге Э.Ф., Томмассен Дж. де Йонге Э.Ф. и др. FEMS Microbiol Lett. 2022 1 июля; 369 (1): fnac047. doi: 10.1093/femsle/fnac047. FEMS Microbiol Lett. 2022. PMID: 35700015 Бесплатная статья ЧВК.
Тепловой шок усиливает высвобождение пузырьков внешней мембраны у Bordetella spp.
де Йонге Э.Ф., Балхуйзен М.Д., ван Бокстель Р., Ву Дж., Хаагсман Х.П., Томмассен Дж. де Йонге Э.Ф. и др. Curr Res Microb Sci.
Пертактин способствует выделению и передаче Bordetella bronchiseptica.
Ма Л., Деван К.К., Тейлор-Малнейкс Д.Л., Вагнер С.М., Линц Б., Ривера И., Су Ю., Колфилд А.Д., Блас-Мачадо У., Харвилл И.Т. Ма Л и др. PLoS Патог. 2021 4 августа; 17 (8): e1009735. doi: 10.1371/journal.ppat.1009735. Электронная коллекция 2021 авг. PLoS Патог. 2021. PMID: 34347835 Бесплатная статья ЧВК.
Коклюшные вакцины следующего поколения, основанные на индукции защитных Т-клеток в дыхательных путях.
Chasaide CN, Mills KHG. Chasaide CN и соавт.

