Ответы на часто задаваемые вопросы о прививке от гриппа
Может ли прививка от гриппа не сработать?
Есть мнение, что вакцина бесполезна: человек прививался, потом заболел, врачи диагностировали грипп. Что не так? Дело в том, что многие вирусные заболевания дают одну и ту же симптоматику. Если вы не сдавали анализы крови на выявление конкретного заболевания, то это может быть не оно.
Остается вероятность, что прививка не распространяется на подтип гриппа, которым инфицирован пациент. Но даже в этом случае она может ослабить действие вируса, и человек переболеет с наименьшими последствиями для здоровья.
Что можно и нельзя делать после прививки?
Вакцина не может заразить человека гриппом, но у некоторых могут возникнуть реакции, схожие по симптомам. Иногда пациенты испытывают мышечную слабость и фиксируют небольшое повышение температуры в течение пары дней после прививки; это является побочным эффектом в выработке антител и абсолютно нормально. Чтобы вакцина подействовала, должны пройти две недели, так что в этот период вы все еще рискуете заразиться.
Чтобы вакцина подействовала, должны пройти две недели, так что в этот период вы все еще рискуете заразиться.
Непосредственно после прививки не спешите покидать поликлинику. Можно посидеть в приемной и понаблюдать за ощущениями. 10–15 минут достаточно, чтобы исключить редкие аллергические реакции, требующие незамедлительной помощи.
В течение суток после прививки старайтесь не мочить место укола. Его нельзя чесать, в противном случае появится риск занести инфекцию. Придерживайтесь здорового питания, откажитесь хотя бы на первые сутки от жирной и острой пищи. В это время организм бросает все силы на выработку антител, поэтому иммунитет немного ослаблен. Лучше, если вечер после прививки вы проведете дома, избегая многолюдных мест и физических нагрузок.
Противопоказания к прививке от гриппа
Факторы, которые могут стать препятствием для вакцинации, включают в себя возраст человека, состояние здоровья, аллергические реакции и хронические заболевания. Прежде чем делать прививку, стоит обсудить с лечащим врачом возможные последствия. Например, медики уделяют особое внимание людям с аллергией на яйца. Этих пациентов должны вакцинировать в медучреждениях под присмотром врачей. Другие виды аллергии на ингредиенты вакцины, например, антибиотики и желатин, также являются противопоказанием для прививки.
Например, медики уделяют особое внимание людям с аллергией на яйца. Этих пациентов должны вакцинировать в медучреждениях под присмотром врачей. Другие виды аллергии на ингредиенты вакцины, например, антибиотики и желатин, также являются противопоказанием для прививки.
Детям младше полугода не делают прививку от гриппа. Кроме того, явным противопоказанием является синдром Гийена-Барре в анамнезе пациента (парализующее заболевание, также называемое СГБ). Беременным можно делать прививку, но интраназальная вакцина противопоказана.
Важно обсудить с врачом свое самочувствие и особенности здоровья. В период острых инфекционных заболеваний прививку не делают; это возможно только на фоне ремиссии хронических процессов и после выздоровления.
Стоит ли делать прививку от гриппа?
По данным ВОЗ, последствиям вирусов наиболее подвержены люди с хроническими заболеваниями и старше 65 лет, маленькие дети и беременные женщины. Даже у здоровых людей грипп может повлечь легочные осложнения – пневмонию или бронхит, а также сердечно-сосудистые проблемы и сбои в работе нервной системы. Многие переносят болезнь без тяжелых последствий, но само ее течение выбивает из привычного ритма жизни на пару недель, за которыми следует не меньший период восстановления.
Многие переносят болезнь без тяжелых последствий, но само ее течение выбивает из привычного ритма жизни на пару недель, за которыми следует не меньший период восстановления.
В среднем вакцина предотвращает порядка 60% случаев инфицирования у здоровых взрослых людей в возрасте 18–64 лет. К тому же грипп очень заразная болезнь, и чем больше людей будут ее переносчиками, тем больше окружающих подвергнется опасности. Многих пугают побочные эффекты от прививки, но они незначительны по сравнению с рисками самого гриппа.
В группе риска дети, посещающие детские сады и школы, и пожилые люди (старше 65 лет). Врачи рекомендуют им прививаться в обязательном порядке. Беременным женщинам тоже нужна прививка, ее можно делать начиная со второго триместра (после 14-й недели). Люди, пользующиеся общественным транспортом, тоже имеют высокие шансы заразиться. В группе риска курящие люди, а также страдающие хроническими заболеваниями легких и сердца.
Вакцина — самый простой способ профилактики гриппа, и его лучше сочетать с другими превентивными мерами: здоровым образом жизни, отказом от вредных привычек, правильным питанием и подходящими спортивными нагрузками.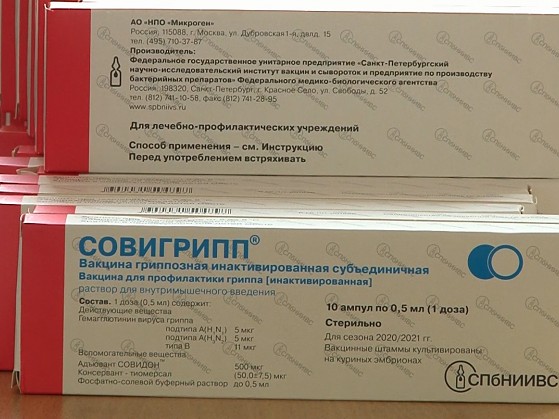 Врачи разрабатывают прививку с учетом возраста пациентов, поэтому существуют варианты для взрослых, пожилых людей и для детей от 6 месяцев. Есть также вакцина в виде назального спрея, подходящая пациентам 2–49 лет, для которой есть противопоказания по состоянию здоровья.
Врачи разрабатывают прививку с учетом возраста пациентов, поэтому существуют варианты для взрослых, пожилых людей и для детей от 6 месяцев. Есть также вакцина в виде назального спрея, подходящая пациентам 2–49 лет, для которой есть противопоказания по состоянию здоровья.
где сделать, сколько действует, какие существуют в 2023 году
Многие люди сегодня не считают грипп опасным заболеванием, поскольку против него разработана вакцина, а в аптеках продается масса препаратов, обещающих «устранение симптомов простуды и гриппа» буквально за пару дней. Но печальный опыт прошлых столетий, например, известная всем пандемия «испанки» напоминает – это коварная, опасная инфекция. А эффективных лекарств, которые бы активно подавляли вирус, очень мало1.
И по сей день грипп опасен своими осложнениями. Один из самых эффективных способов защититься от болезни – вовремя сделать прививку.
Прививка против гриппа в нашей стране входит в Национальный календарь профилактических прививок2. Ежегодно вакцинируются все желающие, но есть определенные категории, кому данная прививка обязательна. Это работники медицинских и образовательных учреждений, транспорта, коммунальной сферы.
Ежегодно вакцинируются все желающие, но есть определенные категории, кому данная прививка обязательна. Это работники медицинских и образовательных учреждений, транспорта, коммунальной сферы.
Где сделать прививку от гриппа в России
Вакцинация проходит в поликлиниках и частных медицинских учреждениях. Инъекция вакцины осуществляется внутримышечно в плечо.
Обычно вакцины российского производства предоставляются бесплатно (при вакцинации в муниципальных поликлиниках, по полису ОМС), при желании сделать зарубежную – может потребоваться доплата. К процедуре не нужно готовиться – главное, чтобы не было признаков других заболеваний, даже простуды3.
В России вакцинируется довольно мало людей, до 37% населения. В других странах ситуация несколько иная, например в США прививку против гриппа делает минимум половина жителей.
Сколько действует прививка от гриппа
Иммунитет после прививки против гриппа недолог. Обычно его хватает только на один сезон – в следующем прививка уже не защитит от гриппа. Только в 20 — 40% случаев проведенная в прошлом сезоне прививка против гриппа поможет. Это связано с высокой изменчивостью вируса в природе, он постоянно мутирует. Поэтому проводится ежегодная вакцинная, при этом используются только новые прививки текущего сезона4.
Обычно его хватает только на один сезон – в следующем прививка уже не защитит от гриппа. Только в 20 — 40% случаев проведенная в прошлом сезоне прививка против гриппа поможет. Это связано с высокой изменчивостью вируса в природе, он постоянно мутирует. Поэтому проводится ежегодная вакцинная, при этом используются только новые прививки текущего сезона4.
Какие существуют прививки от гриппа в России
Первые вакцины делали из обезвреженных вирусов, а некоторые были и «живыми». Практически все современные прививки против гриппа относятся к вакцинам из «убитых» вирусов. Вирусы гриппа выращиваются на куриных эмбрионах, и это основная причина возможных аллергий – из-за следов куриного белка в составе.
В России сложилась практически традиция не доверять отечественным лекарствам, часто считают, что зарубежная прививка лучше. Но число вакцинированных именно отечественными вакцинами растет год от года, при этом заболеваемость гриппом падает. Это говорит о высокой эффективности отечественных вакцин, которые ничем не отличаются от зарубежных.
Это говорит о высокой эффективности отечественных вакцин, которые ничем не отличаются от зарубежных.
В весенне-осенний сезон в медицинские учреждения поступают вакцины от российских и зарубежных фармацевтических компаний. В России в основном используются препараты: Совигрипп, Ультрикс, Флю-М, Ультрикс кварди, Ваксигрип, Гриппол, Гриппол плюс, Инфлювак. Всего таких вакцин зарегистрировано около двух десятков.
Есть данные о том, что некоторые зарубежные вакцины против гриппа в этом сезоне в Россию поступать не будут (это Ваксигрип / Инфлювак).
Состав прививок меняется каждый год. Это делается для максимальной защиты от изменившегося за год вируса гриппа. Всемирная организация здравоохранения прогнозирует, какой именно штамм вируса гриппа ожидается в этом сезоне. Новые прививки производятся, основываясь на этих данных, поэтому каждый год могут быть разными5.
Популярные вопросы и ответы
Обо всех тонкостях производства вакцин и их безопасности расскажет врач-терапевт, врач-гастроэнтеролог Марина Малыгина.
Кому нельзя делать прививку от гриппа?
Нельзя делать прививку против гриппа, если человек имеет злокачественные заболевания крови и новообразования, а также страдает аллергией на куриный белок (нельзя вводить только те вакцины, которые сделаны с использованием куриного белка и содержат его частицы). Не прививают пациентов тогда, когда у них обостряется бронхиальная астма и атопический дерматит, а во время ремиссии этих болезней прививаться против гриппа можно. Не делают прививку, если у подлежащего вакцинации человека повышена температура тела и есть признаки ОРВИ. Проведение прививки откладывается на 3 недели, если человек перенес острое заболевание. Противопоказана прививка людям, у которых предыдущая прививка от гриппа вызвала острую аллергическую реакцию.
Нужно ли делать прививку от гриппа, если уже переболел?
Вирус гриппа ежегодно мутирует, поэтому антитела, вырабатываемые в организме, не смогут в полной мере защитить от нового варианта штамма гриппа. Если человек переболел в прошлом сезоне, то это не защитит его от вируса в этом сезоне. Это относится и к тем людям, которые сделали прививку от гриппа в прошлом году. На основании этих данных, можно с уверенностью сказать, что прививку против гриппа делать надо, даже если уже переболел.
Если человек переболел в прошлом сезоне, то это не защитит его от вируса в этом сезоне. Это относится и к тем людям, которые сделали прививку от гриппа в прошлом году. На основании этих данных, можно с уверенностью сказать, что прививку против гриппа делать надо, даже если уже переболел.
Можно ли делать прививку от гриппа беременным?
Беременные женщины имеют повышенный риск заражения гриппом. Это связано с изменениями в работе их кровеносной, иммунной и дыхательной систем. Одновременно увеличивается тяжесть течения, что приводит к учащению случаев госпитализации. Исследования доказали безопасность вакцины против гриппа для этой категории лиц. Антитела, образовавшиеся в организме после вакцинации, могут передаваться ребенку через грудное молоко, снижая для него риск заболеть. Беременным во 2 и 3 триместре беременности, а также при кормлении грудью можно проводить вакцинацию против гриппа.
Можно ли мочить место прививки против гриппа?
После проведения прививки против гриппа можно принимать душ, при этом место введения инъекции нельзя растирать губкой, потому что может появиться гематома.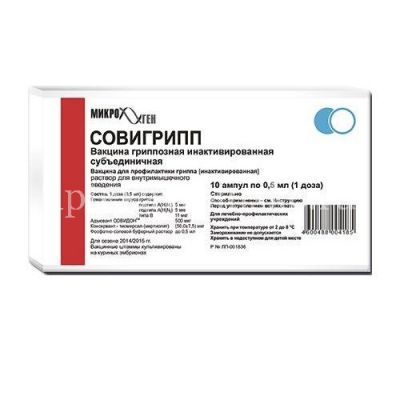 Вакцина делается внутримышечно, поэтому незначительно повреждается только кожа и это никак не отражается на действии прививки.
Вакцина делается внутримышечно, поэтому незначительно повреждается только кожа и это никак не отражается на действии прививки.
Можно ли пить алкоголь после прививки против гриппа?
Нет, любая нагрузка на печень запрещена. Употреблять спиртное после прививки не рекомендуется, потому что химические вещества в составе алкоголя могут препятствовать формированию хорошего иммунитета и повышать риск развития аллергии.
Когда можно сделать прививку против гриппа после прививки от коронавируса?
Сделать прививку против гриппа можно через один месяц после прививки вторым компонентом вакцины против COVID-19. Оптимальный срок вакцинации – сентябрь-ноябрь.
Какие могут быть осложнения после прививки от гриппа?
У вакцин самое большое соотношение пользы и риска по сравнению с другими лекарственными препаратами. Последствия от вызванных инфекциями заболеваний намного серьезнее возможных нежелательных реакций после прививки.
Благодаря новым технологиям побочных реакций у вакцины против гриппа становится все меньше. Например, в конце 70-х в процессе производства вакцины вирус убивали, чуть-чуть «чистили» и на его основе создавали так называемую цельновирионную вакцину. Сегодня же ученые понимают, что целый вирус уже не нужен, достаточно нескольких белков, на которые в организме формируется иммунный ответ. Поэтому сначала вирус разрушают и удаляют все лишнее, оставляя только необходимые белки, вызывающие формирование иммунитета против гриппа. Организм при этом воспринимает их как настоящий вирус. Так получается субъединичная вакцина четвертого поколения. Такую вакцину можно применять даже у тех, кто имеет аллергию, в том числе на куриный белок. Технология доведена до такого уровня, что содержание куриного белка в вакцине практически невозможно обнаружить.
Например, в конце 70-х в процессе производства вакцины вирус убивали, чуть-чуть «чистили» и на его основе создавали так называемую цельновирионную вакцину. Сегодня же ученые понимают, что целый вирус уже не нужен, достаточно нескольких белков, на которые в организме формируется иммунный ответ. Поэтому сначала вирус разрушают и удаляют все лишнее, оставляя только необходимые белки, вызывающие формирование иммунитета против гриппа. Организм при этом воспринимает их как настоящий вирус. Так получается субъединичная вакцина четвертого поколения. Такую вакцину можно применять даже у тех, кто имеет аллергию, в том числе на куриный белок. Технология доведена до такого уровня, что содержание куриного белка в вакцине практически невозможно обнаружить.
На прививку может быть небольшая местная реакция, покраснение, иногда немного повышается температура, появляется головная боль. Но даже такая реакция бывает нечасто – около 3% от всех привитых.
Как понять, что вакцина безопасна?
Как и на любой лекарственный препарат, на вакцину могут возникать индивидуальные реакции. При этом современные иммунобиологические препараты являются высокотехнологичными продуктами, которые проходят длительные испытания (от 2 до 10 лет) на эффективность и безопасность применения. Поэтому небезопасных вакцин, вышедших на рынок, не бывает.
При этом современные иммунобиологические препараты являются высокотехнологичными продуктами, которые проходят длительные испытания (от 2 до 10 лет) на эффективность и безопасность применения. Поэтому небезопасных вакцин, вышедших на рынок, не бывает.
Даже после того, как вакцина получает разрешение к использованию для иммунизации людей, контролирующие органы здравоохранения продолжают следить за ее качеством и безопасностью. Профильные институты Минздрава России регулярно осуществляют контроль над показателями выпускаемых вакцин.
Во время всего цикла производства вакцины проводится порядка 400 контролей сырья, сред, качества полупродуктов и готовой продукции. На каждом предприятии существует своя контрольная лаборатория, которая отделена от производства и действует независимо.
Производители и поставщики также следят за строгим соблюдением правил хранения и транспортировки вакцин, то есть за обеспечением условий так называемой «холодовой цепи».
Можно ли прийти на вакцинацию со своей вакциной?
Именно из-за того, что в безопасности вакцины можно быть уверенным только в случае соблюдения всех правил транспортировки и т.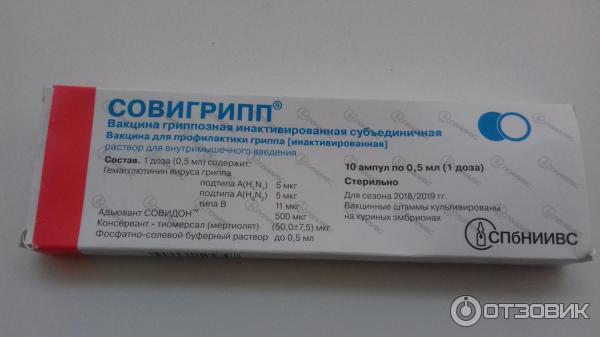 д., не стоит покупать и приносить свою вакцину. Ее качество может пострадать. Намного надежнее то, что правильно хранится в медицинском учреждении. Большинство из них отказываются вводить принесенную вакцину именно по этой причине.
д., не стоит покупать и приносить свою вакцину. Ее качество может пострадать. Намного надежнее то, что правильно хранится в медицинском учреждении. Большинство из них отказываются вводить принесенную вакцину именно по этой причине.
Как быстро начинает действовать вакцина?
«Защита» от гриппа вырабатывается не сразу после прививки. Сначала иммунная система распознает компоненты вакцины, это занимает около двух недель. Пока вырабатывается иммунитет, нужно по-прежнему избегать инфицированных людей, чтобы не заразиться гриппом до того, как вакцина подействует.
Источники
:- Орлова Н.В. Грипп. Диагностика, стратегия выбора противовирусных препаратов // МС. 2017. №20. https://cyberleninka.ru/article/n/gripp-diagnostika-strategiya-vybora-protivovirusnyh-preparatov
- Приложение N 1. Национальный календарь профилактических прививок (Приложение 1 изменено с 23 октября 2020 г. — Приказ Минздрава России от 14 сентября 2020 г. N 967Н) https://base.
 garant.ru/70647158/53f89421bbdaf741eb2d1ecc4ddb4c33/#friends
garant.ru/70647158/53f89421bbdaf741eb2d1ecc4ddb4c33/#friends - Информация Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека от 20 сентября 2021 г. «О гриппе и мерах его профилактики» https://www.garant.ru/products/ipo/prime/doc/402715964/
- Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека. О вакцинации против гриппа в вопросах и ответах. https://www.rospotrebnadzor.ru/about/info/news/news_details.php?ELEMENT_ID=15586
- Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека. Рекомендации Роспотребнадзора населению по вакцинации https://www.rospotrebnadzor.ru/region/zika/recomendation.php
Изменения протеома мочи до и после четырехвалентной вакцины против гриппа и вакцины против COVID-19
1. Гао Ю. Моча — неиспользованная золотая жила для открытия биомаркеров? Sci China Life Sci (2013) 56: 1145–6. doi: 10.1007/s11427-013-4574-1 [PubMed] [CrossRef] [Google Scholar]
2. Родригес-Суарес Э., Сиви Дж., Зурбиг П., Мишак Х. Моча как источник для клинического анализа протеома: от открытия до клинического применения. Biochim Biophys Acta (2014) 1844: 884–98. doi: 10.1016/j.bbapap.2013.06.016
[PubMed] [CrossRef] [Академия Google]
Родригес-Суарес Э., Сиви Дж., Зурбиг П., Мишак Х. Моча как источник для клинического анализа протеома: от открытия до клинического применения. Biochim Biophys Acta (2014) 1844: 884–98. doi: 10.1016/j.bbapap.2013.06.016
[PubMed] [CrossRef] [Академия Google]
3. Xiao X, Zou L, Sun W. «Протеом мочи человека: мощный источник для клинических исследований», In: Gao Y, редактор. Моча. Сингапур: Springer Сингапур; (2019). п. 9–24. [Google Scholar]
4. Чен З., Лю Дж., Лин Л., Се Х., Чжан В., Чжан Х. и др.. Анализ дифференциально экспрессированного протеома в моче пациентов с немелкоклеточным раком легкого. Чжунго Фей Ай За Чжи (2015) 18: 138–45. doi: 10.3779/j.issn.1009-3419.2015.03.03 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
5. Wang W, Wang S, Zhang M. Идентификация биомаркеров мочи, связанных с аденокарциномой легких. Онкотаргет (2017) 8:38517–29. doi: 10.18632/oncotarget.15870 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
6. Zhang C, Leng W, Sun C, Lu T, Chen Z, Men X и др. Профилирование протеома мочи предсказывает рак легких при контрольных случаях и других опухолях. EBioMedicine (2018) 30:120–8. doi: 10.1016/j.ebiom.2018.03.009
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Zhang C, Leng W, Sun C, Lu T, Chen Z, Men X и др. Профилирование протеома мочи предсказывает рак легких при контрольных случаях и других опухолях. EBioMedicine (2018) 30:120–8. doi: 10.1016/j.ebiom.2018.03.009
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
7. Zhang H, Cao J, Li L, Liu Y, Zhao H, Li N и др.. Идентификация биомаркеров белков мочи с возможностью раннего выявления рака легких. Научный представитель (2015) 5:11805. дои: 10.1038/srep11805 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
8. Беретов Дж., Васингер В.К., Миллар Э.К., Шварц П., Грэм П.Х., Ли Ю. Протеомный анализ мочи для выявления кандидатов в биомаркеры рака молочной железы с использованием безметочного метода ЖХ-МС/МС. PloS One (2015) 10:e0141876. doi: 10.1371/journal.pone.0141876 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
9.
Гаджбхие А., Дабхи Р., Таунк К., Ваннурусвами Г., РойЧоудхури С., Адхав Р. и др.. Изменения протеома мочи при раке молочной железы, обогащенном HER2, выявленные с помощью многоаспектной количественной протеомики.
10. Duriez E, Masselon CD, Mesmin C, Court M, Demeure K, Allory Y и др.. Крупномасштабный SRM-скрининг биомаркеров-кандидатов на уротелиальный рак мочевого пузыря в моче. J Proteome Res (2017) 16: 1617–31. doi: 10.1021/acs.jproteome.6b00979 [PubMed] [CrossRef] [Google Scholar]
11. Lei T, Zhao X, Jin S, Meng Q, Zhou H, Zhang M. Открытие потенциальных биомаркеров рака мочевого пузыря с помощью сравнительной протеомики и анализа мочи. Clin Genitourin Cancer (2013) 11:56–62. DOI: 10.1016/j.clgc.2012.06.003 [PubMed] [CrossRef] [Google Scholar]
12. Сантони Г., Морелли М.Б., Амантини С., Баттелли Н. Мочевые маркеры при раке мочевого пузыря: обновление. Фронт Онкол (2018) 8:362. doi: 10.3389/fonc.2018.00362 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
13.
Shimura T, Dayde D, Wang H, Okuda Y, Iwasaki H, Ebi M, et al. Новая панель биомаркеров белка мочи для ранней диагностики рака желудка.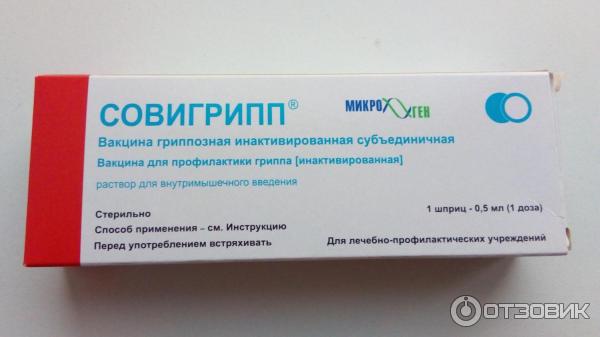 Бр Дж Рак (2020) 123: 1656–64. doi: 10.1038/s41416-020-01063-5
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Бр Дж Рак (2020) 123: 1656–64. doi: 10.1038/s41416-020-01063-5
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
14. Чен Ю.Т., Цай Ч.Х., Чен К.Л., Ю Дж.С., Чанг Ю.Х. Разработка биомаркеров рака мочеполовой системы с использованием клинической протеомики на основе масс-спектрометрии. J Food Drug Anal (2019) 27: 387–403. DOI: 10.1016/j.jfda.2018.090,005 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
15. Xiao K, Yu L, Zhu L, Wu Z, Weng X, Qiu G. Профилирование протеомики мочи и функциональная характеристика остеоартрита коленного сустава с использованием технологии iTRAQ. Horm Metab Res (2019) 51: 735–40. дои: 10.1055/a-1012-8571 [PubMed] [CrossRef] [Google Scholar]
16. М., Гао Ю. Мочевые биомаркеры заболеваний головного мозга. Геномика, протеомика, биоинформация (2015) 13:345–54. doi: 10.1016/j.gpb.2015.08.005 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
17.
Декрамер С., Гонсалес де Передо А., Брейль Б., Мишак Х. , Монсаррат Б., Баскандс Дж.Л. и др. Моча в клинической протеомике. Молекулярная клеточная протеомика (2008) 7:1850–62. doi: 10.1074/mcp.R800001-MCP200
[PubMed] [CrossRef] [Google Scholar]
, Монсаррат Б., Баскандс Дж.Л. и др. Моча в клинической протеомике. Молекулярная клеточная протеомика (2008) 7:1850–62. doi: 10.1074/mcp.R800001-MCP200
[PubMed] [CrossRef] [Google Scholar]
18. Winter SV, Karayel O, Strauss MT, Padmanabhan S, Surface M, Merchant K и др. Профилирование протеома мочи для стратификации пациентов с семейной болезнью Паркинсона. (2020). дои: 10.1101/2020.08.09.243584 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
19. Shen B, Yi X, Sun Y, Bi X, Du J, Zhang C и др. Протеомная и метаболомная характеристика сыворотки пациентов с COVID-19. Cell (2020) 182: 59–72.e15. DOI: 10.1016/j.cell.2020.05.032 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
20. Bi X, Liu W, Ding X, Liang S, Zheng Y, Zhu X и др.. Протеомное и метаболическое профилирование мочи позволяет выявить иммунный ответ у пациентов с COVID-19. Cell Rep (2022) 38:110271. DOI: 10.1016/j.celrep.2021.110271 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
21. Милн Г., Хеймс Т., Скоттон С., Гент Н., Джонсен А., Андерсон Р.М. и др. Приводит ли заражение или вакцинация против SARS-CoV-2 к стойкому иммунитету? Lancet Respir Med (2021) 9: 1450–66. дои: 10.1016/S2213-2600(21)00407-0
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Милн Г., Хеймс Т., Скоттон С., Гент Н., Джонсен А., Андерсон Р.М. и др. Приводит ли заражение или вакцинация против SARS-CoV-2 к стойкому иммунитету? Lancet Respir Med (2021) 9: 1450–66. дои: 10.1016/S2213-2600(21)00407-0
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
22. Wiśniewski JR, Zougman A, Nagaraj N, Mann M. Универсальный метод подготовки образцов для анализа протеома. Nat Methods (2009) 6: 359–62. doi: 10.1038/nmeth.1322 [PubMed] [CrossRef] [Академия Google]
23. Yu Y, Sikorski P, Smith M, Bowman-Gholston C, Cacciabeve N, Nelson KE, et al. Комплексный метапротеомный анализ мочи при наличии и отсутствии нейтрофильного воспаления в мочевыводящих путях. Тераностика (2017) 7: 238–52. doi: 10.7150/thno.16086 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
24.
Тьянова С., Тему Т., Кокс Дж. Вычислительная платформа MaxQuant для протеомики дробовика на основе масс-спектрометрии. Нат Проток (2016) 11: 2301–19. DOI: 10.1038/nprot.2016. 136
[PubMed] [CrossRef] [Академия Google]
136
[PubMed] [CrossRef] [Академия Google]
25. Yu Y, Singh H, Kwon K, Tsitrin T, Petrini J, Nelson KE, et al. Белковые сигнатуры из плазмы крови и мочи предполагают изменения в сосудистой функции и передаче сигналов IL-12 у пожилых людей с хроническими заболеваниями в анамнезе по сравнению с сопоставимая по возрасту здоровая когорта. Геронаука (2021) 43: 593–606. doi: 10.1007/s11357-020-00269-y [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
26. Кокс Дж., Нойхаузер Н., Михальски А., Шелтема Р.А., Олсен Дж.В., Манн М. Андромеда: поисковая система пептидов, интегрированная в среду MaxQuant. J Proteome Res (2011) 10:1794–805. дои: 10.1021/pr101065j [PubMed] [CrossRef] [Google Scholar]
27.
Кокс Дж., Хейн М.Ю., Любер К.А., Парон И., Нагарадж Н., Манн М. Точная количественная оценка без меток по всему протеому с помощью отсроченной нормализации и извлечения максимального соотношения пептидов, называемая MaxLFQ. Молекулярная клеточная протеомика (2014) 13:2513–26.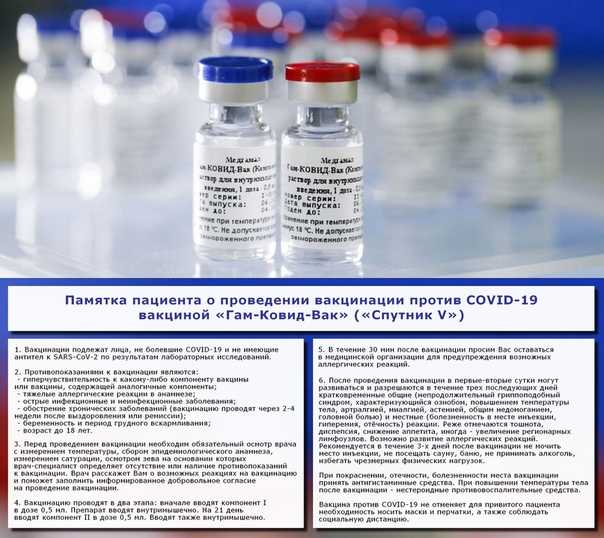
28. Тьянова С., Кокс Дж. Персей: биоинформатическая платформа для интегративного анализа протеомных данных в исследованиях рака. Методы Мол Биол (2018) 1711:133–48. дои: 10.1007/978-1-4939-7493-1_7 [PubMed] [CrossRef] [Google Scholar]
29. Тьянова С., Тему Т., Синицын П., Карлсон А., Хайн М.Ю., Гейгер Т. и др.. Вычислительная платформа Perseus для всестороннего анализа данных (проте)омики. Nat Methods (2016) 13: 731–40. doi: 10.1038/nmeth.3901 [PubMed] [CrossRef] [Google Scholar]
30. Goldman AR, Bitler BG, Schug Z, Conejo-Garcia JR, Zhang R, Speicher DW. Основным эффектом на протеом светлоклеточной карциномы яичников с мутацией ARID1A является подавление мевалонатного пути на посттранскрипционном уровне. Молекулярная клеточная протеомика (2016) 15:3348–60. doi: 10.1074/mcp.M116.062539[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
31.
Лазар С., Гатто Л. , Ферро М., Брюли С., Бургер Т. Учет множественной природы пропущенных значений в наборах данных количественной протеомики без меток для сравнения стратегий вменения. J Proteome Res (2016) 15:1116–25. doi: 10.1021/acs.jproteome.5b00981
[PubMed] [CrossRef] [Google Scholar]
, Ферро М., Брюли С., Бургер Т. Учет множественной природы пропущенных значений в наборах данных количественной протеомики без меток для сравнения стратегий вменения. J Proteome Res (2016) 15:1116–25. doi: 10.1021/acs.jproteome.5b00981
[PubMed] [CrossRef] [Google Scholar]
32. Брудерер Р., Бернхардт О.М., Ганди Т., Миладинович С.М., Ченг Л.Ю., Месснер С. и др.. Расширение границ количественного профилирования протеома за счет независимого от данных сбора и применения к обработанным ацетаминофеном трехмерным микротканям печени. Молекулярная клеточная протеомика (2015) 14:1400–10. doi: 10.1074/mcp.M114.044305 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
33. Callister SJ, Barry RC, Adkins JN, Johnson ET, Qian WJ, Webb-Robertson B-JM и др. Подходы к нормализации для устранения систематических ошибок, связанных с масс-спектрометрией и протеомикой без меток. J Proteome Res (2006) 5: 277–86. дои: 10.1021/pr050300l [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
34. Чжан Б., Чемберс М.С., Табб Д.Л. Протеомная экономия за счет анализа двудольных графов повышает точность и прозрачность. J Proteome Res (2007) 6: 3549–57. дои: 10.1021/pr070230d
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Чжан Б., Чемберс М.С., Табб Д.Л. Протеомная экономия за счет анализа двудольных графов повышает точность и прозрачность. J Proteome Res (2007) 6: 3549–57. дои: 10.1021/pr070230d
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
35. Бенджамини Ю., Хохберг Ю. Контроль уровня ложных открытий: практичный и мощный подход к множественному тестированию. JR Stat Society: Ser B (методологический) (1995) 57: 289–300. doi: 10.1111/j.2517-6161.1995.tb02031.x [CrossRef] [Google Scholar]
36. Хуанг Д.В., Шерман Б.Т., Лемпицки Р.А. Систематический и комплексный анализ больших списков генов с использованием ресурсов биоинформатики DAVID. Нат Проток (2009) 4:44–57. DOI: 10.1038/nprot.2008.211 [PubMed] [CrossRef] [Академия Google]
37. Franz M, Lopes CT, Huck G, Dong Y, Sumer O, Bader GD. Cytoscape.js: библиотека теории графов для визуализации и анализа. Биоинформатика (2016) 32: 309–11. doi: 10.1093/биоинформатика/btv557 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
38. Ali YM, Lynch NJ, Haleem KS, Fujita T, Endo Y, Hansen S и др.. Лектиновый путь активации комплемента является критическим компонентом врожденного иммунного ответа на пневмококковую инфекцию. PloS Pathog (2012) 8: e1002793. doi: 10.1371/journal.ppat.1002793
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Ali YM, Lynch NJ, Haleem KS, Fujita T, Endo Y, Hansen S и др.. Лектиновый путь активации комплемента является критическим компонентом врожденного иммунного ответа на пневмококковую инфекцию. PloS Pathog (2012) 8: e1002793. doi: 10.1371/journal.ppat.1002793
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
39. Ларги Э.Л., Кауфман Т.С. Модуляторы активации комплемента: обзор патентов (2008–2013 гг.). Экспертное мнение Тер Пэт (2014) 24: 665–86. дои: 10.1517/13543776.2014.898063 [PubMed] [CrossRef] [Google Scholar]
40. Кунду Р., Нареан Дж. С., Ван Л., Фенн Дж., Пиллэй Т., Фернандес Н. Д. и др. Перекрестно-реактивные Т-клетки памяти связаны с защитой от инфекции SARS-CoV-2 при контактах с COVID-19. Нацкоммуна (2022) 13:80. doi: 10.1038/s41467-021-27674-x [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
41.
Гарсия-Торре А., Буэно-Гарсия Э., Лопес-Мартинес Р., Риосерас Б., Моро-Гарсия М.А., Алонсо-Альварес С. и др.. У выживших пожилых пациентов сохраняется клеточная и гуморальная иммунологическая память через несколько месяцев после SARS-CoV-2 Инфекционное заболевание. J Gerontol A Biol Sci Med Sci (2022) 77: 33–40. doi: 10.1093/gerona/glab206
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
J Gerontol A Biol Sci Med Sci (2022) 77: 33–40. doi: 10.1093/gerona/glab206
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
42. Ma J, Chen T, Wu S, Yang C, Bai M, Shu K и др.. iProX: интегрированный ресурс протеома. Нуклеиновые кислоты Res (2019)) 47:D1211–7. дои: 10.1093/nar/gky869 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Динамика метаболизма мочи Дискриминация ответа на вакцинацию против гриппа
. 2023 14 января; 15 (1): 242.
дои: 10.3390/v15010242.
Тори С Родрик 1 , Йик Сиу 1 , Майкл А. Карлок 2 , Тед М Росс 2 , Дрю Р. Джонс 1 3
Принадлежности
- 1 Лаборатория основных ресурсов по метаболомике, NYU Langone Health, Нью-Йорк, NY 10016, США.
- 2 Центр вакцин и иммунологии, Университет Джорджии, Афины, Джорджия 30602, США.
- 3 Кафедра биохимии и молекулярной фармакологии, NYU Langone Health, Нью-Йорк, NY 10016, США.
- PMID: 36680282
- PMCID: PMC9861122
- DOI: 10.3390/v15010242
Бесплатная статья ЧВК
Тори С. Родрик и др. Вирусы. .
Бесплатная статья ЧВК
. 2023 14 января; 15 (1): 242.
2023 14 января; 15 (1): 242.
дои: 10.3390/v15010242.
Авторы
Тори С Родрик 1 , Йик Сиу 1 , Майкл А. Карлок 2 , Тед М Росс 2 , Дрю Р. Джонс 1 3
Принадлежности
- 1 Лаборатория основных ресурсов по метаболомике, NYU Langone Health, Нью-Йорк, NY 10016, США.
- 2 Центр вакцин и иммунологии, Университет Джорджии, Афины, Джорджия 30602, США.
- 3 Кафедра биохимии и молекулярной фармакологии, NYU Langone Health, Нью-Йорк, NY 10016, США.

- PMID: 36680282
- PMCID: PMC9861122
- DOI: 10.3390/v15010242
Абстрактный
Грипп представляет собой серьезную и постоянную опасность для здоровья населения. Текущие совместные усилия направлены на создание универсальной вакцины против гриппа с целью как улучшения реакции на вакцинацию, так и расширения защиты от нескольких штаммов и кладов с помощью одной вакцины. В качестве промежуточного шага к этим целям текущая работа сосредоточена на оценке системного ответа хозяина на вакцинацию как в нормальных, так и в группах высокого риска, таких как тучные и гериатрические группы населения, которые были связаны с плохой реакцией на вакцинацию. Поэтому мы использовали метаболомический подход, используя временной ход (n = 5 временных точек) реакции человека на вакцинацию против гриппа от времени до вакцинации (до) до 90 дней после вакцинации. Мы проанализировали профили мочи когорты субъектов (n = 179), предназначенные для равномерной выборки по возрасту, полу, ИМТ и другим демографическим факторам, стратифицируя их реакцию на вакцинацию как «Высокую», «Низкую» или «Нет» на основе на сероконверсию, измеренную методом ингибирования гемагглютинации (HAI) из образцов плазмы на 28-й день после вакцинации. В целом, мы предположительно идентифицировали 15 903 различных названных низкомолекулярных структуры (4473 при 10% FDR) среди 895 проанализированных образцов с целью идентификации метаболитов, коррелирующих с ответом на вакцину, а также прогностических и диагностических маркеров из периодов до и после вакцинации соответственно. Примечательно, что мы обнаружили, что метаболические профили могут непредвзято отделить высокоответчиков с высоким риском от неответчиков с высоким риском (с ожирением/пожилым возрастом) в течение 3 дней после вакцинации.
Поэтому мы использовали метаболомический подход, используя временной ход (n = 5 временных точек) реакции человека на вакцинацию против гриппа от времени до вакцинации (до) до 90 дней после вакцинации. Мы проанализировали профили мочи когорты субъектов (n = 179), предназначенные для равномерной выборки по возрасту, полу, ИМТ и другим демографическим факторам, стратифицируя их реакцию на вакцинацию как «Высокую», «Низкую» или «Нет» на основе на сероконверсию, измеренную методом ингибирования гемагглютинации (HAI) из образцов плазмы на 28-й день после вакцинации. В целом, мы предположительно идентифицировали 15 903 различных названных низкомолекулярных структуры (4473 при 10% FDR) среди 895 проанализированных образцов с целью идентификации метаболитов, коррелирующих с ответом на вакцину, а также прогностических и диагностических маркеров из периодов до и после вакцинации соответственно. Примечательно, что мы обнаружили, что метаболические профили могут непредвзято отделить высокоответчиков с высоким риском от неответчиков с высоким риском (с ожирением/пожилым возрастом) в течение 3 дней после вакцинации. Метаболиты пурина гуанин и гипоксантин отрицательно связаны с высокой сероконверсией (p = 0,0032, p <0,0001 соответственно), тогда как ацетил-лейцин и 5-амивалериановая кислота связаны положительно. Дальнейшие изменения цистина, глутаминовой кислоты, кинуренина и других метаболитов связаны с ранним окислительным стрессом (через 3 дня) после вакцинации, что является отличительной чертой лиц с высоким ответом. Текущие усилия направлены на проверку этих предполагаемых маркеров с использованием модели гриппозной инфекции на хорьках, а также независимой когорты сезонной вакцинации людей и исследований заражения людей живым вирусом.
Метаболиты пурина гуанин и гипоксантин отрицательно связаны с высокой сероконверсией (p = 0,0032, p <0,0001 соответственно), тогда как ацетил-лейцин и 5-амивалериановая кислота связаны положительно. Дальнейшие изменения цистина, глутаминовой кислоты, кинуренина и других метаболитов связаны с ранним окислительным стрессом (через 3 дня) после вакцинации, что является отличительной чертой лиц с высоким ответом. Текущие усилия направлены на проверку этих предполагаемых маркеров с использованием модели гриппозной инфекции на хорьках, а также независимой когорты сезонной вакцинации людей и исследований заражения людей живым вирусом.
Ключевые слова: ЖХМС; грипп; метаболомика; вакцина.
Заявление о конфликте интересов
Авторы заявляют об отсутствии конфликта интересов.
Цифры
Рисунок 1
Общий дизайн и метаданные…
Рисунок 1
Общий дизайн и метаданные когорты. ( A ) Схематическое изображение…
Рисунок 1 Общий дизайн и метаданные когорты. ( A ) Схематическое изображение течения времени. Образцы мочи собирали каждый из 5 дней для каждого субъекта. HAI рассчитывали с использованием образцов на 0-й и 28-й день для определения статуса сероконверсии. ( Б – E ) Пропорциональный состав когорты по ИМТ, статусу респондента (сероконверсия), этнической принадлежности и полу. ( F ) Гистограмма ИМТ субъекта в когорте вакцинированных. ( G ) Гистограмма возраста и пола субъектов в когорте вакцинированных.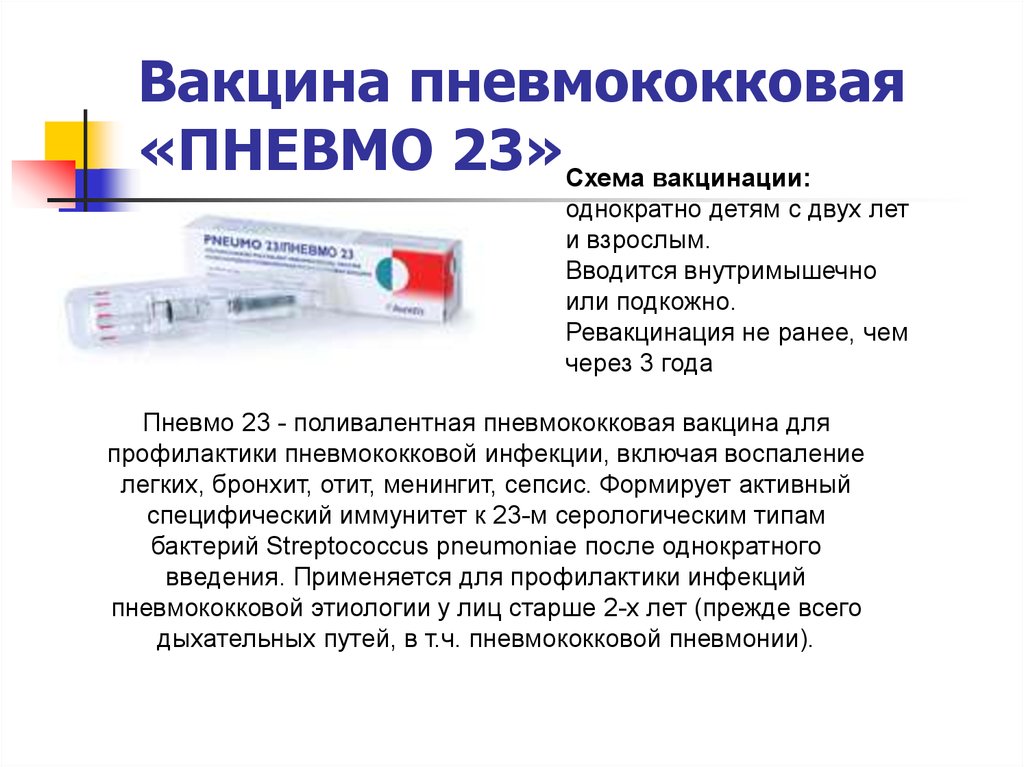 ( H ) Пропорциональный состав ИМТ по отношению к этнической принадлежности субъекта, о которой он сообщил сам. Все предметы были набраны из Афин, штат Джорджия.
( H ) Пропорциональный состав ИМТ по отношению к этнической принадлежности субъекта, о которой он сообщил сам. Все предметы были набраны из Афин, штат Джорджия.
Рисунок 2
Резюме данных метаболомики и…
Рисунок 2
Сводка данных метаболомики и реакции субъекта на сероконверсию. ( A ) Общий…
фигура 2 Сводка данных метаболомики и реакции субъекта на сероконверсию. ( A ) Общая полуконтролируемая иерархическая кластеризация для метаболомного анализа; n = 895 образцов, проанализированных с относительной количественной оценкой 15 903 предположительно идентифицированных метаболитов. ( B – D ) Вулканический график, представляющий кратное изменение метаболитов конкретного субъекта между днем 3 после вакцинации и днем 0 до вакцинации.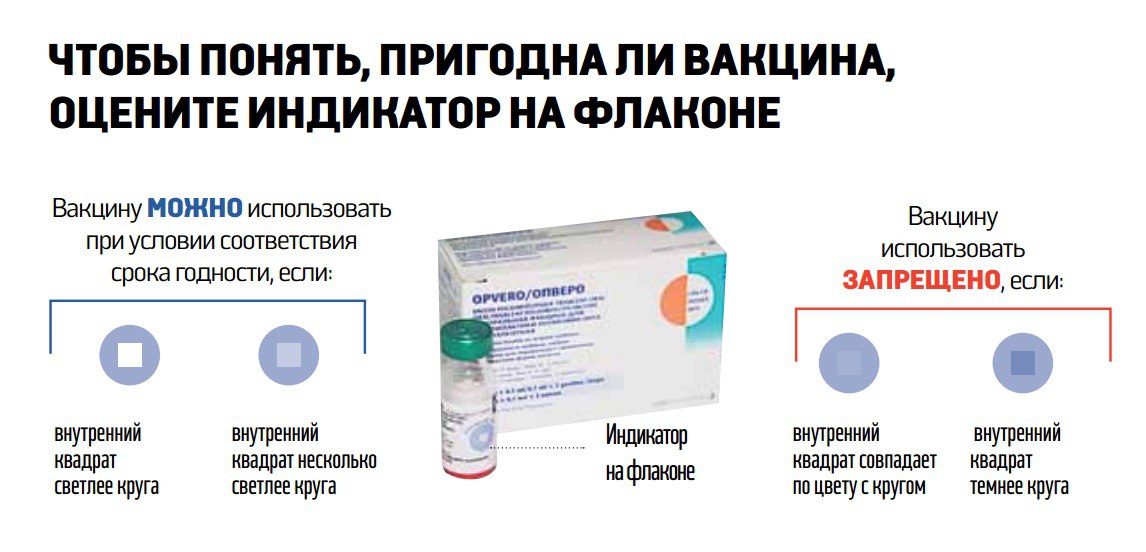 Ось X представляет кратное изменение и Log2, а ось Y представляет статистическую значимость (t-критерий, двусторонний, с равной дисперсией, без поправки). ( E ) Диаграмма Венна перекрывающихся значимых метаболитов между тремя сравнениями D3 и D0 у лиц с высоким, низким и нулевым ответом соответственно.
Ось X представляет кратное изменение и Log2, а ось Y представляет статистическую значимость (t-критерий, двусторонний, с равной дисперсией, без поправки). ( E ) Диаграмма Венна перекрывающихся значимых метаболитов между тремя сравнениями D3 и D0 у лиц с высоким, низким и нулевым ответом соответственно.
Рисунок 3
Метаболиты, связанные с реакцией…
Рисунок 3
Метаболиты, связанные с реакцией лиц с высоким ответом на вакцинацию. ( А )…
Рисунок 3 Метаболиты, связанные с реакцией лиц с высоким ответом на вакцинацию. ( A ) Индивидуальные изменения метаболитов в зависимости от статуса сероконверсии на 3-й день по сравнению с 0-м днем. Столбики погрешностей представляют собой стандартное отклонение.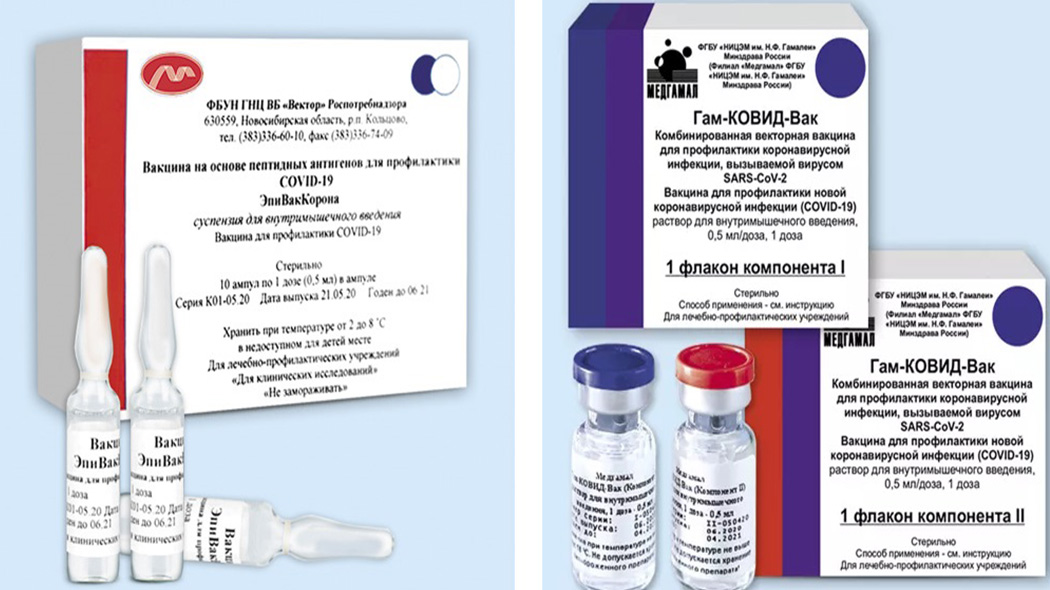 ( B ) Общая корреляция маркеров метаболитов с показателем сероконверсии субъекта, n = 179, где значение p представляет значимость ненулевого наклона для линейной регрессии. Красная линия представляет наиболее подходящую регрессию, а серая область представляет 95% доверительный интервал для линии регрессии. ( C , D ) Анализ метаболических путей у лиц с высоким ответом и без ответа, соответственно. Ось x представляет влияние пути (% пройденного пути), а ось y представляет статистическую значимость.
( B ) Общая корреляция маркеров метаболитов с показателем сероконверсии субъекта, n = 179, где значение p представляет значимость ненулевого наклона для линейной регрессии. Красная линия представляет наиболее подходящую регрессию, а серая область представляет 95% доверительный интервал для линии регрессии. ( C , D ) Анализ метаболических путей у лиц с высоким ответом и без ответа, соответственно. Ось x представляет влияние пути (% пройденного пути), а ось y представляет статистическую значимость.
Рисунок 4
Дифференциальные метаболические профили…
Рисунок 4
Дифференциальные метаболические профили пациентов с высоким и нулевым ответом на ожирение. ( A ) Без присмотра…
Рисунок 4 Дифференциальные метаболические профили пациентов с высоким и нулевым ответом на ожирение. ( A ) Неконтролируемая иерархическая кластеризация профилей метаболитов пациентов с ожирением с высоким ответом и пациентов с ожирением без ответа, с n = 523 предположительно идентифицированных метаболитов с необработанным p -значением <0,01 (t-критерий). ( B ) График рассеяния корреляции ИМТ субъекта с изменением D3/D0 относительных уровней метаболитов. Красная линия представляет наиболее подходящую регрессию, а серая область представляет 95% доверительный интервал для линии регрессии. ( C ) Диаграмма Венна перекрывающихся значимых метаболитов между ожирением с высоким ответом и ожирением без ответа на 3-й день (D3), а также на 0-й день (D0). ( D ) Характеристическая кривая оператора приемника (кривая ROC) для предположительно идентифицированного метаболита D-Psicose, отличающая людей с ожирением с высоким ответом (синий) от людей с ожирением без ответа (фиолетовый). AUC = площадь под кривой. Красная линия указывает порог теста для групповой дискриминации.
( A ) Неконтролируемая иерархическая кластеризация профилей метаболитов пациентов с ожирением с высоким ответом и пациентов с ожирением без ответа, с n = 523 предположительно идентифицированных метаболитов с необработанным p -значением <0,01 (t-критерий). ( B ) График рассеяния корреляции ИМТ субъекта с изменением D3/D0 относительных уровней метаболитов. Красная линия представляет наиболее подходящую регрессию, а серая область представляет 95% доверительный интервал для линии регрессии. ( C ) Диаграмма Венна перекрывающихся значимых метаболитов между ожирением с высоким ответом и ожирением без ответа на 3-й день (D3), а также на 0-й день (D0). ( D ) Характеристическая кривая оператора приемника (кривая ROC) для предположительно идентифицированного метаболита D-Psicose, отличающая людей с ожирением с высоким ответом (синий) от людей с ожирением без ответа (фиолетовый). AUC = площадь под кривой. Красная линия указывает порог теста для групповой дискриминации. ( E ) Анализ метаболических путей прогностических (исходных) метаболитов между тучными пациентами с высоким ответом и страдающими ожирением без ответа. ( F ) Гистограмма ИМТ для лиц с высоким и неответившим ответом. ( G ) Гистограмма возраста для высокореспондентов и нереспондентов.
( E ) Анализ метаболических путей прогностических (исходных) метаболитов между тучными пациентами с высоким ответом и страдающими ожирением без ответа. ( F ) Гистограмма ИМТ для лиц с высоким и неответившим ответом. ( G ) Гистограмма возраста для высокореспондентов и нереспондентов.
Рисунок 5
Дифференциальные метаболические профили гериатрических…
Рисунок 5
Дифференциальные метаболические профили гериатрических пациентов с высоким и нулевым ответом. ( А – Д )…
Рисунок 5 Дифференциальные метаболические профили гериатрических пациентов с высоким и нулевым ответом. ( A – D ) Распределение возраста всех субъектов когорты в зависимости от категории ИМТ. ( E ) Неконтролируемая иерархическая кластеризация профилей метаболитов гериатрических пациентов с высоким ответом и гериатрических пациентов без ответа, с n = 624 предположительно идентифицированных метаболита с необработанным значением p <0,05 (t-критерий). ( F ) Диаграмма Венна перекрывающихся значимых метаболитов между гериатрическими пациентами с высоким уровнем ответа и гериатрическими пациентами без ответа на 3-й день (D3), а также на 0-й день (D0). ( G ) Анализ метаболических путей уникально измененных метаболитов среди пожилых людей, не ответивших на лечение. ( H – K ) Диаграмма рассеяния корреляции показателя сероконверсии субъекта с изменением D3/D0 относительных уровней метаболитов. Красная линия представляет наиболее подходящую регрессию, а серая область представляет 95% доверительный интервал для линии регрессии, n = 179 для всех корреляций.
( E ) Неконтролируемая иерархическая кластеризация профилей метаболитов гериатрических пациентов с высоким ответом и гериатрических пациентов без ответа, с n = 624 предположительно идентифицированных метаболита с необработанным значением p <0,05 (t-критерий). ( F ) Диаграмма Венна перекрывающихся значимых метаболитов между гериатрическими пациентами с высоким уровнем ответа и гериатрическими пациентами без ответа на 3-й день (D3), а также на 0-й день (D0). ( G ) Анализ метаболических путей уникально измененных метаболитов среди пожилых людей, не ответивших на лечение. ( H – K ) Диаграмма рассеяния корреляции показателя сероконверсии субъекта с изменением D3/D0 относительных уровней метаболитов. Красная линия представляет наиболее подходящую регрессию, а серая область представляет 95% доверительный интервал для линии регрессии, n = 179 для всех корреляций.
Рисунок 6
Динамика изменения метаболизма…
Рисунок 6
Динамика реакции метаболизма на вакцину IAV во времени. ( А – Я )…
( А – Я )…
Метаболитная динамика реакции на вакцину IAV во времени. ( A – I ) Линейный график относительного изменения уровней метаболитов мочи субъекта по отношению к исходному уровню в течение 90-дневного периода времени. Для каждого метаболита планки погрешностей представляют собой стандартное отклонение кратности изменения по сравнению с исходным уровнем, а ось Y представляет значения Log2. Каждый метаболит анализировали в двухфакторном дисперсионном анализе. I = взаимодействие двух факторов, R = фактор ряда, дни после вакцинации, C = фактор столбца, статус сероконверсии (высокий ответ или отсутствие ответа).
См. это изображение и информацию об авторских правах в PMC
Похожие статьи
Выявление защитных антител против широкого спектра вирусов h2N1 у хорьков, невосприимчивых к историческим вирусам гриппа h2N1.

Картер Д.М., Дарби К.А., Джонсон С.К., Карлок М.А., Кирхенбаум Г.А., Аллен Д.Д., Фогель Т.Ю., Делагрейв С., ДиНаполи Дж., Клеантус Х., Росс ТМ. Картер Д.М. и соавт. Дж Вирол. 2017 30 ноября; 91(24):e01283-17. doi: 10.1128/ОВИ.01283-17. Печать 2017 15 декабря. Дж Вирол. 2017. PMID: 28978709 Бесплатная статья ЧВК.
Обоснование вакцинации трехвалентными или четырехвалентными живыми аттенуированными вакцинами против гриппа: защитная эффективность вакцины на модели хорьков.
Руденко Л., Киселева И., Крутикова Е., Степанова Е., Рекстин А., Донина С., Писарева М., Григорьева Е., Крышень К., Мужикян А., Макарова М., Воробей Е. Г., Торелли Г., Киений М.П. Руденко Л. и соавт. ПЛОС Один. 3 декабря 2018 г .; 13 (12): e0208028. doi: 10.1371/journal.pone.0208028. Электронная коллекция 2018.
 ПЛОС Один. 2018.
PMID: 30507951
Бесплатная статья ЧВК.
ПЛОС Один. 2018.
PMID: 30507951
Бесплатная статья ЧВК.Анализ конкурентного ингибирования гемагглютинации для анализа функциональной активности антител против вируса гриппа.
Кирхенбаум Г.А., Саутто Г.А., Ричардсон Р.А., Экер Дж.В., Росс Т.М. Кирхенбаум Г.А. и соавт. Дж Вирол. 2021 9 ноября; 95 (23): e0237920. doi: 10.1128/ОВИ.02379-20. Epub 2021 15 сентября. Дж Вирол. 2021. PMID: 34523961 Бесплатная статья ЧВК.
Реакция антител на вакцину против гриппа у медицинских работников.
Сакадура-Лейте Э., Соуза-Ува А., Ребело-де-Андраде Х. Sacadura-Leite E, et al. вакцина. 2012 5 января; 30 (2): 436-41. doi: 10.1016/j.vaccine.2011.10.061. Epub 2011 4 ноября.
 вакцина. 2012.
PMID: 22064268
вакцина. 2012.
PMID: 22064268Интраназальная трехвалентная вакцина против гриппа с протеосомным адъювантом является безопасной, иммуногенной и эффективной в модели заражения вирусным гриппом человека. Сывороточный IgG и слизистый IgA являются важными коррелятами защиты от заболеваний, связанных с инфекцией.
Ламбкин-Уильямс Р., Гелдер С., Бротон Р., Маллет С.П., Гилберт А.С., Манн А., Хе Д., Оксфорд Дж.С., Берт Д. Ламбкин-Уильямс Р. и соавт. ПЛОС Один. 22 декабря 2016 г .; 11 (12): e0163089. doi: 10.1371/journal.pone.0163089. Электронная коллекция 2016. ПЛОС Один. 2016. PMID: 28005959 Бесплатная статья ЧВК. Клиническое испытание.
Посмотреть все похожие статьи
Рекомендации
- Кейлман Л.
 Дж. Сезонный грипп (грипп) Nurs. клин. Н. Ам. 2019;54:227–243. doi: 10.1016/j.cnur.2019.02.009.
—
DOI
—
пабмед
Дж. Сезонный грипп (грипп) Nurs. клин. Н. Ам. 2019;54:227–243. doi: 10.1016/j.cnur.2019.02.009.
—
DOI
—
пабмед
- Кейлман Л.
- Paget J., Spreeuwenberg P., Charu V., Taylor R.J., Iuliano A.D., Bresee J., Simonsen L., Viboud C., Глобальная сеть сотрудничества по вопросам смертности от сезонного гриппа и сотрудничающие группы GLaMOR Глобальная смертность, связанная с эпидемиями сезонного гриппа: Новые оценки и предикторы бремени от проекта GLaMOR. Дж. Глоб. Здоровье. 2019;9:020421. doi: 10.7189/jogh.09.020421. — DOI — ЧВК — пабмед
- Аяри А.
 , Роса-Калатрава М., Лансель С., Бартелеми Дж., Пиццорно А., Майеф-Лушар А., Барон М., Хот Д., Деруйтер Л., Сулард Д. и др. Инфекция гриппа изменяет энергетический обмен и вызывает признаки потемнения в жировых клетках и тканях. коммун. биол. 2020;3:237. doi: 10.1038/s42003-020-0965-6.
—
DOI
—
ЧВК
—
пабмед
, Роса-Калатрава М., Лансель С., Бартелеми Дж., Пиццорно А., Майеф-Лушар А., Барон М., Хот Д., Деруйтер Л., Сулард Д. и др. Инфекция гриппа изменяет энергетический обмен и вызывает признаки потемнения в жировых клетках и тканях. коммун. биол. 2020;3:237. doi: 10.1038/s42003-020-0965-6.
—
DOI
—
ЧВК
—
пабмед
- Аяри А.
- Нолан К.Е., Баер Л.А., Карекар П., Нельсон А.М., Стэнфорд К.И., Дулиттл Л.М., Росас Л.Е., Хикман-Дэвис Дж.М., Сингх Х.
 , Дэвис И.К. Метаболические сдвиги модулируют повреждение легких, вызванное инфекцией вирусом гриппа А h2N1. Вирусология. 2021; 559: 111–119. doi: 10.1016/j.virol.2021.03.008.
—
DOI
—
ЧВК
—
пабмед
, Дэвис И.К. Метаболические сдвиги модулируют повреждение легких, вызванное инфекцией вирусом гриппа А h2N1. Вирусология. 2021; 559: 111–119. doi: 10.1016/j.virol.2021.03.008.
—
DOI
—
ЧВК
—
пабмед
- Нолан К.Е., Баер Л.А., Карекар П., Нельсон А.М., Стэнфорд К.И., Дулиттл Л.М., Росас Л.Е., Хикман-Дэвис Дж.М., Сингх Х.
- Рамос И., Смит Г., Руф-Замойски Ф., Мартинес-Ромеро К., Фрибург М., Карбахал Э.А., Хартманн Б., Наир В.Д., Марьянович Н., Монтеагудо П.Л. и др. Врожденный иммунный ответ на вирус гриппа при одноклеточном разрешении в эпителиальных клетках человека.
- Рамос И., Смит Г., Руф-Замойски Ф., Мартинес-Ромеро К., Фрибург М., Карбахал Э.А., Хартманн Б., Наир В.Д., Марьянович Н., Монтеагудо П.Л. и др. Врожденный иммунный ответ на вирус гриппа при одноклеточном разрешении в эпителиальных клетках человека.
