Эталон ответов
1б 2г 3в 4б 5в 6в 7б 8б 9в 10в 11г 12б 13б 14а 15б 16б 17а 18б 19б 20г
1. Основная причина развития бронхитов
а) алкоголизм
б) курение
в) бактериальная и вирусная инфекция
г) переохлаждение
2. Основной симптом бронхита
а) головная боль
б) слабость
в) лёгочное кровотечениее
г) кашель с мокротой
3. Основной фактор риска хронического бронхита
а) курение
б) бактериальная и вирусная инфекция
в) переохлаждение
г) гиповитаминоз
4. Основной симптом обструктивного бронхита
а) головная боль
б) недомогание
в) повышение температуры
г) одышка
5. Характер мокроты при остром бронхите
а) слизистая
б) стекловидная
в) «ржавая»
г) розовая пенистая
6. Осложнения хронического бронхита
Осложнения хронического бронхита
а) лёгочное кровотечение
б) острая сосудистая недостаточность
в) острая сердечная недостаточность
г) хроническая дыхательная недостаточность
7. При кашле с отделением гнойной мокроты не назначается
а) бромгексин
б) кодеин
в) мукалтин
г) отхаркивающая микстура
8. Для разжижения густой вязкой мокроты используется
а) йодид калия
б) кодеин
в) сальбутамол
г) теофиллин
9. Кратность приема отхаркивающей микстуры в течение дня
а) 1-2
б) 3-4
г) 10-12
10. При лечении гнойного бронхита используется
а) амоксициллин, бромгексин
б) бекотид, интал
в) кодеин, либексин
г) кофеин, кордиамин
11. К этиологическому лечению бронхиальной астмы относится:
а) бронхолитическая терапия
б) ферментативная терапия
в) элиминационная терапия
г) физиотерапия
12. Основной симптом при бронхиальной
астме
Основной симптом при бронхиальной
астме
а) инспираторная одышка
б) кашель с гнойной мокротой
в) кровохарканье
г) приступ удушья
13. Вынужденное положение пациента при приступе бронхиальной астмы
а) горизонтальное
б) горизонтальное с приподнятыми ногами
в) лежа на боку
г) сидя, с упором на руки
14. Пациент должен тщательно полоскать рот после применения ингалятора:
а) вентолина
б) бектида
в) беротека
г) астмопента
15. Небольшое количество вязкой стекловидной мокроты выделяется при
а) абсцессе легкого
б) бронхиальной астме
в) крупозной пневмонии
г) экссудативном плеврите
16. При приступе удушья на фоне бронхиальной астмы применяется
а) кодеин
б) либексин
в) сальбутамол
г) тусупрекс
17. Для профилактики приступов удушья
при бронхиальной астме используется
Для профилактики приступов удушья
при бронхиальной астме используется
а) астмопент
б) беротек
в) интал
г) теофиллин
18. Пикфлоуметрия – это определение
а) дыхательного объема
б) жизненной емкости легких
в) остаточного объема
г) пиковой скорости выдоха
а) вирус
б) микобактерия
в) пневмококк
г) кишечная палочка
20. Воспаление целой доли легкого наблюдается при
а) остром бронхите
б) бронхиальной астме
в) крупозной пневмонии
г) сухом плеврите
21. «Ржавый» характер мокроты наблюдается при
а) остром бронхите
б) бронхиальной астме
в) крупозной пневмонии
г) сухом плеврите
22. Наиболее информативный метод диагностики пневмонии
а) анализ крови
б) анализ мокроты
в) плевральная пункция
г) рентгенография органов грудной клетки
23. Этиотропное лечение пневмонии – это
применение
Этиотропное лечение пневмонии – это
применение
а) бронхолитиков
б) отхаркивающих
в) антибиотиков
г) жаропонижающих
24. Осложнение пневмонии
а) лёгочное кровотечение
б) лихорадка
в) боль в грудной клетке
г) острая дыхательная недостаточность
25. При критическом снижении температуры тела может развиться
а) острая дыхательная недостаточность
б) коллапс
в) острая коронарная недостаточность
г) легочное кровотечение
26. Частота дыхательных движений в норме в мин.
а) 6-10
б) 20-40
в) 60-80
г) 16-20
27. Частота сердечных сокращений в норме в мин.
а) 80-100
б) 50-60
в) 100-120
г) 60-80
28. Основная причина приобретенных бронхоэктазов
а) бронхиальная астма
б) крупозная пневмония
в) хронический бронхит
г) сухой плеврит
29. Заболевание, характеризующееся
развитием воспаления в расширенных
бронхах
Заболевание, характеризующееся
развитием воспаления в расширенных
бронхах
а) абсцесс легкого
б) бронхоэктатическая болезнь
в) крупозная пневмония
г) экссудативный плеврит
30. Основной симптом бронхоэктатической болезни
а) слабость
б) снижение аппетита
в) недомогание
г) кашель с гнойной мокротой
31. Пациент выделяет мокроту по утрам полным ртом при
а) бронхиальной астме
б) бронхоэктатической болезни
в) крупозной пневмонии
г) экссудативном плеврите
32. Характер мокроты при бронхоэктатической болезни
а) гнойная
б) «ржавая»
г) стекловидная
33. Наиболее информативный метод диагностики бронхоэктатической болезни
а) бронхография
б) рентгеноскопия
в) спирометрия
г) флюорография
34. Пальцы в виде «барабанных палочек»
и ногти в виде «часовых стекол»
встречаются при
Пальцы в виде «барабанных палочек»
и ногти в виде «часовых стекол»
встречаются при
а) хронических заболеваниях дыхательной системы
б) острых заболеваниях дыхательной системы
в) острых заболеваниях пищеварительной системы
г) хронических заболеваниях пищеварительной системы
35. Дренажное положение придается пациенту с целью
а) снижения лихорадки
б) уменьшения одышки
в) расширения бронхов
г) облегчения отхождения мокроты
36. Осложнения бронхоэктатической болезни
а) лихорадка
б) приступ экспираторного удушья
в) кашель с гнойной мокротой
г) легочное кровотечение
37. Профилактика обострения бронхиальной астмы:
а) усиление питания
б) устранение гиподинамии
в) отказ от алкоголя
г) прекращение контакта с аллергеном
38. При сборе мокроты на общий анализ пациента необходимо обеспечить
б) сухой банкой
в) стерильной пробиркой
г) стерильной банкой
39. При выделении гнойной мокроты пациента
необходимо обеспечить
При выделении гнойной мокроты пациента
необходимо обеспечить
а) чашкой Петри
б) стерильной банкой
в) индивидуальной плевательницей
г) стерильной пробиркой
40. Индивидуальная карманная плевательница должна быть заполнена на 1/4
а) водой
б) физраствором
в) 25% раствор соды
г) хлорамином
41. При выделении большого количества гнойной мокроты в питании пациента рекомендуется
а) увеличить количество соли
б) увеличить количество белка
в) уменьшить количество соли
г) уменьшить количество белка
42. Рентгенологическое исследование бронхов с применением контрастного вещества
а) бронхоскопия
б) бронхография
в) томография
г) флюорография
43. Абсцесс легкого – это
а) воспаление легкого
б) воспаление плевры
в) образование полости с гноем
г) накопление жидкости в плевральной полости
44.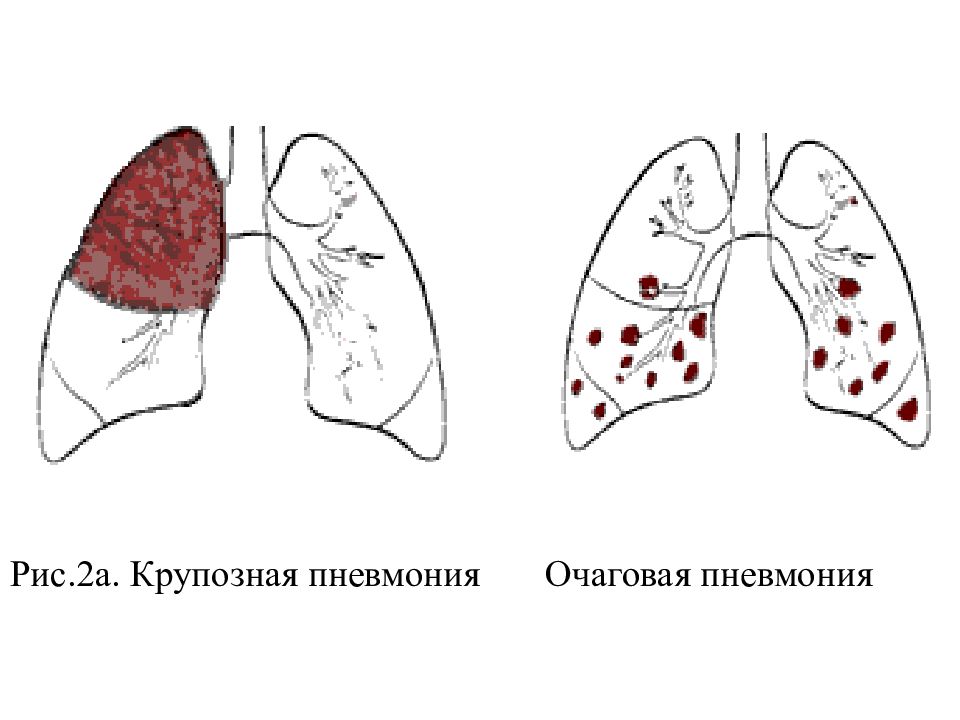
а) острый бронхит
б)я пневмония
в) бронхиальная астма
г) сухой плеврит
45. Внезапное появление обильной гнойной мокроты на фоне гектической лихорадки наблюдается при
а) абсцессе легкого
б) бронхиальной астме
в) крупозной пневмонии
г) сухом плеврите
46. Для абсцесса легкого характерна лихорадка
а) волнообразная
б) гектическая
в) извращенная
г) постоянная
47. Приоритетная проблема пациента после прорыва абсцесса легкого в бронх
а) лихорадка
б) слабость
в) кровохарканье
г) кашель с гнойной мокротой
48. Осложнения абсцесса легкого
а) недомогание
б) головная боль
в) кашель с гнойной мокротой
г) легочное кровотечение
49. Характер мокроты при абсцессе легкого
а) гнойная
б) слизистая
в) стекловидная
г) «ржавая»
50. При лечении абсцесса легкого
используются препараты
При лечении абсцесса легкого
используются препараты
а) антибиотики
б) диуретики
в) антигистаминные
г) кортикостероиды
51. Возбудителем туберкулеза является
а) пневмококк
б) микобактерия
в) риккетсия
г) вирус
52. В органах и тканях при туберкулёзе образуются:
а) бугорки
б) папулы
в) пустулы
г) везикулы
53. Наиболее частый путь передачи туберкулеза
а) алиментарный
б) аэрогенный
в) водный
г) контактно-бытовой
54. Ранние симптомы туберкулеза
а) лихорадка, кашель с гнойной мокротой
б) приступ удушья, стекловидная мокрота
в) длительный субфебрилитет, покашливание
г) одышка, «ржавая» мокрота
55. При туберкулезе в мокроте можно обнаружить
а) атипичные клетки
б) микобактерии
в) спирали Куршмана
г) эозинофилы
56. Диета № 11 назначается при
Диета № 11 назначается при
а) бронхиальной астме
б) бронхите
в) пневмонии
г) туберкулезе
57. Антибиотик, эффективный при лечении туберкулеза
а) ампициллин
б) гентамицин
в) рифампицин
г) эритромицин
58. Побочное действие рифампицина
а) гепатотоксическое
б) нейротоксическое
в) нефротоксическое
г) ототоксическое
59. При лечении туберкулеза применяют
а) амоксициллин, фурагин
б) димедрол, пипольфен
в) изониазид, рифампицин
г) преднизолон, циклофосфан
60. Для профилактики нейротоксического действия изониазида используются
а) антибиотики
б) витамины группы В
в) витамин С
г) диуретики
61. При применении стрептомицина медсестра должна следить за
а) диурезом
б) остротой слуха
в) остротой зрения
г) цветом кожи
62. Метод ранней диагностики туберкулеза
легких
Метод ранней диагностики туберкулеза
легких
а) бронхография
б) спирография
в) томография
г) флюорография
63. Специфическая профилактика туберкулеза
а) АКДС
б) БЦЖ
в) реакция Манту
г) реакция Пирке
64. Вакцина БЦЖ –это
а) анатоксин
б) комплекс противотуберкулёзных иммуноглобулинов
в) живая ослабленная вакцина
г) сывортка
65. Вакцинация БЦЖ проводится
а) на 3-5 день жизни
б) в 1 месяц
в) в 1 год
г) в 2 года
66. Место введения вакцины БЦЖ
а) верхняя треть плеча
б) верхняя треть предплечья
в) средняя треть плеча
г) средняя треть предплечья
67. Вакцина БЦЖ вводится
а) внутривенно
б) внутрикожно
в) внутримышечно
г) подкожно
68. Проба Манту используется для
Проба Манту используется для
а) диагностики рака легкого
б) диагностики туберкулеза
в) лечения рака легкого
г) лечения туберкулеза
69. Для проведения пробы Манту используют:
а) анатоксин
б) комплекс противотуберкулёзного иммуноглобулина
в) сыворотку
г) туберкулин
70. При проведении пробы Манту туберкулин вводят
а) внутривенно
б) внутрикожно
в) внутримышечно
г) подкожно
71. Проба Манту оценивается через (час.)
а) 12
б) 24
в) 36
г) 72
72. Проба Манту считается положительной при
а) инфильтрате размером 1 — 2 мм
б) инфильтрате размером 2 — 4 мм
в) инфильтрате размером 5 мм и более
г) отсутствии инфильтрата
73. Количество дней, в течение которых можно собирать мокроту для обнаружения микобактерий туберкулеза
а) 1
б) 2
в) 3
г) 4
74. Осложнение туберкулёза лёгких
Осложнение туберкулёза лёгких
а) острая коронарная недостаточность
б) острая сердечная недостаточность
в) острая почечная недостаточность
г) легочное кровотечение
75. При длительном применении антибиотиков у пациента могут развиться
а) отёки
б) лихорадка
в) дисбактериоз
г) увеличение массы тела
76. Неспецифические включения в мокроте при бронхиальной астме:
а) лейкоциты
б) эластические волокна
в) спирали Куршмана и кристаллы Шарко -Лейдена
г) атипичные клетки
77. Похудание, кровохарканье, боль в грудной клетке наблюдаются при
а) остром бронхите
б) бронхиальной астме
в) очаговой пневмонии
г) раке легкого
78. Фактор риска рака легкого
а) ожирение
б) переохлаждние
в) инфекция
г) курение
79. Решающее значение в диагностике рака
лёгкого имеет:
Решающее значение в диагностике рака
лёгкого имеет:
а) спирография
б) лабораторная диагностика
в) ЭКГ
г) рентгенография органов грудной клетки
80. Потенциальная проблема пациента при раке легкого
а) лихорадка
б) прибавка массы тела
в) головная боль
г) легочное кровотечение
81. Метод ранней диагностики рака легкого
а) бронхография
б) анализ крови
в) анализ мокроты
г) флюорография
82. При раке легкого в мокроте определяются
а) атипичные клетки
б) микобактерии
в) пневмококки
г) эозинофилы
83. Осложнение рака легкого
а) бронхиальная астма
б) хронический бронхит
в) эмфизема легких
г) экссудативный плеврит
84. При легочном кровотечении характерна мокрота:
а) алая, пенистая
б) темная, со сгустками
в) цвета «кофейной гущи»
г) вязкая, стеклвидная
85. Независимое сестринское вмешательство
при легочном кровотечении
Независимое сестринское вмешательство
при легочном кровотечении
а) введение хлорида кальция внутривенно
б) введение аминокапроновой кислоты
в) тепло на грудную клетку
г) холод на грудную клетку
86. Зависимое сестринское вмешательство при легочном кровотечении
а) введение хлорида кальция внутривенно
б) введение гепарина
в) банки на грудную клетку
г) горчичники на грудную клетку
87. Заболевание, которое может осложниться плевритом
а) бронхит
б) бронхиальная астма
в) рак легкого
г) эмфизема легких
88. Основной симптом при сухом плеврите
а) одышка
б) слабость
в) лихорадка
г) боль в грудной клетке
89. Основной симптом экссудативного плеврита
а) боль в грудной клетке
б) слабость
в) кровохарканье
г) нарастающая одышка
90. Пациент занимает вынужденное положение
лежа на больной стороне при
Пациент занимает вынужденное положение
лежа на больной стороне при
а) бронхите
б) бронхиальной астме
в) бронхоэктатической болезни
г) сухом плеврите
91. Зависимое сестринское вмешательство при сухом плеврите – это применение
а) анальгетиков
б) спазмолитиков
в) нитратов
г) цитостатиков
92. Скопление воспалительной жидкости в полости плевры наблюдается при
а) бронхите
б) бронхиальной астме
в) экссудативном плеврите
г) эмфиземе легких
93. Для плевральной пункции м/сестра готовит:
а) иглу длинной 10-15 см
б) иглу Дюфо
в) иглу Кассирского
г) троакар
94. Плевральную пункцию с лечебной целью проводят при
а) бронхиальной астме
б) крупозной пневмонии
в) хроническом бронхите
г) экссудативном плеврите
95. Подготовка пациента к плевральной
пункции
Подготовка пациента к плевральной
пункции
а) поставить очистительную клизму
б) промыть желудок
в) опорожнить мочевой пузырь
г) разъяснить сущность манипуляции
96. При проведении плевральной пункции врачом одномоментно извлекается жидкости не более: (в литрах)
а) 0,5
б) 1-1,5
в) 3
г) 5
97. Повышенная воздушность легких — это
а) гидроторакс
б) гемоторакс
в) пневмосклероз
г) эмфизема
98. Основной симптом эмфиземы легких
а) боль в грудной клетке
б) влажный кашель
в) кровохарканье
г) одышка
99. Форма грудной клетки при эмфиземе легких
а) астеническая
б) гиперстеническая
в) нормостеническая
г) бочкообразная
100. Основные симптомы крупозной пневмонии
а) слабость, головная боль, стекловидная мокрота
б) боль в грудной клетке, одышка, лихорадка
в) длительный субфебрилитет, утомляемость
г) отеки, повышение АД, нарушение ритма
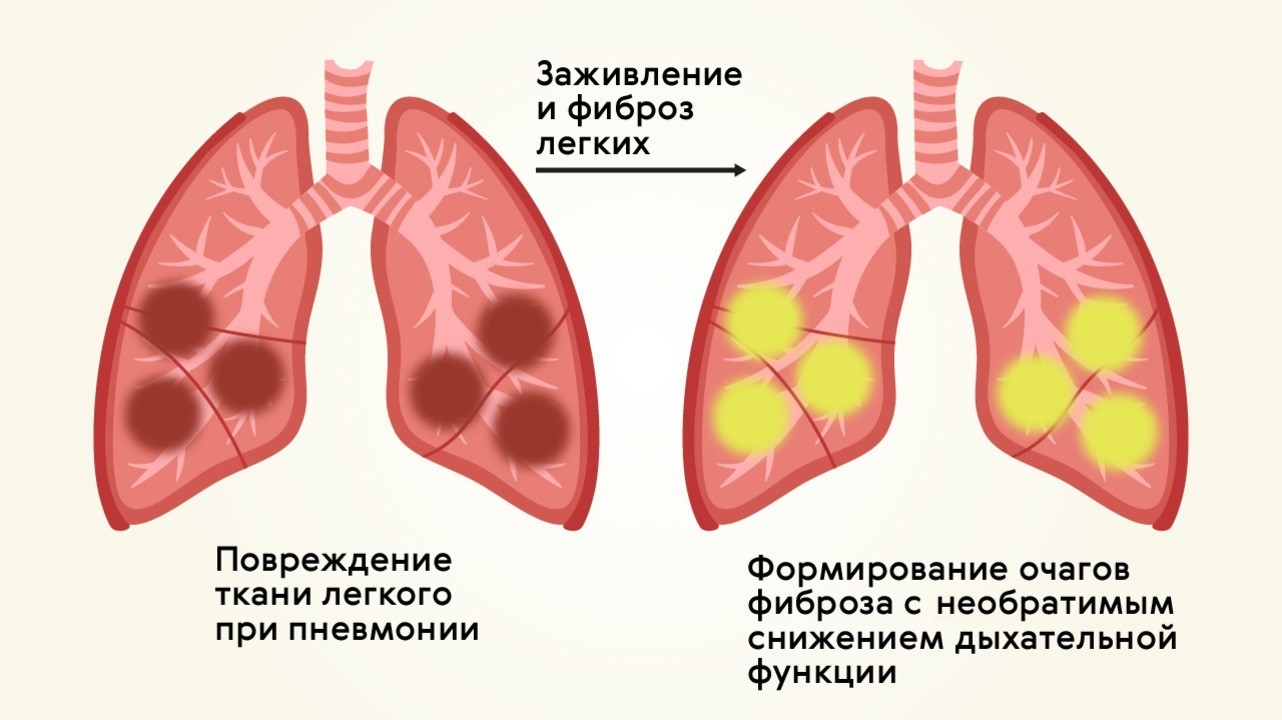
Когда «заклинивают» ворота в легкие / Здоровье / Независимая газета
Для определения степени распространенности бронхоэктаза используют компьютерную томографию.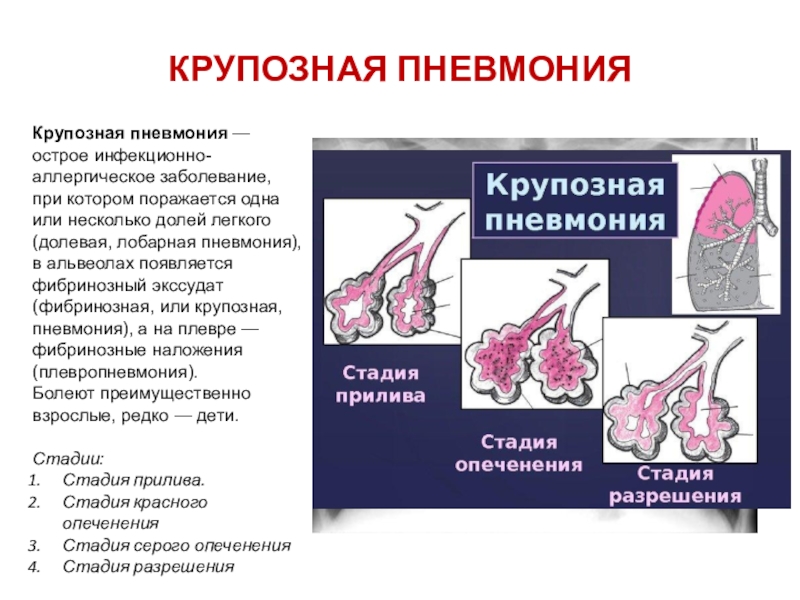 Фото агентства «Москва»
Фото агентства «Москва»
Более 200 лет назад выдающийся французский врач и анатом Рене Лаэннек изобрел знаменитый стетоскоп, которым широко пользовались врачи в XIX и долгое время в XX веке. С помощью этого простейшего приспособления, призванного выслушивать звуковые явления при различных заболеваниях, Лаэннек впервые открыл и описал в 1819 году недуг, поражающий бронхи.
Сегодня по международной классификации он называется бронхоэктатической болезнью. Ею страдает около 1,5% населения Земли. Она характеризуется хроническим гнойным процессом в бронхах и развивается, как правило, на фоне бронхоэктазов. Что это такое?
Бронхоэктазы появляются вследствие расширения отдельных участков бронхов иногда в два и более раз. Это нередко происходит в результате врожденной слабости их стенок или, например, из-за того, что у человека не до конца вылечена пневмония. Это патологическое расширение негативно отражается на механических свойствах дыхательных путей, снижая их тонус и эластичность. Оно часто вызывает воспаление, отеки, застойные явления в пораженных бронхах и приводит к развитию бронхоэктатической болезни. У взрослых она встречается преимущественно у мужчин молодого трудоспособного возраста. А у детей этот недуг – зачастую следствие перенесенных пневмонии или бронхита, но порой бывает и врожденным.
Оно часто вызывает воспаление, отеки, застойные явления в пораженных бронхах и приводит к развитию бронхоэктатической болезни. У взрослых она встречается преимущественно у мужчин молодого трудоспособного возраста. А у детей этот недуг – зачастую следствие перенесенных пневмонии или бронхита, но порой бывает и врожденным.
Основной симптом заболевания – кашель с выделением большого количества гнойной мокроты. Иногда он сопровождается кровохарканьем, особенно в период обострения. При легкой форме бронхоэктатической болезни кашель продолжается 1–2 недели, а при тяжелой – длится месяцами. В случае длительного течения развивается эмфизема легких (растяжение органа воздухом), прогрессирует дыхательная недостаточность, которая со временем осложняется сердечно-сосудистой недостаточностью. У больного наблюдаются общая слабость, одышка, боли в груди, периодическое повышение температуры, отсутствие аппетита, раздражительность, нарушения сна. Для бронхоэктатической болезни характерен также такой внешний признак, как утолщение кончиков пальцев больного типа «барабанных палочек».
При появлении кашля и других вышеперечисленных признаков необходимо без промедления обратиться к врачу – терапевту или пульмонологу. Диагностика заболевания включает анализы крови (общий и биохимический) и мочи, а также бактериологическое и цитологическое (клеточное) исследования мокроты больного. Проводятся также бронхоскопия (исследование бронхов с помощью специального эндоскопа) и биопсия – взятие небольшого объема содержимого бронхоэктаза с целью определения его чувствительности к антибактериальным препаратам. Еще один важный диагностический метод – бронхография (рентгенологическое исследование бронхов с помощью контрастного вещества). Для определения степени распространенности бронхоэктаза, его локализации и формы прибегают к компьютерной томографии.
Что касается лечения бронхоэктатической болезни, то в зависимости от состояния и возраста конкретного больного врачи могут выбрать консервативный или хирургический способ борьбы. Последний вариант заключается в удалении пораженных сегментов или целой доли легкого. Операция в большинстве случаев позволяет достичь практического излечения при одностороннем бронхоэктазе и хороших функциональных показателях легочной вентиляции.
Операция в большинстве случаев позволяет достичь практического излечения при одностороннем бронхоэктазе и хороших функциональных показателях легочной вентиляции.
Однако имеется ряд противопоказаний для хирургического вмешательства. Например, если у больного наблюдается выраженная дыхательная недостаточность или при начальных расширениях бронхов у детей, которые могут оказаться обратимыми. Поэтому врачи чаще прибегают к консервативному лечению, направленному в первую очередь на устранение причины недуга, в частности инфекции.
При этом подчеркнем, что антибактериальная терапия, которая применяется для лечения, используется только после предварительного микробиологического анализа мокроты. Он предназначен для правильного выбора того или иного лекарства для конкретного больного. Еще один лечебный метод – бронхоскопический дренаж, который помогает улучшить отток жидкости из пораженных болезнью дыхательных путей. Для этого с помощью специального бронхоскопа (медицинского эндоскопа для визуального исследования трахеи и бронхов) проводят процедуру промывания бронхов и вводят в них необходимые лекарства.
С целью улучшения эвакуации мокроты больному назначаются также препараты, способствующие ее разжижению, и отхаркивающие средства, а также щелочное питье, массаж грудной клетки и дыхательная гимнастика. С целью стимуляции иммунобиологических механизмов организма лечащий врач нередко назначает витаминные чаи, рекомендует сбалансированное, богатое белками и витаминами питание и соблюдение необходимого для скорейшего выздоровления режима дня.
Типичная бактериальная пневмония — StatPearls
Непрерывное обучение
Тяжелая форма острой инфекции нижних дыхательных путей, поражающая легочную паренхиму в одном или обоих легких, известна как пневмония. Это распространенное заболевание и потенциально серьезное инфекционное заболевание со значительной заболеваемостью и смертностью. Пневмония является шестой ведущей причиной смерти и единственным инфекционным заболеванием в десятке основных причин смерти в Соединенных Штатах. Внебольничная пневмония диагностируется у негоспитализированных или ранее амбулаторных больных в течение 48 ч после поступления в стационар. ВП подразделяют на «типичные» и «атипичные». ГП развивается более чем через 48 часов после госпитализации. У пациентов, находящихся на искусственной вентиляции легких более 48 часов после эндотрахеальной интубации, может развиться пневмония, известная как ВАП. HCAP возникает у амбулаторных пациентов, которые не были госпитализированы и имели обширный контакт с врачом в течение последних 3 месяцев. В этом упражнении рассматривается оценка и лечение типичной внебольничной пневмонии и подчеркивается роль членов межпрофессиональной бригады в сотрудничестве для обеспечения хорошо скоординированного ухода и улучшения результатов лечения пациентов.
ВП подразделяют на «типичные» и «атипичные». ГП развивается более чем через 48 часов после госпитализации. У пациентов, находящихся на искусственной вентиляции легких более 48 часов после эндотрахеальной интубации, может развиться пневмония, известная как ВАП. HCAP возникает у амбулаторных пациентов, которые не были госпитализированы и имели обширный контакт с врачом в течение последних 3 месяцев. В этом упражнении рассматривается оценка и лечение типичной внебольничной пневмонии и подчеркивается роль членов межпрофессиональной бригады в сотрудничестве для обеспечения хорошо скоординированного ухода и улучшения результатов лечения пациентов.
Цели:
Объясните причины Типичная внебольничная пневмония.
Опишите обследование пациента с типичной внебольничной пневмонией.
Обобщите варианты лечения типичной внебольничной пневмонии.
Изучение способов улучшения координации помощи между членами межпрофессиональной бригады с целью улучшения результатов лечения пациентов с типичной внебольничной пневмонией.

Получите доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Тяжелая форма острой инфекции нижних дыхательных путей, поражающая легочную паренхиму в одном или обоих легких, известна как пневмония. Это распространенное заболевание и потенциально серьезное инфекционное заболевание со значительной заболеваемостью и смертностью. Пневмония является шестой ведущей причиной смерти и единственным инфекционным заболеванием в десятке основных причин смерти в Соединенных Штатах.
Пневмонию можно разделить на 2 типа в зависимости от способа заражения:
Внебольничная пневмония (ВП): наиболее распространенный тип
Внутрибольничная пневмония (HAP Внебольничная пневмония ранее амбулаторный больной в течение 48 часов после поступления в больница. ВП подразделяют на «типичные» и «атипичные».
ГП развивается более чем через 48 часов после госпитализации.
 У пациентов, находящихся на искусственной вентиляции легких более 48 часов после эндотрахеальной интубации, может развиться пневмония, известная как ВАП. HCAP возникает у амбулаторных пациентов, которые не были госпитализированы и имели обширный контакт с врачом в течение последних 3 месяцев.
У пациентов, находящихся на искусственной вентиляции легких более 48 часов после эндотрахеальной интубации, может развиться пневмония, известная как ВАП. HCAP возникает у амбулаторных пациентов, которые не были госпитализированы и имели обширный контакт с врачом в течение последних 3 месяцев.Этиология
Пневмония возникает вторично по отношению к инфекциям, передающимся воздушно-капельным путем, включая бактерии, вирусы, грибки, паразиты и другие.
Типичными бактериями, вызывающими пневмонию, являются S Treptococcus pneumoniae , Staphylococcus aureus , группа A Streptococcus , Klebsiella pneumoniae , Haemophilus influenzae , Moraxella catarrhali s, анаэробы и грамотрицательные микроорганизмы. Эти организмы можно легко культивировать на стандартных средах или увидеть при окрашивании по Граму, в отличие от атипичных организмов.
Streptococcus pneumoniae является наиболее часто выявляемой бактериальной причиной ВП во всех возрастных группах во всем мире.
 Метициллин-резистентный Staphylococcus aureu s (MRSA), Escherichia coli и другие Enterobacteriaceae являются преобладающими причинами HAP, VAP и HCAP.
Метициллин-резистентный Staphylococcus aureu s (MRSA), Escherichia coli и другие Enterobacteriaceae являются преобладающими причинами HAP, VAP и HCAP.Хотя нет необходимости иметь предрасполагающее состояние к заболеванию пневмонией, наличие таких факторов делает человека более склонным к развитию легочной инфекции. Любое состояние или заболевание, которое ослабляет иммунный ответ хозяина, например, пожилой возраст (старше 65 лет), иммуносупрессия, диабет, муковисцидоз, рак легких и т. д. Состояния, повышающие риск макро- или микроаспирации, включают инсульт, судороги, анестезию, лекарственную интоксикацию. Курение сигарет, алкоголизм, недоедание, закупорка бронхов опухолями — другие распространенные предрасполагающие состояния.
Эпидемиология
Общая частота ВП составляет 5-7 на 1000 человек в год. Частота ВП выше у мужчин и увеличивается с возрастом. Чаще наблюдается в зимние месяцы. Сочетание пневмонии и гриппа вызывает высокую смертность и было восьмой по частоте причиной смерти в США и седьмой по частоте причиной смерти в Канаде в 2005 году.

Патофизиология
Легочная система и дыхательные пути постоянно подвергаются веществ и патогенов окружающей среды. Здоровые дыхательные пути обычно содержат некоторые виды бактерий и не стерильны. Наиболее распространенный механизм, посредством которого микроорганизмы или патогены достигают легких, известен как микроаспирация. Другими механизмами являются гематогенное распространение и макроаспирация.
Однако механизмы защиты легких, такие как кашлевой рефлекс, система мукоцилиарного клиренса, иммунный ответ, помогают поддерживать низкий уровень микробиома. ВП возникает, когда имеется дефект в нормальной защите хозяина, или вирулентный патоген подавляет иммунный ответ, или большой инфекционный микробный инокулят. Вторжение и размножение этих вирулентных штаммов бактерий в паренхиме легкого после микроаспирации вызывает активацию иммунного ответа хозяина, что приводит к каскаду воспалительной реакции, вызывающей пневмонию.
Альвеолярные макрофаги являются преобладающей иммунной клеткой, которая реагирует на бактерии нижних дыхательных путей.
 Однако более сильный иммунный ответ вступает в игру, когда подавляющий вирулентный патоген или большой инокулят заставляет эти альвеолярные макрофаги привлекать полиморфноядерные нейтрофилы (PMN) для фагоцитоза и поглощения этих бактерий. Альвеолярные макрофаги выделяют цитокины, а именно фактор некроза опухоли-альфа и интерлейкины. Интерлейкин-8 и гранулоцитарный колониестимулирующий фактор способствуют хемотаксису и созреванию нейтрофилов. Утечка альвеолярно-капиллярной мембраны из-за цитокинов может привести к снижению растяжимости и, следовательно, к одышке. Цитокины, такие как IL-1 и TNF, могут вызывать конституциональные симптомы, такие как лихорадка. Бактериальная пневмония является результатом этой воспалительной реакции. Эти цитокины необходимы для иммунитета, но их избыток может привести к сепсису и полиорганной недостаточности. Организм пытается сбалансировать пагубные эффекты цитокинов за счет ослабления нескольких воспалительных механизмов с помощью IL-10.
Однако более сильный иммунный ответ вступает в игру, когда подавляющий вирулентный патоген или большой инокулят заставляет эти альвеолярные макрофаги привлекать полиморфноядерные нейтрофилы (PMN) для фагоцитоза и поглощения этих бактерий. Альвеолярные макрофаги выделяют цитокины, а именно фактор некроза опухоли-альфа и интерлейкины. Интерлейкин-8 и гранулоцитарный колониестимулирующий фактор способствуют хемотаксису и созреванию нейтрофилов. Утечка альвеолярно-капиллярной мембраны из-за цитокинов может привести к снижению растяжимости и, следовательно, к одышке. Цитокины, такие как IL-1 и TNF, могут вызывать конституциональные симптомы, такие как лихорадка. Бактериальная пневмония является результатом этой воспалительной реакции. Эти цитокины необходимы для иммунитета, но их избыток может привести к сепсису и полиорганной недостаточности. Организм пытается сбалансировать пагубные эффекты цитокинов за счет ослабления нескольких воспалительных механизмов с помощью IL-10.Факторы микробной вирулентности и предрасполагающие условия хозяина делают человека более уязвимым к пневмонии.
 [3]
[3]Гистопатология
В зависимости от пораженной области легкого гистологически пневмонию можно разделить на дольковую, крупозную, бронхопневмонию и интерстициальную. К основным типам острой бактериальной пневмонии относятся:
Бронхопневмония: Нисходящая инфекция начинается вокруг бронхов и бронхиол, которая затем распространяется локально в легкие. Обычно поражаются нижние доли. Очаговые участки консолидации, которые представляют собой скопление нейтрофилов в альвеолах и бронхах.
Крупозная пневмония: Острое экссудативное воспаление всей доли. Равномерное уплотнение с полным или почти полным уплотнением доли легкого. Большинство этих случаев вызваны Streptococcus pneumoniae.
Крупозная пневмония имеет 4 классические стадии воспалительной реакции, если ее не лечить, а именно:
Застой/консолидация в первые 24 часа, когда легкие тяжелые, красные и заболоченные. Микроскопически характеризуется набуханием сосудов и внутриальвеолярным отеком.
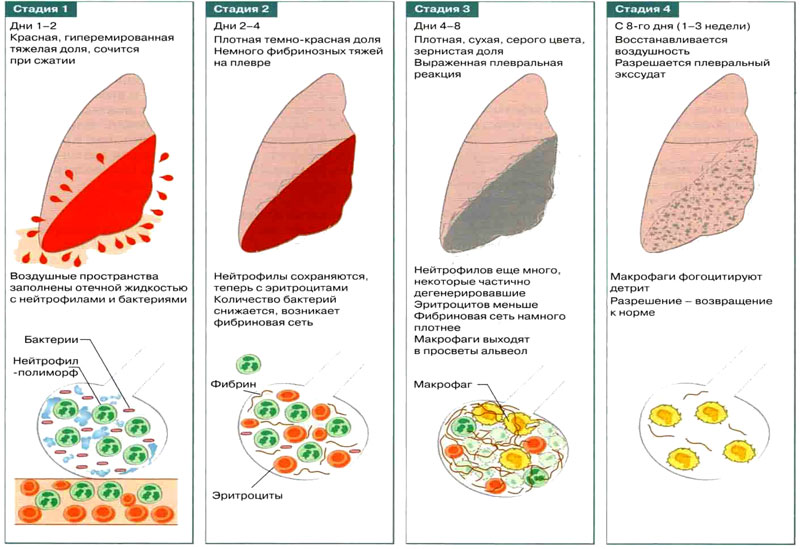 Присутствует много бактерий и мало нейтрофилов.
Присутствует много бактерий и мало нейтрофилов.Красное опеченение/ранняя консолидация начинается через 2-3 дня после консолидации и длится 2-4 дня и названа из-за твердой печеночной консистенции. Пораженное легкое красно-розовое, сухое, зернистое, безвоздушное. Нити фибрина замещают отек жидкости предыдущей фазы. Видны микроскопически отмеченный клеточный экссудат нейтрофилов, некоторые из которых показывают проглоченные бактерии, экстравазацию эритроцитов, слущенные эпителиальные клетки и фибрин в альвеолах. Альвеолярные перегородки становятся менее заметными из-за экссудата.
Серое опеченение/поздняя консолидация возникает через 2–3 дня после красного опеченения и длится от 4 до 8 дней. Легкие выглядят серыми с печеночной консистенцией из-за фибринозно-гнойного экссудата, прогрессирующего распада эритроцитов и гемосидерина. Макрофаги начинают появляться.
Рассасывание и восстановление легочной архитектуры начинается на восьмой день.
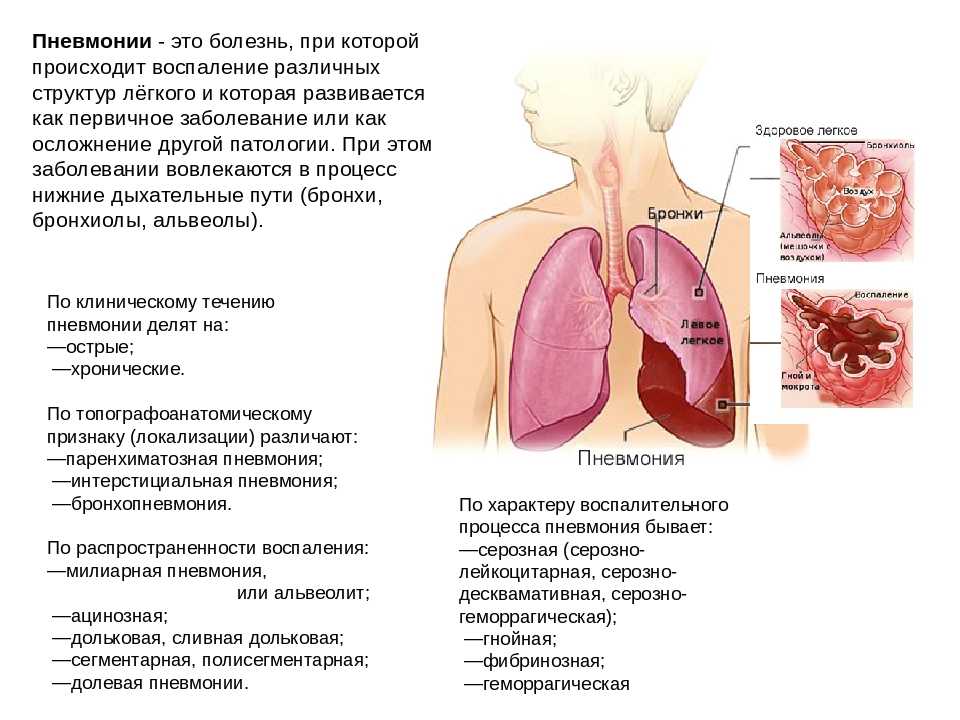 Ферментативное действие начинается в центре и распространяется по периферии, что приводит к разжижению прежнего твердого фибринозного содержимого и, в конечном счете, к восстановлению аэрации. Макрофаги являются преобладающими клетками, которые содержат поглощенные нейтрофилы и дебрис.
Ферментативное действие начинается в центре и распространяется по периферии, что приводит к разжижению прежнего твердого фибринозного содержимого и, в конечном счете, к восстановлению аэрации. Макрофаги являются преобладающими клетками, которые содержат поглощенные нейтрофилы и дебрис.
Токсикокинетика
Наиболее частой причиной типичной бактериальной пневмонии во всем мире является Pneumococcus . Полисахаридная капсула Streptococcus pneumoniae ингибирует связывание комплемента с клеточной поверхностью и, следовательно, ингибирует фагоцитоз. Вирулентные пневмококковые белки, такие как протеаза IgA1, нейраминидаза, пневмолизин, аутолизин и поверхностный белок А, дополнительно помогают организму противодействовать иммунному ответу хозяина и позволяют ему вызывать инфекцию у людей.
Генетические мутации, вызывающие активный отток лекарственного средства и, в конечном итоге, резистентность, привели к увеличению количества лекарственно-устойчивых Streptococcus Pneumoniae (DRSP) за последние несколько лет.

Изменение в пенициллин-связывающем белке увеличило резистентность к пенициллину и увеличило число резистентных к пенициллину S. pneumoniae . Резистентность к пенициллину возникает из-за невозможности связывания с клеточной стенкой микроба.[1][2]
Анамнез и физикальное исследование
Признаки и симптомы варьируют в зависимости от тяжести заболевания. Общие симптомы бактериальной пневмонии включают лихорадку, кашель, выделение мокроты (может отсутствовать). Цвет и качество мокроты указывают на микробиологическую этиологию. Бактериальная пневмония чаще всего проявляется слизисто-гнойной мокротой.
Плевритическая боль в груди из-за локализованного воспаления плевры может наблюдаться при любом виде пневмонии, но чаще встречается при крупозной пневмонии. Также могут наблюдаться конституциональные симптомы, такие как утомляемость, головная боль, миалгия и артралгия.
Тяжелая пневмония может привести к одышке и одышке. В тяжелых случаях также могут проявляться спутанность сознания, сепсис и полиорганная недостаточность.
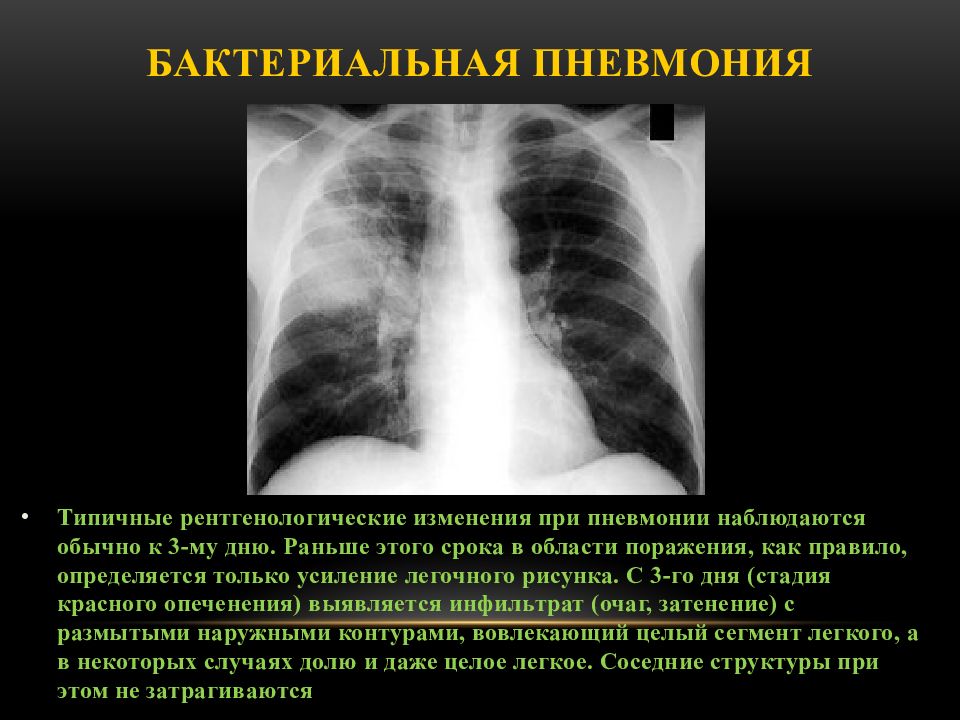
Тахипноэ, усиленное голосовое дрожание, эгофония (изменения от E до A), притупление перкуссии являются основными клиническими признаками в зависимости от степени консолидации и наличия/отсутствия плеврального выпота. При аускультации грудной клетки выявляют хрипы, хрипы, бронхиальное дыхание.
Частота дыхания тесно связана со степенью оксигенации и, следовательно, важна для определения тяжести. Гипоксия наблюдается при тяжелой пневмонии, что приводит к гипервентиляции.
Оценка
Чтобы начать с оценки любой пневмонии, клинические подозрения, основанные на тщательном изучении истории болезни и физическом осмотре, всегда должны сопровождаться рентгенографией грудной клетки, которая является наиболее важным первоначальным тестом.
Рентген грудной клетки не только показывает наличие заболевания и демонстрирует легочный инфильтрат, но также дает ключ к постановке диагноза, независимо от того, является ли он долевым, интерстициальным, односторонним или двусторонним.
 Типичная бактериальная пневмония обычно представляет собой крупозную пневмонию с парапневмоническими плевральными выпотами. Однако рентген грудной клетки не может надежно отличить бактериальную причину от небактериальной. Когда лабораторные и клинические признаки положительны, положительная рентгенограмма грудной клетки считается золотым стандартом диагностики пневмонии. Хотя компьютерная томография (КТ) является более надежным и точным тестом, ее использование ограничено из-за относительно высокой лучевой нагрузки и высокой стоимости. Иногда это можно сделать при выраженном клиническом синдроме, благоприятствующем пневмонии, с отрицательным результатом рентгенограммы грудной клетки. У госпитализированного пациента с высоким клиническим подозрением и отрицательной рентгенограммой следует начать эмпирическую презумптивную антибактериальную терапию с последующим повторным рентгенологическим исследованием органов грудной клетки через 24–48 часов.
Типичная бактериальная пневмония обычно представляет собой крупозную пневмонию с парапневмоническими плевральными выпотами. Однако рентген грудной клетки не может надежно отличить бактериальную причину от небактериальной. Когда лабораторные и клинические признаки положительны, положительная рентгенограмма грудной клетки считается золотым стандартом диагностики пневмонии. Хотя компьютерная томография (КТ) является более надежным и точным тестом, ее использование ограничено из-за относительно высокой лучевой нагрузки и высокой стоимости. Иногда это можно сделать при выраженном клиническом синдроме, благоприятствующем пневмонии, с отрицательным результатом рентгенограммы грудной клетки. У госпитализированного пациента с высоким клиническим подозрением и отрицательной рентгенограммой следует начать эмпирическую презумптивную антибактериальную терапию с последующим повторным рентгенологическим исследованием органов грудной клетки через 24–48 часов.Общий анализ крови (CBC) с дифференциацией, воспалительными биомаркерами СОЭ и реагентами острой фазы показан для подтверждения признаков воспаления и оценки тяжести.
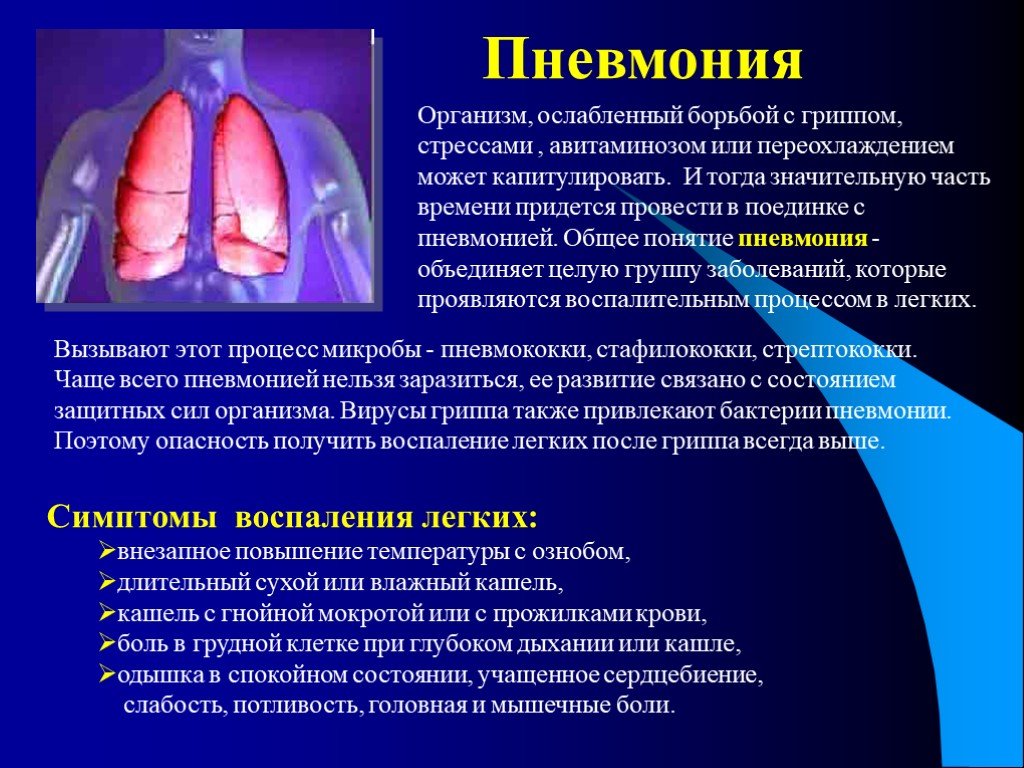 Лейкоцитоз со сдвигом влево является серьезной аномалией анализа крови, тогда как лейкопения может возникать и указывает на неблагоприятный прогноз.
Лейкоцитоз со сдвигом влево является серьезной аномалией анализа крови, тогда как лейкопения может возникать и указывает на неблагоприятный прогноз.Мокрота Окрашивание по Граму и посев должны быть выполнены следующим образом, если подозревается крупозная пневмония. Наиболее специфическим диагностическим тестом при крупозной пневмонии является посев мокроты. Очень важно выявить причину для правильного лечения.
Желательно проводить тест на грипп в зимние месяцы, так как сочетание гриппа и пневмонии приводит к летальному исходу.
CURB-65 и индекс тяжести пневмонии помогают стратифицировать пациентов и определить необходимость госпитализации для лечения.
Рутинные диагностические тесты необязательны для амбулаторных пациентов с пневмонией, но госпитализированные пациенты должны пройти посев мокроты, посев крови и/или определение антигена в моче предпочтительно до назначения антибиотикотерапии.
Торакоцентез, бронхоскопия, биопсия плевры или посев плевральной жидкости являются инвазивными тестами и проводятся очень редко.

Открытая биопсия легкого является окончательным специфическим диагностическим тестом.[6]
Лечение/управление
Лечение зависит от тяжести заболевания. Важно определить, нужно ли пациенту лечиться стационарно или амбулаторно. Шкала тяжести пневмонии CURB-65 или расширенная шкала CURB-65 могут использоваться для стратификации пациентов. По одному баллу за каждый фактор, который включает:
Спутанность сознания
Уремия (АМК более 20 мг/дл
Частота дыхания более 30 в минуту
Гипотензия (САД менее 90 и ДАД менее 60)
Возраст старше 65 лет
Пациенты с сопутствующими заболеваниями, такими как заболевания почек, печени, рак, хронические заболевания легких, обычно лучше переносят стационарное лечение внутривенными препаратами
Оценка по шкале CURB-65, превышающая или равная 2, является показанием для госпитализации. Оценка выше или равная 4 является показанием для госпитализации в отделение интенсивной терапии (ОИТ) и более интенсивной терапии.
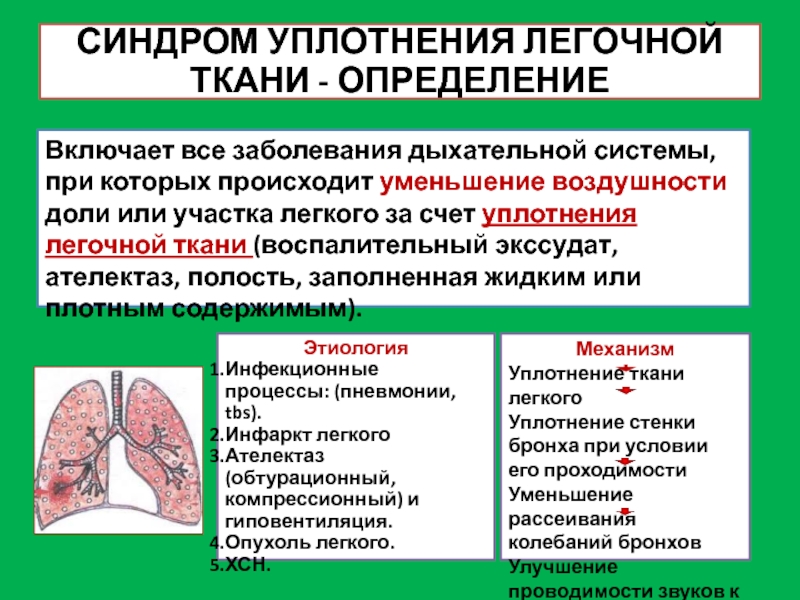
В зависимости от клинического ответа терапия показана в течение 5–7 дней. Благоприятным клиническим ответом является разрешение тахипноэ, тахикардии, гипотензии; отсутствие лихорадки более 48 часов. В случае отсроченного ответа терапию следует продлить.
Эмпирическая терапия рекомендуется для следующих :
Амбулаторное/негоспитализированное ведение пациентов: Эмпирическая терапия почти всегда успешна, и обычно тестирование не требуется. У пациентов без сопутствующих заболеваний монотерапия макролидами, такими как азитромицин и кларитромицин, является первым выбором. В качестве альтернативы можно использовать более новые фторхинолоны, такие как левофлоксацин, моксифлоксацин или гемифлоксацин. Терапия направлена против микоплазмы и хламидийной пневмонии, которые являются распространенными причинами менее тяжелой ВП. Пациенты с сопутствующими заболеваниями (хронические болезни легких или сердца, сахарный диабет, курение, ВИЧ и др.) хорошо себя чувствуют при монотерапии новыми фторхинолонами или в комбинации с бета-лактамом и макролидом.
Стационарное лечение вне отделений интенсивной терапии: Рекомендуемая терапия включает только новые фторхинолоны или комбинацию бета-лактамов/цефалоспоринов второго или третьего поколения и макролидов.
Стационарное лечение в отделении интенсивной терапии: Рекомендуемая терапия представляет собой комбинацию макролидов/новых фторхинолонов и бета-лактамов. У пациентов с риском аспирации можно использовать ампициллин-сульбактам или эртапенем. Если существует риск заражения Pseudomonas, показана комбинация бета-лактама против псевдомонадокса с фторхинолоном против псевдомонада. Для MRSA следует добавить ванкомицин или линезолид. В случае осложнений, таких как эмпиема, требуется дренирование плевральной полости. Хирургическая декортикация необходима в случае множественных локализаций.
Всех госпитализированных пациентов с положительным результатом теста на вирус гриппа следует лечить осельтамивиром независимо от начала заболевания.

После установления точной причины следует начать специфическую терапию.[3][4][5]
Дифференциальный диагноз
Астма или реактивное заболевание дыхательных путей
Вирусная пневмония
Пневмония, грибковая
9001 4Пневмония, атипичная бактериальная
Абсцесс легкого
Бронхоэктазы
Бронхиолит
Астма
9 0011
Острый и хронический бронхит
Ателектаз
Круп
Респираторный дистресс-синдром
- 900 04 Стремление инородного тела[6][7]
Плевральный выпот
Эмпиема
Абсцесс легкого
Септицемия
Бактериемия
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
- 1.
Yamaguchi M, Minamide Y, Terao Y, Isoda R, Ogawa T, Yokota S, Hamada S, Kawabata S. Nrc Streptococcus pneumoniae подавляет экспрессию капсулы и усиливает антифагоцитоз. Biochem Biophys Res Commun.
 2009 г., 04 декабря; 390 (1): 155–60. [PubMed: 19799870]
2009 г., 04 декабря; 390 (1): 155–60. [PubMed: 19799870]- 2.
Cools F, Torfs E, Vanhoutte B, de Macedo MB, Bonofillio L, Mollerach M, Maes L, Caljon G, Delputte P, Cappoen D, Cos P. Streptococcus pneumoniae galU генная мутация оказывает прямое влияние на рост биопленки, адгезию и фагоцитоз in vitro и патогенность in vivo. Патог Дис. 2018 01 октября; 76 (7) [PubMed: 30215741]
- 3.
Segreti J, House HR, Siegel RE. Принципы антибактериальной терапии внебольничной пневмонии в амбулаторных условиях. Am J Med. 2005 июль; 118 Приложение 7A: 21S-28S. [PubMed: 15993674]
- 4.
Пинеда Л., Эль Солх А.А. Тяжелая внебольничная пневмония: подход к терапии. Эксперт Опин Фармаколог. 2007 Апрель; 8 (5): 593-606. [PubMed: 17376015]
- 5.
Liu JL, Xu F, Zhou H, Wu XJ, Shi LX, Lu RQ, Farcomeni A, Venditti M, Zhao YL, Luo SY, Dong XJ, Falcone M. Исправление : Расширенный CURB-65: новая система оценки позволяет прогнозировать тяжесть внебольничной пневмонии с превосходной эффективностью.
 Научный представитель, 9 августа 2018 г.;8:47005. [Бесплатная статья PMC: PMC6083369] [PubMed: 30091425]
Научный представитель, 9 августа 2018 г.;8:47005. [Бесплатная статья PMC: PMC6083369] [PubMed: 30091425]- 6.
Hauswaldt J, Blaschke S. [Одышка]. Терапевт (Берл). 2017 сен; 58 (9): 925-936. [PubMed: 28608125]
- 7.
Berliner D, Schneider N, Welte T, Bauersachs J. Дифференциальный диагноз одышки. Dtsch Arztebl Int. 2016 09 декабря; 113 (49): 834-845. [Бесплатная статья PMC: PMC5247680] [PubMed: 28098068]
Осложнения
Усиление бригады здравоохранения Исходы
Пневмония — распространенное инфекционное заболевание легких. Это требует межпрофессиональной заботы и участия более чем одной узкой специальности. Этот подход, ориентированный на пациента , в котором участвуют врач с командой других специалистов в области здравоохранения, физиотерапевтов, респираторных терапевтов, медсестер, фармацевтов и групп поддержки, работающих вместе для пациента, играет важную роль в повышении качества лечения пациентов с пневмонией. Это не только снижает частоту госпитализаций, но и положительно влияет на исход заболевания. У здоровых пациентов результаты после лечения превосходны, но у пожилых людей и людей с сопутствующими заболеваниями результаты сомнительны.
Это требует межпрофессиональной заботы и участия более чем одной узкой специальности. Этот подход, ориентированный на пациента , в котором участвуют врач с командой других специалистов в области здравоохранения, физиотерапевтов, респираторных терапевтов, медсестер, фармацевтов и групп поддержки, работающих вместе для пациента, играет важную роль в повышении качества лечения пациентов с пневмонией. Это не только снижает частоту госпитализаций, но и положительно влияет на исход заболевания. У здоровых пациентов результаты после лечения превосходны, но у пожилых людей и людей с сопутствующими заболеваниями результаты сомнительны.
Контрольные вопросы
Рисунок
Абсцесс легкого, КТ, компьютерная томография, Толстостенное полостное образование в правом легком — абсцесс. Диффузные инфильтраты по типу матового стекла в обоих легких свидетельствуют о пневмонии. Предоставлено Wikimedia Commons, Йель Розен (CC by 2.0) https://creativecommons.org/licenses/by/2.0/ (подробнее…)
Предоставлено Wikimedia Commons, Йель Розен (CC by 2.0) https://creativecommons.org/licenses/by/2.0/ (подробнее…)
Рисунок
Комбинация двух рентгеновских снимков, A представляет собой нормальную здоровую рентгенографию грудной клетки, B представляет рентгенографию грудной клетки, документирующую Ку-лихорадочную пневмонию, патологию. Предоставлено Wikimedia Commons (Public Domain)
Рисунок
Рентгенограмма легких пациента, показывающая инфекцию pneumocystis carinii, пневмония. Предоставлено Национальным институтом здравоохранения (NIH)
Рисунок
MAI пневмония. Изображение предоставлено S Bhimji MD
Рисунок
Пример антибиотикограммы Streptococcus Pneumoniae. Предоставлено Закари Сэндманом, BA
Ссылки
Механизмы воспаления в легких
1. Oliveira ES, Hancock JT, Hermes-Lima M, et al. Последствия работы с переносимыми по воздуху веществами и активными формами кислорода: что могут сказать легкие млекопитающих, животные и растения. Интег Комп Биол. 2007; 47: 578–59.1. [PubMed] [Google Scholar]
2. Адлер К.Б., Фишер Б.М., Райт Д.Т., Кон Л.А., Беккер С. Взаимодействие между респираторными эпителиальными клетками и цитокинами: связь с воспалением легких. Энн Н.Ю. Академия наук. 1994; 725:128–145. [PubMed] [Google Scholar]
3. Kuroki Y, Takahashi M, Nishitani C. Легочные коллекторы во врожденном иммунитете легких. Клеточная микробиология. 2007; 9: 1871–1879. [PubMed] [Google Scholar]
Kuroki Y, Takahashi M, Nishitani C. Легочные коллекторы во врожденном иммунитете легких. Клеточная микробиология. 2007; 9: 1871–1879. [PubMed] [Google Scholar]
4. Kaisho T, Akira S. Функция Toll-подобных рецепторов и передача сигналов. J Аллергия Клин Иммунол. 2006;117:979–987. [PubMed] [Google Scholar]
5. Nittoh T, Fujimori H, Kozumi Y, Ishihara K, Mue S, Ohuchi K. Влияние глюкокортикоидов на апоптоз инфильтрированных эозинофилов и нейтрофилов у крыс. Евр Дж Фармакол. 1998; 354:73–81. [PubMed] [Google Scholar]
6. Фадок В.А., Браттон Д.Л., Коновал А., Фрид П.В., Весткотт Дж.Ю., Хенсон П.М. Макрофаги, поглотившие апоптотические клетки in vitro, ингибируют продукцию провоспалительных цитокинов за счет аутокринных/паракринных механизмов, включающих TGF-бета, PGE2 и PAF. Джей Клин Инвест. 1998;101:890–898. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Lipscomb MF, Bice DE, Lyons CR, Schuyler MR, Wilkes D. Регуляция легочного иммунитета. Ад Иммунол. 1995; 59: 369–455. [Бесплатная статья PMC] [PubMed] [Google Scholar]
1995; 59: 369–455. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Nakata K, Gotoh H, Watanabe J, et al. Повышенная пролиферация альвеолярных макрофагов человека после аллогенной трансплантации костного мозга. Кровь. 1999; 93: 667–673. [PubMed] [Google Scholar]
9. Bender AT, Ostenson CL, Wang EH, Beavo JA. Селективная активация PDE1B2 при дифференцировке моноцитов в макрофаги. Proc Natl Acad Sci U S A. 2005; 102:497–502. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Burns AR, Smith CW, Walker DC. Уникальные структурные особенности, влияющие на эмиграцию нейтрофилов в легкие. Physiol Rev. 2003; 83: 309–336. [PubMed] [Google Scholar]
11. Язданбахш М., Кремснер П.Г., ван Р.Р. Аллергия, паразиты и гигиеническая гипотеза. Наука. 2002; 296: 490–494. [PubMed] [Google Scholar]
12. Yokoyama WM. Иммунный ответ естественных клеток-киллеров. Иммунол Рез. 2005; 32: 317–325. [PubMed] [Академия Google]
13. Brigl M, Bry L, Kent SC, Gumperz JE, Brenner MB. Механизм CD1d-ограниченной активации Т-клеток естественных киллеров во время микробной инфекции. Нат Иммунол. 2003; 4: 1230–1237. [PubMed] [Google Scholar]
Механизм CD1d-ограниченной активации Т-клеток естественных киллеров во время микробной инфекции. Нат Иммунол. 2003; 4: 1230–1237. [PubMed] [Google Scholar]
14. Пруссин С., Меткалф Д.Д. 5. IgE, тучные клетки, базофилы и эозинофилы. J Аллергия Клин Иммунол. 2006; 117 (2 Suppl Mini-Primer): S450–456. [PubMed] [Google Scholar]
15. Kariyawasam HH, Robinson DS. Роль эозинофилов в ремоделировании тканей дыхательных путей при астме. Курр Опин Иммунол. 2007;19: 681–686. [PubMed] [Google Scholar]
16. Suratt BT, Parsons PE. Механизмы острого повреждения легких/острого респираторного дистресс-синдрома. Клин Грудь Med. 2006; 27: 579–589. [PubMed] [Google Scholar]
17. Тусси З., Хирш К.С., Гамильтон Б.Д., Кнут К.К., Фридлендер М.А., Рич Э.А. Снижение продукции TGF-бета 1 альвеолярными макрофагами человека по сравнению с моноцитами крови. Дж Иммунол. 1996; 156:3461–3468. [PubMed] [Google Scholar]
18. Moore SA, Strieter RM, Rolfe MW, Standiford TJ, Burdick MD, Kunkel SL. Экспрессия и регуляция антагониста рецептора интерлейкина-1, происходящего из альвеолярных макрофагов человека. Am J Respir Cell Mol Biol. 1992;6:569–575. [PubMed] [Google Scholar]
Экспрессия и регуляция антагониста рецептора интерлейкина-1, происходящего из альвеолярных макрофагов человека. Am J Respir Cell Mol Biol. 1992;6:569–575. [PubMed] [Google Scholar]
19. Дин Л., Линсли П.С., Хуанг Л.И., Жермен Р.Н., Шевач Э.М. IL-10 ингибирует костимулирующую активность макрофагов путем селективного ингибирования повышающей регуляции экспрессии B7. Дж Иммунол. 1993; 151:1224–1234. [PubMed] [Google Scholar]
20. Holgate ST. Патогенез астмы. Клин Эксперт Аллергия. 2008; 38: 872–897. [PubMed] [Google Scholar]
21. Sarir H, Henricks PA, van Houwelingen AH, Nijkamp FP, Folkerts G. Клетки, медиаторы и Toll-подобные рецепторы при ХОБЛ. Евр Дж Фармакол. 2008; 585: 346–353. [PubMed] [Академия Google]
22. Suter PM, Suter S, Girardin E, Roux-Lombard P, Grau GE, Dayer JM. Высокий бронхоальвеолярный уровень фактора некроза опухоли и его ингибиторов, интерлейкина-1, интерферона и эластазы у пациентов с респираторным дистресс-синдромом взрослых после травмы, шока или сепсиса. Ам преподобный Респир Дис. 1992; 145:1016–1022. [PubMed] [Google Scholar]
Ам преподобный Респир Дис. 1992; 145:1016–1022. [PubMed] [Google Scholar]
23. Армстронг Л., Миллар А.Б. Относительная продукция фактора некроза опухоли альфа и интерлейкина 10 при респираторном дистресс-синдроме взрослых. грудная клетка. 1997;52:442–446. [Бесплатная статья PMC] [PubMed] [Google Scholar]
24. Stockley RA. Легочные инфекции. 1. Роль бактерий в патогенезе и прогрессировании острой и хронической легочной инфекции. грудная клетка. 1998; 53: 58–62. [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Wilson R, Pitt T, Taylor G, et al. Пиоцианин и 1-гидроксифеназин, продуцируемые Pseudomonas aeruginosa, ингибируют биение дыхательных ресничек человека in vitro. Джей Клин Инвест. 1987; 79: 221–229. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Menendez R, Torres A. Неэффективность лечения внебольничной пневмонии. Грудь. 2007; 132:1348–1355. [PubMed] [Google Scholar]
27. Shaw MH, Reimer T, Kim YG, Nunez G. NOD-подобные рецепторы (NLR): добросовестные внутриклеточные микробные сенсоры. Курр Опин Иммунол. 2008; 20: 377–382. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Курр Опин Иммунол. 2008; 20: 377–382. [Бесплатная статья PMC] [PubMed] [Google Scholar]
28. Sutterwala FS, Ogura Y, Flavell RA. Инфламмасома в распознавании патогенов и воспалении. Дж. Лейкок Биол. 2007; 82: 259–264. [PubMed] [Академия Google]
29. Хайр О.А., Девалия Дж.Л., Абдельазиз М.М., Сапсфорд Р.Дж., Тарраф Х., Дэвис Р.Дж. Влияние эндотоксина Haemophilus influenzae на синтез IL-6, IL-8, TNF-альфа и экспрессию ICAM-1 в культивируемых бронхиальных эпителиальных клетках человека. Eur Respir J. 1994; 7: 2109–2116. [PubMed] [Google Scholar]
30. Wardlaw A. Адгезия лейкоцитов к эндотелию. Клин Эксперт Аллергия. 1990; 20: 619–626. [PubMed] [Google Scholar]
31. Takahashi GW, Andrews DF, III, Lilly MB, Singer JW, Alderson MR. Влияние гранулоцитарно-макрофагального колониестимулирующего фактора и интерлейкина-3 на продукцию интерлейкина-8 нейтрофилами и моноцитами человека. Кровь. 1993;81:357–364. [PubMed] [Google Scholar]
32. Nakamura H, Yoshimura K, McElvaney NG, Crystal RG. Эластаза нейтрофилов в жидкости, выстилающей респираторный эпителий, у людей с муковисцидозом индуцирует экспрессию гена интерлейкина-8 в клеточной линии бронхиального эпителия человека. Джей Клин Инвест. 1992; 89: 1478–1484. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Эластаза нейтрофилов в жидкости, выстилающей респираторный эпителий, у людей с муковисцидозом индуцирует экспрессию гена интерлейкина-8 в клеточной линии бронхиального эпителия человека. Джей Клин Инвест. 1992; 89: 1478–1484. [Бесплатная статья PMC] [PubMed] [Google Scholar]
33. Гордон С. Макрофаг: прошлое, настоящее и будущее. Евр Дж Иммунол. 2007; 37 (Приложение 1): S9–17. [PubMed] [Академия Google]
34. Мизгерд Дж.П. Острая инфекция нижних дыхательных путей. N Engl J Med. 2008; 358: 716–727. [Бесплатная статья PMC] [PubMed] [Google Scholar]
35. Matute-Bello G, Liles WC, Radella F, et al. Апоптоз нейтрофилов при остром респираторном дистресс-синдроме. Am J Respir Crit Care Med. 1997; 156:1969–1977. [PubMed] [Google Scholar]
36. Wang JP, Kurt-Jones EA, Finberg RW. Врожденный иммунитет к респираторным вирусам. Клеточная микробиология. 2007; 9: 1641–1646. [PubMed] [Google Scholar]
37. Вудленд Д.Л. Клеточный иммунитет к респираторным вирусным инфекциям. Курр Опин Иммунол. 2003; 15: 430–435. [PubMed] [Академия Google]
Курр Опин Иммунол. 2003; 15: 430–435. [PubMed] [Академия Google]
38. Coban C, Ishii KJ, Uematsu S, et al. Патологическая роль передачи сигналов Toll-подобных рецепторов при церебральной малярии. Инт Иммунол. 2007; 19: 67–79. [PubMed] [Google Scholar]
39. Kropf P, Freudenberg N, Kalis C, et al. Заражение мышей C57BL/10ScCr и C57BL/10ScNCr Leishmania major выявляет роль Toll-подобного рецептора 4 в контроле репликации паразита. Дж. Лейкок Биол. 2004; 76: 48–57. [PubMed] [Google Scholar]
40. Ршич-Арсениевич В., Дзамич А., Митрович С., Радонич И., Краничич-Зец И. Характеристики иммунного ответа при протозойных инфекциях. Мед Прегл. 2003; 56: 557–563. [PubMed] [Академия Google]
41. Лью Ф.Ю., О’Доннелл, Калифорния. Иммунология лейшманиоза. Ад Паразитол. 1993; 32: 161–259. [PubMed] [Google Scholar]
42. McGuinness DH, Dehal PK, Pleass RJ. Молекулы распознавания образов и врожденный иммунитет к паразитам. Тенденции Паразитол. 2003; 19: 312–319. [PubMed] [Google Scholar]
43. Anthony RM, Rutitzky LI, Urban JF, Jr, Stadecker MJ, Gause WC. Защитные иммунные механизмы при гельминтозах. Нат Рев Иммунол. 2007; 7: 975–987. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Anthony RM, Rutitzky LI, Urban JF, Jr, Stadecker MJ, Gause WC. Защитные иммунные механизмы при гельминтозах. Нат Рев Иммунол. 2007; 7: 975–987. [Бесплатная статья PMC] [PubMed] [Google Scholar]
44. Злотник А., Йоши О. Хемокины: новая система классификации и их роль в иммунитете. Иммунитет. 2000; 12: 121–127. [PubMed] [Google Scholar]
45. Frevert CW, Farone A, Danaee H, Paulauskis JD, Kobzik L. Функциональная характеристика крысиного хемокинового макрофагального воспалительного белка-2. Воспаление. 1995; 19: 133–142. [PubMed] [Google Scholar]
46. Tsai WC, Strieter RM, Mehrad B, Newstead MW, Zeng X, Standiford TJ. Хемокиновый рецептор CXC CXCR2 необходим для защитного врожденного ответа хозяина у мышей Pseudomonas aeruginosa пневмония. Заразить иммун. 2000;68:4289–4296. [Бесплатная статья PMC] [PubMed] [Google Scholar]
47. Barnes PJ, Shapiro SD, Pauwels RA. Хроническая обструктивная болезнь легких: молекулярные и клеточные механизмы. Eur Respir J. 2003; 22: 672–688. [PubMed] [Google Scholar]
2003; 22: 672–688. [PubMed] [Google Scholar]
48. Fabbri LM, Romagnoli M, Corbetta L, et al. Различия в воспалении дыхательных путей у пациентов с фиксированной обструкцией дыхательных путей вследствие бронхиальной астмы или хронической обструктивной болезни легких. Am J Respir Crit Care Med. 2003; 167: 418–424. [PubMed] [Академия Google]
49. Vignola AM, Chanez P, Chiappara G, et al. Оценка апоптоза эозинофилов, макрофагов и Т-лимфоцитов в биоптатах слизистой оболочки больных астмой и хроническим бронхитом. J Аллергия Клин Иммунол. 1999; 103: 563–573. [PubMed] [Google Scholar]
50. Sutherland ER, Martin RJ. Воспаление дыхательных путей при хронической обструктивной болезни легких: сравнение с астмой. J Аллергия Клин Иммунол. 2003; 112: 819–827. [PubMed] [Google Scholar]
51. Di SA, Capelli A, Lusuardi M, et al. Тяжесть ограничения воздушного потока связана с тяжестью воспаления дыхательных путей у курильщиков. Am J Respir Crit Care Med. 1998;158:1277–1285. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
52. O’Shaughnessy TC, Ansari TW, Barnes NC, Jeffery PK. Воспаление в биоптатах бронхов у пациентов с хроническим бронхитом: обратная связь CD8+ Т-лимфоцитов с ОФВ 1 . Am J Respir Crit Care Med. 1997; 155: 852–857. [PubMed] [Google Scholar]
53. Силаси М., Долинай Т., Немес З., Штраус Дж. Патология хронической обструктивной болезни легких. Патол Онкол Рез. 2006; 12:52–60. [PubMed] [Академия Google]
54. Стритер Р.М., Кин М.П. Врожденный иммунитет диктует поляризацию цитокинов, имеющую отношение к развитию легочного фиброза. Джей Клин Инвест. 2004; 114: 165–168. [Бесплатная статья PMC] [PubMed] [Google Scholar]
55. Gerke AK, Hunninghake G. Иммунология саркоидоза. Клин Грудь Med. 2008; 29: 379–390. vii. [PubMed] [Google Scholar]
56. Hernandez C, Cetner AS, Jordan JE, Puangsuvan SN, Robinson JK. Туберкулез в эпоху биологической терапии. J Am Acad Дерматол. 2008; 59: 363–380. [PubMed] [Академия Google]
57. Хельмих Б., Чернок Э., Гросс В.Л. Провоспалительные цитокины и аутоиммунитет при синдроме Чарга-Стросса. Энн Н.Ю. Академия наук. 2005; 1051:121–131. [PubMed] [Google Scholar]
Хельмих Б., Чернок Э., Гросс В.Л. Провоспалительные цитокины и аутоиммунитет при синдроме Чарга-Стросса. Энн Н.Ю. Академия наук. 2005; 1051:121–131. [PubMed] [Google Scholar]
58. Nocentini G, Cuzzocrea S, Bianchini R, Mazzon E, Riccardi C. Модуляция острого и хронического воспаления легких с помощью GITR и его лиганда. Энн Н.Ю. Академия наук. 2007; 1107: 380–391. [PubMed] [Google Scholar]
59. Hayashi T, Beck L, Rossetto C, et al. Ингибирование экспериментальной астмы индоламин-2,3-диоксигеназой. Джей Клин Инвест. 2004; 114: 270–279.. [Бесплатная статья PMC] [PubMed] [Google Scholar]
60. Raychaudhuri B, Fisher CJ, Farver CF, et al. Опосредованное интерлейкином 10 (IL-10) ингибирование продукции воспалительных цитокинов альвеолярными макрофагами человека. Цитокин. 2000; 12:1348–1355. [PubMed] [Google Scholar]
61. Pittet JF, Griffiths MJ, Geiser T, et al. TGF-бета является важным медиатором острого повреждения легких. Джей Клин Инвест. 2001; 107:1537–1544. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
62. Otmishi P, Gordon J, El-Oshar S, et al. Нейроиммунное взаимодействие при воспалительных заболеваниях. Clin Med Circ Respir Pulm Med. 2008; 2:35–44. [Бесплатная статья PMC] [PubMed] [Google Scholar]
63. Лин С., Уокер Дж., Сюй Л., Гозал Д., Ю Дж. Дыхательная система: поведение сенсорных рецепторов легких при развитии острого повреждения легких у кролика. Опыт физиол. 2007; 92: 749–755. [PubMed] [Google Scholar]
64. Yu J, Lin S, Zhang J, Otmishi P, Guardiola JJ. Ноцицепторы дыхательных путей активируются провоспалительными цитокинами. Респир Физиол Нейробиол. 2007; 156: 116–119. [PubMed] [Google Scholar]
65. Трейси К.Дж. Воспалительный рефлекс. Природа. 2002; 420:853–859. [PubMed] [Академия Google]
66. Bozic CR, Lu B, Hopken UE, Gerard C, Gerard NP. Нейрогенное усиление воспаления иммунного комплекса. Наука. 1996; 273:1722–1725. [PubMed] [Google Scholar]
67. Veronesi B, Carter JD, Devlin RB, Simon SA, Oortgiesen M. Нейропептиды и капсаицин стимулируют высвобождение воспалительных цитокинов в клеточной линии бронхиального эпителия человека. Нейропептиды. 1999; 33: 447–456. [PubMed] [Google Scholar]
Нейропептиды и капсаицин стимулируют высвобождение воспалительных цитокинов в клеточной линии бронхиального эпителия человека. Нейропептиды. 1999; 33: 447–456. [PubMed] [Google Scholar]
68. Kohlmeier JE, Miller SC, Smith J, et al. Хемокиновый рецептор CCR5 играет ключевую роль в раннем ответе Т-клеток CD8+ памяти на респираторные вирусные инфекции. Иммунитет. 2008;29: 101–113. [Бесплатная статья PMC] [PubMed] [Google Scholar]
69. Guillot L, Le GR, Bloch S, et al. Участие толл-подобного рецептора 3 в иммунном ответе клеток эпителия легких на двухцепочечную РНК и вирус гриппа А. Дж. Биол. Хим. 2005; 280:5571–5580. [PubMed] [Google Scholar]
70. Diebold SS, Kaisho T, Hemmi H, Akira S, Reis e Sousa C. Врожденные противовирусные ответы с помощью TLR7-опосредованного распознавания одноцепочечной РНК. Наука. 2004; 303:1529–1531. [PubMed] [Академия Google]
71. Курт-Джонс Э.А., Попова Л., Квинн Л. и соавт. Рецепторы распознавания образов TLR4 и CD14 опосредуют ответ на респираторно-синцитиальный вирус. Нат Иммунол. 2000; 1: 398–401. [PubMed] [Google Scholar]
Нат Иммунол. 2000; 1: 398–401. [PubMed] [Google Scholar]
72. Nociari M, Ocheretina O, Schoggins JW, Falck-Pedersen E. Обнаружение инфекции аденовирусом: распознавание вирусной ДНК, независимое от Toll-подобного рецептора, сигнализирует об активации главного регулятора фактора 3 регуляции интерферона. Дж Вирол. 2007;81:4145–4157. [Бесплатная статья PMC] [PubMed] [Google Scholar]
73. Курт-Джонс Э.А., Чан М., Чжоу С. и др. Взаимодействие вируса простого герпеса 1 с Toll-подобным рецептором 2 способствует летальному энцефалиту. Proc Natl Acad Sci U S A. 2004; 101:1315–1320. [Бесплатная статья PMC] [PubMed] [Google Scholar]
74. Круг А., Лукер Г.Д., Барчет В., Лейб Д.А., Акира С., Колонна М. Вирус простого герпеса типа 1 активирует мышиные естественные клетки, продуцирующие интерферон, посредством толл-подобных рецептор 9. Кровь. 2004; 103:1433–1437. [PubMed] [Google Scholar]
75. Yoshimura A, Lien E, Ingalls RR, Tuomanen E, Dziarski R, Golenbock D. Передовой опыт: распознавание компонентов клеточной стенки грамположительных бактерий врожденной иммунной системой происходит через Toll- подобный рецептору 2. J Immunol. 1999;163:1–5. [PubMed] [Google Scholar]
J Immunol. 1999;163:1–5. [PubMed] [Google Scholar]
76. Zhang Z, Louboutin JP, Weiner DJ, Goldberg JB, Wilson JM. Эпителиальные клетки дыхательных путей человека воспринимают инфекцию Pseudomonas aeruginosa посредством распознавания флагеллина Toll-подобным рецептором 5. Infect Immun. 2005; 73: 7151–7160. [Бесплатная статья PMC] [PubMed] [Google Scholar]
77. Xu F, Droemann D, Rupp J, et al. Модуляция воспалительной реакции на S. pneumoniae в модели острой инфекции легочной ткани. Am J Respir Cell Mol Biol. 2008;39: 522–529. [PubMed] [Google Scholar]
78. Happel KI, Zheng M, Young E, et al. Передний край: роль Toll-подобного рецептора 4 и IL-23 в экспрессии IL-17 в ответ на инфекцию Klebsiella pneumoniae . Дж Иммунол. 2003; 170:4432–4436. [Бесплатная статья PMC] [PubMed] [Google Scholar]
79. Ye P, Rodriguez FH, Kanaly S, et al. Необходимость передачи сигналов рецептора интерлейкина 17 для экспрессии хемокинов CXC легких и гранулоцитарного колониестимулирующего фактора, рекрутирования нейтрофилов и защиты хозяина. J Эксперт Мед. 2001;194: 519–527. [Бесплатная статья PMC] [PubMed] [Google Scholar]
J Эксперт Мед. 2001;194: 519–527. [Бесплатная статья PMC] [PubMed] [Google Scholar]
80. Означает TK, Jones BW, Schromm AB, et al. Дифференциальные эффекты антагониста Toll-подобных рецепторов на реакции макрофагов, индуцированные Mycobacterium tuberculosis. Дж Иммунол. 2001; 166:4074–4082. [PubMed] [Google Scholar]
81. Весоски Б., Флаэрти Д.К., Тернер Дж. Цитокины Th2 облегчают опосредованную CD8-Т-клетками раннюю устойчивость к инфекции Mycobacterium tuberculosis у старых мышей. Заразить иммун. 2006; 74:3314–3324. [Бесплатная статья PMC] [PubMed] [Google Scholar]
82. Фишер Г.Б., Сарриа Э.Е., Лейте А.Дж., де Бритто М.С. Паразитарная инфекция легких и детские легкие. Pediatr Respir Respir. 2008; 9:57–65. [PubMed] [Google Scholar]
83. Рейес Дж. Л., Террасас Л. И. Различные роли альтернативно активированных макрофагов при гельминтозах. Иммунол от паразитов. 2007; 29: 609–619. [PubMed] [Google Scholar]
84. Kropf P, Freudenberg MA, Modolell M, et al. Толл-подобный рецептор 4 способствует эффективному контролю инфекции простейшим паразитом Leishmania major. Заразить иммун. 2004;72:1920–1928. [PMC free article] [PubMed] [Google Scholar]
Толл-подобный рецептор 4 способствует эффективному контролю инфекции простейшим паразитом Leishmania major. Заразить иммун. 2004;72:1920–1928. [PMC free article] [PubMed] [Google Scholar]
85. D’Ombrain MC, Hansen DS, Simpson KM, Schofield L. Гаммадельта-Т-клетки, экспрессирующие NK-рецепторы, преобладают над NK-клетками и обычными Т-клетками во врожденном IFN- гамма-ответ на малярию Plasmodium falciparum. Евр Дж Иммунол. 2007; 37: 1864–1873. [PubMed] [Google Scholar]
86. Ware LB, Matthay MA. Острый респираторный дистресс-синдром. N Engl J Med. 2000; 342:1334–1349. [PubMed] [Google Scholar]
87. Донг Л., Ван С., Чен М., Ли Х., Би В. Активация макрофагов и активация костимулирующей молекулы CD40 при остром повреждении легких, вызванном липополисахаридами. Дж. Биомед Биотехнолог. 2008; 2008:852571. [Бесплатная статья PMC] [PubMed] [Google Scholar]
88. Gropper MA, Wiener-Kronish J. Эпителий при остром повреждении легких/остром респираторном дистресс-синдроме.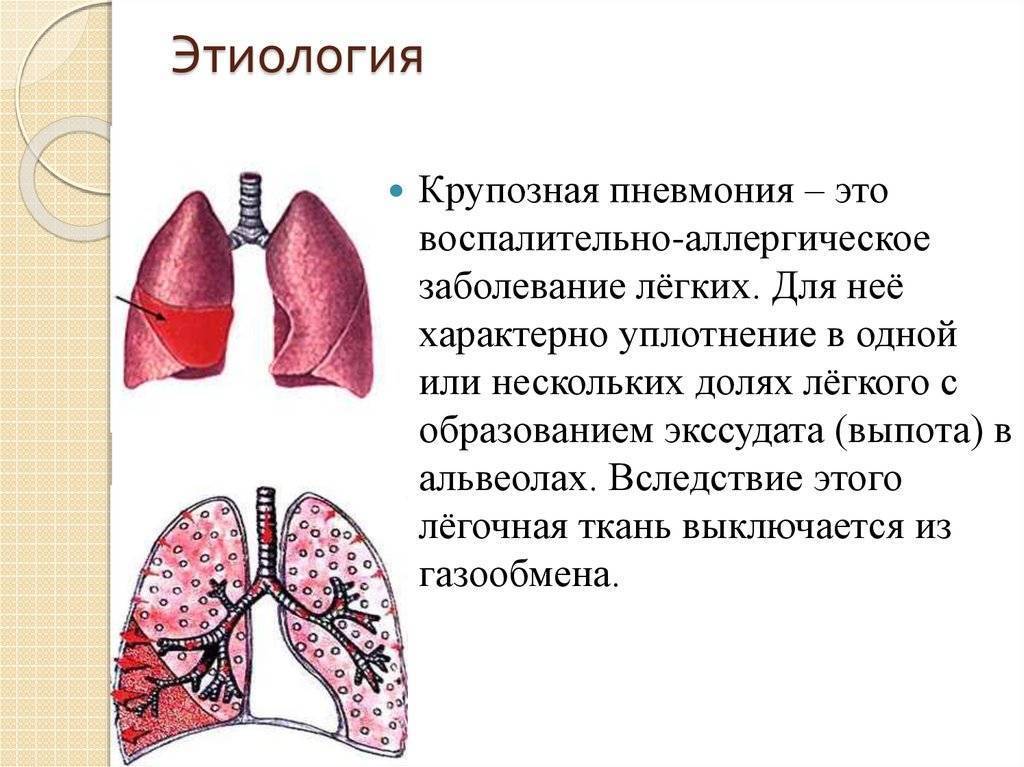 Curr Opin Crit Care. 2008; 14:11–15. [PubMed] [Google Scholar]
Curr Opin Crit Care. 2008; 14:11–15. [PubMed] [Google Scholar]
89. Luh SP, Chiang CH. Острое повреждение легких/острый респираторный дистресс-синдром (ALI/ARDS): механизм, существующие стратегии и будущие перспективы терапии. J Zhejiang Univ Sci B. 2007; 8: 60–69. [PMC free article] [PubMed] [Google Scholar]
90. Гроппер М.А., Винер-Крониш Дж. Эпителий при остром повреждении легких/остром респираторном дистресс-синдроме. Curr Opin Crit Care. 2008; 14:11–15. [PubMed] [Академия Google]
91. Segura-Valdez L, Pardo A, Gaxiola M, Uhal BD, Becerril C, Selman M. Активация желатиназ A и B, коллагеназ 1 и 2 и повышенная гибель паренхиматозных клеток при ХОБЛ. Грудь. 2000; 117: 684–694. [PubMed] [Google Scholar]
92. Канадзава Х., Асаи К., Хирата К., Йошикава Дж. Возможные эффекты фактора роста эндотелия сосудов в патогенезе хронической обструктивной болезни легких. Am J Med. 2003; 114: 354–358. [PubMed] [Google Scholar]
93. Шапиро С.Д. Протеолиз в легких. Eur Respir J Suppl. 2003;44:30с–2с. [PubMed] [Академия Google]
Eur Respir J Suppl. 2003;44:30с–2с. [PubMed] [Академия Google]
94. Грумелли С., Корри Д.Б., Сонг Л.З. и др. Иммунная основа деструкции паренхимы легких при хронической обструктивной болезни легких и эмфиземе легких. ПЛОС Мед. 2004;1:e8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
95. Шарафхане А., Ханания Н.А., Ким В. Патогенез эмфиземы: от скамейки к постели. Proc Am Thorac Soc. 2008; 5: 475–477. [Бесплатная статья PMC] [PubMed] [Google Scholar]
96. De Monchy JG, Kauffman HF, Venge P, et al. Бронхоальвеолярная эозинофилия при аллерген-индуцированных поздних астматических реакциях. Ам преподобный Респир Дис. 1985;131:373–376. [PubMed] [Google Scholar]
97. Bousquet J, Jeffery PK, Busse WW, Johnson M, Vignola AM. Астма. От бронхоконстрикции до воспаления и ремоделирования дыхательных путей. Am J Respir Crit Care Med. 2000; 161:1720–1745. [PubMed] [Google Scholar]
98. Koh YY, Dupuis R, Pollice M, Albertine KH, Fish JE, Peters SP. Нейтрофилы, рекрутированные в легкие человека при заражении сегментарным антигеном, демонстрируют сниженный хемотаксический ответ на лейкотриен B4.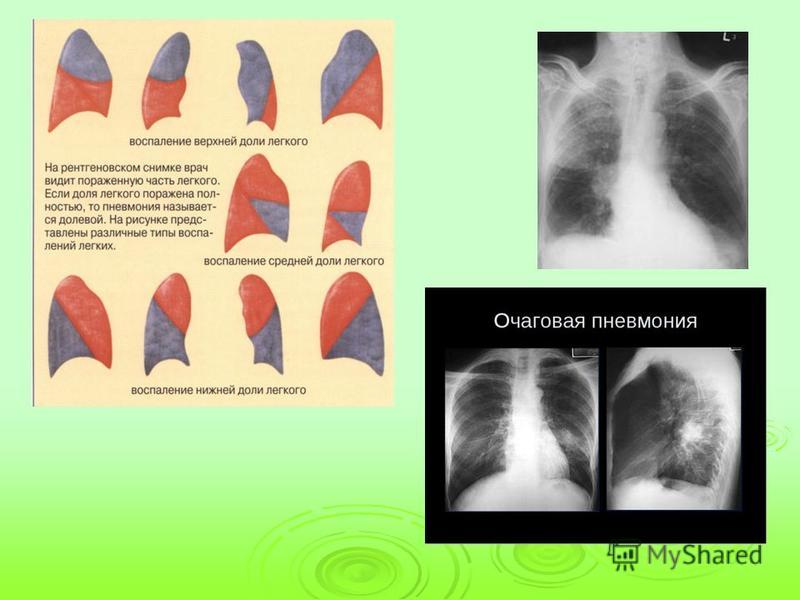 Am J Respir Cell Mol Biol. 1993;8:493–499. [PubMed] [Google Scholar]
Am J Respir Cell Mol Biol. 1993;8:493–499. [PubMed] [Google Scholar]
99. Doucet C, Brouty-Boye D, Pottin-Clemenceau C, Canonica GW, Jasmin C, Azzarone B. Интерлейкин (IL) 4 и IL-13 действуют на фибробласты легких человека. Влияние на астму. Джей Клин Инвест. 1998; 101:2129–2139. [Бесплатная статья PMC] [PubMed] [Google Scholar]
100. Robinson D, Hamid Q, Bentley A, Ying S, Kay AB, Durham SR. Активация CD4+ Т-клеток, увеличение экспрессии мРНК цитокинов Th3-типа и рекрутирование эозинофилов в бронхоальвеолярном лаваже после ингаляции аллергена у пациентов с атопической астмой. J Аллергия Клин Иммунол. 1993;92:313–324. [PubMed] [Google Scholar]
101. Guo CB, Liu MC, Galli SJ, Bochner BS, Kagey-Sobotka A, Lichtenstein LM. Идентификация IgE-содержащих клеток в поздней фазе ответа на антиген в легких в виде базофилов. Am J Respir Cell Mol Biol. 1994; 10: 384–390. [PubMed] [Google Scholar]
102. Hawrylowicz CM. Регуляторные Т-клетки и ИЛ-10 при аллергическом воспалении. J Эксперт Мед. 2005; 202:1459–1463. [PMC free article] [PubMed] [Google Scholar]
J Эксперт Мед. 2005; 202:1459–1463. [PMC free article] [PubMed] [Google Scholar]
103. Scherf W, Burdach S, Hansen G. Снижение экспрессии трансформирующего фактора роста бета 1 усугубляет патологию в экспериментальной модели астмы. Евр Дж Иммунол. 2005;35:198–206. [PubMed] [Google Scholar]
104. Schnyder-Candrian S, Togbe D, Couillin I, et al. Интерлейкин-17 является негативным регулятором установленной аллергической астмы. J Эксперт Мед. 2006; 203: 2715–2725. [Бесплатная статья PMC] [PubMed] [Google Scholar]
105. Willis BC, Liebler JM, Luby-Phelps K, et al. Индукция эпителиально-мезенхимального перехода в альвеолярных эпителиальных клетках с помощью трансформирующего фактора роста-бета1: возможная роль в идиопатическом легочном фиброзе. Ам Джей Патол. 2005; 166:1321–1332. [Бесплатная статья PMC] [PubMed] [Google Scholar]
106. Ноубл П.В., Гомер Р.Дж. Идиопатический легочный фиброз: новый взгляд на патогенез. Клин Грудь Med. 2004; 25: 749–758. vii. [PubMed] [Google Scholar]
107.
