Нет следа и рубца от бцж у ребенка — что это значит
Как должен выглядеть рубец после прививки БЦЖ? Когда он появляется? Какой должна быть правильная реакция организма? Что делать, если нет следа после поставленной вакцины? Эти вопросы волнуют мамочек, потому что формирование иммунитета от туберкулезной палочки имеет важное значение для ребенка.
Методика противотуберкулезного вакцинирования
Прививку БЦЖ ставят новорожденным в роддоме перед выпиской, если нет противопоказаний. Назначение данной прививки — формирование иммунитета против заболевания туберкулезом. Препарат вводят внутрикожно в левое плечо, соблюдая правила методики введения инъекций. В исключительных случаях вакцинируют не в область плеча, а в бедро.
Если ребенка не иммунизировали в роддоме, вакцинацию проводят в поликлинике под наблюдением лечащего педиатра. В иных случаях прививки БЦЖ можно ставить в домашних условиях при соответствующей оплате выезда бригады медиков.
После введения вакцины у ребенка образуется папула до 10 мм диаметром — белая и плоская.
Важно! Через три месяца образуется корочка в виде коросты, и ранка постепенно начинает заживать. Эти явления считаются нормой, и срывать корочку категорически запрещается. Также запрещается лечить корочку зеленкой!
Когда корочка отсохнет и отшелушится, на ее месте образуется характерный для БЦЖ рубец. У рубца может быть красноватый оттенок, а в диаметре он может быть 10 мм.
Если рубчика на месте введения вакцины нет, значит, прививка была неэффективной.
Многие родители пугаются, когда видят нагноение ранки, однако, такая реакция организма говорит о правильном процессе формирования иммунитета после прививки.
Нормальная реакция на вакцину
Какой должна быть правильная реакция на прививку? Перечислим признаки правильной реакции на препарат вакцины БЦЖ:
- образование плоской белой папулы сразу после прививки;
- покраснение места инъекции через полтора месяца после вакцинирования;
- формирование гнойничка или красного пузырька с коростой на месте инъекции;
- периодическое вытекание гноя из-под коросты и образование нового гнойничка;
- образование на месте инъекции рубца красного цвета диаметром 3-10 мм.

Важно! Нельзя пытаться удалять гной из ранки или присыпать нагноение порошком с антибиотиками!
Перечисленные признаки являются свидетельством качественно введенной вакцины БЦЖ. Если у ребенка наблюдается обильное вытекание гноя из ранки, можно покрыть этот участок кожи стерильной салфеточкой, периодически заменяя ее чистой.
Размеры рубцов
Рубец может быть разных размеров, по которым определяют качество постановки вакцины и формирования иммунитета:
- малый размер рубца: меньше 4 мм;
- средний размер рубца: до 8 мм;
- большой размер рубца: до 10 мм.
Если размеры рубца меньше 4 мм, процесс вакцинирования проведен неэффективно и действие иммунитета не превысит трех лет. Размеры рубца от 5 мм и больше говорят об эффективной иммунизации БЦЖ. Размер до восьми мм. покажет положительный результат иммунизации сроком до семи лет.
Отсутствие реакции на вакцину
Почему у некоторых деток нет следа после вакцинации? Это показывает, что противотуберкулезный иммунитет не сформировался.
Что делать при отсутствии следа от рубца? В этом случае необходимо провести тестирование Манту. Если нет положительной реакции, следует провести повторное вакцинирование против туберкулеза.
В некоторых случаях, если нет следа от рубца, вакцинирование БЦЖ проводят в семилетнем возрасте.
Правильной реакции на БЦЖ нет примерно у 10% вакцинируемых детей. О чем свидетельствует отсутствие следа от БЦЖ? Это может быть:
- несформированный иммунитет при неправильном введении препарата;
- врожденный иммунитет против туберкулеза.
Примерно 2% людей на земле имеют врожденный стойкий иммунитет к палочке Коха. У таких людей на плече нет следа рубца после прививки: он не формируется.
Как узнать, что отсутствие следа является нормой, а не причиной нарушения методики постановки инъекций или некачественного препарата? У ребенка с врожденным иммунитетом к туберкулезу нет следа и после проверочной пробы Манту: на ручке остается лишь след самого укола.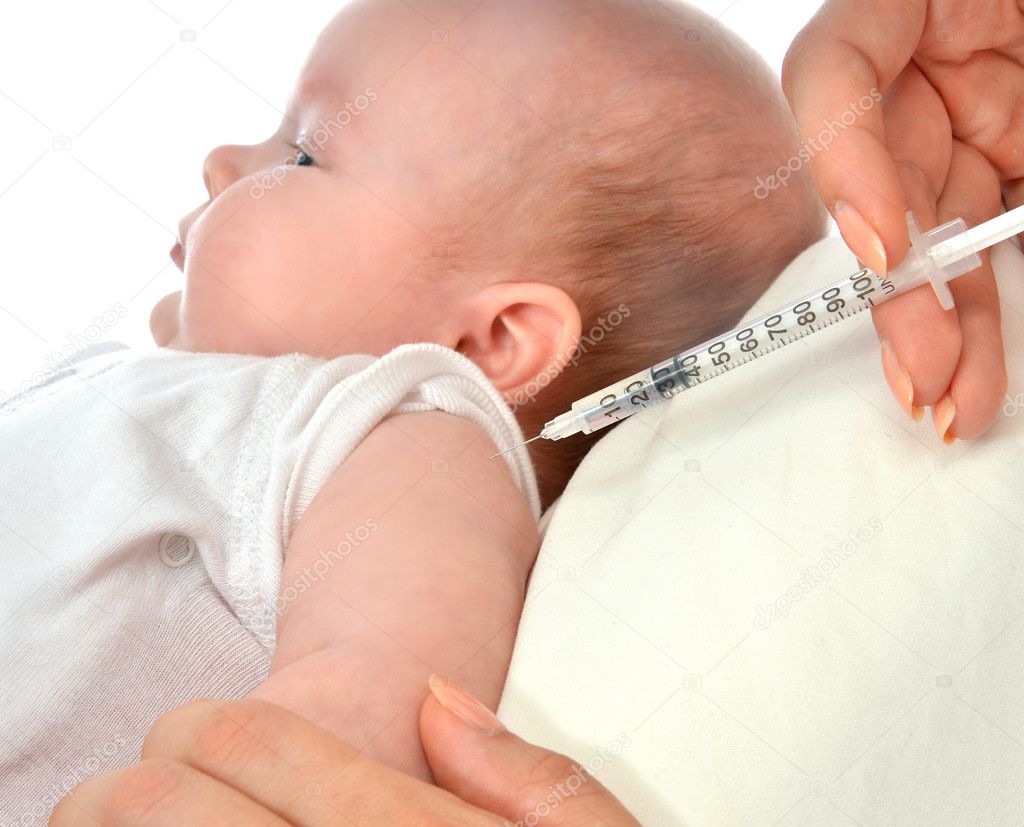
Также можно выделить случаи формирования рубцов внутри кожи. При визуальном осмотре — рубцов нет, однако, опытный фтизиатр сможет обнаружить скрытый рубчик на месте инъекции. Скрытые рубцы можно заранее определить по изменению цвета кожи от вакцинации: она должна быть красной или розовой. Это свидетельствует о проходящих внутри кожного покрова локальных изменениях.
Почему рубчик исчез? Что значит, если на месте инъекции отсутствуют следы? Рубчик был изначально, а потом пропал! Это обозначает окончание действия вакцины. Проба Манту в этом случае покажет либо сомнительный результат, либо его отсутствие (отрицательный).
Келоидные и гипертрофические рубцы
Из-за неправильно введенной вакцины могут образоваться келоидные рубцы. Что это такое? Такие образования начинают формироваться через год после иммунизации. Келоидные рубцы похожи на послеожоговые узлы. Среди них можно выделить разрастающиеся и не растущие формы.
Растущие рубцы имеют характерный красноватый (иногда коричневый) оттенок, неправильную форму и развитую сеть капилляров внутри образования.
Келоид напоминает небольшую опухоль, возвышающуюся над кожным покровом, имеет плотную текстуру и гладкую поверхность. Растущие рубцы не имеют обратного хода развития, то есть, склонны только к увеличению.
Реакцией на келоид бывает боль при прикосновении и периодический зуд.
Причины появления келоидов пока не изучены до конца. Предполагается:
- наследственная несостоятельность соединительной ткани;
- длительно незаживающий воспалительный очаг;
- качество вакцины и нарушение техники введения инъекции.
Иногда келоид образуется в ответ на повторное введение препарата. Реакция на первичное введение препарата образованием келоида встречается крайне редко.
В некоторых случаях интенсивная терапия помогает замедлить разрастание келоида, иногда удается полностью прекратить рост измененной ткани. Удачное исцеление возможно только у новорожденных при первичном вакцинировании. Убрать келоид после ревакцинации практически не удается. Терапия приводит к еще большему разрастанию келоида , порой, по всей поверхности плеча.
Терапия приводит к еще большему разрастанию келоида , порой, по всей поверхности плеча.
Следует отличать келоид от гипертрофических узлов, которые не возвышаются над поверхностью кожного покрова и никогда не имеют внутри своей структуры сеть капилляров. Гипертрофические узлы имеют неяркую окраску и шероховатую поверхность, в отличие от глянцевитых келоидов. Гипертрофический узел не вызывает зуд и через какой-то промежуток времени просто рассасывается сам.
Прививка от ротавирусной инфекции младенцу
Местная реакция на прививку БЦЖ у детей: почему остается рубец и что значит, если нет следа?
БЦЖ – это прививка от туберкулеза. Вакцинация на сегодняшний день является наиболее эффективным методом профилактики опасного заболевания. После инъекции остается папула, которая позже рубцуется.
След от БЦЖ – поствакцинальный знак, являющийся нормальной реакцией организма. В некоторых случаях рубца не остается, поэтому важно понимать, как распознать вариант нормы от неэффективно проведенной вакцинации.
Как проявляется туберкулезная прививка у грудничка?
Постепенно в области укола появляется гнойничок. Наблюдается такое через 1-1,5 месяца после введения препарата. Многие родители волнуются, когда папула становится синюшной, бордовой или лиловой.Изменения подобного характера совершенно естественны. Окончательно иммунитет к туберкулезу сформируется через 4-4,5 месяца после ввода инъекции.
За этот период папула может наполняться гнойным содержимым, прорываться, покрываться корочкой. Все именно так и должно быть.
Чтобы не возникло осложнений, важен своевременный уход за папулой. После заживления образуется рубец от БЦЖ. След от прививки является показателем того, как вырабатывается иммунитет против туберкулеза.
Размеры рубцов после вакцинации от туберкулеза
- малый размер – меньше 4 мм;
- средний – до 8 мм;
- большой размер – до 10 мм.

Небольшой рубец говорит о минимальной степени защиты от заболевания. В этом случае вакцинация была проведена неэффективно. Иммунитет действует в этом случае только 3 года.
Размер до 8 мм дает положительный результат сроком до 7 лет, это значит, что организм защищен надежно. Когда шрам слишком большой, более 10 мм, то это говорит об отсутствии иммунитета. Возможно медперсоналом была допущена ошибка при вводе вакцины.
Нет следа от БЦЖ у новорожденного ребенка: что это значит?
Когда у ребенка не остается следа после прививки, это значит, что иммунитет против туберкулеза не сформировался. В этой ситуации следует провести тестирование Манту.
При отсутствии положительного результата, требуется повторная вакцинация. Встречаются случаи, когда при отсутствии следа, прививка БЦЖ делается в семилетнем возрасте.
Примерно у 10% детей нет правильной реакции. Это значит:
- препарат был введен неверно, из-за чего иммунитет не сформировался;
- врожденный иммунитет к туберкулезу.

Стойкую защиту от палочки Коха имеют с рождения около 2% людей на земле. У них на плече рубец попросту не формируется. Узнать об этом можно после проверочной пробы Манту. На руке виден только след от укола.
Возможны случаи формирования внутреннего рубца. Опытный фтизиатр всегда его обнаружит. Скрытый шрам определяется по изменившемуся цвету кожи: она становится розовой или красной.
Если рубец изначально наблюдался, а потом исчез, это говорит об окончании действия вакцины. Результат после пробы Манту будет сомнительным или отрицательным.
Почему от прививки БЦЖ остается шрам?
Вакцина имеет в своем составе живые бактерии, при введении которых, организм реагирует на чужеродные антигены долгим воспалительным процессом в зоне инъекции.
Заживление происходит длительное время и протекает с периодическими нагноениями, такой процесс приводит к смене здоровой ткани на фиброзную, формируя шрам.
Заживление места инъекции после ревакцинации БЦЖ в 7 лет, проходит быстрее, так как ответ организма на антигены протекает уже не так бурно. При таком иммунном ответе, шрам формируется небольшого размера или вовсе отсутствует.
При таком иммунном ответе, шрам формируется небольшого размера или вовсе отсутствует.
Такая реакция считается естественной на введенный туберкулин. Это свидетельствует о правильно сделанной прививке и о начале формирования иммунитета.
Что делать при образовании келоидных и гипертрофических рубцов?
Келоидные рубцы появляются из-за неправильного введения препарата. Впервые образование можно заметить через год после иммунизации.
Напоминают они послеожоговые узлы. В некоторых случаях они могут разрастаться, тогда рубец имеет красноватый оттенок и неправильную форму.
Реакцией на келоид является боль в результате прикосновения, периодический зуд.
Порой образование такого рубца происходит после вторичного введения препарата. Подобная реакция на первичную вакцинацию встречается очень редко.
Применяемая интенсивная терапия может замедлить разрастание келоида, иногда ее рост можно полностью остановить. После ревакцинации избавиться от рубца очень сложно. Терапия в этом случае может только спровоцировать еще больший рост рубца.
После ревакцинации избавиться от рубца очень сложно. Терапия в этом случае может только спровоцировать еще больший рост рубца.
Гипертрофические узлы над поверхностью кожного покрова не возвышаются. Их структура не состоит из сети капилляров, в отличие от келоидных рубцов. Их поверхность неяркая и шероховатая, они не вызывают зуда и со временем рассасываются сами по себе.
Методы лечения
Используемые методы лечения рубцов можно разделить на 5 групп:
- медикаментозная терапия;
- лучевая;
- терапия физическими факторами;
- хирургическое вмешательство;
- косметологические процедуры.
Видео по теме
Доктор Комаровский об опасности туберкулеза и вакцинации БЦЖ:
Рубец – это естественная реакция организма на вакцину. Бороться с его образованием после прививки БЦЖ не стоит. Кроме этого, он является доказательством того, что человек был привит от туберкулеза, даже если и не помнит об этом.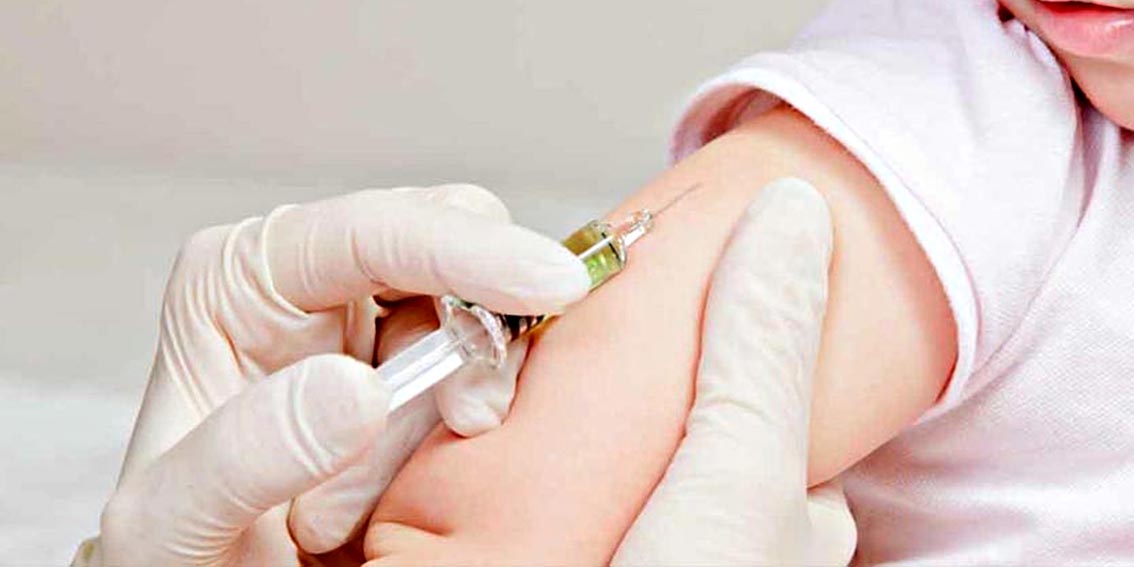
О чем говорит след оставшийся от прививки бцж
- Сокращение БЦЖ знакомо всем, однако не все понимают, что это за вакцина и почему у некоторых людей она оставляет характерный шрам на руке.
- Эта процедура проводится около 100 лет и спасает миллионы жизней.
- Несмотря на то, что процедура вакцинации является безопасной, нелишним будет узнать, что же за лекарство вводит врач.
Что такое БЦЖ?
БЦЖ — придуманный в 1923 году состав, который позволяет выработать в организме человека иммунитет к туберкулезу. Инъекцию делают внутрикожно; «болезнь» развивается локально, позволяя лейкоцитам бороться с ней и выработать иммунитет .
Вакцина вводится в левое плечо, между первой и второй его третью (кожа в этом месте толстая). Если же по каким-то причинам ввести вакцину в плечо не представляется возможным, выбирают бедро.
Само вещество хранится в сухом виде и перед введением разводится физраствором , который прилагается к вакцине. Шприц для инъекции специальный — туберкулиновый, объемом в 1 мл .
Шприц для инъекции специальный — туберкулиновый, объемом в 1 мл .
Ввести вакцину необходимо строго внутрикожно. Делают это следующим образом: сначала вводят небольшое количество вещества, чтобы убедиться, что попали именно под кожу. Если это так, вводят оставшийся туберкулин.
На месте инъекции образуется белая папула 5-10 мм величиной. Через 30 минут она исчезает. Место укола нельзя мазать зеленкой или йодом. В течение 2-3 месяцев с кожей в месте укола происходят нормальные изменения: образование папулы, пустулы и даже небольшого нагноения, которое покрывается корочкой.
Внимание! Когда корочка отпадает, образуется шрамик, к виду которого мы привыкли.
Место укола после прививки — образование шрама
Реакции кожи и стадии образования шрама после вакцинации типичны для большинства пациентов.
- Возникает небольшая папула , исчезающая через полчаса .
- Место укола краснеет или даже приобретает лиловый оттенок, но это считается абсолютно нормальным.

- Кожа немного опухает (небольшая опухоль продержится 2-3 дня ).
- После уменьшения припухлости место укола будет неотличимо от кожи вокруг него — это нормальная реакция организма.
- Через 1,5 месяца после введения вакцины появляется гнойничок, из него может вытекать гной (иногда это продолжается до 4 месяцев ). Гнойничок возникает не всегда — на месте укола может образоваться пузырек с жидкостью.
- После появления гнойничка возникнет красный прыщик , который через некоторое время трансформируется в рубец.
Важно! Обрабатывать ранку запрещено, даже несмотря на нагноение. Необходимо без каких-либо средств промывать или протирать место укола, избегая занесения в рану химических веществ. Выдавливать гной нельзя.
На разных стадиях заживления, особенно начиная с появления гнойничка, место укола может зудеть и чесаться. Не удивляйтесь, если ребенок будет говорить, что у него под кожей «кто-то живет». Такая реакция организма на заживление после введения препарата является нормальной.
Такая реакция организма на заживление после введения препарата является нормальной.
Необходимо попросить ребенка не чесать ранку ; если он не может с собой справиться, на нее аккуратно накладывается марлевая повязка .
Размеры рубчика
Рубец отличается светлым цветом и диаметром от 2 до 10 мм . Величина рубца — единица индивидуальная.
- Малые рубцы (до 4 мм) .
- Рубцы средней величины (от 4 до 8 мм)
- Большие рубцы (до 10 мм).
Считается, что если размер рубца маленький, то вакцина была малоэффективна. Ее следует повторить через 3 года.
Осложнения на месте укола
Несмотря на простоту и относительную безопасность процедуры, в редких случаях могут возникать осложнения.
- Образование инфильтрата под кожей . На месте укола с внутренней стороны образуется шарик с вакциной. Это происходит, когда инъекция сделана слишком глубоко. Если фтизиатр вовремя не выведет вещество, пузырек может разорваться, а туберкулин — попасть в кровь. Допускать этого нельзя, следует сразу обратиться к врачу.
- Образование грубого рубца . Такая реакция является редкой, обычно она связана с кожными заболеваниями. Обычно такого грубого шрама нет. Келоидный рубец выпуклый и часто имеет красный цвет. Стоит узнать, есть ли подобные отклонения у кого-то из родственников.
 В целом такая реакция не является критической, но, если рубец чешется (или появляется зуд), лучше обратиться к фтизиатру.
В целом такая реакция не является критической, но, если рубец чешется (или появляется зуд), лучше обратиться к фтизиатру. - Образование язвы на коже. Такая реакция говорит о непереносимости ребенком препарата. Врачи должны провести местное лечение, устранить язвы и покраснения. Кроме того, в карту ребенка обязательно должна быть занесена информация о такой реакции — она будет нужна при дальнейших вакцинациях.
Введение инъекции не в кожу, а в кровь . Такая ситуация встречается крайне редко. Врач сам забьет тревогу и сделает все необходимое, чтобы восстановить состояние ребенка.
Задача родителя — не паниковать и обратиться к опытному фтизиатру.
Выделение инфильтрата и нарывы на месте укола — гнойные выделения при заживлении — это нормальная реакция организма.
Но если место укола начинает болеть и нарывать, необходимо показаться фтизиатру. Ни в коем случае нельзя пытаться лечить нарывы самостоятельно, давить на них, наносить мази.
Вам также будет интересно:
Почему нет рубца?
Примерно у 10 процентов детей след после прививки БЦЖ отсутствует. Происходит это из-за того, что после введения препарата у этих людей не сформировался иммунитет, вакцина не сработала. Также существует небольшая группа людей (2% ), которые имеют врожденный иммунитет к туберкулезу.
Если нет рубца после БЦЖ, есть два варианта:
- поставить пробу Манту; если реакция отрицательная, нужно повторить БЦЖ;
- подождать, пока ребенку исполнится 7 лет ; каждый год ставить Манту, и в 7 повторить вакцинацию.

Встречаются редкие случаи, когда рубец образуется под кожей. Опытные врачи умеют предсказать такой сценарий развития уже после самой вакцинации: кожа на месте укола изменяет цвет и становится красной или розовой. Рубец под кожей допустим — вакцина сработала.
Если вакцину ввели неправильно (например, под кожу), то рубчика нет. Но это очень нежелательная ситуация, которая говорит о некомпетентности врача — препарат может попасть в кровь, а допускать это нельзя. Если произошла ошибка, необходимо сразу же обратиться к опытному фтизиатру.
Если рубец был, но исчез
В большинстве случаев это происходит через 7 лет , как и должно, но в некоторых ситуациях (если рубец был маленьким) место укола может оказаться чистым уже через 3 года .
Такая реакция организма со временем является нормой. Исчезновение рубца от БЦЖ означает, что прививка отработала и ее нужно повторять.
Чтобы удостовериться, что прививку необходимо повторить, достаточно провести тест Манту: если введение препарата не вызывает покраснения, т. е. реакция отрицательная, необходима ревакцинация.
е. реакция отрицательная, необходима ревакцинация.
Что делать, если нет следа от БЦЖ у маленького ребенка? Этот вопрос вводит в недоумение многих мам, потому что иммунитет против туберкулеза имеет значение для новорожденного.
Туберкулез – острое инфекционное заболевание, локализующееся преимущественно в легких и представляющее серьезную угрозу для жизни человека. Возбудители инфекции очень часто встречаются в окружающей среде, поэтому человеку очень важно иметь хороший иммунитет против данной болезни.
В связи с этим прививку от туберкулеза или БЦЖ, делают детям еще в раннем возрасте – при выписке из роддома. По поводу данной прививки у родителей часто возникают разнообразные вопросы.
Но больше всего молодые мамы и папы не понимают, что делать, если через несколько месяцев после введения вакцины в плечо ребенка на месте укола не остаётся рубца. Почему его наличие необходимо и чем грозит его отсутствие?
Как происходит вакцинация БЦЖ
При нормальных обстоятельствах, если нет противопоказаний и иных факторов, запрещающих осуществление вакцинации, прививку от туберкулеза ставят младенцу перед его выпиской из роддома.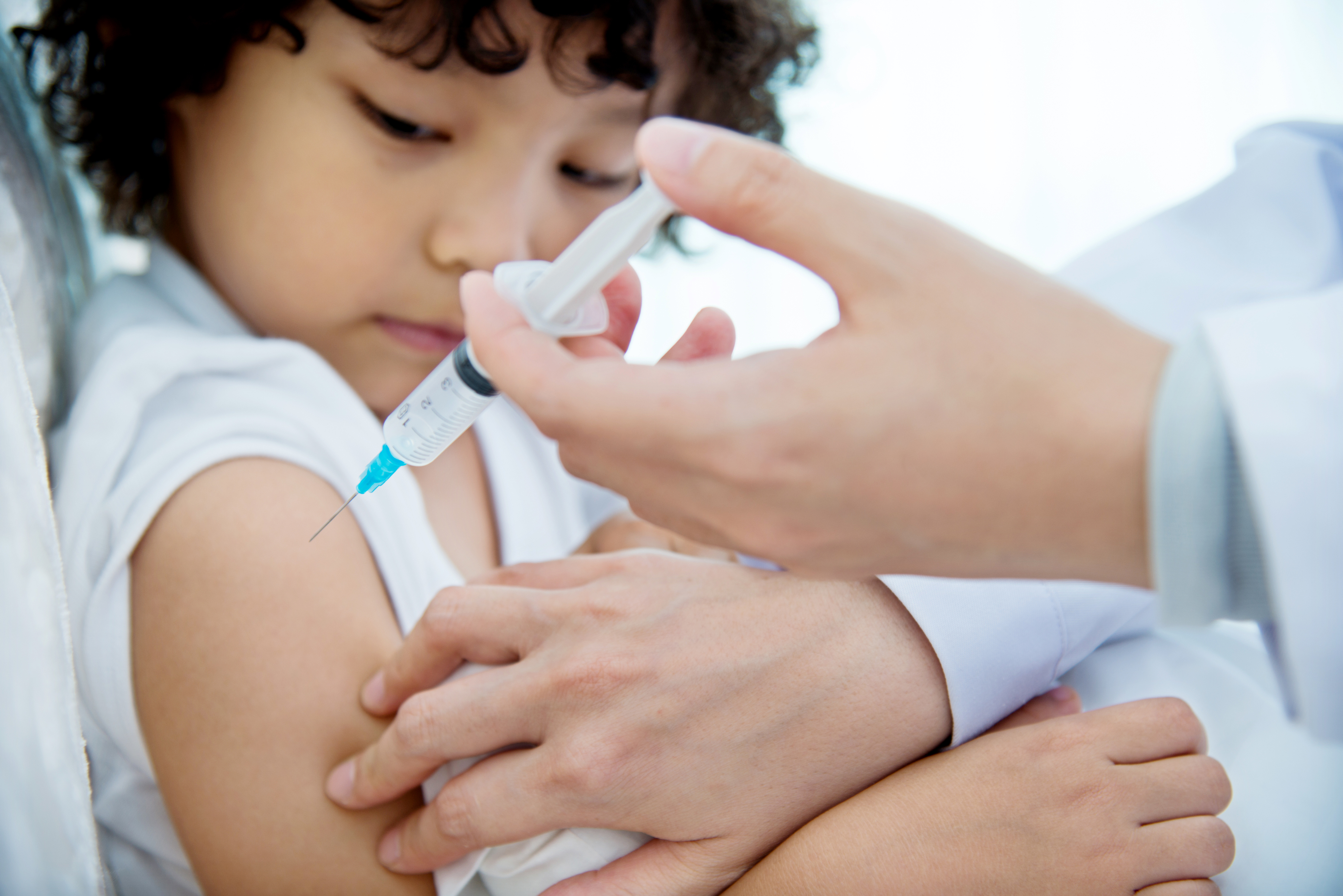 При этом вакцину вводят внутрикожно в левое плечо. Кроме того, существуют исключительные случаи, когда прививку делают в бедро, но они происходят отнюдь не часто, и в основном укол проводится в плечо.
При этом вакцину вводят внутрикожно в левое плечо. Кроме того, существуют исключительные случаи, когда прививку делают в бедро, но они происходят отнюдь не часто, и в основном укол проводится в плечо.
Если по какой-либо причине вакцинацию БЦЖ не сделали в роддоме, ее можно провести в своей поликлинике либо не выходя из дома, если вызвать медицинскую бригаду.
Таким образом, выделяются три основных способа проведения прививки БЦЖ:
- В роддоме.
- В местной поликлинике.
- Дома, с вызовом медицинской бригады.
После правильного ввода вакцины в слой кожи на месте укола появляется папула – небольшая круглая подушечка диаметром до 10 мм, как от Манту. Спустя полчаса папула рассасывается. Это сигнализирует о правильно сделанной прививке.
Если в дальнейшем все будет идти «по инструкции», то по истечении полутора месяцев на месте прививки должна появиться пустула с явными гнойными процессами. Некоторые родители пугаются, заметив такую болячку у своего ребенка. На самом деле воспалительный процесс на месте укола является абсолютно нормальной реакцией организма на БЦЖ.
На самом деле воспалительный процесс на месте укола является абсолютно нормальной реакцией организма на БЦЖ.
Из пустулы может выделяться гной, который надо убирать чистой салфеткой. Пользоваться зеленкой или другими антибактериальными средствами категорически нельзя.
Еще через полмесяца ранка начнет заживать и покрываться характерной корочкой. Необходимо, чтобы она отсохла и отшелушилась сама, без чьей-либо помощи. Когда это произойдет, на месте укола останется след от прививки БЦЖ характерный рубец. По нему можно судить об успешности проведенной вакцинации.
Эффективность БЦЖ
Как узнать, насколько эффективной оказалась проведенная процедура? Об этом скажут размеры, которыми обладает след от БЦЖ.
О нормальной реакции организма на вакцину сигнализируют следующие проявления:
- появление круглой «подушечки» сразу после укола;
- формирование покраснения, а затем и образование гнойного очага;
- выделение гноя из-под коросты и формирование нового очага;
- появление рубца.
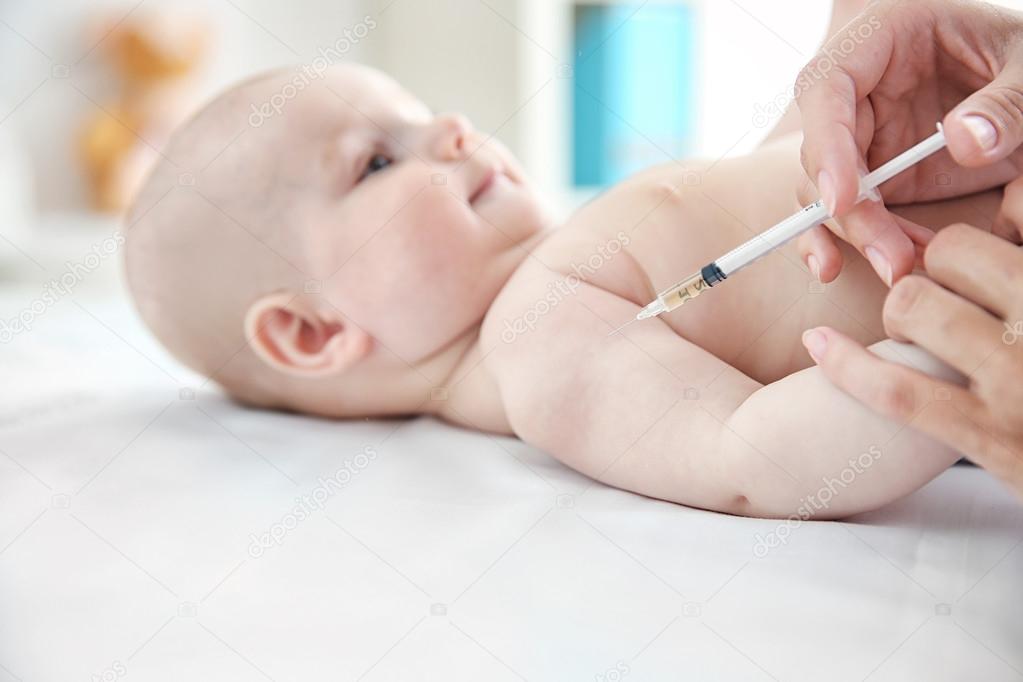
Хороший след от гнойного очага должен иметь размеры от 3-х до 10-и миллиметров в диаметре. Рубец – явный признак устоявшегося противотуберкулезного иммунитета у ребенка. Также по диаметру следа от укола можно узнать, как долго будет держаться иммунитет.
Различают три вида рубцов:
- Маленькие (имеют размер менее 4 мм). В данном случае можно говорить о малой эффективности вакцинации. Иммунитет вряд ли продержится более трех лет.
- Средние – от 5 до 8 мм. Вакцинация хорошего качества. Должно хватить на 5-7 лет.
- Большие – от 8 мм и более. Как правило, в таких случаях иммунитет против туберкулеза длится 7 и более лет.
Большой вопрос, которым озадачены некоторые родители, это: «Почему нет следа от БЦЖ, и что это может значить?» Ведь у некоторых детей после укола вообще не остается никаких следов, за исключением маленькой точки от самой иглы.
Почему нет рубца
По каким причинам у ребенка нет следа от прививки БЦЖ? Если было проведено вакцинирование, но по истечении трех месяцев с момента укола на коже не появилось никаких следов, узнать причину отсутствия нормальной реакции поможет тест Манту.
В основном, рубец не возникает по двум причинам:
- Либо имеют место нарушения в технологии введения вакцины в кожу, либо испорчен сам состав вакцины.
- Когда организм имеет мощный противотуберкулезный иммунитет от природы, и в дополнительной защите не нуждается.
Если тест Манту окажется отрицательным, необходимо будет провести повторную вакцинацию. В таком случае, скорее всего, были допущены ошибки в процессе вакцинации. Иногда повторную прививку делают через семь лет. Однако тогда на протяжении всего этого времени такие дети должны проходить тест Манту не как обычно раз в год, а два раза в год, чтобы избежать заболевания туберкулезом.
Если первая причина отсутствия рубца говорит об отсутствии иммунитета, то вторая причина свидетельствует об обратном. Почти 2% всех жителей планеты имеют мощную врожденную защиту от туберкулеза и некоторых других заболеваний.
Организм таких людей ликвидирует возбудители инфекции еще до того, как начинают вырабатываться антитела. Поэтому рубца после БЦЖ нет, как нет и покраснения после теста Манту.
Как правило, такие дети не могут заболеть туберкулезом при нормальных условиях, если нет факторов, сильно ослабляющих иммунную систему, как, например, ВИЧ.
Рубец после БЦЖ исчез спустя несколько лет – что это значит? Это говорит о том, что действие вакцины закончилось, и требуется ревакцинация.
- Необходимость в повторной прививке легко подтверждается тестом Манту – он показывает отрицательный результат, в то время как при наличии искусственно созданного противотуберкулезного иммунитета после Манту на руке ребенка будет образовываться покраснение.
Какой может быть след от прививки БЦЖ
БЦЖ – сокращённое название вакцины от туберкулёза. Прививка создаётся из штаммов туберкулёзных палочек, утративших способность развиться в человеческом организме.
Инъекцию вакцины делают в первую неделю жизни ребёнка. Последующая ревакцинация проводится в 7 лет.
После укола остаётся специфический след от БЦЖ на левом предплечье у большинства людей, но рубец иногда может и не сформироваться.
Существует две разновидности вакцины против туберкулёза: БЦЖ и БЦЖ-М (для недоношенных младенцев с низкой массой тела). Перед прививанием исключаются противопоказания: неудовлетворительное состояние здоровья новорождённого ребёнка и матери, вес – ниже 2,5 кг. Вакцину вводят в левое плечо внутрикожно как минимум дважды в жизни.
Ревакцинация назначается, если эффективность первых двух прививок поставлена под сомнение.
Каждый год проводится дополнительное исследование – проба Манту. Она заключается в том, что в зону чуть выше запястья вводят туберкулин – препарат, содержащий продукты жизнедеятельности искусственно культивированных микобактерий.
Введенный туберкулин инициирует активность выработанных при вакцинации антител, это выражается в специфической кожной реакции. Контрольный замер зоны воспаления (папулы) производят спустя 72 часа после укола.
Если её размеры соответствуют принятой норме, считается, что иммунитет против туберкулёза продолжает действовать.
Норма заживления прививки. Почему остается шрам
Шрам от БЦЖ – прямое подтверждение эффективности вакцинации против болезни. Принято считать, что выраженный рубец подчёркивает крепость иммунитета. Повторная прививка перед школой проводится в обязательном порядке, поскольку действие первичной начинает к этому времени ослабевать. Наличие рубца подтверждает формирование иммунной защиты против туберкулёза.
Действующее вещество введённой вакцины поражает клетки в месте укола. Формируется локальное заражение. Человеческий организм начинает вырабатывать антитела, приобретая иммунитет к возбудителю заболевания.
Особенности образования шрама на месте прививки
Внутрикожная инъекция провоцирует локальное заражение, вследствие которого на коже образуется воспалённая папула. Средний диаметр составляет не более 1 см. Покраснение постепенно сходит в течение 30 минут после укола. Такая последовательность этапов – свидетельство правильного введения вакцины.
Другая особенность состоит в нагноении ранки. Покраснение сменяется синим либо фиолетовым оттенком, свидетельствующем о скоплении крови под кожей. Полость папулы наполняется видимым гнойным содержимым. Такая реакция более характерна для ослабленных младенцев. Формирование рубца у здоровых детей происходит быстро, без видимых осложнений.
Синюшный цвет и гной на месте прививки – не повод для волнения. Рана самостоятельно очищается через некоторое время. В исключительных случаях может пройти несколько дней либо даже недель и месяцев. Весь процесс свидетельствует о постепенной выработке антител.
Третья особенность – вакцинация проводится строго внутрикожно, а не подкожно. Последнее ведёт к образованию абсцесса, иммунитет не вырабатывается. Келоидный рубец развивается как вид осложнения.
При нормальном восприятии вакцины постепенно образуется небольшой рубчик, называемый поствакцинальным знаком. Он – свидетельство того, что человек был привит от туберкулёза. Образование рубца считается нормальной реакцией организма на БЦЖ, и его отсутствие должно тревожить.
Размеры рубчика
Рубец от БЦЖ бывает разных размеров, по нему определяется качество сформировавшегося иммунитета. Приняты за стандарт следующие величины:
- менее 4 мм – малая;
- до 8 мм – норма;
- до 10 мм и выше – большая.
Размеры менее 4 мм признаются следствием неэффективной вакцинации – организм не выработал достаточно антител для сопротивления заболеванию. Величина более 5 мм считается хорошим знаком. До 10 мм – не следует волноваться, но если рубчик после БЦЖ ещё больше, то иммунитет, вероятно, не был выработан.
Можно ли его удалять
Шрам образуется навсегда. После проведения ревакцинации БЦЖ в 7 лет увеличивается размер повреждения, поскольку укол ставится в то же место. Рубец ни в коем случае нельзя обрабатывать спиртом, мазями и зелёнкой с йодом. Поверхностная попытка залечить рану приведёт к осложнениям или даже некрозу тканей.
Шрамированный участок можно удалять спустя несколько лет после двух вакцинаций. Применяются лазерная терапия и пластика кожи как наиболее эффективные способы. Иммунитет не ослабнет от отсутствия шрама. Единственный недостаток – в дальнейшем врачи не увидят реальную картину и динамику развития иммунной защиты.
Почему может не образоваться шрам после БЦЖ
Выявлены случаи, когда нет следа от сделанной прививки БЦЖ. Причины заключаются в следующем:
- некачественная вакцина;
- неправильно проведённая процедура;
- наличие врождённого иммунитета.
Врождённый иммунитет против туберкулеза наблюдается редко. Антитела уже присутствуют в крови, потому введённые локально бактерии незамедлительно уничтожаются. На плече после прививки БЦЖ нет следа, поскольку не образуется папула.
Первые два случая свидетельствуют о том, что иммунитет не развился. А вот почему нет реакции на БЦЖ у новорожденного, нужно разобраться, это тревожный сигнал о необходимости проверки либо ревакцинации.
Если БЦЖ не проявилась в течение дня после введения вакцины, сначала делают пробу Манту. Она помогает выявить признаки туберкулеза легких и других форм на ранних стадиях. Вводят слабый возбудитель под кожу на предплечье: если формируется папула нормальных размеров, есть сопротивляемость. Если же результат пробы отрицательный, иммунитета нет, и, возможно, произошло заражение.
Если рубец был, но исчез
След от БЦЖ у новорожденных сначала образуется, а в период с младенчества и до 7 лет исчезает, это означает окончание действия вакцины. У большинства взрослых нет видимого шрама от БЦЖ на руке. У детей же постепенное исчезновение подтверждает снижение иммунитета.
Келоидный рубец как форма осложнения
В норме рубец БЦЖ – небольшой и однородный, но иногда может преобразовываться в келоидный рубец. Осложнение развивается спустя 10-12 месяцев.
Что это такое
Келоидный рубец – редко встречающаяся реакция на введённую вакцину. Фактически вследствие повреждения кожного покрова неконтролируемо разрастается соединительная ткань. Удалить подобный шрам можно только хирургическим путем.
Внешне образование похоже на небольшой ожог, поскольку кожа вздувается, приобретая ярко-красный оттенок. Форма либо остается прежней, либо шрам начинает разрастаться в разные стороны. Место вакцинации болит и зудит.
Почему остается рубец, до конца неизвестно, причин множество, но они не изучены до конца:
- наследственная предрасположенность к разрастанию соединительной ткани;
- незаживающее воспаление;
- некачественная вакцина;
- неправильно сделанная инъекция.
Достаточно редко келоид начинает расти после первой вакцинации. Зачастую такое осложнение возникает вследствие ревакцинации.
Чем опасен
Келоид относится к доброкачественным новообразованиям. Его легко повредить – задеть ногтями, сорвать одеждой или при мытье. Заживление – длительное, часто осложняется инфицированием. Без своевременного лечения он разрастается по всему телу.
Шрам свидетельствует о том, что организм выработал антитела к туберкулёзу. Следует провести дополнительное исследование, если нет видимого рубца от БЦЖ. Возможно, уже есть врождённая сопротивляемость, либо у ребенка нет рубчика БЦЖ из-за ошибки введения или некачественной вакцины.
Зная, о чём говорит след, оставшийся от прививки БЦЖ, можно не беспокоиться понапрасну. Ведь, перенеся небольшой дискомфорт, ребёнок будет защищён от туберкулезной инфекции.
О чем говорит оставшийся след от прививки бцж и что значит если у ребенка нет рубца
БЦЖ у новорожденных проводится на 3-5 сутки после рождения. Это прививка от смертельных форм туберкулеза. Защитные силы против опасных форм данного заболевания формируются в течение месяцев и проявляются в образовании шрама в месте введения вакцины. Случается, что след от БЦЖ у ребенка отсутствует.
О чем говорит оставшийся след
Вакцинацией невозможно защититься от заражения туберкулезом. Данная прививка снижает вероятность развития генерализованных смертельных форм данной инфекции, которым подвержены лица с различными иммунодефицитами и дети.
След от прививки демонстрирует, как сформировались иммунитетные силы организма против заболевания. Если в месте инъекции остается шрам от БЦЖ — это норма, которая говорит о том, что вакцинация прошла положительно, и у человека сформирован иммунитет против данного заболевания.
В вакцине БЦЖ присутствуют ослабленные штаммы микобактерий туберкулеза бычьего типа.
При проведении прививки происходит локальное заражение данной инфекцией в месте ее введения.
В нормальном состоянии организм вакцинированного человека эффективно справляется с инфекцией, и в его крови образуются специфические антитела.
Инъекция осуществляется внутрикожно. В месте прививки сначала образуется папула, которая составляет до 1 см в диаметре. Через какое-то время (иногда достаточно получаса) папула исчезает полностью. Иногда место прививки может нагнаиваться, приобретать синюшную или фиолетовую окраску, но после все заживляется, и формируется рубец от БЦЖ.
Признаки правильно проведенной вакцины БЦЖ:
- сразу после укола формируется плоская белая папула;
- спустя 30-40 дней после проведения вакцинации можно увидеть покраснение в месте инъекции;
- на месте прививки образуется красный пузырек или гнойничок, а в последующем — корочка;
- появляется красный рубец 3-10 мм.
Иногда возникает избыточная положительная реакция на введение БЦЖ в виде местного воспалительного инфильтрата, сопровождающегося повышением температуры и местной реакцией лимфоузлов. Такое явление называется БЦЖит.
Если развилось такое состояние, то ребенку требуется назначение курса противотуберкулезных препаратов (изониазид, рифампицин) длительностью 3 месяца.
Какие по Вашему мнению наиболее важные факторы при выборе медицинского учреждения?
Почему образуется след от БЦЖ
Туберкулез — опасная и достаточно распространенная болезнь, поражающая и детей, и взрослых. Чтобы сократить случаи заболевания и предотвратить возникновение тяжелых форм этой патологии, в России проводится регулярная вакцинация. Это прививка №1 в национальном календаре вакцинации.
Начальный этап приходится на первые дни жизни новорожденного. Инъекцию делают ребенку еще в роддоме. Предварительно у младенца проверяют реакцию Манту, она должна быть отрицательной.
На месте укола образуется характерный след от БЦЖ. По нему можно определить, насколько эффективной была вакцинация. Считается, что чем больше в диаметре рубец (до 1 см), тем более крепкий образовался иммунитет.
Продолжают профилактику туберкулеза в школе. Ревакцинацию проводят в семилетнем возрасте. Считается, что к этому времени след от 1 прививки становится едва различимым. Это значит, что действие вакцины закончилось и нужна новая прививка.
Медики утверждают, что после ревакцинации смертность от туберкулеза снижается, потому проводить ее нужно обязательно.
Особенности образования шрама на месте прививки
Характерный шрам от БЦЖ на левом предплечье — это норма. Рубец свидетельствует, что вакцинация прошла эффективно и человек привит от туберкулеза.
После введения вакцины, в которой присутствуют ослабленные бактерии, в месте укола возникает локальное заражение туберкулезом. Организм справляется с инфекцией, в крови вырабатываются антитела, и человек считается защищенным от вируса туберкулеза.
После инъекции, которую делают внутрикожно, на месте укола образуется папула. Это нормальная реакция на прививку. Она имеет средний диаметр — не более 1 см. Спустя 0,5 часа папула должна рассосаться без следа. Это свидетельствует о правильно сделанной прививке, а также о том, что формирование иммунитета началось.
Через некоторое время на месте введения вакцины начинается нагноение, ранка может приобретать синюшный или фиолетовый цвет, полость может периодически наполняться гнойным содержимым.
Это означает, что процесс формирования иммунитета продолжается. Нередко такая реакция организма пугает родителей. Однако это не повод для волнения — со временем рана очистится. Может пройти несколько месяцев, прежде чем завершится формирование иммунитета.
В месте инъекции образуется небольшой рубец, который медики называют поствакцинальным знаком.
Осложнения на месте укола
Если вакцина была сделана с нарушением, на месте укола может возникнуть осложнение.
Если препарат введен неправильно — не внутрикожно, а подкожно, в этом месте может образоваться холодный абсцесс — болезненное уплотнение. В этом случае необходимо обратиться к врачу.
Неправильно сделанный укол может привести к образованию келоидного рубца из соединительной ткани, который имеет плотную структуру и неправильную форму. Удаляют его хирургическим путем.
Почему нет рубца
Если в месте введения препарата не образуется характерный след, врачи утверждают, что вакцинация не удалась и ребенок остается не привитым, т. е. находится в группе риска.
Если не остается нормальной реакции организма на БЦЖ, это повод для консультации с врачом. Он может назначить дополнительное обследование ребенка и решить вопрос о повторном введении препарата.
Если шрам не образуется вовсе, это может свидетельствовать о том, что у ребенка высокий врожденный иммунитет к туберкулезу. Ослабленный вирус после введения вакцины сразу же погибает, не успевая создать искусственный иммунитет.
Если рубец был но исчез
Если нет следа от БЦЖ, значит, действие вакцины закончилось. У большинства взрослых людей такой шрам отсутствует.
У детей исчезновение шрама БЦЖ означает, что иммунитет к заболеванию снизился и необходима ревакцинация.
Профилактика
Чтобы рубчик БЦЖ был более аккуратным, можно принять некоторые меры.
Прививаться нужно только в условиях медицинского учреждения и качественной вакциной.
Тем самым можно исключить возможность инфицирования ранки.
После проведения ревакцинации важно правильно ухаживать за ранкой. Нельзя вскрывать образовавшуюся полость, выдавливать гной, мазать больное место спиртосодержащими препаратами — зеленкой или йодом.
Нужно объяснить ребенку, что язвочку нельзя расчесывать. Нельзя также заклеивать это место лейкопластырем.
Нужно дождаться, пока процесс завершится естественным путем, и ранка очистится самостоятельно после образования шрама.
Чтобы избежать заболевания туберкулезом, нельзя отказываться от прививки БЦЖ. Не имея иммунитета, сформированного в детстве, при инфицировании вирусом можно получить тяжелую форму заболевания, которая может привести к негативным последствиям, в том числе и к летальному исходу.
БЦЖ: что делать если нет следа
Туберкулез является распространенным заболеванием с высоким уровнем смертности. Так, опасная болезнь диагностируется почти у 9 миллионов людей. Причем до 4 миллионов человек ежегодно умирают от инфекции, вызванной палочкой Коха.Чтобы не допустить развития болезни, на 3-5 сутки после рождения и в 7 лет каждому человеку делают БЦЖ. Показателем того, что прививка была введена правильно является след от БЦЖ.Но у некоторых детей не остается шрама после вакцины. Чтобы понять, считается ли это нормой, необходимо более подробно узнать о БЦЖ, и ознакомиться с отзывами врачей.
Что такое БЦЖ
БЦЖ – это противотуберкулезная вакцина, изготавливаемая из живой, но ослабленной бактерии Mycobacterium bovis, взращённой в искусственных условиях.
БЦЖ применяют для предотвращения развития туберкулеза у детей на 3-5 день после рождения. Ревакцинация проводится в семилетнем возрасте.
Противопоказания к вакцинации:
- Гнойно-септические процессы
- Недоношенность (до 2500 г)
- Иммунодефицит первичный
- Рак
- Аллергия
- Обострения любых болезней
- Генерализованные болезни кожи
- Радиотерапия
- Внутриутробная инфекция
- Поражения НС
- Туберкулез
- Применение иммунодепрессантов и прочее.
Вакцину рекомендовано делать внутрикожно в область поверхностной мышцы плеча. После в месте введения появляется специфический шрам.
Прививка может поспособствовать появлению ложноположительной реакции на пробу Пирке. Если реагирование сильное, то вероятно наличие туберкулеза, но только при отсутствии аллергии.
Из возможных побочных реакций БЦЖ выделяют лимфаденит, холодные абсцессы, келоидные рубцы. Также после вакцинации могут развиться кожные аллергические реакции.
Нормально ли если нет шрама от БЦЖ
Чтобы отличить нормальную реакцию ребенка на прививку, следует знать, как происходит процесс появления ответа. Шрам после проведения БЦЖ возникает постепенно. Так, через 30-45 дней в области введения укола возникает гнойник, который покрывается коркой и заживает около 120-140 дней.
Вначале область, куда была сделана прививка, становится фиолетовой либо черной, что указывает на нормальную реакцию ребенка на прививку. О том, что вакцина была сделана правильно и сформировался иммунный ответ говорит характерный рубец, длина которого составляет 2-10 мм.
Размер шрама указывает на продолжительность иммунной реакции:
- 2-4 мм – защита сохраняется 3-4 года
- 5-8 мм – иммунитет держится от 4 до 7 лет
- От 8 мм – реакция сохраняется больше 7 лет.
След от прививки БЦЖ не образуется приблизительно у 10% детей. Если вакцина была введена правильно, то это может считаться нормой, что указывает на наличие у ребенка врожденной иммунной защиты от туберкулезной инфекции.
Однако такое явление отмечается лишь у 2% детей. Наличие иммунитета подтверждается, если у ребенка после пробы Манту на руке остается только след от укола.
Кроме того, изредка шрамы появляются под кожей, что делает их незаметными визуально. На наличие рубца указывает покраснение области, куда была сделана прививка.
Если след был, но пропал, то БЦЖ перестала действовать. Поэтому Манту в данной ситуации будет отрицательной либо сомнительной.
Что делать если нет следа от БЦЖ? Почему нет?
Ведущие факторы, из-за которых нет следа от БЦЖ у ребенка – применение просроченной или испорченной вакцины, наличие врожденной иммунной противотуберкулезной защиты.
Также, если нет шрама от БЦЖ, то это может указывать на неправильную технологию проведения вакцинации. При отсутствии реакции, вызванной применением недоброкачественного препарата, либо в случае некорректного введения средства ребенок находится в категории риска. Это увеличивает вероятность инфицирования и последующей смерти.
Когда все дети были вакцинированы, но у ребенка нет рубца от БЦЖ, то необходимо проконсультироваться с физиатром или педиатром. При отсутствии шрама врачи рекомендуют сделать прививку повторно через 2 года.
Если после БЦЖ нет рубчика, то перед тем, как проводить ревакцинацию нужно сделать пробу Манту, ее реакция должна быть отрицательной. Если результат положительный либо сомнительный, то вводить прививку от туберкулеза нельзя.
Если была сделана вакцина и после прививки БЦЖ нет следа, то родители обязаны ограничить контакт ребенка с категорией людей, которые могут быть инфицированы туберкулезом. Также необходим регулярно укреплять детский иммунитет, посредством закаливания, сбалансированного питания, занятий спортом и своевременного лечения любых заболеваний.
Нет следа от БЦЖ — результаты пробы Манту
Среди общего количества больных туберкулезом 10 процентов всегда составляют дети, даже в благополучной Европе. Ежегодно в мире туберкулезом заболевают не менее 1 млн детей младше 15 лет. Во всех странах планеты только в 2016 году от туберкулеза умерли 253 тысячи детей.
Тем не менее детские фтизиатры часто сталкиваются с тем, что у родителей нет настороженности по отношению к этому заболеванию, они не понимают важности вакцинации БЦЖ, не разбираются, чем отличаются проба Манту и Диаскинтест. Наверное, именно от незнания появилось так много мифов о туберкулезе, которые приходится развеивать нашему эксперту.
Вакцина БЦЖ от туберкулеза
Миф 1. Прививка живой вакциной БЦЖ бесполезна, поскольку она нисколько не уменьшает риск заболеть туберкулезом.
На самом деле. БЦЖ — самая старая вакцина, проверенная уже не на одном поколении. Цель ее не та, что у вакцины против оспы — сделать прививку младенцу и стопроцентно гарантировать, что теперь человек ни разу в жизни не заболеет оспой. Задача БЦЖ ограничить туберкулезный процесс на уровне лимфатической системы, не дать развиться тяжелым генерализованным формам туберкулеза. Вот почему в стране нет туберкулезного менингита, костного туберкулеза, от которых защищает БЦЖ.
Сегодня ученые работают над более эффективной прививкой, но все равно пока это будет живая вакцина. Хотя в идеале нужна инактивированная.
По России охват вакцинацией БЦЖ среди новорожденных 81,2 процента. 10 лет назад было 95−97 процентов. Участковые педиатры стараются, чтобы невакцинированные дети все же получили прививку к году. Но в течение года эти дети могут заболеть туберулезом.
Миф 2. Иногда рубец поcле БЦЖ не появляется.
На самом деле. Эффективность прививки БЦЖ оценивается по двум позициям: сформировался ли рубец после вакцинации и есть ли положительная чувствительность к туберкулину в год. Если нет рубца и положительной реакции на пробу – значит, прививка не была сделана, что бы ни было указано в карте. Вакцинацию надо срочно делать.
Реакция на пробу Манту и ранняя диагностика туберкулеза
Миф 3. Проба Манту и Диаскинтест взаимозаменяемы.
На самом деле. Проба Манту нужна для отбора на прививку, а Диаскинтест необходим для раннего выявления туберкулеза. В России принят такой порядок: проба Манту остается для детей до 7 лет, а школьникам с 21 марта прошлого года применяется Диаскинтест. Его следует проводить ежегодно. Диаскинтест — оптимальный вариант скрининга, поскольку в отличие от пробы Манту он не дает аллергии. Но детям до 7 лет фтизиатры вынуждены оставить пробу Манту, которая, в отличие от других методов позволяет увидеть реакцию не только на туберкулез, но и на вакцину БЦЖ, а значит провести отбор на прививку – найти тех детей, кому нужна ревакцинация. Но в случае сомнительной пробы все равно должен проводиться Диаскинтест.
Миф 4. Нельзя мочить руку, на которой сделана проба Манту.
На самом деле. Мочить можно. Миф о том, что на пробу Манту ни в коем случае не должна попасть вода, зародился, когда много десятилетий тому назад туберкулин вводился накожно, для чего поверхностный слой кожи — эпидермис — рассекали ланцетом, предварительно капнув на это место туберкулином. Боялись, что если на раненый эпидермис попадет грязная вода, может случиться инфицирование ранки. Сейчас туберкулин вводят между эпидермисом и собственно дермой.
Миф 5. У родителей есть право отказаться от туберкулинодиагностики.
Да, это так. Но они должны понимать, что дети, не прошедшие ее, не допускаются ни в сад, ни в школу, ни в другое образовательное учреждение. Родители должны выбирать соответствующий вид образования – семейную, домашнюю, дистанционую формы обучения. Непроверенного ребенка нельзя вести в коллектив и подвергать других детей детей опасности. И если законный представитель ребенка отказался от прививки, он должен оповестить об этом органы опеки. И только в Самарской области 25 детей официально отстранены от посещений детсадов и школ.
Миф 6. Флюорография поможет выявить туберкулез у ребенка.
На самом деле, нет. Изменения в легких менее 1 см на ней не видны. Статистика говорит, что по флюорографии выявляется лишь 0,6% заболевших, тогда как с помощью Диаскинтеста и последующей мультиспиральной компьютерной томографии – 10%.
Когда на прием к фтизиатру приходят дети с плохой пробой Манту, врач просит родителей и других родственников ребенка принести ему и их флюорограммы. Иногда это вызывает возмущение взрослых. Но очень часто по пробе манту ребенка врачи выявляют бабушку на пенсии, которая ни разу не делала снимков легких и уже много лет болеет туберкулезом. Получается, флюорография поможет обеспечить ребенку здоровое окружение.
Симптомы туберкулеза у детей
Миф 7. У туберкулеза очевидные проявления. Они должны насторожить родителей, и тогда ребенка надо показать фтизиатру.
На самом деле. Чаще всего туберкулез у детей протекает бессимптомно. Если есть заметные признаки – это запущенный туберкулез. Если кашель продолжается более 2−3 недель, несмотря на то, что ребенок получает адекватное лечение, нужно обязательно показать его фтизиатру для исключения туберкулеза. Любые проявления интоксикационного характера – субфебрильная температура, потливость ночью – тоже должны насторожить родителей и врача. Ребенку часто ставят диагнозы бронхит или пневмония? Это также повод обратиться к фтизиатру и провести внеплановые пробы. Помните, с диагностической целью пробы можно делать столько, сколько нужно.
Читайте также
Как правильно лечить кашель. 4 вопроса пульмонологу
Как узнать, делали ли прививку БЦЖ? | Вопрос-ответ
В нескольких странах ученые начали масштабное тестирование противотуберкулезной вакцины, которую все новорожденные у нас в стране получают в роддоме. Исследователи выдвинули предположение о том, что БЦЖ может помочь людям справиться с коронавирусной инфекцией COVID-19.
Кому и когда вводят вакцину БЦЖ?
Вакцину БЦЖ вводят внутрикожно в роддоме на границе верхней и средней трети наружной поверхности левого плеча. На месте внутрикожного введения вакцины БЦЖ развивается специфическая реакция в виде папулы размером 5-10 мм в диаметре. У новорожденных нормальная прививочная реакция появляется через 4-6 недель. У ревакцинированных местная реакция развивается через 1-2 недели.
Как узнать, делали ли в роддоме прививку БЦЖ?
У 90-95% вакцинированных на месте прививки должен образоваться поверхностный рубец до 10,0 мм в диаметре. Размеры рубца могут быть разными. Считается, что если он меньше 4 мм, процесс вакцинирования проведен неэффективно и действие иммунитета не превысит трех лет. Размеры рубца от 5 мм и больше говорят об эффективной иммунизации БЦЖ. Размер до 8-10 мм говорит о положительном результате иммунизации сроком до семи лет.
След от прививки БЦЖ обычно сохраняется и во взрослом возрасте. Кроме того, дату прививки, серию и контрольный номер вакцины, предприятие-изготовитель, срок годности препарата указывают в истории новорожденного (медицинской карте).
А если рубец после вакцинации не образовался?
Отсутствие рубца после вакцинации показывает, что противотуберкулезный иммунитет не сформировался. Примерно у 10% детей нет правильной реакции после вакцинации, что может означать, что препарат был введен неверно, из-за чего иммунитет не сформировался, или же ребенок имеет врожденный иммунитет к туберкулезу. В таком случае необходимо провести тестирование Манту и при необходимости сделать повторное вакцинирование против туберкулеза.
Кому делают ревакцинацию?
Ревакцинации подлежат дети в возрасте 7 и 14 лет, имеющие отрицательную реакцию на пробу Манту. Реакцию считают отрицательной при полном отсутствии инфильтрата, гиперемии или при наличии уколочной реакции (1 мм). Инфицированные туберкулезными микобактериями дети, имеющие отрицательную реакцию на пробу Манту, ревакцинации не подлежат.
Интервал между постановкой пробы Манту и ревакцинацией должен быть не менее 3 дней и не более 2 недель.
Прививки в роддоме
Как правило, ещё в роддоме, новорождённым должны сделать две вакцины. В первую очередь это вакцина БЦЖ, то есть против туберкулёза, а также вакцина от гепатита В. Однако, в наши дни увеличиваются масштабы отказа родителей от вакцинации новорождённых.
Данный вопрос скорей всего является крайне спорным, так как, в первую очередь отказываются от вакцинации молодые родители, которые за 9 месяцев успевают осведомиться обо всех сторонах жизни ещё не родившегося ребёнка.Насколько правы в своих рассуждениях об отказе молодые родители, и правы ли судить не нам. В наших силах дать информацию для размышления.
Как правило, ещё в роддоме, новорождённым должны сделать две вакцины. В первую очередь это вакцина БЦЖ, то есть против туберкулёза, а также вакцина от гепатита В.
Вакцинация против туберкулёзаИз-за крайне высокой вероятности заражения, а также из-за ежедневно растущего количества заражённых людей всевозможными инфекционными болезнями, уже при рождении, ребёнку незамедлительно делают вакцину против туберкулёза. Это необходимая защита вашего малыша, так как у туберкулёза воздушно-капельный механизм передачи инфекции, при этом абсолютно незаметным образом для самой «жертвы». Поражает туберкулёз органы и ткани человека, чаще всего оставаясь незаметным до определённого момента. Именно из-за высокой опасности заражения нашим крошечным и пока ещё беззащитным деткам, так необходима данная вакцина. Благодаря ей, вы получаете грандиозную возможность защитить вашего ребёнка от этого страшного заболевания, уносящего ежегодно около двух миллионов людских жизней.
Вакцина помогает организму разработать иммунитет против туберкулёза, ведь иногда даже не обязательно находиться в прямом контакте с человеком, заражённым и при этом попасть в сети этой беспощадной болезни.
Вакцинация против туберкулёза проводится уже на третий день жизни ребёнка. После ввода вакцины в левое плечо младенца, на этом месте образуется белый «волдырь», который проходит достаточно быстро, буквально в течение 20 минут. Не позже, чем через год, проходит и след на плече малыша, в виде небольшого уплотнения.
Вакцинация против гепатита ВОпасным недугом, от которого следует защитить своего малыша с рождения, является гепатит В. Тем более, что именно младенцы в первую очередь находятся в группе риска.
Вирус гепатита В поражает печень приводя к ряду ещё более неприятных последствий (один из которых это рак). Крайне опасен тот факт, что гепатит может развиваться бессимптомно первое время, что даёт время вирусу как можно глубже «засесть» в организме инфицированного.
В случаях, когда ребёнок родился у женщины с хронических гепатитом, ему проводится вакцинация в первые же часы после рождения (не более чем через 12 часов). Если же ребёнок родился недоношенным, то вакцину проводят только тогда, когда его вес достигнет двух килограмм. При обычной вакцинации, ребёнку делают соответствующий укол в любой день до момента выписки из роддома. Вакцинация ребёнка проводится в область бедра, по разным сценариям. Это может быть трижды, с периодичностью: до выписки из роддома, через месяц после этого, и последняя вакцина по истечении шести месяцев после первой. Или, при экстренном вакцинировании, в течение первых 12-ти часов, затем так же через месяц, и потом по истечении двух месяцев.
Если одна из схем была проведена, то это станет гарантом иммунитета ребёнка от гепатита на первые 15 лет жизни.
Могут быть и последствия после вакцины против гепатита, такие как: след в виде покраснения или уплотнения на месте укола, температура, сыпь, боль в мышцах или суставах. Несмотря на все последствия, иногда нелицеприятные, выбор о том, делать или нет вакцину, должен быть сделан на основе существенных аргументов. Ведь вы, в первую очередь, ставите под вопрос здоровье вашего малыша — не забывайте об этом.
почему не осталось следа, не видно прививку
Вакцина от туберкулеза создается из штамма ослабленных живых коровьих туберкулезных палочек, которые утратили вирулентность для человеческого организма. В организм здоровых новорожденных ее вводят на 3–5 день жизни.
Ревакцинация БЦЖ проводится в семилетнем возрасте. У большинства людей формируется специфический рубец. Но бывают случаи, когда шрам не остается.
Google+
Vkontakte
Odnoklassniki
Характеристика БЦЖ у ребенка
Вакцинация необходима для предотвращения тяжелых форм туберкулеза. БЦЖ не уменьшает распространенность заболевания, она предназначена для профилактики развития тех типов туберкулеза, которые отличаются высокой летальностью.
Решение о необходимости проведения поголовной вакцинации обусловлено неблагополучной эпидемиологической обстановкой.
Новорожденным детям вакцину вводят внутрикожно в левое плечо в районе прикрепления дельтовидной мышцы. Этот участок расположен между центральной и верхней третью плеча. В зависимости от состояния новорожденного ему могут ввести БЦЖ или БЦЖ-м (ослабленный вариант, предназначенный для недоношенных, маловесных детей).
При правильном введении сразу после инъекции образуется папула. Ее диаметр не превышает 10 мм. На протяжении получаса она рассасывается. Это основной признак правильно сделанной прививки.
Справка! Неправильное введение вакцины приводит к появлению осложнений. При подкожной инъекции у некоторых начинается абсцесс, который изъявляется. Нормализовать состояние можно путем длительного приема антибиотиков.
Реакция на БЦЖ появляется не сразу. Она должна быть отсроченной. Как правило, спустя 4–6 недель на месте инъекции формируется гнойничок. Со временем он покрывается корочкой и постепенно заживает.
При отсутствии осложнений процесс заживления длится до 4,5 месяцев. Изначально место инъекции краснеет или окрашивается в фиолетовый, синий, черный цвет. Пугаться родители не должны – это вариант нормы. На месте потемнения, покраснения появляется гнойник, в центре которого расположена короста. Но у некоторых образуется красноватый пузырек, наполненный жидкостью. Иногда гнойники прорываются, их содержимое выливается.
Внимание! Обрабатывать ранку антисептиками, посыпать порошковыми антибактериальными средствами или делать йодную сетку не надо. Не советуют также выдавливать из ранки гной.
Об удачно проведенной прививке БЦЖ и формировании иммунного ответа свидетельствует образовавшийся шрам. Формируется рубчик длиной от 2 до 10 мм. При его отсутствии разберитесь с тем, почему возникла такая ситуация. Чем больше размер рубца, тем сильнее выработанный иммунитет:
- 2–4 мм: защита действует на протяжении 3–4 лет;
- 5–8 мм: действия вакцины хватит на 4–7 лет;
- от 8 мм: иммунитет от туберкулеза сформировался на период более 7 лет.
Фото 1. Размер рубца от БЦЖ у ребенка около 5-8 мм, поэтому действия вакцины хватит на 4-7 лет.
Правильная реакция на прививку выглядит следующим образом.
- На месте инъекции появляется белая папула, которая исчезает через 10–30 минут.
- Через 4–6 недель место ввода вакцины краснеет, появляется гнойник или пузырек с жидким содержимым, на поверхности образуется короста. У некоторых гной может вытекать. В этом случае рекомендуется покрыть участок стерильной салфеткой и менять ее по мере необходимости.
- Спустя 3–4 месяца место инъекции полностью заживает, образуется шрам.
Это нормальная реакция организма на БЦЖ.
Почему нет следа от прививки
У некоторых привитых малышей рубец после инъекции не видно. Эта ситуация встречается часто: у 5–10% детей от первой прививки не остается никаких следов. К основным причинам этого относят:
- нарушение технологии вакцинации;
- использование испорченной либо просроченной вакцины;
- наличие врожденного мощного противотуберкулезного иммунитета.
Врожденная устойчивость к микобактериальным поражениям наблюдается у 2% населения. У этих людей след не появится даже после многократных инъекций БЦЖ. Туберкулезом они не болеют, а реакция Манту всегда отрицательная. Инфицирование возможно только при сильном снижении иммунитета, например, на фоне ВИЧ-инфекции.
Но выяснить, вызвано ли отсутствие рубца врожденной иммунной защитой, или его нет из-за использования некачественной вакцины, сложно. Контролировать состояние позволяет регулярная проверка с помощью реакции Манту. Если она будет отрицательной, то делают ревакцинацию.
Некоторые рекомендуют повторно сделать вакцинацию БЦЖ после того, как было выявлено, что от шрама не осталось следа. Другие говорят дожидаться семилетнего возраста для проведения плановой ревакцинации.
У людей с врожденным противотуберкулезным иммунитетом шрам не появится. Если иммунный ответ не сформировался из-за использования некачественного сырья либо его неправильного введения, то человек находится в группе риска. При инфицировании риск перехода заболевания в открытую форму и летального исхода повышается. У привитых людей вероятность появления менингита и прочих диссеминированных типов туберкулезного поражения, которые приводят к смерти, намного ниже.
Вам также будет интересно:
Не осталось следа после проведения ревакцинации
Повторное введение вакцины необходимо даже детям, у которых остался след от вакцинации. Оно проводится для повышения невосприимчивости организма к воздействию микобактерий.
Как правило, поголовную ревакцинацию проводят в регионах, где туберкулез широко распространен. Она обязательна для детей, в семье которых есть люди с этим заболеванием.
У некоторых малышей рубец на месте введения вакцины не формируется вовсе, у других – исчезает со временем. Это свидетельствует об отсутствии поствакцинального иммунитета. Дети с пропавшим шрамом от БЦЖ приравниваются к тем, кому не проводили вакцинацию. Ситуации, когда рубец рассасывается, встречаются нечасто. Медики говорят о том, что это свидетельствует об отсутствии иммунитета. Ревакцинацию в такой ситуации советуют проводить в кратчайшие сроки.
В случаях, когда рубца от БЦЖ не осталось, повторное введение препарата является обязательным. Это необходимо для формирования иммунитета. Иначе риски развития тяжелых форм болезни, приводящих к смерти, остаются на высоком уровне.
Но предварительно делают пробу Манту. Вакцинацию БЦЖ проводят лишь при условии, что местная реакция на предплечье от туберкулиновой пробы отсутствует: допустима визуализация следа от укола. Введение вакцины проводят сразу после подтверждения отрицательной реакции на введенный туберкулин. Максимально допустимый временной промежуток между постановкой Манту и БЦЖ составляет 2 недели.
Если нет следа и отрицательной Манту рекомендуют повторное введение живой вакцины не в стандартные сроки (в 7 либо 14 лет), а через 2 года. Если первая туберкулиновая проба была отрицательной, а через год наблюдается вираж (появилась положительная реакция), то обязательна консультация фтизиатра.
Делать БЦЖ при положительной либо сомнительной Манту нельзя. Эта ситуация попадает в перечень противопоказаний к проведению ревакцинации.
Справка! Если Т-лимфоциты ранее контактировали с палочкой Коха, то в месте введения туберкулина возникнет специфическое воспаление. Если иммунная система не знакома с возбудителем туберкулезной инфекции, то папула будет отсутствовать.
Вводить БЦЖ детям, у которых иммунная система отреагировала на туберкулин, категорически запрещено.
Инструкция для родителей: что делать, если не видно прививку БЦЖ
Если малышу ввели БЦЖ или БЦЖ-м, то через несколько месяцев у него появляется характерный шрам на плече. При его отсутствии проконсультируйтесь с педиатром и, при необходимости, с фтизиатром.
Такая ситуация возникает при использовании некачественной (просроченной) вакцины, неправильном введении препарата либо при наличии мощного врожденного иммунитета.
Фото 2. На месте введения вакцины у ребенка остался шрам, значит, вакцина была качественная.
Обратите внимание на такие моменты:
- при отсутствии следа от БЦЖ медики рекомендуют повторную вакцинацию через 2 года после первой прививки;
- обязательным условием ревакцинации является отрицательная реакция Манту;
- при появлении сомнительных или положительных результатов туберкулиновой пробы БЦЖ ставить запрещено.
Если у ребенка нет рубца после введения ослабленной палочки Коха, то родители должны минимизировать контакт малыша с потенциальными туберкулезными больными. Ведь вероятность инфицирования и перехода заболевания в тяжелую форму у них выше. Таких пациентов педиатры и фтизиатры рекомендуют ревакцинировать.
Полезное видео
Мнение доктора Комаровского о вакцине БЦЖ: можно ли уберечься от заболевания, сделав прививку, в каких местах есть риск заражения?
Оцени статью:Будь первым!
Средняя оценка: 0 из 5.
Оценили: 0 читателей.
Google+
Vkontakte
Odnoklassniki
нет у ребенка, рубца, прививки, шрам, норма, почему остается, у новорожденных, отзывы, на плече, втянутый, что значит, доктор Комаровский, по месяцам у детей, келоидный, поствакцинальный, когда появляется, формирование
Туберкулез — опасная и достаточно распространенная болезнь, поражающая и детей, и взрослых. Чтобы сократить случаи заболевания и предотвратить возникновение тяжелых форм этой патологии, в России проводится регулярная вакцинация. Это прививка №1 в национальном календаре вакцинации.
Начальный этап приходится на первые дни жизни новорожденного. Инъекцию делают ребенку еще в роддоме. Предварительно у младенца проверяют реакцию Манту, она должна быть отрицательной.
На месте укола образуется характерный след от БЦЖ. По нему можно определить, насколько эффективной была вакцинация. Считается, что чем больше в диаметре рубец (до 1 см), тем более крепкий образовался иммунитет.
Продолжают профилактику туберкулеза в школе. Ревакцинацию проводят в семилетнем возрасте. Считается, что к этому времени след от 1 прививки становится едва различимым. Это значит, что действие вакцины закончилось и нужна новая прививка.
Медики утверждают, что после ревакцинации смертность от туберкулеза снижается, потому проводить ее нужно обязательно.
Особенности образования шрама на месте прививки
Характерный шрам от БЦЖ на левом предплечье — это норма. Рубец свидетельствует, что вакцинация прошла эффективно и человек привит от туберкулеза.
После введения вакцины, в которой присутствуют ослабленные бактерии, в месте укола возникает локальное заражение туберкулезом. Организм справляется с инфекцией, в крови вырабатываются антитела, и человек считается защищенным от вируса туберкулеза.
После инъекции, которую делают внутрикожно, на месте укола образуется папула. Это нормальная реакция на прививку. Она имеет средний диаметр — не более 1 см. Спустя 0,5 часа папула должна рассосаться без следа. Это свидетельствует о правильно сделанной прививке, а также о том, что формирование иммунитета началось.
Через некоторое время на месте введения вакцины начинается нагноение, ранка может приобретать синюшный или фиолетовый цвет, полость может периодически наполняться гнойным содержимым.
Это означает, что процесс формирования иммунитета продолжается. Нередко такая реакция организма пугает родителей. Однако это не повод для волнения — со временем рана очистится. Может пройти несколько месяцев, прежде чем завершится формирование иммунитета.
В месте инъекции образуется небольшой рубец, который медики называют поствакцинальным знаком.
Осложнения на месте укола
Если вакцина была сделана с нарушением, на месте укола может возникнуть осложнение.
Если препарат введен неправильно — не внутрикожно, а подкожно, в этом месте может образоваться холодный абсцесс — болезненное уплотнение. В этом случае необходимо обратиться к врачу.
Неправильно сделанный укол может привести к образованию келоидного рубца из соединительной ткани, который имеет плотную структуру и неправильную форму. Удаляют его хирургическим путем.
Почему нет рубца
Если в месте введения препарата не образуется характерный след, врачи утверждают, что вакцинация не удалась и ребенок остается не привитым, т. е. находится в группе риска.
Если не остается нормальной реакции организма на БЦЖ, это повод для консультации с врачом. Он может назначить дополнительное обследование ребенка и решить вопрос о повторном введении препарата.
Если шрам не образуется вовсе, это может свидетельствовать о том, что у ребенка высокий врожденный иммунитет к туберкулезу. Ослабленный вирус после введения вакцины сразу же погибает, не успевая создать искусственный иммунитет.
Если рубец был но исчез
Если нет следа от БЦЖ, значит, действие вакцины закончилось. У большинства взрослых людей такой шрам отсутствует.
У детей исчезновение шрама БЦЖ означает, что иммунитет к заболеванию снизился и необходима ревакцинация.
Профилактика
Чтобы рубчик БЦЖ был более аккуратным, можно принять некоторые меры.
Прививаться нужно только в условиях медицинского учреждения и качественной вакциной.
Тем самым можно исключить возможность инфицирования ранки.
После проведения ревакцинации важно правильно ухаживать за ранкой. Нельзя вскрывать образовавшуюся полость, выдавливать гной, мазать больное место спиртосодержащими препаратами — зеленкой или йодом. Нужно объяснить ребенку, что язвочку нельзя расчесывать. Нельзя также заклеивать это место лейкопластырем. Нужно дождаться, пока процесс завершится естественным путем, и ранка очистится самостоятельно после образования шрама.
Чтобы избежать заболевания туберкулезом, нельзя отказываться от прививки БЦЖ. Не имея иммунитета, сформированного в детстве, при инфицировании вирусом можно получить тяжелую форму заболевания, которая может привести к негативным последствиям, в том числе и к летальному исходу.
Нет следа от прививки БЦЖ или от Манту у ребенка
Что делать, если нет следа от БЦЖ у маленького ребенка? Этот вопрос вводит в недоумение многих мам, потому что иммунитет против туберкулеза имеет значение для новорожденного.
Туберкулез – острое инфекционное заболевание, локализующееся преимущественно в легких и представляющее серьезную угрозу для жизни человека. Возбудители инфекции очень часто встречаются в окружающей среде, поэтому человеку очень важно иметь хороший иммунитет против данной болезни. В связи с этим прививку от туберкулеза или БЦЖ, делают детям еще в раннем возрасте – при выписке из роддома. По поводу данной прививки у родителей часто возникают разнообразные вопросы. Но больше всего молодые мамы и папы не понимают, что делать, если через несколько месяцев после введения вакцины в плечо ребенка на месте укола не остаётся рубца. Почему его наличие необходимо и чем грозит его отсутствие?
Как происходит вакцинация БЦЖ
При нормальных обстоятельствах, если нет противопоказаний и иных факторов, запрещающих осуществление вакцинации, прививку от туберкулеза ставят младенцу перед его выпиской из роддома. При этом вакцину вводят внутрикожно в левое плечо. Кроме того, существуют исключительные случаи, когда прививку делают в бедро, но они происходят отнюдь не часто, и в основном укол проводится в плечо.
Если по какой-либо причине вакцинацию БЦЖ не сделали в роддоме, ее можно провести в своей поликлинике либо не выходя из дома, если вызвать медицинскую бригаду.
Таким образом, выделяются три основных способа проведения прививки БЦЖ:СЕНСАЦИЯ ! Перейди по ссылке:
- В роддоме.
- В местной поликлинике.
- Дома, с вызовом медицинской бригады.
После правильного ввода вакцины в слой кожи на месте укола появляется папула – небольшая круглая подушечка диаметром до 10 мм, как от Манту. Спустя полчаса папула рассасывается. Это сигнализирует о правильно сделанной прививке. Если в дальнейшем все будет идти «по инструкции», то по истечении полутора месяцев на месте прививки должна появиться пустула с явными гнойными процессами. Некоторые родители пугаются, заметив такую болячку у своего ребенка. На самом деле воспалительный процесс на месте укола является абсолютно нормальной реакцией организма на БЦЖ. Из пустулы может выделяться гной, который надо убирать чистой салфеткой. Пользоваться зеленкой или другими антибактериальными средствами категорически нельзя.
Еще через полмесяца ранка начнет заживать и покрываться характерной корочкой. Необходимо, чтобы она отсохла и отшелушилась сама, без чьей-либо помощи. Когда это произойдет, на месте укола останется след от прививки БЦЖ характерный рубец. По нему можно судить об успешности проведенной вакцинации.
Эффективность БЦЖ
Как узнать, насколько эффективной оказалась проведенная процедура? Об этом скажут размеры, которыми обладает след от БЦЖ.
О нормальной реакции организма на вакцину сигнализируют следующие проявления:
- появление круглой «подушечки» сразу после укола;
- формирование покраснения, а затем и образование гнойного очага;
- выделение гноя из-под коросты и формирование нового очага;
- появление рубца.
Хороший след от гнойного очага должен иметь размеры от 3-х до 10-и миллиметров в диаметре. Рубец – явный признак устоявшегося противотуберкулезного иммунитета у ребенка. Также по диаметру следа от укола можно узнать, как долго будет держаться иммунитет.
Различают три вида рубцов:
СЕНСАЦИЯ ! Перейди по ссылке:
- Маленькие (имеют размер менее 4 мм). В данном случае можно говорить о малой эффективности вакцинации. Иммунитет вряд ли продержится более трех лет.
- Средние – от 5 до 8 мм. Вакцинация хорошего качества. Должно хватить на 5-7 лет.
- Большие – от 8 мм и более. Как правило, в таких случаях иммунитет против туберкулеза длится 7 и более лет.
Большой вопрос, которым озадачены некоторые родители, это: «Почему нет следа от БЦЖ, и что это может значить?» Ведь у некоторых детей после укола вообще не остается никаких следов, за исключением маленькой точки от самой иглы.
Почему нет рубца
По каким причинам у ребенка нет следа от прививки БЦЖ? Если было проведено вакцинирование, но по истечении трех месяцев с момента укола на коже не появилось никаких следов, узнать причину отсутствия нормальной реакции поможет тест Манту.В основном, рубец не возникает по двум причинам:
- Либо имеют место нарушения в технологии введения вакцины в кожу, либо испорчен сам состав вакцины.
- Когда организм имеет мощный противотуберкулезный иммунитет от природы, и в дополнительной защите не нуждается.
Если тест Манту окажется отрицательным, необходимо будет провести повторную вакцинацию. В таком случае, скорее всего, были допущены ошибки в процессе вакцинации. Иногда повторную прививку делают через семь лет. Однако тогда на протяжении всего этого времени такие дети должны проходить тест Манту не как обычно раз в год, а два раза в год, чтобы избежать заболевания туберкулезом.
Если первая причина отсутствия рубца говорит об отсутствии иммунитета, то вторая причина свидетельствует об обратном. Почти 2% всех жителей планеты имеют мощную врожденную защиту от туберкулеза и некоторых других заболеваний. Организм таких людей ликвидирует возбудители инфекции еще до того, как начинают вырабатываться антитела. Поэтому рубца после БЦЖ нет, как нет и покраснения после теста Манту. Как правило, такие дети не могут заболеть туберкулезом при нормальных условиях, если нет факторов, сильно ослабляющих иммунную систему, как, например, ВИЧ.Рубец после БЦЖ исчез спустя несколько лет – что это значит? Это говорит о том, что действие вакцины закончилось, и требуется ревакцинация.
Необходимость в повторной прививке легко подтверждается тестом Манту – он показывает отрицательный результат, в то время как при наличии искусственно созданного противотуберкулезного иммунитета после Манту на руке ребенка будет образовываться покраснение.
Отсрочка вакцинации БЦЖ от рождения до возраста 10 недель может привести к усилению ответа Т-лимфоцитов CD4
Резюме
Общие сведения
В большинстве эндемичных по туберкулезу стран бацилла Кальметта Герена (БЦЖ) обычно вводится при рождении. предотвратить тяжелую форму туберкулеза у младенцев. Иммунная система новорожденного еще не сформировалась. Наша гипотеза заключалась в том, что отсрочка вакцинации БЦЖ от рождения до 10-недельного возраста усилит иммунный ответ, индуцированный вакциной.
Методы
В рандомизированном клиническом исследовании БЦЖ вводили внутрикожно либо при рождении (n = 25), либо в возрасте 10 недель (n = 21).Через десять недель после вакцинации и в возрасте 1 года были измерены вакцино-специфические Т-клеточные ответы CD4 и CD8 с помощью анализа внутриклеточных цитокинов цельной крови.
Результаты
Младенцы, получившие отсроченную вакцинацию БЦЖ, демонстрировали более высокую частоту БЦЖ-специфических Т-лимфоцитов CD4, особенно полифункциональных Т-клеток, коэкспрессирующих IFN-γ, TNF-α и IL-2, и особенно ярко в возрасте 1 года.
Выводы
Отсрочка вакцинации БЦЖ от рождения до возраста 10 недель усиливает количественный и качественный БЦЖ-специфический Т-клеточный ответ при измерении в возрасте одного года.
Ключевые слова: БЦЖ, вакцинация, рождение, отсроченное, полифункциональные Т-лимфоциты CD4
Введение
Бацилла Кальметта Герена (БЦЖ), единственная современная вакцина против туберкулеза (ТБ), представляет собой живой аттенуированный штамм Mycobacterium bovis. Ежегодно более 100 миллионов детей во всем мире получают вакцину БЦЖ [1]. Вакцинация БЦЖ обеспечивает защиту от тяжелых форм детского туберкулеза, т. Е. Туберкулезного менингита и милиарного туберкулеза [1, 2]. Защита, обеспечиваемая вакцинацией БЦЖ от легочного туберкулеза, наиболее распространенной формы туберкулеза, неодинакова и в основном низка [3].Факторы, которые участвуют в различной защите БЦЖ от туберкулеза, включают штамм БЦЖ, дозу БЦЖ, предшествующее воздействие нетуберкулезных микобактерий (NTM) из окружающей среды, генетические вариации хозяина, штамм Mycobacterium tuberculosis ( M.tb ) и способ вакцинации. [3–7].
CD4 Т-клетки, которые продуцируют Т-хелперные цитокины типа 1 (Th2) IFN-γ, TNF-α и IL-2, считаются критическими для защиты от туберкулеза [8, 9]. Такой ответ Th2 характерен для вакцинации БЦЖ [10, 11].В регионах, где широко распространен ТБ, вакцинация БЦЖ широко проводится при рождении или вскоре после него из-за риска раннего контакта с M.tb [12]. Существуют доказательства того, что ответ Th2 при рождении является «незрелым», например, прогрессивное повышение специфического опосредованного клетками Th2 иммунитета было показано, когда вакцина против кори вводилась в возрасте 6, 9 и 12 месяцев соответственно [13]. Мы предположили, что созревание иммунной системы новорожденных до 10-недельного возраста до вакцинации БЦЖ повысит индуцированный вакцинацией Т-клеточный иммунитет.Эффект оптимизации сроков вакцинации может иметь важные последствия для улучшения защиты от туберкулеза с помощью вакцинации БЦЖ.
Марчант, и др. сообщил, что изменение возраста вакцинации БЦЖ не влияет на иммуногенность БЦЖ при оценке продукции интерферона гамма (IFN-γ) мононуклеарными клетками периферической крови (PBMC), стимулированными микобактериальными антигенами [10]. В небольшом исследовании Hussey, et al. также сообщил, что отсрочка вакцинации БЦЖ от рождения до возраста 10 недель не влияет на секрецию IFN-γ, пролиферативные ответы или цитотоксический потенциал БЦЖ-специфичных Т-клеток после инкубации PBMC с микобактериальными антигенами [14].С тех пор как появились эти результаты, мы показали, что измерение одного IFN-γ недооценивает сложность Th2-ответа, индуцированного БЦЖ. Вакцинация БЦЖ у младенцев индуцирует множественные подмножества Th2, что определяется экспрессией различных комбинаций IFN-γ, TNF-α и IL-2 специфическими клетками [11]. Мы хотели всесторонне изучить влияние возраста на величину и качество Th2-иммунитета, индуцируемого БЦЖ у младенцев.
Материалы и методы
Набор участников и последующее наблюдение
Участники были зарегистрированы в период с апреля 2006 г. по март 2008 г. в Хайелитше, пригороде Кейптауна с чрезвычайно высокой заболеваемостью туберкулезом, составившей 1614 на 100000 в первом квартале. 2008 г. (Уровень уведомления о случаях, город Кейптаун).
Это было частью более крупного исследования, посвященного изучению клинических и иммунологических характеристик новорожденных, подвергшихся и не подвергавшихся воздействию ВИЧ. Короче говоря, в государственную женскую консультацию к беременным обращались с просьбой принять их младенцев. Для исследования, представленного здесь, младенцы, которые родились от ВИЧ-инфицированных женщин или женщин с неизвестным ВИЧ-статусом, подвергались активному туберкулезу в семье, родились преждевременно (гестационный возраст ≤36 недель) или имели низкий вес при рождении (≤2,5 кг), или те, у кого были значительные перинатальные осложнения, были исключены.Кроме того, были исключены все младенцы с положительным ответом IFN-γ на ESAT-6 / CFP-10 в возрасте 10 недель (подробности анализа см. Ниже). Младенцы были случайным образом распределены во время дородового набора для получения вакцины БЦЖ (внутрикожный датский штамм 1331, Statens Serum Institute) в первый день жизни («вакцинация при рождении») или аналогичной вакцинации БЦЖ в возрасте 10 недель («отложенная вакцинация»). Младенцы наблюдались в возрасте 10, 20 и 50 недель. Был разрешен период окна от -2 до +4 недель вокруг посещения 10-й недели (например,грамм. От 8 до 14 недель). Период времени для 20-недельного посещения составлял от 18 до 28 недель и от 41 до 54 недель для 50-недельного посещения.
Разрешение регулирующих органов было получено от комитетов по этике исследований Стелленбошского и Кейптаунского университетов. Письменное информированное согласие было получено от всех матерей на их родном языке. Все тесты на ВИЧ проводились в сочетании с информированным согласием и консультированием до и после тестирования.
Сбор крови и анализ внутриклеточных цитокинов
Один мл крови собирали в возрасте 10, 20 и 50 недель в гепаринизированные шприцы.Цельную кровь обрабатывали в течение 2 часов после сбора, как описано ранее [15]. Вкратце, 250 мкл цельной крови инкубировали в течение 12 часов при 37 ° C с жизнеспособной БЦЖ (восстановленной из флакона с вакциной, датский штамм, Staten Serum Institute, 1,2 × 10 6 КОЕ / мл) и костимулирующими антителами анти-CD28. и анти-CD49d (BD Biosciences, 0,5 мкг / мл каждый). 250 мкл крови, инкубированной со стафилококковым энтеротоксином B (SEB, Sigma, 10 мкг / мл), и 250 мкл крови, инкубированной только с костимулирующими антителами (нестимулированными), служили в качестве положительного и отрицательного контролей соответственно.Брефельдин A (Sigma, 10 мкг / мл) добавляли в течение последних 5 часов инкубации. После инкубации эритроциты лизировали и лейкоциты фиксировали лизирующим раствором BD FACS Lysing Solution (BD Biosciences), а клетки криоконсервировали.
Криоконсервированные клетки позже оттаивали и промывали 1% бычьим сывороточным альбумином (Sigma) в фосфатно-солевом буфере (PBS, BioWhittaker) и повышали проницаемость, используя раствор Perm / Wash Solution (BD Biosciences). Затем клетки окрашивали следующими антителами: анти-CD3 Pacific Blue (клон UCHT1), анти-CD4 PerCPCy5.5 (SK3), анти-CD45RA PECy7 (L48), анти-IFN-γ AlexaFluor700 (B27), анти-IL-2 FITC (5344.111), анти-TNF-α PE (MAb11; все от BD Biosciences), анти- CD8 Qdot605 (3B5, Invitrogen) и анти-CCR7 APC (150503, R&D Systems). После промывок клетки собирали на проточном цитометре LSR II (BD Biosciences), для этого эксперимента использовали 3 лазера и 10 детекторов с использованием программного обеспечения FACS Diva 6.1. Параметры компенсации были установлены с использованием каппа-шариков против мышей (BD Biosciences), меченных соответствующими антителами, конъюгированными с флуорохромом.Flowjo 8.7.1 (Treestar) использовался для компенсации и анализа данных проточной цитометрии. Для создания комбинаций цитокинов, экспрессирующих субнаборы Т-клеток CD4 и CD8, применяли логическое стробирование ().
Стратегия гейтинга, используемая для анализа Т-клеточных цитокиновых ответов CD4 и CD8Цельную кровь инкубировали с БЦЖ для завершения проточного цитометрического анализа внутриклеточных цитокинов, как описано в Методиках.
( A ) Дублетные клетки были исключены путем стробирования по площади прямого рассеяния (FSC-A) против высоты прямого рассеяния (FSC-H), а затем лимфоциты были отобраны в FSC-A против площади бокового рассеяния ( SSC-A) точечный график.Т-клетки отбирали путем стробирования событий CD3 + , которые далее дифференцировались в Т-клетки CD4 и CD8. ( B) Типичные точечные диаграммы паттернов коэкспрессии цитокинов в CD4 Т-клетках в нестимулированных, стимулированных БЦЖ и SEB условиях.
Анализ интеркуррентной инфекции
M. tuberculosisВ каждый момент времени цельную кровь разбавляли 1: 5 в среде для культивирования тканей RPMI-1640 (Sigma), содержащей 1% L-глутамин (Sigma), и инкубировали с ESAT -6 / CFP-10 слитый белок (предоставлен Томом Оттенхоффом, Медицинский центр Лейденского университета, 10 мкг / мл), фитогемагглютинин (PHA, Sigma, 5 мкг / мл) и SEB (1 мкг / мл; оба положительных контроля) или отсутствие антигена ( отрицательный контроль) в трех экземплярах в 96-луночных планшетах (модифицировано из Black et al ) [16].Планшеты инкубировали при 37 ° C с 5% CO 2 в течение 7 дней, супернатанты собирали, три лунки объединяли и хранили при -80 ° C. Позже супернатанты оттаивали, и сэндвич-ELISA на IFN-γ использовали для количественного определения IFN-γ в супернатантах, полученных в результате 7-дневного анализа цельной крови (BD Pharmingen). Положительный ответ IFN-γ был определен как 62 пг / мл после вычитания фона (удвоенный предел обнаружения анализа 31 пг / мл). Младенцы с признаками интеркуррентной инфекции / контакта M. tuberculosis в возрасте 10, 20 или 50 недель были исключены из анализа.
Анализ данных
Для анализа внутриклеточных цитокинов уровни экспрессии цитокинов в нестимулированной крови вычитали из уровней, полученных после стимуляции БЦЖ. (Средний уровень экспрессии IFN-γ, IL-2 и TNF среди Т-лимфоцитов CD4 в нестимулированной крови составлял 0,002%, 0,03% и 0,06% соответственно.) Различия в массе тела при рождении и полу участников оценивались с помощью параметрических тестов. U-критерий Манна-Уитни использовался для оценки различий в частотах экспрессии цитокинов CD4 и CD8 Т-клеток между двумя группами.Значения P ниже 0,05 считались значимыми.
Результаты
Характеристики участников
Всего в исследование было включено 46 младенцев: 25 в группе рождения и 21 в группе отсроченной вакцинации. Младенцы, не явившиеся для проведения флеботомии в определенный момент времени, с кровотечением за пределами определенного периода окна на 10 неделе посещения или положительными на инфекцию M.tb , были исключены из анализа (). Результаты для младенцев с инфекцией M.tb были исключены из временной точки, в которой это было диагностировано, и из последующих временных точек.На исходном уровне не наблюдалось различий в массе тела при рождении или полу между группой рождения и группы отсроченной вакцинации (средний вес при рождении, (SD): 3306 г (435,6) при рождении против 3200 г (371,9) при задержке; p = 0,390). Шестнадцать (64%) младенцев в группе рождения были мальчиками по сравнению с 9 (43%) младенцами в группе отсроченных родов (p = 0,235).
Обзор правомочности, потока исследования и участников
Обнаружение БЦЖ-специфичных CD4 Т-клеток с использованием жизнеспособной БЦЖ в качестве антигена
Перед тем, как сравнивать БЦЖ-индуцированный иммунитет между новорожденными и отложенной вакцинацией, мы оценили, была ли инкубация целых кровь с жизнеспособной БЦЖ может привести к неспецифической активации Т-клеток или к обнаружению вакцино-специфического ответа.Мы сравнили Т-клеточный иммунитет CD4, измеренный в возрасте 10 недель с помощью анализа внутриклеточного определения цитокинов (: пример результатов анализа), между участниками, которые получали БЦЖ при рождении, и теми, кто еще не принимал БЦЖ (младенцы в группе отсроченного приема). . Продукция цитокинов CD4 Т-клетками легко определялась у младенцев из группы, вакцинированной при рождении, но не обнаруживалась или обнаруживалась только на очень низких уровнях у младенцев, не получивших вакцину при рождении (). Младенцы, вакцинированные при рождении, имели высокие частоты полифункциональных Т-лимфоцитов CD4, специфичных для БЦЖ, т.е.е. Т-клетки CD4, которые вместе экспрессируют IFN-γ, TNF-α и IL-2, и Т-клетки CD4, экспрессирующие другие комбинации цитокинов Th2. Полифункциональные БЦЖ-специфические CD4 Т-клетки отсутствовали у младенцев в группе отсроченной вакцинации. У всех младенцев был положительный ответ на положительный контроль, SEB (данные не показаны). Мы пришли к выводу, что ответы Т-клеток, измеренные с помощью нашей системы анализа, когда БЦЖ используется в качестве антигена, являются антиген-специфическими, а не обусловлены неспецифической активацией Т-клеток.
Сравнение ответов Т-лимфоцитов CD4 после инкубации цельной крови из крови вакцинированных БЦЖ и невакцинированных младенцев с БЦЖ в возрасте 10 недельЧастоты Т-лимфоцитов CD4, экспрессирующих цитокины, обнаруженные с помощью анализа внутриклеточных цитокинов цельной крови (см. Методы) показаны.Медиана представлена горизонтальной линией, межквартильный размах — прямоугольником, а диапазон — усами. U-критерий Манна-Уитни использовался для расчета значений p различий между двумя группами.
Отсроченная вакцинация привела к умеренно более высокой частоте БЦЖ-специфичных Т-клеток CD4 через 10 недель после вакцинации
Чтобы оценить различия в ответах Т-лимфоцитов CD4 и CD8, когда вакцина вводилась при рождении или в возрасте 10 недель, мы измерили Паттерн экспрессии Th2-цитокинов, индуцированный БЦЖ через 10 недель после вакцинации, т.е.е., в возрасте 10 недель в группе рождения и в возрасте 20 недель в группе отсроченного рождения. В обеих группах наблюдались высокие частоты полифункциональных Т-лимфоцитов CD4 или клеток, экспрессирующих другие комбинации цитокинов Th2 (). IFN-γ + и IFN-γ + IL-2 + Частота субпопуляций CD4-Т-клеток, специфичных для БЦЖ, была значительно выше в группе отсроченной вакцинации по сравнению с группой вакцинации при рождении (). Поскольку частота индуцированных специфических субпопуляций CD8 Т-клеток была очень низкой, в обеих группах вакцинации оценивались только общие БЦЖ-специфические Т-клеточные ответы CD8: не было никакой разницы между двумя группами ().Мы пришли к выводу, что отсрочка вакцинации БЦЖ на 10 недель может привести к увеличению частоты БЦЖ-специфических CD4 Т-клеток через 10 недель после вакцинации.
БЦЖ-специфические Т-клеточные ответы через 10 недель после вакцинации у младенцев, получавших БЦЖ при рождении и тех, кто получил БЦЖ в возрасте 10 недель(A) Частоты БЦЖ-специфических цитокинов, экспрессирующих Т-клетки CD4, показаны в виде обнаруживается с помощью анализа внутриклеточных цитокинов цельной крови. (B) Частоты всех экспрессирующих CD8 Т-клеток, оцененные вместе, после инкубации цельной крови с БЦЖ.Медиана представлена горизонтальной линией, межквартильный размах — прямоугольником, а диапазон — усами. U-критерий Манна-Уитни использовался для расчета значений p различий между двумя группами.
Отсроченная вакцинация увеличивала частоту полифункциональных БЦЖ-специфических CD4 Т-клеток в возрасте одного года
Мы также сравнили БЦЖ-специфический ответ памяти в возрасте 50 недель. Мы наблюдали значительно более высокие частоты БЦЖ-специфичных полифункциональных IFN-γ + TNF-α + IL-2 + CD4 Т-клеток в группе отсроченной вакцинации по сравнению с группой вакцинации при рождении ().Частота специфических субпопуляций Т-клеток, коэкспрессирующих TNF-α и IL-2, TNF-α и IFN-γ или только TNF-α, также была выше в группе отсроченной вакцинации. В этом возрасте общие ответы Т-лимфоцитов CD8, специфичные для БЦЖ, были слишком низкими для надежного анализа данных (данные не показаны). При сравнении ответов на положительный контроль, SEB, различий между двумя группами не наблюдалось (дополнительная фигура 1). Мы пришли к выводу, что отсрочка вакцинации БЦЖ с рождения до возраста 10 недель приводит к количественному увеличению и качественно более оптимальному БЦЖ-специфическому ответу памяти CD4 Т-клеток в возрасте одного года.
БЦЖ-специфические ответы Т-лимфоцитов CD4 в 2 группах младенцев в возрасте 1 годаПоказаны частоты цитокин-экспрессирующих CD4 Т-клеток, обнаруженные с помощью анализа внутриклеточных цитокинов цельной крови. Медиана представлена горизонтальной линией, межквартильный размах — прямоугольником, а диапазон — усами. U-критерий Манна-Уитни использовался для расчета значений p различий между двумя группами.
Пики общего БЦЖ-специфического ответа Т-лимфоцитов CD4 в группах родов и отсроченной вакцинации достигаются через 10 недель после вакцинации. через 10 недель мы измерили общий ответ памяти Т-лимфоцитов CD4, специфичный для БЦЖ, в возрасте 10, 20 и 50 недель.Общие ответы обозначаются БЦЖ-специфическими CD4 Т-клетками, которые экспрессируют IFN-γ, TNF-α или IL-2, по отдельности или в комбинации. В группах рождаемости и отсроченной вакцинации БЦЖ-специфические ответы CD4 достигли пика через 10 недель после вакцинации и постепенно уменьшались в течение первого года жизни ().
Кинетика общих БЦЖ-специфичных ответов Т-лимфоцитов CD4 в группах отсроченной вакцинации и вакцинации при рождении в течение одного годаСредние частоты БЦЖ-специфичных общих цитокин-экспрессирующих CD4 Т-клеток, обнаруженных с помощью краткосрочного анализа внутриклеточных цитокинов цельной крови при 10, Возраст 20 и 50 недель.
Сопоставимый БЦЖ-специфический фенотип памяти Т-лимфоцитов CD4 в группах рождения и отсроченной вакцинации
Чтобы оценить, приводит ли отсрочка вакцинации БЦЖ к измененному вакцино-специфическому фенотипу памяти Т-клеток CD4, мы охарактеризовали цитокин, экспрессирующий БЦЖ-специфические Т-клетки. Фенотип памяти специфических Т-клеток, определяемый поверхностной экспрессией CD45RA и CCR7, на животных моделях, как было показано, определяет исход вакцинации [17]. Как в группе вакцинации при рождении, так и в группе отложенной вакцинации эффекторная память (CD45RA-CCR7-, T EM ) преобладала и во всех временных точках оценивалась (для данных в возрасте 1 года).В возрасте одного года не было значительных различий для T EM или центральной памяти (T CM , CD45RA — CCR7 + ) в двух группах младенцев ().
Сравнение фенотипа поверхностной памяти БЦЖ-специфических Т-лимфоцитов CD4 между двумя группами младенцев в возрасте 1 годаАнтигенспецифические Т-клетки CD4 были идентифицированы по экспрессии цитокинов с помощью анализа внутриклеточных цитокинов цельной крови. (A) Графики в виде прямоугольников и усов, изображающие фенотип памяти всех BCG-специфичных CD4 T-клеток, проанализированных вместе.(B) Репрезентативные точечные графики поверхностного фенотипа БЦЖ-специфических CD4 T-клеток (точки), наложенные на поверхностный фенотип памяти всех CD4 T-клеток (контурные графики). Медиана представлена горизонтальной линией, межквартильный размах — прямоугольником, а диапазон — усами. U-критерий Манна-Уитни использовался для расчета значений p различий между двумя группами.
Обсуждение
Наше исследование показало, что отсрочка вакцинации БЦЖ от рождения до возраста 10 недель приводит к индукции более высокой частоты детектируемых специфических Т-лимфоцитов CD4.Кроме того, специфические CD4 Т-клетки с большей вероятностью будут полифункциональными в группе отсроченной вакцины, что указывает на повышение «качества» индуцированного БЦЖ ответа.
Наши результаты отличаются от результатов двух предыдущих исследований, в которых не было выявлено различий в индуцированном иммунитете, когда вакцинация БЦЖ откладывалась после периода ближайшего новорожденного [10, 14]. Важно отметить, что в обоих этих исследованиях в качестве результата использовалось только измерение IFN-γ. Наши результаты показывают, что подробное изучение ответа Т-лимфоцитов позволяет провести более полную и контрастную оценку результата.Мы показали, что наиболее разительные различия в индуцированном иммунитете наблюдались в возрасте 1 года, что подчеркнуло важность лонгитюдного дизайна таких исследований. Данные о кинетике иммунного ответа, индуцированного БЦЖ, в детских когортах ограничены, особенно в условиях высокой эндемичности по ТБ.
Иммунные корреляты защиты от туберкулеза, вызванной вакцинацией, неизвестны. Таким образом, остается вопрос, могут ли частоты конкретных клеток, паттерны продукции цитокинов и фенотип памяти важны для долгосрочной защиты от туберкулеза.Большинство вакцинологов сочли бы более оптимальным количественно более высокий антиген-специфический ответ после новой вакцинации против туберкулеза в клинических испытаниях. Это мнение было подтверждено многочисленными исследованиями на животных, которые продемонстрировали, что более высокая частота специфических Т-клеток приводит к улучшенной защите от ТБ [18–20]. Напротив, другие исследования показали, что частота антиген-специфических Т-клеток, индуцированных противотуберкулезной вакциной, не обязательно может коррелировать с исходом после вирулентного M.tb [21–24]. Переменные дизайна исследования, такие как оцениваемый момент времени и проанализированный отсек, могут быть ответственны за эти противоречивые результаты. Кроме того, во многих из этих исследований оценивались специфические ответы Т-клеток только за счет продукции IFN-γ. Защита от ТБ без оптимального ответа IFN-γ невозможна. Однако постулируется, что измерение других цитокинов Th2 в дополнение к IFN-γ позволит лучше оценить «качество» Т-клеточного ответа. Например, наличие полифункциональных Т-клеток, коэкспрессирующих IFN-γ, TNF-α и IL-2, стало полезным показателем «качественных» иммунных ответов [25, 26].В моделях вакцинации животных против Leishmania major [27] и против туберкулеза [28] стратегии, которые вызывают наибольшую частоту полифункциональных антиген-специфических CD4 Т-клеток, связаны с наилучшей защитой от последующего заражения патогеном. Кроме того, у людей, инфицированных ВИЧ-1, медленное прогрессирование заболевания тесно связано с более высокой частотой полифункциональных ВИЧ-специфических Т-клеток [29].
Классически CD45RA и CCR7 использовались для разделения Т-клеток на 4 подмножества памяти, а именно на наивные клетки (CD45RA + CCR7 + , T Naive ), клетки центральной памяти (CD45RA — CCR7 + , T CM ), эффекторные клетки памяти (CD45RA — CCR7 — , T EM ) и эффекторные клетки памяти, которые повторно экспрессировали CD45RA (CD45RA + CCR7 — , T EMRA ) [30, 31].Долгоживущие T CM расширяются в лимфатических узлах и дифференцируются в эффекторные клетки [30]. Напротив, популяции T EM или более терминально дифференцированные популяции T EMRA могут немедленно стать домом для очага заболевания для выполнения эффекторных функций, но их пролиферативная способность и продолжительность жизни ограничены [30]. С гипотетической точки зрения, индукция долгоживущего T CM должна быть целью вакцинации — эта точка зрения была подтверждена на животных моделях заражения макак вирусом иммунодефицита обезьян (SIV) [17].Напротив, индукция T EM или T EMRA может быть не столь оптимальной, поскольку эти короткоживущие популяции не могут расширяться и более склонны к истощению [32]. Интересно, что в большинстве исследований Т-клеток человека, специфичных к микобактериям, преобладают популяции T EM и относительно нечасто T CM [11, 33–35]. Наши выводы подтверждают это; однако не было значительных различий в этих субпопуляциях Т-клеток после отсрочки вакцинации БЦЖ.
Считается, что на иммунитет, индуцированный БЦЖ, влияют многие переменные, как описано во введении выше.Например, Lalor и др. [36] сообщили, что сезонные изменения влияют на ответ IFN-γ у младенцев, вакцинированных БЦЖ, при измерении с помощью стимуляции PPD цельной крови в течение 6 дней. В нашем исследовании в возрасте 50 недель, когда наблюдались наиболее значимые различия в иммунитете, специфичном для БЦЖ, не было значительной разницы в распределении сезона родов между группами отсроченной вакцинации и вакцинацией при рождении. Кроме того, возможно, что различное воздействие микобактерий окружающей среды могло искажать наши результаты, хотя мы считаем это маловероятным, поскольку все младенцы были включены в исследование из одной географической области.Мы не можем исключить, что другие переменные могли повлиять на результаты.
Почему после отложенной вакцинации БЦЖ иммунный ответ усилился? Иммунный ответ новорожденного часто считается «незрелым» по сравнению с иммунным ответом взрослых [37]. «Незрелый» может быть неправильным названием, поскольку реакция может быть очень подходящей для ребенка, попадающего в мир непрерывного антигенного воздействия, и где чрезмерный иммунитет к этим стимулам может быть пагубным. Однако это может привести к неоптимальному ответу на определенные вакцины, такие как БЦЖ.Мы предполагаем, что различная природа иммунитета, индуцированного БЦЖ в возрасте 10 недель, по сравнению с рождением, может быть приписана ранним «созревающим» изменениям иммунитета младенца. Существуют очень ограниченные данные о «созревании» иммунного ответа младенца в течение первых нескольких месяцев жизни, но факторы, которые, возможно, способствовали этому, включают неэффективную функцию антигенпредставляющих клеток, в том числе ограниченную способность продуцировать IL-12 [37], критический цитокин для индукция ответов Th2, характерных для успешного микобактериального иммунитета.Кроме того, данные животных и людей свидетельствуют о том, что иммунная система новорожденного смещена в сторону ответа Th3 [38-40], который может подавлять индукцию иммунитета Th2.
В отличие от многих детских вакцин, которые обеспечивают повышенную защиту при бустинге, было показано, что вторая вакцинация БЦЖ не усиливает защиту [41]. Новые стратегии вакцинации против туберкулеза направлены на повышение иммунитета, вызванного вакциной БЦЖ, за счет использования гетерологичных вакцин. Поэтому крайне важно использовать первичную вакцину наиболее оптимальным образом.Наши результаты показывают, что возраст, в котором вводят БЦЖ, может быть критической переменной. Следующим шагом будет подтверждение этих результатов в другой когорте до проведения более крупных исследований, чтобы оценить, приводит ли отсроченная вакцинация к усилению защиты от заболевания туберкулезом. В этом случае потребуется всесторонняя оценка последствий отсрочки вакцинации БЦЖ до возраста 6–14 недель, когда другие детские вакцины вводятся регулярно.
Отсрочка вакцинации БЦЖ от рождения до возраста 10 недель может привести к усилению Т-клеточного ответа CD4
Резюме
Общие сведения
В большинстве эндемичных по туберкулезу стран бацилла Кальметта Герена (БЦЖ) обычно вводится при рождении для предотвращения тяжелой формы туберкулеза у младенцев.Иммунная система новорожденного еще не сформировалась. Наша гипотеза заключалась в том, что отсрочка вакцинации БЦЖ от рождения до 10-недельного возраста усилит иммунный ответ, индуцированный вакциной.
Методы
В рандомизированном клиническом исследовании БЦЖ вводили внутрикожно либо при рождении (n = 25), либо в возрасте 10 недель (n = 21). Через десять недель после вакцинации и в возрасте 1 года были измерены вакцино-специфические Т-клеточные ответы CD4 и CD8 с помощью анализа внутриклеточных цитокинов цельной крови.
Результаты
Младенцы, получившие отсроченную вакцинацию БЦЖ, демонстрировали более высокую частоту БЦЖ-специфических Т-лимфоцитов CD4, особенно полифункциональных Т-клеток, коэкспрессирующих IFN-γ, TNF-α и IL-2, и особенно ярко в возрасте 1 года.
Выводы
Отсрочка вакцинации БЦЖ от рождения до возраста 10 недель усиливает количественный и качественный БЦЖ-специфический Т-клеточный ответ при измерении в возрасте одного года.
Ключевые слова: БЦЖ, вакцинация, рождение, отсроченное, полифункциональные Т-лимфоциты CD4
Введение
Бацилла Кальметта Герена (БЦЖ), единственная современная вакцина против туберкулеза (ТБ), представляет собой живой аттенуированный штамм Mycobacterium bovis. Ежегодно более 100 миллионов детей во всем мире получают вакцину БЦЖ [1].Вакцинация БЦЖ обеспечивает защиту от тяжелых форм детского туберкулеза, т. Е. Туберкулезного менингита и милиарного туберкулеза [1, 2]. Защита, обеспечиваемая вакцинацией БЦЖ от легочного туберкулеза, наиболее распространенной формы туберкулеза, неодинакова и в основном низка [3]. Факторы, которые участвуют в различной защите БЦЖ от туберкулеза, включают штамм БЦЖ, дозу БЦЖ, предшествующее воздействие нетуберкулезных микобактерий (NTM) из окружающей среды, генетические вариации хозяина, штамм Mycobacterium tuberculosis ( M.tb ) и способ вакцинации. [3–7].
CD4 Т-клетки, которые продуцируют Т-хелперные цитокины типа 1 (Th2) IFN-γ, TNF-α и IL-2, считаются критическими для защиты от туберкулеза [8, 9]. Такой ответ Th2 характерен для вакцинации БЦЖ [10, 11]. В регионах, где широко распространен ТБ, вакцинация БЦЖ широко проводится при рождении или вскоре после него из-за риска раннего контакта с M.tb [12]. Существуют доказательства того, что ответ Th2 при рождении является «незрелым», например, прогрессивное повышение специфического опосредованного клетками Th2 иммунитета было показано, когда вакцина против кори вводилась в возрасте 6, 9 и 12 месяцев соответственно [13].Мы предположили, что созревание иммунной системы новорожденных до 10-недельного возраста до вакцинации БЦЖ повысит индуцированный вакцинацией Т-клеточный иммунитет. Эффект оптимизации сроков вакцинации может иметь важные последствия для улучшения защиты от туберкулеза с помощью вакцинации БЦЖ.
Марчант, и др. сообщил, что изменение возраста вакцинации БЦЖ не влияет на иммуногенность БЦЖ при оценке продукции интерферона гамма (IFN-γ) мононуклеарными клетками периферической крови (PBMC), стимулированными микобактериальными антигенами [10].В небольшом исследовании Hussey, et al. также сообщил, что отсрочка вакцинации БЦЖ от рождения до возраста 10 недель не влияет на секрецию IFN-γ, пролиферативные ответы или цитотоксический потенциал БЦЖ-специфичных Т-клеток после инкубации PBMC с микобактериальными антигенами [14]. С тех пор как появились эти результаты, мы показали, что измерение одного IFN-γ недооценивает сложность Th2-ответа, индуцированного БЦЖ. Вакцинация БЦЖ у младенцев индуцирует множественные подмножества Th2, что определяется экспрессией различных комбинаций IFN-γ, TNF-α и IL-2 специфическими клетками [11].Мы хотели всесторонне изучить влияние возраста на величину и качество Th2-иммунитета, индуцируемого БЦЖ у младенцев.
Материалы и методы
Набор участников и последующее наблюдение
Участники были зарегистрированы в период с апреля 2006 г. по март 2008 г. в Хайелитше, пригороде Кейптауна с чрезвычайно высокой заболеваемостью туберкулезом, составившей 1614 на 100000 в первом квартале. 2008 г. (Уровень уведомления о случаях, город Кейптаун).
Это было частью более крупного исследования, посвященного изучению клинических и иммунологических характеристик новорожденных, подвергшихся и не подвергавшихся воздействию ВИЧ.Короче говоря, в государственную женскую консультацию к беременным обращались с просьбой принять их младенцев. Для исследования, представленного здесь, младенцы, которые родились от ВИЧ-инфицированных женщин или женщин с неизвестным ВИЧ-статусом, подвергались активному туберкулезу в семье, родились преждевременно (гестационный возраст ≤36 недель) или имели низкий вес при рождении (≤2,5 кг), или те, у кого были значительные перинатальные осложнения, были исключены. Кроме того, были исключены все младенцы с положительным ответом IFN-γ на ESAT-6 / CFP-10 в возрасте 10 недель (подробности анализа см. Ниже).Младенцы были случайным образом распределены во время дородового набора для получения вакцины БЦЖ (внутрикожный датский штамм 1331, Statens Serum Institute) в первый день жизни («вакцинация при рождении») или аналогичной вакцинации БЦЖ в возрасте 10 недель («отложенная вакцинация»). Младенцы наблюдались в возрасте 10, 20 и 50 недель. Был разрешен период окна от -2 до +4 недель вокруг визита на 10 неделе (например, от 8 до 14 недель). Период времени для 20-недельного посещения составлял от 18 до 28 недель и от 41 до 54 недель для 50-недельного посещения.
Разрешение регулирующих органов было получено от комитетов по этике исследований Стелленбошского и Кейптаунского университетов. Письменное информированное согласие было получено от всех матерей на их родном языке. Все тесты на ВИЧ проводились в сочетании с информированным согласием и консультированием до и после тестирования.
Сбор крови и анализ внутриклеточных цитокинов
Один мл крови собирали в возрасте 10, 20 и 50 недель в гепаринизированные шприцы. Цельную кровь обрабатывали в течение 2 часов после сбора, как описано ранее [15].Вкратце, 250 мкл цельной крови инкубировали в течение 12 часов при 37 ° C с жизнеспособной БЦЖ (восстановленной из флакона с вакциной, датский штамм, Staten Serum Institute, 1,2 × 10 6 КОЕ / мл) и костимулирующими антителами анти-CD28. и анти-CD49d (BD Biosciences, 0,5 мкг / мл каждый). 250 мкл крови, инкубированной со стафилококковым энтеротоксином B (SEB, Sigma, 10 мкг / мл), и 250 мкл крови, инкубированной только с костимулирующими антителами (нестимулированными), служили в качестве положительного и отрицательного контролей соответственно. Брефельдин A (Sigma, 10 мкг / мл) добавляли в течение последних 5 часов инкубации.После инкубации эритроциты лизировали и лейкоциты фиксировали лизирующим раствором BD FACS Lysing Solution (BD Biosciences), а клетки криоконсервировали.
Криоконсервированные клетки позже оттаивали и промывали 1% бычьим сывороточным альбумином (Sigma) в фосфатно-солевом буфере (PBS, BioWhittaker) и повышали проницаемость, используя раствор Perm / Wash Solution (BD Biosciences). Затем клетки окрашивали следующими антителами: анти-CD3 Pacific Blue (клон UCHT1), анти-CD4 PerCPCy5.5 (SK3), анти-CD45RA PECy7 (L48), анти-IFN-γ AlexaFluor700 (B27), анти-IL. -2 FITC (5344.111), анти-TNF-α PE (MAb11; все от BD Biosciences), анти-CD8 Qdot605 (3B5, Invitrogen) и анти-CCR7 APC (150503, R&D Systems). После промывок клетки собирали на проточном цитометре LSR II (BD Biosciences), для этого эксперимента использовали 3 лазера и 10 детекторов с использованием программного обеспечения FACS Diva 6.1. Параметры компенсации были установлены с использованием каппа-шариков против мышей (BD Biosciences), меченных соответствующими антителами, конъюгированными с флуорохромом. Flowjo 8.7.1 (Treestar) использовался для компенсации и анализа данных проточной цитометрии.Для создания комбинаций цитокинов, экспрессирующих субнаборы Т-клеток CD4 и CD8, применяли логическое стробирование ().
Стратегия гейтинга, используемая для анализа Т-клеточных цитокиновых ответов CD4 и CD8Цельную кровь инкубировали с БЦЖ для завершения проточного цитометрического анализа внутриклеточных цитокинов, как описано в Методиках.
( A ) Дублетные клетки были исключены путем стробирования по площади прямого рассеяния (FSC-A) против высоты прямого рассеяния (FSC-H), а затем лимфоциты были отобраны в FSC-A против площади бокового рассеяния ( SSC-A) точечный график.Т-клетки отбирали путем стробирования событий CD3 + , которые далее дифференцировались в Т-клетки CD4 и CD8. ( B) Типичные точечные диаграммы паттернов коэкспрессии цитокинов в CD4 Т-клетках в нестимулированных, стимулированных БЦЖ и SEB условиях.
Анализ интеркуррентной инфекции
M. tuberculosisВ каждый момент времени цельную кровь разбавляли 1: 5 в среде для культивирования тканей RPMI-1640 (Sigma), содержащей 1% L-глутамин (Sigma), и инкубировали с ESAT -6 / CFP-10 слитый белок (предоставлен Томом Оттенхоффом, Медицинский центр Лейденского университета, 10 мкг / мл), фитогемагглютинин (PHA, Sigma, 5 мкг / мл) и SEB (1 мкг / мл; оба положительных контроля) или отсутствие антигена ( отрицательный контроль) в трех экземплярах в 96-луночных планшетах (модифицировано из Black et al ) [16].Планшеты инкубировали при 37 ° C с 5% CO 2 в течение 7 дней, супернатанты собирали, три лунки объединяли и хранили при -80 ° C. Позже супернатанты оттаивали, и сэндвич-ELISA на IFN-γ использовали для количественного определения IFN-γ в супернатантах, полученных в результате 7-дневного анализа цельной крови (BD Pharmingen). Положительный ответ IFN-γ был определен как 62 пг / мл после вычитания фона (удвоенный предел обнаружения анализа 31 пг / мл). Младенцы с признаками интеркуррентной инфекции / контакта M. tuberculosis в возрасте 10, 20 или 50 недель были исключены из анализа.
Анализ данных
Для анализа внутриклеточных цитокинов уровни экспрессии цитокинов в нестимулированной крови вычитали из уровней, полученных после стимуляции БЦЖ. (Средний уровень экспрессии IFN-γ, IL-2 и TNF среди Т-лимфоцитов CD4 в нестимулированной крови составлял 0,002%, 0,03% и 0,06% соответственно.) Различия в массе тела при рождении и полу участников оценивались с помощью параметрических тестов. U-критерий Манна-Уитни использовался для оценки различий в частотах экспрессии цитокинов CD4 и CD8 Т-клеток между двумя группами.Значения P ниже 0,05 считались значимыми.
Результаты
Характеристики участников
Всего в исследование было включено 46 младенцев: 25 в группе рождения и 21 в группе отсроченной вакцинации. Младенцы, не явившиеся для проведения флеботомии в определенный момент времени, с кровотечением за пределами определенного периода окна на 10 неделе посещения или положительными на инфекцию M.tb , были исключены из анализа (). Результаты для младенцев с инфекцией M.tb были исключены из временной точки, в которой это было диагностировано, и из последующих временных точек.На исходном уровне не наблюдалось различий в массе тела при рождении или полу между группой рождения и группы отсроченной вакцинации (средний вес при рождении, (SD): 3306 г (435,6) при рождении против 3200 г (371,9) при задержке; p = 0,390). Шестнадцать (64%) младенцев в группе рождения были мальчиками по сравнению с 9 (43%) младенцами в группе отсроченных родов (p = 0,235).
Обзор правомочности, потока исследования и участников
Обнаружение БЦЖ-специфичных CD4 Т-клеток с использованием жизнеспособной БЦЖ в качестве антигена
Перед тем, как сравнивать БЦЖ-индуцированный иммунитет между новорожденными и отложенной вакцинацией, мы оценили, была ли инкубация целых кровь с жизнеспособной БЦЖ может привести к неспецифической активации Т-клеток или к обнаружению вакцино-специфического ответа.Мы сравнили Т-клеточный иммунитет CD4, измеренный в возрасте 10 недель с помощью анализа внутриклеточного определения цитокинов (: пример результатов анализа), между участниками, которые получали БЦЖ при рождении, и теми, кто еще не принимал БЦЖ (младенцы в группе отсроченного приема). . Продукция цитокинов CD4 Т-клетками легко определялась у младенцев из группы, вакцинированной при рождении, но не обнаруживалась или обнаруживалась только на очень низких уровнях у младенцев, не получивших вакцину при рождении (). Младенцы, вакцинированные при рождении, имели высокие частоты полифункциональных Т-лимфоцитов CD4, специфичных для БЦЖ, т.е.е. Т-клетки CD4, которые вместе экспрессируют IFN-γ, TNF-α и IL-2, и Т-клетки CD4, экспрессирующие другие комбинации цитокинов Th2. Полифункциональные БЦЖ-специфические CD4 Т-клетки отсутствовали у младенцев в группе отсроченной вакцинации. У всех младенцев был положительный ответ на положительный контроль, SEB (данные не показаны). Мы пришли к выводу, что ответы Т-клеток, измеренные с помощью нашей системы анализа, когда БЦЖ используется в качестве антигена, являются антиген-специфическими, а не обусловлены неспецифической активацией Т-клеток.
Сравнение ответов Т-лимфоцитов CD4 после инкубации цельной крови из крови вакцинированных БЦЖ и невакцинированных младенцев с БЦЖ в возрасте 10 недельЧастоты Т-лимфоцитов CD4, экспрессирующих цитокины, обнаруженные с помощью анализа внутриклеточных цитокинов цельной крови (см. Методы) показаны.Медиана представлена горизонтальной линией, межквартильный размах — прямоугольником, а диапазон — усами. U-критерий Манна-Уитни использовался для расчета значений p различий между двумя группами.
Отсроченная вакцинация привела к умеренно более высокой частоте БЦЖ-специфичных Т-клеток CD4 через 10 недель после вакцинации
Чтобы оценить различия в ответах Т-лимфоцитов CD4 и CD8, когда вакцина вводилась при рождении или в возрасте 10 недель, мы измерили Паттерн экспрессии Th2-цитокинов, индуцированный БЦЖ через 10 недель после вакцинации, т.е.е., в возрасте 10 недель в группе рождения и в возрасте 20 недель в группе отсроченного рождения. В обеих группах наблюдались высокие частоты полифункциональных Т-лимфоцитов CD4 или клеток, экспрессирующих другие комбинации цитокинов Th2 (). IFN-γ + и IFN-γ + IL-2 + Частота субпопуляций CD4-Т-клеток, специфичных для БЦЖ, была значительно выше в группе отсроченной вакцинации по сравнению с группой вакцинации при рождении (). Поскольку частота индуцированных специфических субпопуляций CD8 Т-клеток была очень низкой, в обеих группах вакцинации оценивались только общие БЦЖ-специфические Т-клеточные ответы CD8: не было никакой разницы между двумя группами ().Мы пришли к выводу, что отсрочка вакцинации БЦЖ на 10 недель может привести к увеличению частоты БЦЖ-специфических CD4 Т-клеток через 10 недель после вакцинации.
БЦЖ-специфические Т-клеточные ответы через 10 недель после вакцинации у младенцев, получавших БЦЖ при рождении и тех, кто получил БЦЖ в возрасте 10 недель(A) Частоты БЦЖ-специфических цитокинов, экспрессирующих Т-клетки CD4, показаны в виде обнаруживается с помощью анализа внутриклеточных цитокинов цельной крови. (B) Частоты всех экспрессирующих CD8 Т-клеток, оцененные вместе, после инкубации цельной крови с БЦЖ.Медиана представлена горизонтальной линией, межквартильный размах — прямоугольником, а диапазон — усами. U-критерий Манна-Уитни использовался для расчета значений p различий между двумя группами.
Отсроченная вакцинация увеличивала частоту полифункциональных БЦЖ-специфических CD4 Т-клеток в возрасте одного года
Мы также сравнили БЦЖ-специфический ответ памяти в возрасте 50 недель. Мы наблюдали значительно более высокие частоты БЦЖ-специфичных полифункциональных IFN-γ + TNF-α + IL-2 + CD4 Т-клеток в группе отсроченной вакцинации по сравнению с группой вакцинации при рождении ().Частота специфических субпопуляций Т-клеток, коэкспрессирующих TNF-α и IL-2, TNF-α и IFN-γ или только TNF-α, также была выше в группе отсроченной вакцинации. В этом возрасте общие ответы Т-лимфоцитов CD8, специфичные для БЦЖ, были слишком низкими для надежного анализа данных (данные не показаны). При сравнении ответов на положительный контроль, SEB, различий между двумя группами не наблюдалось (дополнительная фигура 1). Мы пришли к выводу, что отсрочка вакцинации БЦЖ с рождения до возраста 10 недель приводит к количественному увеличению и качественно более оптимальному БЦЖ-специфическому ответу памяти CD4 Т-клеток в возрасте одного года.
БЦЖ-специфические ответы Т-лимфоцитов CD4 в 2 группах младенцев в возрасте 1 годаПоказаны частоты цитокин-экспрессирующих CD4 Т-клеток, обнаруженные с помощью анализа внутриклеточных цитокинов цельной крови. Медиана представлена горизонтальной линией, межквартильный размах — прямоугольником, а диапазон — усами. U-критерий Манна-Уитни использовался для расчета значений p различий между двумя группами.
Пики общего БЦЖ-специфического ответа Т-лимфоцитов CD4 в группах родов и отсроченной вакцинации достигаются через 10 недель после вакцинации. через 10 недель мы измерили общий ответ памяти Т-лимфоцитов CD4, специфичный для БЦЖ, в возрасте 10, 20 и 50 недель.Общие ответы обозначаются БЦЖ-специфическими CD4 Т-клетками, которые экспрессируют IFN-γ, TNF-α или IL-2, по отдельности или в комбинации. В группах рождаемости и отсроченной вакцинации БЦЖ-специфические ответы CD4 достигли пика через 10 недель после вакцинации и постепенно уменьшались в течение первого года жизни ().
Кинетика общих БЦЖ-специфичных ответов Т-лимфоцитов CD4 в группах отсроченной вакцинации и вакцинации при рождении в течение одного годаСредние частоты БЦЖ-специфичных общих цитокин-экспрессирующих CD4 Т-клеток, обнаруженных с помощью краткосрочного анализа внутриклеточных цитокинов цельной крови при 10, Возраст 20 и 50 недель.
Сопоставимый БЦЖ-специфический фенотип памяти Т-лимфоцитов CD4 в группах рождения и отсроченной вакцинации
Чтобы оценить, приводит ли отсрочка вакцинации БЦЖ к измененному вакцино-специфическому фенотипу памяти Т-клеток CD4, мы охарактеризовали цитокин, экспрессирующий БЦЖ-специфические Т-клетки. Фенотип памяти специфических Т-клеток, определяемый поверхностной экспрессией CD45RA и CCR7, на животных моделях, как было показано, определяет исход вакцинации [17]. Как в группе вакцинации при рождении, так и в группе отложенной вакцинации эффекторная память (CD45RA-CCR7-, T EM ) преобладала и во всех временных точках оценивалась (для данных в возрасте 1 года).В возрасте одного года не было значительных различий для T EM или центральной памяти (T CM , CD45RA — CCR7 + ) в двух группах младенцев ().
Сравнение фенотипа поверхностной памяти БЦЖ-специфических Т-лимфоцитов CD4 между двумя группами младенцев в возрасте 1 годаАнтигенспецифические Т-клетки CD4 были идентифицированы по экспрессии цитокинов с помощью анализа внутриклеточных цитокинов цельной крови. (A) Графики в виде прямоугольников и усов, изображающие фенотип памяти всех BCG-специфичных CD4 T-клеток, проанализированных вместе.(B) Репрезентативные точечные графики поверхностного фенотипа БЦЖ-специфических CD4 T-клеток (точки), наложенные на поверхностный фенотип памяти всех CD4 T-клеток (контурные графики). Медиана представлена горизонтальной линией, межквартильный размах — прямоугольником, а диапазон — усами. U-критерий Манна-Уитни использовался для расчета значений p различий между двумя группами.
Обсуждение
Наше исследование показало, что отсрочка вакцинации БЦЖ от рождения до возраста 10 недель приводит к индукции более высокой частоты детектируемых специфических Т-лимфоцитов CD4.Кроме того, специфические CD4 Т-клетки с большей вероятностью будут полифункциональными в группе отсроченной вакцины, что указывает на повышение «качества» индуцированного БЦЖ ответа.
Наши результаты отличаются от результатов двух предыдущих исследований, в которых не было выявлено различий в индуцированном иммунитете, когда вакцинация БЦЖ откладывалась после периода ближайшего новорожденного [10, 14]. Важно отметить, что в обоих этих исследованиях в качестве результата использовалось только измерение IFN-γ. Наши результаты показывают, что подробное изучение ответа Т-лимфоцитов позволяет провести более полную и контрастную оценку результата.Мы показали, что наиболее разительные различия в индуцированном иммунитете наблюдались в возрасте 1 года, что подчеркнуло важность лонгитюдного дизайна таких исследований. Данные о кинетике иммунного ответа, индуцированного БЦЖ, в детских когортах ограничены, особенно в условиях высокой эндемичности по ТБ.
Иммунные корреляты защиты от туберкулеза, вызванной вакцинацией, неизвестны. Таким образом, остается вопрос, могут ли частоты конкретных клеток, паттерны продукции цитокинов и фенотип памяти важны для долгосрочной защиты от туберкулеза.Большинство вакцинологов сочли бы более оптимальным количественно более высокий антиген-специфический ответ после новой вакцинации против туберкулеза в клинических испытаниях. Это мнение было подтверждено многочисленными исследованиями на животных, которые продемонстрировали, что более высокая частота специфических Т-клеток приводит к улучшенной защите от ТБ [18–20]. Напротив, другие исследования показали, что частота антиген-специфических Т-клеток, индуцированных противотуберкулезной вакциной, не обязательно может коррелировать с исходом после вирулентного M.tb [21–24]. Переменные дизайна исследования, такие как оцениваемый момент времени и проанализированный отсек, могут быть ответственны за эти противоречивые результаты. Кроме того, во многих из этих исследований оценивались специфические ответы Т-клеток только за счет продукции IFN-γ. Защита от ТБ без оптимального ответа IFN-γ невозможна. Однако постулируется, что измерение других цитокинов Th2 в дополнение к IFN-γ позволит лучше оценить «качество» Т-клеточного ответа. Например, наличие полифункциональных Т-клеток, коэкспрессирующих IFN-γ, TNF-α и IL-2, стало полезным показателем «качественных» иммунных ответов [25, 26].В моделях вакцинации животных против Leishmania major [27] и против туберкулеза [28] стратегии, которые вызывают наибольшую частоту полифункциональных антиген-специфических CD4 Т-клеток, связаны с наилучшей защитой от последующего заражения патогеном. Кроме того, у людей, инфицированных ВИЧ-1, медленное прогрессирование заболевания тесно связано с более высокой частотой полифункциональных ВИЧ-специфических Т-клеток [29].
Классически CD45RA и CCR7 использовались для разделения Т-клеток на 4 подмножества памяти, а именно на наивные клетки (CD45RA + CCR7 + , T Naive ), клетки центральной памяти (CD45RA — CCR7 + , T CM ), эффекторные клетки памяти (CD45RA — CCR7 — , T EM ) и эффекторные клетки памяти, которые повторно экспрессировали CD45RA (CD45RA + CCR7 — , T EMRA ) [30, 31].Долгоживущие T CM расширяются в лимфатических узлах и дифференцируются в эффекторные клетки [30]. Напротив, популяции T EM или более терминально дифференцированные популяции T EMRA могут немедленно стать домом для очага заболевания для выполнения эффекторных функций, но их пролиферативная способность и продолжительность жизни ограничены [30]. С гипотетической точки зрения, индукция долгоживущего T CM должна быть целью вакцинации — эта точка зрения была подтверждена на животных моделях заражения макак вирусом иммунодефицита обезьян (SIV) [17].Напротив, индукция T EM или T EMRA может быть не столь оптимальной, поскольку эти короткоживущие популяции не могут расширяться и более склонны к истощению [32]. Интересно, что в большинстве исследований Т-клеток человека, специфичных к микобактериям, преобладают популяции T EM и относительно нечасто T CM [11, 33–35]. Наши выводы подтверждают это; однако не было значительных различий в этих субпопуляциях Т-клеток после отсрочки вакцинации БЦЖ.
Считается, что на иммунитет, индуцированный БЦЖ, влияют многие переменные, как описано во введении выше.Например, Lalor и др. [36] сообщили, что сезонные изменения влияют на ответ IFN-γ у младенцев, вакцинированных БЦЖ, при измерении с помощью стимуляции PPD цельной крови в течение 6 дней. В нашем исследовании в возрасте 50 недель, когда наблюдались наиболее значимые различия в иммунитете, специфичном для БЦЖ, не было значительной разницы в распределении сезона родов между группами отсроченной вакцинации и вакцинацией при рождении. Кроме того, возможно, что различное воздействие микобактерий окружающей среды могло искажать наши результаты, хотя мы считаем это маловероятным, поскольку все младенцы были включены в исследование из одной географической области.Мы не можем исключить, что другие переменные могли повлиять на результаты.
Почему после отложенной вакцинации БЦЖ иммунный ответ усилился? Иммунный ответ новорожденного часто считается «незрелым» по сравнению с иммунным ответом взрослых [37]. «Незрелый» может быть неправильным названием, поскольку реакция может быть очень подходящей для ребенка, попадающего в мир непрерывного антигенного воздействия, и где чрезмерный иммунитет к этим стимулам может быть пагубным. Однако это может привести к неоптимальному ответу на определенные вакцины, такие как БЦЖ.Мы предполагаем, что различная природа иммунитета, индуцированного БЦЖ в возрасте 10 недель, по сравнению с рождением, может быть приписана ранним «созревающим» изменениям иммунитета младенца. Существуют очень ограниченные данные о «созревании» иммунного ответа младенца в течение первых нескольких месяцев жизни, но факторы, которые, возможно, способствовали этому, включают неэффективную функцию антигенпредставляющих клеток, в том числе ограниченную способность продуцировать IL-12 [37], критический цитокин для индукция ответов Th2, характерных для успешного микобактериального иммунитета.Кроме того, данные животных и людей свидетельствуют о том, что иммунная система новорожденного смещена в сторону ответа Th3 [38-40], который может подавлять индукцию иммунитета Th2.
В отличие от многих детских вакцин, которые обеспечивают повышенную защиту при бустинге, было показано, что вторая вакцинация БЦЖ не усиливает защиту [41]. Новые стратегии вакцинации против туберкулеза направлены на повышение иммунитета, вызванного вакциной БЦЖ, за счет использования гетерологичных вакцин. Поэтому крайне важно использовать первичную вакцину наиболее оптимальным образом.Наши результаты показывают, что возраст, в котором вводят БЦЖ, может быть критической переменной. Следующим шагом будет подтверждение этих результатов в другой когорте до проведения более крупных исследований, чтобы оценить, приводит ли отсроченная вакцинация к усилению защиты от заболевания туберкулезом. В этом случае потребуется всесторонняя оценка последствий отсрочки вакцинации БЦЖ до возраста 6–14 недель, когда другие детские вакцины вводятся регулярно.
Защищает ли вакцинация БЦЖ новорожденных и младенцев?
Бесплатная статья PMCЭлемент в буфере обмена
Клиническое исследование
H G ten Dam et al.Bull World Health Organ. 1980 г.
Бесплатная статья PMC Показать детали Показать вариантыПоказать варианты
Формат АннотацияPubMedPMID
Полнотекстовые ссылки Опции CiteDisplayПоказать варианты
Формат АннотацияPubMedPMID
Абстрактный
PIP: Вакцинация БЦЖ в последние несколько десятилетий стала применяться все шире.В настоящее время эта вакцинация применяется к новорожденным, несмотря на то, что прямых данных о степени защиты, предоставляемой очень маленьким детям, мало. В этом обсуждении рассматриваются имеющиеся данные о вакцинации новорожденных из 3 контролируемых испытаний, проведенных в 1930-х годах, и единственное доступное в последнее время свидетельство по этому вопросу, полученное в результате ретроспективных исследований. Первая попытка изучить эффективность вакцинации БЦЖ младенцев раннего возраста в рамках контролируемого исследования была начата в Нью-Йорке в 1926 году.До 1933 г. половина младенцев (до 1 года, многие до 4 недель), поступивших из противотуберкулезных учреждений, были вакцинированы, остальные служили контрольной группой. Было 3 случая смерти от туберкулеза среди 445 вакцинированных детей, но 18 случаев смерти среди 545 контрольных детей. В течение 14 лет контролируемого испытания на младенцах из Индии в Саскачеване (начатого в 1933 г.) было 53 случая смерти среди вакцинированных БЦЖ и 63 смерти среди детей контрольной группы. Среди 306 вакцинированных детей было 6 случаев туберкулеза, 2 из которых умерли.Среди 303 контрольных случаев было 29 случаев, 9 из которых умерли. Исследование вакцинации новорожденных БЦЖ методом множественной чрескожной пункции было начато Rosenthal et al. в 1937 году. В него вошли 3381 младенец, из которых около половины были вакцинированы в течение первой недели после рождения, если члены домохозяйства не болели туберкулезом. Что касается туберкулеза, разница в заболеваемости была очень значительной. Было 17 случаев среди 1716 вакцинированных и 65 случаев среди 1665 контрольных. Интересный анализ статистики заболеваемости для разных стран был проведен Бьяртвейтом и Ваалером, которые изучали связь между снижением заболеваемости туберкулезом в различных возрастных группах и возрастом, в котором была сделана вакцинация.Эта связь была выраженной и, таким образом, свидетельствовала об эффективности вакцинации БЦЖ. Недавно были опубликованы результаты ретроспективного исследования, в котором участвовало 6364 ребенка, вакцинированных при рождении в Гамбурге в 1954 году, и 9524 ребенка, не вакцинированных. До 1971 года 9 привитых и 130 непривитых детей заболели туберкулезом. Из 30 370 детей, родившихся в 1963 году, 27 371 был вакцинирован, а 2999 — нет. За 8-летний период наблюдения выявлено 11 случаев туберкулеза среди вакцинированных и 16 случаев среди непривитых детей.На первый взгляд, данные свидетельствуют о том, что вакцинация новорожденных БЦЖ обеспечивает значительную защиту от туберкулеза у младенцев и детей раннего возраста, однако следует помнить, что доказательства являются скудными и поверхностными.
Похожие статьи
- Исследования по вакцинации БЦЖ.
десять плотин HG.десять плотин HG. Adv Tuberc Res. 1984; 21: 79-106. Adv Tuberc Res. 1984 г. PMID: 6433675 Клиническое испытание.
- Эффективность вакцинации против бациллы Кальметта-Герена новорожденных и младенцев в профилактике туберкулеза: метаанализ опубликованной литературы.
Colditz GA, Berkey CS, Mosteller F, Brewer TF, Wilson ME, Burdick E, Fineberg HV. Colditz GA, et al.Педиатрия. 1995 июл; 96 (1 п.1): 29-35. Педиатрия. 1995 г. PMID: 7596718
- [Ретроспективная оценка эффективности вакцинации БЦЖ методом множественных пункций (игла Кучики) при детском туберкулезе].
Камигавара Н. Камигавара Н. Кеккаку. 1989 Апрель; 64 (4): 305-11. Кеккаку. 1989 г. PMID: 2787444 Японский.
- Благоприятные нецелевые эффекты БЦЖ — этические последствия для предстоящего внедрения новых противотуберкулезных вакцин.
Рот AE, Stensballe LG, Garly ML, Aaby P. Рот А.Е. и др. Туберкулез (Edinb). 2006 ноябрь; 86 (6): 397-403. DOI: 10.1016 / j.tube.2006.02.001. Epub 2006 8 августа. Туберкулез (Edinb). 2006 г. PMID: 165 Рассмотрение.
- [Программа политики по минимизации распространения инфекции. Продолжительный кашель может быть признаком туберкулеза].
Фредлунд Х., Ларссон Л.О., Блом-Бюлов Б., Юландер I, Норманн Б., Романус В., Вальстрём Х.Fredlund H, et al. Lakartidningen. 1998 4 марта; 95 (10): 1010-2, 1015-6. Lakartidningen. 1998 г. PMID: 9528251 Рассмотрение. Шведский.
Процитировано
18 артикулов- Сочетанная инфекция туберкулеза и криптококкоза в Китае с 1965 по 2016 год.
Fang W, Zhang L, Liu J, Denning DW, Hagen F, Jiang W, Hong N, Deng S, Lei X, Deng D, Liao W., Xu J, Boekhout T, Chen M, Pan W.Fang W и др. Emerg Microbes Infect. 2017 23 августа; 6 (8): e73. DOI: 10.1038 / emi.2017.61. Emerg Microbes Infect. 2017 г. PMID: 28831193 Бесплатная статья PMC. Рассмотрение.
- Шрам от БЦЖ у матери связан с усилением провоспалительных иммунных реакций у младенцев.
Мава П.А., Уэбб Э.Л., Филали-Мухим А., Нкурунунги Г., Секали Р.П., Луле С.А., Прентис С., Нэш С., Докрелл Х.М., Эллиотт А.М., Коз С.Mawa PA, et al. Вакцина. 2017, 5 января; 35 (2): 273-282. DOI: 10.1016 / j.vaccine.2016.11.079. Epub 2016 30 ноября. Вакцина. 2017 г. PMID: 27914741 Бесплатная статья PMC.
- Вакцинация БЦЖ в трех разных возрастных группах: ответ и эффективность.
Бриасулис Г., Карабацу И., Гогоглов В., Цорва А. Briassoulis G, et al. J. Иммунные тервакцины. 2005 апр 1; 3 (1): 1.DOI: 10.1186 / 1476-8518-3-1. J. Иммунные тервакцины. 2005 г. PMID: 15804351 Бесплатная статья PMC.
- Защитный эффект БЦЖ у детей, вакцинированных по программе универсальной иммунизации.
Чадха В.К., Сурьянараяна Л., Сурьянараян Х.В., Шрикантараму Н., Кумар П. Чадха В.К. и др. Индийский J Pediatr. 2004 декабрь; 71 (12): 1069-74. DOI: 10.1007 / BF02829816.Индийский J Pediatr. 2004 г. PMID: 15630313
- Осложнения вакцинации БЦЖ в сельских районах Гаити.
Bonnlander H, Rossignol AM. Bonnlander H, et al. Am J Public Health. 1993 Апрель; 83 (4): 583-5. DOI: 10.2105 / ajph.83.4.583. Am J Public Health. 1993 г. PMID: 8460741 Бесплатная статья PMC.
Условия MeSH
- Вакцина БЦЖ / способ применения и дозировка *
- Младенцы, Новорожденные, Заболевания / иммунология
- Младенцы, новорожденные, болезни / профилактика и борьба *
- Туберкулез легких / профилактика и борьба *
Вакцинация БЦЖ при рождении и госпитализация в раннем детском возрасте: рандомизированное клиническое многоцентровое исследование
Мы предположили, что вакцинация БЦЖ при рождении будет иметь неспецифический положительный эффект и снизит общую госпитализацию детей по поводу соматических приобретенных заболеваний (исключая травмы) с рождения до 15 месяцев после рождения. возраст на 20% в странах с высоким уровнем дохода Дании.Мы не смогли это подтвердить.
Сильные и слабые стороны
Сильные стороны настоящего исследования заключаются в рандомизированном клиническом многоцентровом исследовании с адекватной мощностью. Данные о первичном исходе исследования, а именно о госпитализации по всем причинам, собирались независимо от исследования, что уменьшало риск систематической ошибки. За всеми участниками можно было следить через публичные реестры.
Исследование может быть ограничено нашим выбором госпитализации по любой причине в качестве первичного результата, который был выбран из-за его потенциально сильного воздействия на общественное здоровье, а также потому, что этот результат включал как инфекции, требующие госпитализации, так и тяжелые проявления атопического заболевания.Однако, учитывая высокую частоту госпитализаций, этот результат, возможно, не был достаточно специфичным, чтобы выявить потенциальный полезный иммунный тренирующий эффект БЦЖ.
Сравнение с другими исследованиями
В странах с низким уровнем дохода два рандомизированных контролируемых испытания среди детей с низкой массой тела при рождении показали, что БЦЖ снижает нетуберкулезную смертность до 6 месяцев, в частности неонатальный сепсис и респираторные инфекции.2, 3 Недавние иммунологические исследования. предоставили потенциальный механизм, показав, что БЦЖ индуцирует тренированный врожденный иммунитет посредством эпигенетического перепрограммирования моноцитов 13, 14, который все еще присутствовал через 12 месяцев после БЦЖ.13, 15 У гвинейских младенцев БЦЖ ассоциировалась с повышенным ответом на гетерологичную врожденную стимуляцию.16
Отсутствие влияния БЦЖ на госпитализацию по любой причине в Дании могут быть другими объяснениями.
Во-первых, в системе с бесплатным медицинским обслуживанием госпитализация по поводу приобретенного соматического заболевания может не представлять собой достаточно конкретную меру заболевания. Высокий уровень родительской озабоченности в сочетании с низким профессиональным порогом госпитализации младенцев младшего возраста, вероятно, приведет к увеличению количества госпитализаций.Частота госпитализаций по любой причине оказалась на 50% выше ожидаемой.
Во-вторых, существуют очевидные различия в подверженности инфекциям между Данией и странами с низким доходом, где наблюдались благоприятные неспецифические эффекты БЦЖ на смертность. У большинства детей, участвовавших в настоящем исследовании, не было братьев и сестер, таким образом, предположительно, подверженность инфекциям была ограничена до тех пор, пока они не перешли в детский сад в возрасте около 1 года.
В-третьих, мы ранее обнаружили, что материнский иммунитет также может иметь значение для неспецифического ответа на вакцинацию против кори у ребенка; 17 поэтому мы также спросили, были ли матери, участвовавшие в датском исследовании Calmette, вакцинировали БЦЖ.В странах с низким уровнем доходов большинство матерей будут вакцинированы БЦЖ, тогда как в нашем исследовании только 17% матерей были вакцинированы БЦЖ, поскольку вакцинация БЦЖ была прекращена в начале 1980-х годов. На то, что раннее воздействие может иметь значение для реакции ребенка на БЦЖ, также указали два исследования, в которых сравнивались цитокиновые ответы после БЦЖ у младенцев в Великобритании и Малави и обнаруживались существенные различия, которые были приписаны воздействию очень раннего, внутриутробного или в течение первого периода. несколько месяцев жизни.18, 19 Кроме того, было показано, что Т-хелперные клетки плода могут быть сенсибилизированы к производным очищенного микобактериального белка в утробе матери . 20 В соответствии с этим, в заранее запланированном вторичном анализе госпитализаций по поводу инфекции в рамках настоящего исследования наблюдался значительный положительный эффект БЦЖ у детей матерей, вакцинированных БЦЖ (личное сообщение, Stensballe LG, Greisen G, Jeppesen DL, и др. Влияние вакцинации БЦЖ при рождении на риск госпитализации по поводу инфекции в Дании. Рандомизированное клиническое многоцентровое исследование. 2015. Неопубликованная работа). Если воздействие БЦЖ или микобактерий на мать является важным для развития благоприятных неспецифических эффектов БЦЖ, это может объяснить положительный эффект БЦЖ, наблюдаемый в странах с низким уровнем дохода, но не в целом в настоящем исследовании.
В-четвертых, генетика различается между популяциями Западной Африки и Дании; 21–23, однако, влияние этого неясно, и следует отметить, что другие обнаружили доказательства положительного воздействия БЦЖ в Дании24.
Ранний по сравнению с поздняя вакцинация БЦЖ младенцев, контактировавших с ВИЧ-1, в Уганде: протокол рандомизированного контролируемого исследования | Испытания
Эльгуэро Э., Симондон К.Б., Ваугелад Дж., Марра А., Симондон Ф. Неспецифические эффекты вакцинации на выживаемость детей? Перспективное исследование в Сенегале.Trop Med Int Health. 2005. 10 (10): 956–60.
PubMed Статья Google Scholar
Кришнан А., Шривастава Р., Двиведи П., Нг Н., Бьясс П., Пандав К.С. Неспецифический дифференцированный по полу эффект вакцинации АКДС может частично объяснить повышенную смертность девочек в Баллабгархе, Индия. Trop Med Int Health. 2013. 18 (11): 1329–37.
Аби П., Бенн С.С., Нильсен Дж., Равн Х. Неспецифические эффекты БЦЖ и АКДС, дифференцированные по полу, в Себу, Филиппины.Int J Epidemiol. 2009. 38 (1): 320–3. ответ автора 323-324.
PubMed Статья Google Scholar
Шенн Ф. Неспецифические эффекты вакцин и расширенная программа иммунизации. J Infect Dis. 2011. 204 (2): 182–4.
PubMed Статья Google Scholar
Шенн Ф. Неспецифические эффекты вакцин. Arch Dis Child. 2010. 95 (9): 662–7.
PubMed Статья Google Scholar
Hirve S, Bavdekar A, Juvekar S, Benn CS, Nielsen J, Aaby P. Неспецифические и дифференцированные по полу эффекты вакцинации на выживаемость детей в сельских районах западной Индии. Вакцина. 2012. 30 (50): 7300–8.
PubMed Статья Google Scholar
Рот А., Гарли М.Л., Дженсен Х., Нильсен Дж., Оби П. Вакцинация против бактерий Кальметта-Герена и младенческая смертность. Экспертные ревакцины. 2006; 5 (2): 277–93.
PubMed Статья Google Scholar
Шенн Ф. Комментарий: вакцинация БЦЖ снижает неонатальную смертность вдвое. Pediatr Infect Dis J. 2012; 31 (3): 308–9.
PubMed Статья Google Scholar
Aaby P, Roth A, Ravn H, Napirna BM, Rodrigues A, Lisse IM, Stensballe L, Diness BR, Lausch KR, Lund N, et al. Рандомизированное испытание вакцинации БЦЖ детям с низкой массой тела при рождении: положительные неспецифические эффекты в неонатальном периоде? J Infect Dis. 2011. 204 (2): 245–52.
CAS PubMed Статья Google Scholar
Биринг-Соренсен С., Оби П., Напирна Б.М., Рот А., Равн Х., Родригес А., Уиттл Х., Бенн С.С.. Небольшое рандомизированное исследование среди детей с низкой массой тела при рождении, получивших вакцинацию против бациллы Кальметта-Герена при первом обращении в медицинский центр. Pediatr Infect Dis J. 2012; 31 (3): 306–8.
PubMed Статья Google Scholar
Roth AE, Stensballe LG, Garly ML, Aaby P. Благоприятные нецелевые эффекты БЦЖ — этические последствия для предстоящего внедрения новых противотуберкулезных вакцин. Туберкулез (Edinb). 2006. 86 (6): 397–403.
CAS Статья Google Scholar
Stensballe LG, Nante E, Jensen IP, Kofoed PE, Poulsen A, Jensen H, Newport M, Marchant A, Aaby P. Острые инфекции нижних дыхательных путей и респираторно-синцитиальный вирус у младенцев в Гвинее-Бисау: a Благоприятный эффект вакцинации БЦЖ для девочек в рамках исследования методом случай-контроль.Вакцина. 2005. 23 (10): 1251–7.
CAS PubMed Статья Google Scholar
Джейсон Дж., Арчибальд Л.К., Нваньянву О.К., Казембе П.Н., Чатт Дж. А., Нортон Е., Добби Х., Джарвис В. Р.. Клиническое и иммунное воздействие Mycobacterium bovis рубцевание после вакцинации БЦЖ. Заражение иммунной. 2002. 70 (11): 6188–95.
CAS PubMed PubMed Central Статья Google Scholar
Nankabirwa V, Tumwine JK, Mugaba PM, Tylleskar T, Sommerfelt H, Group P-ES. Выживание детей и вакцинация БЦЖ: проспективное когортное исследование на уровне общины в Уганде. BMC Public Health. 2015; 15: 175.
PubMed PubMed Central Статья Google Scholar
Rousseau MC, Parent ME, St-Pierre Y. Потенциальные последствия для здоровья от неспецифической стимуляции иммунной функции в раннем возрасте: пример вакцинации БЦЖ.Pediatr Allergy Immunol. 2008. 19 (5): 438–48.
PubMed Статья Google Scholar
Aaby P, Shaheen SO, Heyes CB, Goudiaby A, Hall AJ, Shiell AW, Jensen H, Marchant A. Ранняя вакцинация БЦЖ и снижение атопии в Гвинее-Бисау. Clin Exp Allergy. 2000. 30 (5): 644–50.
CAS PubMed Статья Google Scholar
Ota MO, van der Sande MA, Walraven GE, Jeffries D, Nyan OA, Marchant A, McAdam KP.Отсутствие связи между гиперчувствительностью замедленного типа к туберкулину и атопией у детей в Гамбии. Clin Exp Allergy. 2003. 33 (6): 731–6.
CAS PubMed Статья Google Scholar
Choi IS, Koh YI. Терапевтические эффекты вакцинации БЦЖ у взрослых пациентов с астмой: рандомизированное контролируемое исследование. Ann Allergy Asthma Immunol. 2002. 88 (6): 584–91.
PubMed Статья Google Scholar
Эллиотт А.М., Накииинги Дж., Куигли Массачусетс, Френч Н., Гилкс К.Ф., Уитворт Дж. А.. Обратная связь между иммунизацией БЦЖ и заражением кишечными нематодами среди ВИЧ-1-положительных людей в Уганде. Ланцет. 1999. 354 (9183): 1000–1.
CAS PubMed Статья Google Scholar
Баррето М.Л., Родригес Л.С., Силва Р.К., Ассис А.М., Рейс М.Г., Сантос, Калифорния, Блэнтон, RE. Снижение заболеваемости, распространенности и интенсивности инфекции у детей с шрамом от вакцинации Bacillus Calmette-Guerin.J Infect Dis. 2000. 182 (6): 1800–3.
CAS PubMed Статья Google Scholar
Рэндалл А.Е., Перес М.А., Флойд С., Блэк Г.Ф., Крампин А.С., Нгвира Б., Пистони В.Н., Мулава Д., Сичали Л., Мваунгулу Л. и др. Характер заражения гельминтами и связь с вакцинацией БЦЖ в районе Каронга на севере Малави. Trans R Soc Trop Med Hyg. 2002. 96 (1): 29–33.
CAS PubMed Статья Google Scholar
Всемирная организация здравоохранения. Глобальный доклад о туберкулезе, 2013 г. Женева: Всемирная организация здравоохранения; 2013.
Google Scholar
Рабочая группа SAGE по неспецифическим эффектам вакцин (март 2013 г. — июнь 2013 г.). http://www.who.int/immunization/sage/sage_wg_non_specific_effects_vaccines_march3013/en/. По состоянию на 15 декабря 2015 г.
Fine PE, Williams TN, Aaby P, Kallander K, Moulton LH, Flanagan KL, Smith PG, Benn CS, Working Group on Non-specific Effects of Vaccines.Эпидемиологические исследования «неспецифических эффектов» вакцин: I – сбор данных в обсервационных исследованиях. Trop Med Int Health. 2009. 14 (9): 969–76.
PubMed Статья Google Scholar
Фаррингтон С.П., Ферт М.Дж., Моултон Л.Х., Равн Х., Андерсен П.К., Эванс С., Рабочая группа по неспецифическим эффектам вакцин. Эпидемиологические исследования неспецифических эффектов вакцин: II – методологические вопросы планирования и анализа когортных исследований.Trop Med Int Health. 2009. 14 (9): 977–85.
CAS PubMed Статья Google Scholar
Кристенсен И., Оби П., Дженсен Х. Рутинные вакцинации и выживаемость детей: последующее исследование в Гвинее-Бисау, Западная Африка. BMJ. 2000. 321 (7274): 1435–8.
CAS PubMed PubMed Central Статья Google Scholar
Vaugelade J, Pinchinat S, Guiella G, Elguero E, Simondon F.Неспецифические эффекты вакцинации на выживаемость детей: проспективное когортное исследование в Буркина-Фасо. BMJ. 2004; 329 (7478): 1309.
CAS PubMed PubMed Central Статья Google Scholar
Кандасами Р., Войси М., Маккуэйд Ф., де Ни К., Райан Р., Орр О., Улиг Ю., Санде С., О’Коннор Д., Поллард А.Дж. Неспецифические иммунологические эффекты выбранных плановых детских иммунизаций: систематический обзор. BMJ. 2016; 355: i5225.
PubMed PubMed Central Статья Google Scholar
Хиггинс Дж. П., Соарес-Вайзер К., Лопес-Лопес Дж. А., Какуру А., Чаплин К., Кристенсен Х., Мартин Н. К., Стерн Дж. А., Рейнгольд А. Л.. Связь вакцины, содержащей БЦЖ, АКДС и кори, с детской смертностью: систематический обзор. BMJ. 2016; 355: i5170.
PubMed PubMed Central Статья Google Scholar
Wilson CB. Применение современной иммунологии для выяснения гетерологичных эффектов детских вакцин и лучшего информирования о методах иммунизации матери и ребенка.Фронт Иммунол. 2015; 6: 64.
PubMed PubMed Central Статья Google Scholar
Netea MG, Quintin J, van der Meer JW. Тренированный иммунитет: память о врожденной защите хозяина. Клеточный микроб-хозяин. 2011. 9 (5): 355–61.
CAS PubMed Статья Google Scholar
Саид С., Квинтин Дж., Керстенс Х.Х., Рао Н.А., Агаджанирефа А., Матарезе Ф., Ченг С.К., Раттер Дж., Берентсен К., ван дер Энт М.А. и др.Эпигенетическое программирование дифференцировки моноцитов и макрофагов и тренированный врожденный иммунитет. Наука. 2014; 345 (6204): 1251086.
PubMed PubMed Central Статья Google Scholar
Kleinnijenhuis J, Quintin J, Preijers F, Joosten LA, Ifrim DC, Saeed S, Jacobs C., van Loenhout J, de Jong D, Stunnenberg HG, et al. Бацилла Кальметта-Герена индуцирует NOD2-зависимую неспецифическую защиту от повторного заражения посредством эпигенетического репрограммирования моноцитов.Proc Natl Acad Sci U S. A. 2012; 109 (43): 17537–42.
CAS PubMed PubMed Central Статья Google Scholar
Селин Л.К., Варга С.М., Вонг IC, Валлийский РМ. Защитный гетерологичный противовирусный иммунитет и усиленный иммунопатогенез, опосредованный популяциями Т-клеток памяти. J Exp Med. 1998. 188 (9): 1705–15.
CAS PubMed PubMed Central Статья Google Scholar
Маццола Т.Н., да Силва М.Т., Абрамчук Б.М., Морено Ю.М., Лима СК, Зорзето Т.К., Пассето А.С., Вилела М.М. Нарушение клеточного иммунного ответа Bacillus Calmette-Guerin у неинфицированных младенцев, контактировавших с ВИЧ. СПИД. 2011. 25 (17): 2079–87.
PubMed Статья Google Scholar
Hesseling AC, Cotton MF, Fordham von Reyn C, Graham SM, Gie RP, Hussey GD. Заявление о консенсусе по пересмотренным рекомендациям Всемирной организации здравоохранения по вакцинации БЦЖ у ВИЧ-инфицированных младенцев.Int J Tuberc Lung Dis. 2008. 12 (12): 1376–9.
CAS PubMed Google Scholar
Hesseling AC, Caldwell J, Cotton MF, Eley BS, Jaspan HB, Jennings K, Marais BJ, Nuttall J, Rabie H, Roux P и др. Вакцинация БЦЖ младенцев, контактировавших с ВИЧ в Южной Африке, — риски и преимущества. S Афр Мед Ж. 2009; 99 (2): 88–91.
CAS PubMed PubMed Central Google Scholar
Miles DJ, Gadama L, Gumbi A, Nyalo F, Makanani B, Heyderman RS. Инфекция вируса иммунодефицита человека (ВИЧ) во время беременности вызывает дифференцировку Т-лимфоцитов CD4 и модулирует ответы на вакцину Бациллы Кальметта-Герена (БЦЖ) у младенцев, не инфицированных ВИЧ. Иммунология. 2010. 129 (3): 446–54.
CAS PubMed PubMed Central Статья Google Scholar
Ота МО, О’Донован Д., Марчант А., Ямуа Л., Хардинг Э., Джаффар С., Макадам К.П., Корра Т., Уиттл Х.У ВИЧ-отрицательных младенцев, рожденных от ВИЧ-1, но не ВИЧ-2-положительных матерей, не развивается рубец Bacillus Calmette-Guerin. СПИД. 1999. 13 (8): 996–8.
CAS PubMed Статья Google Scholar
Мселлати П., Дабис Ф., Лепаж П., Хитимана Д.Г., Ван Гётем К., Ван де Перре П. Вакцинация БЦЖ и детская ВИЧ-инфекция — Руанда, 1988–1990. MMWR. 1991. 40 (48): 833–6.
Google Scholar
Garly ML, Martins CL, Bale C, Balde MA, Hedegaard KL, Gustafson P, Lisse IM, Whittle HC, Aaby P. Шрам от БЦЖ и положительная реакция на туберкулин, связанные со снижением детской смертности в Западной Африке. А неспецифический положительный эффект БЦЖ? Вакцина. 2003. 21 (21-22): 2782–90.
PubMed Статья Google Scholar
Clerici M, Saresella M, Colombo F, Fossati S, Sala N, Bricalli D, Villa ML, Ferrante P, Dally L, Vigano A.Нарушения созревания Т-лимфоцитов у неинфицированных новорожденных и детей с вертикальным контактом с ВИЧ. Кровь. 2000. 96 (12): 3866–71.
CAS PubMed Google Scholar
Nielsen SD, Jeppesen DL, Kolte L, Clark DR, Sorensen TU, Dreves AM, Ersboll AK, Ryder LP, Valerius NH, Nielsen JO. Нарушение функции клеток-предшественников у ВИЧ-отрицательных младенцев от ВИЧ-положительных матерей приводит к снижению выработки тимуса и снижению числа CD4.Кровь. 2001. 98 (2): 398–404.
CAS PubMed Статья Google Scholar
Эмбри Дж., Буэйо Дж., Нагелькерке Н., Ньенга С., Ньянге П., Ндинья-Ахола Дж., Памба Х., Пламмер Ф. Субпопуляции лимфоцитов у детей, инфицированных и неинфицированных вирусом иммунодефицита человека типа 1, в Найроби. Pediatr Infect Dis J. 2001; 20 (4): 397–403.
CAS PubMed Статья Google Scholar
Chougnet C, Kovacs A, Baker R, Mueller BU, Luban NL, Liewehr DJ, Steinberg SM, Thomas EK, Shearer GM. Влияние материнской среды, инфицированной вирусом иммунодефицита человека, на развитие продукции детского интерлейкина-12. J Infect Dis. 2000. 181 (5): 1590–7.
CAS PubMed Статья Google Scholar
Кун Л., Коутсудис А., Мудли Д., Мнгкунданисо Н., Трабаттони Д., Ширер Г.М., Клеричи М., Кувадия Х.М. Продукция интерферона-гамма и интерлейкина-10 среди ВИЧ-1-инфицированных и неинфицированных младенцев ВИЧ-1-инфицированных матерей.Pediatr Res. 2001. 50 (3): 412–6.
CAS PubMed Статья Google Scholar
Леви Дж. А., Сюэ Ф, Блэкборн Диджей, Вара Д., Вайнтруб ПС. Нецитотоксическая противовирусная активность клеток CD8 у детей, инфицированных и неинфицированных вирусом иммунодефицита человека. J Infect Dis. 1998. 177 (2): 470–2.
CAS PubMed Статья Google Scholar
Кагина Б.М., Абель Б., Боумейкер М., Скриба Т.Дж., Гелдерблоем С., Смит Э., Эразмус М., Нене Н., Вальцл Г., Блэк Г. и др.Отсрочка вакцинации БЦЖ с рождения до 10-недельного возраста может привести к усилению Т-клеточного ответа CD4 в памяти. Вакцина. 2009. 27 (40): 5488–95.
CAS PubMed PubMed Central Статья Google Scholar
Blakney AK, Tchakoute CT, Hesseling AC, Kidzeru EB, Jones CE, Passmore JA, Sodora DL, Gray CM, Jaspan HB. Отсроченная вакцинация БЦЖ приводит к минимальным изменениям Т-клеточной иммуногенности бесклеточных иммунизаций против коклюша и столбняка у новорожденных, контактировавших с ВИЧ.Вакцина. 2015; 33 (38): 4782–9.
CAS PubMed PubMed Central Статья Google Scholar
ЮНЭЙДС. Глобальный отчет: доклад ЮНЭЙДС о глобальной эпидемии СПИДа 2010. 2010.
Обновленная информация об эпидемии СПИДа, региональное резюме: Африка к югу от Сахары. http://data.unaids.org/pub/Report/2008/JC1526_epibriefs_subsaharanafrica_en.pdf. По состоянию на 20 января 2014 г.
Mofenson LM. Достижения в профилактике вертикальной передачи вируса иммунодефицита человека.Semin Pediatr Infect Dis. 2003. 14 (4): 295–308.
PubMed Статья Google Scholar
Аганги А., Торн С., Ньюэлл М.Л. Повышение вероятности дальнейших живорождений у ВИЧ-инфицированных женщин в последние годы. BJOG. 2005. 112 (7): 881–8.
PubMed Статья Google Scholar
Филто С. Неинфицированный африканский ребенок, контактировавший с ВИЧ. Trop Med Int Health.2009. 14 (3): 276–87.
PubMed Статья Google Scholar
Афран Л., Гарсия Найт М., Ндуати Е., Урбан БК, Хейдерман Р.С., Роуленд-Джонс С.Л. Неинфицированные дети, контактирующие с ВИЧ: растущее население с уязвимой иммунной системой? Clin Exp Immunol. 2014. 176 (1): 11–22.
CAS PubMed PubMed Central Статья Google Scholar
Slogrove A, Reikie B, Naidoo S, De Beer C, Ho K, Cotton M, Bettinger J, Speert D, Esser M, Kollmann T.Неинфицированные младенцы, контактировавшие с ВИЧ, подвергаются повышенному риску тяжелых инфекций в первый год жизни. J Trop Pediatr. 2012. 58 (6): 505–8.
Slogrove AL, Cotton MF, Esser MM. Тяжелые инфекции у неинфицированных младенцев, контактировавших с ВИЧ: клинические доказательства иммунодефицита. J Trop Pediatr. 2010. 56 (2): 75–81.
CAS PubMed Статья Google Scholar
Taron-Brocard C, Le Chenadec J, Faye A, Dollfus C, Goetghebuer T., Gajdos V, Labaune JM, Perilhou A, Mandelbrot L, Blanche S и др.Повышенный риск серьезных бактериальных инфекций из-за подавления материнского иммунитета у неинфицированных младенцев, контактировавших с ВИЧ, в одной из европейских стран. Clin Infect Dis. 2014. 59 (9): 1332–45.
CAS PubMed Статья Google Scholar
Heresi GP, Caceres E, Atkins JT, Reuben J, Doyle M. Pneumocystis carinii пневмония у младенцев, которые подверглись воздействию вируса иммунодефицита человека, но не были инфицированы: исключение из определения случая эпиднадзора за СПИДом.Clin Infect Dis. 1997. 25 (3): 739–40.
CAS PubMed Статья Google Scholar
Адхикари М., Каучали С., Мудли А. Клинический профиль и картина заболеваемости младенцев, рожденных ВИЧ-инфицированными матерями в Дурбане, Южная Африка. Indian Pediatr. 2006. 43 (9): 804–8.
PubMed Google Scholar
фон Моллендорф С., фон Готтберг А., Темпиа С., Мейринг С., де Гувейя Л., Куан В., Ленгана С., Авенант Т., дю Плесси Н., Элей Б. и др.Повышенный риск и смертность от инвазивной пневмококковой инфекции у контактировавших с ВИЧ, но неинфицированных младенцев в возрасте <1 года в Южной Африке, 2009-2013 гг. Clin Infect Dis. 2015; 60 (9): 1346–56.
Артикул Google Scholar
Изаднегадар Р., Фокс М.П., Джина П., Кази С.А., Теа Д.М. Пересмотр пневмонии и контактного статуса у младенцев, рожденных от ВИЧ-инфицированных матерей. Pediatr Infect Dis J. 2014; 33 (1): 70–2.
PubMed Статья Google Scholar
Manicklal S, van Niekerk AM, Kroon SM, Hutto C, Novak Z, Pati SK, Chowdhury N, Hsiao NY, Boppana SB. Распространенность при рождении врожденного цитомегаловируса среди младенцев от ВИЧ-инфицированных женщин, получающих пренатальную антиретровирусную профилактику в Южной Африке. Clin Infect Dis. 2014. 58 (10): 1467–72.
CAS PubMed Статья Google Scholar
Пайфер Л.Л., Хьюз В.Т., Стагно С., Вудс Д. Инфекция Pneumocystis carinii : данные о высокой распространенности у здоровых детей и детей с ослабленным иммунитетом.Педиатрия. 1978. 61 (1): 35–41.
CAS PubMed Google Scholar
Кун Л., Касонде П., Синкала М., Канкаса К., Семрау К., Скотт Н., Цай В.Й., Вермунд С.Х., Альдрованди Г.М., Теа Д.М. Влияет ли тяжесть ВИЧ-инфекции у ВИЧ-инфицированных матерей на смертность и заболеваемость среди их неинфицированных младенцев? Clin Infect Dis. 2005. 41 (11): 1654–61.
PubMed PubMed Central Статья Google Scholar
Kleinnijenhuis J, Quintin J, Preijers F, Joosten LA, Jacobs C, Xavier RJ, van der Meer JW, van Crevel R, Netea MG. БЦЖ-индуцированный обученный иммунитет в NK-клетках: роль в неспецифической защите от инфекции. Clin Immunol. 2014; 155 (2): 213–9.
CAS PubMed PubMed Central Статья Google Scholar
Тайлескар Т., Джексон Д., Меда Н., Энгебретсен И.М., Чопра М., Диалло А.Х., Доэрти Т., Экстром ЕС, Фаднес Л.Т., Гога А. и др.Эксклюзивная пропаганда грудного вскармливания со стороны равных консультантов в Африке к югу от Сахары (PROMISE-EBF): кластерное рандомизированное исследование. Ланцет. 2011. 378 (9789): 420–7.
PubMed Статья Google Scholar
Всемирная организация здравоохранения. Стандарты роста детей ВОЗ: длина тела / рост к возрасту, масса тела к возрасту, масса тела к длине тела, масса тела к росту и индекс массы тела к возрасту: методы и разработка. Женева: Всемирная организация здравоохранения; 2006. с. 312.
Google Scholar
Всемирная организация здравоохранения. Надлежащая клиническая лабораторная практика (GCLP). Женева: Всемирная организация здравоохранения; 2009.
Каммингс П. Методы оценки скорректированных соотношений рисков. Стата Дж. 2009; 9 (2): 175–96.
Артикул Google Scholar
Шпигельман Д., Герцмарк Э. Простые расчеты SAS для соотношений риска или распространенности и различий.Am J Epidemiol. 2005. 162 (3): 199–200.
PubMed Статья Google Scholar
Zou G. Модифицированный подход регрессии Пуассона к проспективным исследованиям с бинарными данными. Am J Epidemiol. 2004. 159 (7): 702–6.
PubMed Статья Google Scholar
Исследовательская группа ДАМОКЛА. Предлагаемый устав комитетов по мониторингу данных клинических испытаний: помогать им хорошо выполнять свою работу.Ланцет. 2005; 365 (9460): 711–22.
Артикул Google Scholar
Грант А.М., Альтман Д.Г., Бабикер А.Б., Кэмпбелл М.К., Клеменс Ф.Дж., Дарбишир Дж. Х., Элбурн Д.Р., МакЛир С.К., Пармар М.К., Покок С.Дж. и др. Проблемы мониторинга данных и промежуточного анализа исследований. Оценка медицинских технологий. 2005. 9 (7): 1–238. iii-iv.
CAS PubMed Статья Google Scholar
Siegfried N, van der Merwe L, Brocklehurst P, Sint TT.Антиретровирусные препараты для снижения риска передачи ВИЧ-инфекции от матери ребенку. Кокрановская база данных Syst Rev.2011; 7: CD003510.
Google Scholar
Rieder HL. Возможность заражения и риск заражения: топливо для пандемии туберкулеза. Инфекционное заболевание. 1995; 23 (1): 1–3.
CAS PubMed Статья Google Scholar
Kesho Bora Study G, de Vincenzi I.Тройной антиретровирусный препарат по сравнению с зидовудином и профилактикой однократной дозы невирапина во время беременности и грудного вскармливания для предотвращения передачи ВИЧ-1 от матери ребенку (исследование Кешо Бора): рандомизированное контролируемое исследование. Lancet Infect Dis. 2011; 11 (3): 171–80.
Артикул Google Scholar
Bernatowska EA, Wolska-Kusnierz B, Pac M, Kurenko-Deptuch M, Zwolska Z, Casanova JL, Piatosa B, van Dongen J, Roszkowski K, Mikoluc B, et al.Распространенная бацилла Кальметта-Герена, инфекция и иммунодефицит. Emerg Infect Dis. 2007. 13 (5): 799–801.
PubMed PubMed Central Статья Google Scholar
Правила и процедуры. https://helseforskning.etikkom.no/ikbViewer/page/reglerogrutiner/loverogregler?p_dim=34770&_ikbLanguageCode=us. По состоянию на 23 июня 2014 г.
Старая противотуберкулезная вакцина обретает новую жизнь в испытаниях на коронавирус
Одна из самых старых вакцин может защитить нас от новейшего инфекционного заболевания COVID-19.Вакцина вводилась младенцам для защиты от туберкулеза почти столетие, но было показано, что она защищает их и от других инфекций, что побудило ученых исследовать, может ли она защитить от коронавируса.
Эта вакцина с бациллой Кальметта-Герена (БЦЖ), названная в честь двух французских микробиологов, состоит из живого ослабленного штамма Mycobacterium bovis, двоюродного брата M. tuberculosis, бактерии, вызывающей туберкулез. БЦЖ была введена более чем 4 миллиардам человек, что делает ее наиболее широко применяемой вакциной в мире.
Поскольку вакцина БЦЖ защищает детей не только от туберкулеза, но и от некоторых вирусных инфекций, исследователи решили сравнить данные из стран с обязательной вакцинацией БЦЖ и без нее, чтобы выяснить, связана ли политика иммунизации с количеством или серьезностью инфекций COVID-19. В нескольких препринтных публикациях за последние два месяца отмечалось, что страны, в которых действует программа вакцинации БЦЖ, имеют более низкий уровень смертности от COVID-19, чем страны без них.
Эти неспецифические эффекты [от BCG] наиболее сильны, когда мы смотрим на исходы респираторных инфекций.
—Кристин Стабелл Бенн, Университет Южной Дании
Одно исследование, например, показало, что обязательная БЦЖ была связана со значительно более медленным ростом как подтвержденных случаев, так и смертей в течение первых 30 дней вспышки. Другой смоделировал смертность в двух десятках стран и сообщил, что те, кто не получил всеобщей вакцинации БЦЖ, такие как Италия, США и Нидерланды, пострадали от пандемии сильнее, чем те, кто получил всеобщую вакцинацию.
Обратной стороной препринтов является то, что они показывают статистическую корреляцию, а не причинно-следственную связь. «Есть много источников предвзятости, присущих этим межстрановым сравнениям», — предупреждает Зои Макларен, профессор общественного здравоохранения в Университете Мэриленда. Например, по ее словам, страны, внедряющие вакцину БЦЖ, могут с большей вероятностью также принять упреждающие меры для защиты своего населения от COVID-19, такие как приказы о предоставлении убежища на месте. Макларен говорит, что в этих исследованиях она может вспомнить почти 20 источников предвзятости.В другом примере те, кто получил вакцину БЦЖ, могут с большей вероятностью иметь лучший старт в жизни, что выведет их на более здоровый путь. Исследования не могут учесть все смешивающие факторы.
Эпидемиолог Кристин Стабелл Бенн из Университета Южной Дании изучала вакцину БЦЖ в течение последних двух десятилетий и сообщила, что она снижает общую детскую смертность от инфекционных заболеваний. Она предостерегает от чрезмерного чтения препринтов. «Это самое слабое свидетельство, которое есть в нашей пирамиде доказательств», — говорит она.«Он просто связывает преобладание одного с преобладанием другого».
Но вместо того, чтобы отказываться от идеи связи BCG с меньшим количеством случаев COVID или смертей, она говорит, что есть веская причина серьезно задуматься над этим. У нее есть более прямые доказательства того, что вакцинация БЦЖ может подготовить нашу иммунную систему к вирусным инфекциям. В настоящее время начался ряд клинических испытаний, чтобы выяснить, может ли прививка БЦЖ, сделанная тем, кто наиболее подвержен риску заражения инфекцией, защитить их от болезни.
Доказательства того, что вакцина БЦЖ защищает от других инфекций
Работа Бенна относится к числу накопленных доказательств, как подробно описано в недавнем обзоре, о том, что вакцинация БЦЖ детям защищает от других заболеваний, так называемых побочных эффектов.Большая часть доказательств в поддержку новых клинических исследований основана на исследованиях, проведенных ее группой, и на работе Михая Нетеа из Медицинского центра Университета Радбауд в Нидерландах, который придумал механистическое объяснение того, почему БЦЖ — предназначена для предотвращения бактериальной инфекции. —Может повысить иммунный ответ на вирусы.
Исследование, проведенное в 2000 году супругой Бенна и его давним сотрудником Питером Аби из Bandim Health Project, показало значительное снижение смертности, которое было намного больше, чем можно было бы объяснить профилактикой туберкулеза у младенцев, получавших БЦЖ, в Гвинее-Бисау.А исследование 2005 года показало снижение инфекций нижних дыхательных путей у младенцев, вакцинированных БЦЖ, в той же стране. В более поздних исследованиях, в том числе опубликованном в 2017 году, Бенн и Аби рандомизировали тысячи детей с низкой массой тела при рождении в этой западноафриканской стране для получения вакцины БЦЖ прямо при рождении или для вакцинации в возрасте шести недель, что является обычной практикой. «Было снижение неонатальной смертности на треть у тех, кто получал БЦЖ [ранее]», — говорит Бенн. По ее словам, в основном это было связано с уменьшением заболеваемости респираторными заболеваниями и сепсисом у младенцев.
В Гвинее-Бисау исследователи также сравнили детей, у которых появился шрам после вакцинации, с детьми, получившими вакцину, но не получившими шрама. Рубец сигнализирует о соответствующем иммунном ответе на вакцину. В 2003 году Аби и его коллеги сообщили о значительно более низкой смертности у детей с шрамом от вакцины. В последующем метаанализе аналогичных исследований они предположили, что следует учитывать эффект ревакцинации детей без рубцов.
«Мы увидели снижение общей смертности более чем на 40 процентов среди тех, у кого был шрам, по сравнению с теми, у кого шрам не был», — говорит Бенн.
Бенн говорит, что она надеется, что BCG может дать некоторые преимущества при тяжелой форме COVID-19. Несколько недель назад она сделала себе прививку. «Эти неспецифические эффекты [от BCG] наиболее сильны, когда мы смотрим на исходы респираторных инфекций», — говорит Бенн.
изменено с сайта © ISTOCK.COM, VISUAL GENERATION, FAIRYWONG, WENMEI ZHOU; © TASHA DIBIAGIOВозможный механизм
Когда Бенн и Аби сообщили, что БЦЖ снижает уровень инфекционных заболеваний более десяти лет назад, в то время это было отклонено как биологически неправдоподобное, вспоминает она.Вакцины индуцируют долгоживущие В-клетки памяти, которые настраивают свои собственные гены, чтобы вырабатывать антитела против определенного микроба. Эти В-клетки затем остаются в костном мозге в резерве. Они быстро размножаются, если хозяин снова сталкивается с возбудителем, давая долгоживущий иммунитет. В-клетки не объясняют, почему вакцина позволит кому-то лучше реагировать на неродственный микроб.
Netea предложила в 2012 году, что БЦЖ работает, переводя «врожденное» звено иммунной системы, такое как макрофаги, в состояние повышенной готовности, явление, названное «тренированным иммунитетом».«Задача макрофагов — идентифицировать, поглощать и уничтожать чужеродные объекты. Они также могут сигнализировать о подкреплении с помощью цитокинов. Предполагалось, что эти охранники не запомнили конкретных патогенов, а выступали в качестве прямой защиты. Двадцать лет назад эта врожденная система большинством считалась грубой и неспецифической, говорит иммунолог Люк О’Нил из Тринити-колледжа в Дублине. «Затем в иммунологии произошла коперниканская революция. Внезапно стало понятно, насколько важна врожденная сторона.
См. «Спасибо за воспоминания»
Нобелевские премии в 2011 году получили ученые, открывшие врожденные рецепторы в качестве привратников иммунной системы. Их исследования пробудили больший интерес исследователей к клеткам врожденного иммунитета. Впоследствии Netea предположил, что БЦЖ запускает передовые иммунные клетки посредством эпигенетических изменений и метаболической перестройки. Это то, что позволяет им не быть в состоянии повышенной боевой готовности.
Приготовление врожденной иммунной системы имеет значение для вакцин и для будущих инфекций.«Если вы сначала сделаете вакцинацию БЦЖ, а затем сделаете вакцину против гриппа, вакцина от гриппа подействует лучше», — говорит Нетеа. Он сообщил об этом в 2015 году в ходе рандомизированного плацебо-контролируемого исследования вакцины против пандемического штамма 2009 года. В эксперименте приняли участие 40 человек. Этой осенью Бенн проверит, может ли введение БЦЖ за 14 дней до вакцинации от сезонного гриппа вызвать лучший ответ у людей старше 65 лет.
Чтобы понять, как БЦЖ может защитить от будущего патогена, Netea заразила здоровых добровольцев ослабленным желтым цветом. вирус лихорадки в рандомизированном плацебо-контролируемом исследовании.Субъекты, которые были вакцинированы БЦЖ за месяц до заражения, показали значительно меньшее количество циркулирующего вируса желтой лихорадки, чем те, которым вместо этого вводили плацебо. В исследовании, опубликованном в прошлом году, сделан вывод, что БЦЖ индуцирует эпигенетическое перепрограммирование моноцитов человека и приводит к более устойчивому ответу на вирус желтой лихорадки.
После введения БЦЖ «увеличивается выработка провоспалительных цитокинов. Они легче привлекают иммунные клетки к месту заражения, и эти клетки лучше убивают и устраняют вирус », — говорит Нетеа.
Согласно гипотезе Netea, БЦЖ может подготовить макрофаги таким образом, чтобы локально усилить цитокиновый ответ, направленный против SARS-CoV-2, сосредоточенный на месте инфекции. «Это предотвратит неэффективную системную реакцию позже, которая может нанести вред пациенту», — объясняет он, так называемый цитокиновый шторм. Макрофаги вызывают в руки В- и Т-клетки, а это означает, что те, которые были примированы БЦЖ, должны быть более эффективными в борьбе с инфекцией SARS-CoV-2.
Врожденный иммунизация после БЦЖ, вероятно, оптимальна в течение двух или трех лет, говорит Нетеа, оценка основана на эпидемиологических данных у детей.По его мнению, «тот факт, что кто-то был вакцинирован 50 или 60 лет назад, вероятно, не защищает». Это противоречит связям в эпидемиологических данных, предполагающих, что БЦЖ теперь помогает взрослым в ответ на COVID-19. Макларен говорит, что даже вакцина против туберкулеза длится всего два десятилетия. О’Нил тоже скептически относится к такому продолжительному врожденному праймингу. Он говорит, что ему интересно, могут ли страны с высоким уровнем вакцинации детей БЦЖ, такие как Япония, косвенно защитить пожилых людей от COVID-19, потому что вакцинированные дети не передают им эту болезнь в такой степени.
Бенн считает, что врожденная память еще может нас удивить. «Мы точно знаем, что эффект [БЦЖ] сохраняется у детей не менее одного года. У нас также есть признаки того, что он может длиться намного дольше, — говорит она, — в принципе, до сорока лет. Одно датское исследование, проведенное Оби и Бенном, показало, что у людей, получивших вакцину против оспы и / или БЦЖ при поступлении в школу, риск смерти до 45 лет снижался более чем на 40 процентов. «Это наблюдалось при инфекционных заболеваниях, а также сердечно-сосудистых заболеваниях. болезни и неврологические заболевания », — объясняет Бенн.
Начало клинических испытаний БЦЖ
Нетеа, который сотрудничает с Беном, опасается предполагать, что вакцина БЦЖ, сделанная несколько десятилетий назад, защищает от COVID-19, но остается непредубежденной в отношении эффективности более поздних прививок БЦЖ. «Нам нужны рандомизированные клинические испытания, чтобы сделать выводы», — говорит он. По словам Нетеа, испытания начинаются в Нидерландах, Греции, Австралии, Дании, Франции, Германии и США, в основном для тестирования БЦЖ у медицинского персонала.
Эта вакцина защищает детей от туберкулеза.Если мы начнем использовать его для чего-то недоказанного, есть опасность, что маленькие дети заплатят цену.
— Найджел Кертис, Детский научно-исследовательский институт Мердока и Мельбурнский университет
В австралийском испытании с участием 4000 медицинских работников «мы определим, получают ли те, кто получает вакцину, меньше COVID-19, и если они ее получают, если они недомогают в течение меньшего времени или имеют менее серьезные симптомы », — говорит Найджел Кертис, клиницист и исследователь Детского исследовательского института Мердока и Мельбурнского университета.
В Нидерландах Netea набирает 1500 добровольных поставщиков медицинских услуг, половина из которых будет случайным образом выбрана для приема БЦЖ. Он также скоро начнет испытание на 1600 добровольцах старше 60 лет, половина из которых получит инъекцию плацебо, а другая половина — БЦЖ. Netea рекомендует БЦЖ как возможную профилактическую меру только для групп риска, чтобы избежать дефицита. «Это могло бы стать мостом к вакцине», — говорит О’Нил, который отмечает, что туберкулезные бактерии живут в легких, поэтому БЦЖ, возможно, может повысить там иммунитет.«Я, конечно, жду испытаний».
Бенн планирует провести исследование в Дании с участием 1500 медицинских работников, рандомизированных для получения БЦЖ или плацебо, а затем наблюдаемых на COVID-19 и другие инфекционные заболевания. Дания использовала БЦЖ до 1980-х годов, поэтому будет подгруппа среди недавно вакцинированных, которые ранее получали вакцину БЦЖ в школе. Бенн предполагает, что польза от вакцины БЦЖ будет более выражена среди этой подгруппы медицинских работников, чем среди тех, кому не делали прививку БЦЖ в детстве.
Риск нехватки БЦЖ
Ввиду отсутствия данных клинических испытаний Всемирная организация здравоохранения не рекомендует вакцину БЦЖ для профилактики COVID-19. Есть опасения, что люди могут отказаться от применения препарата и решить, что вакцина БЦЖ эффективна, до того, как станут известны результаты испытаний. Макларен говорит, что ее беспокоит, что серия сравнительных исследований препринтов может нанести вред. «Если люди интерпретируют эти корреляционные исследования как высококачественные доказательства или присоединятся к БЦЖ, тогда мы можем инвестировать в неэффективные меры политики и отнимать ресурсы у младенцев и детей, нуждающихся в вакцинах БЦЖ», — говорит она.
Кертис тоже обеспокоен. Он говорит, что слышал о том, что в некоторых частях Африки вакцины, предназначенные для детей, передаются медицинским работникам. «Это трагедия», — говорит Кертис. «Эта вакцина защищает детей от туберкулеза. Если мы начнем использовать его для чего-то недоказанного, есть опасность, что маленькие дети заплатят за это цену ».
Шрамы от вакцины БЦЖ связаны со снижением детской смертности
13 февраля, 2019
2 мин чтения
ДОБАВИТЬ ТЕМУ В ОПОВЕЩЕНИЯ ПО ЭЛЕКТРОННОЙ ПОЧТЕ
Получать электронное письмо, когда новые статьи публикуются на
Укажите свой адрес электронной почты, чтобы получать сообщения о публикации новых статей.Подписаться Нам не удалось обработать ваш запрос. Пожалуйста, повторите попытку позже. Если у вас по-прежнему возникает эта проблема, обратитесь по адресу [email protected].Вернуться в Healio
Питер Аби
По данным рандомизированного контролируемого исследования, опубликованного в журнале Journal of the Pediatric Infectious Disease с Общество. Исследователи написали, что влияние противотуберкулезной вакцины на смертность было не таким сильным, когда рубцы были только у ребенка.
Предыдущие исследования продемонстрировали преимущества некоторых живых вакцин, в том числе БЦЖ, для выживаемости детей за счет «усиления защиты от нецелевых инфекций».
«Рубцы БЦЖ являются сильными маркерами правильно проведенной вакцинации БЦЖ, и они указывают на то, что иммунная система обучена обеспечивать некоторую защиту от нетуберкулезных заболеваний», — Питер Аби, доктор медицинских наук, , профессор Bandim Health Project, рассказал Инфекционные болезни у детей . «Если у матери есть рубец от БЦЖ, вакцинация ребенка БЦЖ обеспечит дополнительную защиту от других заболеваний, не связанных с туберкулезом. Приготовление от матери может быть очень важным для реакции ребенка на вакцинацию, и в современной практике это не принимается во внимание ».
Исследователи включили почти 6500 детей в возрасте 4,5 месяцев в исследование, посвященное ранней вакцинации против кори. Дети находились под наблюдением до возраста 36 месяцев. Аби и его коллеги сравнили уровни нравственности детей в зависимости от того, есть ли у матери, ребенка или обоих шрам от БЦЖ.
Исследователи сосредоточили свое внимание на 2213 детях, которые не получали неонатальную добавку витамина А или раннюю вакцинацию против кори. Они выявили рубцевание БЦЖ у 83% этих детей и 44% матерей. Дети, чьи матери имели рубцы от БЦЖ, были более склонны к рубцеванию после БЦЖ (отношение рисков = 1,01; 95% ДИ, 0,98–1,05).
У матери и ребенка есть видимые рубцы от вакцинации БЦЖ. Эти рубцы у матерей и их младенцев связывают со снижением младенческой смертности.
Источник: Ребекка Фабрициус, Bandim Health Project
У детей, у которых были рубцы от БЦЖ, уровень смертности в возрасте от 4,5 до 36 месяцев был на 41% (95% ДИ, 5–64%) ниже. Исследователи подсчитали, что у детей уровень смертности на 66% (95% ДИ, 33% -83%) был ниже, если у их матерей также были рубцы от БЦЖ, но у детей, рожденных от матерей без рубцов, был только 8% (95% ДИ, –83%). % до 53%) снижение смертности ( P = 0,04).
«Программы охраны здоровья матери и ребенка должны контролировать состояние рубцов БЦЖ как у матери, так и у ребенка», — сказал Аби.
Он добавил, что люди, проживающие в регионах, где используется БЦЖ, включая Гвинею-Бисау, у которых нет рубца от БЦЖ, должны быть ревакцинированы.
«В настоящее время этого не происходит и может серьезно повлиять на выживание детей», — сказал он. «В педиатрических отделениях можно использовать отсутствие рубца БЦЖ для выявления детей из группы высокого риска». — Кэтрин Борц
Раскрытие информации: Авторы не сообщают о раскрытии соответствующей финансовой информации.
ДОБАВИТЬ ТЕМУ В ОПОВЕЩЕНИЯ ПО ЭЛЕКТРОННОЙ ПОЧТЕ
Получать электронное письмо, когда новые статьи публикуются на
Укажите свой адрес электронной почты, чтобы получать сообщения о публикации новых статей.Подписаться Нам не удалось обработать ваш запрос. Пожалуйста, повторите попытку позже. Если у вас по-прежнему возникает эта проблема, обратитесь по адресу [email protected].Вернуться в Healio
.