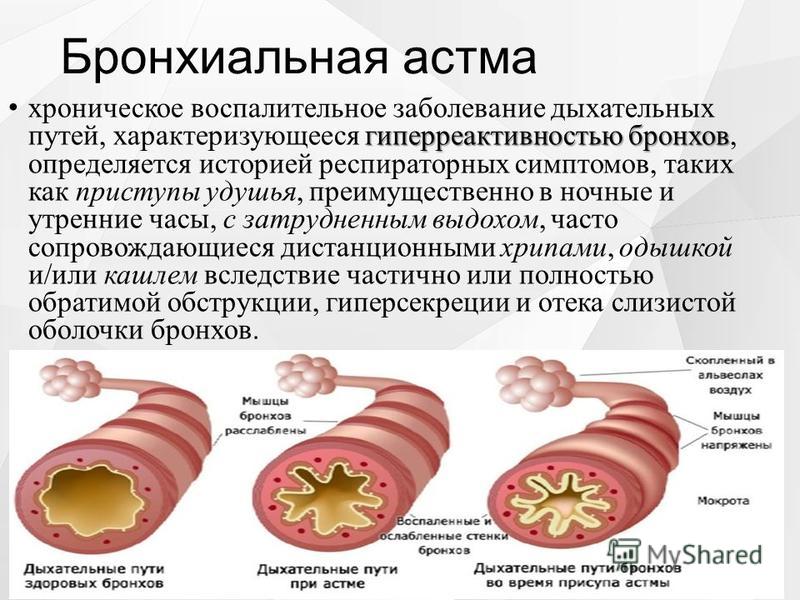
ГИПЕРРЕАКТИВНОСТЬ ДЫХАТЕЛЬНЫХ ПУТЕЙ ПРИ АСТМЕ: МЕХАНИЗМЫ РАЗВИТИЯ И ВЛИЯНИЕ ТЕРАПИИ | Черняк А.В.
В статье описаны физиологические механизмы развития гиперреактивности дыхательных путей, отражена роль эффекторных клеток воспаления и их медиаторов в ранней и поздней астматической реакции. На бронхиальную гиперреактивность влияют также повреждение эпителия, повышение сосудистой проницаемости, нарушение нейрогенной регуляции дыхательной системы. В заключение представлены медикаментозные средства, используемые при бронхиальной астме, и описано их воздействие на различные компоненты гиперреактивности бронхов.
The paper is concerned with the physiological mechanisms responsible for hyperreactivity of the respiratory tract, outlines the role of effector cells of inflammation and their mediators in early and late asthmatic reactions. Epithelial damage, higher vascular permeability, impaired neurogenic regulation of the respiratory system have also an impact on bronchial hyperreactivity. The conclusion deals with the drugs used in bronchial asthma and describes their effects on different components of bronchical hyperreactivity.
The conclusion deals with the drugs used in bronchial asthma and describes their effects on different components of bronchical hyperreactivity.
А.В. Черняк, канд. мед. наук. Старший научный сотрудник НИИ Пульмонологии, г. Москва
A. V. Chernyak, Candidate of Medical Sciences, senior research worker, Inst. of Pulmonology, Moscow
У больных бронхиальной астмой при функциональном исследовании отмечается ограничение воздушного потока. Обструктивные нарушения у этих больных достаточно вариабельны и их выраженность может изменяться спонтанно или под воздействием проведенной терапии. Такие изменения указывают на то, что у больных повышена чувствительность дыхательных путей к окружающим раздражителям, приводящая к острому сужению просвета бронхов.
Механизмы развития бронхиальной гиперреактивности
Гиперреактивность дыхательных путей является комплексным физиологическим нарушением, обусловленным гетерогенностью механизмов при астме. Множество эндо- и экзогенных факторов влияют на формирование повышенной реактивности дыхательных путей. Однако механизмы, лежащие в основе развития гиперреактивности бронхов, все еще мало изучены. Предполагают, что среди этих механизмов основную роль играют повреждение эпителия, повышение сосудистой проницаемости, отек стенки бронхов, медиаторы эффекторных клеток воспаления и нарушение функции вегетативной нервной системы. Важным является представление о том, что в становлении феномена бронхиальной гиперреактивности участвует нехолинергическая и неадренергическая иннервация и что этот феномен возникает как результат воспалительного процесса в слизистой оболочке бронхов [1]. Это позволило выдвинуть концепцию нейрогенного воспаления в дыхательных путях.
Множество эндо- и экзогенных факторов влияют на формирование повышенной реактивности дыхательных путей. Однако механизмы, лежащие в основе развития гиперреактивности бронхов, все еще мало изучены. Предполагают, что среди этих механизмов основную роль играют повреждение эпителия, повышение сосудистой проницаемости, отек стенки бронхов, медиаторы эффекторных клеток воспаления и нарушение функции вегетативной нервной системы. Важным является представление о том, что в становлении феномена бронхиальной гиперреактивности участвует нехолинергическая и неадренергическая иннервация и что этот феномен возникает как результат воспалительного процесса в слизистой оболочке бронхов [1]. Это позволило выдвинуть концепцию нейрогенного воспаления в дыхательных путях.
Эффекторные клетки воспаления и их медиаторы
В патогенезе астмы принимают участие многие клетки, среди которых особое внимание уделяют тучным клеткам, эозинофилам и лимфоцитам [2 – 5]. В ранней астматической реакции, возникающей после контакта с аллергеном, тучные клетки легких в результате опосредованной IgE дегрануляции выбрасывают хемотаксический фактор эозинофилов и нейтрофилов и такие медиаторы, как гистамин, серотонин, лейкотриены B Таким образом, тучные клетки выступают в роли триггера, запускающего воспалительную реакцию в дыхательных путях. Кроме того, они могут поддерживать ее [8]. В патогенезе бронхиальной гиперреактивности активное участие принимают и другие эффекторные клетки воспаления. Макрофаги могут быть активированы через IgE-зависимые механизмы и неаллергическими раздражителями. Это позволяет предположить, что они также могут быть вовлечены в воспалительный процесс при бронхиальной астме. Стимуляция альвеолярных макрофагов приводит к выработке таких медиаторов воспаления, как тромбоксан, простагландины и ФАТ [9], определяющих развитие поздней фазы аллергических реакций. Исследования на модели аллергического воспаления дыхательных путей in vitro показали, что повышение гиперреактивности коррелирует с эозинофильной и нейтрофильной инфильтрацией [10]. Нейтрофилы высвобождают такие воспалительные медиаторы, как деструктивные протеазы, способные повреждать ткань легкого [11]. Кроме того, они являются источником цитокинов, таких как интерлейкин (ИЛ) 8, воспалительный белок макрофагов 1a и 1b [12].
Таким образом, тучные клетки выступают в роли триггера, запускающего воспалительную реакцию в дыхательных путях. Кроме того, они могут поддерживать ее [8]. В патогенезе бронхиальной гиперреактивности активное участие принимают и другие эффекторные клетки воспаления. Макрофаги могут быть активированы через IgE-зависимые механизмы и неаллергическими раздражителями. Это позволяет предположить, что они также могут быть вовлечены в воспалительный процесс при бронхиальной астме. Стимуляция альвеолярных макрофагов приводит к выработке таких медиаторов воспаления, как тромбоксан, простагландины и ФАТ [9], определяющих развитие поздней фазы аллергических реакций. Исследования на модели аллергического воспаления дыхательных путей in vitro показали, что повышение гиперреактивности коррелирует с эозинофильной и нейтрофильной инфильтрацией [10]. Нейтрофилы высвобождают такие воспалительные медиаторы, как деструктивные протеазы, способные повреждать ткань легкого [11]. Кроме того, они являются источником цитокинов, таких как интерлейкин (ИЛ) 8, воспалительный белок макрофагов 1a и 1b [12].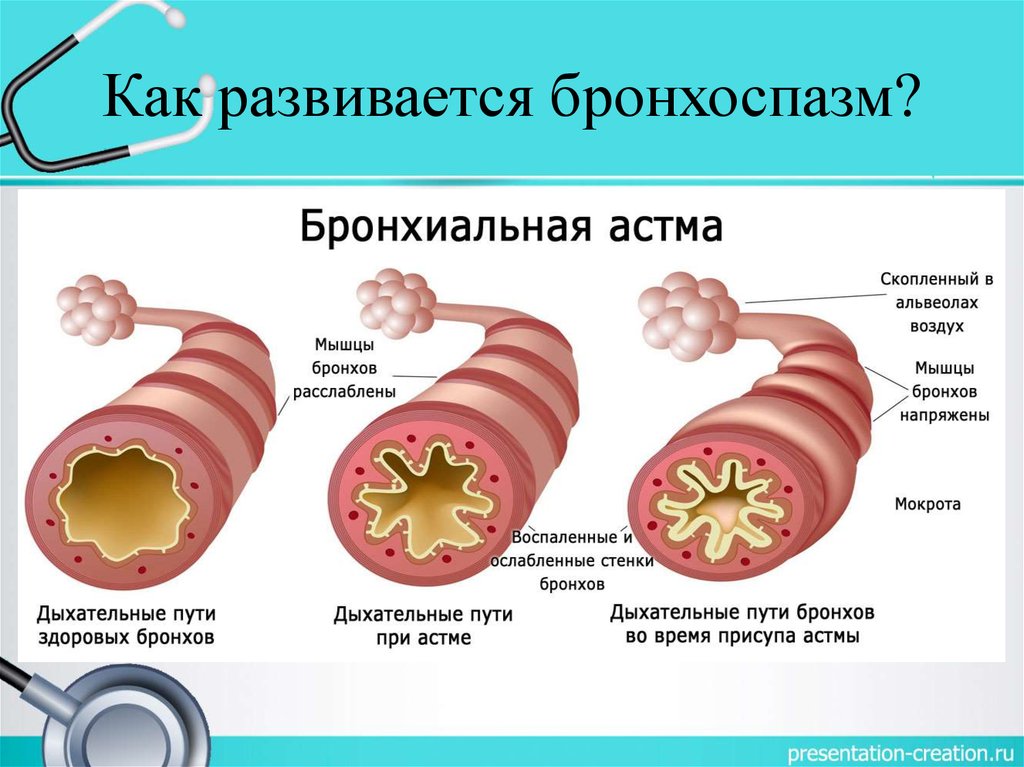
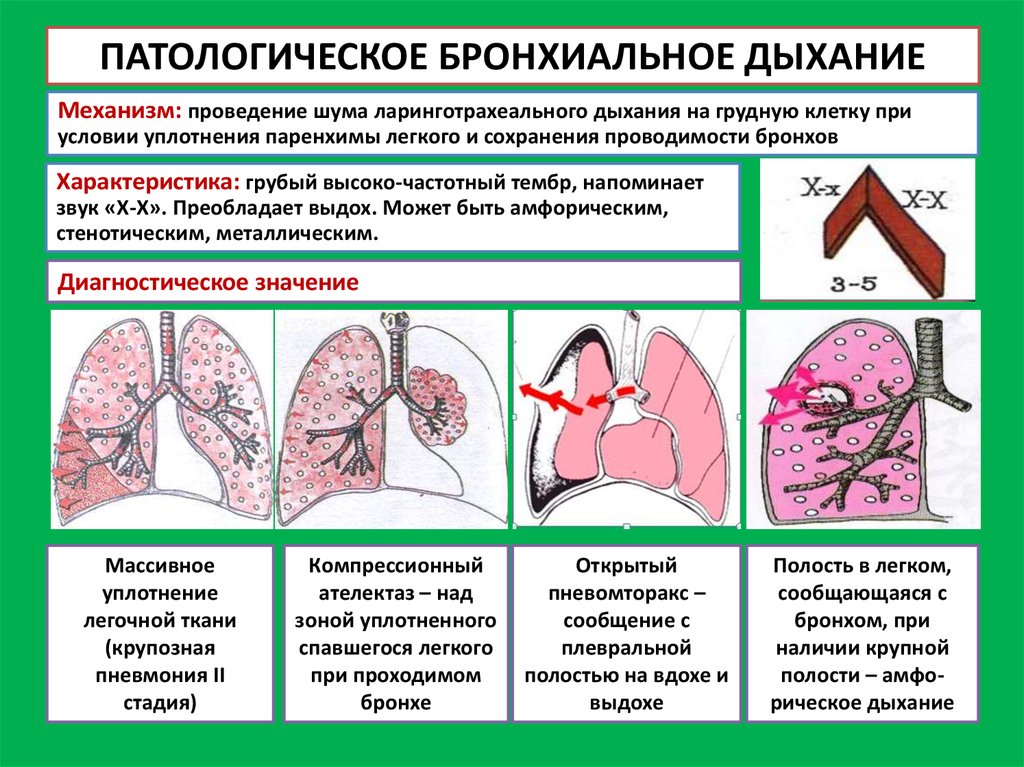
Повреждение эпителия
При астме наблюдается десквамация эпителия дыхательных путей с обтурацией просвета бронхов слизистыми пробками с примесью эозинофилов [6, 13]. Было обнаружено, что мокрота больных астмой содержит агглютинаты эпителиальных клеток и их количество значительно увеличивается во время обострения астмы [17]. Десквамация эпителия является наиболее характерной находкой на аутопсии у больных бронхиальной астмой, аналогичные изменения были обнаружены и при бронхобиопсии у пациентов с астмой легкого течения [9]. Различные эпителиальные повреждения могут быть следствием высвобождения из эозинофилов основных белков, а также результатом высвобождения различными эффекторными клетками воспаления кислородных радикалов и, возможно, следствием отека подслизистой оболочки.

Повышение сосудистой проницаемости
Многие медиаторы воспаления при астме, включая гистамин, брадикинин, лейкотриены и ФАТ, приводят к повышению проницаемости сосудов в дыхательных путях [6, 13]. Вследствие повышенной сосудистой проницаемости к бронхиальному секрету примешивается серозный белковый компонент, вязкость которого возрастает при пропотевании из сосудов легких альбумина [13]. Повышение проницаемости сосудов приводит к отеку слизистой оболочки дыхательных путей, который может привести к увеличению реактивности по геометрическим причинам. Известно, что сопротивление дыхательных путей воздушному потоку обратно пропорционально радиусу в 4-й степени. Поэтому даже небольшое уменьшение просвета дыхательных путей может привести к значительному повышению аэродинамического сопротивления.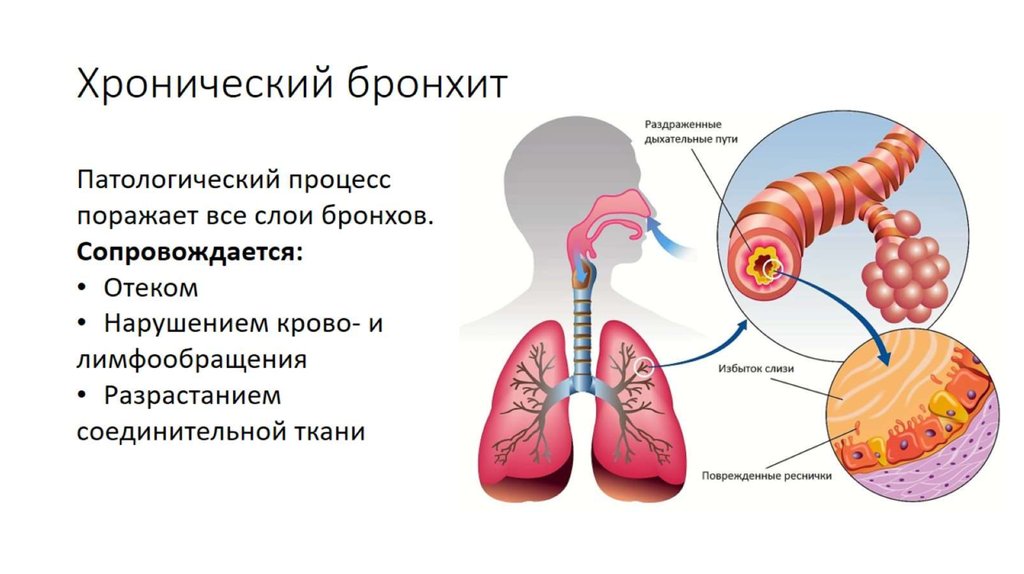
Нейрогенная регуляция
Нейрогенный контроль дыхательных путей человека сложен, и роль нейрогенных механизмов в патогенезе бронхиальной гиперреактивности все еще остается неясной [19]. Поскольку изменения в тонусе мускулатуры бронхов при астме происходят быстро, давно было сделано предположение, что при этом заболевании может иметь место расстройство регуляции вегетативной нервной системы, проявляющееся дисбалансом между возбуждающим и тормозящим влиянием, приводящее к чрезмерной «судорожности» дыхательных путей.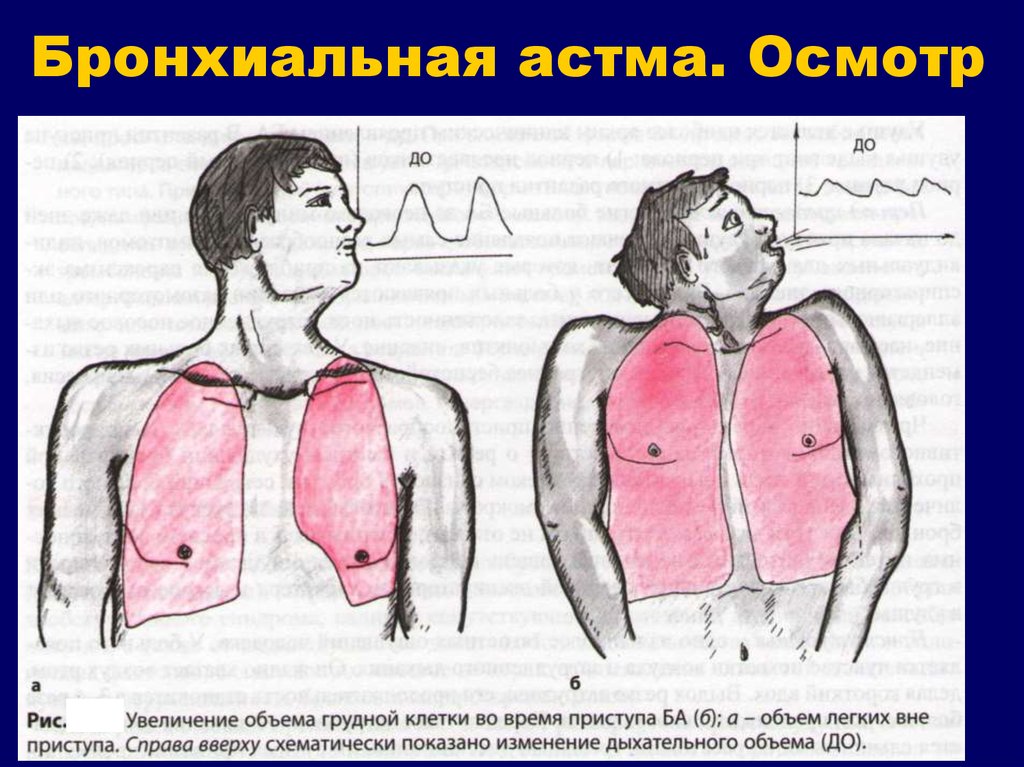 В дополнение к классическим адренергическим и холинергическим механизмам существуют неадренергические и нехолинергические (НАНХ). Однако трудно определить, первичны нарушения функционирования вегетативной нервной системы или вторичны по отношению к заболеванию и его терапии.
В дополнение к классическим адренергическим и холинергическим механизмам существуют неадренергические и нехолинергические (НАНХ). Однако трудно определить, первичны нарушения функционирования вегетативной нервной системы или вторичны по отношению к заболеванию и его терапии.
Предполагают, что существует некоторое взаимодействие между нейрогенными и воспалительными механизмами [20]. Некоторые из воспалительных медиаторов влияют на высвобождение нейротрансмиттеров из нервных окончаний дыхательных путей или могут действовать на рецепторы вегетативной нервной системы. Нейрогенные механизмы также вносят свой вклад в развитие воспалительной реакции. Таким образом, концепция нейрогенного воспаления может быть применена к дыхательным путям.
Так как холинергические нервы являются доминантным нервным путем бронхоконстрикции у человека, предполагали, что имеет место нарушение функционирования мускариновых холинорецепторов. Было продемонстрировано наличие тормозящих мускариновых рецепторов (ауторецепторов) в дыхательных путях у животных in vivo и у человека in vitro и in vivo [21].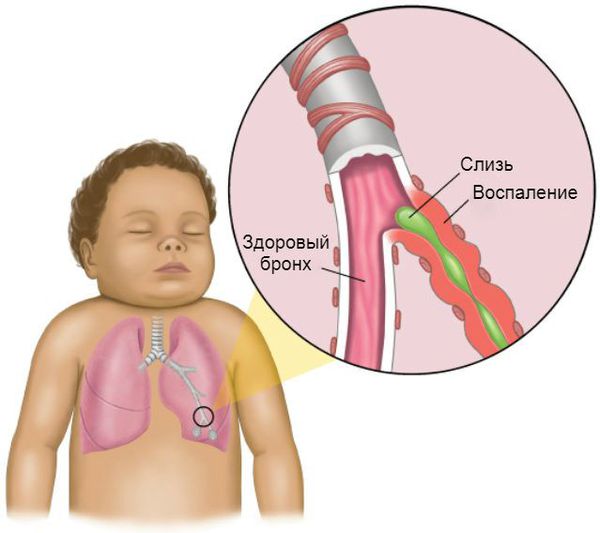 Мускариновые ауторецепторы принадлежат к подтипу М2 и отличны от мускариновых рецепторов М3 гладкой мускулатуры дыхательных путей [22]. Холинергические агонисты, которые селективно активируют ауторецепторы, ингибируют холинергическую рефлекторную бронхоконстрикцию у здоровых, но не у больных бронхиальной астмой; это позволило сделать предположение о некотором нарушении функции этих ауторецепторов [9].
Мускариновые ауторецепторы принадлежат к подтипу М2 и отличны от мускариновых рецепторов М3 гладкой мускулатуры дыхательных путей [22]. Холинергические агонисты, которые селективно активируют ауторецепторы, ингибируют холинергическую рефлекторную бронхоконстрикцию у здоровых, но не у больных бронхиальной астмой; это позволило сделать предположение о некотором нарушении функции этих ауторецепторов [9].
Поскольку адренергические агонисты оказывают значительное влияние на астматическую бронхоконстрикцию, облегчая ее, возможно, что при бронхиальной астме существует нарушение адренергической регуляции. В модели аллергениндуцированного воспаления дыхательных путей на животных было показано, что количество b-адренорецепторов в легких снижено, тогда как a-адренорецепторов – увеличено [17]. Была выявлена дисфункция b-адренорецепторов гладкой мускулатуры у больных бронхиальной астмой [6]. Однако, вероятно, она является вторичной по отношению к интенсивному воспалению дыхательных путей или к адренергической терапии.
Остается неясной роль НАНХ-нервов. Нарушение функционирования может возникнуть при повреждении этих нервов (что представляется маловероятным) или быть результатом повышенного разрушения нейротрансмиттера (которым может быть вазоактивный интестинальный пептид – ВИП). При введении ВИП больным бронхиальной астмой он вызывал бронходилатацию и оказывал протективное дейстие на бронхоконстрикторные раздражители [17]. Воспалительные клетки высвобождают ряд пептидаз, которые могут привести к быстрому разрушению ВИП в дыхательных путях при астме, что в свою очередь может привести к повышенной бронхоконстрикции [23]. Однако более вероятным нарушением является повышение активности возбуждающих НАНХ-нервов. Данные экспериментальных работ позволили сделать предположение, что НАНХ-бронхоконстрикция является следствием высвобождения нейропептидов из сенсорных нервных окончаний С-волокон, таких как субстанция P и нейрокинин А [20]. В результате воздействия на терминалы С-фибрилл эпителиальных клеток и высвобождения таких медиаторов, как брадикинин, активируются эти сенсорные нервные окончания и может быть запущен аксоновый рефлекс. Высвобождение сенсорных нейропептидов будет приводить к бронхоконстрикции, гиперемии, повышению сосудистой проницаемости и гиперсекреции слизи. Так как эпителиальные клетки могут играть важную роль в разрушении тахикининов, любое повреждение целостности пласта эпителия будет приводить к усилению эффекта нейропептидов, высвобождаемых из сенсорных нервных окончаний при астме [18]. Дополнительно сенсорные нервы могут передавать сигнал в холинергические ганглии дыхательных путей, приводя к местной рефлекторной бронхоконстрикции. Таким образом, нейрогенное воспаление может играть важную роль в усилении воспаления дыхательных путей при астме и развитии гиперреактивности бронхов.
Высвобождение сенсорных нейропептидов будет приводить к бронхоконстрикции, гиперемии, повышению сосудистой проницаемости и гиперсекреции слизи. Так как эпителиальные клетки могут играть важную роль в разрушении тахикининов, любое повреждение целостности пласта эпителия будет приводить к усилению эффекта нейропептидов, высвобождаемых из сенсорных нервных окончаний при астме [18]. Дополнительно сенсорные нервы могут передавать сигнал в холинергические ганглии дыхательных путей, приводя к местной рефлекторной бронхоконстрикции. Таким образом, нейрогенное воспаление может играть важную роль в усилении воспаления дыхательных путей при астме и развитии гиперреактивности бронхов.
Влияние терапии на степень гиперреактивности
В основе лечения бронхиальной астмы лежит использование препаратов, которые можно разделить на две большие группы: базисные (противовоспалительные средства: кромогликат натрия, недокромил-натрий и кортикостероиды) и разнообразные по своему фармакологическому воздействию бронхолитические средства. Бронхорасширяющие препараты подразделяют на три большие группы: симпатомиметические, холинолитические и ксантиновые.
Бронхорасширяющие препараты подразделяют на три большие группы: симпатомиметические, холинолитические и ксантиновые.
Бронхорасширяющие препараты. Из всех видов бронходилататоров b-агонисты являются наиболее эффективными и доступными препаратами, действующими на гладкую мускулатуру дыхательных путей. Кроме того, они очень эффективны в предотвращении немедленной бронхоконстрикторной реакции при аллергенной провокации, которая может быть частично обьяснена их сильно выраженным стабилизирующим действием на тучные клетки [24]. Использующиеся до последнего времени в клинической практике селективные b2-агонисты не предотвращали ни позднюю астматичсекую реакцию после аллергенной провокации, ни последующее развитие бронхиальной гиперреактивности [25]. Более того, при длительном приеме они не снижают бронхиальную реактивность у больных астмой [26], а по некоторым данным, могут даже ее увеличивать [27]. Это позволило некоторым авторам предположить, что b2-агонисты за счет быстрого купирования клинических проявлений астмы могут маскировать лежащий в основе воспалительный процесс и их чрезмерное применение могло повлиять на повышение смертности от астмы и заболеваемости ею, наблюдаемое во многих странах [9]. Однако создание новой генерации b2-агонистов (например, сальметерола), оказывающих пролонгированное действие и способных полностью подавлять раннюю и позднюю астматические реакции после аллергенной провокации, а также последующее развитие бронхиальной гиперреактивности [28, 29], поколебало эти воззрения. В отличие от использования b2-агонистов короткого действия длительный прием сальметерола приводит к достоверному снижению гиперреактивности дыхательных путей у больных с бронхиальной астмой [30, 31].
Однако создание новой генерации b2-агонистов (например, сальметерола), оказывающих пролонгированное действие и способных полностью подавлять раннюю и позднюю астматические реакции после аллергенной провокации, а также последующее развитие бронхиальной гиперреактивности [28, 29], поколебало эти воззрения. В отличие от использования b2-агонистов короткого действия длительный прием сальметерола приводит к достоверному снижению гиперреактивности дыхательных путей у больных с бронхиальной астмой [30, 31].
Противовоспалительные средства. В настоящее время кортикостероиды являются наиболее эффективными препаратами, хотя и кромогликат натрия, и недокромил-натрий обладают противовоспалительным свойством. Как системные, так и ингаляционные глюкокортикоиды не оказывают прямого бронхорасширяющего действия, но они улучшают эффективность b-адренергических препаратов. Более того, кортикостероиды блокируют позднюю астматическую реакцию после аллергенной провокации и высокоэффективны в плане предотвращения развития бронхиальной гиперреактивности [25].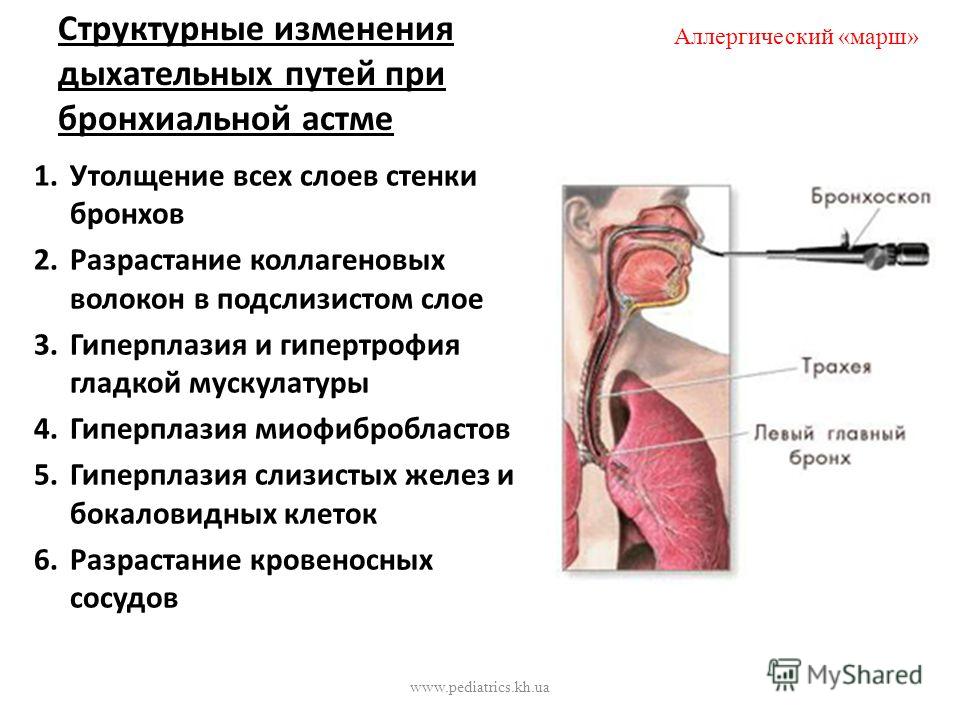 Однако однократное применение ингаляционных кортикостероидов при немедленной бронхоконстрикторной реакции на аллерген неэффективно [25]. По-видимому, это обусловлено тем, что стероиды не оказывают прямого действия на тучные клетки легких человека, но ингибируют высвобождение медиаторов из альвеолярных макрофагов и эозинофилов [32, 33]. Кортикостероиды снижают количество как тканевых эозинофилов, так и эозинофилов периферической крови [33]. Более того, имеются данные, что при длительном применении ингаляционные стероиды снижают степень бронхиальной гиперреактивности, хотя необходимо принимать их несколько недель, чтобы достигнуть максимального улучшения [26, 34 – 36]. Но даже высокие дозы противовоспалительных препаратов в течение длительного периода могут не оказать существенного влияния на степень бронхиальной реактивности и не изменить выраженности обструктивных нарушений дыхательных путей у больных бронхиальной астмой [37]. Это может быть следствием необратимых структурных изменений, таких как гипертрофия гладкой мускулатуры дыхательных путей или утолщение базальной мембраны.
Однако однократное применение ингаляционных кортикостероидов при немедленной бронхоконстрикторной реакции на аллерген неэффективно [25]. По-видимому, это обусловлено тем, что стероиды не оказывают прямого действия на тучные клетки легких человека, но ингибируют высвобождение медиаторов из альвеолярных макрофагов и эозинофилов [32, 33]. Кортикостероиды снижают количество как тканевых эозинофилов, так и эозинофилов периферической крови [33]. Более того, имеются данные, что при длительном применении ингаляционные стероиды снижают степень бронхиальной гиперреактивности, хотя необходимо принимать их несколько недель, чтобы достигнуть максимального улучшения [26, 34 – 36]. Но даже высокие дозы противовоспалительных препаратов в течение длительного периода могут не оказать существенного влияния на степень бронхиальной реактивности и не изменить выраженности обструктивных нарушений дыхательных путей у больных бронхиальной астмой [37]. Это может быть следствием необратимых структурных изменений, таких как гипертрофия гладкой мускулатуры дыхательных путей или утолщение базальной мембраны. Необходимо подчеркнуть, что современные международные рекомендации «Глобальная стратегия. Бронхиальная астма» предлагают применять кортикостероиды у пациентов со среднетяжелым и тяжелым течением бронхиальной астмы [38]. Однако существуют убедительные данные, которые указывают, что назначение даже низких доз ингаляционных кортикостероидов больным с легким течением бронхиальной астмы позволяет хорошо контролировать клинические симптомы заболевания, снижает степень бронхиальной гиперреактивности [39, 40]. Следовательно, чтобы предотвратить развитие необратимых структурных модификаций дыхательных путей, которые часто встречаются при хронической астме, необходимо более раннее введение противовоспалительных препаратов.
Необходимо подчеркнуть, что современные международные рекомендации «Глобальная стратегия. Бронхиальная астма» предлагают применять кортикостероиды у пациентов со среднетяжелым и тяжелым течением бронхиальной астмы [38]. Однако существуют убедительные данные, которые указывают, что назначение даже низких доз ингаляционных кортикостероидов больным с легким течением бронхиальной астмы позволяет хорошо контролировать клинические симптомы заболевания, снижает степень бронхиальной гиперреактивности [39, 40]. Следовательно, чтобы предотвратить развитие необратимых структурных модификаций дыхательных путей, которые часто встречаются при хронической астме, необходимо более раннее введение противовоспалительных препаратов.
Литература:
1. Чучалин А. Г. Бронхиальная астма: глобальная стратегия. Тер. архив. 1994;3:3–8.
2. Arm JP, Lee TH. The pathology of bronchial asthma. Adv Immunol 1992;51:323–82.
3. Bradley B, Azzawi M, Jacobson M, Durham SR, Jeffery PK.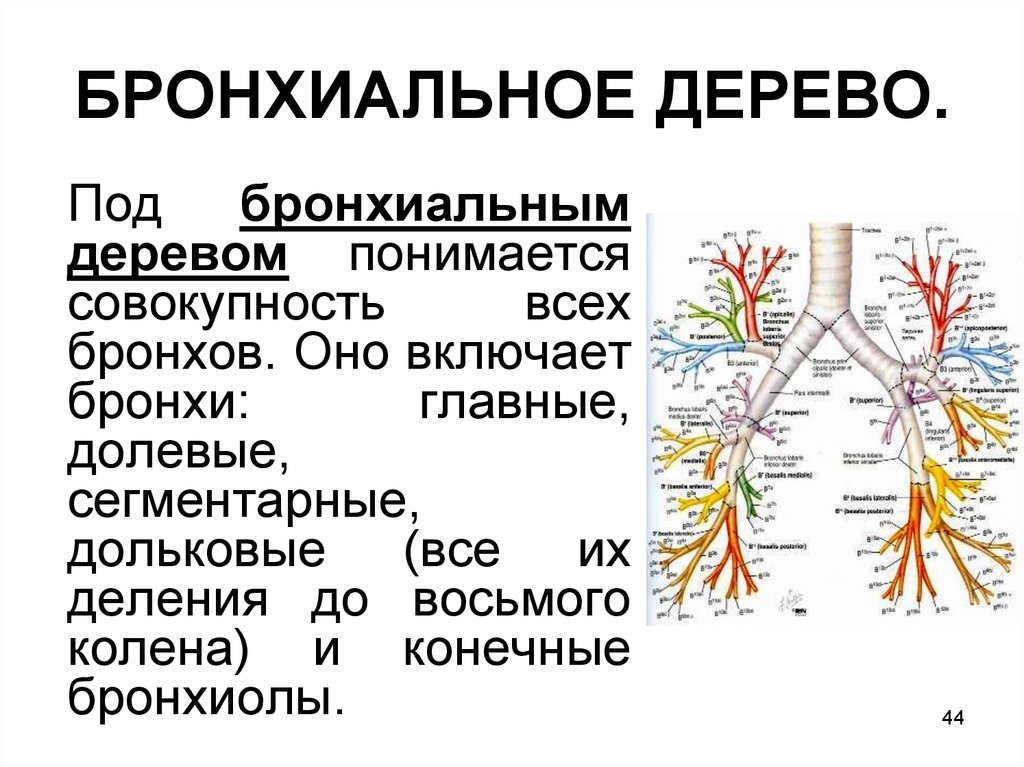 Eosinophils, T-lymphocytes, mast cells, neutrophils, and macrophages in bronchial biopsy specimens from atopic subjects with asthma: comparison with biopsy specimens from atopic subjects without asthma and normal control subjects and relationship to bronchial hyperresponsiveness. J Allergy Clin Immunol 1991;88:61–74.
Eosinophils, T-lymphocytes, mast cells, neutrophils, and macrophages in bronchial biopsy specimens from atopic subjects with asthma: comparison with biopsy specimens from atopic subjects without asthma and normal control subjects and relationship to bronchial hyperresponsiveness. J Allergy Clin Immunol 1991;88:61–74.
4. Corrigan CJ, Kay AB. Role of T-lymphocytes and lymphokines. Br Med Bull 1992;48:72–84.
5. Ohashi Y, Motojima S, Fukuda T, Makino S. Airway hyperresponsiveness, increased intracellular spaces of bronchial epithelium, and increased infiltration of eosinophils and lymphocytes in bronchial mucosa in asthma. Am Rev Respir Dis 1992;145:1246–8.
6. Абросимов В. Н., Порядин В. Г. Воспаление и гиперреактивность дыхательных путей при бронхиальной астме. Тер. арх. 1994;11:60–4.
7. Holgate ST. Mast cells, Mediators and Disease. Academic Publishers, London. 1988.
8. Pin I, Godard P. Mechanisms of bronchial hyperreactivity: role of airway inflammation and atopy.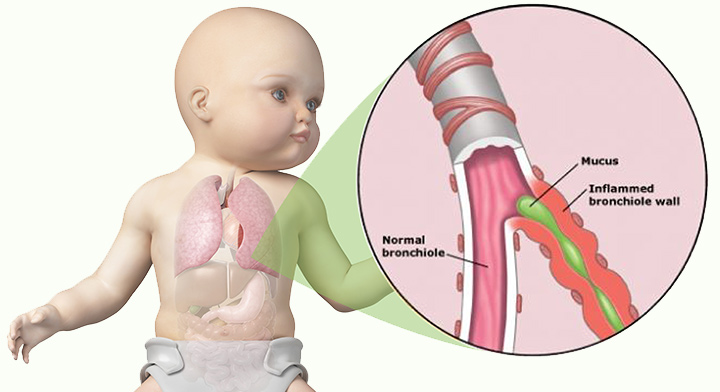 Revue des Maladies Respir 1994;11(2):111–22. [french].
Revue des Maladies Respir 1994;11(2):111–22. [french].
9. Barnes PJ. New concepts in the pathogenesis of bronchial responsiveness and asthma. J Allergy Clin Immunol 1989;83:1013–26.
10. Lukacs NW, Strieter RM, Kunkel SL. Leukocyte infiltration in allergic airway inflammation. Respir Cell Mol Biology 1995;13(1):1–6.
11. Kay AB, Corrigan CJ. Asthma, eosinophils and neutrophils. Br Med Bull 1992;48:51–64.
12. Kasama T, Strieter RM, Lukacs NW, Burdick MD, Kunkel SL. Regulation of neutrophil-derived chemokine expression by IL-10. J Immunol 1994;152:3559–69.
13. Чучалин А. Г. Бронхиальная астма. Сальбутамол. Под ред. А.Г.Чучалина, И.Хамида. М.,ФАРМЕДИНФО. 1992;4–66.
14. Vrugt B, Aalbers R. Inflammation and bronchial hyperresponsiveness in allergic asthma and chronic obstructive pulmonary disease. Respir Medicine 1993;87(Suppl.B):3–7.
15. Berman JS. Airway eosinophils and lymphocytes in asthma. Birds of a feather? Am Rev Respir Dis 1992;145:1246–8.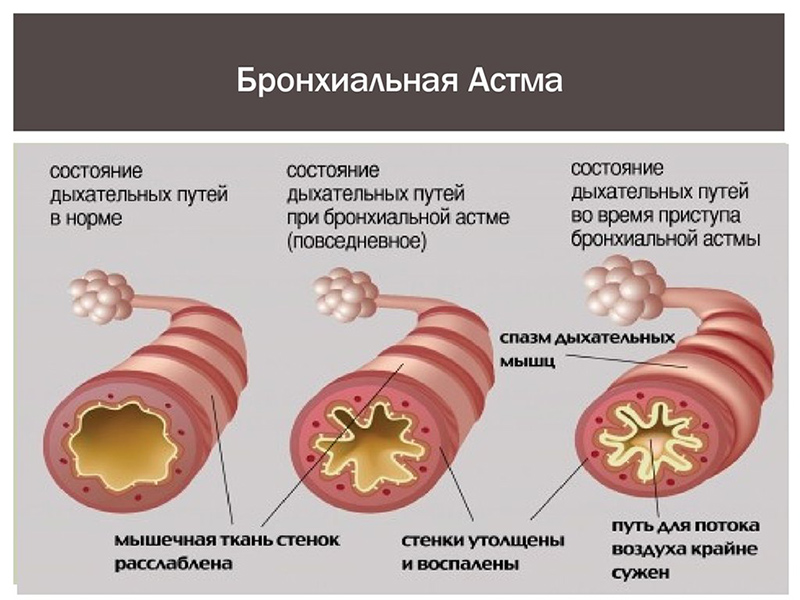
16. Kay AB. ‘Helper’ (CD4+) cells and eosinophils in allergy and asthma. Am Rev Respir Dis 1992;145:S22–S26.
17. Holgate ST, Beasley R, Twentyman OP. The pathogenesis and significance of bronchial hyperresponsiveness in airways disease. Clin Sci 1987;73:561–72.
18. Frossard N, Rhoden KJ, Barnes PJ. Influence of epithelium removal on guinea pig airway responses to tachykinins: role of endopeptidase and cyclooxygenase. J Pharmacol Exp Ther 1989;248:292–7.
19. Barnes PJ. Neural control of human airways in health and disease. Am Rev Respir Dis 1986;134:1289–314.
20. Barnes PJ. Airway inflammation and autonomic control. Eur J Respir Dis 1986;69(Suppl.147):80–7.
21. Minette PA, Barnes PJ. Prejunctional inhibitory muscarinic receptors on cholinergic nerves in human and guinea pig airways. J Appl Physiol 1988;64:2532–7.
22. Шварц Г.Я. Сальбутамол и м-холинолитические средства. Сальбутамол. Под ред. А. Г.Чучалина, И. Хамида. М.,ФАРМЕДИНФО. 1992,214–21.
Под ред. А. Г.Чучалина, И. Хамида. М.,ФАРМЕДИНФО. 1992,214–21.
23. Barnes P. J. Neuropeptides in the lung: localization, function, and pathophysiologic implications. J Allergy Clin Immunol 1987;79:285–95.
24. Church MK, Hiroi J. Inhibition of IgE-depedent histamine release from human dispersed lung mast cells by antiallergic drugs and salbutamol. Br J Pharmacol 1987;90:421–9.
25. Cockcroft DW, Murdock KY. Comparative effects of inhaled salbutamol, sodium cromoglycate, and beclomethasone dipropionate on allergen-induced early asthmatic responses, late asthmatic responses, and increased bronchial responsiveness to histamine. J Allergy Clin Immunol 1987;79:734–40.
26. Wong CS, Wahedna I, Pavord ID, Tattersfield AE. Effect of regular terbutaline and budesonide on bronchial reactivity to allergen challenge. Am J Respir Crit Care Med 1994;150:1268–73.
27. O’Connor BJ, Aikman SL, Barnes PJ. Tolerance to the nonbronchodilatator effects of inhaled beta2-agonists in asthma.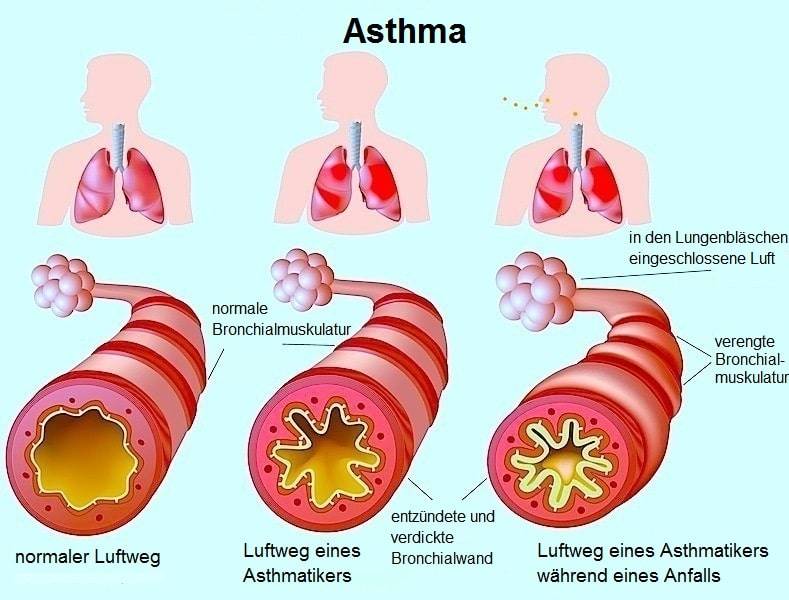 N Engl J Med 1992;327:1204–8.
N Engl J Med 1992;327:1204–8.
28. Holgate ST. Allergen challenge studies. Eur Respir Review 1991;1(4):268–72.
29. Palmqvist M, Balder B, Lowhagen O, et al. Late asthmatic reaction prevented by inhaled salbutamol and formoterol. J Allergy Clin Immunol 1989;83(1):244.
30. Черняк А. В., Княжеская Н. П., Болошина Н. А., Соколов А. С., Пашкова Т. Л., Чучалин А. Г. Эффективность сальметерола при длительной терапии у больных бронхиальной астмой. Пульмонология. 1996,1:47–50.
31. Dahl R, Pedersen B, Venge P. Bronchoalveolar lavage studies. Eur Respir Rev 1991;1(4):272–5.
32. Joseph M, Tonnel AB, Tarpier G, Carpon A. Involvement of immunoglobulin E in the secretory process of alveolar macrophages from asthmatic patients. J Clin Invest 1983;71:221–30.
33. Yukawa T, Chanez P, Dent G, Kroegel C, Roberts NM, Chung KF, Barnes PJ. Bronchodilator agents do not inhibit oxygen-free radical release from guinea pig eosinophils. Am Rev Respir Dis 1988;137(Suppl):27.
Am Rev Respir Dis 1988;137(Suppl):27.
34. Кахановский И. М., Соломатин А. С. Беклометазона дипропионат, будесонид и флунизолид в лечении бронхиальной астмы (обзор литературы и собственные исследования). Тер. архив. 1995;3:34–8.
35. Суточникова О. А., Самсонова М. В., Черняк А. В., Черняев А. Л., Соколов А. С., Чучалин А. Г. Влияние отечественного ингаляционного глюкокортикостероида будесонида на воспаление и гиперреактивность бронхов при длительном лечении больных бронхиальной астмой. Тер. архив. 1996;68(3):48–50.
36. Juniper EF, Kline PA, Vanzieleghem MA, Hargreave FE. Reduction of budesonide after a year on increased use: a randomized controlled trial to evaluate whether improvements in airway responsiveness and clinical asthma are maintained. J Allergy Clin Immunol 1991;87:483–9.
37. Woolcock AJ, Yan K, Salome CM. Effect of therapy on bronchial hyperresponsiveness in the long-term management of asthma. Clin Allergy 1988;18:65.
38. Global initiative for asthma. Global strategy for asthma management and prevention NHLBI/WHO workshop report. March 1993. National Heart, Lung and Blood Institute, National Institutes of Health. January 1995.
Global initiative for asthma. Global strategy for asthma management and prevention NHLBI/WHO workshop report. March 1993. National Heart, Lung and Blood Institute, National Institutes of Health. January 1995.
39. Суточникова О. А., Самсонова М. В., Черняк А. В., Чучалин А. Г. Ингаляционная глюкокортикостероидная терапия больных бронхиальной астмой легкого течения. Влияние на воспаление и гиперреактивность. Пульмонология. 1996;4:21–8.
40. Haahtela T, Jarvinen M, Kava T, Kiviranta K, Koskinen S, Lehtonen K, Nikander K, Persson T, Selroos O, Sovijarvi A, Stenius-Aarniala B, Svahn T, Tammivaara R, Laitinen LA. Effects of reducing or discontinuing inhaled budesonide in patients with mild asthma. New Engl J Med 1994;331:700–5.
Бронхиальная астма — Пульмонология | Медицинский центр «САДКО» Нижний Новгород
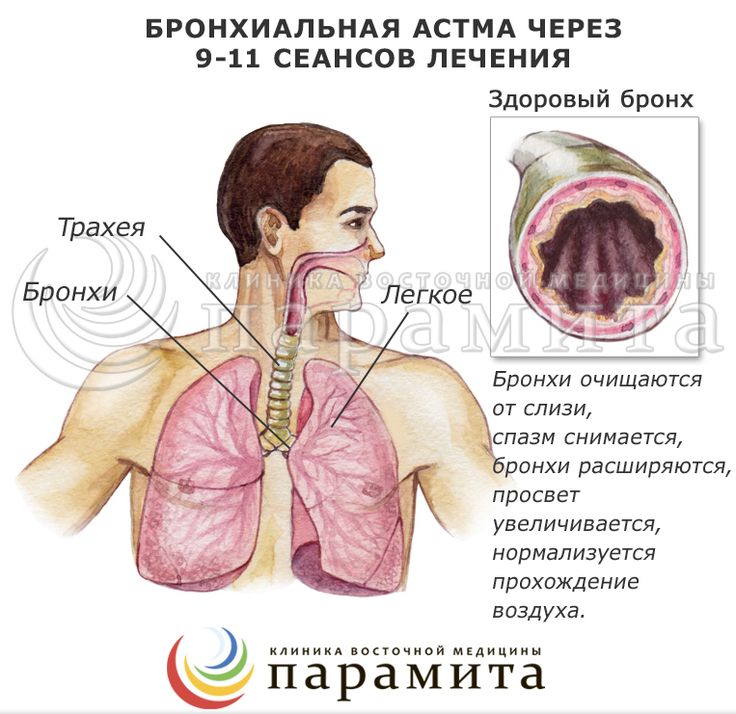
Бронхиальная астма — это хроническое воспалительное заболеваний дыхательной системы, характеризующееся бронхиальной обструкцией и гиперактивностью бронхов.
В результате чего образуется отек слизистой оболочки бронхиального дерева и рецидивирующий приступ спазма гладкой мускулатуры бронхов.
Гипперактивность бронхов- следствие воспалительного процесса в бронхиальной стенке и является реакцией бронхов в виде приступа удушья на вдыхание аллергенов, физическую нагрузку, влажный воздух.
Бронхиальная астма – широко распространенная болезнь. В настоящее время число больных продолжает увеличиваться, несмотря на более раннюю диагностику и современные подходы к лечению. В мире насчитывается более 150 миллионов человек, страдающих бронхиальной астмой.
При бронхиальной астме в дыхательных путях имеется хроническое воспаление, которое при обострении вызывает приступ удушья. Приступ может быть кратковременным или длительным. Часто на ранних стадиях заболевания приступы проходят сами по себе, и человек не подозревает о развитии астмы. С течением времени, без лечения и профилактики приступы удушья возникают чаще и протекают тяжелее. Именно на этой стадии человек обращается к врачу. Бронхиальная астма имеет семейный характер, передается по наследству.
Именно на этой стадии человек обращается к врачу. Бронхиальная астма имеет семейный характер, передается по наследству.
Причин развития бронхиальной астмы может быть несколько:
- бытовые аллергены (домашняя и бумажная пыль), аллергены домашних животных (шерсть собак, кошек), споры грибов;
- аллергены, широко распространенные в окружающей среде: пыльца трав, цветов, кустарников, деревьев,
- пищевые аллергены,
- курение активное и пассивное,
- профессиональные аллергены, например, краски, лаки и т.д.,
- частые вирусные инфекции дыхательных путей,
- холодный и влажный климат,
- стресс.
Основные симптомы бронхиальной астмы:
- ночные и утренние хрипы,
- свистящее дыхание,
- повторяющиеся приступы удушья,
- одышка (затрудненное дыхание),
- нехватка воздуха при физической нагрузке.
Может наблюдаться острое или более постепенное начало приступа удушья. Во время приступа требуется срочная медицинская помощь.
Лечение бронхиальной астмы
В Лечебно-диагностическом центре «Садко» проводится комплексная диагностика и амбулаторное лечение бронхиальнойастма астмы. Курс лечения бронхиальной астмы подбирается строго индивидуально на основе общего анамнеза, состояния общего здоровья пациента и данных о развитии болезни.
Выделяется несколько степеней развития бронхиальной астмы:
- Бронхиальная астма легкой степени: приступы редкие (в среднем 1-2 раза в месяц), быстро проходят без лечения или с использованием лекарств. Вне приступа самочувствие не страдает.
- Средняя степень характеризуется приступами более тяжелыми с удушьем и вовлечением системы кровообращения (учащенного сердцебиения). Требуются ингаляции бронхоспазмолитиков.
- Тяжелая астма – частые приступы, каждый день или 2-3 раза в неделю, опасны для жизни и требуют экстренных мер. Между приступами сохраняется сильная одышка.
Противовоспалительная терапия включает в себя медикаментозную терапию в таблетках и ингаляциях. Эти препараты принимают длительными курсами. При обострении болезни приходится назначать дополнительные лекарства, а после приступа базисную терапию продолжают.
Эти препараты принимают длительными курсами. При обострении болезни приходится назначать дополнительные лекарства, а после приступа базисную терапию продолжают.
При бронхиальной астме должен быть постоянный тесный контакт пациента с лечащим врачом пульмонологом. Важно в лечении бронхиальной астмы применять ступенчатый подход. При нарастании симптомов бронхиальной астмы больной переходит на более высокую ступень и меняется лечение. При ослаблении симптомов и сохранении их проявления на таком уровне в течение 3 месяцев ступень снижается до практически полной отмены лекарств.
Главная цель такого лечения — достижение длительной ремиссии (полное отсутствие или сокращение приступов удушья). В результате комплексного подхода к лечению бронхиальной астмы, врачи пульмонологи Лечебно-диагностического центра «Садко» могут контролировать болезнь и предотвращать приступы.
Профилактика
В качестве профилактики бронхиальной астмы врачи пульмонологи рекомендуют занятия лечебной физкультурой, плаванием в бассейне. Эффективна дыхательная гимнастика.
Эффективна дыхательная гимнастика.
Бронхиальная гиперреактивность: необходимость различать гиперчувствительность и чрезмерное сужение дыхательных путей
Сохранить цитату в файл
Формат: Резюме (текст)PubMedPMIDAbstract (текст)CSV
Добавить в коллекции
- Создать новую коллекцию
- Добавить в существующую коллекцию
Назовите свою коллекцию:
Имя должно содержать менее 100 символов
Выберите коллекцию:
Не удалось загрузить вашу коллекцию из-за ошибки
Повторите попытку
Добавить в мою библиографию
- Моя библиография
Не удалось загрузить делегатов из-за ошибки
Повторите попытку
Ваш сохраненный поиск
Название сохраненного поиска:
Условия поиска:
Тестовые условия поиска
Электронная почта: (изменить)
Который день? Первое воскресеньеПервый понедельникПервый вторникПервая средаПервый четвергПервая пятницаПервая субботаПервый деньПервый рабочий день
Который день? ВоскресеньеПонедельникВторникСредаЧетвергПятницаСуббота
Формат отчета: SummarySummary (text)AbstractAbstract (text)PubMed
Отправить максимум:
1 шт. 5 шт. 10 шт. 20 шт. 50 шт. 100 шт. 200 шт.
5 шт. 10 шт. 20 шт. 50 шт. 100 шт. 200 шт.
Отправить, даже если нет новых результатов
Необязательный текст в электронном письме:
Создайте файл для внешнего программного обеспечения для управления цитированием
Обзор
. 1989 марта; 2(3):267-74.
П. Дж. Стерк 1 , E H Bel
принадлежность
- 1 Отделение пульмонологии Университетской больницы, Лейден, Нидерланды.
- PMID: 2659385
Обзор
P J Sterk et al. Эур Респир Дж. 1989 марта
. 1989 март; 2(3):267-74.
1989 март; 2(3):267-74.
Авторы
П. Дж. Стерк 1 , Э Х Бел
принадлежность
- 1 Отделение пульмонологии Университетской больницы, Лейден, Нидерланды.
- PMID: 2659385
Абстрактный
Бронхиальная гиперреактивность в настоящее время определяется как повышение чувствительности к широкому спектру раздражителей, вызывающих сужение дыхательных путей. Большинство пациентов с астмой и хронической обструктивной болезнью легких (ХОБЛ) проявляют такую повышенную чувствительность. В частности, при астме эта гиперчувствительность сопровождается чрезмерным сужением дыхательных путей. Это поднимает вопрос о том, могут ли меры чувствительности, т. е. провокационная концентрация или доза, вызывающая снижение ОФВ1 на 20 % (PC20 или PD20), содержат всю необходимую информацию о бронхиальной гиперреактивности. В дополнение к модельным исследованиям имеются экспериментальные данные о том, что у человека потенциальные механизмы гиперреактивности бронхов можно разделить на механизмы, вызывающие гиперчувствительность, и механизмы, ответственные за увеличение максимально достижимой степени сужения дыхательных путей. Распознавание и различие этих компонентов гиперреактивности имеет клиническое значение в диагностике и терапии астмы и ХОБЛ. Бронхиальная гиперреактивность представляет собой сложное функциональное расстройство, требующее лечения каждого из его компонентов.
е. провокационная концентрация или доза, вызывающая снижение ОФВ1 на 20 % (PC20 или PD20), содержат всю необходимую информацию о бронхиальной гиперреактивности. В дополнение к модельным исследованиям имеются экспериментальные данные о том, что у человека потенциальные механизмы гиперреактивности бронхов можно разделить на механизмы, вызывающие гиперчувствительность, и механизмы, ответственные за увеличение максимально достижимой степени сужения дыхательных путей. Распознавание и различие этих компонентов гиперреактивности имеет клиническое значение в диагностике и терапии астмы и ХОБЛ. Бронхиальная гиперреактивность представляет собой сложное функциональное расстройство, требующее лечения каждого из его компонентов.
Похожие статьи
Модель сужения дыхательных путей при астме и хронической обструктивной болезни легких.
Wiggs BR, Bosken C, Paré PD, James A, Hogg JC.
 Wiggs BR, et al.
Ам преподобный Респир Дис. 1992 г., июнь; 145 (6): 1251-8. doi: 10.1164/ajrccm/145.6.1251.
Ам преподобный Респир Дис. 1992.
PMID: 1595987
Wiggs BR, et al.
Ам преподобный Респир Дис. 1992 г., июнь; 145 (6): 1251-8. doi: 10.1164/ajrccm/145.6.1251.
Ам преподобный Респир Дис. 1992.
PMID: 1595987Предшествует ли гиперреактивность бронхов или следует за обструкцией дыхательных путей при астме или ХОБЛ?
ван Шайк С.П., Домпелинг Э., Молема Дж., Фольгеринг Х., ван Грунсвен П.М., ван Вил С. ван Шайк С.П. и соавт. Нет J Med. 1994 г., октябрь; 45 (4): 145–53. Нет J Med. 1994. PMID: 7808576
Воспаление бронхов и реакция дыхательных путей на глубокий вдох при астме и хронической обструктивной болезни легких.
Слатс А.М., Янссен К., ван Шадевийк А., ван дер Плас Д.Т., Шот Р., ван ден Аардвег Дж.Г., де Йонгсте Дж.К., Химстра П.С., Моад Т., Рабе К.
 Ф., Стерк П.Дж.
Слэтс А.М. и др.
Am J Respir Crit Care Med. 2007 г., 15 июля; 176 (2): 121-8. doi: 10.1164/rccm.200612-1814OC. Epub 2007 22 марта.
Am J Respir Crit Care Med. 2007.
PMID: 17379851
Ф., Стерк П.Дж.
Слэтс А.М. и др.
Am J Respir Crit Care Med. 2007 г., 15 июля; 176 (2): 121-8. doi: 10.1164/rccm.200612-1814OC. Epub 2007 22 марта.
Am J Respir Crit Care Med. 2007.
PMID: 17379851Воспаление дыхательных путей при астме и хронической обструктивной болезни легких с особым акцентом на антигенпрезентирующие дендритные клетки: влияние лечения флутиказона пропионатом.
Hoogsteden HC, Verhoeven GT, Lambrecht BN, Prins JB. Hoogsteden HC, et al. Клин Эксперт Аллергия. 29 июня 1999 г. Приложение 2: 116-24. doi: 10.1046/j.1365-2222.1999.00020.x. Клин Эксперт Аллергия. 1999. PMID: 10421834 Обзор.
Характеристики гиперреактивности дыхательных путей при астме и хронической обструктивной болезни легких.

Постма Д.С., Керстенс Х.А. Постма Д.С. и др. Am J Respir Crit Care Med. 1998 г., ноябрь; 158 (5, часть 3): S187-92. doi: 10.1164/ajrccm.158.supplement_2.13tac170. Am J Respir Crit Care Med. 1998. PMID: 9817744 Обзор.
Посмотреть все похожие статьи
Цитируется
Чрезмерное использование бета-2-агонистов короткого действия (SABA) у элитных спортсменов: гипотезы, объясняющие это.
Vertadier N, Trzepizur W, Faure S. Вертадье Н. и др. Спорт (Базель). 2022 март 2;10(3):36. дои: 10.3390/спорт10030036. Спорт (Базель). 2022. PMID: 35324645 Бесплатная статья ЧВК. Обзор.
Одорантный рецептор OR2W3 на гладких мышцах дыхательных путей вызывает бронходилатацию за счет кооперативного хемосенсорного компромисса между TMEM16A и CFTR.

Хуан Дж., Лам Х., Козиол-Уайт К., Лимджунявонг Н., Ким Д., Ким Н., Кармачарья Н., Раджкумар П., Файрер Д., Далезио Н.М., Джуд Дж., Куртен Р.С., Плузник Д.Л., Дешпанде Д.А., Пенн Р.Б., Лиггетт SB, Panettieri RA Jr, Dong X, An SS. Хуан Дж. и др. Proc Natl Acad Sci U S A. 10 ноября 2020 г.; 117 (45): 28485-28495. doi: 10.1073/pnas.2003111117. Epub 2020 23 октября. Proc Natl Acad Sci U S A. 2020. PMID: 33097666 Бесплатная статья ЧВК.
Астма: потеря постнатального гомеостатического контроля гладкой мускулатуры дыхательных путей с регрессией к пренатальному состоянию.
Антракопулос МБ, Эверард МЛ. Антракопулос М.Б. и соавт. Фронт Педиатр. 2020 16 апр;8:95. doi: 10.3389/fped.2020.00095. Электронная коллекция 2020. Фронт Педиатр. 2020. PMID: 32373557 Бесплатная статья ЧВК. Обзор.
β2-агонисты длительного действия при астме: необходимы энантиоселективные исследования безопасности.

Джейкобсон Г.А., Райдал С., Хострап М., Кальцетта Л., Вуд-Бейкер Р., Фарбер М.О., Пейдж С.П., Уолтерс Э.Х. Джейкобсон Г.А. и соавт. Препарат Саф. 2018 май; 41(5):441-449. doi: 10.1007/s40264-017-0631-1. Препарат Саф. 2018. PMID: 29332144 Обзор.
Влияние гликопиррония и индакатерола в качестве монотерапии и в комбинации на кривую доза-реакция метахолина у больных с легкой астмой: рандомизированное трехстороннее перекрестное исследование.
Блейс К.М., Дэвис Б.Е., Кокрофт Д.В. Blais CM и соавт. Дыхание Рез. 2017 авг. 2;18(1):146. doi: 10.1186/s12931-017-0628-4. Дыхание Рез. 2017. PMID: 28768531 Бесплатная статья ЧВК. Клиническое испытание.
Просмотреть все статьи «Цитируется по»
Типы публикаций
термины MeSH
Ссылка
Формат: ААД АПА МДА НЛМ
Отправить по номеру
[Бронхиальная гиперреактивность, отличная от наблюдаемой при астме]
Сохранить цитату в файл
Формат: Резюме (текст)PubMedPMIDAbstract (текст)CSV
Добавить в коллекции
- Создать новую коллекцию
- Добавить в существующую коллекцию
Назовите свою коллекцию:
Имя должно содержать менее 100 символов
Выберите коллекцию:
Не удалось загрузить вашу коллекцию из-за ошибки
Повторите попытку
Добавить в мою библиографию
- Моя библиография
Не удалось загрузить делегатов из-за ошибки
Повторите попытку
Ваш сохраненный поиск
Название сохраненного поиска:
Условия поиска:
Тестовые условия поиска
Электронная почта: (изменить)
Который день? Первое воскресеньеПервый понедельникПервый вторникПервая средаПервый четвергПервая пятницаПервая субботаПервый деньПервый рабочий день
Который день? ВоскресеньеПонедельникВторникСредаЧетвергПятницаСуббота
Формат отчета: SummarySummary (text)AbstractAbstract (text)PubMed
Отправить максимум:
1 шт. 5 шт. 10 шт. 20 шт. 50 шт. 100 шт. 200 шт.
5 шт. 10 шт. 20 шт. 50 шт. 100 шт. 200 шт.
Отправить, даже если нет новых результатов
Необязательный текст в электронном письме:
Создайте файл для внешнего программного обеспечения для управления цитированием
Обзор
. 1994;11(2):179-87.
[Статья в Французский]
M Обье 1 , DW Cockcroft
принадлежность
- 1 Больница Биша, INSERM U 226, Факультет Ксавье-Биша, Париж.
- PMID: 8202608
Обзор
[Статья в французский]
M Aubier et al.
Преподобный Мал Респир. 1994.
1994.
. 1994;11(2):179-87.
Авторы
М Обье 1 , Д. В. Кокрофт
принадлежность
- 1 Больница Биша, INSERM U 226, Факультет Ксавье-Биша, Париж.
- PMID: 8202608
Абстрактный
Хотя гиперреактивность бронхов, как правило, связана с астмой, она наблюдалась в нескольких клинических ситуациях. Действительно, было ясно показано, что пациенты с аллергическим ринитом часто проявляют гиперреактивность бронхов. Последнее может быть важным фактором в развитии хронической обструкции дыхательных путей. Гиперреактивность дыхательных путей к прямым бронхоконстрикторам, гистамину и метахолину наблюдается также у пациентов с хроническим ограничением скорости воздушного потока. Несколько направлений рассуждений предполагают, что это может отличаться от гиперреактивности дыхательных путей, наблюдаемой у астматиков, и может быть преимущественно связано со степенью обструкции дыхательных путей. Следовательно, при наличии обструкции дыхательных путей в состоянии покоя тесты на гистамин и метахолин трудно интерпретировать в отношении диагноза астмы. Некоторые исследования предполагают ускоренное снижение функции легких у пациентов с хроническим ограничением скорости воздушного потока и гиперреактивностью дыхательных путей. При интерстициальном заболевании легких предварительные данные, полученные от субъектов с заболеваниями легких, локализованными в легочном интерстиции, предполагают отсутствие (или очень небольшую) склонность к гиперреактивности дыхательных путей. Однако необходимо больше данных. У субъектов с двусторонней трансплантацией легких развивается легкая, как правило, бессимптомная гиперреактивность дыхательных путей, которая, как предполагается, связана с гиперчувствительностью к холинергической денервации.
Несколько направлений рассуждений предполагают, что это может отличаться от гиперреактивности дыхательных путей, наблюдаемой у астматиков, и может быть преимущественно связано со степенью обструкции дыхательных путей. Следовательно, при наличии обструкции дыхательных путей в состоянии покоя тесты на гистамин и метахолин трудно интерпретировать в отношении диагноза астмы. Некоторые исследования предполагают ускоренное снижение функции легких у пациентов с хроническим ограничением скорости воздушного потока и гиперреактивностью дыхательных путей. При интерстициальном заболевании легких предварительные данные, полученные от субъектов с заболеваниями легких, локализованными в легочном интерстиции, предполагают отсутствие (или очень небольшую) склонность к гиперреактивности дыхательных путей. Однако необходимо больше данных. У субъектов с двусторонней трансплантацией легких развивается легкая, как правило, бессимптомная гиперреактивность дыхательных путей, которая, как предполагается, связана с гиперчувствительностью к холинергической денервации. Наконец, как у астматиков, так и у неастматиков может развиться повышенная степень реактивности дыхательных путей после вирусных инфекций дыхательных путей. Индуцированное вирусом воспаление дыхательных путей, вероятно, играет важную роль в патогенезе астмы у некоторых субъектов.
Наконец, как у астматиков, так и у неастматиков может развиться повышенная степень реактивности дыхательных путей после вирусных инфекций дыхательных путей. Индуцированное вирусом воспаление дыхательных путей, вероятно, играет важную роль в патогенезе астмы у некоторых субъектов.
Похожие статьи
Может ли тест на дыхательные пути предсказать респираторные заболевания? Международное популяционное исследование.
Маркон А., Сервери И., Вджст М., Анто Дж., Генрих Дж., Янсон С., Джарвис Д., Лейнарт Б., Пробст-Хенш Н., Сванес С., Торен К., Берни П., де Марко Р. Маркон А. и др. J Аллергия Клин Иммунол. 2014 янв;133(1):104-10.e1-4. doi: 10.1016/j.jaci.2013.03.040. Epub 2013 15 мая. J Аллергия Клин Иммунол. 2014. PMID: 23683511
Реакция дыхательных путей на метахолин и риск развития астмы у пациентов с аллергическим ринитом.

Прието Л., Берто Х.М., Гутьеррес В. Прието Л. и др. Энн Аллергия. 1994 июнь; 72 (6): 534-9. Энн Аллергия. 1994. PMID: 8203797
Гиперреактивность дыхательных путей: сравнительное исследование метахолина и физических нагрузок при сезонном аллергическом рините с астмой или без нее.
Син Б.А., Йылдыз О.А., Дурсун А.Б., Мисирлигиль З., Демирель Ю.С. Син Б.А. и соавт. Дж Астма. 2009 г., июнь; 46 (5): 486–91. дои: 10.1080/027702855936. Дж Астма. 2009. PMID: 19544170
[Функциональное тестирование бронхиальной реактивности].
Тохда Ю., Кубо Х., Фукуока М., Накадзима С. Тохда Ю. и др. Нихон Ринсё. 1996 ноябрь; 54 (11): 2903-7. Нихон Ринсё. 1996. PMID: 8950928 Обзор.
 Японский язык.
Японский язык.Спровоцированные модели астмы: чему мы научились?
О’Бирн П.М., Говро Г.М., Браннан Д.Д. О’Бирн П.М. и др. Клин Эксперт Аллергия. 2009 г., февраль; 39 (2): 181–92. doi: 10.1111/j.1365-2222.2008.03172.x. Клин Эксперт Аллергия. 2009. PMID: 19187330 Обзор.
Посмотреть все похожие статьи
Цитируется
Клинические характеристики пациентов с ХОБЛ, связанной с курением биомассы, и хроническим бронхитом, 2004–2014 гг.
Перес-Падилья Р., Рамирес-Венегас А., Сансорес-Мартинес Р. Перес-Падилья Р. и др. Хроническая обструкция легких Dis. 2014 6 мая; 1(1):23-32. doi: 10.15326/jcopdf.1.1.2013.0004. Хроническая обструкция легких Dis.