Лимфаденопатия. Что делать? | Рак. Клиника. Диагностика. Лечение
Проблема дифференциального диагноза лимфаденопатий имеет большое значение для врачей многих специальностей, включая терапевтов общего профиля, гематологов, онкологов, педиатров, хирургов, инфекционистов. К кому обратится больной с увеличенными лимфоузлами — вопрос случая, особенно если учесть, что к увеличению лимфатических узлов приводит множество причин. Однако в большинстве случаев врач общей практики участвует только на первых этапах обследования больного и вскоре обращается к специалисту, обычно онкогематологу. Задача гематолога и любого врача, исследующего больного с лимфаденопатией, — поставить нозологический диагноз. Если врач придерживается позиции «исключить свое», он обречен на частые ошибки. При таком подходе резко сужается диагностический кругозор. Приступая к диагностическому поиску, надо быть готовым к любому заболеванию .
В связи с чрезвычайным разнообразием болезней, проявляющихся увеличением лимфоузлов, любой диагностический алгоритм будет несовершенным.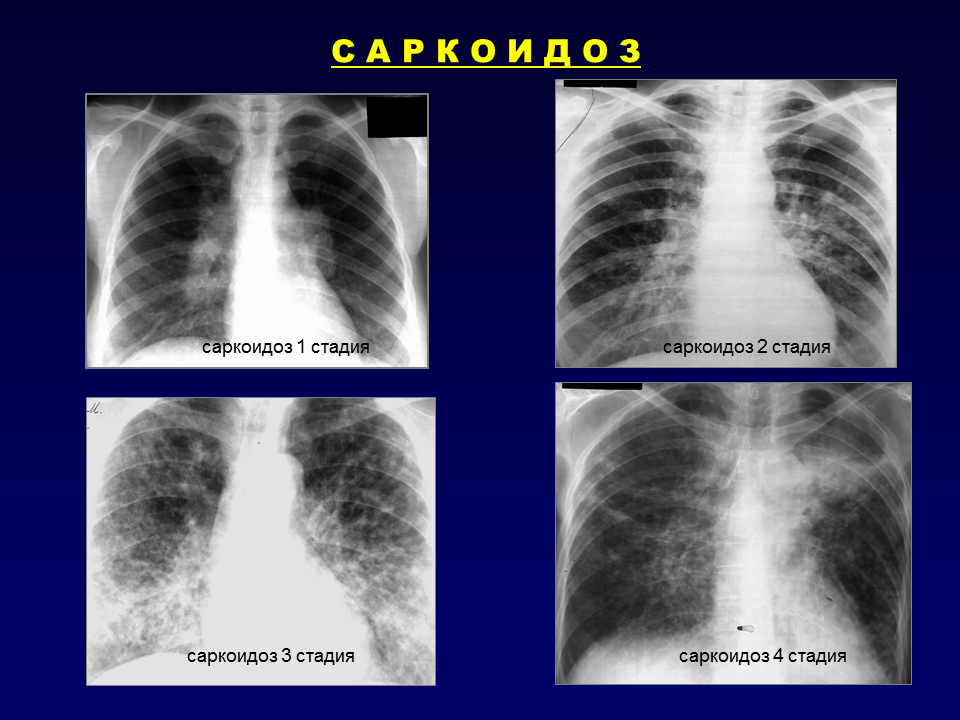
В данной работе представлены алгоритмы диагиосгики по обследованию и тактике ведения больных с лимфаденопатиями в виде протоколов и рекомендацией с целью улучшения диаг ностики неопушлевых лимфаденопатий. Они основаны на многодетном опыте работы ГНЦ, а также анализе литературы отечественных и зарубежных авторов, посвященной алгоритмам диагностики лимфаденопатий]
Основные понятия, используемые в рекомендациях.
Лимфаденопатия (ЛАП)-увеличение лимфоузлов любой природы.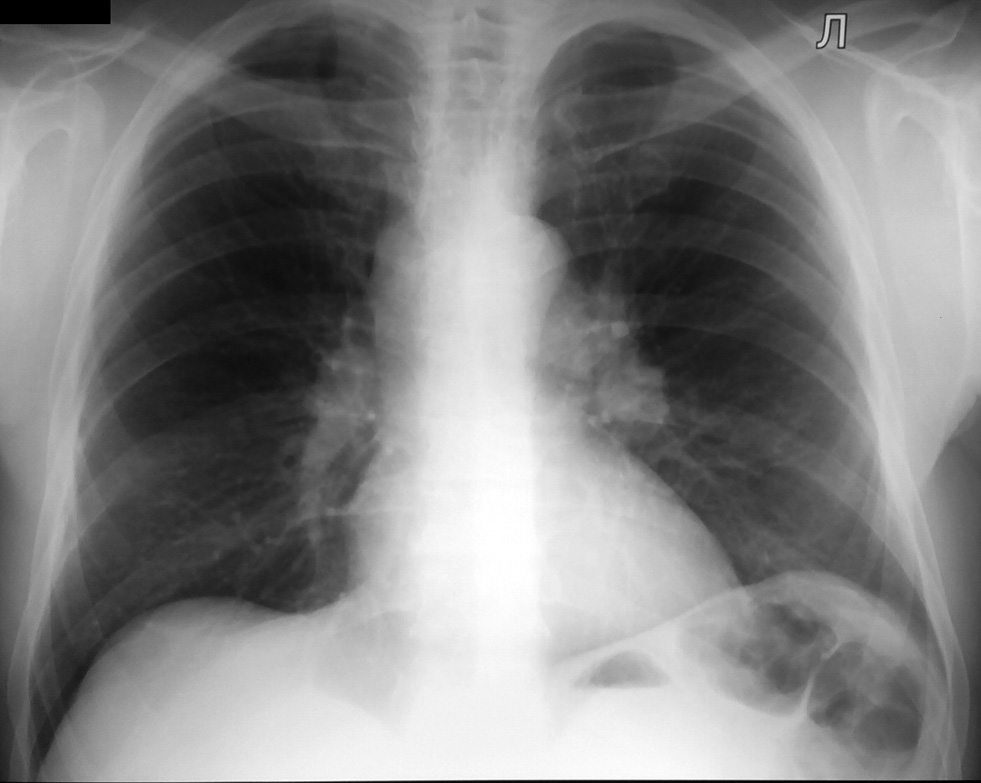 Термин носит исключительно обобщающий характер. Понятие «лимфаденопатия» употребляется:
Термин носит исключительно обобщающий характер. Понятие «лимфаденопатия» употребляется:
I при обсуждении дифференциального диагноза
- для обозначения случаев, когда диагноз по разным причинам так и не был установлен.
Лимфаденит — увеличение лимфоузла, обусловленное воспалительной реакцией непосредственно в ткани узла. При этом воспалительная реакция вызвана тем, что возбудитель или иные субстанции попадают непосредственно в лимфоузел. Лимфаденит отличается от увеличения лимфоузла, обусловленного иммунной реакцией на удаленный очаг инфекции, генерализованную инфекцию или аутоиммунный процесс. Характер воспаления и гистологических изменений в лимфоузле может быть разным.
Реактивная гиперплазия лимфоузла — увеличение лимфоузла, обусловленное иммунной реакцией на удаленный очаг инфекции, генерализованную инфекцию, аутоиммунные процессы. Клинически, до биопсии, провести границу между лимфаденитом и реактивной гиперплазией лимфоузла невозможно у большинства больных.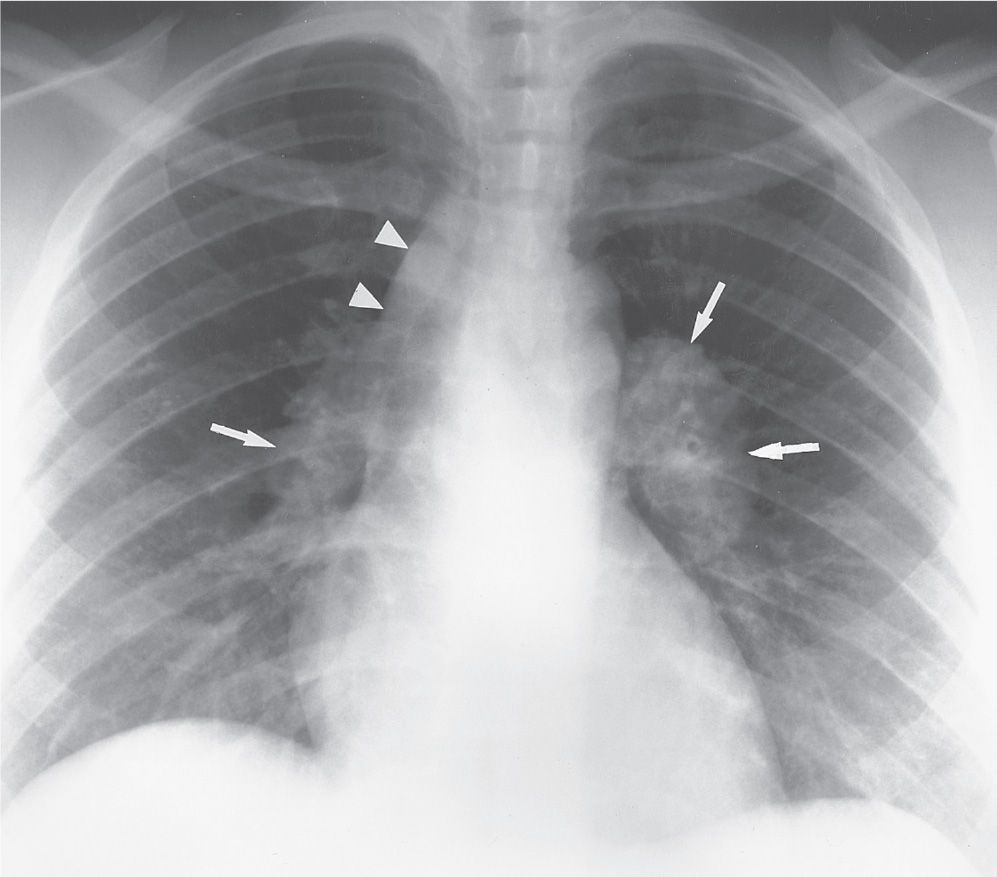 Увеличение лимфоузлов до/без биопсии можно трактовать как лимфаденит в следующих случаях:
Увеличение лимфоузлов до/без биопсии можно трактовать как лимфаденит в следующих случаях:
- четкая ассоциация увеличенных лимфоузлов с первичным очагом
- наличие отчетливых признаков локального воспаления: покраснение кожи над лимфоузлом, спаянность лимфоузла с кожей или подкожной клетчаткой, флюктуация, образование свища
- увеличение лимфоузлов в контексте инфекционного заболевания, сопровождающегося лимфаденитами, когда диагноз установлен исходя из других доминирующих признаков.
В других случаях логично употребление термина «увеличение лимфоузлов» или «лимфаденопатия», подчеркивая неясность процесса.
Принципиальное значение имеет разделение лимфаденопатий на локальные и генерализованные. При неопухолевых лимфаденопатиях уместно также выделить понятие «регионарная лимфаденопатия», т.е. увеличение одной или нескольких смежных групп лимфатических узлов при наличии фиксированного очага проникновения инфекта. Локальная лимфаденопатия — это увеличение строго одной группы лимфатических узлов.
Исходя из природы увеличения лимфоузлов, выделяются опухолевые и неопухолевые формы ЛАП. По давности процесса ЛАП можно разделить на непродолжительную (менее 2 месяца), затяжную (более 2 месяца), по течению — острую, хроническую и рецидивирующую.
Размер. Вопрос нормы применительно к лимфатическим узлам имеет относительное значение: нормальные размеры и локализация зависят от возраста, географического региона, профессии и других факторов. Пальпируемые лимфоузлы выявляются чаще у детей и подростков, чем у взрослых, поскольку в детском возрасте происходят многочисленные контакты с «новыми» возбудителями. У взрослых лимфоузлы размером до 1,0-1,5 см считаются нормальными.
Болезненность. Болевой симптом лимфоузлов обычно возникает вследствие воспалительного процесса или нагноения, но он может вызываться кровоизлиянием в ткань лимфоузла и некрозом. Наличие или отсутствие болезненности совершенно не позволяет исключить опухоль.
Консистенция Каменная плотность лимфоузла — признак рака, метаста- зировавшего в лимфоузел. Плотные лимфоузлы характерны для лимфатических опухолей. Более мягкие лимфоузлы — признак инфекционного, воспалительного процесса. В лимфоузлах с нагноением может выявляться флюктуация.
Более мягкие лимфоузлы — признак инфекционного, воспалительного процесса. В лимфоузлах с нагноением может выявляться флюктуация.
Спаянность. К спаянности могут приводить как неопухолевые процессы (туберкулез, саркоидоз, паховая лимфогранулема), так и опухоли.
Локализация. Увеличение лимфоузлов в некоторых областях поражения чаще связано с определенными болезнями.
Однако, основное правило, которым следует руководствоваться при диагностике опухолевых и неопухолевых лимфаденопатий и в решении вопроса о диагностической биопсии состоит в том, что возраст больного, размер и локализация лимфоузла не имеют решающего дифференциально-диагностического значения у конкретного бального.
Основные принципы рекомендаций:
1 При первичном осмотре необходимо констатировать локальную и генерализованную лимфаденопатию
- Биопсия по показаниям может быть выполнена на любом этапе диагностического поиска
- Биопсия не является конечным этапом диагностического поиска, если она установила неопухолевую природу лимфаденопатии!
Обследование больных подразделяется на три этапа:
- осмотр
- обследование
- ревизия данных
Каждый из этапов приводит к одному из перечисленных результатов
Результаты осмотра:
1 . Заподозрено заболевание, для подтверждения которого требуется специфическое исследование
Заподозрено заболевание, для подтверждения которого требуется специфическое исследование
- Намечен план диагностического поиска для исключения нескольких заболеваний
3 .Диагностической гипотезы или концепции не возникло
После проведения обследования могут быть сделаны следующие выводы:
- диагноз установлен
I для подтверждения диагноза требуются дополнительные обследования
- диагноз не установлен
В случае, если диагноз после обследования не установлен, выполняется ревизия полученных данных.
Алгоритм добиопсийной диагностики лимфаденопатий (локальной и регионарной).
Локальная лимфаденопатия может быть констатирована только после всестороннего осмотра больного. Даже если, по мнению пациента, проблема носит локальный характер, необходимо обязательно осмотреть все группы лимфоузлов.
1 этап. Первичный осмотр
Необходимо оценить клиническую картину, обращая внимание на следующее:
- Есть ли клиника острого инфекционного заболевания?
- Оценить локальные признаки воспаления.
 Нет ли очага в зоне дренирования лимфоузла, в том числе:
Нет ли очага в зоне дренирования лимфоузла, в том числе: - локальные инфекционные процессы, в т.ч. стоматогенные, ЛОР-
патология, воспалительные изменения глаз (окулогландулярный синдром).
| высыпания на коже
- опухоли
- укусы, царапины
- имплантат
- недавние операции
- Необходимо убедиться, что локальное образование является лимфоузлом.
В шейной области за лимфоузлы часто принимаются:
- боковые и срединные кисты шеи,
- заболевания слюнных желез,
- извитость (кинкинг синдром) и аневризмы сонных артерий (при пальпации выявляется пульсация)
- последствия перенесенного миозита или травматического повреждения
грудиноключично-сосцевидной мышцы в виде оссификации или склерозирования и уплотнения ее части,
- меганофиз VII шейного позвонка (шейные ребра — ортопедическая аномалия, как правило, двусторонняя).
- уплотнение соединительной клетчатки в области затылочных бугров.
Чаще всего шейные лимфоузлы путают с боковыми кистами шеи. Несолитарность объемного образования и наличие одновременно других воспалительных заболеваний в регионарной зоне приводит к нередкой ошибочной диагностике лимфаденита. Нередко этим больным с диагностической целью назначается биопсия предполагаемого увеличенного лимфоузла. Такая тактика неверна. Удаление кисты представляет собой отдельную операцию, существенно отличающуюся от биопсии лимфатического узла. Неверное проведение операции приводит к рецидивам кисты. Рецидивы, безусловно, возможны и при правильном проведении операции, однако вероятность рецидива при этом существенно ниже.
В диагностике боковой кисты шеи имеет значение типичная локализация (внутренняя поверхность кивательной мышцы, средняя треть с одной стороны).
Дифференциальный диагноз одностороннего объемного образования в области шеи типичной локализации требует обязательного ультразвукового исследования.
Меганофиз VII шейного позвонка представляет собой плотное и неподвижное образование. Диагностируется ультразвуковым и рентгенологическим исследованием.
Диагностируется ультразвуковым и рентгенологическим исследованием.
В подмышечной области за лимфоузлы часто принимается:
- добавочная долька молочной железы
-гидраденит
- привычный вывих плечевого сустава.
Диагноз добавочной дольки молочной железы ставится по консистенции образования, напоминающего молочную железу и наличием связи увеличения размеров и болезненности образования с менструальным циклом.
Гидраденит в отличие от лифмоузла располагается поверхностно. Такие случаи диагностируются с помощью ультразвукового исследования.
Привычный вывих диагностируется следующим образом: при поднятии руки на вверх у пациента появляется образование, которое имеет костную плотность. При опускании руки — образование исчезает.
- Оценить вероятность опухоли.
При веских подозрениях на опухоль необходимо немедленно делать биопсию.
- Оценить другие клинические признаки.
Если после осмотра диагноз высоко предположителен, могут потребоваться специфические исследования.
Необходимо помнить, что у одного больного может быть сочетание двух заболеваний!
Кроме того, у многих пациентов с опухолями поводом для обращения к врачу является именно инфекционное заболевание.
В Приложении, таблица I, приводятся основные клинические признаки заболеваний, сопровождающихся ЛАП.
II этап. Обследование.
План обследования больных зависит от предположений, возникших после осмотра.Рал обтеклнннческнх методов обследования должен быть назначен всем пациентам!
Эти исследовали* отнесены в группу облигатных методов. В случае, если на этапе первичного осмотра, либо при анализе результатов облигатных методов. возникает специфическая гипотеза, необходимо назначать дополнительные, факультативные методы обследования.
Ш
1 этап. Ревизия данных
На этом этапе необходимо провести анализ анамнестических и эпидемиологических данных, оценить значимость лимфаденопатии, решить вопрос о проведении биопсии и/или динамического наблюдения.
- Ревизия анамнестических и эпидемиологических данных.
Минорные или кажущиеся незначительными анамнестические данные часто помогают направить диагностический поиск в правильном русте, особенно при наличии инфекционных заболеваний. Кроме того, лнмфаденопа- тиа часто объясняется каким-то перенесенным процессом Очень распространенной является клиническая ситуация, при которой лимфоузлы остаются увеличенными после затихания местного инфекционного процесса в срок от нескольких дней до 2 месяцев, т.е. процесс регрессии лимфатического узла запаздывает по отношению к регрессии процесса в локальном очаге.
Лимфаденопатия может объясняться рецидивирующими инфекциями, дробен но часто в полости рта и носоглотки. Распространенной является затяжная 1 остаточная лимфаденопатия после EBV-инфекшш
Лимфаденопатия может быть связана с образом жизни больного, ролом занятий. путешествием, профессией, географическими факторами, контактом с асивотнымн. применением лекарственных препаратов, особенно антиконвульсантов (феннтоин <
Основные эпидемиологические данные, способные подсказать направление диагностического поиска, перечислены в Приложении, таблицы 3,4. Целый ряд рнккетсноэод вызывают эндемичные инфекционные заболевания, сопровождающиеся лнмфаденопатней и передаются с укусами клешей. Эти заболевания проявляются однотипной клиникой и носят эндемичный характер.
Целый ряд рнккетсноэод вызывают эндемичные инфекционные заболевания, сопровождающиеся лнмфаденопатней и передаются с укусами клешей. Эти заболевания проявляются однотипной клиникой и носят эндемичный характер.
- Оценка значимости лимфаденопатии. Она определяется по размерам лимфоузлов и давности лимфаденопатии, а также по наличию других
- Решение вопроса о проведении биопсии.
Необходимость биопсии может быть очевидна при первичном осмотре. В таких случаях ее следует натачать сразу. Если необходимость в биопсии не очевидна, вопрос решается по совокупности признаков, иногда после динамического наблюдения. Кроме экстренных ситуаций, пациент должен быть исследован по приведенному списку до биопсии, поскольку, во- первых, хирург должен знать о возможных вирусных инфекциях, во-вторых, диагноз может быть поставлен и без биопсии.
Необъяснимая лимфаденопатия является показанием к биопсии. При недифференцированном подходе частота выполнения ненужных биопсий может достигать 20%. Даже в опытных руках частота выполнения ненужных биопсий не может быть сведена к нулю в силу онкологической настороженности.
Даже в опытных руках частота выполнения ненужных биопсий не может быть сведена к нулю в силу онкологической настороженности.
Динамическое наблюдение. Когда диагноз установить не удалось, целесообразно придерживаться динамического наблюдения — активное наблюдение не реже I раза в три месяца, обращая внимание на увеличение размеров лимфоузлов, селезенки, показатели ЛДГ, развернутый анализ периферической крови
Генерализованная лимфаднопатия. Добиопсийная диагностика
Генерализованной лимфаденопатией называется увеличение лимфоузлов в двух и более непересекающихся зонах.
Генерализованная лимфаденопатия у взрослых является предметом детального обследования!
Воздержаться от развернутого обследования допустимо в случаях явной инфекционной природы заболевания (ОРЗ, краснуха). В диагностике этого синдрома большое значение имеют другие клинические признаки и данные обследования. Поиск диагноза на I этапе у больных с локальной и генерализованной ЛАП различен. II этап (обследование) и III этап (ревизия данных) одинаковы.
II этап (обследование) и III этап (ревизия данных) одинаковы.
I этап. Первичный осмотр.
Необходимо оценить клиническую картину, обращая внимание на признаки, способные выявить наиболее частые причины генерализованной лим- фаднопатии.
- Есть ли клиника острого инфекционного заболевания? Прежде всего, необходимо выявить мононуклеозоподобный синдром.
- Необходимо убедиться, что лимфаденопатия действительно является генерализованной, а не обусловлена несколькими заболеваниями. Чаще всего этот вопрос возникает при одновременном увеличении шейных и паховых лимфоузлов.
- Необходимо оценить вероятность опухоли. При веских подозрениях на опухоль, например, лимфому Беркитта, необходимо немедленно делать биопсию.
- Другие важные клинические признаки, включая наличие параллельных синдромов и признаков поражения других органов (Приложение, таблица 1).
Лимфаденопатия, которую не удалось расшифровать после выполнения исследований, перечисленных в Приложении, таблица 2, называется необъяснимой. В редких случаях генерализованная лимфаденопатия может быть конституциональной. Часто она выявляется у худых людей. Генерализованная лимфаденопатия может быть остаточной после перенесенных тяжелых инфекций, тяжелых травм, операций. Больные с генерализованной ЛАП подлежат регулярному наблюдению. Если лимфаденопатия персистирует в течение 3 месяцев, показана биопсия.
В редких случаях генерализованная лимфаденопатия может быть конституциональной. Часто она выявляется у худых людей. Генерализованная лимфаденопатия может быть остаточной после перенесенных тяжелых инфекций, тяжелых травм, операций. Больные с генерализованной ЛАП подлежат регулярному наблюдению. Если лимфаденопатия персистирует в течение 3 месяцев, показана биопсия.
Л имфадсноиа гия остаточная, незначимая и конституциональная
Анализ больных с лимфалснопатиями позволил нам также выделить я сформулировать различия между тремя вариантами затяжногоувеличения лимфоузлов.
Остаточную лимфаденопатию констатируют, если в анамнезе имеется четкий эпизод инфекции. Она может быть как локальной, так и генерализованной.
Лимфаденопатия в таких случаях может быть обусловлена ш тниннм угасанием напряженного иммунного ответа, продолжающимся иммунным ответом в силу того, что возбудитель перс и сти руст, или склерозированием лимфоузла.
Незначимая лимфаденопатия в отличие от остаточной мшезапфуспюа только после обследования. Она связана с инфекцией, но в огличве от остаточной, в анамнезе нет документированного эпизода инфекции. Особенно часто встречается у детей и молодых людей. Наиболее характерным примером незначимой лимфаденопатии является увеличение подчелюстных в ия- ховых лимфоузлов. Увеличение лимфоузлов в этой зоне связано с их близостью к «входным воротам» множества инфекций, большинство из которых протекают субклинически. Пациенты с незначимой ЛАП подлежа! наблюдению.
Она связана с инфекцией, но в огличве от остаточной, в анамнезе нет документированного эпизода инфекции. Особенно часто встречается у детей и молодых людей. Наиболее характерным примером незначимой лимфаденопатии является увеличение подчелюстных в ия- ховых лимфоузлов. Увеличение лимфоузлов в этой зоне связано с их близостью к «входным воротам» множества инфекций, большинство из которых протекают субклинически. Пациенты с незначимой ЛАП подлежа! наблюдению.
Конституциональная ЛАП. Встречается у детей. У взрослых это казуистическая редкость. Наблюдается преимущественно у худых лиц и характеризуется со значительной давностью лимфаденопатии («сколько помню, всегда были увеличены лимфоузлы»).
Послебиопсийная диагностика лимфаденопатий
В случае, если в результате проведенной биопсии диагноз остается не ясен (прежде всего, это актуально для случаев, когда морфологическое исследование не выявило наличие опухоли), необходимо продолжение диагностического поиска. Алгоритм послебиопсийной диагностики представлен в Приложении, рисунок 2. Принцип послебиопсийной диагностики неопухолевых ЛАП основан на выделении гистологических групп изменений в тканях лимфоузла, которые должны направлять клинициста в определенное русло диагностического поиска. В большинстве случаев гистологическая диагностика при неопухолевых лимфаденопатиях не позволяет констатировать нозологический диагноз, и эта трудность является объективной. Мы полагаем, что один из способов улучшения качества диагностики состоит в тесной кооперации гистологов и клиницистов. Эта кооперация может осуществляться при наличии стандартизированных заключений. Если гистологические данные не позволяют установить диагноз, в заключении может быть указан доминирующий признак или дано подробное описание морфологии.
Алгоритм послебиопсийной диагностики представлен в Приложении, рисунок 2. Принцип послебиопсийной диагностики неопухолевых ЛАП основан на выделении гистологических групп изменений в тканях лимфоузла, которые должны направлять клинициста в определенное русло диагностического поиска. В большинстве случаев гистологическая диагностика при неопухолевых лимфаденопатиях не позволяет констатировать нозологический диагноз, и эта трудность является объективной. Мы полагаем, что один из способов улучшения качества диагностики состоит в тесной кооперации гистологов и клиницистов. Эта кооперация может осуществляться при наличии стандартизированных заключений. Если гистологические данные не позволяют установить диагноз, в заключении может быть указан доминирующий признак или дано подробное описание морфологии.
Нам показалось важным выделение из многообразных изменений лимфоузлов нескольких простых групп, которые могут служить отправной точкой для диагностики в сложных случаях.
На основании ведущего признака нами выделены 8 дифференциальнодиагностических групп:
- фолликулярная гиперплазия
- паракортикальная гиперплазия
- гранулематозный лимфаденит
- гнойно-некротический гранулематозный и гнойный лимфаденит
- синусный гистиоцитоз как ведущий признак
- некроз узла как ведущий признак
- атрофические изменения
- дерматопатический лимфаденит.

Выделенные группы не оригинальны и частично соответствуют подразделению, которого придерживаются гистологи. Как показывают наши данные, установить этиологический диагноз в результате гистологического исследования удается нечасто, поскольку морфологические проявления многих процессов сходны. Так, имея сходную картину, гранулематозное воспаление вызывается множеством причин. Поэтому логично объединить в группы процессы, обладающие сходной морфологической картиной. Сформиро- ванные нами группы носят патогенетический характер, приближены К ЮВ- нике, и каждая из них требует определенных дополнительных исследований. Таким образом, сужается диагностический поиск.
- Фолликулярная гиперплазия отражает преимущественно В- клеточный иммунный ответ. Она выявляется чаще всего, наименее следи- финна и обусловлена разными инфекциями и аутоиммунными заболеваниями. Наиболее частыми причинами фолликулярной гиперплазии вне связи с инфекцией в регионарной зоне являлись токсоплазмоз, СПИД, сифилис, системная красная волчанка, ревматоидный артрит, болезнь Кастлемана (ангио- фолликулярная гиперплазия лимфоузла), другие бактериальные и вирусные инфекции, как реакция лимфоузла на расположенный в зоне дренирования очаг инфекции — например наличие раны на коже, очага воспаления во рту.
 кариес и так далее.
кариес и так далее.
Выраженную фолликулярную гиперплазию необходимо дифференцировать от фолликулярной лимфомы (необходимо иммуногистохимическое исследование, выявление транслокации t( 14; 18), доказательство клональности).
- Паракортикальная гиперплазия возникает в результате пролиферации клеток в паракортикальной зоне и часто вызывается вирусами, запускающими преимущественно Т-клеточный иммунный ответ. Паракортикаль- ную гиперплазию чаще всего вызывают вирус Эпштейна-Барр, цитомегало- вирусная и другие вирусные инфекции, поствакцинальная реакция, а также изменений, сопутствующих разнообразным кожным процессам (дерматопа- тический лимфаденит). Основная сложность в трактовке паракортикальной гиперплазии связана с трудностью ее дифференциации от Т-клеточных лимфом. Это особенно касается случаев затяжной лимфаденопатии у лиц с ослабленной иммунной системой. Картина инфекционного мононуклеоза и других вирусных инфекций может быть неотличима от опухолевой. Определение Т-клеточной клональности не всегда помогает в дифференциальном диагнозе, поскольку у многих больных с вирусными инфекциями, особенно в острой фазе, наблюдается экспансия Т-клеточных клонов.
 Поэтому целесообразно определение Т-клеточной клональности в динамике. Во всех случаях, где речь идет о вирусной инфекции, наблюдается исчезновение доминирующего «клона» Т-лимфоцитов.
Поэтому целесообразно определение Т-клеточной клональности в динамике. Во всех случаях, где речь идет о вирусной инфекции, наблюдается исчезновение доминирующего «клона» Т-лимфоцитов.
То же самое касается иммунофенотипирования. Констатация опухоли по факту преобладания одной популяции клеток, например CD8+, не говорит об опухоли, поскольку в острой фазе инфекционного мононуклеоза может наблюдаться значительное увеличение числа CD8-I- клеток. Данные аберрантного иммунофенотипа также должны интерпретироваться с осторожностью. Активация Т-лимфоцитов может приводить к временной экспрессии антигенов, которые в обычных условиях не экспрессируются или слабо экспрессируются Т-лимфоцитами.
- Гранулематозный лимфаденит является следствием продуктивного воспаления, которое вызывается микобактериальными и, по литературным данным, грибковыми инфекциями, а также неинфекционными причинами. Диагностическое значение имеет только гранулематозный лимфаденит как доминирующий признак.
 Мелкие эпителиоидно-клеточные гранулемы и единичные скопления эпителиоидных гистиоцитов не имеют дифференциально-диагностического значения. Гранулематозный лимфаденит обусловлен туберкулезом, саркоидозом и токсоплазмозом, лимфаденитами, вызванными атипичными микобактериями (Mycobacteriumscrofulaceum и kansasii) и грибковыми инфекциями.
Мелкие эпителиоидно-клеточные гранулемы и единичные скопления эпителиоидных гистиоцитов не имеют дифференциально-диагностического значения. Гранулематозный лимфаденит обусловлен туберкулезом, саркоидозом и токсоплазмозом, лимфаденитами, вызванными атипичными микобактериями (Mycobacteriumscrofulaceum и kansasii) и грибковыми инфекциями.
Частота установления нозологического диагноза в категории гранулематозный лимфаденит относительно высока, поскольку гранулематозное воспаление часто носит специфический характер. Причинами неудовлетворительной диагностики могут быть редкие и трудно идентифицируемые возбудители, такие как М. scrofulaceum и М. kansasii, часто вызывающие шейные лимфадениты, особенно у детей и лиц молодого возраста. По-видимому, эти инфекции наблюдаются довольно часто и остаются недиагностированными. В связи с ростом числа иммунокомпрометированных больных можно предполагать недиагностированные грибковые инфекции.
- Гнойно-некротический гранулематозный лимфаденит и гнойный лимфаденит отражает гнойное воспаление и вызывается преимущественно бактериальными агентами, хотя встречается и при грибковых инфекциях.
 Наиболее частой причиной гранулематозного гнойно-некротического лимфаденита вне связи с инфекцией в регионарной зоне является фелиноз (болезнь кошачьей царапины), хламидийная инфекция, а также другие инфекционные болезни, характеризующиеся первичным аффектом в области входных ворот и регионарным лимфаденитом. Целый ряд инфекционных болезней, характеризующихся первичным аффектом в области ворот инфекции и регионарным лимфаденитом, также проявляет гистологическую картину гной- ВОГР или гнойно-некрш ического гранулематозного лимфаденита. К ним относятся клещевые пятнистые лихорадки (марсельская лихорадка, ЮММИЩр сыпной гиф Северной Азии и др,), лихорадка цуцугамуши, везукулярный риккетсиоз, содоку (болезнь укуса крысы).
Наиболее частой причиной гранулематозного гнойно-некротического лимфаденита вне связи с инфекцией в регионарной зоне является фелиноз (болезнь кошачьей царапины), хламидийная инфекция, а также другие инфекционные болезни, характеризующиеся первичным аффектом в области входных ворот и регионарным лимфаденитом. Целый ряд инфекционных болезней, характеризующихся первичным аффектом в области ворот инфекции и регионарным лимфаденитом, также проявляет гистологическую картину гной- ВОГР или гнойно-некрш ического гранулематозного лимфаденита. К ним относятся клещевые пятнистые лихорадки (марсельская лихорадка, ЮММИЩр сыпной гиф Северной Азии и др,), лихорадка цуцугамуши, везукулярный риккетсиоз, содоку (болезнь укуса крысы).
Гнойные лимфадениты имеют характерную клиническую но выявляются в лимфоузлах, регионарных для гнойных очагов, таких как фурункул, панариций, флегмона, мастит, абсцесс. В связи с распространенностью особую группу составляют одонтогенные лимфадениты,cunyKnf’ ющие заболеваниям зубов, рта и носоглотки. В гематологической практике таких больных почти нет, поскольку клиническая картина типична и биопсия лимфоузла выполняется редко.
В гематологической практике таких больных почти нет, поскольку клиническая картина типична и биопсия лимфоузла выполняется редко.
- Синусный гистиоцитоз — один из самых частых признаков в лимфоузлах, удаленных по поводу разных причин. Как ведущий признак он наблюдается при синусном гистиоцитозе с массивной лимфаденопатией (болезнь Розаи Дорфмана). Кроме того, синусный гистиоцитоз может быть проявлением неспецифической реакции лимфатических узлов на инфекцию или опухоль, реакция на лимфангиографию. Выявление выраженного синусного гистиоцитоза должно быть показанием к повторной биопсии или для проведения онкопоиска, в связи с частой ассоциацией его с опухолями, особенно у больных, имеющих генерализованную лимфаденопатию или конгломераты лимфоузлов. Таким образом, синусный гистиоцитоз — это гистологическая находка, на основании которой необходимо заподозрить опухоль и рассмотреть вопрос о повторной биопсии или поиска опухоли.
- Некроз узла как ведущий признак выделен в отдельную группу так же в связи с тем, что часто предшествует развитию опухоли.
 При гранулематозных и гнойно-некротических лимфаденитах некроз носит казеозный или гнойный характер, соответственно, и окружен гранулемами или грануляционной тканью. Здесь речь о коагуляционном, «сухом» некрозе узла. При выявлении некроза узла показано повторное проведение биопсии имеющихся или появляющихся в динамике увеличенных лимфоузлов. В редких случаях некроз может сопутствовать тяжелым инфекциям или выявляется на фоне обычных инфекций у больных с иммунодефицитом.
При гранулематозных и гнойно-некротических лимфаденитах некроз носит казеозный или гнойный характер, соответственно, и окружен гранулемами или грануляционной тканью. Здесь речь о коагуляционном, «сухом» некрозе узла. При выявлении некроза узла показано повторное проведение биопсии имеющихся или появляющихся в динамике увеличенных лимфоузлов. В редких случаях некроз может сопутствовать тяжелым инфекциям или выявляется на фоне обычных инфекций у больных с иммунодефицитом. - Атрофические изменения обнаруживаются в мелких лимфоузлах, удаленных в связи с онкопоиском преимущественно у пожилых людей, а также лиц, перенесших химиотерапию, лучевую терапию, получавших преднизо- лон. Выявление атрофических изменений не предполагает дополнительных диагностических исследований. Их следует трактовать как финальный диагноз, если нет других оснований, требующих продолжения дифференциально-диагностического поиска. В связи с этим атрофия лимфоузла, как ведущий признак, должна выноситься в гистологическое заключение.
8) Дерматопический лимфаденит имеет характерную морфологическую картину и выявляется в лимфатических узлах, прилегающих к пораженным областям кожи при различных кожных процессах.
Синдромы, важные в диагностике лимфаденопатий
Характерные клинические синдромы могут помочь клиницисту установить причину лимфаденопатии.
Мононуклеозоподобный синдром
Мононуклеозоподобный синдром характеризуется лимфаденопатией, фарингитом, утомляемостью, слабостью, лихорадкой и появлением атипичных мононуклеаров в периферической крови. Классическим возбудителем инфекционного мононуклеоза является вирус Эпштейна-Барр. Однако этот синдром может вызываться цитомегаловирусом, ВИЧ, токсоплазмой, а также вирусами гепатитов В и С.
Существует категория пациентов с затяжной и рецидивирующей лимфаденопатией, у которых диагноз установить не удается. Многие из этих больных имеют лихорадку и жалуются на выраженную утомляемость вплоть до развития нетрудоспособности. Обследование на многочисленные инфекции не дает результата. Вместе с тем, у многих из этих пациентов по серологическим данным выявляется картина реактивации или перенесенной инфекции вирусом Эпштейна-Барр (EBV) с необычно высоким титром антител к ядерным антигенам EBNA (ЕВV Nuclear Antigen). Интерпретация результатов серологических тестов у этих больных имеет большое значение для определения клинических вариантов ЕВ V инфекции.
Обследование на многочисленные инфекции не дает результата. Вместе с тем, у многих из этих пациентов по серологическим данным выявляется картина реактивации или перенесенной инфекции вирусом Эпштейна-Барр (EBV) с необычно высоким титром антител к ядерным антигенам EBNA (ЕВV Nuclear Antigen). Интерпретация результатов серологических тестов у этих больных имеет большое значение для определения клинических вариантов ЕВ V инфекции.
Серологическая диагностика CMV инфекции основана на выявлении нарастающего титра антител класса IgM в парных сыворотках в динамике.
Иифекции группы TORCH. К этим инфекциям относится токсоплазмоз (То — toxoplasmosis), краснуха (R — rubella), цитомегаловирусная (С — CMV) инфекция и герпетическая инфекция (Н — herpes simplex virus). Все они могут проявляться с лимфаденопатией и в период беременности вызывать тяжелые пороки развития у плода. Поэтому обследование беременных должно обязв» тельно включать скрининговые исследования этих инфекций.
Первичный очаг и регионарный лимфаденит
Синдром характеризуется наличием кожного очага и регионарным увеличением лимфатических узлов. В этот синдром попадает большинство случаев локальных лимфаденопатий, поскольку первичным очагом может быть любая локальная инфекция. Особую группу составляют риккетсиозы, пере- даваемые с укусами клещей семейства иксодовых. Все риккетсиозы имеют сходную клинику. Инкубационный период составляет чаше всего от 2 до 7 дней, клиническая картина характеризуется лихорадкой и розеолезно- папулезной сыпью, продолжительность заболевания — не более 2 недель. Во многих случаях наблюдается регионарный лимфаденит. В диагностике этих заболеваний имеет значение географический регион. При риккетсиозах комплекс первичного очага (первичный аффект), регионарного лимфаденита и (иногда) лимфангоита носит название первичного комплекса. Под первичным аффектом понимается локальный специфический дерматит в месте присасывания клеща — участок инфильтрации с гиперемией 5-30 мм, часто эволюционирующий в язву.
В этот синдром попадает большинство случаев локальных лимфаденопатий, поскольку первичным очагом может быть любая локальная инфекция. Особую группу составляют риккетсиозы, пере- даваемые с укусами клещей семейства иксодовых. Все риккетсиозы имеют сходную клинику. Инкубационный период составляет чаше всего от 2 до 7 дней, клиническая картина характеризуется лихорадкой и розеолезно- папулезной сыпью, продолжительность заболевания — не более 2 недель. Во многих случаях наблюдается регионарный лимфаденит. В диагностике этих заболеваний имеет значение географический регион. При риккетсиозах комплекс первичного очага (первичный аффект), регионарного лимфаденита и (иногда) лимфангоита носит название первичного комплекса. Под первичным аффектом понимается локальный специфический дерматит в месте присасывания клеща — участок инфильтрации с гиперемией 5-30 мм, часто эволюционирующий в язву.
Болезнь кошачьей царапины (БКЦ) не является редким заболеванием, однако на практике этот диагноз устанавливается редко. БКЦ следует предполагать в случаях, когда у пациента имеется лимфаденопатия и соответствующий эпидемиологический анамнез (контакт с кошкой). Диагностическое значение имеют серологические методы выявления антител к возбудителю заболевания I Bartonella henselae и проведение ПЦР анализа из биоп- татов лимфатических узлов или образования, развившегося в месте проникновения бартонеллы в организм человека (первичного аффекта).
БКЦ следует предполагать в случаях, когда у пациента имеется лимфаденопатия и соответствующий эпидемиологический анамнез (контакт с кошкой). Диагностическое значение имеют серологические методы выявления антител к возбудителю заболевания I Bartonella henselae и проведение ПЦР анализа из биоп- татов лимфатических узлов или образования, развившегося в месте проникновения бартонеллы в организм человека (первичного аффекта).
Бубоны
Под бубонами понимают значительное увеличение лимфатических узлов, которое сопровождается их нагноением и распадом. Классическая причина — чума. К этой же категории относятся тулярмия, содоку (болезнь укуса крысы), болезнь кошачьей царапины. В зарубежной литературе для обозначения бубонных поражений используется термин ульцерогландулярный синдром.
Окулогландулярный синдром (офтальмогландулярный синдром)
Определяется как конъюнктивит и увеличение переднеушных лимфоузлов. Чаще всего он обусловлен вирусным кератоконъюнктивитом. Этот синдром может быть манифестацией болезни кошачьей царапины, когда внедрение возбудителя происходит через конъюнктиву, или туляремии. В литературе окулогландулярный синдром нередко называется синдромом Парино. Синдром Парино относится ко всем случаям конъюнктивита и увеличения переднеушных лимфоузлов, включая бартонеллез, грибковые заболевания, в частности паракокцидиоидоз. Отметим, что существует и второй синдром Парино, представляющий собой парез взора вверх, возникающий при гидроцефалии, опухолях шишковидного тела, инсультах.
В литературе окулогландулярный синдром нередко называется синдромом Парино. Синдром Парино относится ко всем случаям конъюнктивита и увеличения переднеушных лимфоузлов, включая бартонеллез, грибковые заболевания, в частности паракокцидиоидоз. Отметим, что существует и второй синдром Парино, представляющий собой парез взора вверх, возникающий при гидроцефалии, опухолях шишковидного тела, инсультах.
Язва половых органов + паховый лимфаденит
Этот синдром может быть обусловлен следующими заболеваниями: герпетическая инфекция половых органов, сифилис, мягкий шанкр, венерическая лимфогранулема, травмированные остроконечные кондиломы.
Лимфадениты в паховой зоне могут быть вызваны кандидозом, хламидиозом (другие серотипы хламидий) и микоплазмозом.
Персистирующая генерализованная лимфаденопатия
Увеличение лимфоузлов как минимум в двух областях, кроме паховой, сохраняющееся в течение 3 месяцев, определяется как персистирующая генерализованная лимфаденопатия (ПГЛ). ПГЛ — одно из самых частых проявлений острой фазы ВИЧ-инфекции. Генерализованная лимфаденопатия у больных СПИД может быть вызвана не только вирусом иммунодефицита человека, но и HHV 8-го типа, цитомегаловирусной инфекцией, токсоплазмой, микобактериями, криптококками, трепонемами и, наконец, лимфомой.
ПГЛ — одно из самых частых проявлений острой фазы ВИЧ-инфекции. Генерализованная лимфаденопатия у больных СПИД может быть вызвана не только вирусом иммунодефицита человека, но и HHV 8-го типа, цитомегаловирусной инфекцией, токсоплазмой, микобактериями, криптококками, трепонемами и, наконец, лимфомой.
Синдром затяжной, персистирующей лимфаденопатии характерен хроническому токсоплазмозу, туберкулезу, бруцеллезу, саркоидозу.
Клинические варианты EBV-инфекции на основании серологических данных
| Клинические варианты | Антитела к IgM-VCA | Антитела к IgG-EA | Антитела к IgG-EBNA |
| Наивный статус | — | — | — |
| Ранняя фаза острой инфекции | + | + | — |
| Поздняя фаза острой инфекции | — | + | + |
| Латентная инфекция | — | — | + |
| Реактивация/атипичная реактивация | + | +/- | + |
| Хроническая персистирующая инфекция | — | -/+ | +, высокий титр |
| VCAI капсидный антиген, ЕА — ранний антиген, EBNA — ядерный антиген
|
Значение клинических признаков при лимфаденопатии
Увеличение селезенки
инфекционный мононуклеоз
лимфатические опухоли
острые н хронические лейкозы
ревматоидный артрит
системная красная волчанка
хронический гепатит с системными проявлениями
Кожные проявления
инфекционный мононуклеоз цитомегаловирусная инфекция ревматоидный артрит системная красная волчанка саркоидоз
лимфатические опухоли сывороточная болезнь риккетсиозы боррелиоз
чума, туляремия и др. инфекции
инфекции
ВИЧ-инфекция
сифилис
лейшманиоз
Увеит, хориоретинит, конъюнктивит
саркоидоз
токсоплазмоз
болезнь кошачьей царапины, туляремия герпесвирусные инфекции сифилис
Поражение легких и плевры
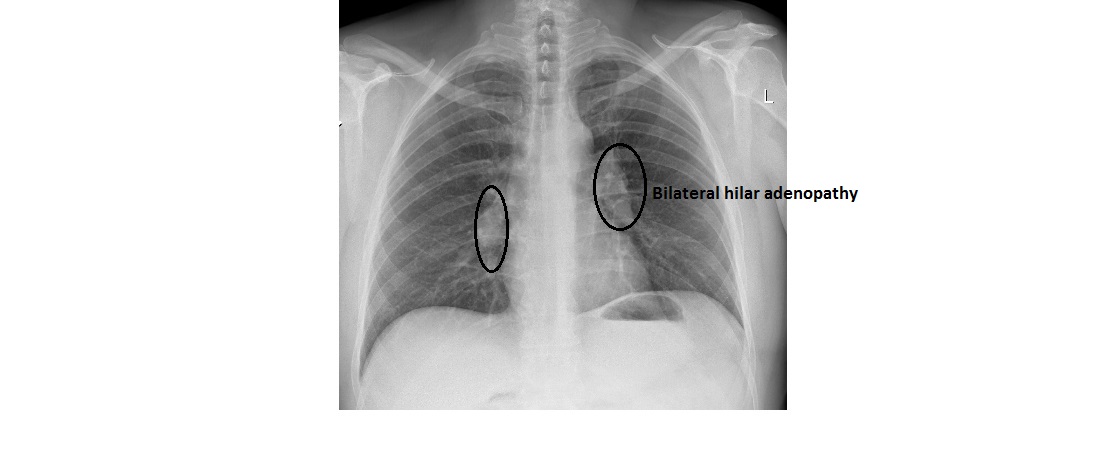
саркоидоз туберкулез рак легкого
системная красная волчанка герпесвирусные инфекции лимфатические опухоли острые и хронические лейкозы
Суставной синдром
ревматоидный артрит системная красная волчанка саркоидоз
сывороточная болезнь хронический вирусный гепатит ВИЧ-инфекция бруцеллез
иерсиниоз
Лихорадка, резистентная к антибиотикам
инфекционный моноиуклеоз
лимфатические опухоли
ревматоидный артрит
системная красная волчанка
сепсис (включая бактериальный эндокардит)
ВИЧ-инфекция
туберкулез, лейшманиоз
Методы обследования при лимфаденпатиях
Облигатные
- Общий анализ кропи, общий анализ мочи
- ВИЧ, сифилис, гепатиты
- Рентген или КТ грудной клетки
- УЗИ органов брюшной полости
Факультативные_________________________________________________ ____________
- Исследования на герпесвирусы:,СМУ, IBV, вирус простого герпеса 1,2 и др.
| Серологическая диагностика токсоплазмоза, бартонеллеза (болезнь кошачьей
царапины), бруцеллеза, риккетсиозы, боррелиоз и др. инфекционные заболевания
- Биохимия крови (белки, ферменты, билирубин, холестерин, ревматоидные пробы)
- Проба Манту, количественный ИФА на противотуберкулезные антитела
- Специфическая диагностика системной красной волчанки и ревматоидного артрита
- Биопсия лимфатического узла и/или экстранодального очага поражения с гистологическим, цитологическим, иммуногистохимическим и молекулярно-биологическим исследованиями.
- УЗИ лимфатических узлов с допплерографией
- Направление на консультацию к специалисту___________________________________
Таблица 3. Эпидемиологические данные, профессиональные факторы важные в диагностике лимфаденопатий.
| ||||||||||||||||||||||||||||||||||||
Лекарственные препараты, применение которых может вызвать увеличение лимфоузлов (в контексте гиперчувствительность)
| Препарат | Г руина |
| Аллопуринол | Антиметаболит |
| Атенолол (Тенормин) | Антигипертензивнь» препараты |
| Каптоприл | |
| Гидралазин (Апресолин) | |
| Карбамазепин (Тегретол) | Противосудорожные препараты |
| I Фенитоин (Дилантин) | |
| Примидон (Мизолин) | |
| Пенициллин | Антибиотические препфаты |
| Цефалоспорины | |
| Сульфаниламиды | |
| Пириметамин | Противомалярийныепрепараты |
| Хинин | |
| Сулиндак (Клинорил) | НСПВСипротиворевматические препараты |
| Препараты золота |
Заключение по лимфаденопатиям
Увеличение лимфоузлов — симптом, вызывающий серьезные опасения и тревогу у большинства больных. Нам кажется уместным там возможные причины лимфаденопатий, ход диагностичесгого поиска. Решение о временном отказе от биопсии обычно вызывает много вопросов. Необходимо объяснять пациентам, почему мы придерживаемся выжидательной тактики. Однако, воздерживаясь от биопсии необходимо продолжать активное наблюдение, поскольку при многих вариантах лимфом лимфоузлы могут временно уменьшаться в размере. Частота установления этнологического диагноза при неопухолевой лимфаденопатий не может быть равна 100%, поскольку это требует неоправданно обширных исследований при незначимой клинической ситуации. При проведении биопсии и учете харякго* ра изменений в лимфоузлах, указание в заключении доминирующего гистологического признака может повысить диагностическую эффективность,по скольку биопсия не является конечным этапом диагностического поиска при неопухолевых лимфаденопатиях. Важным фактором, позволяющим повысить эффективность диагностики, является тщательность обследования больного перед биопсией, это приводит к уменьшению числа ненужных биопсий.
Нам кажется уместным там возможные причины лимфаденопатий, ход диагностичесгого поиска. Решение о временном отказе от биопсии обычно вызывает много вопросов. Необходимо объяснять пациентам, почему мы придерживаемся выжидательной тактики. Однако, воздерживаясь от биопсии необходимо продолжать активное наблюдение, поскольку при многих вариантах лимфом лимфоузлы могут временно уменьшаться в размере. Частота установления этнологического диагноза при неопухолевой лимфаденопатий не может быть равна 100%, поскольку это требует неоправданно обширных исследований при незначимой клинической ситуации. При проведении биопсии и учете харякго* ра изменений в лимфоузлах, указание в заключении доминирующего гистологического признака может повысить диагностическую эффективность,по скольку биопсия не является конечным этапом диагностического поиска при неопухолевых лимфаденопатиях. Важным фактором, позволяющим повысить эффективность диагностики, является тщательность обследования больного перед биопсией, это приводит к уменьшению числа ненужных биопсий. С другой стороны, важнейшим аспектом диагностики лимфадешиан тий является раннее выявление опухолей. Синдром увеличенных периферических лимфатических узлов представляет собой сложную клиническую и патоморфологическую проблему. Необходимо четкое знание многообразия причин увеличения лимфатических узлов, алгоритмов диагностики, наличие лабораторных возможностей в дифференциальной диагностике этого синдрома. Предложенные нами алгоритмы не являются специализированными (для каждой нозологии), но ориентированы на амбулаторный прием гематолога и онколога. А также может быть использованы терапевтами, семейными врачами, хирургами, особенно работающими в амбулаторнополиклиническом звене.
С другой стороны, важнейшим аспектом диагностики лимфадешиан тий является раннее выявление опухолей. Синдром увеличенных периферических лимфатических узлов представляет собой сложную клиническую и патоморфологическую проблему. Необходимо четкое знание многообразия причин увеличения лимфатических узлов, алгоритмов диагностики, наличие лабораторных возможностей в дифференциальной диагностике этого синдрома. Предложенные нами алгоритмы не являются специализированными (для каждой нозологии), но ориентированы на амбулаторный прием гематолога и онколога. А также может быть использованы терапевтами, семейными врачами, хирургами, особенно работающими в амбулаторнополиклиническом звене.
Наиболее частые причины неопухолевой лимфаденопатии, встречающиеся в практике гематолога и методы их диагностики
| Болезнь | Подтверждающий метод диагностики |
| Инфекционный мононуклеоз | Антитела класса IgM к 1 |
| Цитомегаловирусная инфекция | Антитела класса IgM к CMV (нарастающий тигр), ПЦР |
| Токсоплазмоз | Антитела класса IgM к Toxoplasma gondii |
| СПИД | Серологическое исследование |
| Болезнь кошачьей царапины (фелиноз) | Антитела к Bartonella henselae |
| Сифилис | Серологическое исследование |
| Саркоидоз | Биопсия |
| Туберкулез | Проба Манту, биопсия, ПЦР |
| Хламидии, микоплазмы | Специфические антитела, ПЦР |
| Аутоиммунные заболевания (системная красная волчанка, ревматоидный артрит, болезнь Шегрена, дерматомиозит) | Биопсия |
НЕКОТОРЫЕ СТАТИСТИЧЕСКИЕ ДАННЫЕ ТЕСТОВОГО ИССЛЕДОВАНИЯ АЛГОРИТМОВ ДИАГНОСТИКИ ЛИМФАДЕНОПАТИЙ
Алгоритмы диагностики лимфаденопатий были тестированы у 446 больных с лимфаденопатией в специальном исследовании поликлинического отделения ГНЦ. Из них в конечном итоге 148 больных (30%) имели неопухолевую лимфаденопатию, 298 больных (70%) — опухоли. Среди них у 217 (49%) больных была констатирована локальная, у 229 (51%) генерализованная лимфаденопатия.
Из них в конечном итоге 148 больных (30%) имели неопухолевую лимфаденопатию, 298 больных (70%) — опухоли. Среди них у 217 (49%) больных была констатирована локальная, у 229 (51%) генерализованная лимфаденопатия.
Полученные данные показали, что спектры этиологической структуры при локальной и генерализованной лимфаденопатиях радикально отличаются. Если при локальной лимфаденопатии соотношение опухоль/не опухоль составляет 1:1 (48% и 52% соответственно), то при генерализованной лимфаденопатии 90% больных имели опухоль, и только 10% — неопухолевую лимфаденопатию. Анализ 217 больных с локальной лимфаденопатией показал, что в 64% случаев локально были увеличены лимфоузлы шейной области, среди них 63% пациентов имели неопухолевую лимфаденопатию, 33%-лимфоидные опухоли, 4%-метастазы рака. В 17% случав выявлено локальное увеличение подмышечных лимфоузлов. Среди них пациенты с неопухолевой лимфаденопатией составили 35%, опухолями лимфоидной при- роды-65%, метастазами рака -6%. В 11% случаев были увеличены надключичные лимфоузлы — в 30% случаев выявлена неопухолевая лимфадснопа- тия, 65% случаев — опухоли лимфоидной природы и в 5%-метастазы раза. Н 8% случаев I локальное увеличение паховых лимфоузлов, среди них соотношение опухоль/неопухоль составило 1:1. Метастазы рака в паховых лимфоузлах выявлено в 6% случаев. Поэтапная диагностика (осмотр, обследование, ревизия полученных данных), на которой основывается диагностический поиск, позволила повысить эффективность дифференциальной диагностики больных с неопухолевыми лимфаденопатиями. Результаты исследования показали, что при локальной ЛАП ключевым диагностическим этапом является осмотр (локальные инфекционные процессы, укусы, царапины, имплантат, высыпание на коже и оценка вероятности опухоли). У 50% больных с локальной лимфаденопатией диагноз был очевиден на первом этапе. При генерализованной ЛАП осмотр позволяет заподозрить диагноз у меньшего числа больных (30%). В основном диагноз ставится после второго этапа- этапа обследований (50%), оставшихся 20% больных диагноз ставится после повторного прохождения этапов диагностического поиска.
Н 8% случаев I локальное увеличение паховых лимфоузлов, среди них соотношение опухоль/неопухоль составило 1:1. Метастазы рака в паховых лимфоузлах выявлено в 6% случаев. Поэтапная диагностика (осмотр, обследование, ревизия полученных данных), на которой основывается диагностический поиск, позволила повысить эффективность дифференциальной диагностики больных с неопухолевыми лимфаденопатиями. Результаты исследования показали, что при локальной ЛАП ключевым диагностическим этапом является осмотр (локальные инфекционные процессы, укусы, царапины, имплантат, высыпание на коже и оценка вероятности опухоли). У 50% больных с локальной лимфаденопатией диагноз был очевиден на первом этапе. При генерализованной ЛАП осмотр позволяет заподозрить диагноз у меньшего числа больных (30%). В основном диагноз ставится после второго этапа- этапа обследований (50%), оставшихся 20% больных диагноз ставится после повторного прохождения этапов диагностического поиска.
В результате внедрения алгоритмов диагностики лимфаденопатий в виде рекомендаций в практику ФГБУ ГНЦ Минздравсоцразвития России диагностика некоторых инфекционных заболеваний (инфекции, вызванной гер- песвирусами, болезнь кошачьей царапины, СПИД, сифилис, токсоплазмоз) стала доступной без биопсии, благодаря прицельной диагностике инфекций и усовершенствования их интерпретации. Анализ этиологической структуры у больных с неопухолевыми лимфаденопатиями, подвергшихся диагностической биопсии, показал, что биопсия имела решающее значение в постановке нозологического диагноза в 42% случаев. Это пациенты с туберкулезным лимфаденитом, саркоидозом, с отложениями чужеродных материалов в лимфоузлах (силикон, липиды, меланин), с системной красной волчанкой и ревматоидным артритом, а также с разными кожными заболеваниями, обследуемые с целью исключения опухоли. В остальных 58% случаев диагноз был установлен по комплексу клинико-лабораторных данных. Число диагностических биопсий лимфатических узлов у больных с неопухолевыми лимфаденопатиями в два раза уменьшилось. Снижение числа биопсий привело к некоторым изменениям в распределении гистологических вариантов.
Анализ этиологической структуры у больных с неопухолевыми лимфаденопатиями, подвергшихся диагностической биопсии, показал, что биопсия имела решающее значение в постановке нозологического диагноза в 42% случаев. Это пациенты с туберкулезным лимфаденитом, саркоидозом, с отложениями чужеродных материалов в лимфоузлах (силикон, липиды, меланин), с системной красной волчанкой и ревматоидным артритом, а также с разными кожными заболеваниями, обследуемые с целью исключения опухоли. В остальных 58% случаев диагноз был установлен по комплексу клинико-лабораторных данных. Число диагностических биопсий лимфатических узлов у больных с неопухолевыми лимфаденопатиями в два раза уменьшилось. Снижение числа биопсий привело к некоторым изменениям в распределении гистологических вариантов.
В частности, более чем в 2 раза (со статистически достоверной разницей) снизилась частота выявления в лимфоузлах фолликулярной гиперплазии. Эго показывает, что снижение было обусловлено именно ненужными биопсиями. Кроме того, достоверно выросла частота выявления синусного гнети* оцитота как ведущего признака. Это говорит о том, что биопсии подвергаются диагностически трудные случаи.
Кроме того, достоверно выросла частота выявления синусного гнети* оцитота как ведущего признака. Это говорит о том, что биопсии подвергаются диагностически трудные случаи.
Основную трудность в диагностике представляют больные с гистологически неясной лимфаденопатией и клиническими проявлениями персистирующей инфекции (10% больных). Они были включены в группу шши- ных лимфопролиферативных синдромов». Проведенное исследование позволило нам выявить несколько частых диагностических проблем. Самая важная из них — игнорирование характера поражения лимфоузла при реак- тивной гиперплазии. В результате детального анализа морфологии лимфатических узлов у больных с неопухолевыми лимфаденопатиями были выделены главные и ведущие гистологические признаки, имеющие дифференциально-диагностические значения. Восемь характерных гистологических вариантов поражения лимфоузла для клинициста служили отправной точкой диагностики. Указание гистологом этих вариантов ориентирует клинициста на определенные диагностические исследования. Краткие заключения о том, что в лимфоузле выявлена картина вторичных (неспецифическнх, реактивных) изменений полностью лишает клинициста важного диагностического оружия.
Краткие заключения о том, что в лимфоузле выявлена картина вторичных (неспецифическнх, реактивных) изменений полностью лишает клинициста важного диагностического оружия.
Во многих случаях причиной диагностических ошибок стало недостаточное обследование больных перед биопсией. ВИЧ инфекция всегда должна быть исключена до биопсии! Биопсия лимфоузла при инфекционноммоно- нуклеозе и при других острых вирусных инфекциях нецелесообразна, так как может привести к ошибочной диагностике опухоли. Наше исследование показывает, что СПИД, инфекционный мононуклеоз, фелиноз, токсоплаз- моз, сифилис необходимо исключить серологическими методами до биопсии. Перечисленные инфекции, а также вирусные гепатиты, нередко вызывают мононуклеозоподобный синдром. Поэтому важен целенаправленный поиск атипичных мононуклеаров в мазке периферической крови и определение Т-клеточной клональности.
Нередкой проблемой является неверный выбор лимфоузла. Биопсии подлежат наиболее измененные лимфоузлы, а не наиболее удобные для хирургического удаления. Мы располагаем данными 40 (10%) больных у которых реактивные изменения предшествовали выявлению лимфатических опухолей. Дана характеристика изменений в непораженных опухолью лимфатических узлах у больных с лимфомами и лимфогранулематозом, а именно выявление таких ведущих признаков, как некроза узла и синусного гистиоцитоза, которые с высокой вероятностью свидетельствуют о наличии опухоли в организме. В конечном итоге, у этих больных после повторной биопсии диагностированы лимфома Ходжкина — у 19 больных и неходжкинские лимфомы -у 21 больного. Были вывялены случаи (6%) назначения химиотерапии по поводу предполагаемой лимфомы, тогда как на самом деле изменения в лимфоузле носили реактивный характер. Эти ошибки нередко связаны с плохим качеством гистологических препаратов и невозможностью выполнения иммуногистохимического исследования.
Мы располагаем данными 40 (10%) больных у которых реактивные изменения предшествовали выявлению лимфатических опухолей. Дана характеристика изменений в непораженных опухолью лимфатических узлах у больных с лимфомами и лимфогранулематозом, а именно выявление таких ведущих признаков, как некроза узла и синусного гистиоцитоза, которые с высокой вероятностью свидетельствуют о наличии опухоли в организме. В конечном итоге, у этих больных после повторной биопсии диагностированы лимфома Ходжкина — у 19 больных и неходжкинские лимфомы -у 21 больного. Были вывялены случаи (6%) назначения химиотерапии по поводу предполагаемой лимфомы, тогда как на самом деле изменения в лимфоузле носили реактивный характер. Эти ошибки нередко связаны с плохим качеством гистологических препаратов и невозможностью выполнения иммуногистохимического исследования.
Разработанные нами алгоритмы диагностики лимфаденопатий, в которых ключевую роль играет организация диагностического поиска с обязательным исследованием широкого спектра инфекций, а также клинических, цитоморфологических, иммунологических, молекулярных и серологических методов, позволили повысить диагностическую эффективность при неопухолевых лимфаденопатиях с 58% до 90%. Таким образом, современные диагностические возможности позволяют установить нозологический диагноз в большинстве случаев. Основными требованиями для установления верного диагноза лимфаденопатий является правильный алгоритм действий, а также тесная кооперация разных специалистов.
Таким образом, современные диагностические возможности позволяют установить нозологический диагноз в большинстве случаев. Основными требованиями для установления верного диагноза лимфаденопатий является правильный алгоритм действий, а также тесная кооперация разных специалистов.
Разработанные нами алгоритмы диагностики лимфаденопатий имеют несколько принципиальных отличий от всех предложенных ранее алгоритмов диагностики.
- Рекомендации прошли проверку в специальном исследовании.
- Рекомендации не являются специализированными, но ориентированы на амбулаторный прием гематолога и онколога.
- В рекомендации включена диагностика объемных нелимфоидных образований в шейной и подмышечной областях, которые часто принимаются за лимфоузлы.
- Биопсия лимфоузла не считается конечным этапом исследования. Предложен алгоритм послебиопсийной диагностики.
- Значительное место уделено молекулярным и иммуногистохимическим методам диагностики.
Основные заболевания, сопровождающиеся синдромом лимфаденопатии
Опухоли
I опухоли кроветворной системы, чаще всего лимфомогранулематоз, неходжкинские лимфомы и хронический лимфолейкоз. Увеличением лимфоузлов могут сопровождаться любые гемобластозы.
Увеличением лимфоузлов могут сопровождаться любые гемобластозы.
1 метастатические опухоли: чаще всего опухоли молочной железы, опухоли головы и шеи, опухоли легкого, опухоли ЖКТ, почек, предстательной железы, меланома. Большинство опухолей может метастазировать в лимфоузлы.__________________________________________
Иммунные реакции, реакции гиперчувствительности | сывороточная болезнь
- реакции на антиконвульсанты (дифенилгидантоин, карбамазепин), примидон, аллопуринол, индометацин, сульфаниламиды
- поствакцинальные лимфадениты__________________________________
БАКТЕРИАЛЬНЫЕ ИНФЕКЦИИ
Инфекции, передающиеся преимущественно через кожу и слизистые
- пиогенные бактерии, вызывающие банальные лимфадениты (ангины, рожа, и т.д.]
- болезнь кошачьей царапины
- бациллярный ангиоматоз
- содоку (болезнь укуса крысы)
- риккетсиозы (укус клеща плюс лимфаденит):
Марсельская лихорадка (в России — побережье Черного моря)
клещевой сыпной тиф Северной Азии (Новосибирская и Тюменская области, Красноярский край)
дальневосточный клещевой риккетсиоз (Дальний Восток РФ)
- лихорадка цуцугамуши (Приморский край) везикулярный риккетсиоз (Молдавия, Донецк)
- клещевой энцефалит (повсеместно)
- сифилис
- мягкий шанкр
- венерическая лнмфограиулема
- лимфадениты, вызванные другими серотипами хламидий
- микоплазменные инфекции 4
- донованоз (в развивающихся странах)
| споротрихоз (повреждение кожи)
I кожный нокардиоз (повреждение кожи)
I гранулема купальщиков (повреждение кожи)
| кожный лейшманиоз (укус москита)
- мелиоидоз (повреждение кожи)
Имеющие разные пути передачи
- туляремия
- бруцеллез
- чума
- лептоспироз
- листериоз
Передающиеся фекально-оральным путем
- иерсиниоз
- псевдотуберкулез
- брюшной тиф и паратифы А и В ВИРУСНЫЕ ИНФЕКЦИИ
- вирус Эпштейна-Барр I цитомегаловирус
- вирусы простого герпеса
I вирус опоясывающего лишая / ветрянки
- вирус иммунодефицита человека
- вирус кори
- вирус краснухи
- аденовирусы
- парагрипп вирусы, вызывающие острые респираторные инфекции
- вирус гепатита С
МИКОБАКТЕРИАЛ ЬНЫЕ ИНФЕКЦИИ | туберкулез, БЦЖит
- атипичные микобактерии (Mycobacteriurm viumintra cellulara M.
 scrofulact, М.kansasik др)
scrofulact, М.kansasik др) - лепра ГРИБЫ
- криптококкоз
- гистоплазмоз
- кокцидиомикоз
ИНФЕКЦИИ, ВЫЗВАННЫЕ ПРОСТЕЙШИМИ И ПАРАЗИТАМИ
- токсоплазмоз
- пневмоцистная инфекция
- трипаносомоз, филяриоз и другие_________
Аутоиммунные заболевания
- ревматоидный артрит
- системная красная волчанка
- дерматомиозит
- болезнь Шегрена
смешанные заболевания соедини тельной ткани
I аутоиммунный гепатит
- Аутоиммунный тирсондит
Неопухолевые лимфадепопатии в контексте клинико-лабораторных синдромов
I | болезнь Кимура
- болезнь Кикучи
- болезнь Кавасаки
I болезнь Кастлемана (ангиофолликулярная лимфоидная гиперплазия)
| синусный гистиоцитоз Розаи-Дорфмана с массивной лимфаденопатией
- прогрессивная трансформация герминальных центров__________________
Атипичные лимфопролиферативные заболевания
■ неклассифицируемые лимфопролиферативные заболевания
- затяжная фолликулярная гиперплазия
| затяжная паракортикальная гиперплазия
- EBV-ассоциированные и другие лимфопролиферативные синдромы у лиц с | иммунодефицитом:
- на фоне врожденных иммунодефицитов
- на фоне иммуносупрессивной терапии (введение антитимоцитарного глобулина, длительный прием метотрексата, азатиоприна, кортикостероидов, циклоспорина, такролимуса)
| после трансплантации
- Х-сцепленная лимфопролиферативная болезнь
- аутоиммунный лимфопролиферативный синдром_____________________
Лимфадепопатии, обусловленные отложениями чужеродных материалов
- дерматопатический лимфаденит (увеличение лимфоузлов, сопутствующее разнообразным кожным процессам)
- белковая лимфаденопатия (отложения в лимфоузлах амилоида)
- липидная лимфаденопатия
- силиконовая лимфаденопатия
- лимфаденопатия, вызванная отложениями металлов (после протезирования суставов, после приема препаратов золота)
- лимфаденопатия после лимфангиографии_________________________
Болезни накопления (инфильтрация лимфоузлов макрофагами, заполненными
отложениям метаболитов липидов)
I болезнь Гоше
| болезнь Ниманна-Пика ___________________________________
Прочие
Основные заболевания, сопровождающиеся синдромом лимфаденопатии
Опухоли
I опухоли кроветворной системы, чаще всего лимфомогранулематоз, неходжкинские лимфомы и хронический лимфолейкоз. Увеличением лимфоузлов могут сопровождаться любые гемобластозы.
Увеличением лимфоузлов могут сопровождаться любые гемобластозы.
1 метастатические опухоли: чаще всего опухоли молочной железы, опухоли головы и шеи, опухоли легкого, опухоли ЖКТ, почек, предстательной железы, меланома. Большинство опухолей может метастазировать в лимфоузлы.__________________________________________
Иммунные реакции, реакции гиперчувствительности | сывороточная болезнь
- реакции на антиконвульсанты (дифенилгидантоин, карбамазепин), примидон, аллопуринол, индометацин, сульфаниламиды
- поствакцинальные лимфадениты__________________________________
БАКТЕРИАЛЬНЫЕ ИНФЕКЦИИ
Инфекции, передающиеся преимущественно через кожу и слизистые
- пиогенные бактерии, вызывающие банальные лимфадениты (ангины, рожа, и т.д.]
- болезнь кошачьей царапины
- бациллярный ангиоматоз
- содоку (болезнь укуса крысы)
- риккетсиозы (укус клеща плюс лимфаденит):
Марсельская лихорадка (в России — побережье Черного моря)
клещевой сыпной тиф Северной Азии (Новосибирская и Тюменская области, Красноярский край)
дальневосточный клещевой риккетсиоз (Дальний Восток РФ)
- лихорадка цуцугамуши (Приморский край) везикулярный риккетсиоз (Молдавия, Донецк)
- клещевой энцефалит (повсеместно)
- сифилис
- мягкий шанкр
- венерическая лнмфограиулема
- лимфадениты, вызванные другими серотипами хламидий
- микоплазменные инфекции 4
- донованоз (в развивающихся странах)
| споротрихоз (повреждение кожи)
I кожный нокардиоз (повреждение кожи)
I гранулема купальщиков (повреждение кожи)
| кожный лейшманиоз (укус москита)
- мелиоидоз (повреждение кожи)
Имеющие разные пути передачи
- туляремия
- бруцеллез
- чума
- лептоспироз
- листериоз
Передающиеся фекально-оральным путем
- иерсиниоз
- псевдотуберкулез
- брюшной тиф и паратифы А и В ВИРУСНЫЕ ИНФЕКЦИИ
- вирус Эпштейна-Барр I цитомегаловирус
- вирусы простого герпеса
I вирус опоясывающего лишая / ветрянки
- вирус иммунодефицита человека
- вирус кори
- вирус краснухи
- аденовирусы
- парагрипп вирусы, вызывающие острые респираторные инфекции
- вирус гепатита С
МИКОБАКТЕРИАЛ ЬНЫЕ ИНФЕКЦИИ | туберкулез, БЦЖит
- атипичные микобактерии (Mycobacteriurm viumintra cellulara M.
 scrofulact, М.kansasik др)
scrofulact, М.kansasik др) - лепра ГРИБЫ
- криптококкоз
- гистоплазмоз
- кокцидиомикоз
ИНФЕКЦИИ, ВЫЗВАННЫЕ ПРОСТЕЙШИМИ И ПАРАЗИТАМИ
- токсоплазмоз
- пневмоцистная инфекция
- трипаносомоз, филяриоз и другие_________
Аутоиммунные заболевания
- ревматоидный артрит
- системная красная волчанка
- дерматомиозит
- болезнь Шегрена
смешанные заболевания соедини тельной ткани
I аутоиммунный гепатит
- Аутоиммунный тирсондит
Неопухолевые лимфадепопатии в контексте клинико-лабораторных синдромов
I | болезнь Кимура
- болезнь Кикучи
- болезнь Кавасаки
I болезнь Кастлемана (ангиофолликулярная лимфоидная гиперплазия)
| синусный гистиоцитоз Розаи-Дорфмана с массивной лимфаденопатией
- прогрессивная трансформация герминальных центров__________________
Атипичные лимфопролиферативные заболевания
■ неклассифицируемые лимфопролиферативные заболевания
- затяжная фолликулярная гиперплазия
| затяжная паракортикальная гиперплазия
- EBV-ассоциированные и другие лимфопролиферативные синдромы у лиц с | иммунодефицитом:
- на фоне врожденных иммунодефицитов
- на фоне иммуносупрессивной терапии (введение антитимоцитарного глобулина, длительный прием метотрексата, азатиоприна, кортикостероидов, циклоспорина, такролимуса)
| после трансплантации
- Х-сцепленная лимфопролиферативная болезнь
- аутоиммунный лимфопролиферативный синдром_____________________
Лимфадепопатии, обусловленные отложениями чужеродных материалов
- дерматопатический лимфаденит (увеличение лимфоузлов, сопутствующее разнообразным кожным процессам)
- белковая лимфаденопатия (отложения в лимфоузлах амилоида)
- липидная лимфаденопатия
- силиконовая лимфаденопатия
- лимфаденопатия, вызванная отложениями металлов (после протезирования суставов, после приема препаратов золота)
- лимфаденопатия после лимфангиографии_________________________
Болезни накопления (инфильтрация лимфоузлов макрофагами, заполненными
отложениям метаболитов липидов)
I болезнь Гоше
| болезнь Ниманна-Пика ___________________________________
Прочие
ОСОБЕННОСТИ ДИАГНОСТИКИ И ВЕДЕНИЯ БОЛЬНЫХ С ЛИМФАДЕНОПАТИЯМИ
Консультация гематолога или направление в специализированное гематологическое учреждение пациентов с увеличенными лимфоузлами показано в следующих случаях:
- Любая необъяснимая лимфаденопатия
- Лимфаденопатия с наличием выраженных симптомов интоксикации
- Лимфаденопатия с увеличением печени и селезенки
- Лимфаденопатия с изменениями показателей периферической крови | Отсутствие эффекта от эмпирической антибактериальной терапии
I Персистирование лимфоузлов после адекватного периода наблюдения
Показания к биопсии
Основные показания к биопсии следующие:
- высокая вероятность опухоли по клиническим данным
- необъяснимая ЛАП: после выполнения всех неинвазивных исследований, диагноз не установлен
- диагноз установлен по результатам неинвазивных методов исследования, однако, несмотря на лечение, лимфаденопатия персистирует.
Нельзя назвать размер лимфоузла, который обязательно подлежит биопсии. Тем не менее, у взрослых размер лимфоузла более 3 см вне связи с инфекцией должен рассматриваться как потенциальное показание к биопсии.
Показания к повторной биопсии
В гематологической практике нередко встречаются случаи лимфом, когда для подтверждения диагноза приходится выполнять несколько биопсий,особенно, у пациентов с реактивными лимфоузлами, прилежащих к опухоли или реактивными изменениями, предшествующими выявлению лимфатических опухолей. В редких случаях это связано с неверным выбором лимфоузла. У большинства таких пациентов биопсии подвергается один из наиболее измененных лимфоузлов, и, несмотря на значительное увеличение лимфоузлов и длительный анамнез, по результатам первой биопсии диагноз В установить не удается.
Показанием к повторной биопсии являются следующие гистологические изменения, выявленные в биопсированных лимфоузлах, не пораженных опухолью: 1) синусный гистиоцитоз, 2) паракортикальная реакция с обилием плазматических клеток и макрофагов, 3) склеротические изменения/сосудистая реакция, 4) некроз лимфоузла.
Выбор лимфоузла для биопсии
Неверный выбор лимфоузла ведет к диагностическим ошибкам. Целесообразно придерживаться следующих правил:
- для биопсии выбирают наиболее крупный, измененный и недавно увеличившийся лимфоузел
- физикальные характеристики лимфоузла имеют большее значение, чем локализация. При наличии нескольких конкурирующих лимфоузлов в разных зонах, порядок выбора по информативности: надключичный — шейный — подмышечный — паховый
- не следует биопсировать маленькие лимфоузлы, прилежащие к конгломерату. В таких случаях предпочтительнее парциальная резекция опухоли.
Организация процесса биопсии
Перед выполнением биопсии необходимо сформулировать наиболее ожидаемые результаты, поскольку от этого зависит, куда направить материал. Идеальным способом сохранения ткани лимфоузла для дальнейших исследований является глубокая заморозка ткани. Во многих случаях одного морфологического исследования недостаточно. Кроме него материалы, полученные при биопсии, могут быть исследованы:
- микробиологическими методами (посевы на среды, культуру ткани и пр.
 )
) - ПЦР на разнообразные инфекционные агенты (герпесвирусы, бартонел- лы, микобактерии, токсоплазмы и пр.) и для определения Т и В клеточной клональности.
Пункция лимфоузла
Может использоваться исключительно как ориентировочный метод диагностики в онкогематологической практике. Постановка диагноза лимфопролиферативного заболевания по пункции лимфоузла принципиально невозможна. Если вопрос касается первичной диагностики, следует выполнять биопсию. Обязательно проводить наряду с гистологическим также цитологическое исследование отпечатка биоптата.
Показания к пункции лимфатического узла:
- солитарное увеличение лимфоузла, без образования конгломератов (метастатическое поражение лимфоузлов, как правило, не сопровождается образованием конгломератов) при отсутствии косвенных данных за лимфопролиферативный процесс;
- жидкостный характер образования по ультразвуковым данным;
- получение материала для дополнительных исследований (например, молекулярных), когда биопсия уже выполнена.
Значение дополнительных исследований
Ультразвуковое исследование лимфатических узлов помогает:
- отличить лимфоузел от других образований
- точно определить размеры лимфоузлов, их количество и локализацию
- определить структуру лимфоузла
- дополнительное цветовое допплеровское картирование показывает варианты кровотока, т. е. васкуляризацию лимфоузла и позволяет отличить свежий процесс в лимфоузле от перенесенного в прошлом и оставившего только склеротические изменения, а иногда позволяет с высокой вероятностью недозревать опухолевый процесс и оценить активность остаточного опухолевого образования.
Компьютерная томография имеет преимущество перед УЗИ в тех случаях, когда необходимо оценить состояние лимфоузлов в недоступной для ультразвука локации, например, ретроперитонеальных и средостенных лимфоузлов.
Вопрос назначения антибиотиков
Чрезвычайно распространена практика назначения больным с необъяснимой лимфаденопатией эмпирической антибактериальной терапии. Антибиотики должны назначаться только при наличии четких данных о бактериальной природе заболевания и, при возможности, с учетом чувствительности возбудителя.
Антибиотики должны назначаться только при наличии четких данных о бактериальной природе заболевания и, при возможности, с учетом чувствительности возбудителя.
Вопрос о назначении эмпирической антибактериальной терапии при необъяснимой ЛАП не решен до сих пор, однако, широкое распространение антибиотикоустойчивых форм микроорганизмов говорит о необходимости воздерживаться от назначения антибиотиков без прямых показаний. Поскольку лимфаденопатия является не самостоятельным заболеванием, а синдромом, назначение антибактериального лечения зависит от установленного диагноза. Тем не менее, практика назначения антибиотиков чрезвычайно распространена, и этот вопрос обсуждается в литературе [10]. Большинство авторов отмечают, что антибиотики могут быть назначены при наличии явного инфекционного очага в регионарной зоне.
Если очага нет, показанием к эмпирической терапии антибиотиком широкого спектра является комбинация следующих признаков [14]:
- увеличение боковых шейных лимфоузлов, воспалительного характера
- возраст — моложе 30 лет
- недавно перенесенная инфекция верхних дыхательных путей
- негативные результаты серологических исследований на самых частых и вероятных возбудителей
- отсутствие признаков острофазной реакции (повышение СОЭ, С- реактивного белка, ЛДГ, 2-микроглобулина)
Физиотерапия
Физиотерапия включена в стандарты оказания медпомощи при абсцедирующих лимфаденитах и аденофлегмонах в центрах амбулаторной хирургии с однодневным стационаром (см.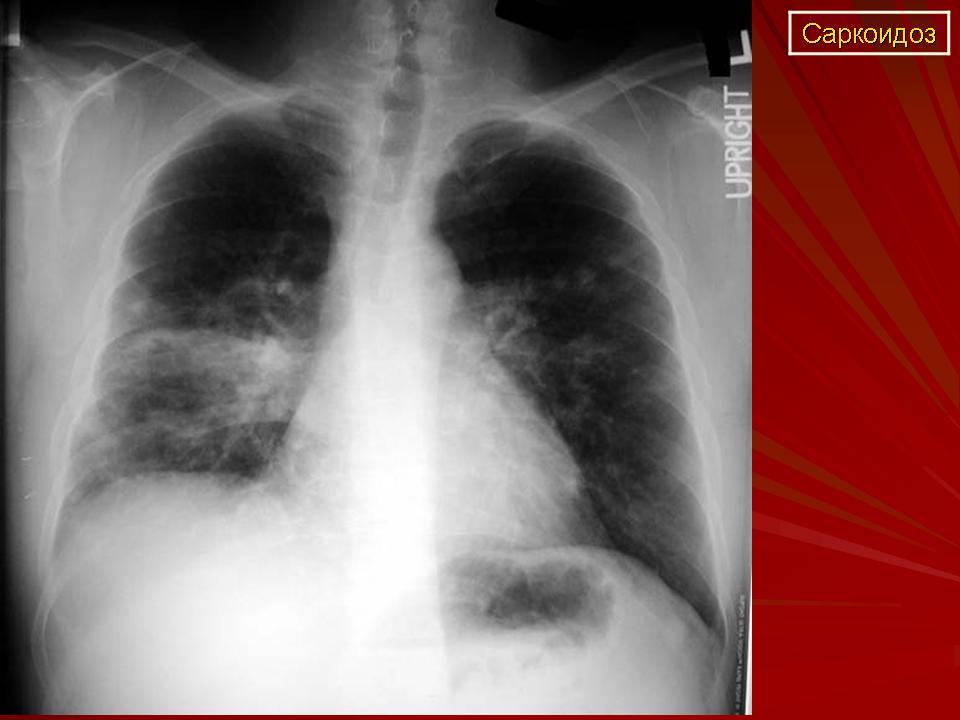 приказ Комитета Здравоохранения Правительства Москвы от 27 мая 2002 г N270). Физиотерапия может применяться в стадии реконвалесценции после гнойных лимфаденитов. Применение физиотерапии при лимфаденопатии неясного генеза опасно и недопустимо.
приказ Комитета Здравоохранения Правительства Москвы от 27 мая 2002 г N270). Физиотерапия может применяться в стадии реконвалесценции после гнойных лимфаденитов. Применение физиотерапии при лимфаденопатии неясного генеза опасно и недопустимо.
Группы периферических лимфоузлов, зоны дренирования и дифференциальный диагноз по локализации.
Увеличение лимфоузлов в некоторых областях поражения чаще связано с определенными болезнями. Увеличение затылочных лимфоузлов обычно вызвано инфекцией кожи головы, краснухой. Одностороннее увеличение передних околоушных лимфоузлов связано с патологией конъюнктивы и век, болезнью кошачьей царапины, эпидемическим кераз’иконыонктивитом и аденовирусной инфекцией. Увеличение подчелюстных и шейных лимфоузлов вызвано инфекцией зубов, десен, щек, гортани и глотки, но может быть проявлением метастаза рака и лимфомы. Увеличение надключичных лимфоузлов I очень серьезный симптом, практически всегда свидетельствующий об опухоли — метастазе рака или лимфомы, располагающихся в грудной клетке или животе (90% у лиц старше 40 лет и 25% у лиц моложе 40 лет).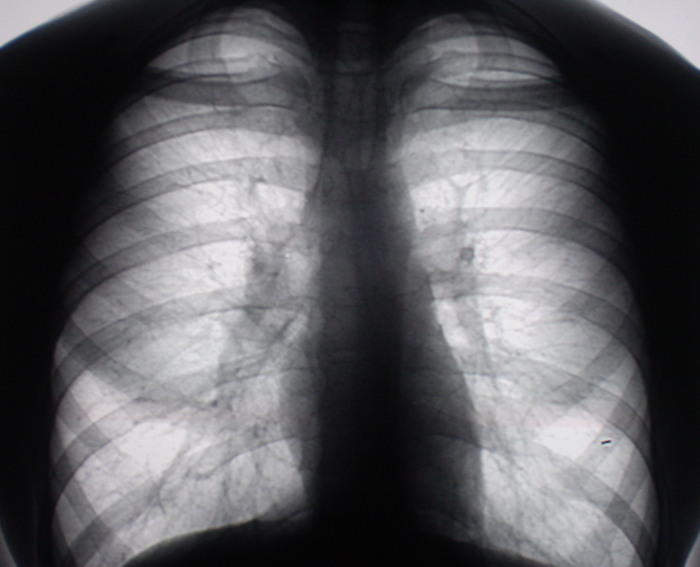 Увеличение надключичного лимфоузла справа обычно вызвано опухолью средостения, легкого, пищевода. К левому лимфатическому узлу лимфа приходит от органов грудной клетки и брюшной полости (Вирховская железа). Его увеличение может быть симптомом опухоли яичников, семенников и предстательной железы, мочевого пузыря, почек, поджелудочной железы, желудка. Нечасто увеличение надключичных лимфоузлов обусловлено воспалительным процессом в грудной клетке и брюшной полости. Увеличение подмышечных и локтевых лимфоузлов может быть вызвано травмой кистей и рук. Увеличение подмышечных и паховых лимфоузлов обычно обусловлено грибковой инфекцией или травмами ног и стоп или инфекцией урогенитальной сферы. Очень редко обнаруживаемый параумбиликальный лимфоузел (узел сестры Джозефины) может быть признаком опухоли органов живота или таза. Суммарные данные локализации лимфоузлов, зоны дренирования и наиболее частые причины увеличения лимфоузлов представлены в Приложении, таблица 8. На практике точное соответствие лимфоузла зоне дренирования не всегда соответствует, поэтому такая таблица носит условный, ориентировочный характер.
Увеличение надключичного лимфоузла справа обычно вызвано опухолью средостения, легкого, пищевода. К левому лимфатическому узлу лимфа приходит от органов грудной клетки и брюшной полости (Вирховская железа). Его увеличение может быть симптомом опухоли яичников, семенников и предстательной железы, мочевого пузыря, почек, поджелудочной железы, желудка. Нечасто увеличение надключичных лимфоузлов обусловлено воспалительным процессом в грудной клетке и брюшной полости. Увеличение подмышечных и локтевых лимфоузлов может быть вызвано травмой кистей и рук. Увеличение подмышечных и паховых лимфоузлов обычно обусловлено грибковой инфекцией или травмами ног и стоп или инфекцией урогенитальной сферы. Очень редко обнаруживаемый параумбиликальный лимфоузел (узел сестры Джозефины) может быть признаком опухоли органов живота или таза. Суммарные данные локализации лимфоузлов, зоны дренирования и наиболее частые причины увеличения лимфоузлов представлены в Приложении, таблица 8. На практике точное соответствие лимфоузла зоне дренирования не всегда соответствует, поэтому такая таблица носит условный, ориентировочный характер.
Перечень заболеваний, протекающих с лимфаденопатией
Перечень болезней, приводящих к увеличению лимфоузлов можно упорядочить по-разному. Некоторые авторы предпочитают классифицировать причины лимфаденопатий по патогенетическому принципу [3,4]. Другие работы носят более практичный характер и ориентированы на дифференциальный диагноз [1,11,12,16,18]. Сравнение перечней болезней и выделяемых авторами групп показывает два основных отличия:
- Перечень причин может быть более или менее подробным. Это особенно касается такого раздела как метастатическое поражение лимфоузлов.
Большинство опухолей может метастатировать в лимфатические лнмфвуэ» лы, поэтому перечень всегда будет неполным
Авторы придерживаются ратной группировки лимфаденошггаш,В‘ЯвОТ» симости от большей направленности на этиологическое или сиидромвлиое подразделение. Так, несколько болезней с неизвестной этиологией незом включаются авторами в разные категории. Например, граиулемяоз- ные лимфадениты относятся к разным категориям. В Приложении,таблица 9, представлены обобщенные данные перечней заболеваний, протекшищпк с лимфаденопатией, созданной на основании анализа литературы и собственного опыта [7]. В списке включены те заболевании, при которых лимфаденопатия может быть предметом дифференциального диагноза.
В Приложении,таблица 9, представлены обобщенные данные перечней заболеваний, протекшищпк с лимфаденопатией, созданной на основании анализа литературы и собственного опыта [7]. В списке включены те заболевании, при которых лимфаденопатия может быть предметом дифференциального диагноза.
Клинические и морфологические особенности лимфаденопатии средостения при гранулематозных заболеваниях легких | Семенова
1. Струков А.И., Кауфман О.Я. Гранулематозное воспаление и гранулематозные болезни. М.: Медицина; 1989.
2. Демихова О.В., Карпина Н.Л., Лепеха Л.Н. и др. Пути оптимизации диагностики и дифференциальной диагностики диссеминированного туберкулеза легких. Вестник Российской академии наук. 2012; 67 (11): 15–21. Доступно на: https://cyberleninka.ru/article/n/puti-optimizatsii-diagnostiki-i-differentsialnoy-diagnostiki-disseminirovannogo-tuberkuleza-legkih/viewer
3. Lescoat A., Lederlin M., Ballerie A. et al. Interstitial lung disease and mediastinal lymph nodes: a computed tomography-based biomarker beyond nosological and etiological borders? Am. J. Respir. Crit. Care Med. 2019; 199 (8): 1038–1040. DOI: 10.1164/rccm.201811-2123LE.
Lescoat A., Lederlin M., Ballerie A. et al. Interstitial lung disease and mediastinal lymph nodes: a computed tomography-based biomarker beyond nosological and etiological borders? Am. J. Respir. Crit. Care Med. 2019; 199 (8): 1038–1040. DOI: 10.1164/rccm.201811-2123LE.
4. Илькович М.М., Новикова Л.Н., Орлова Г.П. Экзогенный аллергический альвеолит. В кн.: Илькович М.М., ред. Диссеминированные заболевания легких. М.: ГЭОТАР-Медиа; 2011: 84–112.
5. Шмелев Е.И. Дифференциальная диагностика интерстициальных болезней легких. Consilium Medicum. 2003; 5 (4): 176–181.
6. Визель А.А., ред. Саркоидоз: от гипотезы к практике. Казань: ФЭН, Академия наук Республики Татарстан; 2004.
7. Miller B.H., Rosado-de-Christenson M.L., Mc Adams H.P., Fishback N.F. Thoracic sarcoidosis: radiologic-pathologic correlation. Radiographics. 1995; 15 (2): 421–437. DOI: 10.1148/radiographics.15.2.7761646.
Miller B.H., Rosado-de-Christenson M.L., Mc Adams H.P., Fishback N.F. Thoracic sarcoidosis: radiologic-pathologic correlation. Radiographics. 1995; 15 (2): 421–437. DOI: 10.1148/radiographics.15.2.7761646.
8. Мотус И.Я., Баженов А.В., Раевская Н.В. и др. Хирургическая диагностика диффузных поражений легких и внутригрудных лимфаденопатий: состояние вопроса. Русский медицинский журнал. 2017; 25 (3): 214–217. Доступно на: https://www.rmj.ru/articles/bolezni_dykhatelnykh_putey/Hirurgicheskaya_diagnostika_diffuznyh_poragheniy_legkih_i_vnutrigrudnyh_limfadenopatiy_Sostoyanie_voprosa/
9. Erbay M., Özsu S., Ayaydın Mürtezaoğlu E.S. et al. [Causes of mediastinal/hilar granulomatous lymphadenitis]. Tuberk. Toraks. 2018; 66 (3): 212–216. (in Turkish).
10. Потанин А.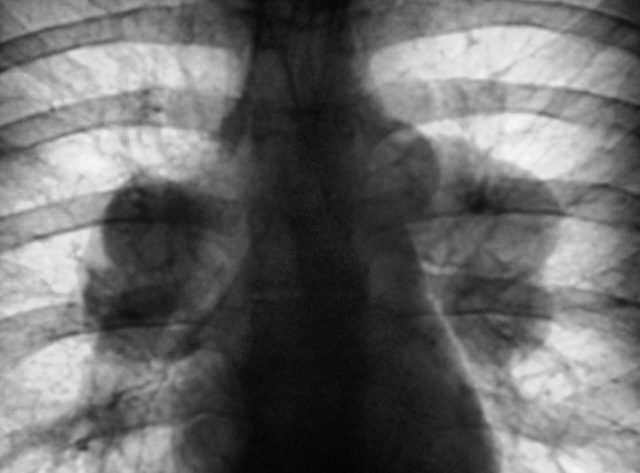 В., Визель И.Ю., Потанин В.П., Визель А.А. Инвазивная диагностика при синдромах внутригрудной лимфаденопатии и диссеминации. Вестник современной клинической медицины. 2011; 4 (3): 56–60. Доступно на: https://cyberleninka.ru/article/n/invazivnaya-diagnostika-pri-sindromah-vnutrigrudnoy-limfadenopatii-i-disseminatsii/viewer
В., Визель И.Ю., Потанин В.П., Визель А.А. Инвазивная диагностика при синдромах внутригрудной лимфаденопатии и диссеминации. Вестник современной клинической медицины. 2011; 4 (3): 56–60. Доступно на: https://cyberleninka.ru/article/n/invazivnaya-diagnostika-pri-sindromah-vnutrigrudnoy-limfadenopatii-i-disseminatsii/viewer
11. Двораковская И.В., Майская М.Ю., Насыров Р.А. и др. Морфологическое исследование в дифференциальной диагностике туберкулеза и саркоидоза. Архив патологии. 2014; 76 (1): 27–31. Доступно на: https://www.mediasphera.ru/issues/arkhiv-patologii/2014/1/030004-1955201415
12. Борисов С.Е. Дифференциальная диагностика саркоидоза. Вестник Научно-исследовательского института фтизиопульмонологии. 1999; (1): 34–45.
13. Терпигорев С.А., Сташук Г.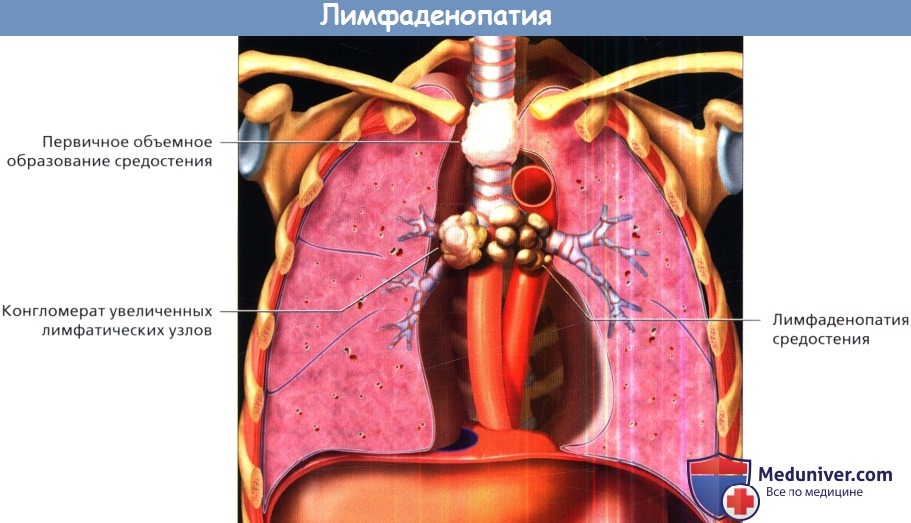 А., Дуброва С.Э. Рентгенологическая семиотика саркоидоза. Клиническая медицина. 2008; 86 (12): 13–18.
А., Дуброва С.Э. Рентгенологическая семиотика саркоидоза. Клиническая медицина. 2008; 86 (12): 13–18.
14. Амосов В.И. Современные компьютерно-томографические признаки саркоидоза органов дыхания и их прогностическое значение. В кн.: Амосов В.И., Сперанская А.А. Лучевая диагностика интерстициальных заболеваний легких. СПб: ЭЛБИ-СПб; 2015: 78–80.
15. Амансахедов Р.Б, Демихова О.В., Лепеха Л.Н. и др. Лучевая семиотика диссеминированного туберкулеза легких. Уральский медицинский журнал. 2018; 8 (163): 10–14.
16. Амансахедов Р.Б, Лимарова И.В., Перфильев А.В. и др. Сравнительный анализ семиотики диссеминированного туберкулеза легких и экзогенного аллергического альвеолита по данным компьютерной томографии. Вестник рентгенологии и радиологии. 2016; 97 (2): 79–84.
17. Дмитриева Л.И., Шмелев Е.И., Степанян И.Э., Сигаев А.Т. Принципы лучевой диагностики интерстициальных заболеваний легких. Пульмонология. 1999; (4): 11–17.
18. Антипова А.В., Лепеха Л.Н., Макарьянц Н.Н. и др. Дифференциальная диагностика диссеминированного туберкулеза легких и экзогенного альвеолита различной природы (по данным морфологического исследования). Туберкулез и болезни легких. 2011; 88 (4): 36–37.
19. Макарьянц Н.Н., Лепеха Л.Н., Шмелев Е.И. и др. Дифференциальная диагностика и лечение различных вариантов экзогенного аллергического альвеолита. Врач. 2013; (2): 7–12.
заболевание легких: причины, симптомы, диагностика и методы лечения на сайте «Альфа-Центр Здоровья»
Системное заболевание легких, характеризующееся образованием гранулем в ткани легких, сопровождается кашлем, болью в грудной клетке, слабостью, повышением температуры.
Саркоидоз — более частое заболевание, чем принято думать. Заболеваемость саркоидозом в мире составляет от 11 до 640 на 100,000 населения. Болезнь развивается в любом возрасте, даже после 70 лет, однако пик заболеваемости приходится на 40 лет. Считалось, что женщины болеют саркоидозом чаще мужчин. Однако, по-видимому, это не так: просто у женщин более выражены симптомы заболевания, а значит, они чаще обращаются к врачам.
Причина саркоидоза не известна, поэтому до сих пор нет исчерпывающего определения заболевания. Основной находкой при нем являются саркоидозные гранулемы (эпителиоидноклеточная гранулема без казеозного некроза).
Жалобы
Более чем в 90% случаев поражены легкие или внутригрудные лимфоузлы, однако жалоб при этом нет, по крайней мере на ранней стадии заболевания. Даже при обширном поражении легких (по данным рентгенографии грудной клетки) может не быть ни одышки, ни кашля. Одышка и другие жалобы обычно появляются на поздней стадии заболевания.
Первым проявлением саркоидоза может стать поражение глаз. Иридоциклит, хориоидит, конъюнктивит и поражение слезных желез с ксерофтальмией (сухостью глаз) отмечаются в 25% случаев. Примерно у 20% больных первым проявлением саркоидоза бывает поражение кожи: бляшки от оранжево-розового до коричневого цвета. Приблизительно у 10% больных страдает нервная система. Саркоидоз можно заподозрить при нарушении функции гипофиза или гиперкальциемии (повышении уровня кальция крови). Кроме того, проявлениями саркоидоза бывают гепатоспленомегалия (увеличение печени и селезенки), поражение костей (чаще фаланг пальцев) и симметричное поражение суставов. Значимая патология сердца встречается редко, но в ряде случаев возникают нарушения ритма сердца, кардиомиопатия. У 10% больных, особенно с обширным поражением лимфоузлов, наблюдается лихорадка.
Стадии
Стадии саркоидоза определяют по данным обзорной рентгенографии грудной клетки.
Стадия I: двустороннее увеличение бронхолегочных лимфоузлов
Стадия II: двустороннее увеличение бронхолегочных лимфоузлов и диффузное поражение легочной паренхимы, сетчатая перестройка легочного рисунка, но иногда множественные очаговые или милиарные тени
Стадия III: поражение легочной паренхимы без увеличения бронхолегочных лимфоузлов
Вероятность спонтанной ремиссии (самостоятельного выздоровления) при стадиях I, II и III составляет 80, 50 и 30% соответственно.
Диагностика
У 90% больных заболевание ограничивается поражением внутригрудных лимфоузлов и легких и часто протекает бессимптомно. В таких случаях рентгенологические изменения могут быть случайной находкой, например при профилактическом осмотре или обследовании по поводу другого заболевания. Как уже сказано, первым проявлением саркоидоза может быть поражение других органов. В любом случае, прежде чем поставить диагноз, врач должен получить гистологическое подтверждение саркоидоза.
Лечение
Несмотря на то что глюкокортикоиды применяют уже более 45 лет, о целесообразности лечения ими саркоидоза легких до сих пор нет единого мнения. Практика показывает, что лечение глюкокортикоидами оправдано у всех больных со стадиями II и III, если в течение 6—12 месяцев не появились признаки спонтанной ремиссии или есть признаки ухудшения (по данным рентгенографии и исследования функции внешнего дыхания). Как правило, достаточно приема 40 мг преднизолона через день
Хотя некоторые специалисты рекомендуют начинать лечение только при появлении жалоб, исследования показали, что одышка появляется в необратимой фазе заболевания. Поэтому глюкокортикоиды лучше назначать до появления жалоб, чтобы предупредить развитие необратимых изменений.
Поэтому глюкокортикоиды лучше назначать до появления жалоб, чтобы предупредить развитие необратимых изменений.
Большинство специалистов придерживаются следующих показаний к назначению глюкокортикоидов: 1) увеит (начинают с местного лечения), 2) гиперкальциемия, 3) поражение миокарда (особенно кардиомиопатия), 4) неврологические нарушения. Если глюкокортикоиды по каким-либо причинам противопоказаны, рекомендуются следующие препараты: метотрексат, хлорохин, азатиоприн и оксифенбутазон.
Наблюдение
Наблюдение за больными саркоидозом обязательно включает регулярную рентгенографию грудной клетки и исследование функции внешнего дыхания (спирометрию). Частота обследования зависит от течения заболевания, а также предпочтений лечащего врача. Течение саркоидоза можно оценить по активности ангиотензин-превращающего фермента в крови. Частота рецидивов после лечения больных со стадиями II и III составляет около 25%. Поэтому по завершении курса лечения за больными нужно наблюдать в течение нескольких лет. Вероятность рецидива значительно снижается, если на протяжении более года состояние остается стабильным и отсутствуют признаки активности саркоидоза.
Вероятность рецидива значительно снижается, если на протяжении более года состояние остается стабильным и отсутствуют признаки активности саркоидоза.
Саркоидоз
«От ложного знания к истинному незнанию» В.Я.Александров
ОПРЕДЕЛЕНИЕ
Системное гранулематозное заболевание, поражающее чаще легкие и внутригрудные лимфатические узлы.Саркоидоз лимфатического узла
Саркоидозная гранулема грудного лимфоузла.
КЛИНИКА
• Одышка.• Кашель сухой.
• Торакалгия.
• Утомляемость.
• Снижение массы тела.
• Ночная потливость.
Синдромы
• Lofgren: узловатая эритема, двустороння прикорневая лимфаденопатия, полиартрит.
• Lupus pernio: плотные бляшки красноватого цвета на на носу, щеках, губах и ушах.
• Heerfordt: паралич лицевого нерва, увеличение слюнных желез, передний увеит, лихорадка.
Рентгенография грудной клетки
ДИАГНОСТИКА (ATS)
• Рентгенография грудной клетки: двусторонняя прикорневая лимфаденопатия, усиление легочного рисунка, инфильтрация диффузная или верхней доли.
• Мультиспиральная компьютерная томография: увеличение лимфоузлов средостения и корней легких, мелкоочаговая диссеминация, интерстициальные изменения.
• Трансбронхиальная тонкоигольная аспирация лимфоузлов корня легких, средостения под контролем эндобронхиальной сонографии: при наличии клиники и целесообразности.
• Офтальмоскопия: увеит, неврит зрительного нерва.
• Общий анализ крови: анемия, лейкопения, лимфопения, тромбоцитопения.
• Повышение креатинина, щелочная фосфатаза >3 норм, гиперкальциемия.
• Электрокардиограмма: нарушения проведения, желудочковые аритмии.
• Магнитнорезонансная томография сердца с гадолиниевым усилением (предпочтительнее): миокардит.
• Эхокардиография: дисфункция левого желудочка, легочная гипертензия.
• Холтеровское мониторирование: аритмии.
• Сонография почек: кальциевые камни, кальциноз.
• Туберкулиновая проба (Манту).
РЕНТГЕНОЛОГИЧЕСКИЕ СТАДИИ
• 0 стадия: нет изменений.
• I стадия: двусторонняя прикорневая лимфаденопатия.
• II стадия: лимфаденопатия + легочные инфильтраты.
• III стадия: легочные инфильтраты без лимфаденопатии.
• IV стадия: легочной фиброз.
Передний увеит
Передний гранулематозный увеит.
ВНЕЛЕГОЧНОЙ САРКОИДОЗ
• Узловатая эритема, бляшки на коже.• Миокардит, сердечная недостаточность, блокада атриовентрикулярная/внутрижелудочковая, желудочковая тахикардия, внезапаная сердечная смерть.
• Артрит мигрирующий, с периатртитом.
• Передний увеит.
• Поражение почек, нефрокальциноз, нефролитиаз.
• Поражения центральной и периферической нервной системы.
Компьютерная томография
Двусторонние мелкие очаги, лимфаденопатия.
ФОРМУЛИРОВКА ДИАГНОЗА
□ Саркоидоз внутригрудных лимфоузлов и легких, ДН II ст.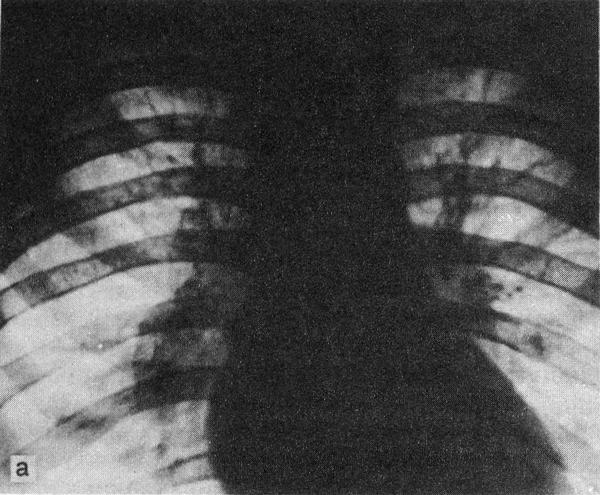 [D86.2]
[D86.2] □ Саркоидный миокардит, АВ блокада 2 степени тип II, сердечная недостаточность. [I41.8]
ЛЕЧЕНИЕ
• На I–II стадиях не показано (спонтанное разрешение 40–90%).• Преднизолон 20–40 мг/сут 4–6 нед с постепенным снижением дозы на 5 мг за 6–8 нед, 5–10 мг/сут длительно до 12–24 мес.
• Гидроксихлорохин 200–400 мг/сут.
• Метотрексат 5–15 мг/сут, азатиоприн 50–200 мг/сут, лефлуномид 10–20 мг/сут, инфликсимаб.
• Трансплантация легких.
Атипичные проявления саркоидоза органов дыхания: клинические наблюдения
Авторы: В.К. Гаврисюк, д.м.н., профессор, Г.Л. Гуменюк, к.м.н., Е.А. Меренкова, к.м.н., О.В. Страфун, к.м.н., Н.С. Шкуренко, О.В. Быченко, ГУ «Национальный институт фтизиатрии и пульмонологии им. Ф.Г. Яновского НАМН Украины», г. Киев
Атипичные изменения внутригрудных лимфатических узлов и паренхимы легких при компьютерной томографии (КТ) больных саркоидозом органов дыхания в большинстве случаев сочетаются с классическими высокоспецифичными симптомами, в связи с чем не создают особых трудностей для диагностики. Однако примерно в 2% случаев атипичные КТ-симптомы являются единственными проявлениями заболевания, что обусловливает необходимость применения дополнительных методов диагностики.
Однако примерно в 2% случаев атипичные КТ-симптомы являются единственными проявлениями заболевания, что обусловливает необходимость применения дополнительных методов диагностики.
Частота бессимптомного течения саркоидоза органов дыхания составляет в среднем от 30% (II-III стадии) до 80% (I стадия) случаев. При этом клинические проявления саркоидоза (сухой кашель, одышка, общая слабость, повышение температуры тела) являются неспецифичными, в связи с чем их присутствие не позволяет не только диагностировать, но даже заподозрить наличие саркоидоза.
По этой причине международное положение Statement on Sarcoidosis, опубликованное в 1999 году [1], предусматривало обязательную верификацию диагноза с помощью патогистологических методов исследования. Однако за 16 лет, прошедших от момента опубликования Положения, диагностические возможности КТ органов грудной полости возросли настолько, что, по результату морфологической диагностики интерстициальных заболеваний легких, КТ в настоящее время успешно конкурирует с методами патогистологического исследования.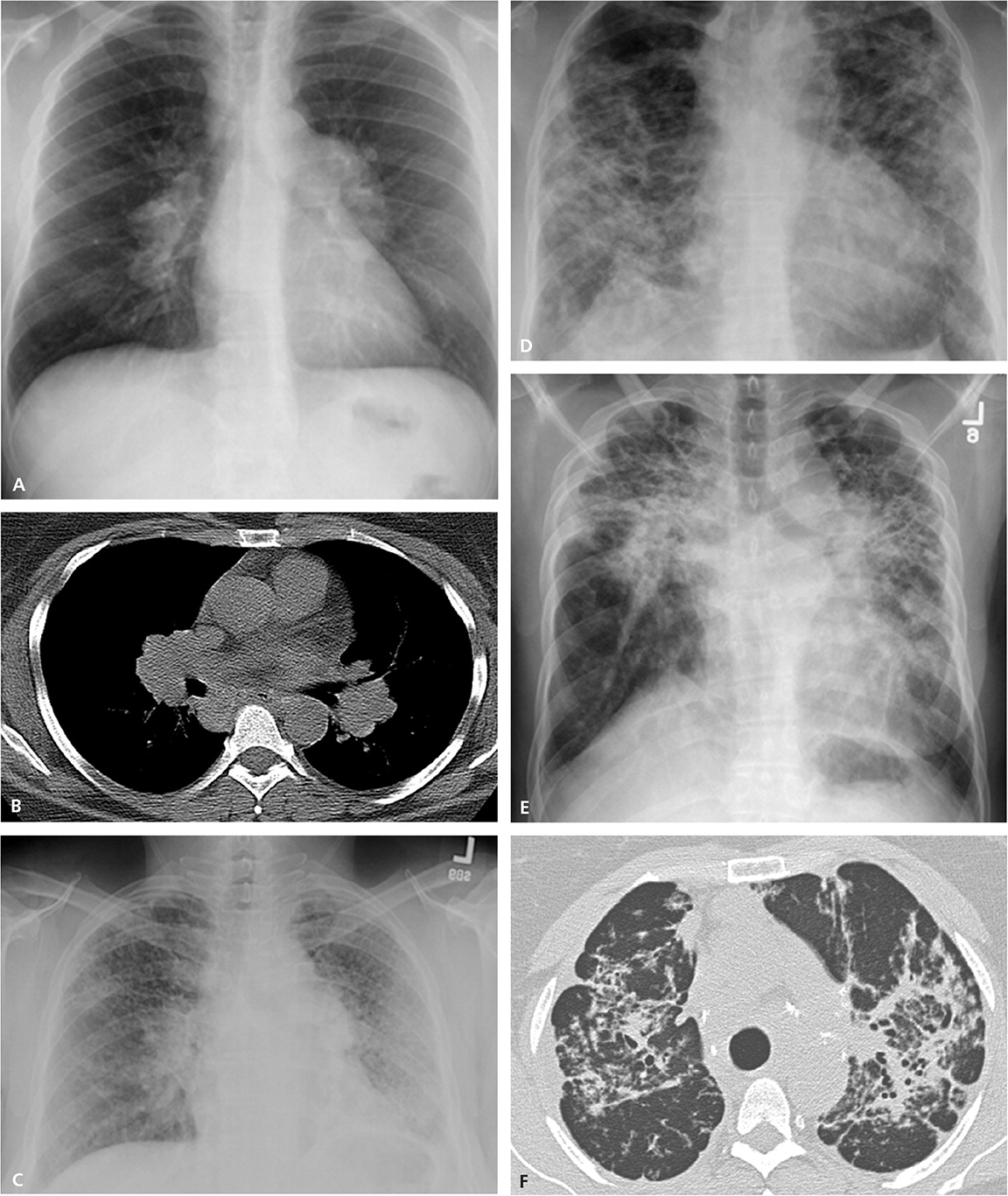 В связи с этим в Унифицированном клиническом протоколе «Саркоидоз» (приказ МЗ Украины от 08.09.2014 № 634) [2] показания к проведению биопсии легкого с целью верификации диагноза значительно сужены – биопсия показана только при наличии весомых оснований для исключения лимфаденопатии или легочной диссеминации другого происхождения.
В связи с этим в Унифицированном клиническом протоколе «Саркоидоз» (приказ МЗ Украины от 08.09.2014 № 634) [2] показания к проведению биопсии легкого с целью верификации диагноза значительно сужены – биопсия показана только при наличии весомых оснований для исключения лимфаденопатии или легочной диссеминации другого происхождения.
Необходимо отметить, что даже качественно выполненная рентгенография органов грудной полости позволяет уверенно диагностировать саркоидоз примерно в 80% случаев – именно с такой частотой у больных саркоидозом органов дыхания встречается двусторонняя прикорневая лимфаденопатия (ДПЛ) [1, 3]. Если учесть, что симметричная ДПЛ у больных с лимфомами наблюдается только в 3,8% случаев, при бронхогенной карциноме – в 0,8%, при злокачественных опухолях экстраторакальной локализации – в 0,2% [4], а дифференциальная диагностика с бронхоаденитом туберкулезной этиологии не представляет особых трудностей, то можно заключить, что рентгенологический симптомокомплекс ДПЛ является в высшей степени специфичным для саркоидоза.
Вместе с тем возможности рентгенографии в диагностике саркоидозного поражения паренхимы легких весьма ограниченны, в связи с чем все больные с подозрением на саркоидоз органов дыхания должны быть обследованы методом КТ высокого разрешения.
В таблице представлены современные критерии КТ-диагностики саркоидоза органов дыхания [5], которые подразделяются на классические и атипичные.
К классическим относятся симптомы, характерные для саркоидоза и редко наблюдаемые при других заболеваниях. Например, симптомокомплекс ДПЛ наблюдается у 80% больных саркоидозом и только у 4% пациентов с лимфомами. И наоборот, атипичные изменения чаще характерны для других заболеваний органов грудной полости и редко встречаются при саркоидозе.
Например, лимфаденопатия передних медиастинальных узлов характерна для лимфогранулематоза и редко встречается при саркоидозе.
Атипичные КТ-признаки в большинстве случаев сочетаются с классическими высокоспецифичными симптомами. Однако в редких случаях атипичные КТ-симптомы являются единственными проявлениями заболевания, что обусловливает значительные трудности в диагностике саркоидоза.
Клинический случай 1
Пациентка М., 1963 года рождения, направлена в Национальный институт фтизиатрии и пульмонологии (НИФП) им. Ф.Г. Яновского для уточнения диагноза.
Жалобы на умеренно выраженный сухой кашель, субфебрильную температуру тела, умеренную общую слабость и повышенную утомляемость.
Считает себя больной на протяжении трех месяцев. Начало заболевания малозаметное – появился незначительный сухой кашель, затем стала беспокоить общая слабость, повышенная утомляемость, через некоторое время появилась субфебрильная температура. Безуспешно самостоятельно лечилась антибиотиками и муколитическими средствами.
При рентгенографии была выявлена правосторонняя прикорневая лимфаденопатия, для уточнения диагноза больная была направлена в НИФП.
Хронических заболеваний органов дыхания в анамнезе нет. Не курит, работа с неблагоприятными производственными факторами не связана.
Кожа и периферические лимфатические узлы без изменений. Аускультативно: дыхание везикулярное, хрипов нет.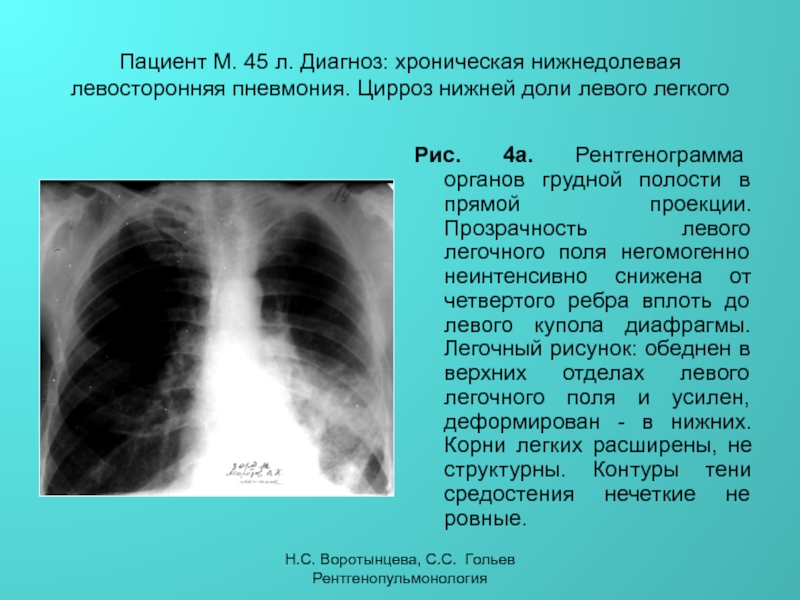 Тоны сердца ритмичные, звучные. ЧСС – 84 уд/мин. АД – 130/80 мм рт. ст. Тоны сердца ритмичные, звучные. Живот мягкий, при пальпации безболезненный. Периферические отеки не определяются. Другие органы и системы – без видимой патологии.
Тоны сердца ритмичные, звучные. ЧСС – 84 уд/мин. АД – 130/80 мм рт. ст. Тоны сердца ритмичные, звучные. Живот мягкий, при пальпации безболезненный. Периферические отеки не определяются. Другие органы и системы – без видимой патологии.
Клинический анализ крови: Hb – 122 г/л, эритроциты – 4,1×1012/л, лейкоциты – 11,4×109/л, СОЭ – 61 мм/ч.
Уровень ионизированного кальция в крови: 1,37 ммоль/л – гиперкальциемия (норма до 1,32 ммоль/л).
Многосрезовая КТ (МСКТ) органов грудной полости: правосторонняя прикорневая лимфаденопатия (рис. 1 слева) в сочетании с увеличением бифуркационных и нижних паратрахеальных узлов справа; мелкоузелковая диссеминация преимущественно в средних и верхних легочных полях.
Показатели легочной вентиляции в норме, снижение диффузионной способности легких (DLCO) – 66,6% от должного.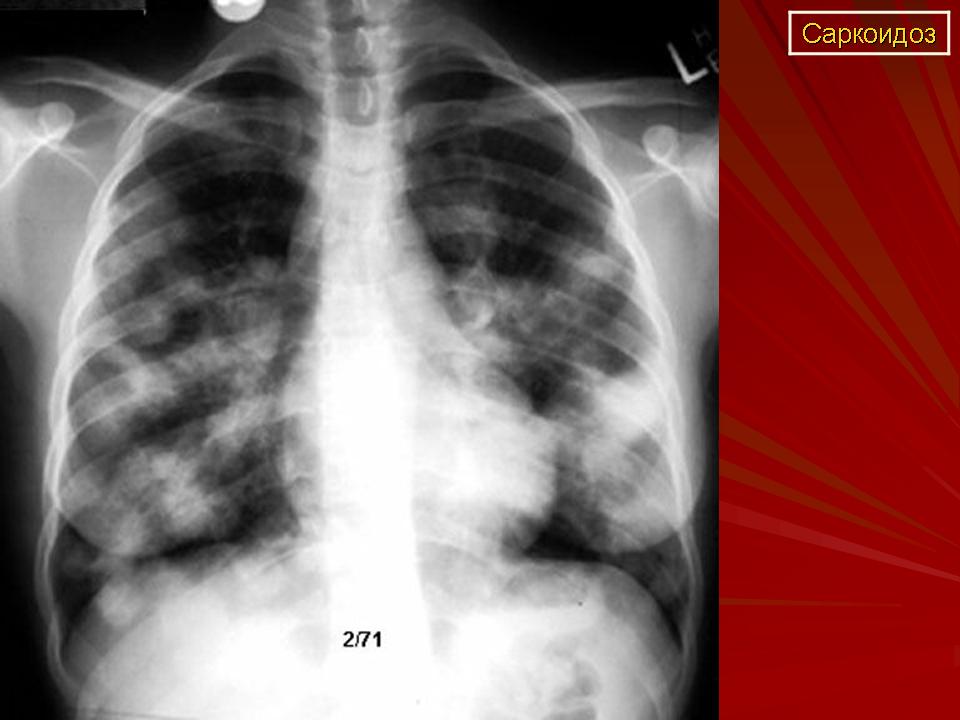
Учитывая то, что атипичное проявление саркоидоза (односторонняя прикорневая лимфаденопатия) сочеталось с гиперкальциемией и классическими КТ-изменениями (увеличение бифуркационных и нижних паратрахеальных узлов справа, микроузелковый паттерн легочной диссеминации), больной без применения дополнительных методов исследования был установлен диагноз: саркоидоз органов дыхания, впервые выявленный, II стадия. Назначена терапия метилпреднизолоном в дозе 0,4 мг/кг массы тела в течение 8 недель с последующим снижением дозы до 0,2 мг/кг к концу третьего месяца.
На втором визите через 3 мес лечения: субъективные проявления заболевания исчезли; СОЭ – 18 мм/ч; уровень кальция в крови – 1,28 ммоль/л; DLCO – 74,5% от должного.
МСКТ: отмечается регрессия прикорневой лимфаденопатии (рис. 1 справа), уменьшение бифуркационных и нижних паратрахеальных узлов справа, сохраняется необильная мелкоузелковая диссеминация.
Диагноз: саркоидоз органов дыхания, II стадия, фаза регрессии.
Пациентке рекомендовано продолжение лечения метилпреднизолоном в режиме постепенного снижения дозы до 0,1 мг/кг к третьему визиту (конец 6-го месяца).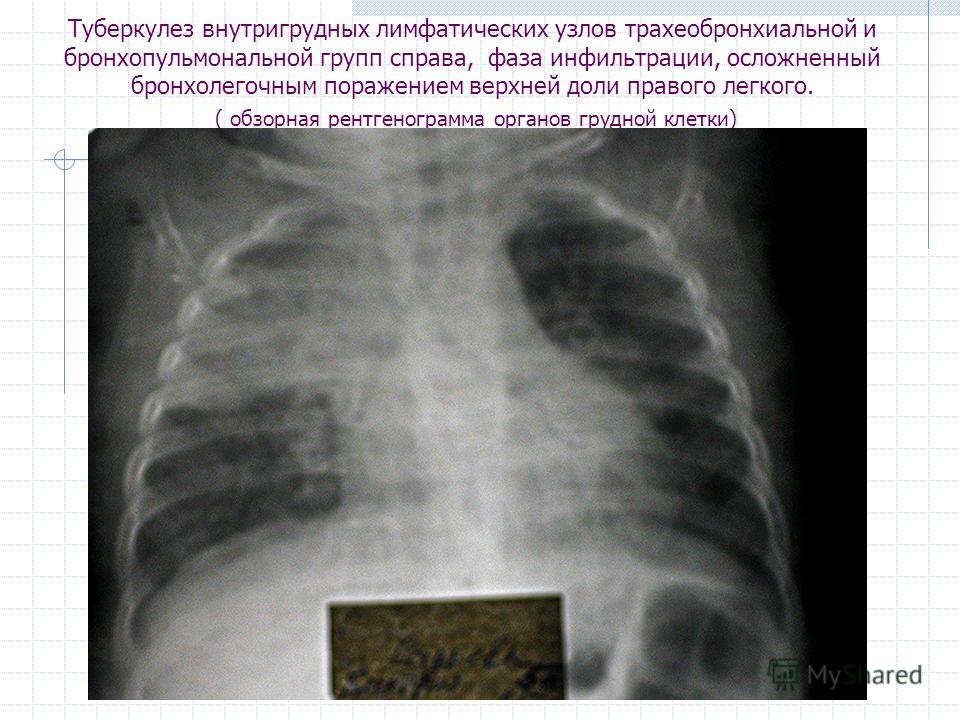
Клинический случай 2
Пациент П., 1993 года рождения, направлен в НИФП для уточнения диагноза после проведения профилактического рентгенологического исследования, на котором были выявлены патологические изменения легких и внутригрудных лимфатических узлов.
Жалоб нет. В анамнезе острые респираторные вирусные инфекции, хронических заболеваний внутренних органов не отмечает. Не курит, в контакте с неблагоприятными производственными факторами не работал.
При объективном обследовании: кожа обычной окраски, без высыпаний, периферические лимфатические узлы не увеличены. Аускультативно: дыхание везикулярное, хрипов нет. ЧСС – 64 уд/мин, АД – 110/70 мм рт. ст. Тоны сердца ритмичные, звучные. Другие органы и системы без видимой патологии.
МСКТ: значительное увеличение передних медиастинальных (рис. 2, слева) и бронхопульмональных (рис. 3, слева) лимфатических узлов. Билатерально в легких определяется мелкоузелковая диссеминация преимущественно в верхних и средних отделах с распределением узелков вдоль бронхо-сосудистых пучков.
Рис. 3. МСКТ больного П., слева – первичное обследование: мелкоузелковая диссеминация паренхимы легких, увеличение прикорневых лимфатических узлов; справа – после трехмесячного периода наблюдения: регрессия лимфаденопатии, сохраняется мелкоузелковая диссеминация. Рис. 4. МСКТ больного К., слева – первичное обследование: диффузное снижение прозрачности паренхимы легких по типу «матового стекла», плотность паренхимы: –609 HU; увеличение прикорневых лимфатических узлов; справа – через 12 мес лечения: повышение прозрачности паренхимы, плотность паренхимы: –683 HU; регрессия лимфаденопатии. Рис. 5. МСКТ больного К. (фрагмент среза правого легкого в режиме увеличения), слева – первичное обследование: интенсивное диффузное снижение прозрачности паренхимы легких по типу «матового стекла»; справа – через 12 мес лечения: повышение прозрачности паренхимы, на срезе более отчетливо дифференцируется легочный рисунок.
При бодиплетизмографии отмечено незначительное уменьшение общей емкости и остаточного объема легких, показатели кривой форсированного выдоха в пределах нормы. DLCO – 72,7%.
Содержание кальция в крови – 1,31 ммоль/л.
В данном случае атипичное проявление (увеличение передних медиастинальных лимфатических узлов) также сочеталось с высокоспецифичными КТ-признаками саркоидоза (ДПЛ, микроузелковый паттерн диссеминации с распределением узелков вдоль бронхо-сосудистых пучков). Кроме того, отсутствовали клинические проявления лимфопролиферативного заболевания. В связи с этим больному без проведения дополнительных методов исследования был установлен диагноз: саркоидоз органов дыхания, впервые выявленный, II стадия.
Учитывая отсутствие клинических проявлений, изменений функции дыхания, нормальный уровень кальция в крови, лечение не назначалось, больному было рекомендовано контрольное обследование через 3 месяца.
При повторном обследовании на МСКТ органов грудной полости констатирована регрессия медиастинальной (рис. 2 справа) и прикорневой (рис. 3 справа) лимфаденопатии, при этом сохранялась мелкоузелковая диссеминация паренхимы. В соответствии с клиническим протоколом противовоспалительная терапия не назначалась, больному было рекомендовано очередное обследование через 3 месяца.
2 справа) и прикорневой (рис. 3 справа) лимфаденопатии, при этом сохранялась мелкоузелковая диссеминация паренхимы. В соответствии с клиническим протоколом противовоспалительная терапия не назначалась, больному было рекомендовано очередное обследование через 3 месяца.
Клинический случай 3
Пациент К., 1977 года рождения, поступил в отделение интерстициальных заболеваний легких НИФП с жалобами на одышку при незначительной физической нагрузке (ходьбе по ровной местности), сухой кашель, выраженную общую слабость, повышенную утомляемость.
Заболевание началось три года назад без очевидных причин с малозаметной одышки, которая медленно прогрессировала. Периодически отмечался сухой кашель. На протяжении последних двух месяцев одышка значительно усилилась, появилась выраженная общая слабость, в связи с чем впервые обратился к врачу.
В анамнезе частые ОРВИ, трижды болел пневмонией. Не курит. Работал водителем дальних рейсов, строителем.
Объективно: одышки в покое и при разговоре нет. Частота дыхания – 22 в 1 мин. При аускультации дыхание с жестким оттенком, над базальными отделами билатерально – крепитирующие хрипы. ЧСС – 104 уд/мин, АД – 130/90 мм рт. ст. Тоны сердца ритмичны, приглушены. Другие органы и системы при физикальном обследовании без изменений.
Частота дыхания – 22 в 1 мин. При аускультации дыхание с жестким оттенком, над базальными отделами билатерально – крепитирующие хрипы. ЧСС – 104 уд/мин, АД – 130/90 мм рт. ст. Тоны сердца ритмичны, приглушены. Другие органы и системы при физикальном обследовании без изменений.
СОЭ – 15 мм/ч, содержание кальция в крови в пределах нормы (1,29 ммоль/л).
МСКТ (рис. 4 слева): диффузное снижение прозрачности паренхимы легких по типу «матового стекла», небольшое увеличение бронхопульмональных лимфатических узлов с обеих сторон.
Функция внешнего дыхания: значительное уменьшение общей (44,7%) и жизненной (31,6%) емкости легких, резкое снижение диффузионной способности легких (DLCO – 22,6%).
Газовый состав крови: выраженная гипоксемия (РаО2 – 44 мм рт. ст., SaO2 – 82%).
Анализ результатов обследования не позволил уверенно предположить характер заболевания, при этом диагноз саркоидоза представлялся маловероятным по следующим причинам.
Симптом «матового стекла» без наличия мелкоузелковой диссеминации относится к перечню атипичных КТ-признаков саркоидоза и является не следствием альвеолита, а результатом атипичного диффузного распределения гранулем в интерстиции.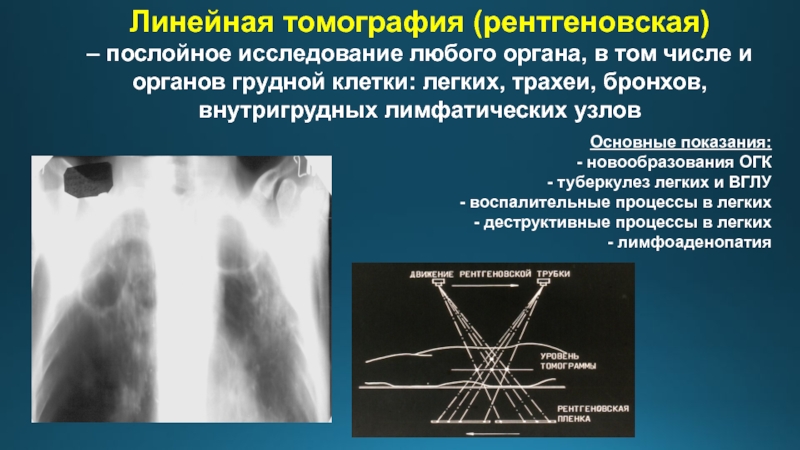 Однако при саркоидозе феномен «матового стекла» обычно представлен отдельными изолированными участками, а в нашем случае наблюдалось диффузное снижение прозрачности паренхимы, что при саркоидозе встречается крайне редко.
Однако при саркоидозе феномен «матового стекла» обычно представлен отдельными изолированными участками, а в нашем случае наблюдалось диффузное снижение прозрачности паренхимы, что при саркоидозе встречается крайне редко.
Двустороннее небольшое увеличение бронхопульмональных лимфатических узлов также имело сомнительную диагностическую ценность, поскольку при саркоидозе прикорневая лимфаденопатия обычно выражена в значительно большей степени.
Кроме того, клинические и функциональные симптомы тяжелой респираторной недостаточности несовместимы с диагнозом саркоидоза II стадии, они характерны для IV стадии заболевания – распространенного пневмосклероза.
Наиболее вероятным был диагноз: гиперсенситивный пневмонит неустановленной природы, хроническая форма. При этом заболевании КТ-признаки диффузного снижения прозрачности паренхимы в виде «матового стекла» в сочетании с умеренной и тяжелой респираторной недостаточностью наблюдаются достаточно часто.
Вместе с тем диагноз требовал верификации. С этой целью пациенту была проведена видеоторакоскопия с биопсией паренхимы легких и внутригрудного лимфатического узла. При патогистологическом исследовании выявлены эпителиоидноклеточные гранулемы, характерные для саркоидоза.
С этой целью пациенту была проведена видеоторакоскопия с биопсией паренхимы легких и внутригрудного лимфатического узла. При патогистологическом исследовании выявлены эпителиоидноклеточные гранулемы, характерные для саркоидоза.
Таким образом, больному был установлен диагноз: саркоидоз органов дыхания, впервые выявленный, II стадия, легочная недостаточность II степени.
Больному был назначен метилпреднизолон по 24 мг/сут на протяжении 4 нед с последующим снижением дозы по схеме до 12 мг к концу 3-го месяца. Однако пациент самостоятельно снизил дозу до 2 мг/сут. При обследовании на визите 2 через 3 мес клиническая картина заболевания и КТ-семиотика сохранялись на прежнем уровне, в связи с чем доза метилпреднизолона была увеличена до 16 мг/сут на протяжении 4 нед с постепенным ее снижением до 8 мг/сут к концу 6-го месяца. Однако и на третьем визите (6 мес) улучшения клинического состояния больного и признаков регрессии изменений в легких при КТ-исследовании не наблюдалось. Дополнительно к лечению метилпреднизолоном (8 мг/сут) назначен гидроксихинолин по 200 мг 2 раза в сутки.
На визите 4 (12 мес) выявлены признаки регрессии саркоидоза – уменьшение бронхопульмональных лимфатических узлов и повышение прозрачности паренхимы (рис. 4 справа), при этом на фоне «матового стекла» стали отчетливо дифференцироваться бронхо-сосудистые структуры (рис. 5 справа). При исследовании функции внешнего дыхания отмечено увеличение жизненной емкости легких (35,6%), вместе с тем диффузионная способность сохранялась на крайне низком уровне (21,8%).
Результаты газового состава крови свидетельствовали о существенном уменьшении степени артериальной гипоксемии (РаО2 – 57 мм рт. ст., SaO2 – 89%).
Вместе с тем темпы регрессии патологического процесса были явно недостаточны – сохранялось значительное снижение прозрачности паренхимы легких, были крайне низкими показатели легочной вентиляции и диффузии. В связи с этим больному была назначена иммуносупрессивная терапия метотрексатом по 10 мг/нед в комбинации с фолиевой кислотой на фоне лечения метилпреднизолоном, рекомендовано наблюдение пульмонологом по месту жительства с целью мониторинга возможных побочных эффектов терапии и контрольное обследование в НИФП через 3 месяца.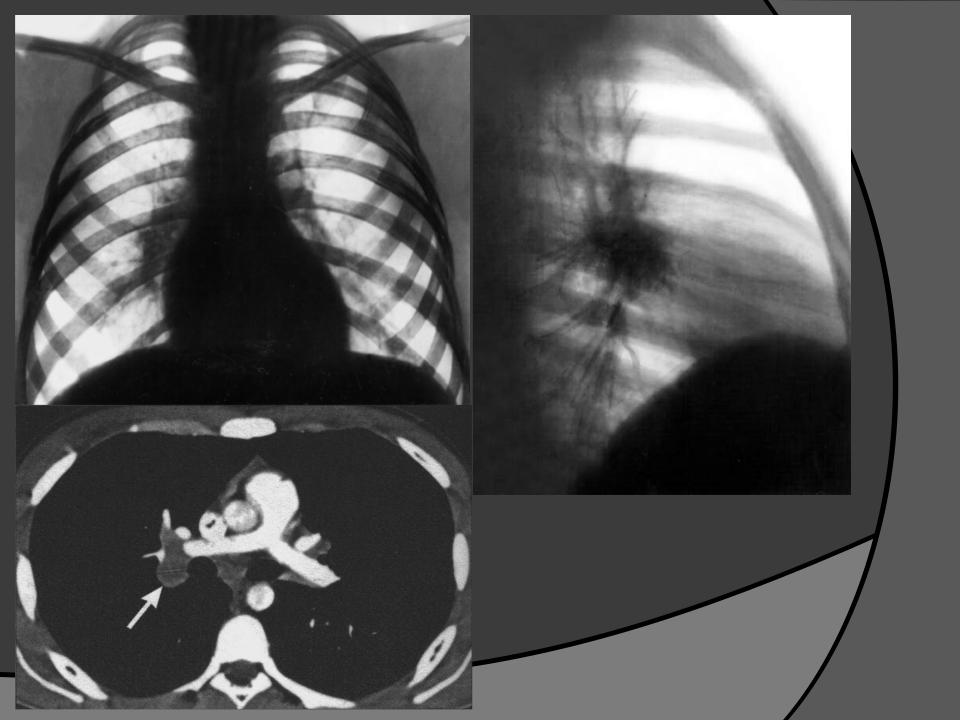
Заключение
По нашим данным, атипичные проявления саркоидоза при КТ органов грудной полости в группе больных с поражением паренхимы наблюдаются с частотой от 0,7% (односторонняя прикорневая лимфаденопатия) до 36,5% (сluster-симптом – скопление микроузелков в виде куста или грозди). При этом классические высокоспецифичные симптомы регистрируются значительно чаще – от 67,1% (перилимфатическое распределение узелков) до 91,1% (ДПЛ). В связи с этим атипичные признаки, как правило, сочетаются с классическими (случаи 1 и 2) и не создают особых трудностей для диагностики. Однако примерно в 2% случаев атипичные КТ-симптомы являются единственными проявлениями заболевания, что иллюстрирует случай 3. Это обусловливает необходимость применения методов трансбронхиальной или хирургической биопсии.
Литература
1. American Thoracic Society (ATS), European Respiratory Society (ERS), World Association of Sarcoidosis and Other Granulomatous Disoders (WASOG).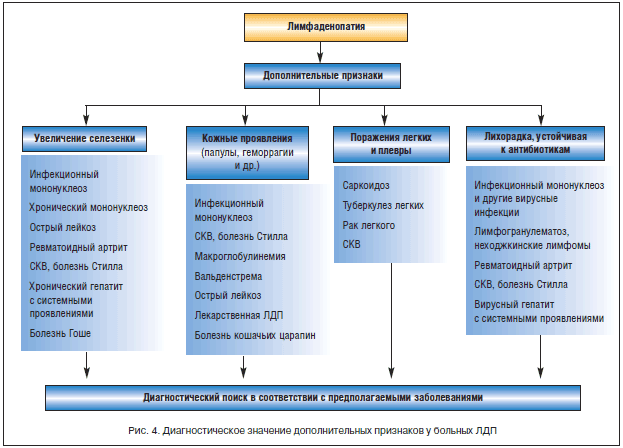 Statement on Sarcoidosis // Am. J. Respir. Crit. Care Med. – 1999. – Vol. 160. – P. 736-755.
Statement on Sarcoidosis // Am. J. Respir. Crit. Care Med. – 1999. – Vol. 160. – P. 736-755.
2. Уніфікований клінічний протокол первинної, вторинної (спеціалізованої) та третинної (високоспеціалізованої) медичної допомоги «Саркоїдоз» // Наказ МОЗ України № 634 від 08.09.2014.
3. Nunes H. Imaging of sarcoidosis of the airways and lung parenchyma and correlation with lung function / H. Nunes, Yu. Uzunhan, T. Gille et al. // Eur. Respir. J. – 2012. – Vol. 40. – P. 750-765.
4. Winterbauer R.H. Clinical interpretation of bilateral hilar adenopathy / R.H. Winterbauer, N. Belik, K.D. Moores // Ann. Intern. Med. – 1973. – Vol. 78. – P. 65-71.
5. Veltkamp M. The pulmonary manifestations of sarcoidosis / M. Veltkamp, J.C. Grutters // Pulmonary sarcoidosis. M.A. Judson Editor. – Humana Press – brand of Springer, 2014. – P. 19-40.
СТАТТІ ЗА ТЕМОЮ Пульмонологія та оториноларингологія
01.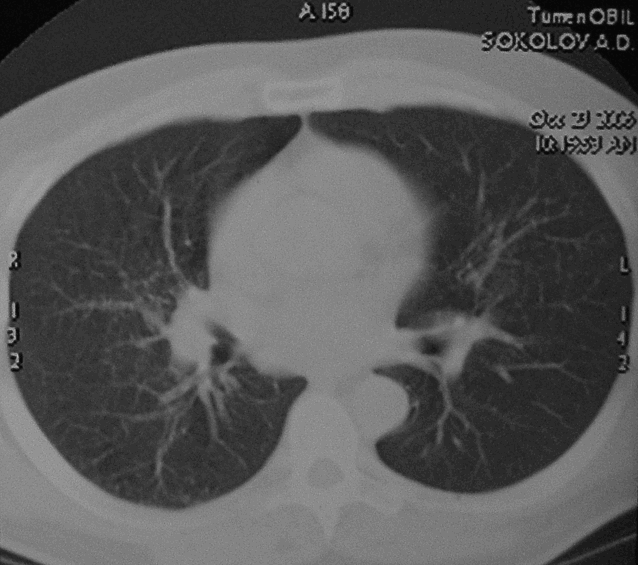 03.2021
Пульмонологія та оториноларингологія Негоспітальна пневмонія: діагностика та лікування
03.2021
Пульмонологія та оториноларингологія Негоспітальна пневмонія: діагностика та лікуванняМинулого року проводилося доволі багато різноманітних онлайн-заходів: конференції та клінічні розбори, відкриті дискусії та симпозіуми, які сприяли подальшому професійному розвитку лікарів, а також відкрили новий формат наукового спілкування. Однією з найвідоміших інтернет-подій став Міжнародний віртуальний конгрес для отоларингологів і лікарів первинної ланки – EPOS2020. Новітній формат, насичена наукова програма, розподіл на два окремих потоки для ЛОР-лікарів і представників первинної допомоги, виступи провідних фахівців – зіркові ознаки та характерні риси EPOS2020….
02. 02.2021
Пульмонологія та оториноларингологія Новини оториноларингології: сучасні підходи до діагностики та лікування ЛОР-захворювань
02.2021
Пульмонологія та оториноларингологія Новини оториноларингології: сучасні підходи до діагностики та лікування ЛОР-захворюваньМинулого року в грудні відбувся «Міжнародний віртуальний конгрес для отоларингологів і лікарів первинної ланки», під час якого розглядалися питання щодо діагностики й лікування патологій носа, глотки та вуха. У заході взяли участь провідні спеціалісти України й інших країн. Найцікавіші доповіді висвітлено в цьому огляді….
27. 01.2021
Пульмонологія та оториноларингологія
Терапія та сімейна медицина Цефдінір у лікуванні інфекцій дихальних шляхів: ефективність, безпечність, зручність застосування
01.2021
Пульмонологія та оториноларингологія
Терапія та сімейна медицина Цефдінір у лікуванні інфекцій дихальних шляхів: ефективність, безпечність, зручність застосуванняУ цій статті розглянуті особливості застосування цефалоспорину ІІІ покоління – цефдініру в лікуванні таких респіраторних інфекцій, як позалікарняна пневмонія (ПЛП), загострення хронічного бронхіту (ЗХБ), гострий середній отит, фарингіт, тонзиліт і гострий бактеріальний риносинусит (ГБРС). Представлені дані клінічних досліджень з ефективності цефдініру та результати порівняльних випробувань препарату з фторхінолонами, пеніцилінами, а також з іншими цефалоспоринами. …
27.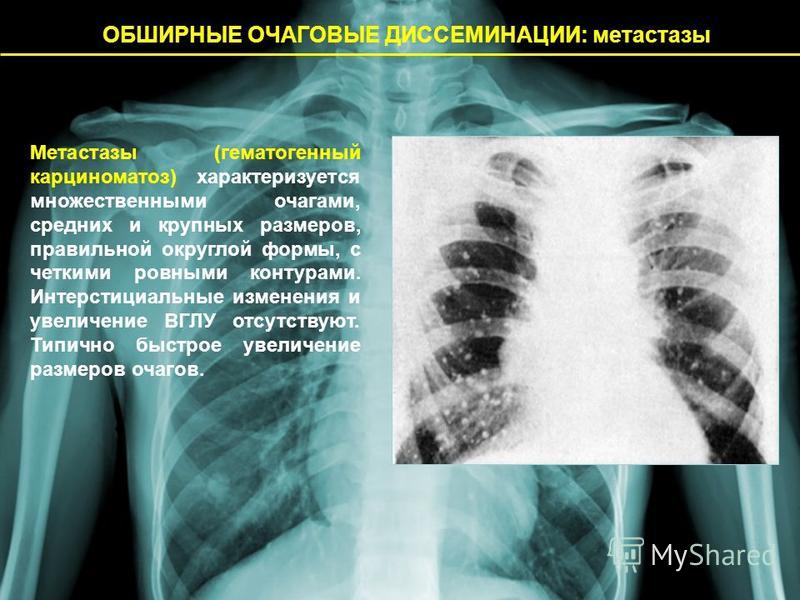 01.2021
Алергія та імунологія
Пульмонологія та оториноларингологія
Терапія та сімейна медицина GINA-2020: що нового? Global Initiative for Asthma, перегляд 2020 р.
01.2021
Алергія та імунологія
Пульмонологія та оториноларингологія
Терапія та сімейна медицина GINA-2020: що нового? Global Initiative for Asthma, перегляд 2020 р.Бронхіальна астма (БА) – гетерогенне захворювання, що зазвичай характеризується хронічним запаленням дихальних шляхів. Діагностується за наявності в анамнезі респіраторних симптомів, таких як свистячі хрипи, задишка, стиснення в грудях і кашель, які змінюються з часом та за інтенсивністю, а також нестійкого обмеження повітряного потоку на видиху….
Рак прямой кишки
Вам поставили диагноз: рак прямой кишки?
Наверняка Вы задаётесь вопросом: что же теперь делать?
Подобный диагноз всегда делит жизнь на «до» и «после».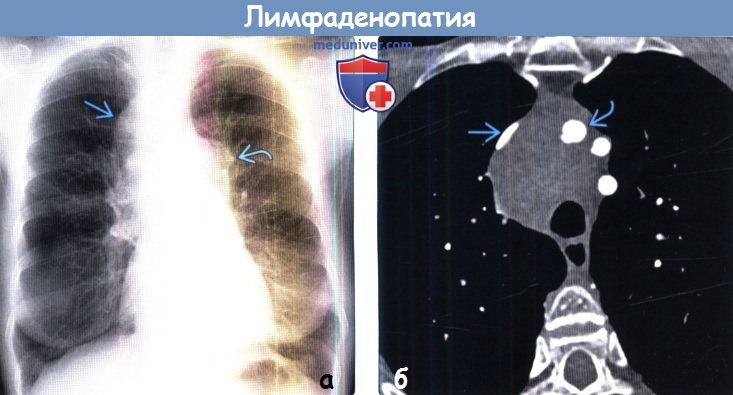 Все эмоциональные ресурсы пациента и его родных брошены на переживания и страх. Но именно в этот момент необходимо изменить вектор «за что» на вектор «что можно сделать».
Очень часто пациенты чувствуют себя безгранично одинокими вначале пути. Но вы должны понимать — вы не одни. Мы поможем вам справиться с болезнью и будем идти с Вами рука об руку через все этапы вашего лечения.
Все эмоциональные ресурсы пациента и его родных брошены на переживания и страх. Но именно в этот момент необходимо изменить вектор «за что» на вектор «что можно сделать».
Очень часто пациенты чувствуют себя безгранично одинокими вначале пути. Но вы должны понимать — вы не одни. Мы поможем вам справиться с болезнью и будем идти с Вами рука об руку через все этапы вашего лечения.
Рак прямой кишки прогрессирует среди онкологических заболеваний. В 2017 году было выявлено 29918 новых случаев данного заболеваний у мужчин и у женщин в Российской Федерации. Смертность от этого заболевания также остаётся очень высокой. В 2017 году от этой локализации умерло 16360 человек.
Предлагаем Вашему вниманию краткий, но очень подробный обзор рака прямой кишки. Его подготовили высоко квалифицированные специалисты Абдоминального отделения МНИОИ имени П.А. Герцена – филиала ФГБУ «НМИЦ радиологии» Минздрава России.
Рак прямой кишки. Эпидемиология
Эпидемиология Рак прямой кишки становится одной из наиболее распространенных форм злокачественных новообразований.
Эта тенденция за последние десятилетия все отчетливее проявляет себя во всех экономически развитых странах Европы и Северной Америки.
По данным одного из крупнейших исследований по эпидемиологии рака, World Cancer Report, заболеваемость раком прямой кишки стоит на третьем месте среди всех онкологических новообразований.
Анатомия прямой кишки
Прямая кишка (rectum) является дистальным отделом толстой кишки. Ее верхняя граница находится на уровне верхнего края 3-го крестцового позвонка , внизу прямая кишка переходит в анальный канал. Длина прямой кишки колеблется от 12 до 18 см, в месте перехода сигмовидной кишки в прямую ее диаметр составляет 3—4 см, ниже кишка значительно расширяется (ампула прямой кишки).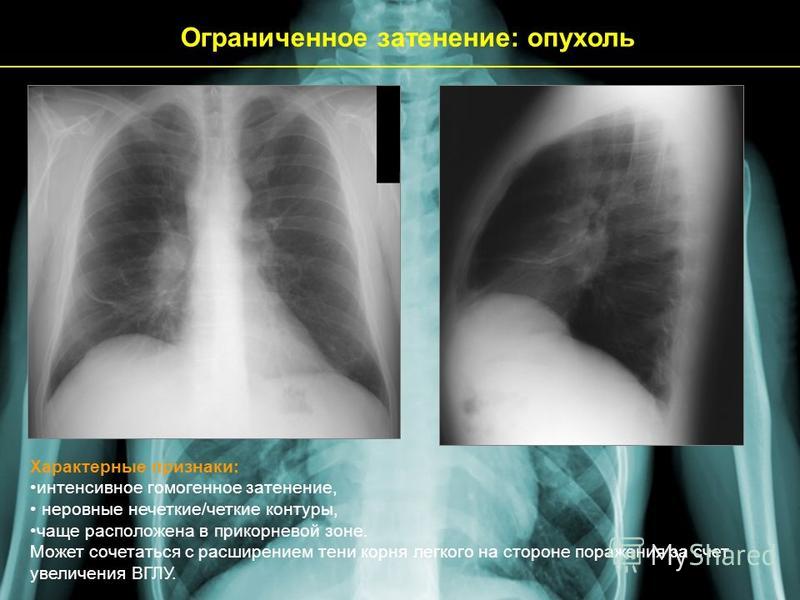 Ампулу прямой кишки делят на верхний, средний и нижний отделы. Форма и ширина просвета ампулы во многом зависят от наполнения кишки. Верхний отдел прямой кишки расположен в брюшной полости, он смещен во фронтальной плоскости и располагается немного левее срединной линии, являясь как бы продолжением сигмовидной ободочной кишки.
Ампулу прямой кишки делят на верхний, средний и нижний отделы. Форма и ширина просвета ампулы во многом зависят от наполнения кишки. Верхний отдел прямой кишки расположен в брюшной полости, он смещен во фронтальной плоскости и располагается немного левее срединной линии, являясь как бы продолжением сигмовидной ободочной кишки.
1. Возраст старше 50 лет. Риск возникновения рака прямой кишки увеличивается с возрастом. Более 90 % случаев диагностируется у людей после 50 лет, причём он в равной степени касается мужчин и женщин. Риск развития рака прямой кишки удваивается с каждым прожитым десятилетием.
2. Наследственный фактор. Около 5% раков толстой кишки составляет наследственный рак, предрасположенность к которому передаётся по аутосомно-доминантному типу. Так, если риск возникновения рака толстой кишки у лиц, не имеющих предрасполагающих факторов, составляет 1–3%, то при его наличии у родственников первого порядка, риск повышается до 5%.
3. Генетические изменения. Изменения в определенных генах также повышают риск развития рака прямой кишки.
4. Наличие онкологического заболевания в прошлом. В некоторых случаях возможно повторное возникновение рака. К факторам риска также следует относить злокачественные опухоли других органов. Так, у женщин, имеющих рак молочной железы или репродуктивной системы, риск заболеть раком толстой кишки значительно увеличивается.
5. Хронические неспецифические воспалительные заболевания толстой кишки. У больных с хроническими воспалительными заболеваниями толстой кишки, особенно с язвенным колитом, частота возникновения колоректального рака значительно выше, чем в общей популяции.
6. Питание. Исследования показали, что прием пищи с высоким содержанием жиров, недостаток кальция, фолиевой кислоты и клетчатки, ограниченное количество фруктов и овощей увеличивает риск развития колоректального рака.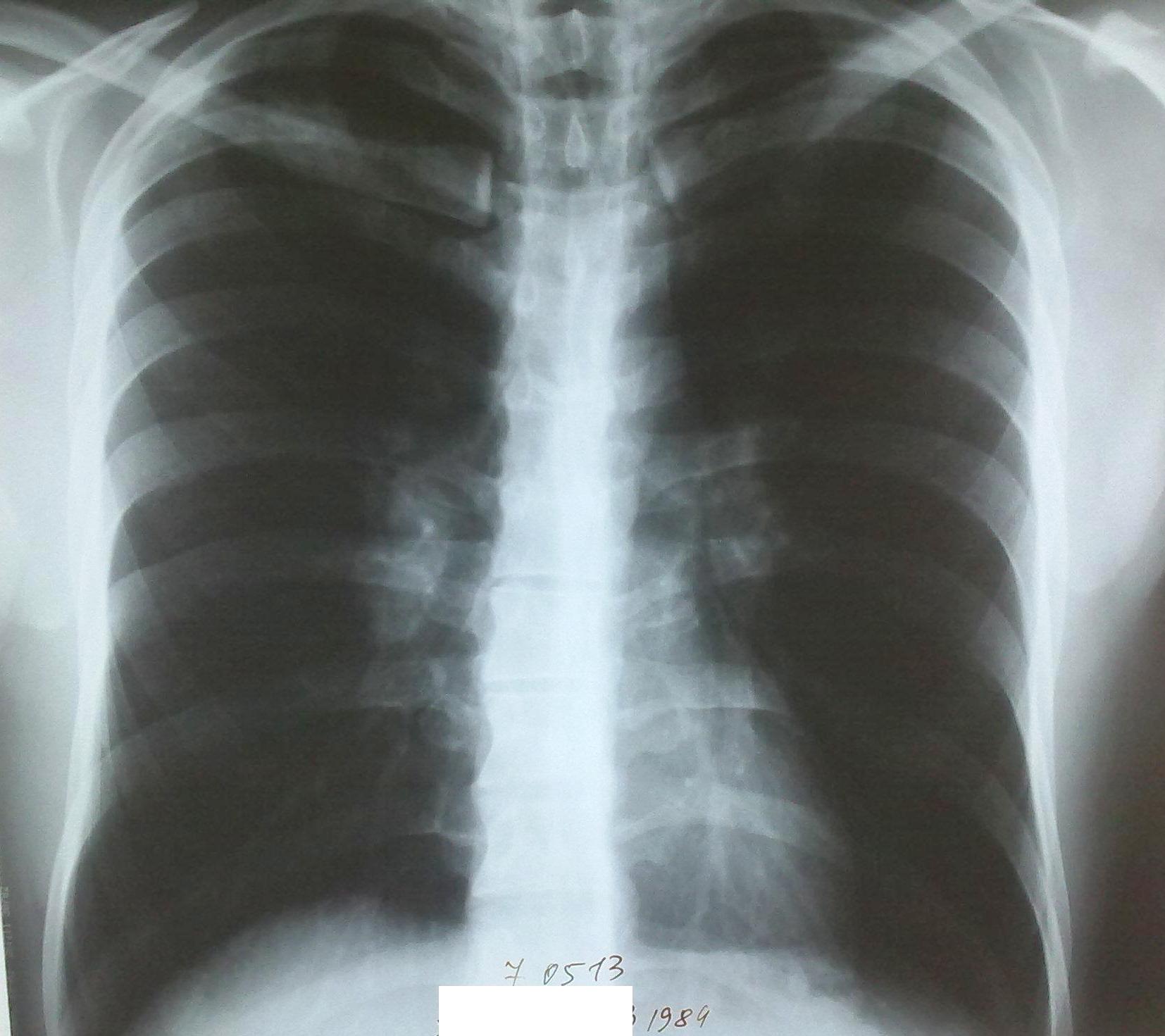
В настоящее время рак прямой кишки классифицируют:
- — по стадии опухолевого процесса (TNM, Dukes, Dukes в модификации Aster et Coller)
- -по гистологической структуре опухоли
- — по типу роста опухоли.
Классификация TNM, 8-издание.
| Т | первичная опухоль |
| ТХ | первичный очаг невозможно выявить. |
| Т0 | отсутствие признаков первичной опухоли. |
| Tis | неинвазивный (карцинома in situ, внутриэпителиальный) рак (без прорастания собственной пластинки слизистой оболочки). Сюда относят и элементы опухоли в пределах кишечных желёз при отсутствии поражения мышечного слоя слизистой оболочки и подслизистого слоя.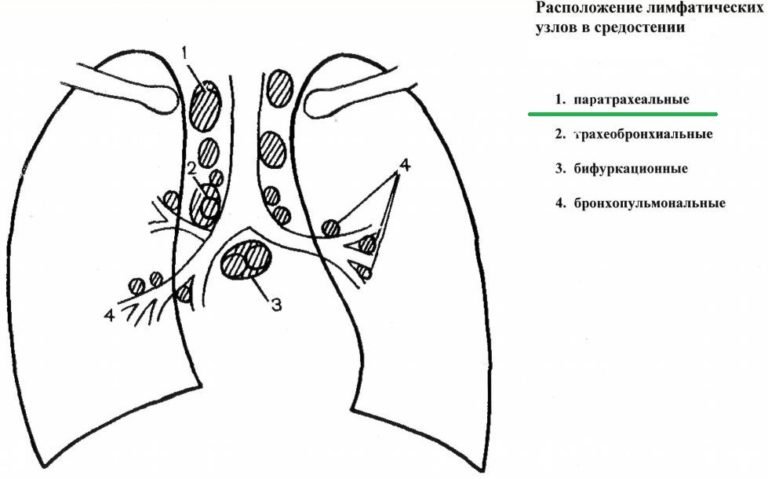 |
| Т1 | опухоль инфильтрирует подслизистый слой. |
| Т2 | прорастание собственной мышечной оболочки. |
| Т3 | опухоль прорастает субсерозный слой или неперитонизированные отделы стенки с выходом в прилежащую ткань (брыжейку ободочной кишки). |
| T4 | опухоль распространяется на соседние органы или структуры и/или прорастает висцеральную брюшину. |
| Т4а | опухоль прорастает висцеральную брюшину |
| Т4b | опухоль непосредственно прорастает другие органы и/или структуры |
| N | регионарные лимфатические узлы |
| NX | состояние регионарных зон оценить невозможно.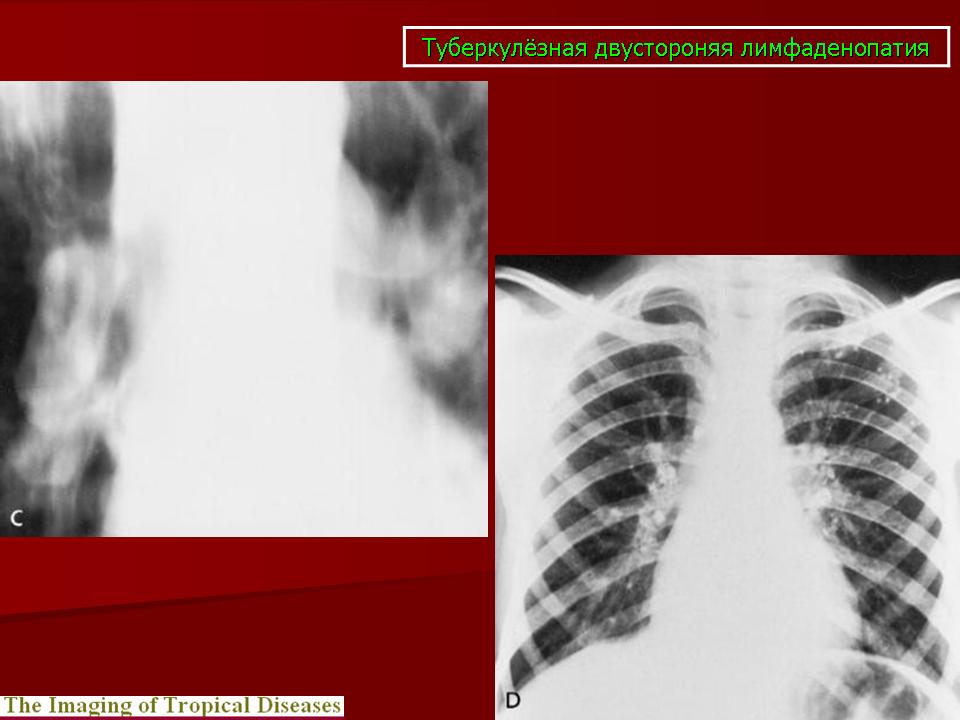 |
| N0 | регионарных метастазов нет. |
| N1 | метастатическое поражение от 1 до 3 регионарных лимфоузлов; |
| N1a | в одном лимфоузле |
| N1b | в 2-3 лимфоузлах |
| N1c | опухолевые отсевы в субсерозном слое без наличия поражения лимфоузлов* |
| N2 | метастазы определяются в 4 и более регионарных ЛУ. |
| N2a | 4-6 поражённых лимфоузла |
| N2b | 7 и более поражённых лимфоузлов |
| М | отдалённые метастазы |
| Mx | отдалённые метастазы не могут быть подтверждены. |
| М0 | отдалённых метастазов нет. |
| M1a | поражение одного органа |
| M1b | поражение более одного органа или диссеминация по брюшине |
| M1c | Перитонеальные метастазы самостоятельные или с метастазами в другие органы или анатомические участки. |
| Duke`s А | рост опухоли ограничен стенкой кишки. |
| Duke`s В | опухоль распространена на окружающие ткани; метастазы в лимфатических узлах отсутствуют. |
| Duke`s С | опухоль с любой степенью местного распространения при наличии метастазов в регионарных лимфатических узлах.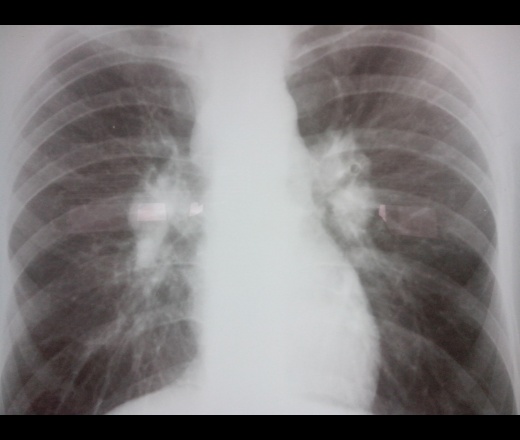 |
При разделении опухолей по гистологическому строению учитывается преобладание тканевой структуры паренхимы, характер клеточных элементов и их способность к секреции.
Ниже представлены четыре наиболее распространённые формы рака прямой кишки.
Аденокарцинома — наиболее часто встречаемая форма рака прямой кишки.
Выделяют три степени ее дифференцировки: высокодифференцированная; умеренно дифференцированная; низкодифференцированная.
Клиническая картина рака прямой кишки находится в прямой зависимости от уровня расположения опухоли, характера ее роста, стадии заболевания. В начальных стадиях симптомокомплекс выражен слабо.
Выделяют несколько симптомокомплексов при раке прямой кишки. Наиболее частым являются патологические выделения из прямой кишки. Кровь темного цвета со сгустками выделяется до кала, во время тенезмов, или вне акта дефекации. Кроме крови при раке прямой кишки из заднего прохода может выделяться слизь. При распространенных формах и вовлечении в опухолевый процесс соседних органов и тканей возможно выделение гноя с калом.
Кровь темного цвета со сгустками выделяется до кала, во время тенезмов, или вне акта дефекации. Кроме крови при раке прямой кишки из заднего прохода может выделяться слизь. При распространенных формах и вовлечении в опухолевый процесс соседних органов и тканей возможно выделение гноя с калом.
Другим частым симптомокомплексом является нарушение функции толстой кишки. Характерным являются ложные позывы к дефекации – тенезмы. При тенезмах вместо кала выделяется кровь, слизь. При обтурации опухолью просвета кишки развивается запор. При этом изменяется вид кала – он становится лентовидный или «овечий». При вовлечении в процесс сфинктеров прямой кишки может развиться недержание.
Развитие болевого синдрома является характерным симптомом лишь при вовлечении в опухолевый процесс анального канала. Выше аноректальной линии болевых рецепторов в слизистой оболочке прямой кишки нет. Поэтому при ампулярном раке боль появляется в поздних стадиях, при прорастании опухолью соседних органов.
К неспецифическим клиническим проявлениям относится нарушение общего состояния пациента. Снижение массы тела, изменение цвета кожных покровов (бледный, землистый, иногда чуть желтушный) связано с хронической опухолевой интоксикацией. Анемия развивается из-за длительной кровопотери. Однако эти симптомы развиваются в поздних стадиях опухолевого процесса. Возникновение регионарных и отдаленных метастазов, как правило, изменение клинической картины не сопровождаются и специальной симптоматики не имеют.
Снижение массы тела, изменение цвета кожных покровов (бледный, землистый, иногда чуть желтушный) связано с хронической опухолевой интоксикацией. Анемия развивается из-за длительной кровопотери. Однако эти симптомы развиваются в поздних стадиях опухолевого процесса. Возникновение регионарных и отдаленных метастазов, как правило, изменение клинической картины не сопровождаются и специальной симптоматики не имеют.
Одним из основных методов обследования пациентов раком прямой кишки является пальцевое исследование прямой кишки и/или бидигитальное исследование через прямую кишку и влагалище (у женщин). При исследовании оценивается высота расположения нижнего полюса опухоли над уровнем аноректальной линии, протяженность и форму роста опухоли, состояние регионарных лимфатических узлов. При локализации нижнего полюса опухоли в верхне-среднеампулярных отделах прямой кишки необходимо выполнение ректороманоскопии. При этом удается осмотреть все отделы прямой кишки (до 25 см). Во время исследования проводится визуализация патологического процесса и объективизации данных пальцевого исследования. В ходе исследования, с целью определения гистологического строения первичной опухоли, производится забор материала для цитологического и/или гистологического исследования.
Во время исследования проводится визуализация патологического процесса и объективизации данных пальцевого исследования. В ходе исследования, с целью определения гистологического строения первичной опухоли, производится забор материала для цитологического и/или гистологического исследования.
Колоноскопия выполняется с целью выявления патологических изменений толстой и прямой кишки проксимальнее опухоли.
Рентгенологическое исследование толстой и прямой кишок проводится методом трехэтапной ирригоскопии в прямой и боковой проекциях (полутугое-тугое наполнение, двойное контрастирование после опорожнения кишки, двойное контрастирование с нагнетанием воздуха). При исследовании оценивается протяженность опухолевого процесса и наличие сопутствующих заболеваний толстой кишки на участках, расположенных проксимальнее опухоли (синхронный рак, дивертикулез и др.).
Ультрасонография органов брюшной полости и малого таза позволяет оценить глубину инвазии первичной опухоли, вовлеченность в процесс соседних органов и тканей, наличие увеличенных регионарных лимфатических узлов, наличие отдаленных метастазов.
Рентгенологическое исследование органов грудной клетки в прямой и боковой проекции осуществлялось в условиях рентгенологического отделения на стандартном рентгенологическом оборудовании с целью выявления патологических изменений в легких и органах средостения.
КТ органов брюшной полости используют для диагностики наличия отдаленных метастазов.
МРТ органов малого таза следует выполнить для оценки вовлеченности смежных органов в опухолевый процесс. Также методика позволяет оценить латеральный клиренс распространения опухоли и поражение параректальных лимфатических узлов.
Определение уровня онкомаркёров. Наиболее часто используемые в практике при раке прямой кишки — раковоэмбриональный антиген (РЭА) и СА19-9. Маркеры неспецифичны и их концентрация не всегда коррелирует с распространённостью процесса и степенью дифференцировки опухоли, хотя чаще повышается при распространённом раке, особенно при метастазах в печени.
Хирургический метод
Единственным радикальным методом лечения рака прямой кишки является хирургический.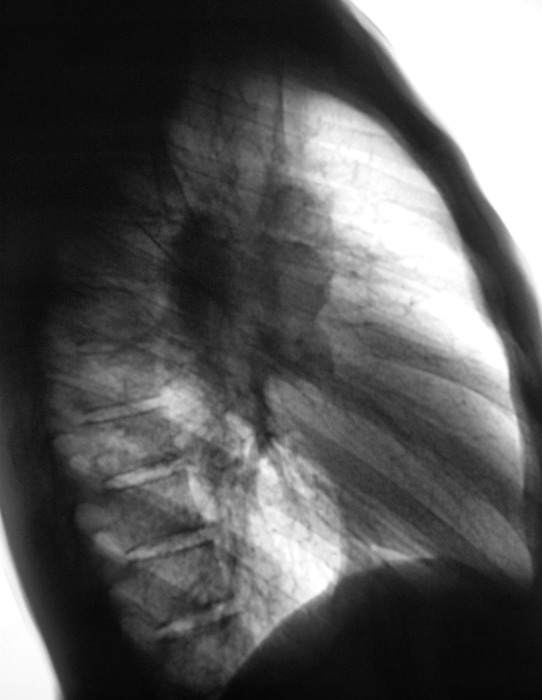 При локализации опухоли в нижнеампулярном отделе прямой кишки в стадии сT3-4 с поражением регионарных лимфатических узлов перед оперативным вмешательством, при отсутствии противопоказаний, возможно проведение предоперационной лучевой/химиолучевой терапии.
При локализации опухоли в нижнеампулярном отделе прямой кишки в стадии сT3-4 с поражением регионарных лимфатических узлов перед оперативным вмешательством, при отсутствии противопоказаний, возможно проведение предоперационной лучевой/химиолучевой терапии.
Выбор объема операции зависит от:
— Локализация опухоли
— степени распространенности опухолевого процесса
— общее состояние больного.
Для радикального удаления опухоли прямой кишки при ее резекции необходимо отступать в проксимальном направлении от верхнего края новообразования на 12-15см, в дистальном до 2- 5см.
Лучевая / химиолучевая терапия
Основными задачами применения лучевой / химиолучевой терапия на дооперационном этапе при раке прямой кишки являются уменьшение распространенности опухолевого процесса и улучшение местного контроля.
При локализации опухоли в нижнеампулярном отделе прямой кишки, прорастанием всех слоев кишечной стенки и выходом в мезоректальную клетчатку, при наличии поражения регионарных лимфатических узлов, при отсутствии противопоказаний, всем пациентам на дооперационном этапе проводится предоперационная лучевая терапия. Послеоперационное облучение призвано снизить частоту возникновения локальных рецидивов, особенно у пациентов с R1-R2 резекцией.
Послеоперационное облучение призвано снизить частоту возникновения локальных рецидивов, особенно у пациентов с R1-R2 резекцией.
Лекарственная терапия
Цель адъювантной терапии после радикальной операции является уничтожение отдаленных микрометастазов, что приводит к увеличению общей и безрецидивной выживаемости. Вопрос о её назначении следует решать с учётом исходной стадии заболевания. Показанием для проведения адьювантной химиотерапии больным раком прямой кишки служит III стадии (Dukes C) опухолевого процесса.
Минимальный объем адъювантной химиотерапии включает в себя назначение фторпиримидинов, которые можно применять в различных вариантах: струйном (режим клиники Mayo, Roswell Park), инфузионном (режимы DeGramont, AIO) или пероральном (капецитабин).
Оптимальный объем адъювантной химиотерапии включает в себя комбинацию оксалиплатина с фторпиримидинами. Наиболее оптимальными являются режимы FOLFOX или XELOX.
Основной целью диспансерного наблюдение за пациентами, перенесших радикальное лечение по поводу рака прямой кишки, является ранняя диагностика рецидива и метастазов опухоли.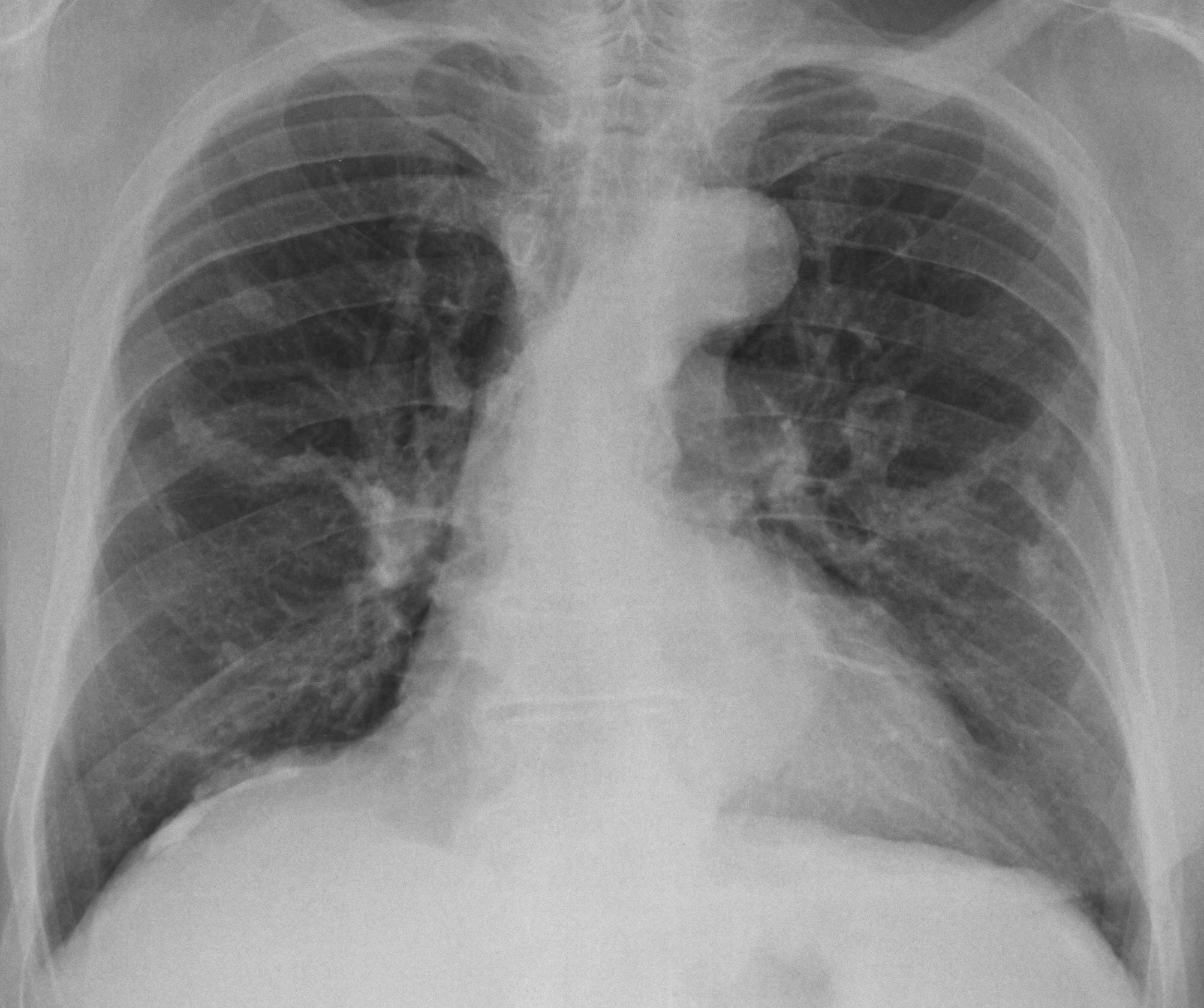 Все больные, перенесшие оперативное вмешательство по поводу рака прямой кишки, должны находится под строгим динамическим контролем.
Все больные, перенесшие оперативное вмешательство по поводу рака прямой кишки, должны находится под строгим динамическим контролем.
КОМПЛЕКСНОЕ ЛЕЧЕНИЕ РАКА ПРЯМОЙ КИШКИ
Комплексного лечения больных раком прямой кишки включает предоперационную лучевую терапию, хирургическое вмешательство и адъювантную химиотерапию. Использование подобного подхода позволяет снизить частоту местных рецидивов, увеличить 5-летнюю выживаемость, улучшить качество жизни больных раком прямой кишки. Комплексное лечение с предоперационной лучевой (химиолучевой) терапией и адъювантной полихимиотерапией показано при наличии прорастания опухоли за пределы стенки кишки либо при метастатическом поражении лимфатических узлов.
После завершения предоперационной лучевой терапии выполняют хирургический этап лечения. После завершения данного этапа и полной реабилитации пациента через 3-4 недели проводят адъювантную химиотерапию. Проведение адъювантной химиотерапии показано пациентам при III стадии рака прямой кишки, а также ее можно рассматривать у отдельных больных при II стадии и наличии высокого риска рецидива заболевания.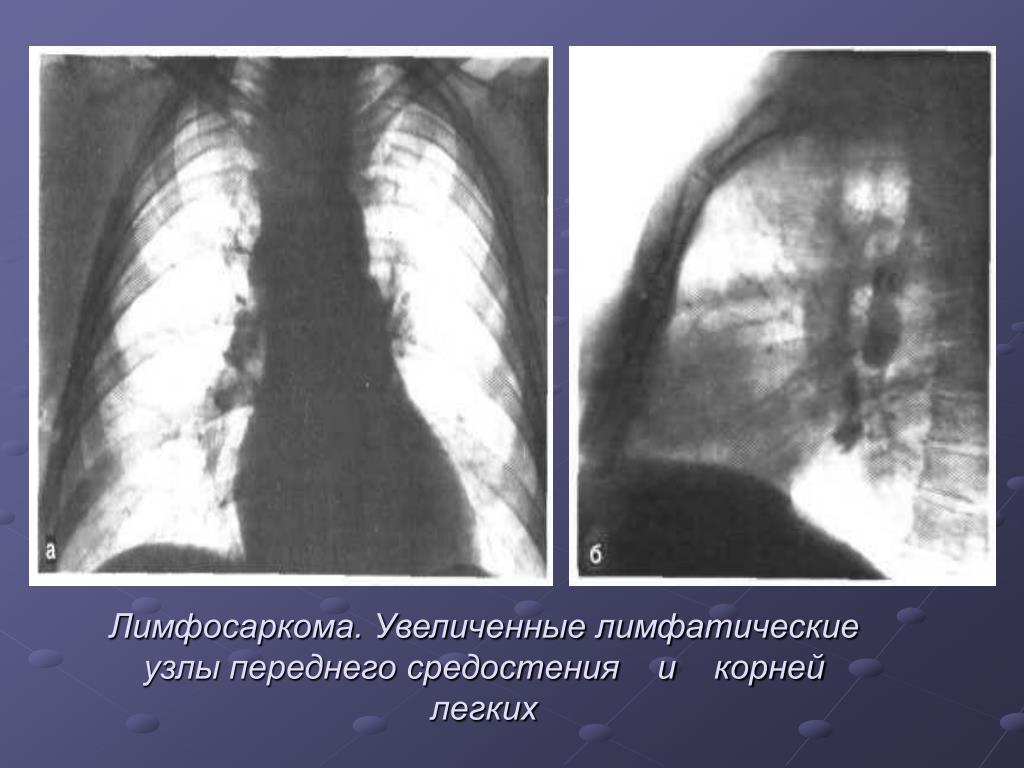
ФГБУ «НМИЦ радиологии Минздрава России обладает всем спектром методик проведения комплексного лечения у больных раком прямой кишки, что позволяет достигнуть таких же результатов лечения пациентов, как в ведущих мировых клиниках.
НЕРВОСБЕРЕГАЮЩИЕ ОПЕРАЦИИ
Наряду с усовершенствованием методики и техники операций, обеспечивающих радикальность оперативного вмешательства, в последнее время все большее внимание уделяется разработке комплекса мер, направленных на профилактику ранних и отсроченных осложнений, в частности, проблеме послеоперационной мочеполовой дисфункции у оперированных больных. По данным разных авторов частота нарушения функции мочевого пузыря в послеоперационном периоде может достигать 40% и более. Основными признаками нарушения уродинамики являются: увеличение емкости мочевого пузыря, увеличение остаточного объема мочи, ослабление чувства наполнения пузыря, снижение внутрипузырного давления и другие. Все это зачастую приводит к необходимости больным производить самокатетеризацию мочевого пузыря или постановке постоянного катетера.
Указанные осложнения снижают качество жизни, а также социальную, психо-эмоциональную и семейную реабилитацию у оперированных больных. Одной из причин развития подобного рода осложнений является травма нервных стволов, отвечающих за иннервацию мочевого пузыря.
В ФГБУ «НМИЦ радиологии Минздрава России используется техника нервосберегающих операций при раке нижне — и среднеампулярного отделов прямой кишки, которая включает в себя выполнение стандартного хирургического вмешательства с использованием приемов, направленных на максимально возможное сохранение элементов вегетативной нервной системы таза.
СФИНКТЕРОСОХРАНЯЮЩИЕ ОПЕРАЦИИ
Стремление любого онкопроктолога при вмешательствах на прямой кишке направлено с одной стороны на попытку улучшения онкологических результатов лечения, а с другой – выполнение органосохраняющих операций, что позволило бы улучшить качество жизни пациентов. В связи с этим, на протяжении долгого времени, не ослабевает интерес к определению оптимальной дистальной линии резекции, разработке подходов, обеспечивающих сохранение интактных от опухолевого процесса тканей, и вместе с тем расширению объема оперативного вмешательства с целью максимально возможной санации тканей с высоким риском опухолевого поражения.
До настоящего времени, во многих медицинских учреждениях, единственным радикальным оперативным вмешательством при раке средне- и нижнеампулярного отдела считалось выполнение брюшно-промежностной экстирпации прямой кишки с формированием противоестественного заднего прохода на передней брюшной стенки. Однако, многочисленные исследования, проведенные как в России, так и за рубежом, показали, что при определенных показаниях, возможно сохранение сфинктерного аппарата прямой кишки, что позволяет в последующем сохранить естественный пассаж по кишечнику у оперированных пациентов.
ФГБУ «НМИЦ радиологии Минздрава России в абдоминальной онкологии активно применяются современные методики оперативных вмешательств, направленные на сохранение «жома» прямой кишки, что позволяет улучшить качество жизни и психо-социальную адаптацию оперированных пациентов.
Филиалы и отделения Центра, в которых лечат рак прямой кишкиФГБУ «НМИЦ радиологии» Минздрава России обладает всеми необходимыми технологиями лучевого, химиотерапевтического и хирургического лечения, включая расширенные и комбинированные операции. Все это позволяет выполнить необходимые этапы лечения в рамках одного Центра, что исключительно удобно для пациентов. Однако надо помнить, что тактику лечения определяет консилиум врачей.
Все это позволяет выполнить необходимые этапы лечения в рамках одного Центра, что исключительно удобно для пациентов. Однако надо помнить, что тактику лечения определяет консилиум врачей.
Рак прямой кишки можно лечить:
В Абдоминальном отделении МНИОИ имени П.А. Герцена – филиала ФГБУ «НМИЦ радиологии» Минздрава России
Заведующий отделения – д.м.н. Дмитрий Владимирович Сидоров.
Контакты: (495) 150 11 22
В Отделении лучевого и хирургического лечения заболеваний абдоминальной области МРНЦ имени А.Ф. Цыба — филиала ФГБУ «НМИЦ радиологии» Минздрава России
Заведующий отделением — к.м.н. Леонид Олегович Петров
Контакты: (484) 399-30-08
что это такое, причины, виды, диагностика
Лимфаденопатия подмышечных лимфоузлов – явление частое в повседневной практике врача. Данный симптом встречается при ряде патологий, лечению которых необходимо уделять серьезное внимание.
Причины увеличения лифмоузлов
В организме человека насчитывается около 1 000 лимфатических узлов, расположенных в разных отделах тела. Узел представляет собой периферический орган иммунитета, определяется по ходу лимфососудов.
Лимфоузлы, находящиеся в стенке полости и у органов, называются пристеночными и висцеральными. Те узлы, что определяются в области шеи, затылка, подколенных ямок, локтя, подмышечной впадины, паха, являются периферическими. Для них характерно групповое скопление, например, в подмышечной впадине число их варьирует от 12 до 40-45 штук.
Размер лимфатический узлов в среднем до 1 см, связан с возрастом обладателя и конституционными особенностями. Процесс увеличения лимфатического узла принято называть лимфаденопатией. Причинами могут быть различные болезни. Чаще всего это патология близлежащих органов, возникновение в них инфекционного агента или иной патологический комплекс.
Лимфаденопатия может возникать при болезненном ощущении в руках, шее, ногах. Это происходит потому, что выполняется защитная функция лимфатических узлов, которые являются барьером между организмом человека и любым патологическим объектом.
Это происходит потому, что выполняется защитная функция лимфатических узлов, которые являются барьером между организмом человека и любым патологическим объектом.
Этот барьер возникает из так называемых антител и лимфоцитов, которые блокируют проход в кровяное русло бактериальной или вирусной инфекции, различных токсинов, помогают уничтожить опухолевые клетки. Кроме этого, в них происходит очищение лимфы, притекающей от органов, ее скопление и распределение во всем организме. Лимфоузел имеет выносящий путь по лимфатическим сосудам, по которому армия лимфоцитов спешит в патологический очаг для уничтожения чужеродных тел.
Причины подмышечной лимфаденопатии
Подмышечная лимфаденопатия возникает при повышении активности узлов, стремящихся помочь организму в борьбе с чужеродным агентом. Однако подмышечная область иногда страдает от разрастающихся клеток злокачественного новообразования.
Чаще всего этиологическим фактором возникновения данной болезни является следующее.
- Из-за неправильного соблюдения личной гигиены и чрезмерного использования косметических средств для борьбы с неприятным запахом подмышек (дезодоранты, антиперспиранты, спреи, кремы и прочее), гипергидроза, при сахарном диабете и у людей с повышенной массой тела происходит закупорка потовой железы и волосяного фолликула. Процесс чаще всего двусторонний. Запускается воспалительный процесс, и при лечении в домашних условиях самостоятельно процесс распространяется глубже.
- В момент гормональной перестройки у женщин (беременность и период кормления грудью) происходит увеличение подмышечных и внутригрудных лимфатических узлов, напоминающих дольку молочной железы. Не каждый специалист сможет это обнаружить, к тому же этот доброкачественный процесс не несет какой-либо опасности организму женщины. Состояние самопроизвольно устраняется.
- Наличие гнойных поражений в области рук, груди и плеч, например, фурункул и гнойная рана, приводят к увеличению лимфатических узлов.
- У детей вирусная патология приводит к изменениям.
 Это ветряная оспа, мононуклеоз и другие. Положительный эффект даст лечение основного заболевания.
Это ветряная оспа, мононуклеоз и другие. Положительный эффект даст лечение основного заболевания. - Некоторые кожные патологии приводят к этому процессу – это псориатические изменения, нейродермиты и прочее.
- Иммунодефицитные состояния проявляются в первую очередь лимфоаденопатией, причем сразу в нескольких местах.
- При патологии грудных желез, например, при мастите или мастопатии, возникает увеличение подмышечных лимфатических узлов. В тех же местах этот симптом развивается при ряде инфекционных заболеваний: туберкулез, бруцеллез, сифилис, чума.
- Системные аутоиммунные патологии также изобилуют лимфаденопатией различных групп лимфатических узлов – это ревматическая лихорадка (хроническая или острая), системная склеродермия, болезнь Бехтерева, артриты, системная красная волчанка.
Судя по серьезным заболеваниям, для которых характерен симптом, следует помнить, что при незначительном увеличении подмышечных и других лимфоузлов консультация врача обязательна! Не факт, что обнаружится страшный диагноз, однако лучше лишний раз перестраховаться и сдать все необходимые анализы.
Виды лимфаденопатии
Современная медицина делит патологию на 2 вида: воспалительной природы и невоспалительной. Кроме этого, их можно группировать на специфические и неспецифические. Для первых характерна трудноизлечимая и опасная инфекция – туберкулезная палочка, бледная трепонема (сифилис), актиномикоз, чума и туляремия. Ко второй группе относят грамположительную флору и вирусы.
Процесс может протекать остро или хронически. Для острого характерно покраснение в области подмышечных впадин, болезненность, припухлость, при ощупывании – горячая кожа над ним. Общее состояние при этом тоже ухудшается, отмечается озноб, повышение общей температуры тела, чувство недомогания.
В воспалительный процесс может включаться 1 узел или же группа, сохраняется их подвижность, или они срастаются с окружающей тканью. В лечение такой симптоматики необходимо включать антибактериальные средства.
Для хронического течения такие яркие клинические проявления не характерны. Обычно ощущается подкожное округлое спаянное или свободно расположенное образование, которое не болит при надавливании, лишь дает неприятное ощущение. При этом больной отмечает, что когда-то в этой области отмечалась боль, при этом лечение не проводилось или же не было доведено до конца.
Обычно ощущается подкожное округлое спаянное или свободно расположенное образование, которое не болит при надавливании, лишь дает неприятное ощущение. При этом больной отмечает, что когда-то в этой области отмечалась боль, при этом лечение не проводилось или же не было доведено до конца.
К сожалению, болезненность не всегда сопровождает увеличение лимфоузла, например, при туберкулезной патологии или сифилисе, что значительно усугубляет процесс и ведет к большим страданиям человека. Отсутствие боли характерно при не воспалительной природе — это лимфаденопатия молочной железы при онкологическом процессе, заболевании крови.
Диагностика
Самостоятельно определять причины, сидеть в догадках крайне опасно. Возможно, это лишь признак наличия гнойной раны на соответствующей руке. Но внутригрудная лимфаденопатия не всегда определяется так просто, чаще возникает при туберкулезе, поэтому следует тщательно провериться. Если есть подозрение, что это аксиллярная лимфаденопатия, необходимо обратиться к специалисту.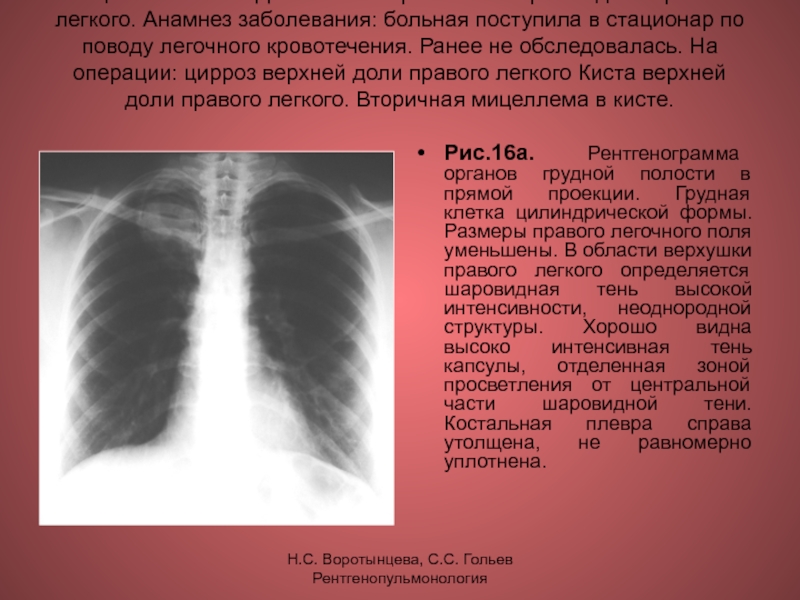
Когда узел увеличен более 21 дня, и причину этого найти не удается, при невоспалительных состояниях у женщин подозревают вторичную лимфаденопатию. Пациентке в этом случае рекомендовано провести пункцию.
При хирургическом вмешательстве по поводу мастопатии биопсию узлов проводят всегда, что смягчает вопрос об их удалении в онкологии. Для начала определяют наличие метастатических клеток в сигнальных лимфоузлах, и только при положительном анализе проводят их удаление.
Лечение
Лечение назначает только врач, подбирая не только препараты, но и дозировку индивидуально для каждого больного. После определения причины врач дает назначение, например, лечение туберкулеза по специальной системе ДОТС+, или при гнойных процессах – антибиотикотерапия и вскрытие гнойника.
Видео
О чем сигнализируют воспаленные лимфоузлы и общее состояние подмышечных впадин, вы сможете узнать из нашего видео.
Что это значит, если ваш преаурикулярный лимфатический узел опух или болезнен
Что такое преаурикулярный лимфатический узел?
У вас есть сотни маленьких лимфатических узлов овальной или фасолевой формы (также известных как лимфатические узлы) по всему телу. Ваши лимфатические узлы, наряду с лимфатическими сосудами, являются частью вашей иммунной системы. Лимфатические узлы содержат иммунные клетки, которые помогают защищаться от болезней.
Ваша лимфатическая система фильтрует жидкость, чтобы удалить вредные вещества из вашего тела. Когда лимфатическая система работает, жидкость выводится.
Обычно ваши лимфатические узлы маленькие и твердые. Когда они здоровы, вы даже не должны их замечать. Скопление жидкости может вызвать их набухание. Увеличенные лимфатические узлы могут ощущаться нежными на ощупь или даже болезненными.
Преаурикулярные лимфатические узлы — это те, которые расположены прямо перед вашими ушами. Они отводят лимфатическую жидкость из глаз, щек и кожи головы возле висков.
Обычно лимфатические узлы увеличиваются только в одной области тела (локализованная лимфаденопатия).Проблема, например инфекция, обычно находится поблизости.
Но есть определенные состояния, такие как вирусные заболевания, которые вызывают увеличение лимфатических узлов во многих частях тела (генерализованная лимфаденопатия).
Продолжайте читать, чтобы узнать несколько причин увеличения предаурикулярных лимфатических узлов и узнать, когда вам следует обратиться к врачу.
Каждый раз, когда возникает инфекция, травма или рак, лимфатические узлы срабатывают, чтобы бороться с ней. В процессе они могут увеличиваться.
Если у вас увеличились лимфатические узлы, значит, что-то не так. Обычно проблема находится в непосредственной близости от пораженных лимфатических узлов. Ниже приведены некоторые причины, по которым у вас могут быть опухшие или болезненные предаурикулярные лимфатические узлы.
Инфекция уха
Инфекция уха может вызвать увеличение лимфатических узлов перед ушами или за ними. У вас также может быть боль в ушах и жар. Уши могут инфицироваться, когда в них скапливается жидкость. Это может произойти, если у вас аллергия, инфекция носовых пазух или простуда.
Инфекция глаз
Окулогландулярный синдром Парино — это тип конъюнктивита (розового глаза), который может вызывать увеличение предаурикулярных лимфатических узлов. Это состояние может быть вызвано многими причинами, наиболее распространенной из которых является лихорадка от кошачьих царапин. Лихорадка от кошачьих царапин передается от бактерий, когда кошка царапает или кусает вас. Также можно получить его, когда кошка зализывает открытую рану. Другие симптомы могут включать:
- слизистые выделения из глаз
- отечность вокруг глаз
- опухоль век
- язва роговицы
- субфебрильная температура и боль
Некоторые из менее распространенных причин окулогландулярного синдрома Парино: :
Инфекция зуба
Абсцесс зуба — это скопление гноя из-за бактериальной инфекции.Близлежащие лимфатические узлы могут увеличиваться, когда они пытаются бороться с этой инфекцией. Другие симптомы:
- боль во рту
- боль в челюсти
- опухшие десны
- неприятный запах изо рта
Инфекция кожи или волосистой части головы
Инфекции кожи и волосистой части головы могут распространяться на преаурикулярные лимфатические узлы. Инфекция лимфатических узлов (лимфаденит) может сопровождаться повышением температуры тела. У вас также может развиться абсцесс, и кожа над лимфатическими узлами может стать красной и теплой.
Краснуха (немецкая корь)
Одним из симптомов краснухи является увеличение лимфатических узлов за шеей или ушами. Но краснуха может вызвать увеличение лимфатических узлов в других частях тела, помимо преаурикулярных узлов. Некоторые другие симптомы краснухи:
- сыпь, которая начинается на лице и распространяется вниз
- лихорадка
- головная боль
- насморк
- болезненные суставы
другие состояния
Увеличение лимфатических узлов не входит в число основных симптомов эти другие состояния могут иногда вызывать генерализованную лимфаденопатию:
Лимфома — это тип рака, который начинается в лимфатической системе, включая лимфатические узлы, селезенку, тимус и костный мозг.Существует много разных типов, включая лимфому Ходжкина и неходжкинскую лимфому. Помимо увеличения лимфатических узлов, другие признаки и симптомы:
- усталость
- лихорадка, ночная потливость
- одышка
- потеря веса
лейкемия — рак кроветворной ткани. Это включает лимфатическую систему. Есть несколько различных типов лейкемии. Некоторые из них очень агрессивны (острые), а некоторые имеют тенденцию прогрессировать медленнее (хронические).Помимо увеличения лимфатических узлов, лейкемия может вызвать:
- легкое кровотечение или образование синяков
- увеличение печени или селезенки
- усталость, слабость
- лихорадку
- частые инфекции
- потерю веса
биопсию пораженного лимфатического узла может помочь диагностировать рак.
Кроме того, любой тип рака может распространяться в лимфатическую систему и вызывать опухшие или болезненные лимфатические узлы. Вот почему при диагностировании рака обычно исследуют близлежащие лимфатические узлы.
Увеличение или болезненность лимфатических узлов — это симптом, а не болезнь. Лечение зависит от причины опухоли предаурикулярных лимфатических узлов. Как правило, лимфатические узлы имеют тенденцию возвращаться к нормальному размеру после лечения основного заболевания.
Инфекции ушей, глаз, кожи и волосистой части головы обычно можно лечить с помощью антибиотиков. Также следует лечить любые состояния, вызывающие эти инфекции.
При абсцедировании зуба может потребоваться корневой канал, чтобы избавиться от инфекции.После этого на зуб насаживают коронку. В качестве альтернативы вы можете дренировать зуб, разрезав ткань десны. После этого будет проведен курс антибиотиков. В некоторых случаях единственным выходом может быть удаление зуба.
Стандартного лечения краснухи не существует. Антибиотики неэффективны, но без осложнений должно поправиться само. Это заболевание можно предотвратить с помощью вакцины против кори, эпидемического паротита и краснухи (MMR).
Лечение рака может быть сложным.Это может включать некоторую комбинацию химиотерапии, лучевой терапии, а также биологических и таргетных препаратов.
Лечение лимфомы и лейкемии зависит от конкретного типа и стадии рака. Другие факторы — это ваш возраст, общее состояние здоровья и личные предпочтения. В некоторых случаях трансплантация стволовых клеток (также называемая трансплантацией костного мозга) является вариантом лечения лимфомы и лейкемии.
В большинстве случаев увеличение лимфатических узлов не свидетельствует об опасной проблеме со здоровьем. Они должны вернуться в нормальное состояние в течение короткого периода времени, когда исчезнет основное заболевание.Но поскольку они иногда могут быть симптомами серьезного состояния, обратитесь к врачу, если:
- у вас также постоянная лихорадка или необъяснимая потеря веса
- нет видимой причины для опухоли
- опухоль продолжается более двух недель
- лимфатические узлы кажутся твердыми или эластичными
- лимфатические узлы не двигаются, когда вы нажимаете на них
- кожа над лимфатическими узлами красная или воспаленная
- у вас есть личный анамнез рака
- у вас семейная история лимфомы или лейкоз
Лимфатическая система и лимфангиогенез в глазу
Лимфатическая система — необходимое условие для поддержания баланса тканевой жидкости и иммунитета в организме.Совокупность доказательств также показывает, что лимфангиогенез играет важную роль в патогенезе таких заболеваний, как метастазирование опухоли и воспаление. Считалось, что в глазу отсутствуют лимфатические сосуды, кроме конъюнктивы; однако достижения в этой области, включая идентификацию лимфатических эндотелиальных маркеров (например, LYVE-1 или подопланин) и лимфангиогенных факторов (например, VEGF-C), показали наличие и возможную роль лимфатических сосудов и лимфангиогенеза в глазу. Недавние исследования показали, что лимбы роговицы, цилиарное тело, слезная железа, мозговые оболочки глазницы и экстраокулярные мышцы содержат лимфатические сосуды и что сосудистая оболочка может иметь лимфатическую систему.Лимфатический отток из глаза неизвестен. Однако несколько лимфатических каналов, включая увеолимфатический путь, могут служить гомеостазу глазной жидкости. Кроме того, лимфангиогенез играет важную роль в патологических состояниях глаза, включая отторжение трансплантата роговицы и прогрессирование опухоли глаза. Тем не менее, роль лимфангиогенеза в большинстве глазных заболеваний, особенно воспалительных заболеваний или отеков, остается неизвестной. Лучшее понимание лимфатического и лимфангиогенеза в глазу откроет новые терапевтические возможности для предотвращения потери зрения при глазных заболеваниях.
1. Введение
Лимфатическая система человека была впервые описана Гаспером Аселли в 1627 году в статье «De Lacteibus sive Lacteis Venis», Quarto Vasorum Mesarai corum Genere novo Invento. Теперь хорошо известно, что лимфатические сосуды удаляют интерстициальную жидкость и макромолекулы, включая белки, и транспортируют их к лимфатическим узлам перед тем, как попасть в кровоток. Из лимфатических капилляров лимфа транспортируется через преколлекторы к собирающим лимфатическим сосудам и возвращается через лимфатические соединения между грудным или лимфатическим протоками и подключичными венами в кровоток [1].Еще одна роль лимфатических сосудов — переносить иммунные клетки к лимфатическим узлам и контролировать иммунитет при здоровье и болезни.
Хотя наличие лимфатических сосудов было давно известно из гистологии [2], систематические лимфатические исследования начинались позже, чем кровеносные сосуды, из-за отсутствия специфических маркеров. Недавняя идентификация лимфатических эндотелиальных маркеров облегчила лимфатические исследования [3, 4]. Кроме того, обнаружение лимфангиогенных факторов выявляет различные механизмы лимфангиогенеза при здоровье и болезни.Например, лимфангиогенез играет решающую роль при различных заболеваниях, включая метастазирование рака и воспаление [5, 6].
За последние два десятилетия изучались лимфатические процессы и лимфангиогенез в глазу, а также фенотипы при различных глазных заболеваниях. Гистологические исследования показывают расположение и наличие лимфатических сосудов в глазу [7]. Эти исследования показали, что лимфатические сосуды способствуют гомеостазу глаза и что лимфангиогенез глаза может играть важную роль в заболеваниях глаз.В этой статье рассматриваются современные знания о лимфатических процессах и лимфангиогенезе в глазу и обсуждается возможность терапии, направленной на лимфатические сосуды.
2. Система VEGF / VEGFR в лимфангиогенезе
Семейство VEGF важно для васкулогенеза, ангиогенеза и лимфангиогенеза [8]. Семейство VEGF млекопитающих в настоящее время включает пять членов: VEGF-A, фактор роста плаценты (PlGF), VEGF-B, VEGF-C и VEGF-D. VEGF-A играет важную роль в развитии сосудов у млекопитающих и в заболеваниях, связанных с аномальным ростом кровеносных сосудов.Недавние клинические исследования продемонстрировали значение VEGF-A в неоваскуляризации глаза (например, диабетическая ретинопатия и возрастная дегенерация желтого пятна) с использованием нейтрализующих антител к VEGF-A [9]. VEGF-C и VEGF-D являются основными лимфангиогенными факторами как при физиологических, так и при патологических состояниях. Семейство рецепторов VEGF состоит из трех членов: VEGFR-1 (Flt-1), VEGFR-2 (KDR / Flk-1) и VEGFR-3 (Flt-4). VEGF-A связывает и активирует два рецептора тирозинкиназ: VEGFR-1 и VEGFR-2 [8]. VEGF-A не проявляет заметной аффинности связывания с VEGFR-3.VEGFR-3 является лигандом для VEGF-C и VEGF-D. Известно, что зрелая форма VEGF-C и VEGF-D человека связывают и активируют VEGFR-2 [10, 11]. Различные исследования проясняют участие системы VEGF-C и -D / VEGFR-3 в лимфатической инвазии рака и метастазировании в лимфатические узлы [12, 13]. Кроме того, передача сигналов VEGF-C и -D / VEGFR-3 участвует в воспалительных заболеваниях и трансплантации органов [6, 14, 15].
3. Другие факторы, связанные с лимфангиогенезом
Лимфангиогенные факторы включают не только семейство VEGF, но и другие факторы роста и цитокины, такие как инсулиноподобные факторы роста (IGF), фактор роста гепатоцитов (HGF), факторы роста фибробластов (FGFs). ) и интерлейкины (ИЛ).Эти факторы роста и цитокины хорошо известны как ангиогенные. Некоторые из этих факторов могут вызывать лимфангиогенез напрямую, а некоторые могут индуцировать лимфангиогенез через семейство VEGF косвенно. Эти результаты показаны с помощью анализов на роговице.
4. Аваскуляризация роговицы и ее лимфатические характеристики
Нормальная роговица, но не конъюнктива, лишена как лимфатических сосудов, так и кровеносных сосудов (рис. 1). Аллимфатический механизм был неизвестен до недавнего времени. Исследование показало, что растворимая форма VEGFR-2 секретируется эпителиальными клетками роговицы, избирательно подавляя физиологический рост лимфатических сосудов [16].Это открытие является первой идентификацией специфического ингибитора лимфангиогенеза.
5. Анализ лимфангиогенеза роговицы
Из-за отсутствия сосудов роговица широко используется для исследования лимфангиогенеза. Одним из наиболее надежных методов исследования лимфангиогенеза является модель воспаления роговицы с помощью наложения швов или щелочного ожога (раствор NaOH) [17, 18] (рис. 2). Другой аутентичный метод — это анализ микрокарманов роговицы, который используется для оценки ангиогенеза с 1970-х годов [19, 20] (рис. 2).В обеих моделях лимфангиогенез происходит из уже существующих лимбальных лимфатических сосудов. Модель микрокармана роговицы показала, что большинство ангиогенных факторов также индуцируют лимфангиогенез (таблица 1). Это может указывать на то, что механизм лимфангиогенеза частично сходен с ангиогенезом. IGF-1 и IGF-2, которые значительно стимулируют пролиферацию и миграцию лимфатических эндотелиальных клеток, могут вызывать лимфангиогенез роговицы. IGF-1-индуцированный лимфангиогенез не опосредуется передачей сигналов VEGFR-3 [21].Также показано, что мощный ангиогенный фактор, VEGF-A, является лимфангиогенным фактором в роговице мышей [22]. В VEGF-A-индуцированном лимфангиогенезе существуют оба механизма: VEGFR-3-зависимый и VEGFR-3-независимый. VEGF-A может напрямую индуцировать пролиферацию лимфатических эндотелиальных клеток, которая не опосредуется VEGFR-3 [23]. Этот лимфангиогенез также опосредуется VEGF-C, происходящим из макрофагов, с моделью воспалительного шва [24]. Баланс между прямым и косвенным эффектом в лимфангиогенезе, индуцированном VEGF-A, может зависеть от ситуации.Было подтверждено, что VEGF-C, мощный лимфангиогенный фактор, индуцирует лимфангиогенез роговицы [25]. VEGF-C156S, который является специфическим лигандом для VEGFR-3, также вызывает лимфангиогенез, а также ангиогенез в роговице [26]. Этот VEGFR-3-опосредованный лимфангиогенез может быть индуцирован прямым воздействием на лимфатический эндотелий, а также рекрутирование макрофагов. Фактор роста тромбоцитов (PDGF) вызывает лимфангиогенез роговицы посредством прямой стимуляции лимфатического эндотелия [27]. HGF также вызывает лимфангиогенез роговицы, который может частично блокироваться ингибированием VEGFR-3 [28].FGF-2, который является хорошо известным мощным ангиогенным фактором, может вызывать лимфангиогенез с помощью анализа микрокарманов роговицы [29]. Лимфангиогенез, индуцированный FGF-2, блокировался ингибированием VEGFR-3 [29]. Эти исследования предполагают, что каждый GF (фактор роста) имеет различную зависимость от передачи сигналов VEGFR-3 в лимфангиогенезе. Некоторые GF непосредственно вызывают пролиферацию или миграцию лимфатических эндотелиальных клеток, тогда как некоторые GF активируют VEGF-C / -D, чтобы активировать VEGFR-3 в лимфангиогенезе. Интересно, что анализ микрокарманов роговицы показывает, что низкая доза FGF-2 вызывает избирательный лимфангиогенез [30].Это наблюдение обеспечивает доказательство того, что рост лимфатических сосудов возможен без ангиогенеза. Однако подробный механизм FGF-2-опосредованного лимфангиогенеза был загадочным. Недавнее исследование с использованием роговицы мыши представило физиологическую экспрессию лимфатических сосудов без наличия кровеносных сосудов, что указывает на то, что ангиогенез и лимфангиогенез могут происходить независимо [25]. В исследовании у мышей с дефицитом FGF-2 обнаруживается значительно меньшее количество предсуществующих лимфатических отростков без влияния на ангиогенез в роговице по сравнению с их аналогами дикого типа [25].Следовательно, это предполагает, что лимфо- и ангиогенез могут происходить независимо.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
6.Генетическая гетерогенность лимфангиогенеза
Недавно две разные группы независимо друг от друга сообщили о генетической гетерогенности лимфангиогенеза роговицы у разных линий мышей с помощью модели роговичного шва и модели роговичного микрокармана [25, 34] (Рисунок 3). Это говорит о том, что неоднородность лимфатических сосудов роговицы показывает разные воспалительные реакции у пациентов. В сравнительном анализе лимфатических сосудов с различными штаммами, мыши nu / nu , у которых значительно снижено количество Т-клеток, показали аналогичное лимфатическое развитие и GF-индуцированный лимфангиогенез с другими штаммами, что позволяет предположить, что Т-клетки могут быть ненужными для лимфатической системы. развитие, а также индуцированный GF лимфангиогенез в роговице [25] (Рисунок 3).Модель воспаления наложенным швом также выявила различные представления о лимфангиогенезе. После воспаления роговицы патологический лимфангиогенез роговицы может регрессировать раньше, чем ангиогенные сосуды [17].
7. Взаимодействие между ангиогенезом и лимфангиогенезом
Как описано выше, лимфангиогенез и ангиогенез происходят согласованно [6]. Однако неизвестно, как кровеносные и лимфатические сосуды регулируют друг друга. Недавно было сообщено, что ангиогенные сосуды задерживают лимфангиогенез с помощью анализа микрокарманов роговицы [31].В ответ на VEGF-A лимфатические сосуды роговицы растут с задержкой по сравнению с кровеносными сосудами. Для лимфангиогенеза необходимы более высокие концентрации VEGF-A, чем для ангиогенеза. Уравновешенная временная и пространственная ассоциация ангио- и лимфангиогенеза указывает на взаимозависимость между кровеносными и лимфатическими сосудами. Протеолитически обработанный VEGF-C связывается с VEGFR-2 и активирует его. Повышенная регуляция VEGFR-2 в ангиогенных кончиках может улавливать VEGF-C, а захваченный VEGF-C не может достигать лимфангиогенеза из-за расстояния друг от друга от лимфатических сосудов [31].Это взаимодействие VEGF-C / VEGFR-2 может регулировать соотношение между ангио- и лимфангиогенезом. Задержка лимфангиогенеза может позволить иммунным клеткам дополнительное время в очагах воспаления, потому что иммунные клетки происходят из ангиогенных сосудов и выводятся через лимфангиогенные сосуды [35].
8. Макрофаги в лимфангиогенезе
Макрофаги хорошо изучены на предмет их роли в неоваскуляризации при различных заболеваниях глаз, включая кератит [36, 37], ангиогенез сетчатки [38, 39] и хориоидальную неоваскуляризацию [40, 41].Макрофаги участвуют в лимфангиогенезе роговицы двумя разными способами. Маруяма и др. показали, что макрофаги CD11b (+) инфильтрируют воспалительную роговицу и трансдифференцируются в лимфатический эндотелий, что способствует лимфангиогенезу [42]. Другая роль макрофагов заключается в обеспечении лимфангиогенных факторов. Во время воспаления роговицы инфильтрирующий макрофаг активирует передачу сигналов NF- κ B и секретирует нижестоящие цитокины (например, VEGF-A, -C и -D), чтобы вызвать лимфангиогенез роговицы [32].Ингибирование NF- κ B может блокировать лимфангиогенез роговицы, а также ангиогенез. В недавней статье был показан механизм инфильтрации макрофагов в участки лимфангиогенеза роговицы. Белок сосудистой адгезии-1 (VAP-1) представляет собой эндотелиальный гликопротеин, регулирующий трансмиграцию лейкоцитов [43, 44]. Ингибирование VAP-1 блокирует воспалительный лимфангиогенез роговицы за счет уменьшения инфильтрации макрофагами [33]. Недавно было обнаружено, что поляризация макрофагов (классический M1 по сравнению с альтернативно активированными макрофагами M2) регулирует различные воспалительные заболевания [45].Количество макрофагов с маркером M2 (+) в воспалительной роговице мышей, получавших ингибитор VAP-1, было значительно ниже, чем у мышей, получавших носитель [33]. Таким образом, макрофаги M2 могут играть важную роль в лимфангиогенезе роговицы. Однако необходимы дальнейшие исследования, чтобы понять роль поляризации макрофагов в лимфангиогенезе. VAP-1 может стать терапевтической мишенью для различных глазных заболеваний, связанных с лимфангиогенезом. Более того, недавний отчет показал, что антиангиогенный фактор тромбоспондин-1 (TSP-1) также является эндогенным антилимфангиогенным фактором [46].TSP-1 может подавлять производные макрофагов VEGF-C и VEGF-D путем лигирования CD36 на клетках. В результате TSP-1 может стать терапевтической молекулой для лимфангиогенеза роговицы.
9. Лимфангиогенез при заболеваниях роговицы
В роговице человека во время развития отсутствуют лимфатические сосуды [47]. Васкуляризация роговицы нарушает остроту зрения, тогда как лимфангиогенез роговицы — нет. Однако лимфангиогенез в роговице может модулировать иммунитет роговицы или воспаление. Все больше исследований лимфатического и лимфангиогенеза показали, что лимфатические сосуды играют важную роль в различных заболеваниях роговицы (Таблица 2).Инфекция роговицы, вызванная вирусом простого герпеса-1 (ВПГ-1), является основной причиной слепоты. Инфекция роговицы HSV-1 вызывает лимфангиогенез, и лимфатические сосуды роговицы сохраняются после разрешения инфекции (таблица 2). Лимфангиогенез, вызванный HSV-1, строго зависит от передачи сигналов VEGF-A / VEGFR-2, но не от лигандов VEGFR-3 [48]. Недавнее исследование также показало, что сухой глаз, воспалительное заболевание роговицы низкой степени, индуцирует лимфангиогенез за счет активации рекрутирования макрофагов VEGF и VEGFR и CD11b (+).Интересно, что лимфангиогенез роговицы при сухом глазу не сопровождает ангиогенез (таблица 2). Однако этот механизм не полностью изучен, и дальнейшие исследования должны включать оценку того, что лимфангиогенез может быть терапевтической мишенью для болезни сухого глаза [49].
| |||||||||||||||||||||||||
