Бронхиальная астма: облегчить симптомы
05.05.2020
5 мая отмечается Всемирный день борьбы с бронхиальной астмой.
Бронхиальная астма на сегодня является одним из самых распространенных заболеваний, как среди взрослого населения, так и среди детей. Сегодня в мире астмой страдает 235 миллионов человек. При этом за последние годы число заболевших существенно увеличилось.
В Челябинской области проживает более 30 тысяч астматиков.
Признаками астмы не обязательно являются свистящее дыхание и удушье. Больной также может жаловаться на тяжесть в грудной клетке, сухой кашель, хрипы, затрудненное дыхание, бледность. Симптомы могут усиливаться ночью или рано утром. У детей астма обычно начинается с часто повторяющихся бронхитов на фоне простудных заболеваний, а также частых острых респираторных заболеваний, и получающих необоснованные курсы антибиотикотерапии.
Развитие астмы начинается с частых вирусных инфекций. Здесь важно вовремя выявить аллергическую направленность заболевания и найти причинно-значимый аллерген, чтобы избежать развития осложнений.
Как проводится диагностика астмы?
При осмотре пациента врач ориентируется, в основном, на клиническую картину заболевания, а также оценивается уровень эозинофилов в крови и мокроте, историю развития заболевания, связь с аллерго (сезонное) обострение, связь с приемом пищи, медикаментами, животными, бытовой фактор. Проводится исследование функции внешнего дыхания с помощью спирографии и дополнительно выявляются причинно-значимые аллергены по крови.
Каковы причины возникновения заболевания?
Причины возникновения астмы еще недостаточно ясны медикам. Здесь имеет значение, как наследственная предрасположенность, так и внешние факторы: воздействие аллергенов, частые вирусные болезни, неправильный образ жизни, условия окружающей среды, социальная принадлежность. У детей главным толчком к развитию заболевания становятся аллергия и частые болезни. Особое внимание хочется обратить на курение. Если родители курят возле ребенка или в доме, они должны осознавать, что вся вина за учащение приступов астмы у ребенка ложится на них.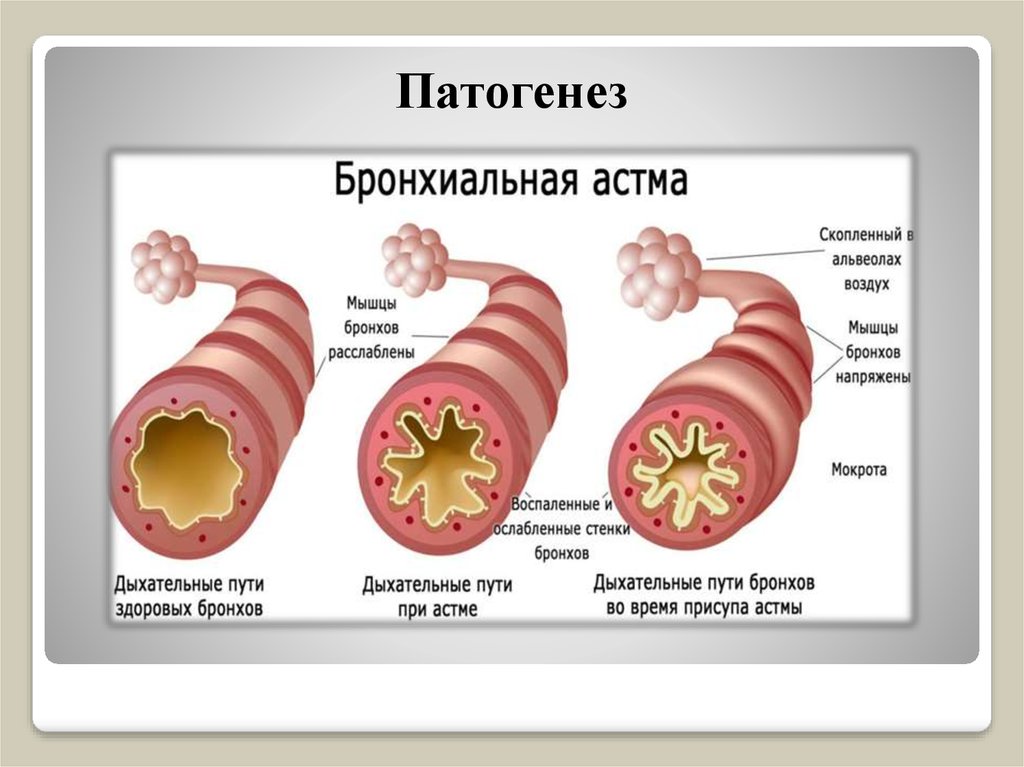
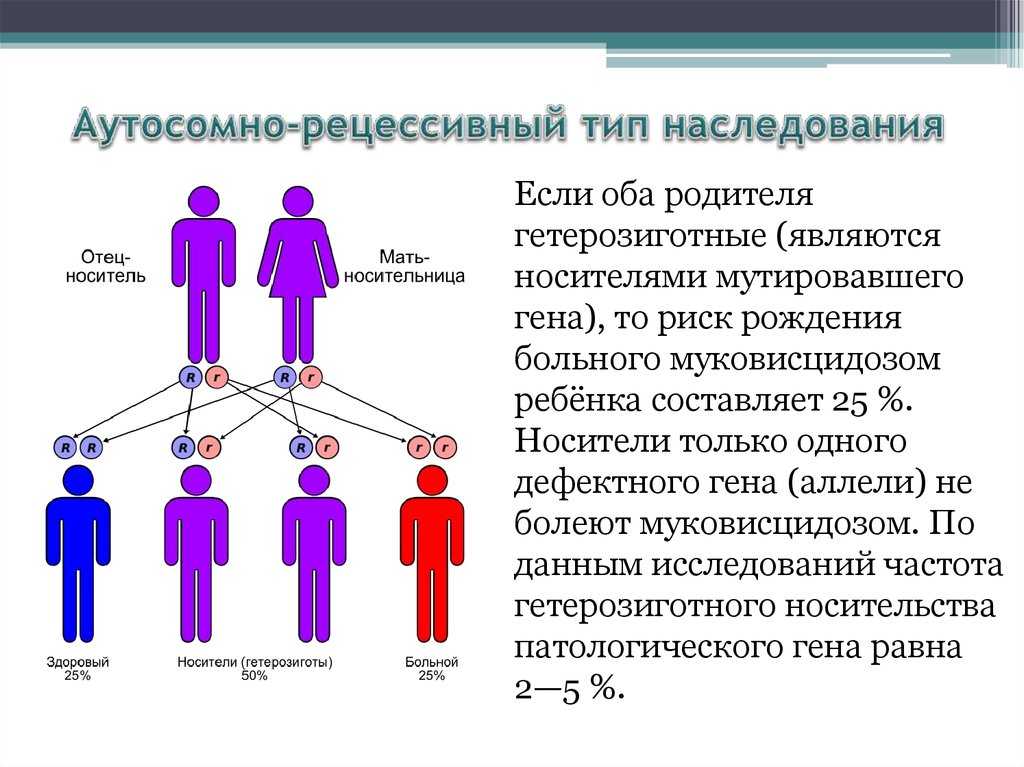
Астма всегда передается по наследству?
Если у кого-то из родственников есть астма, то вероятность заболеть у следующего поколения достаточно высока. Но у некоторых больных с бронхиальной астмой в родне ею никто не страдает, и, наоборот, не у всех родителей с астмой появляются больные дети. Причины такого явления еще не выявлены.
Аллергия является обязательной «спутницей» астмы? Как они связаны друг с другом.
Аллергия является ключевым фактором при формировании астмы, но не обязательным. Появление астмы при аллергии провоцирует постоянное воспаление дыхательных путей. Например, началом развития болезни могут послужить: курение, промышленный фактор, пищевые аллергены, частые вирусные и бактериальные. С возрастом опасными становятся уже ингаляционные аллергены – клещ домашней пыли, аллергены животных и птиц, пыльцевые и грибковые аллергены.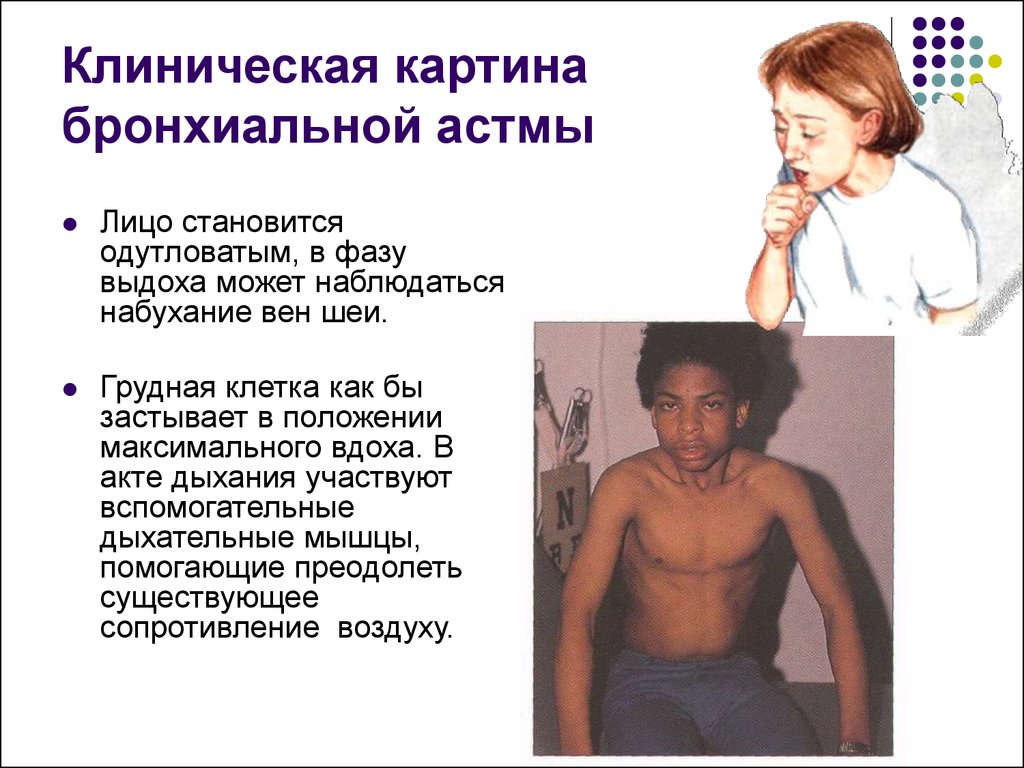
Излечима ли астма?
Астма – это хроническое заболевание, избавиться от него нельзя, можно лишь увеличить срок ремиссии и улучшить качество жизни пациента. При этом нередки случаи, когда ребенок с бронхиальной астмой в подростковом возрасте просто «перерастает» ее, она исчезает, но может снова возникнуть уже в более зрелом возрасте. Особенно часто это встречается у мальчиков.
Поэтому у школьников особенно важно проводить качественное лечение и профилактику бронхиальной астмы и аллергии, чтобы облегчить их течение во взрослой жизни. Своевременная диагностика, адекватное лечение и налаживание быта позволяют добиться значительного улучшения жизни пациентов
с астмой.
Какие методы лечения астмы существуют?
Врач индивидуально подбирает базисную терапию с учетом тяжести заболевания. Она может быть в форме ингаляций или таблеток. Препараты помогают достичь длительной ремиссии и предупредить обострения. Противовоспалительные препараты могут использоваться также и для профилактики развития приступов, поскольку воспалительный процесс в бронхах идет и в период ремиссии. Кроме того, больной и его близкие должны знать, как действовать в случае приступа.
Какие существуют немедикаментозные методы борьбы с астмой?
Такие методы существуют, но они применяются только в совокупности с лекарственной терапией. В первую очередь, необходимо создать для больного гипоаллергенный быт и питание. Ежедневно проводить дома влажную уборку, прогулки на природе. Категорически запрещено курить.

Для развития органов дыхания активно используется дыхательная гимнастика, которая учит больного спокойно и правильно дышать, астматикам полезно пение, игра на духовых музыкальных инструментах. Хорошо помогает массаж с вибрацией, он уменьшает бронхоспазм, помогает отделению мокроты и повышает выносливость дыхательной мускулатуры. Больным астмой показано санаторно-курортное лечение в горном климате, а также спелеотерапия, то есть лечение в специальных пещерах. Эффект даже от однократного горноклиматического лечения может сохраняться на протяжении 2-3 лет. Но важно, чтобы лечение длилось не менее месяца, поскольку адаптация организма к новому климату проходит примерно в течение 10 дней и в этот период состояние больного может ухудшиться.
Можно ли делать прививки больным астмой.
Прививки пациентам, страдающим астмой, можно ставить только в период ремиссии не менее 4 недель, а также при отсутствии острых заболеваний и аллергии на компоненты конкретной вакцины. При этом необходимо продолжать плановую базисную терапию.
Какая физическая нагрузка показана астматикам?
При правильно подобранной базисной терапии бронхиальная астма не должна препятствовать занятиям спортом. В западных странах спортсмены с астмой участвуют даже в олимпийских играх. Приступы бронхоспазма может вызвать бег, особенно на холодном воздухе и в горной местности. При этом реакция может возникнуть, как сразу же после нагрузки, так и через 3-6 часов. Для больных астмой очень полезна лечебная физкультура. Специальные техники дыхания и релаксации могут существенно облегчить состояние пациента. Астматикам также показано плавание и спокойная ходьба, но не в сырую и влажную погоду.
Возможна ли профилактика астмы?
Если у кого-то из родственников есть аллергическое заболевание. Стоит обратить внимание на организацию быта, максимально ограничить ребенка от всевозможных бытовых и промышленных аллергенов. Дети и подростки, проживающие в городе Челябинске, могут получить консультацию врача аллерголога-иммунолога, в рамках Территориальной программы государственных гарантий оказания бесплатной медицинской помощи жителям Челябинской области медицинскую помощь по специальности «аллергология-иммунология» в — 14 детских поликлиниках (МБУЗ ДГКП №1, ДГП №3, ДГП №4, ДГП №5, ДГП №7, ДГП №8, ДГП № 9, ДГП №11 , ДГКБ №1, ДГКБ №2, ДГКБ №7, ДГКБ № 8, ДГКБ №9, ГБУЗ ОКБ № 2).
В городской клинической больнице регулярно проходят профилактические акции и занятия в «Астма-школе» и «Школе ХОБЛ», постоянно работает «Кабинет отказа от курения» (ул. Воровского, 16, кабинет №345 с понедельника по пятницу с 9-00 до 12-00).
В городской клинической больнице № 1 организован городской аллергологический кабинет, ведет прием врач-пульмонолог, врач-аллерголог.
О режиме работы врача аллерголога-иммунолога можно узнать по телефону единого колл-центра ГКБ №1: 8 (351) 728-49-99.
Специализированную стационарную медицинскую помощь по направлению «аллергология-иммунология» оказывают детям и подросткам, жителям города Челябинска, в детском аллергологическом отделении МАУЗ ОТКЗ ГКБ №1.
В период обострения взрослые больные направляются в пульмонологическое отделение терапевтического стационара, в детское аллергологическое отделение стационара педиатрии. Пациенты направляются врачом — пульмонологом, аллергологом поликлиники или в ситуациях требующих экстренного оказания медицинской помощи врачом скорой медицинской помощи или неотложной медицинской помощи.
Назад к списку статей
Астма
Астма- Вопросы здравоохранения »
- A
- Б
- В
- Г
- Д
- Е
- Ё
- Ж
- З
- И
- К
- Л
- М
- Н
- О
- П
- Р
- С
- Т
- У
- Ф
- Х
- Ц
- Ч
- Ш
- Щ
- Ъ
- Ы
- Ь
- Э
- Ю
- Я
- Популярные темы
- Загрязнение воздуха
- Коронавирусная болезнь (COVID-19)
- Гепатит
- Данные и статистика »
- Информационный бюллетень
- Факты наглядно
- Публикации
- Найти страну »
- А
- Б
- В
- Г
- Д
- Е
- Ё
- Ж
- З
- И
- Й
- К
- Л
- М
- Н
- О
- П
- Р
- С
- Т
- У
- Ф
- Х
- Ц
- Ч
- Ш
- Щ
- Ъ
- Ы
- Ь
- Э
- Ю
- Я
- ВОЗ в странах »
- Репортажи
- Регионы »
- Африка
- Америка
- Юго-Восточная Азия
- Европа
- Восточное Средиземноморье
- Западная часть Тихого океана
- Центр СМИ
- Пресс-релизы
- Заявления
- Сообщения для медиа
- Комментарии
- Репортажи
- Онлайновые вопросы и ответы
- События
- Фоторепортажи
- Case studies
- Вопросы и ответы
- Выступления
- Последние сведения
- Чрезвычайные ситуации »
- Новости »
- Новости о вспышках болезней
- Данные ВОЗ »
- Приборные панели »
- Приборная панель мониторинга COVID-19
- Основные моменты »
- Информация о ВОЗ »
- Генеральный директор
- Информация о ВОЗ
- Деятельность ВОЗ
- Где работает ВОЗ
- Руководящие органы »
- Всемирная ассамблея здравоохранения
- Исполнительный комитет
- Главная страница/
- Центр СМИ/
- Информационные бюллетени/
- Подробнее/
- Астма
ВОЗ/M. Kokic
Kokic
© Фото
Основные факты- Астма является одним из основных неинфекционных заболеваний (НИЗ), которым страдают как дети, так и взрослые.
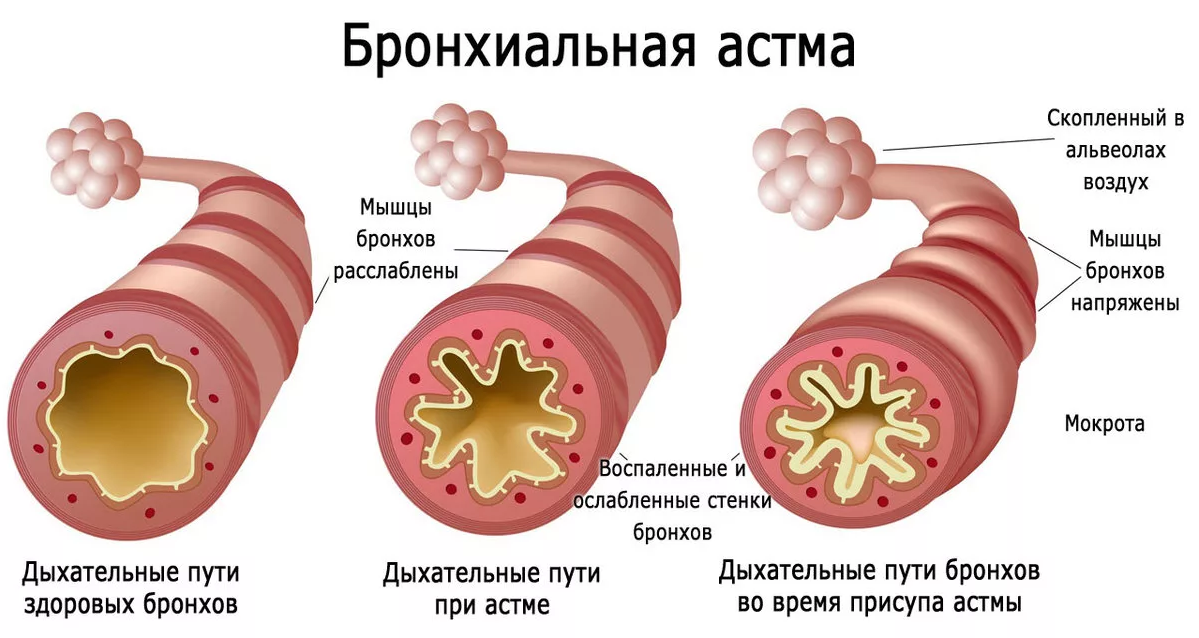
- Воспаление и сужение малых дыхательных путей в легких вызывают симптомы астмы, которыми могут являться кашель, хрип, одышка и чувство сдавленности в груди в любой комбинации.
- По имеющимся оценкам, в 2019 г. число больных астмой составило 262 миллиона человек, и было зарегистрировано 461 000 случаев смерти от этой болезни (1).
- Астма является одним из наиболее распространенных хронических заболеваний у детей.
- Ингаляционные препараты могут облегчать симптомы астмы и позволять людям с астмой вести нормальную, активную жизнь.
- Исключение факторов, провоцирующих приступы астмы, также может помочь уменьшить симптомы астмы.
- Большинство случаев смерти, связанных с астмой, происходят в странах с низким и средним уровнем дохода, где показатели выявления и лечения астмы находятся на недостаточно высоком уровне.
- ВОЗ стремится улучшить диагностику, лечение и мониторинг астмы, уменьшить глобальное бремя НИЗ и добиться прогресса на пути к всеобщему охвату услугами здравоохранения.
Что такое астма?
Астма является хроническим заболеванием, которым страдают как дети, так и взрослые. Воздушные каналы в легких сужаются из-за воспаления и сжимания мышц вокруг малых дыхательных путей. Это вызывает симптомы астмы – кашель, хрип, одышку и чувство
сдавленности в груди. Эти симптомы носят эпизодический характер и часто усугубляются в ночное время или во время физической нагрузки. Симптомы астмы могут усугубляться и под воздействием других распространенных «провоцирующих факторов».
Такими провоцирующими факторами у разных людей могут служить вирусные инфекции (простуда), пыль, дым, пары, изменения погоды, пыльца трав и деревьев, шерсть животных и перья птиц, сильнопахнущее мыло и духи.
Показатели выявления и лечения астмы находятся на недостаточно высоком уровне, особенно в странах с низким и средним уровнем дохода.
У больных астмой, не получающих надлежащего лечения, могут развиваться нарушения сна, усталость в течение дня и низкая концентрация внимания. Больные астмой и их семьи могут пропускать занятия в школе и не выходить на работу, что приводит к финансовым последствиям для семьи и общества в целом. Если симптомы являются тяжелыми, людям, страдающим астмой, может потребоваться неотложная медицинская помощь, и они могут быть помещены в больницу для лечения и мониторного наблюдения. В наиболее тяжелых случаях астма может привести к смерти.
Причины астмыПовышенный риск развития астмы связывают с большим числом различных факторов, хотя установить единственную непосредственную причину заболевания бывает трудно.
- Вероятность астмы возрастает при наличии астматиков в семье, особенно среди близких родственников – родителей или братьев/сестер.
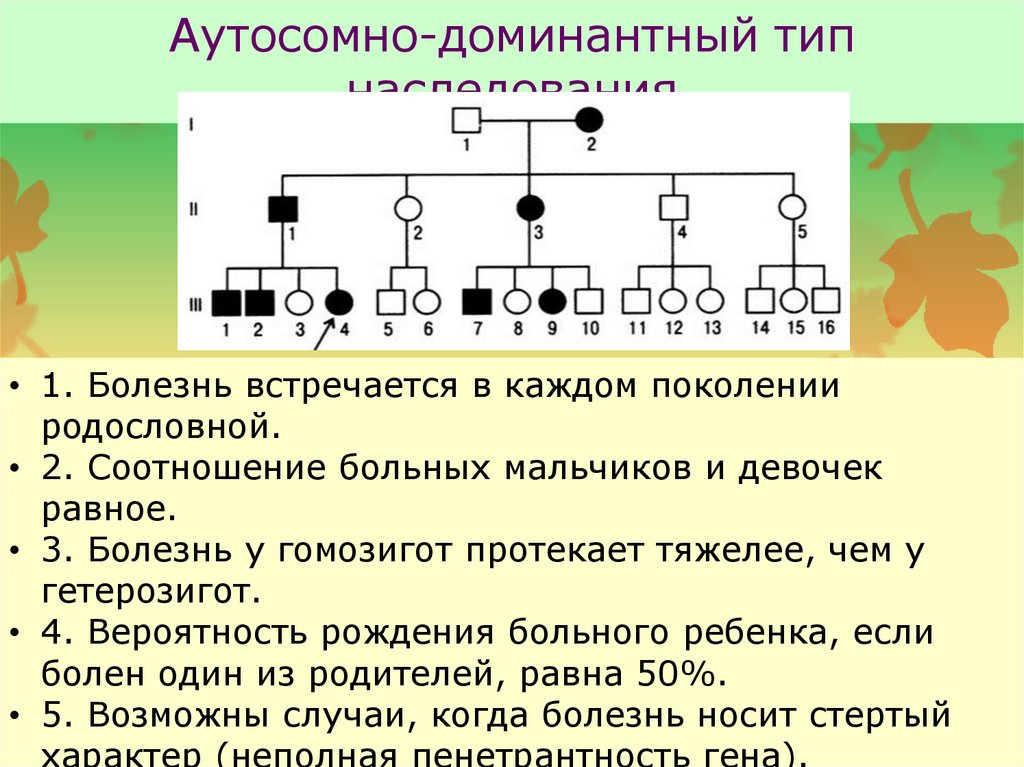
- Астма чаще развивается у людей, страдающих другими аллергическими заболеваниями, в частности экземой и ринитом (сенной лихорадкой).
- Распространенность астмы возрастает в условиях урбанизации, возможно, из-за воздействия множественных факторов, связанных с образом жизни.
- Нарушения на раннем этапе жизни влияют на развитие легких и могут повышать риск астмы. К ним относятся низкая масса тела при рождении, недоношенность, воздействие табачного дыма и других источников загрязнения воздуха, а также вирусные респираторные инфекции.
- Предполагается также, что риск астмы увеличивается при контакте с целым рядом аллергенов и раздражающих веществ, присутствующих в окружающей среде, в том числе при загрязнении воздуха в помещениях и атмосфере, присутствии клещей домашней пыли, плесени, а также при контакте с химическими веществами, выхлопными газами или пылью на производстве.
- Повышенному риску развития астмы подвергаются дети и взрослые с избыточной массой тела или ожирением.
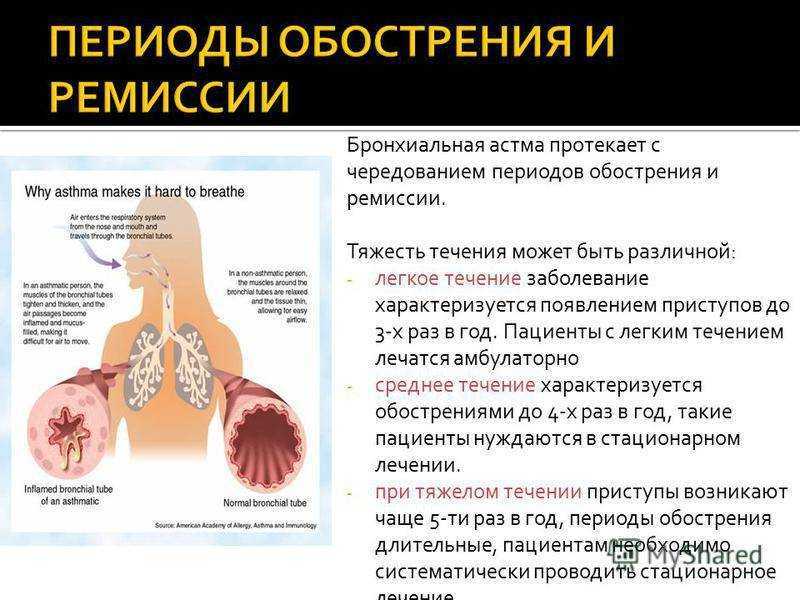
Несмотря на то, что астму нельзя излечить, надлежащее ведение пациентов с помощью ингаляционных препаратов позволяет людям с астмой держать болезнь под контролем и вести нормальную, активную жизнь.
Существует два основных типа ингаляторов:
- бронходилататоры (например, сальбутамол), которые расширяют дыхательные пути и облегчают симптомы; и
- стероиды (такие как беклометазон), которые уменьшают воспаление в дыхательных путях. Это облегчает симптомы астмы и снижает риск тяжелых приступов астмы и смерти.
Людям, страдающим астмой, может потребоваться использовать ингалятор ежедневно. Их лечение будет зависеть от частоты симптомов и имеющихся типов ингаляторов.
Координация дыхания при использовании ингалятора может являться сложной задачей, особенно для детей и в чрезвычайных ситуациях. Применение специального устройства облегчает использование аэрозольного ингалятора и помогает лекарству более эффективно достигать
легких. Спейсер представляет собой пластиковый контейнер с загубником или маской на одном конце и отверстием для ингалятора на другом. Самодельный спейсер, изготовленный из пластиковой бутылки объемом 500 мл, может быть столь же эффективным,
как и ингалятор промышленного производства.
Спейсер представляет собой пластиковый контейнер с загубником или маской на одном конце и отверстием для ингалятора на другом. Самодельный спейсер, изготовленный из пластиковой бутылки объемом 500 мл, может быть столь же эффективным,
как и ингалятор промышленного производства.
Доступ к ингаляторам является проблемой во многих странах. В 2019 г. лишь половина больных астмой имели доступ к бронходилататорам и менее 20% – к стероидным ингаляторам в государственных учреждениях первичной медико-санитарной помощи в странах с низким уровнем дохода (2).
Люди, страдающие астмой, и их семьи нуждаются в просвещении, с тем чтобы они лучше понимали, что такое астма, как ее лечить, как избежать и как справляться с симптомами этой болезни дома. Важно также повышать уровень осведомленности населения и в ряде случаев бороться с мифами и стигматизацией, связанных с астмой.
Стратегия ВОЗ в области профилактики астмы и борьбы с нейАстма включена в Глобальный план действий ВОЗ по профилактике НИЗ и борьбе с ними, а также в принятую Организацией Объединенных Наций Повестку дня в области устойчивого развития на период до 2030 г.
ВОЗ принимает целый ряд мер по расширению масштабов диагностики и лечения астмы.
В целях повышения эффективности ведения НИЗ в учреждениях первичной медико-санитарной помощи в условиях низкой обеспеченности ресурсами был разработан Пакет основных мер ВОЗ в отношении неинфекционных заболеваний (PEN). Пакет PEN включает протоколы оценки, диагностики и лечения хронических респираторных заболеваний (астмы и хронической обструктивной болезни легких), а также модули для консультирования по вопросам здорового образа жизни, включая отказ от употребления табака и самопомощь.
Снижение воздействия табачного дыма имеет важное значение как для первичной профилактики астмы, так и для лечения этой болезни. Достижению прогресса в этой области способствует Рамочная конвенция по борьбе против табака, а также такие инициативы ВОЗ, как MPOWER и mTobacco cessation.
Глобальный альянс по борьбе с хроническими респираторными болезнямиГлобальный альянс по борьбе с хроническими респираторными болезнями (ГАХРБ) вносит вклад в работу ВОЗ по профилактике хронических респираторных болезней и борьбе с ними. Это добровольный альянс национальных и международных организаций и учреждений из
многих стран, приверженных идее мира, в котором все люди могут дышать свободно.
Это добровольный альянс национальных и международных организаций и учреждений из
многих стран, приверженных идее мира, в котором все люди могут дышать свободно.
Библиография
1. Global burden of 369 diseases and injuries in 204 countries and territories, 1990-2019: a systematic analysis for the Global Burden of Disease Study 2019. Lancet. 2020;396(10258):1204-22 https://www.thelancet.com/gbd/summaries
2. Assessing national capacity for the prevention and control of noncommunicable diseases: report of the 2019 global survey. Geneva: World Health Organization; 2020. Licence: CC BY-NC-SA 3.0 IGO https://www.who.int/teams/ncds/surveillance/monitoring-capacity/ncdccs
Генетика астмы: введение для клинициста
Eur Clin Respir J. 2015; 2: 10.3402/ecrj.v2.24643.
Опубликовано в Интернете 16 января 2015 г. doi: 10.3402/ecrj.v2.24643
Информация об авторе Примечания к статье Сведения об авторских правах и лицензии Отказ от ответственности
Астма передается по наследству, и дети родителей, страдающих астмой, подвержены повышенному риску астмы.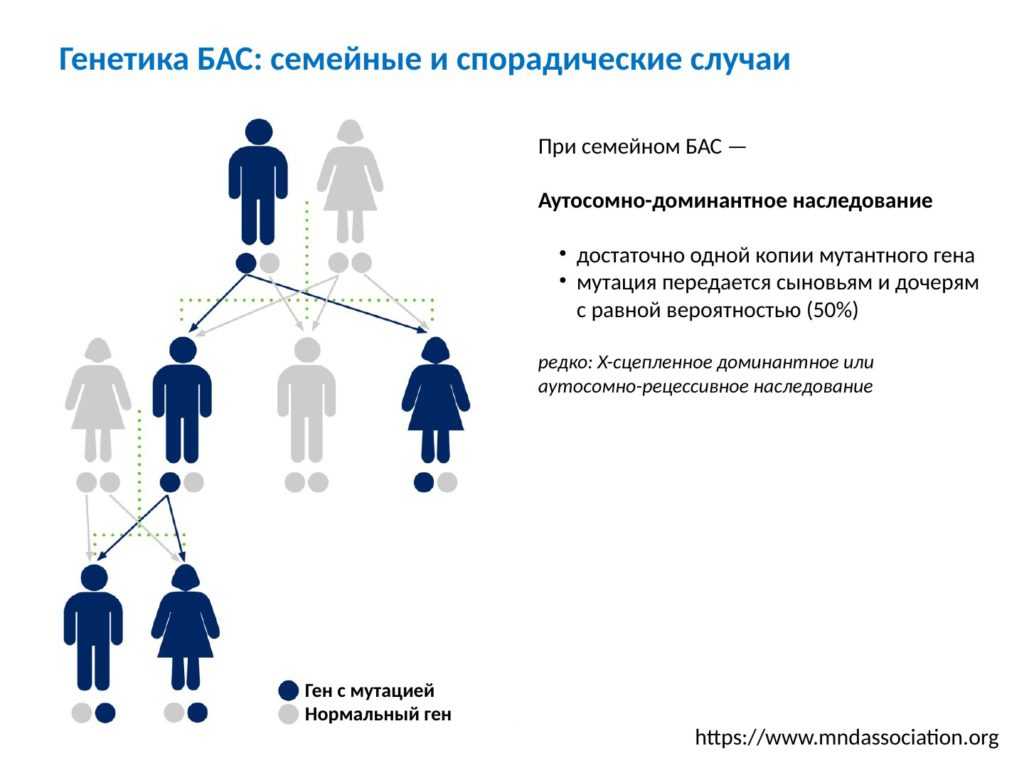 Прогнозирование риска заболевания имеет решающее значение для клинициста при консультировании семей с атопией. Однако это не всегда простая задача, учитывая обширные и постоянно расширяющиеся знания о генетике астмы. Появление новых технологий генотипирования позволило очень подробно секвенировать геном человека на наличие вариантов, связанных с астмой, и, соответственно, в последние десятилетия произошел взрыв числа редких и распространенных вариантов, связанных с риском заболевания. В этом обзоре представлен обзор методов и достижений в области генетики астмы, призванный помочь клиницисту отслеживать наиболее важные знания в этой области.
Прогнозирование риска заболевания имеет решающее значение для клинициста при консультировании семей с атопией. Однако это не всегда простая задача, учитывая обширные и постоянно расширяющиеся знания о генетике астмы. Появление новых технологий генотипирования позволило очень подробно секвенировать геном человека на наличие вариантов, связанных с астмой, и, соответственно, в последние десятилетия произошел взрыв числа редких и распространенных вариантов, связанных с риском заболевания. В этом обзоре представлен обзор методов и достижений в области генетики астмы, призванный помочь клиницисту отслеживать наиболее важные знания в этой области.
Ключевые слова: ассоциативный анализ , астма, эпигенетика, генетика, генетическая эпидемиология, открытие генов, анализ сцепления, фармакогенетика
Давно известно, что астма передается по наследству и что дети родителей-астматиков подвержены повышенному риску астмы. Однако астма не вызывается единичной мутацией в одном гене, и поэтому передача болезни через поколения не следует простому менделевскому наследованию, характерному для классических моногенных заболеваний, таких как болезнь Хантингтона (аутосомно-доминантный) или серповидно-клеточная анемия (аутосомно-доминантный). рецессивный). Скорее, астма является полигенным, многофакторным заболеванием, что означает, что многие факторы способствуют ее развитию. Эти факторы являются как генетическими, так и экологическими; соответственно, совместное действие нескольких генов, взаимодействующих друг с другом и с факторами окружающей среды, вызывает состояние (1).
рецессивный). Скорее, астма является полигенным, многофакторным заболеванием, что означает, что многие факторы способствуют ее развитию. Эти факторы являются как генетическими, так и экологическими; соответственно, совместное действие нескольких генов, взаимодействующих друг с другом и с факторами окружающей среды, вызывает состояние (1).
Характерной чертой многофакторных расстройств является то, что риск заболевания у человека зависит от степени генетического родства между этим человеком и родственником с заболеванием. Кроме того, риск обычно выше, если родственник тяжело поражен или если родственник заболел в раннем возрасте. В отличие от нарушений с одним геном, фенотип астмы выражен нелинейно и сильно варьирует. Это затрудняет прогнозирование статуса астмы для данного генотипа или комбинации генотипов.
Анализ населения дает представление о том, что астма является наследственным признаком. Во-первых, существуют большие географические и расовые различия в заболеваемости. Например, распространенность астмы во многих западных популяциях высока, до 20%, в то время как в популяциях развивающихся стран показатели распространенности гораздо ниже, некоторые из них составляют всего 1% или даже ниже (2). Это указывает только на генетическую причину астмы, поскольку разные популяции также имеют очень разные экологические условия. Во-вторых, потомство родителей-астматиков подвержено повышенному риску заболевания астмой (4). Риск рецидива астмы у детей с одним больным родителем составляет около 25%, тогда как риск, если оба родителя страдают, составляет около 50%. Исследования близнецов также подтверждают, что астма гораздо чаще возникает у человека, если у этого человека есть генетически близкий родственник с этим заболеванием. Например, риск рецидива астмы у монозиготных близнецов намного выше, чем у дизиготных близнецов, что подчеркивает роль генетических факторов риска развития астмы (3). Тем не менее тот факт, что конкордантность по астме у монозиготных близнецов составляет не 100%, а около 75%, указывает на то, что факторы риска окружающей среды также играют важную роль.
Например, распространенность астмы во многих западных популяциях высока, до 20%, в то время как в популяциях развивающихся стран показатели распространенности гораздо ниже, некоторые из них составляют всего 1% или даже ниже (2). Это указывает только на генетическую причину астмы, поскольку разные популяции также имеют очень разные экологические условия. Во-вторых, потомство родителей-астматиков подвержено повышенному риску заболевания астмой (4). Риск рецидива астмы у детей с одним больным родителем составляет около 25%, тогда как риск, если оба родителя страдают, составляет около 50%. Исследования близнецов также подтверждают, что астма гораздо чаще возникает у человека, если у этого человека есть генетически близкий родственник с этим заболеванием. Например, риск рецидива астмы у монозиготных близнецов намного выше, чем у дизиготных близнецов, что подчеркивает роль генетических факторов риска развития астмы (3). Тем не менее тот факт, что конкордантность по астме у монозиготных близнецов составляет не 100%, а около 75%, указывает на то, что факторы риска окружающей среды также играют важную роль.
Таблица 1
Рецидив риск астмы
| Потрошенный | . | 10 |
|---|---|---|
| Half Birtch | 10 | |
| Полный сестры | 25 | |
| Один родитель | 25 | .0037 | 35 |
| Два родителя | 50 | |
| Монозиготический двойник | 75 |
 фенотипическое проявление астмы может быть изменено другими генетическими факторами и факторами окружающей среды. Считается, что небольшое количество генов задает индивидуальный фоновый риск, на который воздействует другой набор модифицирующих генов, а также факторы окружающей среды. Например, люди с ранним началом астмы чаще имеют семейный анамнез астмы, чем люди с поздним началом астмы, что позволяет предположить, что гены влияют на возраст начала заболевания (4). Кроме того, тяжесть астмы, судя по частоте симптомов, уровню функции легких, степени реактивности дыхательных путей и воспалению дыхательных путей, накапливается в пределах семьи, что позволяет предположить, что если у человека есть положительный семейный анамнез тяжелой астмы, этот человек с большей вероятностью для развития тяжелой астмы (5).
фенотипическое проявление астмы может быть изменено другими генетическими факторами и факторами окружающей среды. Считается, что небольшое количество генов задает индивидуальный фоновый риск, на который воздействует другой набор модифицирующих генов, а также факторы окружающей среды. Например, люди с ранним началом астмы чаще имеют семейный анамнез астмы, чем люди с поздним началом астмы, что позволяет предположить, что гены влияют на возраст начала заболевания (4). Кроме того, тяжесть астмы, судя по частоте симптомов, уровню функции легких, степени реактивности дыхательных путей и воспалению дыхательных путей, накапливается в пределах семьи, что позволяет предположить, что если у человека есть положительный семейный анамнез тяжелой астмы, этот человек с большей вероятностью для развития тяжелой астмы (5). Существуют различные экспериментальные подходы к установлению связи между геном и таким заболеванием, как астма. Двумя основными вариантами являются анализ генетического сцепления и анализ генетической (аллельной) ассоциации (6). Анализ сцепления полезен для охвата более крупных областей генома, в которых, вероятно, находится ген предрасположенности, тогда как анализ ассоциации можно использовать для идентификации конкретных генотипов, например однонуклеотидных полиморфизмов (SNP), которые непосредственно связаны с риском заболевания. .
Анализ сцепления полезен для охвата более крупных областей генома, в которых, вероятно, находится ген предрасположенности, тогда как анализ ассоциации можно использовать для идентификации конкретных генотипов, например однонуклеотидных полиморфизмов (SNP), которые непосредственно связаны с риском заболевания. .
Анализ сцепления
Анализ сцепления проводится в пораженных семьях и использует тот факт, что определенные генетические локусы или аллели, находящиеся в непосредственной близости на одной и той же хромосоме, имеют тенденцию наследоваться вместе, то есть оставаться вместе во время мейоза. Предпосылкой анализа сцепления является использование генетических маркеров (последовательности ядерной ДНК с известным расположением в геноме), расположенных вдоль хромосомы. Таким образом, если заболевание часто передается потомству вместе со специфическими маркерами, то можно сделать вывод, что ген(ы), вызывающие заболевание, расположен на хромосоме близко к этим маркерам. В этом случае важно отметить, что, хотя многофакторные расстройства, такие как астма и аллергия, регулируются многими генетическими локусами, действующими согласованно, способ наследования может быть сведен к менделевскому наследованию в каждом из этих локусов. Следовательно, анализ специфических генов астмы и аллергии основан на тех же принципах, что и анализ моногенных признаков. Генетический анализ сцепления выявил множество участков генома, связанных с астмой и аллергией. Некоторые из самых ранних генетических исследований этих заболеваний, проведенных в 19 в.В 80-х и 1990-х годах использовался анализ сцепления (7). Однако анализ сцепления идентифицирует относительно большие области хромосомы в зависимости от геномного расстояния между маркерами, и такой большой фрагмент ДНК может легко содержать 10 генов предполагаемой важности. Например, область 5q31–32, которая во многих исследованиях была связана с атопическими заболеваниями, содержит гены IL4 , IL13 , CD14 и SPINK5 , которые связаны с активностью Т-клеток и морфогенезом кожи.
В этом случае важно отметить, что, хотя многофакторные расстройства, такие как астма и аллергия, регулируются многими генетическими локусами, действующими согласованно, способ наследования может быть сведен к менделевскому наследованию в каждом из этих локусов. Следовательно, анализ специфических генов астмы и аллергии основан на тех же принципах, что и анализ моногенных признаков. Генетический анализ сцепления выявил множество участков генома, связанных с астмой и аллергией. Некоторые из самых ранних генетических исследований этих заболеваний, проведенных в 19 в.В 80-х и 1990-х годах использовался анализ сцепления (7). Однако анализ сцепления идентифицирует относительно большие области хромосомы в зависимости от геномного расстояния между маркерами, и такой большой фрагмент ДНК может легко содержать 10 генов предполагаемой важности. Например, область 5q31–32, которая во многих исследованиях была связана с атопическими заболеваниями, содержит гены IL4 , IL13 , CD14 и SPINK5 , которые связаны с активностью Т-клеток и морфогенезом кожи. (8, 9). Соответственно, чтобы иметь возможность локализовать сам ген, требуется более плотное картирование маркеров (точное картирование) или анализ аллельной ассоциации.
(8, 9). Соответственно, чтобы иметь возможность локализовать сам ген, требуется более плотное картирование маркеров (точное картирование) или анализ аллельной ассоциации.
Ассоциативный анализ
Ассоциативный анализ может проводиться как внутри семьи (семейная ассоциация), так и среди лиц, не состоящих в родстве, как правило, в популяции случай-контроль. В классическом смысле частоты генотипов среди больных людей, например, страдающих астмой, сравнивают с частотами генотипов в здоровой контрольной популяции (здоровые люди). Если частоты генов различаются между случаями и контролем, говорят, что аллели связаны с заболеванием. Классический анализ ассоциации генов-кандидатов основан на знании роли конкретного гена в регуляции патогенного процесса, например, связанного с репарацией клеток слизистой оболочки или иммунными механизмами. Расширение анализа аллельных ассоциаций, которое не требует предположений, составляет полногеномная ассоциация (GWA), где многочисленные генетические варианты, часто > 500 000 SNP, охватывающие весь геном, проверяются на связь с конкретным заболеванием. Было проведено несколько исследований астмы и аллергии GWA, в ходе которых был идентифицирован ряд генов-кандидатов (8, 9).
Было проведено несколько исследований астмы и аллергии GWA, в ходе которых был идентифицирован ряд генов-кандидатов (8, 9).
Более сотни различных генов связаны с астмой, и этот список продолжает расти. Гены предрасположенности к астме делятся в основном на три категории, связанные с 1) функционированием иммунной системы, 2) биологией и функцией слизистой оболочки и 3) функцией легких и проявлением болезни (8, 9).). Однако тот факт, что ген был связан с астмой в одном исследовании, не обязательно устанавливает связь между этим геном и заболеванием. Основной проблемой многих генетических исследований астмы является отсутствие повторения результатов предыдущих исследований. Примечательно, что более чем в одном исследовании было обнаружено, что только подмножество идентифицированных генов связано с астмой; и многие рассматривают репликацию как одну из наиболее важных характеристик гена-кандидата (8, 9). Однако некоторые гены могут быть важны только для подмножества астматиков, например, при астме с дебютом в детстве, атопической астме, астме, чувствительной к клещам домашней пыли, или профессиональной астме, и поэтому не всегда можно ожидать репликации в этих разных популяциях. Более того, некоторые гены экспрессируются только в определенных условиях окружающей среды, например, у детей, растущих с кошкой (10), или у тех, кто подвергается пассивному курению в первые годы жизни (11, 12). Не следует недооценивать важность взаимодействия генов и окружающей среды в возникновении астмы; роль каждого гена следует рассматривать в контексте благоприятной среды.
Более того, некоторые гены экспрессируются только в определенных условиях окружающей среды, например, у детей, растущих с кошкой (10), или у тех, кто подвергается пассивному курению в первые годы жизни (11, 12). Не следует недооценивать важность взаимодействия генов и окружающей среды в возникновении астмы; роль каждого гена следует рассматривать в контексте благоприятной среды.
ADAM33
Дезинтегрин и металлопротеиназа 33 ( ADAM33 ) были первым позиционно клонированным геном восприимчивости к астме, что означает, что его точное положение в геноме было определено до того, как стало известно о функции гена (13). ADAM33 расположен на хромосоме 20p13 и экспрессируется в гладкомышечных клетках бронхов и фибробластах легких. Когда он впервые был обнаружен в 2002 году, было показано, что он тесно связан как с астмой, так и с гиперреактивностью бронхов. Совсем недавно его роль была расширена за счет включения более тонких аспектов патогенеза астмы, таких как ремоделирование дыхательных путей, прогрессирование заболевания, а также хроническая обструктивная болезнь легких (14).
Филагрин
Филаггрин — это белок, который помогает поддерживать эффективный кожный барьер. Мутации потери функции в гене филаггрина, расположенном на хромосоме 1q21, сначала были связаны с вульгарным ихтиозом кожи (15), а совсем недавно с атопическим дерматитом (16). Мутации присутствуют у чуть менее 10% людей из западных популяций и до 50% людей с атопическим дерматитом. Он считается самой сильной генетической детерминантой атопического дерматита, увеличивая риск примерно в четыре раза (17). Более того, мутации филаггрина связаны с развитием аллергической сенсибилизации, сенной лихорадки и астмы, но только у пациентов с атопическим дерматитом (18). Интересно, что исследования показали, что дисфункция кожного барьера не только усиливает сенсибилизацию к аллергенам, но также приводит к системным аллергическим реакциям, таким как повышение уровня IgE и гиперреактивность дыхательных путей, что указывает на то, что абсорбция аллергенов через кожу у пациентов с атопическим дерматитом является необходимым условием. для развития других аллергических состояний, таких как астма и сенная лихорадка (19).
для развития других аллергических состояний, таких как астма и сенная лихорадка (19).
Крупнейшее исследование генетики астмы
Крупнейшее и наиболее полное исследование генетики астмы на сегодняшний день было проведено в 2010 г. консорциумом из более чем ста центров по всему миру (20). Они провели исследование GWA (исследование GABRIEL), в котором генотипировали 10 365 человек с астмой и 16 110 здоровых людей, чтобы проверить связь между 582 892 SNP и астмой. Это крупное исследование выявило гены на хромосомах 2 ( IL1RL1/IL18R1 ), 6 ( HLA-DQ ), 9 ( IL33 9).0096), 15 ( SMAD3 ), 17 ( ORMDL3/GSDMB ) и 22 ( IL2RB ), связанных с астмой. Ген ORMDL3 , в частности, был связан с началом заболевания в детстве, тогда как ген HLA-DQ был связан с более поздним началом астмы. Кроме того, результаты показали, что 38% всех случаев детской астмы были связаны с комбинацией идентифицированных генов.
Исследование также выявило связь между общим IgE в сыворотке и HLA-DRB1 в области класса II главного комплекса гистосовместимости (MHC) на хромосоме 6. Однако этот локус не был связан с астмой; большинство идентифицированных локусов предрасположенности к астме не были связаны с IgE, что позволяет предположить, что повышение уровня общего IgE в сыворотке играет лишь незначительную роль в развитии астмы.
Однако этот локус не был связан с астмой; большинство идентифицированных локусов предрасположенности к астме не были связаны с IgE, что позволяет предположить, что повышение уровня общего IgE в сыворотке играет лишь незначительную роль в развитии астмы.
Молекулярно-генетические исследования астмы внесли значительный вклад в понимание патогенеза и естественного течения болезни. Тем не менее, все усилия лишь в незначительной степени, если вообще были переведены, в новые методы лечения или модифицируемые варианты лечения астмы. В настоящее время очевидно, что астма регулируется многими генами, каждый из которых вносит лишь незначительный вклад в риск заболевания (21). Примечательно, что большинство известных генов предрасположенности к астме могут повышать риск заболевания примерно в 1,2 раза или даже меньше. Исследования GWA и глубокого секвенирования обещали стать «дизайном, который положит конец всем дизайнам», но эти исследования также подтвердили наши «худшие» ожидания: астма как генетически, так и фенотипически является очень гетерогенным заболеванием.
Секвенирование нового поколения и геномный анализ
Геном человека содержит около 21 000 генов. Недавнее полное секвенирование всего генома человека является знаменательным событием, оказавшим глубокое влияние на то, как мы будем диагностировать, лечить и, возможно, предотвращать ряд заболеваний в будущем. Тем не менее, проект «Геном человека» полагался только на несколько человек, и чтобы уловить более тонкие различия между людьми и создать «эталонный геном» для генетического анализа человека, Проект 1000 геномов был инициирован для секвенирования геномов большого числа людей и предоставления всестороннего ресурса генетической изменчивости человека (22). Основной проблемой для будущего использования этого ресурса является биоинформационная обработка и интерпретация такого большого объема данных, а также внедрение в клиническую практику и генетическое консультирование семей с аллергией.
Персонализированная медицина и фармакогенетика
Персонализированная медицина приобретает все большее значение в постгеномную эпоху. Идея персонализированной медицины состоит в том, чтобы предсказать, основываясь в основном на генетической информации, у каких пациентов будет наилучший ответ на лечение. По мере развития этой области станет возможным индивидуализировать фармакотерапию на основе генетических полиморфизмов, чтобы определенные лекарства назначались только тем пациентам, у которых наиболее высока вероятность ответа, а вредные эффекты избегались у пациентов, которые с наибольшей вероятностью испытают токсичность и побочные реакции. (23). Генами-кандидатами для таких исследований являются гены, кодирующие рецепторные белки и ферменты, участвующие в транспортировке, процессинге, деградации и выведении лекарств. Продолжающееся выяснение биологических путей, лежащих в основе астмы и аллергии, поможет определить новые возможные цели для вмешательства. Например, в рандомизированном исследовании экспериментального препарата, блокирующего путь ИЛ-4/ИЛ-13, определенные аминокислотные вариации в рецепторе ИЛ-4, по-видимому, предсказывали, у каких пациентов будет наилучший ответ на терапевтическое лечение с точки зрения улучшения функции легких (24).
Идея персонализированной медицины состоит в том, чтобы предсказать, основываясь в основном на генетической информации, у каких пациентов будет наилучший ответ на лечение. По мере развития этой области станет возможным индивидуализировать фармакотерапию на основе генетических полиморфизмов, чтобы определенные лекарства назначались только тем пациентам, у которых наиболее высока вероятность ответа, а вредные эффекты избегались у пациентов, которые с наибольшей вероятностью испытают токсичность и побочные реакции. (23). Генами-кандидатами для таких исследований являются гены, кодирующие рецепторные белки и ферменты, участвующие в транспортировке, процессинге, деградации и выведении лекарств. Продолжающееся выяснение биологических путей, лежащих в основе астмы и аллергии, поможет определить новые возможные цели для вмешательства. Например, в рандомизированном исследовании экспериментального препарата, блокирующего путь ИЛ-4/ИЛ-13, определенные аминокислотные вариации в рецепторе ИЛ-4, по-видимому, предсказывали, у каких пациентов будет наилучший ответ на терапевтическое лечение с точки зрения улучшения функции легких (24). ).
).
Эпигенетика и анализ экспрессии генов
Эпигенетика – это изучение наследственных изменений болезни, которые не вызваны изменениями в последовательности нуклеотидов самого генетического кода. Считается, что эпигенетические механизмы объясняют геномную адаптацию к различным воздействиям окружающей среды; Эпигенетические изменения могут способствовать развитию болезни, как и генетические изменения. В эпигенетическую модификацию вовлечено несколько молекулярных механизмов, например, метилирование ДНК, посттранскрипционная модификация гистонов и модификация некодирующих РНК. Считается, что эти изменения изменяют экспрессивность генов, что, в свою очередь, приводит к различиям в выраженности болезни у разных людей. Однако мало что известно об эпигенетических механизмах астмы и аллергии, и в настоящее время проводятся исследования для их разгадки (25). Изучение монозиготных близнецов, несовместимых по астме и аллергии, может дать ценную информацию, поскольку эпигенетические механизмы могут частично объяснить относительно высокую степень дискордантности между монозиготными близнецами по этим заболеваниям (26). Примечательно, что, поскольку оба монозиготных близнеца в паре близнецов имеют в принципе идентичные геномы, а также, как правило, в значительной степени разделяют факторы риска окружающей среды, вызывает недоумение тот факт, что во многих случаях только у одного близнеца развивается астма и аллергия, в то время как другой остается незатронутым. или затронуты в меньшей степени. Возможно, что воздействие окружающей среды, уникальное для отдельного близнеца, например комменсальная микрофлора, табачный дым в окружающей среде, диетические факторы и выхлопные газы, вызывают эпигенетические модификации, которые приводят к индивидуальным различиям в экспрессии генов и, следовательно, также в проявлении болезни. Экспрессию генов можно изучать в образцах живых тканей с помощью РНК-микрочипов. Возрастает интерес к активности генов, связанных с астмой и аллергией, поскольку степень экспрессии гена предрасположенности может влиять на клиническую тяжесть заболевания. Идентификация механизмов, лежащих в основе регуляции и экспрессии этих генов, может дать ключ к пониманию тонкого взаимодействия между окружающей средой и генетикой в развитии и прогрессировании астмы и аллергии.
Примечательно, что, поскольку оба монозиготных близнеца в паре близнецов имеют в принципе идентичные геномы, а также, как правило, в значительной степени разделяют факторы риска окружающей среды, вызывает недоумение тот факт, что во многих случаях только у одного близнеца развивается астма и аллергия, в то время как другой остается незатронутым. или затронуты в меньшей степени. Возможно, что воздействие окружающей среды, уникальное для отдельного близнеца, например комменсальная микрофлора, табачный дым в окружающей среде, диетические факторы и выхлопные газы, вызывают эпигенетические модификации, которые приводят к индивидуальным различиям в экспрессии генов и, следовательно, также в проявлении болезни. Экспрессию генов можно изучать в образцах живых тканей с помощью РНК-микрочипов. Возрастает интерес к активности генов, связанных с астмой и аллергией, поскольку степень экспрессии гена предрасположенности может влиять на клиническую тяжесть заболевания. Идентификация механизмов, лежащих в основе регуляции и экспрессии этих генов, может дать ключ к пониманию тонкого взаимодействия между окружающей средой и генетикой в развитии и прогрессировании астмы и аллергии.
Авторы не получали никакого финансирования или льгот от промышленности или других источников для проведения этого исследования.
1. Палмер Л.Дж., Куксон, WOCM. Атопия и астма. В: Бишоп Т., Шам П., редакторы. Анализ многофакторного заболевания. Оксфорд: БИОС; 2000. С. 215–37. [Google Scholar]
2. Asher MI, Montefort S, Björkstén B, Lai CK, Strachan DP, Weiland SK, et al. Мировые тенденции распространенности симптомов астмы, аллергического риноконъюнктивита и экземы в детском возрасте: ISAAC Phases One и Three повторяют многострановые перекрестные исследования. Ланцет. 2006; 368: 733–43. [PubMed] [Академия Google]
3. Thomsen SF, van der Sluis S, Kyvik KO, Skytthe A, Backer V. Оценки наследственности астмы в большой выборке близнецов. Клин Эксперт Аллергия. 2010;40:1054–61. [PubMed] [Google Scholar]
4. Томсен С.Ф., Даффи Д.Л., Кивик К.О., Бакер В. Генетическое влияние на возраст начала астмы: исследование близнецов. J Аллергия Клин Иммунол. 2010; 126: 626–30. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
5. Thomsen SF, van der Sluis S, Kyvik KO, Backer V. Исследование тяжести астмы у взрослых близнецов. Клин Респир Дж. 2012; 6: 228–37. [PubMed] [Академия Google]
6. McGuffin P, Owen MJ, Gottesman II. Психиатрическая генетика и геномика. Оксфорд: Издательство Оксфордского университета; 2002. [Google Scholar]
7. Cookson WO, Sharp PA, Faux JA, Hopkin JM. Связь между ответами иммуноглобулина Е, лежащими в основе астмы и ринита, и хромосомой 11q. Ланцет. 1989; 1:1292–5. [PubMed] [Google Scholar]
8. Bossé Y, Hudson TJ. На пути к полному набору генов предрасположенности к астме. Анну Рев Мед. 2007; 58: 171–84. [PubMed] [Академия Google]
9. Vercelli D. Открытие генов предрасположенности к астме и аллергии. Нат Рев Иммунол. 2008; 8: 169–82. [PubMed] [Google Scholar]
10. Bisgaard H, Simpson A, Palmer CN, Bønnelykke K, McLean I, Mukhopadhyay S, et al. Взаимодействие генов и окружающей среды при возникновении экземы в младенчестве: мутации потери функции филаггрина, усиленные воздействием неонатальной кошки. ПЛОС Мед. 2008;5:e131. [Бесплатная статья PMC] [PubMed] [Google Scholar]
ПЛОС Мед. 2008;5:e131. [Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Ramadas RA, Sadeghnejad A, Karmaus W, Arshad SH, Matthews S, Huebner M, et al. Ген антагониста интерлейкина-1R и внутриутробное воздействие дыма связаны с детской астмой. Евр Респир Дж. 2007; 29: 502–8. [Статья бесплатно PMC] [PubMed] [Google Scholar]
12. Садегнежад А., Кармаус В., Аршад С.Х., Курукулаарачи Р., Хюбнер М., Юарт С. Полиморфизмы гена IL13 изменяют влияние воздействия табачного дыма на стойкие хрипы и астму. в детстве лонгитюдное исследование. Дыхание Рез. 2008;9:2. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Holloway JW, Arshad SH, Holgate ST. Использование генетики для предсказания естественного течения астмы? J Аллергия Клин Иммунол. 2010;126:200–9. [PubMed] [Академия Google]
14. Aierken H, Wang J, Wushouer Q, Shayhidin E, Hu X, Syed I, et al. Полиморфизмы гена ADAM33 и риск хронической обструктивной болезни легких: метаанализ. Клин Респир Дж. 2014; 8: 108–15. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
15. Smith FJ, Irvine AD, Terron-Kwiatkowski A, Sandilands A, Campbell LE, Zhao Y, et al. Мутации с потерей функции в гене, кодирующем филаггрин, вызывают вульгарный ихтиоз. Нат Жене. 2006; 38: 337–42. [PubMed] [Google Scholar]
16. Palmer CN, Irvine AD, Terron-Kwiatkowski A, Zhao Y, Liao H, Lee SP, et al. Распространенные варианты белка эпидермального барьера филаггрина с потерей функции являются основным предрасполагающим фактором для атопического дерматита. Нат Жене. 2006; 38: 441–6. [PubMed] [Академия Google]
17. Ван ден Оорд Р.А., Шейх А. Дефекты гена филаггрина и риск развития аллергической сенсибилизации и аллергических расстройств: систематический обзор и метаанализ. БМЖ. 2009; 339:2433. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. Spergel JM. От атопического дерматита к астме: атопический марш. Энн Аллергия Астма Иммунол. 2010;105:99–106. [PubMed] [Google Scholar]
19. Де Бенедетто А., Кубо А., Бек Л. А. Нарушение кожного барьера: условие сенсибилизации аллергеном? Джей Инвест Дерматол. 2012;132:949–63. [Бесплатная статья PMC] [PubMed] [Google Scholar]
А. Нарушение кожного барьера: условие сенсибилизации аллергеном? Джей Инвест Дерматол. 2012;132:949–63. [Бесплатная статья PMC] [PubMed] [Google Scholar]
20. Moffatt MF, Gut IG, Demenais F, Strachan DP, Bouzigon E, Heath S, et al. Крупномасштабное консорциумное полногеномное исследование ассоциации астмы. N Engl J Med. 2010;363:1211–21. [Бесплатная статья PMC] [PubMed] [Google Scholar]
21. Гибсон Г. Деканализация и происхождение сложных заболеваний. Нат Рев Жене. 2009; 10: 134–40. [PubMed] [Google Scholar]
22. Консорциум проекта 1000 геномов. Abecasis GR, Auton A, Brooks LD, DePristo MA, Durbin RM, et al. Интегрированная карта генетической изменчивости от 1,092 генома человека. Природа. 2012; 491:56–65. [Бесплатная статья PMC] [PubMed] [Google Scholar]
23. Wechsler ME. Лечение астмы в 21 веке: роль фармакогенетики. Педиатр Энн. 2006; 35: 660–2. 664–9. [PubMed] [Google Scholar]
24. Slager RE, Hawkins GA, Ampleford EJ, Bowden A, Stevens LE, Morton MT, et al. Полиморфизмы альфа-рецептора ИЛ-4 являются предикторами фармакогенетической реакции на новый антагонист ИЛ-4/ИЛ-13. J Аллергия Клин Иммунол. 2010; 126:875–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Полиморфизмы альфа-рецептора ИЛ-4 являются предикторами фармакогенетической реакции на новый антагонист ИЛ-4/ИЛ-13. J Аллергия Клин Иммунол. 2010; 126:875–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Кабеш М., Мишель С., Тост Дж. Эпигенетические механизмы и связь с детской астмой. Eur Respir J. 2010; 36: 950–61. [PubMed] [Google Scholar]
26. Bell JT, Saffery R. Значение близнецов в эпигенетической эпидемиологии. Int J Эпидемиол. 2012;41:140–50. [PubMed] [Google Scholar]
Является ли астма генетической? Причины и факторы риска
Астма может быть генетической, хотя не все случаи астмы передаются по наследству. Астма имеет ряд других причин и факторов риска.
Астма — это хроническое заболевание легких, вызывающее воспаление дыхательных путей. Воспаление может вызвать отек дыхательных путей и сделать их очень чувствительными, что приводит к свистящему дыханию и стеснению в груди.
Астма поражает людей всех возрастов и полов. В Соединенных Штатах 8% взрослых болеют астмой. Тем не менее, некоторые люди могут быть более склонны к развитию астмы, чем другие.
Тем не менее, некоторые люди могут быть более склонны к развитию астмы, чем другие.
В этой статье обсуждаются генетические связи различных типов астмы, другие причины и факторы риска, а также методы лечения.
Большинство типов астмы могут иметь генетический компонент. Некоторые различные типы астмы включают:
- астму взрослых
- бронхоспазм, вызванный физической нагрузкой
- аллергическую астму
- неаллергическую астму
- профессиональную астму
- астму с хронической обструктивной болезнью легких4 астма, если у них есть семейная история этого состояния. Это означает, что астма может быть генетической. Некоторые исследователи описывают его как «высоко наследуемое заболевание».
Согласно обзорному исследованию 2014 года, генетические факторы составляют около 70% риска развития астмы у человека, а это означает, что гены играют большую роль в развитии заболевания у человека.
Однако генетика не единственная причина астмы.
 У некоторых людей это развивается, когда у них нет известной семейной истории этого заболевания. У человека может быть генетическая предрасположенность к астме, но на самом деле она никогда не разовьется.
У некоторых людей это развивается, когда у них нет известной семейной истории этого заболевания. У человека может быть генетическая предрасположенность к астме, но на самом деле она никогда не разовьется.Генетика играет меньшую роль в развитии астмы в более позднем возрасте, поэтому астма у взрослых и профессиональная астма в меньшей степени зависят от генов.
У человека также может развиться астма без какой-либо генетической предрасположенности к этому заболеванию. На самом деле, многие факторы окружающей среды могут вызвать у человека его развитие.
Генетика и окружающая среда играют роль в развитии астмы, но ученые до сих пор не знают точных причин. Тем не менее, они определили ряд триггеров для симптомов астмы.
Триггеры астмы могут различаться у разных людей и могут включать:
- респираторные инфекции, включая простуду или грипп
- irritants in the air
- air pollution
- tobacco smoke
- exercise
- cold air
- medications, including beta-blockers and nonsteroidal anti-inflammatory drugs
- stress
- food and drink preservatives
- allergens, including dust , перхоть и пыльца
Ряд факторов риска может увеличить вероятность развития астмы.
Генетика или семейный анамнез астмы повышают вероятность развития астмы у человека в какой-то момент его жизни.
Другие факторы риска развития астмы включают:
- избыточный вес
- курение
- наличие аллергии или других состояний, связанных с аллергией
- частое воздействие вторичного табачного дыма к профессиональным раздражителям, включая химические вещества и пыль
Симптомы астмы и их тяжесть зависят от человека. Некоторые люди могут иметь симптомы часто, в то время как другие могут испытывать их только время от времени.
Симптомы астмы могут включать:
- свистящее дыхание
- стеснение в груди
- затрудненное дыхание
- одышка
- кашель
Иногда симптомы астмы, называемые триггерами обострения, могут вызвать короткий период обострения астмы. Когда у человека случается приступ астмы, его бронхи сужаются.
Во время приступа астмы симптомы астмы могут стать тяжелыми и потребовать экстренного ингалятора или, в некоторых случаях, неотложной медицинской помощи.

Симптомы приступа астмы включают:
- ощущение быстрого стеснения в груди
- учащенное дыхание
- синеватый оттенок кожи и ногтей
- одышка, не связанная с физической нагрузкой
- втяжение грудной клетки
- и невозможность сделать полный вдох
Не все люди с астмой имеют все эти симптомы. Кроме того, если у человека есть эти симптомы, это не означает, что у него астма.
Лечение астмы направлено на то, чтобы помочь человеку справиться с симптомами и предотвратить приступы астмы. Лечение также может уменьшить долгосрочное повреждение легких, которое может возникнуть при плохо контролируемой астме.
Врач может порекомендовать комбинацию методов лечения.
Длительное медикаментозное лечение астмы может включать:
- длительные ингаляционные препараты для контроля астмы, включая кортикостероиды, бронходилататоры и комбинированные ингаляторы
- лекарства от аллергии
Врачи могут также прописать быстродействующие препараты краткосрочного действия при приступах астмы. Они могут включать:
Они могут включать:
- пероральные или внутривенные стероиды для уменьшения отека дыхательных путей при тяжелых приступах
- быстродействующие бронходилататоры, такие как ингаляторы альбутерола
Врач также, вероятно, порекомендует некоторые изменения образа жизни, чтобы помочь человеку контролировать свои симптомы.
Изменения образа жизни, которые может попробовать человек с астмой, могут включать:
- выявление и предотвращение триггеров
- использование кондиционера для предотвращения триггеров астмы на открытом воздухе
- регулярная уборка дома во избежание пыли и плесени
- закрытие рта и носа в холодную погоду
- управление стрессом и сильными эмоциями
компонентов, но она также может иметь другие причины и факторы риска, особенно при астме с началом во взрослом возрасте.
Люди обычно хорошо справляются с астмой с помощью лекарств. Однако некоторым людям трудно контролировать симптомы астмы.
