Карта сайта
|
|
«Клинические рекомендации «Пневмония (внебольничная)» (утв.
 Минздравом России) \ КонсультантПлюс
Минздравом России) \ КонсультантПлюс
- Главная
- Документы
Документ применяется с 1 января 2023 года.
- Клинические рекомендации
- Список сокращений
- Термины и определения
- 1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
- 1.1. Определение заболевания или состояния (группы заболеваний или состояний)
- 1.2. Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
- 1.2.1. Этиология пневмоний у детей
- Дети первых месяцев жизни
- Дети 6 мес — 5 лет
- Дети старше 5 лет и подростки
- 1.2.2. Чувствительность возбудителей ВП к противомикробным препаратам системного действия (ПМП)
- 1.2.3. Патогенез пневмонии, вызванной инфекционными возбудителями у детей
- 1.3. Эпидемиология заболевания или состояния (группы заболеваний или состояний)
- 1.4. Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статической классификации болезней и проблем, связанных со здоровьем
- 1.
 5. Классификация заболевания или состояния (группы заболеваний или состояний)
5. Классификация заболевания или состояния (группы заболеваний или состояний) - 1.6. Клиническая картина заболевания или состояния (группы заболеваний или состояний)
- Осложненная ВП
- 2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
- 2.1. Жалобы и анамнез
- 2.2. Физикальное обследование
- 2.3. Лабораторные диагностические исследования
- 2.3.1. Исследование лейкоцитарной формулы и маркеров бактериального воспаления
- 2.3.2. Микробиологические исследования
- 2.3.3. Исследования на вирусы
- 2.3.4. Диагностика атипичных инфекций
- 2.3.5. Биохимические исследования
- 2.3.6. Исследование кислотно-основного состояния
- 2.4. Инструментальные диагностические исследования
- 2.4.1. Определение нарушения газового состава крови
- 2.4.2. Лучевые методы исследования
- 2.
 5. Иные диагностические исследования
5. Иные диагностические исследования - 3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
- 3.1. Консервативное лечение пневмонии
- 3.1.1. Антибактериальная терапия внебольничной пневмонии
- 3.1.2. Противовирусная терапия
- 3.1.3. Другие виды лечения ВП
- 3.1.4. Терапия осложненных пневмоний.
- 3.1.4.1. Оксигенотерапия
- 3.1.4.2. Ведение пациентов с абсцессом легкого или некротизирующей (деструктивной) пневмонией
- 3.2. Хирургическое лечение пневмонии
- 4. Медицинская реабилитация, медицинские показания и противопоказания к применению методов реабилитации
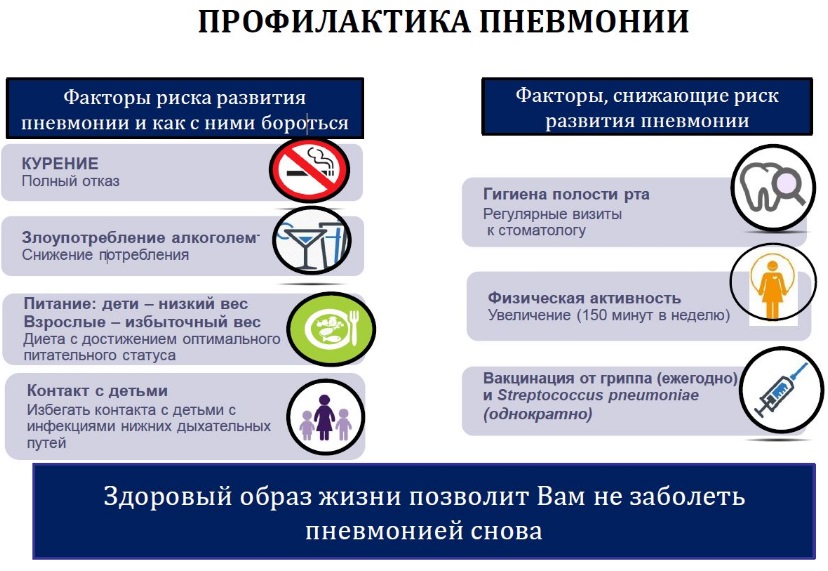
- 5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
- 6. Организация оказания медицинской помощи
- Ведение пациентов с недостаточным ответом на проводимую терапию
- Критерии выписки из стационара
- 7.
 Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния) - Критерии оценки качества медицинской помощи
- Таблица 1. Организационно-технические условия оказания медицинской помощи
- Таблица 2. Критерии качества медицинской помощи детям при ВП
- Список литературы
- Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
- Приложение А2. Методология разработки клинических рекомендаций
- Целевая аудитория данных клинических рекомендаций
- Методы, использованные для сбора/селекции доказательств
- Описание методов, использованных для сбора/селекции доказательств
- Методы, использованные для оценки качества и силы доказательств
- Методы, использованные для анализа доказательств
- Описание методов, использованных для анализа доказательств
- Методы, использованные для формулирования рекомендаций
- Метод валидации рекомендаций
- Описание метода валидации рекомендаций
- Экономический анализ
- Консультация и экспертная оценка
- Рабочая группа
- Таблица 1.
 Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств) - Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
- Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
- Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
- Приложение Б. Алгоритмы действий врача
- Приложение В. Информация для пациента
- Приложение Г1 — ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Клинические рекомендации
Рекомендации по пневмококковой вакцине | CDC
Ниже приведены краткие рекомендации Консультативного комитета CDC по практике иммунизации (ACIP). Полный текст рекомендаций см. в разделе Рекомендации по пневмококковой вакцине ACIP.
Полный текст рекомендаций см. в разделе Рекомендации по пневмококковой вакцине ACIP.
Плановая вакцинация младенцев, детей и взрослых в возрасте 65 лет и старше
Младенцы и дети
CDC рекомендует рутинное введение пневмококковой конъюгированной вакцины (ПКВ13 или ПКВ15) всем детям в возрасте до 2 лет:
- Дайте PCV13 или PCV15 младенцам в виде серии из 4 доз, по одной дозе в каждом из следующих возрастов: 2 месяца, 4 месяца, 6 месяцев и от 12 до 15 месяцев.
- Дети, пропустившие прививку или начавшие серию позже, все равно должны пройти вакцинацию. Рекомендуемое количество доз и интервалы между дозами будут зависеть от возраста ребенка на момент начала вакцинации. Дополнительную информацию см. в руководстве по наверстыванию.
Взрослые 65 лет и старше
Посмотреть текущие расписания для детей, подростков и взрослых.
CDC рекомендует регулярное введение пневмококковой конъюгированной вакцины (ПКВ15 или ПКВ20) всем взрослым в возрасте 65 лет и старше, которые никогда не получали пневмококковой конъюгированной вакцины или чья предыдущая вакцинация неизвестна:
- Если используется ПКВ15, это следует с последующей дозой PPSV23 через год.
 Минимальный интервал составляет 8 недель, и его можно рассматривать у взрослых с иммунодефицитом†, кохлеарным имплантом или утечкой спинномозговой жидкости.
Минимальный интервал составляет 8 недель, и его можно рассматривать у взрослых с иммунодефицитом†, кохлеарным имплантом или утечкой спинномозговой жидкости. - Если используется PCV20, доза PPSV23 НЕ указывается.
- См. «Вакцинация против пневмококка: Краткий обзор того, кто и когда вакцинировать», чтобы получить рекомендации CDC по вариантам вакцинации для взрослых, которые ранее получали конъюгированную пневмококковую вакцину.
Сноска
† Иммунодефицитные состояния включают хроническую почечную недостаточность, врожденную или приобретенную асплению, генерализованное злокачественное новообразование, ВИЧ-инфекцию, болезнь Ходжкина, ятрогенную иммуносупрессию, лейкемию, лимфому, множественную миелому, нефротический синдром, серповидно-клеточную анемию или другие гемоглобинопатии, а также заболевания паренхиматозных органов. пересадка.
Вакцинация детей старшего возраста и взрослых по определенным показаниям
В определенных ситуациях дети в возрасте 2 лет и старше и взрослые моложе 65 лет также должны получать пневмококковые вакцины. Все рекомендации по вакцинации против пневмококка в зависимости от вакцины и возраста см. в разделе Вакцинация против пневмококка: сводка о том, кого и когда вакцинировать.
Все рекомендации по вакцинации против пневмококка в зависимости от вакцины и возраста см. в разделе Вакцинация против пневмококка: сводка о том, кого и когда вакцинировать.
Вспомогательное руководство для здоровых детей в возрасте от 4 месяцев до 4 лет
Следующее «рабочее пособие» содержит рекомендации в отношении ЦВС13 или ЦВС15 для здоровых детей в возрасте от 4 месяцев до 4 лет. Он включает подробные сценарии по возрастным группам и предыдущему количеству полученных доз. Это должно помочь клиницистам в интерпретации рисунка 2 графика догоняющей иммунизации детей/подростков.
- Пневмококковая конъюгированная вакцина (ПКВ). Рекомендации для здоровых детей в возрасте от 4 месяцев до 4 лет [3 страницы]
Варианты завершения серии вакцинации для взрослых, получивших ранее конъюгированную вакцину
ПКВ13: Взрослые, получившие ПКВ13, имеют варианты завершения серии вакцинации против пневмококка.
- См. Вакцинация против пневмококка: Краткая информация о том, кто и когда вакцинировать для получения рекомендаций CDC по этим вариантам вакцинации.

- См. Примеры: Полные календари вакцинации против пневмококка для взрослых [4 страницы] для наглядной иллюстрации этих вариантов вакцин.
PCV7: Лечите взрослых, получивших PCV7, так же, как и людей, которые никогда не получали никаких пневмококковых вакцин.
Вакцинация против ПКВ20 для пожилых людей, завершивших серию прививок более ранними конъюгированными вакцинами
На основе совместного принятия клинических решений взрослые в возрасте 65 лет и старше имеют возможность получить ПКВ20, если они получили
- ПКВ13 (но не ПКВ15 или ПКВ20) в любом возрасте
и
- PPSV23 в возрасте 65 лет или старше
Дополнительные указания см. в методическом пособии по совместному принятию клинических решений: вакцинация против пневмококка [1 страница].
Противопоказания и меры предосторожности
Не вводить пневмококковую конъюгированную вакцину:
- Лицам, у которых когда-либо была тяжелая аллергическая реакция (например, анафилаксия) после предыдущей дозы ПКВ7, ПКВ13, ПКВ15 или ПКВ20, или любая вакцина, содержащая дифтерийный анатоксин
- Человек с тяжелой аллергией на любой компонент этих вакцин
Не назначайте PPSV23:
- Человеку, у которого когда-либо была тяжелая аллергическая реакция (например, анафилаксия) после предыдущей дозы
- Человек с тяжелой аллергией на любой компонент этой вакцины
Клиницисты могут вводить пневмококковые вакцины, если поставщик и родитель или пациент считают, что преимущества вакцинации перевешивают риски, по адресу:
- Человек с умеренным или тяжелым острым заболеванием с лихорадкой или без нее
Обзор пневмококковых вакцин: текущие рекомендации по полисахаридным вакцинам и будущие белковые антигены
1. Bridy-Pappas AE, Margolis MB, Center KJ, Isaacman DJ. Streptococcus pneumoniae: описание возбудителя, эпидемиология заболевания, лечение и профилактика. Фармакотерапия . 2005;25(9):1193–1212. [PubMed] [Google Scholar]
Bridy-Pappas AE, Margolis MB, Center KJ, Isaacman DJ. Streptococcus pneumoniae: описание возбудителя, эпидемиология заболевания, лечение и профилактика. Фармакотерапия . 2005;25(9):1193–1212. [PubMed] [Google Scholar]
2. Уордлоу Т., Уайт Йоханссон Э., Ходж М. Пневмония: забытый убийца детей. Нью-Йорк: Детский фонд Организации Объединенных Наций/Всемирная организация здравоохранения; 2006. [Google Академия]
3. Камерлинг Дж.П. Пневмококковые полисахариды: химический взгляд. В: Томаш А, редактор. Streptococcus pneumoniae: молекулярная биология и механизмы заболевания . Нью-Рошель, штат Нью-Йорк: Mary Ann Liebert, Inc.; 2000. С. 81–114. (ed) [Google Scholar]
4. Bogaert D, Hermans PW, Adrian PV et al. Пневмококковые вакцины: обновленная информация о текущих стратегиях. Вакцина . 2004;22(17–18):2209–2220. [PubMed] [Google Scholar]
5. Pneumovax23 (поливалентная пневмококковая вакцина) [вкладыш в упаковку] Whitehouse Station, NJ: Merck & Co.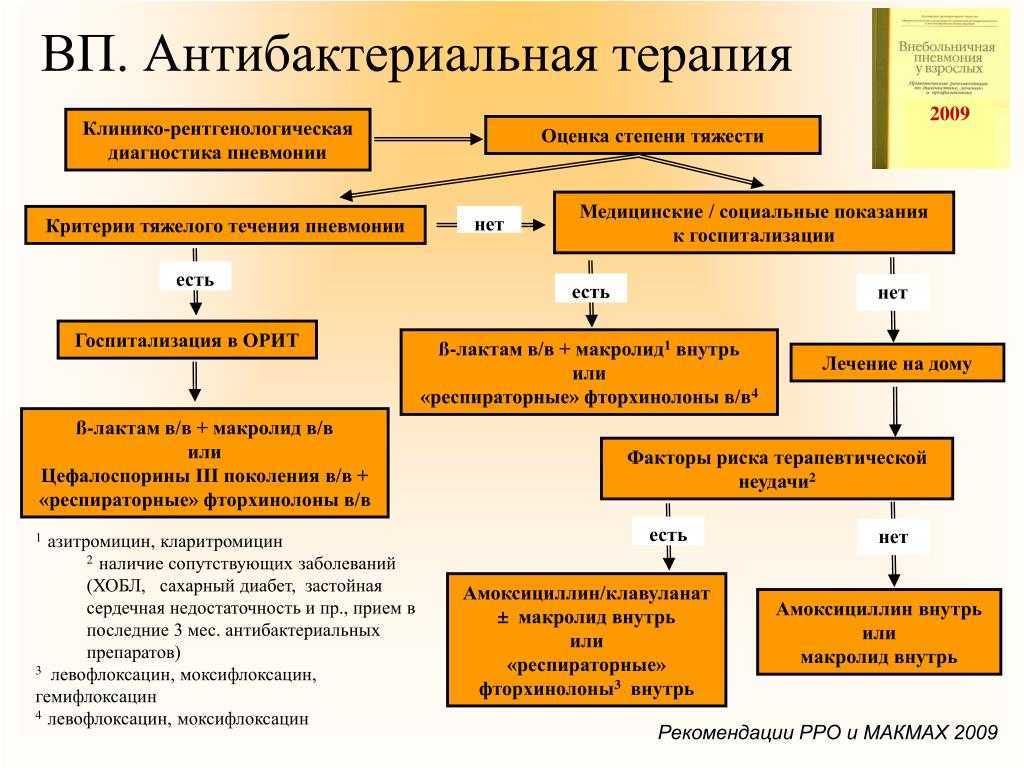 , Inc.; 2011. [Google Академия]
, Inc.; 2011. [Google Академия]
6. Центры по контролю и профилактике заболеваний, Консультативный комитет по практике иммунизации. Обновленные рекомендации по профилактике инвазивной пневмококковой инфекции среди взрослых с помощью 23-валентной пневмококковой полисахаридной вакцины (PPSV23) MMWR Morb Mortal Wkly Rep . 2010;59(34):1102–1106. [PubMed] [Google Scholar]
7. Shapiro ED, Berg AT, Austrian R et al. Защитная эффективность поливалентной пневмококковой полисахаридной вакцины. N Английский J Med . 1991;325(21):1453–1460. [PubMed] [Google Scholar]
8. Hamborsky J, Kroger A, Wolfe S, редакторы. Центры по контролю и профилактике заболеваний. Эпидемиология и профилактика вакциноуправляемых заболеваний . 13-е изд. Вашингтон, округ Колумбия: Фонд общественного здравоохранения; 2015. [Google Scholar]
9. Heilmann C. Реакция В- и Т-лимфоцитов человека на вакцинацию пневмококковыми полисахаридами. Приложение APMIS .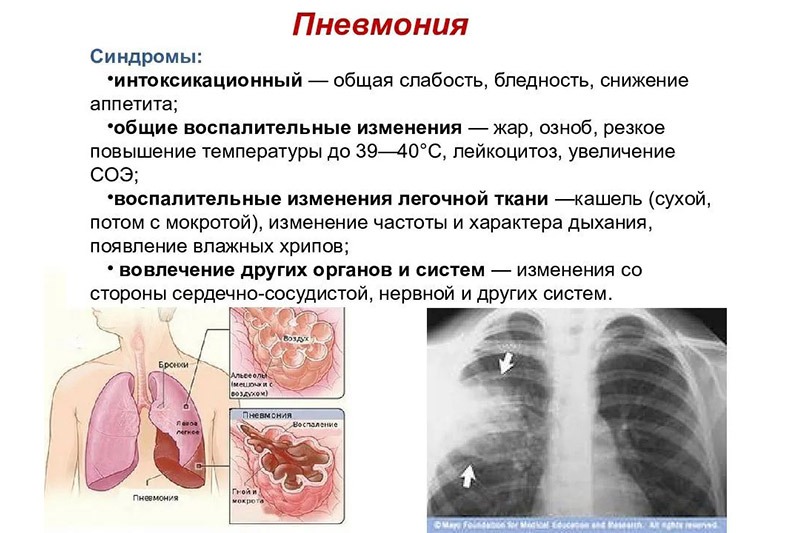 1990; 15:1–23. [PubMed] [Google Scholar]
1990; 15:1–23. [PubMed] [Google Scholar]
10. Hammitt LL, Bruden DL, Butler JC et al. Косвенное влияние конъюгированной вакцины на носительство Streptococcus pneumoniae у взрослых: объяснение тенденций инвазивной пневмококковой инфекции. J Заражение Dis . 2006;193(11):1487–1494. [PubMed] [Google Scholar]
11. Whitney CG, Farley MM, Hadler J et al. Снижение инвазивной пневмококковой инфекции после введения белково-полисахаридной конъюгированной вакцины. N Английский J Med . 2003;348(18):1737–1746. [PubMed] [Google Scholar]
12. Richter SS, Heilmann KP, Dohrn CL et al. Пневмококковые серотипы до и после внедрения конъюгированных вакцин, США, 1999–2011 гг. Возникновение инфекции Dis . 2013;19(7):1074–1083. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Griffin MR, Zhu Y, Moore MR et al. Госпитализации в США по поводу пневмонии после десяти лет пневмококковой вакцинации. N Английский J Med . 2013;369(2):155–163.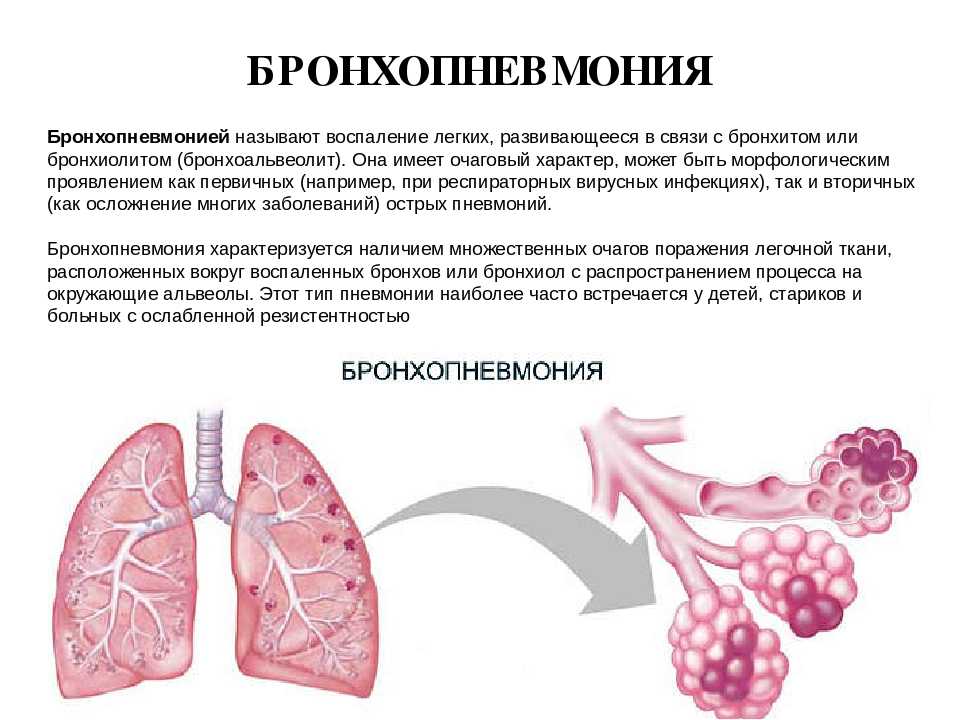 [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
14. Haber M, Barskey A, Baughman W et al. Коллективный иммунитет и пневмококковая конъюгированная вакцина: количественная модель. Вакцина . 2007;25(29):5390–5398. [PubMed] [Академия Google]
15. Федсон Д.С., Мушер Д.М. Пневмококковая полисахаридная вакцина. В: Плоткин С.А., Оренштейн В.А., ред. Вакцины . Филадельфия: В. Б. Сондерс; 2004. стр. 529–588. [Google Scholar]
16. Bryant KA, Block SL, Baker SA et al. Безопасность и иммуногенность 13-валентной пневмококковой конъюгированной вакцины. Педиатрия . 2010;125(5):866–875. [PubMed] [Google Scholar]
17. Singleton RJ, Hennessy TW, Bulkow LR et al. Инвазивная пневмококковая инфекция, вызванная невакцинными серотипами, среди детей коренных народов Аляски с высоким уровнем охвата 7-валентной пневмококковой конъюгированной вакциной. ЯМА . 2007; 297(16):1784–1792. [PubMed] [Google Scholar]
18. Hsu HE, Shutt KA, Moore MR et al. Влияние пневмококковой конъюгированной вакцины на пневмококковый менингит. N Английский J Med . 2009;360(3):244–256. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Влияние пневмококковой конъюгированной вакцины на пневмококковый менингит. N Английский J Med . 2009;360(3):244–256. [Бесплатная статья PMC] [PubMed] [Google Scholar]
19. Moore MR, Link-Gelles R, Schaffner W et al. Влияние использования 13-валентной пневмококковой конъюгированной вакцины у детей на инвазивную пневмококковую инфекцию у детей и взрослых в США: анализ многоцентрового популяционного эпиднадзора. Ланцет Infect Dis . 2015;15(3):301–309. [Бесплатная статья PMC] [PubMed] [Google Scholar]
20. Fortanier AC, Venekamp RP, Boonacker CW et al. Пневмококковые конъюгированные вакцины для профилактики среднего отита. Кокрановская система базы данных, ред. 2014; 4:CD001480. [PubMed] [Google Scholar]
21. Центры по контролю и профилактике заболеваний, Консультативный комитет по практике иммунизации. Профилактика пневмококковой инфекции среди младенцев и детей — использование 13-валентной пневмококковой конъюгированной вакцины и 23-валентной пневмококковой полисахаридной вакцины — рекомендации Консультативного комитета по практике иммунизации (ACIP) MMWR Morb Moratl Wkly Rep . 2010;59(RR11):1–18. [PubMed] [Google Scholar]
2010;59(RR11):1–18. [PubMed] [Google Scholar]
22. Prevnar 13 (пневмококковая 13-валентная конъюгированная вакцина [белок дифтерии CRM197]) [вкладыш в упаковку] Филадельфия, Пенсильвания: Pfizer, Inc.; 2013. [Google Scholar]
23. Vernacchio L, Neufeld EJ, MacDonald K et al. Комбинированный график 7-валентной пневмококковой конъюгированной вакцины с последующей 23-валентной пневмококковой вакциной у детей и молодых людей с серповидно-клеточной анемией. J Педиатр . 1998;133(2):275–278. [PubMed] [Google Scholar]
24. Abzug MJ, Pelton SI, Song LY et al. Иммуногенность, безопасность и предикторы ответа на серию пневмококковой конъюгированной и пневмококковой полисахаридной вакцины у детей, инфицированных вирусом иммунодефицита человека, получающих высокоактивную антиретровирусную терапию. Pediatr Infect Dis J . 2006;25(10):920–929. [PubMed] [Google Scholar]
25. Национальные институты здравоохранения Национальный институт сердца, легких и крови, Отдел болезней крови и ресурсов. Лечение серповидноклеточной анемии . 4-е изд. Bethesda, MD: Национальные институты здравоохранения США; 2002. [Google Scholar]
Лечение серповидноклеточной анемии . 4-е изд. Bethesda, MD: Национальные институты здравоохранения США; 2002. [Google Scholar]
26. Daniels CC, Shelton CM, Bass PJ et al. Отек конечностей у детей с серповидно-клеточной анемией после ревакцинации пневмококковой вакциной. Int J Clin Pharm . 2014;36(2):261–263. [PubMed] [Google Scholar]
27. Джексон Л.А., Бенсон П., Снеллер В.П. и соавт. Безопасность ревакцинации пневмококковой полисахаридной вакциной. ЯМА . 1999;281(3):243–8. [PubMed] [Google Scholar]
28. Jackson LA, Nelson JC, Whitney CG et al. Оценка безопасности третьей дозы пневмококковой полисахаридной вакцины в популяции Vaccine Safety Datalink. Вакцина . 2006;24(12):151–6. [PubMed] [Google Scholar]
29. Hollingshead SK, Becker R, Briles DE. Разнообразие PspA: мозаичные гены и доказательства прошлой рекомбинации у Streptococcus pneumoniae. Заразить Иммуном . 2000;68(10):5889–5900. [Бесплатная статья PMC] [PubMed] [Google Scholar]
30. Crain MJ, Waltman WD, II, Turner JS et al. Пневмококковый поверхностный белок А (PspA) серологически сильно варьирует и экспрессируется всеми клинически важными капсульными серотипами Streptococcus pneumoniae. Заразить Иммуном . 1990;58(10):3293–3299. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Crain MJ, Waltman WD, II, Turner JS et al. Пневмококковый поверхностный белок А (PspA) серологически сильно варьирует и экспрессируется всеми клинически важными капсульными серотипами Streptococcus pneumoniae. Заразить Иммуном . 1990;58(10):3293–3299. [Бесплатная статья PMC] [PubMed] [Google Scholar]
31. Ren B, Szalai AJ, Thomas O et al. Белки PspA как семейства 1, так и семейства 2 могут ингибировать отложение комплемента и придавать вирулентность капсульному штамму Streptococcus pneumoniae серотипа 3. Заражение Иммуном . 2013;71(1):75–85. [Бесплатная статья PMC] [PubMed] [Google Scholar]
32. Shaper M, Hollingshead SK, Benjamin WH, Jr, Briles DE. PspA защищает Streptococcus pneumoniae от уничтожения аполактоферрина, а антитела к PspA усиливают уничтожение пневмококков аполактоферрином [исправлено] Infect Immun . 2004;72(9):5031–5040. [Бесплатная статья PMC] [PubMed] [Google Scholar]
33. Briles DE, King JD, Gray MA et al. PspA, вызывающий защиту пневмококковый белок: иммуногенность изолированного нативного PspA у мышей. Вакцина . 1996;14(9):858–867. [PubMed] [Google Scholar]
Вакцина . 1996;14(9):858–867. [PubMed] [Google Scholar]
34. Briles DE, Hollingshead SK, King J et al. Иммунизация людей рекомбинантным пневмококковым поверхностным белком А (rPspA) вырабатывает антитела, которые пассивно защищают мышей от фатальной инфекции Streptococcus pneumoniae, несущей гетерологичный PspA. J Заразить Dis . 2000;182(6):1694–1701. [PubMed] [Google Scholar]
35. Daniels CC, Coan P, King J et al. Богатая пролином область поверхностных белков пневмококка А и С содержит поверхностно-доступные эпитопы, общие для всех пневмококков, и вызывает опосредованную антителами защиту от сепсиса. Заражение Иммуном . 2010;78(5):2163–2172. [Бесплатная статья PMC] [PubMed] [Google Scholar]
36. Frey SE, Lottenbach KR, Hill H et al. Фаза I, испытание с увеличением дозы трех рекомбинантных аттенуированных вакцинных векторов Salmonella Typhi у взрослых, продуцирующих антиген поверхностного белка Streptococcus pneumoniae PspA. Вакцина . 2013;31(42):4874–4880. [PubMed] [Google Scholar]
2013;31(42):4874–4880. [PubMed] [Google Scholar]
37. Херст Р.А., Кадиоглу А., О’Каллаган С., Эндрю П.В. Роль пневмолизина при пневмококковой пневмонии и менингите. Клин Эксп Иммунол . 2004;138(2):195–201. [Бесплатная статья PMC] [PubMed] [Google Scholar]
38. Alexander JE, Lock RA, Peeters CC et al. Иммунизация мышей пневмолизиновым анатоксином обеспечивает значительную степень защиты по меньшей мере от девяти серотипов Streptococcus pneumoniae. Заразить Иммуном . 1994;62(12):5683–5688. [Бесплатная статья PMC] [PubMed] [Google Scholar]
39. Briles DE, Hollingshead SK, Paton JC et al. Иммунизация пневмококковым поверхностным белком А и пневмолизином защищает от пневмонии в мышиной модели легочной инфекции Streptococcus pneumoniae. J Заражение Dis . 2003;188(3):339–348. [PubMed] [Google Scholar]
40. Kamtchoua T, Bologa M, Hopfer R et al. Безопасность и иммуногенность пневмококкового производного пневмолизина PlyD1 в кандидатной вакцине с одним антигенным белком у взрослых.
