Противопоказания к прививкам | Сургутская городская клиническая поликлиника № 4
Вакцина | Противопоказания |
1. Все вакцины | Сильная реакция или поствакцинальное осложнение на предыдущее введение |
2. Все живые вакцины, в т.ч. оральная живая полиомиелитная вакцина (ОПВ) | Иммунодефицитное состояние (первичное) Вес ребенка при рождении менее 2000 г |
5. Живая коревая вакцина (ЖКВ), живая паротитная вакцина (ЖПВ), краснушная, а также комбинированные ди- и тривакцины (корь — паротит, корь — краснуха — паротит) | Тяжелые формы аллергических реакций на аминогликозиды |
6. | Аллергическая реакция на пекарские дрожжи |
7. Вакцины АДС, АДС-М, АД-М | Постоянных противопоказаний, кроме упомянутых в п. п. 1 и 2, не имеют |
Острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний являются временными противопоказаниями для проведения прививок. Плановые прививки проводятся через 2 — 4 недели после выздоровления или в период реконвалесценции или ремиссии. При нетяжелых ОРВИ, острых кишечных заболеваниях и другие прививки проводятся сразу после нормализации температуры.
Следует учесть, что наличие противопоказания не означает, что в случае проведения прививки у вакцинированного обязательно возникнет осложнение, речь идет лишь о повышении риска неблагоприятной реакции, что, однако, должно рассматриваться как препятствие к проведению вакцинации в большинстве случаев.
Ложные противопоказания к вакцинации
Противопоказания, указанные выше, встречаются реже, чем у 1% детей. Не намного чаще выявляются состояния, которые требуют не «отвода», а лишь отсрочки иммунизации Все эти состояния должны рассматриваться как ложные противопоказания.
Не намного чаще выявляются состояния, которые требуют не «отвода», а лишь отсрочки иммунизации Все эти состояния должны рассматриваться как ложные противопоказания.
Состояния | Указания в анамнезе на: |
Перинатальная энцефалопатия | Недоношенность Эпилепсия в семье Внезапная смерть в семье |
Перинатальная энцефалопатия — собирательный термин, обозначающий повреждение ЦНС травматического и/или гипоксического генеза, ее острый период заканчивается в течение первого месяца жизни. В практике этот термин используют (нередко у 80 — 90% детей первых месяцев жизни) и как диагноз для обозначения непрогрессирующих остаточных расстройств (мышечная дистония, нарушения периодичности сна и бодрствования, запаздывание становления статических и моторных функций и др.). Если педиатру неясен характер изменений ЦНС, он направляет ребенка к невропатологу для исключения прогрессирующего процесса, после чего он сам принимает решение о проведении вакцинации.
В практике этот термин используют (нередко у 80 — 90% детей первых месяцев жизни) и как диагноз для обозначения непрогрессирующих остаточных расстройств (мышечная дистония, нарушения периодичности сна и бодрствования, запаздывание становления статических и моторных функций и др.). Если педиатру неясен характер изменений ЦНС, он направляет ребенка к невропатологу для исключения прогрессирующего процесса, после чего он сам принимает решение о проведении вакцинации.
Анемия нетяжелая, алиментарного генеза не должна быть причиной отвода от прививки, после которой ребенку назначают соответствующее лечение. Тяжелая анемия требует выяснения причины с последующим решением вопроса о времени вакцинации.
Дисбактериоз как диагноз оправдан только у больного с расстройством стула на фоне массивной антибиотикотерапии, когда вопрос о прививке не возникает до выздоровления. У ребенка с нормальным стулом диагноз «дисбактериоз» не имеет под собой каких-либо оснований, при неустойчивом стуле речь обычно идет о непереносимости молочного сахара или синдроме раздражимой кишки.
Увеличение тени тимуса на рентгенограмме выявляется обычно случайно при обследовании по поводу ОРЗ, оно является анатомическим вариантом либо результатом его послестрессовой гиперплазии. Такие дети хорошо переносят прививки, дают нормальный иммунный ответ, а частота поствакцинальных реакций у них не больше, чем у детей без видимой тени вилочковой железы. Срок вакцинации определяется течением заболевания, по поводу которого был сделан снимок.
Аллергические заболевания являются скорее показанием к вакцинации, чем противопоказанием, поскольку у этих детей инфекции протекают особенно тяжело (например, коклюш у больного астмой). Педиатр, консультируя такого ребенка с аллергологом, должен ставить вопрос не о допустимости прививок, а о выборе оптимального времени их проведения и необходимости лекарственной защиты (противогистаминные препараты при кожных формах атопии, ингаляции стероидов и бета-агонистов при астме).
Врожденные пороки развития, в т.ч. пороки сердца, не являются поводом для отвода от прививок в отсутствие других причин, они проводятся по достижении компенсации имеющихся расстройств.
Поддерживающее лечение хронического заболевания антибиотиками, эндокринными препаратами, сердечными, противоаллергическими, гомеопатическими средствами и т.д. само по себе не должно служить поводом для отвода от прививок.
Местное применение стероидов в виде мазей, капель в глаза, спреев или ингаляций не сопровождается иммуносупрессией и не препятствует вакцинации.
Анамнестические данные о тяжелых заболеваниях не должны служить поводом для отсрочки прививок: дети первых месяцев жизни, перенесшие тяжелые заболевания (сепсис, гемолитическую анемию, пневмонию, болезнь гиалиновых мембран и др.) после выздоровления могут и должны прививаться.
Минздрав России утвердил перечень медицинских противопоказаний к проведению вакцинации от COVID-19
Главная
/
Новости
/
Минздрав России утвердил перечень медицинских противопоказаний к проведению вакцинации от COVID-19
Ваше уведомление успешно отправлено. Спасибо за ваш отзыв!
Спасибо за ваш отзыв!
Министерство здравоохранения в соответствии с п. 3 ст. 11 Федерального закона «Об иммунопрофилактике инфекционных болезней» утвердило медицинских перечень противопоказаний к проведению прививок против новой коронавирусной инфекции. Приказ N 8н от 13.01.2022 зарегистрирован Минюстом России 17 января 2022 г.
Так, согласно перечню, острые инфекционные заболевания, протекающие в средней и тяжелой степени тяжести, обострение хронических заболеваний являются временными медицинскими противопоказаниями. Вакцинация против новой коронавирусной инфекции возможна через 2-4 недели после выздоровления или после ремиссии неинфекционного заболевания.
Острые респираторные вирусные заболевания, протекающие в легкой форме, а также инфекционные заболевания ЖКТ также являются временным медицинским противопоказанием к вакцинации против COVID-19 — до нормализации температуры тела.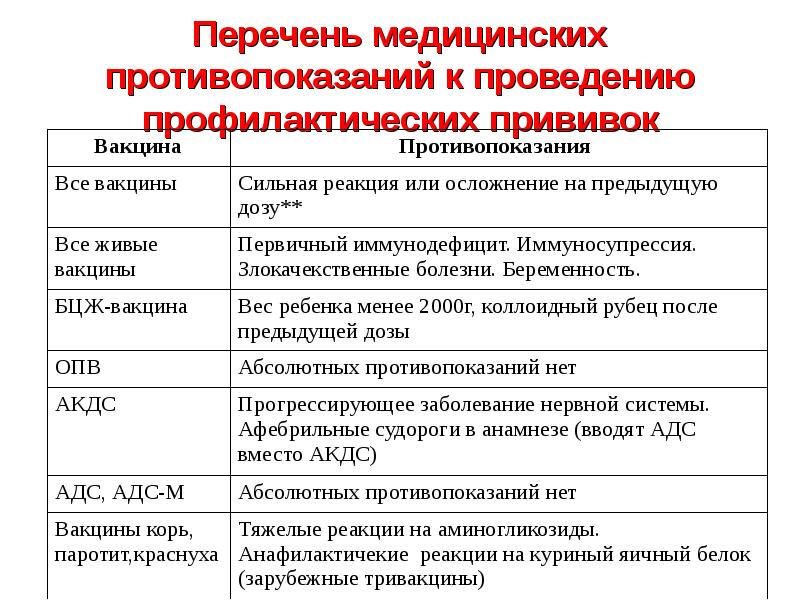
Согласно перечню, гиперчувствительность к веществам, входящим в состав вакцины против COVID-19, или вакцине, в состав которой входят аналогичные вещества, а также тяжелые аллергические реакции в анамнезе или тяжелые поствакцинальные осложнения (анафилактический шок, тяжелые генерализованные аллергические реакции, судорожный синдром, температура тела выше 40, гиперемия или отек в месте инъекции) являются бессрочными медицинскими противопоказаниями.
В перечень также внесен ряд медицинских противопоказаний в соответствии с инструкциями по медицинскому применению вакцин. В перечень также внесен ряд медицинских противопоказаний в соответствии с инструкциями по медицинскому применению вакцин. Так, согласно перечню, беременность сроком от 22 недель и период грудного вскармливания не является противопоказанием к вакцинации препаратом Спутник V. Согласно Временным методическим рекомендациям Минздрава России по профилактике и лечению COVID-19 у беременных женщин, новая коронавирусная инфекция особенно опасна для беременных женщин, имеющих сердечно-сосудистые заболевания, ожирение, сахарный диабет хронические заболевания лёгких, печени или почек, а также имеющих онкологическое заболевание.
Минздрав России напоминает, что люди, имеющие медицинские противопоказания к вакцинации против новой коронавирусной инфекции, относятся к группе риска по развитию тяжелый осложнений новой коронавирусной инфекции и постковидного синдрома. Людям, имеющим медицинские противопоказания к вакцинации, необходимо тщательно соблюдать меры неспецифической профилактики инфекции — носить маски, соблюдать социальную дистанцию и по возможности избегать больших скоплений людей.
Категории: вакцинация; противопоказания; коронавирус; коронавирусная инфекция; COVID-19.
О вакцине против COVID-19: часто задаваемые вопросы
Какие вакцины против COVID-19 были одобрены и/или разрешены для использования в США?
В США есть две мРНК-вакцины, одна вирусная векторная и одна белковая субъединичная вакцины против COVID-19 для использования в ответ на пандемию. CDC рекомендовал вакцины против COVID-19, отдавая предпочтение вакцине мРНК (Pfizer-BioNTech и Moderna) или вакцине с белковыми субъединицами (Novavax). Вакцина Janssen (вирусный вектор) доступна для лиц, которые не могут получить другую вакцину. CDC перечисляет следующие причины для получения вакцины Janssen:
Вакцина Janssen (вирусный вектор) доступна для лиц, которые не могут получить другую вакцину. CDC перечисляет следующие причины для получения вакцины Janssen:
- У человека есть противопоказания к мРНК-вакцинам (например, Moderna, Pfizer-BioNTech) и Novavax COVID-19 (например, тяжелая аллергическая реакция после предыдущей дозы или на компонент мРНК-вакцины против COVID-19)
- В противном случае человек остался бы непривитым от COVID-19 из-за ограниченного доступа к другим вакцинам против COVID-19
- Человек хочет получить вакцину Janssen против COVID-19, несмотря на выявленные проблемы безопасности.
В настоящее время компании Pfizer-BioNTech и Moderna предлагают несколько двухвалентных мРНК-вакцин.
Моновалентная вакцина Novavax также может использоваться в качестве первой бустерной вакцины для взрослых в возрасте 18 лет и старше, если они прошли первичную серию вакцинаций, но ранее не получали бустерную вакцину против COVID-19, а также если они не могут или не хотят получить ревакцинацию. обновленный бустер мРНК.
обновленный бустер мРНК.
Вакцина мРНК Pfizer-BioNTech
- Разрешение FDA BLA для лиц в возрасте 16 лет и старше
- FDA EUA на 6 месяцев – 15 лет
- Рекомендации CDC ACIP для лиц в возрасте 16 лет и старше
- Рекомендации CDC ACIP для подростков 12–15 лет
- Рекомендации CDC ACIP для детей 5–11 лет
- Рекомендации CDC ACIP для детей в возрасте от 6 месяцев до 4 лет
- Рекомендации CDC ACIP для бивалентных бустерных доз
Вакцина мРНК Moderna
- FDA BLA для лиц в возрасте 18 лет и старше
- FDA EUA от 6 месяцев до 17 лет
- Рекомендации CDC ACIP для лиц в возрасте 18 лет и старше
- Рекомендации CDC ACIP для детей и подростков в возрасте 6–11 лет
- Рекомендации CDC ACIP для детей и подростков в возрасте 12–17 лет
- Рекомендации CDC ACIP для детей в возрасте от 6 месяцев до 5 лет
- Рекомендации CDC ACIP для бивалентных бустерных доз
Janssen (J&J) Вакцина против вирусного вектора
- FDA EUA для лиц в возрасте 18 лет и старше / FDA EUA Поправка / CDC ACIP Рекомендация
- FDA EUA для бустерной дозы по крайней мере через 2 месяца после 1 дозы Janssen (J&J) / CDC ACIP Рекомендация
Вакцина с белковой субъединицей Novavax
FDA EUA для лиц в возрасте 12 лет и старше / Информационный бюллетень для поставщиков медицинских услуг, вводящих вакцину
Какую вакцину против COVID-19 я должен рекомендовать своим пациентам?
AAP рекомендует использовать вакцины против COVID-19, одобренные через разрешение на использование в чрезвычайных ситуациях (EUA) или заявление на получение лицензии на биологические препараты (BLA), рекомендованные CDC и соответствующие возрасту и состоянию здоровья ваших пациентов. Педиатры должны назначать любой препарат, доступный в их сообществах, для достижения максимального охвата вакцинацией.
Педиатры должны назначать любой препарат, доступный в их сообществах, для достижения максимального охвата вакцинацией.
Дети и подростки в возрасте 6 месяцев и старше, не имеющие противопоказаний, должны быть вакцинированы для защиты от COVID-19 как можно скорее. Вакцины от COVID-19 спасают жизни. Отсрочка иммунизации делает человека уязвимым для инфекции в течение более длительного периода времени, подвергая его большему риску серьезного заболевания и смерти. AAP также поддерживает совместное введение вакцин против COVID-19 с другими вакцинами из календаря иммунизации. См. политику AAP.
Для первичной серии какую дозу вакцины Moderna или Pfizer-BioNTech должен получить ребенок, если между дозами у него будет день рождения?
Как правило, размер дозы, которую получает ребенок, зависит от его возраста в день, когда ему делают прививку от COVID. Тем не менее, есть несколько вещей, которые нужно знать о вакцине против COVID для детей из разных возрастных групп.
Вакцина Pfizer-BioNTech COVID и вакцина Moderna COVID — это два продукта, разрешенных для детей в возрасте от 6 месяцев до 12 лет. Независимо от того, получили ли они сначала Pfizer или Moderna, дети должны получать один и тот же продукт во всех дозах, рекомендованных для их возраста в начальной серии.
Независимо от того, получили ли они сначала Pfizer или Moderna, дети должны получать один и тот же продукт во всех дозах, рекомендованных для их возраста в начальной серии.
Вакцина Pfizer-BioNTech COVID-19
Ребенок, достигший возраста от 4 до 5 лет между дозами первичной серии Pfizer, должен получить один из следующих двух вариантов:
- Моновалентная вакцина Pfizer в возрасте от 6 месяцев до 4 лет лет (бордовая крышка) для дозы 1 и дозы 2, бивалентная вакцина Pfizer для дозы 3 (бордовая крышка) и бустерная доза бивалентной вакцины на 5-11 лет (оранжевая крышка) или
- Моновалентная вакцина Pfizer на 5-11 лет (оранжевая крышка) для Дозы 1 и Дозы 2; и ревакцинация бивалентной вакциной в течение 5-11 лет (оранжевая крышка).
Ребенок, достигший возраста от 11 до 12 лет , между дозами первичной серии Pfizer должен получить:
- Вакцину Pfizer для возраста от 5 до 11 лет для дозы 1
- Вакцина Pfizer для детей в возрасте 12 лет и старше для дозы 2
- Бивалентная вакцина Pfizer для детей от 12 лет и старше для бустерной вакцины
Вакцина Moderna против COVID-19
Ребенок, достигший возраста от 5 до 6 лет , между дозами первичной серии Moderna должен получить:
- Вакцина Moderna для детей от 6 месяцев до 5 лет для дозы 1
- Вакцина Moderna для детей от 6 до 11 лет для дозы 2
- Двухвалентная вакцина Moderna для детей от 6 до 11 лет для ревакцинации
Ребенок, достигший возраста от 11 до 12 лет между дозами первичной серии Moderna, должен получить:
- Вакцину Moderna для возраста от 6 до 11 лет для дозы 1
- Вакцина Moderna для детей в возрасте от 12 до 17 лет для дозы 2
- Двухвалентная вакцина Moderna для детей 12–17 лет для бустерной вакцины
Дополнительные ресурсы:
- Краткое справочное руководство по дозированию вакцины против COVID-19 для детей AAP
- CDC Moderna Вакцина против COVID-19 для детей, переходящих из младшей в старшую возрастную группу
- CDC Pfizer-BioNTech Вакцина против COVID-19 для детей, переходящих из младшей в старшую возрастную группу
- Выпуск новостей FDA: Обновление коронавируса (COVID-19): FDA разрешает обновленный (двухвалентный) COVID-19Вакцины для детей в возрасте до 6 месяцев
Каковы рекомендации по вакцинации детей и подростков с ослабленным иммунитетом от умеренной до тяжелой степени?
Дети и подростки с определенными иммунодефицитными заболеваниями или получающие лечение, вызывающее умеренную или тяжелую иммуносупрессию, должны быть вакцинированы в соответствии со схемой, изложенной на страницах 3-4 Краткого справочного руководства по дозированию педиатрической вакцины AAP.
До и после COVID-19введения вакцины, следует продолжать меры по профилактике инфекции, такие как ношение маски, физическое дистанцирование и избегание скоплений людей и плохо проветриваемых помещений, поскольку люди с ослабленным иммунитетом могут по-прежнему подвергаться повышенному риску заражения COVID-19. Тесные контакты лиц с ослабленным иммунитетом, которые имеют право на вакцинацию, должны пройти вакцинацию против COVID-19 (первичная серия и бустерная доза) для обеспечения дополнительной защиты.
Информацию об иммунизации детей и подростков с ослабленным иммунитетом можно найти в:
- Красная книга: Иммунизация и другие аспекты у детей с ослабленным иммунитетом | Красная книга® 2021 | Красная книга онлайн | AAP Point-of-Care Solutions
- Клинические рекомендации CDC: https://www.cdc.gov/vaccines/covid-19/clinical-considerations/covid-19-vaccines-us.html
- CDC COVID-19 Вакцинация для людей с умеренным или тяжелым иммунодефицитом: https://www.
 cdc.gov/vaccines/covid-19/clinical-considerations/interim-considerations-us.html#immunocompromised
cdc.gov/vaccines/covid-19/clinical-considerations/interim-considerations-us.html#immunocompromised
Должны ли пациенты получать бустерную дозу вакцины против COVID-19?
Да. Защита, которую обеспечивают вакцины против COVID-19, со временем снижается. CDC рекомендует использовать бустерную дозу бивалентной мРНК для всех лиц в возрасте 5 лет и старше. Некоторые дети младшего возраста также могут иметь право на получение бустерной дозы.
Дети в возрасте 5 лет и старше должны получить одну соответствующую возрасту обновленную (бивалентную) бустерную дозу не менее чем через 2 месяца после:вакцина, или
Дети в возрасте от 6 месяцев до 4 лет, ранее прошедшие курс первичной вакцинации Moderna или получившие 3 моновалентные дозы первичной серии Pfizer-BioNTech, имеют право на получение двухвалентной бустерной дозы через 2 месяца после последней дозы первичной серии.
Дети в возрасте от 6 месяцев до 4 лет, которые уже завершили первичную серию из трех доз, получив две дозы оригинального (моновалентного) Pfizer-BioNTech COVID-19вакцину и третью дозу обновленной (бивалентной) вакцины Pfizer-BioNTech против COVID-19, в настоящее время не будет даваться право на бустерную дозу обновленной бивалентной вакцины; однако они получают право на получение двухвалентной бустерной дозы, когда им исполняется 5 лет. Ожидается, что дети в этой возрастной группе, получившие бивалентную дозу в рамках своей первичной серии, будут защищены от наиболее серьезных последствий циркулирующего в настоящее время варианта омикрон.
Novavax моновалентный COVID-19бустеры доступны для взрослых в возрасте 18 лет и старше, если они прошли первичную серию вакцинаций, но ранее не получали бустерную дозу COVID-19, а также если они не могут или не хотят получать обновленную бустерную дозу мРНК.
CDC предлагает дополнительную информацию о бустерных дозах, включая соответствие критериям и ответы на часто задаваемые вопросы.
Эксперты продолжают рекомендовать вакцинацию и ревакцинацию всем, независимо от того, переболели ли они COVID-19 в прошлом. COVID-19вакцинация обеспечивает более сильную и более длительную защиту от будущего заболевания COVID-19, чем восстановление только после естественной инфекции. Люди могут заразиться COVID-19 несколько раз, особенно по мере распространения новых штаммов в сообществах. По мере роста числа случаев заболевания по всей стране бустерная доза безопасно поможет восстановить и усилить защиту от тяжелого заболевания.
Могу ли я ввести вакцину против COVID-19 пациенту, который в настоящее время болен COVID-19?
Вакцинация против COVID-19 должна быть отложена для пациентов с текущей инфекцией SARS-CoV-2 до тех пор, пока они не выздоровеют от острого заболевания и не будут соблюдены критерии прекращения изоляции. Пациенты с бессимптомным течением должны получать COVID-19вакцину после рекомендованного периода изоляции. Это также относится к людям, заразившимся COVID-19 между первой и второй дозой вакцины, или к тем, кому предстоит ревакцинация.
Лица, недавно перенесшие инфекцию SARS-CoV-2 и завершившие период изоляции, могут рассмотреть возможность отсрочки введения первичной серии доз или первой или второй бустерной дозы вакцины против COVID-19 на 3 месяца с момента появления симптомов или положительного результата теста (если инфекция была бессимптомной). ). Исследования показали, что увеличение времени между заражением и вакцинацией может привести к улучшению иммунного ответа на вакцинацию.
В чем разница между мРНК COVID-19, вирусным вектором и белковыми субъединичными вакцинами?
Вакцины с матричной РНК (мРНК)
В этих вакцинах используется более новая технология, при которой мРНК обертывается оболочкой (липидными наночастицами), чтобы она могла проникать в наши клетки. мРНК в вакцине учит наши клетки, как делать копии спайкового белка. Как только спайковый белок произведен, происходят две вещи: (1) клетка расщепляет мРНК (инструкции) и избавляется от них, и (2) спайковый белок запускает иммунный ответ внутри нашего тела, который вырабатывает антитела. Эти антитела защищают нас от заражения, если настоящий вирус попадает в наш организм.
Эти антитела защищают нас от заражения, если настоящий вирус попадает в наш организм.
Вакцины с вирусным вектором
Вакцины с вирусным вектором используют модифицированную, безвредную версию другого вируса для передачи инструкций нашим клеткам. Вирус проникает в клетку и учит ее, как делать копии шиповидного белка, который затем запускает иммунный ответ внутри нашего тела. Этот иммунный ответ приводит к выработке антител, которые защищают нас от заражения, если настоящий вирус попадает в наш организм.
Белковые субъединичные вакцины
Субъединичные вакцины включают часть (белок) вируса, которая наилучшим образом стимулирует вашу иммунную систему. Как только ваша иммунная система распознает белковую субъединицу, она создает антитела и защитные лейкоциты. Если вы впоследствии заразитесь COVID-19вирус, антитела будут бороться с вирусом. Эти вакцины часто включают адъювант для усиления иммунного ответа организма.
Побочные эффекты и мониторинг безопасности
Существуют ли какие-либо опасения по поводу безопасности новых технологий (мРНК и нанотехнологий), используемых при разработке вакцин Pfizer-BioNTech и Moderna против COVID-19?
Нет никаких известных дополнительных рисков, связанных с мРНК-вакцинами или липидными наночастицами. Живые аттенуированные вирусные вакцины, такие как вакцина против кори, вызывают иммунный ответ, сходный с естественной инфекцией. С другой стороны, мРНК-вакцины просто дают организму инструкции производить одну очень специфическую часть вируса — в данном случае так называемый шиповидный белок — для того, чтобы затем вызвать иммунный ответ. Поскольку мРНК очень быстро расщепляется в организме человека, для выполнения своей работы она должна иметь возможность попасть в наши клетки, поэтому она обернута в липидную наночастицу. Как только она попадает в клетки для доставки инструкций, мРНК очень быстро разрушается. Он не проникает в ядро клетки или в наши гены. С тех пор как были введены новые мРНК-вакцины, их профили безопасности обнадеживают.
Живые аттенуированные вирусные вакцины, такие как вакцина против кори, вызывают иммунный ответ, сходный с естественной инфекцией. С другой стороны, мРНК-вакцины просто дают организму инструкции производить одну очень специфическую часть вируса — в данном случае так называемый шиповидный белок — для того, чтобы затем вызвать иммунный ответ. Поскольку мРНК очень быстро расщепляется в организме человека, для выполнения своей работы она должна иметь возможность попасть в наши клетки, поэтому она обернута в липидную наночастицу. Как только она попадает в клетки для доставки инструкций, мРНК очень быстро разрушается. Он не проникает в ядро клетки или в наши гены. С тех пор как были введены новые мРНК-вакцины, их профили безопасности обнадеживают.
С апреля 2021 г. сообщалось о редких случаях миокардита и перикардита у подростков и молодых людей (в возрасте до 30 лет) после введения мРНК-вакцины, чаще всего после введения 2-й дозы. Вакцинация против COVID-19 снижает риск развития у пациентов миокардита, вызванного инфицированием SARS-CoV-2 и развитием болезни COVID-19. Исследования показали, что риск миокардита был в 6 раз выше после заражения SARS-CoV-2, чем после введения мРНК-вакцины. Поствакцинальный миокардит протекает легче и требует более короткого пребывания в больнице (1-2 дня) по сравнению с миокардитом, вызванным инфекцией SARS-CoV-2, который протекает более тяжело и требует пребывания в больнице в среднем 5 дней. Педиатры должны выявлять миокардит и перикардит у подростков или молодых людей с острой болью в груди, одышкой или учащенным сердцебиением и сообщать о любых подозрительных случаях после COVID-19.прививка от ВАЕРС. История миокардита перикардита после дозы мРНК-вакцины также указана в качестве меры предосторожности для будущих доз. CDC продолжает следить за ситуацией и разработал руководство для медицинских работников
Исследования показали, что риск миокардита был в 6 раз выше после заражения SARS-CoV-2, чем после введения мРНК-вакцины. Поствакцинальный миокардит протекает легче и требует более короткого пребывания в больнице (1-2 дня) по сравнению с миокардитом, вызванным инфекцией SARS-CoV-2, который протекает более тяжело и требует пребывания в больнице в среднем 5 дней. Педиатры должны выявлять миокардит и перикардит у подростков или молодых людей с острой болью в груди, одышкой или учащенным сердцебиением и сообщать о любых подозрительных случаях после COVID-19.прививка от ВАЕРС. История миокардита перикардита после дозы мРНК-вакцины также указана в качестве меры предосторожности для будущих доз. CDC продолжает следить за ситуацией и разработал руководство для медицинских работников
Клинические соображения: миокардит после введения мРНК вакцин против COVID-19 | CDC
Какие побочные эффекты отмечены на сегодняшний день при применении мРНК-вакцин против COVID-19 (Pfizer-BioNTech и Moderna)?
Побочные эффекты были аналогичны другим обычным вакцинам — боль в руке, покраснение, усталость, лихорадка, озноб, головная боль, миалгия и артралгия. Побочные эффекты носят временный характер и в основном легкие или умеренные. Побочные эффекты могут ухудшиться после второй дозы у некоторых людей. После заражения COVID-19 наблюдалась анафилаксия.мРНК-вакцины, но это было редко. Сообщалось о чрезвычайно редких случаях миокардита или перикардита — чаще всего у мужчин в возрасте от 12 до 39 лет — и чаще всего после 2-й дозы. Дополнительную информацию о распространенных побочных эффектах и редких побочных реакциях можно найти здесь:
Побочные эффекты носят временный характер и в основном легкие или умеренные. Побочные эффекты могут ухудшиться после второй дозы у некоторых людей. После заражения COVID-19 наблюдалась анафилаксия.мРНК-вакцины, но это было редко. Сообщалось о чрезвычайно редких случаях миокардита или перикардита — чаще всего у мужчин в возрасте от 12 до 39 лет — и чаще всего после 2-й дозы. Дополнительную информацию о распространенных побочных эффектах и редких побочных реакциях можно найти здесь:
Возможные побочные эффекты после получения вакцины против COVID-19 | CDC
Отдельные нежелательные явления после вакцинации против COVID-19 | CDC
Какие побочные эффекты отмечены на сегодняшний день у Janssen COVID-19вакцина против вирусного вектора? Есть ли противопоказания?
Наиболее частыми побочными эффектами после вакцинации являются боль, покраснение и отек в руке, в которую сделали прививку, а также усталость, головная боль, мышечная боль, озноб, лихорадка и тошнота в течение первых нескольких дней.
CDC считает следующее противопоказанием к получению Janssen COVID-19: Тяжелая аллергическая реакция или немедленная аллергическая реакция любой степени тяжести на предыдущую дозу или компонент вакцины Janssen против COVID-19. Меры предосторожности следует принимать лицам, у которых в анамнезе была немедленная аллергическая реакция на другую вакцину или инъекционную терапию, а также лицам с умеренным или тяжелым острым заболеванием.
Кроме того, в декабре 2021 года FDA пересмотрело информационный бюллетень EUA для вакцины Janssen против COVID-19, включив в него: (1) противопоказание для лиц с историей тромбоза с тромбоцитопенией после введения вакцины Janssen против COVID-19 или любого другого аденовируса; векторные вакцины против COVID-19; и (2) предупреждение и меры предосторожности в отношении тромбоза с синдромом тромбоцитопении (ТТС), поскольку случаи ТТС после введения были зарегистрированы у мужчин и женщин в возрасте 18 лет и старше, с самым высоким показателем среди женщин в возрасте 30-49 лет. годы. Медицинские работники должны поддерживать высокий уровень настороженности в отношении симптомов, которые могут свидетельствовать о серьезных тромботических явлениях или тромбоцитопении у пациентов, недавно получивших вакцину Janssen против COVID-19. Дополнительную информацию см. в Сети предупреждений о здоровье CDC.
годы. Медицинские работники должны поддерживать высокий уровень настороженности в отношении симптомов, которые могут свидетельствовать о серьезных тромботических явлениях или тромбоцитопении у пациентов, недавно получивших вакцину Janssen против COVID-19. Дополнительную информацию см. в Сети предупреждений о здоровье CDC.
12 июля 2021 года FDA объявило о добавлении предупреждающей этикетки к вакцине Janssen против COVID-19 из-за повышенного риска редкого неврологического синдрома, называемого синдромом Гийена-Барре (СГБ). Новая предупредительная этикетка основана на предварительных данных после того, как в Системе отчетности о побочных эффектах вакцины было обнаружено около 100 сообщений о GBS из более чем 12,8 миллионов введенных доз вакцины Janssen. Каждый год примерно от 3000 до 6000 человек в США заболевают СГБ по разным причинам. Большинство людей полностью выздоравливают от расстройства.
Провайдеры вакцинации обязаны сообщать о случаях миокардита и перикардита после получения вакцины Janssen против COVID-19 в Систему отчетности о побочных эффектах вакцины (VAERS).
Центры по контролю и профилактике заболеваний (CDC) рекомендовали вакцины против COVID-19, отдавая предпочтение вакцине мРНК (Pfizer-BioNTech и Moderna) или вакцине с белковыми субъединицами (Novavax). Вакцина Janssen (вирусный вектор) доступна для лиц, которые не могут или не хотят получать другую вакцину и осведомлены о профиле безопасности.
Какие побочные эффекты отмечены на сегодняшний день при применении белковой субъединичной вакцины Novavax? Есть ли противопоказания?
Побочные эффекты, подобные другим вакцинам (например, лихорадка, озноб, усталость и головная боль), чаще возникают после введения второй дозы вакцины. Тяжелые аллергические реакции на вакцины редки, но могут случиться. Сообщалось о случаях миокардита и перикардита у людей, получивших вакцину Novavax COVID-19.
Вакцина Novavax COVID-19 не должна вводиться лицам с известной историей тяжелой аллергической реакции (например, анафилаксии) на любой компонент Novavax COVID-19Вакцина, адъювант.
Имеются ли какие-либо противопоказания для получения мРНК-вакцины против COVID-19 от Pfizer-BioNTech и Moderna?
CDC считает следующее противопоказанием к вакцинации вакцинами Pfizer-BioNTech и Moderna COVID-19: тяжелая аллергическая реакция (например, анафилаксия) после предыдущей дозы мРНК вакцины COVID-19 или любого из ее компонентов, немедленная аллергическая реакция любой степени тяжести на предыдущую дозу мРНК-вакцины COVID-19 или любого из ее компонентов (включая полиэтиленгликоль [ПЭГ]) и немедленная аллергическая реакция любой степени тяжести на полисорбат (из-за потенциальной перекрестной реактивной гиперчувствительности с ингредиент вакцины ПЭГ)*
У лиц, сообщающих об анафилаксии в анамнезе на другую вакцину (т. е. любую другую вакцину, кроме вакцин Pfizer-BioNTech и Moderna COVID-19) или инъекционную терапию, следует провести оценку риска для определения типа реакции и достоверности информации . У небольшого числа реципиентов после вакцинации Pfizer развилась анафилаксия. Рассмотрите возможность наблюдения за людьми со следующими медицинскими историями в течение 30 минут после вакцинации против COVID-19 для контроля аллергических реакций:
Рассмотрите возможность наблюдения за людьми со следующими медицинскими историями в течение 30 минут после вакцинации против COVID-19 для контроля аллергических реакций:
- Аллергическое противопоказание к другому типу вакцины против COVID-19
- Нетяжелая, немедленная (начало в течение 4 часов) аллергическая реакция после предыдущей дозы вакцины против COVID-19.
- Анафилаксия после введения вакцины, отличной от COVID-19, или инъекционной терапии
Пациентам с анафилаксией после первой дозы вакцины против COVID-19 следует рекомендовать не вводить вторую дозу и направлять к аллергологу-иммунологу для соответствующего наблюдения.
Нужно ли нам беспокоиться о росте MIS-C у детей, получающих вакцину против COVID-19?
На сегодняшний день MIS-C не возникало после получения вакцины против COVID-19 без инфекции SARS-CoV-2. Фактически, вакцина против COVID-19 обеспечивает защиту от MIS-C, поскольку недавнее исследование показало, что введение 2 доз вакцины Pfizer-BioNTech против COVID-19 высокоэффективно для предотвращения MIS-C у лиц в возрасте 12–18 лет.
Какие испытания безопасности были проведены для вакцин против COVID-19? Откуда мы знаем, что это безопасно в долгосрочной перспективе?
Последующее наблюдение за безопасностью вакцин против COVID-19 практически такое же, как и для всех испытаний вакцин. Все вакцины считаются безопасными и эффективными до того, как они будут одобрены или лицензированы.
Педиатрические исследования вакцин включают очень тщательное наблюдение и отслеживание состояния здоровья пациента и медицинской помощи после вакцинации (например, мониторинг побочных эффектов, визиты к врачу, использование новых лекарств или изменение предыдущих лекарств и другие взаимодействия после вакцинации). Все зарегистрированные медицинские события регистрируются и анализируются исследовательской группой, спонсором, независимым советом по мониторингу безопасности, комитетом по этике и FDA. Детей в этих исследованиях часто наблюдают в течение одного-двух лет после вакцинации, и их состояние здоровья контролируется на предмет безопасности вакцины.
Даже после авторизации или лицензирования данные о безопасности собираются через Систему отчетности о побочных эффектах вакцин (VAERS), канал передачи данных о безопасности вакцин (VSD), фармаконадзор, а для вакцин против COVID-19 — через систему под названием V-SAFE. Эти программы собирают информацию о еще большем количестве вакцинированных лиц, чем можно собрать в ходе клинических исследований.
Данные о безопасности за период более 2 лет собираются в ходе исследований, проводимых после лицензирования. Не было обнаружено ни одной лицензированной вакцины, которая имела бы неожиданную долгосрочную проблему безопасности, которая была бы обнаружена только спустя годы или десятилетия после внедрения.
Какие существуют программы надзора за безопасностью вакцин?
Все вакцины против COVID-19, одобренные и/или получившие разрешение на экстренное использование (EUA) Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA), а также вакцины, указанные в Рекомендованном календаре иммунизации детей и подростков, включая совместно вводимые вакцины, контролируются надежными службами FDA и CDC системы, которые контролируют безопасность вакцин в Соединенных Штатах. Эта система безопасности вакцин включает в себя Систему отчетности о побочных эффектах вакцины (VAERS), канал передачи данных о безопасности вакцины (VSD), оценку безопасности клинической иммунизации (CISA) и V-SAFE, новую систему на базе смартфона, добавленную в систему мониторинга безопасности специально для следить за побочными эффектами COVID-19вакцина. Эти системы доказали, что они работают, улавливая сигнал безопасности для чрезвычайно редкого осложнения вакцины Janssen против COVID-19. VAERS и VSD специально разработаны для мониторинга сигналов безопасности при одновременном введении нескольких вакцин (т. е. одновременном введении). Педиатры должны делиться с пациентами информацией о VAERS и поощрять регистрацию в программе V-SAFE во время посещения вакцинации.
Эта система безопасности вакцин включает в себя Систему отчетности о побочных эффектах вакцины (VAERS), канал передачи данных о безопасности вакцины (VSD), оценку безопасности клинической иммунизации (CISA) и V-SAFE, новую систему на базе смартфона, добавленную в систему мониторинга безопасности специально для следить за побочными эффектами COVID-19вакцина. Эти системы доказали, что они работают, улавливая сигнал безопасности для чрезвычайно редкого осложнения вакцины Janssen против COVID-19. VAERS и VSD специально разработаны для мониторинга сигналов безопасности при одновременном введении нескольких вакцин (т. е. одновременном введении). Педиатры должны делиться с пациентами информацией о VAERS и поощрять регистрацию в программе V-SAFE во время посещения вакцинации.
Обеспечение безопасности вакцин против COVID-19 в США | ЦКЗ
V-safe Проверка здоровья после вакцинации | CDC
Введение вакцины и клиническое руководство
Информация для специалистов в области здравоохранения и общественного здравоохранения по обмену информацией относительно решений в отношении вакцин и конкретных рекомендаций по введению вакцин.
Соблюдение рекомендуемых в настоящее время календарей прививок для детей, подростков и взрослых обеспечивает наилучшую защиту от серьезных заболеваний, которые можно предотвратить с помощью вакцин. Коалиция действий по иммунизации создала несколько ресурсов в виде резюме рекомендаций по иммунизации, в том числе «Сводка рекомендаций по иммунизации детей и подростков», «Сводка рекомендаций по иммунизации взрослых» и «Рекомендации по вакцинации медицинского персонала»9.0005
MDPH также описывает профессиональные рекомендации и требования в документе «Профессиональная иммунизация взрослых: Массачусетские рекомендации и требования».
CDC рекомендует, чтобы весь медицинский персонал, который вводит вакцины, прошел всестороннее компетентностное обучение правилам и процедурам введения вакцин ПЕРЕД введением вакцин. Всеобъемлющая подготовка на основе навыков должна быть интегрирована в существующие программы обучения персонала, такие как ориентация нового персонала и ежегодные требования к обучению. Доступно бесплатное электронное обучение по вакцинации, которое предлагает непрерывное обучение для медицинского персонала, включая CME, CNE, CEU, CPE, CPH и CHES.
Доступно бесплатное электронное обучение по вакцинации, которое предлагает непрерывное обучение для медицинского персонала, включая CME, CNE, CEU, CPE, CPH и CHES.
Медицинские работники штата Массачусетс, участвующие в Программе иммунизации, также должны соблюдать требования, изложенные в Руководстве по соблюдению требований Федерального управления по вакцинам (PDF) l (DOC). Посетите страницу управления вакцинами для получения дополнительной информации.
Информирование о преимуществах и рисках вакцинации
Хотя вы можете сделать ряд вещей, чтобы помочь сделать вакцины максимально безопасными и эффективными, предоставление пациентам или родителям/опекунам информации о вакцинах и иммунизации не менее важно.
Перед тем, как вводить каждую дозу определенных вакцин, по закону вы обязаны предоставить копию самого последнего Информационного бюллетеня о вакцинах (VIS) либо взрослому вакцинируемому, либо родителю/законному представителю ребенка. VIS разработаны CDC и обсуждают преимущества и риски, связанные с конкретными вакцинами. Вы также должны указать в карте пациента дату выдачи ВИС и дату публикации ВИС. Текущие VIS доступны на странице информационных заявлений CDC о вакцинах. Переводы на более чем 40 языков доступны на веб-сайте информационных заявлений о вакцинах Коалиции действий по иммунизации.
VIS разработаны CDC и обсуждают преимущества и риски, связанные с конкретными вакцинами. Вы также должны указать в карте пациента дату выдачи ВИС и дату публикации ВИС. Текущие VIS доступны на странице информационных заявлений CDC о вакцинах. Переводы на более чем 40 языков доступны на веб-сайте информационных заявлений о вакцинах Коалиции действий по иммунизации.
Другие материалы, такие как брошюры, видеоролики и наборы материалов, могут помочь вам в общении с пациентами или родителями о преимуществах и рисках вакцинации. Эти заслуживающие доверия ресурсы могут помочь поставщикам медицинских услуг и родителям/пациентам в обсуждениях и принятии решений о вакцинах:
- Создано Отделом иммунизации MDPH , Доверительное общение Разговор с пациентами о вакцине l (DOCX) лучшие ресурсы по:
- Методы связи для поставщиков услуг
- Статьи о недоверии к вакцинам
- Безопасность вакцин
- Работа с конкретными группами населения, сомневающимися в вакцинах
- Приложения, связанные с иммунизацией, для пациентов и медицинских работников
- CDC, AAP и AAFP создали веб-сайт «Ресурсы поставщиков для бесед с родителями о вакцинах», чтобы помочь ответить на вопросы о вакцинах и обеспечить успешные стратегии коммуникации, связанные с доверием к вакцинам.

- Образовательный центр по вакцинам Детской больницы Филадельфии предоставляет полную, актуальную и достоверную информацию о вакцинах родителям и медицинским работникам.
- Учебное пособие по иммунизации AAP охватывает все аспекты иммунизации в медицинском учреждении (включая безопасность вакцин и общение с родителями) для врачей, медсестер, практикующих медсестер, фельдшеров, фельдшеров и офис-менеджеров.
- Массачусетское отделение AAP обновляет этот список ресурсов, отражая новейшие инструменты для повышения уверенности в вакцинах и показателей иммунизации.
- Веб-сайт CDC по безопасности вакцин для поставщиков медицинских услуг и родителей описывает надежную систему, действующую в США для мониторинга и обеспечения безопасности вакцин.
- Веб-сайт ресурсов по безопасности вакцин Коалиции действий по иммунизации содержит список ссылок на более надежные источники информации о вакцинах
- Коалиция действий по иммунизации создала информационный бюллетень «Что делать, если вы не сделаете прививку своему ребенку» для родителей, в котором описаны последствия для их собственных детей и то, как их решения могут повлиять на других.
- Voices for Vaccines — это организация, управляемая родителями при поддержке ученых, врачей и представителей общественного здравоохранения, которая предоставляет родителям четкую, научно обоснованную информацию о вакцинах и болезнях, которые можно предотвратить с помощью вакцин, а также возможность присоединиться к общенациональной дискуссии о важности своевременной вакцинации.
- Вакцинируйте свою семью — это некоммерческая организация, стремящаяся уменьшить бремя болезней, которые можно предотвратить с помощью вакцин, в семьях и отдельных лицах.
- Руководство Американского колледжа врачей по иммунизации взрослых содержит важные ресурсы, а также информацию о вакцинах, чтобы помочь врачам повысить эффективность иммунизации взрослых в своей практике.
Экран для действительных противопоказаний и мер предосторожности
Противопоказания и меры предосторожности при вакцинации указывают, когда вакцины не следует вводить. Противопоказанием является состояние пациента, которое увеличивает вероятность серьезной нежелательной реакции. Как правило, вакцину не следует вводить при наличии противопоказаний. Мерой предосторожности является состояние пациента, при котором может увеличить вероятность серьезного побочного эффекта или сделать вакцину менее эффективной. Обычно вакцинацию откладывают, когда есть меры предосторожности. Однако могут возникнуть ситуации, когда польза от вакцинации перевешивает риск побочных эффектов, и врач может принять решение о вакцинации пациента. Большинство мер предосторожности и некоторые противопоказания носят временный характер, и вакцина может быть сделана позднее. Для получения подробной информации обратитесь к Руководству CDC по противопоказаниям к вакцинации детей.
Противопоказанием является состояние пациента, которое увеличивает вероятность серьезной нежелательной реакции. Как правило, вакцину не следует вводить при наличии противопоказаний. Мерой предосторожности является состояние пациента, при котором может увеличить вероятность серьезного побочного эффекта или сделать вакцину менее эффективной. Обычно вакцинацию откладывают, когда есть меры предосторожности. Однако могут возникнуть ситуации, когда польза от вакцинации перевешивает риск побочных эффектов, и врач может принять решение о вакцинации пациента. Большинство мер предосторожности и некоторые противопоказания носят временный характер, и вакцина может быть сделана позднее. Для получения подробной информации обратитесь к Руководству CDC по противопоказаниям к вакцинации детей.
Одним из ключей к предотвращению серьезных побочных реакций на вакцины является скрининг на противопоказания и меры предосторожности. Каждый медицинский работник, который вводит вакцины, должен обследовать каждого пациента перед введением дозы вакцины. Образцы анкет для скрининга доступны на сайте Коалиции действий по иммунизации.
Образцы анкет для скрининга доступны на сайте Коалиции действий по иммунизации.
Многие состояния часто ошибочно рассматриваются как противопоказания к вакцинации. В большинстве случаев , а не противопоказания:
- Легкие острые заболевания (например, диарея и незначительные заболевания верхних дыхательных путей, включая средний отит) с субфебрильной температурой или без нее
- Местные реакции от легкой до умеренной и/или субфебрильная или умеренная лихорадка после предшествующей дозы вакцины
- Современная антимикробная терапия
- Фаза выздоровления
- Недавний контакт с инфекционным заболеванием
- Преждевременные роды
- Грудное вскармливание
Введение вакцины
Правильное введение вакцины имеет решающее значение для обеспечения безопасности и эффективности вакцинации.
Посетите веб-сайт CDC Vaccine Administration или Immunization Action Coalition для получения информации и ресурсов по введению вакцин.
Это специальные ресурсы для помощи в введении вакцин:
- Введение вакцин: доза, путь, место и размер иглы
- Введение вакцин взрослым: доза, путь, место и размер иглы
- Вакцины с разбавителями: как их использовать
- Рекомендуемый и минимальный возраст и интервалы между дозами обычно рекомендуемых вакцин
- Контрольный список навыков по введению вакцин
Комиссар Департамента общественного здравоохранения штата Массачусетс в августе 2017 года разослал циркулярное письмо, озаглавленное «Управление иммунизацией фельдшерами» (DOC), чтобы проинформировать поставщиков первичной медико-санитарной помощи об утвержденных сертификатах, позволяющих фельдшерам проводить иммунизацию.
Выполнение действующих распоряжений в вашей практике может дать возможность другому медицинскому персоналу вводить вакцины и повысить уровень вакцинации. Образцы постоянных поручений и дополнительную информацию можно найти на странице Типовые постоянные поручения.
Клиники вакцинации
Руководство для клиник иммунизации (DOC) было разработано, чтобы помочь в планировании и работе клиник вакцинации, включая ежегодные клиники гриппа, школьные клиники и клиники вакцинации в ответ на небольшие чрезвычайные ситуации. В этом документе обобщаются ключевые моменты успешной работы клиники и приводятся ссылки на многие другие полезные ресурсы. Вы также можете ознакомиться с Руководством CDC по планированию вакцинационных клиник, проводимых во вспомогательных, временных или удаленных местах, в котором изложены логистика и соображения, необходимые для планирования крупномасштабной вакцинационной клиники. У Национального саммита по иммунизации взрослых и гриппу также есть много ресурсов для проведения вакцинационных клиник.
Документирование вакцин
Медицинские работники обязаны по закону записывать определенную информацию в медицинскую карту пациента. В штате Массачусетс медицинские работники, проводящие любую иммунизацию в Содружестве, должны отчитываться перед Информационной системой иммунизации штата Массачусетс (MIIS). Дополнительную информацию см. на веб-сайте MIIS.
Дополнительную информацию см. на веб-сайте MIIS.
Эти ресурсы MDPH могут помочь поставщикам с документированием вакцин:
- Форма регистрации введения вакцины (DOC)
- Сертификат иммунизации (DOC)
- Протокол введения вакцины в клинику иммунизации (DOC)
У Коалиции действий по иммунизации есть много ресурсов для ведения историй болезни пациентов и документирования вакцин.
Сообщите о предполагаемых побочных эффектах и ошибках вакцинации
Поставщики медицинских услуг, которые подозревают побочные эффекты вакцины, должны сообщать как в VAERS, так и в ISMP, как подробно описано ниже.
Система сообщений о побочных эффектах вакцин (VAERS) VAERS обеспечивает общенациональный механизм, с помощью которого можно сообщать о нежелательных явлениях после иммунизации, анализировать их и делать доступными для общественности. Медицинские работники должны сообщать о нежелательных явлениях, как указано в Таблице повреждений от вакцин (PDF). Также включены в качестве подлежащих регистрации явления, перечисленные во вкладыше производителя вакцины в качестве противопоказаний к получению дополнительных доз вакцины, и любые другие серьезные или необычные явления. Поставщики медицинских услуг и общественность могут сообщать о нежелательных явлениях, зайдя на веб-сайт VAERS и заполнив отчет онлайн, или заполнив форму VAERS в формате PDF и загрузив ее на веб-сайт VAERS. Дополнительную помощь можно получить по электронной почте [email protected] или по телефону (800) 822-7967.
Также включены в качестве подлежащих регистрации явления, перечисленные во вкладыше производителя вакцины в качестве противопоказаний к получению дополнительных доз вакцины, и любые другие серьезные или необычные явления. Поставщики медицинских услуг и общественность могут сообщать о нежелательных явлениях, зайдя на веб-сайт VAERS и заполнив отчет онлайн, или заполнив форму VAERS в формате PDF и загрузив ее на веб-сайт VAERS. Дополнительную помощь можно получить по электронной почте [email protected] или по телефону (800) 822-7967.
В дополнение к сообщениям о нежелательных явлениях, MDPH также рекомендует сообщать об ошибках введения вакцины (например, неверный путь, неправильная доза и неправильный возраст) в Институт безопасной медицинской практики (ISMP) через вакцину Программа сообщений об ошибках (VERP). ISMP — это некоммерческая организация, которая знакомит медицинское сообщество и потребителей с безопасными методами лечения. Провайдеры могут сообщать об этих ошибках, используя веб-сайт ISMP. Об ошибках введения вакцины также следует сообщать в VAERS (как описано выше) и НЕОБХОДИМО сообщать, если они привели к нежелательным явлениям.
Провайдеры могут сообщать об этих ошибках, используя веб-сайт ISMP. Об ошибках введения вакцины также следует сообщать в VAERS (как описано выше) и НЕОБХОДИМО сообщать, если они привели к нежелательным явлениям.
Помогите нам улучшить Mass.gov своими отзывами
Вы нашли то, что искали на этой веб-странице?Если у вас есть предложения по сайту, сообщите нам. Как мы можем улучшить страницу? *
Пожалуйста, не указывайте личную или контактную информацию.
Отзывы будут использованы только для улучшения сайта. Если вам нужна помощь, пожалуйста, свяжитесь с Департаментом общественного здравоохранения. Пожалуйста, ограничьте ввод до 500 символов.
Пожалуйста, удалите любую контактную информацию или личные данные из вашего отзыва.
Если вам нужна помощь, обратитесь в Департамент общественного здравоохранения.

 Вакцина против вирусного гепатита B
Вакцина против вирусного гепатита B