Устойчивость микробов к антибиотикам – глобальная проблема человечества
В конце апреля 2019 года ООН опубликовала поворотный по своей значимости отчет о масштабах и последствиях одной из глобальных проблем человечества – развития у опасных инфекций устойчивости (резистентности) к лекарствам, в том числе к антибиотикам. 700 тысяч человек ежегодно умирает из-за инфекций, вызванных микробами, которые стали невосприимчивыми к действию лекарственных препаратов. По прогнозам ученых, через 10 лет жертвами антибиотикорезистентности каждый год будут более 10 млн человек.
В этой статье старший научный сотрудник ФГБУ «ВГНКИ» Дмитрий Макаров рассказывает о причинах и масштабах проблемы и дает рекомендации, как избежать заражения опасными устойчивыми инфекциями.
Что такое антибиотикорезистентность?
Антибиотикорезистентность – это способность микробов противостоять действию антимикробных средств, в том числе антибиотиков. С 2000-х годов Всемирная организация здравоохранения называет антибиотикорезистентность одной из самых серьезных угроз для здоровья животных и человека.
Каждый год в мире более 700 тысяч человек умирает от инфекций, вызванных устойчивыми микробами. Для других пациентов удлиняется время госпитализации. Известный британский экономист профессор лорд Джим О’Нил прогнозирует, что через 30 лет от устойчивых микробов будет умирать уже 10 миллионов человек в год. Экономический ущерб исчисляется миллиардами долларов. Колоссальный урон наносится и отрасли животноводства.
При этом масштаб проблемы в мире неуклонно растет. В начале этого года в медицинском журнале The Lancet опубликована статья; авторы оценили, что урон для жизни и здоровья населения Европы от устойчивых инфекций с 2007 по 2015 год удвоился. Воспаление легких, дизентерия, сепсис, туберкулез, малярия – это всего лишь несколько болезней, при лечении которых врачи сталкиваются с устойчивостью возбудителей к антибиотикам.
Обнаруживают все больше патогенных бактерий с устойчивостью сразу к нескольким группам антибиотиков и даже так называемых ПАНРЕЗИСТЕНТНЫХ, т. е. устойчивых ко всем используемым против них препаратам. Если раньше такие бактерии находили только в больницах, то сейчас их находят даже в продуктах питания.
е. устойчивых ко всем используемым против них препаратам. Если раньше такие бактерии находили только в больницах, то сейчас их находят даже в продуктах питания.
Как микробы становятся устойчивыми к антибиотикам?
Антибиотикорезистентность возникла и развивалась еще ДО открытия антибиотиков человеком.
Миллиарды лет бактерии вырабатывали вещества для борьбы с другими бактериями – антибиотики. Другие микроорганизмы, в свою очередь, приобретали механизмы защиты от таких соединений. Таким образом, антибиотикорезистентность – это древнее явление.
Она всегда определяется генами и передается из поколения в поколение. Ученые нашли такие гены даже в арктической вечной мерзлоте возрастом 30 тысяч лет и в образцах кишечной микрофлоры Тирольского человека. Это найденная в Альпах мумия возрастом более 5 тысяч лет. И сейчас в окружающей среде и у диких животных устойчивые бактерии и гены устойчивости встречаются повсеместно.
Микробы становятся устойчивыми к антибиотикам либо в результате случайного изменения генов – мутаций, либо в результате передачи генов устойчивости от другого микроба, который уже обладает этим свойством.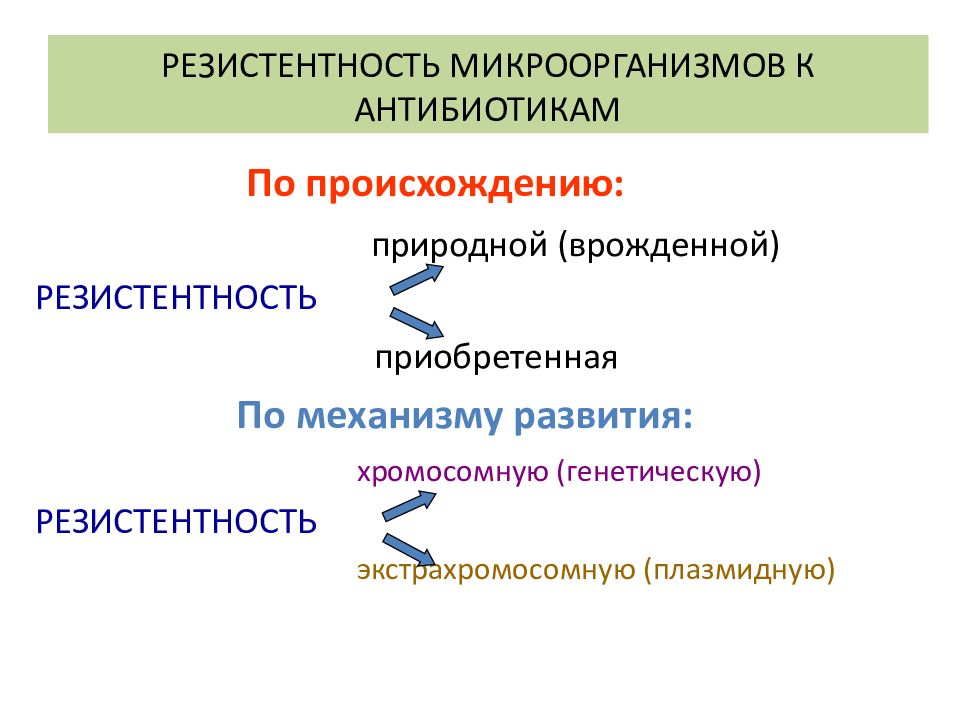 Даже если устойчивость приобрели безобидные бактерии, населяющие кишечник животных или человека, или свободные бактерии в окружающей среде – эти гены могут передаться оказавшимся рядом болезнетворным бактериям.
Даже если устойчивость приобрели безобидные бактерии, населяющие кишечник животных или человека, или свободные бактерии в окружающей среде – эти гены могут передаться оказавшимся рядом болезнетворным бактериям.
Если на группу бактерий (популяцию) в организме человека, животного или в окружающей среде воздействует антимикробное средство, в такой популяции выживают только устойчивые бактерии. Выиграв конкурентную борьбу, они размножаются, распространяются и передают свои гены дальше. Это явление под названием «селективное давление» и определяет опасность использования антибиотиков.
Когда впервые появилась проблема?
На момент внедрения антибиотиков в практику устойчивость к ним бактерий была редким явлением. Это привело к беспрецедентному прорыву в медицине.
Однако специалисты уже тогда понимали, что долго такое благоденствие не продлится. Еще сэр Александр Флеминг, первооткрыватель пенициллина, первого антибиотика, в лекции по случаю вручения ему Нобелевской премии в 1945 году предупреждал об опасности приобретения патогенными бактериями устойчивости к пенициллину.
С учетом масштабов применения антибиотиков в животноводстве и медицине, рост и распространение устойчивости были всего лишь вопросом времени. Довольно долго ущерб от резистентности сдерживался открытием новых антибиотиков. Но если в период «антибиотикового бума» середины ХХ века в год ученые открывали десятки новых препаратов, то с начала XXI века медицина получила всего два новейших класса антибактериальных препаратов.
У проблемы антибиотикорезистентности есть две стороны: медицинская и ветеринарная. Конечно, основная проблема для здравоохранения – это применение антибиотиков в медицине, в особенности неправильное: например, назначения в отсутствие показаний, безрецептурная продажа и самолечение, изобилие контрафактных и некачественных антибиотиков.
Распространению резистентности способствует и то, что в развивающихся странах значительно возросла доступность препаратов для населения, а также все более активное перемещение по миру людей, животных, обмен продуктами питания и другими товарами, а с ними – и устойчивыми микроорганизмами.
Но и сельское хозяйство играет немаловажную роль в процессе развития и распространения резистентности.
На животноводство приходится приблизительно ¾ производимых в мире объемов антибактериальных средств. При этом большинство классов антимикробных средств – общие для медицины и ветеринарии. В сельском хозяйстве их используют для профилактики и лечения инфекций животных и даже в качестве стимуляторов роста.
Да-да, никто точно не знает как, но небольшое количество антибиотиков, добавляемое в корм скоту, действительно способствует увеличению привесов. Однако самая большая опасность для здоровья населения как раз и скрывается в таком постоянном использовании малых доз антибиотиков.
В хозяйствах появляются и распространяются устойчивые бактерии. Среди них есть и зоонозные, то есть те, которые могут вызывать заболевания как животных, так и человека.
Сальмонеллез, кампилобактериоз, колибактериоз, йерсиниоз… Эти инфекционные заболевания чаще всего характеризуются тошнотой, рвотой, диареей и сильными болями в течение нескольких дней. Намного опаснее зоонозные инфекции для людей с ослабленным иммунитетом, детей и пожилых, а некоторые штаммы вируса могут привести к летальному исходу. В тяжелых случаях для лечения необходимы антибиотики, поэтому заражение устойчивыми бактериями особенно опасно.
Намного опаснее зоонозные инфекции для людей с ослабленным иммунитетом, детей и пожилых, а некоторые штаммы вируса могут привести к летальному исходу. В тяжелых случаях для лечения необходимы антибиотики, поэтому заражение устойчивыми бактериями особенно опасно.
Возникающие в хозяйствах устойчивые бактерии заражают людей тремя основными способами:
– Через продукцию животноводства. Часто причиной заражения является плохо прожаренный фарш, сырые куриные яйца и молоко, но источниками заразы могут быть даже овощи с фруктами.
– Через контакт с зараженными животными – в зоне риска в первую очередь работники животноводческих предприятий.
– Через воду, почву и другие компоненты окружающей среды, животных-переносчиков, таких как насекомые, грызуны.
Вклад в проблему вносят, вероятно, и остатки антибиотиков в продуктах питания животного происхождения, способствуя селекции устойчивых бактерий в организме потребителей.
Бывает и так, что антибиотик снижает эффективность в медицине исключительно из-за его применения в животноводстве. Хороший пример – колистин. Долгое время этот препарат против кишечной палочки почти не применяли в медицине из-за тяжелых побочных эффектов, но его активно использовали в качестве стимулятора роста для скота. Однако, несмотря на побочные эффекты, препарат недавно был отнесен к резервным антибиотикам для людей, то есть таким, которые применяют, когда ничего другое уже не помогает.
Хороший пример – колистин. Долгое время этот препарат против кишечной палочки почти не применяли в медицине из-за тяжелых побочных эффектов, но его активно использовали в качестве стимулятора роста для скота. Однако, несмотря на побочные эффекты, препарат недавно был отнесен к резервным антибиотикам для людей, то есть таким, которые применяют, когда ничего другое уже не помогает.
В Китае несколько лет назад колистин в медицине не использовали совсем, но неожиданно в госпиталях одного города врачи обнаружили устойчивую к нему кишечную палочку. Сравнив гены бактерий из больниц и с окрестных ферм, ученые выяснили: устойчивая к колистину кишечная палочка появилась на фермах и была занесена в больницы на лапках мух.
В результате в Китае запретили добавлять колистин в корм скоту для увеличения привесов.
Что мировое сообщество предпринимает для решения проблемы
Стратегия борьбы с устойчивостью к антибиотикам сегодня есть во многих странах, в том числе в сфере животноводства. Здесь им помогают организации, такие как Всемирная организация здравоохранения (ВОЗ) и Всемирная организация здравоохранения животных (МЭБ), которые разрабатывают стратегии борьбы и полезные рекомендации.
Здесь им помогают организации, такие как Всемирная организация здравоохранения (ВОЗ) и Всемирная организация здравоохранения животных (МЭБ), которые разрабатывают стратегии борьбы и полезные рекомендации.
Основа таких мер, конечно же, – это ограничение применения антибиотиков за счет разумного и рационального их использования. Многочисленные научные исследования показали, что снижение применения антибиотиков ведет и к снижению распространения устойчивых бактерий.
В сфере животноводства ключевые пункты стратегий – это ограничения использования важных для медицины препаратов, таких как уже упоминавшийся колистин, ципрофлоксацин, цефалоспорины последних поколений, которые следует использовать только в том случае, если ничего другого животному уже не поможет, но никак не для профилактики или стимуляции роста.
Другой важный пункт – соблюдение правил санитарии, которое предотвращает занос инфекций.
Хорошее подспорье в профилактике и борьбе – это средства, альтернативные действию антибиотиков: вакцины, бактериофаги, пробиотики, эфирные масла растений и так далее.
Важно и обучение ветеринарных врачей грамотному назначению антимикробных препаратов.
Лидеры по снижению использования антибиотиков в животноводстве – страны Европы: Нидерланды, Дания, Норвегия, Франция, Бельгия, Германия и другие. Работают над этим и страны Азии, например Япония и Таиланд. США больше рассчитывают на открытие новых антибиотиков.
Россией уже принята собственная Стратегия противодействия антибиотикорезистентности, составленная в соответствии с международными принципами. Исследования в рамках этой стратегии проводит в том числе наш институт – подведомственный Россельхознадзору Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов. Мы проводим научную работу, в которой изучаем устойчивость зоонозных бактерий ко всем группам антибиотиков. Бактерий – сальмонелл, кампилобактера, кишечную палочку, энтерококков – мы выделяем из продуктов питания животного происхождения и получаем от разных видов животных (коров, свиней и даже оленей) и птицы.
Как же снизить риск заражения устойчивыми бактериями?
Необходим помнить, что один из основных путей заражения – пищевой. Чтобы обезопасить себя от пищевых инфекций, необходимо соблюдать несколько несложных правил, сформулированных ВОЗ:
- Подвергайте пищу тщательной термической обработке. Температура продукта должна быть минимум 70 °С.
- Съедайте приготовленную пищу горячей, поскольку при остывании велика вероятность размножения в ней различного рода бактерий. Если разогреваете пищу, то делайте это при той же температуре – не ниже 70 °С.
- Храните пищу при температуре не выше 10 °С.
- Не допускайте контакта сырой и приготовленной пищи. Например, не стоит резать ножом сырое мясо, а потом сразу сыр.
- Мойте руки перед приготовлением еды. Тщательно мойте фрукты и овощи.
- Держите кухню и все кухонные принадлежности в чистоте, не допускайте появления насекомых и тем более мышей и крыс.
- Помните, что опасные бактерии могут попасть в пищу от собак, кошек, птиц и других домашних животных.
 Соблюдайте простые правила гигиены и следите за здоровьем ваших питомцев.
Соблюдайте простые правила гигиены и следите за здоровьем ваших питомцев.
Дмитрий Макаров, Анастасия Мазнева
Резистентность к антибактериальной терапии (краткий обзор)
ПРОБЛЕМА РЕЗИСТЕНТНОСТИ
Штаммы микроорганизмов, устойчивые к антибактериальным препаратам, могут образовываться либо путем мутации (вертикальная передача признака), либо путем передачи генов резистентности от одних бактерий к другим (горизонтальная передача) (Rosamund W., 2001).
Чтобы лучше понять механизм развития резистентности, остановимся на двух аспектах этого процесса: с одной стороны, во время экспозиции антибиотика в макроорганизме происходит очень быстрая селекция устойчивых штаммов, обусловленная тем, что антибактериальный препарат устраняет конкурирующие микроорганизмы, тем самым освобождая путь для прогрессивного размножения устойчивых штаммов; с другой стороны, феномен плазмидной конверсии приводит к передаче плазмидных генов резистентности от устойчивого микроорганизма к чувствительному.
В экономическом плане повышение резистентности микроорганизмов означает увеличение стоимости терапии во много раз. Например, если ранее стоимость курса лечения больных туберкулезом составляла 20 долларов США, то теперь она возросла в 100 раз.
Способствует ли применение антибиотиков повышению антибиотикорезистентности?
Применение антибиотиков не вызывает резистентности, поскольку, приобретение ее микроорганизмами — естественный процесс, считает Вильямс Розамунд, координатор отдела ВОЗ по вопросам резистентности к антибактериальным препаратам и сдерживанию ее распространения. Однако в результате неправильного применения антибактериальной терапии этот процесс значительно ускоряется. Происходит естественный отбор, способствующий селекции тех микроорганизмов, которые случайно (путем мутации или плазмидной конверсии) приобрели устойчивость к антибактериальным средствам (Rosamund W., 2001).
Подобные неблагоприятные процессы могут многократно ускоряться вследствие бесконтрольного применения антибиотиков. Причиной этого является отсутствие единой политики относительно назначения антибактериальных средств на национальном или международном уровне. Во многих странах антибиотики можно приобрести без рецепта, к тому же наблюдается бесконтрольное их применение в животноводстве, рыбном и сельском хозяйстве.
Причиной этого является отсутствие единой политики относительно назначения антибактериальных средств на национальном или международном уровне. Во многих странах антибиотики можно приобрести без рецепта, к тому же наблюдается бесконтрольное их применение в животноводстве, рыбном и сельском хозяйстве.
ПРИЧИНЫ НЕОБОСНОВАННОГО НАЗНАЧЕНИЯ АНТИБАКТЕРИАЛЬНЫХ ПРЕПАРАТОВ
Чрезмерное и неуместное использование антибактериальных препаратов не помогает пациентам, а лишь повышает резистентность микроорганизмов. На уровне первичного звена медико-санитарной помощи 30–60% пациентов получают антибиотики, возможно, в два раза чаще, чем это требуется по клиническим показаниям (Holloway K., 2001).
Причины частого и необоснованного назначения антибактериальных препаратов:
-
недостаток знаний и объективной информации
-
боязнь неудачного исхода лечения
-
требование пациента
-
продажа лекарственных средств — источник заработка врача.

Кетлин Холовей, сотрудник Департамента основных лекарственных средств и политики в области медикаментов ВОЗ, комментирует тезис о недоступности достоверной информации для врачей. В развивающихся странах многим врачам недоступна доказательная информация в отношении диагностики и антибактериальной терапии, к тому же их работа не контролируется. Во многих развивающихся странах проводимых методов диагностики часто недостаточно для назначения обоснованной этиотропной терапии (применяется так называемая эмпирическая антибиотикотерапия. — Прим. авт.) (Holloway K., 2001).
РОЛЬ СОЦИАЛЬНОГО ФАКТОРА
Бурное развитие и распространение резистентных штаммов микроорганизмов наблюдается в развивающихся странах. Причиной этого является частое и неправильное использование антибактериальных препаратов. Вследствие недостатка финансовых средств для проведения полного курса лечения антибактериальные препараты принимаются в заниженных дозах.
Согласованный список мер вмешательства для сдерживания устойчивости
к антибактериальным препаратам (Holloway K., 2001)
| Целевая группа | Рекомендуемая мера вмешательства |
А |
|
В |
|
С |
|
D |
|
Е |
|
F |
|
Неадекватная практика назначения антибактериальных препаратов (включая неправильные выбор препарата, его дозы или определение продолжительности курса лечения), несоблюдение пациентом режима лечения и использование некачественных (иногда фальсифицированных) препаратов способствуют развитию резистентности (Rosamund W. , 2001).
, 2001).
Социальный аспект проблемы резистентности состоит в том, что любой фактор нестабильности в обществе — бедность, массовая миграция, загрязнение окружающей среды и др. — способствует росту заболеваемости среди населения, а следовательно, и появлению большого количества резистентных штаммов микроорганизмов. Широкое и быстрое распространение резистентных штаммов за пределы эндемической зоны происходит в результате развития туризма и торговых связей (Rosamund W., 2001):
-
резистентные к антибиотикам штаммы гонореи были завезены в Австралию туристами из стран Юго-Восточной Азии;
-
заболевание туберкулезом в странах Западной Европы вызвано полирезистентными штаммами, источники распространения которых были обнаружены в странах Восточной Европы, где борьба с этим заболеванием ведется не на должном уровне;
-
источниками госпитальной инфекции MRSA (Staphylococcus aureus, резистентный к метициллину), две вспышки которой зарегистрированы в Канаде, были пациенты, прибывшие из Индии.

Таким образом, в настоящее время одной из основных задач является замедление развития и распространения антибиотикорезистентных микроорганизмов. Для эффективной борьбы с РАБ необходимо установить причины необоснованного назначения лекарственных средств и предпринять соответствующие меры во избежание подобных случаев проведения антибиотикотерапии (Holloway K., 2001).
МЕРЫ, ПРЕДПРИНИМАЕМЫЕ ВОЗ
Несомненным является факт, что поскольку проблема антибиотикорезистентности микроорганизмов признана глобальной, должны предприниматься меры для ее решения на уровне межправительственных органов, каким является ВОЗ.
ВОЗ возглавила деятельность, направленную на разработку Глобальной стратегии сдерживания распространения устойчивости к антибактериальным препаратам. Стратегия основывается на публикации научных данных, мнений экспертов, дискуссиях специалистов. В ее функции также входит публикация обзоров, посвященных изучению факторов, обусловливающих развитие и распространение РАБ, а также предложенных и апробированных эффективных мер вмешательства для решения этой проблемы. Глобальная стратегия предполагает рекомендовать основные меры вмешательства для внедрения в практику.
Глобальная стратегия предполагает рекомендовать основные меры вмешательства для внедрения в практику.
Целью стратегии является также то, что нужно обратить внимание на пробелы в современных научных исследованиях и определить основные их направления. Это прежде всего касается создания новых лекарственных средств для борьбы с резистентными штаммами, разработки действенных стимулов научного поиска, а также содействия партнерству между частными и государственными предприятиями для решения проблемы распространения антибиотикорезистентности.
Возникновению РАБ способствуют различные факторы, подобно тому, что может существовать множество подходов для торможения роста и сдерживания распространения антибиотикорезистентности. В разработанной ВОЗ Глобальной стратегии сдерживания распространения устойчивости к антибактериальным препаратам (http://www.who.int/tmc/amr.htmlrel=»nofollow»>) упоминается 64 возможные меры вмешательства. Из них 44 направлены на повышение эффективности использования антибактериальных препаратов (исключая меры, касающиеся использования этих препаратов у животных; создание новых вакцин и лекарственных средств; международные мероприятия) (Holloway K. , 2001).
, 2001).
Денис Сухинин
* По материалам «Монитора основных лекарственных средств» («Essential Drug Monitor»), № 12–13, 2001 г.
Бактерии научились приобретать устойчивость к антибиотикам в два шага
Движение двух фронтов бактериальных колоний навстречу друг другу. В центре концентрация антибиотика максимальная.
Michael Baym et al., Science
Микробиологи обнаружили, что резистентность бактерий к антибиотикам гораздо стремительнее
развивается на фоне толерантности и находится с ней в тесной связи. Возможно, предотвращение
развития толерантности способно решить проблему возникновения лекарственной
устойчивости. Исследование опубликовано в журнале Science, кратко с его результатами можно ознакомиться в пресс-релизе Еврейского университета в Иерусалиме.
Возможно, предотвращение
развития толерантности способно решить проблему возникновения лекарственной
устойчивости. Исследование опубликовано в журнале Science, кратко с его результатами можно ознакомиться в пресс-релизе Еврейского университета в Иерусалиме.
С самого первого применения пенициллина и до наших дней бактерии усердно эволюционируют в сторону невосприимчивости к антибиотикам, а ученые непрерывно придумывают, что этому противопоставить. К несчастью, пока человечество скорее проигрывает в этой борьбе.
К лекарственной устойчивости можно прийти разными путями
— приобрести молекулярный насос, выкачивающий молекулы антибиотика из клетки,
научиться заблаговременно разрушать их, переделать до неузнаваемости мишень, на
которую направлено действие препарата или, например, подставить антибиотику «ложные цели», как это научился делать золотистый
стафилококк. В любом случае, для человечества результат закономерен — снижение
эффективности лекарств, а в конце концов — полная их бесполезность в пока еще некоторых случаях.
Известно, что для бактерий приобретение резистентности не единственный способ выживания — существует еще толерантность, подразумевающая «замирание» микроорганизма, при котором он не может расти и размножаться, но и не умирает. Попав в благоприятную среду, бактерии не сразу переходят к экспоненциальному росту — ему предшествует латентная фаза, когда микробы обживаются на новом месте. Некоторые антибиотики, например ампициллин, препятствуют строительству клеточной стенки бактерий, то есть действуют только в фазу активного роста. А значит микроорганизмам ради спасения не обязательно изобретать способы борьбы с лекарством — достаточно просто задержаться в латентной фазе и потом продолжить беззаботное существование. В основе обоих путей борьбы с антибиотиками лежат мутации, но толерантность позволяет лишь переждать неблагоприятные условия, а резистентность — справиться с ними раз и навсегда.
Единого мнения о том, как именно на эволюцию
резистентности влияют толерантные штаммы, у научного сообщества до сих пор нет.
Чтобы разобраться в этом вопросе, ученые взяли кишечную палочку и устроили эволюцию в лабораторном масштабе. Для этого культуры помещали в питательную среду с высокой, но сопоставимой с терапевтическими дозами концентрацией ампициллина. Через 4,5 часа клетки возвращали в среду с небольшой, в сто раз меньшей, концентрацией антибиотика, где они восстанавливались и нарастали в течение ночи. Затем клетки ночной культуры снова высевали на среду с высокой концентрацией и повторяли цикл до тех пор, пока у бактерий не выработалась резистентность.
Эффект от возникших толерантных мутаций оценивали по проценту колоний, находившихся в латентной фазе дольше 4,5 часов, а эффект резистентных — по минимальной концентрации антибиотика, ингибирующей рост бактерий (МИК).
В результате, когда ученые добились
резистентности, МИК оказалась по меньшей мере в семь раз выше по сравнению со
значением для обычных популяций. Последующий геномный анализ устойчивых культур
показал, что все они приобрели усиливающие экспрессию мутации промоторной
области гена ampC, который кодирует
разрушающий ампициллин фермент.
Последующий геномный анализ устойчивых культур
показал, что все они приобрели усиливающие экспрессию мутации промоторной
области гена ampC, который кодирует
разрушающий ампициллин фермент.
При дальнейшем анализе ученые обнаружили, что уже после 3-4 циклов эксперимента большинство бактерий даже на нормальной среде демонстрируют отложенный рост — ту самую задержку в латентной фазе. При этом свидетельствующая о развитии резистентности МИК начинает расти существенно позже — между 7 и 17 циклом. Не объясненным оставалось только как именно происходит переход между обычной популяцией и резистентной — через толерантную или напрямую.
Предлагаемый авторами механизм возникновения резистентной популяции на фоне толерантной. Обыкновенная популяция эволюционирует в толерантную (синяя стрелка), что способствует выживанию большего числа бактерий и служит опорой для развития резистентности (красная стрелка)
Генетический анализ показал, что обладатели резистентных мутаций в ampC несут также и мутации, приводящие к толерантности, причем последние появились раньше, а значит резистентность возникла на фоне толерантности. Более того, оказалось, что
на ее фоне резистентность развивается гораздо быстрее. Причина, судя по всему,
в том, что при таком цикличном протоколе возможность возникновения и
закрепления мутаций зависит от двух ключевых моментов — вероятности возникновения мутации как таковой и вероятности того, что тот, у кого она
возникла, пережил воздействие антибиотика. К тому же приводящие к толерантности
мутации возникают чаще — хотя бы потому, что могут происходить во многих местах генома,
в то время как резистентные ограничены зоной промотора гена ampC.
Более того, оказалось, что
на ее фоне резистентность развивается гораздо быстрее. Причина, судя по всему,
в том, что при таком цикличном протоколе возможность возникновения и
закрепления мутаций зависит от двух ключевых моментов — вероятности возникновения мутации как таковой и вероятности того, что тот, у кого она
возникла, пережил воздействие антибиотика. К тому же приводящие к толерантности
мутации возникают чаще — хотя бы потому, что могут происходить во многих местах генома,
в то время как резистентные ограничены зоной промотора гена ampC.Вероятно, большее число толерантных особей создает
потенциал, дающий преимущество для возникновения редких резистентных мутаций.
Иными словами, толерантность способствует возникновению мутаций резистентности
тем, что снижает вероятность потерять их. Ученые посчитали, что при выбранной
схеме эксперимента переход от обычной популяции к резистентной напрямую, минуя
толерантную, состоялся бы более чем через 100 циклов (против 17, наблюдавшихся в эксперименте).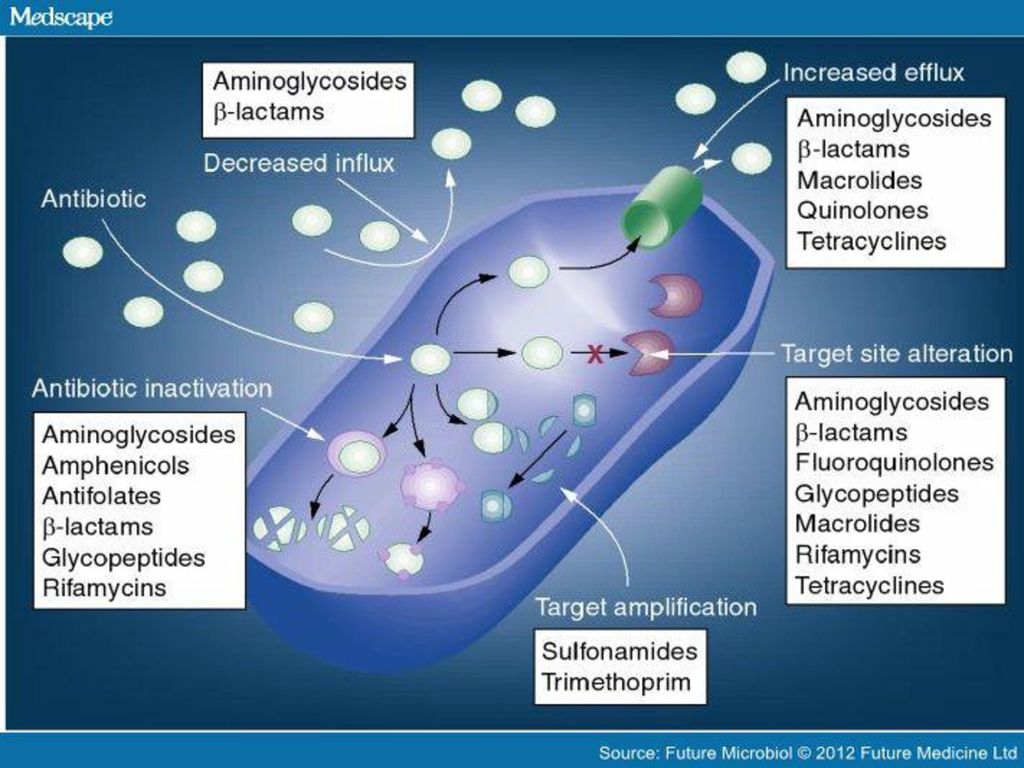
В свете новых данных механизм приобретения полной резистентности представляется следующим образом — часто происходящие мутации приносят в популяцию толерантность, которая более чем на порядок увеличивает выживаемость, а следующие за ними более узконаправленные мутации в ampC существенно повышают МИК, увеличивая выживаемость еще сильнее. Особенно важно то, что происходит это даже при очень высоких концентрациях антибиотика — толерантность позволяет закрепиться частичной резистентности, которая затем легко переходит в полную.
В целом, значимая для развития резистентности роль толерантности открывает возможность использовать ее в разработке новых подходов лечения, препятствующих возникновению устойчивости.
Юрий Солюс
Резистентность к антибиотикам в свиноводстве: частые вопросы (1 из 2) — Статьи
Что такое антимикробная резистентность, почему и как она возникает?
Резистентность к антибиотикам – это явление, благодаря которому на бактерии не влияет летальное или ингибирующее воздействие антимикробной молекулы.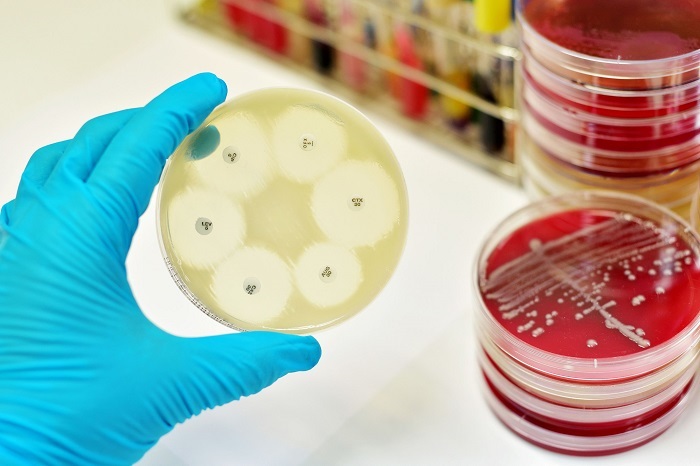 Этот процесс происходит регулярно в природе в течение тысяч лет: антибиотики производятся бактериями и грибами в природе с целью устранения конкуренции в конкретной экологической нише.
Этот процесс происходит регулярно в природе в течение тысяч лет: антибиотики производятся бактериями и грибами в природе с целью устранения конкуренции в конкретной экологической нише.
Бактерии, которые контактируют с этими антибиотиками, разрабатывают механизмы, чтобы противостоять им, позволяя им колонизировать места с питательными веществами и малым числом конкурентов.
Большинство антибиотиков, используемых как в медицине человека, так и в ветеринарной медицине, происходят из природы от этих соединений, и это всего лишь вопрос времени, чтобы клиническое использование антибиотиков позволяло выбирать эти очень эффективные механизмы сопротивления, созданные природой.
Передается ли резистентность к антибиотикам между различными типами бактерий?
Да, и это одна из главных проблем. В общем, бактерии имеют три способа противодействовать воздействию антибиотиков: путем изменения мишени антибиотика, путем разрушения антибиотика или путем вытеснение антибиотика наружу. Как правило, эти механизмы сопротивления могут передаваться как по вертикали, так и по горизонтали, что означает, что они могут передаваться как следующим поколениям, так и другим бактериям того же или другого вида.
Как правило, эти механизмы сопротивления могут передаваться как по вертикали, так и по горизонтали, что означает, что они могут передаваться как следующим поколениям, так и другим бактериям того же или другого вида.
Могут ли одни и те же бактерии быть устойчивыми к нескольким антибиотикам?
Бактерии способны аккумулировать резистентные механизмы в отношении нескольких антибиотиков. Это происходит главным образом в местах с большим уровнем присутствия антибиотиков, таких как больницы или, в некоторой степени, животноводческие фермы. В такой среде бактерии должны развиваться, чтобы выжить, поэтому они адаптируются и приобретают резистентные гены из окружающей среды. Примером этого в условиях ферм являются бактерии из окружающей среды или бактерии, присутствующие в микробиоте животных, которые, возможно, недавно были определены в стада.
Являются ли резистентные гены общераспространенными для нас?
Без сомнений. Поскольку это естественный защитный механизм против естественных антимикробных молекул, резистентные гены обнаруживаются во всех экологических нишах. Кроме того, распространение резистентных генов является глобальной проблемой, поскольку использование антибиотиков или их присутствие в окружающей среде привело к позитивному отбору бактерий с этими генами. В сегодняшнем мире, где человек, животное, еда или материал могут легко перемещаться с одного места на другое за тысячи километров в течение нескольких часов, не являются нереалистичными мысли, и даже доказано, что резистентные гены распространяются так легко. Также верно, что уровень резистентности в некоторых странах выше, и это связано, в частности, с их национальными планами по борьбе с антимикробной резистентностью.
Поскольку это естественный защитный механизм против естественных антимикробных молекул, резистентные гены обнаруживаются во всех экологических нишах. Кроме того, распространение резистентных генов является глобальной проблемой, поскольку использование антибиотиков или их присутствие в окружающей среде привело к позитивному отбору бактерий с этими генами. В сегодняшнем мире, где человек, животное, еда или материал могут легко перемещаться с одного места на другое за тысячи километров в течение нескольких часов, не являются нереалистичными мысли, и даже доказано, что резистентные гены распространяются так легко. Также верно, что уровень резистентности в некоторых странах выше, и это связано, в частности, с их национальными планами по борьбе с антимикробной резистентностью.
Как может антимикробная резистентность быть измерена/ оценена?
Уровень антимикробной резистентности можно измерить с использованием нескольких методов. Классические методы, такие как определение антимикробной активности посредством диффузии и метод микроразведений, позволяют нам, когда выделен возбудитель, определить антибиотики, к которым он устойчив или чувствителен, и знать его уровень резистентности. Эти методы, широко используемые в медицине человека, должны быть в значительной степени реализованы в области ветеринарии, так как они имеют высокий уровень рентабельности.
Эти методы, широко используемые в медицине человека, должны быть в значительной степени реализованы в области ветеринарии, так как они имеют высокий уровень рентабельности.
С другой стороны, современные методы молекулярной биологии позволяют нам знать уровень резистентности в более широких пределах. В настоящее время наша лаборатория является частью самого важного европейского проекта ветеринарной медицины для борьбы с резистентностью к антибиотикам в пищевой цепи под названием EFFORT (Мониторинг экологии антимикробной резистентности от фермы до стола потребителя). Этот проект осуществляется согласованным образом в 10 странах Европейского Союза, где были взяты образцы на всех уровнях, начиная от животноводческих хозяйств (свиноводческих хозяйств, птицеводческих хозяйств, хозяйств по выращиванию индеек, форели и крупного рогатого скота мясного направления) до бойни и розничных продавцов. Благодаря этому проекту мы сможем узнать уровень антимикробной резистентности в Европе, начиная от фермы и до стола.
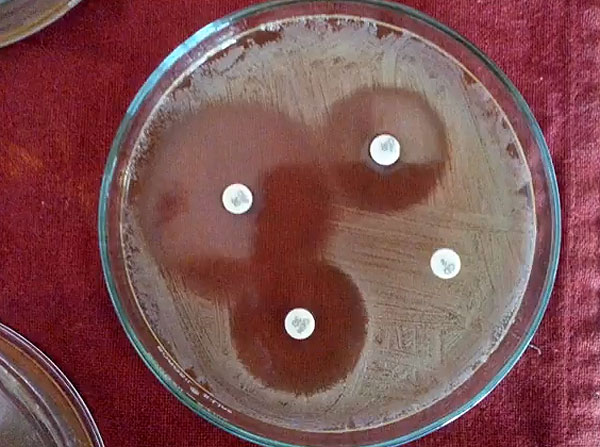
Классические методы для оценки антимикробной резистентности. Рисунок с левой стороны показывает Е-TEST для измерения минимальной концентрации антибиотика, который предотвращает бактериальный рост. Правая сторона показывает тест на определение чувствительности микроорганизмов к антимикробным препаратам с различными зонами подавления роста, вызванными действием антибиотиков.
Проблема резистентности микроорганизмов к антибиотикам (лекция)
SOVREMENNAYA PEDIATRIYA.2017.2(82):52-56; doi 10.15574/SP.2017.82.52
Цимбалиста О. Л.
ГВНУ «Ивано/Франковский национальный медицинский университет», Украина
Цель работы: расширить знания педиатров относительно формирования резистентности микрорганизмов к антибиотикам. В лекции представлены современные взгляды на факторы риска, причины и механизмы формирования первичной и вторичной резистентности микрорганизмов к антибиотикам. В основе развития последней являються мутации: изменения генетической эндогенной информации, которая передается с помощью хромосом, и появление экзогенной генетической информации (плазмиды и транспозоны). Обоснована роль многофункционального характера системы эфлюкса, которую контролируют хромосомные гены. Основными механизмами приобретенной резистентности возбудителей различных инфекций к антибиотикам являются нарушения проникаемости препарата внутрь возбудителя, синтез новых b-лактамаз и изменения экспрессии существующих, нарушения цитоплазматического транспорта антибиотиков к мишени, изменение структуры самой мишени или формированиеметаболического шунта. Обоснована роль формирования биопленки в развитии резистентности микроорганизмов к антибиотикам при использовании их в ветеринарии. С целью уменьшения развития антибиотикорезистентности микроорганизмов необходимо четко придерживаться показаний, дозировки, продолжительности лечения противомикробными препаратами; учитывать спектр микрофлоры и ее резистентность в данном лечебном учреждении; ограничить использование антибиотиков и найти альтернативу этим препаратам в ветеринарии.
В основе развития последней являються мутации: изменения генетической эндогенной информации, которая передается с помощью хромосом, и появление экзогенной генетической информации (плазмиды и транспозоны). Обоснована роль многофункционального характера системы эфлюкса, которую контролируют хромосомные гены. Основными механизмами приобретенной резистентности возбудителей различных инфекций к антибиотикам являются нарушения проникаемости препарата внутрь возбудителя, синтез новых b-лактамаз и изменения экспрессии существующих, нарушения цитоплазматического транспорта антибиотиков к мишени, изменение структуры самой мишени или формированиеметаболического шунта. Обоснована роль формирования биопленки в развитии резистентности микроорганизмов к антибиотикам при использовании их в ветеринарии. С целью уменьшения развития антибиотикорезистентности микроорганизмов необходимо четко придерживаться показаний, дозировки, продолжительности лечения противомикробными препаратами; учитывать спектр микрофлоры и ее резистентность в данном лечебном учреждении; ограничить использование антибиотиков и найти альтернативу этим препаратам в ветеринарии.
Ключевые слова: антибиотики, микрорганизмы, резистентность естесственная и приобретенная.
Литература:
1. Антибактериальная терапия: практическое руководство / под ред. Л. С. Страчунского, Ю. Б. Белоусова, С. Н. Козлова. — Москва : РЦ «Фармединфо», 2000. — 358 с.
2. Антибактеріальна та протигрибкова терапія в педіатрії: навчально-практичний посібник / за ред. В. В. Бережного. — Хмельницький, 2016. — 416 с.
3. Волосовец А. П. Современные взгляды на проблему антибиотикорезистентности и её преодоление в клинической педиатрии / А. П. Волосовец, С. П. Кривопустов, Е. И. Юлиш // Здоровье ребенка. — 2007. — № 6. — С. 62—70.
4. Волосовець О. П. Раціональна антибіотикотерапія респіраторних захворювань у дітей / О. П. Волосовець, Є. І. Юліш. — Тернопіль : Укрмедкнига, 2003. — 400 с.
5. Волянский Ю. Л. SOS в прямом и переносном смысле. Новая стратегия борьбы с развитием устойчивости к антибиотикам (обзор литературы) / Ю. Л. Волянский, Т. Ю. Колотова, И. Ю. Кучма // Журнал НАМН України. — 2013. — Т. 19, № 2. — С. 162—170.
Л. Волянский, Т. Ю. Колотова, И. Ю. Кучма // Журнал НАМН України. — 2013. — Т. 19, № 2. — С. 162—170.
6. Дьяченко А. Г. Устойчивость бактерий к антибиотикам и её эволюция / А. Г. Дьяченко // Клінічна імунол. Алергол. Інфектол. — 2012. — № 4. — С. 5—11.
7. Крючко Т. О. Шляхи подолання антибіотикорезистентності в педіатрії / Т. О. Крючко, О. Я. Ткаченко // Педіатрія, акушерство і гінекологія. — 2011. — № 1. — С. 48—51.
8. Майданник В. Г. Современные макролиды и их применение в клинической практике / В. Г. Майданник. — Киев : В.Б. «Аванпост-Прим», 2012. — 326 с.
9. Мальцев В. Что такое биопленка?/ С. В. Мальцев, Г. Ш. Мансурова // Medical Nature. — 2013. — № 1. — С. 86—89.
10. Механизмы изменения генома прокариот / Ю. Л. Волянский, Т. Ю. Колотова, И. Ю. Кучма [и др.] — Харьков : НТМТ, 2012. — 320 с.
11. Рациональная антимикробная терапия: руководство для практикуючих врачей : под ред. С. В. Яковлева. — Москва : Литтера, 2015. — 1040 с.
12. Таточенко В. К. Антибиотико- и химиотерапия инфекций у детей / В. К. Таточенко. — Москва : Континент-Преса, 2008. — 256 с.
13. Устойчивость микроорганизмов к антибиотикам: резистома и её объём, разнообразие и развитие / К. А. Виноградова, В. Г. Булгакова, В. Н. Полин, П. А. Кожевин // Антибиотики и химиотерапия. — 2013. — Т. 58, № 5—6. — С. 38—50.
14. Фещенко Ю. І. Антибіотикорезистентність мікроорганізмів. Стан та шляхи їх вирішення / Ю. І. Фещенко, М. І. Гуменюк, О. С. Денисов // Український хіміотерапевт. журн. — 2010. — № 1—2. — С. 4—8.
15. Характеристика и клиническое значение бета-лактамаз расширенного спектра / А. Г. Березин, О. М. Ромашов, С. В. Яковлев, С. В. Сидоренко // Антибиотики и химиотерапия. — 2003. — Т. 48, № 7. — С. 5—11.
16. Acceleration of cmergence of bacterial antibiotic resistance in connected microenoironments / Q. Zhang, G. Zambert, D. Ziae [et al.] // Science. — 2011. — № 333. — P. 1764—767. https://doi.org/10. 1126/science.1208747; PMid:21940899
1126/science.1208747; PMid:21940899
17. Beaber J. W. SOS responsepromotes porixontal clissemination of antibiotic resistance genes / J. W. Beaber, B. Hochhut, M. K. Waldor // Nature. — 2004. — Vol. 427. — P. 72—74. https://doi.org/10.1038/nature02241; PMid:14688795
18. Daccord A. Intergrating conjugative dements of the SXT/R 391 family trigger the excision and drive the mobilization of a new class of Vibrio genomic islands / A. Daccord, D. Ceccarelli, G. Burrus // Mol. Microbiol. — 2010. — № 78. — P. 576—588. https://doi.org/10.1111/j.1365-2958.2010.07364.x; PMid:20807202
19. Highthroughput screening for RecA inhibitor using a transcreener adenosine 5′-0-diphosphate assay / E. J. Reterson, W. P. Zanzen, D. Kireev, S. F Singleton // Assay Drug. Dev. Technol. — 2012. — № 10. — P. 260—268. https://doi.org/10.1089/adt.2011.0409; PMid:22192312 PMCid:PMC3374383
20. Infectious Diseases Socilty of America / American Thoracis Society consensus guidelines on the management of community-gepic acquired pneumonia in adults / Z. A. Mandell, R. G. Wenderink, A. Anzueto [et al.] // Clin. Infect. Dis. — 2007. — № 44. — P. 27—72. https://doi.org/10.1086/511159; PMid:17278083
A. Mandell, R. G. Wenderink, A. Anzueto [et al.] // Clin. Infect. Dis. — 2007. — № 44. — P. 27—72. https://doi.org/10.1086/511159; PMid:17278083
21. Novel Jnhibitors of E.Coli RecA ATPase Actioty / J. Z. Sexton, N. J. Wigle, Q. He [at al.] // Curr. Chem. Genomics. — 2010. — № 4. — P. 34—42. https://doi.org/10.2174/1875397301004010034; PMid:20648224 PMCid:PMC2905775
22. Zhu Z. Inhibition of competence development, horizontal gene transfer and vizulence in Strenfocjccuspneumoniae by a modified complence stimulation peptide / Z. Zhu, G. W. Zau // PLiS Pathog. — 2011. — № 7. — P. 100—122. https://doi.org/10.1371/journal.ppat.1002241; PMid:21909280 PMCid:PMC3164649
23. β-lactam antibiotics promote bacterial mutagenesis via an RpoS-mediated reduction in replication fidelity / A. Gutierrez. Z. Zaureti, S. Crussand [et al.] // Nat.Commun. — 2013. — № 4. — P. 1610—1623. https://doi.org/10.1038/ncomms2607; PMid:23511474 PMCid:PMC3615471
Устойчивость микробов к антибиотикам • Джеймс Трефил, энциклопедия «Двести законов мироздания»
Все мы слышали пугающие истории о микробах, нечувствительных к антибиотикам. И действительно, многим в процессе лечения приходилось заменять один антибиотик на другой из-за того, что первый оказался неэффективным. Такое появление лекарственной устойчивости у популяции микроорганизмов — не странная месть матери-природы человечеству, а закономерное следствие теории эволюции.
И действительно, многим в процессе лечения приходилось заменять один антибиотик на другой из-за того, что первый оказался неэффективным. Такое появление лекарственной устойчивости у популяции микроорганизмов — не странная месть матери-природы человечеству, а закономерное следствие теории эволюции.
Существование различий между членами популяции составляет один из основополагающих принципов эволюции. Сегодня известно, что эти различия заложены в генах. Более того, жизнь любого организма (будь то бактерия или человек) по существу представляет собой серию химических превращений молекул. Действие антибиотика состоит в том, что он служит ингибитором, то есть тормозит или подавляет какую-либо химическую реакцию, жизненно важную для микроба. Например, пенициллин блокирует молекулы, участвующие в строительстве новых клеточных оболочек бактерий. Действие пенициллина можно упрощенно сравнить с жевательной резинкой, наклеенной на ключ, которая будет препятствовать открыванию замка. (Пенициллин не оказывает влияния на человека или животных, потому что наружные оболочки наших клеток коренным образом отличаются от клеток бактерий. )
)
У определенной популяции бактерий возможны различия в форме молекул, на которые направлено действие антибиотиков. Одни молекулы оказываются более чувствительными к «наклеиванию» лекарства, другие — менее. Чисто случайно у небольшого количества бактерий молекулы окажутся такой формы, которая менее чувствительна к отрицательному влиянию какого-то антибиотика (например, пенициллина). При воздействии лекарства на данную популяцию это небольшое количество устойчивых бактерий уцелеет. Через много поколений натуральный отбор приведет к преобладанию бактерий, в геноме которых закодированы менее чувствительные к лекарству молекулы. В конце концов появится популяция микробов, полностью невосприимчивых к данному антибиотику.
Необходимо еще раз отметить, что этот эффект проявляется через много поколений. Ни одна отдельно взятая бактерия не может приобрести иммунитет — форма молекулы определяется генами и обычно не меняется в течение жизни организма.
В 1952 году американские генетики Джошуа и Эстер Ледерберг провели классический эксперимент по изучению устойчивости микробов к антибиотикам.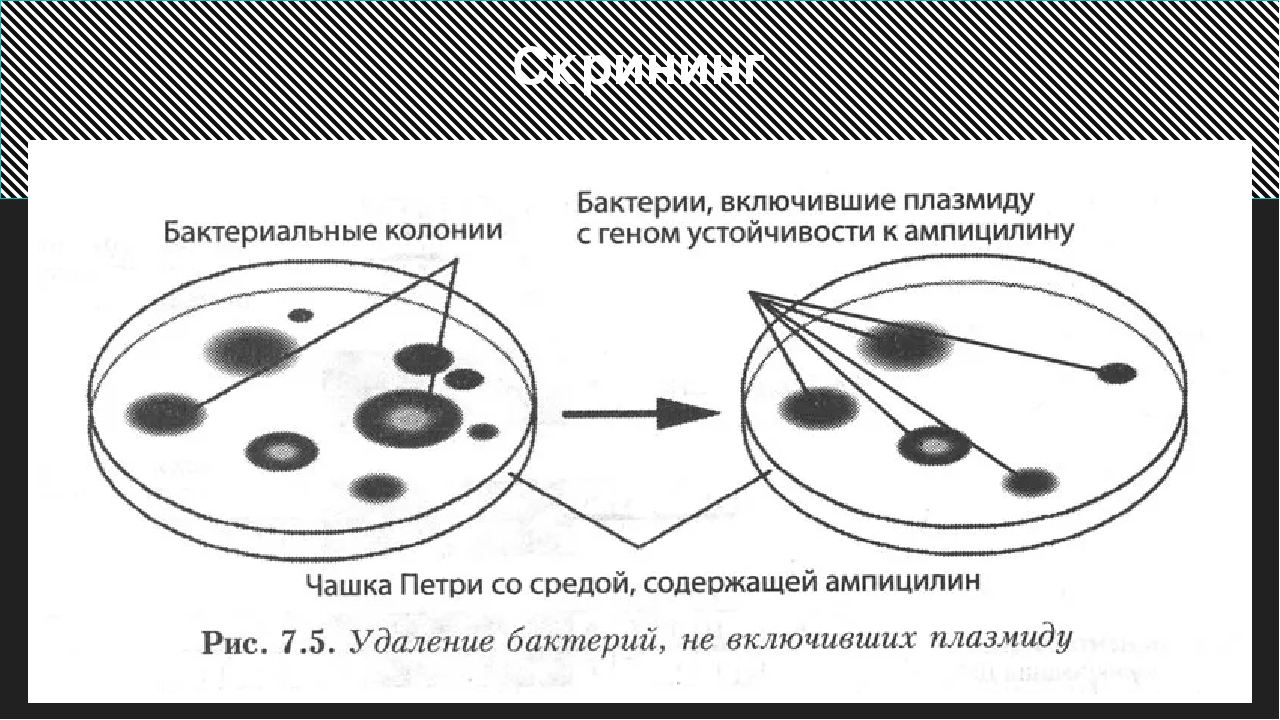 В чашках Петри на обычных питательных средах были выращены колонии бактерий, затем часть каждой колонии перенесли на другие чашки, где в питательную среду был добавлен пенициллин. Большинство колоний после этого пересева погибли, но одна из них выжила. Тогда ученые вновь вернулись к первичной колонии (от которой отсевали уцелевшую) и снова перенесли ее на питательную среду с пенициллином. Колония вновь выжила, доказав, что она обладает устойчивостью к пенициллину, хотя никогда не подвергалась его воздействию. Этот эксперимент подтвердил представление о случайном характере устойчивости в популяции и о том, что устойчивость обусловлена естественным отбором.
В чашках Петри на обычных питательных средах были выращены колонии бактерий, затем часть каждой колонии перенесли на другие чашки, где в питательную среду был добавлен пенициллин. Большинство колоний после этого пересева погибли, но одна из них выжила. Тогда ученые вновь вернулись к первичной колонии (от которой отсевали уцелевшую) и снова перенесли ее на питательную среду с пенициллином. Колония вновь выжила, доказав, что она обладает устойчивостью к пенициллину, хотя никогда не подвергалась его воздействию. Этот эксперимент подтвердил представление о случайном характере устойчивости в популяции и о том, что устойчивость обусловлена естественным отбором.
Подобные эффекты наблюдаются и у высших организмов: например, у насекомых в процессе эволюции выработалась устойчивость к пестицидам, а у растений — к гербицидам. Механизм приспособления здесь такой же, как и у бактерий, которые приобрели устойчивость к антибиотикам. Случайным образом у некоторых особей в популяции появляются какие-то химические изменения в их природе, что позволяет им противодействовать влиянию пестицидов или гербицидов. Например, это могут быть особые молекулы, которые захватывают молекулы пестицида или гербицида и не позволяют им действовать. Или у этих особей могут вырабатываться химические вещества, удаляющие пестициды или гербициды из клеток организма прежде, чем эти яды успеют сильно повредить клетки. В результате естественного отбора организмы с такими особенностями выживают в первую очередь, и в конце концов вся популяция приобретет эту полезную особенность.
Например, это могут быть особые молекулы, которые захватывают молекулы пестицида или гербицида и не позволяют им действовать. Или у этих особей могут вырабатываться химические вещества, удаляющие пестициды или гербициды из клеток организма прежде, чем эти яды успеют сильно повредить клетки. В результате естественного отбора организмы с такими особенностями выживают в первую очередь, и в конце концов вся популяция приобретет эту полезную особенность.
Зная о работах в области естественного отбора, ученые должны были бы ожидать такого поведения исследуемых организмов. Тот факт, что они этого не сделали, говорит нам скорее о несовершенстве человеческой природы, нежели о недостаточном эффекте антибиотиков и других химикатов. Однако эта приобретенная лекарственная устойчивость микробов вовсе не зачеркивает всего положительного, что принесли нам антибиотики и другие химические вещества. Это просто значит, что войну с болезнью нельзя выиграть в одной битве. Здесь можно провести аналогию с гонкой вооружений, в которой одна сторона добивается временного преимущества, а другая учится наносить ответный удар. Затем первая сторона разрабатывает контрудар на этот ответный удар, а другая сторона — противостоит контр-контрудару… Гонка вооружений никогда не кончается — так же, я подозреваю, никогда не закончится и наша битва с эволюционным потенциалом микробов. Главное — быть далеко впереди, чтобы держать болезни под контролем. И этого будет достаточно для победы.
Затем первая сторона разрабатывает контрудар на этот ответный удар, а другая сторона — противостоит контр-контрудару… Гонка вооружений никогда не кончается — так же, я подозреваю, никогда не закончится и наша битва с эволюционным потенциалом микробов. Главное — быть далеко впереди, чтобы держать болезни под контролем. И этого будет достаточно для победы.
Мурашко назвал устойчивость бактерий к антибиотикам фактором биологической угрозы
ФОТО: ROSZDRAVNADZOR.RU
Министр здравоохранения Михаил Мурашко в ходе интерактивного диалога высокого уровня Генассамблеи ООН по вопросам устойчивости к противомикробным препаратам заявил, что антимикробная резистентность в России на законодательном уровне рассматривается как фактор биологической угрозы. По его словам, большой вклад в ухудшение ситуации внесла пандемия коронавируса.
Глава ведомства отметил, что во всем мире последние два года стали периодом проверки на прочность мер, применяемых в борьбе с устойчивостью к противомикробным препаратам. «Широкое применение, а подчас и нецелевой прием антибиотиков и противовирусных препаратов во время пандемии оказал свое влияние на ситуацию. Всем нам теперь придется говорить и об устойчивости к противомикробным препаратам, и, возможно, к противовирусным в связи с „ускользанием“ штаммов от некоторых препаратов», — цитирует ТАСС его слова.
«Широкое применение, а подчас и нецелевой прием антибиотиков и противовирусных препаратов во время пандемии оказал свое влияние на ситуацию. Всем нам теперь придется говорить и об устойчивости к противомикробным препаратам, и, возможно, к противовирусным в связи с „ускользанием“ штаммов от некоторых препаратов», — цитирует ТАСС его слова.
По его словам, сегодня мировое сообщество объединяет усилия, направленные на противодействие распространения антимикробной резистентности, в том числе Россия.
«В РФ на законодательном уровне антимикробная резистентность рассматривается как фактор биологической угрозы», — сказал Мурашко.
«В настоящее время государственная политика России направлена на поддержку исследований и разработку новых противомикробных и альтернативных препаратов, которые в будущем станут полноценной заменой антибиотикам. Пандемия COVID-19 ускорила разработку средств лечения и профилактики инфекционных заболеваний. И вакцина от коронавируса стала одним из таких средств», — отметил глава Минздрава.
И вакцина от коронавируса стала одним из таких средств», — отметил глава Минздрава.
Мурашко допустил, что в дальнейшем именно вакцины станут одним из основных средств против антимикробной резистентности. Доступность вакцинации и широкая иммунизация населения от инфекционных заболеваний позволят ограничить необходимость применения антибиотиков, противовирусных и ряда других лекарств, полагает он.
Бактерии, устойчивые к антибиотикам — Better Health Channel
Антибиотики используются для уничтожения бактерий, которые могут вызывать болезни. Они внесли большой вклад в здоровье человека. Многие болезни, которые когда-то убивали людей, теперь можно эффективно лечить с помощью антибиотиков. Однако некоторые бактерии стали устойчивыми к обычно используемым антибиотикам.
Бактерии, устойчивые к антибиотикам, — это бактерии, которые не контролируются или не уничтожаются антибиотиками. Они способны выживать и даже размножаться в присутствии антибиотика. Большинство бактерий, вызывающих инфекцию, могут стать устойчивыми, по крайней мере, к некоторым антибиотикам. Бактерии, устойчивые ко многим антибиотикам, известны как организмы с множественной устойчивостью (MRO).
Большинство бактерий, вызывающих инфекцию, могут стать устойчивыми, по крайней мере, к некоторым антибиотикам. Бактерии, устойчивые ко многим антибиотикам, известны как организмы с множественной устойчивостью (MRO).
Устойчивость к антибиотикам — серьезная проблема общественного здравоохранения. Это можно предотвратить, сведя к минимуму ненужное назначение и чрезмерное назначение антибиотиков, правильное использование назначенных антибиотиков, а также хорошую гигиену и инфекционный контроль.
Некоторые бактерии обладают естественной устойчивостью к некоторым антибиотикам. Например, бензилпенициллин очень мало влияет на большинство организмов, обнаруженных в пищеварительной системе (кишечнике) человека.
Бактерии, устойчивые к антибиотикам
У некоторых бактерий выработалась устойчивость к антибиотикам, которые когда-то обычно использовались для их лечения. Например, золотистый стафилококк («золотой стафилококк» или MRSA) и Neisseria gonorrhoeae (причина гонореи) теперь почти всегда устойчивы к бензилпенициллину. В прошлом эти инфекции обычно контролировались пенициллином.
В прошлом эти инфекции обычно контролировались пенициллином.
Самая серьезная проблема, связанная с устойчивостью к антибиотикам, заключается в том, что некоторые бактерии стали устойчивыми почти ко всем легкодоступным антибиотикам.Эти бактерии могут вызывать серьезные заболевания, и это серьезная проблема общественного здравоохранения. Важными примерами являются:
- метициллин-устойчивый золотистый стафилококк (MRSA)
- ванкомицин-устойчивый энтерококк (VRE)
- микобактерии туберкулеза с множественной лекарственной устойчивостью (МЛУ-ТБ)
- устойчивые к карбапенемам бактерии Enterobacteriaceae (CRE) g
Способы предотвращения устойчивости к антибиотикам
Наиболее важными способами предотвращения устойчивости к антибиотикам являются:
- Сведение к минимуму ненужных и чрезмерных назначений антибиотиков.Это происходит, когда люди ожидают, что врачи пропишут антибиотики при вирусном заболевании (антибиотики не действуют против вирусов) или когда антибиотики прописаны при состояниях, для которых они не требуются.

- Завершите полный курс любого прописанного антибиотика, чтобы он был полностью эффективным и не приводил к возникновению резистентности.
- Соблюдайте правила гигиены, такие как мытье рук, и используйте соответствующие процедуры инфекционного контроля.
Передача устойчивых к антибиотикам бактерий в больницах
Распространенные способы передачи бактерий от человека к человеку включают:
- контакт с зараженными руками персонала больницы
- контакт с загрязненными поверхностями, такими как дверные ручки, чрезмерное проникновение прикроватные столики и звонки
- контакт с зараженным оборудованием, таким как стетоскопы и манжеты для измерения кровяного давления.
Инфекционный контроль в больницах
Стандартные меры предосторожности в больницах — это методы работы, которые обеспечивают базовый уровень инфекционного контроля для оказания помощи всем людям, независимо от их диагноза или предполагаемого инфекционного статуса.
Эти меры предосторожности должны соблюдаться во всех больницах и медицинских учреждениях и включают:
- соблюдение правил личной гигиены, например мытье рук до и после контакта с пациентом и надлежащее использование спиртовых растворов для протирания рук такие как перчатки, халаты, маски и очки.
- надлежащее обращение с острыми предметами (например, иглами) и клиническими отходами (отходы, образующиеся во время ухода за пациентами) и их утилизация.
Применение стандартных мер предосторожности сводит к минимуму риск передачи инфекции от человека к человеку даже в ситуациях повышенного риска.
Дополнительные меры предосторожности при обращении с устойчивыми к антибиотикам бактериями
Дополнительные меры предосторожности используются при уходе за людьми, о которых известно или предполагается, что они инфицированы или колонизированы высокоинфекционными патогенами (микроорганизмами, вызывающими заболевания).
Микроорганизмы могут быть классифицированы как «высокорисковые», если:
- путь их передачи делает их более заразными — они могут передаваться через контакт или воздушно-капельным путем
- они вызываются бактериями, устойчивыми к антибиотикам
- они устойчивы к стандартным процедурам стерилизации.

Дополнительные меры предосторожности адаптированы к конкретному патогену и пути передачи. Дополнительные меры предосторожности могут включать:
- использование отдельной комнаты с ванными комнатами или специального туалета
- специальное оборудование для ухода за этим человеком
- ограничение передвижения человека и его медицинских работников.
Бактерии, устойчивые к антибиотикам, также могут передаваться от человека к человеку внутри сообщества. Это становится все более распространенным явлением.
Способы предотвращения передачи микроорганизмов, в том числе устойчивых к антибиотикам бактерий, включают:
- Мыть руки до и после обработки пищи, посещения туалета и смены подгузников.
- Прикрывайте нос и рот при кашле и чихании.
- Используйте салфетки, чтобы высморкаться или вытереть нос.
- Утилизируйте салфетки надлежащим образом — в мусор или в туалет.
- Не плевать.
- Оставайтесь дома, если вы нездоровы и не можете справиться с повседневными обязанностями.
- Не отдавать детей в детский сад, в детский сад или школу, если они нездоровы.
- Если вам прописали антибиотики, пройдите весь курс — не прекращайте, потому что вы чувствуете себя лучше.
- Если вы продолжаете чувствовать себя плохо, вернитесь к врачу.
- Избегайте использования продуктов, в которых рекламируется, что они содержат антибиотики, являются антибактериальными или противомикробными, если это не рекомендовано вашим лечащим врачом.
Куда обратиться за помощью
- Ваш врач
- Фармацевт
- Общественный центр здоровья
Бактерии, устойчивые к антибиотикам — канал лучшего здоровья
Антибиотики используются для уничтожения бактерий, которые могут вызывать болезни.Они внесли большой вклад в здоровье человека. Многие болезни, которые когда-то убивали людей, теперь можно эффективно лечить с помощью антибиотиков. Однако некоторые бактерии стали устойчивыми к обычно используемым антибиотикам.
Бактерии, устойчивые к антибиотикам, — это бактерии, которые не контролируются или не уничтожаются антибиотиками. Они способны выживать и даже размножаться в присутствии антибиотика. Большинство бактерий, вызывающих инфекцию, могут стать устойчивыми, по крайней мере, к некоторым антибиотикам. Бактерии, устойчивые ко многим антибиотикам, известны как организмы с множественной устойчивостью (MRO).
Устойчивость к антибиотикам — серьезная проблема общественного здравоохранения. Это можно предотвратить, сведя к минимуму ненужное назначение и чрезмерное назначение антибиотиков, правильное использование назначенных антибиотиков, а также хорошую гигиену и инфекционный контроль.
Некоторые бактерии обладают естественной устойчивостью к некоторым антибиотикам. Например, бензилпенициллин очень мало влияет на большинство организмов, обнаруженных в пищеварительной системе (кишечнике) человека.
Бактерии, устойчивые к антибиотикам
У некоторых бактерий выработалась устойчивость к антибиотикам, которые когда-то обычно использовались для их лечения. Например, золотистый стафилококк («золотой стафилококк» или MRSA) и Neisseria gonorrhoeae (причина гонореи) теперь почти всегда устойчивы к бензилпенициллину. В прошлом эти инфекции обычно контролировались пенициллином.
Например, золотистый стафилококк («золотой стафилококк» или MRSA) и Neisseria gonorrhoeae (причина гонореи) теперь почти всегда устойчивы к бензилпенициллину. В прошлом эти инфекции обычно контролировались пенициллином.
Самая серьезная проблема, связанная с устойчивостью к антибиотикам, заключается в том, что некоторые бактерии стали устойчивыми почти ко всем легкодоступным антибиотикам. Эти бактерии могут вызывать серьезные заболевания, и это серьезная проблема общественного здравоохранения. Важными примерами являются:
- метициллин-устойчивый золотистый стафилококк (MRSA)
- ванкомицин-устойчивый энтерококк (VRE)
- микобактерии туберкулеза с множественной лекарственной устойчивостью (МЛУ-ТБ)
- устойчивые к карбапенемам бактерии Enterobacteriaceae (CRE) g
Способы предотвращения устойчивости к антибиотикам
Наиболее важными способами предотвращения устойчивости к антибиотикам являются:
- Сведение к минимуму ненужных и чрезмерных назначений антибиотиков.
 Это происходит, когда люди ожидают, что врачи пропишут антибиотики при вирусном заболевании (антибиотики не действуют против вирусов) или когда антибиотики прописаны при состояниях, для которых они не требуются.
Это происходит, когда люди ожидают, что врачи пропишут антибиотики при вирусном заболевании (антибиотики не действуют против вирусов) или когда антибиотики прописаны при состояниях, для которых они не требуются. - Завершите полный курс любого прописанного антибиотика, чтобы он был полностью эффективным и не приводил к возникновению резистентности.
- Соблюдайте правила гигиены, такие как мытье рук, и используйте соответствующие процедуры инфекционного контроля.
Передача устойчивых к антибиотикам бактерий в больницах
Распространенные способы передачи бактерий от человека к человеку включают:
- контакт с зараженными руками персонала больницы
- контакт с загрязненными поверхностями, такими как дверные ручки, чрезмерное проникновение прикроватные столики и звонки
- контакт с зараженным оборудованием, таким как стетоскопы и манжеты для измерения кровяного давления.
Инфекционный контроль в больницах
Стандартные меры предосторожности в больницах — это методы работы, которые обеспечивают базовый уровень инфекционного контроля для оказания помощи всем людям, независимо от их диагноза или предполагаемого инфекционного статуса.
Эти меры предосторожности должны соблюдаться во всех больницах и медицинских учреждениях и включают:
- соблюдение правил личной гигиены, например мытье рук до и после контакта с пациентом и надлежащее использование спиртовых растворов для протирания рук такие как перчатки, халаты, маски и очки.
- надлежащее обращение с острыми предметами (например, иглами) и клиническими отходами (отходы, образующиеся во время ухода за пациентами) и их утилизация.
Применение стандартных мер предосторожности сводит к минимуму риск передачи инфекции от человека к человеку даже в ситуациях повышенного риска.
Дополнительные меры предосторожности при обращении с устойчивыми к антибиотикам бактериями
Дополнительные меры предосторожности используются при уходе за людьми, о которых известно или предполагается, что они инфицированы или колонизированы высокоинфекционными патогенами (микроорганизмами, вызывающими заболевания).
Микроорганизмы могут быть классифицированы как «высокорисковые», если:
- путь их передачи делает их более заразными — они могут передаваться через контакт или воздушно-капельным путем
- они вызываются бактериями, устойчивыми к антибиотикам
- они устойчивы к стандартным процедурам стерилизации.
Дополнительные меры предосторожности адаптированы к конкретному патогену и пути передачи. Дополнительные меры предосторожности могут включать:
- использование отдельной комнаты с ванными комнатами или специального туалета
- специальное оборудование для ухода за этим человеком
- ограничение передвижения человека и его медицинских работников.
Бактерии, устойчивые к антибиотикам, также могут передаваться от человека к человеку внутри сообщества. Это становится все более распространенным явлением.
Способы предотвращения передачи микроорганизмов, в том числе устойчивых к антибиотикам бактерий, включают:
- Мыть руки до и после обработки пищи, посещения туалета и смены подгузников.
- Прикрывайте нос и рот при кашле и чихании.
- Используйте салфетки, чтобы высморкаться или вытереть нос.
- Утилизируйте салфетки надлежащим образом — в мусор или в туалет.
- Не плевать.
- Оставайтесь дома, если вы нездоровы и не можете справиться с повседневными обязанностями.
- Не отдавать детей в детский сад, в детский сад или школу, если они нездоровы.
- Если вам прописали антибиотики, пройдите весь курс — не прекращайте, потому что вы чувствуете себя лучше.
- Если вы продолжаете чувствовать себя плохо, вернитесь к врачу.
- Избегайте использования продуктов, в которых рекламируется, что они содержат антибиотики, являются антибактериальными или противомикробными, если это не рекомендовано вашим лечащим врачом.
Куда обратиться за помощью
- Ваш врач
- Фармацевт
- Общественный поликлиник
Устойчивость бактерий к антибиотикам | Лабораторные тесты онлайн
Устойчивость к антибиотикам.ReAct. Доступно в Интернете по адресу https://www.group.org/toolbox/understand/antibiotic-resistance/health-care-associated-infections-and-resistance/. По состоянию на 30 мая 2018 г.
(редакция апрель 2011 г.). Факты об устойчивости к антибиотикам. Общество инфекционных болезней Америки. Доступно в Интернете по адресу http://www.idsociety.org/AR_Facts/. По состоянию на 30 мая 2018 г.
(2013). Угрозы устойчивости к антибиотикам в Соединенных Штатах, 2013. Центры по контролю и профилактике заболеваний. Доступно в Интернете по адресу https: // www.cdc.gov/drugresistance/threat-report-2013/. По состоянию на 30 мая 2018 г.
(© 2014). Общие сведения: об устойчивости к антибиотикам. Альянс за разумное использование антибиотиков. Доступно в Интернете по адресу http://emerald.tufts.edu/med/apua/about_issue/about_antibioticres.shtml. По состоянию на 30 мая 2018 г.
(февраль 2014 г.). Остановите распространение супербактерий. Новости NIH в области здравоохранения. Доступно в Интернете по адресу https://newsinhealth.nih.gov/2014/02/stop-spread-superbugs. По состоянию на 30 мая 2018 г.
Вентола, Л.С. (2015 апрель). Кризис устойчивости к антибиотикам, часть 1: причины и угрозы. Аптека и терапия . Доступно в Интернете по адресу https://www.ncbi.nlm.nih.gov/pm c / article / PMC4378521 /. По состоянию на 30 мая 2018 г.
Вентола, Л.С. (май 2015 г.). Кризис устойчивости к антибиотикам: Часть 2: Стратегии управления и новые агенты. Аптека и терапия . Доступно на сайте https://www.ncbi.nlm.nih.gov/pubmed/25987823. По состоянию на 30 мая 2018 г.
(обновлено 3 марта 2016 г.).Повышение безопасности здравоохранения. Центры по контролю и профилактике заболеваний. Доступно в Интернете по адресу https://www.cdc.gov/vitalsigns/protect-patients/index.html. По состоянию на 30 мая 2018 г.
Deak, D. et al. (6 сентября 2016 г.). Прогресс в борьбе с бактериями с множественной лекарственной устойчивостью? Обзор антибиотиков, одобренных Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США, 2010–2015 гг. Анналы внутренней медицины. Доступно на сайте http://annals.org/aim/article-abstract/2526197/progress-fight-against-multidrug-resistant-bacteria-review-u-s-food.По состоянию на 30 мая 2018 г.
Martens and Demain. (2017). Кризис устойчивости к антибиотикам, с особым вниманием к США Журнал антибиотиков . Доступно на сайте https://www.nature.com/articles/ja201730. По состоянию на 30 мая 2018 г.
(8 марта 2017 г.). Устойчивость к антибиотикам / противомикробным препаратам, роль CDC. Центры по контролю и профилактике заболеваний. Доступно в Интернете по адресу https://www.cdc.gov/drugresistance/cdc_role.html. По состоянию на 30 мая 2018 г.
(обновлено 10 апреля 2017 г.).Национальная стратегия борьбы с устойчивостью к антибиотикам. Центры по контролю и профилактике заболеваний. Доступно в Интернете по адресу https://www.cdc.gov/drugresistance/federal-engagement-in-ar/national-strategy/index.html. По состоянию на 30 мая 2018 г.
(обновлено 15 сентября 2017 г.). Устойчивость к антибиотикам в домах престарелых и детских садах. Центры по контролю и профилактике заболеваний. Доступно в Интернете по адресу https://www.cdc.gov/healthcommunication/toolstemplates/entertainmented/tips/AntibioticResistance.html. По состоянию на 30 мая 2018 г.
(обновлено 22 декабря 2017 г.). Устойчивость к антибиотикам от фермы к столу. Центры по контролю и профилактике заболеваний. Доступно в Интернете по адресу https://www.cdc.gov/foodsafety/challenges/from-farm-to-table.html
(© 2018). Что такое антибиотики и как они действуют? Общество микробиологов. Доступно в Интернете по адресу https://microbiologysociety.org/education-outreach/antibiotics-unearthed/antibiotics-and-antibiotic-resistance/what-are-antibiotics-and-how-do-they-work.html. По состоянию на 30 мая 2018 г.
(© 2018). Различные типы антибиотиков и их применение. Omics International. Доступно в Интернете по адресу https://www.omicsonline.org/conferences-list/different-types-of-antibiotics-and-their-applications. По состоянию на 30 мая 2018 г.
Rifai, N. et al. (© 2018). Учебник Тиц по клинической химии и молекулярной диагностике, шестое издание. Устойчивость к противомикробным препаратам и рекомендации по тестированию основных бактериальных патогенов, стр. 173700014 — 173700024. Доступно на сайте https: // expertconsult.inkling.com/read/rifai-tietz-textbook-clinical-chemistry-molecular-diagnost-6e/chapter-75/antimicrobial-resistance-and. По состоянию на 30 мая 2018 г.
(© 2018). Профилактика инфекций, устойчивых к антибиотикам. NYU Langone Health. Доступно в Интернете по адресу https://nyulangone.org/conditions/antibiotic-resistant-infections/prevention. По состоянию на 30 мая 2018 г.
(обновлено 8 января 2018 г.). Борьба с устойчивостью к антибиотикам. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Доступно на сайте https://www.fda.gov/ForConsumers/ConsumerUpdates/ucm092810.htm. По состоянию на 30 мая 2018 г.
(обновлено 31 января 2018 г.). Действия США по борьбе с AR. Центры по контролю и профилактике заболеваний. Доступно в Интернете по адресу https://www.cdc.gov/drugresistance/us-activities.html. По состоянию на 30 мая 2018 г.
(5 февраля 2018 г.). Устойчивость к антибиотикам. Всемирная организация здоровья. Доступно в Интернете по адресу http://www.who.int/mediacentre/factsheets/antibiotic-resistance/en/. По состоянию на 30 мая 2018 г.
(23 февраля 2018 г.). Устойчивые к карбапенемам Enterobacteriaceae в медицинских учреждениях.Центры по контролю и профилактике заболеваний. Доступно в Интернете по адресу https://www.cdc.gov/hai/organisms/cre/index.html. По состоянию на 30 мая 2018 г.
(5 марта 2018 г.). Об устойчивости к противомикробным препаратам. Центры по контролю и профилактике заболеваний. Доступно в Интернете по адресу https://www.cdc.gov/drugresistance/about.html. По состоянию на 30 мая 2018 г.
(обновлено 30 марта 2018 г.). Сеть лабораторий по устойчивости к антибиотикам (AR). Центры по контролю и профилактике заболеваний. Доступно в Интернете по адресу https://www.cdc.gov/drugresistance/solutions-initiative/ar-lab-networks.html. По состоянию на 30 мая 2018 г.
(обновлено 3 апреля 2018 г.). Сдерживая необычное сопротивление. Центры по контролю и профилактике заболеваний. Доступно в Интернете по адресу https://www.cdc.gov/vitalsigns/contain-unusual-resistance/index.html. По состоянию на 30 мая 2018 г.
(обновлено 6 апреля 2018 г.). Гонорея, устойчивая к антибиотикам. Центры по контролю и профилактике заболеваний. Доступно в Интернете по адресу https://www.cdc.gov/std/gonorrhea/arg/default.htm. По состоянию на 30 мая 2018 г.
(обновлено 25 апреля 2018 г.).Устойчивость к антибиотикам. MedlinePlus. Доступно в Интернете по адресу https://medlineplus.gov/antibioticresistance.html. По состоянию на 30 мая 2018 г.
(обновлено 11 мая 2018 г.). О лабораторных испытаниях и ресурсах AR. Центры по контролю и профилактике заболеваний. Доступно в Интернете по адресу https://www.cdc.gov/drugresistance/laboratories.html. По состоянию на 30 мая 2018 г.
(обновлено 25 мая 2018 г.). Защита пациентов и предотвращение вспышек заболеваний. Центры по контролю и профилактике заболеваний. Доступно в Интернете по адресу https: // www.cdc.gov/drugresistance/protecting_patients.html. По состоянию на 30 мая 2018 г.
Устойчивость к антибиотикам
Проблема устойчивости к антибиотикам является активной областью исследований в отделении. Некоторые ученые исследуют детали и механизмы того, как бактерии приобретают устойчивость к различным группам антибиотиков. Другие ищут новые способы борьбы с инфекциями, которые сопротивляются доступным антибиотикам. Одна из этих групп использует бактериофаги, в то время как другая группа работает над разработкой пробиотического коктейля, который можно было бы использовать для лечения лекарственно-устойчивых заболеваний.
Устойчивость к фторхинолоновым антибиотикам
Доктор Линн Зехидрих изучает проблему устойчивости к антибиотикам более 25 лет. Одно из исследований в ее лаборатории было направлено на понимание механизма действия и механизмов устойчивости к антибиотикам, известным как фторхинолоны, одним из самых мощных, широко назначаемых антибиотиков широкого спектра действия, используемых во всем мире. Класс фторхинолоновых антибиотиков включает, среди прочего, ципрофлоксацин и левофлоксацин.
Фторхинолоны действуют, воздействуя на два основных бактериальных фермента, известных как топоизомеразы, гиразу и топоизомеразу IV, которые помогают контролировать наматывание и раскручивание цепей ДНК во время важных клеточных процессов, таких как репликация ДНК, рекомбинация, транскрипция и сегрегация хромосом. Во время этих клеточных процессов цепи ДНК временно разрушаются топоизомеразами. Промежуточная форма разрушенной ДНК обычно недолговечна, но в присутствии фторхинолоновых антибиотиков промежуточная форма стабилизируется, что приводит к гибели бактериальных клеток.Лаборатория Цехидриха использует биохимические, биофизические и генетические подходы для определения того, как топоизомеразы выполняют свои клеточные роли и как лекарства блокируют их функцию.
В другом направлении исследований д-р Зехидрих и его коллеги изучают, можно ли повторно использовать препарат циклопирокс, противогрибковое средство, на которое не выдан патент, в качестве кандидата для использования в качестве антибиотика, особенно против грамотрицательных бактерий с множественной лекарственной устойчивостью. Возможность использовать лекарство, предназначенное для борьбы с одним типом микроорганизмов, для использования против другого, может обойтись без времени и денег, связанных с разработкой нового лекарства.
Группа Zechiedrich сообщила, что циклопирокс подавлял рост даже грамотрицательных бактерий с множественной лекарственной устойчивостью Acinetobacter baumannii , Escherichia coli и Klebsiella pneumoniae . Далее они исследовали механизм действия и обнаружили, что препарат влияет на метаболизм сахара в бактериях, изменяя состав молекул на внешней мембране бактериальной клетки. В своих текущих исследованиях в этой области они рассматривают лекарственную мишень как потенциально новую мишень для разработки новых антибиотиков.
Устойчивость к бета-лактамным антибиотикам
Бета-лактамные антибиотики — наиболее широко используемый класс препаратов для лечения бактериальных инфекций. Они включают пенициллин и его производные, такие как метициллин и амоксициллин, а также другие группы антибиотиков, известные как цефалоспорины, карбапенемы и монобактамы. Часть бета-лактамного кольца антибиотика нацелена на пенициллин-связывающие белки (PBP), обнаруженные в мембране бактериальной клетки, которые участвуют в синтезе клеточной стенки.Связывание антибиотика с PBP предотвращает выполнение PBP своей основной роли и приводит к гибели бактериальной клетки.
Доктор Тимоти Палцкилл, профессор фармакологии, химической биологии, молекулярной вирусологии и микробиологии, и его исследовательская группа изучали механизмы устойчивости к бета-лактамным антибиотикам. У грамотрицательных бактерий наиболее распространенным механизмом устойчивости является гидролиз или разрушение антибиотиков ферментами, называемыми бета-лактамазами.Существует два широких класса бета-лактамаз: серин-бета-лактамазы и металло-бета-лактамазы. Доктор Палцкилл и его группа используют множество передовых генетических, биохимических и физических методов, чтобы понять детали структуры и функции обеих групп бета-лактамаз и их взаимодействия с лекарственно-устойчивыми формами антибиотиков, которые подвержены лекарственной устойчивости. .
Вместо лекарственной устойчивости за счет действия бета-лактамаз грамположительные бактерии приобретают устойчивость к бета-лактамным антибиотикам за счет выработки белка под названием PBP2a, который позволяет избежать ингибирующего действия антибиотиков.Это механизм, благодаря которому устойчивый к метициллину Staphylococcus aureus (MRSA) может сохраняться, несмотря на лечение несколькими бета-лактамными антибиотиками. Доктор Палцкилл и его коллеги провели исследование, в котором они обнаружили, что белок BLIP-II способен слабо связывать и ингибировать PBP2a, что делает его чувствительным к бета-лактамным антибиотикам. Они продолжают это направление исследований, ища мутации, которые увеличивают сродство BLIP-II к PBP2a.
Устойчивость к колистину
Сокращение вариантов лечения из-за увеличения распространенности бета-лактамаз, расщепляющих бета-лактамные антибиотики, привело к увеличению использования полимиксиновых антибиотиков, таких как колистин.Полимиксины — это полипептиды, которые действуют путем связывания с бактериальной мембраной и последующего ее разрушения. Недавнее появление и распространение кодируемого плазмидой переносимого гена устойчивости к колистину, mcr-1, вызывает озабоченность. Ген mcr-1 кодирует фермент MCR-1, который модифицирует компонент мембраны и блокирует связывание колистина.
Доктор Палцкилл и его группа определили рентгеновскую структуру одной важной функциональной области белка MCR-1. Чтобы более полно понять механизм MCR-1, они работают над определением структуры полноразмерного фермента MCR-1.Кроме того, лаборатория работает над обнаружением ингибиторов фермента MCR-1, которые позволили бы обойти устойчивость и расширить возможности лечения колистина.
Использование бактериофагов для борьбы с устойчивыми к антибиотикам бактериями
Бактериофаги — это вирусы, которые специфически убивают бактерии. Доктора Энтони Марессо, Фрэнк Рамиг, Барбара Траутнер и их коллеги изучали возможность использования бактериофагов или фагов для борьбы с устойчивыми к лекарствам бактериями.Эта идея была первоначально предложена Феликсом д’Эреллем в 1926 году, но после открытия и первых успехов антибиотиков от этого подхода в значительной степени отказались (хотя несколько стран Восточной Европы использовали этот подход для успешного лечения некоторых бактериальных инфекций).
Учитывая текущие ограничения в лечении устойчивых к лекарствам бактериальных инфекций, исследователи пересмотрели эту идею и приступили к определению, могут ли фаги быть эффективными при уничтожении большой группы бактерий, устойчивых к антибиотикам.Их бактериальной мишенью была специфическая группа Escherichia coli, , называемая ST131, которая колонизирует желудочно-кишечный тракт, но может инфицировать участки вне кишечника (эта категория E. coli известна как внекишечная патогенная E. coli ), и считается основной причиной всех устойчивых к антибиотикам инфекций E. coli в США. Бактерии обладают множественной лекарственной устойчивостью, а также продуцируют смертельные факторы вирулентности; неспособность контролировать их рост может привести к сепсису, который может быть фатальным.
В своем исследовании они стремились идентифицировать фаги, которые убивали бы 12 штаммов устойчивых к антибиотикам бактерий, выделенных от пациентов. Они сделали это, сначала выделив фаги из фекалий птиц и собак, которые, как известно, являются резервуарами бактерий E. coli ST131 , а затем проверили, лизируют ли фаги или убивают бактерии в лабораторных условиях. . Хотя ни один фаг не мог убить все 12 штаммов бактерий в лабораторных культурах, они обнаружили комбинации двух или трех фагов, которые были эффективны против всех протестированных бактерий.
Затем они проверили фаги, чтобы выяснить, могут ли они также убить устойчивые к антибиотикам бактерии на мышиной модели сепсиса. При попадании в организм животных фаги снижали уровень бактерий и существенно улучшали здоровье мышей. Результаты продемонстрировали, что фаги, выделенные из окружающей среды, с небольшими экспериментальными манипуляциями, могут быть эффективными в борьбе даже с очень серьезными инфекциями супербактерий E. coli .
Использование фагов вместо антибиотиков для борьбы с бактериальными инфекциями дает несколько преимуществ.Фаги не заражают клетки человека. Они очень специфичны для определенных видов или штаммов бактерий, поэтому их можно использовать для борьбы с «плохими» бактериями, не нанося вреда «хорошей» кишечной микробиоте. Тем не менее, при желании их можно заставить действовать широко через коктейли. Кроме того, фаги могут развиваться, поэтому в случае развития устойчивости к набору фагов новые фаги могут быть идентифицированы в окружающей среде или развиваться в лаборатории за считанные дни, в отличие от антибиотиков, разработка которых может занять много лет и при больших затратах. .Хотя ученые все еще несколько осторожны в отношении этого подхода, поскольку иногда иммунная система хозяина может нейтрализовать активность фагов, а некоторые фаги могут плохо работать у животных, они продолжают исследовать этот вариант.
В другом исследовании эти исследователи обнаружили, что определенные металлы усиливают уничтожение бактерий E. coli ST131 фагами в крови. Они заметили, что при обработке фагом E. coli ST131 фаг эффективно убивал бактерии в культуральной среде, но не в крови.Образцы крови содержали химическое вещество, называемое ЭДТА, которое использовалось для предотвращения свертывания крови и, как известно, связывается с металлами. Они увидели более эффективное уничтожение бактерий в крови, обработанной гепарином, естественным фактором, препятствующим свертыванию, что предполагает, что разные результаты могут быть связаны с уровнем металлов в крови.
Когда они добавили металлы, кальций, магний и железо, которые обычно присутствуют в крови, они обнаружили, что ингибирование уничтожения ST131 с помощью ЭДТА было преодолено добавлением металлов.Более того, усиленный металлами киллинг наблюдали для нескольких других штаммов внекишечного патогенного E. coli , а не только для ST131. Металлы также улучшили уничтожение ST131 в модельной системе мыши. Эта работа указывает на важную роль металлов в уничтожении бактерий фагами в крови.
Лечение антибиотиками изменяет микробиоту кишечника, что приводит к возникновению трудноизлечимых Clostridium difficile инфекций
Clostridium difficile — это грамположительная спорообразующая бактерия, которая по классификации CDC считается одной из трех лекарственно-устойчивых инфекций в США с самым высоким риском.Это условно-патогенная инфекция, поражающая толстую кишку пациентов после лечения антибиотиками. Микробиота, населяющая кишечник, обычно предотвращает колонизацию C. difficile и подавляет C. difficile -ассоциированное заболевание, но лечение антибиотиками приводит к изменениям в составе микробиоты, которые позволяют C. difficile расти и вызывать заболевание.
C. difficile продуцирует токсины, которые повреждают клетки кишечника и вызывают воспаление, вызывая диарею, и могут быть смертельными.Из почти 500 000 инфекций ежегодно примерно 29 000 приводят к смерти. Это наиболее частая причина внутрибольничных инфекций в развитых странах. Инфекция очень трудно поддается лечению, и многие пациенты страдают от рецидивирующих инфекций. Бактерия от природы устойчива ко многим распространенным антибиотикам, таким как фторхинолоны, поэтому исследователи ищут альтернативные способы лечения болезни.
Доктор Роберт Бриттон и его исследовательская группа заинтересованы в понимании того, как кишечная микробиота обеспечивает барьер для входящих патогенов и как нарушение микробиоты может приводить к инфекциям, в первую очередь C.difficile инфекции . Они разработали мини-биореакторы и мышей, колонизированных кишечной микробиотой человека, чтобы определить, какие члены микробного сообщества ответственны за подавление инвазии C. difficile . Их цель — разработать пробиотический коктейль, полученный из кишечной микробиоты человека, который подавит инвазию C. difficile .
Исследователи обнаружили, что две линии C. difficile , RT027 и RT078, стали более преобладающими и вирулентными за последние пару десятилетий, вызвав крупные вспышки.Чтобы определить факторы, которые увеличили вирулентность этих двух линий, доктор Бриттон и его коллеги исследовали, какие источники пищи предпочитают RT027 и RT078. Их исследование показало, что вирулентные клоны очень эффективно использовали диетическую сахарную трегалозу (которая содержится в диетической газировке и используется для стабилизации обработанных пищевых продуктов), что дает этим микробам конкурентное преимущество перед другими, менее вирулентными бактериями.
Используя свою мышиную модель, они обнаружили, что мыши, получавшие трегалозу в своем рационе, имели более тяжелое заболевание, с более высокими показателями смертности и производили более высокие уровни токсинов.Эти результаты предполагают, что введение трегалозы в качестве пищевой добавки в рацион человека незадолго до появления этих двух эпидемических линий помогло отобрать для их появления и способствовало вирулентности. Это исследование также демонстрирует, что диета может влиять на состав микробиоты и реакцию на инфекцию.
MedlinePlus: Антибиотики против бактерий: борьба с резистентностью
Расшифровка стенограммы
MedlinePlus представляет: Антибиотики против бактерий: борьба с резистентностью.
Что, если мы не сможем дать отпор?
Туберкулез. Гонорея. MRSA.
Эти вредные насекомые считаются одними из самых опасных организмов на планете сегодня, по мнению Национального института аллергии и инфекционных заболеваний (NIAID).
Все они присоединились к СОПРОТИВЛЕНИЮ.
Это устойчивость к противомикробным препаратам, чтобы прояснить. Такие бактерии быстро приобретают способность препятствовать нашим антибиотикам, в результате чего инфекции становится гораздо труднее лечить.И это большая проблема.
По оценкам CDC, ежегодно более двух миллионов человек в США заболевают инфекциями, устойчивыми к противомикробным препаратам, что приводит как минимум к 23 000 смертей. Беспокойство заключается в том, что другие бактерии могут присоединиться к этой устойчивости быстрее, чем мы сможем разработать решения, или что бактерии станут невосприимчивыми к еще большему количеству антибиотиков, что приведет к практически неизлечимым заболеваниям.
Кто эти бактерии?
Устойчивость к противомикробным препаратам развилась у многих различных видов бактерий, но некоторые из них вызывают большее беспокойство, чем другие.
Туберкулез, или туберкулез, является убийцей инфекционных заболеваний номер один в мире, унося более полутора миллионов жизней каждый год. Туберкулез трудно поддается лечению, и некоторые устойчивые штаммы требуют многолетнего ежедневного лечения несколькими лекарствами, включая месяцы болезненных инъекций и серьезных побочных эффектов, которые могут привести к потере слуха у пациентов.
Гонорея вызывает беспокойство, потому что штаммы стали устойчивыми ко всем, кроме некоторых антибиотиков. Это заболевание, передающееся половым путем, может иметь общие гены устойчивости между бактериями, что увеличивает скорость устойчивости.
Золотистый стафилококк, или стафилококк, повсюду: на наших личных вещах, на коже, в носу. Staph обычно не вреден. Но когда это происходит, лечение может быть затруднено, особенно в случае устойчивых к метициллину Staphylococcus aureus или MRSA, которые в настоящее время переносятся 2% американцев.
Это лишь некоторые из ведущих бактерий по устойчивости. Есть и другие, и еще больше.
Как возникает сопротивление?
Устойчивость возникает быстро из-за чрезмерного и неправильного использования антибиотиков в течение длительного периода времени, например, невыполнения предписанных курсов антибиотиков и использования антибиотиков в сельском хозяйстве для стимулирования роста животных.Бактерии размножаются так быстро, что даже если бы у нас был идеальный антибиотик, резистентность все равно возникла бы.
И каждый раз, когда мы используем антибиотики, есть шанс, что некоторые бактерии выживают из-за изменений в их ДНК. ДНК может кодировать преимущества выживания, такие как:
Изменение поверхности бактериальных клеток, предотвращение прикрепления или попадания антибиотиков.
Создание насосов, которые выплевывают антибиотики до того, как они начнут работать.
Или создание ферментов, которые «нейтрализуют» антибиотики.
Антибиотики убивают большинство бактерий, включая полезные бактерии в нашем организме.
Но бактерии с преимуществами могут выжить и размножаться.
Устойчивые бактерии могут передавать изменения ДНК своему потомству, а иногда даже друг другу, чтобы создать новые штаммы устойчивых к антибиотикам бактерий.
Что вы можете сделать, чтобы бороться с сопротивлением?
Использование меньшего количества антибиотиков в обществе может помочь предотвратить резистентность, сэкономив антибиотики на тот момент, когда они наиболее подходят.
Первым шагом является предотвращение потребности в антибиотиках путем предотвращения инфекций, например, путем мытья рук, иммунизации и безопасного приготовления пищи.
Правильное использование антибиотиков также помогает, например, прохождение предписанных курсов антибиотиков, направленных на то, чтобы не оставлять бактерии и дать им шанс стать устойчивыми. Пропущенные дозы антибиотиков могут улучшить среду для размножения устойчивых бактерий и вызвать устойчивую инфекцию.
Сопоставляя определенные антибиотики с бактериями, вызывающими инфекции, медицинские работники могут бороться с устойчивостью к противомикробным препаратам, уменьшая количество и силу антибиотиков, принимаемых пациентами.Следует позаботиться о том, чтобы инфекции еще не были устойчивы к антибиотикам! Также не следует назначать антибиотики при вирусных инфекциях, таких как простуда или грипп, потому что антибиотики не действуют на вирусы.
Исследования в NIAID
NIAID изучает способы борьбы с проблемой устойчивости к противомикробным препаратам. Изучаются многие возможности, в том числе поиск новых антибиотиков, которые выявляют слабые места в жизненном цикле бактерий, поиск способов усиления иммунной системы для борьбы с бактериальными инфекциями, создание бактериальных сообществ, которые заглушают воздействие инфекционных бактерий, с использованием специальных вирусов, нацеленных на и убивают инфекционные бактерии, а также улучшают диагностические тесты, чтобы лучше воздействовать на бактерии с помощью наиболее подходящих антибиотиков.
При наличии надлежащей практики общественного здравоохранения и передовых исследований мы, возможно, сможем не отставать от резистентности и инфекционных заболеваний в целом, но нам всем нужно работать вместе, чтобы оставаться на шаг впереди.
Узнайте о конкретных последних исследованиях и историях на medlineplus.gov и в журнале NIH MedlinePlus, medlineplus.gov/magazine, а также узнайте больше об исследованиях NIAID на niaid.nih.gov.
Устойчивость к антибиотикам | Сидарс-Синай
Не то, что вы ищете?Что такое устойчивость к антибиотикам?
Антибиотики — это лекарства, убивают бактерии.Со временем определенные группы этих микробов могут адаптироваться к этим лекарствам. Они могут измениться так, что антибиотики не смогут их убить. Срок для этого является устойчивость к антибиотикам.
Бактерии — очень маленькие организмы. Они могут попасть в ваше тело. Некоторые из них безвредны и могут быть полезны. Но некоторые из эти микробы могут быть вредными. Когда они размножаются внутри вашего тела, они могут вызвать болезнь.
До приема антибиотиков люди часто сильно заболела бактериальной инфекцией. С помощью этих лекарств теперь легко лечить многие из этих инфекций.
Устойчивость к антибиотикам — серьезное беспокойство во всем мире. Это может привести к заболеваниям, которые очень трудно вылечить. Стандартные антибиотики для лечения заболевания в этих случаях могут больше не работать. Другой лекарства тоже могут не помочь.В результате устойчивость к антибиотикам становится все более высокой. общий.
Что вызывает устойчивость к антибиотикам?
Устойчивость к антибиотикам может возникнуть при лечении бактерий антибиотиками. Лекарство убивает большинство этих микробов. Но небольшая группа может выжить. Это могло произойти по-разному. Микробы могут:
- Развить способность останавливать действие лекарства
- Развить способность качать лекарство вне клетки
- Измените (мутируйте), чтобы лекарство больше не работает
Когда бактерии становятся устойчивыми, оригинальный антибиотик больше не может их убить.Эти микробы могут расти и распространяться. Они может вызывают трудноизлечимые инфекции. Иногда они могут даже распространять сопротивление другим бактериям, с которыми они встречаются.
Когда вы используете антибиотик, есть риск того, что некоторые из бактерий станут устойчивыми. Использование этих лекарств при Они не нужны — основная причина, почему это становится все более распространенным. Итак, вы должны использовать эти лекарства только при необходимости.
Устойчивость к антибиотикам часто связаны с конкретным микробом и антибиотиком. Например, золотистый стафилококк (или «Стафилококк») — это тип бактерий, вызывающих болезни. Метициллин-устойчивый S. aureus (MRSA) — это особый штамм бактерий стафилококка. MRSA больше не реагирует на антибиотик метициллин (и родственные ему лекарства). В результате он может вызвать множество инфекций. которые трудно поддаются лечению.
Кто подвержен риску устойчивости к антибиотикам?
Чем больше людей используют антибиотики, тем больше вероятность того, что сопротивление произойдет. Иногда люди используют антибиотики, когда Они они действительно не нужны. Например, антибиотики не действуют против вирусов. Нравиться бактерии, вирусы — крошечные организмы, которые могут проникнуть в ваше тело и вызвать инфекцию. А простуда или грипп — это разновидность вируса.Прием антибиотика в этих случаях не лечит болезнь. Это действительно может повысить риск устойчивости к антибиотикам.
Неполный прием антибиотика также повышает риск. Если вы перестанете принимать его слишком рано, вы не сможете убить всех бактерии. Оставшиеся микробы могут стать устойчивыми.
Как распространяются устойчивые к антибиотикам инфекции
Устойчивые бактерии распространяются в так же, как и неустойчивые бактерии.Кто-то инфицирован бактериями (или просто нося его на коже) может коснуться какого-либо предмета. Когда вы касаетесь того же объекта, микробы могут попасть в ваше тело. Часто это происходит из-за пореза на коже. Некоторые инфекции может распространяться в воздухе при чихании или кашле. Другие могут распространяться через делиться едой с инфицированным человеком. Половой контакт — еще один способ заражения. распространение.
Вы можете помочь предотвратить распространение всех бактериальных инфекций:
- Всегда тщательно мыть руки с мылом и водой
- Не делиться едой или напитками с другие
- Практика безопасного секса
- Использование салфеток для прикрытия рта при кашле или чихании
- Не касаясь другого раны людей
- Не делиться личными вещами, такими как бритвы, полотенца или щетки
Обычное мыло лучше всего подходит для стирки руки и общие поверхности.Мыло с антибактериальными ингредиентами не помогает остановить распространение инфекции в домашних условиях. Они также могут способствовать сопротивлению.
Каковы симптомы устойчивости к антибиотикам? инфекционное заболевание?
Инфекции, вызываемые этими бактериями, могут влияют почти на все системы организма. Они могут вызывать множество симптомов. Но симптомы один не могу сказать, вызвана ли инфекция микробами, устойчивыми к антибиотикам.
Как диагностируются устойчивые к антибиотикам инфекции?
Ваш лечащий врач может образец инфицированной ткани и отправьте его в лабораторию. Там тип заразы может быть разобрался. Тесты также могут показать, какие антибиотики убивают микробы. Ты можешь иметь ан инфекция, резистентная к антибиотикам, если вам не станет лучше после лечения стандартными антибиотики.
Как лечат инфекции, устойчивые к антибиотикам?
Лечение этих инфекций может отличаться. Ваш лечащий врач может прописать другой антибиотик, который борется с инфекцией. Но у него могут быть определенные недостатки. Это может иметь больше побочных эффектов или риск содействие большему сопротивлению. В некоторых случаях у вашего провайдера может не быть другого варианта. В этом случае вам будет оказана поддерживающая помощь.
Что я могу сделать, чтобы предотвратить устойчивость к антибиотикам?
Лучший способ предотвратить антибиотик устойчивость заключается в правильном применении антибиотиков. Берите их только при необходимости. Вот некоторые из способы, которыми вы можете помочь:
- Не принимайте антибиотики при вирус.
- Не оставляйте антибиотик для следующего время, когда ты заболеешь.
- Принимайте антибиотики точно так же, как предписано. Не пропускайте дозы. Завершите полный курс лечения, даже если вы чувствую себя лучше.
- Никогда не принимайте предписанные антибиотики для кого-то другого.
Медицинские работники также могут помочь от:
- Назначение только антибиотиков, нужный
- Нацеливание на лекарство, как только возможно для конкретных вовлеченных бактерий
- Лекарства выписываются только на срок по мере необходимости
Другие меры общественного здравоохранения могут также помогают снизить сопротивление.Это включает сокращение использования антибиотиков в домашний скот.
Поставщикам медицинских услуг также необходимо принять меры, чтобы остановить распространение этих инфекций. Эти бактерии очень распространены в настройки здравоохранения. Они всегда должны соблюдать правила гигиены. Они также всегда должны использовать методы борьбы с инфекцией.
Основные сведения об устойчивости к антибиотикам
- Стандартные антибиотики не убивают бактерии, ставшие устойчивыми.Многие из этих микробов распространились по Мир.
- Эти бактерии могут вызывать инфекции. Их бывает очень сложно лечить.
- Если у вас инфекция, устойчивый к антибиотикам, ваш лечащий врач может назначить или не назначить другое лечение параметры.
- Прием ненужных антибиотиков способствует рост устойчивых бактерий.
- Соблюдайте правила гигиены. Помогает предотвратить распространение инфекций, устойчивых к антибиотикам.
Следующие шаги
Советы, которые помогут получить максимальную отдачу от визит к вашему лечащему врачу:
- Знайте причину вашего визита и что вы хотите.
- Перед визитом запишите вопросы, на которые вы хотите получить ответы.
- Возьмите с собой кого-нибудь, чтобы помочь вам спросить вопросы и запомните, что вам говорит ваш провайдер.
- При посещении запишите имя новый диагноз и любые новые лекарства, методы лечения или тесты. Также запишите любые новые инструкции, которые дает вам ваш провайдер.
- Знайте, почему новое лекарство или лечение прописан, и как это вам поможет.Также знайте, каковы побочные эффекты.
- Спросите, можно ли вылечить ваше состояние другими способами.
- Знайте, почему тест или процедура рекомендуются и что могут означать результаты.
- Знайте, чего ожидать, если вы не возьмете лекарство или пройти тест или процедуру.
- Если вам назначен повторный прием, запишите дату, время и цель визита.
- Узнайте, как можно связаться с вашим провайдером Если у вас есть вопросы.
Медицинский обозреватель: Дайан Хоровиц, доктор медицины
Медицинский обозреватель: Раймонд Терли младший PA-C
Медицинский обозреватель: Дафна Пирс-Смит, RN MSN
© 2000-2021 Компания StayWell, LLC. Все права защищены. Эта информация не предназначена для замены профессиональной медицинской помощи.Всегда следуйте инструкциям лечащего врача.
Не то, что вы ищете?Борьба с устойчивостью к антибиотикам | FDA
Узнайте больше о том, почему вам могут не понадобиться антибиотики во время болезни, и о проблемах, которые могут вызвать антибиотики, если их принимать без надобности.
Антибиотики — это лекарства, используемые для лечения инфекций, вызванных бактериями. Антибиотики, также известные как противомикробные препараты, спасли бесчисленное количество жизней.
Однако неправильное и чрезмерное употребление этих препаратов способствовало возникновению явления, известного как устойчивость к антибиотикам. Эта устойчивость развивается, когда потенциально опасные бактерии изменяются таким образом, что снижает или устраняет эффективность антибиотиков.
Проблема общественного здравоохранения
Устойчивость к антибиотикам — растущая проблема общественного здравоохранения во всем мире.Когда человек инфицирован устойчивой к антибиотикам бактерией, не только лечение этого пациента становится более трудным, но и устойчивые к антибиотикам бактерии могут распространяться на других людей.
Когда антибиотики не действуют, результат может быть
- более длительные болезни
- Болезни более сложные
- больше посещений врача
- Употребление более сильных и дорогих препаратов
- человек больше смертей от бактериальных инфекций
Примеры бактерий, которые стали устойчивыми к антибиотикам, включают бактерии, вызывающие кожные инфекции, инфекции мочевыводящих путей, менингит, заболевания, передаваемые половым путем, и инфекции дыхательных путей, такие как пневмония.
В сотрудничестве с другими правительственными учреждениями Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) выступило с рядом инициатив по борьбе с устойчивостью к антибиотикам.
Агентство издало правила маркировки лекарств, в которых подчеркивается разумное использование антибиотиков. Правила побуждают медицинских работников назначать антибиотики только в случае клинической необходимости и консультировать пациентов о правильном использовании таких лекарств и важности их приема в соответствии с указаниями. FDA также поощряет разработку новых лекарств, вакцин и улучшенных диагностических тестов для инфекционных заболеваний.
Антибиотики борются с бактериями, а не с вирусами
Антибиотики предназначены для лечения бактериальных инфекций. Например, они используются для лечения ангины, вызываемой стрептококковыми бактериями, и кожных инфекций, вызванных стафилококковыми бактериями.
Хотя антибиотики убивают бактерии, они не эффективны против вирусов. Следовательно, они не будут эффективны против вирусных инфекций, таких как простуда, кашель, многие виды боли в горле и грипп.
Использование антибиотиков против вирусных инфекций
- не вылечит инфекцию
- не будет удерживать других людей от заражения вирусом
- не поможет человеку почувствовать себя лучше
- может вызывать ненужные, вредные побочные эффекты
- может способствовать развитию устойчивых к антибиотикам бактерий
Пациенты и медицинские работники могут сыграть важную роль в борьбе с устойчивостью к антибиотикам. Пациентам не следует требовать антибиотики, если медицинский работник говорит, что они не нужны.Медицинские работники должны назначать антибиотики только при инфекциях, которые, по их мнению, вызваны бактериями.
Как пациент, лучше всего спросить у своего лечащего врача, будет ли антибиотик эффективным при вашем заболевании. Также спросите, что еще вы можете сделать, чтобы облегчить симптомы.
Так как же узнать, что у вас простуда или бактериальная инфекция?
Джозеф Тёрнер, доктор медицины, магистр здравоохранения, медицинский сотрудник Центра оценки и исследований лекарственных средств FDA, говорит, что симптомы простуды или гриппа обычно уменьшаются в течение недели.Но если у вас жар и другие симптомы, которые сохраняются и ухудшаются с течением времени, возможно, у вас бактериальная инфекция, и вам следует проконсультироваться с врачом.
Следуйте инструкциям по использованию по назначению
Когда вам прописывают антибиотик для лечения бактериальной инфекции, важно принимать лекарство точно в соответствии с указаниями. Вот еще несколько советов по правильному использованию антибиотиков.
- Принимайте антибиотики в соответствии с предписаниями. Важно принимать лекарства в соответствии с предписаниями врача, даже если вы чувствуете себя лучше.Если лечение прекратится слишком рано и вы снова заболеете, оставшиеся бактерии могут стать устойчивыми к принимаемому вами антибиотику.
- Не пропускайте дозы. Антибиотики наиболее эффективны, когда их принимают по назначению.
- Не экономьте на антибиотиках. Вы можете подумать, что можете приберечь антибиотик на случай следующего заболевания, но антибиотик предназначен для лечения вашей конкретной инфекции в данный момент. Никогда не принимайте остатки лекарства. Принятие неправильного лекарства может отложить получение соответствующего лечения и может привести к ухудшению вашего состояния.
- Не принимайте антибиотики, назначенные другим лицам. Они могут не подходить для вашего заболевания, могут отсрочить правильное лечение и привести к ухудшению вашего состояния.
- Поговорите со своим лечащим врачом. Задавайте вопросы, особенно если вы не уверены, когда вам нужен антибиотик или как его принимать.
- Все препараты имеют побочные эффекты. Сообщите своему лечащему врачу, если у вас появятся новые или необычные симптомы или побочные эффекты.Возможно, вам потребуется остановить прием антибиотика, вызывающего неприятный побочный эффект, и завершить лечение другим антибиотиком.
Потребители и медицинские работники также могут сообщать о нежелательных явлениях в программу FDA MedWatch по телефону 800-FDA-1088 или онлайн в MedWatch.
Что делает FDA
FDA борется с устойчивостью к антибиотикам с помощью мероприятий, включающих
- Утверждение некоторых новых антибиотиков. С 2015 года FDA одобрило новые антибиотики, которые могут лечить определенные устойчивые бактерии.Медицинским работникам рекомендуется использовать новые антибиотики надлежащим образом, а некоторые антибиотики использовать только у пациентов, у которых есть ограниченные возможности лечения или нет других вариантов лечения.
- Правила маркировки, касающиеся правильного использования антибиотиков. Маркировка антибиотиков содержит обязательные заявления в нескольких местах, рекомендующие медицинским работникам использовать эти препараты только для лечения инфекций, которые, как считается, вызваны бактериями. Маркировка также побуждает медицинских работников консультировать пациентов по поводу правильного использования.
- Партнерство для повышения осведомленности общественности. FDA сотрудничает с Центрами по контролю и профилактике заболеваний (CDC) в рамках кампании «Стань умнее: знай, когда антибиотики работают», предлагая веб-страницы, брошюры, информационные бюллетени и другие источники информации, направленные на то, чтобы помочь общественности узнать о профилактике устойчивые к антибиотикам инфекции.
- Поощрение разработки новых антибиотиков. FDA разработало руководство для промышленности по типам клинических исследований, которые можно проводить для оценки эффективности антибактериального препарата при лечении различных типов инфекций.FDA организовало и участвовало в семинарах, направленных на разработку новых антибиотиков для лечения устойчивых бактериальных инфекций.
к началу
.