как выбрать лучший препарат — эффективные средства от дисбактериоза кишечника
{{if type === ‘partner-stocks’}}
{{/if}}
{{/if}} {{each list}}${this} {{if isGorzdrav}}
Удалить
{{/if}}
{{/each}} {{/if}} Поиск по лекарствам, болезням, веществу: ДЕРМАКОСМЕТИКА, Ньюрексан, Durex, От боли, ВольтаренСтатьи
Лекарство от дисбактериоза – как выбрать лучший препарат?
Проблемы со стулом, неприятное чувство в животе может быть связано не только с отравлением пищей. У взрослых и детей за этими симптомами часто скрывается дисбактериоз. Врачи не считают его заболеванием, это состояние часто сопровождает другие патологии или является их следствием. Но устранять нарушение микрофлоры нужно как можно раньше.
У взрослых и детей за этими симптомами часто скрывается дисбактериоз. Врачи не считают его заболеванием, это состояние часто сопровождает другие патологии или является их следствием. Но устранять нарушение микрофлоры нужно как можно раньше.
Что такое дисбактериоз
Ребенок появляется на свет стерильным, в его организме в норме нет бактерий. Кишечник, кожа заселяются постепенно, начиная с первого прикладывания младенца к груди. Чем старше становится ребенок и более разнообразна его пища, тем больше различных бактерий попадают в кишечник и формируют его микрофлору. У взрослых людей состав микроорганизмов стабилизируется, но становится разнообразным. Его можно сравнить с отпечатком пальцев, несмотря на сходство, он не повторяется ни у одного человека.
Среди кишечных бактерий насчитывается сотни видов хороших микроорганизмов, но в норме встречаются и плохие, рост которых организм может сдерживать. Условно выделяют три типа микробов:
- доминирующие – присутствуют у всех здоровых людей, к ним относятся эубактеры, бактероиды, бифидобактерии, лактобактерии;
- непостоянные виды – встречаются не у всех или при определенных условиях, это стрептококки, кишечная палочка, протей, цитобактер;
- транзиторные виды – иногда попадают в кишечник, но долго там не задерживаются, это такие типы, как дрожжевые грибы, клостридии, синегнойная палочка.

Хорошими микроорганизмами являются доминирующие бактерии, их должно быть большинство. Благодаря присутствию нормальной микрофлоры переваривается пища. Бактерии помогают ферментировать некоторые неперевариваемые продукты, участвуют в всасывании витаминов, аминокислот, сахаров. Сами они тоже синтезируют витамины группы В, К, жирные кислоты. Поэтому при дисбактериозе появляются признаки гиповитаминоза.
Хорошие бактерии выполняют роль живого щита. Они формируют защитный слой на кишечной стенке, которые не позволяет прикрепиться патогенным микроорганизмам и ограничивает их в питательных веществах. Иммунная функция заключается в тренировке клеток иммунитета и регуляции его ответа на проникновение чужеродных микроорганизмов или белков.
Но при изменении соотношения бактерий, увеличении количества транзиторных видов, появлении дрожжевых грибков, развивается дисбактериоз. Его нельзя назвать заболеванием, но самочувствие у человека нарушается. При дисбактериозе в кишечнике нет патогенных микроорганизмов (сальмонелл, холерного вибриона, иерсиний, патогенных эшерихий, а также вирусов).
Причины
Микрофлора кишечника у взрослых находится в состоянии динамического равновесия. В нем присутствуют определенные бактерии, которые составляют большинство, и около 3 % микроорганизмов, которые меняют свой состав. В норме колебания происходят под влиянием продуктов питания и пищевых привычек. На микрофлору влияет преобладание в рационе сладкого и жирного или преимущественно растительная пища.
Исследования показывают, что жирная еда угнетает бифидобактерии и энтерококки, но в этих условиях размножаются бактероиды. Преимущественно углеводная диета стимулирует размножение бифидобактерий и общего количество микроорганизмов. Но таки перемены носят временный характер и не ведут к появлению симптомов дисбактериоза. Они сами исчезают после изменения питания.
Дисбактериоз кишечника у взрослых появляется в результате других заболеваний. Основными причинами нарушения микрофлоры являются:
Основными причинами нарушения микрофлоры являются:
- длительное лечение антибиотиками;
- патологии вышележащих отделов пищеварительного тракта;
- продолжительные монодиеты и постоянное неправильное питание;
- кишечные инфекции.
Антибиотики широкого спектра действия действуют неселективно. Они угнетают рост или вызывают гибель всех микроорганизмов. Чем дольше курс лечения, тем выше вероятность, что после него разовьется дисбактериоз. Особенно опасны тетрациклиновые антибиотики. Они значительно угнетают размножение кишечной микрофлоры, что приводит к гиповитаминозу В, К, увеличению риска кровотечений.
Гастрит, холецистит, панкреатит, гепатит или дискинезия желчных путей могут привести к развитию дисбактериоза. Опасны цирроз печени, опухолевые процессы в желудке или язва. Эти патологии сопровождаются нарушением переваривания пищи, выработки ферментов. Поэтому в кишечник пища поступает недостаточно обработанной и не может служить питательной средой для бактерий.
Разгрузочный день, когда рацион строится на употреблении одного продукта питания, не наносит вреда организму. Но монодиета, которая длится несколько недель или становится образом жизни, может привести к дисбактериозу. Опасно постоянное употребление еды, содержащей простые углеводы, животные жиры. Это сладкое, мучное, блюда из фаст-фуда. Такой рацион угнетает размножение нормальной флоры, в кишечнике активируются процессы брожения, появляется большое количество дрожжевых грибков.
Двойной вред кишечнику наносят пищевые инфекции. Они повреждают слизистую оболочку, а лечение антибиотиками убивает полезные бактерии. Поэтому восстановление после болезни проходит особенно тяжело.
Негативно на состояние кишечника влияет курение. Оно создает условия для размножения дрожжевых грибков, поэтому курильщики часто мучаются неприятными симптомами.
Симптомы дисбактериоза
Нет строгих симптомов, которые с большой вероятностью указывают на дисбактериоз.
- урчание в животе;
- метеоризм, усиленное газообразование;
- вздутие живота;
- нарушения стула;
- появление в кале патологических примесей.
Усиление газообразования на начальном этапе происходит после нарушения питания. Если в определенный день в рационе присутствовало молоко, бобовые, большое количество мучного и сладкого, симптомы проявляются ярко.
Нарушения стула изменчивы. Чаще всего дисбактериоз проявляется диареей. Она может сопровождаться спазмами и болью в животе. Иногда неоформленный стул появляется всего раз в сутки, поэтому не попадает под критерий диареи.
Понос может сменяться запором. Такой процесс наблюдается у людей, которые ограничивают количество клетчатки и пищевых волокон в рационе. Это лишает бактерии необходимых питательных веществ, не позволяет удерживать в просвете кишечника воду. Слизистые патологические примеси в каловых массах, боль в животе появляются при запущенных формах дисбактериоза.
Слизистые патологические примеси в каловых массах, боль в животе появляются при запущенных формах дисбактериоза.
Нарушение состава микрофлоры приводит к дефициту витаминов. Если он не компенсируется при помощи питания или приема поливитаминных препаратов, появляются симптомы гиповитаминоза:
- ухудшается состояние волос, ногтей;
- на коже появляются высыпания;
- проявляются аллергические реакции или пищевая непереносимость;
- повышается утомляемость, снижается работоспособность;
- нарушается сон.
Кишечные микроорганизмы синтезируют витамин К, который участвует в свертывании крови. При гиповитаминозе учащается появление синяков, гематом под кожей от небольшого механического воздействия. При язве желудка, небольших травмах увеличивается риск продолжительного кровотечения.
В тяжелых случаях дисбактериоз, который сопровождается диареей, приводит к обезвоживанию. У многих пациентов снижается масса тела.
Какое нужно обследование
Симптомы дисбактериоза неспецифические. За одинаковыми признаками могут маскироваться патология органов пищеварения или гиповитаминоз. Поэтому дисбактериоз считается клинико-лабораторным синдромом.
За одинаковыми признаками могут маскироваться патология органов пищеварения или гиповитаминоз. Поэтому дисбактериоз считается клинико-лабораторным синдромом.
Диагностика начинается с копрологического исследования, которое позволяет оценить пищеварительную функцию, состояние ферментных систем, перистальтику и скорость продвижения пищевого комка.
Но изменение состава кала еще не говорит о дисбактериозе. Необходимо подтвердить изменение состава бактерий в просвете кишечника. В Москве во многих клиниках применяют методы газожидкостной и ионной хроматографии. Они позволяют определить состав микрофлоры по полученным метаболитам.
Часто используют бактериологическое исследование. Для этого смывы со слизистой оболочки кишечника, фекалии или соскоб высевают на специальные питательные среды. Этот способ позволяет получить колонии бактерий и с высокой точностью определить их тип. Также используют специальный анализ кала на дисбактериоз. Но обязательное условие – биологический материал должен попасть в лабораторию не позже, чем через час после его получения от пациента. Кал необходимо поддерживать в теплом виде, чтобы не вызвать гибель бактерий. Метод не оправдывает себя тем, что дает представление только о состоянии флоры толстого кишечника.
Кал необходимо поддерживать в теплом виде, чтобы не вызвать гибель бактерий. Метод не оправдывает себя тем, что дает представление только о состоянии флоры толстого кишечника.
Золотой стандарт диагностики дисбактериоза – интестиноскопия. Это эндоскопический метод, во время которого в полость тонкой кишки через рот и желудок или прямую и толстую кишку вводят гибкий зонд с видеокамерой. Он необходим для осмотра слизистой кишечника и получения аспирата его содержимого. Полученную жидкость также засевают на питательную среду. Недостаток метода – необходимость общей анестезии, специальных бактериологических сред и долгое ожидание результата. Иногда для диагностики дисбактериоза применяют дыхательный тест с меченным Н2.
Препараты и их действиеСамый эффективный способ восстановить микрофлору и избавиться от дисбактериоза – использовать препараты из группы пробиотиков. Производители предлагают лекарственные средства в разных формах:
- капсулы;
- таблетки;
- порошок;
- капли;
- раствор.

Лекарственную форму подбирает врач в зависимости от возраста пациента. Детям и пожилым людям, которым тяжело глотать таблетки, назначают раствор или порошок для его приготовления. В возрасте 0-3 лет ребенку легче дать капли с пробиотиком. Всем остальным рекомендованы средства в виде капсул или таблеток.
Препараты от дисбактериоза – это лекарства, которые можно приобрести без рецепта врача. Но самолечением заниматься не рекомендуется, только специалист может подсказать, какой тип лучше принимать.
В составе пробиотиков обычно 1-2 типа бактерий, которые хорошо восстанавливают слизистую. Обычно это лакто- и бифидобактерии. Они являются нормальными обитателями кишечника, которые помогают улучшить микробный баланс. Механизм действия этой терапевтической группы связан с подавлением роста патогенной флоры. Молочнокислые бактерии конкурируют за рецепторы на эпителии слизистой оболочки, питательные вещества. Они выделяют молочную кислоту, цитокины, которые оказывают угнетающее действие на патогены.
Эффективно вылечить дисбактериоз помогают препараты из группы пребиотиков. Это лекарства, которые относятся к группе пищевых волокон: инулин и лактулоза, а также препараты на их основе (например, Бифиформ, Дюфалак)..
Они не расщепляются пищеварительными ферментами и попадают в неизменном виде в толстый кишечник, где становятся питательным субстратом для лакто- и бифидобактерий. Поэтому микробы хорошо размножаются, увеличивают объем бактериальной массы, восстанавливают стенку кишечника. Чтобы лечение было максимально эффективное, рекомендуется пить одновременно пребиотики и пробиотики (Энтерол и др.).
Лечение дисбактериоза не противопоказано при сопутствующих патологиях пищеварительного тракта. Пробиотики не наносят вреда пациентам с язвой желудка, заболеваниями печени или желчного пузыря. А в некоторых случаях они ускорят восстановление.
В запущенных случаях дисбактериоза кишечника и когда симптомы диспепсии слишком мучительны, могут помочь лекарства из группы ферментов (Мезим и др. ). Их должен подбирать врач, в зависимости от типа нарушения пищеварения. Эти средства необходимо пить ежедневно до еды
). Их должен подбирать врач, в зависимости от типа нарушения пищеварения. Эти средства необходимо пить ежедневно до еды
Сколько времени придется лечить дисбактериоз, сказать тяжело. В некоторых случаях это может растянуться на несколько недель, а при запущенном состоянии – несколько месяцев.
Профилактика дисбактериозаДаже если использовать эффективные препараты и избавиться от дисбактериоза, нельзя точно сказать, не придется ли его лечить еще раз. Поэтому врачи рекомендуют соблюдать меры профилактики.
Самый эффективный – постоянно придерживаться диеты. Она подбирается в зависимости от типа диспепсии. Универсальное средство профилактики – употреблять продукты, которые содержат естественные пробиотики. К ним относятся крупяные каши, кисломолочные продукты с закваской из бифидобактерий, некоторые сорта хлеба. Если постоянно ощущается брожение в кишечнике, на время терапии нужно исключить из рациона углеводы, молоко, горох и сою. Не рекомендуют употреблять продукты, богатые эфирными маслами. У ним относятся лук, чеснок, редька, редис.
Не рекомендуют употреблять продукты, богатые эфирными маслами. У ним относятся лук, чеснок, редька, редис.
Хорошо пить не менее 1,5 л чистой воды в сутки. Действенный способ стабилизировать состав микрофлоры – принимать растительные соки. В этом помогают морковный, тыквенный, картофельный. Помогают многие растительные продукты: ягоды черники, земляники, абрикосы, клюква. Врач может назначить отвары лекарственных растений.
Лечить дисбактериоз при преобладании грибковой флоры можно растворимым цикорием. В некоторых случаях эффективны эвкалипт, календула, соя, зверобой.
В список полезных веществ при дисбактериозе входит инулин. Он ускоряет рост и размножение бифидобактерий, чем помогает увеличить объем полезных микробов в кишечнике. Инулин помогает восстановить слизистую за счет увеличения выработки слизи, изменения степени рН и создания благоприятной среды для бактерий.
К мерам профилактики дисбактериоза относится использование пробиотиков заранее у пациентов, которым необходимо пройти курс лечения антибиотиками или химиотерапию. Это позволяет поддержать нормальный состав микрофлоры и избежать неприятных симптомов после окончания терапии.
Это позволяет поддержать нормальный состав микрофлоры и избежать неприятных симптомов после окончания терапии.
Все о дисбактериозе | Медицинский центр «Новая медицина»
ВСЁ О ДИСБАКТЕРИОЗЕ
Дисбактериоз очень распространенное заболевание. По данным Минздрава дисбактериоз выявляют у 90% взрослого населения и свыше 25% детей в возрасте до года. Многие заболевания, в том числе и хронические, связаны с нарушением микробиоценоза кишечника и часто являются следствием дисбактериоза, а не его причиной.
Дисбактериоз считается основной социальной болезнью 21-го века. Актуальность проблемы требует постоянного поиска новых средств лечения дисбактериоза и его коррекции.
ДИСБАКТЕРИОЗ У ДЕТЕЙ
Дисбактериоз у детей, как и у взрослых, возникает вследствие нарушения баланса микрофлоры кишечника. Определить его наличие без анализа в лаборатории крайне сложно, поскольку это не является самостоятельным заболеванием, а возникает вследствие воспалительного процесса в организме или же в случае нарушения баланса витаминов. В медицинской терминологии также применяется определение «дисбиоз», которое является синонимом «дисбактериоза».
В медицинской терминологии также применяется определение «дисбиоз», которое является синонимом «дисбактериоза».
Чаще всего возникает дисбактериоз у детей грудного возраста. К основному фактору его появления относится искусственное вскармливание малыша и недостаток витаминов, получаемых с дополнительной пищей. Также дисбактериоз у детей может возникнуть при аллергических реакциях организма, приема антибиотиков, зоны повышенной радиации, острых и хронических заболеваний пищеварительной системы или нарушения нормального функционирования кишечника из-за недостатка бактерий, расщепляющих кислоты и питательные вещества. Источник, как правило, устанавливает врач.
Кишечно-желудочный тракт взрослого человека содержит примерно 1,5 кг бактерий, около 400—500 разных видов, а у детей до двух лет, вскармливаемых грудным молоком, преобладают в основной массе бифидобактерии, которые препятствуют развитию кишечно-желудочных заболеваний. У малышей, которых вскармливают искусственным путем, из-за невозможности кормить грудью, не формируется преобладание какой-то определенной группы бактерий — бифидо бактерий, такое питание не сможет предотвратить дисбактериоз у ребенка и защитить организм от других заболеваний. Поэтому врачи рекомендуют кормить теми кисломолочными смесями, которые способствуют их размножению. Информацию о свойствах смесей можно прочитать на упаковке и выбрать оптимальную для ребенка.
Поэтому врачи рекомендуют кормить теми кисломолочными смесями, которые способствуют их размножению. Информацию о свойствах смесей можно прочитать на упаковке и выбрать оптимальную для ребенка.
Преобладание бифидобактерий в детском организме важно тем, что они помогают регулировать обмен желчных кислот, а также принимают участие в формировании органических веществ и кислот, необходимых для работы кишечника. Способствуют усваиванию витаминов К, группы В, D, солей, никотиновой и фолиевой кислоты, получаемых с питанием. Имеют антиаллергическое, антирахитическое и антианемическое действие на организм, а кроме того формируют иммунитет.
Как мы уже говорили, симптомов, по которым можно однозначно сделать вывод, что это дисбактериоз — нет, поэтому нужно искать в первую очередь причину — то заболевание, которое может сопровождаться дисбактериозом.
Раньше дисбактериоз определяли с помощью анализа состава кала, но так как осуществить правильный сбор кала в стерильную посуду не возможно, результат такого анализа не до конца объективен. На сегодняшний день в современной медицине применяются более сложные и точные методы, такие как исследование с помощью биохимии; для гастроскопии — анализ соскоба слизистой 12-перстнойлибо тощей кишки, для колоноскопии — анализ соскоба прямой и толстой кишки. Но такие сложные исследования проводятся только по назначению лечащего врача.
На сегодняшний день в современной медицине применяются более сложные и точные методы, такие как исследование с помощью биохимии; для гастроскопии — анализ соскоба слизистой 12-перстнойлибо тощей кишки, для колоноскопии — анализ соскоба прямой и толстой кишки. Но такие сложные исследования проводятся только по назначению лечащего врача.
Каким же образом происходит лечение?
Первостепенно необходимо лечить причину его возникновения — основное заболевание, которое устанавливает один из врачей, назначенных педиатром. Курс лечения будет состоять из лечения очага заболевания и специализированного питания смесями, способствующими либо образованию правильной (здоровой) микрофлоры кишечника либо смесями, которые уже содержат микроорганизмы.
Предотвращается возможный дисбактериоз у ребенка в первую очередь длительным грудным кормлением и своевременным введением дополнительного прикорма к молоку. Лучше всего все этапы вскармливания ребенка согласовывать с наблюдающим педиатром, собственная интуиция важна, но совет профессионала не менее важен, тем более в этом возрасте закладывается основа иммунитета на всю жизнь. Дополнять рацион питания рекомендуется специальными кисло-молочными смесями, которые содержат в себе бифидо и лактобактерии полезные деткам.
Дополнять рацион питания рекомендуется специальными кисло-молочными смесями, которые содержат в себе бифидо и лактобактерии полезные деткам.
В том случае, если врач установил дисбактериоз у ребенка, к основному питанию добавляются кисло-молочные продукты, в зависимости от направления лечения. Наринэ-Форте, Биовестин, Биовестин-лакто содержат бифидо и лактобактерии в пропорциях и состояние, которые способны стимулировать развитие микроорганизмов нормальной флоры.
Но не забывайте — не только питанием лечится дисбактериоз у детей, а также предупреждением первоисточника его возникновения, который определяет врач. Лучше всего сразу применять смеси, которые способствуют образованию бифидобактерий, как прикорм к основному питанию, для того, чтобы поддерживать необходимую микрофлору кишечника и предотвратить дисбактериоз у ребенка, а именно лечение смесями уже осуществлять под руководством врача в сочетании с лечением очага воспаления.
ДИСБАКТЕРИОЗ — ВРАГ ЗДОРОВЬЯ
Каждый день наш организм нуждается в еде. Без пищи человек не может существовать. Прием пищи становится ритуалом, который человек должен соблюдать изо дня в день. Однако не всегда наш организм в силе переварить ее. Особенно, если мы позволяем себе лишнего.
Без пищи человек не может существовать. Прием пищи становится ритуалом, который человек должен соблюдать изо дня в день. Однако не всегда наш организм в силе переварить ее. Особенно, если мы позволяем себе лишнего.
Например, переедаем за ужином или перед сном, едим не совсем полезную и здоровую пищу. Полноценное пищеварение возможно только в случае наличия в желудке каждого человека самых разнообразных микробов. Причем эти микробы могут быть как положительными, так и, как это ни странно, отрицательными. Именно они помогают нашему желудку все это переварить.
Если говорить о дисбактериозе, то это состояние, во время которого все микробы нашего организма изменяют свой состав. Это изменение в свою очередь ведет к нарушению работы желудка и кишечника.
Вполне правильным будет вопрос — почему же все это происходит? Изменение состава Вашего кишечника происходит в результате каких-либо изменений в Вашем организме. Что это значит? Ваш организм чем-то заражен или в него попала какая-то инфекция. Все это приводит к появлению дисбактериоза.
Все это приводит к появлению дисбактериоза.
Рассмотрим подробнее причины появления дисбактериоза. Этот сбой работы кишечника может произойти в результате неправильного применения различных антибиотиков. Если Вы страдаете заболеваниями пищеварительного тракта, у Вас также может появиться дисбактериоз. Слабый иммунитет, послеоперационное состояние или неправильное питание — еще три причины появления дисбактериоза.
Во время дисбактериоза кишечник перестает обладать полезными микробами. Он наполнен только вредными бактериями, которые приводят к болям в области кишечника. В этот момент организм человека практически не получает никаких витаминов, жиров и других важных для организма веществ. Все это приводит к сильному снижению веса больного. При дисбактериозе у больного болит и вздувается живот. У него обязательно меняется стул.
Чтобы выявить наличие этого заболевания, Вам необходимо обратиться к врачу-гастроэнтерологу. Он назначит Вам гастроскопию, то есть проверят Ваш кишечник при помощи специального аппарата. Вам также проверят кишку и возьмут анализы кала. Все эти процедуры помогут врачу назначить Вам правильный курс лечения.
Вам также проверят кишку и возьмут анализы кала. Все эти процедуры помогут врачу назначить Вам правильный курс лечения.
При любом курсе лечения этого заболевания Вы должны будете соблюдать диету. Эта диета обязательно будет включать в свой состав различные продукты, которые богаты полезными бактериями. Чаще всего таковыми являются различные кисломолочные продукты. Также Вам пропишут антибиотики или бактериофаги. Это препараты, которые помогут Вам очистить кишечник от вредных бактерий. Также Ваше лечение не обойдется без лекарственных препаратов, которые помогут Вашему кишечнику нормализоваться. Это такие препараты как: Нарине-Форте, Бификол, Биовестин, Нарине Ф-баланс и др.
Чаще всего для полного выздоровления хватает двух месяцев. Однако есть одно но. Как правило, после лечения ни один врач не даст Вам стопроцентной гарантии, что Вы не заболеете дисбактериозом вновь. Микрофлора кишечника имеет один большой минус. Она очень быстро реагирует на любые изменения Вашего организма. Чтобы избежать всех этих неприятностей, Вам необходимо вовремя избавляться от любых неполадок Вашего органи. Например можно проводить профилактику — время от времени пропивать препараты, которые нормализуют микрофлору кишечника. Для этих целей отлично подойдет Нарине-Форте или Нарине Ф-баланс. При регулярном применение эти препараты не дадут развиться дисбактериозу, а так же нормализуют микрофлору пищеварительного тракта, что улучшит аппетит, стул и защитит Ваш кишечник от патогенных микробов. Также Вам не стоит принимать никакие антибиотики без консультации у врача.
Чтобы избежать всех этих неприятностей, Вам необходимо вовремя избавляться от любых неполадок Вашего органи. Например можно проводить профилактику — время от времени пропивать препараты, которые нормализуют микрофлору кишечника. Для этих целей отлично подойдет Нарине-Форте или Нарине Ф-баланс. При регулярном применение эти препараты не дадут развиться дисбактериозу, а так же нормализуют микрофлору пищеварительного тракта, что улучшит аппетит, стул и защитит Ваш кишечник от патогенных микробов. Также Вам не стоит принимать никакие антибиотики без консультации у врача.
Если говорить честно, то все в Ваших руках. Здоровье каждого человека в огромнейшей степени зависит исключительно от него самого. Если Вы будете себя беречь, Вы навсегда останетесь здоровыми и счастливыми.
БАД — ЭТО ТО, ЧТО НАМ НЕ ХВАТАЕТ В ПИЩЕ?
Относятся ли БАДы к разряду медикаментозных препаратов? Вызывают ли пищевые добавки привыкание? Могут ли добавки заменить обычное питание? Как правильно их применять? Что входит в их состав? Есть ли у БАДов противопоказания, и в каких случаях необходимо посоветоваться с врачом, прежде чем их принимать? На вопросы отвечает директор направления по улучшению качества пищевых продуктов канадского Института Здоровья Nutrilite.
Кто из нас не мечтает укрепить здоровье и продлить отпущенный природой срок жизни? Для этих целей вроде бы и выпускаются различные биологически активные добавки (БАДы). О них ходит множество мифов. Кто-то считает их панацеей от всего, кто-то убежден, что они не дают никакого эффекта, а их производители — шарлатаны…
Так что же такое БАДы и как правильно их принимать? С этим вопросом «Правда.ру» обратилась к Одре Дэвис — директору направления по улучшению качества пищевых продуктов канадского Института Здоровья Nutrilite.
— Относятся ли БАДы к разряду медикаментозных препаратов?
— Биологически активные добавки к пище — не лекарства. Но использовать их в комплексе с лекарственными средствами вполне разумно и оправданно. Они помогают оздоровить организм, сократить длительность болезни, снизить риск развития осложнений и обострений, позволяют увеличить продолжительность жизни. Лекарства хороши, когда человек уже заболел. А БАДы применяются как средства профилактики, предупреждения болезней. Ведь, за исключением травм и инфекций, болезнь никогда не возникает внезапно. Зачастую развитие заболевания являет собой длительный процесс, на протяжении которого организм пытается бороться с патологическими изменениями… Если в это время прибегнуть к БАДам, возможно, удастся восстановить нормальную работу органов еще до того, как нарушения станут очевидны.
Ведь, за исключением травм и инфекций, болезнь никогда не возникает внезапно. Зачастую развитие заболевания являет собой длительный процесс, на протяжении которого организм пытается бороться с патологическими изменениями… Если в это время прибегнуть к БАДам, возможно, удастся восстановить нормальную работу органов еще до того, как нарушения станут очевидны.
— Вызывают ли пищевые добавки привыкание?
— Физиологического привыкания не вызывают. Но есть люди, «зацикленные» на приеме различных витаминов, добавок и лекарств. На самом деле в состав добавок входят вещества, которые должны присутствовать в нашем ежедневном рационе. Но мало кто из нас умеет питаться рационально. Вот и бежим покупать БАДы!
— Могут ли добавки заменить обычное питание? Как правильно их применять?
— БАДы являются именно добавками к пище, а не ее заменителями. С их помощью организм адаптируется к воздействию различных внешних и внутренних факторов. Биодобавки и витаминно-минеральные комплексы рекомендуется принимать регулярно в осенно-зимне-весенний период, когда организм ослаблен непогодой и гиповитоминозами. Кроме того, они могут оказать незаменимую помощь в восстановлении после стрессов и физических нагрузок.
Кроме того, они могут оказать незаменимую помощь в восстановлении после стрессов и физических нагрузок.
— А что входит в их состав?
— БАДы включают в себя компоненты животного, растительного и минерального происхождения. В их состав могут входить как природные ингредиенты, так и соединения, полученные биотехнологическими или химическими методами. Могу с уверенностью сказать, что генетически модифицированные продукты при производстве биологически активных добавок не используются. В России утвержден и действует список из 190 разрешенных компонентов. Есть и перечень запрещенных: это, во-первых, сильнодействующие психотропные и ядовитые вещества, а также вещества, не являющиеся аналогами элементов нашего пищевого рациона, неприродные синтетические продукты, гормоны и ряд других…
— Есть ли у БАДов противопоказания, и в каких случаях необходимо посоветоваться с врачом, прежде чем их принимать?
— Предупреждения о возможных противопоказаниях потребитель может прочитать на этикетке к препарату. В России БАДы обязательно проходят государственную регистрацию. Но за консультацией к врачу не мешает обратиться, если вы беременны, кормите грудью, а также, если препарат предназначается для ребенка. Стоит помнить и о том, что у разных людей организм может по-разному реагировать на те или иные продукты и препараты, даже, на первый взгляд, безвредные. Поэтому совет грамотного специалиста никогда не помешает.
В России БАДы обязательно проходят государственную регистрацию. Но за консультацией к врачу не мешает обратиться, если вы беременны, кормите грудью, а также, если препарат предназначается для ребенка. Стоит помнить и о том, что у разных людей организм может по-разному реагировать на те или иные продукты и препараты, даже, на первый взгляд, безвредные. Поэтому совет грамотного специалиста никогда не помешает.
РОДИТЕЛЯМ ОБ АНТИБИОТИКАХ
Вторую половину ХХ века можно смело назвать антибактериальной эрой, и это не будет преувеличением: число жизней, спасенных с помощью антибиотиков, давно перешагнуло за миллиард! Об их чудотворной силе ходят легенды, но и хулы в их адрес приходится слышать не меньше. Виной тому поверхностное знание, провоцирующее неоправданные ожидания, а стало быть — и многочисленные обвинения антибиотиков в бедах, за которые они на самом деле ответственности вовсе не несут.
А хуже всего то, что антибиотики применяют гораздо чаще, чем это необходимо, нанося тем самым серьезнейший вред не только больным, но и обществу в целом. Я далек от мысли научить родителей самостоятельно использовать антибиотики — это дело врача. Но я убежден, что понимать логику назначения врача современные родители не только могут, но и обязаны.
Я далек от мысли научить родителей самостоятельно использовать антибиотики — это дело врача. Но я убежден, что понимать логику назначения врача современные родители не только могут, но и обязаны.
О ПОЛЬЗЕ ГРЯЗНОЙ ПОСУДЫ
Слово «антибиотик» образовано из двух элементов греческого происхождения: anti- – «против» и bios — «жизнь». Антибиотиками называют образуемые микроорганизмами, высшими растениями или тканями животных организмов вещества, избирательно подавляющие развитие микроорганизмов (или клеток злокачественных опухолей).
Любопытна история открытия первого антибиотика — пенициллина — шотландским бактериологом Александером Флемингом в 1829 г.: будучи по природе человеком неряшливым, он очень не любил… мыть чашки с бактериологическими культурами. Каждые 2—3 недели на его рабочем столе вырастала целая груда грязных чашек, и он скрепя сердце приступал к очистке «авгиевых конюшен». Одна из таких акций дала неожиданный результат, масштаб последствий которого сам ученый оценить в тот момент не мог. В одной из чашек обнаружилась плесень, подавляющая рост высеянной культуры болезнетворной бактерии группы staphylococcus. Кроме того, «бульон», на котором разрослась плесень, приобрел отчетливо выраженные бактерицидные свойства по отношению ко многим распространенным патогенным бактериям. Плесень, которой была заражена культура, относилась к виду penicillium.
В одной из чашек обнаружилась плесень, подавляющая рост высеянной культуры болезнетворной бактерии группы staphylococcus. Кроме того, «бульон», на котором разрослась плесень, приобрел отчетливо выраженные бактерицидные свойства по отношению ко многим распространенным патогенным бактериям. Плесень, которой была заражена культура, относилась к виду penicillium.
В очищенном виде пенициллин был получен лишь в 1940 г., т. е. спустя 11 лет после его открытия, в Великобритании. Сказать, что это произвело революцию в медицине, — значит не сказать ничего. Но у любой медали, увы, две стороны…
ОБОРОТНАЯ СТОРОНА МЕДАЛИ
Открыв столь мощное оружие в борьбе с болезнетворными микроорганизмами, человечество впало в эйфорию: к чему долго и кропотливо подбирать лекарственную терапию, если можно «шарахнуть» по зловредным микробам антибиотиком? Но и микробы «не лыком шиты» — они весьма эффективно защищаются от грозного оружия, вырабатывая устойчивость к нему. Если антибиотик, скажем, блокирует синтез необходимых микробу белков — микроб в ответ на это просто… меняет белок, обеспечивающий его жизнедеятельность. Некоторые микроорганизмы ухитряются научиться выработке ферментов, разрушающих сам антибиотик. Короче говоря, способов множество, и «хитроумные» микробы ни одним из них не пренебрегают. Но самое печальное заключается в том, что устойчивость микробов может передаваться от одного вида другому путем межвидового скрещивания! Чем чаще применяется антибиотик, тем быстрее и успешнее микробы приспосабливаются к нему. Возникает, как вы понимаете, порочный круг — чтобы разорвать его, ученые вынуждены вступить в навязанную микробами «гонку вооружений», создавая все новые и новые виды антибиотиков.
Некоторые микроорганизмы ухитряются научиться выработке ферментов, разрушающих сам антибиотик. Короче говоря, способов множество, и «хитроумные» микробы ни одним из них не пренебрегают. Но самое печальное заключается в том, что устойчивость микробов может передаваться от одного вида другому путем межвидового скрещивания! Чем чаще применяется антибиотик, тем быстрее и успешнее микробы приспосабливаются к нему. Возникает, как вы понимаете, порочный круг — чтобы разорвать его, ученые вынуждены вступить в навязанную микробами «гонку вооружений», создавая все новые и новые виды антибиотиков.
НОВОЕ ПОКОЛЕНИЕ ВЫБИРАЕТ…
К настоящему времени создано более 200 противомикробных препаратов, из них более 150 используются для лечения детей. Их мудреные названия нередко ставят в тупик людей, не имеющих отношения к медицине. Как же разобраться в обилии замысловатых терминов? На помощь, как всегда, приходит классификация. Все антибиотики делятся на группы — в зависимости от способа воздействия на микроорганизмы.
Пенициллины и цефалоспорины разрушают оболочку бактериальной клетки.
Аминогликозиды, макролиды, левомицетин, рифампицин и линкомицин убивают бактерии, подавляя синтез разных ферментов — каждый своего.
Фторхинолоны уничтожают микроорганизмы более «изощренно»: подавляемый ими фермент отвечает за размножение микробов.
В непрекращающемся состязании с микробами ученым приходится придумывать все новые и новые методы борьбы — каждый из них дает начало новому поколению соответствующей группы антибиотиков.
Теперь о названиях. Увы, здесь царит изрядная неразбериха. Дело в том, что помимо основных международных (так называемых генерических) названий многие антибиотики имеют и фирменные, запатентованные тем или иным конкретным производителем (в России их более 600). Так, например, один и тот же препарат может называться амоксициллином, Оспамоксом и Флемоксин Солютабом. Как же разобраться? По закону наряду с патентованным фирменным названием на упаковке лекарства обязательно указывается и его генерическое название — мелким шрифтом, нередко по-латыни (в данном случае — amoxycillinum).
При назначении антибиотика часто говорят о препаратепервого выбора и резервных препаратах. Препарат первого выбора — это тот препарат, назначение которого определяется диагнозом — если у больного нет устойчивости или аллергии к этому лекарственному средству. В последнем случае обычно назначаются резервные препараты.
ЧЕГО ЖДАТЬ И ЧЕГО НЕ ЖДАТЬ ОТ АНТИБИОТИКОВ?
Антибиотики способны излечить заболевание, вызванное бактериями, грибками и простейшими, но не вирусами. Именно поэтому бесполезно ожидать эффекта от антибиотика, назначенного при ОРВИ, точнее, эффект в таких случаях бывает негативным: температура держится несмотря на прием антибиотика — вот вам и «питательная среда» для распространения молвы о якобы потерянной эффективности антибиотиков или же о повальной устойчивости микробов.
Назначение антибиотика при вирусной инфекции не предотвращает бактериальных осложнений. Напротив, подавляя рост чувствительных к препарату микробов, например обитающих в дыхательных путях, антибиотик облегчает заселение дыхательных путей устойчивыми к нему патогенными бактериями, легко вызывающими осложнение.
Антибиотики не подавляют воспалительного процесса, обусловливающего подъем температуры, так что «сбить температуру» через полчаса, как парацетамол, антибиотик не может. При приеме антибиотика падение температуры наступает лишь через несколько часов или даже через 1—3 дня. Именно поэтому нельзя давать одновременно антибиотик и жаропонижающее: падение температуры от парацетамола может замаскировать отсутствие эффекта от антибиотика, а при отсутствии эффекта антибиотик, естественно, необходимо как можно скорее сменить.
Однако сохранение температуры нельзя считать признаком, однозначно свидетельствующим о неэффективности принимаемого антибиотика: порой выраженная воспалительная реакция, образование гноя требуют дополнительного к антибактериальному лечения (назначения противовоспалительных средств, вскрытия гнойника).
ВЫБОР ЗА ВРАЧОМ
Для лечения заболеваний, вызываемых чувствительными к антибиотикам микробами, обычно используются препараты первого выбора. Так, ангину, отит, пневмонию лечат амоксициллином или оспеном, микоплазменную инфекцию или хламидиоз эритромицином или другим антибиотиком из группы макролидов.
Возбудители кишечных инфекций зачастую быстро вырабатывают устойчивость к антибиотикам, поэтому при лечении кишечных инфекций антибиотики применяются лишь в тяжелых случаях — обычно цефалоспорины 2—3-го поколений или хинолоны.
Инфекции мочевых путей вызываются представителями кишечной флоры, их лечат амоксициллином или, при устойчивости возбудителей, резервными препаратами.
Как долго принимают антибиотик? При большинстве острых болезней его дают в течение 2—3 дней после падения температуры, однако есть много исключений. Так, отит обычно лечат амоксициллином не более 7—10 дней, а ангину — не менее 10 дней, иначе может быть рецидив.
ТАБЛЕТКИ, СИРОПЫ, МАЗИ, КАПЛИ…
Для детей особенно удобны препараты в детских формах. Так, препарат амоксициллина Флемоксин Солютаб выпускается в растворимых таблетках, их легко дать с молоком или чаем. Многие препараты, такие как джосамицин (Вильпрафен), азитромицин (Сумамед), цефуроксим (Зиннат), амоксициллин (Оспамокс) и др., выпускаются в сиропе или в гранулах для его приготовления.
Есть несколько форм антибиотиков для наружного применения — левомицетиновая, гентамициновая, эритромициновая мази, тобрамициновые глазные капли и др.
ОПАСНЫЕ ДРУЗЬЯ
Опасности, связанные с приемом антибиотиков, часто преувеличивают, но помнить о них необходимо всегда.
Поскольку антибиотики подавляют нормальную флору организма, они могут вызывать дисбактериоз, т. е. размножение бактерий или грибов, не свойственных тому или иному органу, прежде всего кишечнику. Однако лишь в редких случаях такой дисбактериоз опасен: при недлительном (1—3 недели) лечении антибиотиками проявления дисбактериоза фиксируются крайне редко, к тому же пенициллин, макролиды, цефалоспорины 1-го поколения не подавляют роста флоры кишечника. Так что противогрибковые (нистатин) и бактериальные (Бифидумбактерин, Лактобактерин) препараты применяются для предупреждения дисбактериоза лишь в случаях длительного лечения несколькими лекарственными препаратами широкого антибактериального спектра.
Термином «дисбактериоз», однако, в последнее время стали злоупотреблять — ставят его в качестве диагноза, списывая на него чуть ли не любые нарушения функционирования желудочно-кишечного тракта. Есть ли вред от такого злоупотребления? Да, поскольку это мешает постановке правильного диагноза. Так, например, у многих детей с пищевой непереносимостью диагностируют дисбактериоз, а потом «лечат» Бифидумбактерином, обычно без успеха. Да и стоят анализы кала на дисбактериоз немало.
Есть ли вред от такого злоупотребления? Да, поскольку это мешает постановке правильного диагноза. Так, например, у многих детей с пищевой непереносимостью диагностируют дисбактериоз, а потом «лечат» Бифидумбактерином, обычно без успеха. Да и стоят анализы кала на дисбактериоз немало.
Еще одна опасность, подстерегающая при приеме антибиотиков, — аллергия. У некоторых людей (в том числе и у грудных детей) имеется аллергия к пенициллинам и другим препаратам-антибиотикам: сыпи, шоковые реакции (последние, к счастью, встречаются очень редко). Если у вашего ребенка уже наблюдалась реакция на тот или иной антибиотик, об этом надо обязательно сообщить врачу, и он легко подберет замену. Особенно часты аллергические реакции в тех случаях, когда антибиотик дают больному, страдающему заболеванием небактериальной природы: дело в том, что многие бактериальные инфекции как бы снижают «аллергическую готовность» больного, что уменьшает риск реакции на антибиотик.
Аминогликозиды могут вызывать поражение почек и глухоту, их без большой надобности их не применяют. Тетрациклины окрашивают эмаль растущих зубов, их дают детям только после 8 лет. Препараты фторхинолонов детям не назначают из-за опасности нарушения роста, их дают лишь по жизненным показаниям.
Тетрациклины окрашивают эмаль растущих зубов, их дают детям только после 8 лет. Препараты фторхинолонов детям не назначают из-за опасности нарушения роста, их дают лишь по жизненным показаниям.
Принимая во внимание все вышеперечисленные «факторы риска», врач обязательно оценивает вероятность осложнений и применяет препарат только тогда, когда отказ от лечения сопряжен с большой степенью риска.
В заключение остается лишь сказать несколько слов об экономических аспектах назначения антибиотиков. Новые антибиотики стоят очень дорого. Спору нет, бывают ситуации, когда их применение необходимо, однако я часто сталкиваюсь со случаями, когда эти препараты назначаются без надобности, при заболеваниях, которые можно легко вылечить дешевыми лекарствами «старого образца». Я согласен с тем, что не следует скупиться, если речь идет о лечении ребенка. Но траты должны быть разумными! (Можно, например, купить антибиотик в форме сиропа: сиропы довольно дороги, но дети их принимают охотно, да и дозировать сироп или капли очень удобно. ) Однако это не означает, что при выборе препарата вовсе не следует принимать во внимание финансовую сторону дела. Не надо стесняться спросить у врача, во что обойдется вам выписанный рецепт, и если он вас не устраивает (слишком дорог или слишком дешев — это тоже нередко настораживает родителей), поищите вместе с врачом удовлетворяющую вас замену. Хочу еще раз повторить: десятки препаратов, имеющиеся сегодня в аптеках, почти всегда позволяют найти эффективное лекарство, соответствующее вашим возможностям.
) Однако это не означает, что при выборе препарата вовсе не следует принимать во внимание финансовую сторону дела. Не надо стесняться спросить у врача, во что обойдется вам выписанный рецепт, и если он вас не устраивает (слишком дорог или слишком дешев — это тоже нередко настораживает родителей), поищите вместе с врачом удовлетворяющую вас замену. Хочу еще раз повторить: десятки препаратов, имеющиеся сегодня в аптеках, почти всегда позволяют найти эффективное лекарство, соответствующее вашим возможностям.
ДИСБАКТЕРИОЗ — АКТУАЛЬНОСТЬ ПРОБЛЕМЫ
Проблема сохранения здоровья, поиск путей снижения неблагоприятного воздействия на организм внешней среды являются в настоящее время крайне актуальными для нашей страны. По данным Российской академии наук, более 90% населения Российской Федерации в настоящее время имеют отклонения от физиологической нормы по тем или иным показателям, характеризующим здоровье человека.
Техногенные и экологические катастрофы, инфекционные болезни, экспансия некачественных лекарственных средств и продуктов питания, самоотравление алкоголем и наркотиками, психоэмоциональное напряжение и множество других вредоносных факторов истощают защитные силы организма, снижают его адаптационный потенциал.
Одной из важнейших систем поддержания и сохранения гомеостаза организма является его нормальная микрофлора, населяющая желудочно-кишечный тракт, мочеполовую систему, кожные покровы. Она оказывает многоплановое влияние на защитные, адаптационные и обменно-трофические механизмы организма, а ее нарушения под влиянием факторов эндогенной или экзогенной природы могут привести к утрате или искажению этих функций, которые влекут за собой проявления дисбактериоза — изменения качественного и количественного состава микрофлоры организма. Спектр клинических синдромов и патологических состояний, патогенез которых связан с дисбактериозом, в настоящее время очень широк и имеет тенденцию к увеличению.
Это возводит проблему разработки средств, повышающих адаптационный потенциал организма человека, в ранг первостепенных задач не только медицинского, но и экономического и политического характера.
В настоящее время одним из наиболее доступных и эффективных способов экологической реабилитации являются пробиотики — продукты, биологически активные добавки и фармацевтические препараты на основе полезных микроорганизмов, прежде всего, бифидобактерий и лактобацилл, оказывающих многофакторное регулирующее и стимулирующее воздействиие на организм человека, укрепляющих иммунную систему, защищающих от болезнетворных микробов. И не случайно, согласно данным российских маркетологов, занятых анализом объемов потребления фармпрепаратов и БАД, начиная с 2000 года только два сегмента этого рынка имеют тенденцию к росту — антиканцерогенные и пробиотические препараты. Им принадлежит ведущая роль в нормализации микробиоценоза кишечника, поддержании неспецифической резистентности организма, улучшении процессов всасывания и гидролиза жиров, белкового и минерального обмена, синтезе биологически активных веществ.
И не случайно, согласно данным российских маркетологов, занятых анализом объемов потребления фармпрепаратов и БАД, начиная с 2000 года только два сегмента этого рынка имеют тенденцию к росту — антиканцерогенные и пробиотические препараты. Им принадлежит ведущая роль в нормализации микробиоценоза кишечника, поддержании неспецифической резистентности организма, улучшении процессов всасывания и гидролиза жиров, белкового и минерального обмена, синтезе биологически активных веществ.
Представители нормофлоры синтезируют витамины группы В, никотиновую кислоту, биотин, витамин К. Большая роль принадлежит им в защите организма от токсических элементов экзогенного происхождения и эндогенных субстратов и метаболитов. Они принимают активное участие в метаболизации разнообразных веществ растительного, животного и микробного происхождения, рециркуляции желчных кислот, активно влияют на метаболизм билирубина и холестерина. Установлена их антиканцерогенная и антимутагенная активность. Известна способность инактивировать гистамин, играющий важную роль в проявлении аллергии.
Все эти положительные эффекты позволяют рассматривать представителей нормальной микрофлоры как эффективный биокорректор и основу для создания различных форм пробиотиков.
По материалам сайта www.disbakterioza.net
Влияние антибиотиков на микробиом кишечника
Хидайя Алиуш, бакалавр наук
Введение
Что такое микробиом кишечника?
Функциональное влияние антибиотиков на кишечник
Антибиотики изменяют баланс микробных видов
Влияние антибиотиков на микробиоту кишечника до и после рождения
Иммуномодулирующее действие антибиотиков на микробиоту кишечника
Ссылки
количество полученных видов микробиоты. В целом антибиотики снижают разнообразие видов и включают потерю ключевых функциональных таксонов, что приводит к сдвигам в метаболизме, повышению восприимчивости кишечника к колонизации и стимуляции устойчивости бактерий к антибиотикам.
Терапевтическое или профилактическое применение противомикробных препаратов на микробиоту желудочно-кишечного тракта вызывает нарушение микробного равновесия. Степень этих изменений, наряду с отсутствием равновесия в экологии микробиоты, зависит от природы и фармакокинетического профиля препарата.
Степень этих изменений, наряду с отсутствием равновесия в экологии микробиоты, зависит от природы и фармакокинетического профиля препарата.
Изображение предоставлено: Fahroni/Shutterstock.com
Что такое микробиом кишечника?
Микробиота представляет собой совокупность микроорганизмов, присутствующих в определенной среде. Термин микробиом относится к окружающей среде, включая совокупность всех микроорганизмов (бактерий, эукариот, архей и вирусов) и их геномов, а также условия окружающей среды, присутствующие в окружающей среде. Совокупность бактерий, архей, эукариот и вирусов, присутствующих в желудочно-кишечном тракте человека, в совокупности называется микробиотой кишечника человека.
Функциональное влияние антибиотиков на кишечник
Существует обратная связь между использованием антибиотиков и микробным разнообразием. Более того, способ доставки антибиотиков оказывает разное действие.
После антибактериального лечения восстановление разнообразия занимает ~1 месяц; у взрослых для восстановления требуется ~1,5 месяца.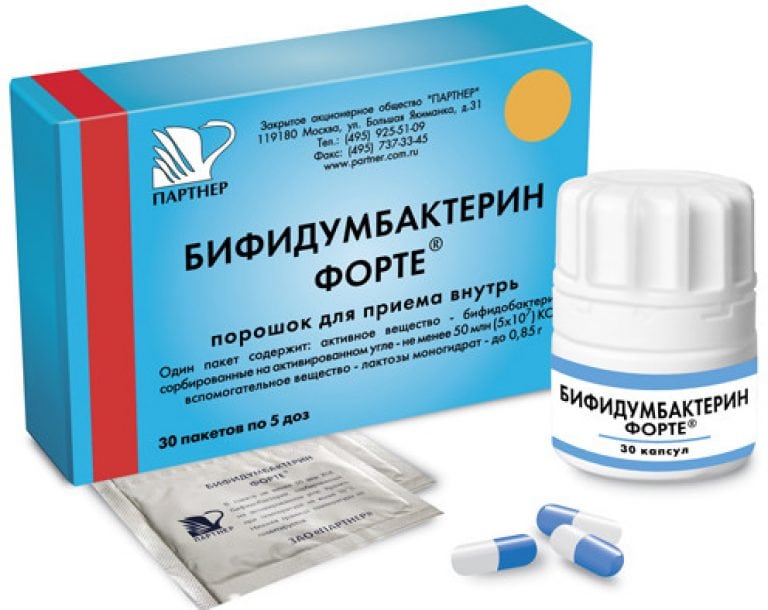 У взрослых назначение комбинации нескольких различных типов антибиотиков (меропенем, гентамицин и ванкомицин) может увеличить распространенность определенных видов энтеробактерий наряду с другими патобионтами с сопутствующим снижением количества видов, продуцирующих бутират.
У взрослых назначение комбинации нескольких различных типов антибиотиков (меропенем, гентамицин и ванкомицин) может увеличить распространенность определенных видов энтеробактерий наряду с другими патобионтами с сопутствующим снижением количества видов, продуцирующих бутират.
Антибиотики изменяют баланс микробных видов
Антибиотики являются дестабилизирующими агентами, нарушающими баланс микробных видов кишечника. Это нарушение баланса проявляется в уменьшении видового разнообразия с сопутствующим избыточным ростом патогенных видов, известных как патобионты, таких как C. difficile.
Лечение антибиотиками успешно устраняет чувствительные к антибиотикам виды. Однако устойчивые к антибиотикам бактерии обычно размножаются и занимают их место. Было отмечено, что общая микробная нагрузка увеличивается после лечения антибиотиками, несмотря на уменьшение видового разнообразия. В исследовании пациентов, получавших антибиотики широкого спектра действия, микробная нагрузка в образцах фекалий увеличилась в два раза в течение семи дней после лечения B-лактамами с повышенным соотношением Bacteroidetes и Firmicute.
Кроме того, метаболизм лекарств происходит в кишечнике благодаря наличию большого количества ферментов цитохрома Р450 (CYP). Эти ферменты CYP ответственны за выбор катализаторов первой и второй фазы реакций метаболизма лекарств. В ответ на пероральную антибактериальную терапию с использованием макролидов происходят сдвиги в кишечной микробиоте, особенно в отношении относительного содержания бактероидов и бифидобактерий. Как указывалось ранее, это создает нишу, которая обеспечивает рост C. difficile.
Аналогичным образом чрезмерное использование антибиотиков может негативно повлиять как на пролиферацию, так и на апоптоз кишечных клеток, от энтероцитов до эндокринных клеток. Это приводит к высвобождению внутриклеточных белков, полезных маркеров дисрегуляции микробиома кишечника. В исследовании микробиоты кишечника 1135 участников исследователи обнаружили связь между микробиомом и различными факторами хозяина; в частности, фекальный хромогранин А был связан с присутствием определенного вида микробов.
В исследовании, проведенном в Финляндии, детей в возрасте от двух до семи лет лечили макролидами, классом антибиотиков, который включает эритромицин, рокситромицин, азитромицин и кларитромицин. Это лечение было связано со сдвигом в составе кишечной флоры, который сохранялся в течение длительного времени. Этот сдвиг привел к сдвигу в метаболизме кишечника человека; это было отмечено, когда детей, получавших лечение макролидами, сравнивали с группой, не получавшей антибиотиков.
Среди детей, не подвергавшихся воздействию антибиотиков, наблюдалось обилие Collinsella, Lactobacillus и Anaaerostipes; эти популяции были ниже у тех, кто лечился антибиотиками. Другие изменения, наблюдаемые в микробных популяциях, включают сокращение разнообразия и зрелости микробиоты в течение двух лет. Более того, некоторые популяции восстанавливались быстрее, чем другие, при этом Bacteroides и Bifidobacterium восстанавливались до состояния, предшествующего антибиотикам, в течение года после введения макролидов.
Интересно, что у детей, получавших антибиотики, чаще возникали бактериальные инфекции по сравнению с теми, кто этого не делал; это связано с взаимозависимостью взаимосвязи микробов в кишечнике; удаление большого количества бактерий приводит к общему снижению функции комменсальных бактерий.
Изображение предоставлено: Anatomy Image/Shutterstock.com
Влияние антибиотиков на микробиоту кишечника до и после рождения
В настоящее время недостаточно изучена передача устойчивых к антибиотикам штаммов от матери к ребенку. Однако известно, что на программирование иммунной системы сильно влияют бактерии, которые первыми колонизируют кишечник. Эта форма колонизации называется вертикальной передачей. Вертикальный механизм переноса антибиотикорезистентных штаммов происходит как во время плацентарных, так и вагинальных родов, через грудное молоко и перенос антибиотиков внутриутробно.
Воздействие антибиотиков на когорту новорожденных из 12 422 человек показало увеличение роста и веса у мальчиков с более высоким индексом массы тела. У обоих полов наблюдалось снижение разнообразия фекальных бифидобактерий. Последующее исследование с использованием модельных экспериментов на мышах, в которых фекальная микробная передача от детей, подвергшихся воздействию антибиотиков, влияла на рост. Это было связано с уменьшением таламокортикальных аксонов, плохим ростом таламических аксонов и таламокортикогенезом — это продемонстрировало, что воздействие материнских антибиотиков на новорожденных может неблагоприятно повлиять на развитие нервной системы плода.
У обоих полов наблюдалось снижение разнообразия фекальных бифидобактерий. Последующее исследование с использованием модельных экспериментов на мышах, в которых фекальная микробная передача от детей, подвергшихся воздействию антибиотиков, влияла на рост. Это было связано с уменьшением таламокортикальных аксонов, плохим ростом таламических аксонов и таламокортикогенезом — это продемонстрировало, что воздействие материнских антибиотиков на новорожденных может неблагоприятно повлиять на развитие нервной системы плода.
Аллергическое воспаление легких у потомства также тесно связано с пренатальным воздействием антибиотиков. Обнаружено, что индуцированная анафилаксия является обычным явлением в развитии иммунной системы новорожденных в результате воздействия ампициллина широкого спектра действия. В этих случаях возникает дефицит Т-регуляторных клеток (в частности, регуляторных Т-клеток толстой кишки), поскольку иммунная система не может генерировать CD4+ Т-клетки. Таким образом, возникают нерегулируемые ответы Th2.
Иммуномодулирующее действие антибиотиков на микробиоту кишечника
Существует двунаправленная связь между кишечным микробиомом и антибиотиками. Наряду с прямыми эффектами антибиотики могут оказывать косвенное действие.
Вследствие дисбактериоза кишечной микробиоты (нарушение гомеостаза микробиоты, вызванное дисбалансом между типами организмов) и дисрегуляции иммунная система нарушается. Исследования как in vitro, так и ex vivo показали, что краткосрочное лечение антибиотиками широкого спектра действия может влиять на гуморальный и клеточный иммунный ответ.
Кроме того, некоторые антибиотики обладают иммуномодулирующим действием, а также противомикробной активностью. Например, исследование показало, что макролиды, такие как кларитромицин, могут индуцировать in vitro и in vivo нейтрофильные внеклеточные ловушки (НЭО). Сети представляют собой сети внеклеточных волокон, в основном состоящие из ДНК нейтрофилов, которые связывают патогены.
Это одна из трех основных стратегий борьбы с микробами; другие включают фагоцитоз и дегрануляцию. NETS также «украшены» функциональным антимикробным пептидом LL-37. IL-37 может ингибировать рост штаммов с множественной лекарственной устойчивостью и защищать баланс микробиоты толстой кишки. Это открытие иллюстрирует двунаправленный эффект антибиотиков и микробиоты, которую также может определять индуцируемый гипоксией фактор-1α (HIF-1α), фактор транскрипции, необходимый для активации эффекторов врожденного иммунитета, таких как кателицидин IL-37 человека.0020 Candida albicans колонизационная резистентность.
NETS также «украшены» функциональным антимикробным пептидом LL-37. IL-37 может ингибировать рост штаммов с множественной лекарственной устойчивостью и защищать баланс микробиоты толстой кишки. Это открытие иллюстрирует двунаправленный эффект антибиотиков и микробиоты, которую также может определять индуцируемый гипоксией фактор-1α (HIF-1α), фактор транскрипции, необходимый для активации эффекторов врожденного иммунитета, таких как кателицидин IL-37 человека.0020 Candida albicans колонизационная резистентность.
Этот интерлейкин также влияет на заживление ран и активацию нескольких иммунорегулируемых генов. Т-клетки также реагируют на стимуляцию IL-37 из-за пролиферации Т-клеток, активации и образования регуляторных Т-клеток.
Влияние антибиотиков на разнообразие кишечных бактерий и длительное злоупотребление ими также было определено как фактор риска развития метаболических нарушений. В экспериментальной модели на животных наблюдалась корреляция между потерей разнообразия кишечного микробиома, вызванной антибиотиками, и усилением атеросклероза. В частности, это было вызвано сокращением Bacteroidetes и Clostridia.
В частности, это было вызвано сокращением Bacteroidetes и Clostridia.
Микробиота кишечника представляет собой сложное сообщество, организованное вокруг стартовых сетей метаболических взаимозависимостей. Хорошо зарекомендовавшие себя исследования показывают, что микробиота кишечника жизненно важна для нормального развития и функционирования человеческого организма. Он особенно функционален при созревании адаптивной иммунной системы. Антибиотики могут привести к ряду негативных последствий для кишечной микробиоты, от уменьшения разнообразия видов, изменения метаболической активности и отбора устойчивых к антибиотикам организмов, что приводит к последующим последствиям, таким как антибиотикоассоциированная диарея и рецидивирующие инфекции C. difficile.
Имеются также данные о том, что раннее воздействие антибиотиков может повлиять на желудочно-кишечные, иммунологические и нейрокогнитивные системы. Это проблематично из-за более широкого использования антибиотиков, что предполагает будущее увеличение распространенности острых состояний. Чтобы решить эту проблему, необходимо продолжать исследования состава и функции кишечной микробиоты.
Чтобы решить эту проблему, необходимо продолжать исследования состава и функции кишечной микробиоты.
Изображение предоставлено: Катерина Кон/Shutterstock.com
Ссылки:
- Константинидис Т., Цигалу С., Карвелас А. и др. (2020) Влияние антибиотиков на микробиом кишечника: обзор литературы. Биомедицины. doi: 10.3390/биомедицины8110502.
- Рамирес Дж., Гарнер Ф., Бустос Фернандес Л. и др. (2020) Антибиотики как основные разрушители кишечной микробиоты. Front Cell Infect Microbiol. doi: 10.3389/fcimb.2020.572912.
- Ян Л., Баджинка О., Джарджу П.О. и др. (2021) Различное влияние антибиотиков на микробиоту кишечника. АМБ Экспресс. doi: 10.1186/s13568-021-01274-w.
- Безирцоглу Э.Е.В. (2012)Кишечные цитохромы P450, регулирующие микробиоту кишечника и ее пробиотический профиль. микроб. Экол. Здоровье Дис. дои: 10.3402/mehd.v23i0.18370.
- Korpela K, de Vos WM (2016)Использование антибиотиков в детстве изменяет микробиоту кишечника и предрасполагает к избыточному весу.
 Микробная клетка. doi: 10.15698/mic2016.07.514.
Микробная клетка. doi: 10.15698/mic2016.07.514. - Аморозо С., Перилло Ф., Страти Ф. и др. (2020) Роль биомодуляторов микробиоты кишечника в иммунитете слизистой оболочки и воспалении кишечника. Клетки. Дои: 10.3390/ячейки9051234.
- Fan D, Coughlin LA, Neubauer MM, et al. (2015) Активация HIF-1α и LL-37 комменсальными бактериями ингибирует колонизацию Candida albicans. Нац. Мед. дои: 10.1038/nm.3871.
Дополнительная литература
- Все содержание антибиотиков
- Влияет ли то, что вы едите, на эффективность антибиотиков?
- Влияет ли длительный прием антибиотиков на костную массу?
- История антибиотиков
Воздействие антибиотиков, особенно фторхинолонов, до…
Результаты когортного исследования на уровне населения
В крупном популяционном исследовании воздействие антибиотиков и особенно фторхинолонов до лечения ингибитором контрольных точек иммунного ответа (ICI) было связано с ухудшением общей выживаемости (ОВ), при этом воздействие фторхинолонов повышало риск смертности до 65% среди пожилых людей с раком. Дозовые эффекты также наблюдались в зависимости от продолжительности и общих доз фторхинолонов. Последствия воздействия антибиотиков за 1 год до ICI могут повлиять на последующие результаты ICI, что указывает на то, что клиницисты должны учитывать предшествующее воздействие антибиотиков. Эта взаимосвязь наблюдалась среди пациентов, получавших анти-PD1-препараты, которые были наиболее часто назначаемыми ИКИ, а также среди пациентов с раком легкого и меланомой. Результаты опубликованы доктором Лоусоном Энгом из отделения медицинской онкологии и гематологии медицинского факультета Онкологического центра принцессы Маргарет Университетской сети здравоохранения в Торонто, Онтарио, Канада, и его коллег 24 февраля 2023 г.0020 Журнал клинической онкологии .
Дозовые эффекты также наблюдались в зависимости от продолжительности и общих доз фторхинолонов. Последствия воздействия антибиотиков за 1 год до ICI могут повлиять на последующие результаты ICI, что указывает на то, что клиницисты должны учитывать предшествующее воздействие антибиотиков. Эта взаимосвязь наблюдалась среди пациентов, получавших анти-PD1-препараты, которые были наиболее часто назначаемыми ИКИ, а также среди пациентов с раком легкого и меланомой. Результаты опубликованы доктором Лоусоном Энгом из отделения медицинской онкологии и гематологии медицинского факультета Онкологического центра принцессы Маргарет Университетской сети здравоохранения в Торонто, Онтарио, Канада, и его коллег 24 февраля 2023 г.0020 Журнал клинической онкологии .
Доклинические исследования показали, что разнообразие стула и определенные виды бактерий в кишечнике могут оказывать прямое влияние на эффективность ИКИ и побочные эффекты, связанные с иммунной системой. Поскольку воздействие антибиотиков может изменить микробиом кишечника, возник интерес к оценке влияния воздействия антибиотиков на результаты ИКИ. Предыдущие исследования, в том числе два систематических обзора и метаанализы, предполагают, что воздействие антибиотиков может негативно повлиять на результаты ИКИ, включая ОВ. Тем не менее, многие отдельные исследования, включенные в мета-анализ, были небольшими, с размером выборки менее 200, проведенными в одном центре, и характеризовались неоднородностью периода воздействия антибиотиков до ICI, класса ICI и типов опухолей.
Предыдущие исследования, в том числе два систематических обзора и метаанализы, предполагают, что воздействие антибиотиков может негативно повлиять на результаты ИКИ, включая ОВ. Тем не менее, многие отдельные исследования, включенные в мета-анализ, были небольшими, с размером выборки менее 200, проведенными в одном центре, и характеризовались неоднородностью периода воздействия антибиотиков до ICI, класса ICI и типов опухолей.
Оценка воздействия антибиотиков с использованием более крупной популяционной когорты в нескольких центрах может позволить провести оценку конкретных подгрупп на основе типа ICI и класса антибиотиков. Цели этого ретроспективного когортного исследования на уровне популяции состояли в том, чтобы оценить связь предшествующего воздействия антибиотиков с общей выживаемостью у пациентов, получавших первую ИКИ, и выявить любые конкретные ассоциации, основанные на препарате ИЦИ, типе опухоли или классе антибиотиков.
Пациенты с онкологическими заболеваниями в возрасте 65 лет и старше, начавшие лечение с помощью ИКИ в период с июня 2012 г. по октябрь 2018 г. в Онтарио, Канада, были выявлены с использованием данных о назначении системного лечения. Когорта была детерминистически связана с другими базами данных здравоохранения, чтобы получить ковариаты и данные о выписанных рецептах на антибиотики как за 1 год, так и за 60 дней до лечения ICI. Многофакторные модели Кокса оценивали связь между воздействием и ОВ.
по октябрь 2018 г. в Онтарио, Канада, были выявлены с использованием данных о назначении системного лечения. Когорта была детерминистически связана с другими базами данных здравоохранения, чтобы получить ковариаты и данные о выписанных рецептах на антибиотики как за 1 год, так и за 60 дней до лечения ICI. Многофакторные модели Кокса оценивали связь между воздействием и ОВ.
Среди 2737 больных раком, получавших ИКИ, 59% получали антибиотики за 1 год до лечения ИКИ и 19% получали антибиотики за 60 дней до ИКИ. Медиана ОС составила 306 дней. Любое воздействие антибиотиков в течение 1 года до ICI ассоциировалось с ухудшением ОВ (скорректированное отношение рисков [aHR] 1,12, 95% доверительный интервал [CI] 1,12–1,23; p = 0,03).
При анализе классов антибиотиков воздействие фторхинолонов в течение 1 года (aHR 1,26, 95% ДИ от 1,13 до 1,40; p < 0,001) или за 60 дней до ICI (aHR 1,20, 95% ДИ от 0,99 до 1,45; р = 0,06) ассоциировался с ухудшением ОВ, с эффектом дозы, наблюдаемым на основе общего количества недель воздействия в течение 1 года (сЧ 1,07 в неделю, 95% ДИ от 1,03 до 1,11; р <0,001) и 60 дней (сЧ 1,12 в неделю, 95% ДИ от 1,03 до 1,23; р = 0,01).
Эти результаты свидетельствуют о том, что клиницисты должны потенциально учитывать применение антибиотиков в прошлом году, когда пациенты начинают лечение с помощью ИКИ. Необходимы дополнительные данные для механистического изучения взаимосвязи между воздействием антибиотиков, лечением ИКИ и результатами выживаемости у различных пациентов и условий. Вмешательства, направленные на изменение микробиома кишечника для повышения иммуногенности, могут помочь улучшить результаты для пациентов, получающих ИКИ с предшествующим воздействием антибиотиков.
В сопроводительной редакционной статье Drs. Дэвид Дж. Пинато из отделения хирургии и рака медицинского факультета Имперского колледжа Лондона, больницы Хаммерсмит в Лондоне, Великобритания и отделения онкологии отделения трансляционной медицины Восточного университета Пьемонте в Новаре, Италия, и Алессио Кортеллини из отделения Хирургии и рака, медицинского факультета, Имперского колледжа Лондона, больницы Хаммерсмит в Лондоне, Великобритания, и медицинской онкологии, Fondazione Policlinico Universitario Campus BioMedico в Риме, Италия, написали, что теперь, когда ИКИ стали стандартным вариантом системного лечения первой линии для пациентов с рака, длительный латентный период между воздействием антибиотиков и лечением ИКИ, продолжающийся до года, делает это исследование особенно провокационным, поскольку предполагает, что опосредованное антибиотиками нарушение микробиома кишечника может предопределять противораковый иммунитет еще до клинической диагностики рака.
В связи с постоянно растущим объемом данных и пониманием механизмов, подтверждающих взаимосвязь между гомеостазом кишечника и исходами ICI, ключевая цель в настоящее время состоит в том, чтобы продемонстрировать, может ли реверсия опосредованного антибиотиками дисбактериоза кишечника быть полезным для отмены все более хорошо охарактеризованного механизма ICI. сопротивление. Возобновление энтузиазма в отношении терапевтического потенциала вмешательств на основе микробиоты было подтверждено новаторскими ранними клиническими испытаниями, изучающими переносимость и эффективность трансплантации фекальной микробиоты, полученной от доноров, реагирующих на иммунотерапию, в качестве механизма преодоления рефрактерности к ИКИ.
Дальнейшие исследования, направленные на характеристику механизмов, лежащих в основе терапевтической эффективности терапии, модулирующей микробиом, являются, пожалуй, самой большой проблемой, влияющей на их успешное и рациональное развитие в качестве вариантов лечения больных раком. Поскольку все большее число биотерапевтических подходов, включая пищевые добавки с пребиотиками, использование одного или нескольких бактериальных консорциумов, селективное лечение антибиотиками или фекальную микробную трансплантацию, соревнуются за то, чтобы доказать свою эффективность в качестве противоопухолевого лечения в клинике, это исследование поддерживает эти усилия, предоставляя достоверные доказательства долговременные вредные эффекты, возникающие из-за дисбиотической микросреды кишечника, сохраняют здоровье кишечника на первом месте в повестке дня исследований по разработке лекарств.
Поскольку все большее число биотерапевтических подходов, включая пищевые добавки с пребиотиками, использование одного или нескольких бактериальных консорциумов, селективное лечение антибиотиками или фекальную микробную трансплантацию, соревнуются за то, чтобы доказать свою эффективность в качестве противоопухолевого лечения в клинике, это исследование поддерживает эти усилия, предоставляя достоверные доказательства долговременные вредные эффекты, возникающие из-за дисбиотической микросреды кишечника, сохраняют здоровье кишечника на первом месте в повестке дня исследований по разработке лекарств.
Ранее исследование было частично представлено на Конгрессе ESMO 2021 в Париже, Франция (16–21 сентября), и на Симпозиуме качества ASCO 2021 в Бостоне, Массачусетс, США (24–25 сентября).
Исследование проводилось при поддержке Института клинических оценочных наук, который финансируется за счет ежегодного гранта Министерства здравоохранения Онтарио и Министерства долгосрочного ухода.
