Авторизация
Размер:
AAA
Цвет: C C C
Изображения Вкл. Выкл.
Обычная версия сайта
Сведения об образовательной организации Контакты Старая версия сайта Версия для слабовидящих Версия для слабовидящих
Южно-Уральский государственный медицинский университет
- Университет
- События
- Новости
- ЮУГМУ сегодня
- Историческая справка
- Руководство
- Выборы ректора
- Лицензия, аккредитация и сертификаты
- Организационная структура
- Противодействие коррупции
- Первичная профсоюзная организация ЮУГМУ Профсоюза работников здравоохранения РФ
- Абитуриенту
- Новости для абитуриентов
- Центр довузовской подготовки
- Поступающим на специалитет
- Поступающим в ординатуру
- Поступающим в медицинский колледж
- Документы на право ведения образовательной деятельности
- Положения о приемной, экзаменационной и апелляционной комиссиях
- Информация об общежитиях
- Часто задаваемые вопросы
- Результаты приема студентов
- Информация для инвалидов
- Обучающемуся
- Факультеты
- Кафедры
- Медицинский колледж
- Ординатура
- Аспирантура
- Научная библиотека
- Образовательный портал
- Расписание
- Совет обучающихся ЮУГМУ
- Этический кодекс студентов медицинских вузов
- О допуске студентов к работе в медицинских организациях
- Иностранным обучающимся
- Медицинское обслуживание
- Информация об общежитиях
- Стипендиальное обеспечение
- Порядок перехода обучающихся с платного на бесплатное обучение
- Часто задаваемые вопросы
- Студенческие отряды
- Противодействие терроризму и экстремизму
- Специалисту
- Институт дополнительного профессионального образования
- Аккредитация специалистов
- Пациенту
- Клиника ФГБОУ ВО ЮУГМУ Минздрава России
- Профилактика новой коронавирусной инфекции, гриппа, ОРВИ, вакцинация
- Здоровый образ жизни
- Научная работа
- Управление по научной и инновационной работе
- Экспериментально-биологическая клиника (виварий)
- Отдел международных связей
- НИИ иммунологии
- Центральная научно-исследовательская лаборатория
- НОЦ «Проблемы фундаментальной медицины»
- НОЦ «Клиническая фармакология»
- Диссертационные советы
- Журнал «Непрерывное медицинское образование и наука»
- Студенческое научное общество
- Совет молодых ученых и специалистов
Перед вакцинацией
Комплексное лабораторное обследование крови с определением IgE-антител к аллергенам куриного яйца, коровьего молока, дрожжам, желатина, а также уровня формальдегида методом ImmunoCAP в целях оценки возможного риска развития системных анафилактических реакций после введения вакцины.
Синонимы русские
Определение уровня формальдегида, IgE-антител к куриному яйцу и пекарским дрожжам.
Синонимы английские
Allergy testing before vaccination:
ImmunoCAP f245, Egg, IgE;
ImmunoCAP f45 (Yeast, Saccharomyces cerevisiae), IgE.
Метод исследования
Иммунофлюоресценция на твердой фазе (ImmunoCAP).
Единицы измерения
kU/l (килоединица на литр).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Плановая вакцинация населения по всему миру предотвращает миллионы смертей. Регулярный мониторинг безопасности вакцин подтвердил, что риск развития побочных реакций минимальный, а польза от их применения многократно превышает возможный вред. Однако, как и у любого медицинского препарата, у вакцин есть нежелательные явления. Наиболее частыми побочными эффектами от применения вакцин являются повышение температуры тела и болезненность в месте инъекции, которые возникают у 1 из 10 детей и проходят в течение 1-2 дней. Более серьезные осложнения в виде тяжелых анафилактических реакций возникают в 0,5-1 случае на 100000 доз вакцин.
Однако, как и у любого медицинского препарата, у вакцин есть нежелательные явления. Наиболее частыми побочными эффектами от применения вакцин являются повышение температуры тела и болезненность в месте инъекции, которые возникают у 1 из 10 детей и проходят в течение 1-2 дней. Более серьезные осложнения в виде тяжелых анафилактических реакций возникают в 0,5-1 случае на 100000 доз вакцин.
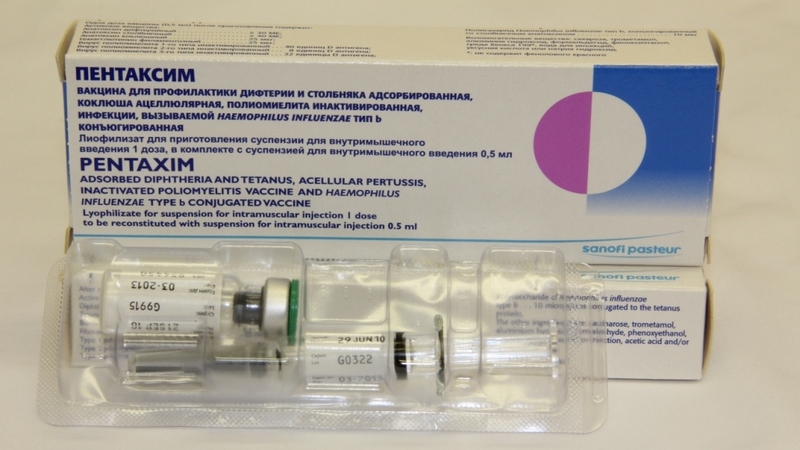
Аллергические реакции на вакцинные препараты обычно связаны не с самой вакциной, а с белковыми компонентами, оставшимися в составе в процессе производства. В состав вакцины входят активный иммунизирующий компонент, конъюгирующий компонент, консервант, адъювант, стабилизатор, антимикробный агент, следы питательной среды, применяемой для изготовления вакцин. Аллергическую реакцию может вызвать практически любой компонент. Среди возможных аллергенных белков в составе вакцин особое внимание уделяют белкам куриного яйца, желатину и дрожжам. Однако многие исследования показали безопасность введения даже вакцины от гриппа, содержащей следовые количества белка куриного яйца, сенсибилизированным лицам после грамотной медикаментозной подготовки.
Аллергия на вакцины чаще развивается по механизмам реакций немедленного I (IgE-опосредованного) и отсроченного (IV) типов, реже – II и III типов. Реакция I типа возникает в течение нескольких минут или в редких первых 4 часов после иммунизации. Наиболее частыми симптомами реакции немедленного типа являются крапивница и ангиоотеки, реже отек слизистой носа, кашель, бронхоспазм, боли в животе, диарея, снижение артериального давления, а в крайне редких, но особо тяжелых случаях возможен анафилактический шок. Реакции IV типа чаще связаны с тиомерсалом, алюминием или антимикробными веществами в составе вакцин и обычно не представляют угрозы здоровью.
Белки пекарских дрожжей (Saccharomyces cerevisiae) выявляются в составе вакцин от вирусов гепатита В и папиллома-вируса человека. Аллергические реакции на них крайне редки и могут быть подтверждены с помощью кожного тестирования или выявления специфических IgE-антител. Сенсибилизация к пекарским дрожжам не является противопоказанием для введения вакцин, однако у пациентов с гиперчувствительностью к 
Белки куриного яйца в следовых количествах присутствуют в вакцинах от кори, краснухи, паротита, гриппа, желтой лихорадки, вируса клещевого энцефалита. Несмотря на потенциальную опасность развития аллергических реакций, даже у пациентов с тяжелыми реакциями на белки куриного яйца вакцинация вышеперечисленными препаратами редко вызывает серьезные осложнения. Тем не менее при планировании иммунизации лиц, сенсибилизированных к белку куриного яйца, рекомендовано дробное введение вакцин, содержащих данный белок, и продолжительное наблюдение врача. В случаях отсутствия сенсибилизации вакцины вводятся по стандартной схеме, а пациент остается под наблюдением 30 минут после введения препарата.
Бычий сывороточный альбумин – термолабильный белок весом 67 кДа. Он является главным (мажорным) аллергеном говядины и второстепенным (минорным) аллергеном молока. Данный сывороточный альбумин составляет около 1 % всех белков коровьего молока и около 5 % от белков сыворотки. По физическим и иммунологическим свойствам он очень похож на человеческий сывороточный белок. Термическая обработка в домашних условиях снижает, но полностью не убирает аллергенные свойства данного белка.
Термическая обработка в домашних условиях снижает, но полностью не убирает аллергенные свойства данного белка.
Формальдегид является достаточно распространенным органическим веществом, хорошо известным как загрязнитель воздуха. В помещениях источником формальдегида могут быть испарения от пенополиуретана, древесностружечных плит, панелей, фанеры, некоторых ковровых покрытий и мебели, а также он содержится в табачном дыме и отработанных газах внутреннего сгорания. Также он используется в косметике, бытовой химии, бумажных изделиях, красочных покрытиях и др.
Реакция на формальдегид может зависеть от типа воздействия. Помимо сенсибилизирующего, он имеет первичное раздражающее действие, что следует различать в клинической практике. Пары формальдегида могут вызывать жжение в глазах, в носоглотке, дерматит и крапивницу, бронхоспазм, головные боли и резкое утомление.
Важные аспекты профилактики осложнений — врачебный осмотр перед вакцинацией, тщательный сбор аллергологического анамнеза, выявление противопоказаний, исключение возможных рисков развития побочных эффектов, правильная подготовка при наличии неблагоприятных факторов, а также возможность выполнения грамотных лечебных мероприятий при возникновении аллергических реакций немедленного типа. Поэтому при планировании иммунизации лиц с возможной или подтвержденной сенсибилизацией к некоторым компонентам вакцины необходимо дополнительное лабораторное обследование у аллерголога-иммунолога с решением вопросов о медикаментозной подготовке к вакцинации (например, антигистаминными препаратами), вакцинации в специализированных медицинских центрах, дробном введении вакцин и с тщательным наблюдением за пациентом в первые часы после иммунизации.
Поэтому при планировании иммунизации лиц с возможной или подтвержденной сенсибилизацией к некоторым компонентам вакцины необходимо дополнительное лабораторное обследование у аллерголога-иммунолога с решением вопросов о медикаментозной подготовке к вакцинации (например, антигистаминными препаратами), вакцинации в специализированных медицинских центрах, дробном введении вакцин и с тщательным наблюдением за пациентом в первые часы после иммунизации.
Для чего используется исследование?
- Для оценки возможного риска развития аллергических реакций на компоненты вакцин;
- для правильной подготовки к иммунизации пациентов с возможным развитием аллергических реакций.
Когда назначается исследование?
- Перед планируемой иммунизацией некоторыми вакцинами у лиц с отягощенным аллергологическим анамнезом;
- при наличии проявлений аллергических реакций после введения вакцин в анамнезе.
Что означают результаты?
Референсные значения
Для каждого показателя, входящего в состав комплекса:
- [21-689] Аллерген f45 — пекарские дрожжи, IgE (ImmunoCAP)
- [21-682] Аллергокомпонент f232 — овальбумин яйца nGal d2, IgE (ImmunoCAP)
- [21-837] Аллерген k80 — формальдегид / формалин, IgE (ImmunoCAP)
- [21-710] Аллергокомпонент f76 — альфа-лактальбумин nBos d 4, IgE (ImmunoCAP)
- [21-630] Аллергокомпонент f78 – казеин nBos d8, IgE (ImmunoCAP)
- [21-712] Аллергокомпонент e204 — бычий сывороточный альбумин nBos d6, IgE (ImmunoCAP)
- [21-781] Аллерген c74 — желатин коровий, IgE (ImmunoCAP)
Важные замечания
- Положительные результаты данных анализов не являются абсолютными противопоказаниями к вакцинации.
 Требуется дополнительная консультация врача-аллерголога-иммунолога.
Требуется дополнительная консультация врача-аллерголога-иммунолога.
Также рекомендуется
[02-029] Клинический анализ крови: общий анализ, лейкоцитарная формула, СОЭ (с микроскопией мазка крови при выявлении патологических изменений)
[08-017] Суммарные иммуноглобулины E (IgE) в сыворотке
[21-673] Аллергочип ImmunoCAP ISAC (112 аллергокомпонентов)
Кто назначает исследование?
Аллерголог, иммунолог, педиатр, терапевт, врач общей практики, инфекционист.
Литература
- Chung E. H. Vaccine allergies. Clin Exp Vaccine Res. 2014 Jan; 3(1): 50–57.
- Parente R, Pucino V, Magliacane D, Petraroli A, Loffredo S, Marone G, et al. Evaluation of vaccination safety in children with mastocytosis. Pediatr Allergy Immunol. 2017 Feb; 28(1):93–95.
- Schwartz LB. Diagnostic value of tryptase in anaphylaxis and mastocytosis. Immunol Allergy Clin North Am 2006;26:451-63.
- World Allergy Organization Anaphylaxis Guidelines: 2013 Update of the Evidence Base. Simons FE, Ardusso LR, Dimov V, Ebisawa M, El-Gamal YM, Lockey RF, Sanchez-Borges M, Senna GE, Sheikh A, Thong BY, Worm M; World Allergy Organization. Int Arch Allergy Immunol. 2013;162(3):193-204.
- Barclay L. Most Patients With Vaccine Allergy May Be Safely Vaccinate. Ann Allergy Asthma Immunol. 2009;103:S1-14.
Краткая история вакцинации
Краткая история вакцинации- All topics »
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- 5 Y
5
- З
- Ресурсы »
- Бюллетени
- Факты в картинках
- Мультимедиа
- Публикации
- Вопросы и Ответы
- Инструменты и наборы инструментов
- Популярный »
- Загрязнение воздуха
- Коронавирусная болезнь (COVID-19)
- Гепатит
- оспа обезьян
- Все страны »
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
43
- Африка
- Америка
- Юго-Восточная Азия
- Европа
- Восточное Средиземноморье
- Западная часть Тихого океана
- ВОЗ в странах »
- Статистика
- Стратегии сотрудничества
- Украина ЧП
- все новости »
- Выпуски новостей
- Заявления
- Кампании
- Комментарии
- События
- Тематические истории
- Выступления
- Прожекторы
- Информационные бюллетени
- Библиотека фотографий
- Список рассылки СМИ
- Заголовки »
- Сосредоточиться на »
- Афганистан кризис
- COVID-19 пандемия
- Кризис в Северной Эфиопии
- Сирийский кризис
- Украина ЧП
- Вспышка оспы обезьян
- Кризис Большого Африканского Рога
- Последний »
- Новости о вспышках болезней
- Советы путешественникам
- Отчеты о ситуации
- Еженедельный эпидемиологический отчет
- ВОЗ в чрезвычайных ситуациях »
- Наблюдение
- Исследовать
- Финансирование
- Партнеры
- Операции
- Независимый контрольно-консультативный комитет
- Призыв ВОЗ о чрезвычайной ситуации в области здравоохранения 2023 г.
- Данные ВОЗ »
- Глобальные оценки здоровья
- ЦУР в области здравоохранения
- База данных о смертности
- Сборы данных
- Панели инструментов »
- Информационная панель COVID-19
- Приборная панель «Три миллиарда»
- Монитор неравенства в отношении здоровья
- Основные моменты »
- Глобальная обсерватория здравоохранения
- СЧЕТ
- Инсайты и визуализации
- Инструменты сбора данных
- Отчеты »
- Мировая статистика здравоохранения 2022 г.
- избыточная смертность от COVID
- DDI В ФОКУСЕ: 2022 г.
- О ком »
- Люди
- Команды
- Состав
- Партнерство и сотрудничество
- Сотрудничающие центры
- Сети, комитеты и консультативные группы
- Трансформация
- Наша работа »
- Общая программа работы
- Академия ВОЗ
- Деятельность
- Инициативы
- Финансирование »
- Инвестиционный кейс
- Фонд ВОЗ
- Подотчетность »
- Аудит
- Программный бюджет
- Финансовые отчеты
- Портал программного бюджета
- Отчет о результатах
- Управление »
- Всемирная ассамблея здравоохранения
- Исполнительный совет
- Выборы Генерального директора
- Веб-сайт руководящих органов
- Портал государств-членов
- Дом/
- Отдел новостей/
- Прожектор/
- История вакцинации/
- Краткая история вакцинации
На протяжении веков люди искали способы защитить друг друга от смертельных болезней. От экспериментов и риска к глобальное развертывание вакцины в разгар беспрецедентной пандемии иммунизация имеет долгую историю.
От экспериментов и риска к глобальное развертывание вакцины в разгар беспрецедентной пандемии иммунизация имеет долгую историю.
Исследования вакцин могут поднимать сложные этические вопросы, и некоторые из экспериментов, проводившихся для разработки вакцин в прошлом, сегодня были бы неприемлемы с этической точки зрения. Вакцины спасли больше человеческих жизней, чем любое другое медицинское изобретение в истории.
Пролистайте дальше, чтобы совершить путешествие в прошлое тысячелетие и увидеть, как эти выдающиеся открытия и достижения изменили нашу жизнь.
1400–1700 гг.
По крайней мере, с 15-го века люди в разных частях мира пытались предотвратить заболевание, преднамеренно подвергая здоровых людей воздействию оспы.
практика, известная как вариоляция (по названию оспы «la variole»). Некоторые источники предполагают, что эти практики имели место еще в 200 г. до н.э.
до н.э.
По крайней мере, с 15-го века люди в разных частях мира пытаются предотвратить болезнь, преднамеренно подвергая здоровых людей оспе.
© Кредиты
В 1721 году леди Мэри Уортли Монтегю привезла в Европу прививку от оспы, попросив двух своих дочерей сделать прививку от оспы, как она наблюдала в Турции.
В 1774 году Бенджамин Джести совершает прорыв. Проверяя свою гипотезу о том, что заражение коровьей оспой — вирусом крупного рогатого скота, который может передаваться человеку, — может защитить человека от оспы
Доктор Эдвард Дженнер создал первую в мире успешную вакцину. Он обнаружил, что люди, зараженные коровьей оспой, невосприимчивы к оспе.
© Кредиты
В мае 1796 года английский врач Эдвард Дженнер расширяет свое открытие и прививает 8-летнему Джеймсу Фиппсу вещество, взятое из болячки коровьей оспы на руке доярки. Несмотря на местную реакцию и плохое самочувствие в течение нескольких дней,
Фиппс полностью выздоровел.
Два месяца спустя, в июле 1796 года, Дженнер прививает Фиппсу вещество из болячки оспы человека, чтобы проверить устойчивость Фиппса. Фиппс остается в полном здравии и становится первым человеком, получившим прививку от оспы. Термин «вакцина» позже придумано, взято из латинского слова для коровы, vacca.
Узнайте больше об истории вакцинации против оспы.
Французский император Наполеон Бонапарт и американский президент Томас Джефферсон признают работу доктора Эдварда Дженнера и одобряют вакцину против оспы.
© Кредиты
1800-е годы
В 1872 году, несмотря на перенесенный инсульт и смерть двух дочерей от брюшного тифа, Луи Пастер создает первую лабораторно произведенную вакцину: вакцину на холеру кур у кур.
В 1885 году Луи Пастер успешно предотвратил бешенство с помощью постконтактной вакцинации. Лечение спорное. Пастер безуспешно пытался
уже дважды применяли вакцину на людях, а введение человеку возбудителя болезни все еще является новым и неопределенным методом.
Луи Пастер успешно предотвращает бешенство с помощью постконтактной вакцинации.
© Кредиты
Пастер не врач. Но, несмотря на риск, он начинает с пациентом Джозефом Мейстером курс из 13 инъекций, каждая из которых содержит более сильную дозу вируса бешенства. Мейстер выживает и позже становится смотрителем гробницы Пастера. в Париже.
В 1894 году доктор Анна Весселс Уильямс выделила штамм дифтерийной бактерии. это имеет решающее значение в разработке антитоксина для этой болезни.
1900-е годы
С 1918 по 1919 год пандемия испанского гриппа унесла жизни примерно 20–50 миллионов человек во всем мире, в том числе 1 из 67 солдат США, что сделало вакцину против гриппа военным приоритетом США. Проводятся ранние эксперименты с вакцинами против гриппа: Медицинская школа армии США тестирует 2 миллиона доз в 1918, но результаты неубедительны.
Узнайте больше об истории вакцинации против гриппа.
В 1937 году Макс Тейлер, Хью Смит и Ойген Хааген разработали вакцину 17D против желтой лихорадки. Вакцина одобрена в 1938 году и более миллиона человек получили его в этом году. Тайлер получает Нобелевскую премию.
В 1939 году бактериологи Перл Кендрик и Грейс Элдеринг продемонстрировали эффективность вакцины против коклюша. Ученые показывают, что вакцинация снижает заболеваемость детей с 15,1 на 100 детей до 2,3 на 100.
К 1945 году первая вакцина против гриппа одобрена для военных использования, после чего в 1946 году было получено разрешение на использование в гражданских целях. Исследование возглавляют врачи Томас Фрэнсис-младший и Джонас Солк, которые в дальнейшем тесно связаны с вакциной против полиомиелита.
В 1952–1955 годах Джонас Солк разработал первую эффективную вакцину против полиомиелита, и начались ее испытания. Солк испытывает вакцину на себе и своей семье
в следующем году, а в 1954.
К 1960 году второй тип вакцины против полиомиелита, разработанный Альбертом Сабином, был одобрен для использования. Вакцина Сэбина была живой аттенуированной (с использованием вируса в ослабленной форме) и могла вводиться перорально, в виде капель или на кусочке сахара. Пероральная вакцина против полиомиелита (ОПВ) был впервые испытан и произведен в Советском Союзе и Восточной Европе. Чехословакия становится первой страной в мире, ликвидировавшей полиомиелит.
Узнайте больше об истории вакцинации против полиомиелита.
В 1967 году Всемирная организация здравоохранения объявляет об Интенсивной программе искоренения оспы, целью которой является искоренение оспы.
более чем в 30 странах посредством эпиднадзора и вакцинации. Ликвидация означает больше, чем ликвидация болезни в одной области – ВОЗ определяет ее как «постоянное сокращение до нуля определенного патогена в результате преднамеренного
усилий, без риска реинтродукции».
К настоящему времени оспа в основном ликвидирована в Западной Европе, Северной Америке и Японии. После объявления наблюдается беспрецедентная глобальная солидарность. Несмотря на продолжающуюся холодную войну, Соединенные Штаты и Советский Союз едины в поддержке программы.
В 1969 году, через четыре года после открытия вируса гепатита В доктором Барухом Блумбергом, он работает с микробиологом Ирвингом Миллманом над разработкой первого вируса гепатита. Вакцина B с использованием термически обработанной формы вируса.
Полученная из плазмы инактивированная вакцина одобрена для коммерческого использования с 1981 по 1990 год, а генно-инженерная (или рекомбинантная ДНК) вакцина, разработанная в 1986 году, используется до сих пор.
В 1971 г. вакцина против кори (1963) объединена с недавно разработанными вакцинами против эпидемического паротита (1967 г.) и краснухи (1969 г.) в единую вакцину (MMR) доктора Мориса Хиллемана.
Узнайте больше об истории вакцинации против кори.
В 1974 г. Расширенная программа иммунизации (РПИ, ныне Основная программа иммунизации) создана ВОЗ для разработки программ иммунизации во всем мире. Первыми заболеваниями, на которые нацелен РПИ, являются дифтерия, корь, полиомиелит, столбняк, туберкулез и коклюш.
В 1978 г. была лицензирована полисахаридная вакцина, защищающая от 14 различных штаммов пневмококковой пневмонии, а в 1983 г. она была расширена для защиты от 23 штаммов.
В 1980 г. Всемирная ассамблея здравоохранения, действуя по рекомендации Глобальной комиссии ВОЗ по сертификации ликвидации оспы, провозгласила ликвидацию оспы:
в форме эпидемии во многих странах с древнейших времен, оставляя за собой смерть, слепоту и увечья».
С 1970-х по 1980-е годы в США число случаев коклюша достигло рекордно низкого уровня в 1976 году. эффект целой клетки
вакцина начинает перевешивать страх перед самой болезнью.
В 1985 году была лицензирована первая вакцина против болезней, вызываемых Haemophilus influenzae типа b (Hib), после того как Дэвид Х. Смит основал компанию по ее производству. Смит и Портер В. Андерсон-младший работали вместе над вакцинацией с 19 лет.68
В 1988 г., после ликвидации оспы, ВОЗ обратила внимание на полиомиелит, запустив Глобальную инициативу по ликвидации полиомиелита. В конце 1980-х годов полиомиелит был эндемичным в 125 странах. Инициатива направлена на ликвидацию полиомиелита к 2000 г.
К 1994 г. полиомиелит ликвидирован в Америке, затем в Европе в 2002 г., а к 2003 г. это заболевание стало эндемичным всего в 6 странах. Усилия продолжаются.
В 1995 году Энн Шаревски возглавляет группу, которая обрисовывает в общих чертах роль вируса папилломы человека (ВПЧ) в обнаружении и скрининге рака шейки матки, и исследователи начинают работу над вакциной против ВПЧ.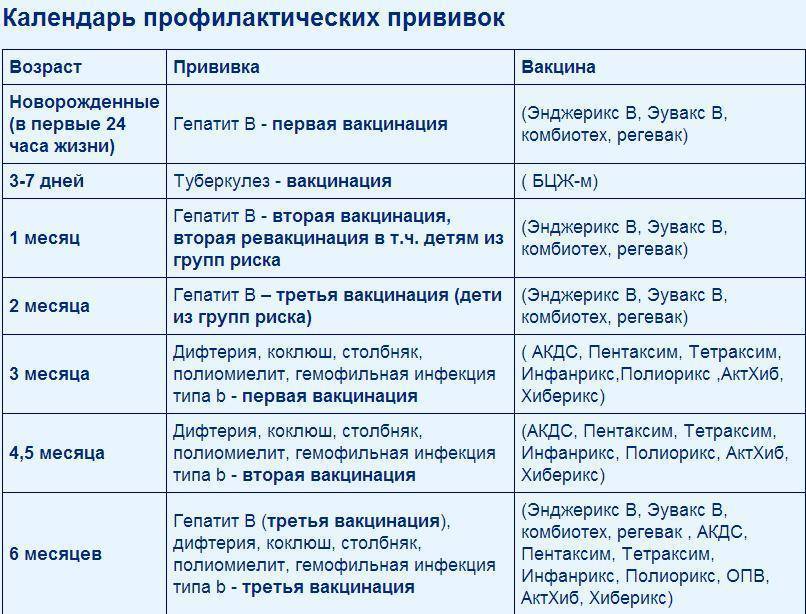
Вирусы ВПЧ очень распространены, часто с минимальными симптомами, но штаммы ВПЧ высокого риска могут вызывать другие заболевания, в частности рак шейки матки. Шаревски продолжает быть главным исследователем в разработке двухвалентной вакцины против ВПЧ.
В 1999 году первая вакцина против ротавируса, наиболее частая причина тяжелой диареи у детей младшего возраста, отменяется только через год после его утверждения из-за опасений по поводу риска кишечных проблем. Версия вакцины с более низким уровнем риска представлена в 2006 году. 2019для использования в более чем 100 странах.
В 2006 году одобрена первая вакцина против вируса папилломы человека (ВПЧ). Вакцинация против ВПЧ становится ключевой частью усилий по искоренению рака шейки матки.
Успех проекта вакцины против менингита подчеркивает ключевую роль государственно-частного партнерства в разработке вакцин.
© Кредиты
Успех Проекта вакцин против менингита в 2016 году подчеркивает ключевую роль государственно-частного партнерства в разработке вакцин. За первые 5 лет использования вакцина почти ликвидировала менингококковую инфекцию серогруппы А в странах менингитного пояса Африки, и в настоящее время она интегрируется в рутинные национальные программы иммунизации.
За первые 5 лет использования вакцина почти ликвидировала менингококковую инфекцию серогруппы А в странах менингитного пояса Африки, и в настоящее время она интегрируется в рутинные национальные программы иммунизации.
Всемирная ассамблея здравоохранения приветствует R&D Blueprint, глобальную стратегию и план обеспечения готовности что позволяет быстро активизировать исследования и разработки во время эпидемий. Его цель — ускорить доступность эффективных тестов, вакцин и лекарств, которые можно использовать для спасения жизней и предотвращения крупномасштабных кризисов.
После нескольких лет ускоренной вакцинации регион Америки объявлен свободным от эндемичной кори. Вспышки в ряде стран, вызванные пробелами в охвате вакцинацией, в 2018 г. болезнь вновь начнет появляться. ВОЗ и ПАОЗ усиливают эпиднадзор и запускают кампании по вакцинации.
ВОЗ проводит предварительную квалификацию вакцины против Эболы для использования в странах с высоким риском.
© Кредиты
В 2019 г. начато пилотное внедрение противомалярийной вакцины в Гане, Малави и Кении. Вакцина RTS/S является первой вакциной, которая может значительно снизить риск заражения самым смертоносным и наиболее распространенным штаммом малярии у детей младшего возраста, группы с самым высоким риском смерти от этой болезни.
ВОЗ проводит предварительную квалификацию вакцины против Эболы для использования в странах с высоким риском в рамках более широкой комплекс средств в ответ на болезнь. В 2021 г. глобальный запас вакцины создан для обеспечения реагирования на вспышки.
Вакцина против оспы третьего поколения одобрена для профилактики оспы обезьян, став, таким образом, первой вакциной против оспы обезьян.
ВОЗ призывает государства-члены уделять приоритетное внимание вакцинации против COVID-19 медицинских работников и групп риска во всех странах.
© Кредиты
30 января 2020 г. Генеральный директор ВОЗ объявляет вспышку нового коронавируса 2019 (SARS-CoV-2) чрезвычайной ситуацией в области общественного здравоохранения, имеющей международное значение. 11 марта ВОЗ подтверждает, что COVID-19является пандемией.
Генеральный директор ВОЗ объявляет вспышку нового коронавируса 2019 (SARS-CoV-2) чрезвычайной ситуацией в области общественного здравоохранения, имеющей международное значение. 11 марта ВОЗ подтверждает, что COVID-19является пандемией.
Эффективные вакцины против COVID-19 разрабатываются, производятся и распространяются с беспрецедентной скоростью, некоторые из них используют новую технологию мРНК. В декабре 2020 года, всего через год после выявления первого случая COVID-19, вводятся первые дозы вакцины против COVID-19.
В 2021 году продолжается развертывание вакцины против COVID-19, при этом дозы доставляются и вводятся на разных континентах. Но усилиям по сдерживанию пандемии угрожает неравенство в охвате вакцинацией: по состоянию на июль 2021 года почти 85% вакцин было введено в странах с высоким уровнем дохода и уровнем дохода выше среднего, а более 75% было введено только в 10 странах. .
ВОЗ призывает государства-члены уделить первоочередное внимание вакцинации работников здравоохранения и групп риска
группам населения в странах с низким уровнем дохода, чтобы остановить тяжелые заболевания и смерть, обеспечить безопасность работников здравоохранения и вновь открыть общество и экономику.
Уже более 2 столетий людей прививают от смертельных болезней, с тех пор как была изобретена первая в мире вакцина против оспы. История научила нас, что полный и эффективный глобальный ответ на вакциноуправляемые заболевания требует времени, финансовой поддержки и сотрудничества – и требует постоянной бдительности.
От новаторских практик 1500-х годов до новых технологий, используемых в вакцинах против COVID-19, мы прошли долгий путь. В настоящее время вакцины помогают защитить от более чем 20 болезней, от пневмонии до рака шейки матки и лихорадки Эбола; и только за последние 30 лет детская смертность снизилась более чем на 50%, во многом благодаря вакцинам. Но необходимо сделать больше.
Во многих частях мира каждый пятый ребенок до сих пор не вакцинирован. Ближайшие десятилетия потребуют глобального сотрудничества, финансирования, приверженности
и видение для обеспечения того, чтобы ни один ребенок или взрослый не пострадал и не умер от болезни, которую можно предотвратить с помощью вакцин.
Узнайте больше на g.co/historyofvaccination.
Связанная история историй о прививках
Разработка вакцин — Консультативный центр по иммунизации
Краткая история вакцин
Концепция иммунизации далека от современной идеи. До Эдварда Дженнера (ученого 18 го века, считающегося основателем вакцинологии) практика иммунизации была зафиксирована в Китае 17 го века, где буддийские монахи пили змеиный яд, чтобы создать иммунитет к укусам змей. Концепция вариоляции (преднамеренного заражения) возникла еще раньше в истории, когда выживших после оспы в 430 г. до н.э. призвали ухаживать за больными.
Чтобы узнать больше об истории вакцин, посетите: https://historyofvaccines.org/
Типы вакцин
Антиген – это активный ингредиент вакцины, который вызывает иммунный ответ против определенного болезнетворного организма . Вакцины широко классифицируются по способу приготовления антигена(ов). Вакцины могут быть вирусными (живыми или инактивированными), вирусными векторами, субъединицами (белковыми или полисахаридными) или нуклеиновыми кислотами (ДНК или РНК). Комбинированные вакцины могут включать инактивированные, белковые и/или конъюгированные с белками полисахаридные компоненты вакцины.
Вакцины могут быть вирусными (живыми или инактивированными), вирусными векторами, субъединицами (белковыми или полисахаридными) или нуклеиновыми кислотами (ДНК или РНК). Комбинированные вакцины могут включать инактивированные, белковые и/или конъюгированные с белками полисахаридные компоненты вакцины.
Дополнительную информацию о классификации вакцин см. в разделе 1.4 Справочника по иммунизации.
Классификация вакцин
Живые вакцины
Живые аттенуированные вакцины
не вызывать заболевания. Иммунитет от живых вакцин обычно очень долгоживущий.
Примеры вакцин: MMR, ветряная оспа, ротавирус
Неживые вакцины
Инактивированные или цельные убитые:
Убитые вакцины содержат целые бактерии, которые были убиты.
Пример вакцины: цельноклеточная вакцина против коклюша
Инактивированные вакцины содержат вирусы, которые каким-то образом были инактивированы, поэтому они не способны размножаться или вызывать заболевание.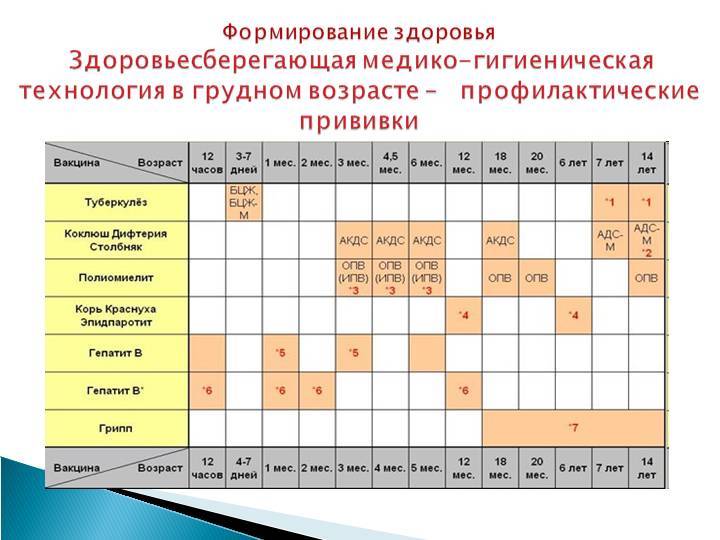
Примеры вакцин: грипп, гепатит А и полиовакцины.
Субъединица:
Субъединичные вакцины содержат кусочки патогенов, от которых они защищают. Существует несколько различных типов субъединичных вакцин:
— Токсоид
Токсоидные вакцины производятся путем сбора бактериального токсина и его химического изменения (обычно с помощью формальдегида) для преобразования токсина в анатоксин. Токсоидные вакцины индуцируют антитела, которые нейтрализуют вредные токсины, выделяемые этими бактериями.
Примеры вакцин: дифтерия, столбняк
— Полисахаридные и конъюгированные вакцины
Полисахариды представляют собой цепочки сахаров. Некоторые бактерии, такие как Streptococcus pneumoniae , имеют на своей поверхности большое количество полисахарида, который инкапсулирует бактерии. Полисахаридные вакцины плохо иммуногенны и могут индуцировать только первичный иммунный ответ, поэтому иммунная память для защиты в дальнейшем не создается./90/90.jpg)
Полисахаридные конъюгированные вакцины содержат белки-носители, химически связанные с полисахаридными антигенами. Это добавление приводит к активации Т-клеточного ответа, индуцирующего как высокоаффинные антитела против полисахаридных антигенов, так и иммунную память, и может использоваться у младенцев.
Примеры вакцин: Hib-PRP, PCV13 и MenACWY. Ген встраивают в клеточную систему, способную продуцировать большие количества интересующего белка. Образующийся белок может генерировать защитный иммунный ответ.
Примеры вакцин: вакцина против гепатита В и вакцина против ВПЧ
Нуклеиновая кислота
Недавние разработки в области вакцинных технологий позволили использовать информационную рибонуклеиновую кислоту (мРНК) для доставки генетического кода в наши дендритные клетки для производства специфических вирусных белков. Поскольку мРНК легко разрушается вездесущими ферментами рибонуклеазами, она защищена внутри липидной наночастицы, что также способствует поглощению дендритными клетками. Внутри дендритной клетки рибосомы и мРНК вакцины генерируют вирусный белок, который затем презентируется Т- и В-клеткам в лимфатических узлах.
Внутри дендритной клетки рибосомы и мРНК вакцины генерируют вирусный белок, который затем презентируется Т- и В-клеткам в лимфатических узлах.
Пример вакцины: Вакцина Pfizer против COVID-19 (мРНК-CV)
Вирусный вектор
клетки разные. Вирусный вектор будет использовать безвредный аденовирус для введения белка в иммунные клетки. Затем иммунная клетка создает белок из инструкций мРНК и запускает иммунный ответ.
Пример вакцины: AstraZeneca COVID-19вакцина (ChAd-CV)
Компоненты вакцины
В дополнение к антигену вакцина может содержать ряд других веществ; например, иммунный усилитель (адъювант) и/или консервант.
Продукты животного происхождения
Некоторые люди обеспокоены продуктами животного происхождения, такими как желатин в вакцинах. Это может быть связано с религиозными соображениями или опасениями по поводу безопасности продуктов животного происхождения. Дополнительную информацию о продуктах животного происхождения в вакцинах можно найти на странице письменных источников на веб-сайте Консультативного центра по иммунизации
Аллергия на ингредиенты вакцины
Очень редко вакцины вызывают серьезную аллергическую реакцию, называемую анафилаксией.