Туберкулез
Бактериальные инфекции
ТУБЕРКУЛЕЗ
Туберкулез представляет собой острое или хронически протекающее инфекционное заболевание, вызываемое микобактерией туберкулеза, при котором могут поражаться все органы человеческого организма, но чаще всего больные страдают туберкулезом легких.
Микобактерией туберкулеза инфицирована третья часть населения всей планеты. Приблизительно 3 миллиона больных погибают от туберкулеза. Это самая частая инфекционная причина смерти на земле. Начиная с 1950 года благодаря применению эффективных антибиотиков, на протяжении более 30 лет, до середины 1980-ых в Соединенных Штатах Америки и в странах Западной Европы в обществе наблюдалась эйфория, связанная с резким уменьшением заболеваемости туберкулезом. В конце 80-х годов была отмечена массовая вспышка заболеваемости в США, Европе и особенно в Африке, частично за счет лиц, инфицированных вирусом иммунодефицита. Туберкулез у лиц, страдающих СПИДом развивается намного чаще и протекает намного тяжелее (ранняя диссеминация и быстрая деструкция легочной ткани), чем у раннее здоровых людей. Кроме того, у этих лиц выделяется мультистойкий по отношению к лекарственным препаратам штамм микобактерии туберкулеза. Микобактерии растут от 20 до 100 раз медленнее, чем другие бактерии. Требуется от 4 до 6 недель, чтобы получить колонию M. туберкулеза для определения чувствительности к лекарственным средствам. Все это создает угрозу для широкого распространения инфекции. Общее количество больных туберкулезом достигает 50 млн., причем половина из них не старше 45 лет. 75% всех больных и умерших от туберкулеза приходятся на развивающиеся страны Азии, Африки и Южной Америки, где туберкулез должен быть отнесен к эпидемическим заболеваниям без тенденции к уменьшению. В России, по данным официальной статистики, в период с 1991 по 1996 годы заболеваемость туберкулезом увеличилась на 98,5% (детей — на 76%), а смертность за этот же период повысилась в 2,2 раза.
Этиология и патогенез туберкулеза
Туберкулез вызывает микобактерия туберкулеза, открытая Кохом в 1882 г. Различают 4 типа микобактерий:
Ворота инфекции. Две первые разновидности микобактерий способны вызывать развитие туберкулеза у человека:
Большое значение для развития туберкулеза имеют факторы предрасположенности к этой болезни. В настоящее время доказана роль генов HLA в патогенезе туберкулезной инфекции и показано, что HLA-фенотип (в первую очередь DR) различается у больных с локальными и генерализованными формами заболевания. Туберкулез расцветает там, где бедность, плохое питание, скверные условия жизни и слабая медицина. Существуют также национальные различия: у кавказцев и монголов, может быть в силу вековых контактов с туберкулезной бациллой, выработалась чрезвычайно высокая резистентность к ней. И наоборот, африканцы, американские индейцы, северные народы и эскимосы чрезвычайно восприимчивы, может быть потому, что до последнего времени не приобрели генетического фактора подобного расового различия. Например, уровень смертности в армии США гораздо выше у черных, чем у белых, хотя все они живут в одинаковых условиях. Следует, однако, отметить, что первоначальные условия жизни (социально-экономические, питание) у них были разными. Мужчины во всех странах болеют туберкулезом чаще, чем женщины. Благоприятными факторами для развития туберкулеза являются сахарный диабет, врожденные заболевания сердца, хронические легочные заболевания (в частности силикоз), все, что ослабляет иммунитет. Профессиональному риску подвергаются врачи и медицинский персонал больниц.
Микобактерии являются аэробными, споронеобразующими, неподвижными кислотоустойчивыми палочками. Кислотоустойчивость ей придает большое содержание в стенке бациллы липидов (от20 до 40% от ее массы). Эта липидная фракция содержит воски, нейтральные жиры и фосфатиды. Вместе с тем, описаны и ее коккообразные L-формы, которые под влиянием ряда препаратов могут терять свою клеточную стенку и длительно персистировать в организме.
В патогенезе туберкулеза значение имеют три важных механизма:
факторы вирулентности микроорганизма;
соотношение гиперчувствительности и иммунитета к возбудителю;
фактор деструкции тканей и казеозного некроза.
Микобактерия туберкулеза не выделяет каких-либо экзотоксинов, эндотоксинов или гистолитических ферментов. Бациллы туберкулеза очень резистентны, сохраняясь даже в высушенных капельках слюны или мокроты в течение нескольких недель. Если же инфицированные выделения остаются влажными, то их вирулентная способность сохраняется месяцами. Непрямая передача с пылью или утварью возможна, но редка. У человека существует естественная резистентность к
Эти микробы имеют и другие биологические свойства, которые позволяют лучше понять болезнь человека. Mycobacterium tuberculosis являются строгими аэробами. Они лучше всего размножается в тканях с высоким содержанием кислорода (РО2 равном 100 мм Hg). Реактивация вторичного туберкулеза происходит в верхушках легких. Эти зоны хорошо не аэрируются, но легочная циркуляция относительно в этих участках медленная, захватывает минимальное количество альвеолярного кислорода. Оставшаяся часть альвеолярного кислорода вполне достаточна для мультипликации бацилл. По мере ее усиления создается состояние анаэробиоза, препятствующее мультипликации бацилл. В центре казеозных очагов, лишенных кислорода, бактериальная пролиферация резко угнетена. Однако, при прогрессировании казеоза и разрушении стенок воздухоносных путей (бронхиол) создаются условия, позволяющие глубже расположенным микробам увеличить доступ к кислороду и усилить их размножение.
Жирные кислоты, особенно с длинными цепями, тормозят рост туберкулезных палочек, в особенности, когда рН падает ниже 6,5. Эти экспериментально полученные данные могут иметь большое значение в понимании патогенеза туберкулезной инфекции. Оказывается, что в очагах воспаления липазы при рН 6,5 высвобождают алифановые кислоты с длинными или короткими цепями, предназначенные для замедления репродукции бацилл или для их повреждения и даже разрушения. Эти жирные кислоты, падение рН и возрастающий анаэробиоз в воспалительном туберкулезном очаге в совокупности могут объяснить прогрессирующее исчезновение бацилл в центре казеозных повреждений.
Первым таким веществом является корд-фактор, который является гликолипидом и позволяет микобактерии in vitro расти в змеином спинном мозге. Вирулентные штаммы Mycobacterium tuberculosis обязательно содержат этот фактор на клеточной поверхности. Если корд-фактор извлечен из бацилл, то они теряют свою вирулентность. При введении очищенного корд-фактора мышам в месте введения образуется
Второй фактор вирулентности — это сульфатиды, которые также являются поверхностными гликолипидами, содержащими серу. Они препятствуют слиянию фагосом макрофагов с лизосомами.
Третьим фактором вирулентности является LAM (lipoarabinoman), представляющий собой гетерополисахарид, который по строение сходен с эндотоксинами грам-негативных бактерий. Этот фактор ингибирует активацию макрофагов гамма-интерфероном. Под влиянием LAM макрофаги секретируют TNF-?, под действием которого развиваются лихорадка, снижение веса и повреждение тканей
Четвертым фактором вирулентности является высокоиммуногенный микобактериальный белок температурного шока, который по строению похож на белки температурного шока человека, поэтому данный белок может играть роль в аутоиммунных реакциях, вызванных микобактерией. На поверхности микобактерии активируется комплемент, что приводит к ее опсонизации и облегчает ее фагоцитоз макрофагами через CR3-рецептор (МАС-1 интегрин) без последующего уничтожения внутри макрофага (незавершенный фагоцитоз).
Патогенез туберкулеза сводится к проникновению микобактерий в организм и взаимодействию с его тканями и органами. Возникновение, течение и исход туберкулеза в значительной степени обусловлены иммунным состоянием организма, его реактивностью. Реактивность определяет необычное разнообразие клинико-морфологических проявлений туберкулеза, что составляет одну из ярких его особенностей как болезни и создает большие трудности в клинической диагностике. У несенсибилизированных субъектов бациллы могут быстро размножаться и, не будучи остановленными, они нередко проникают по лимфатическим и кровеносным сосудам в отдаленные от первичного очага ткани, вызывая, таким образом, генерализацию процесса. Тканевой некроз в этих случаях ограничен. У сенсибилизированных субъектов быстрое появление активных макрофагов тормозит размножение бацилл, ограничивает распространение инфекции и быстро блокирует диссеминацию микробов, но некроз в этих случаях тяжелее.
При любом попадании в организм человека туберкулезная палочка в воротах инфекции вызывает воспалительный процесс. По типу тканевой реакции при туберкулезе воспаление может быть альтеративным, экссудативным и пролиферативным. Тип тканевой реакции зависит от перечисленных выше факторов.
Альтеративный тип тканевой реакции при туберкулезе характеризуется развитием казеозного некроза, при этом другие компоненты воспаления выражены слабо. Это очень тяжелая форма воспаления, которая свидетельствует о гипо- или анергии организма и встречается у новорожденных, стариков или в любом возрасте у тяжелых кахектичных больных (например, у больных злокачественными новообразованиями). Эта форма обычно заканчивается смертью больного.
Экссудативный тип тканевой реакции при туберкулезе характеризуется формированием специфического экссудата. Две особенности отличают этот экссудат. Этот экссудат состоит преимущественно из лимфоцитов; вторая его особенность в том, что не только клетки экссудата, но и ткани, в которых развивается воспаление, склонны к казеозному некрозу. Экссудативный тип тканевой реакции возникает у лиц, не имеющих иммунитета, которые впервые соприкасаются с туберкулезной палочкой, на фоне сенсибилизации организма, а также он возникает у больных при снижении общих защитных сил организма. Иммунитет при туберкулезе нестерильный, т.е. он существует при наличии туберкулезной палочки в организме.
Пролиферативный тип тканевой реакции при туберкулезе свидетельствует об относительно благоприятном течении процесса — это начало активизации иммунных реакций организма. Эта форма характеризуется развитием в тканях гранулематозного воспаления и обозначается как туберкулезный бугорок. Туберкулезный бугорок характеризуется специфическим клеточным составом и характером расположения этих клеток. Три типа клеток входят в состав бугорка — лимфоциты, эпителиоидные и многоядерные гигантские клетки Пирогова — Лангханса. В центральной части гранулемы выявляются макрофаги и многоядерные гигантские клетки Пирогова-Лангханса. Если макрофаги (гистиоциты) активированы, их размер увеличивается и они принимают вид эпителиоидных клеток. При обычной световой микроскопии и окраске гематоксилином и эозином эти клетки имеют обильную цитоплазму, розовую, мелкогранулированную, в которой содержатся иногда целые интактные бациллы или их фрагменты. Гигантские многоядерные клетки формируются при слиянии макрофагов или после ядерного деления без разрушения клетки (цитодиэреза). Т-лимфоциты располагаются по периферии бугорка. Количественный состав туберкулезных бугорков различный. Поэтому различают — преимущественно эпителиоидный, лимфоцитарный, гигантоклеточный или смешанный варианты. В бугорке отсутствуют сосуды. По величине бугорки бывают субмилиарные (до 1 мм), милиарные (от. лат. -milium -просо) — 2-3 мм, солитарные до нескольких см в диаметре. Туберкулезные бугорки, в отличие от других подобных, склонны к казеозному некрозу. Предполагают, что казеозный некроз обусловлен либо прямым действием высвобождающихся цитотоксичных продуктов сенсибилизированных Т-лимфоцитов или макрофагов, либо эти продукты опосредовано, вызывая спазм сосудов, ведут к коагуляционному некрозу, либо гиперактивные макрофаги умирают очень быстро, высвобождая лизосомные энзимы.
Исход бугорков. Туберкулезные бугорки при благоприятном течении процесса подвергаются рубцеванию. Неблагоприятный исход — колликвация, т.е. разжижение казеозных масс.
Различают три основных вида клинико-морфологических проявлений туберкулеза:
Первичный туберкулез характеризуется:
развитием заболевания в период инфицирования, т. е. при первой встрече организма с инфектом;
сенсибилизацией и аллергией, реакциями гипер-чувствительности немедленного типа;
преобладанием экссудативно-некротических изменений;
склонностью к гематогенной и лимфогенной (лимфожелезистой) генерализации;
параспецифическими реакциями в виде васкулитов, артритов, серозитов и т. д.
Как правило, путь заражения аэрогенный, возможен и алиментарный путь. Болеют преимушественно дети, но в настоящее время первичный туберкулез наблюдается у подростков и взрослых.
Патологическая анатомия. Морфологическим выражением первичного туберкулеза является первичный туберкулезный комплекс. Он состоит из трех компонентов:
первичного очага или аффекта— очага поражения в органе;
лимфангита -туберкулезного воспаления отводящих лимфатических сосудов;
лимфаденита -туберкулезного воспаления регионарных лимфатических узлов.
При аэрогенном заражении в легких возникает туберкулезный воспалительный очаг, обозначаемый как первичный туберкулезный аффект. Чаще всего он расположен субплеврально в наиболее аэрируемых сегментах в нижней части верхних долей или в верхней части нижних долей (чаще правого легкого — III, VIII, IX, Х). Вначале туберкулезная бацилла вызывают неспецифическую банальную воспалительную реакцию. На второй неделе, при появлении сенсибилизации, этот очаг уплотняется и образуется участок казеозной пневмонии, окруженный зоной перифокального неспецифического воспаления. Размеры аффекта различны: иногда выявляется лишь альвеолит, едва различимый микроскопически, но чаще воспаление охватывает ацинус или дольку, реже — сегмент и в очень редких случаях — всю долю, чаще всего это участок от 1 до 1,5 см. в диаметре, четко отграничен от окружающих тканей. Одновременно в плевре развивается фибринозный или серозно-фибринозный плеврит. В специфический воспалительный процесс очень быстро вовлекаются лимфатические сосуды, в которых выявляется туберкулезный лимфангит. Макроскопически они видны в виде серовато-желтоватых полос, которые напоминают тропинку от первичного очага к прикорневым лимфатическим узлам. Воспалительный процесс очень быстро распространяется на регионарные бронхопульмональные, бронхиальные и бифуркационные лимфатические узлы. Возникает туберкулезный лимфаденит. Лимфатические узлы увеличиваются в несколько раз и на разрезе представлены казеозными, сухими, легко крощащимися, желтоватыми массами.
При алиментарном заражении первичный туберкулезный комплекс развивается в кишечнике и также состоит из трех компонентов. В лимфоидной ткани нижнего отдела тощей или слепой кишки формируются первичный туберкулезный аффект, макроскопически имеющий нередко вид язвы. Затем возникают туберкулезный лимфангит с появлением бугорков по ходу лимфатических сосудов и туберкулезный лимфаденит регионарных к первичному аффекту лимфатических узлов. Изредка первичный туберкулезный аффект может развиться в миндалине с вовлечение в воспалительный процесс лимфатических узлов шеи, а также в коже (язва в коже, лимфангит, регионарный казеозный лимфаденит).
Возможны три варианта течения первичного туберкулеза:
заживление очагов первичного комплекса;
прогрессирование первичного туберкулеза с генерализацией процесса;
хроническое течение (хронически текущий первичный туберкулез).
Заживление очагов первичного комплекса. При локализации первичного туберкулезного аффекта в легких первоначально рассасывается перифокальное воспаление. Экссудативная тканевая реакция сменяется продуктивной: вокруг очага казеозной пневмонии образуется вал из эпителиоидных и лимфоидных клеток, как бы отграничивающий очаг от окружающей легочной ткани. Кнаружи от этого вала появляются фиброзирующиеся туберкулезные гранулемы. Вокруг первичного аффекта формируется капсула, наружные слои которой состоят из рыхлой соединительной ткани с наличием мелких сосудов, окруженных лимфоцитами. Происходит формирование капсулы (инкапсуляция). Казеозные массы постепенно обезвоживаются, становятся плотными и обызвествляются (петрификация). С течением времени путем метаплазии образуются костные балки с клетками в межбалочных пространствах. Так, петрифицированный первичный очаг превращается в оссифицированный. Такой заживший первичный очаг называют очагом Гона, по имени чешского патологоанатома описавшего его впервые.
На месте туберкулезного лимфангита фиброзный тяж. Заживление в лимфатических узлах происходит так же, как и в легочном очаге. Однако, в связи с большими размерами поражения в лимфатических узлах оно протекает медленнее, чем в легочном очаге. Очаг казеоза в лимфатическом узле постепенно обезвоживается, обызвествляется и окостеневает.
Обызвествленные очаги в легких обнаруживаются у многих практически здоровых людей. Таким образом, попадание туберкулезных микобактерий в организм человека ведет не только к заболеванию, но и к инфицированию, которое может оказать благоприятное влияние на становление иммунитета и предупреждение нового заражения. Доказано, что противотуберкулезный иммунитет является инфекционным, нестерильным, т. е. он осуществляется в организме при наличии слабовирулентных микобактерий, которые могут проявлять свою жизнедеятельность при ослаблении защитных сил организма. В кишечнике на месте первичной туберкулезной язвы при заживлении образуется рубец, а в лимфатических узлах — петрификаты.
Прогрессирование первичного туберкулеза с генерализацией процесса. Оно проявляется в 4 формах: гематогенной, лимфогенной (лимфожелезистой), росте первичного аффекта и смешанной.
Гематогенная форма прогрессирования (генерализация) при первичном туберкулезе развивается в связи с ранним попаданием микобактерий в кровь (диссеминация) из первичного аффекта или из казеозно-измененных лимфатических узлов. Микобактерий оседают в различных органах и вызывают образование в них бугорков размером от милиарных (просовидных) — милиарный туберкулез до крупных очагов величиной с горошину и более. В связи с этим различают милиарную и крупноочаговую формы гематогенной генерализации.
Термин «милиарный» отражает точечный характер повреждений. Эти маленькие желтовато-белые очажки напоминают просяные зерна. Если микробы проникают в a. pulmonalis, то милиарная диссеминация может быть ограничена легкими, так как они будут блокированы в альвеолярных капиллярах. Если бацилл слишком много и они преодолевают легочные капилляры или казеозному некрозу подвергается v. pulmonalis, происходит системное обсеменение. Милиарные очажки в этих случаях могут образовываться в любом органе. Однако хорошо известно, что некоторые ткани чрезвычайно устойчивы к туберкулезной инфекции и очень редко можно наблюдать развитие бугорков в сердце, гладких мышцах, щитовидной и поджелудочной железе. Предпочтительная локализация милиарных повреждений: костный мозг, глазное дно, лимфатические узлы, печень, селезенка, почки, надпочечники, простата, семенные пузырьки, фаллопиевы трубы, эндометрий и оболочки головного мозга.
Особенно опасно высыпание милиарных туберкулезных бугорков в мягких мозговых оболочках с развитием туберкулезного лептоменингита. Иногда при гематогенной генерализации появляются единичные разной величины отсевы в различные органы, в том числе в верхушки обоих легких (очаги Симона), которые спустя много лет после затихания первичной инфекции дают начало туберкулезному поражению в месте локализации этого очага отсева.
Лимфогенная (лимфожелезистая) форма прогрессирования (генерализации) при первичном туберкулезе проявляется вовлечением в процесс специфического воспаления бронхиальных, бифуркационных, околотрахеальных, над- и подключичных, шейных и других лимфатических узлов. Особенно большое значение в клинике приобретает туберкулезный бронхоаденит. В тех случаях, когда пакеты лимфатических узлов напоминают опухоль, говорят об опухолевидном бронхоадените. При этом казеозно-измененные увеличенные лимфатические узлы сдавливают просветы бронхов, что ведет к развитию очагов ателектаза легких и пневмонии.
При первичном туберкулезе кишечника лимфогенная (лимфожелезистая) генерализация ведет к увеличению всех групп мезентериальных лимфатических узлов. Развивается туберкулезный мезаденит, который может доминировать в клинической картине заболевания.
Рост первичного аффекта — наиболее тяжелая форма прогрессирования первичного туберкулеза. При ней наступает казеозный некроз зоны перифокального воспаления, вокруг первичного аффекта образуются свежие участки экссудативного воспаления, подвергающиеся омертвению и сливающиеся между собой. Первичный очаг из ацинозного превращается в лобулярный, затем в сливной лобулярный, сегментарный лобарный — возникает лобарная казеозная пневмония. Это самая тяжелая форма первичного туберкулеза, быстро заканчивающаяся гибелью больного. В прошлом такую форму называли «скоротечная чахотка». Иногда первичный очаг лобулярной или сегментарной казеозной пневмонии расплавляется и на его месте образуется первичная легочная каверна. Процесс принимает хроническое течение, развивается первичная легочная чахотка, напоминающая вторичный фиброзно-кавернозный туберкулез, но отличающаяся от него наличием казеозного бронхоаденита. Первичный туберкулезный аффект в кишечнике растет за счет увеличения размеров туберкулезной язвы обычно в области слепой кишки. Появляются ограниченный туберкулезный перитонит, спайки, пакеты казеозно-измененных илеоцекальных лимфатических узлов. Образуется плотный конгломерат тканей, который клинически иногда принимается за опухоль (опухолевидный первичный кишечный туберкулез). Процесс имеет обычно хроническое течение.
Смешанная форма прогрессирования при первичном туберкулезе наблюдается при ослаблении организма после перенесенных острых инфекций, например, кори, при авитаминозах, голодании и т.д. В таких случаях обнаруживаются крупный первичный аффект, казеозный бронхоаденит, нередко осложненный расплавлением некротических масс и образованием свищей. В легких и во внутренних органах видны многочисленные туберкулезные воспалительные очаги.
Исходы прогрессирующего первичного туберкулеза различны. В неблагоприятных случаях смерть больного наступает от интоксикации (при генерализации процесса) и туберкулезного менингита. При благоприятном течении заболевания и применении эффективных лекарственных препаратов прогрессирование первичного туберкулеза может быть приостановлено, удается перевести экссудативную реакцию в продуктивную, вызвать инкапсуляцию и обызвествление очагов первичного комплекса, рубцевание его отсевов.
Хроническое течение (хронически текущий первичный туберкулез). Возникает, прежде всего, в тех случаях, когда при зажившем первичном аффекте воспалительный специфический процесс в лимфожелезистом компоненте первичного комплекса принимает медленно прогрессирующее течение с чередованием вспышек и затиханий. При этом наступает сенсибилизация организма — повышается его чувствительность ко всякого рода неспецифическим воздействиям. Повышенная реактивность организма клинически выявляется кожными туберкулиновыми пробами и появлением в тканях и органах параспецифических изменений, под которыми понимают различные мезенхимальные клеточные реакции в виде диффузной или узелковой пролиферации лимфоцитов и макрофагов, гиперпластических процессов в кроветворной ткани, фибриноидных изменений соединительной ткани и стенок артериол в органах, диспротеиноз, иногда развитие амилоилоза. О хронически текущем первичном туберкулезе говорят также тогда, когда образуется первичная легочная каверна и развивается первичная легочная чахотка.
Гематогенный туберкулез объединяет ряд проявлений заболевания, возникающего и развивающегося в организме человека через значительный срок после перенесенной первичной инфекции. Его еще обозначают как послепервичньш туберкулез. В этих случаях речь идет о людях, клинически выздоровевших от первичного туберкулеза, но сохранивших повышенную чувствительность к туберкулину и выработавших значительный иммунитет к туберкулезной микобактерии. Гематогенный туберкулез возникает у тех больных, у которых первичная инфекция оставила изменения в виде очагов отсевов в различные органы или не вполне заживших фокусов в лимфатических узлах. Эти очаги долгое время могут оставаться латентными, их обострение происходит под влиянием каких-либо неблагоприятных факторов при наличии повышенной реактивности. Поэтому при гематогенном туберкулезе преобладает продуктивная тканевая реакция (туберкулезный бугорок), выражена наклонность к гематогенной генерализации, которая ведет к поражению различных органов и тканей.
studfile.net
Этиология и патогенез туберкулеза — Первый по туберкулезу
Оглавление: [скрыть]
- Этиология туберкулеза
- Первичный патогенез
- Патогенез клинического туберкулеза
- Патологическая анатомия туберкулеза
- Патогенетическое лечение
Туберкулез — это опаснейшее инфекционное заболевание, с которым борются на протяжении многих столетий с переменным успехом. Патогенез туберкулеза основан на специфических воспалительных процессах, разрушающих ткани органов человека, в основном легких.

Многие выдающиеся ученые изучали туберкулез, этиологию, патогенез, и значительно продвинули вперед возможности медицины в борьбе с этим недугом. Но и в наше время, несмотря на то что его этиология и патогенез достаточно исследованы, туберкулез остается серьезным заболеванием, грозящим эпидемиями.
Этиология туберкулеза
Возбудителем туберкулеза становятся микобактерии специфичного туберкулезного комплекса. Источником появления бактерий являются люди, больные туберкулезом легких. Очень редко инфекция может передаваться от животных. Болезнетворные бактерии могут выделиться в виде мокроты, только через рот больного человека (при кашле, чихании, разговоре). Затем ее мельчайшие частицы (размером до 5 мкм) формируют аэрозольные облачка, которые много часов могут распространяться в воздухе.
Вдыхая воздух, здоровый человек получает порцию инфекции, которая и становится возбудителем болезни при благоприятных условиях. Такой аэрогенный путь проникновения бактерий в организм человека является основным в этиологии туберкулеза. Обычно заражение происходит в помещениях, где опасные аэрозоли сохраняются длительное время. Проветривание и вентиляция значительно уменьшают риск инфекции; кроме того, бактерии погибают под действием прямых солнечных лучей.
 Помимо воздушно-дыхательного пути, инфекция может передаваться алиментарным, контактным и внутриутробным способами. Однако алиментарный (через загрязненные продукты и вещи) путь инфицирования встречается в 10000 раз реже, чем аэрогенный способ. Контактный путь проникновения бактерий может наблюдаться в основном при попадании зараженной крови. В целом туберкулез принято относить к социальным заболеваниям, связанным с низким уровнем жизни. К группе риска относятся лица без определенного места жительства, обитатели трущоб, люди, находящиеся в исправительных организациях.
Помимо воздушно-дыхательного пути, инфекция может передаваться алиментарным, контактным и внутриутробным способами. Однако алиментарный (через загрязненные продукты и вещи) путь инфицирования встречается в 10000 раз реже, чем аэрогенный способ. Контактный путь проникновения бактерий может наблюдаться в основном при попадании зараженной крови. В целом туберкулез принято относить к социальным заболеваниям, связанным с низким уровнем жизни. К группе риска относятся лица без определенного места жительства, обитатели трущоб, люди, находящиеся в исправительных организациях.
Вернуться к оглавлению
Первичный патогенез
В общем случае патогенез туберкулеза можно охарактеризовать как воспалительный процесс гранулематозного типа, который вызывает появление многочисленных бугорков, склонных к разложению. Первичный патогенез заключается в локальном инфицировании входных ворот и регионарном лимфадените.
В абсолютном большинстве случаев (до 98%) легкие человека становятся входными воротами для инфекции. Несмотря на то что большинство возбудителей болезни погибает, небольшая их часть попадает в макрофаги, которые переносят бактерии в регионарные лимфатические узлы. В течение 10-80 дней в паренхиме легких и в лимфатических узлах активизируется воспалительный процесс. В паренхиме легких возникает казеозный некроз и инкапсуляция, которые заживляются при фиброзе. Очаг разрушения паренхимы может расшириться, что приводит к пневмонии или плевриту. При значительном размере некроза ядро очага разжижается и выделяет мокроту в бронхи, образуя каверну.
 Очаги в лимфатических узлах также подвергаются фиброзу, и заживление их более затруднительно. Бактерии могут сохраняться в них несколько десятков лет. При первичном патогенезе лимфатические узлы могут не увеличиваться. В то же время прикорневые узлы могут значительно расшириться и сдавить бронх, что ведет к ателектазу. Возникает опасность разрушения стенки бронха с образованием свища. В результате всех процессов возникает очаг уплотнения.
Очаги в лимфатических узлах также подвергаются фиброзу, и заживление их более затруднительно. Бактерии могут сохраняться в них несколько десятков лет. При первичном патогенезе лимфатические узлы могут не увеличиваться. В то же время прикорневые узлы могут значительно расшириться и сдавить бронх, что ведет к ателектазу. Возникает опасность разрушения стенки бронха с образованием свища. В результате всех процессов возникает очаг уплотнения.
Первичный патогенез туберкулеза протекает с проникновением бактерий практически во все ткани органа. Активное их размножение происходит в верхней части легких, почках и костях. При недостаточном клеточном иммунитете начинает проявляться диссеминированный туберкулез.
Вернуться к оглавлению
Патогенез клинического туберкулеза
При недостаточном функционировании макрофагов процесс размножения бактерий начинает развиваться в геометрической прогрессии. В пространство между клетками ткани проникает значительное число медиаторов и ферментов, приводящее к разрушению ткани путем ее разжижения. Воспалительный процесс распространяется на весь орган. Увеличивается проницаемость стенок сосудов, а в ткань проникают лейкоциты и моноциты. Появляются туберкулезные гранулемы с преобладанием некроза. Таким образом, первичная форма заболевания перерастает в клиническую форму.
Продолжительность периода до проявления клинических симптомов зависит от многих факторов. К первым таким признакам можно отнести возникновение диссеминированного туберкулеза и туберкулезного менингита. Время до их проявления составляет 2-6 месяцев. Туберкулезный бронхит может появиться через 3-9 месяцев. Развитие туберкулеза до клинической формы в костях может продолжаться несколько лет, а в почках — до 10 лет.
Вернуться к оглавлению
Патологическая анатомия туберкулеза
 Патологическая анатомия туберкулеза характеризуется рядом специфических повреждений тканей. При диссеминированном туберкулезе наиболее характерны единичные бугорки в легких. В других органах они практически не встречаются. Генерализованный гематогенный туберкулез может проявиться в виде казеозных очагов, в основном в легких, но иногда встречается в других органах человека. В редких случаях диссеминированная форма заболевания ведет к сепсису.
Патологическая анатомия туберкулеза характеризуется рядом специфических повреждений тканей. При диссеминированном туберкулезе наиболее характерны единичные бугорки в легких. В других органах они практически не встречаются. Генерализованный гематогенный туберкулез может проявиться в виде казеозных очагов, в основном в легких, но иногда встречается в других органах человека. В редких случаях диссеминированная форма заболевания ведет к сепсису.
Патологическая анатомия острой формы болезни указывает на многочисленные небольшие очаги, характерные при милиарном туберкулезе. Возникают благоприятные условия для миграции бактерий и возникновения лимфангитов. Вокруг капилляров возникают желтоватые выпуклости с размером до 2 мм. Процессы в легких ведут к поражению сосудов — вен и ветвей легочной артерии. В самом легком развиваются очаги размером до 10 мм.
В целом патологическая анатомия туберкулеза описывается такой картиной: специфические гранулемы, васкулиты и альвеолиты явственно проступают в тканях легких.
На следующей стадии преобладает интерстициальный сетчатый склероз.
Вернуться к оглавлению
Патогенетическое лечение
Обычное терапевтическое лечение туберкулеза ведет борьбу с общим воспалительным процессом. Патогенетическая терапия направлена воздействовать на определенные зоны, ответственные за патогенез туберкулеза.
Патогенетическое лечение основывается на выделении двух основных типов протекания туберкулеза. К первому типу относят резкое начало болезни через туберкулезную интоксикацию и разрушение тканей, заметное на рентгенограмме уже на первичной стадии. В легких главенствуют экссудативные реакции. Инфильтрационный процесс проходит с появлением очагов некроза. Ко второму типу причисляется слабовыраженный процесс (без явных симптомов). В этом случае в ткани легких имеют преимущество продуктивные реакции, а патологических отклонений не наблюдается. Вокруг очагов некроза образуются оболочки. Признаки туберкулеза диагностируются только при томографических исследованиях.
 Номенклатура препаратов, используемых при патогенетическом лечении, достаточно широка. Для снижения воспалительных реакций вводятся глюкокортикоиды и гепарин натрия. Если возникает риск проявления фиброзных аномалий, то назначается гиалуронидаза, пирогенал, пеницилламин. Важное значение имеет устранение побочных воздействий антибиотиков, для чего рекомендуются антигистаминные средства, пиридоксин, глутаминовая кислота, пирацетам. Для укрепления защитных функций внутреннего органа используются иммуномодуляторы и иммунокорректоры. Особо выделяется применение поливалентных патогенетических препаратов, которые могут предотвращать и устранять некоторые патологические изменения.
Номенклатура препаратов, используемых при патогенетическом лечении, достаточно широка. Для снижения воспалительных реакций вводятся глюкокортикоиды и гепарин натрия. Если возникает риск проявления фиброзных аномалий, то назначается гиалуронидаза, пирогенал, пеницилламин. Важное значение имеет устранение побочных воздействий антибиотиков, для чего рекомендуются антигистаминные средства, пиридоксин, глутаминовая кислота, пирацетам. Для укрепления защитных функций внутреннего органа используются иммуномодуляторы и иммунокорректоры. Особо выделяется применение поливалентных патогенетических препаратов, которые могут предотвращать и устранять некоторые патологические изменения.
Патогенетическое лечение назначается с учетом переносимости человеком лекарственных средств и степени устойчивости бактерий к ним. Вид терапии зависит от этапа развития болезни и применяемого противотуберкулезного лечения. В первой фазе патогенетическая терапия туберкулеза использует противовоспалительные и антигипоксические препараты, направленные на устранение побочных воздействий и выведение токсико-аллергических веществ. На втором этапе лечения патогенетическая терапия применяет методы активизации репаративных процессов.
Важными препаратами, используемыми в патогенетической терапии, являются глюкокортикоиды. Они уменьшают миграцию клеток из сосудов, оказывают противовоспалительное действие, обладают иммунодепрессивным и антигистаминным свойствами, участвуют в подавлении биологического синтеза коллагена. К наиболее эффективным препаратам этого ряда можно отнести преднизолон, триамианолон, дексаметазон. Они достаточно надежно помогают бороться с туберкулезом первого типа течения.
Туберкулез характеризуется специфичным патогенезом и этиологией. При лечении туберкулеза важно учитывать патогенетические процессы.
Использование методов патогенетической терапии позволяет повысить эффективность медикаментозного лечения.
1tuberkulez.ru
Этиология и патогенез туберкулеза легких (фтизиатрия)
 Этиология и патогенез туберкулеза легких (фтизиатрия).
Этиология и патогенез туберкулеза легких (фтизиатрия).
Туберкулезом болеет множество людей в мире.
По данным статистики, болезни подвержены люди с низким уровнем жизни (бомжи, наркоманы, алкоголики, проститутки), а также медицинские работники, которые обслуживают данный контингент.
Мужчины болеют чаще женщин. Это объясняется тем, что у мужской части населения чаще встречаются вредные привычки и характерна меньшая устойчивость к стрессам.
Туберкулезная микобактерия

В 19 веке Робертом Кохом открыта палочка туберкулеза (Mycobacterium tuberculosis). Существует около 100 штаммов бактерий.
Палочка микобактерии очень устойчива к факторам внешней среды.
При высыхании биоматериала (слюна, мокрота) бактерии сохраняются около двух недель.
Если материал остается влажным – до одного месяца. В водной среде сохраняют жизнеспособность больше года.
При высоких температурах, около 80 градусов, бациллы гибнут в течение 5 минут.
Микобактерия не обладает способностью к самостоятельному передвижению.
Размножение происходит медленно при помощи простого деления.
Особенность полочки в том, что она поражает ткани с высоким содержанием кислорода.
Этиология и патогенность микобактерии

Микобактерия не позволяет защитным клеткам крови (макрофагам) разрушить себя. Этому способствуют некоторые вещества мембраны клетки.
Корд фактор — первое защитное вещество, позволяющее расти бактерии вне человеческого организма.
Второе вещество — сульфатиды, они препятствуют слиянию макрофагальных фагосом с лизосомальной клеткой.
Третьим защитным фактором является гетерополисахарид (LAM), который не дает активироваться макрофагам клеткам.
Существует теория, что именно этот сахарид участвует в формировании фактора некроза опухоли (TNF).
Последний фактор патогенности — шоковый температурный белок.
При помощи этого белка происходит фагоцитоз микобактерии макрофагом без последующего ее разрушения.
В данном процессе участвуют специфические рецепторы на поверхности мембраны.
При длительном лечении заболевания или других факторов, микобактерия способна превращаться в малопатогенную L-форму, которая мирно существует в организме, обеспечивая иммунную защиту.
Инфекционный процесс запускается, если происходит ослабление иммунитета.
Провоцирующим фактором в развитии туберкулеза является патология эндокринной, дыхательной и сердечно-сосудистой систем.
Пути проникновения в организм

Существуют два основных способа попадания в организм: аэрогенный, через воздух, (при чихании и кашле бактерии разносятся на расстояние около двух метров) и алиментарный, через употребления зараженного молока.
Очень редкий путь передачи через плаценту, от матери к ребенку.
Алиментарный путь заражения практически искоренен во многих странах, по причине государственного надзора над молочной продукцией, но остается проблемой для экономически неразвитых стран, где уровень жизни ниже среднего.
Доказана взаимосвязь между наличием гена HLA в организме и приверженности к появлению туберкулеза.
Основным источником туберкулеза является больной человек или носитель болезни без ее проявления (бактерионоситель).
Для заражения необходим длительный и тесный контакт человека с носителем инфекции.
Семьи, детские сада, рабочие коллективы – группы риска при контакте с бациллоносителем.
Только изоляция такого контингента избавляет от заражения других членов общества.
Патогенетические основы туберкулеза

Существуют несколько ключевых факторов в патогенезе развития туберкулеза.
К ним относятся: показатель вирулентности микобактерии (возможность разрушать ткани и подвергать их казеозному некрозу) и фактор чувствительности человеческого организма к возбудителю.
Основные антигены микобактерии — это туберкулиновые белки. В практике используется туберкулин для определения содержания в организме бациллы.
Во внешней оболочке содержатся вещества, которые вызывают воспаление в организме и в результате образуется гранулема.
Вместе с ней проявляется гиперчувствительность, имеющая замедленный тип или ответ иммунитета IV типа.
Данная реакция используется при проведении туберкулиновой пробы для оценки ответа организма на введенный белок.
В месте внутрикожной инъекции через двое суток оценивается кожный покров. У носителей инфекции в месте укола появляется участок индурации.
В несенсибилизированном организме бактерии размножаются очень быстро и покидают первичный очаг. По лимфатическим путям попадают в отдаленные органы и ткани.
После этого процесс становится генерализованным. У сенсибилизированных людей, при помощи макрофагов, процесс распространения бацилл по организму останавливается, но происходит тяжелый некроз тканей.
Попавшие в организм палочки туберкулеза могут вызывать разные типы воспалительного ответа:
- альтернативная тканевая реакция или очень тяжелый воспалительный ответ, который происходит в виде казеозного распада тканей. Характерен данный тип реакции для людей с ослабленным иммунитетом. Альтернативная реакция может привести к смертельному исходу.
- экссудативная реакция протекает с формированием экссудата. В состав экссудата входит большое количество лимфоцитов. Они подвергаются казеозному некрозу вместе с воспаленными тканями. Этот тип реакции наблюдается у людей, впервые столкнувшихся с микобактерией.
- пролиферативное воспаление обычно заканчивается благоприятно. В организме начинают активизироваться реакции иммунитета, формирование гранулемы и бугорка туберкулеза. В составе бугорка содержится большое количество клеток (многоядерные клетки, лимфоциты, макрофаги) и отсутствуют кровеносные сосуды. Они способны к казеозному некрозу. Постепенно туберкулезные бугорки рубцуются или, при неблагоприятном течении, распадаются. При распаде инфекционный процесс продолжается.
Этапы в патогенезе туберкулеза

Первым этапом происходит инфицирование организма. Бактерионоситель выделяет бациллы во внешнюю среду при чихании, кашле, разговоре.
Частицы высыхают и превращаются в пыль, которую вдыхает здоровый человек. С потоком воздуха, через бронхи, они попадают в альвеолы и поглощаются макрофагами.
Дальнейший процесс зависит от реакции организма и способности макрофагов ликвидировать инфекцию.
При выживании микобактерии, начинается второй этап патогенеза – диссеминация.
Палочки начинают размножаться в альвеолах и уничтожать макрофаги, Т-киллеры и лимфоциты.
Затем бациллы с током крови перемещаются в лимфатическую систему и распространяются по всему организму.
Третьим этапом является иммунный ответ организма. Многие люди обладают устойчивостью к проявлению туберкулеза на протяжении жизни.
У людей с ослабленным иммунитетом происходит прогрессирование болезни.
Формируются цитокины, которые стремительно повреждают клетки и ткани, что приводит к появлению очагов в легких. Некроз легочного очага приводит к образованию полости.
Опасной формой туберкулеза является скрытая инфекция, при которой клинические проявления отсутствуют, а выделение бацилл в окружающую среду продолжается.
Причинами являются неразвившийся первичный процесс и не законченный перенесенный туберкулез.
Видео по теме
tuberkulezstop.ru
причины, симптомы, диагностика и лечение
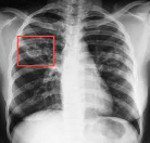
Туберкулез – хроническая инфекция, вызываемая бактериями Mycobacterium tuberculosis complex. При поражении туберкулезными микобактериями чаще всего страдают органы дыхания, кроме того, встречается туберкулез костей и суставов, мочеполовых органов, глаз, периферических лимфоузлов. Диагностика туберкулеза состоит в проведении туберкулиновой пробы, рентгенологического исследования легких, выявлении микобактерий туберкулеза в мокроте, смывах с бронхов, отделяемом кожных элементов, дополнительном инструментальном обследовании пораженных туберкулезом органов. Лечение туберкулеза представляет собой комплексную и длительную системную антибиотикотерапию. По показаниям проводится хирургическое лечение.
Общие сведения
Туберкулез – хроническая инфекция, вызываемая бактериями Mycobacterium tuberculosis complex. При поражении туберкулезными микобактериями чаще всего страдают органы дыхания, кроме того, встречается туберкулез костей и суставов, мочеполовых органов, глаз, периферических лимфоузлов. Наиболее часто инфицирование происходит воздушно-капельным путем, реже — контактным или алиментарным.
Причины туберкулеза
Характеристика возбудителя
Mycobacterium tuberculosis complex представляет собой группу видов бактерий, способных вызывать у человека туберкулез. Наиболее часто возбудителем является Mycobacterium tuberculosis (устар. – палочка Коха), представляет собой грамположительные кислотоустойчивые палочки семейства актиномицетов, рода микобактерий. В редких случаях туберкулез вызывается другими представителями этого рода. Эндотоксинов и экзотоксинов не выделяют.
Микобактерии крайне устойчивы к воздействию окружающей среды, длительно сохраняются вне организма, но погибают под воздействием прямого солнечного света и ультрафиолетового облучения. Могут образовывать маловирулентные L-формы, способствующие при присутствии в организме формировать специфический иммунитет без развития заболевания.
Механизм заражения
Резервуаром инфекции и источником заражения туберкулезом являются больные люди (чаще всего заражение происходит при контакте с больными туберкулезом легких в открытой форме – когда туберкулезные бактерии выделяются с мокротой). При этом реализуется респираторный путь заражения (вдыхание воздуха с рассеянными бактериями). Больной с активным выделением микобактерий и выраженным кашлем способен в течение года заразить более десятка человек.
Инфицирование от носителей со скудным выделением бактерий и закрытой формой туберкулеза возможно только при близких постоянных контактах. Иногда случается заражение алиментарным (бактерии попадают в пищеварительный тракт) или контактным путем (через повреждения кожных покровов). Источником заражения может стать больной крупнорогатый скот, домашняя птица. Туберкулез при этом передается с молоком, яйцами, при попадании испражнений животных в водные источники. Далеко не всегда попадание туберкулезных бактерий в организм вызывает развитие инфекции. Туберкулез – заболевание, зачастую связанное с неблагоприятными условиями жизни, снижением иммунитета, защитных свойств организма.
Патогенез
В течении туберкулеза выделяют первичную и вторичную стадии. Первичный туберкулез развивается в зоне внедрения возбудителя и характеризуется высокой чувствительности к нему тканей. В первые же дни после заражения активизируется иммунная система, вырабатывая специфические антитела для уничтожения возбудителя. Чаще всего в легких и внутригрудных лимфоузлах, а при алиментарном или контактном пути инфицирования – и в желудочно-кишечном тракте и коже, формируется очаг воспаления. При этом бактерии могут рассеиваться с током крови и лимфы по организму и формировать первичные очаги в других органах (почках, костях, суставах).
Вскоре первичный очаг заживает, а организм приобретает стойкий противотуберкулезный иммунитет. Однако при снижении иммунных свойств (в юношеском или старческом возрасте, при ослаблении организме, синдроме иммунодефицита, гормональной терапии, сахарном диабете и др.) происходит активизация инфекции в очагах и развивается вторичный туберкулез.
Классификация
Туберкулез различают на первичный и вторичный. Первичный в свою очередь может быть долокальным (туберкулезная интоксикация у детей и подростков) и локализованным (первичный туберкулезный комплекс, представляющий собой очаг в месте проникновения инфекции, и туберкулез внутригрудных лимфатических узлов).
Вторичный туберкулез различается по локализации на легочные и нелегочные формы. Легочный туберкулез в зависимости от распространенности и степени поражения бывает милиарный, диссеминированный, очаговый, инфильтративный, кавернозный, фиброзно-кавернозный, цирротический. Также выделяют казеозную пневмонию и туберкулему. В качестве отдельных форм выделен туберкулезный плеврит, эмпиема плевры и саркоидоз.
Вне легких встречается туберкулез головного и спинного мозга и мозговых оболочек, туберкулез кишечника, брюшины, мезентериальных лимфоузлов, костей, суставов, почек, половых органов, молочных желез, кожи и подкожной клетчатки, глаз. Иногда отмечается поражение других органов. В развитии туберкулеза выделяют фазы инфильтрации, распада, обсеменения, рассасывания, уплотнения, рубцевания и обызвествления. В отношении выделения бактерий различают открытую форму (с выделением бактерий, МБТ-положительную) и закрытую (без выделения, МБТ-отрицательную).
Симптомы туберкулеза
В силу многочисленности клинических форм, туберкулез может проявляться самыми разнообразными симптомокомплексами. Течение заболевания хроническое, обычно начинается постепенно (долгое время может протекать бессимптомно). Со временем, проявляются симптомы общей интоксикации – гипертермия, тахикардия, слабость, снижение работоспособности, потеря аппетита и похудание, потливость. При прогрессировании инфекции и ее распространении по организму интоксикация может быть довольно интенсивной. Больные значительно теряют в массе тела, черты лица заостряются, появляется болезненный румянец. Температура тела не поднимается выше субфебрильных цифр, но держится продолжительное время. Лихорадка возникает только в случае массивного поражения.
- Туберкулез легких, как правило, сопровождается кашлем (первоначально сухим), обостряющимся ночью и с утра. Существование упорного кашля на протяжении более чем трех недель является тревожным симптомом, и следует в таких случаях обязательно обращаться к врачу. При прогрессировании заболевания может появляться кровохарканье. Туберкулез легких может осложниться опасным для жизни состоянием – легочным кровотечением.
Туберкулез других органов и систем случается намного реже и выявляется, как правило, после исключения других патологий.
- Туберкулез мозговых оболочек и головного мозга. Развивается постепенно на протяжении 1-2 недель, чаще всего у детей и лиц с иммунодефицитом, у больных сахарным диабетом. Первоначально, помимо симптомов интоксикации, появляются расстройства сна, и головные боли, со второй недели заболевания присоединяется рвота, головная боль становится интенсивной и упорной. К концу первой недели отмечается менингеальная симптоматика (ригидность затылочных мышц, симптомы Кернига и Брудзинского), неврологические расстройства.
- Туберкулез органов пищеварительного тракта характеризуется сочетанием общей интоксикации с нарушением стула (запоры, чередующиеся с поносами), симптоматикой диспепсии, болью в животе, иногда кровянистыми примесями в кале. Туберкулез кишечника может способствовать развитию непроходимости.
- Туберкулез костей, суставов и позвоночника. При туберкулезе суставов отмечается симптоматика артритов (боль в пораженных суставах, ограничение в подвижности), При поражении костей отмечается их болезненность, склонность к переломам.
- Туберкулез органов мочеполовой системы. При локализации очага инфекции в почках больные отмечают симптоматику нефрита, боль в спине, возможно появление крови в моче. Довольно редко может развиваться туберкулез мочевыводящих путей, в этом случае проявлениями будет дизурия (нарушение процесса мочеиспускания), болезненность при мочеиспускании. Туберкулез половых органов (генитальный туберкулез) может быть причиной бесплодия.
- Туберкулез кожи характеризуется появлением плотных узелков под кожей, при прогрессировании увеличивающихся и вскрывающихся на кожу с выделением белых творожистых масс.
Осложнения
Диагностика
Диагностика туберкулеза легких
Поскольку зачастую туберкулез первое время протекает бессимптомно, значительную роль в его диагностике играют профилактические обследования. В диагностике легочной формы туберкулеза применяются:
- Методы скрининга. Взрослым ежегодно необходимо произвести флюорографию органов грудной клетки, детям – пробу Манту (методика туберкулинодиагностики, выявляющая степень инфицированности организма туберкулезной палочкой и реактивности тканей). В качестве альтернативы туберкулиновой пробе и диаскин-тесту предложены лабораторне методики, позволяющие выявить латентную и активную тубинфекцию: T-SPOT тест и квантиферон-тест.
- Топическая лучевая диагностика. Основным методом диагностики туберкулеза является рентгенография легких. При этом можно обнаружить очаги инфекции, как в легких, так и в других органах и тканях. При необходимости выполняют КТ легких.
- Исследование биологических сред. Для определения возбудителя производят посев мокроты, промывных вод бронхов и желудка, отделяемого из кожных образований. При невозможности высеять бактерию из биологических материалов, можно говорить о МКБ-отрицательной форме.
- Биопсия. В некоторых случаях для уточнения диагноза проводят бронхоскопию с биопсией, биопсию лимфатических узлов.
Диагностика внелегочного туберкулеза
Данные лабораторных анализов неспецифичны и указывает на воспаление, интоксикацию, иногда (протеинурия, кровь в кале) могут говорить о локализации очага. Однако всестороннее исследование состояния организма при туберкулезе имеет значение при выборе тактики лечения.
При подозрении на внелегочную форму туберкулеза нередко прибегают к более углубленной, чем Манту, туберкулиновой диагностике – пробе Коха. Диагностику туберкулезного менингита или энцефалита нередко проводят неврологи. Пациента обследуют при помощи реоэнцефалографии, ЭЭГ, КТ или МРТ головного мозга. Для выделения возбудителя из ликвора производят люмбальную пункцию.
При развитии туберкулеза органов пищеварения необходима консультация гастроэнтеролога, УЗИ органов брюшной полости, копрограмма. Туберкулез опорно-двигательной системы требует проведения соответствующих рентгенологических исследований, КТ позвоночника, артроскопии пораженного сустава. К дополнительным методам обследования при туберкулезе мочеполовой системы относится УЗИ почек и мочевого пузыря. Пациенты с подозрением на туберкулез кожи нуждаются в консультации дерматолога.
Лечение туберкулеза
Лечение туберкулеза направлено на заживление очагов и ликвидацию симптоматики. Запущенный туберкулез поддается лечению заметно хуже, чем своевременно выявленный, даже более тяжелого течения (деструктивные формы). Лечение туберкулеза занимает год и более, является комплексным (сочетает методы медикаментозной терапии, физиотерапию). Первоначально лечение проводят в туберкулезном диспансере до прекращения выделения микроорганизмов. После чего больные выписываются для продолжения амбулаторного лечения. Пациентам, прошедшим курс терапии туберкулеза рекомендовано лечение в специализированных санаториях и профилакториях.
Хирургическое лечение показано в случаях, когда консервативная терапия не достаточна для достижения излечения (кавернозная форма туберкулеза легких, различные осложнения). Наиболее частой хирургической методикой лечения туберкулеза является частичная резекция легкого с иссечением пораженных сегментов. Применяется также оперативная коллапсотерапия. Пациентам, страдающим туберкулезом, назначается специальная высококалорийная диета (стол №11), богатая легкоусвояемым белком, витаминами С и группы В.
Постельный режим прописан только больным с высокой степенью деструкции легких, выраженным кровохарканьем. В остальных случаях больным рекомендованы прогулки, лечебная физкультура, активная физическая деятельность.
Прогноз
В настоящее время в большинстве случаев при своевременном выявлении и соблюдении необходимых лечебных мер прогноз благоприятный – происходит заживление туберкулезных очагов и стихание клинических признаков, что можно считать клиническим выздоровлением. После лечения в месте локализации очагов могут оставаться рубцы, участки фиброза, инкапсулированные очаги, содержащие бактерии в дремлющем состоянии. При ухудшении состояния организма возможно рецидивирование заболевания, поэтому больные после клинического излечения находятся на диспансерном учете у фтизиатра и подвергаются регулярному обследованию. После перенесения и излечения туберкулеза туберкулиновая проба остается положительной.
В случае отсутствия лечения или несоблюдения рекомендаций смертность от туберкулеза достигает 50% случаев. Кроме того, прогноз ухудшается у лиц пожилого возраста, ВИЧ-инфицированных и людей, страдающих сахарным диабетом.
Профилактика
Профилактические меры, проводимые специализированными противотуберкулезными лечебными учреждениями вместе с заведениями общего лечебного профиля, включают профилактические осмотры граждан (обязательная ежегодная флюорография), выявление больных, страдающих открытыми формами туберкулеза, их изолирование, обследование контактных лиц, специфическую профилактику туберкулеза.
Специфическая профилактика (вакцинация) направлена на формирование противотуберкулезного иммунитета, включает введение вакцины БЦЖ или профилактических химических средств. У лиц, вакцинированных БЦЖ, туберкулез протекает в более легких, доброкачественных формах, проще поддается лечению. Иммунитет обычно формируется через 2 месяца после вакцинации и стухает через 5-7 лет. Меры химиопрофилактики применяются среди лиц с повышенным риском заражения: лицам, контактировавшим с больными туберкулезом с отрицательной туберкулиновой пробой (первичная химиопрофилактика) и инфицированным лицам (вторичная).
www.krasotaimedicina.ru
Этиология туберкулеза
Возбудителем туберкулеза являются микобактерии туберкулеза (МБТ), которые в 1882 г. открыл Роберт Кох.
Классификация микобактерий
Домен: Baсteria; Отдел: Актиномицеты; Порядок: Actinomycetales; Подпорядок: Corynebacterineae; Семейство: Mycobacteriaceae; Род: Mycobacterium.
Основным признаком, по которому микобактерии были отнесены к тому или другому виду, является различная патогенность их для разных видов животных и для человека. По патогенным свойствам род Mycobacterium подразделяют на две группы:
1) патогенные и условно-патогенные (потенциально патогенные). 2) сапрофиты.
В настоящее время используется разделение клинически значимых микобактерий на комплексы:
комплекс M. tuberculosis – микобактерии туберкулезного комплекса – это комплекс микобактерий, вызывающих туберкулез (M. tuberculosis, M. bovis, M. bovisBCG, M. africanum, M. microti, M. canetti),
комплекс M. avium (M. avium, M. intracellulare),
комплекс M. fortuitum,
комплекс M. terrae.
Такая классификация позволяет объединить виды микобактерий одинаковой клинической значимости. Более тонкая характеристика их до видов в большинстве клинических случаев не требуется. Патогенными для человека является только МБТ человеческого, бычьего и африканского типов.
По скорости роста род Mycobacterium подразделяют на 3 группы:
Быстрорастущие — крупные видимые колонии появляются ранее 7-го дня инкубации (18 видов).
Медленнорастущие — крупные видимые колонии появляются после 7 и более дней инкубации (20 видов).
Микобактерии, которые требуют специальных условий для роста или не растут на искусственных питательных средах. К этой группе относятся два вида: М. leprae и M. lepraemurium.
По способности к пигментообразованию микобактерии также делят на 3 группы:
1. Фотохромогенные — образуют пигмент лимонно-желтого цвета при росте на свету.
2. Скотохромогенные — образуют пигмент оранжево-желтого цвета при инкубировании в темноте.
3. Нефотохромогенные — пигмента не образуют (независимо от наличия света), иногда культуры имеют светло-желтоватую окраску.
МБТ имеют продолговатый палочковидый вид длиной 1-6 мкм и шириной 0,2-0,5 мкм, неподвижные, имеют большой полиморфизм. Размножение происходит в основном путем простого клеточного деления. Споры и капсулы не образуют. Растут медленно, оптимальная температура роста 37-38°С. Удвоение МБТ наступает через 20-24 часов. При снижении температуры к 29°С, или повышении к 45°С рост МБТ прекращается. За ростовыми свойствами выделяют МБТ, которые растут быстро или медленно и МБТ, что находятся в латентном состоянии. Электронно-микроскопическое исследование МБТ позволило дифференцировать в них микрокапсулу, многослойную клеточную мембрану, цитоплазму с органеллами (гранулы, вакуоли, рибосомы) и ядерную субстанцию (нуклеотид).
Отличительным свойством МБТ является химическая устойчивость, которая проявляется в способности сохранять окраску даже при интенсивном обесцвечивании кислотами, щелочами и спиртом, что обусловлено высоким содержанием в клеточных стенках МБТ миколевой кислоты (С88Н17604), липидов и белков. Микрокапсула состоит из полисахаридов и играет важную роль в жизнедеятельности МБТ, в том числе придает им устойчивость к неблагоприятным воздействиям внешней среды.
Толстая клеточная стенка, насыщенная липидами, ограничивает клетку снаружи, обеспечивая механическую и осмотическую защиту. Стенка МБТ состоит из четырех слоев. Первый, внутренний, слой образован пептидогликаном; последующие слои включают в себя миколевые кислоты, гликолипиды, воск и корд-фактор, связывающий отдельные клетки в косы и оказывающий токсическое действие на макрофаги при фагоцитозе. Такой состав клеточной стенки определяет устойчивость МБТ к воздействию кислот и щелочей, а также высокую гидрофобность клетки в целом.
Согласно современным представлениям, в состав цитоплазматической мембраны, расположенной под клеточной стенкой, входят липопротеидные комплексы. С мембраной связаны ферментные системы. В цитоплазматической мембране осуществляются процессы, ответственные за специфичность реакций МБТ клетки на факторы окружающей среды.
Цитоплазма МБТ состоит из гранул и вакуолей различной величины. Основная часть мелкогранулярных включений представлена рибосомами, на которых синтезируется специфический белок. Ядерная субстанция М БТ определяет специфические свойства клетки, важнейшими из которых являются синтез белка и передача наследственных признаков потомству.
Для нормального развития МБТ нуждаются в кислороде, поэтому их относят к аэробам. Потребление кислорода микробной клеткой связано с окислительно-восстановительным и процессами в тканях макроорганизма. При формировании гранулем размножение МБТ из-за снижения в них парциального давления кислорода (Р02) замедляется, однако имеются сведения, что некоторые виды МБТ можно рассматривать, как факультативные анаэробы.
В настоящее время полностью расшифрован геном МБТ. Он имеет длину 4 411 529 пар нуклеотидов, которые почти в 70% представлены гуанином и цитозином. Нуклеотид содержит 4000 генов, из которых 60 кодируют компоненты РНК. Для МБТ имеются уникальные гены, в частности гены mtp40n mpb 70, которые применяются для выявления МБТ в полимеразно-цепной реакции (ПЦР).
В естественных условиях МБТ устойчивые к факторам внешней среды и сохраняют жизнеспособность в течение нескольких месяцев. В жидкой среде МБТ погибают при кипячении через 5 минут, а в сухой мокроте при температуре 100° С – через 45 минут. Под воздействием солнечных лучей они погибают через 1-2 минуты, а в мокроте – через 4 часа. Под воздействием дезинфицирующих средств (хлорамин, пюржавель, жавелион, дезоксон-1 и 4, клорсепт и т.д.) МБТ погибают через 3-5 часов. Под воздействием неблагоприятных условий и противотуберкулезных препаратов МБТ способные к изменчивости: они трансформируются в более стойкие, не чувствительные к этим условиям формы (фильтрующиеся, L- формы) – персистенция МБТ, но при благоприятных условиях они способны к реверсии – приобретать классическую форму МБТ с патогенными свойствами. При этом у них может формироваться резистентность к противотуберкулезным препаратам (ПТП).
Патогенность– основной видовой признак МБТ — возможность МБТ вызвать заболевание. Главный фактор патогенности — токсичный гликолипид — корд-фактор. Корд-фактор обусловливает токсическое действие на ткани и защищает МБТ от элиминации.
Вирулентность— степень патогенности; возможность роста и размножения микобактерий в определенном макроорганизме и способность вызвать специфические патологические изменения в органах. Вирулентным считают штамм микобактерий, если он в дозе 0,1- 0,01 мг вызывает заболевание туберкулезом, а через 2 месяца — смерть морской свинки массой 250-300 г. Если после введения этой дозы животные умирает через 5-6 месяцев, то этот штамм считают слабовирулентным. У МБТ не выявлено каких-либо эндотоксинов, экзотоксинов или гистолитических ферментов. Их патогенное действие связано, главным образом, со способностью избегать губительного влияния макрофагов и вызывать реакции гиперчувствительности замедленного типа. Это обеспечивается5 компонентами клеточной стенки МБТ. Первым таким компонентом являетсякорд-фактор (фактор жгутообразования), «вынуждающий» МБТ растиin vitroв виде извитых жгутов. Вирулентные штаммы возбудителя имеют этот фактор на поверхности бактериальной клетки, а авирулентные штаммы им не обладают. Доказано, что введение очищенного корд-фактора подопытным мышам вызывает у них формирование типичных туберкулезных гранулем. Вторым компонентом считаютсясульфамиды, представляющие собой серосодержащие гликолипиды бактериальной поверхности и присущие тоже только вирулентным штаммам. Они предупреждают слияние фагосом макрофагов, содержащих фагоцированные МБТ, с лизосомами. Третий компонент клеточной стенки —фактор, подавляющий активацию макрофагов — липоарабиноманнан (LAM-фактор). Он представляет собой главный гетерополисахарид, по строению сходный с эндотоксином грамотрицательных микробов и выполняющий функцию подавления ИФН-γ. LAM обеспечивает также выработку макрофагами ФНО-а, вызывающего лихорадку, снижение массы тела и повреждение тканей, а также выработку интерлейкина-10, тормозящего пролиферацию Т-лимфоцитов. Четвертым компонентом является высокоиммуногенныйбелок теплового шока с молекулярной массой 65 кДа. Этот белок возбудителей туберкулеза, по строению сходный с белками теплового шока человека, возможно, играет определенную роль в развитии аутоиммунных реакций, вызываемых микобактериями. Пятый компонент —комплемент, активированный на поверхности микобактерии и способный опсонизировать возбудителей и облегчать их поглощение посредством макрофагального комплементного рецептора CR3 (интегрина МАС-1).
Микобактерии выделяются в различных странах мира от людей, теплокровных и холоднокровных животных, страдающих заболеваниями легких, кожи, мягких тканей и лимфатических узлов. Эти заболевания получили название микобактериозов, которые вызываются представителями рода нетуберкулезными микобактериями (НТМБ), по клинической картине иногда очень схожи с туберкулезом. В среднем распространенность НТМБ в ряде территорий России составила от 0,5 до 6,2%. Наиболее часто встречаемые виды – M.avium—intracellularae, вызывающий до 60% случаев микобактериозов легких,M.kansasii, M.xenopiiи другие. Микобактериозы часто встречаются у больных с ВИЧ-инфекцией, являясь своеобразным маркером иммунодефицита человека. Другие виды микобактерий, такие какM.smegmatis,могут обнаруживаться на внешних тканях и органах в качестве сапрофитов. Отдельную группу составляют возбудители проказыM.leprae.
Различают три типа микобактериозов, зависящих от вида МБТ и иммуннитета:
I. Генерализованные инфекции с развитием видимых невооруженным глазом патологических изменений, внешне напоминающих туберкулезные, но гистологически несколько отличающиеся от них.
II. Локализованные инфекции, характеризующиеся наличием макро — и микроскопических поражений, выявляемых в определенных участках тела.
III. Инфекции, протекающие без развития видимых поражений; возбудитель обнаруживается в лимфатических узлах внутриклеточно или внеклеточно.
studfile.net
Туберкулёз известен с глубокой древности и до сих пор представляет важную медицинскую и социальную проблему. Ежегодно в мире 8 млн человек заболевают, а 3 млн — умирают от туберкулёза. Величина пандемии настолько велика, что в 1993 г. ВОЗ объявила туберкулёз проблемой «великой опасности». В последние годы во всём мире повысилась заболеваемость туберкулёзом. Основные причины повышения заболеваемости: снижение уровня жизни населения, повлекшее ухудшение качества питания; возросшая миграция населения из эпидемически неблагополучных районов, уменьшение масштабов и качества проведения комплекса противотуберкулёзных мероприятий и появление устойчивых в специфической терапии штаммов. Чтобы снизить остроту проблемы, ВОЗ определила в качестве главных компонентов программы борьбы с этой болезнью активное выявление больных и иммунизацию против туберкулёза. Этиология Туберкулёз у человека вызывают микобактерии: в 92% случаев — Mycobacterium tuberculosis, в остальных случаях — М. bovis (вид, вызывающий туберкулёз у крупного рогатого скота и человека). М. tuberculosis — неподвижные тонкие палочки, аэробы. Кислотоустойчивы, для их окрашивания необходима особая методика (по Цилю-Нильсену). Возбудитель может размножаться как в макрофагах, так и внеклеточно. Палочки устойчивы во внешней среде: на страницах книг сохраняются 3-4 мес, в уличной пыли — 10 дней, в воде — до года, в замороженном состоянии — десятилетиями. При УФО и кипячении погибают в течение нескольких минут. Медленно растут на классических питательных средах — появление первых колоний отмечают через 4-8 нед. Эпидемиология Туберкулёзом болеют люди всех возрастных групп — от новорождённых до лиц старческого возраста. Источники инфекции: больной человек, мясо-молочные продукты от животных, больных туберкулёзом. Пути передачи: чаще — воздушно-капельный, реже — алиментарный; также возможен трансплацентарный путь инфицирования (от беременной к плоду). Факторы передачи инфекции — длительный контакт с бактериовыделителем, плохие социально-бытовые условия, голодание, иммунодепрессия. Контагиозность невысока, во многом зависит от состояния защитных сил макроорганизма. Сезонность и периодичность заболеваемости не характерны. Хотя туберкулёз не относят к высококонтагиозным заболеваниям, 25-50% людей, тесно контактирующих с бактериовыделителями, инфицируются. Каждый больной-бацилловыделитель способен заразить 10-15 человек. Следует помнить, что заразиться туберкулёзом — не значит заболеть. Манифестная форма туберкулёза развивается в 5-15% случаев, у остальных заражённых формируется нестерильный иммунитет. Почти в 90% случаев не удаётся установить источник инфицирования, что свидетельствует о наличии значительного резервуара туберкулёзной инфекции среди населения. Риск развития заболевания тем выше, чем младше ребёнок в период инфицирования. Патогенз Патогенез складывается из трёх основных этапов: инфицирования, развития первичного очага в каком-либо органе, прогрессирования заболевания с появлением новых симптомов. Проникновение микобактерий в первичный очаг даёт начало процессу взаимодействия макро- и микроорганизма. Одна часть возбудителей остаётся на месте внедрения, другая часть попадает с макрофагами в регионарные лимфатические узлы. Первичный очаг, лимфангиит и регионарный лимфаденит образуют первичный туберкулёзный комплекс. Фагоцитарные реакции незавершённые, поэтому в области первичного туберкулёзного комплекса микобактерий размножаются и, периодически попадая в кровеносные и лимфатические сосуды, разносятся по всему организму. Первичная бактериемия клинически никак не проявляется. Спустя 4-8 нед развивается сенсибилизация, туберкулиновые пробы становятся положительными (вираж). Формируется «нестерильный» иммунитет. У большинства детей и взрослых развивающиеся защитные реакции подавляют инфекционный агент в зоне первичного аффекта, последний постепенно фиброзируется и обызвествляется. В противном случае микобактерий могут распространиться из первичного очага на близлежащие ткани или по току крови в отдалённые органы, вызывая в них прогрессирующие морфологические изменения. Проявлением этого процесса на начальных этапах становятся параспецифические, аллергические и токсико-аллергические реакции, соответствующие понятию «ранняя туберкулёзная интоксикация». Особенность туберкулёзной инфекции — длительное (в течение многих лет, а иногда и пожизненное) сохранение жизнеспособного возбудителя в первичном очаге, лимфатических узлах, очагах диссеминации. Ослабление организма, снижение иммунитета при инфекционных (корь, вирусный гепатит, ВИЧ-инфекция) и других заболеваниях приводят к активации казалось бы полностью «заживших» очагов. Классификация В соответствии с существующей классификацией 1973 г., принятой на VIII Всесоюзном съезде фтизиатров, выделяют 3 группы основных клинических форм туберкулёза.
Клиническая картина Клиническая картина туберкулёза зависит от места внедрения микобактерий, фазы патологического процесса, наличия осложнений. Заболевание развивается медленно, может продолжаться долго, иногда десятилетиями. У детей и подростков чаще выявляют первичный туберкулёз, возникающий при заражении микобактериями туберкулёза ранее неинфицированного организма. Среди всех форм первичного туберкулёза преобладает туберкулёз внутригрудных лимфатических узлов, реже диагностируют туберкулёзную интоксикацию, первичный туберкулёзный комплекс, плеврит и др. Чаще всего при туберкулёзе у детей поражаются лёгкие (85,3% среди локальных форм туберкулёза). Внелёгочные формы возникают в результате гематогенной диссеминации инфекции из первичного очага. Преобладают симптомы интоксикации, признаки локального воспаления выражены меньше. Характерно состояние гиперсенсибилизации, проявляющееся параспецифическими реакциями. Чем младше заболевший ребёнок, тем выше вероятность развития тяжёлых локальных и генерализованных форм туберкулёза. Ниже представлены наиболее частые или тяжёлые клинические формы туберкулёза у детей. Туберкулёзная интоксикация у детей и подростков Это самая частая форма болезни. Развивается обычно в дошкольном и младшем школьном возрастах. Появляются субфебрилитет, повышенная раздражительность, утомляемость, нарушения сна, аппетита. При осмотре можно выявить бледность кожи, снижение массы тела, тургора мягких тканей, микрополиадению. При этой форме туберкулёза иногда возникают следующие параспецифические проявления.
Для диагностики туберкулёзной интоксикации важно обнаружение виража туберкулиновых проб — впервые выявленной положительной реакции Манту или увеличение размеров папулы на 6 мм и более по сравнению с данными предыдущей реакции. При инструментальном исследовании внутренних органов специфического поражения выявить не удаётся. Исходы. Инфекционный процесс может годами протекать волнообразно с возможным самоизлечением после формирования иммунитета или переходом в локальную форму. Первичный туберкулёзный комплекс Протекает бессимптомно (до развития осложнений) и может быть обнаружен только при рентгенологическом исследовании. В таких случаях выявляют участок затенения в лёгком, увеличенные лимфатические узлы корня и связующую их «дорожку», образуемую тенью сосудов и бронхов. Осложнения. Пневмония, вовлечение плевры при субплевральной локализации очага. Исходы. При благоприятном течении происходит кальцификация лимфатических узлов и казеозного очага в лёгких, при осложнённом течении возможны развитие гематогенной диссеминации, ателектаза, лимфогенной диссеминации и образование каверны. Туберкулёзный бронхаденит Туберкулёз внутригрудных лимфатических узлов (туберкулёзный бронхаденит) — самая частая локальная форма первичного туберкулёза у детей. Увеличение лимфатических узлов приводит к сдавлению трахеобронхиального дерева. При нерезкой гиперплазии лимфатических узлов у больных появляются только признаки туберкулёзной интоксикации. При выраженном бронхадените развиваются довольно характерные клинические проявления: битональный, коклюшеподобный кашель, осиплость голоса, признаки хронической или острой интоксикации. Вследствие увеличения лимфатических узлов средостения возможно развитие локальных изменений: расширение подкожной венозной сети на коже груди, расширение поверхностной капиллярной сети в зоне С (симптом Франка), укорочение перкуторного звука над областью средостения. Аускультативная картина бедна. Для подтверждения диагноза проводят рентгенологическое исследование, а также бронхоскопию. Осложнения. Нарушение проходимости бронхов, туберкулёз бронхов, плеврит. Исходы. При благоприятном течении происходит кальцификация лимфатических узлов, при осложнённом течении возможны развитие гематогенной диссеминации, ателектаза, лимфогенной диссеминации и образование каверны. Диссеминированный туберкулёз лёгких У детей и подростков диссеминированный туберкулёз лёгких возникает редко, протекает в острой (милиарный туберкулёз лёгких) и подострой формах. Заболевание развивается вследствие обширного гематогенного распространения туберкулёзной инфекции. Начинается внезапно с фебрильной лихорадки. Быстро нарастают симптомы интоксикации, сухой кашель, одышка. Характерно несоответствие между выраженной дыхательной недостаточностью и минимальными изменениями в лёгких (по данным рентгенографии). Развиваются лимфаденопатия, гепатолиенальный синдром. При рентгенографии лёгких выявляют мелкие многочисленные тени по всем лёгочным полям (картина «снежной бури»), что позволяет установить диагноз. Бактериоскопия и бактериологическое исследование мокроты малоинформативны — мокрота редко содержит микобактерии. Более чувствительные и специфичные методы лабораторной диагностики — ПЦР и ИФА. Туберкулиновые пробы часто отрицательны (туберкулиновая анергия). Диагноз можно подтвердить трансбронхиальной биопсией. Осложнения. Сердечно-лёгочная недостаточность, анемия, гематогенные отсевы в различные органы, штампованные «очковые» каверны в верхних долях обоих лёгких (при подостром диссеминированном туберкулёзе). Исходы. Несвоевременная диагностика этой формы при отсутствии лечения приводит к гибели больного в течение нескольких месяцев («скоротечная чахотка»). Туберкулёз мочевых и половых органов В настоящее время это наиболее распространённая форма внелёгочного туберкулёза. Преимущественно поражаются почки. Клиническая картина мало отличается от неспецифического воспалительного процесса в мочевой системе и характеризуется пиурией и эритроцитурией. Для диагностики обязательно проводят бактериологический посев мочи, модифицированные туберкулиновые пробы (оценку степени лейкоцитурии после подкожного введения 2 ТЕ туберкулина), исследование крови методом ПЦР, а также УЗИ и рутинные рентгеноконтрастные исследования почек и мочевых путей. Осложнения. Кавернозный туберкулёз почки, стриктура мочеточников. Исходы. При адекватной своевременной терапии исход благоприятный. В противном случае развиваются осложнения и пионефроз, при котором необходимо удаление почки. Туберкулёз костей и суставов Туберкулёз костей и суставов возникает преимущественно у детей раннего возраста в течение первых 3 лет после инфицирования. Обычно страдают средние отделы позвоночника. Эрозия передней поверхности тел позвонков приводит к их спадению и выраженному кифозу без сколиоза. Клинические проявления: боль, ограничение подвижности, отёк поражённых отделов позвоночника. При прогрессировании процесс распространяется на нижележащие отделы, появляются «холодные абсцессы». Среди всех суставов туберкулёзом чаще всего поражаются тазобедренный и коленный суставы. Туберкулёзный артрит обычно протекает с выраженной экссудацией и хорошо поддаётся специфической терапии. Рентгенологические изменения позвоночника и суставов в виде деструкции костной и хрящевой тканей появляются поздно, в силу чего важное диагностическое значение имеет поиск первичного очага инфекции. Осложнения. При прогрессирующем спондилите возможно развитие натёчников — новых абсцессов, удалённых от основного очага, образовавшихся вследствие перемещения гноя по межмышечным пространствам. Исходы. Ранняя инвалидизация, образование горба, контрактура поражённого сустава. Туберкулёзный менингит Достаточно редкая, но прогностически неблагоприятная форма туберкулёза, развивающаяся преимущественно у детей раннего возраста. Заболевание начинается постепенно с изменения поведения ребёнка, общих симптомов недомогания, субфебрильной лихорадки. Позже появляются головная боль, светобоязнь, сонливость, менингеальные знаки, судороги, поражение черепных нервов, развивается кома. В диагностических целях показана поясничная пункция. Ликвор прозрачный, вытекает под давлением, на его поверхности (в термостате в течение суток) образуется фибриновая плёнка, в жидкости обнаруживают микобактерии туберкулёза. Для туберкулёзного менингита характерна белково-клеточная диссоциация — высокое содержание белка при низком лимфоцитарном плеоцитозе, что свидетельствует о блоке ликворных путей и преобладании застойных явлений над воспалительными. Осложнения. Отёк мозга, гипертензионно-гидроцефальный синдром. Исходы. Без лечения летальность при этой форме составляет 100%. Ранняя диагностика и специфическая терапия позволяют радикально улучшить прогноз. Диагностика Диагноз туберкулёза основывается на клинико-анамнестических и лабораторных данных (бактериоскопическое, бактериологическое, серологическое исследования, ПЦР), определении чувствительности к туберкулину и результатах инструментальных исследований. Ведущий метод раннего выявления туберкулёза у детей — туберкулинодиагностика, основанная на определении уровня специфической сенсибилизации, развившейся вследствие инфицирования микобактериями. Туберкулиновая проба — аллергическая реакция замедленного типа. Для массовой туберкулинодиагностики применяют внутрикожную пробу Манту с 2 ТЕ очищенного туберкулина PPD-R. Во внутреннюю поверхность предплечья специальным одноразовым туберкулиновым шприцем вводят внутрикожно 0,1 мл стандартного раствора туберкулина. На месте введения через 24-72 ч возникает гиперемия, а в центре её — папула. Для оценки пробы через 48-72 ч измеряют диаметр папулы перпендикулярно продольной оси руки. Примерная схема обследования при подозрении на туберкулёзную инфекцию
Оценка реакции Манту по величине папулы
Реакцию Манту проводят ежегодно всем детям в возрасте от 1 года до 18 лет, желательно в один и тот же сезон, независимо от предыдущих результатов. В условиях массовой внутрикожной вакцинации и ревакцинации БЦЖ с помощью туберкулиновых проб возможно выявление не только инфекционной, но и поствакцинальной аллергии. Для их отличия принимают во внимание срок, прошедший с момента вакцинации или ревакцинации, характер и динамику предыдущих реакций. Резко положительную реакцию, в том числе и гиперергическую, всегда следует расценивать как инфицирование. При выявлении положительной реакции Манту ребёнка следует направить на обследование к фтизиатру. В 7-10% случаев у инфицированных и даже больных туберкулёзом детей туберкулиновые пробы могут быть отрицательными [при тяжёлой дистрофии, некоторых инфекционных заболеваниях (кори, коклюше и др.), а также у больных соматическими заболеваниями, получающих иммуносупрессоры (глюкокортикоиды и др.)]. При постановке диагноза указывают локализацию поражения, фазу патологического процесса (инфильтрации, распада, обсеменения или рассасывания, уплотнения, рубцевания, обызвествления), осложнения. По наличию или отсутствию выделения больным туберкулёзной палочки (БК — бацилла Коха) туберкулёз характеризуют как БК (+) или БК (-). Перечисляют также остаточные изменения перенесённого туберкулёза. Дифференциальная диагностика Дифференциальную диагностику проводят в зависимости от клинических проявлений. При туберкулёзной интоксикации исключают хроническую очаговую инфекцию другой этиологии. При наличии признаков поражения лёгких или трахеобронхиальных лимфатических узлов исключают банальную пневмонию, саркоидоз, лимфопролиферативное заболевание. Варианты с внелёгочной локализацией туберкулёза дифференцируют с неспецифическими поражениями данных систем. Лечение Лечение проводит фтизиатр совместно с педиатром и врачами других специальностей (урологом, окулистом, неврологом, ортопедом и т.д.). Основа лечения — этиотропная химиотерапия. Её проводят с учётом возраста ребёнка, его анатомо-физиологических особенностей, формы и активности туберкулёзного процесса. Особое внимание уделяют организации режима, питанию, физической нагрузке. Лечение больных туберкулёзом осуществляют длительно (6-18 мес), поэтапно (стационар-санаторий-противотуберкулёзный диспансер). Химиотерапию начинают немедленно после установления диагноза, проводят длительно и непрерывно. Обычно назначают комбинацию из 2 и более лекарственных средств. Противотуберкулёзные препараты классифицируют в зависимости от их эффективности.
Обязательные составляющие любого кратковременного курса химиотерапии — изониазид и рифампицин (препараты выбора), а также пиразинамид, этамбутол и стрептомицин (дополнительные препараты). Остальные препараты менее эффективны и/или обладают большим количеством побочных эффектов, поэтому их применяют преимущественно при длительном лечении и выявлении у больного полирезистентных микобактерий. Лекарственные противотуберкулёзные препараты обладают многими побочными действиями, поэтому необходимы строгое соблюдение режима применения препарата, профилактика побочных эффектов (например, назначение витаминов группы В, особенно витамина В6). Также необходимо соблюдать следующие правила проведения химиотерапии.
Помимо химиотерапии проводят посиндромное патогенетическое лечение. Оперативное лечение у детей проводят преимущественно при костно-суставном туберкулёзе (иссечение поражённой ткани) и туберкулёзе мочеполовой системы. Проводят комплекс неспецифических мероприятий, направленных на укрепление защитных сил организма (лечебное питание, витаминотерапию, физиопроцедуры, ЛФК, лечение иммуномодуляторами и др.). Профилактика Профилактика туберкулёза у детей направлена на предотвращение инфицирования (имеет важное значение в раннем возрасте) и предупреждение заболевания.
Прогноз Прогноз при туберкулёзе зависит от клинической формы заболевания, возраста ребёнка, своевременности и эффективности лечения. Инфекционный процесс может годами протекать волнообразно, при этом вероятность неблагоприятных исходов и ранней инвалидизации высока в раннем детском возрасте и пубертатном периоде. Оригинал статьи www.eurolab.uaИллюстрации с сайта: © 2011 Thinkstock. Источник: Детские болезни. Баранов А.А. // 2002. |
www.whiteclinic.ru
Эпидемиология туберкулеза.
Туберкулез – хроническая инфекционная болезнь, при которой поражаются все органы человеческого организма, чаще легкие.
Источником туберкулезной инфекции являются больные туберкулезом люди, животные и птицы. Последнее десятилетие ознаменовалось ухудшением эпидемиологической ситуации по туберкулезу во многих странах мира.
За 1991-1997 г.г. заболеваемость туберкулезом в России возросла на 117,4% и составляет 73б9 на 100 тыс населения ( данные без республики Чечня). Смертность от туберкулеза увеличилась на 97,4% и составила 16,8 на 100 тыс населения. Заболеваемость туберкулезом детей в России за 5 лет возросла более чем на 60%. Всего во всех группах диспансерного учета на конец 1997 года состоит 2 288 100 пациентов, причем больные активным туберкулезом составляют 320904 человека. Значительно ухудшают эпидемиологическую ситуацию в стране больные туберкулезом, освободившиеся из мест лишения свободы, заболеваемость которых в 1997 г. была в 62 раза выше, чем всего населения Российской федерации. В связи с вышеизложенным становится видно, что резервуар туберкулезной инфекции в России высок и требует от медицинских работников и всего государства напряженной и кропотливой работы по выявлению больных туберкулезом и их лечению.
Этиология и патогенез туберкулеза.
Этиологию туберкулеза установил в 1882 г. немецкий ученый Кох, который обнаружил в туберкулезных очагах микроб, получивший название палочки Коха. В настоящее время она называется микобактерией туберкулеза. Различают несколько ее типов: человеческий, бычий, птичий и холоднокровный. Для человека патогенны два первых, реже — третий.
Патогенез туберкулеза очень сложен и не все его стороны полностью выяснены. Установлено, что проникновение туберкулезных микобактерий в организм человека обычно происходит аэрогенным путем. Однако наряду с этим существует еще и алиментарный путь заражения через желудочно- кишечный тракт (с молоком, содержащим туберкулезные микобактерии бычьего типа). Очень редко заражение происходит через поврежденную кожу, плаценту, измененную патологическим процессом и т. д. В зависимости от места внедрения микобактерий туберкулеза воспалительный очаг или первичный аффект может образовываться в легких, ротовой полости, миндалинах, кишечнике и т.д. В ответ на образование первичного аффекта развивается специфический процесс в регионарных лимфатических узлах и формируется первичный туберкулезный комплекс. Установлено, что первичный туберкулез, развивающийся в результате первичного контакта микроорганизма с возбудителем может появляться не только в виде первичного туберкулезного комплекса, как это считалось ранее. В результате первичного заражения возможно развитие туберкулеза внутригрудных лимфатических узлов, туберкулезного плеврита, туберкуломы, очагового процесса. Проникновение микобактерий в организм еще не означает обязательного развития туберкулеза. Организм отвечает на вторжение микобактерий мобилизацией своих защитных сил, клеточными реакциями, фагоцитозом, выработкой антител.
Нередко микобактерии долгое время остаются в тканях, не вызывая специфического воспаления, и это состояние обозначают как “латентный микробизм”. Особенно часто такое явление наблюдается в лимфатических узлах, в которых отмечается макрофагальная лимфоидноклеточная и плазмоклеточная реакция как проявление образования антител в ответ на внедрение антигена (токсин микобактерий). Вместе с тем при нарушении иммунологического состояния организма и срыве его защитных сил микобактерии проявляют свое патогенное действие, и развивается туберкулез как болезнь.
После периода первичного инфицирования в легких могут оставаться минимальные или довольно выраженные остаточные изменения. В оставшихся очагах сохраняются персистирующие микобактерии, которые не только поддерживают нестерильный иммунитет, но одновременно создают риск эндогенной реактивации туберкулезного процесса при наличии факторов, снижающих иммунитет. К факторам, способствующим реактивации, относятся такие заболевания как сахарный диабет, лимфогрануломатоз, силикоз, язвенная болезнь желудка и двенадцатиперстной кишки, хронические воспалительные заболевания легких, психические заболевания, протекающие с депрессивным синдромом, алкоголизм, стрессовые ситуации, СПИД, длительный прием глюкокортикоидов, цитостатиков и иммунодепрессантов. Таким образом, между моментом заражения туберкулезной микобактерией и началом развития туберкулеза может пройти иногда очень длительный срок.
В одних случаях болезнь протекает на фоне повышенной аллергии и нестойкого иммунитета, в других отмечаются обратные соотношения, или чувствительность к туберкулезному токсину и иммунитет к туберкулезу остаются как бы на одном уровне. Все это отражается на морфологических проявлениях туберкулеза, его клиническом течении и создает необычный полиморфизм, разнообразие клинико-морфологических проявлений заболевания. Вопрос о том, почему при туберкулезе поражаются чаще те или иные органы, в полной мере не решен. Большое значение имеют попадание микобактерий в ток крови (бактериемия) и оседание их в органах с развитием туберкулезного процесса. Как правило, это диссеминированный туберкулез легких с “метастазами”, “отсевами” в моче-половой, костной системе, периферических лимфатических узлах, реже- в других органах. За последние 10 лет удельный вес этой формы туберкулеза вырос в 2 раза. Обычно же процесс локализуется в одном, реже в двух органах (например, в костях, мочеполовой системе, коже и т.д.). Предполагается, что для развития туберкулеза органа, помимо попадания в него микобактерий, имеют значение местные факторы, такие как особенности кровоснабжения, аллергическая чувствительность, какие – либо перенесенные воздействия, например травма и т. д. Состояние организма в целом имеет решающее значение для возникновения болезни.
studfile.net

 Туберкулёз — инфекционное заболевание, вызываемое микобактериями туберкулёза и характеризующееся развитием клеточной аллергии, специфических гранулём в различных органах и тканях и полиморфной клинической картиной.
Туберкулёз — инфекционное заболевание, вызываемое микобактериями туберкулёза и характеризующееся развитием клеточной аллергии, специфических гранулём в различных органах и тканях и полиморфной клинической картиной.