БЦЖ и коронавирус: защищает ли от COVID-19 прививка от туберкулеза? | События в мире — оценки и прогнозы из Германии и Европы | DW
Может ли известная с начала прошлого столетия прививка БЦЖ (бациллы Кальмета — Герена), применяемая для профилактики туберкулеза у детей, защитить организм и от опасного коронавируса SARS-CoV-2? Ученые сразу в нескольких странах мира, в том числе Германии, приступили к исследованиям в этой области.
Создание вакцины-кандидата VPM1002
При этом речь не идет о том, чтобы переквалифицировать вакцину БЦЖ в вакцину от SARS-CoV-2. Однако если подтвердится предположение ученых, что она усиливает естественный иммунитет человека к вирусным заболеваниям дыхательных путей, то не исключено, что прививку БЦЖ можно будет использовать с этой целью до тех пор, пока на рынке не появится специальная вакцина от коронавируса.
Штефан Кауфман
В пользу этой гипотезы говорят, помимо прочего, опубликованные в конце марта научным Обществом Макса Планка (Max-Plank-Gesellschaft) результаты лабораторных опытов на мышах.
Профессор Штефан Кауфман (Stefan Kaufmann) руководит отделением иммунологии Института инфекционной биологии имени Макса Планка в Берлине, он — один из ведущих мировых специалистов в области исследований по защите от туберкулеза. Несколько лет назад под его руководством путем генетических изменений вакцины БЦЖ была создана вакцина-кандидат VPM1002, которая, по оценке немецких специалистов, может быть еще более эффективной в области борьбы с туберкулезом, чем вакцина БЦЖ.
Вакцина БЦЖ как способ укрепить иммунитет к коронавирусу
Как рассказал профессор Кауфман в интервью DW, теперь он и его коллеги готовятся к проведению клинических испытаний этой вакцины-кандидата. Цель — проверить, способна ли она также усилить иммунитет организма к вирусам гриппа и вирусным заболеваниям дыхательных путей, в том числе пневмонии COVID-19, которую вызывает коронавирус SARS-CoV-2.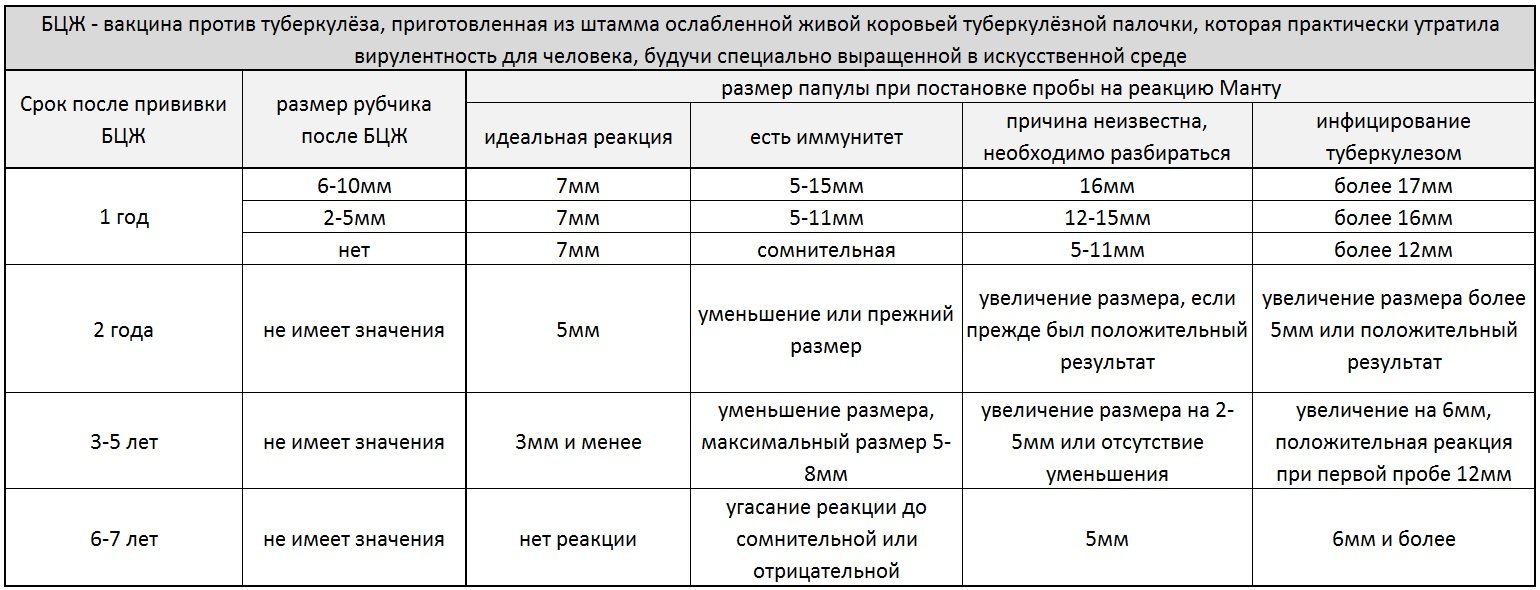 Ожидается, что в этих исследованиях примет участие медицинский персонал ряда клиник по всей Германии — как группа, особенно часто сталкивающаяся с источником подобной инфекции.
Ожидается, что в этих исследованиях примет участие медицинский персонал ряда клиник по всей Германии — как группа, особенно часто сталкивающаяся с источником подобной инфекции.
Так выглядит коронавирус под электронным микроскопом
По словам профессора Кауфмана, пока нельзя сказать, какое именно воздействие будет иметь прививка вакциной-кандидатом VPM1002. «В идеале привитые люди перестанут заболевать. Другой вариант воздействия — тот, при котором заболевание будет протекать у них в приглушенной форме», — поясняет он. «Сказать, что после прививки люди получат стопроцентную защиту, нельзя. Однако этого нельзя утверждать и в отношении других вакцин», — добавляет Кауфман.
По его словам, в случае успеха этих клинических испытаний — их первые результаты, вероятно, будут готовы уже к осени — вакцина VPM1002 может быть зарегистрирована на рынке в течение всего нескольких месяцев. «По отношению к заболеванию COVID-19 прививка VPM1002 не является классической вакцинацией, — отметил ученый в беседе с DW.
Как долго сохраняется эффект от прививки БЦЖ?
Означает ли это, что люди, привитые в детстве вакциной БЦЖ, в условиях пандемии коронавируса лучше защищены от него, чем те, у кого нет такой прививки? На этот вопрос Штефан Кауфман не дает однозначного ответа. По словам профессора, сегодня нет доказательств того, что защита организма, которую обеспечивает прививка БЦЖ, сохраняется в течение десятилетий: «Думаю, что ее хватает примерно на год».
Проверка анализов на туберкулез
В ГДР прививку БЦЖ активно применяли для профилактики туберкулеза у детей. Но после воссоединения Германии вакцинацию БЦЖ отменили по всей стране, поскольку риск заболевания туберкулезом оценивался как очень низкий. Из-за этого сегодня в ФРГ доступ к этой вакцине ограничен.
Однако Институт инфекционной биологии имени Макса Планка является партнером индийского концерна Serum Institute of India — одного из крупнейших частных производителей вакцины БЦЖ в мире.
По информации научного онлайн-издания Sciencemag, кроме Германии, исследования в области возможного укрепления иммунитета против коронавируса SARS-CoV-2 с помощью прививки БЦЖ недавно начались в Нидерландах. Ожидается, что в ближайшее время к аналогичным исследованиям приступят ученые в Австралии и США. При этом в Соединенных Штатах, как и в Германии, по словам профессора Кауфмана, объектом исследования станет именно вакцина-кандидат VPM1002, а не классическая вакцина БЦЖ.
Прививка от пневмококков и препараты от ВИЧ как средство от коронавируса
Что касается дополнительной защиты от коронавируса при помощи прививки от пневмококка, которую, как известно, недавно сделали и канцлеру Германии Ангеле Меркель (Angela Merkel), то она, по словам профессора Кауфмана, не дает общей защиты от коронавирусов.
Меркель сделали прививку от пневмококка незадолго до того, как она ушла на домашний карантин
«Однако если пациент защищен такой прививкой от данного возбудителя типичных заболеваний дыхательных путей, ему не грозит так называемая коинфекция (заражение одной клетки различными видами вируса одновременно. —
В свою очередь эффективность препаратов от лихорадки Эбола и медикаментов против ВИЧ, рекомендуемых Минздравом России для защиты от коронавируса, еще предстоит проверить в ходе специальных исследований, подчеркивает Кауфман. «Иногда результат испытаний в лабораторной пробирке не подтверждается на практике», — заключил он.
Смотритетакже:
Смех и солидарность в эпоху коронавируса
Охота на медведей
Чем занять детей, когда школы и детские сады закрыты неделями? Тысячи бельгийцев и голландцев решили немного развлечь малышей и выставили в окна плюшевых мишек в качестве «мишеней» для прогулочной «охоты».
 Многие медведи в окнах зарегистрированы на интерактивных картах. Так родители могут спланировать свою прогулку по «медвежьему маршруту». Мол, мы не бесцельно шатаемся по городу, а ищем мишек!
Многие медведи в окнах зарегистрированы на интерактивных картах. Так родители могут спланировать свою прогулку по «медвежьему маршруту». Мол, мы не бесцельно шатаемся по городу, а ищем мишек!Смех и солидарность в эпоху коронавируса
Помощь уязвимым
Наибольшую опасность коронавирус представляет для пожилых людей. Чтобы уберечь их от инфицирования SARS-CoV-2, супермаркеты во многих странах ввели временные интервалы, когда только пожилые люди могут делать покупки.
Смех и солидарность в эпоху коронавируса
Музыка против вируса
Турция выбрала другой путь: людям старше 65 лет и тем, кто страдает хроническими заболеваниями, запрещено покидать пределы своего дома. Для их же собственной безопасности! 25-летний житель Мерсина скрашивает вынужденное одиночество стариков игрой на гитаре. В других странах люди поют под окнами домов престарелых.
Смех и солидарность в эпоху коронавируса
«Италия, мы с тобой!»
Солидарность существует! В российском Беслане жители города зажгли свечи, сопереживая вместе с итальянцами, потерявшими родных и близких.
 В Парагвае, Польше и Боснии в ночной подсветке общественных зданий использованы цвета итальянского флага. В Китае моральную поддержку итальянцам демонстрирует раскрашенный в зеленый, белый и красный цвета автобус.
В Парагвае, Польше и Боснии в ночной подсветке общественных зданий использованы цвета итальянского флага. В Китае моральную поддержку итальянцам демонстрирует раскрашенный в зеленый, белый и красный цвета автобус.Смех и солидарность в эпоху коронавируса
Надежда на небосклоне
Швейцария также солидарна с Италией. Маттерхорн, знаменитая гора и символ Швейцарии (расположена на границе с Италией), шлет в эти дни световой сигнал со свой вершины. А время от времени на пике появляется проекция #stayathome — как призыв серьезно относиться к пандемии и оставаться дома.
Смех и солидарность в эпоху коронавируса
Веселый карантин
Литовский фотограф Адас Василяускас остался без работы из-за пандемии. Но он не стал унывать, а отправил дрон с камерой к окнам друзей и соседей (конечно, с их позволения). Оказалось, что они тоже не хотят придаваться унынию. Во время вынужденного затворничества, как выяснилось, можно загорать на крыше, тренироваться на балконе, устраивать маскарад и мечтать о следующем отпуске!
Смех и солидарность в эпоху коронавируса
Животные тоже страдают
Локдаун в Бангладеш.
 Бездомные животные остались без пропитания, потому что люди перестали покидать дома и их подкармливать. Поэтому уличных собак в Дакке теперь кормят добровольцы. Кстати, в Германии природоохранные организации предупредили о том, что голодная смерть угрожает местным городским голубям.
Бездомные животные остались без пропитания, потому что люди перестали покидать дома и их подкармливать. Поэтому уличных собак в Дакке теперь кормят добровольцы. Кстати, в Германии природоохранные организации предупредили о том, что голодная смерть угрожает местным городским голубям.Смех и солидарность в эпоху коронавируса
Признание медикам
Во многих странах медицинский персонал уже несколько недель работает на абсолютном пределе сил и возможностей. В Европе люди по вечерам открывают окна, выходят на балконы и аплодируют героям в белых халатах. Пакистанцы машут белыми флагами в знак уважения к медикам.
Смех и солидарность в эпоху коронавируса
Посильная помощь
Волонтеры во всем мире сели за швейные машинки, чтобы шить простые защитные маски. Они не гарантируют защиту от заражения, но могут снизить темпы распространения вируса. Маски, которые шьют эти женщины в Сирии, предназначены для бедных в Алеппо.
Смех и солидарность в эпоху коронавируса
Арт-профилактика
Каждый помогает так, как может.
 Мастера граффити из группы RBS Crew в Сенегале своими просветительскими рисунками на стенах домов в Дакаре наглядно показывают населению, как надо вести себя, чтобы замедлить распространение коронавируса. Чихать следует в локтевой сгиб! Это — одно из важных правил.
Мастера граффити из группы RBS Crew в Сенегале своими просветительскими рисунками на стенах домов в Дакаре наглядно показывают населению, как надо вести себя, чтобы замедлить распространение коронавируса. Чихать следует в локтевой сгиб! Это — одно из важных правил.Смех и солидарность в эпоху коронавируса
С улыбкой против вируса
Кризис легче пережить в хорошем настроении. Так решил один 29-летний житель Вашингтона и отправился гулять по американской столице в костюме тираннозавра Рекса — чтобы развеселить людей и отвлечь их от мыслей о пандемии.
Смех и солидарность в эпоху коронавируса
Спорные стилизации
В Германии путь к улыбке ведет через желудок! Конфеты в виде вирусов, пироги в форме рулонов туалетной бумаги, съедобные пасхальные зайцы в защитных масках… Но это была бы не Германия, если бы не было жалоб! Недовольные считают, что такие кулинарные изыски безвкусны и бестактны.
Смех и солидарность в эпоху коронавируса
Рулон в подарок
Туалетная бумага пользуется сейчас особенно большим спросом не только в Германии.
 Один ресторан в штате Миннесота, США, добавляет рулон к каждому заказу на сумму больше 25 долларов. «Клиенты смеются, когда получают свой заказ. И сейчас этот смех — самое лучшее», — сказал владелец ресторана местному телеканалу. Интеллигентная маркетинговая стратегия!
Один ресторан в штате Миннесота, США, добавляет рулон к каждому заказу на сумму больше 25 долларов. «Клиенты смеются, когда получают свой заказ. И сейчас этот смех — самое лучшее», — сказал владелец ресторана местному телеканалу. Интеллигентная маркетинговая стратегия!Смех и солидарность в эпоху коронавируса
Сатира в знак протеста
Искусство реагирует на кризис и едкой сатирой. Бразильский художник Айра Окрешпу — не единственный, кто критикует президента Болсонару за его скептическое отношение к карантинным мерам. Поэтому художник изобразил его с красным носом клоуна: мол, это — единственная маска, которую президент носит ради защиты от коронавируса.
Автор: Ута Штайнвер, Элла Володина
Есть версия, что прививка БЦЖ дает иммунитет против Covid-19. Что говорят ученые и что мы знаем наверняка?
- Николай Воронин
- Корреспондент по вопросам науки
Автор фото, Getty Images
В конце марта, когда эпидемия Covid-19 распространилась по всему миру, а число подтвержденных случаев стало измеряться сотнями тысяч, многие обратили внимание на подозрительное совпадение.
В разных государствах заболевание распространяется с разной скоростью. И почему-то коронавирус — во всяком случае на первый взгляд — проявляет значительно меньшую активность в странах, где детей в обязательном порядке прививают от туберкулеза при помощи вакцины БЦЖ, в том числе и в России.
Что это — простое совпадение? Или тут есть какая-то закономерность?
Учитывая масштаб эпидемии и страх перед новым вирусом, который у многих лишь подогревают введенные по всему миру беспрецедентные ограничительные меры, в соцсетях и на разного рода околонаучных сайтах мгновенно стали появляться самые разнообразные версии.
Кто-то всерьез полагает, что изобретенная 100 лет назад вакцина от туберкулеза может заодно защитить и от коронавирусной инфекции, о существовании которой ученые ничего не знали еще в декабре.
Автор фото, GETTY/Universal History Archive
Подпись к фото,В начале 1960-х гг. в Китае проходила массовая кампания по вакцинации от туберкулеза
Другие, напротив, утверждают, что никакой связи нет и быть не может: совпадения случайны, а иммунитет от коронавируса, который якобы дает вакцина и в который многим так хочется верить, — выдумка, никаких научных подтверждений этому нет.
Так что говорит наука и что мы знаем наверняка?
Подозрительное совпадение
Примерно до середины февраля, пока практически не изученная болезнь бушевала только в Китае, казалось, что новый вирус косит всех без разбора широкой косой — правда, чаще отдавая предпочтение мужчинам.
Однако когда вирус добрался до самых отдаленных уголков планеты, стало очевидно, что в разных странах эпидемия развивается по-разному.
Где-то — как в Италии или США — число подтвержденных случаев заражения и погибших пациентов вскоре начинает расти не по дням, а по часам. А где-то — например, в Японии или Таиланде — эпидемия распространяется гораздо медленнее, несмотря на то что первых больных там выявили гораздо раньше.
На это влияет много факторов: огромную роль играет средний возраст населения, а также культурные нормы, состояние системы здравоохранения, опыт ранее пережитых эпидемий и т.д. Кроме того, описание течения эпидемий в конкретных странах зависит и от того, как организовано тестирование, каким образом ведется статистика и предоставляется информация.
Тем не менее ряд ученых и аналитиков предположили, что есть еще один фактор — скорость развития и тяжесть эпидемии в той или иной стране коррелируется с тем, делают ли там детям в обязательном порядке БЦЖ.
Эта теория основывается, главным образом, на публичной статистике заражения коронавирусом. Занимающиеся исследованиями медики говорят, что наличие БЦЖ у конкретного человека совершенно точно не дает ему иммунитета от нового вируса. Вакцинированные пациенты есть и среди тяжело больных, и в числе погибших от Covid-19.
В то же время нельзя исключать, что в ходе пандемии прививка может оказаться полезной в национальных масштабах: во всяком случае предварительные данные этой теории не противоречат.
Первое профильное исследование на эту тему было опубликовано в конце марта группой ученых из Нью-Йорка. Оно еще не было официально отрецензировано другими учеными, работающими в этой области, однако авторы работы делают очень смелое заявление.
«Наши данные дают основания предполагать, что вакцинация БЦЖ, по-видимому, значительно снижает смертность, связанную с Covid-19, — пишут они. — Мы также обнаружили, что, чем раньше та или иная страна начала практику вакцинации БЦЖ, тем значительнее снижается число смертей на каждый миллион жителей».
Эпидемиологи из Университета Техаса провели еще более масштабное исследование, изучив статистику 178 стран, и пришли к тому же выводу. По их подсчетам, число инфицированных на душу населения в странах с обязательной вакцинацией от туберкулеза ниже примерно в десять раз, а жертв Covid-19 — в 20 раз меньше, чем там, где БЦЖ больше не делают.
Что же это за вакцина такая, что в ней особенного?
«Прививка от всего»: попытка первая
Разработанная во Франции еще в 1921 году, БЦЖ (от французского Bacillus Calmette-Guérin — бацилла Кальмета-Герена) и сегодня остается единственной доступной и эффективной прививкой от туберкулеза, рекомендованной ВОЗ.
Действует она точно так же, как и любая другая вакцина. Здоровому человеку вводится ослабленный возбудитель инфекции, чтобы «познакомить» организм с потенциальной опасностью и выработать специфический иммунитет.
Специфический — значит направленный против какого-то конкретного вируса или бактерии, вызывающего то или иное заболевание. Именно поэтому прививок так много: для каждой болезни — своя.
Вакцина БЦЖ разработана именно для защиты от туберкулеза, и по идее ни от чего больше она защищать не может и не должна.
Однако пара ученых Петер Ааби и Кристина Стабелл Бенн (оба датчане, но работают преимущественно в Гвинее-Бисау) много лет изучают побочные эффекты вакцинирования и утверждают, что БЦЖ обеспечивает эффективную защиту и от других болезней, укрепляя иммунитет в целом.
Если верить их исследованиям, которые ведутся уже несколько десятилетий, люди, вакцинированные БЦЖ, становятся в среднем на 30% менее восприимчивы ко всем известным науке инфекциям без исключения. Будь то патогенный вирус, бактерия или грибок — без разницы: вероятность заражения снижается почти на треть.
Будь то патогенный вирус, бактерия или грибок — без разницы: вероятность заражения снижается почти на треть.
Впрочем, все эти годы научное сообщество относилось к работам Ааби и Бенн довольно прохладно. Их публикации в научных журналах неоднократно критиковали за неточности методологии, а проведенное в 2014 году масштабное исследование ВОЗ окончательно постановило: если у БЦЖ и есть какие-то дополнительные преимущества, то они настолько малы, что их не стоит принимать в расчет.
На этом историю можно было бы считать закрытой. Но в 2020 году грянула пандемия коронавируса — и ученые заметили неожиданные цифры и странные корреляции.
Италия, США… кто следующий?
В мире не так много стран, где вакцинация от туберкулеза никогда не была обязательной и поголовной. Их можно буквально пересчитать по пальцам: Бельгия, Италия, Канада, Ливан, Нидерланды, США.
БЦЖ там ставят выборочно — отдельным категориям населения и лишь в рекомендательном порядке.
Две страны из этого списка давно входят в число печальных лидеров по числу подтвержденных случаев Covid-19. В США живет больше четверти всех «официально инфицированных» мира. В Италии, население которой впятеро меньше, — каждый десятый.
Еще три страны не входят в первую десятку по абсолютным цифрам, но идут друг за другом сразу после нее: Бельгия на 11-м месте, Нидерланды — на 12-м, Канада — 13-я.
При этом все три сильно опережают, скажем, Японию или Таиланд, где население в несколько раз больше, а первые случаи коронавируса были зафиксированы гораздо раньше. Если в 126-миллионной Японии за все время эпидемии от Covid-19 умерло меньше 100 человек, то в 11-миллионной Бельгии — уже свыше 2000.
В Институте экономического анализа, основанном экономистом Андреем Илларионовым, изучили статистику погибших и инфицированных из 36 стран, где «взрывная» стадия эпидемии коронавируса началась больше месяца назад, и сравнили их с проводимой там политикой вакцинации.
Приведенные Институтом расчеты показали: в шести «невакцинированных» государствах эпидемия Covid-19 разрастается значительно быстрее, чем в странах, где БЦЖ в обязательном порядке ставят до сих пор. Как по общему числу инфицированных на 1 млн населения, так и по количеству погибших.
Страны, где раньше прививку делали всем поголовно, но в какой-то момент перестали, по числу выявленных случаев не уступают «невакцинированным», но при этом доля смертельных исходов там меньше в несколько раз.
Похожий анализ провели эксперты Института биологии развития (ИБР) РАН и и казахстанского Университета Назарбаева. Там страны разделили не на три, а на две категории: те, где обязательная вакцинация БЦЖ не проводится по меньшей мере 30 лет (Бельгия, Германия, Испания, Нидерланды, Швейцария), и те, где она по-прежнему входит в национальный календарь прививок — как в ЕС (Болгария, Венгрия, Латвия, Польша, Румыния, Словакия), так и в других регионах (Гонконг, Индонезия, Казахстан, Китай, Мексика, Филиппины, Южная Корея, Япония).
В отличие от Илларионова, биологи намеренно не включили в список США и Россию, где эпидемия началась позже, однако в остальном результаты обоих исследований оказались очень близки.
«Во второй группе распространенность Covid-19 была существенно ниже, что подтверждает гипотезу о возможной протективности вакцины БЦЖ против Covid-19», — говорится в письме, которое ученые направили в журнал Lancet.
В то же время эксперты ИБР подчеркивают: «Различия между этими группами стран потенциально могут быть обусловлены другими факторами и лишь косвенно быть связанными с вакцинацией БЦЖ».
Ловушка цифр
Возможно ли, что столь очевидная связь, подтвержденная сразу несколькими исследованиями, объясняется каким-то другими причинами?
Безусловно, и статистика знает массу подобных примеров. Например, число пожарных машин, отправленных к месту возгорания, находится в прямой зависимости с ущербом от огня, поскольку оба показателя зависят в первую очередь от размеров пожара. Однако это совершенно не означает, что ущерб можно снизить, выслав на место меньше пожарных расчетов.
Профессор ИБР РАН Ирина Лядова приводит два возможных альтернативных объяснения тесной связи между БЦЖ и распространением коронавируса.
Во-первых, обязательную вакцинацию БЦЖ проводят страны с относительно высоким уровнем заболеваемости туберкулезом. Многие из них (хотя далеко не все) — очень небогатые государства, а это может снижать уровень и качество тестирования и создавать видимость более благополучной ситуации по Covid-19.
Во-вторых, на тяжесть эпидемии в разных странах сильно влияет скорость принятия и уровень введенных карантинных мер.
«Мы не можем полностью исключить наличие связи между этим показателем и политикой по БЦЖ-вакцинации, поскольку оба показателя зависят от исторически сложившихся особенностей организации эпидемиологических служб и систем здравоохранения», — отмечает она.
«Таким образом, полностью исключить то, что в странах, применяющих вакцину БЦЖ, более благоприятное течение эпидемиологического процесса связано не непосредственно с протективной активностью БЦЖ, а с другими факторами, пока нельзя», — заключает профессор Лядова.
«Тренированный иммунитет»
Есть ли у биологов в принципе какие-либо фундаментальные основания предполагать, что противотуберкулезная вакцина может помогать при других вирусных инфекциях?
Такие основания есть, и впервые этот механизм был описан в статье, опубликованной в журнале Science в 2016 г. Ее авторы из Нидерландов высказывали предположение, что память нашей иммунной системы может формироваться не только за счет мутации или рекомбинации каких-то генов (так работают прививки), но и без физических изменений в ДНК.
Работа группы ученых из Нидерландов так и называлась «Тренированный иммунитет», и про БЦЖ там не было ни слова. Однако проверить свою теорию исследователи решили именно с помощью этой прививки (и двойного слепого тестирования).
В итоге им удалось на практике доказать, что БЦЖ может защитить организм и от инфекции, не имеющей к туберкулезу никакого отношения. Сначала это сработало с желтой лихорадкой, а потом — и с другими вирусами. Вакцинированные заражались реже контрольной группы, а, даже подхватив инфекцию, болели не так тяжело и выздоравливали быстрее.
Но как насчет коронавируса? Значит ли это, что БЦЖ и тут может оказывать аналогичный эффект?
Все эксперты подчеркивают: утверждать, что вакцина действительно делает людей менее восприимчивыми к вирусу SARS-CoV-2, можно будет только по результатам соответствующих клинических испытаний.
Это единственный научный способ проверить, имеет ли обнаруженная корреляция причинно-следственную связь.
«Да, это лишь корреляция, но гипотеза имеет под собой научное основание — в виде как недавних, так и довольно старых исследований, опубликованных в серьезных журналах, — считает профессор кафедры иммунологии МГУ и член-корреспондент РАН Дмитрий Купраш. — Медики правильно делают, что проверяют эту гипотезу».
Испытания уже начались и проводятся сразу в нескольких странах. В Австралии, где БЦЖ не делают уже почти 40 лет, БЦЖ планируется поставить 4000 молодым сотрудникам больниц.
Хотя профессор Школы системной биологии в американском Университете Джорджа Мэнсона Анча Баранова высказывает сомнение, что защитный эффект БЦЖ от тяжелого течения болезни можно будет убедительно доказать на взрослых. Есть немало доказательств того, что прививка, сделанная в детстве более эффективна.
В ожидании результатов
В российском НИИ вакцин и сывороток подтверждают: доказательства связи вакцинации БЦЖ со сниженным риском различных немикобактериальных инфекций, аллергий, онкологических заболеваний и общей смертности действительно существуют.
«Подобные неспецифические эффекты вакцинации БЦЖ могут быть опосредованы клетками врожденной иммунной системы, а не специфическими Т-клетками памяти», — объясняет директор института, член-корреспондент РАН Оксана Свитич.
Если не вдаваться в подробности, после прививки клетки врожденного иммунитета достаточно долгое время остаются в активированном состоянии: они выделяют вещества, препятствующие воспалению, и приобретают способность «сдвигать» иммунный ответ, оказывая защиту от любых бактериальных и вирусных инфекций.
Кроме того, вакцина может стимулировать так называемый гетерологичный иммунитет, попутно активируя и специфические Т-лимфоциты других антигенов.
«Таким образом, вакцинация БЦЖ не может дать специфического защитного иммунитета против коронавируса, однако возможно неспецифическое защитное воздействие вследствие активации системы врожденного иммунитета», — считает Свитич.
В то же время она полагает, что даже в таком случае «это вряд ли скажется скорости распространения эпидемии в странах с разными подходами к вакцинации против туберкулеза».
Так это или нет, можно будет сказать лишь по результатам ретроспективных исследований, когда пандемия будет позади. Даже результаты текущих клинических испытаний появятся не раньше конца декабря.
Правовая информация. Эта статья содержит только общие сведения и не должна рассматриваться в качестве замены рекомендаций врача или иного специалиста в области здравоохранения. Би-би-си не несет ответственности за любой диагноз, поставленный читателем на основе материалов сайта. Би-би-си не несет ответственности за содержание других сайтов, ссылки на которые присутствуют на этой странице, а также не рекомендует коммерческие продукты или услуги, упомянутые на этих сайтах. Если вас беспокоит состояние вашего здоровья, обратитесь к врачу.
ВГВ | Прививки.уз — Предупредить. Защитить. Привить.
Вы спрашивали
Следующий вопросВирусный гепатит B
Ребенок родился в 37 недель, маловесный, последствия гипоксии еще присутствуют, понижен мышечный тонус, снижен уровень гемоглобина. Можно ли на таком фоне прививать против гепатита В?
Иммунизация против ВГВ недоношенных детей проводится по всему миру
Подробнее
Вирусный гепатит B
Кому не рекомендуется введение вакцины против ВГВ?
Вакцина против ВГВ противопоказана только тем, у кого ранее наблюдались тяжелые аллергические реакции
Подробнее
Вирусный гепатит B
Слышала, что между прививками против гепатита лучше не делать других прививок, правда ли это?
Информация о том, что между прививками против гепатита нежелательно делать другие прививки
Подробнее
Вирусный гепатит B
Когда можно привить против ВГВ ребенка с хроническим заболеванием?
Вакцинация временно откладывается до купирования обострения.
Подробнее
Вирусный гепатит B
В три месяца ребенку прививку против ВГВ делать не стали, так как был низкий гемоглобин. Когда лучше сделать третью прививку? Врач сказала – только при наличии нормального анализа крови.
Анемия, выявленная при обследовании, никак не может являться медицинским отводом к вакцинации.
Подробнее
Вирусный гепатит B
Каков график вакцинации против ВГВ в Узбекистане?
По национальному календарю Республики Узбекистан первая вакцинация против ВГВ
Подробнее
Вирусный гепатит B
Безопасна ли вакцина против ВГВ?
Да, безопасна. Вакцина против ВГВ безопасна при введении новорожденным, младенцам, детям, подросткам и взрослым
Подробнее
Вирусный гепатит B
Как долго защищает вакцинация против ВГВ? Нужна ли ревакцинация?
Подробнее
Вирусный гепатит B
Можно ли прививать против ВГВ новорожденных с желтухой?
Желтуха встречается у большинства (приблизительно от 40 до 70%) совершенно здоровых доношенных новорожденных и обычно является результатом естественных процессов, происходящих в его организме
Подробнее
Вирусный гепатит B
Если у ребенка с момента первой прививки против ВГВ в роддоме прошло более 3 месяцев, по какой схеме его прививать далее?
Если первичный курс прерван после первой дозы
Подробнее
Вирусный гепатит B
Можно ли прививать против ВГВ на фоне приема различных лекарств?
В инструкциях по применению рекомбинантных вакцин против ВГВ не указано никаких лекарственных веществ
Подробнее
Вирусный гепатит B
Взаимозаменяемость рекомбинантных вакцин
Первую прививку против ВГВ ребенку сделали в роддоме вакциной одной вакциной.
Подробнее
Вирусный гепатит B
Не является ли грудное вскармливание противопоказанием для прививки ребенка против ВГВ?
Кормление грудью не является противопоказанием к вакцинации против ВГВ
Подробнее
Вирусный гепатит B
Можно ли заразиться от вакцины вирусом гепатита В? Заразен ли привитой?
Вирусный гепатит B
Как производятся рекомбинантные вакцины против ВГВ?
Рекомбинантные вакцины, зарегистрированные в Республике Узбекистан, производятся с применением культуры пекарских дрожжевых грибков
Подробнее
Вирусный гепатит B
Когда можно привить против ВГВ ребенка с острым заболеванием?
Как и в случае вакцинации против других инфекций
Подробнее
Вирусный гепатит B
Можно ли вводить вакцину против ВГВ одновременно с другими вакцинами?
Допускается введение вакцин (кроме вакцин для профилактики туберкулеза), применяемых в рамках Календаря профилактических прививок, в один день разными шприцами в разные участки тела.
Подробнее
Вирусный гепатит B
У нас в семье нет носителей вируса ВГВ, зачем прививать ребенка в роддоме?
Ребенок в первые же месяцы жизни подвергается множеству медицинских манипуляций при осмотрах и обследованиях.
Подробнее
Вирусный гепатит B
Прививали ребенка от ВГВ перед детским садом. Успели сделать 2 прививки, между 2 и 3 прививкой получается интервал 2 года. Нам рекомендуют начинать прививаться снова. Правильно ли это?
При увеличении интервалов между прививками против ВГВ никаких дополнительных прививок не требуется
Подробнее
Вирусный гепатит B
Если ребенку вакцинация против ВГВ в роддоме не проведена, по какой схеме его прививать?
Если новорожденный не был привит против ВГВ в родильном доме
Подробнее
Вирусный гепатит B
Ребенок ранее привит против ВГВ (в роддоме получал прививку ВГВ, в 2 ,3 и 4 месяц – пентавалентную вакцину). Недавно у отца ребенка выявлен хронический ВГВ. Нужны ли ребенку дополнительные прививки?
Вирусный гепатит B
В какую часть тела лучше получать прививку против ВГВ? Можно ли делать эту прививку в ягодицу?
Вакцины должны вводиться только тем способом, который указан в инструкции по их применению.
Подробнее
Вирусный гепатит B
Мой ребенок не был привит в родильном доме из-за болезни (сепсис новорожденного). Когда можно привить против ВГВ?
Вакцина против ВГВ не содержит цельного вируса ни в живом, ни в инактивированном виде, только фрагмент его оболочки.
Подробнее
Вирусный гепатит B
Можно ли бесплатно получить прививку против ВГВ и кому?
В медицинских учреждениях по месту жительства бесплатно (за счет государственного финансирования) можно привиться против ВГВ детям в сроки
Подробнее
Вирусный гепатит B
Ребенку 4 месяца. В поликлинике делают 4 прививки сразу в один день (Пентавалентная вакцина -3, включающая в свой состав и ВГВ), ОПВ-3 и ИПВ . Можно ли их делать сразу? Стоит ли сделать все три прививки, или лучше отказаться временно от ОПВ и ИПВ?
Одновременное введение вакцин – международный стандарт, применяющийся для обеспечения безопасности ребенка.
Подробнее
Вирусный гепатит B
Вакцинация детей с частыми ОРВИ
Нужно ли дожидаться окончания катаральных явлений после снижения температуры?
Подробнее
Вирусный гепатит B
Почему надо обязательно начинать делать прививки сразу после рождения ребёнка? Можно ли подождать хотя бы год?
Вакцинацию против ВГВ проводят сразу после рождения ребенка, так как он уязвим и не имеет защитного иммунитета, вирус легко передается при медицинских манипуляциях и в быту.
Подробнее Все вопросы
Пента | Прививки.уз — Предупредить. Защитить. Привить.
Новые инфо материалы по иммунизации во время пандемии COVID-19
для медицинский работников и родителей
Вакцинация во время пандемии COVID-19
Вопросы и ответы для РОДИТЕЛЕЙ
Вакцинация во время пандемии COVID-19
Вопросы и ответы для МЕДРАБОТНИКОВ
В ВОЗ отмечают 40-летие победы над оспой
и призывают проявить такую же солидарность в борьбе с COVID-19
Может ли БЦЖ вакцина помочь в борьбе с коронавирусом?
Международные исследования анализируют влияние БЦЖ вакцины на коронавирус
Совместное заявление ВОЗ и ЮНИСЕФ
Во время пандемии COVID-19 крайне важно сохранить услуги плановой иммунизации
В условиях пандемии COVID-19 вакцинацию необходимо продолжать, чтобы она сохраняла свою эффективность
Европейская неделя иммунизации — 2020
ГАВИ, ВОЗ, ЮНИСЕФ: успешное сотрудничество и новые планы
22-23 ноября 2019 года в конференц-зале гостиницы Hyatt Regency Tashkent при поддержке ВОЗ Министерство здравоохранения провело ежегодную национальную конференцию по иммунизации
Первый этап вакцинации против ВПЧ прошел успешно и эффективно
Минздрав провел конференцию по итогам первого этапа прививочной кампании против ВПЧ в Узбекистане.
Первые результаты вакцинации от ВПЧ!
Как вы знаете, с 21 октября 2019 года по всей республике проводится вакцинация против ВПЧ.
В Узбекистане дан старт вакцинации против вируса папилломы человека
В столице состоялась пресс-конференция, посвященная началу вакцинации против вируса папилломы человека.
Встреча с блогерами о ВПЧ
«Мероприятие полностью меня поглотило».
Профилактика рака шейки матки и внедрение ВПЧ вакцины в Узбекистане
Все о вакцинации от ВПЧ
Встреча с Ассоциацией частных школ Узбекистана по внедрению ВПЧ вакцины
Научно-практическая конференция по профилактике, раннему выявлению и лечению рака шейки матки.
20 августа 2019 года В Ташкенте под слоганом «Будущее без рака шейки матки» прошла научно-практическая конференция по профилактике, раннему выявлению и лечению рака шейки матки.
Техническая поддержка Узбекистану в оценке температурных рисков в системе холодовой цепи для вакцин
В рамках оказания технической поддержки Узбекистану в достижении лучших стандартов качества и безопасности вакцин, с 13 по 24 августа 2019 года проходит миссия в составе консультантов ВОЗ г-жи Claire Frijs-Madsen и г-жи Erida Nelaj.
Рабочий визит делегации Республики Узбекистан по опыту внедрения внедрения вакцинации против ВПЧ в Молдове
«Это наши мамы, наши сестры, наши дочери, которых мы можем защитить от рака шейки матки уже сегодня благодаря вакцине от ВПЧ и программе скрининга», — неоднократно повторяли представители Молдовы.
Прививки: абсолютно исчерпывающая инструкция для взрослых и детей Даже для тех, кто не верит в вакцинацию
Антипрививочное движение продолжает шириться, а вместе с ним растети частота вспышек инфекций
Совсем недавно в рамках Европейской недели иммунизации состоялась очень необычная и интересная встреча
Вакцинация против кори
Как быть, если произошел контакт с больным корью?
Действия регламентируются Санитарно-эпидемиологические правила СП 3.1.2952-11 «Профилактика кори, краснухи и эпидемического паротита»
5.10. Иммунизации против кори по эпидемическим показаниям подлежат лица, имевшие контакт с больным (при подозрении на заболевание), не болевшие корью ранее, не привитые, не имеющие сведений о прививках против кори, а также лица, привитые против кори однократно – без ограничения возраста.
Иммунизация против кори по эпидемическим показаниям проводится в течение первых 72 часов с момента выявления больного. При расширении границ очага кори (по месту работы, учебы, в пределах района, населенного пункта) сроки иммунизации могут продлеваться до 7 дней с момента выявления первого больного в очаге.
5.12. Детям, не привитым против кори или эпидемического паротита (не достигшим прививочного возраста или не получившим прививки в связи с медицинскими противопоказаниями или отказом от прививок) не позднее 5-го дня с момента контакта с больным вводится иммуноглобулин человека нормальный (далее – иммуноглобулин) в соответствии с инструкцией по его применению.
5.14. Контактные лица из очагов кори, краснухи или эпидемического паротита, не привитые и не болевшие указанными инфекциями ранее, не допускаются к плановой госпитализации в медицинские организации неинфекционного профиля и социальные организации в течение всего периода медицинского наблюдения, указанного в пункте 5.7 настоящих санитарных правил.
Госпитализация таких пациентов в период медицинского наблюдения в медицинские организации неинфекционного профиля осуществляется по жизненным показаниям, при этом в стационаре организуются дополнительные санитарно-противоэпидемические (профилактические) мероприятия в целях предупреждения распространения инфекции.
БЦЖ расшифровка
Что такое БЦЖ и зачем ее делать своему новорожденному малышу в большей мере интересует молодых мамочек. Ведь они дают свое согласие на то, чтобы их крохе в первые же часы его жизни была сделана прививка от туберкулеза.
История вопроса
В русской литературе XIX литераторы при помощи тогда еще неизвестной палочки Коха умертвили множество вполне положительных персонажей. Все они погибли от грудной жабы или чахотки, болезни, которую в XX веке уже знали как туберкулез.
Возбудителя обнаружил немецкий микробиолог Роберт Кох в 1882 г. Бактерию назвали в его честь бациллой Коха. Но выявление возбудителя никак не отразилось на ходе войны с недугом: люди по-прежнему гибли, действенного лекарства не существовало.
В 1923 г. французские ученые А. Кальметт и Ш. Герен смогли создать противотуберкулезную вакцину. Новая культура была названа: бацилла Кальметта — Герена. Ее международное наименование — Bacillus Calmette—Guérin. Получилась аббревиатура — BCG, а русифицированный вариант – БЦЖ не расшифровывается. По факту это буквальное переложение сокращения медицинского термина, принятого международным сообществом врачей.
Французские ученые после 10 лет экспериментов смогли добиться того, что:
- появилась возможность хранить палочку Коха во внешней среде;
- полученный препарат вызывал болезнь в той слабой степени, чтобы человек заболел, но ему не было причинено никакого вреда.
Впервые прививка была введена в 1923 г. в институте Пастера (Франция). Тогда ее могли делать только через рот. Первые опыты вакцинирования были неудачными и вызывали осложнения.
В СССР массово прививка ставилась с 1962 г. До этого – и в довоенный период – она была доступна только жителям крупных городов.
Вакцинация новорожденных
Сегодня детям прививка БЦЖ ставится внутрикожно, что необходимо для локального развития туберкулезного процесса, который не опасен для общего состояния. В ответ на введение минимальной дозы микобактерий туберкулеза организм малыша вырабатывает антитела.
Зачем прививка ставится новорожденным еще в роддоме? Заражение туберкулезом происходит воздушно-капельным путем. Для ребенка достаточно, чтобы больной просто дыхнул на него.
Полноценный иммунитет против туберкулеза формируется в течение года. О том насколько прививка оказалась эффективна, свидетельствует наличие рубца и его величина: чем больший след на коже ребенка он оставил, тем более надежную систему защиты выработал организм.
Ревакцинация
Зачем делать ревакцинацию? Иммунитет, сформированный после первичного введения препарата, сохраняется в течение 5 лет. Для его поддержания требуется делать ревакцинацию. Повторно прививка ставится в возрасте 7 и 14 лет. В ходе исследований доказано, что делать ревакцинацию в дальнейшем нецелесообразно.
Контроль за способностью организма сопротивляться коварной бактерии осуществляется через пробу Манту. Это не прививка, и ее следует делать ежегодно.
Резюме
Нужна ли прививка БЦЖ ребенку, и стоит ли ее делать, решают родители. Противотуберкулезная вакцинация, как и все прочие медицинские манипуляции, имеет противопоказания, возможны осложнения. Важно разумно подойти к решению данного вопроса, оценив все сопутствующие риски.
Прививка АКДС (дифтерия, коклюш, столбняк) в Днепре
Впервые вакцина назначается на 2 месяце жизни ребенка, каждая последующая не менее чем через 45 суток после предыдущей. Первая ревакцинация осуществляется через год после последней прививки.
Реакция на прививку АКДС
Независимо от состояния здоровья ребенка, реакция иммунитета на препарат возможна и этого не стоит бояться. Это случается из-за того, что в организм вводится инородный материал и защитная система организма обязана на это отреагировать. Поэтому, считается, что прививка от дифтерии, столбняка или коклюша может вызывать типичные реакции (не вызывающие опасений) и нетипичные (те, с которыми лучше обратиться в больницу).
Возможные реакции, которые могут наблюдаться в течении нескольких дней:
- местные реакции в места укола появляется из-за того, что нарушена целостность кожного покрова и мышцы. К тому же, в этом месте лимфоциты начинают воздействовать на чужеродные элементы;
- температура может повышаться до 39 С из-за коклюшного компонента препарата. Однако высокая температура, которая не спадает в течении более 2 дней — тревожный симптом, с которым следует обращаться в больницу;
- реакции, подобные реакциям на вирусную инфекцию.
Нетипичные реакции, при возникновении которых, обращайтесь к врачу:
- судороги нередко наблюдаются при повышенной температуре или неврологии. Бывают как единичные, так и частые. Вне зависимости от вида судорог следует немедленно за неотложной помощью;
- ухудшение состояние здоровья возникает при скрытом течении какого-либо заболевания на момент вакцинации, в следствии чего иммунитет не в состоянии нормально принять компоненты вакцины;
- аллергические проявления на компоненты вакцины проявляются как симптомы отравления. Зачастую эти признаки проходят довольно быстро, но присутствует риск анафилактического шока — поэтому не стоит медлить, обратитесь сразу же в медучреждение.
Как подготовиться к прививке
Перед прохождением процедуры вакцинации одной из важнейших задач родителей является подготовка ребенка. Необходимо пройти обследование о врача — это делается для того, чтобы выявить наличие или отсутствие заболеваний у ребенка. Причина заключается в том, что прививка от столбняка, коклюша и дифтерии оказывает дополнительную нагрузку на иммунитет. Поэтому при не выявленных болезнях возможно появление серьезных побочных эффектов, о которых мы писали выше.
Куда делают прививку
Прививка от коклюша, столбняка и дифтерии должна вводиться внутримышечно. Это вызвано тем, что компоненты препарата должны высвобождаться с правильной скоростью для формирования иммунитета.
Детям вакцина АКДС вводится в бедро, поскольку мышцы ног лучше развиты у малышей. В более взрослом возрасте прививка осуществляется в плечо при хорошо развитой мышечной системе.
Противопоказания для прививки АКДС
Общие противопоказания:
- острые заболевания у ребенка с температурой;
- иммунодефицит;
- непереносимость компонентов вакцины.
Временные противопоказания, в виде острых заболеваний исключаются путем назначения лечения, и после полного восстановления состояния здоровья проводится вакцинация.
Для соблюдения схемы вакцинации при повышенной температуре или неврологических симптомах, может назначаться инъекция препаратом без коклюшной составляющей.
Не позволяет осуществлять прививку АКДС — наличие аллергических или неврологических реакций на компоненты препарата.
Вакцины АКДС в клинике Семейный Доктор
Прививка АКДС в Днепре в МЦ «Семейный Доктор» осуществляется европейскими препаратами, зарегистрированными в Украине:
Препараты производства «Санофи Пастер С.A.», Франция: «Тетраксим» (АаКДС-ИПВ), «Пентаксим» (АаКДС-ИПВ-Хиб), «Гексаксим» (АаКДС-ИПВ-Хиб-ГепВ).
Препараты производства «ГлаксоСмитКляйн Байолоджикалз С.А.», Бельгия: «Инфанрикс (АаКДС), «Инфанрикс ИПВ» (АаКДС-ИПВ), «Инфанрикс Гекса» (АаКДС-ИПВ-Хиб-ГепВ), «Бустрикс» (АаКДС-м), «Бустрикс полио».
В состав перечисленных выше вакцин, включен ацелюлярный(безклеточный) коклюшный компонент, благодаря чему снижается риск возникновения реакций на прививку в более чем 30 раз (в отличии от цельноклеточных вакцин).
Разовая доза вакцины составляет 0,5 мл, упаковка представлена шприцом со специальной конструкцией, который оснащен иглой, благодаря которой боль от инъекции становится минимальной. Кроме того, такой шприц не может быть использован дважды и его формат исключает введение излишнего количества препарата.
После инъекции не следует торопиться домой — некоторое время за ребенком должен наблюдать медперсонал, который сможет вовремя предпринять меры при появлении аллергических реакций.
Медицинский центр Семейный Доктор
- Комфорт и удобные условия для пациентов и посетителей;
- Внимательный персонал;
- Оформление справок и больничных листов для наших пациентов;
- Ведется предварительная запись, которая исключает формирование очередей и гарантирует экономию времени;
- Ведение электронной медицинской документации.
ДОВЕРЬТЕ СВОЕ ЗДОРОВЬЕ СПЕЦИАЛИСТАМ МЦ «СЕМЕЙНЫЙ ДОКТОР»!
Транскрипционное профилирование микобактериальных антиген-индуцированных ответов у младенцев, вакцинированных БЦЖ при рождении
BMC Med Genomics. 2009; 2: 10.
, 1 , 2 , 2 , 3 , 4 , 2 , 1 и 2Хелен А. Флетчер
1 Институт Дженнера , ORCRB, Оксфордский университет, больница Черчилля, Оксфорд, OX3 7DQ, Великобритания
Алана Кейзер
2 Южноафриканская инициатива по созданию вакцины против туберкулеза, Институт инфекционных заболеваний и молекулярной медицины и Школа здоровья детей и подростков, Кейптаунский университет Таун, Южная Африка
Марк Боумейкер
2 Южноафриканская инициатива по созданию вакцины против туберкулеза, Институт инфекционных заболеваний и молекулярной медицины и Школа здоровья детей и подростков, Кейптаунский университет, Южная Африка
Питер Сэйлз
3 Trudeau Institute Inc., Saranac Lake, NY, USA
Gilla Kaplan
4 Лаборатория микобактериального иммунитета и патогенеза, Научно-исследовательский институт общественного здравоохранения, Ньюарк, Нью-Джерси, США
Грег Хасси
2 Южноафриканская инициатива по вакцинации против туберкулеза, Институт Инфекционные заболевания и молекулярная медицина, Школа здоровья детей и подростков, Университет Кейптауна, Южная Африка
Адриан В.С. Хилл
1 Институт Дженнера, ORCRB, Оксфордский университет, Больница Черчилля, Оксфорд, OX3 7DQ, Великобритания
Willem A Hanekom
2 Южноафриканская инициатива по созданию вакцины против туберкулеза, Институт инфекционных болезней и молекулярной медицины и Школа здоровья детей и подростков, Кейптаунский университет, Южная Африка
1 Институт Дженнера, ORCRB, Университет Оксфорд, больница Черчилля, Оксфорд, OX3 7DQ, Великобритания
2 Южноафриканская инициатива по вакцине против туберкулеза, Ins титул инфекционных болезней и молекулярной медицины и Школа здоровья детей и подростков, Университет Кейптауна, Южная Африка
3 Trudeau Institute Inc., Саранак Лейк, Нью-Джерси, США
4 Лаборатория микобактериального иммунитета и патогенеза, Научно-исследовательский институт общественного здравоохранения, Ньюарк, Нью-Джерси, США
Автор, отвечающий за переписку.Поступило 23 июня 2008 г .; Принято 24 февраля 2009 г.
Copyright © 2009 Fletcher et al; лицензиат BioMed Central Ltd.Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License (http://creativecommons.org/licenses/by/2.0), которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе. при условии правильного цитирования оригинала.
Эта статья цитируется в других статьях в PMC.- Дополнительные материалы
Дополнительный файл 1 Праймеры, разработанные для подтверждения дифференциальной экспрессии генов, идентифицированных с помощью микроматричного анализа. Подробная информация о последовательности праймеров, температурах отжига праймеров и размерах продуктов ПЦР.
GUID: D9C0FB2B-C853-488F-AADF-D9BF259AA0A7
Дополнительный файл 2 BCG и PPD p -значения. Log-кратное изменение, p -значения, скорректированные p -значения, модерированные t-статистика и модерированные значения B-статистики для каждого гена, дифференциально выраженного между стимулированными и нестимулированными PBMC, с скорректированным p -значение <0.01.
GUID: EE69319B-AB9D-457F-A8FB-ABFE539D85BD
Дополнительный файл 3 BCGvPPD Venn lists. Список генов, дифференциально экспрессируемых при стимуляции БЦЖ и PPD, по данным анализа Венна.
GUID: C14F0C1D-2212-48D2-9DE0-593E69D40E64
Дополнительный файл 4 Гены с более чем двукратной разницей в экспрессии в ответ на стимуляцию БЦЖ по сравнению с PPD. Подробная аннотация генов, по-разному экспрессируемых при стимуляции БЦЖ и PPD.
GUID: F8B2096B-943B-4D08-AEC4-A5FC8C350CB7
Дополнительный файл 5 Гены в категориях GO. Списки генов, которые попадают в различные категории GO, с инвентарным номером и символом гена.
GUID: 088FE7B6-4608-40D9-ACB4-059CEFF5AB61
Дополнительный файл 6 Экспресс-списки путей . Списки генов, представленных в путях Кегга (символы генов).
GUID: 3CFF46B3-CB25-4D67-8E8E-2E44F20F6709
Резюме
Предпосылки
Новые вакцины против туберкулеза (ТБ), недавно испытанные на людях, были разработаны для повышения иммунитета, индуцированного нынешней вакциной, 9010ov Bacillebacterium Mycobacterium Кальмет-Герен (BCG).Поскольку вакцинация БЦЖ широко используется у младенцев, эта группа населения, вероятно, станет первой, в которой будут проводиться испытания эффективности новых вакцин. Однако наше понимание сложности иммунитета к БЦЖ у младенцев недостаточно, что затрудняет интерпретацию иммунных ответов, вызванных вакциной.
Методы
Чтобы лучше понять иммунитет, индуцированный БЦЖ, мы выполнили профили экспрессии генов у пяти 10-недельных младенцев, регулярно вакцинированных БЦЖ при рождении.РНК экстрагировали из 12-часового BCG-стимулированного или очищенного белкового производного PBMC, стимулированного туберкулином (PPD), выделенного из крови новорожденных, собранных через 10 недель после вакцинации. РНК гибридизовали с чипом Sentrix ® HumanRef-8 Expression BeadChip (Illumina) для измерения экспрессии> 16000 генов.
Результаты
Мы обнаружили, что стимуляция ex vivo PBMC с помощью PPD и BCG индуцировала в значительной степени сходные профили экспрессии генов, за исключением того, что BCG индуцировала большую активацию макрофагов.Сигнальный путь рецептора, активируемого пролифератором пероксисом (PPAR), включая PPAR-γ, участвующий в активации альтернативного противовоспалительного ответа макрофагов, подавлялся после стимуляции обоими антигенами. Напротив, была отмечена повышающая регуляция генов, связанных с классическим провоспалительным ответом макрофагов. Дальнейший анализ выявил снижение экспрессии молекул клеточной адгезии (CAM), включая интегрин альфа M (ITGAM), который, как известно, важен для проникновения микобактерий в макрофаг.Интересно, что больше генов лейкоцитов подвергалось подавлению, чем повышению.
Заключение
Наши результаты предполагают, что комбинация подавленных и активируемых генов может быть ключевой в определении развития защитного иммунитета против ТБ, индуцированного вакцинацией БЦЖ.
Общие сведения
Во всем мире ежегодно от туберкулеза (ТБ) умирают два миллиона человек, и, по оценкам, два миллиарда человек, треть населения мира, латентно инфицированы Mycobacterium tuberculosis ( M.тб) . Туберкулез является ведущей идентифицируемой причиной смерти среди ВИЧ-инфицированных [1]: по оценкам, четверть миллиона смертей среди ВИЧ-инфицированных в год связаны с туберкулезом. Улучшенная вакцина против туберкулеза была бы наиболее эффективным вмешательством в борьбе с болезнью. Бацилла Кальметта-Герена (БЦЖ), впервые использованная в качестве вакцины для человека в 1921 году, является одной из наиболее широко применяемых вакцин в мире. БЦЖ обеспечивает 80% защиту от тяжелого детского туберкулеза; однако защита от легочного туберкулеза различна и в большинстве случаев недостаточна для всех возрастов [2].Поэтому существует острая необходимость в разработке улучшенных противотуберкулезных вакцин. Появилось множество новых вакцин-кандидатов, которые демонстрируют некоторую защиту у мышей, зараженных вирулентным M.tb [3]. Большинство новых вакцин-кандидатов разработаны для повышения иммунитета, который был вызван предыдущей вакцинацией БЦЖ; однако об иммунитете, индуцируемом БЦЖ у взрослых, известно недостаточно. Еще меньше известно об иммунитете у вакцинированных новорожденных . В этом исследовании была предпринята попытка восполнить некоторые пробелы в наших знаниях путем изучения профилей экспрессии мРНК после вакцинации новорожденных БЦЖ.
ДНК-микрочипы все чаще используются для оценки профилей экспрессии мРНК, связанных с взаимодействиями хозяин-патоген. В области исследований ТБ микроматрицы использовались для изучения изменений в экспрессии генов в макрофагах, инфицированных ТБ [4,5]. Также были изучены различия в ответах хозяина между больными туберкулоидной и лепроматозной лепрой [6], а также между пациентами с легочным и диссеминированным туберкулезом [7]. В целом, отчеты о применении массивов у младенцев скудны и включают оценку различий в профилировании транскрипции между острой и выздоравливающей инфекцией гриппа младенцев в качестве инструмента для различения острых инфекционных состояний у младенцев [8,9].Более того, микроматричный анализ младенческих PBMC не использовался в исследованиях туберкулеза, возможно, из-за больших объемов крови, обычно требуемых для матричного анализа. PBMC все чаще используются в качестве суррогатной ткани для молекулярной диагностики заболеваний, затрагивающих менее доступные ткани, такие как легкие, почки и сердце. Это связано с тем, что изменения в PBMC, вероятно, отражают патологические и иммунологические изменения, которые происходят в других частях тела [10]. Точно так же было обнаружено, что целые популяции PBMC полезны для оценки различий в транскрипционных ответах, индуцированных различными микобактериальными антигенами [7,11].Здесь мы описываем разработку анализа экспрессии генов для обнаружения антиген-специфических ответов в PBMC новорожденных, вакцинированных БЦЖ. Наша цель состояла в том, чтобы оценить специфические различия в профилях экспрессии мРНК, индуцированных 2 микобактериальными антигенами, M. bovis, BCG и M.tb , очищенным производным белка туберкулина (PPD), чтобы направлять использование антигена в будущих более детальных исследованиях. Первый антиген состоит из цельной жизнеспособной авирулентной микобактерии, которая может фагоцитироваться и процессироваться моноцитами в PBMC для представления как белковых, так и небелковых антигенов.Напротив, PPD состоит только из растворимых белков вирулентного M.tb .
Методы
Участники исследования и сбор крови
В исследование были включены здоровые 10-недельные младенцы из региона Кейптаун, Южная Африка. Всех младенцев регулярно вакцинировали внутрикожной БЦЖ (Statens Serum Institute, Копенгаген) в течение 48 часов после рождения. Младенцы, рожденные от ВИЧ-положительных матерей, младенцы, заведомо инфицированные ВИЧ, младенцы с подозрением на или подтвержденное заболевание ТБ, а также младенцы с любыми другими активными или хроническими заболеваниями на момент включения в исследование были исключены.Участие людей соответствовало требованиям Министерства здравоохранения и социальных служб США и руководящим принципам надлежащей клинической практики. Это включало утверждение протокола комитетом по этике исследований Университета Кейптауна и Советом по институциональной проверке (IRB) UMDNJ. Письменное информированное согласие было получено от всех матерей, чьи дети принимали участие в исследовании. У каждого здорового младенца собирали до 10 мл цельной крови.
Выделение, инкубация и очистка РНК РВМС
РВМС выделяли из периферической венозной крови центрифугированием в градиенте плотности и криоконсервировали.Позже PBMC оттаивали, промывали в RPMI 1640 (Biowhittaker, Walkersville, MD, USA) и «отдыхали» в течение 6 часов при 1 × 10 6 клеток в 1 мл 10% объединенной сыворотки AB человека в RPMI 1640 с добавлением L -глутамин в концентрации 2 мМ (Biowhittaker), при 37 ° C и в 5% CO 2 . Затем к клеткам добавляли PPD (20 мкг / мл) или BCG, восстановленные из флакона с вакциной, как описано ранее [12], с MOI 0,18. РВМС, инкубированные только со средой, служили отрицательным (нестимулированным) контролем. Инкубацию продолжали в течение 12 часов при 37 ° C и в 5% CO 2 , после чего клетки собирали и обрабатывали с помощью набора QIAamp RNA Blood Mini (Qiagen, Hilden, Германия) в соответствии с инструкциями производителя для выделения РНК.РНК обрабатывали ДНКазой с использованием набора для расщепления ДНКазой на колонке (Qiagen, Hilden, Германия). Среднее значение 0,37 мкг (0,19-0,52 мкг) РНК было получено из 1 × 10 6 PBMC. Доза БЦЖ и продолжительность инкубации были найдены оптимальными в пилотных экспериментах, в которых оценивали повышающую регуляцию нескольких цитокинов Т-хелперов типа 1 (Th2), апоптоза и регуляторных генов с помощью ОТ-ПЦР в реальном времени (данные не показаны). РНК подвергали криоконсервации при -80 ° C для последующего использования в экспериментах с ДНК-микромассивом и ОТ-ПЦР.
Протокол амплификации РНК
Медиана 124 нг (диапазон 63–174 нг) экстрагированной РНК была амплифицирована с использованием набора для амплификации РНК Illumina (Ambion, Остин, Техас, США) на основе протокола Eberwine [13].Метка биотин-16-UTP была включена в амплифицированную РНК во время процесса транскрипции in vitro (Perkin Elmer Life and Analytical Sciences, Вудбридж, Онтарио, Канада). Амплификация дала выходы от 1 мкг до 25 мкг. Амплифицированную РНК (1000 нг на матрицу) гибридизовали с Illumina HumanRefSeq-8 BeadChip в соответствии с инструкциями производителя (Illumina, San Diego, CA, USA). Чип-бусинка HumanRefSeq-8 состоит из 24 000 последовательностей, представляющих 16 238 генов из тщательно подобранной части базы данных эталонных последовательностей NIH http: // www.ncbi.nlm.nih.gov/RefSeq/. Каждая последовательность представлена в массиве не менее 30 раз. Массивы сканировали с помощью конфокального сканера считывателя шариковых матриц Illumina в соответствии с инструкциями производителя. Обработка и анализ данных массива выполнялись с использованием программного обеспечения Illumina BeadStudio.
ОТ-ПЦР в реальном времени
Среднее значение 124 нг (диапазон 63–174 нг) РНК было обратно транскрибировано в кДНК с использованием oligo-dT и Omniscript Kit (Qiagen). кДНК хранили при -20 ° C до использования. ПЦР в реальном времени выполняли с использованием Roche LightCycler ® и мастермикса Quantitect (Qiagen).
Количественно очищенный и разбавленный продукт ПЦР использовали для построения кривых внешнего стандарта для каждой пары праймеров. Значения числа циклов были преобразованы в число копий с использованием этих кривых после амплификации. Все праймеры (синтезированные Integrated DNA Technologies, Торонто, Канада) были разработаны для охвата последовательностей интрон-экзон, чтобы различать мРНК и геномную ДНК (дополнительный файл 1). В каждой реакции использовали 1 мкл кДНК. Условия цикла состояли из начальной стадии активации продолжительностью 15 минут при 95 ° C, затем 45 циклов продолжительностью 15 секунд при 94 ° C, 20 секунд при 60 ° C и 15 секунд при 72 ° C, использовались для каждой пары праймеров.Для контроля за изменением количества кДНК между образцами число копий интересующего гена делили на количество копий гена домашнего хозяйства HPRT. Все реакции ПЦР проводили в двух экземплярах.
Анализ данных
Данные были нормализованы с помощью программного обеспечения VSN2 «Стабилизация и калибровка дисперсии для данных микроматрицы», которое доступно как часть проекта BioConductor (проект программного обеспечения с открытым исходным кодом для предоставления инструментов для анализа геномных данных) [14 ] Файлы данных доступны в репозитории данных Gene Expression Omnibus: {«type»: «entrez-geo», «attrs»: {«text»: «GSE14408», «term_id»: «14408»}} GSE14408.Перед идентификацией дифференциально экспрессируемых генов был проведен кластерный анализ K-средних (программное обеспечение kmeans, BioConductor) для выявления образцов с выбросами. Было обнаружено, что нестимулированные образцы сгруппированы вместе, а стимулированные образцы сгруппированы вместе (с небольшими различиями между БЦЖ и PPD) без выбросов, поэтому все образцы были включены в последующий анализ.
Дифференциально экспрессируемые гены были идентифицированы с использованием eBayes, который является компонентом программного пакета Limma: Linear Models for Microarray data (BioConductor) [15].eBayes — это эмпирическая байесовская модель, которая оценивает истинный сигнал экспрессии путем заимствования информации из генов и повышения стабильности анализа [16]. Статистика для дифференциальной экспрессии, предоставляемая eBayes, включает (логарифмическое) кратное изменение, модерируемую статистику t- (такая же, как t-статистика, за исключением того, что стандартные ошибки были модерированы по генам), p -значение (на основе модерированного t -статистика), скорректированное значение p (скорректированная частота ложного обнаружения p -значение) и B -статистика (логарифм шансов того, что ген выражается дифференциально).
Уровень экспрессии генов, дифференциально экспрессируемых при стимуляции БЦЖ (с скорректированным значением p <0,01), сравнивали с генами, дифференциально экспрессируемыми при стимуляции PPD (со скорректированным значением p <0,01) с использованием двустороннего Корреляция Спирмана (SPSS).
Подмножество генов с скорректированным значением p <0,01 и> 2-кратной дифференциальной экспрессией в PBMC, стимулированных PPD и BCG, отбирали для подтверждения экспрессии с помощью RT-PCR в реальном времени.Дифференциально экспрессируемые гены также оценивались в соответствии с категориями онтологии генов (GO) (Onto-Express), а анализ пути проводился с использованием Pathway-Express [17].
Результаты
Повышенная или пониженная регуляция генов после инкубации PBMC с БЦЖ или PPD
В исследование были включены пять 10-недельных младенцев, регулярно вакцинированных БЦЖ при рождении. Анализ микромассивов ДНК выполняли с использованием амплифицированной РНК, очищенной из криоконсервированных PBMC, которые позже размораживали и инкубировали только с BCG, PPD или средой (нестимулированной) в течение 12 часов.Используя кластеризацию K-средних по трем условиям инкубации и используя все гены, нестимулированные образцы кластеризовались вдали от образцов, стимулированных БЦЖ и PPD (рисунок). Однако образцы, стимулированные БЦЖ и PPD, не были разделены этим анализом (рисунок). В целом БЦЖ индуцировала дифференциальную экспрессию 411 генов (p <0,01, eBayes) по сравнению с нестимулированным контролем. Из 411 генов 136 были активированы, а 275 - подавлены (дополнительный файл 2). PPD индуцировал дифференциальную экспрессию в 291 гене (p <0.01, eBayes, Дополнительный файл 2). Из 291 гена 95 были активированы, а 196 - подавлены. Из значительно дифференцированно экспрессируемых генов 74 и 73 гена были активированы более чем в 2 раза BCG и PPD, соответственно; Гены 201 и 127 были подавлены более чем в 2 раза в этих соответствующих условиях (дополнительный файл 2). Мы пришли к выводу, что профили экспрессии генов, полученные при стимуляции PBMC с помощью BCG, недостаточно отличались от профилей экспрессии, полученных при стимуляции клеток с помощью PPD, чтобы образцы могли попасть в отдельные кластеры.
Тепловая карта профилей экспрессии генов с более чем 2-кратным изменением экспрессии в ответ на стимуляцию БЦЖ по сравнению с нестимулированным контролем . Гены были упорядочены в соответствии с их кластером, определенным алгоритмом k-средних. Значения увеличиваются от зеленого к красному через черный. Условия инкубации и идентификаторы участников приведены под тепловой картой, например, «UNS.028» относится к РВМС, инкубированным без каких-либо специфических антигенов (нестимулированных) у участника 28.
Подробное сравнение профилей экспрессии, индуцированных БЦЖ и PPD
Ниже оба условия стимуляции: интерлейкин 6 (IL-6), гранулоцитарный моноцитарный колониестимулирующий фактор (GM-CSF) и член семейства интерлейкина 1 8 (IL1F9) показали наибольшее увеличение экспрессии.Гены с наибольшим снижением экспрессии в обоих условиях включают белок, связывающий жирные кислоты 4 (FABP4), рецептор колониестимулирующего фактора 1 (CSF1) и трансформирующий фактор роста бета 1 (TGF-β1) (дополнительный файл 2).
Затем мы сравнили дифференциальную экспрессию генов после стимуляции БЦЖ (411 генов) и стимуляции PPD (291 ген) по сравнению с нестимулированными контролями. Большая часть генов экспрессировалась в обоих условиях стимуляции, при этом только 33 гена экспрессировались в ответ только на PPD (рисунок и дополнительный файл 3).Большинство генов было экспрессировано в эквивалентной степени, и наблюдалась сильная корреляция между PPD и стимуляцией БЦЖ (r = 0,965, P <0,000001; рисунок). Только 29 генов по-разному экспрессировались более чем в 2 раза в двух условиях стимуляции (дополнительный файл 4). БЦЖ вызывала более чем 2-кратное изменение экспрессии фактора, стимулирующего колонии гранулоцитов (G-CSF), матриксной металлопротеиназы 1 (MMP1), гуанилатсвязывающего белка 1 (GBP1) и GM-CSF, по сравнению с PPD. В свою очередь, PPD индуцировал более чем 2-кратное увеличение экспрессии хемокина (мотив CXC), лиганда 5 (CXCL5), тромбомодулина (THBD), цитокиноподобного ядерного фактора n-pac (N-PAC) и тромбоспондина 1 (THBS1), по сравнению с с BCG.Большая разница была замечена в количестве генов, подавляемых BCG и PPD. БЦЖ снижала экспрессию 21 гена более чем в 2 раза по сравнению с PPD (дополнительный файл 4).
Пропорциональное распределение генов Венна со значением p <0,01, выраженное в ответ на стимуляцию БЦЖ или PPD . Диаграмма Венна показывает перекрытие в экспрессии генов между 411 генами, индуцированными БЦЖ, и 291 генами, индуцированными стимуляцией PPD.
Сравнение экспрессии генов, индуцированной в ответ на стимуляцию PPD и BCG .Данные были нормализованы с использованием метода стабилизации дисперсии (VSN2), и гены, значительно индуцированные стимуляцией PPD и BCG, по сравнению с нестимулированным контролем, были объединены в единый список генов: показан разброс этих генов в ответ на любую стимуляцию. Для оценки корреляции использовался ранговый тест Спирмена (r = 0,965, p <0,000001). Линии указывают на разницу в выражении более чем в 2 раза.
Мы пришли к выводу, что большинство генов, активируемых или подавляемых стимуляцией БЦЖ, также активируются или подавляются стимуляцией PPD по сравнению с нестимулированным контролем.
Подтверждение паттернов экспрессии с помощью ОТ-ПЦР в реальном времени
Для подтверждения паттернов экспрессии генов, идентифицированных с помощью массива, была проведена ОТ-ПЦР в реальном времени для конкретных генов с использованием общей РНК от 5 младенцев, использованных для анализа массива, и с использованием РНК от 10 дополнительных 10-недельных младенцев, регулярно вакцинированных БЦЖ при рождении (всего 15 младенцев для анализа RT-PCR). РВМС от последних младенцев были обработаны так же, как РВМС от младенцев, РНК которых была исследована в исследовании массива.Праймеры были сконструированы против выбранных транскриптов, и было определено число копий каждого гена относительно гена домашнего хозяйства HPRT. Было обнаружено соответствие между результатами микроматрицы ДНК и результатами ОТ-ПЦР в реальном времени в отношении экспрессии как высоко, так и умеренно экспрессируемых генов в ответ на БЦЖ (рисунок) и PPD (рисунок). Когда медиана экспрессии массива от 5 младенцев, выбранных для анализа массива, сравнивалась со средней экспрессией ОТ-ПЦР от общей когорты из 15 младенцев, значимая корреляция была обнаружена после обоих PPD (r = 0.806, p = 0,005, тест Спирмена) и стимуляция БЦЖ (r = 0,697, p = 0,025, тест Спирмена). Хотя величина ответа была больше на БЦЖ, чем на PPD, вариабельность ответа на стимуляцию БЦЖ также была больше.
Сравнение экспрессии генов с высокой и умеренной экспрессией с использованием ДНК-микрочипов и ОТ-ПЦР в реальном времени . Показана экспрессия генов по отношению к среде, для BCG (A) и PPD (B). В анализе на микрочипах участвовали 5 младенцев, тогда как в анализе ОТ-ПЦР в реальном времени участвовали эти 5 младенцев плюс еще 10 младенцев (всего n = 15).Коробчатые диаграммы представляют медианное значение плюс 95 -го , 75 -го , 50 -го и 25 -го процентилей.
Мы пришли к выводу, что паттерны экспрессии генов, обнаруженные с помощью анализа массива, могут быть подтверждены анализом ОТ-ПЦР в реальном времени.
Онтология генов, дифференциально экспрессируемых в ответ на стимуляцию BCG
Транскрипты, дифференциально экспрессируемые в ответ на стимуляцию как BCG, так и PPD, анализировали с помощью инструмента Gene Ontology (GO) Onto-Express, инструмента анализа, доступного в ансамбле Onto-Tools [18].Поскольку между двумя условиями стимуляции была небольшая разница в экспрессии генов, результаты GO, полученные для BCG и PPD, были очень похожими (дополнительный файл 5). Следовательно, только результаты GO для 411 генов, экспрессируемых в ответ на БЦЖ, показаны на рисунке.
Анализ генной онтологии генов, дифференциально экспрессируемых в ответ на стимуляцию БЦЖ, по сравнению с нестимулированным контролем (n = 411) . (A) Термины генной онтологии для ответа на родительский термин стимула.(B) Термины генной онтологии для родительского термина «Ответ на внешний стимул».
База данных GO позволяет классифицировать ген на основе его функции, то есть биологической, клеточной или молекулярной функции. Наибольшая доля генов, сопоставленных с GO: Ответ на внешний стимул (120 генов), p = <1,0 × 10 -5 (рисунок). Дополнительное картирование показало сильную статистическую значимость для GO: Ответ на стресс (74 гена), p = <1,0 × 10 -5 (рисунок), который включает большое количество генов воспалительного иммунного ответа (дополнительный файл 5).
Анализ путей дифференциально экспрессируемых генов
Pathway-Express (PE) — это инструмент анализа путей в ансамбле Onto-Tools, использующий доступную информацию о путях Киотской энциклопедии генов и геномов (KEGG) [17,19]. Этот инструмент генерирует, во-первых, значение вероятности ( p) на основе количества генов, присутствующих в конкретном пути. Во-вторых, фактор возмущения (гамма p ) вычисляется с учетом (i) нормализованного кратного изменения гена и (ii) количества генов перед его положением на основе пути.Затем значение p и значение гаммы p объединяются для получения импакт-фактора, который можно использовать для ранжирования путей в порядке их биологической значимости. После стимуляции БЦЖ 21 путь имел статистически значимое значение гамма p <0,01, а 17 путей имели значение гамма p <0,01 после стимуляции PPD (таблица). Путь с самым высоким импакт-фактором после стимуляции БЦЖ - это молекулы клеточной адгезии (CAM) с подавлением 4 генов после стимуляции БЦЖ (дополнительный файл 6).Путь с самым высоким импакт-фактором после стимуляции PPD - это путь клонирования гемопоэтических клеток (дополнительный файл 6). Четыре пути были значимыми после стимуляции БЦЖ, но не после PPD (таблица).
Таблица 1
Анализ уровня пути генов, дифференциально экспрессируемых после стимуляции БЦЖ.
| Стимуляция БЦЖ | Стимуляция PPD | ||||||||||||||||||||||
| Название пути | Рейтинг | 0a Impact Pathway | c p -значение | d гамма p -значение | Rank | a Impact Factor8 Путь | c p -значение | d гамма p -значение | |||||||||||||||
| Молекулы клеточной адгезии (CAM | 44/133 | 0,153 | 9.00E-19 | — | — | — | — | — | |||||||||||||||
| Цитокиновый рецептор | Взаимодействие с цитокин-рецептором34/259 | 1.31E-12 | 3.51E-14 | 15 | 7.2 | 27/259 | -5.50E-14 | 0,006 | |||||||||||||||
| 3 | 30.6 | 14/88 | 8.34E-11 | 1.57E-12 | 1 | 27,3 | 12/88 | 2.68E-10 | 3.86E-11 | ||||||||||||||
| Путь передачи сигнала толл-подобных рецепторов | 4 | 26,4 | 14/102 | 6,39E-10 | 9,56E-11 | 4 | 18,3 | 9/102 | 2.11E3 2,14336 | -07 | |||||||||||||
| Сигнальный путь Fc-эпсилон RI | 5 | 21.6 | 2/77 | 0,336 | 9.24E-09 | 11 | 10,2 | 2/77 | 0,211 | 4.24E-04 | |||||||||||||
| 6 | 21,3 | 13/153 | 8.33E-07 | 1.22E-08 | 6 | 14.0 | 8/153 | 3.24E-04 | 1.21E-05 34 34 | ||||||||||||||
| Болезнь трансплантат против хозяина | 7 | 20.1 | 5/42 | 4.65E-04 | 4.03E-08 | 3 | 18,6 | 5/42 | 9.93E-05 | 1.67E-07 | |||||||||||||
| Сигнальный путь MAPK | 8 | 17,0 | 13/265 | 2,78E-04 | 7,67E-07 | 5 | 16,0 | 9/265 | 0,003 | 1,98 | |||||||||||||
| Сигнальный путь TGF-beta | 9 | 16.9 | 1/89 | 0,752 | 8,29E-07 | 10 | 10,6 | 3/89 | 0,079 | 3.01E-04 | |||||||||||||
| 15,8 | 1/97 | 0,781 | 2,29E-06 | 2 | 26,2 | 1/97 | 0,662 | 1,15E-10 | |||||||||||||||
| 14.1 | 6/84 | 0,002 | 1,13E-05 | 7 | 13,4 | 4/84 | 0,014 | 2,24E-05 | |||||||||||||||
| 13.9 | 6/44 | 5.76E-05 | 1.33E-05 | 8 | 12.9 | 5/44 | 1.25E-04 | 3.43E-05 | 34 34 903|||||||||||||||
| Путь передачи сигналов рецептора Т-клеток | 13 | 13.1 | 6/93 | 0,003 | 2,84E-05 | 13 | 8,8 | 3/93 | 0,085 | 0,001 | |||||||||||||
| 9033 9035 | 8/69 | 1.14E-05 | 5.14E-05 | 9 | 12.0 | 7/69 | 1.16E-05 | 8.11E-05 | |||||||||||||||
| Цитотоксичность, опосредованная киллерными клетками | 15 | 11.4 | 5/131 | 0,054 | 1.34E-04 | 14 | 7,9 | 3/131 | 0,179 | 0,003 | |||||||||||||
| 9,0 | 3/44 | 0,031 | 0,001 | 17 | 6,6 | 1/44 | 0,388 | 0,009 | |||||||||||||||
| 4/72 | 0,026 | 0,001 | — | — | — | — | — | ||||||||||||||||
| Эпителиальная инфекция | 4/69 | 0,022 | 0,002 | 12 | 9,5 | 3/69 | 0,041 | 7,85E-04 | |||||||||||||||
| каскадов и коагуляции 66 | 6/69 | 7.06E-04 | 0,004 | — | — | — | — | — | |||||||||||||||
| / 42 | 0,027 | 0,008 | 16 | 6,9 | 3/42 | 0,011 | 0,008 | ||||||||||||||||
| Острый миелоидный лейкоз | 6,98 | 5/57 | 0,002 | 0,008 | — | — | — | — | — | ||||||||||||||
Мы пришли к выводу, что стимуляция БЦЖ подавляет экспрессию белков, важных для клеточной адгезии. анализ этого пути является полезным инструментом для анализа профилей экспрессии, индуцированных микобактериальными антигенами.
Экспрессия генов, связанных с макрофагами
Микобактерии — это внутриклеточные патогены, которые в первую очередь инфицируют макрофаги.Реакция макрофагов (Mφ) на микобактериальную инфекцию может иметь решающее значение для определения того, исчезла ли инфекция или переходит ли инфекция в заболевание. Макрофаги представляют собой гетерогенную популяцию клеток с различными функциями. Mφ1 поддерживает защитный ответ Th2, тогда как Mφ2 демонстрирует плохую способность к презентации антигена и подавляет функцию Th2 [20-23]. Мы обнаружили, что многие гены, активируемые как BCG, так и PPD в PBMC наших младенцев, ранее были связаны со взрослыми макрофагами Mφ1, включая IL-1β, IL-8, IL-6, фактор некроза опухоли альфа (TNF-α), интерферон-индуцируемый белок 10 (IP10), воспалительный белок макрофагов (MIP) -1β и хемокин, полученный из макрофагов (MDC) (таблица) [4,21,24-26].Путем анализа генов, подавляемых микобактериальными антигенами, мы выявили дополнительные доказательства поляризации макрофагов: гены в сигнальном пути рецептора, активируемого пролифератором пероксисом (PPAR), связанного с поляризацией макрофагов в фенотип Mφ2, подавлялись после стимуляции с помощью PPD и BCG, (Дополнительные файлы 2 и 3) [22,23]. Стимуляция БЦЖ подавляла CD36, PPAR-γ и ретиноид-рецептор (RXR) в сигнальном пути PPAR, предположительно смещая моноциты в сторону развития фенотипа Mφ1.
Таблица 2
Гены, идентифицированные как усиленный ответ на стимуляцию антигеном в предыдущих исследованиях с микобактериальными антигенами.
| Genbank | Символ | * Сложите PPD | * Сверните BCG | * BCG поверх PPD | Тип ячейки | Тип ячейки | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| {«type»: «entrez-нуклеотид», «attrs»: {«text»: «NM_000600», «term_id»: «1531243779», «term_text»: «NM_000600»}} NM_000600 | Ил-6 | 67.97 | 83,42 | 1,23 | Mφ1, Mφ, DC | M.tb, BCG | Chaussabel et. al . 2003 Verrek et. al . 2006 Begum et. al . 2004 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| {«type»: «entrez-нуклеотид», «attrs»: {«text»: «NM_000576», «term_id»: «1653962476», «term_text»: «NM_000576»} } NM_000576 | IL-1 β | 17,34 | 15,10 | 0,87 | Mφ1, Mφ, DC, спленоциты морской свинки | M.tb, BCG, PPD | Chaussabel et. al . 2003 Verrek et. al . 2006 Begum et. al . 2004 Khajoee et. al . 2006 Дерево et. al . 2006 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| {«type»: «entrez-нуклеотид», «attrs»: {«text»: «NM_001511», «term_id»: «1653960476», «term_text»: «NM_001511»} } NM_001511 | GRO-1, CXCL1 | 27,12 | 16,89 | 0,62 | Mφ1, Mφ, DC | M.tb, BCG | Chaussabel et. al . 2003 Khajoee et. al . 2006 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| {«type»: «entrez-нуклеотид», «attrs»: {«text»: «NM_002421», «term_id»: «151 | 80″, «term_text»: «NM_002421»} } NM_002421 | MMP1 | 7,21 | 17,18 | 2,38 | Mφ1, Mφ, DC | M.tb, BCG | Chaussabel et. al . 2003 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| {«type»: «entrez-нуклеотид», «attrs»: {«text»: «NM_002089», «term_id»: «151 52″, «term_text»: «NM_002089»} } NM_002089 | GRO-2, CXCL2, MIP-2A | 19.24 | 24.10 | 1,25 | Mφ1, Mφ, DC | M.tb | Chaussabel et. al . 2003 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| {«type»: «entrez-нуклеотид», «attrs»: {«text»: «NM_002090», «term_id»: «1653960532», «term_text»: «NM_002090»} } NM_002090 | GRO-3, CXCL3 | 15,94 | 9,91 | 0,62 | Mφ1 | M.tb | Chaussabel et. al . 2003 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| {«type»: «entrez-нуклеотид», «attrs»: {«text»: «NM_000594», «term_id»: «15119″, «term_text»: «NM_000594»} } NM_000594 | TNF-α | 4.86 | 9,49 | 1,95 | Mφ1, Mφ, DC | M.tb, BCG | Chaussabel et. al . 2003 Verrek et. al . 2006 Begum et. al . 2004 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
{«type»: «entrez-нуклеотид», «attrs»: {«text»: «NM_000963», «term_id»: «151
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
