Интраназальные кортикостероиды при неаллергическом рините
Вопрос обзора
Мы хотели выяснить, являются ли интраназальные кортикостероиды (стероиды, применяемые в нос) эффективными при лечении ринита, который не вызван аллергией.
Актуальность
Неаллергический ринит является хроническим заболеванием носа, которое не вызвано инфекцией или аллергией. Люди, страдающие неаллергическим ринитом, испытывают симптомы (заложенность носа, насморк и чихание), которые могут влиять на качество их жизни. Неаллергический ринит у пациентов можно разделить на различные подгруппы, в зависимости от причин заболевания. Основные причины, вызывающие неаллергический ринит, полностью не изучены, поэтому лечение таких пациентов часто оказывается безуспешным.
Местные (интраназальные) кортикостероиды используются с целью уменьшения воспалительного процесса. Они являются наиболее часто назначаемыми лекарствами при других хронических заболеваниях носа и околоносовых пазух, таких как аллергический ринит и хронический риносинусит. Лечение интраназальными кортикостероидами можно проводить с помощью спреев или капель и в течение различных периодов времени.
Характеристика исследований
В этот обзор были включены 34 рандомизированных контролируемых испытания (РКИ), с общим числом участников — 4452. Большинство исследований были относительно небольшими, хотя, в общей сложности, в самом большом исследовании принимало участие 983 пациента. Все пациенты были либо взрослыми, либо подростками (в возрасте от 12 до 18 лет) с неаллергическим ринитом. В исследованиях рассматривали целый ряд видов, доз и способов введения (например, спреи, капли) интраназальных кортикостероидов. Девять исследований финансировались фармацевтической промышленностью или коммерческими спонсорами. Одно исследование финансировалось правительством. В ряде исследований фармацевтическая промышленность или коммерческий спонсор могли предоставлять лекарства, однако роль финансирования была неясной.
Основные результаты
Интраназальные кортикостероиды в сравнении с плацебо
Неясно, снижают ли интраназальные кортикостероиды степень тяжести заболевания (оцениваемую пациентами) у пациентов, страдающих неаллергическими ринитом, по сравнению с плацебо, при оценке за период до трех месяцев. Они, возможно, уменьшают степень тяжести заболевания (оцениваемую пациентами), по сравнению с плацебо, при оценке за период до четырех недель, однако определенность этих доказательств низкая. Лечение интраназальными кортикостероидами, вероятно, увеличивает риск эпистаксиса (носовое кровотечение), но на риск возникновения других неблагоприятных эффектов не влияет. В рамках этого обзора невозможно сказать, есть ли различия между разными концентрациями, способами доставки (введения) или планами лечения интраназальными кортикостероидами. Нет исследований хорошего качества, оценивающих изменения в качестве жизни при применении интраназальных кортикостероидов.
Интраназальные кортикостероиды в сравнении с другими видами лечения
Нет достаточных доказательств, что лечение интраназальными кортикостероидами при неаллергическом рините лучше, хуже или такое же, в сравнении с другими способами лечения, например, такими как орошение солевым раствором, интраназальные антигистаминные средства, капсаицин или ипратропия бромид.
Определенность доказательств
В целом, определенность доказательств в отношении интраназальных кортикостероидов в сравнении с плацебо для большинства исходов была либо низкой (наша уверенность в оценке эффекта низкая), либо очень низкой (наша уверенность в оценке эффекта очень низка). Это было связано с тем, что исследования были очень небольшими, а для оценки одних и тех же исходов использовали разные методы. Эти доказательства актуальны по состоянию на июль 2019 года.
Интраназальные глюкокортикостероиды — препараты выбора в лечении аллергического ринита
Пройти тестrel=»nofollow»>
Супрун Элина Владиславовна — доктор медицинских наук, профессор кафедры общей фармации и безопасности лекарств Института повышения квалификации специалистов фармации, Национальный фармацевтический университет, ХарьковПиминов Александр Фомич — доктор фармацевтических наук, профессор, заведующий кафедрой общей фармации и безопасности лекарств Института повышения квалификации специалистов фармации, Национальный фармацевтический университет, Харьков
Губченко Татьяна Дмитриевна — кандидат фармацевтических наук, доцент кафедры общей фармации и безопасности лекарств Института повышения квалификации специалистов фармации, Национальный фармацевтический университет, Харьков
 Специалисты Всемирной организации здравоохранения (ВОЗ) считают, что в течение XXI века аллергические заболевания по распространенности в мире выйдут на 2-е место, уступив только психическим заболеваниям. В тройку лидеров среди всех аллергических заболеваний входят аллергический ринит (АР), бронхиальная астма (БА) и атопический дерматит [1]. Доказано, что каждые 10 лет распространенность аллергического ринита, как и других аллергических заболеваний, увеличивается на 100%. Так, в США только новые случаи заболеваний АР ежегодно регистрируются у 40 млн человек. Повышенный интерес специалистов медицины и фармации к проблеме АР объясняется наличием целого ряда как социальных, так и медицинских аспектов:
Специалисты Всемирной организации здравоохранения (ВОЗ) считают, что в течение XXI века аллергические заболевания по распространенности в мире выйдут на 2-е место, уступив только психическим заболеваниям. В тройку лидеров среди всех аллергических заболеваний входят аллергический ринит (АР), бронхиальная астма (БА) и атопический дерматит [1]. Доказано, что каждые 10 лет распространенность аллергического ринита, как и других аллергических заболеваний, увеличивается на 100%. Так, в США только новые случаи заболеваний АР ежегодно регистрируются у 40 млн человек. Повышенный интерес специалистов медицины и фармации к проблеме АР объясняется наличием целого ряда как социальных, так и медицинских аспектов:- заболеваемость АР составляет от 10 до 25% общей популяции;
- определяется отчетливая тенденция к росту заболеваемости АР и его осложненных вариантов;
- доказано влияние АР на развитие БА, обсуждается концепция «единая дыхательная система, единое заболевание»;
- АР снижает социальную активность пациентов, влияет на работоспособность у взрослых и школьную успеваемость — у детей.
При этом данные о заболеваемости АР не отражают истинной распространенности этой нозологии, так как не учитывают огромное количество лиц, не обратившихся за медицинской помощью, или тех, у кого АР неправильно диагностирован [2]. Кроме этого, хорошо известно, что из-за неправильного диагноза такие больные достаточно часто лечатся по поводу рецидивирующих острых респираторных инфекций, бактериальных риносинуситов, гипертрофических ринитов, подвергаются не всегда обоснованным хирургическим и парахирургическим вмешательствам в полости носа. Некоторые пациенты расценивают проявления АР как «простудные», занимаются самолечением и ежедневно принимают лекарственные препараты, которые вызывают ряд побочных эффектов, например, бесконтрольное длительное использование сосудосуживающих капель приводит к развитию медикаментозного ринита.
АР является причиной значительных финансовых затрат [3]. Прямые расходы на его лечение в Европе составляют не менее 1,5 млрд евро в год. Непрямые затраты, обусловленные АР, достигают в США 9,7 млрд дол. в год, в Швеции — 2,7 млрд евро в год. Однако экономическое значение АР часто недооценивается, поскольку многие пациенты занимаются самолечением и не обращаются к врачам.
Прямые расходы на его лечение в Европе составляют не менее 1,5 млрд евро в год. Непрямые затраты, обусловленные АР, достигают в США 9,7 млрд дол. в год, в Швеции — 2,7 млрд евро в год. Однако экономическое значение АР часто недооценивается, поскольку многие пациенты занимаются самолечением и не обращаются к врачам.
Аллергическим ринитом принято называть хроническое воспаление слизистой оболочки носа, вызываемое аллергенами и характеризующееся IgE-зависимым воспалением слизистой оболочки носа, которое проявляется наличием как минимум двух из следующих симптомов: заложенность носа, водянистые или слизистые выделения из носа, чихание, зуд (жжение) в носу [4]. Перечисленные симптомы обычно возникают ежедневно и претерпевают обратное развитие после прекращения действия аллергена или под влиянием адекватной терапии.
С одной стороны, во многих случаях наблюдается отчетливая сезонность возникновения симптомов АР, совпадающая с периодом цветения растений, пыльца которых является причиной заболевания. С другой — при постоянных воздействиях различных аллергенов (например домашняя пыль, эпидермис животных, профессиональные факторы и др.) клинические проявления АР не зависят от времени года. При этом изменения слизистой оболочки носа носят устойчивый характер, сопровождаются длительными или постоянными функциональными нарушениями (затруднение носового дыхания, снижение обонятельной чувствительности).
В зависимости от этиологии выделяют сезонный, круглогодичный и профессиональный АР. Сезонный АР (САР) обусловлен пыльцой растений и плесенью, обострения возникают в определенные сезоны года (весна, лето, осень). Удельный вес САР зависит от климатогеографических условий. В последние годы в связи с изменением климата и его потеплением в некоторых регионах отмечают изменение и увеличение сроков цветения растений, что приводит как к постоянному повышению распространенности САР, так и отражается на длительности проведения необходимой фармакотерапии. Круглогодичный АР (КАР) связан с бытовыми аллергенами, особенно с клещами домашней пыли, поэтому симптомы заболевания могут проявляться на протяжении всего года.
- международное исследование астмы и аллергии у детей (International Study of Asthma and Allergy in Childhood — ISSAC I) и его продолжение ISSAC III;
- SAPALDIA (Swiss Study on Air Palliation and Lung Diseases in Adults) — швейцарское исследование воздушных поллютантов и легочных болезней у взрослых;
- SCARPOL (Swiss Study on Childhood Allergy and Respiratory Symptoms with Respect to Air Palliation Climate and Pollen) — швейцарское исследование аллергии у детей и респираторных симптомов, обусловленных воздушными поллютантами, климатом и пыльцой.
В этих и других эпидемиологических исследованиях установлено, что АР имеет тенденцию к прогрессирующему ухудшению течения заболевания: со временем увеличиваются выраженность и продолжительность обострений, присоединяются новые симптомы (такие как кашель и удушье), возрастает потребность в медикаментах симптоматической и базисной терапии. У 50–90% больных АР сочетается с аллергическим конъюнктивитом, особенно это характерно для пациентов с сезонными проявлениями АР [6]. У детей АР часто сопровождается гипертрофией и воспалением аденоидных вегетаций, что усугубляет течение основного заболевания. Другим осложнением АР является гипертрофическое изменение слизистой оболочки носа и придаточных пазух с формированием полипов, которые даже после радикальных хирургических вмешательств имеют склонность к повторному произрастанию. Для пациентов с АР, особенно в сочетании с аденоидитом или полипозом носа, характерны частые респираторные вирусные и бактериальные инфекции с развитием синуситов (в том числе пансинуситов). В свою очередь, это приводит к необходимости назначения антибактериальной терапии, пункций верхнечелюстных пазух, неоднократных рентгенологических исследований, а в тяжелых случаях — лечения в условиях стационара [7]. Нередко АР сочетается с серозным средним отитом и евстахиитом.
В свою очередь, это приводит к необходимости назначения антибактериальной терапии, пункций верхнечелюстных пазух, неоднократных рентгенологических исследований, а в тяжелых случаях — лечения в условиях стационара [7]. Нередко АР сочетается с серозным средним отитом и евстахиитом.
АР является фактором риска развития БА [8,9]. По данным разных авторов, у 30–50% больных с АР отмечают атопическую БА, в то же время у 55–85% больных с БА выявляют симптомы АР. В некоторых случаях развитие АР предшествует дебюту БА, в других — оба заболевания начинаются одновременно. Существует взаимосвязь между выраженностью симптомов АР и тяжестью проявлений БА. При наличии бытовой сенсибилизации у больных отмечается повышение неспецифической гиперреактивности слизистой оболочки носа и бронхов, что свидетельствует о хроническом аллергическом воспалении слизистой оболочки дыхательных путей, поддерживаемом бытовыми аллергенами даже в период видимой клинической ремиссии АР.
Основные симптомы АР и сопутствующих заболеваний вызывают физический дискомфорт, головную боль, повышенную раздражительность и утомляемость, снижение концентрации внимания и существенно ограничивают профессиональную деятельность человека и ухудшают качество жизни. Даже легкие и непродолжительные (в течение 2 нед) проявления АР оказывают нежелательное действие на качество жизни больных, на физическое и психологическое состояние и социальную жизнь, ограничивают профессиональную деятельность человека и способность к обучению [10].
Национальные и международные эпидемиологические исследования дали возможность получить информацию о распространенности АР, предполагаемых факторах риска и продемонстрировали, что АР отмечается во всех странах, у представителей любых этнических групп и социально-экономических сословий и у пациентов любого возраста. Все аспекты проблемы АР нашли свое отражение в международном консенсусе «ARIA, 2001» (Allergic Rhinitis and its Impact on Asthma — Аллергический ринит и его влияние на астму) — согласительном документе, созданном в сотрудничестве с ВОЗ еще в 2001 г. Указывались неразрывная связь АР с патологией околоносовых пазух, уха, нижних отделов дыхательных путей, влияние на сопутствующие заболевания. Этот документ лег в основу Соглашения конгресса (2006 г.) Европейской академии аллергологии и клинической иммунологии (EAACI) и отечественного Протокола оказания медицинской помощи больным с АР (далее — Протокол) [11, 12]. Позже программа ARIA была пересмотрена и опубликована ее новая редакция ARIA, 2008 [13].
Указывались неразрывная связь АР с патологией околоносовых пазух, уха, нижних отделов дыхательных путей, влияние на сопутствующие заболевания. Этот документ лег в основу Соглашения конгресса (2006 г.) Европейской академии аллергологии и клинической иммунологии (EAACI) и отечественного Протокола оказания медицинской помощи больным с АР (далее — Протокол) [11, 12]. Позже программа ARIA была пересмотрена и опубликована ее новая редакция ARIA, 2008 [13].
В рекомендациях EAACI/ARIA и отечественного Протокола принята концепция «Единая дыхательная система, единая болезнь» и предложена новая классификация АР, которая учитывает симптомы и показатели качества жизни пациента и предполагает выделение интермиттирующего и персистирующего ринита на основании длительности сохранения симптомов [14]. При интермиттирующем рините (ИАР) проявления аллергии отмечаются менее 4 дней в неделю или менее 4 нед в году, при персистирующем рините (ПАР) — более 4 дней в неделю или более 4 нед в году.
Также предполагается выделение легкого и среднетяжелого или тяжелого АР с учетом выраженности симптомов и степени ухудшения качества жизни.
При легкой форме:
- сохраняется нормальный сон;
- не нарушается повседневная активность, профессиональная деятельность, учеба в школе, занятия спортом;
- отсутствуют мучительные симптомы.
При среднетяжелой или тяжелой форме отмечается один из нижеперечисленных признаков:
- нарушение сна;
- нарушение повседневной активности, профессиональной деятельности, учебы в школе, невозможность занятий спортом, нормального отдыха;
- наличие мучительных симптомов.
Кроме того, полученные факты обосновывают концепцию «единых дыхательных путей», которая демонстрирует тесную связь между АР и БА и доказывает, что воспалительный ответ может поддерживаться и усиливаться взаимосвязанными механизмами. Поэтому руководство ВОЗ «ARIA, 2001» рекомендует:
- больные с ПАР должны быть обследованы на предмет наличия БА;
- пациентам с БА необходимо провести диагностику АР;
- больным БА и АР показано комбинированное лечение верхних и нижних дыхательных путей [11–13, 15].

В основе патогенеза АР лежит гиперчувствительность 1-го типа (по Coombs, Gell) с взаимодействием разнообразных эндогенных и внешнесредовых факторов, сопровождающихся повышенной продукцией иммуноглобулина E и его фиксацией на мембране тучных клеток. При повторном контакте слизистой оболочки носа с аллергеном происходит дегрануляция тучных клеток с выделением биологически активных веществ (гистамина и др.), которые вызывают раздражение нервных окончаний, расширение сосудов, отек, изменение режимов секреции носовой слизи, заложенность, зуд в носу, приступы чихания и другие симптомы воспаления. Это так называемая острая, или ранняя, фаза аллергической реакции. В дальнейшем, через 4–6 ч после первичной реакции, примерно у половины больных развивается поздняя фаза аллергического воспаления — в слизистой оболочке носа формируются длительные воспалительные изменения, поэтому повторные воздействия аллергена сопровождаются более выраженной симптоматикой. Также следует помнить, что при АР особо важным является понятие «минимальное персистирующее воспаление» — аллергическое воспаление, возникающее в слизистой оболочке носа после контакта с аллергеном и затем длительно сохраняющееся после прекращения воздействия аллергена.
Причинно-значимыми факторами АР в основном выступают воздушные аллергены [16]. Наиболее частыми «домашними» аллергенами являются клещи домашней пыли, слюна и перхоть животных, насекомые и аллергены растительного происхождения. К основным «внешним» аллергенам относятся пыльца растений и плесневые грибы. Кроме воздушных аллергенов, причиной развития АР могут быть ацетилсалициловая кислота и другие нестероидные противовоспалительные препараты. В таком случае ринит рассматривается как элемент «аспириновой триады». Существует также профессиональный АР (часто отмечается у специалистов фармации и медицины), зачастую сопровождающийся поражением нижних дыхательных путей и находящийся в компетенции врачей-профпатологов.
Важное значение в развитии АР и его обострений имеют поллютанты — триггерные факторы, увеличивающие выраженность симптомов АР путем стимуляции неспецифических и специфических механизмов назальной реактивности. Основные атмосферные поллютанты — выхлопные газы, озон, оксид азота и диоксид серы, а внутри помещения — табачный дым.
Основные атмосферные поллютанты — выхлопные газы, озон, оксид азота и диоксид серы, а внутри помещения — табачный дым.
Повышенный риск сенсибилизации к данным аллергенам отмечается у детей с наследственной предрасположенностью к атопии [17]. Установлено, что если указанная патология регистрируется лишь у одного из родителей, то риск развития АР у их ребенка составляет около 50%. Однако в тех случаях, когда и мать, и отец ребенка страдают атопическими заболеваниями, риск возникновения АР возрастает до 70%.
Основными симптомами АР являются многократное пароксизмальное чихание, зуд и щекотание в полости носа, реже ощущение жжения в носу, обильные водянистые выделения из носа (ринорея), заложенность носа и снижение обоняния [18]. У больных АР не всегда отмечают все четыре симптома, достаточно наличия только двух или трех основных симптомов. Для пациентов с КАР ведущим симптомом является заложенность носа, вызывающая резкое затруднение носового дыхания, выделения из носа слизистого характера. Для пациентов с САР наиболее характерны приступообразное чихание, зуд в полости носа, обильное водянистое отделяемое из носа и сопутствующий аллергический конъюнктивит. Вследствие обильных выделений из носа, нарушения дренирования околоносовых пазух и проходимости слуховых труб могут развиваться вторичные нарушения: кожные раздражения вокруг носа, носовые кровотечения, боль в горле и покашливание, отиты. Нередко к основным симптомам присоединяются головная боль, расстройства сна, снижение обоняния и др. У детей [19] наряду с классическими симптомами АР отмечают «аллергические тики» (морщат нос), «аллергический салют» (потирают нос ладонью кверху), при этом образуется поперечная полоса в области кончика носа, «аллергические круги» под глазами. У детей младшего возраста выделения из носа могут иметь вид «молочной пены». С возрастом может развиваться неправильный прикус.
Часто АР сопровождается аллергическим конъюнктивитом (вследствие прямого воздействия аллергена на конъюнктиву и назокорнеального рефлекса) и глазными симптомами (зуд, покраснение, слезотечение, ощущение песка в глазах), а также общими неспецифическими симптомами [20].
Учитывая, что симптомы АР неспецифичны, заболевание нередко пропускается под маской «частых ОРЗ». Поэтому во всех случаях клинических проявлений ринита необходимо исключать другие причины заболевания. В первую очередь при этом проводят дифференциацию диагноза по поводу инфекционного ринита, вазомоторного ринита, ринита, обусловленного аномалиями анатомического строения носа, неаллергическим эозинофильным ринитом; медикаментозного ринита (деконгестанты, резерпин, ингибиторы ангиотензинпревращающего фермента, оральные контрацептивы), ринита у больных с непереносимостью ацетилсалициловой кислоты и других нестероидных противовоспалительных средств, аденоидита (у детей), гормонального ринита (половое созревание, беременность, гипотиреоз).
Диагностика АР направлена на выявление причин и факторов, способствующих формированию и манифестации заболевания. Обследование и лечение больных АР должны проводиться параллельно врачами двух специальностей: оториноларингологами и аллергологами, что позволяет в дальнейшем обеспечить оптимальный комплексный подход к терапии АР [21]. Следует особо подчеркнуть, что каждая из представленных клинических форм АР должна быть верифицирована с учетом выявленных этиологических особенностей. Детализация причин АР основана на анализе данных анамнеза, а также результатов физикального и лабораторно-инструментального обследования. При этом среди лабораторных методов диагностики выделяют специфические и неспецифические. К неспецифическим относят определение количества эозинофилов в периферической крови, концентрации общего IgE и цитологическое исследование отделяемого из носа. Специфическими маркерами аллергического заболевания являются положительные аллергопробы (кожное тестирование, специфические IgE и пробы с провокацией in vivo, которые в педиатрии проводятся редко). Ранняя диагностика АР позволяет не только своевременно назначить адекватную терапию и хорошо контролировать все симптомы заболевания, но и в некоторых случаях предотвратить переход легких форм заболевания в тяжелые, а также избежать присоединения новых симптомов и развития БА.
Основная цель терапии АР — уменьшить выраженность симптомов болезни и воспрепятствовать развитию воспаления. Поэтому воздействие всех методов терапии должно быть направлено на отдельные этапы воспалительной реакции. Комплекс терапевтических мероприятий включает такие методы:
- устранение контакта с аллергеном;
- аллергенспецифическая иммунотерапия;
- медикаментозная терапия.
Степень тяжести и течение АР определяются концентрацией аллергенов в окружающем воздухе. Поэтому важным компонентом комплексного лечения АР является идентификация аллергенов и, по возможности, уменьшение контакта с ними [22]. При этом необходимо учитывать, что эффект различных мер, направленных на удаление аллергена из окружающей среды, в полной мере проявляется только через несколько месяцев. Зачастую полное исключение контакта с аллергеном невозможно, так как у большинства пациентов определяется поливалентная сенсибилизация. Однако даже частичное выполнение мер по предупреждению контакта с аллергенами существенно облегчает течение заболевания и позволяет снизить дозу принимаемых лекарств или заменить терапию на более щадящую, особенно в тех случаях, когда применение некоторых препаратов нежелательно (беременность, возраст, сопутствующая патология).
Аллергенспецифическая иммунотерапия — это лечение возрастающими концентрациями аллергена, вводимого чаще всего подкожно, интраназально или сублингвально. Имеются противоречивые данные об эффективности и безопасности подкожной иммунотерапии. Считается, что иммунотерапия эффективна в основном у детей и подростков и должна проводиться строго по показаниям [23].
Тактика медикаментозного лечения зависит от степени тяжести заболевания и включает несколько групп лекарственных веществ, применяемых для лечения АР [11–13]. Среди лекарственных средств особую роль играют антимедиаторные препараты, в первую очередь антагонисты Н1-гистаминовых рецепторов, а также лекарственные средства, подавляющие воспаление, — интраназальные глюкокортикостероиды (ИнГКС) и стабилизаторы мембран тучных клеток — кромоны (кромоглициевая кислота, недокромил натрия).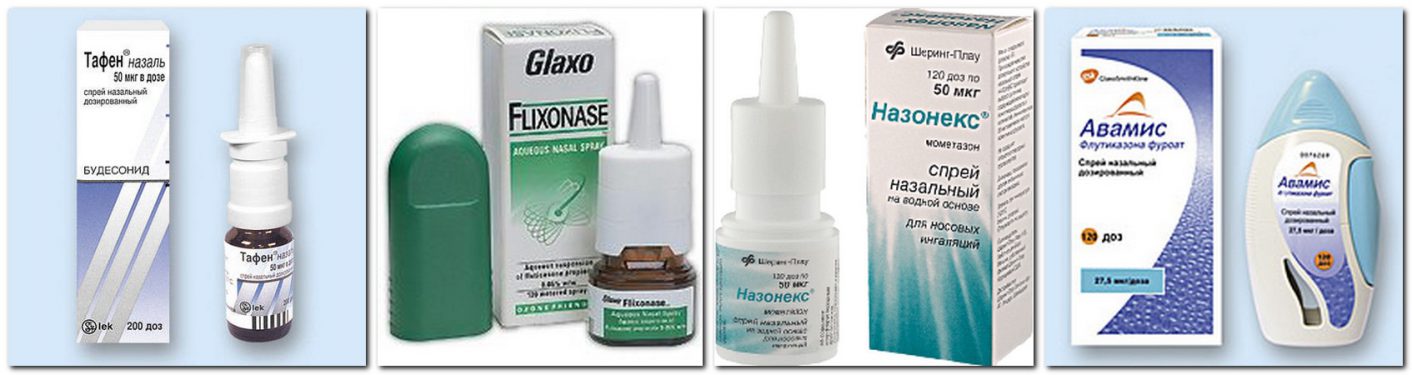 В качестве симптоматической терапии часто используются деконгестанты (сосудосуживающие препараты), антихолинергические препараты, антилейкотриеновые средства. Учитывая, что аллергическое воспаление является хроническим, терапевтические усилия должны быть сконцентрированы на правильном подборе базисной противовоспалительной терапии, препаратами которой могут быть кромоны и глюкокортикостероиды (ГКС) [24, 25].
В качестве симптоматической терапии часто используются деконгестанты (сосудосуживающие препараты), антихолинергические препараты, антилейкотриеновые средства. Учитывая, что аллергическое воспаление является хроническим, терапевтические усилия должны быть сконцентрированы на правильном подборе базисной противовоспалительной терапии, препаратами которой могут быть кромоны и глюкокортикостероиды (ГКС) [24, 25].
Медикаментозное лечение назначается с учетом степени тяжести и течения аллергического заболевания и отражено в ступенчатом подходе, варианты которого отражены в согласительных и рекомендательных документах последних лет (таблица) [2, 5–6, 9, 11, 12, 14, 15, 18, 21–25, 26].
| Таблица | Ступенчатая схема лечения АР |
| Схема лечения | Формы АР | ||||
|---|---|---|---|---|---|
| ИАР | ПАР | ||||
| легкая | среднетяжелая и тяжелая | легкая | среднетяжелая и тяжелая | ||
| Устранение контакта с аллергеном | + | + | + | + | |
| Пероральные препараты | Блокаторы Н1-рецепторов | + | + | + | |
| Интраназальные препараты | Н1-блокаторы | + | + | + | |
| Деконгестанты | ± | ± | ± | ||
| Кромоны | ± | ± | |||
| ГКС | + | + | + | ||
| Тактика лечения | При улучшении состояния | Продолжить лечение в течение 1 мес | Продолжить лечение в течение 1 мес | Продолжить лечение в течение 1 мес | Продолжить лечение в течение 1 мес |
| При неэффективности | Консультация врача | Перейти на одну ступень вверх | Перейти на одну ступень вверх | Консультация врача — пересмотр диагноза и/или другие мероприятия | |
Таким образом, определение формы и оценка степени тяжести течения АР имеют исключительно принципиально важное значение для выбора адекватной лечебной тактики.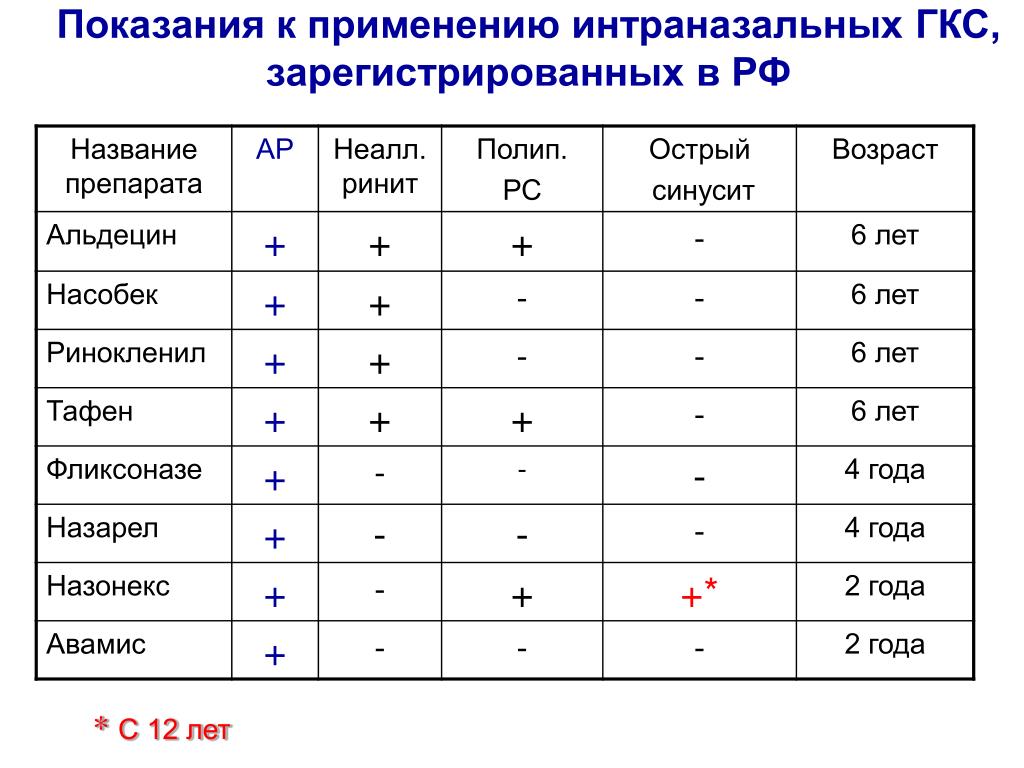 Значительное повышение эффективности лечения АР, улучшение качества жизни больных связано, в частности, с использованием ИнГКС, применение которых насчитывает уже несколько десятилетий [27]. К сожалению, до сих пор наблюдается, с одной стороны, настороженное отношение врачей к применению ИнГКС в повседневной практике, а с другой — некоторые пациенты считают, что их заболевание находится еще не в той стадии, когда необходимо принимать ИнГКС. Нередко пациенты и даже врачи отождествляют осложнения от длительного приема системных ГКС и осложнения ИнГКС, путают понятия «поддерживающая терапия для контроля заболевания» и «привыкание к лекарственным препаратам». Также в практике отмечается тенденция местного применения гормональных препаратов, предназначенных для системного введения (путем закапывания в нос, введения с помощью электро- и фонофореза, инъекций в слизистую оболочку носа). При этом абсолютно не учитывается тот факт, что такие процедуры сопровождаются быстрой резорбцией препарата практически в неизмененных концентрациях и возникновением системных эффектов [28].
Значительное повышение эффективности лечения АР, улучшение качества жизни больных связано, в частности, с использованием ИнГКС, применение которых насчитывает уже несколько десятилетий [27]. К сожалению, до сих пор наблюдается, с одной стороны, настороженное отношение врачей к применению ИнГКС в повседневной практике, а с другой — некоторые пациенты считают, что их заболевание находится еще не в той стадии, когда необходимо принимать ИнГКС. Нередко пациенты и даже врачи отождествляют осложнения от длительного приема системных ГКС и осложнения ИнГКС, путают понятия «поддерживающая терапия для контроля заболевания» и «привыкание к лекарственным препаратам». Также в практике отмечается тенденция местного применения гормональных препаратов, предназначенных для системного введения (путем закапывания в нос, введения с помощью электро- и фонофореза, инъекций в слизистую оболочку носа). При этом абсолютно не учитывается тот факт, что такие процедуры сопровождаются быстрой резорбцией препарата практически в неизмененных концентрациях и возникновением системных эффектов [28].
Топические ГКС (беклометазон, мометазон, флутиказон) являются наиболее эффективными средствами при лечении всех форм АР и считаются признанным стандартом его лечения. В экспериментальных и клинических исследованиях показано, что ГКС воздействуют практически на все звенья патогенеза АР [29]. ГКС проникают в цитоплазму клетки и клеточное ядро, развиваются внегеномные (быстрые) и геномные (медленные) эффекты, поэтому начало действия препаратов отмечается через 8 ч, а полный эффект — через несколько дней. Эти механизмы лежат в основе противоаллергического, противовоспалительного и противоотечного действия ГКС [30]. При этом ГКС снижают чувствительность рецепторов слизистой оболочки носа к гистамину и механическим раздражителям, но никак не изменяют иммунный ответ организма на бактериальную инфекцию.
Возможность местного использования ГКС коренным образом изменила тактику ведения больных с аллергическими заболеваниями. Преимуществами фармакологического противоаллергического эффекта местных ГКС являются одновременное торможение как ранней, так и поздней фазы аллергического ответа и угнетение всех симптомов аллергического воспаления без риска возникновения побочных реакций, свойственных ГКС системного действия. Достоинством ИнГКС перед пероральными является минимальный риск развития системных побочных эффектов на фоне создания адекватных концентраций активного вещества в слизистой оболочке носа, позволяющих контролировать симптомы АР. Результаты клинических исследований и метаанализов позволяют считать их самыми эффективными средствами для лечения АР и рассматривать в качестве препаратов 1-го ряда при этом заболевании [31].
Преимуществами фармакологического противоаллергического эффекта местных ГКС являются одновременное торможение как ранней, так и поздней фазы аллергического ответа и угнетение всех симптомов аллергического воспаления без риска возникновения побочных реакций, свойственных ГКС системного действия. Достоинством ИнГКС перед пероральными является минимальный риск развития системных побочных эффектов на фоне создания адекватных концентраций активного вещества в слизистой оболочке носа, позволяющих контролировать симптомы АР. Результаты клинических исследований и метаанализов позволяют считать их самыми эффективными средствами для лечения АР и рассматривать в качестве препаратов 1-го ряда при этом заболевании [31].
ИнГКС отличаются от системных ГКС своими фармакологическими свойствами: липофильностью, быстрой инактивацией, коротким периодом полувыведения из плазмы крови. Современные ИнГКС обладают низкой биодоступностью и хорошо переносятся больными. При нормально функционирующем мукоцилиарном транспорте основная часть препарата (до 96%) в течение 20–30 мин после интраназального введения переносится в глотку с помощью ресничек слизистой оболочки носа, откуда поступает в желудочно-кишечный тракт и подвергается абсорбции [32]. Поэтому биодоступность при пероральном и интраназальном приеме является важной характеристикой ИнГКС, в значительной степени определяющей их терапевтический индекс, то есть соотношение местной противовоспалительной активности и потенциала неблагоприятного системного действия. Благодаря выраженному противовоспалительному эффекту ИнГКС более эффективны, чем интраназальные кромоны и системные антигистаминные препараты. Клиническое начало действия ИнГКС приходится на 2–3-й день лечения, максимальный эффект развивается через несколько дней от начала лечения и сохраняется на протяжении всего курса. Топические ГКС следует применять регулярно [33]. При наличии соответствующих показаний, соблюдении определенных мер предосторожности такие препараты можно применять длительно. В настоящее время в классе ИнГКС применяются беклометазона дипропионат (БДП), будесонид, мометазона фуроат (МФ), флутиказона пропионат (ФП), флутиказона фуроат (ФФ) [34]. В порядке уменьшения местной активности и сродства к ГКС-рецепторам человека ИнГКС располагаются следующим образом: ФФ > ФП > МФ > будесонид > БДП.
В настоящее время в классе ИнГКС применяются беклометазона дипропионат (БДП), будесонид, мометазона фуроат (МФ), флутиказона пропионат (ФП), флутиказона фуроат (ФФ) [34]. В порядке уменьшения местной активности и сродства к ГКС-рецепторам человека ИнГКС располагаются следующим образом: ФФ > ФП > МФ > будесонид > БДП.
Современным представителем этого класса препаратов является ФФ (препарат Авамис®) — синтетический трифторированный глюкокортикоид с наиболее высокой аффинностью и селективностью к ГКС-рецептору среди всех существующих препаратов этой группы [35]. Он представляет собой комбинацию молекулы флутиказона и 17-α фуроатного эфира, которые обеспечивают его основные свойства. Хотя ФФ структурно похож на ФП, они различаются химическими и фармакологическими свойствами. Ни один из препаратов не метаболизируется в печени до флутиказона. Они инактивируются ферментом CYP 3A4 системы Р450 с преобразованием 17b-фторметилтиоэфирной группы и получением в итоге различных неактивных метаболитов.
Интенсивный печеночный метаболизм и высокий уровень связывания с белками плазмы крови (>99%) объясняют низкую системную биодоступность ФФ при интраназальном введении, при этом введение препарата в дозе 110 мкг 1 раз в сутки обычно не приводит к определению измеримых концентраций в плазме крови (<10 пг/мл). В ходе исследований по оценке биодоступности на здоровых добровольцах общая суточная доза ФФ составляла 2640 мкг, что в 24 раза выше рекомендованной, однако даже несмотря на это биодоступность была минимальной и составила менее 0,5%.
Особенностью ФФ является его высокая тропность к легочной ткани и эпителию слизистой оболочки носовой полости, а также хорошая растворимость в назальном секрете. Он характеризуется высокой внутриклеточной аккумуляцией и низкой скоростью выхода из клетки. Благодаря наличию у ФФ эфирной группы, которая взаимодействует с 17-α липофильным сайтом ГКС-рецептора, молекула характеризуется высоким сродством к рецептору, быстрой ассоциацией и медленной диссоциацией. Высокая аффинность к ГКС-рецептору и длительное персистирование в тканях объясняют высокий противовоспалительный потенциал ФФ [36].
Высокая аффинность к ГКС-рецептору и длительное персистирование в тканях объясняют высокий противовоспалительный потенциал ФФ [36].
Авамис® является хорошо изученным препаратом, с которым проводилось большое число доклинических и клинических исследований. Так, при выборе оптимальной дозы ФФ (оценивались 55; 110; 220; 440 мкг/сут) у больных САР наиболее эффективной и безопасной оказалась доза 110 мкг 1 раз в сутки. Одним из преимуществ Авамиса® является возможность приема 1 раз в сутки, что повышает комплаентность больных.
Местные побочные эффекты для всей группы ИнГКС возникают в 5–10% случаев. Наиболее распространенными являются чихание, жжение, раздражение слизистой оболочки носовой полости, головная боль и носовые кровотечения. В большинстве случаев побочные эффекты слабо выражены и не требуют отмены препарата. На способность к концентрации внимания препарат не влияет [37].
Исследования в США и европейских странах показали, что ФФ уменьшал выраженность всех назальных, глазных симптомов и повышал качество жизни пациентов с САР — препарат начинал действовать через 8 ч, и его эффект сохранялся в течение суток. Профиль нежелательных явлений был одинаков в группе активного лечения и плацебо, за исключением кровянистых выделений из носа, которые отмечали несколько чаще при лечении ФФ, однако частота их появления была такой же, как и при использовании других ИнГКС [38].
Метаанализ 35 двойных слепых плацебо-контролируемых исследований показал, что среди всех ИнГКС только ФФ достоверно продемонстрировал стабильную эффективность в отношении глазных симптомов у пациентов с САР, имеющих сенсибилизацию к пыльце деревьев, трав и сорняков. Это объясняется высокой местной противовоспалительной активностью ФФ и его способностью подавлять назоокулярный рефлекс, обусловленный активацией парасимпатических нервов медиаторами воспаления в слизистой оболочке носа. При этом отпадает необходимость в приеме дополнительных препаратов для коррекции глазных симптомов и тем самым снижаются экономические затраты пациентов на лечения АР, особенно сочетанного с конъюнктивитом [39].
Разработанное устройство препарата Авамис® состоит из резервуара с дозирующей помпой, помещенного во внешний контейнер. Разработка устройства для интраназального введения ФФ происходила в течение 2 лет с обязательным тестированием и последующим интервью пациентов и врачей о достоинствах и недостатках каждой из них [41]. Пациенты отмечали легкость использования системы доставки препарата Авамис®, удобный аппликатор и надежность по сравнению с предшествующими системами интраназального введения препаратов. Инновационная система доставки обеспечивает стабильность и физиологическое распределение препарата в носовой полости, удобство применения и достоверно повышает приверженность пациентов к терапии. Эта система отмечена в 2008 г. золотой наградой Medical Design Excellence Awards за разработку устройства, ориентированного на потребности пациента. По результатам рандомизированного двойного слепого многоцентрового исследования оказалось, что большинство пациентов с САР и КАР отдают предпочтение новому назальному спрею Авамис® по сравнению с ФП.
АЛГОРИТМ БЕСЕДЫ ПРОВИЗОРА С ПОСЕТИТЕЛЕМ АПТЕКИ
Выбор тактики лечения АР у детей. АР отмечают у детей любого возраста [44]. Несмотря на достаточно распространенное убеждение о низкой заболеваемости АР у детей первых лет жизни, его распространенность в этом возрасте также высока. Установлено, что 42% детей имели диагностированный в 6-летнем возрасте АР, причина — запоздалая диагностика. У детей и подростков распространенность САР выше, чем у взрослых. Установлено, что частота АР у детей резко увеличивается к школьному возрасту. У таких детей АР нередко предшествует развитию БА как этап «аллергического марша». Кроме того, АР у детей часто сочетается с другими заболеваниями и имеет четкую тенденцию к выраженному утяжелению течения основного заболевания. При исследовании детей с САР установлено, что у 80% из них отмечается фарингит, у 70% — конъюнктивит и синусит, у 37% — атопический дерматит, у 30–40% детей диагностируют аденоидиты, у 30% — рецидивирующие и экссудативные средние отиты, у 10% — заболевания гортани (в том числе рецидивирующие стенозы гортани — круп). Поэтому выбор эффективных средств лечения у детей с АР обязательно должен проводиться лечащим врачом после всестороннего обследования.
Во избежание развития системных осложнений, особенно у детей, следует выбирать топические ГКС с низкой биодоступностью. Влияние длительной терапии топическими стероидами на рост ребенка и подростка изучали в достаточно многих исследованиях, но они обычно ограничены во времени и не учитывают рост во взрослом возрасте. На основании имеющихся данных Комитет по безопасности лекарственных средств Великобритании при Европейском агентстве по лекарственным средствам (European Medicines Agency — EMA) и Управление по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) разработали классификацию препаратов, определяющую группу с минимальной биодоступностью и рекомендованную для применения у детей. Так, в педиатрической практике используются главным образом МФ, ФП и ФФ [45]. В нескольких многоцентровых двойных слепых плацебо-контролируемых исследованиях эффективности и безопасности ФФ при КАР у взрослых, подростков (12 лет и старше) и детей (2–11 лет) в течение 4–12 нед установлено, что не было выявлено отрицательного влияния ФФ на продукцию кортизола, внутриглазное давление и прозрачность хрусталика. При изучении оценки эффектов препарата Авамис® (110 мкг 1 раз в сутки) на опорно-двигательный аппарат также не выявили влияния препарата на скорость роста детей с САР и КАР. Следовательно, Авамис® может быть препаратом первого выбора у детей старше 6 лет с АР, при необходимости в назначении ИнГКС [46–49] и особенно при наличии выраженных глазных симптомов.
В заключение хотелось бы подчеркнуть, что необходимое условие успешного лечения АР — улучшение взаимодействия между врачами, фармакологами и специалистами фармации. Неправильная оценка жалоб и клинических проявлений ринита могут привести к поздней верификации заболевания и, как следствие, к неадекватному лечению пациента, переходу болезни в затяжное или рецидивирующее течение, утяжелению состояния из-за присоединения других симптомов и болезней, в том числе БА. Внимательное отношение провизора и фармацевта к пациентам с проявлениями ринита и своевременные рекомендации обязательной врачебной консультации особенно важны для пациентов, которые не могут самостоятельно оценить тяжесть проблем своего здоровья.
Особую значимость в современных условиях приобретают ранняя диагностика заболевания специалистами и выбор оптимальных схем терапии с учетом показателя эффективность-безопасность. Опыт применения препарата Авамис® (флутиказона фуроат) свидетельствует, что препарат хорошо контролирует все симптомы АР, способствует уменьшению заложенности носа и восстановлению носового дыхания, способствует уменьшению выраженности глазных симптомов (у пациентов с сопутствующим аллергическим конъюнктивитом), приводит к улучшению качества жизни пациентов при низкой частоте побочных эффектов. Авамис® может быть рекомендован в качестве монотерапии больным АР при комплексном лечении пациентов с тяжелым течением АР, в том числе у детей в возрасте старше 6 лет и пациентов старших возрастных групп. Эффективность и безопасность лечения обеспечиваются оптимизированным способом доставки препарата Авамис®.
Список использованной литературы
1. Носуля Е.В. Аллергический ринит: лечение в повседневной клинической практике/ Е.В.Носуля // Consilium Medicum. — 2008. — Т. 10, №10. — С. 32–39.
2. Туровский А.Б. Аллергический ринит. Диагностика и лечение / А.Б. Туровский, Н.А. Мирошниченко // РМЖ. — 2011. — № 6. — С.3–11.
3. Naclerio R.M. Rhinitis and inhalant allergens / R.M. Naclerio, W. Solomon // JAMA. — 1997. — 278. — Р. 1842–1848.
4. Аллергический ринит и его влияние на астму, 2008. В сотрудничестве с Всемирной организацией здравоохранения, GA2LEN* и AllerGen** (часть 1) // Рос. аллерголог. журн. — 2009. — № 5. — С. 65–76.
5. Аллергический ринит и его влияние на астму, 2008. В сотрудничестве с Всемирной организацией здравоохранения, GA2LEN* и AllerGen** (часть 3) // Рос. аллерголог. журн. — 2010. — № 1. — С. 74–86.
6. Гущин И.С. Аллергический ринит (Пособие для врачей) / Н.И. Ильина, С.А. Польнер — М., 2002.
7. Карпова Е.П. Особенности терапии аллергического ринита у детей / Е.П. Карпова, М.В. Соколова, Н.В. Антонова // Вестн. оториноларингол. — 2009. — № 2. — С. 36–39.
8. Lundback B. Epidemiology of allergic rhinitis and asthma / B. Lundback // Clin Exp Allergy — 1998. — 28 (suppl. 2). — Р. 3–10.
9. Bousquet J, van Cauwenberge P, Khaltaev N et al. Management of allergic rhinitis and its impact on asthma (ARIA). J. Allergy Clin. Immunol. — 2001. — 108. — Р. 147–334.
10. Курбачева О.М. Клинические, патогенетические и экономические аспекты применения аллерген-специфической иммунотерапии. Дис…. докт. мед. наук. — М., 2007.
11. EAACI 2006: XXV congress of the European Academy of Allergology and Clinical Immunology. — Vienna, Austria, 10–14 June 2006. — Abstract book. — 492 p.
12. Протокол надання допомоги хворим на алергічний риніт: Матеріали ІІ з’їзду алергологів України (Одеса, вересень 2006 р.) // Астма та алергія. — 2006. — № 1–2. — С. 146–147.
13. Allergic Rhinitis and its Impact on Asthma (ARIA) 2008 Update. Allergy — 2008. — 63 (Suppl. 86). — Р. 1–160.
14. Аллергический ринит / Клинические рекомендации. Педиатрия / Под ред. А.А.Баранова. М.: Геотар–Медиа, 2005. С. 1–16.
15. Лопатин А.С., Гущин И.С., Емельянов А.В. Клинические рекомендации по диагностике и лечению аллергического ринита. Consilium Medicum — 2001. — Прил. — 33–44.
16. Settipane R.A. Demographics and epidemiology of allergic and nonallergic rhinitis// Allergy Asthma Proc. — 2001. — 22. — Р. 185–189.
17. Детская аллергология / Под ред. А.А.Баранова, И.И.Балаболкина. — М.: Геотар–Медиа, 2006.
18. Хаитов Р.М., Ильина Н.И., Латышева Т.В. Рациональная фармакотерапия аллергических заболеваний. — М., 2007.
19. Vuurman E.F., van Veggel L.M., Uiterwijk M.M. et al. Seasonal allergic rhinitis and antihistamine effects on children’s learning. — Ann. Allergy. — 1993. — 71. — Р. 121–126.
20. Leynaert B., Bousquet J., Neukirch C. et al. Perennial rhinitis: An independent risk factor for asthma in nonatopic subjects: results from the European Community Respiratory Health Survey. J. Allergy. Clin. Immunol. — 1999. — 104. — Р. 301–304.
21. Маркова Т.П. Диагностика, профилактика и лечение аллергических заболеваний // Рус. мед. журн. — 2006. — Т. 14, № 7. — С. 548–553.
22. Клиническая аллергология / Под ред. Р.М. Хаитова. — М.: Медпресс–информ, 2002. — 623 с.
23. Malling H.-J. Allergen immunotherapy efficacy in rhinitis and asthma. Allergy. Clin. Immunol. Int. — 2004. — 1 (3). — Р. 92–95.
24. Гаращенко Т.И. Аллергические риниты: проблемы медикаментозного лечения. Consilium medicum, — 2000. — Экстра выпуск. — С. 12–13.
25. Лопатин А.С. Кортикостероидная терапия в ринологии. Рос. ринол. — 2001. — 2. — С. 138–142.
26. Magnan A., Romanet S., Vervloet D. Rhinitis, nasosinusal poliposis and asthma: clinical aspects // The Nose and Lung Diseases / Ed. By B.Wallaert, P. Chanez, P. Godard. Eur. Resp. Monograph. — 2001. — P. 101–115.
27. Лопатин А.С.Кортикостероидная терапия: исторические аспекты / А.С.Лопатин // Consilium Medicum. — 2004. — Т. 06. — № 4.
28. Лопатин А.С.Кортикостероидная терапия в лечении заболеваний носа / А.С.Лопатин // Consilium Medicum. — 2004. — Т. 06. — № 4.
29. Zhou J, Liu D-F, Liu C et al. Glucocorticoids inhibit degranulation of mast cells in allergic asthma via nongenomic mechanism. Allergy — 2008. — 63 (9). — Р. 1177–1185.
30. Гущин И.С. Аллергическое воспаление и его фармакологический контроль. — М.: Фармарус принт, 1998.
31. Jeffery P.K., Godfrey R.W.A., Adelroth E. et al. Effects of treatment on airway inflammation and thickening of reticular collagen in asthma: a quantitative light and electron microscopic study. Am. Rev. Respir. Dis. — 1992. — 145. — Р. 890–899.
32. Лещенког И.В. Место и значение способа доставки ингаляционных глюкокортикостероидов / И.В.Лещенког // Consilium Medicum. — 2008. — Т. 10, №3 (Болезни дыхательной системы). — С. 2–9.
33. Togias A. Rhinitis and asthma: evidence for respiratory system integration // J. Allergy Clin Immunol. — 2003. — № 6. — P. 1171–1183.
34. Вознесенский Н.А. Влияние фармакокинетических характеристик ингаляционных ГКС / Н.А. Вознесенский // РМЖ. — 2008. — № 2. — С. 3–8.
35. Егорова О.А. Выбор интраназального глюкокортикостероида флутиказона / О.А.Егорова // Справочник поликлинического врача. — 2010. — № 3. — С. 11–16.
36. Rossios C., To Y., To M. et al. Long-acting fluticasone furoate has a superior pharmacological profile to fluticasone propionate in human respiratory cells. Eur J Pharmacol. — 2011. — Nov 16. — 670(1). — Р. 244–51.
37. Allen D.B., Meltzer E.O., Lemanske R.F. et al. No growth suppression in children treated with the maximum recommended dose of fluticasone propionate aqueous nasal spray for one year. Allergy Asthma Proc. — 2002. — 23. — Р. 407–413.
38. Maspero J.F. et al. An integrated analysis of the efficacy of fluticasone furoate nasal spray on individual nasal and ocular symptoms of seasonal allergic rhinitis. Allergy Asthma Proc. — 2010. — 31. — Р. 483–492.
39. Rosenblut A., Bardin P.G., Muller B. et al. Long-term safety of fluticasone furoate nasal spray in adults and adolescents with perennial allergic rhinitis. Allergy — 2007. — 62. — Р. 1071–1077.
40. Мещерякова Н.Н. Показатели качества жизни и кооперативности больных бронхиальной астмой при использовании оптимизированных способов доставки дозированных аэрозолей. Автореф. дис… канд. мед. наук. — М., 2004.
41. Meltzer E.O. et al. Preferences of Adult Patients with Allergic Rhinitis for the Sensory Attributes of Fluticasone Furoate Versus Fluticasone Propionate Nasal Sprays: A Randomized, Multicenter, Double-Blind, Single-Dose, Crossover Study. — Clin Ther — 2008.
42. Руководство по геронтологии и гериатрии. Том 4/Под ред. В.Н. Ярыгина, А.С. Мелентьева, — М., 2003.
43. Шабалин В.В. Диагностика нарушений мукоцилиарного транспорта при хронических воспалительных заболеваниях верхних и нижних дыхательных путей. Геронтология и гериатрия. — 2001. — 1. — Р. 120–126.
44. Гаращенко Т.И. Современная терапия аллергических ринитов у детей. РМЖ. — 2002. — 10 (5). — Р. 273–8.
45. Fokkens W.J., Jogi R., Reinartz S. et al. Once daily fluticasone furoate nasal spray is effective in seasonal allergic rhinitis caused by grass pollen. Allergy — 2007. — 62. — Р. 1078–1084.
46. Meltzer E.O., Lee J., Tripathy I. et al. Efficacy and safety of once-daily fluticasone furoate nasal spray in children with seasonal allergic rhinitis treated for 2 wk. Pediatr Allergy Immunol., — 2009. — v. 20. — P. 279–286.
47. Máspero J.F., Rosenblut A., Finn A. Jr. et al. Safety and efficacy of fluticasone furoate in pediatric patients with perennial allergic rhinitis. Otorhingol Head Neck Surg., — 2008. — v. 138. — P. 30–33.
48. Vasar M., Houle P.A., Douglass J.A. et al. Fluticasone furoate nasal spray: effective monotherapy for symptoms of perennial allergic rhinitis in adults/adolescents // Allergy Asthma Proc 2008. — Vol. 29. — N 3. — P. 313–321.
49. Meltzer E.O., Tripathy I, Máspero J.F. et al. Safety and tolerability of fluticasone furoate nasal spray once daily in paediatric patients aged 6–11 years with allergic rhinitis: subanalysis of three randomized, double-blind, placebo-controlled, multicentre studies. Clin Drug Investig., — 2009. — v. 29. — P. 79–86.
50. Фармацевтическая опека: атлас / И.А. Зупанец, В.П. Черных, С.Б. Попов и др.; под. ред. И.А. Зупанца, В.П. Черныха. — 2-е изд., перераб. — К.: «Фармацевтик Практик», 2007. — 144 с.
Публикуется при поддержке ООО «ГлаксоСмитКляйн Фармасьютикалс Украина»
AVMS/10/UA/20.03.2013/7419
Информация для профессиональной деятельности медицинских и фармацевтических специалистов
АВАМИС™ (AVAMYS™). Р.с.: UA/9306/01/01 от 02.02.2009 г. по 02.02.2014 г. Код ATC: R01A D12. Состав и форма выпуска: спрей назальный, дозированный — 1 доза препарата содержит флутиказона фуроата 27,5 мкг. Показания: симптоматическое лечение аллергических ринитов. Противопоказания: гиперчувствительность к любому из компонентов препарата. Побочные реакции: (очень часто (≥1/10), часто (≥1/100 и <1/10), нечасто (≥1/1 000 и <1/100), редко (≥1/10000 и <1/1000), очень редко (<1/10 000): 1. Со стороны дыхательной системы: очень часто — носовые кровотечения (обычно незначительные или умеренной интенсивности), часто — появление язв в носу, редко — боль в носу, дискомфорт (включая жжение, раздражение, болезненность в носу), сухость в носу. 2. Со стороны иммунной системы: редко — реакции гиперчувствительности, включая анафилаксию, ангионевротический отек, сыпь и крапивницу. Более подробная информация представлена в инструкции по медицинскому применению препарата.
Пройти тестrel=»nofollow»>
АвамісЦікава інформація для Вас:
Риск возникновения побочных эффектов при применении интраназальных кортикостероидов
Согласно современным клиническим рекомендациям [1], интраназальные кортикостероиды (ИКС) широко применяются в клинической практике при лечении воспалительных заболеваний носа и околоносовых пазух различной этиологии. В зависимости от характера патологического процесса длительность применения ИКС может варьировать в широких пределах — от 1—2 нед до нескольких месяцев и лет [1].
В ряде исследований сообщается о случаях возникновения нежелательных эффектов и осложнений на фоне применения ИКС, однако такие публикации часто посвящены описанию отдельных наблюдений и не позволяют сделать вывод о причинно-следственной зависимости между использованием данной группы препаратов и патологическими изменениями в полости носа. В связи с этим очевидна актуальность анализа результатов релевантных исследований, в которых рассматриваются побочные эффекты применения ИКС. В целом побочные явления можно разделить на локальные и системные.
Локальные побочные эффектыК наиболее часто встречающимся локальным побочным эффектам относятся носовые кровотечения, которые после применения ИКС в течение 3 мес и более регистрируются у 5—9% пациентов [2, 3]. Авторы отмечают, что существует связь между возникновением кровотечения и техникой применения ИКС, и считают, что причиной кровотечения скорее являются погрешности при использовании лекарственного средства, а не сами препараты.
Многочисленные публикации свидетельствуют о том, что регулярное использование ИКС сопровождается ощущениями сухости и жжения в носу, чиханием, дискомфортом в горле, неприятным послевкусием [4—6]. Однако данные жалобы, как правило, носят временный характер и разрешаются спонтанно без прекращения курса лечения [7].
Отмечено, что возникающая на фоне применения ИКС атрофия слизистой оболочки полости носа является существенным фактором риска перфорации перегородки носа [5]. А. Cervin и М. Andersson установили, что использование ИКС было общим фактором риска в 11 из 32 случаев, выявленных перфораций перегородки носа [8]. По данным шведского национального регистра, в течение 10 лет было зафиксировано 38 случаев перфорации перегородки носа вследствие применения ИКС. При этом в большинстве случаев перфорация была выявлена у молодых женщин в течение первых 12 мес от начала терапии [8]. Авторы другого исследования [9] скептически относятся к возможности возникновения атрофии слизистой оболочки полости носа под влиянием ИКС. Отмечено, что из 34 соответствующих публикаций термин «атрофия» слизистой оболочки полости носа упоминался в 17 статьях. При этом определение термина приводилось только в 10 публикациях, а в остальных оно значительно варьировало, отсутствовали также четкие гистологические доказательства повреждающего влияния ИКС на слизистую оболочку полости носа. Авторы отмечают, что связь между использованием ИКС и возникновением атрофии слизистой оболочки полости носа является мифом независимо от показаний, типа препарата, его дозы и длительности применения [9]. Такие же данные были получены в двух других независимых исследованиях. Так, при биопсии слизистой оболочки полости носа у пациентов, применявших ИКС от 6 мес до 5 лет, не было выявлено атрофических или других нежелательных изменений [5, 10]. Аналогичные результаты были получены N. Lindqvist и соавт., которые не обнаружили никаких гистологических изменений в слизистой оболочке полости носа 104 пациентов, применявших ИКС длительное время (в течение 12 мес) [11].
Отмечено, что кроме носовых кровотечений риск возникновения других нежелательных эффектов минимален [4, 7]. Менее характерными побочными эффектами от применения ИКС являются головная боль, тошнота, локальные грибковые инфекции [12]. Описан, в частности, единичный случай появления кандидоза полости носа у пациентки, принимавшей ИКС в течение 1,5 года [13]. Кроме полости носа кандидоз также может возникать в глотке [14].
Таким образом, единственным достоверным побочным эффектом от применения топических ИКС на локальном уровне является появление носовых кровотечений. В то же время данные о потенциальном риске возникновения перфораций перегородки носа на фоне терапии ИКС неоднозначны.
Большинство локальных побочных эффектов может быть минимизировано путем правильного применения ИКС. Отмечено, что ключевое значение имеет объяснение пациентам того факта, что распыление препарата должно осуществляться в латеральном направлении для избегания контакта с перегородкой носа [5, 15].
Системные побочные эффектыНесмотря на то что применение системных глюкокортикостероидов сопровождается значительным количеством побочных эффектов, в отношении ИКС ситуация несколько иная. Как известно, для II поколения ИКС (мометазона фуроат, флутиказона пропионат, циклесонид, флутиказона фуроат) характерна минимальная биодоступность (менее 1%) по сравнению с более ранней генерацией данной группы препаратов (триамцинолона ацетонид, флунизолид, беклометазон, дексаметазон), системная биодоступность которых находится в пределах 34—49% [5]. При применении ИКС нового поколения почти 70% дозы препарата проглатывается и в дальнейшем метаболизируется в печени, а 30% дозы задерживается на слизистой оболочке полости носа [5]. Кроме этого, значительная липофильность новых ИКС ограничивает их способность связываться с рецепторами глюкокортикостероидов, минимизируя тем самым системные эффекты [5, 16].
Одним из наименее желаемых эффектов при применении системных кортикостероидов является торможение (задержка) роста детей. Установлено, что при применении рекомендуемых доз ИКС воздействие препарата на гипоталамо-гипофизарно-надпочечниковую систему минимально [17]. В исследовании E. Schenkel и соавт. [18] наблюдение за детьми, получавшими ИКС (мометазона фуроат в дозе 100 мкг 1 раз в сутки в течение 1 года), также не выявило влияния препарата на гипоталамо-гипофизарно-надпочечниковую систему или задержку роста. Указанные изменения не были зафиксированы и в исследовании с применением флутиказона пропионата (в дозе 200 мкг ежедневно) [19].
Вместе с тем при длительном применении ИКС в дозах, превышающих рекомендованные, отмечается возможность влияния препарата на темп роста [5]. D. Skoner и соавт. обследовали 100 детей препубертатного возраста, которые в течение года получали беклометазона дипропионат (в дозе 168 мкг) или плацебо. Было отмечено, что темп роста в группе детей, получавших ИКС, отличался от значений контрольной группы. Так, в исследуемой группе пациентов отставание в росте составило в среднем 1 см, но при этом изменения со стороны гипоталамо-гипофизарно-надпочечниковой системы отсутствовали [20]. В исследовании D. Lee и соавт. [21] небольшая группа пациентов получала 220 мкг триамцинолона ацетонида или 200 мкг мометазона фуроата в течение 3 нед, в итоге не было выявлено изменений в уровнях кортизола в моче и плазме, а также остеокальцина. Однако минимальное снижение утреннего кортизола было обнаружено у пациентов, принимавших ежедневно 400 мг беклометазона 1 или 2 раза в день [22]. Схожие результаты были получены и в исследовании с применением триамцинолона ацетонида [5]. C. Möller и соавт. [23] в своем исследовании также не выявили влияния ИКС (беклометазона дипропионат) на динамику роста детей или эндогенную продукцию кортизола. В обзоре D. Mener и соавт. [24] отмечено, что короткие курсы ИКС при лечении аллергического ринита у детей могут затормаживать краткосрочный рост, но при этом остается неясным, как это сказывается на долгосрочном росте. Кроме этого, ИКС не оказывают влияние на уровень кальция и половых гормонов [17].
Остается неоднозначным влияние ИКС на орган зрения. В ряде исследований обращается внимание на риск развития катаракты [5, 25] и/или глаукомы [26] на фоне применения ИКС, однако в других работах это не нашло достоверных доказательств. N. Ahmadi и соавт. проанализировали 10 исследований, в которых пациенты получали ИКС, и ни в одном не было выявлено различий в частоте возникновения глаукомы между контрольной и основной группами. В 6 других исследованиях также не было выявлено различий в возникновении катаракты и изменении прозрачности хрусталика глаза у лиц, применявших ИКС, и пациентов контрольной группы [27].
Схожие результаты наблюдались и у детей, получавших в течение 1 года мометазона фуроат (в дозе 100 мкг) или беклометазона дипропионат (в дозе 168 мкг), только у 1 пациента, принимавшего беклометазона дипропионат, было выявлено повышение внутриглазного давления [28]. Также не было выявлено появления глауком и катаракт в исследовании L. Derby и W. Maier, в котором в течение 3—9 мес пациенты получали 200 мг будесонида или 200 мкг беклометазона дипропионата [29]. В ретроспективном исследовании, включавшем 286 078 пациентов, принимавших ИКС, оральные стероиды или плацебо, не было выявлено различий в частоте развития катаракты в группе больных, принимавших ИКС, по сравнению с контролем [30].
Несмотря на то что инъекции кортикостероидов в носовые раковины и полипы не являются топическим применением, решение включить соответствующие данные в настоящий обзор связано с тем, что такое использование этой группы препаратов распространено в клинической практике. В исследовании W. Moss и соавт. было выполнено 237 инъекций метилпреднизолона ацетата и триамцинолона ацетонида, из них 152 введения в нижние носовые раковины и 85 — в полипы. После выполнения инъекций в полип только у 1 пациента возникло осложнение в виде транзиторной слепоты, которая купировалась спонтанно. В дополнение авторы проанализировали еще 9 серий исследований, в которых было выполнено в общей сложности 117 669 инъекций, при этом только в 3 (0,003%) случаях возникли осложнения. В этих 3 случаях осложнения разрешились также спонтанно без остаточных явлений. Авторы отмечают, что при правильной технике выполнения инъекции риск развития осложнений минимален [31].
В литературе описано 3 случая полной слепоты, возникшей после инъекции кортикостероидов в слизистую оболочку перегородки носа. Однако при этом отмечается отсутствие достаточных сведений о технике введения препарата и показаний для такого рода вмешательств [32, 33].
Существует также мнение, что применение ИКС может оказывать влияние на уровень глюкозы у пациентов с сахарным диабетом. В исследовании, включавшем 1768 человек, принимавших ИКС в течение не менее 3 мес, было выявлено, что уровень глюкозы был значительно выше у больных, получавших триамцинолона ацетонид, по сравнению с пациентами, принимавшими другие ИКС. Однако уровень гликированного гемоглобина существенно не изменился ни в одной группе пациентов. Установлено, что длительные курсы лечения ИКС в целом являются безопасными для пациентов с сахарным диабетом, однако необходим постоянный мониторинг соответствующих показателей, в особенности у больных, получающих триамцинолона ацетонид [34].
Несмотря на отсутствие серьезных системных побочных эффектов, анализ литературы выявил 1 случай острой надпочечниковой недостаточности, развившейся вследствие применения флутиказона пропионата, однако важно отметить, что данный пациент принимал дозу, превышающую рекомендованную [35]. Важно также подчеркнуть, что применение ИКС в утренние часы снижает нефизиологический эффект стероидов, так как препятствует вечернему снижению уровня кортизола [17].
При беременности не описано случаев тератогенного эффекта ИКС [36].
Отмечено, что терапевтический эффект, а также риск развития нежелательных явлений топических ИКС в значительной степени определяются частотой, длительностью применения и дозировкой препарата [5, 17]. При правильном использовании топических ИКС существенный риск возникновения побочных эффектов как системного, так и локального характера минимален [17].
Таким образом, использование ИКС последнего поколения существенно минимизирует риск возникновения любых побочных эффектов, однако, несмотря на это, необходимо контролировать состояние пациента в процессе лечения.
Автор заявляет об отсутствии конфликта интересов.
Интраназальные кортикостероиды в терапии аллергического ринита :: ТРУДНЫЙ ПАЦИЕНТ
Е.А. Ушкалова, профессор кафедры общей и клинической фармакологии РУДН, Москва
Аллергический ринит относится к числу самых широко встречающихся заболеваний, распространенность и частота которого продолжает расти крайне высокими темпами. Так, за последние 30 лет в течение каждого десятилетия заболеваемость в экономически развитых странах увеличивалась на 100 % [1, 2], что позволило назвать ее эпидемической [3]. По данным эпидемиологических исследований, распространенность аллергического ринита составляет в среднем на планете 10-25 %, в Европе – 20-30, в Новой Зеландии и в Австралии – около 40, в Южной Африке – около 17, в России – 25 % [4-7]. В США аллергический ринит поражает ежегодно около 40 млн человек, в т. ч. примерно 10-30 % взрослого населения и 40 % детей [8, 9]. В 80 % случаев заболевание начинается в возрасте до 20 лет [10]. В России, согласно данным официальной статистики, аллергический ринит встречается у 9-25 % детей 5-8 лет [11]. Однако, по мнению российских и зарубежных специалистов, официальные данные о заболеваемости, основанные на обращаемости пациентов, ни в коей мере не отражают истинной распространенности аллергического ринита, так как не учитывают огромное количество лиц, не обратившихся за медицинской помощью, и больных, которым был поставлен неправильный диагноз [10-13]. Существуют сведения, что в Европе, включая Россию, за медицинской помощью по поводу симптомов аллергического ринита обращается не более 60 % пациентов. Согласно результатам обследования 1000 больных, проведенного в клинике ГНЦ – Института иммунологии Минздрава России, только 12 % пациентов диагноз аллергического ринита ставится в первый год заболевания, 50 % – в первые пять лет, остальным – через 9-30 и более лет после появления симптомов.
Прямые медицинские затраты при аллергическом рините оцениваются в США в 4,5 млрд долларов в год [9]. Непрямые затраты, связанные с потерей 3,8 млн рабочих и 2 млн академических дней, еще больше повышают стоимость этого заболевания для системы здравоохранения и общества в целом [9, 14]. Клиническое и экономическое бремя аллергического ринита обусловлено и снижением качества жизни пациентов, а также риском развития серьезных осложнений со стороны дыхательных путей и ЛОР-органов.
В частности, аллергический ринит считают фактором риска развития бронхиальной астмы [15, 16]. Он встречается у 80-90 % пациентов, страдающих бронхиальной астмой [17], а у 68 % детей с аллергическим ринитом выявляется гиперреактивность бронхов [18]. Тесная взаимосвязь между бронхиальной астмой и аллергическим ринитом позволяет некоторым авторам рассматривать их как единое заболевание [17]. Аллергический ринит также часто сочетается с синуситом, конъюнктивитом, средним отитом, фарингитом, ларингитом, храпом и апноэ во сне [19]. В некоторых исследованиях выявлена ассоциация аллергического ринита с депрессией и болью в нижней части спины [20].
Таким образом, лечение аллергического ринита и предупреждение сопутствующих ему заболеваний имеет важное медицинское, социальное и экономическое значение.
Методы лечения аллергического ринита
Лечение больных аллергическим ринитом включает нефармакологические и фармакологические методы. Первые прежде всего направлены на устранение аллергенов и провоцирующих факторов или уменьшение контакта с ними. Полная элиминация аллергена в большинстве случаев невозможна, особенно у пациентов с круглогодичным (персистирующим) ринитом, которые постоянно подвергаются его воздействию [21]. Во многих ситуациях эффективная элиминация аллергенов невозможна не только по практическим, но и экономическим причинам, так как сопряжена со значительными финансовыми расходами для пациента [22]. Тем не менее, даже уменьшение контакта с аллергеном позволяет улучшить контроль симптомов заболевания и снизить потребность в фармакотерапии.
В многочисленных клинических исследованиях доказана эффективность при аллергическом рините специфической иммунотерапии, однако этот метод лечения также не лишен ряда недостатков. Во-первых, специфическая иммунотерапия эффективна только у пациентов с повышенной чувствительностью к ограниченному спектру (1 или 2) аллергенов [23, 24]. Во-вторых, высокая эффективность (80-90 %) показана в клинических исследованиях лишь при применении парентеральной специфической иммунотерапии, которая не очень удобна для пациентов, поскольку представляет собой медленный постепенный процесс подкожного введения антигена в увеличивающихся дозах [21]. Кроме того, она дорога и небезопасна, так как может вызывать угрожающие жизни анафилактические реакции [25, 26]. Рутинное применение более удобной сублингвальной иммунотерапии на основании результатов анализа 23 плацебо-контролируемых двойных слепых исследований в настоящее время рекомендовано быть не может [27]. Кроме того, дозы аллергена, необходимые для сублингвальной иммунотерапии, в 5-200 раз превышают таковые для парентеральной [28]. С учетом вышеизложенного зарубежные эксперты рекомендуют резервировать иммунотерапию для пациентов с тяжелыми нарушающими повседневную жизнь симптомами, чье заболевание вызвано ограниченным количеством идентифицированных аллергенов и которые не отвечают на лечение другими методами [21].
Таким образом, основное место в профилактике и терапии аллергического ринита принадлежит лекарственным средствам. С этой целью используют препараты нескольких фармакологических групп: блокаторы h2-гистаминовых рецепторов, кортикостероиды, стабилизаторы мембран тучных клеток, сосудосуживающие средства (деконгестанты), М-холиноблокаторы. Изучается эффективность при этом заболевании и препаратов относительно новых групп – антагонистов лейкотриеновых рецепторов и моноклональных антител [29-32]. Один из антагонистов лейкотриенов монтелукаст был недавно одобрен для лечения сезонного аллергического ринита [21].
В целом, все лекарственные средства, применяемые для лечения аллергического ринита, можно подразделить на две группы: 1) препараты, позволяющие контролировать симптомы заболевания, и 2) препараты, действующие на патогенетические факторы, т. е. оказывающие истинно терапевтический эффект [21]. К последней группе прежде всего относятся кортикостероиды, значение которых резко возросло после введения в медицинскую практику в начале 1970-х гг. первого препарата этой группы (беклометазона дипропионата) для интраназального применения.
Место интраназальных кортикостероидов в терапии аллергического ринита
Несмотря на то то глюкокортикоиды уже более века используются для лечения заболеваний ЛОР-органов, их механизм действия продолжает активно изучаться. В экспериментальных и клинических исследованиях показано, что глюкокортикоиды воздействуют практически на все этапы патогенеза аллергического ринита [33]. Их терапевтический эффект при аллергическом рините связывают, прежде всего, с противовоспалительным и десенсибилизирующим действием. Установлено, что глюкокортикоиды тормозят синтез целого ряда цитокинов, в частности ИЛ-1, ИЛ-3, ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-13, ФНО-а и GM-CSF [33]. Кроме того, они уменьшают индукцию синтетазы оксида азота (NO), активация которой приводит к избыточному образованию NO, оказывающего выраженное провоспалительное действие. Глюкокортикоиды также снижают активность генов, кодирующих синтез ферментов, принимающих участие в продукции других провоспалительных белковых молекул: циклооксигеназы, фосфолипазы А2 и эндотелина-1, тормозят экспрессию молекул адгезии: ICAM-1 и Е-селектина. На клеточном уровне глюкокортикоиды вызывают уменьшение количества тучных клеток, базофилов и выделяемых ими медиаторов; снижают количество эозинофилов и их продуктов в эпителии и в собственном слое слизистой оболочки. Они также влияют на процессы апоптоза, уменьшая срок жизни эозинофилов; снижают количество клеток Лангерганса и угнетают захват и транспортировку антигенов этими клетками; снижают количество Т-клеток в эпителии; уменьшают продукцию лейкотриенов в слизистой оболочке; ингибируют продукцию IgE. Глюкокортикоиды снижают секрецию желез слизистой оболочки, экстравазацию плазмы и отек тканей. Кроме того, они уменьшают чувствительность рецепторов слизистой оболочки носа к гистамину и механическим раздражителям, т. е. в определенной степени воздействуют и на неспецифическую назальную гиперреактивность. Воздействие на все звенья патогенеза заболевания и торможение как ранней, так и отсроченной фаз аллергической реакции характерно не только для глюкокортикоидов системного действия, но и для интраназальных препаратов этой группы. Преимуществом интраназальных глюкокортикоидов перед пероральными является минимальный риск системных побочных эффектов на фоне создания адекватных концентраций активного вещества в слизистой оболочке носа, позволяющих контролировать симптомы аллергического ринита [34, 35].
Интраназальные кортикостероиды зарекомендовали себя эффективными средствами как для предупреждения, так и для облегчения симптомов, обусловленных ранней и поздней фазами аллергического ответа [36-38]. Снижение количества Т-лимфоцитов, эозинофилов, базофилов, моноцитов и тучных клеток в верхних дыхательных путях под их влиянием вызывает уменьшение заложенности в носу, ринореи, чихания и зуда [9, 15, 39, 40], что приводит к значительному улучшению качества жизни пациентов [40]. В ряде исследований показано, что интраназальные глюкокортикоиды позволяют почти полностью предотвратить симптомы поздней фазы аллергического ответа [41-43].
Сравнительная характеристика интраназальных кортикостероидов и других широко применяющихся для лечения аллергического ринита лекарственных средств представлена в табл. 1, из которой видно, что интраназальные кортикостероиды в большей степени устраняют симптомы заболевания, чем препараты всех других групп. Результаты клинических исследований и мета-анализов позволяют считать их самыми эффективными средствами для лечения аллергического ринита и рассматривать в качестве препаратов первого ряда при этом заболевании [17, 36, 44-46].
Таблица 1. Сравнительная характеристика кортикостероидов и других лекарственных средств для лечения аллергического ринита [22]
Симптомы | Пероральные антигистаминные средства | Интраназальные антигистаминные средства | Интраназальные кортикостероиды | Интраназальные деконгестанты | M-холиноблокаторы (ипратропия бромид) | Кромоны |
Ринорея | ++ | ++ | +++ | 0 | ++ | + |
Чиханье | ++ | ++ | +++ | 0 | 0 | + |
Зуд | ++ | ++ | +++ | 0 | 0 | + |
Заложенность носа | + | + | +++ | ++++ | 0 | + |
Конъюнктивит | ++ | +++ | ++ | 0 | 0 | +++ |
Начало действия | 1 ч | 15 мин | 12 ч | 5-15 мин | 15-30 мин | 15-30 мин |
Длительность | 12-24 ч | 6-12 ч | 6-12 ч | 3-6 ч | 4-12 ч | 2-6 ч |
В международной клинической практике в настоящее время широко используются следующие интраназальные кортикостероиды: триамцинолона ацетонид, бекламетазона дипропионат, флунизолид, будесонид, флутиказона пропионат и мометазона фуроат.
В России флунизолид и триамцинолон в виде назальных аэрозолей не используются. Применение гидрокортизона и преднизолона интраназально не рационально, так как эти препараты обладают очень высокой биодоступностью и могут вызывать системные побочные эффекты, особенно в случае, когда распыляются в полости носа. Из-за высокой биодоступности теряют свое практическое значение и интраназальные лекарственные формы дексаметазона и бетаметазона. В отличие от них, современные интраназальные глюкокортикоиды обладают низкой биодоступностью (табл. 2) и хорошо переносятся больными. Следует иметь в виду, что биодоступность интраназальных препаратов определяется не только их всасыванием со слизистой оболочки носа, но и абсорбцией той части дозы (менее половины от введенной), которая, осев в глотке, проглатывается и всасывается в кишечнике. Кроме того, при нормально функционирующем мукоцилиарном транспорте основная часть препарата (до 96 %) в течение 20-30 минут после интраназального введения переносится в глотку с помощью ресничек слизистой оболочки носа, откуда поступает в желудочно-кишечный тракт и подвергается абсорбции [48]. Поэтому биодоступность при пероральном и интраназальном приеме является важной характеристикой интраназальных кортикостероидов, которая в значительной степени определяет их терапевтический индекс, т. е. соотношение местной противовоспалительной активности и потенциала неблагоприятного системного действия.
Таблица 2. Биодоступность интраназальных кортикостероидов [48]
| Препарат | Биодоступность при интраназальном введении (%) | Биодоступность при пероральном приеме (%) |
| Беклометазон дипропионат | 44 | 20-25 |
| Триамцинолон ацетонид | нет данных | 10,6-23 |
| Флунизолид | 40-50 | 21 |
| Будесонид | 34 | 11 |
| Флютиказон пропионат | 0,5-2 | |
| Мометазон фуроат |
Низкая биодосупность современных интраназальных кортикостероидов связана не только с их плохой абсорбцией, но и с быстрым и практически полным метаболизмом при первом проходе через печень. Это обусловливает в целом короткий период полувыведения интраназальных кортикостероидов, однако продолжительность его разная для разных препаратов. Интраназальные кортикостероиды также различаются степенью липофильности, определяющей объем их распределения в организме, степенью сродства к рецепторам и силой действия.
Для измерения силы действия топических кортикостероидов используют 2 метода – определение степени сродства к глюкокортикоидным рецепторам и сосудосуживающей активности на модели кожи. По степени сродства к рецепторам препараты располагаются в следующем восходящем порядке: дексаметазон, триамцинолона ацетонид, будесонид, флутиказона пропионат и мометазона фуроат [49]. По показателю сосудосуживающей активности флутиказона пропионат и мометазона фуроат превосходят другие интраназальные препараты [38, 44]. Однако сосудосуживающая активность лишь частично определяет эффективность кортикостероидов при аллергическом рините, так как непосредственно не коррелирует с противовоспалительной активностью [34].
Препараты с высокой липофильностью, например флутиказона пропионат или мометазона фуроат, лучше проникают в ткани и обладают большим объемом распределения в них [50]. Они могут создавать в тканях резервуар, из которого медленно высвобождается активное вещество, что обусловливает их значительно более длительный конечный период полувыведения из организма. Напротив, менее липофильные кортикостероиды, например триамционолона ацетонид или будесонид, имеют меньший объем распределения. Высокая степень липофильности снижает водорастворимость препаратов в слизистой оболочке и, таким образом, увеличивает количество активного вещества, выводимого посредством мукоцилиарного клиренса еще до того, как оно достигнет рецептора в тканях. Это может способствовать снижению местной противовоспалительной активности препарата в носу, но в то же время и уменьшению его абсорбции со слизистой оболочки в системный кровоток. Клиническое значение высокой липофильности требует дальнейшего изучения [50].
Начало терапевтического эффекта интраназальных глюкокортикоидов обычно наблюдается спустя несколько дней после первого введения (табл. 3), однако для достижения максимального эффекта может потребоваться несколько недель [43].
Таблица 3. Начало действия интраназальных кортикостероидов [51]
Препарат | Начало действия |
Беклометазон | В течение 3 дней |
Будесонид | 24 часа |
Флунизолид | 4-7 дней |
Флутиказон | 12 часов – 3 дня |
Mometasone | 12 часов – 3 дня |
Triamcinolone | 24 часа |
Эффективность и переносимость интраназальных кортикостероидов во многом определяются системой их доставки в полость носа [48]. Наиболее широко применяемыми лекарственными формами являются дозированные аэрозоли и назальные спреи. Последние обеспечивают более эффективную доставку действующего вещества и реже вызывают местные побочные эффекты (носовые кровотечения, сухость, жжение в носу, зуд, чихание), которые при применении дозированных аэрозолей в значительной степени обусловлены раздражающим действием фреона и высокой скоростью поступления лекарств в полость носа.
Эффективность современных интраназальных кортикостероидов при аллергическом рините была доказана в многочисленных плацебо-контролируемых исследованиях и сравнительных исследованиях с препаратами других фармакологических групп. Так, в трех мета-анализах рандомизированных контролируемых исследований было показано, что интраназальные кортикостероиды значительно превосходят по способности устранять чихание, ринорею, зуд, заложенность в носу и нарушение обоняния топические и пероральные антигистаминные средства, включая препараты последних поколений [52-54].
В рандомизированном клиническом исследовании у пациентов с аллергическим ринитом монотерапия интраназальным будесонидом (200 мкг) проявляла равную эффективность с комбинацией антигистаминного препарата (цетирзин, 10 мг) и антагонистом лейкотриена (монтелукаст, 10 мг) в отношении заложенности носа и улучшения носового дыхания [55]. Более того, анализ опубликованных данных позволяет прийти к заключению, что интраназальные кортикостероиды значительно в большей степени облегчают симптомы аллергического ринита, чем антигистаминные препараты, антагонисты лейкотриена и их комбинации [32, 56].
Согласно международным рекомендациям (программе ВОЗ ARIA – Allergic rhinitis and its impact on asthma) интраназальные кортикостероиды могут применяться на всех стадиях аллергического ринита, начиная от легких форм интермиттирующего (сезонного) до тяжелых форм персистирующего (круглогодичного), причем при среднетяжелом и тяжелом течении заболевания они рассматриваются в качестве средств первого выбора [17]. Наряду с улучшением симптомов аллергического ринита и влиянием на патогенетические механизмы развития заболевания, интраназальные кортикостероиды играют важную роль и в лечении сопутствующих болезней, таких как бронхиальная астма, синусит и полипы носа [57].
Несмотря на различия физико-химических, фармакодинамических и фармакокинетических свойств топических глюкокортикоидов, в большинстве сравнительных клинических исследований не удалось продемонстрировать терапевтических преимуществ одних препаратов перед другими [44, 58-64]. Например, в сравнительном исследовании будесонида (400 мкг 1 р/сут) и мометазона фуроата (200 мкг 1 р/сут), несмотря на выше указанные фармакодинамические и фармакокинетические преимущества последнего, была показана равная эффективность обоих препаратов в предотвращении симптомов сезонного аллергического ринита, которая оценивалась по количеству дней, прошедших с начала аллергического сезона до появления относительно выраженных симптомов заболевания [65]. Оба препарата значительно превосходили по данному показателю плацебо: при применении мометазона симптомы возникли в среднем через 26 дней, будесонида – 34 дня, плацебо – 9 дней. Более того, в другом исследовании у больных с круглогодичным ринитом будесонид (256 мкг 1 р/сут) достоверно превосходил по эффективности устранения всех симптомов, а также по эффективности устранения заложенности в носу другой препарат с низкой биодоступностью и высоким сродством к глюкокортикоидным рецепторам – флутиказон (200 мкг 1 р/сут) [66]. Возможно, это связано со способностью препарата подвергаться эстерификации, с которой связывают пролонгирование его противовоспалительного действия по сравнению с кортикостероидами, не образующими эфиров, в частности флутиказоном [67]. В клинических исследованиях было подтверждено, что через 6 часов после введения концентрации будесонида, по данным назальной биопсии, превосходили концентрации флутиказона пропионата более чем в 10 раз, а через 24 часа – более чем в три раза [67]. Авторы обзора, посвященного этому вопросу, высказывают предположение, что благодаря данному механизму соотношение местной пользы и системного риска может сдвигаться у будесонида в лучшую сторону вследствие меньшего системного образования эфиров по сравнению с их образованием в дыхательных путях [67]. Однако этот вопрос требует дальнейшего изучения.
Согласно результатам мета-анализа, все топические кортикостероиды во всех лекарственных формах для интраназального введения являются эффективными и безопасными средствами, значительно улучшающими качество жизни пациентов [54]. Тем не менее, в целенаправленных исследованиях удалось показать, что органолептические свойства и лекарственные формы препаратов оказывают выраженное влияние на предпочтения пациентов, а следовательно, и на аккуратность соблюдения ими назначенного режима лечения [68-70].
Так, в одном из исследований, посвященных изучению предпочтений больных, в котором участвовало 503 пациента и 100 врачей, было показано, что 97 % больных предпочитают назальные спреи, лишенные «послевкуса» и/или запаха [68]. Согласно результатам этого исследования, 97 % врачей уверены, что органолептические свойства интраназальных кортикостероидов оказывают влияние на соблюдение пациентами режима лечения, однако в реальной практике более половины из них при назначении препарата не спрашивают пациента о его предпочтениях. Еще в одном многоцентровом рандомизированном слепом исследовании проводилась сравнительная оценка предпочтений пациентов с легким и среднетяжелым аллергическим ринитом в отношении водного назального спрея будесонида и назального спрея флутиказона пропионата [70]. Сенсорное восприятие спрея будесонида больными по разным показателям достоверно превосходило таковое спрея флутиказона, в связи с чем большинство пациентов отдали предпочтение спрею будесонида. В другом плацебо-контролируемом исследовании, где сравнивались интраназальные лекарственные формы тех же препаратов у больных с сезонным аллергическим ринитом, несмотря на равную клиническую эффективность будесонида и флутиказона, качество жизни пациентов в большей степени улучшилось в группе будесонида [71].
Таким образом, способность интраназальных кортикостероидов воздействовать на все симптомы аллергического ринита, включая заложенность носа и нарушение обоняния, выгодно отличает их от препаратов других фармакологических групп, особенно при персистирующем (круглогодичном) рините, когда затруднение носового дыхания является основным симптомом. Все современные препараты этой группы являются эффективными и безопасными средствами. Схемы лечения современными интраназальными кортикостероидами представлены в табл. 4. Продолжительность курса лечения зависит от тяжести ринита и может составлять от 10 дней до 3 месяцев Выбор конкретного препарата определяется преимущественно ценой и предпочтениями пациентов. Оба этих фактора могут оказать существенное влияние на приверженность лечению и эффективность терапии.
Таблица 4. Схемы применения интраназальных кортикостероидов [48]
Препарат | Схема применения |
Беклометазон | 50 мкг в каждую ноздрю 3 р/сут |
Будесонид* | 100 мкг в каждую ноздрю 2 р/сут |
Мометазон | 50 мкг в каждую ноздрю 1 р/сут |
Флутиказон | 50 мкг в каждую ноздрю 1 р/сут |
* Препарат «Бенарин» 30 мкг в каждую ноздрю 2 р/сут.
литература:
Aberg N, Sundell J, Eriksson B, Hesselmar B, Aberg B. Prevalence of allergic disease in schoolchildren in relation to family history, upper respiratory tract infections, and residential characteristics. Allergy. 1996;51:232-237.
Sibbald B, Rink E, D’Souza M. Is the prevalence of atopy increasing? Br J Gen Pract. 1990;40:338-340.
Ceuppens J. Western lifestyle, local defenses and the rising incidence of allergic rhinitis. Acta Otorhinolaryngol Belg. 2000;54:391-395.
Ильина Н.И., Польнер С.А. Круглогодичный аллергический ринит // Consilium medicum. 2001. Т. 3. № 8. С. 384-393.
Лусс Л.В. Аллергический ринит: проблемы, диагностика, терапия // Лечащий врач. 2002 . № 4. С. 24-28.
Пыцкий В.И. и др. Аллергические заболевания. М.: Триада-Х, 1999. 470 с.
Паттерсон Р. и др. Аллергические болезни. М.: Гэотар, 2000. 733 с.
Naclerio RM, Solomon W. Rhinitis and inhalant allergens. JAMA 1997;278:1842-8.
GlaxoWellcome. The health and economic impact of rhinitis. Am J Manag Care 1997;3:S8-18.
Sibbald B. Epidemiology of allergic rhinitis. In: ML B, ed. Epidemiology of Clinical Allergy. Monographs in Allergy. Basel, Switzerland: Karger; 1993:61-69.
Геппе Н.А. Возможности применения антигистаминных препаратов в педиатрической практике // Избранные лекции для практикующих врачей. IX Российский национальный конгресс «Человек и лекарство». М., 2002. С. 250-261.
Хаитов Р.М., Богова А.В., Ильина Н.И. Эпидемиология аллергических заболеваний России // Иммунология.1998. № 3. С. 4-9.
Ильина Н.И. Аллергопатология в разных регионах России по результатам клинико-эпидемиологических исследований: Автореф. докт. дисс. М., 1996. 24 с.
Dykewicz MS, Fineman S, Skoner DP, et al. Diagnosis and management of rhinitis: complete guidelines of the Joint Task Force on Practice Parameters in Allergy, Asthma and Immunology. Ann Allergy Asthma Immunol. 1998;81(5 Pt 2):478-518.
American Academy of Allergy, Asthma, and Immunology. The allergy report. Milwaukee: American Academy of Allergy, Asthma, and Immunology, 2000.
Gasbarro R. Identifying and managing patients with asthma and allergy. Drug Topics 2001;7:68-77.
Bousquet J, van Cauwenberge P, Khaltaev N. et al. Allergic rhinitis and its impact on asthma (ARIA) – Pocket Guide. – WHO. 2001; 23: 5.
Студеникина Н.И., Ревякина В.А., Лукина О.Ф., Куличенко Т.В. Проблемы раннего выявления, профилактики и терапии атопических заболеваний у детей // Сб. тезисов 1-го Всероссийского конгресса по детской аллергологии. М., 29-30 ноября 2001 г., с. 144.
Coste A. ENT diseases associated with allergic rhinitis: a review of the literature. Ann Otolaryngol Chir Cervicofac. 2000;117:168-173.
Hurwitz EL, Morgenstern H. Cross-sectional associations of asthma, hay fever, and other allergies with major depression and low-back pain among adults aged 20-39 years in the United States. Am J Epidemiol. 1999;150:1107-1116.
Trangsrud AJ, Whitaker AL, Small RE. Intranasal Corticosteroids for Allergic Rhinitis. Pharmacotherapy 22(11):1458-1467, 2002.
Лопатин А.С. Алгоритмы диагностики и лечения аллергического и вазомоторного ринита // РМЖ. 2002. Т. 10. № 17.
Malling HJ. Immunotherapy as an effective tool in allergy treatment. Allergy. 1998 May;53(5):461-72.
Varney VA, Edwards J, Tabbah K, Brewster H, Mavroleon G, Frew AJ. Clinical efficacy of specific immunotherapy to cat dander: a double-blind placebo-controlled trial. Clin Exp Allergy. 1997 Aug;27(8):860-7.
Durham SR, Ying S, Varney VA, et al. Cytokine messenger RNA expression for IL-3, IL-4, IL-5 and GM-CSF in the nasal mucosa after local allergen provocation: relationship to tissue eosinophilia. J Immunol 1992;148:2390-4.
Anonymous. Guidelines to minimize the risk from systemic reaction caused by immunotherapy with allergen extracts. J Allergy Clin Immunol 1994;93(5):811-12.
Malling H-J. Is Sublingual Immunotherapy Clinically Effective? Curr Opin Allergy Clin Immunol 2002;2:523-32.
Guez S, Vatrinet C, Fadel R, Andre C. House-dust mite sublingual swallow immunotherapy (SLIT) in perennial rhinitis: a double-blind, placebo-controlled study. Allergy. 2000;55:369-375.
Casale TB, Bernstein IL, Busse WW, et al. Use of an anti-IgE humanized monoclonal antibody in ragweed-induced allergic rhinitis. J Allergy Clin Immunol 1997;100:110-21.
Shields RL, Whether WR, Zioncheck K, et al. Inhibition of allergic reactions with antibodies to IgE. Int Arch Allergy Immunol 1995;7:308-12.
Philip G, Malmstrom K, Hampel FC Jr, et al. Montelukast for treating seasonal allergic rhinitis: a randomized, double-blind, placebo-controlled trial performed in the spring. Clin Exp Allergy. 2002;32:1020-1028.
Nathan RA. Pharmacotherapy for allergic rhinitis: a critical review of leukotriene receptor antagonists compared with other treatments. Ann Allergy Asthma Immunol. 2003;90:182-191.
Лопатин А.С. Кортикостероидная терапия в лечении заболеваний носа и околоносовых пазух: исторические аспекты // Consilium-medicum. 2004. Т. 6. № 4.
Mygind N, Nielsen LP, Hoffmann HJ, et al. Mode of action of intranasal corticosteroids. J Allergy Clin Immunol 2001;108(suppl 1):S16-25.
Mygind N, Dahl R. The rationale for use of topical corticosteroids in allergic rhinitis. Clin Exp Allergy 1996;26(suppl 3):2-10.
Mygind N. Glucocorticosteroids and rhinitis. Allergy 1993;48:476-90.
Wiseman LR, Benfield P. Intranasal fluticasone propionate: a reappraisal of its pharmacology and clinical efficacy in the treatment of rhinitis. Drugs 1997;53:885-907.
Onrust SV, Lamb HM. Mometasone furoate: a review of its intranasal use in allergic rhinitis. Drugs 1998;56:725-45.
Gasbarro R. Identifying and managing patients with asthma and allergy. Drug Topics 2001;7:68-77.
Tripathy A, Patterson R. Impact of allergic rhinitis treatment on quality of life. Pharmacoeconomics 2001;19(9):891-9.
Lund V. International rhinitis management working group. International consensus report on the diagnosis and management of rhinitis. Allergy 1994;49(suppl 19):1-34.
Rak S, Jacobson MR, Suderick RM, et al. Influence of prolonged treatment with topical corticosteroid (fluticasone propionate) on early and late phase responses and cellular infiltration in the nasal mucosa after allergen challenge. Clin Exp Allergy 1994;24(10):930-9.
Konno A, Yamakoshi T, Terada N, Fujita Y. Mode of action of a topical steroid on immediate phase reaction after antigen challenge and nonspecific nasal hyperreactivity in nasal allergy. Int Arch Allergy Immunol 1994;103(1):79-87.
Corren J. Intranasal corticosteroids for allergic rhinitis: how do different agents compare? J Allergy Clin Immunol 1999;104(4):S144-9.
Mabry RL. Pharmacotherapy of allergic rhinitis: corticosteroids. Otolaryngol Head Neck Surg 1995;113:120-5.
Lund V. International rhinitis management working group. International consensus report on the diagnosis and management of rhinitis. Allergy 1994;49(suppl 19):1-34.
LaForce C. Use of nasal steroids in managing allergic rhinitis. J Allergy Clin Immunol 1999;103:S388-94.
Емельянов А.В., Лукьянов С.В. Назальные глюкокортикоиды // Рациональная фармакотерапия заболеваний органов дыхания. М.: «Литтера», 2004. С. 93-97.
Smith CL, Kreutner W. In vitro glucocorticoid receptor binding and transcriptional activation by topically active glucocorticoids. Arzneimittelforschung/Drug Res 1998;48:956-60.
Lipworth BJ, Jackson CM. Safety of inhaled and intranasal corticosteroids: lessons for the new millennium. Drug Saf. 2000 Jul;23(1):11-33.
Buck ML. Intranasal Steroids for Children With Allergic Rhinitis. Pediatr Pharm 7(5), 2001.
Yanez A, Rodrigo GJ. Intranasal corticosteroids versus topical h2 receptor antagonists for the treatment of allergic rhinitis: a systemic review with meta-analysis. Ann Allergy Asthma Immunol. 2002;89:479-484.
Weiner JM, Abramson MJ, Puy RM. Intranasal corticosteroids versus oral h2 receptor antagonists in allergic rhinitis: systematic review of randomised controlled trials. BMJ. 1998;317:1624-1629.
Stempel DA, Thomas M. Treatment of allergic rhinitis: an evidence-based evaluation of nasal corticosteroids versus nonsedating antihistamines. Am J Manag Care 1998;4:89-96.
Wilson A., Orr L., Sims E., Dempsey O., Lipworth B. Antiasthmatic activity of combined oral histamine and leukotriene antagonism versus inhaled and intra-nasal corticosteroid in seasonal allergic rhinitis (SAR) and asthma // 56th An-nual Meeting. American Academy of Allergy Asthma & Immunology. 03-Mar-2000. Abs.1078. San Diego. United States.
Nelson HS. Advances in upper airway diseases and allergen immunotherapy. J Allergy Clin Immunol. 2003;111:S793-S798.
Stanaland BE. Treatment of Allergic Rhinitis and Its Comorbidities. June 24, 2003 http://www.medscape.com/viewprogram/2344_pnt
Meltzer EO. Clinical and antiinflammatory effects of intranasal budesonide aqueous pump spray in the treatment of perennial allergic rhinitis. Ann Allergy Asthma Immunol 1998;81:128-34.
Brannan MD, Herron JM, Affrime MB. Safety and tolerability of once-daily mometasone furoate aqueous nasal spray in children. Clin Therapeut 1997;19:1330-9.
Meltzer EO, Berger WE, Berkowitz RB, et al. A dose-ranging study of mometasone furoate aqueous nasal spray in children with seasonal allergic rhinitis. J Allergy Clin Immunol 1999;104:107-14.
Ngamphaiboon J, Thepchatri A, Chatchatee P, et al. Fluticasone propionate aqueous nasal spray treatment for perennial allergic rhinitis in children. Ann Allergy Asthma Immunol 1997;78:479-84.
Fluticasone Propionate Collaborative Pediatric Working Group. Treatment of seasonal allergic rhinitis with once-daily intranasal fluticasone propionate therapy in children. J Pediatr 1994;125:628-34.
Small P, Houle P, Day JH, et al. A comparison of triamcinolone acetonide nasal aqueous spray and fluticasone propionate aqueous solution spray in the treatment of spring allergic rhinitis. J Allergy Clin Immunol 1997;100:592-5.
Mandl M, Nolop K, Lutsky BN, et al. Comparison of once daily mometasone furoate and fluticasone propionate aqueous nasal sprays for the treatment of perennial rhinitis. Ann Allergy Asthma Immunol 1997;79:237-45.
Marazzi P, Nolop K, Lutsky BN, et al. Prophylactic use of once-daily mometasone furoate (Nasonex) aqueous nasal spray in patients with seasonal allergic rhinitis. J Allergy Clin Immunol 1997;99:S440.
Day J, Carrillo T. Comparison of the efficacy of budesonide and fluticasone propionate aqueous nasal spray for once daily treatment of perennial allergic rhinitis, J Allergy Clin Immunol 1998;102:902-8.
Edsbacker S, Brattsand R. Budesonide fatty-acid esterification: a novel mechanism prolonging binding to airway tissue. Review of available data. Ann Allergy Asthma Immunol. 2002 Jun;88(6):609-16.
Kaliner MA. Patient preferences and satisfaction with prescribed nasal steroids for allergic rhinitis. Allergy Asthma Proc. 2001;22(6 suppl):S11-S15.
Bachert C, EI-Akkad T. Patient preferences and sensory comparisons of three intranasal corticosteroids for the treatment of allergic rhinitis. Ann Allergy Asthma Immunol. 2002;89:292-297.
Shah SR, Miller C, Pethick N, O’Dowd L. Patients with allergic rhinitis prefer budesonide aqueous nasal spray to fluticasone propionate nasal spray based on sensory attributes. Program and abstracts of the 58th Annual Meeting of the American Academy of Allergy, Asthma and Immunology; March 1-6, 2002; New York, NY.
Ciprandi G, Canonica WG, Grosclaude M, Ostinelli J, Brazzola GG, Bousquet J. Effects of budesonide and fluticasone propionate in a placebo-controlled study on symptoms and quality of life in seasonal allergic rhinitis. Allergy. 2002;57:586-591.
положение инициативной группы «Аллергический ринит и его влияние на астму»
Авторы: J Bousquet et al
Опубликовано: Allergy, 31.03.2020
Перевод: Надежда Кнауэр, Фонд профилактики рака
Недавно обнаруженный штамм коронавируса человека, получивший от Международного комитета по таксономии вирусов (ICTV) [1] название SARS-CoV-2 (коронавирус 2, вызывающий тяжелый острый респираторный синдром), вызывает инфекционное заболевание, обозначенное Всемирной организацией здравоохранения (ВОЗ) как «коронавирусная болезнь 2019» (COVID-19). С момента первого сообщения об этом заболевании в декабре 2019 г. в Ухани, Китай [2, 3], COVID-19 активно распространился по всему миру. ВОЗ объявила о пандемии 11 марта 2020 года.
COVID-19 имеет множество различных клинических проявлений, от бессимптомных случаев до легких и тяжелых заболеваний как с пневмонией, так и без нее [4]. У пациентов с аллергическими заболеваниями отчетливая дополнительная симптоматика не наблюдается; по-видимому, риск тяжелого течения заболевания для них не повышен. Дети с аллергией демонстрируют легкое течение заболевания, как и остальные дети [5]. Случаи COVID-19, при наличии ранее существовавшей ХОБЛ или осложненные вторичной бактериальной инфекцией, протекают тяжелее, что может быть связано с более сложным иммунопатогенезом.
Ответ на вопрос, оказывают ли системные кортикостероиды негативное влияние на течение COVID-19, все еще остается предметом обсуждения. Клинические данные не поддерживают идею лечения кортикостероидами при пневмонии, вызванной SARS-CoV-2 [6]. Более того, кортикостероидная терапия у пациентов с ближневосточным респираторным синдромом (MERS, Middle East Respiratory Syndrome) не была связана с разницей в смертности (учитывая изменяющиеся во времени дополнительные искажающие факторы), но была связана с задержкой клиренса РНК коронавируса, вызывающего MERS [7]. Согласно текущим рекомендациям ВОЗ [8], не следует использовать кортикостероиды при SARS-CoV-2-индуцированном повреждении легких или шоке, кроме как в условиях клинических испытаний. В то же время китайские врачи, находившиеся на передней линии, имели другую точку зрения на этот счет [9]. Учитывая неубедительность доказательств и неотложную клиническую потребность, врачи из Китайского Торакального Общества разработали согласованное экспертное положение по использованию кортикостероидов при SARS-CoV-2-пневмонии, позволяющее ограниченное использование низких доз кортикостероидов в течение короткого периода времени [10].
Что касается ингаляционных кортикостероидов при астме, группа Глобальной инициативы по астме (GINA, Global INitiative for Asthma) недавно заявила следующее (ginasthma.org): «Некоторые источники предполагают, что следует избегать «кортикостероидов» во время эпидемии SARS-CoV-2. Этот совет касается использования пероральных кортикостероидов при отсутствии четких показаний к их применению. Тем не менее, пациенты с астмой не должны прекращать прием назначенных им ингаляционных кортикостероидных препаратов (или пероральных кортикостероидов). Прекращение использования ингаляционных кортикостероидов часто приводит к потенциально опасному ухудшению течения астмы, а отказ от пероральных кортикостероидов во время тяжелых приступов астмы может иметь тяжелые последствия. Для лечения тяжелой астмы иногда может требоваться длительное использование пероральных кортикостероидов, и внезапное прекращение их приема может быть опасно. Всегда обсуждайте со своим доктором или медсестрой прекращение приема любых лекарств от астмы. Продолжайте принимать ваши ингаляционные препараты для контроля астмы, и, если течение астмы ухудшается, следуйте инструкциям в вашем плане лечения, чтобы понять, как менять прием ваших препаратов и когда обращаться за медицинской помощью».
Некоторые научные сообщества разработали рекомендации по аносмии и предложили использовать интраназальные кортикостероиды. Однако Главное управление здравоохранения Франции (Direction Générale de la Santé) считает противопоказанным их использование при аносмии и агезии без заложенности носа [11]. Также они расширили противопоказания на промывание носа физиологическим раствором, постольку оно может способствовать распространению вируса.
ARIA и EAACI последовали примеру Голландского общества оториноларингологов и разослали членам группы ARIA опросник по поводу рекомендаций при аллергическом рините и аносмии. По итогам опроса ARIA и EAACI сформировали общее положение.
ОпросникАнна Бедбрук инициировала процесс рассылки членам группы ARIA (509 членов, 84 страны) 3-x вопросов, предложенных Голландским обществом оториноларингологов, с предложением согласиться или не согласиться с этими положениями. Через 48 часов было получено 209 ответов из 61 страны (Таблица 1). Вопрос №3 слишком часто оставался без ответа и поэтому не может быть проанализирован; более того, научная база для вынесения подобных рекомендаций отсутствует.
закрыть менюРекомендацииСогласно имеющимся представлениям, пациенты с COVID-19 могут продолжать прием интраназальных кортикостероидов (в т.ч. спреи) в рекомендованной дозе при аллергическом рините.
Останавливать прием интраназальных кортикостероидов не рекомендуется. Подавление иммунной системы не было подтверждено, а усиление чихания после прекращения терапии может способствовать большему распространению коронавируса.
Эти рекомендации условны вследствие недостаточности данных, их следует регулярно пересматривать при получении новой информации.
Данные, полученные на отдельных наблюденияхВ детской больнице г.Ухань было зарегистрировано около 40 случаев заболевания COVID-19 у детей с аллергическим ринитом. Среди них примерно в трети случаев интраназальные кортикостероиды использовались регулярно, как во время болезни, так и до нее; в оставшихся двух третях кортикостероиды не использовались. Между этими двумя группами не было выявлено разницы в тяжести и прогнозе течения COVID-19, все они благополучно выздоровели (личное сообщение Ядун Гао и Хуэй Ду, данные не опубликованы).
Литература- Coronaviridae Study Group of the International Committee on Taxonomy of Viruses. The species
Severe acute respiratory syndrome-related coronavirus: classifying 2019-nCoV and naming it SARSCoV-2. Nat Microbiol. 2020; doi:10.1038/s41564-020-0695-z [Epub ahead of print]. - Zhu N, Zhang D, Wang W, Li X, Yang B, Song J, et al. A Novel Coronavirus from Patients with
Pneumonia in China, 2019. N Engl J Med. 2020;382(8):727-33. - Li Q, Guan X, Wu P, Wang X, Zhou L, Tong Y, et al. Early Transmission Dynamics in Wuhan, China, of Novel Coronavirus-Infected Pneumonia. N Engl J Med. 2020.
- Dong X, Cao YY, Lu XX, Zhang JJ, Du H, Yan YQ, et al. Eleven Faces of Coronavirus Disease 2019. Allergy. 2020.
- Zhang JJ, Dong X, Cao YY, Yuan YD, Yang YB, Yan YQ, et al. Clinical characteristics of 140 patients infected with SARS-CoV-2 in Wuhan, China. Allergy. 2020.
- Russell CD, Millar JE, Baillie JK. Clinical evidence does not support corticosteroid treatment for 2019-nCoV lung injury. Lancet. 2020;395(10223):473-5.
- Arabi YM, Mandourah Y, Al-Hameed F, Sindi AA, Almekhlafi GA, Hussein MA, et al. Corticosteroid Therapy for Critically Ill Patients with Middle East Respiratory Syndrome. Am J Respir Crit Care Med. 2018;197(6):757-67.
- Clinical management of severe acute respiratory infection when novel coronavirus (nCoV) infection is suspected. https://www.who.int/publications-detail/clinical-management-of-severe-acute-respiratory-infection-whennovelcoronavirus-(ncov)-infection-is-suspected. 2020.
- Shang L, Zhao J, Hu Y, Du R, Cao B. On the use of corticosteroids for 2019-nCoV pneumonia. Lancet. 2020;395(10225):683-4.
- Zhao JP, Hu Y, Du RH, Chen ZS, Jin Y, Zhou M, et al. [Expert consensus on the use of corticosteroid in patients with 2019-nCoV pneumonia]. Zhonghua Jie He He Hu Xi Za Zhi. 2020;43(3):183-4.
- 2020-INF-16 Information sur les formes cliniques atypiques de COVID-19. DGS. dgs-urgent@dgsurgentsantegouvfr. 2020.
Аллергический ринит: современная оценка медико-социальных аспектов и способов лечения интраназальные кортикостероиды в лечении ринитов | Царев
1. http: //www.worldallergy.org/wao-white-bookonallergy
2. Pols DHJ, Wartna JB, Moed H, van Alphen EI, Bohnen AM, Bindels PJ. Atopic dermatitis, asthma and allergic rhinitis in general practice and the open population: a systematic review. Scand J Prim Health Care, 2016, 34: 143-150.
3. Hill DA, Grundmeier RW, Ram G, Spergel JM. The epidemiologic characteristics of healthcare provider-diagnosed eczema, asthma, allergic rhinitis, and food allergy in children: retrospective cohort study. BMC Pediatr, 2016, 16: 133.
4. Kim JL, Brisman JAl, Aberg MA, Forslund HB, Winkvist A, Toren K. Trends in the prevalence of asthma, rhinitis and eczema in 15 year old adolescents over an 8 year period. Respir Med, 2014, 108: 701-708.
5. Wood RA, Sicherer SH, Vickery BP, Jones SM, Liu AH, Fleischer DM еt al. The natural history of milk allergy in an observational cohort. J Allergy Clin Immunol, 2013, 131: 805-812.
6. Hatzler L, Panetta V, Lau S, Wagner P, Bergmann RL, Illi S et al. Molecular spreading and predictive value of preclinical IgE response to Phleum pratense in children with hay fever. J Allergy Clin Immunol, 2012, 130: 894-901.
7. Bousquet J, Khaltaev N, Cruz AA, Denburg J, Fokkens WJ, Togias A еt al. Allergic Rhinitis and its Impact on Asthma (ARIA) 2008 update (in collaboration with the World Health Organiza tion, GA(2)LEN and AllerGen). Allergy, 2008, 63: 8-160.
8. Богова А.В., Ильина Н.И., Лусс Л.В. Тенденции в изучении эпидемиологии аллергических заболеваний в России за последние 10 лет. Российский аллергологический журнал, 2008, 6: 3-14.
9. Lindner M. When allergies attack. Fortune, 2010, 162(2): 14.
10. Cardell L-O, Olsson P, Andersson M, Welin KO, Svensson J, Tennvall GR et al. TOTALL: high cost of allergic rhinitis – a national Swedish population-based questionnaire study. NPJ Prim Care Respir Med, 2016, 26: 15082.
11. Linneberg A, Dam Petersen K, Hahn-Pedersen J, Hammerby E, Serup-Hansen N, Boxall N. Burden of allergic respiratory disease: a systematic review. Clin Mol Allergy, 2016, 14: 12.
12. Canonica GW, Mullol J, Pradalier A, Didier A. Patient perceptions of allergic rhinitis and quality of life: findings from a survey conducted in Europe and the United States. World Allergy Organ J, 2008, 1: 138-144.
13. Meltzer EO, Gross GN, Katial R, Storms, WW. Allergic rhinitis substantially impacts patient quality of life: findings from the Nasal Allergy Survey Assessing Limitations. J Fam Pract, 2012, 61: 5-10.
14. Brożek JL, Bousquet J, Agache I, Agarwal A, Bachert C, Bosnic-Anticevich S et al. Allergic Rhinitis and its Impact on Asthma (ARIA) guidelines – 2016 revision. J Allergy Clin Immunol, 2017, 140: 950-958.
15. Poddighe D, Gelardi M, Licari A, del Giudice M M, Marseglia GL. Non-allergic rhinitis in children: Epidemiological aspects, pathological features, diagnostic methodology and clinical management. World J Methodol, 2016, 6: 200–213.
16. Vandenplas O, Vinnikov D, Blanc PD, Agache I, Bachert C, Bewick M et al. Impact of Rhinitis on Work Productivity: A Systematic Review. J Allergy Clin Immunol Pract, 2017, 6: 1274-1286.
17. Leynaert B, Neukirch C, Liard R, Bousquet J, Neukirch F. Quality of life in allergic rhinitis and asthma. A population-based study of young adults. Am J Respir Crit Care Med, 2000, 162: 1391-1396.
18. Schatz M, Zeiger RS. Telephone-based environmental control interventions in asthmatic patients: what are patients willing to do? Ann Allergy Asthma Immunol, 2012, 109: 99-102.
19. Braido F, Arcadipane F, Marugo F, Hayashi M, Pawankar R. Allergic rhinitis: current options and future perspectives. Curr Opin Allergy Clin Immunol, 2014, 2: 168-176.
20. Suzaki H. Action mechanisms of glucocorticoids on rhinosinusitis. Asian Rhinology Journal, 2013, 1: 3-13.
21. Johnson M. Development of fluticasone propionate and comparison with other inhaled corticosteroids. J Allergy Clin Immunol, 1998, 101: 434-439.
22. Smith CL, Kreutner W. In vitro glucocorticoid receptor binding and transcriptional activation by topically active glucocorticoids. Arzneimittelforschung, 1998, 48: 956-960.
23. Demoly P. Safety of intranasal corticosteroids in acute rhinosinusitis. Am J Otolaryngol, 2008, 29: 403-413.
24. Canonica GW, Compalati E. Minimal persistent inflammation in allergic rhinitis: implications for current treatment strategies. Clin Exp Immunol, 2009, 158(3): 260-271.
25. Kaliner MA. Nonallergic rhinopathy (formerly known as vasomotor rhinitis). Immunol Allergy Clin North Am, 2011, 31: 441-455.
26. Kern R. Allergy: a constant factor in the etiology of so-called mucous nasal polyps. J Allergy, 1993, 4: 483.
27. Fokkens WJ, Lund VJ, Mullol J, Bachert C, Alobid I, Baroody F et al. European position paper on rhinosinusitis and nasal polyps 2012. Rhinol. Suppl, 2012, 50: 1-298.
28. Suzaki H. Action mechanisms of glucocorticoids on rhinosinusitis. Asian Rhinology Journal, 2013, 1: 3-13.
29. Potter PC, Pawankar R. Indications, efficacy, and safety of intranasal corticosteriods in rhinosinusitis. World Allergy Organ J, 2012, 5: 14-17.
30. Ahmadiafshar A, Farjd HR, Moezzi F, Mousavinasab N. Nasal polyposis in patients with asthma and allergic rhinitis. J Laryngol Otol, 2012, 126: 780-783.
31. Польнер С.А., Козаренко Е.А., Шевцов Е.А. Целесообразность и место риносептопластики в комплексном лечении аллергического ринита и бронхиальной астмы. Цитокины и воспаление, 2012, 12(3): 130-132.
32. Canonica GW, Bousquet J, Mullol J, Scadding GK, Virchow JC. A survey of the burden of allergic rhinitis in Europe. Allergy, 2007, 62: 17–25.
33. Hellings PW, Klimek L, Cingi C, Agache I, Akdis C, Bachert C et al. Non-allergic rhinitis: Position paper of the European Academy of Allergy and Clinical Immunology. Allergy, 2017, 72: 1657-1665.
34. Saco TV, Pepper A, Casale TB. Uses of biologics in allergic diseases: What to choose and when. Ann Allergy Asthma Immunol, 2018, 120: 357-366.
Что мы знаем о безопасности интраназальных кортикостероидов? Текст научной статьи по специальности «Фундаментальная медицина»
В помощь врачу
122
В.В. Шиленкова
Ярославская государственная медицинская академия
Что мы знаем о безопасности интраназальных кортикостероидов?
Контактная информация:
Шиленкова Виктория Викторовна, доктор медицинских наук, профессор кафедры оториноларингологии ГБОУ «Ярославская государственная медицинская академия» Минздравсоцразвития РФ
Адрес: 150000, Россия, Ярославль, ул. Революционная, д. 5, тел.: (4852) 30-56-41, e-mail: [email protected] Статья поступила: 13.03.2012 г., принята к печати: 12.04.2012 г.
Анализ 62 литературных источников и клинических исследований, основанных на принципах доказательной медицины, позволил авторам статьи заключить, что современные интраназальные глюкокортикостероиды обладают хорошим профилем безопасности и могут широко использоваться для лечения аллергических и воспалительных заболеваний носа и околоносовых пазух как у взрослых, так и у детей.ег с соавт., проанализировав 54 рандомизированных, плацебоконтролируемых исследования, в которых участвовало более 14 тыс. взрослых пациентов и 1580 детей, страдающих АР, пришли к выводу, что интраназальные глюкокортикостероиды оказывают более выраженный эффект в отношении назальных симптомов ринита по сравнению с оральными и интра-назальными антигистаминными препаратами [15]. Кроме того, в последнее время ИнГКС позиционируют не только как препараты, эффективно справляющиеся с назальными симптомами, но и как средства для
устранения глазных симптомов аллергического ринита. Во многих работах отмечается, что это класс-эффект ИнГКС [16, 17].
В настоящее время топические стероиды находят все большую популярность в практике педиатра, причем не только в лечении АР, но и распространенных ассоциированных с ним состояний. Имеются, например, исследования, которые демонстрируют эффективность ИнГКС при гипертрофии глоточной миндалины [18-20], секреторном отите на фоне аллергического ринита [21].
Первым топическим (назальным) стероидом был беклометазона дипропионат, прочно вошедший в практику лечения аллергического ринита в 70-х гг. прошлого века. В настоящее время в России зарегистрировано
5 интраназальных глюкокортикостероидов: бекломета-зона дипропионат, будесонид, флутиказона дипропионат, флутиказона фуроат и мометазона фуроат. Их противовоспалительная активность зависит от ряда факторов, в частности от степени сродства к глюкокортикоидному рецептору; липофильности, обеспечивающей лучшее преодоление мембраны клетки; вязкости; комплаентно-сти пациента; удобства дозирующего устройства и способности больного правильно им пользоваться. Вопрос
V.V. Shilenkova
State Budget Educational Institution of Higher Professional Education «Yaroslavl State Medical Academy of the Ministry of Health and Social Development» of Russia Federation
What do we know about the safety of nasal corticosteroids?
Analysis of articles and clinical studies conducted in accordance with the principles of evidence-based medicine allows making a conclusion that new nasal corticosteroids have a favorable of safety profile and they can be widely used for the management of allergy and inflammatory diseases of nose and paranasal sinuses in adults and childhood.
Key words: intranasal corticosteroids, safety, efficacy.
о преимуществах того или иного ИнГКС в купировании воспалительных процессов в полости носа и околоносо-вых пазухах до сих пор остается весьма дискутабельным [22-24].
Помимо указанных выше различий, топические формы ГКС имеют разный уровень биодоступности, от которого непосредственно зависит наличие побочных эффектов. Самая высокая биодоступность у беклометазона дипропионата — 44%. На втором месте — будесонид (34%). Наиболее низкой биодоступностью характеризуются современные ИнГКС: флутиказона пропионат (< 2%), флутиказона фуроат (< 0,5%) и мометазона фуроат (< 0,1%). Несмотря на долгую историю применения топических стероидов, совершенствование структур молекул, направленное на повышение их противовоспалительной активности, исключение возможности неблагоприятного воздействия на гипоталамическую систему человека, внушительный опыт использования на практике, назначение их по-прежнему вызывает опасение как у пациентов (и родителей), так и у многих врачей.
В 2010 г. в официальном журнале Европейского общества оториноларингологов «European archives of otorhinolaryngology» была опубликована статья C. Cingi и М. Songu (Турция) «Перспективы назальных стероидов: знания и отношения», в которой авторы заметили, что, несмотря на широкое применение ИнГКС в клинической практике, частота их назначения растет непропорционально числу случаев аллергического ринита [25]. При анкетировании врачей и их пациентов, страдающих АР, авторы установили, что большинство опрошенных оказались недостаточно осведомлены о безопасности ИнГКС. Поэтому озабоченность по поводу возможных системных эффектов интраназальных глюкокортикостероидов привела к позиционированию их как препаратов второй линии выбора. Причем это в одинаковой мере касалось как больных, так и врачей. Хотя и те и другие признавали ведущую роль ИнГКС в терапии аллергического ринита, тем не менее, многие предпочитали использовать более безопасные, по их мнению, лекарственные средства.
Нами проанализировано более 50 литературных источников, которые содержат те или иные сведения об использовании ИнГКС, большинство из них свидетельствуют о хорошей переносимости топических стероидов [23, 26-29]. Еще в 1977 г. H. M. Brown с соавт. представили пятилетний опыт длительного и многократного назначения беклометазона дипропионата у 315 больных с АР [26]. Авторы подсчитали, что в общей сложности терапия составила 534 пациенто-лет без каких-либо доказательств побочных эффектов. Через 20 лет R. J. Davies и H. S. Nelson обобщили результаты 20 клинических исследований эффективности мометазона фуроа-та в сравнении с другими ИнГКС [23]. Исследования проводились в различных странах мира, в них участвовало более 6000 пациентов с сезонной и круглогодичной формой аллергического ринита. Доказана хорошая переносимость мометазона фуроата в рекомендуемых дозировках, в т. ч. и при длительном применении, что крайне важно, поскольку во многих случаях больным требуется именно длительное назначение этой группы препаратов. Интересно, что на таком репрезентативном клиническом материале не было зафиксировано ни одного случая развития атрофических процессов в полости носа. Напротив, продемонстрировано восстановление слизистой оболочки до нормальной структуры.
В настоящее время бесспорным является факт отсутствия реального воздействия большинства ИнГКС на гипоталамо-гипофизарно-надпочечниковую систему человека [30, 31]. Причем это в равной мере касается не только современных лекарственных средств, таких как флутиказона пропионат, мометазона фуроат и флутиказона фуроат, но и так называемых «старых» топических стероидов, за исключением беклометазона. Результаты многочисленных исследований, проводившихся у детей, свидетельствуют, что применение ИнГКС в терапевтических дозах не влияет на рост ребенка. Достаточно упомянуть работы S. M. Gawchik и C. L. Saccar, а также S. Weinstein с соавт., посвященные ретроспективному анализу длительного, в течение 6-12 мес, использования триамцинолона ацетонида у детей младшего возраста [32, 33]. Авторами не было зафиксировано замедления роста детей, в равной степени как и снижения прибавки в весе. Не отмечено и подавления функции коры надпочечников, что подтверждено результатами измерения уровня кортизола в сыворотке крови.
Подобные исследования были выполнены в отношении других ИнГКС [4, 6, 24, 28, 34-38]. Доказано отсутствие влияния будесонида, мометазона фуроата, флутиказона пропионата и флутиказона фуроата не только на содержание кортизола в крови и моче, но и на уровень остеокальцина — информативного маркера формирования кости [16, 31, 39]. Лишь беклометазона дипропионат можно считать потенциально опасным для детского возраста. D. P. Skoner с соавт. на примере использования этого препарата у детей в возрасте 6-9 лет в течение 52 нед показали, что он достоверно замедляет рост ребенка [40]. Поэтому нужно регулярно следить за динамикой роста детей, длительно получавших ИнГКС, вне зависимости от того, какой препарат был выбран для терапии [41]. Соответствующее предупреждение вносят в инструкции препаратов, относящихся к классу ИнГКС.
М. Zitt с соавт. на примере мометазона фуроата попытались объяснить системную безопасность стероида изначально низкой растворимостью препарата в воде [42]. По мнению авторов, уникальное свойство мометазона фуроата позволяет лишь малой части действующего вещества проникнуть через слизистую оболочку полости носа в кровоток. По-видимому, именно этот факт явился пусковым моментом в рекомендации добавить ИнГКС в терапию первой линии АР у беременных в случаях тяжелого течения заболевания. Терапия триамциноло-ном, флутиказоном и мометазоном оказалась эффективной в отношении улучшения симптомов аллергического ринита и не вызвала развития аномалий у родившихся младенцев [43]. Хотя в отношении большинства топических стероидов значимые научные исследования по изучению возможного тератогенного эффекта отсутствуют. Важно обратить внимание врачей на требования регулирующих инстанций разных стран к составлению инструкций по применению. Если какой-либо побочный эффект был зарегистрирован для одного представителя конкретного класса препаратов, то регулирующие инстанции обычно требуют включать предупреждение о возможности этого побочного эффекта в инструкции всех препаратов данного класса, даже если при применении других препаратов этот побочный эффект никогда не наблюдался.
Стандартным требованием к инструкции является также упоминание об отсутствии качественных клинических исследований или достоверных данных о применении
123
ВОПРОСЫ СОВРЕМЕННОЙ ПЕДИАТРИИ /2012/ ТОМ 11/ № 2
В помощь врачу
124
препарата у беременных и о действии на развивающийся плод. Естественно, что клинические исследования препаратов, не предназначенных для применения исключительно у беременных, не проводятся у этой категории лиц по этическим соображениям. Поэтому данные о терато-генности, репродуктивной токсичности и возможности применения у беременных ограничиваются исследованиями in vitro у животных, данными о женщинах, у которых во время клинического исследования случилась незапланированная беременность, и данными, полученными в результате отслеживания случаев беременности при применении препаратов в реальной клинической практике.
Частота возможных побочных эффектов в реальной клинической практике, а также в условиях применения на фармацевтическом рынке (так называемый опыт пост-маркетингового применения) определяется следующим образом: возникновение побочных эффектов с частотой
& 1/10 (т. е. & 10%) классифицируется как «очень часто»; с частотой & 1/100, но < 1/10 (т. е. & 1%, но < 10%) — как «часто»; с частотой & 1/1000, но < 1/100 (т. е. & 0,1%, но < 1%) — как «нечасто»; & 1/10000, но < 1/1000 (т. е. & 0,01%, но < 0,1%) — как «редко», менее 1/10000 (< 0,01%) — «очень редко». Указываются также единичные случаи побочных эффектов, когда-либо зарегистрированные во время применения препарата. Важно помнить, что развитие во время применения препарата побочных эффектов не всегда отражает прямую причинную связь. Необходимо обращать внимание на сравнение частоты побочных эффектов при применении препарата с их частотой при применении плацебо, в качестве которого при изучении ИнГКС обычно используется физиологический раствор. При применении плацебо в таком же ингаляционном устройстве также возможны побочные эффекты за счет механического воздействия носика ингалятора и некоторого раздражающего действия вводимого неактивного раствора.
Как и при назначении практически любого лекарственного средства, побочные эффекты от применения ИнГКС все же возможны. Считается, что они возникают в 5-10% случаев и одинаковы для всех представителей этой группы препаратов [44]. Но частота их между разными препаратами может значительно варьировать. В большинстве случаев побочные эффекты носят характер нежелательных явлений, свойственных не только ИнГКС, но и другим лекарственным препаратам, применяемым интраназально. Наиболее распространенными являются чихание, кашель, зуд, жжение и сухость в полости носа, ощущение дискомфорта в глотке, головная боль [33, 45-47]. В большинстве случаев эти явления обусловлены индивидуальными особенностями пациента, слабо выражены и не требуют отмены препарата. Частота побочных эффектов может также зависеть от ингаляционного устройства (возможность механического травмирования слизистой оболочки) и неактивных составляющих препарата (эксципиентов). Предварительная беседа с больным или родителями о возможности возникновения неприятных ощущений в полости носа и глотке после ингаляции топического стероида позволяет в большинстве случаев избежать негативной реакции на прием препарата.
Среди осложнений ИнГКС в литературе упоминаются ларингит, носовые кровотечения, кандидоз полости носа [6, 48]. Однако их частота во многих случаях соизмерима с частотой этих нежелательных явлений при применении плацебо, а по данным некоторых исследований,
даже ниже, чем плацебо. Например, С. Е. Baena-Cagnani и Р. Patel, наблюдая за детьми в возрасте 3-11 лет, страдающими круглогодичным аллергическим ринитом, установили, что по истечении 4 нед ежедневного применения мометазона фуроата носовое кровотечение имело место в 4% случаев, в то время как после приема плацебо — у 5% детей [49].
До настоящего времени возникают вопросы о действии ИнГКС, содержащих консервант бензалкония хлорид, на мерцательный эпителий [50]. Действительно, в нескольких исследованиях in vitro, т. е. в культурах клеток слизистой оболочки носа животных и человека, было показано некоторое уменьшение частоты биения ресничек при нанесении на клетки растворов препаратов, содержащих бензалкония хлорид (мометазона фуроат, флутиказона пропионат) [51, 52]. Экспериментальные данные важны для понимания потенциально возможных эффектов лекарственных средств. Однако следует учесть, что описанные эксперименты in vitro проводились в культуре клеток, т. е. в ситуации, когда клетки лишены такого важнейшего защитного фактора как слизь, и невозможно учесть действия других факторов — анатомических особенностей, действия различных медиаторов и т. д. В то же время в длительных исследованиях in vivo не было выявлено отрицательного воздействия ИнГКС на реснитчатый эпителий, поэтому совершенно обоснованно можно говорить об отсутствии отрицательного влияния ИнГКС при лечении этими препаратами. В частности, Е. Minshall с соавт. сравнили гистологическую картину слизистой оболочки полости носа до и после годичного применения мометазона фуроата у взрослых [53]. Анализ биоптатов показал отсутствие каких-либо атрофических изменений эпителия. Авторами доказано, что даже длительное использование препарата не вызывает формирования в слизистой оболочке воспалительных процессов. Более того, мометазона фуроат способствовал восстановлению целостности эпителиального покрова полости носа и редукции клеточных инфильтратов, в т. ч. и эозинофильных.
Одним из вызывающих наибольшее опасение у врача и пациента побочных эффектов ИнГКС является перфорация носовой перегородки [33, 54]. Механизм ее развития неизвестен и, к сожалению, это осложнение недостаточно описано в литературе. В связи с этим следует отметить статью шведских ученых A. Cervin и M. Andersson, которые, обследовав 32 пациента с перфорацией носовой перегородки, обратившихся в клинику в течение 5 лет, пришли к выводу, что только в 11 случаях заболевание можно было связать с терапией стероидами [55]. Преимущественно это были женщины (10 случаев из 11) молодого возраста (19-49 лет). По данным авторов, риск развития перфорации возрастает при длительном приеме ИнГКС, наличии деформации носовой перегородки, одновременном использовании вазоконстрикторов, а также при отсутствии контроля врача за пациентом. Большинство больных на фоне приема ИнГКС испытывали выраженную сухость в носу, у них наблюдались эпизоды носовых кровотечений. Однако они продолжали использовать препарат.
По мнению разных авторов, причиной перфораций носовой перегородки в большинстве случаев служит неправильное применение ингаляционного устройства: направление струи препарата не в сторону латеральной стенки полости носа, а на носовую перегородку. Избежать осложнения позволяет предварительное
обучение пациента или родителей технике нанесения спрея на слизистую оболочку полости носа и предпочтительное применение водных растворов топических стероидов [56].
Интересными также представляются работы, посвященные изучению влияния топических стероидов на орган зрения, в частности потенцирование развития глаукомы и катаракты. Приведем лишь некоторые из этих трудов. В 2001 г. J. Dibildox описал результаты длительного, в течение года, применения мометазона фуроата у детей с персистирующим АР и с достоверной точностью доказал отсутствие изменений на сетчатке глаза и влияния препарата на внутриглазное давление [57]. Впоследствии к тем же выводам пришел P. H. Ratner c соавт. в подобном исследовании [58]. Аналогичные данные были получены в отношении других, не менее популярных среди оториноларингологов топических стероидов — флутиказона пропионата и флутиказона фуроата [16, 59]. Таким образом, доказано, что современные ИнГКС не провоцируют развитие катаракты и глаукомы.
Часто пациентов интересует влияние лекарственных препаратов на общее состояние организма. В 1993 г. L. Agertoft соавт. доказали, что применение ИнГКС существенно не влияет на жизненно важные функции человека, о чем свидетельствуют данные электрокардиограммы и лабораторных исследований, выполненных у пациентов, длительно использовавших мометазона фуроат [37].
С недавнего времени Европейским консенсусом по риносинуситам и назальным полипам (European Position Paper on Rhinosinusitis and Nasal Polyps, EPOS, 2007) интраназальные глюкокортикостероиды рекомендованы как препараты выбора для лечения острого риносинусита в качестве адъювантной терапии с системными антибиотиками (в России — с 12-летнего возраста). При легких формах заболевания, без признаков тяжелой бактериальной инфекции, топические стероиды (мометазона фуроат) могут применяться и в виде монотерапии, с большим успехом заменяя антибиотики [13]. Неизбежным является вопрос о возможной провокации развития инфекции в околоносовых пазухах (ОНП) в ответ на применение ИнГКС. Однако имеется достаточное число работ, указывающих на отсутствие каких-либо доказа-
тельств «вредного» воздействия топических стероидов, использующихся в терапевтических дозах, на микрофлору слизистых оболочек.ег с соавт. [13, 58]. В значительном (981 пациент с острым риноси-нуситом) рандомизированном двойном слепом контролируемом исследовании авторами доказано, что моме-тазона фуроат даже в удвоенной дозировке не вызывает суперинфекции и не провоцирует обострения воспалительного процесса в ОНП. Более того, в работе канадских ученых (М. Desrosiers с соавт.) показано, что мометазона фуроат способствует снижению бактериальной колонизации слизистой оболочки у больных, перенесших хирургические вмешательства на ОНП, что, по-видимому, связано с уменьшением отека и улучшением дренажной функции носа [60].
ЗАКЛЮЧЕНИЕ
ИнГКС широко используются как у взрослых, так и у детей для лечения аллергического ринита и других заболеваний полости носа и околоносовых пазух. Широкое применение этого класса препаратов основано на сочетании их эффективности, хорошей переносимости и безопасности. При необходимости долгосрочного применения ИнГКС важным для врача становится обучение пациентов и/или родителей правильной технике ингаляций, а также обсуждение потенциальных побочных эффектов препаратов, разъяснение отсутствия действия ИнГКС на гипоталамо-гипофизарно-надпочечниковую систему, органы зрения и другие важные органы и функции организма, а также разъяснение безопасности использования ИнГКС одновременно с ингаляциями у больных бронхиальной астмой и преимуществ одновременного назначения этих препаратов для достижения контроля астмы. Каждый пациент должен знать о возможных побочных эффектах интраназальных глюкокортикостероидов. Рассматривать каждую клиническую ситуацию всегда необходимо индивидуально. В случае применения ИнГКС непосредственная польза от топического стероида в большинстве случаев превышает потенциальные риски, а сама терапия позволяет избежать возможных осложнений и последствий АР и риносинуситов у детей.
СПИСОК ЛИТЕРАТУРЫ
1. Гущин И. С. Аллергическое воспаление и его фармакологический контроль. М.: Фармарус принт. 1998. 252 c.
2. Гущин И. С., Ильина Н. И., Польнер С. А. Аллергический ринит: методическое пособие. Москва. 2002. 68 с.
3. Карпова Е. П. Лечение аллергического ринита у детей. М.: ГЭОТАР-Медиа. 2007. 192 с.
4. Stjarne P. et al. A randomized controlled trial of mometasone furoate nasal spray for the treatment of nasal polyposis. Arch. Otolaryngol. Head Neck Surg. 2006; 132 (2): 179-185.
5. Benninger M. S., Ahmad N., Marple B. F. The safety of intranasal steroids. Otolaryngol. Head Neck Surg. 2003; 129: 739-750.
6. Demoly P. Safety of intranasal corticosteroids in acute rhinosinusitis. Am. J. Otolaryngol. 2008; 29 (6): 403-413.
7. Small C. B. Efficacy and safety of mometasone furoate nasal spray in nasal polyposis. J. Allergy Clin. Immunol. 2005; 116 (6): 1275-1281.
8. Penagos M. et al. Efficacy of mometasone furoate nasal spray in the treatment of allergic rhinitis. Meta-analysis of randomized, double-blind, placebo-controlled, clinical trials. Allergy. 2008; 63 (10): 1280-1291.
9. Given J. T. Fluticasone furoate nasal spray is effective and well tolerated for perennial allergic rhinitis in adolescents and adults. Am. J. Rhinol. Allergy. 2010; 24 (6): 444-450.
10. Klossek J. M. Efficacy and safety of mometasone furoate nasal spray in the treatment of sinusitis or acute rhinosinusitis. Rev. Laryngol. Otol. Rhinol. 2007; 128 (3): 187-192.
11. Jankowski R. et al. Long-term study of fluticasone propionate aqueous nasal spray in acute and maintenance therapy of nasal polyposis. Allergy. 2009; 64 (6): 944-950.
12. Mabry R. L. Intranasal steroid injection during pregnancy. South Med. J. 1980; 73: 1176-1179.
13. Meltzer E. O., Bachert C., Staudinger H. Treating acute rhino-sinusitis: comparing efficacy and safety of mometasone furoate nasal spray, amoxicillin, and placebo. Allergy Clin. Immunol. 2005; 116 (6): 1289-1295.
14. Anolik R. Mometasone furoate improves nasal and ocular symptoms of seasonal allergic rhinitis in adolescents. Allergy Asthma Proc. 2009; 30 (4): 406-412.
15. Benninger M. et al. Evaluating approved medications to treat allergic rhinitis in the United States: an evidence-based review of
125
ВОПРОСЫ СОВРЕМЕННОЙ ПЕДИАТРИИ /2012/ ТОМ 11/ № 2
В помощь врачу
126
efficacy for nasal symptoms by class. Ann. Allergy Asthma Immunol. 2010; 104 (1): 13-29.
16. Rosenblut A. Long-term safety of fluticasone furoate nasal spray in adults and adolescents with perennial allergic rhinitis. Allergy. 2007; 62 (9): 1071-1077.
17. Martin B. G. Optimal dose selection of fluticasone furoate nasal spray for the treatment of seasonal allergic rhinitis in adults and adolescents. Allergy Asthma Proc. 2007; 28: 216-225.
18. Гаращенко Т. И. Лечение аллергических ринитов у детей. Вестник оториноларингологии. 2005; 3: 66-69.
19. Berlucchi M., Tomenzoli D. Intranasal steroid therapy in inflammatory nasal-sinus pathology in pediatric age. Minerva Pediatr. 2009; 61 (3): 323-331.
20. Demain J. C., Goetz D. W. Pediatric adenoidal hypertrophy and nasal airways obstruction: reduction with aqueous nasal beclomethasone. Pediatrics. 1995; 95 (3): 355-364.
21. Cengel S., Akyol M. U. The role of nasal steroids in treatment of children with otitis media with effusion and/or adenoid hypertrophy. Int. J. Pediatr. Otorhinolaryngol. 2006; 70: 639-645.
22. Small P. et al. A comparison of triamcinolone acetonide nasal aerosol spray and fluticasone propionate aqueous solution spray in the treatment of spring allergic rhinitis. J. Allergy Clin. Immunol. 1997; 100 (5): 592-595.
23. Davies R. J., Nelson H. S. Once-daily mometasone furoate nasal spray: efficacy and safety of a new intranasal glucocorticoid for allergic rhinitis. Clin. Ther. 1997; 19 (1): 27-38.
24. Herman H. Once-daily administration of intranasal corticosteroids for allergic rhinitis: a comparative review of efficacy, safety, patient preference, and cost. Am. J. Rhinol. 2007; 21: 70-79.
25. Cingi C., Songu M. Nasal steroid perspective: knowledge and attitudes. Eur. Arch. Otorhinolaryngol. 2010; 267 (5): 725-730.
26. Brown H. M., Storey G., Jackson F. A. Beclomethasone dipropionate aerosol in treatment of perennial and seasonal rhinitis: a review of five years’ experience. Br. J. Clin. Pharmacol. 1977; 4 (Suppl. 3): 283-286.
27. Jacobs R. et al. Effectiveness of fluticasone furoate 110 microg once daily in the treatment of nasal and ocular symptoms of seasonal allergic rhinitis in adults and adolescents sensitized to mountain cedar pollen. Curr. Med. Res. Opin. 2009; 25 (6): 1393-1401.
28. Toogood J. H. Efficacy of safety of concurrent use of intranasal flunisolide and oral beclomethasone aerosols in treatment of asthmatics with rhinitis. Clin. Allergy. 1982; 12 (1): 95-105.
29. Luskin A. T. Is there a role for aerosol nasal sprays in the treatment of allergic rhinitis: a white paper? Allergy Asthma Proc. 2011; 32 (2): 168-177.
30. Wilson A. M. Effects of intranasal corticosteroids on adrenal, bone, and blood markers of systemic activity in allergic rhinitis. J. Allergy Clin. Immunol. 1998; 102: 598-604.
31. Zhuang H., Wen W. Clinical observation on intranasal bude-sonide in chronic nonallergic rhinitis. Lin. Chuang Er. Bi. Yan. Hou. Ke. Za. Zhi. 2006; 20 (2): 67-69.
32. Weinstein S. et al. Efficacy and safety of triamcinolone acetonide aqueous nasal spray in children aged 2 to 5 years with perennial allergic rhinitis: a randomized, double-blind, placebo-controlled study with an open-label extension. Ann. Allergy Asthma Immunol. 2009; 102 (4): 339-347.
33. Gawchik S. M., Saccar C. L. A risk-benefit assessment of intranasal triamcinolone acetonide in allergic rhinitis. Drug Saf. 2000; 23 (4): 309-322.
34. Schenkel E. J. Absence of growth retardation in children with perennial allergic rhinitis after one year of treatment with mometasone furoate aqueous nasal spray. Pediatrics. 2000; 105: 22.
35. Pitsios C. Efficacy and safety of mometasone furoate vs nedocromil sodium as prophylactic treatment for moderate/severe seasonal allergic rhinitis. Ann. Allergy Asthma Immunol. 2006; 96 (5): 673-678.
36. Tripathy I. et al. HPA axis safety of fluticasone furoate nasal spray once daily in children with perennial allergic rhinitis. Pediatr. Allergy Immunol. 2009; 20 (3): 287-294.
37. Agertoft L. Nasal powder administration of budesonide for seasonal rhinitis in children and adolescents. Ped. Allergy Immunol. 1993; 4: 152-156.
38. Vaidyanathan S., Barnes M., Lipworth B. J. Comparative safety and efficacy of 2 formulations of fluticasone aqueous nasal spray in persistent allergic rhinitis. Ann. Allergy Asthma Immunol. 2009; 102 (1): 76-83.
39. Galant S. P Lack of effect of fluticasone propionate aqueous nasal spray on the hypothalamic-pituitary-adrenal axis in 2- and 3-year-old patients. Pediatrics. 2003; 112 (1): 96-100.
40. Skoner D. A. et al. Detection of growth suppression in children during treatment with intranasal beclomethasone dipropionate. Pediatrics. 2000; 105: 23.
41. Baena-Cagnani C. E. Safety and tolerability of treatments for allergic rhinitis in children. Drug Saf. 2004; 27 (12): 883-898.
42. Zitt M., Kosoglou T., Hubbell J. Mometasone furoate nasal spray: a review of safety and systemic effects. Drug Saf. 2007; 30 (4): 317-326.
43. Keles N. Treatment of allergic rhinitis during pregnancy. Am. J. Rhinol. 2004; 18 (1): 23-28.
44. Suissa S. et al. Inhaled and nasal corticosteroids use and the risk of fracture. Am. J. Respir. Crit. Care Med. 2004; 169: 83-88.
45. Clissold S. P., Heel R. C. Budesonide. A preliminary review of its pharmacodynamic properties and therapeutic efficacy in asthma and rhinitis. Drugs. 1984; 28 (6): 485-518.
46. Mosges R. et al. Efficacy and safety of Mometasone Furoate nasal spray in the treatment of chronic rhinosinusitis. Adv. Ther. 2011; 28 (3): 238-249.
47. Bekowitz R. B. Mometasone furoate nasal spray is rapidly effective in the treatment of seasonal allergic rhinitis in an outdoor (park), acute exposure setting. Allergy and Asthma Proc. 1999; 20: 167-172.
48. Berlucchi M. Pedruzzi B. Intranasal Mometasone Furoate for treatment of allergic rhinitis. Therapeutics. 2010; 2: 761-769.
49. Baena-Cagnani C. E., Patel P. Efficacy and long-term safety of mometasone furoate nasal spray in children with perennial allergic rhinitis. Curr. Med. Res. Opin. 2010; 26 (9): 2047-2055.
50. Jacobs R. et al. Weather/temperature-sensitive vasomotor rhinitis may be refractory to intranasal corticosteroid treatment. Allergy Asthma Proc. 2009; 30 (2): 120-127.
51. Berg O., Lie K., Steinsvag S. The effect of decongestive nosedrops on human respiratory mucosa in vitro. Laryngoscope. 1994; 104: 1153-1158.
52. Hofmann T., Wolf G., Koidl B. In vitro Untersuchungen uber die Wirkung vasokonstriktorischer Nasentropfen auf das Flimmere-pithel der menschlichen Nasenschleimhaut. Laryngol. Rhinol. Otol. 1995; 74: 564-567.
53. Minshall E. et al. Assessment by nasal biopsy of long-term of mometasone furoate aqueous nasal spray (Nasonex) in the treatment of perennial rhinitis. Otolaryngol. Head Neck Surg. 1998; 118: 648-654.
54. Devillier P Pharmacology of glucocorticoids and ENT pathology. Presse Med. 2001; 30: 59-69.
55. Cervin A., Andersson M. Intranasal steroids and septum perforation — an overlooked complication? A description of the course of events and a discussion of the causes. Rhinology. 1998; 36: 128-132.
56. Курбачева О. М., Ильина Н. И. Лечение аллергического ринита: когда, как и зачем? Рос. аллергол. журнал. 2006; 2: 71-80.
57. Dibildox J. Safety and efficacy of mometasone furoate aqueous nasal spray in children with allergic rhinitis: results of recent clinical trials. J. Allergy Clin. Immunol. 2001; 108: 54-58.
58. Ratner P H., Meltzer E. O., Teper A. Mometasone furoate nasal spray is safe and effective for 1-year treatment of children with perennial allergic rhinitis. Int. J. Pediatr. Otorhinolaryngol. 2009; 73 (5): 651-657.
59. Schafer T. et al. Therapeutic Index (TIX) for intranasal corticosteroids in the treatment of allergic rhinitis. Rhinology. 2011; 49: 1-9.
60. Desrosiers M. et al. Intranasal corticosteroid use is associated with lower rates of bacterial recovery in chronic rhinosinusitis. Otolaryngol. Head Neck Surg. 2007; 136 (4): 605-609.
Интраназальные кортикостероиды: понимание безрецептурных вариантов
Приблизительно от 30 до 60 миллионов человек в США страдают аллергическим ринитом (АР), в том числе от 10 до 30% взрослых и до 40% детей. 1 Симптомы АР могут включать заложенность носа, ринорею, чихание и зуд в носу. Эти симптомы могут возникать в ответ на внутренние или наружные аллергены, либо на то и другое вместе.
Прерывистый АР характеризуется наличием симптомов менее 4 дней в течение 1 недели или менее 4 недель в течение 1 года, тогда как стойкий АР характеризуется наличием симптомов более 4 дней в течение 1 недели и более чем 4 недели в 1 год. 1,2 Несмотря на то, что его часто неправильно характеризовали как неприятное состояние, если его не контролировать, он может привести к серьезным последствиям, таким как плохая посещаемость школы или работы, плохой сон, нарушение обучаемости и снижение активности на работе, в социальных сетях, и домашние настройки. 1
Руководства по ведению АР, опубликованные совместно Американской академией аллергии, астмы и иммунологии (AAAAI) и Американским колледжем аллергии, астмы и иммунологии (ACAAI), назначают интраназальные кортикостероиды (ИНС) как наиболее эффективный класс. лекарств для контроля назальных симптомов АР. 1 Пациенты, принимающие ИНС, могут ожидать начала терапевтического эффекта от назальных симптомов в течение 3–12 часов, хотя для оптимального контроля может потребоваться несколько дней использования. При правильном использовании в рекомендуемых дозах ИНС, как правило, не связаны со значительными системными побочными эффектами (НЯ) 1 ; однако могут возникать местные НЯ, такие как раздражение носа и кровотечение. Частоту НЯ можно свести к минимуму, распыляя лекарство от носовой перегородки. 1,3
Рекомендации при выборе безрецептурных интраназальных стероидов
В США доступны девять фирменных препаратов INS (таблица). 4-6 На момент написания этой статьи без рецепта можно приобрести 2 INS: Nasacort Allergy 24HR (триамцинолона ацетонид) и Flonase Allergy Relief (флутиказона пропионат). Управление по санитарному надзору за качеством пищевых продуктов и медикаментов одобрило, что переключатели Nasacort и Flonase будут доступны не только по рецепту, но и без рецепта 11 октября 2013 г. и 23 июля 2014 г., соответственно. 5,6
Благодаря наличию безрецептурных INS, пациенты теперь могут выбрать вариант самообслуживания. Однако при рассмотрении вариантов лечения любого состояния необходимо учитывать общие факторы, включая эффективность, безопасность и характеристики продукта, такие как состав.Что касается ИНС для лечения АР, в руководящих принципах AAAAI / ACAAI отмечается, что среди тех, которые доступны в настоящее время, клинический ответ, по-видимому, существенно не различается, а INS обычно не связаны с клинически значимыми системными НЯ. 1 Таким образом, поскольку профили эффективности и безопасности ИНС схожи, при оказании помощи пациентам в выборе продукта ИНС, подходящего для их нужд, следует принимать во внимание предпочтения пациентов, основанные на характеристиках составов конкретных ИНС. 7
Характеристики препаратов и предпочтения пациентов
В исследовании предпочтений пациентов 18 лет и старше с минимум 2-летней историей АР 109 пациентов были рандомизированы для оценки нескольких характеристик трех схем ИНС по 100-балльной шкале. -балльная шкала. Эти схемы включали триамцинолона ацетонид 220 мкг в день, флутиказона пропионат 200 мкг в день и мометазона фуроат 200 мкг в день. 7 (Обратите внимание, что состав мометазона фуроата был изменен после проведения этого исследования, и текущий состав не имеет запаха. 8 )
После использования лекарств участники оценили запах и вкус препарата триамцинолона ацетонида как значительно менее сильные, чем любой другой препарат ( P ≤ 0,001, оба сравнения по запаху; P ≤ 0,001 vs. мометазона фуроат для вкуса; P ≤,05 по сравнению с пропионатом флутиказона для вкуса). Кроме того, большее ощущение увлажнения слизистой оболочки носа было отмечено при использовании препарата триамцинолона ацетонида по сравнению с любым другим препаратом ( P ≤.001 против мометазона фуроата; P ≤.01 по сравнению с пропионатом флутиказона). Принимая во внимание эти факторы вместе, пациенты в целом предпочли препарат триамцинолона ацетонида по сравнению с другими (рисунок). 7
Подобные результаты наблюдались Бергером и его коллегами при исследовании 295 пациентов с 2-летней историей АР. После 3 недель лечения пациенты сообщали о значительно меньшем количестве жалоб, связанных с запахом (12,3% против 40,7%; P <0,0001) при использовании назального спрея триамцинолона ацетонида по сравнению с препаратом флутиказона пропионата. 9
Поскольку профили эффективности и безопасности INS схожи, 1 важно учитывать предпочтения пациента и конкретные характеристики препаратов при выборе безрецептурных INS. Одной из характеристик препарата, которая может быть важной для пациентов, является присутствие алкоголя в жидком носителе. Многие составы INS содержат спирт, который может вызывать ощущение сухости после приема. 7 Кроме того, присутствие спирта в составе может повлиять на его запах. 10 Следует учитывать запах и вкус, связанные с конкретным составом, поскольку эти атрибуты могут быть важны для принятия пациентом состава INS. 7 Жидкий носитель назального спрея на основе триамцинолона ацетонида, отпускаемого без рецепта, не содержит спирта, а его состав не имеет запаха и вкуса. 7,11 Жидкий носитель внебиржевого пропионата флутиказона содержит фенилэтиловый спирт. 12
Роль фармацевта
Различные варианты лечения АР доступны без рецепта.Руководящие принципы AAAAI / ACAAI по управлению INS уровня AR как наиболее эффективный класс лекарств для контроля назальных симптомов AR. 1 Чтобы помочь пациентам выбрать безрецептурный продукт INS для облегчения их симптомов, фармацевтам важно знать о доступных безрецептурных вариантах INS и характеристиках их рецептур, поскольку различия в рецептурах могут повлиять на восприятие пациентом продукта. Обладая этими знаниями, фармацевты могут участвовать в обсуждении с отдельными пациентами, чтобы определить, что для них важно с точки зрения характеристик препарата, и дать рекомендации по выбору INS.Также важно учитывать стоимость продукта, помогая пациентам выбрать лечение.
Фармацевты также могут обучать пациентов тому, когда и как использовать безрецептурные INS. Например, ИНС работают лучше всего при ежедневном использовании и могут не обеспечить максимального облегчения, пока они не используются последовательно в течение нескольких дней. 1 Кроме того, фармацевты могут предоставить инструкции по заправке баллончика с распылителем и использованию надлежащей техники распыления.
Понимая потребности каждого пациента, фармацевты могут помочь пациенту выбрать формулировку INS и правильно ее использовать для достижения наилучших возможных результатов.
Ссылки
- Wallace DV, Dykewicz MS, Bernstein DI, et al; Совместная целевая группа по практике; Американская академия аллергии, астмы и иммунологии; Американский колледж аллергии, астмы и иммунологии; Объединенный совет аллергии, астмы и иммунологии. Диагностика и лечение ринита: обновленный параметр практики. Дж. Аллергия Клин Иммунол . 2008; 122 (приложение 2): S1-S84. DOI: 10.1016 / j.jaci.2008.06.003.
- Буске Дж., Халтаев Н., Круз А.А. и др .; Всемирная организация здоровья; GA (2) LEN; AllerGen.Аллергический ринит и его влияние на астму (ARIA), обновление 2008 г. (в сотрудничестве с Всемирной организацией здравоохранения, GA [2] LEN и AllerGen). Аллергия . 2008; 63 (доп. 86): 8-160. DOI: 10.1111 / j.1398-9995.2007.01620.x.
- Беннингер М.С., Хэдли Дж. А., Оскуторп Дж. Д. и др. Техники интраназального применения стероидов. Отоларингол Хирургия головы и шеи . 2004; 130 (1): 5-24.
- FDA. Национальный справочник кодов лекарств. Веб-сайт FDA. www.accessdata.fda.gov/scripts/cder/ndc/dsp_searchresult.куб. Обновлено 12 марта 2015 г. Проверено 1 февраля 2015 г.
- FDA. Письмо одобрения Nasacort Allergy 24HR от 11 октября 2013 г. Веб-сайт FDA. www.accessdata.fda.gov/drugsatfda_docs/appletter/2013/020468Orig1s035ltr.pdf. По состоянию на 11 марта 2014 г.
- FDA. Письмо одобрения Flonase Allergy Relief от 23 июля 2014 г. Веб-сайт FDA. www.accessdata.fda.gov/drugsatfda_docs/appletter/2014/205434Orig1s000ltr.pdf. По состоянию на 11 марта 2014 г.
- Bachert C, El-Akkad T. Предпочтения пациентов и сенсорное сравнение трех интраназальных кортикостероидов для лечения аллергического ринита. Ann Allergy Asthma Immunol . 2002; 89 (3): 292-297.
- FDA. Центр оценки лекарственных средств и одобрения исследований для: Номер заявки NDA 20-762 / S007: Назальный спрей Nasonex на водной основе 50 мкг . Роквилл, Мэриленд: Управление по санитарному надзору за качеством пищевых продуктов и медикаментов; 2004. www.accessdata.fda.gov/drugsatfda_docs/nda/2004/020762_S007_NASONEX_AQUEOUS_NASAL_SPRAY.pdf. По состоянию на 11 марта 2014 г.
- Berger WE, Kaiser H, Gawchik SM, et al. Водный назальный спрей триамцинолона ацетонид и флутиказона пропионат одинаково эффективны для облегчения назальных симптомов у пациентов с сезонным аллергическим ринитом. Отоларингол Хирургия головы и шеи . 2003; 129 (1): 16-23.
- Махадевия П.Дж., Шах С., Лейбман С., Клейнман Л., О’Дауд Л. Предпочтения пациентов в отношении сенсорных характеристик интраназальных кортикостероидов и готовность придерживаться предписанной терапии аллергического ринита: совместный анализ. Ann Allergy Asthma Immunol . 2004; 93 (4): 345-350.
- Факты о лекарствах Nasacort Allergy 24HR. Сайт Nasacort. http://nasacort.com/hcp/downloads/NAS_DrugFacts_FNL-4.pdf. По состоянию на 11 марта 2015 г.
- Факты о лекарствах от аллергии на флоназу. Сайт Flonase. www.flonaseprofessional.com/content/dam/NA_Pharma/Country/US/Brands/Flonase/Digital/Web/PDFs/en_us/flute-expert-site/resources/FLONASE_Drug_Facts.pdf. По состоянию на 11 марта 2015 г.
Плюсы и минусы назальных стероидов, отпускаемых без рецепта
Nasacort Allergy 24 Hour (триамцинолон) был первым назальным спреем с кортикостероидами для интраназального введения, доступным без рецепта. Вскоре после этого флоназа (флутиказон) и ринокорт (будесонид) также стали доступны без рецепта в качестве эффективных кортикостероидных спреев.
Решение о том, использовать ли назальный спрей с кортикостероидами или пероральные безрецептурные антигистаминные препараты, такие как Zyrtec или Allegra, может сбить с толку. Что более эффективно? Что длится дольше? Что вызывает наименьшее количество симптомов? Выбор во многом зависит от типа и тяжести ваших симптомов.
Назальные спреи против антигистаминных препаратов
Интраназальные кортикостероиды, Назакорт, Флоназа и Ринокорт, вероятно, являются наиболее эффективными безрецептурными препаратами для лечения симптомов назальной аллергии.Обратной стороной является то, что они не будут работать по мере необходимости.
Чтобы подействовать интраназальные кортикостероиды, нужно время. Они могут начать облегчать симптомы аллергии примерно через шесть-десять часов, но полное облегчение не может быть достигнуто в течение трех-шести недель при ежедневном использовании.
С другой стороны, антигистаминные препараты, такие как Зиртек (цетиризин), Аллегра (фексофенадин) и Кларитин (лоратадин), как правило, действуют довольно быстро, обычно в течение нескольких часов (или меньше) после приема лекарства.Таким образом, эти лекарства хорошо работают, если принимать их по мере необходимости.
Антигистаминные препараты лучше всего подходят для лечения зуда в носу, глазного зуда и чихания, но менее эффективны при симптомах заложенности носа или насморка. Из трех более новых (и менее седативных) пероральных антигистаминных препаратов Зиртек и Аллегра особенно хорошо помогают облегчить симптомы назальной аллергии, обычно в течение часа.
Кларитин, с другой стороны, не работает, и его эффект начинает действовать примерно через три часа.Все три из этих антигистаминных препаратов являются хорошим выбором для снятия весенней аллергии и, как правило, предпочтительнее седативных антигистаминных препаратов, таких как Бенадрил.
Единственными другими лекарственными спреями для носа, доступными без рецепта, являются нестероидные деконгестанты, такие как Африн (оксиметазолин) и NasalCrom (кромолин).
Споры и соображения
Еще один аспект, который следует учитывать, заключается в том, что многие профессиональные организации аллергологов, педиатров и отоларингологов были против того, чтобы интраназальные кортикостероиды были доступны без рецепта.Ранее они выступали против того, чтобы антигистаминный кларитин стал доступным без рецепта.
Однако в течение 1990-х годов FDA обозначило аллергический ринит как заболевание, которое можно распознать и лечить без участия специалиста в области здравоохранения. Это означает, что FDA считает безопасным, чтобы широкая публика самостоятельно диагностировала и лечила аллергический ринит с помощью безрецептурных препаратов.
Однако интраназальные кортикостероиды могут быть не такими безопасными, как антигистаминные, поэтому следует учитывать риски и преимущества.Безрецептурные назальные деконгестанты не следует использовать более двух дней за раз, чтобы избежать повторной заложенности носа и усугубления заложенности носа.
Плюсы
Спреи с кортикостероидами для носа доступны на рынке по рецепту более 30 лет, и за это время было собрано большое количество данных о безопасности. Наиболее частые побочные эффекты включают раздражение носа, чихание, раздражение горла, головные боли и кровь из носа, которые обычно незначительны.
Наиболее тревожным побочным эффектом применения назальных кортикостероидов является перфорация перегородки, хотя это случается крайне редко, учитывая, что большинство людей прекращают использование спрея после появления боли и кровотечения из носа.
Риск перфорации перегородки увеличивается, если вы распыляете в середину носа, а не на внешнюю стенку носового прохода. Вместо этого нанесите один спрей прямо назад и параллельно твердому нёбу, а другой спрей вверх и наружу в сторону ипсилатерального глаза / уха.
Помимо локальных симптомов, интраназальные кортикостероиды редко вызывают побочные эффекты на все тело. Исследования, изучающие использование интраназальных кортикостероидов, еще не продемонстрировали каких-либо доказательств подавления оси гипоталамус-гипофиз-надпочечники (HPA), при которой чрезмерное использование кортикостероидов влияет на собственную выработку кортизола в организме.
Есть некоторые опасения по поводу стоимости интраназальных кортикостероидов, учитывая, что безрецептурные препараты не покрываются медицинской страховкой. Вообще говоря, стоимость посещения врача почти смягчает эту проблему. В конце концов, люди с большей вероятностью попробуют безрецептурный спрей, чем будут пытаться получить рецепт с практически такими же результатами.
Минусы
Некоторые медицинские организации считают, что безрецептурные интраназальные кортикостероиды — плохая идея.Причины в основном связаны с безопасностью продукта, особенно у маленьких детей и пожилых людей.
Высказывались опасения по поводу подавления роста у детей, применяющих интраназальные кортикостероиды, хотя эти эффекты считаются незначительными и непостоянными. Несмотря на это, дети, использующие интраназальные или ингаляционные кортикостероиды, должны находиться под наблюдением медицинского работника.
Большую озабоченность вызывает использование интраназальных кортикостероидов у пожилых людей, которые уже подвержены риску глаукомы.Известно, что использование назальных и пероральных стероидов повышает глазное давление, что способствует развитию болезни.
В настоящее время нет клинических данных о повышенном риске катаракты у пожилых людей, принимающих кортикостероиды. Хотя препараты могут увеличить риск остеопороза при чрезмерном применении, нет никаких доказательств того, что они увеличивают риск переломов.
Противники безрецептурных интраназальных кортикостероидов также считают, что потребители не поймут, что это лекарство необходимо регулярно использовать, чтобы оно работало.
В отличие от местных назальных деконгестантов, которые приносят облегчение за считанные минуты, интраназальные кортикостероиды действуют от нескольких часов до нескольких дней. Поэтому люди могут использовать более высокие дозы, чем рекомендованные, что может привести к большему количеству побочных эффектов.
Многие из побочных эффектов и недопонимания того, как действуют интраназальные кортикостероиды, можно избежать, оставив эти лекарства только по рецепту, что позволяет часто контролировать их со стороны медицинского работника.
Слово Verywell
Понимание правильного использования безрецептурных препаратов для лечения аллергического ринита может помочь вам избежать потенциальных побочных эффектов.Возможно, вы захотите обсудить свой выбор со своим врачом, особенно если вы планируете использовать их для детей или пожилых людей.
Различные виды интраназальных стероидов при хроническом риносинусите
Вопрос для повторения
Мы рассмотрели доказательства пользы и вреда различных типов интраназальных (в нос) стероидов, назначаемых людям с хроническим риносинуситом.
Фон
Хронический риносинусит — распространенное заболевание, которое определяется как воспаление носа и придаточных пазух носа (группа заполненных воздухом пространств за носом, глазами и щеками).Пациенты с хроническим риносинуситом испытывают как минимум два или более из следующих симптомов в течение как минимум 12 недель: заложенность носа, выделения из носа или насморк, боль или давление в лице и / или снижение обоняния (гипосмия). У некоторых людей также могут быть полипы в носу, которые представляют собой вздутие нормальной слизистой оболочки носа в носовых ходах и пазухах, напоминающее виноград. Местные (интраназальные) кортикостероиды используются с целью уменьшения воспаления и улучшения симптомов пациента.
Характеристики исследования
Мы включили в этот обзор девять рандомизированных контролируемых испытаний (РКИ) с участием 910 человек. Исследования различались по размеру: некоторые были небольшими, всего с 20 пациентами, в то время как другие включали более 200 участников. В большинстве исследований участвовали взрослые пациенты, но в одно исследование были включены только дети. В большинстве исследований взрослых большинство участников были мужчинами (от 72% до 79%). Во всех исследованиях у участников был хронический риносинусит с полипами носа.В исследованиях сравнивали различные типы стероидов (три исследования), стероиды в высоких и низких дозах (пять исследований), два раза в день и один раз в день стероиды или разные методы доставки (водный назальный спрей против аэрозоля — одно исследование). Во всех исследованиях была группа плацебо.
Ключевые результаты и качество доказательств
Различные стероиды: флутиказона пропионат в сравнении с беклометазона дипропионатом
Два небольших исследования (56 участников, неясный риск систематической ошибки) оценивали тяжесть заболевания и рассматривали первичный побочный эффект, носовое кровотечение (носовое кровотечение), но не другие исходы.Не было обнаружено различий между двумя стероидами, но мы оценили доказательства как очень низкого качества .
Различные стероиды: флутиказона пропионат в сравнении с мометазона фуроатом
Одно исследование (100 участников, неясный риск систематической ошибки) не обнаружило разницы в тяжести заболевания (оценка назальных симптомов). Мы оценили это доказательство как очень низкого качества .
Высокие дозы стероидов в сравнении с низкими
Мы нашли пять исследований (663 участника, низкий или неясный риск систематической ошибки), в которых сравнивали высокие и низкие дозы стероидов, три — с использованием мометазона фуроата (400 мкг против 200 мкг у взрослых и детей старшего возраста, 200 мкг против 100 мкг у детей младшего возраста. дети), а двое — с использованием капель флутиказона пропионата (800 мкг против 400 мкг).Эффективность (тяжесть заболевания и размер носовых полипов) была одинаковой в группах с высокими и низкими дозами ( доказательства низкого качества, ). Хотя во всех исследованиях сообщалось о большем улучшении показателей полипов в группе, получавшей высокие дозы, значение этого неясно, поскольку наблюдаемые улучшения были небольшими.
Первичный побочный эффект, носовое кровотечение, чаще встречался при использовании более высоких доз (доказательства среднего качества).
Различные способы доставки: водный назальный спрей по сравнению с аэрозольным спреем
Мы выявили только одно исследование с плохой отчетностью и высоким риском систематической ошибки.Неизвестно, сколько было участников: 91 человек был набран в три группы. Также были значительные различия между участниками в двух группах, когда они начали исследование. Мы не смогли сделать каких-либо значимых выводов из этого исследования.
Выводы
Мы не нашли доказательств того, что один тип интраназальных стероидов более эффективен, чем другой у пациентов с хроническим риносинуситом, или что более высокие дозы лучше, чем более низкие, или что эффективность спрея отличается от аэрозоля.Мы не нашли исследований, в которых сравнивали бы капли в нос и спрей. Мы действительно нашли доказательства среднего качества повышенного риска носового кровотечения (носового кровотечения) как побочного эффекта лечения при использовании более высоких доз.
Совершенно очевидно, что необходимы дополнительные исследования в этой области. В будущем исследования должны быть хорошо спланированы: они должны измерять качество жизни, связанное со здоровьем, связанное с хроническим риносинуситом, и побочные эффекты как исходы, а также смотреть, что происходит с пациентами, принимающими интраназальные стероиды в долгосрочной перспективе.
Аллергический ринит и интраназальные кортикостероидные спреи
Фарм США . 2015; 40 (7): 8-11.
Аллергический ринит (АР) — одно из наиболее распространенных хронических заболеваний, поражающих как детей, так и взрослых в Соединенных Штатах. 1 По оценкам, распространенность АР достигает 30% у взрослых и до 40% у детей и является наиболее распространенным аллергическим заболеванием у детей. 2,3 В целом, это пятое по распространенности хроническое заболевание в США.S., затрагивающий примерно 60 миллионов американцев, хотя это число может быть недооценено, поскольку пациенты часто не распознают АР как болезнь и поэтому не обращаются к врачу. 1,3,4 AR может негативно повлиять на качество жизни пациента, приводя к трудностям в повседневной деятельности, ухудшению качества сна и ухудшению психического благополучия. 5
Общая прямая стоимость AR составляет около 3,4 миллиарда долларов, причем почти половина этой стоимости приходится на рецептурные препараты; среднее количество рецептов для пациентов с АР почти вдвое больше, чем для пациентов без аллергии. 6,7 Нередко отпускаемые по рецепту лекарства используются в сочетании с безрецептурными продуктами для облегчения симптомов АР.
Лечение АР обычно начинается в аптеке, когда пациенты обращаются за рекомендациями к фармацевтам. Для фармацевтов важно иметь представление об АР и различных вариантах профилактики и лечения этого состояния.
ПатофизиологияАР — хроническое воспалительное заболевание, поражающее верхние дыхательные пути.Это воспаление слизистой оболочки носа является результатом вдыхания аэроаллергенов, к которым пациент был ранее сенсибилизирован, связывания с иммуноглобулином E (IgE) на поверхности тучных клеток, что приводит к дегрануляции тучных клеток и высвобождению предварительно сформированных медиаторов, таких как гистамин и лейкотриены. 1,8 Эти недавно выпущенные медиаторы связываются с рецепторами в носу, вызывая многие из проявлений АР в течение нескольких минут после воздействия, включая зуд в носу, чихание, чистую ринорею и некоторую степень заложенности носа. 9
Через 4–12 часов после воздействия аллергена пациенты могут испытывать позднюю фазу ответа, характеризующуюся вторым высвобождением тех же медиаторов, реактивируя многие из тех же провоспалительных реакций немедленного ответа. 9 Наиболее распространенным проявлением в этой фазе является заложенность носа, которая часто бывает серьезной и длительной. 8,9
КлассификацияАР можно классифицировать в зависимости от временного характера воздействия аллергенов, частоты симптомов и тяжести. 1 Традиционно использовалась временная категоризация; AR можно разделить на сезонные и многолетние. Сезонный аллергический ринит (SAR) имеет сезонные вариации и зависит от географического положения и климатических условий; деревья, трава, пыльца сорняков и споры плесени на открытом воздухе обычно являются наиболее частыми триггерами. Симптомы SAR обычно появляются в определенное время года, когда эти аэроаллергены в изобилии. 1,10 Многолетний аллергический ринит (PAR) связан с аэроаллергенами, воздействию которых пациент постоянно подвергается, и обычно встречается в помещении.Общие аэроаллергены PAR включают пылевых клещей, тараканов, домашнюю плесень и грибы, аллергены животных, а также пыльцу, где пыльца преобладает постоянно. 10
У других пациентов могут быть эпизодические проявления. Эпизодический АР описывает аллергические назальные симптомы у пациентов, которые время от времени подвергаются воздействию аэроаллергенов, которые обычно не встречаются в их обычных помещениях или на открытом воздухе. 10
Эта традиционная система классификации имеет ограничения, из-за которых иногда трудно определить, страдает ли пациент аллергическими симптомами, вызванными сезонной пыльцой или вызванными воздействием аллергенов, которые являются постоянными.Использование системы классификации, основанной на частоте и степени тяжести, позволяет выбрать более подходящий метод лечения. 1,4 Есть два деления частоты: прерывистая и постоянная. Прерывистая частота определяется как симптомы АР, возникающие ≤4 дней в неделю или ≤4 недель в год, а стойкая частота определяется как симптомы, возникающие> 4 дней в неделю и в течение> 4 недель в году.
По степени тяжести АР классифицируется как легкая или умеренная / тяжелая. 1,4 АР считается легкой, если симптомы присутствуют, но не вызывают беспокойства и не влияют на качество жизни пациента. Умеренная / тяжелая АР — это когда симптомы считаются доставляющими беспокойство и мешают повседневной деятельности пациента, влияя на его сон и успеваемость на работе или в школе.
Стратегии управленияЦели лечения АР включают облегчение симптомов, улучшение качества жизни пациента, минимизацию нарушений сна, улучшение работы и успеваемости в школе, а также ограничение побочных эффектов терапии.
Одна из наиболее важных стратегий, которую следует предложить, — это предотвращение или минимизация контакта с триггерами окружающей среды. 1,4,10 В идеале пациенты должны полностью избегать этих аллергенов, хотя это не всегда практично и трудно достижимо. Из-за этого большинству пациентов потребуется медикаментозная терапия для лечения и профилактики симптомов АР. Идя по проходу аптеки, пациенты могут выбирать из множества вариантов ухода за собой, чтобы облегчить симптомы АР. Безрецептурные препараты включают антигистаминные препараты, стабилизаторы тучных клеток и противоотечные средства.Совсем недавно мы стали свидетелями появления интраназальных кортикостероидов на рынке средств самообслуживания с заменой рецептурных препаратов на безрецептурные препараты триамцинолона ацетонида (Nasacort Allergy 24HR) и флутиказона пропионата (Flonase Allergy Relief).
Интраназальные кортикостероиды
Интраназальные кортикостероиды являются наиболее мощными и эффективными средствами для лечения АР; они рекомендуются в качестве препаратов первого ряда при умеренной / тяжелой или стойкой АР. 1,8,10 Эти агенты эффективно уменьшают воспаление слизистой оболочки носа и улучшают патологию слизистой оболочки за счет своего противовоспалительного механизма действия. 10,11 Исследования показали, что интраназальные кортикостероиды более эффективны, чем антагонисты лейкотриенов, а также интраназальные и пероральные антигистаминные препараты, даже в сочетании с антагонистами лейкотриенов. 1,10 Интраназальные кортикостероиды облегчают четыре основных симптома АР: чихание, зуд, ринорею и заложенность носа при постоянном применении и по мере необходимости; однако использование по мере необходимости может оказаться не таким эффективным, как постоянное использование. 10 Эти агенты, по-видимому, также благотворно влияют на офтальмологические симптомы, включая зуд, слезотечение, покраснение и отечность. 1
При сравнении доступных интраназальных кортикостероидов клиническая эффективность не меняется, что делает сенсорные характеристики важным фактором для предпочтений пациентов и приверженности лечению. 1,10 Начало терапевтического эффекта наступает между 3 и 12 часами, а максимальный эффект проявляется только через 2 недели терапии. 10,12
Интраназальные кортикостероиды хорошо переносятся большинством пациентов. Наиболее частые побочные эффекты возникают в результате местного раздражения и включают сухость, жжение, покалывание и носовое кровотечение; в редких случаях может произойти перфорация носовой перегородки.Этих эффектов можно избежать с помощью правильной техники введения, направленной в сторону от перегородки. 1,10,12 Были опасения по поводу системных побочных эффектов при интраназальном применении кортикостероидов. При использовании в рекомендуемых дозах эти агенты не вызывают надпочечниковой недостаточности или подавления роста у детей, а также не увеличивают частоту переломов костей у пожилых людей. 10
Nasacort Allergy 24HR: Первым интраназальным кортикостероидом, который стал доступен без рецепта, был Nasacort Allergy 24HR (триамцинолона ацетонид). 13 Он был введен в действие в феврале 2014 года, когда назначение Nasacort AQ было прекращено; дженерик триамцинолона ацетонида назальный спрей все еще доступен по рецепту. Nasacort Allergy 24HR доставляет 55 мкг / спрей триамцинолона ацетонида, как и Nasacort AQ. Он одобрен для использования у людей в возрасте ≥2 лет для временного облегчения заложенности носа, насморка и зуда в носу, а также чихания из-за сенной лихорадки или других аллергий на верхние дыхательные пути. Подходящая доза для детей от 2 до <6 лет - один спрей в каждую ноздрю один раз в день.Детям от 6 до <12 лет следует начинать с одного спрея в каждую ноздрю один раз в день и увеличить до двух спреев в каждую ноздрю, если симптомы не улучшаются. Для людей в возрасте ≥12 лет соответствующая доза составляет 2 распыления в каждую ноздрю один раз в день, снижая до одного распыления в каждую ноздрю в день, как только симптомы аллергии улучшатся. Этот продукт не содержит запаха. 13
Flonase Allergy Relief: В феврале 2015 года Flonase Allergy Relief (флутиказона пропионат) стал вторым антигистаминным препаратом для интраназального введения, доступным без рецепта. 14 Это то же самое, что и рецептурная версия, доставляющая 50 мкг / спрей флутиказона пропионата. Так же, как и с Nasacort AQ, рецепт на Flonase был отменен; тем не менее, назальный спрей флутиказона пропионата по-прежнему доступен по рецепту. В отличие от Nasacort Allergy 24HR, Flonase Allergy Relief — единственный безрецептурный назальный спрей, который одобрен как для назальной, так и для глазной аллергии. Он одобрен для использования людьми в возрасте ≥4 лет. Доза для детей от 4 до 11 лет составляет 1 спрей в каждую ноздрю один раз в день.Для детей и взрослых старше 12 лет рекомендуемая дозировка следующая: в течение первой недели используйте 2 спрея в каждую ноздрю один раз в день, затем используйте 1 или 2 спрея в каждую ноздрю один раз в день по мере необходимости для лечения симптомов. После 6 месяцев ежедневного использования пациенты должны проконсультироваться со своим лечащим врачом по поводу продолжения использования. 14
ЗаключениеАР — распространенное заболевание, которое может отрицательно повлиять на качество жизни пациента. Многие пациенты проконсультируются со своими фармацевтами относительно стратегий лечения, чтобы облегчить назойливые симптомы.Благодаря доступности интраназальных кортикостероидов без рецепта, пациенты теперь имеют больший доступ к средствам, которые будут эффективно контролировать их симптомы при правильном использовании.
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТАЧто вызывает аллергический ринит (АР)?
AR отличается от простуды или других болезней тем, что вызывается аллергеном, а не вирусом или инфекцией. Общие аллергены включают пылевых клещей, шерсть животных, плесень, пыльцу деревьев, травы и сорняков.
Как избежать аллергеновОдин из способов лечения симптомов АР — избегать того, что их вызывает. Системы вентиляции и частая тщательная уборка в доме могут помочь уменьшить количество аллергенов в помещении. В случае аллергенов на открытом воздухе старайтесь оставаться в помещении в периоды плохого качества воздуха.
Безрецептурные препаратыОрошение носа: Промывание носовых ходов с помощью солевого раствора для промывания носа или спреев может помочь удалить аллергены и слизь из носа и уменьшить дренаж в заднюю часть глотки.Это очень безопасно, если все сделано правильно, и при необходимости можно выполнять один или два раза в день.
Кортикостероиды для интраназального введения: Эти препараты вводятся непосредственно в нос в виде спрея и снижают воспаление и дискомфорт. В настоящее время они доступны без рецепта как Nasacort Allergy 24HR (триамцинолон) и Flonase Allergy Relief (флутиказон). Улучшение симптомов можно увидеть почти сразу, хотя максимальная эффективность может занять несколько дней. Прекратите использование и обратитесь к врачу, если симптомы не улучшатся в течение 7 дней или появятся новые симптомы.Побочные эффекты минимальны и включают сухость в носу и неприятный запах или вкус. Узнайте у фармацевта, как правильно вводить лекарства для интраназального введения.
Антигистаминные препараты: Эти продукты помогают уменьшить симптомы насморка, зуда в глазах и зуда в горле, но не устраняют заложенность носа. Их принимают внутрь один или два раза в день. Эти продукты можно принимать каждый день в сезон аллергии или по мере необходимости. Используйте не вызывающие сонливость средства, такие как Allegra (фексофенадин), Claritin (лоратадин) или Zyrtec (цетиризин).Побочные эффекты легкие, но могут включать сухость во рту и запор. Не принимайте это лекарство без консультации с врачом или фармацевтом, если вам больше 65 лет, у вас глаукома, затрудненное мочеиспускание, увеличение простаты, заболевания щитовидной железы или другие заболевания.
Противоотечные средства: Назальные и пероральные деконгестанты могут облегчить заложенность или заложенность носа, связанные с АР, и могут работать лучше всего в сочетании с интраназальными кортикостероидами или антигистаминными препаратами.Назальные деконгестанты, такие как Африн (оксиметазолин), не следует использовать более 3 дней из-за риска заложенности носа. Пероральные противозастойные средства, такие как Судафед (псевдоэфедрин), можно принимать в течение дня. Однако побочные эффекты включают учащенное сердцебиение, нервозность и бессонницу, поэтому их лучше всего принимать утром. Эти препараты не следует использовать, если у вас неконтролируемая гипертензия, болезнь сердца, закрытоугольная глаукома или гипертиреоз, или если вы принимаете определенные лекарства.
Помните: если у вас есть вопросы, проконсультируйтесь с фармацевтом.
СПИСОК ЛИТЕРАТУРЫ 1. Зайдман М.Д., Гургель Р.К., Лин С.И. и др. Руководство по клинической практике: аллергический ринит. Отоларингол Хирургия головы и шеи . 2015; 152 (1 доп.): С1-С43.
2. Carr WW. Детский аллергический ринит: текущее и будущее состояние техники. Allergy Asthma Proc . 2008; 29 (1): 14-23.
3. Джентиле Д., Бартолоу А., Валовирта Е. и др. Текущие и будущие направления детской аллергического ринита. J Allergy Clin Immunol Pract . 2013; 1 (3): 214-226; quiz 227.
4. Буске Дж., Халтаев Н., Круз А.А. и др. Аллергический ринит и его влияние на астму (ARIA), обновление 2008 г. (в сотрудничестве с Всемирной организацией здравоохранения, GA (2) LEN и AllerGen). Аллергия . 2008; 63 (доп. 86): 8-160.
5. Мельцер Э.О., Гросс Г.Н., Катиал Р., Штормы WW. Аллергический ринит существенно влияет на качество жизни пациентов: результаты исследования назальной аллергии с оценкой ограничений. Дж. Практик .2012; 61 (2 доп.): S5-S10.
6. Бхаттачарья Н. Дополнительные медицинские услуги и расходы на лечение аллергического ринита в США. Ларингоскоп . 2011; 121 (9): 1830-1833.
7. Мельцер Э.О., Букштейн Д.А. Экономические последствия аллергического ринита и современные рекомендации по лечению. Ann Allergy Asthma Immunol . 2011; 106 (2 доп.): S12-S16.
8. Агентство медицинских исследований и качества. Протокол систематического обзора научно-практического центра. Лечение сезонного аллергического ринита.Март 2012 г. http://effectivehealthcare.ahrq.gov/ehc/products/376/1000/SAR_Protocol_20120308.pdf. По состоянию на 19 мая 2015 г.
9. Сконер Д.П. Аллергический ринит: определение, эпидемиология, патофизиология, выявление и диагностика. J Allergy Clin Immunol . 2001; 108 (приложение 1): S2-S8.
10. Уоллес Д.В., Дикевич М.С., Бернштейн Д.И. и др. Диагностика и лечение ринита: обновленный параметр практики. J Allergy Clin Immunol . 2008; 122 (2 доп.): S1-S84.
11. Смолл П., Ким Х.Аллергический ринит. Allergy Asthma Clin Immunol . 2011; 7 (приложение 1): S3.
12. Scadding GK, Durham SR, Mirakian R, et al; Британское общество аллергии и клинической иммунологии. Рекомендации BSACI по лечению аллергического и неаллергического ринита. Clin Exp Allergy . 2008; 38 (1): 19-42.
13. Nasacort Allergy 24HR. Этикетка с фактами о наркотиках. http://nasacort.com/hcp/. Проверено 17 июня 2015 г.
14. Flonase Allergy Relief. Этикетка с фактами о наркотиках. www.flonaseprofessional.com/resources/#drugFacts.По состоянию на 17 июня 2015 г.
Чтобы прокомментировать эту статью, обращайтесь по адресу [email protected].
Тонкие нюансы интраназальных кортикостероидов | Journal of Otolaryngology — Head & Neck Surgery
Wise SK, Lin SY, Toskala E, Orlandi RR, Akdis CA, Alt JA, Azar A, Baroody FM, Bachert C, Canonica GW, Chacko T. Заявление международного консенсуса по аллергия и ринология: аллергический ринит. Int Forum Allergy Rhinol. 2018; 8 (2): 108–352.
PubMed PubMed Central Google Scholar
Орланди Р.Р., Королевство Т.Т., Хванг PH, Смит Т.Л., Альт Дж.А., Баруди FM, Батра П.С., Бернал-Спрекельсен М., Бхаттачарья Н., Чандра Р.К., Чиу А. Заявление о международном консенсусе по аллергии и ринологии: риносинусит. Int Forum Allergy Rhinol. 2016; 6: S22 – S209.
PubMed Google Scholar
Сконер Д.П., Рахелевский Г.С., Мельцер Е.О., Червинский П., Моррис Р.М., Зельцер Ю.М., Штормз В.В., Вуд РА. Обнаружение подавления роста у детей при лечении интраназальным введением беклометазона дипропионата.Педиатрия. 2000; 105 (2): e23.
CAS PubMed Статья PubMed Central Google Scholar
Беннингер М.С., Ахмад Н., Марпл Б.Ф. Безопасность интраназальных стероидов. Otolaryngol Head Neck Surg. 2003. 129 (6): 739–50.
PubMed Статья Google Scholar
Берлуччи М., Салси Д., Валетти Л., Парринелло Г., Николай П. Роль водного назального спрея мометазона фуроата в лечении гипертрофии аденоидов в детской возрастной группе: предварительные результаты проспективного рандомизированного исследования.Педиатрия. 2007; 119 (6): e1392–7.
PubMed Статья PubMed Central Google Scholar
Родриго Дж., Неффен Х. Эффективность назального спрея флутиказона фуроата по сравнению с плацебо для лечения глазных и назальных симптомов аллергического ринита: систематический обзор. Clin Exp Allergy. 2011; 41: 160–70.
CAS PubMed Статья Google Scholar
Penagos M, Compalati E, Tarantini F, Baena Cagnani CE, Passalacqua G, Canonica GW.Эффективность назального спрея мометазона фуроата при лечении аллергического ринита. Метаанализ рандомизированных двойных слепых плацебо-контролируемых клинических исследований. Аллергия. 2008; 63: 1280–91.
CAS PubMed Статья Google Scholar
Ямада Т., Ямамото Х., Кубо С. и др. Эффективность назального спрея мометазона фуроата для лечения назальных симптомов, качества жизни, нарушения сна при рините и оксида азота в носу у пациентов с хроническим аллергическим ринитом.Аллергия и астма. 2012; 33: e9 – e16.
CAS Статья Google Scholar
Meltzer EO, Munafo DA, Chung W, Gopalan G, Varghese ST. Интраназальная терапия мометазоном фуроатом при симптомах аллергического ринита и нарушении сна. Ann Allergy Asthma Immunol. 2010; 105: 65–74.
CAS PubMed Статья Google Scholar
Kaiser HB, Naclerio RM, Given J, Toler TN, Ellsworth A, Philpot EE.Назальный спрей флутиказона фуроат: единственный вариант лечения симптомов сезонного аллергического ринита. J Allergy Clin Immunol. 2007; 119: 1430–7.
CAS PubMed Статья PubMed Central Google Scholar
ДеВестер Дж., Филпот Е.Е., Вестлунд Р.Э., Кук С.К., Рикард К.А. Эффективность интраназального введения флутиказона пропионата в облегчении глазных симптомов, связанных с сезонным аллергическим ринитом. Аллергия и астма.2003; 24: 331–7.
CAS Google Scholar
Ратнер П., Ван Бавель Дж., Мохар Д. и др. Эффективность ежедневного интраназального введения флутиказона пропионата в отношении глазных симптомов, связанных с сезонным аллергическим ринитом. Ann Allergy Asthma Immunol. 2015; 114: 141–7.
CAS PubMed Статья PubMed Central Google Scholar
Jankowski R, Schrewelius C, Bonfils P, et al.Эффективность и переносимость водного назального спрея будесонида у пациентов с носовыми полипами. Arch Otolaryngol Head Neck Surg. 2001; 127: 447–52.
CAS PubMed Статья Google Scholar
Йоханссон Л., Холмберг К., Мелен И. и др. Чувствительность новой системы оценки для изучения носовых полипов с возможностью выявления ранних изменений размера полипа после лечения местным кортикостероидом (будесонидом).Acta Otolaryngol. 2002; 122: 49–53.
CAS PubMed Статья Google Scholar
Влцкова И., Навратил П., Кана Р. и др. Эффективное лечение полипоза носа от легкой до средней степени тяжести с помощью флутиказона с помощью нового устройства. Ринология. 2009; 47: 419–26.
PubMed Google Scholar
Стьярне П., Олссон П., Алениус М. Использование мометазона фуроата для предотвращения рецидива полипа после эндоскопической хирургии носовых пазух.Arch Otolaryngol Head Neck Surg. 2009. 135: 296–302.
PubMed Статья Google Scholar
Янковски Р., Клоссек Дж. М., Аттали В. и др. Долгосрочное исследование применения водного назального спрея флутиказона пропионата при острой и поддерживающей терапии полипоза носа. Аллергия. 2009; 64: 944–50.
CAS PubMed Статья Google Scholar
Vento SI, Blomgren K, Hytonen M, et al.Профилактика рецидивов назального полипоза интраназальным введением триамцинолона ацетонида после хирургического вмешательства на полипе: проспективное двойное слепое плацебо-контролируемое рандомизированное исследование с периодом наблюдения 9 месяцев. Клин Отоларингол. 2012; 37: 117–23.
CAS PubMed Статья PubMed Central Google Scholar
Day JH, Briscoe MP, Rafeiro E, Ellis AK, Pettersson E, Akerlund A. Начало действия интраназального будесонида (Rhinocort aqua) при сезонном аллергическом рините изучалось на модели контролируемого воздействия.J Allergy Clin Immunol. 2000; 105: 489–94.
CAS PubMed Статья Google Scholar
Fokkens WJ, Cserhati E, dos Santos JM, et al. Спрей для носа на водной основе будесонид — эффективное средство для лечения детей с круглогодичным аллергическим ринитом с началом действия в течение 12 часов. Ann Allergy Asthma Immunol. 2002; 89: 279–84.
CAS PubMed Статья PubMed Central Google Scholar
Торат С. Состав и разработка назального спрея: обзор. Ученые J Appl Med Sci. 2016; 4: 2976–85.
Google Scholar
Neffen H, Wingertzahn MA. Циклезонид, гипотонический интраназальный кортикостероид. Аллергия и астма. 2010; 31 (3).
Шарп С.А., Сандвейс В., Туазон Дж., Джордано М., Витчи-Лакшманан Л., Харт Дж., Секейра Дж. Сравнение свойств текучести водных суспензий кортикостероидных назальных спреев при различных условиях отбора проб.Препарат Дев Инд Фарм. 2003. 29 (9): 1005–12.
CAS PubMed Статья Google Scholar
Кариявасам Х. Х., Scadding GK. Сезонный аллергический ринит: оценена терапия флутиказона пропионатом и флутиказона фуроатом. J Asthma Allergy. 2010; 3:19.
PubMed PubMed Central Google Scholar
Биггадике К. Флутиказона фуроат / флутиказона пропионат — разные препараты с разными свойствами.Клин Респир Дж. 2011; 5 (3): 183.
CAS PubMed PubMed Central Статья Google Scholar
Окубо К., Накашима М., Мияке Н., Комацубара М., Окуда М. Сравнение фуроата флутиказона и пропионата флутиказона для лечения поллиноза японского кедра. Аллергия и астма. 2009. 30 (1): 84–94.
Артикул Google Scholar
Валотис А., Хёггер П.Кинетика рецепторов человека и удержание тканью легких глюкокортикоида с повышенным сродством флутиказона фуроата. Respir Res. 2007; 8 (1): 54.
PubMed PubMed Central Статья CAS Google Scholar
Солтер М., Биггэдайк К., Мэтьюз Дж. Л., Вест М. Р., Хаас М. В., Фэрроу С. Н., Уингс И. Дж., Грей Д. В.. Фармакологические свойства глюкокортикоида флутиказона фуроата с повышенным сродством in vitro и на модели воспалительного заболевания органов дыхания in vivo.Am J Phys Lung Cell Mol Phys. 2007; 293 (3): L660–7.
CAS Google Scholar
Карр В., Бернштейн Дж., Либерман П., Мельцер Е., Бахерт С., Прайс Д., Мюнзель Ю., Буске Дж. Новая интраназальная терапия азеластином с флутиказоном для лечения аллергического ринита. J Allergy Clin Immunol. 2012. 129 (5): 1282–9.
CAS PubMed Статья Google Scholar
Derendorf H, Munzel U, Petzold U, Maus J, Mascher H, Hermann R, Bousquet J. Биодоступность и распределение азеластина и флутиказона пропионата при доставке с помощью MP29-02, нового водного назального спрея. Br J Clin Pharmacol. 2012. 74 (1): 125–33.
CAS PubMed PubMed Central Статья Google Scholar
Хуанг ZZ, Чен XZ, Хуанг JC, Ван Зи, Ли X, Чен XH, Лай XP, Чанг Л.Х., Чжан Г.Х. Орошение носа будесонидом улучшило эндоскопический балл Лунда – Кеннеди у пациентов с хроническим риносинуситом после эндоскопической хирургии носовых пазух.Eur Arch Otorhinolaryngol. 2019; 276 (5): 1397–403.
PubMed Статья Google Scholar
Кан Т.В., Чунг Дж. Х., Чо Ш, Ли Ш, Ким К. Р., Чон Дж. Х. Эффективность орошения носа будесонидом после эндоскопической хирургии носовых пазух при хроническом риносинусите с астмой. Clin Exp Otorhinolaryngol. 2017; 10 (1): 91.
CAS PubMed Статья Google Scholar
Нойбауэр П.Д., Швам З.Г., Манес Р.П. Сравнение интраназального спрея флутиказона, распылителя будесонида и респираторного введения будесонида у пациентов с хроническим риносинуситом с полипозом после эндоскопической хирургии носовых пазух. Int Forum Allergy Rhinol. 2016; 6 (3): 233–7.
PubMed Статья Google Scholar
Харви Р.Дж., Годдард Дж.С., Мудрый СК, Шлоссер Р.Дж. Влияние эндоскопической хирургии носовых пазух и устройства доставки на орошение пазух трупа.Otolaryngol Head Neck Surg. 2008. 139 (1): 137–42.
PubMed Статья Google Scholar
Bhalla RK, Payton K, Wright ED. Безопасность будесонида при орошении носовых пазух солевым раствором при лечении хронического риносинусита с полипозом: отсутствие значительного подавления функции надпочечников. J Otolaryngol Head Neck Surg. 2008 декабрь; 37 (6): 821–5. 19128710.
Welch KC, Thaler ER, Doghramji LL, Palmer JN, Chiu AG.Влияние уровней кортизола в сыворотке и моче при местных интраназальных орошениях с добавлением будесонида к физиологическому раствору у пациентов с рецидивирующим полипозом после эндоскопической хирургии носовых пазух. Am J Rhinol Allergy. 2010. 24 (1): 26–8. 20109316. https://doi.org/10.2500/ajra.2010.24.3418.
Артикул PubMed PubMed Central Google Scholar
Смит К.А., Френч Дж., Мехор Б., Рудмик Л. Безопасность длительных ирригаций с помощью будесонида носовых пазух в больших объемах при хроническом риносинусите.Int Forum Allergy Rhinol. 2016; 6 (3): 228–32.
PubMed Статья PubMed Central Google Scholar
Судри Е., Ван Дж., Везеафшар Р., Кацнельсон Л., Хванг PH. Анализ безопасности длительных орошений носа будесонидом у пациентов с хроническим риносинуситом после эндоскопической хирургии носовых пазух. Int Forum Allergy Rhinol. 2016; 6 (6): 568–72.
PubMed Статья PubMed Central Google Scholar
Петти Д.А., Блэсс М.С. Местные характеристики интраназальных кортикостероидов: побочные эффекты, формулировка и объем. Am J Rhinol Allergy. 2013. 27 (6): 510–3.
PubMed Статья PubMed Central Google Scholar
Клоссек Дж. М., Серрано Э., Дрейфус И., Месбах К., Демоли П. Исследование предпочтений пациентов по поводу отсутствия вкуса и запаха у назального спрея Nasonex. Что влияет на соблюдение режима лечения? Ревю Ларингол-Отол-Ринол.2008. 129 (1): 35–41.
CAS Google Scholar
Gupta R, Fonacier LS. Побочные эффекты несистемных стероидов (ингаляционных, интраназальных и кожных): обзор литературы и предлагаемый инструмент мониторинга. Curr Allergy Asthma Rep.2016; 16 (6): 44.
PubMed Статья CAS PubMed Central Google Scholar
Schenkel EJ, Skoner DP, Bronsky EA, et al.Отсутствие задержки роста у детей с круглогодичным аллергическим ринитом после одного года лечения водным назальным спреем мометазона фуроата. Педиатрия. 2000; 105 (2): E22.
CAS PubMed Статья PubMed Central Google Scholar
Аллен Д.Б., Мельцер Э.О., Леманске РФ и др. Отсутствие подавления роста у детей, получавших максимальную рекомендуемую дозу водного назального спрея флутиказона пропионата в течение одного года.Аллергия и астма. 2002; 23: 407–13.
CAS Google Scholar
Сконер Д.П., Джентиле Д., Анджелини Б. и др. Влияние интраназального триамцинолона ацетонида и интраназального флутиказона пропионата на кратковременный рост костей и ось HPA у детей с аллергическим ринитом. Ann Allergy Asthma Immunol. 2003. 90: 56–62.
CAS PubMed Статья PubMed Central Google Scholar
Gradman J, Caldwell MF, Wolthers OD. Двухнедельное перекрестное исследование для изучения влияния назального спрея флутиказона фуроата на краткосрочный рост у детей с аллергическим ринитом. Clin Ther. 2007. 29 (8): 1738–47.
CAS PubMed Статья PubMed Central Google Scholar
Агертофт Л., Педерсен С. Краткосрочная скорость роста голени и экскреция кортизола с мочой у детей, получавших циклесонид. J Allergy Clin Immunol.2005; 115: 940–5.
CAS PubMed Статья PubMed Central Google Scholar
Шет К. Оценка безопасности интраназальных стероидов при лечении аллергического ринита. Allergy Asthma Clin Immunol. 2008; 4 (3): 125.
CAS PubMed PubMed Central Статья Google Scholar
Valenzuela CV, Liu JC, Vila PM, Simon L, Doering M, Lieu J.E.Интраназальные кортикостероиды не приводят к глазным изменениям: систематический обзор и метаанализ. Ларингоскоп. 2019; 129 (1): 6–12.
CAS PubMed Статья PubMed Central Google Scholar
Састре Дж, Мосгес Р. 1 местная и системная безопасность интраназальных кортикостероидов. Исследование J Allergol Clin Immunol 2012; 1; 22 (1).
Cervin A, Andersson M. Интраназальные стероиды и перфорация перегородки — забытое осложнение? Описание хода событий и обсуждение причин.Ринология. 1998. 36: 128–32.
CAS PubMed PubMed Central Google Scholar
Интраназальные кортикостероиды при остром бактериальном синусите — Кокрановская версия для клиницистов
Кокрановская версия для клиницистов
Применение доказательств на практике
Клинический вопрос
При интраназальных кортикостероидах симптомы или острые антибиотики не разрешаются бактериальный риносинусит?
Ответ на основе доказательств
По сравнению с пациентами, не получавшими интраназальные кортикостероиды, у тех, кто их получает, наблюдается большее улучшение или разрешение симптомов через две-три недели, независимо от того, используются ли антибиотики.В одном непосредственном исследовании пациенты, принимавшие только интраназальные кортикостероиды, показали себя немного лучше, чем пациенты, принимавшие только антибиотики. Более высокие дозы интраназальных кортикостероидов работают лучше, чем более низкие. (Сила рекомендации: A, основанная на последовательных, качественных данных, ориентированных на пациента.)
Практические указатели
Хотя острый бактериальный риносинусит обычно проходит самостоятельно, до 98% визитов в офис по поводу «синусита» приводят к рецепт на антибиотик.Тем не менее, даже при использовании более строгих критериев для постановки диагноза антибиотики приносят скромную пользу.1
Эти авторы оценили роль интраназальных кортикостероидов с антибиотиками и без них в лечении острого бактериального риносинусита у детей и взрослых. Используемые интраназальные кортикостероиды включали флутиказон (Flonase), мометазон (Nasonex) и будесонид (Rhinocort). Были рассмотрены четыре двойных слепых плацебо-контролируемых исследования с участием почти 2000 пациентов, но только три из них были включены в метаанализ, поскольку одно исследование имело методологические недостатки и высокий процент выбывших.Первичный результат исчезновения симптомов или улучшения был измерен через 15 дней в одном исследовании и через 21 день в других исследованиях.
В исследовании с высоким процентом выбывших симптомы улучшались быстрее при применении интраназальных кортикостероидов по сравнению с плацебо (примерно через три-четыре дня). Мета-анализ трех других исследований показал, что пациенты, принимавшие интраназальные кортикостероиды, имели 73% -ный шанс исчезновения симптомов или улучшения по сравнению с 66% пациентов, использующих ингалятор плацебо (относительный риск = 1.11; 95% доверительный интервал от 1,04 до 1,18; количество, необходимое для лечения [NNT] = 15). В одном из исследований, в котором пациенты получали высокие дозы мометазона (400 мкг), NNT составлял 12.
Только в одном исследовании сравнивали интраназальную монотерапию кортикостероидами с монотерапией антибиотиками. В группе, принимавшей только интраназальные кортикостероиды, наблюдалось статистически значимое улучшение на 0,6 балла по 15-балльной средней шкале симптомов по сравнению с группой, принимавшей только антибиотики.
В ходе испытаний не сообщалось о серьезных побочных эффектах, а второстепенные эффекты включали носовое кровотечение, головную боль и раздражение носа.
Американская академия педиатрии обновила свои рекомендации по ведению острого бактериального риносинусита у пациентов в возрасте от 1 до 18 лет. использование интраназальных кортикостероидов. Общество инфекционных заболеваний Америки рекомендует орошение солевым раствором и / или интраназальные кортикостероиды, особенно в рефрактерных случаях или у пациентов с аллергическими симптомами в анамнезе.3 Рекомендации системы здравоохранения Мичиганского университета заявляют, что интраназальные кортикостероиды «вероятно будут эффективными». 4
Кортикостероиды, интраназальные | Лекарства, безрецептурные препараты и травы
О медицинских препаратах и болезнях
Клинический справочникMedscape — это самый авторитетный и доступный медицинский справочник для врачей и медицинских работников, доступный в Интернете и на всех основных мобильных устройствах. Весь контент бесплатный.
Клиническая информация представляет собой опыт и практические знания ведущих врачей и фармацевтов из ведущих академических медицинских центров США и всего мира.
Предоставленные темы являются всеобъемлющими и охватывают более 30 медицинских специальностей, включая:
Заболевания и состоянияБолее 6000 научно обоснованных и проверенных врачами статей о заболеваниях и состояниях организованы для быстрого и исчерпывающего ответа на клинические вопросы и предоставления подробной информации в поддержку диагностики, лечения и принятия других клинических решений. Темы богато иллюстрированы более чем 40 000 клинических фотографий, видео, диаграмм и рентгенографических изображений.
ПроцедурыБолее 1000 статей о клинических процедурах содержат четкие пошаговые инструкции и включают обучающие видео и изображения, позволяющие клиницистам освоить новейшие методы или улучшить свои навыки в процедурах, которые они выполняли ранее.
АнатомияБолее 100 статей по анатомии содержат клинические изображения и схемы основных систем и органов человеческого тела. Статьи помогают понять анатомию, связанную с лечением определенных состояний и выполнением процедур.Они также могут облегчить беседы между врачом и пациентом.
Монографии по лекарствамПредоставлено более 7100 монографий по рецептурным и безрецептурным лекарствам, а также по соответствующим фирменным лекарствам, травам и добавкам. Также включены изображения наркотиков.
Устройство для проверки взаимодействия с наркотикамиНаша программа проверки взаимодействия с лекарствами обеспечивает быстрый доступ к десяткам тысяч взаимодействий между фирменными и непатентованными лекарствами, лекарствами, отпускаемыми без рецепта, и добавками.Отнесите умеренные взаимодействия к серьезным противопоказаниям одновременно с 30 лекарствами, травами и добавками.
Формулярная информацияПолучите доступ к справочной информации по лекарствам в рамках медицинского плана при поиске конкретного лекарства и сэкономьте время и силы для вас и вашего пациента. Выберите из нашего полного списка из более чем 1800 планов страхования во всех 50 штатах США. Настройте свою учетную запись Medscape с учетом планов медицинского страхования, которые вы принимаете, чтобы необходимая вам информация сохранялась и была готова каждый раз, когда вы ищите лекарство на нашем сайте или в приложении Medscape.Легко сравнивайте статус уровня препаратов одного класса при выборе альтернативного препарата для вашего пациента.
Медицинские калькуляторыMedscape Reference содержит 129 медицинских калькуляторов, охватывающих формулы, весы и классификации. Кроме того, более 600 монографий по лекарствам в нашем справочнике по лекарственным средствам включают встроенные калькуляторы дозирования.
Коллекции изображенийСотни слайд-шоу с богатыми изображениями визуально привлекают и бросают вызов читателям, расширяя их знания как об общих, так и о необычных заболеваниях, презентациях клинических случаев и текущих противоречиях в медицине.
MEDLINEЩелкните ссылки по темам о лекарствах и заболеваниях в нашем клиническом справочнике, чтобы просмотреть клинические данные в MEDLINE. Кроме того, поищите в базе данных MEDLINE журнальные статьи.
Medscape — ведущее онлайн-направление для медицинских работников, ищущих клиническую информацию. В дополнение к клиническим справочным инструментам Medscape предлагает:
Новости медицины Узнать большеДополнительное медицинское образование Узнать больше .
