пять вопросов, на которые должен ответить врач перед принятием решения
05.02.2017
Статья в формате PDF.
Инфекции верхних дыхательных путей и среднего уха являются наиболее распространенными заболеваниями в практике отоларингологов и часто (но не всегда!) требуют назначения антибиотикотерапии. В целом на респираторные инфекции приходится около 75% амбулаторных назначений антибиотиков (S.M. Shappert, 1992), причем нередко они бывают необоснованными или неадекватными. Клиницистам важно помнить, что рациональное применение противомикробных средств является важнейшим условием не только для достижения терапевтического эффекта, но и сохранения потенциала антибиотиков для будущего с учетом неуклонно растущей проблемы антибиотикорезистентности.
Какое же использование противомикробных средств можно считать рациональным? Чтобы сделать адекватное назначение, врач должен ответить как минимум на пять перечисленных ниже вопросов.
Нужен ли антибиотик?
Большое количество случаев ЛОР-инфекций вызваны вирусами, на которые, как знают все врачи, антибиотики не действуют. Профилактическое применение антибиотиков при вирусной инфекции имеет значительно больше рисков, чем преимуществ, и поэтому считается ошибкой.
Наиболее простым вариантом определения этиологии заболевания могла бы стать лабораторная диагностика, если бы не несколько «но». Прежде всего, она требует времени, а антибиотики при острой инфекции чаще всего требуется назначать «здесь и сейчас». Экспресс-тесты, разработанные для мгновенной диагностики некоторых инфекций (например, β-гемолитического стрептококка при тонзиллофарингите и пневмококка), являются дорогостоящими, в связи с чем в нашей стране применяются редко. Кроме того, такая диагностика характеризуется достаточно высокой частотой ложноположительных результатов. Следует также помнить, что далеко не все микроорганизмы могут быть высеяны на стандартных питательных средах, в связи с чем почти в половине случаев возбудителя просто не удается идентифицировать.
Согласно рекомендациям Американского общества инфекционных болезней (IDSA) в пользу острого бактериального риносинусита свидетельствуют такие критерии (достаточно одного из трех):
- сохранение симптомов в течение ≥10 дней без каких-либо признаков клинического улучшения;
- тяжелое течение – высокая температура (≥39 °C), гнойные выделения из носа и/или лицевая боль, которые сохраняются не менее 3-4 дней подряд с начала болезни;
- ухудшение клинической картины – повторное повышение температуры тела, появление головной боли или усиление выделений из носа после типичной вирусной инфекции верхних дыхательных путей, которая длилась 5-6 дней с признаками улучшения.
Признаками острого гнойного среднего отита могут быть: резкое ухудшение общего состояния пациента, повышение температуры тела до фебрильных цифр, резкое усиление боли, ее иррадиация по ветвям тройничного нерва в зубы, шею, глотку, глаз (так называемая дистантная оталгия), снижение слуха, усиление шума в ухе. Отоскопически наряду с яркой гиперемией и отечностью определяется выбухание барабанной перепонки различной степени выраженности, возможна перфорация барабанной перепонки с истечением гноя в наружный слуховой проход.
Отоскопически наряду с яркой гиперемией и отечностью определяется выбухание барабанной перепонки различной степени выраженности, возможна перфорация барабанной перепонки с истечением гноя в наружный слуховой проход.
Тонзиллофарингит в большинстве случаев является вирусным, но один из его бактериальных вариантов – стрептококковая ангина –считается абсолютным показанием для антибиотикотерапии. Для ее клинической диагностики и принятия решения относительно назначения противомикробных препаратов рекомендуется использовать критерии, предложенные W.J. McIsaac и соавт. (2000): температура тела выше 38 °C; отсутствие кашля; аденопатия передних шейных лимфоузлов; отек миндалин и/или наличие отделяемого на миндалинах; возраст младше 15 лет. Наличие каждого из перечисленных критериев оценивается в 1 балл. Если больной старше 45 лет, 1 балл вычитается из общей суммы. При сумме 0-1 балл вероятность стрептокковой ангины близка к нулю и антибиотики не показаны. При оценке 2 или 3 балла риск составляет 17 и 35% соответственно, поэтому для назначения антибиотика требуется положительный результат бактериологического или серологического анализа на стрептококк.
Какой антибиотик будет эффективным?
Как было отмечено выше, микробиологическая диагностика не является рутинной процедурой при внебольничных ЛОР-инфекциях, поэтому выбор антибиотика, когда врач считает его оправданным, осуществляется эмпирическим путем. Это значит, что препарат подбирают с учетом основных возбудителей, их природной чувствительности к тем или иным антибиотикам, данных по приобретенной устойчивости патогенов (глобальных, региональных, локальных), а также фармакокинетических и фармакодинамических характеристик.
Наиболее значимыми бактериальными возбудителями острого гнойного среднего отита и острого бактериального синусита являются Streptococcus pneumoniae, Haemophilus influenzae и Moraxella catarrhalis, а тонзиллофарингита – Streptococcus pyogenes.
Обязательно следует учитывать и фактор антибиотикорезистентности. Неадекватным выбором при инфекциях дыхательных путей и среднего уха являются тетрациклины и ко-тримоксазол ввиду очень высокого уровня устойчивости к ним возбудителей. Также в последние годы стремительно растет резистентность S. pneumoniae как к макролидам, так и к аминопенициллинам, в том числе защищенным. В то же время по-прежнему очень высокой активностью в отношении пневмококка и гемофильной палочки обладают цефалоспорины III поколения (более 95%).
В то же время по-прежнему очень высокой активностью в отношении пневмококка и гемофильной палочки обладают цефалоспорины III поколения (более 95%).
Важно учитывать фармакодинамические и фармакокинетические характеристики антибиотиков, оказывающие значительное влияние на клиническую эффективность, которая не всегда четко коррелирует с активностью in vitro. Выбранный препарат должен обладать высокой биодоступностью, хорошо проникать и накапливаться в высоких концентрациях в очаге инфекции (слизистой оболочке и секрете околоносовых пазух, полости среднего уха, миндалинах и т.д.).
Необходимо, чтобы препарат не только обладал подходящими свойствами, но и имел достаточную доказательную базу эффективности, полученную в контролируемых клинических исследованиях.
Не стоит забывать и о правиле пациент-специфической ротации: если в течение последних 3 мес у конкретного больного уже применялся антибиотик, следует выбрать препарат другой группы.
Хорошим выбором для лечения бактериального отита, синусита и тонзиллофарингита может быть цефподоксим – пероральный цефалоспорин III поколения с широким спектром антибактериальной активности. Цефподоксим активен в отношении S. pneumoniae (чувствительных к пенициллину штаммов и штаммов с умеренной устойчивостью), H. influenzae и M. catarrhalis (включая штаммы, продуцирующие β-лактмазы), S. pyogenes и др. В исследовании B. Fulton и C.M. Perry (2001) цефподоксим показал in vitro более высокую активность в отношении S. pneumoniae, чем другие цефалоспорины (цефаклор, цефуроксим, цефпрозил, цефиксим и лоракарбеф). Препарат характеризуется высокой биодоступностью при приеме per os и накапливается в очагах инфекции ЛОР-органов в высокой концентрации, значительно превышающей минимально подавляющую концентрацию (МПК) для основных возбудителей.
Цефподоксим активен в отношении S. pneumoniae (чувствительных к пенициллину штаммов и штаммов с умеренной устойчивостью), H. influenzae и M. catarrhalis (включая штаммы, продуцирующие β-лактмазы), S. pyogenes и др. В исследовании B. Fulton и C.M. Perry (2001) цефподоксим показал in vitro более высокую активность в отношении S. pneumoniae, чем другие цефалоспорины (цефаклор, цефуроксим, цефпрозил, цефиксим и лоракарбеф). Препарат характеризуется высокой биодоступностью при приеме per os и накапливается в очагах инфекции ЛОР-органов в высокой концентрации, значительно превышающей минимально подавляющую концентрацию (МПК) для основных возбудителей.
Эффективность цефподоксима была доказана в ряде клинических исследований, причем во многих из них он превосходил препараты сравнения. Так, например, цефподоксим продемонстрировал достоверно более высокую клиническую эффективность и частоту излечения при остром гнойном отите, чем при цефиксиме (Cohen et al., 1994) и амоксициллин/клавуланат (Gehanno et al.
Какой из эффективных вариантов будет наиболее безопасным?
Предлагаемые для лечения инфекций ЛОР-органов классы антибиотиков характеризуются достаточно высокой безопасностью. Однако при выборе препарата обязательно следует учитывать особенности пациента: возраст, состояние почек и печени, аллергологический анамнез, прием других лекарственных средств, сопутствующие заболевания и особые состояния (беременность, лактация и др.). В разных клинических ситуациях приоритеты по безопасности будут отличаться.
Еще один важный аспект – переносимость. Некоторые побочные эффекты не угрожают здоровью и жизни пациента, но существенно снижают ее качество и ухудшают комплайенс. Речь в первую очередь идет о гастроинтестинальных нежелательных явлениях. Поскольку цефподоксим является пролекарством, превращающимся в активный метаболит уже в кровеносном русле, он не оказывает отрицательного влияния на микрофлору кишечника. Кроме того, в отличие от азитромицина и клавуланата он не стимулирует мотилиновые рецепторы кишечника, поэтому частота диареи на фоне терапии цефподоксимом значительно ниже (J. Meenakshi et al., 2015; K. Hanke et al., 2002).
Речь в первую очередь идет о гастроинтестинальных нежелательных явлениях. Поскольку цефподоксим является пролекарством, превращающимся в активный метаболит уже в кровеносном русле, он не оказывает отрицательного влияния на микрофлору кишечника. Кроме того, в отличие от азитромицина и клавуланата он не стимулирует мотилиновые рецепторы кишечника, поэтому частота диареи на фоне терапии цефподоксимом значительно ниже (J. Meenakshi et al., 2015; K. Hanke et al., 2002).
Как обеспечить хороший комплайенс?
Каким бы правильным не был выбор антибиотика, его эффективность не будет достаточно высокой при низкой приверженности пациента к лечению. Хороший комплайенс, а следовательно, и высокую эффективность терапии обеспечивают удобство применения препарата, в том числе простая схема (1-2 раза в сутки), непродолжительный курс приема (3-7 дней), оптимальная для каждого конкретного случая лекарственная форма, а также хорошая переносимость, о чем говорилось ранее.
Большой ошибкой при лечении инфекций легкой и средней тяжести при отсутствии нарушений сознания и проблем с глотанием у пациента является парентеральное введение антибиотиков, ведь эффективность современных пероральных антибиотиков нисколько не уступает таковой парентеральных. Так, цефподоксим сопоставим с цефтриаксоном по эффективности (Р. Zuck et al., 1990), однако значительно превосходит его по удобству применения.
Кроме того, немаловажную роль в нынешних социально-экономических условиях играет стоимость препарата. Доступным для широкого круга пациентов является препарат цефподоксима Докцеф. Он представлен в двух лекарственных формах – таблетки и суспензия – что делает удобным лечение у пациентов разных возрастных групп.
Какой должна быть продолжительность лечения?
Длительность антибиотикотерапии является важным фактором, влияющим на селекцию устойчивых штаммов возбудителей. Нежелательным является как досрочное прекращение лечения, о чем врач должен предупредить пациента, так и слишком длительный курс. Оптимальная продолжительность курса антибиотикотерапии при инфекциях ЛОР-органов при использовании большинства антибиотиков, в том числе цефподоксима, составляет 5-7 дней. Однако следует помнить, что через 48-72 ч после назначения антибиотика нужно оценить его эффективность и в случае необходимости скорректировать схему лечения.
Оптимальная продолжительность курса антибиотикотерапии при инфекциях ЛОР-органов при использовании большинства антибиотиков, в том числе цефподоксима, составляет 5-7 дней. Однако следует помнить, что через 48-72 ч после назначения антибиотика нужно оценить его эффективность и в случае необходимости скорректировать схему лечения.
Таким образом, правильный выбор антибиотика, пути его введения и длительность курса лечения являются важнейшими условиями эффективности терапии инфекционных заболеваний, в том числе верхних дыхательных путей и среднего уха. Если врач считает целесообразным назначение цефалоспоринов, то хорошим выбором может быть препарат Докцеф (цефподоксим), характеризующийся широким спектром противомикробного действия, включающего основных возбудителей инфекций ЛОР-органов, доказанной клинической эффективностью, высоким профилем безопасности, удобством приема (перорально) и отличным соотношением качества и стоимости.
Подготовила Наталья Мищенко
- Номер:
- Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 4 (36), грудень 2016 р.
22.04.2023 ПедіатріяПульмонологія та оториноларингологіяПозалікарняні пневмонії у дітей
Лікарі різних спеціальностей мають бути обізнані щодо основних клінічних проявів позалікарняної пневмонії (ПП) з метою її ранньої діагностики і призначення лікування пацієнтам із ПП для попередження розвитку ускладнень та запобігання смертності дітей….
22.04.2023 ПедіатріяПульмонологія та оториноларингологіяСучасні аспекти терапії гострого риносинуситу в практиці педіатра
Гострий риносинусит (ГРС) є надзвичайно актуальною проблемою сучасної педіатрії. Кількість випадків цього захворювання, незважаючи на успіхи сучасної медицини, продовжує неухильно зростати з кожним роком. Причиною розвитку цієї патології найчастіше є вірусна інфекція, однак при невчасному та неефективному лікуванні з часом може приєднатися і бактеріальна флора. Терапевтична тактика інфекційних захворювань верхніх дихальних шляхів на тлі вірусної інфекції є симптоматичною та полягає у використанні протизапальних, антигістамінних, аналгетичних засобів, у тому числі й рослинного походження….
Кількість випадків цього захворювання, незважаючи на успіхи сучасної медицини, продовжує неухильно зростати з кожним роком. Причиною розвитку цієї патології найчастіше є вірусна інфекція, однак при невчасному та неефективному лікуванні з часом може приєднатися і бактеріальна флора. Терапевтична тактика інфекційних захворювань верхніх дихальних шляхів на тлі вірусної інфекції є симптоматичною та полягає у використанні протизапальних, антигістамінних, аналгетичних засобів, у тому числі й рослинного походження….
17.04.2023 Пульмонологія та оториноларингологіяШвидке й ефективне полегшення болю в пацієнтів із риногенним болем: очевидні та приховані переваги
Своєчасне та ефективне лікування гострого болю є одним із найважливіших завдань сучасної медицини. Сьогодні чимало пацієнтів, які звертаються по медичну допомогу, страждають через неконтрольований біль. Добре відомо, що некупіруваний (або несвоєчасно купіруваний) гострий біль не лише значно погіршує якість життя пацієнтів, а й зумовлює зростання ризику низки ускладнень. Одним із найпоширеніших видів інтенсивного болю, з яким доводиться мати справу лікарю загальної практики, є головний біль за гострого риносинуситу (РС). Саме тому клініцисти повинні добре розуміти основні підходи до лікування цього типу болю, а також прогностичне значення швидкого й ефективного знеболення….
Сьогодні чимало пацієнтів, які звертаються по медичну допомогу, страждають через неконтрольований біль. Добре відомо, що некупіруваний (або несвоєчасно купіруваний) гострий біль не лише значно погіршує якість життя пацієнтів, а й зумовлює зростання ризику низки ускладнень. Одним із найпоширеніших видів інтенсивного болю, з яким доводиться мати справу лікарю загальної практики, є головний біль за гострого риносинуситу (РС). Саме тому клініцисти повинні добре розуміти основні підходи до лікування цього типу болю, а також прогностичне значення швидкого й ефективного знеболення….
24.03.2023 Пульмонологія та оториноларингологіяТерапія та сімейна медицинаГоловний і лицевий біль при риносинуситі: диференційна діагностика та лікування
Запальні захворювання приносових пазух часто супроводжуються больовими відчуттями – головним і лицевим болем [1]. Неконтрольований гострий біль значно знижує якість життя пацієнтів із цими захворюваннями: спричиняє психоемоційні розлади, знижує працездатність і соціальну активність, сприяє хронізації больового синдрому і збільшує вартість лікування [2]. Призначаючи знеболювальний засіб пацієнту з риносинуситом (РС), варто враховувати не лише аналгетичну ефективність препарату, а й швидкість початку дії, частоту побічних ефектів, вплив на основні ланки патогенезу захворювання тощо….
Неконтрольований гострий біль значно знижує якість життя пацієнтів із цими захворюваннями: спричиняє психоемоційні розлади, знижує працездатність і соціальну активність, сприяє хронізації больового синдрому і збільшує вартість лікування [2]. Призначаючи знеболювальний засіб пацієнту з риносинуситом (РС), варто враховувати не лише аналгетичну ефективність препарату, а й швидкість початку дії, частоту побічних ефектів, вплив на основні ланки патогенезу захворювання тощо….
Антибиотик первого выбора в практике оториноларинголога
Несмотря на прогресс современного общества, доступность информации и медицинской помощи, уровень заболеваемости во всем мире продолжает увеличиваться. Исключением, к сожалению, не являются и ЛОР-заболевания. В связи с этим возникает необходимость разработки и внедрения новых методов профилактики, диагностики и лечения, которые служили бы подспорьем врачу-оториноларингологу в его повседневной практике. Последний из перечисленных аспектов — лечение — нашел свое отражение в проведенной 13–14 октября в г. Ялте (АР Крым) конференции на тему «Новые технологии в оториноларингологии. Современные методы фармакотерапии в оториноларингологии».
Последний из перечисленных аспектов — лечение — нашел свое отражение в проведенной 13–14 октября в г. Ялте (АР Крым) конференции на тему «Новые технологии в оториноларингологии. Современные методы фармакотерапии в оториноларингологии».
Среди множества вопросов внимание было уделено и антибиотикотерапии ЛОР-заболеваний — в своих докладах известные ученые поделились опытом с практикующими врачами и коллегами. Прозвучавшие сообщения нашли краткое отражение в настоящем обзоре.
В ходе конференции профессор Владимир Васильевич Березнюк (г. Днепропетровск) выступил с докладом, посвященным антибактериальной терапии в лечении острых риносинуситов. Профессор напомнил о диагностических признаках риносинусита, предложенных Европейским ринологическим обществом (European Rhinologic Society). Клинические проявления заболевания представлены прежде всего воспалением слизистой носа и околоносовых пазух, характеризующимся двумя или более симптомами, одним из которых является заложенность носа либо выделения из носа (выделения через ноздри или стекание выделений в носоглотку). Пациента могут беспокоить боль или давление в области лица, снижение или отсутствие обоняния. Эндоскопическая картина риносинусита характеризуется наличием полипов
Пациента могут беспокоить боль или давление в области лица, снижение или отсутствие обоняния. Эндоскопическая картина риносинусита характеризуется наличием полипов
и/или слизисто-гнойного содержимого в среднем носовом ходу и/или отека/обструкции прежде всего в среднем носовом ходу. При выполнении компьютерной томографии могут быть отмечены изменения слизистой оболочки в пределах остеомеатального комплекса и/или пазухах.
По длительности течения синуситы делят на острые — до 4 недель, подострые — от 4 до 12 недель, хронические — более 12 недель. Острым рецидивирующим синусит считают в том случае, если отмечают 4 или более эпизодов заболевания в год, каждый эпизод длится свыше 7–10 дней, и при этом отсутствуют признаки хронического синусита. При обострении хронического синусита наблюдается усиление его симптомов, а после лечения состояние больного возвращается к тому же уровню, что и до обострения.
Как свидетельствуют статистические данные, острый риносинусит относится к самым распространенным заболеваниям ЛОР-органов. Так, в Европе частота случаев острого риносинусита среди взрослого населения составляет от 1 до 5 % в год. По данным разных авторов, в Украине от этого заболевания страдает 10–30 % населения. В целом за последние 10 ет заболеваемость риносинуситами возросла в 3 раза.
Так, в Европе частота случаев острого риносинусита среди взрослого населения составляет от 1 до 5 % в год. По данным разных авторов, в Украине от этого заболевания страдает 10–30 % населения. В целом за последние 10 ет заболеваемость риносинуситами возросла в 3 раза.
При высокой распространенности риносинуситов, равно как и неуклонном росте заболеваемости, требуется своевременная адекватная терапия. В лечении больных с риносинуситами выделяют два основных направления: эмпирическую антибиотикотерапию и восстановление дренирования, аэрации, деятельности мукоцилиарной транспортной системы. Выбор того или иного вида лекарственных препаратов во многом зависит от степени рекомендаций терапии, базирующейся, в свою очередь, на уровне доказательности разных типов клинических исследований.
Интерес представляет тот факт, что при остром риносинусите рекомендации назначения антибиотиков имеют степень достоверности А, основанную на метаанализе данных 49 клинических исследований уровня доказательности Ia. Для сравнения: топические стероиды имеют степень рекомендаций A, уровень доказательности — Ib; пероральные антигистаминные средства у пациентов с аллергией — B/Ib, деконгестанты — D/Ib и т.д.
Для сравнения: топические стероиды имеют степень рекомендаций A, уровень доказательности — Ib; пероральные антигистаминные средства у пациентов с аллергией — B/Ib, деконгестанты — D/Ib и т.д.
Антибиотикотерапия относится к этиотропным видам лечения, поскольку в отличие от симптоматической, противовоспалительной и других видов терапии направлена на ликвидацию тех микроорганизмов, которые являются причиной локального воспаления. Известно, что прервать череду рецидивов можно с помощью адекватного антибиотика, который обеспечит не только клинический, но и бактериологический эффект. Цель антибиотикотерапии при остром риносинусите сводится к полной эрадикации возбудителя из синуса, снижению частоты осложнений и предупреждению перехода заболевания в хронический синусит.
Лечение, которое не приводит к полной эрадикации возбудителя, способствует рецидивированию синуситов, отитов, тонзиллофарингитов и других заболеваний. А это, в свою очередь, приводит к селекции и распространению резистентных патогенных микроорганизмов с исходами в пансинусит, гайморит и этмоидит, что неизбежно снижает эффективность последующего лечения.
Таким образом, главная цель антибиотикотерапии при риносинуситах — полная эрадикация возбудителя. Но нужно помнить, что неадекватная стартовая терапия приводит к развитию множества осложнений, как орбитальных (негнойный и гнойный периостит, абсцесс век, флегмона глазницы и т.д.), так и внутричерепных (арахноидит, субдуральный абсцесс, абсцесс мозга и т.д.). Учитывая вышесказанное, не стоит назначать антибиотики сверхширокого спектра действия, которые предназначены для борьбы с госпитальными инфекциями в условиях стационара. Нет необходимости использовать гентамицин и линкомицин из-за неадекватного спектра активности и опасных побочных эффектов, а также фторхинолоны, запрещенные к приему у детей. Не нужно назначать инъекционные формы антибиотиков на догоспитальном этапе. При выборе антибиотика для эмпирической терапии ЛОР-инфекций необходимо отдавать предпочтение препаратам, которые высокоактивны в отношении предполагаемых возбудителей (S.pneumoniae, M.catarrhalis, H. influenzae), создают эффективные терапевтические концентрации в тканях и жидкостях органов дыхания с минимальным риском индукции резистентности. Препараты должны обладать оптимальным профилем безопасности, оптимальным соотношением «цена/качество», быть удобными в применении.
influenzae), создают эффективные терапевтические концентрации в тканях и жидкостях органов дыхания с минимальным риском индукции резистентности. Препараты должны обладать оптимальным профилем безопасности, оптимальным соотношением «цена/качество», быть удобными в применении.
Как свидетельствуют данные исследований, три наиболее значимых для развития ЛОР-заболеваний микроорганизма — S.pneumoniae, M.catarrhalis, H.influenzae имеют очень высокую чувствительность к амоксициллин/клавуланату (Аугментин) — от 95,5 до 100 % (рис. 1). Результаты международного мониторингового исследования Alexander Project, проведенного в 1992–2001 гг., послужили основанием того, что Аугментин рекомендован в качестве препарата первого выбора для лечения инфекций респираторного тракта.
Ожидаемая клиническая эффективность Аугментина при остром бактериальном риносинусите у взрослых и детей составляет более 90 %.
Аугментин отвечает основным требованиям, предъявляемым к антибиотикам, предназначенным для лечения ЛОР-заболеваний. Этот препарат обладает широким спектром противомикробной активности — грамположительные и грамотрицательные бактерии, анаэробы, что не характерно, например, для незащищенных макролидов и цефалоспоринов 1-го и 2-го поколений. Аугментин не разрушается β-лактамазами (в отличие от амоксициллина и некоторых цефалоспоринов), создает высокие концентрации в тканях и полостях организма и проявляет бактерицидную активность (в отличие от макролидов). Для Аугментина (в отличие от макролидов и фторхинолонов) характерно наименьшее количество межлекарственных взаимодействий. Аугментин не имеет возрастных ограничений к применению. Немаловажно и то, что накоплен значительный опыт применения данного препарата (27 лет).
Этот препарат обладает широким спектром противомикробной активности — грамположительные и грамотрицательные бактерии, анаэробы, что не характерно, например, для незащищенных макролидов и цефалоспоринов 1-го и 2-го поколений. Аугментин не разрушается β-лактамазами (в отличие от амоксициллина и некоторых цефалоспоринов), создает высокие концентрации в тканях и полостях организма и проявляет бактерицидную активность (в отличие от макролидов). Для Аугментина (в отличие от макролидов и фторхинолонов) характерно наименьшее количество межлекарственных взаимодействий. Аугментин не имеет возрастных ограничений к применению. Немаловажно и то, что накоплен значительный опыт применения данного препарата (27 лет).
В заключение докладчик отметил, что независимо от тяжести острого риносинусита могут быть использованы пероральные формы Аугментина (таблетки или сироп) либо парентеральные формы (порошки для инъекций). Через 48–72 ч после начала антибиотикотерапии отмечается уменьшение выраженности лихорадки, интоксикации, одышки, улучшаются лабораторные показатели, что свидетельствует об улучшении состояния больного.
В докладе профессора Анатолия Лукьяновича Косаковского (г. Киев) внимание было уделено роли защищенных аминопенициллинов в лечении острых средних отитов у детей.
Докладчик отметил, что острые средние отиты опасны прежде всего своими осложнениями: потерей слуха, внутричерепными осложнениями, развитием сепсиса, переходом в рецидивирующую или хроническую форму. С учетом этого перед врачом стоит задача вовремя начать адекватную терапию данного заболевания. К числу обязательных средств, назначаемых при острых средних отитах, относятся антибиотики и сосудосуживающие препараты. По показаниям может быть назначена симптоматическая терапия, выполнена миринготомия/тимпаноцентез, проведен курс физиотерапевтического лечения.
Задумываясь о назначении антибиотика, врач должен найти ответы на следующие вопросы: нужен ли антибиотик в данной ситуации? Если да, то какой антибиотик выбрать? Какую форму препарата использовать: пероральную или инъекционную? Какова должна быть длительность приема препарата? Ответ на первый из поставленных вопросов представлен в табл. 1.
1.
Следует подчеркнуть, что целью антибиотикотерапии является полная эрадикация возбудителя из организма больного. В том случае, если лечение не приводит к эрадикации, имеется высокий риск развития осложнений, перехода заболевания в хроническую форму, селекции и распространения резистентных патогенных микроорганизмов.
Как и в предыдущем докладе, было отмечено, что «идеальный» антибиотик должен обладать высокой активностью в отношении предполагаемых возбудителей ЛОР-заболеваний, создавать терапевтические концентрации в тканях и жидкостях уха, не индуцировать резистентность у микроорганизмов, иметь оптимальный профиль безопасности, быть удобным в применении и отличаться оптимальным соотношением стоимости и эффективности.
Из числа возможных антибиотиков, назначаемых при остром среднем отите, особого внимания заслуживает Аугментин (амоксициллин/клавуланат). Данный препарат обладает значительной широтой спектра действия, а в отношении типичных возбудителей ЛОР-заболеваний проявляет необычайно высокую активность. Например, согласно результатам исследования PROTEKT, чувствительность S.pneumoniae к Аугментину составляет 97,5 %.
Например, согласно результатам исследования PROTEKT, чувствительность S.pneumoniae к Аугментину составляет 97,5 %.
Аугментин устойчив к воздействию β-лактамаз. В жидкости среднего уха данный препарат создает концентрации, достаточные для эффективной эрадикации возбудителей. Например, для S.рneumoniae и H.influenzae коэффициенты эрадикации составляют около 90 % (рис. 2).
Во многих международных рекомендациях Аугментин назван препаратом первого выбора для лечения инфекций респираторного тракта. Примеры руководств по использованию Аугментина при острых средних отитах представлены в табл. 2.
Аугментин имеет ряд преимуществ перед другими классами антибиотиков. По сравнению с незащищенными пенициллинами у Аугментина лучше выражена клиническая и микробиологическая эффективность (за счет «защищенности»), нет β-лактамазной резистентности, более широкий спектр антимикробного действия, большая экономическая выгода при проведении курса эффективной эмпирической антибиотикотерапии. По сравнению с макролидами Аугментин обладает бактерицидным эффектом, создает высокую концентрацию в месте локализации инфекции, обладает большим спектром антимикробного действия, взаимодействует с некоторыми лекарственными препаратами, разрешен к применению у кормящих женщин и новорожденных, относится к категории В применения у беременных. Наконец, по сравнению с цефалоспоринами 1–2-го поколений Аугментин более активен в отношении ведущих патогенов инфекций ЛОР-органов, устойчив к воздействию β-лактамаз, имеет более широкий спектр активности по сравнению с цефалоспоринами 1–2-го поколений и не уступает цефалоспоринам 3–4-го поколений, экономически выгоден, представлен в различных формах выпуска и дозировках.
По сравнению с макролидами Аугментин обладает бактерицидным эффектом, создает высокую концентрацию в месте локализации инфекции, обладает большим спектром антимикробного действия, взаимодействует с некоторыми лекарственными препаратами, разрешен к применению у кормящих женщин и новорожденных, относится к категории В применения у беременных. Наконец, по сравнению с цефалоспоринами 1–2-го поколений Аугментин более активен в отношении ведущих патогенов инфекций ЛОР-органов, устойчив к воздействию β-лактамаз, имеет более широкий спектр активности по сравнению с цефалоспоринами 1–2-го поколений и не уступает цефалоспоринам 3–4-го поколений, экономически выгоден, представлен в различных формах выпуска и дозировках.
Исходя из вышеизложенного становится понятным, почему во многих странах Аугментин является золотым стандартом в лечении острых отитов среднего уха. Наиболее часто используемые режимы дозирования Аугментина представлены в табл. 3.
Профессор обратил внимание и на тот факт, что острый средний отит является наиболее частой причиной назначения антибиотиков у детей. Согласно статистическим данным, более 90 % детей хотя бы 1 раз переносят острый средний отит, при этом у 19–62 % детей это заболевание проявляется в возрасте до 3 лет. Пик заболеваемости острым средним отитом приходится на 6–18-й месяцы жизни.
Согласно статистическим данным, более 90 % детей хотя бы 1 раз переносят острый средний отит, при этом у 19–62 % детей это заболевание проявляется в возрасте до 3 лет. Пик заболеваемости острым средним отитом приходится на 6–18-й месяцы жизни.
Столь высокий уровень заболеваемости требует от врача ежедневного принятия решения о том, какая же форма антибиотика (пероральная или инъекционная) должна быть назначена на амбулаторном этапе. Пероральные формы Аугментина имеют высокую биодоступность — до 90 % и создают высокие минимальные подавляющие концентрации для ведущих респираторных патогенов (пневмококка, гемофильной палочки и моракселлы), что позволяет прийти к однозначному выводу о том, что на догоспитальном этапе предпочтение должно быть отдано пероральным формам Аугментина.
Следует помнить: в отличие от генерических копий, назначаемых 3 раза в день, Аугментин в виде сиропа назначается 2 раза в день, что позволяет значительно сократить затраты на лечение и снизить количество побочных эффектов в 2,8 раза.
Докладчик также отметил, что Аугментин показан пациентам любой возрастной категории, даже новорожденным.
Доклад профессора Василия Ивановича Поповича (г. Ивано-Франковск) был посвящен особенностям антибактериальной терапии на фоне наиболее распространенных соматических заболеваний.
Антибактериальная терапия является одним из наиболее популярных видов лечения, о чем свидетельствует частота назначения средств данной группы. Так, в амбулаторных условиях антибиотики получают 15 % больных, в условиях стационара — более 30 % больных. Ввиду столь высокой назначаемости вполне закономерно возникает вопрос: всегда ли обеспечивается адекватность антибактериальной терапии?
Критерии выбора антибиотика для антибактериальной эмпирической терапии включают высокую активность препарата в отношении потенциальных возбудителей, создание терапевтических концентраций в органах-мишенях, минимальную индукцию резистентности, приемлемую безопасность, хороший комплайенс, оптимальное соотношение между стоимостью и эффективностью.
При оценке безопасности того или иного антибиотика необходимо учитывать возможное побочное действие, склонность больных к развитию аллергических реакций, наличие сопутствующих заболеваний (почек, печени, сахарного диабета, нарушений ритма сердца и т.д.) и беременности, возможные взаимодействия с другими лекарственными средствами. Одно из главных условий назначения антибиотикотерапии — рациональный баланс между достижением наибольшего эффекта и обеспечением максимальной безопасности.
Необходимо помнить, что резистентность к антибиотикотерапии определяется не только характеристиками микрофлоры (чувствительностью к конкретному антибиотику), но и состоянием макроорганизма в целом. Физиологические и патофизиологические особенности макроорганизма могут сужать терапевтический интервал и, как следствие, увеличивать количество побочных реакций.
В современных условиях при назначении антибактериальной терапии воспалительных заболеваний ЛОР-органов общепринято использовать эмпирический подход. Как правило, выбирать приходится между пенициллинами, цефалоспоринами, макролидами и фторхинолонами. Выбор осложняется тем обстоятельством, что у больных могут наблюдаться сопутствующие заболевания со стороны сердечно-сосудистой системы (аритмии, ишемическая болезнь сердца, тромбофлебиты), эндокринной системы (сахарный диабет), дыхательной системы (обструктивные заболевания легких), центральной нервной системы, костной системы и т.д. Безопасность антибактериальной терапии при сопутствующей патологии зависит от потенциальных взаимодействий антибиотика с другими препаратами.
Как правило, выбирать приходится между пенициллинами, цефалоспоринами, макролидами и фторхинолонами. Выбор осложняется тем обстоятельством, что у больных могут наблюдаться сопутствующие заболевания со стороны сердечно-сосудистой системы (аритмии, ишемическая болезнь сердца, тромбофлебиты), эндокринной системы (сахарный диабет), дыхательной системы (обструктивные заболевания легких), центральной нервной системы, костной системы и т.д. Безопасность антибактериальной терапии при сопутствующей патологии зависит от потенциальных взаимодействий антибиотика с другими препаратами.
Например, при заболеваниях костной и сердечно-сосудистой систем очень часто назначают нестероидные противовоспалительные препараты. Если одновременно будут назначены некоторые фторхинолоны, то увеличится риск развития судорог и нарушения сознания. При ряде заболеваний центральной нервной системы используют противосудорожные средства — карбамазепин и вальпроевую кислоту. Сопутствующее назначение ряда макролидов приводит к повышению их концентрации, что может привести к развитию нежелательных реакций.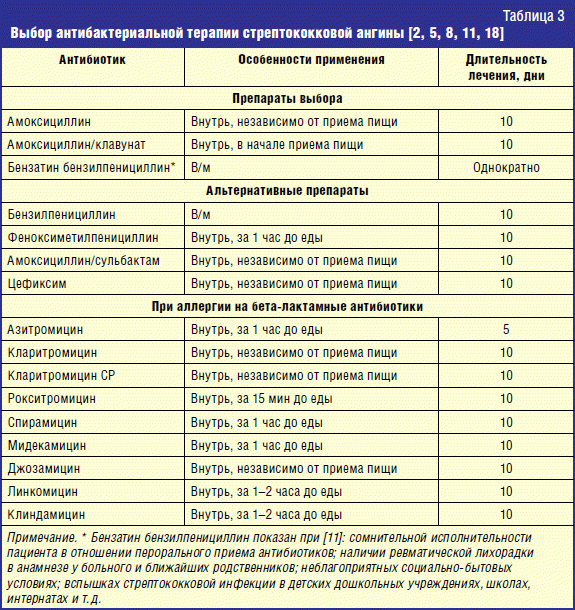 В эндокринологической практике используют инсулин и сахароснижающие препараты. Использование некоторых фторхинолонов совместно с инсулином или сахароснижающими средствами может привести к повышению или понижению содержания сахара в крови. При заболеваниях дыхательной системы совместное назначение макролидов или фторхинолонов с теофиллином существенно увеличивает концентрацию последнего, что может сопровождаться тошнотой, рвотой, судорогами и апноэ. При заболеваниях сердечно-сосудистой системы назначают пероральные антикоагулянты, гепарин, тромболитики и ингибиторы агрегации тромбоцитов. Применение цефалоспоринов усиливает эффекты этих препаратов, что приводит к риску развития кровотечений. Макролиды приводят к росту концентрации ловастатина и симвастатина, используемых для лечения дислипидемий. В результате повышается риск развития рабдомиолиза. Макролиды и фторхинолоны усиливают эффекты варфарина, существенно увеличивая протромбиновое время. Макролиды увеличивают в крови концентрацию сердечного гликозида дигоксина, что может в ряде случаев привести к развитию гликозидной интоксикации.
В эндокринологической практике используют инсулин и сахароснижающие препараты. Использование некоторых фторхинолонов совместно с инсулином или сахароснижающими средствами может привести к повышению или понижению содержания сахара в крови. При заболеваниях дыхательной системы совместное назначение макролидов или фторхинолонов с теофиллином существенно увеличивает концентрацию последнего, что может сопровождаться тошнотой, рвотой, судорогами и апноэ. При заболеваниях сердечно-сосудистой системы назначают пероральные антикоагулянты, гепарин, тромболитики и ингибиторы агрегации тромбоцитов. Применение цефалоспоринов усиливает эффекты этих препаратов, что приводит к риску развития кровотечений. Макролиды приводят к росту концентрации ловастатина и симвастатина, используемых для лечения дислипидемий. В результате повышается риск развития рабдомиолиза. Макролиды и фторхинолоны усиливают эффекты варфарина, существенно увеличивая протромбиновое время. Макролиды увеличивают в крови концентрацию сердечного гликозида дигоксина, что может в ряде случаев привести к развитию гликозидной интоксикации. Прием фторхинолонов совместно с противоаритмическими средствами (прокаинамид, амиодарон) удлиняет интервал QT, что может привести к угрожающим жизни желудочковым экстрасистолам.
Прием фторхинолонов совместно с противоаритмическими средствами (прокаинамид, амиодарон) удлиняет интервал QT, что может привести к угрожающим жизни желудочковым экстрасистолам.
В связи с вышеизложенным следует особо подчеркнуть, что Аугментин не взаимодействует ни с одним из изоферментов системы цитохрома Р-450. Благодаря этому для него характерно наименьшее количество лекарственных взаимодействий. При этом в отличие от фторхинолонов и макролидов у Аугментина нет ни одного лекарственного взаимодействия, потенциально опасного для жизни.
Подводя итоги своего доклада, профессор отметил, что среди препаратов основных групп, используемых для эмпирической антибиотикотерапии воспалительных заболеваний ЛОР-органов, наилучшим профилем безопасности обладают β -лактамные антибиотики. При использовании Аугментина существует минимальный риск развития осложнений вследствие межлекарственных взаимодействий у пациентов с сопутствующей патологией, принимающих препараты других классов. Все сказанное позволяет позиционировать Аугментин как препарат выбора для пациентов с ЛОР-заболеваниями.
Подготовил Андрей Савустьяненко
Антибиотики и синусит | Pediatric Ear, Nose, & Throat Specialist Of Illinois
Антибиотик — это растворимое вещество, полученное из плесени или бактерии, которое подавляет рост других микроорганизмов.
Первым антибиотиком был пенициллин, открытый Александром Флемингом в 1929 году, но только во время Второй мировой войны эффективность антибиотиков была признана, и для их производства были разработаны широкомасштабные процессы ферментации.
Острый синусит является одним из многих заболеваний, которые могут быть вызваны бактериальной инфекцией. Однако важно помнить, что простуда, аллергия и раздражители окружающей среды, которые встречаются чаще, чем бактериальный синусит, также могут вызывать проблемы с носовыми пазухами. Антибиотики эффективны только против проблем с носовыми пазухами, вызванных бактериальной инфекцией.
Следующие симптомы могут указывать на наличие бактериальной инфекции в носовых пазухах:
- Боль в щеках или верхних задних зубах
- Обильные ярко-желтые или зеленые выделения из носа в течение более 10 дней
- Нет облегчения от деконгестантов и/или
- Симптомы, которые ухудшаются, а не улучшаются после того, как простуда прошла.
Состояние большинства пациентов с клиническим диагнозом острого синусита, вызванного бактериальной инфекцией, улучшается без лечения антибиотиками. Сначала специалист предложит соответствующие дозы анальгетиков (обезболивающих), жаропонижающих (жаропонижающих) и противоотечных средств. Однако, если симптомы сохраняются, может быть рекомендовано лечение, состоящее из антибиотиков.
Антибиотики для лечения гайморита
Антибиотики помечены как препараты узкого спектра действия, если они действуют только против нескольких типов бактерий. С другой стороны, антибиотики широкого спектра действия более эффективны, воздействуя на широкий спектр бактерий, но с большей вероятностью способствуют развитию устойчивости к антибиотикам. По этой причине ваш специалист по уху, горлу и носу, скорее всего, назначит антибиотики узкого спектра действия, которые часто стоят дешевле. Он/она может порекомендовать антибиотики широкого спектра действия при инфекциях, которые не реагируют на лечение препаратами узкого спектра действия.
Острый синусит
В большинстве случаев антибиотики назначают пациентам с характерными признаками стойких гнойных выделений из носа и лицевых болей или чувствительности, которые не улучшаются через семь дней, или пациентам с тяжелыми симптомами риносинусита, независимо от продолжительности. На основании клинических испытаний предпочтительными антибиотиками являются амоксициллин, доксициклин или триметоприм-сульфаметоксазол.
Хронический синусит
Даже при длительном лечении антибиотиками симптомы хронического синусита трудно поддаются лечению. Однако в целом лечение хронического синусита, например, антибиотиками и деконгестантами, похоже на лечение острого синусита. При неэффективности лечения антибиотиками в качестве наиболее эффективных средств лечения хронического синусита могут быть рекомендованы тесты на аллергию, десенсибилизация и/или хирургическое вмешательство. Исследования показывают, что подавляющее большинство людей, перенесших операцию, имеют меньше симптомов и лучшее качество жизни.
Детский синусит
Антибиотики, которые вряд ли будут эффективны у детей, которым не помогает амоксициллин, включают триметоприм-сульфаметоксазол (Бактрим) и эритромицин-сульфизоксазол (Педиазол), поскольку многие бактерии устойчивы к этим старым антибиотикам. Для детей, которые не реагируют на два курса традиционных антибиотиков, часто увеличивают дозу и продолжительность лечения антибиотиками или рекомендуют лечение внутривенным введением цефотаксима или цефтриаксона и/или направление к ЛОР-врачу.
Антибиотики | Richmond ENT
Что такое антибиотики?
Антибиотики — это лекарства, полученные из встречающихся в природе химических веществ, вырабатываемых бактериями и плесенью для подавления роста конкурирующих микроорганизмов. Пенициллин был открыт в 1929 году Александром Флемингом, и его популярное производное амоксициллин остается эффективным при 80% острых бактериальных инфекций носовых пазух и 99% инфекций горла. Хотя 60% эпизодов острого бактериального синусита разрешаются без лечения, антибиотики последовательно сокращают течение болезни и снижают частоту осложнений синусита.
Когда следует использовать антибиотики?
Антибиотики рекомендуются при остром бактериальном синусите, продолжающемся более 10 дней или ухудшающемся после первой недели. Наиболее распространенные симптомы включают лицевую боль или давление, заложенность или заложенность носа, а также густые, обесцвеченные выделения из носа. Антибиотики также обычно назначают при хроническом синусите, хотя многие случаи хронического синусита не вызваны бактериями.
Почему мой врач не прописывает антибиотики по телефону?
Исследования показали, что у 80 % пациентов с острым синуситом наступает улучшение в течение недели после приема антибиотиков, в то время как у 73 % пациентов, получавших плацебо , наступает улучшение. Более того, антибиотики никак не сократят течение простуды. Чрезмерное использование антибиотиков может привести к размножению устойчивых штаммов бактерий и вызвать аллергию на лекарства у восприимчивых пациентов. Соответственно, мы не рекомендуем антибиотики при симптомах синуса , которые, по-видимому, спонтанно улучшаются в течение первых 7-10 дней. Если вы злоупотребляете антибиотиками сейчас, у нас может не остаться вариантов, когда они вам действительно понадобятся!
Если вы злоупотребляете антибиотиками сейчас, у нас может не остаться вариантов, когда они вам действительно понадобятся!
Что такое устойчивость к антибиотикам?
Устойчивость бактерий к антибиотикам является серьезной проблемой в Ричмонде, штат Вирджиния, и на всей территории Соединенных Штатов. Многие из распространенных бактерий, вызывающих синусит, несут ген устойчивости к антибиотикам, который может активироваться в присутствии антибиотиков. Через несколько дней лечения ген активируется и может даже перемещаться между бактериями (в капсуле, называемой плазмидой), создавая устойчивость среди большой популяции бактерий. Если вы не реагируете на курс антибиотиков в течение 4–7 дней, у вас может быть устойчивый штамм бактерий. Проконсультируйтесь с вашим врачом для осмотра и возможного посева или анализа ДНК ваших пазух. Анализ ДНК синусового дренажа позволяет выявить наиболее опасные резистентные штаммы в течение 24 часов и провести полный анализ всех бактерий в носу в течение 1 недели.
Подробнее об анализе ДНК хронических ЛОР-инфекций
Какие антибиотики чаще всего используются при синуситах?
Амоксициллин остается препаратом выбора при остром неосложненном бактериальном синусите. Амоксициллин наиболее эффективен, если вводить его достаточно часто, чтобы поддерживать адекватный уровень в инфицированной ткани. Хотя его часто назначают два раза в день, он еще более эффективен, если принимать его в 3 или 4 приема. Амоксициллин обычно назначают на 7-10 дней за раз. Хотя при лечении стрептококкового фарингита крайне важно закончить весь 10-дневный курс антибиотиков, есть свидетельства того, что более коротких курсов лечения может быть достаточно для большинства случаев синусита. Амоксициллин тесно связан с исходным соединением пенициллином и не должен назначаться пациентам с аллергией на пенициллин.
Азитромицин является альтернативным средством для пациентов с аллергией на амоксициллин. Принципиальным преимуществом азитромицина является удобство — рекомендуемая доза при остром синусите составляет 500 мг 1 раз в сутки всего 3 дня. В отличие от амоксициллина, эффективность азитромицина повышается при приеме большой разовой дозы, а не при распределении доз. По этой причине курс азитромицина следует завершить за 3 дня или менее при синусите (как в случае Zithromax Tri-Pak), и его не следует растягивать на 5 дней (как в случае Zithromax Z-Pak). Азитромицин быстро индуцирует устойчивость к антибиотикам, если его назначают в дозах, слишком низких для уничтожения бактерий. Эта резистентность сохраняется не менее 3 мес, поэтому азитромакс не следует назначать дважды в течение 3 мес. Альтернативы, связанные с азитромицином, включают кларитромицин (биаксин), который обычно принимают два раза в день в течение 10 дней, и более старые препараты эритромицин и клиндамицин, которые требуют 3-4 доз в день.
В отличие от амоксициллина, эффективность азитромицина повышается при приеме большой разовой дозы, а не при распределении доз. По этой причине курс азитромицина следует завершить за 3 дня или менее при синусите (как в случае Zithromax Tri-Pak), и его не следует растягивать на 5 дней (как в случае Zithromax Z-Pak). Азитромицин быстро индуцирует устойчивость к антибиотикам, если его назначают в дозах, слишком низких для уничтожения бактерий. Эта резистентность сохраняется не менее 3 мес, поэтому азитромакс не следует назначать дважды в течение 3 мес. Альтернативы, связанные с азитромицином, включают кларитромицин (биаксин), который обычно принимают два раза в день в течение 10 дней, и более старые препараты эритромицин и клиндамицин, которые требуют 3-4 доз в день.
Цефалоспорины и аугментин (амоксициллин с клавулановой кислотой) считаются «антибиотиками широкого спектра действия», поскольку они обладают повышенной эффективностью против более широкого спектра бактерий, включая те, которые устойчивы к обычному пенициллину или амоксициллину.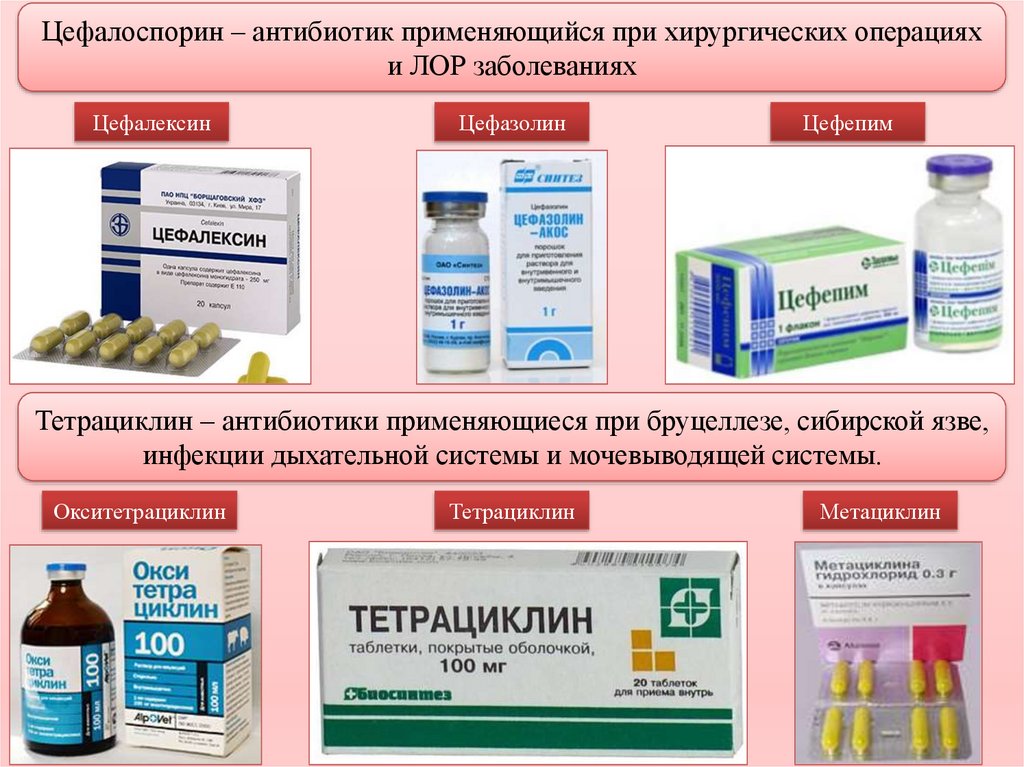 Если состояние пациента не улучшается в течение первой недели приема амоксициллина, целесообразно перейти на аугментин или цефалоспорин, такой как цефтин, цефзил, омницеф или супракс. Хотя эти препараты имеют сходный с пенициллином механизм действия, их обычно можно принимать в адекватных дозах один или два раза в день. Эти препараты следует использовать с особой осторожностью у пациентов с аллергией на пенициллин в анамнезе, так как может возникнуть перекрестная реакция.
Если состояние пациента не улучшается в течение первой недели приема амоксициллина, целесообразно перейти на аугментин или цефалоспорин, такой как цефтин, цефзил, омницеф или супракс. Хотя эти препараты имеют сходный с пенициллином механизм действия, их обычно можно принимать в адекватных дозах один или два раза в день. Эти препараты следует использовать с особой осторожностью у пациентов с аллергией на пенициллин в анамнезе, так как может возникнуть перекрестная реакция.
Ципро, Левахин и Авелокс обычно считаются антибиотиками третьей линии при неосложненном синусите. Эти лекарства по-прежнему имеют очень низкий уровень резистентности и часто являются нашим последним средством перед хирургическим вмешательством. Аллергические реакции возникают нечасто, но у пациентов, принимающих эти препараты, были описаны боли в суставах и разрывы сухожилий. Они также имеют повышенную сложность взаимодействия с другими лекарствами.
Бактрим и тетрациклин – это более старые препараты, которые обычно не охватывают широкий спектр бактерий, которые могут размножаться в пазухах. Однако иногда они могут применяться у пациентов с инфекциями, вызванными известными устойчивыми бактериями. В частности, эти препараты назначают при стафилококковых инфекциях, устойчивых к цефалоспоринам и другим производным пенициллина. Эта инфекция известна как метициллин-резистентный золотистый стафилококк или MRSA.
Однако иногда они могут применяться у пациентов с инфекциями, вызванными известными устойчивыми бактериями. В частности, эти препараты назначают при стафилококковых инфекциях, устойчивых к цефалоспоринам и другим производным пенициллина. Эта инфекция известна как метициллин-резистентный золотистый стафилококк или MRSA.
Местные антибиотики являются относительно новым вариантом лечения, который стал популярным у послеоперационных пациентов с хронически резистентными бактериями. Различные противомикробные препараты, включая ванкомицин и аминогликозиды, которые нельзя вводить внутрь, доступны в виде назального спрея или промывания. Недавние исследования показали, что большие объемы назальных промываний лучше доставляют антибиотики в носовые пазухи, чем распыляемые спреи. Эти антибиотики можно комбинировать с сильнодействующими противогрибковыми препаратами и стероидами, каждый из которых будет выбран вашим врачом на основе результатов посева, а фармацевт, составляющий рецептуру, смешает для вас по индивидуальному заказу. Назальный крем Бактробан (мупироцин) можно наносить внутрь ноздрей, чтобы уменьшить колонизацию метициллинрезистентным золотистым стафилококком (MRSA).
Назальный крем Бактробан (мупироцин) можно наносить внутрь ноздрей, чтобы уменьшить колонизацию метициллинрезистентным золотистым стафилококком (MRSA).
Дополнительные ресурсы:
Клинические рекомендации: синусит у взрослых. Розенфельд Р.М., Андес Д., Бхаттачария Н., Чунг Д., Айзенберг С., Ганиатс Т.Г., Гельцер А., Хамилос Д., Хейдон Р.К. 3-й, Хаджинс П.А., Джонс С., Крауз Х.Дж., Ли Л.Х., Махони М.С., Марпл Б.Ф., Митчелл С.Дж., Натан Р., Шиффман Р.Н., Смит Т.Л., Витселл Д.Л. Отоларингол Head Neck Surg. 2007 Сентябрь; 137 (3 Приложение): S1-31.
Клинические рекомендации по диагностике и лечению острого бактериального синусита у детей в возрасте от 1 до 18 лет. Уолд Э.Р., Эпплгейт К.Е., Бордли С., Дэрроу Д.Х., Глод М.П., Марси С.М., Нельсон К.Э., Розенфельд Р.М., Шейх Н., Смит М.Дж., Уильямс П.В., Вайнберг С.Т.; Американская академия педиатрии. Педиатрия. 2013 июль; 132 (1): e262-80.
Современные концепции местной терапии хронических синоназальных заболеваний.