Противомикробные средства
Бактерии, грибки, вирусы, паразиты являются возбудителями различных патологий в организме человека. Бороться с ними помогают противомикробные, антибактериальные и противогрибковые средства. Существуют препараты широкого спектра действия, позволяющие уничтожить различные вирусы и бактерии. Также имеются средства узконаправленные на определенные вирусы или бактерии.
Вирусы постоянно мутируют, поэтому некоторые препараты, еще недавно считавшиеся эффективными, утрачивают свою значимость. Фармакологическая промышленность постоянно производит инновационные средства, позволяющие бороться с разного рода инфекциями.
Новые противомикробные средства эффективны благодаря тому, что микроорганизмы не смогли еще приспособиться к внедренному активному веществу.
Достоинства антибактериальных средств нового поколения следующие:
- Современные препараты имеют значительно меньший список побочных реакций.

- Их не нужно принимать несколько раз в сутки – достаточно одного или двух приемов.
- Имеется разная форма выпуска противомикробных препаратов: таблетки, мази, растворы для инъекций, суспензии, пластыри, капсулы и пр.
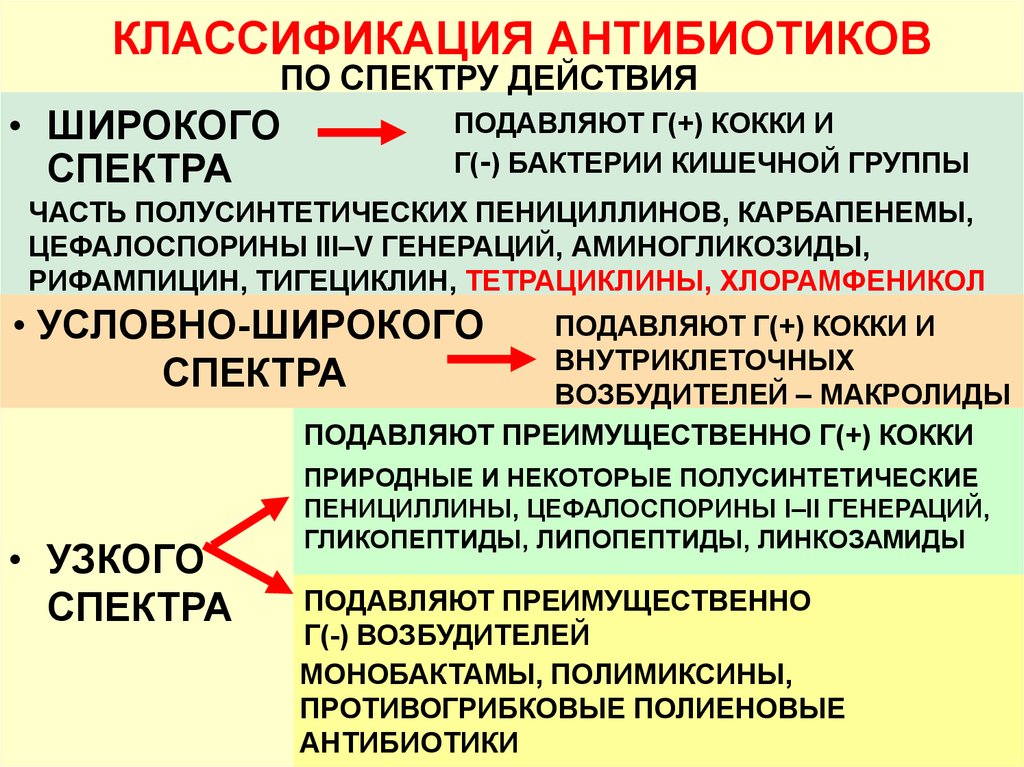
Классификация антибактериальных средств
По типу активности антибактериальные препараты подразделяются на:
- Противобактериальные.
- Противогрибковые.
- Антипротозойные.
По виду воздействия:
- Бактерицидные. Эти препараты способны пагубно влиять на клеточную мембрану бактерий, вызывая их гибель. К таким средствам относятся: Клабакс, Цифрафан, Сумамед и аналогичные антибиотики. Их назначают ослабленным пациентам при значительных заражениях.
- Бактериостатические. Принцип их действия – угнетение синтеза белка, гашение размножения микроорганизмов. Такие препараты используются при лечении и профилактике инфекционных осложнений.
 К ним относятся: Салютаб, Тетрациклина гидрохлорид, Бисептол, Юнидокс, Доксициклин и др. Применяются неослабленным больным и при незначительных инфекциях.
К ним относятся: Салютаб, Тетрациклина гидрохлорид, Бисептол, Юнидокс, Доксициклин и др. Применяются неослабленным больным и при незначительных инфекциях.
Категория противомикробных средств включает в себя:
- Антибактериальные препараты – самая большая группа, используются для системного применения. Их производят с использованием синтетических или полусинтетических методов. Нарушают процессы размножения бактерий или ликвидируют патогенные микроорганизмы.
- Антисептики, обладающие широким спектром действия. Используются для обработки кожных и слизистых поверхностей.
- Антимиотики, подавляющие жизнедеятельность грибов. Используются системно и наружно.
- Противовирусные средства, влияющие на размножение вирусов.
Ассортимент противомикробных средств
- Нолицин таб. п/о 400мг №20. Используются для лечения инфекционно-воспалительных заболеваний, которые вызваны микроорганизмами, чувствительными к данному препарату: инфекционных заболеваний мочевыводящих путей, инфекций половых органов, бактериального гастроэнтерита, гонореи неосложненной и др.
- Монурал пор. д/сусп. 3г №1. Антибиотик широкого спектра действия. Быстро всасывается из желудочно-кишечного тракта. Применяется при цистите, уретрите, бессимптомной массивной бактериурии у беременных, инфекциях послеоперационных и др.
- Метрогил гель 30г, современный популярный препарат, обладающий антибактериальным и противопротозойным эффектом. Содержит метронидазол –
На сайте нашей аптеки вы можете ознакомиться с характеристиками различных противомикробных препаратов.
Так же может быть интересно
Боремся с вирусами у малышей
инъекционные, оральные, водорастворимые для животных, птицы и рыбы
АМОКСИЦИН 70 WS, уп. 500 гр 500 гр порошок для орального применения, хорошо растворим в воде (амоксициллина тригидрат 700 мг) | Препарат широкого спектра действия, хорошо растворим в воде Период ожидания: | |
| АМОКСИЦИН 15%, фл. 100 мл суспензия для инъекций пролонгированного действия (амоксициллина тригидрат 150 мг) | Препарат широкого спектра и пролонгированного действия Период ожидания: | |
| АМОКСИЦИН 80%, уп. 500 гр порошок для орального применения (амоксициллина тригидрат 800 мг ) | Препарат широкого спектра и пролонгированного действия Период ожидания: | |
АПРАВЕТИН, уп. 500 гр 500 гр порошок для орального применения (апрамицина сульфат 50%) | Широкий спектр действия, активен в отношении бактерий и микоплазм,высокая активность против сальмонелл и колибактерий, низкая резорбция из кишечника,не токсичен для животных и птиц Период ожидания по мясу: | |
| АПРАМИН 200, фл. 100 мл раствор для инъекций (апрамицина сульфат 200 мг) | Широкий спектр действия, активен в отношении бактерий и микоплазм,высокая биодоступность Период ожидания по мясу: | |
| БЕНСТРЕП, фл. 100 мл суспензия для инъекций (бензилпенициллина прокаин 200 мг, дигидрострептомицина сульфат 250 мг) | Широкий спектр действия Период ожидания по мясу: | |
ВЕТАЦЕФ 200, фл. 100 мл 100 мл суспензия для инъекций (цефтиофур 200 мг) | ОДНА ИНЪЕКЦИЯ = КУРС ЛЕЧЕНИЯ ! ДЕЙСТВУЕТ 168 ЧАСОВ! НЕ ИМЕЕТ ОГРАНИЧЕНИЙ ПО МОЛОКУ! ЭФФЕКТИВЕН В ЛЕЧЕНИИ КРС И СВИНЕЙ! Период ожидания по мясу: | |
| ВЕТАЦЕФ 50, фл. 100 мл суспензия для инъекций (цефтиофур 50 мг) | Широкий спектр действия Период ожидания по мясу: крс — 8 суток молоко — 2 суток | |
| ГЕНТАМ БТ, фл. 100 мл суспензия для инъекций (амоксициллина тригидрат 150 мг, гентамицина 40 мг) | Комбинация амоксициллина и гентамицина обладает широким спектром антибактериального действия. Период ожидания по мясу: | |
| ДОКСИВЕТ 50% БТ, уп. 500 гр водорастворимый порошок для орального применения (доксициклина гиклат 50%) | Доксициклин обладает широким спектром антибактериального действия, эффективен в отношении большинства бактерий, микоплазм, хламидий, риккетсий и боррелий. Период ожидания по мясу: | |
| КАНАМИЦИН 25%, фл. 100 мл раствор для инъекций (канамицина сульфат 25 мг) | Канамицин является антибиотиком широкого спектра действия из группы аминогликозидов Период ожидания: | |
КЛАМОВЕТИН, уп. 500 гр 500 гр порошок для орального применения (амоксициллина тригидрат 500 мг, калия клавуната 125 мг) | Активнодействующие вещества, входящие в состав препарата, проявляют синергизм действия, тем самым усиливают действие друг друга и расширяют спектр антимикробной активности Период ожидания по мясу: | |
| КОМБИВЕТ, фл. 100 мл раствор для инъекций (эритромицин 50 мг, сульфадиметоксин 200 мг, триметоприм 18 мг, бензокаин 15 мг, дексаметозона натрия фосфата 0,1 мг) | Комбинация входящих в состав препарата компонентов обеспечивает широкий спектр его антибактериального действия, в том числе против микроорганизмов, устойчивых к обычным средствам, а так же противовоспалительный эффект. Период ожидания: | |
| ЛИНДОКСИН 100, фл. 1000 мл раствор для орального применения (доксициклина гиклат 100 мг, линкомицина гидрохлорида 100 мг) | Комбинация доксициклина и линкомицина, входящих в состав препарата, обладает широким спектром антибактериального действия Период ожидания: | |
| ЛИНКОСПЕКТ 150, фл. 100 мл раствор для инъекций (линкомицин 50 мг, спектиномицин 100 мг) | Комбинированный препарат широкого спектра антибактериального действия Период ожидания: | |
| МУЛЬТИОМИЦИН 1%, мешок 20 кг порошок для орального применения (нозигептид — мультиомицин 1%) | Ростостимулирующий, лечебно-профилактический препарат БЕЗ периода ожидания по мясу и яйцу | |
НОРФЛОКС 10% БТ, фл. 100 мл 100 мл раствор для инъекций (норфлоксацин 10 мг) | Антибактериальный препарат из группы фторхинолов широкого спектра действия Период ожидания: | |
| НОРФЛОКСАЦИНА НИКОТИНАТ 20% БТ, уп. 500 гр водорастворимый порошок для орального применения (норфлоксацина никотинат 20%) | Широкий спектр действия (колибактериоз, сальмонеллез, пастереллез, микоплазмоз, гемофилез, стафилококковая инфекция и др.) Период ожидания: | |
ОКСИВЕТРИН 200, фл. 100 мл 100 мл раствор для инъекций (окситетрациклина гидрохлорид 20 мг) | Широкий спектр действия Период ожидания: | |
| ОКСИКИН, уп. 500 гр порошок для орального применения (окситетрациклина гидрохлорид 20%) | Широкий спектр действия Период ожидания: | |
| ОФЛОСТИН, фл. 1000 мл раствор для орального применения (офлоксацин в виду основания 10%, 1 000 000 МЕ колистина сульфат) | Комбинация колистина сульфата и офлоксацина обладает усиленным антибактериальным действием при различных заоблеваниях Период ожидания: | |
ПЕНМИЦИН, фл. 100 мл 100 мл суспензия для инъекций (бензилпенициллина прокаин, неомицина сульфат) | Широкий спектр действия Период ожидания: | |
| РИБАВЕКС, фл. 100 мл рибавекс для инъекций (рибавирин 25 мг, энрофлоксацин 55 мг, триметоприм 10мг) | Антибактериальный препарат с противовирусным действием Период ожидания: | |
| СТРЕПТОФОМ, уп. 100 гр порошок для наружого применения (стрептоцид 0,8г., йодоформ 0,1 г.) | Порошок-присыпка для лечения язв, ран, заболеваний копыт БЕЗ ограничений | |
СУЛЬТРИМ 240, фл. 1000 мл 1000 мл раствор для орального применения (сульфадиазин 200 мг, триметоприм 40мг) | Высокая эффективность против эймерий, стабилен в любой воде, экономное средство Не применяется в яичном птицеводстве. Период ожидания по мясу: | |
| СУЛЬФАПРИМ 48 БТ, уп. 500 гр порошок для орального применения (сульфадиазин 40 мг, триметоприм 8 мг) | Высокая эффективность против эймерий, микоплазм. Широкий спетрк антибактериального действия. Период ожидания: | |
СУЛЬФАПРИМ 480, уп. 500 гр 500 гр таблетки для орального применения (сульфадиазин 40 мг, триметоприм 8 мг) | Высокая эффективность. Удобная форма применения. Короткий срок ожидания по мясу Период ожидания: | |
| СУЛЬФПРИМ 48, фл. 100 мл суспензия для инъекций (сульфадиазин 400 мг, триметоприм 80 мг) | Широкий спектр действия Период ожидания: | |
| ТИАМУЛИН 45% БТ, уп. 500 гр водорастворимый порошок для орального применения (тиамулина гидроген фумарата 45%) | Широкий спектр действия. Задается с кормом и водой Период ожидания: | |
ТИАЦИН, фл. 1000 мл 1000 мл раствор для орального применения (тиамулина гидроген фумарата 125 мг, 200 000 МЕ колистина сульфат) | Широкий спектр и быстрое действие. Период ожидания: | |
| ТИЛАНКИН, уп. 500 гр водорастворимый порошок для орального применения (тилозина тартрат 50%) | Задается с кормом или водой Период ожидания: | |
| ТИЛМИКСОЛ, фл. 1000 мл раствор для орального применения (тилмиколзин 300 мг) | Стабилен в воде любой жесткости, широкий спектр Период ожидания по мясу: | |
ТИЛОЗИНАВЕТ 200, фл. 100 мл 100 мл раствор для инъекций (тилозин 200 мг) | Широкий спектр действия Период ожидания: | |
| ФЛОКСАЦИН 10%, фл. 100 мл раствор для инъекций (энрофлоксацин 100 мг) | Широкий спектр действия Период ожидания: | |
| ФЛОКСАЦИН 10% оральный, фл. 1000 мл раствор для орального применения (энрофлоксацин 100 мг) | Широкий спектр действия Период ожидания: | |
ФЛОРАЛ, фл. 1000 мл 1000 мл раствор для орального применения (флорфеникол 200 мг) | Широкий спектр действия. Особенно эффективен при заболеваниях органов дыхания, жкт и мочеполовой системы Период ожидания: | |
| ФЛОРВЕТИН 300, фл. 100 мл порошок для орального применения (флофеникол 4 %г) | Широкий спектр действия. Особенно эффективен при заболеваниях органов дыхания, жкт и мочеполовой системы Период ожидания: | |
| ФЛОРВЕТИН 4%, фл. 100 мл порошок для орального применения (флофеникол 300 мг) | Широкий спектр действия. Особенно эффективен при заболеваниях органов дыхания, жкт и мочеполовой системы Период ожидания: | |
ФЛЮМЕКСОЛ фл. 1000 мл 1000 мл раствор для орального применения (флюмеквин 200 мг, бромгексин гидрохлорид 10 мг) | Широкий спектр действия. Особенно эффективен при заболеваниях органов дыхания, жкт и мочеполовой системы Период ожидания: | |
| ЭНРОКИН, фл. 100 мл порошок для орального применения (энрофлоксацин 100 мг) | Эффективен для животных, птицы и рыбы Период ожидания: | |
| ЭРИПРИМ БТ, уп. 500 мг водорастворимый порошок для орального применения (тилозин 0,05г, сульфадимидин 0,175 мг, триметоприм 0,035 мг, 300 000 МЕ колистина сульфат) | Широкий спектр действия. Возможно задавать в виде премикса 1,5% Возможно задавать в виде премикса 1,5%Период ожидания: | |
Сужение спектра: новый рубеж прецизионных противомикробных препаратов | Геномная медицина
- Комментарий
- Открытый доступ
- Опубликовано:
- Александра Э. Пахарик 1,3 ,
- Генри Л. Шрайбер IV 1,3 ,
- Кейтлин Н. Сполдинг 1,2,3 ,
- Карен В. Додсон 1,3 и
- …
- Скотт Дж. Халтгрен 1,3
Геномная медицина том 9 , Номер статьи: 110 (2017) Процитировать эту статью
10 тыс.
 обращений
обращений22 Цитаты
14 Альтметрический
Сведения о показателях
Редакционное резюме
Антибиотики стали стандартом лечения бактериальных инфекций. Однако растущие показатели инфекций, устойчивых к антибиотикам, опережают разработку новых противомикробных препаратов. Антибиотики широкого спектра действия также наносят вред полезным микробным сообществам, населяющим человека. Для борьбы с устойчивостью к антибиотикам и защиты этих сообществ необходимо разработать новые прецизионные противомикробные препараты, нацеленные на конкретные патогены.
Микробиота, здоровье человека и действие антибиотиков
Случайное открытие Александром Флемингом антибиотика пенициллина в 1929 г. и последующее открытие стрептомицина в 1943 г. положили начало золотому веку открытия антибиотиков (1950–1970-е гг.), когда примерно половина антибактериальных препаратов, обычно используемых сегодня, была открыта. С этого периода антибиотики стали стандартом лечения бактериальных инфекций. Антибиотики значительно снижают заболеваемость и смертность от инфекционных заболеваний, а также повышают качество и продолжительность жизни миллиардов людей. Однако резистентность бактерий к противомикробным препаратам возникла вскоре после их разработки и в настоящее время представляет собой глобальный кризис в области здравоохранения. Отсутствие рационального использования противомикробных препаратов широкого спектра действия как в здравоохранении, так и в сельском хозяйстве привело к резкому увеличению числа устойчивых к антибиотикам микроорганизмов [1]. Антимикробные препараты широкого спектра действия подвергают резидентную микробиоту человека (совокупность микроорганизмов, живущих в теле человека или на нем) селективному давлению, а невыполнение курса антибиотиков приводит к неполной эрадикации инфекционных микроорганизмов и развитию резистентности у выживших возбудителей.
и последующее открытие стрептомицина в 1943 г. положили начало золотому веку открытия антибиотиков (1950–1970-е гг.), когда примерно половина антибактериальных препаратов, обычно используемых сегодня, была открыта. С этого периода антибиотики стали стандартом лечения бактериальных инфекций. Антибиотики значительно снижают заболеваемость и смертность от инфекционных заболеваний, а также повышают качество и продолжительность жизни миллиардов людей. Однако резистентность бактерий к противомикробным препаратам возникла вскоре после их разработки и в настоящее время представляет собой глобальный кризис в области здравоохранения. Отсутствие рационального использования противомикробных препаратов широкого спектра действия как в здравоохранении, так и в сельском хозяйстве привело к резкому увеличению числа устойчивых к антибиотикам микроорганизмов [1]. Антимикробные препараты широкого спектра действия подвергают резидентную микробиоту человека (совокупность микроорганизмов, живущих в теле человека или на нем) селективному давлению, а невыполнение курса антибиотиков приводит к неполной эрадикации инфекционных микроорганизмов и развитию резистентности у выживших возбудителей. На комменсальные микробы домашнего скота также влияет использование антибиотиков, которые используются в качестве стимуляторов роста и для лечения инфекций. Пищевой перенос затем позволяет резистентным микроорганизмам колонизировать людей. Кроме того, узкие места в открытии и клинических испытаниях новых антибиотиков привели к нехватке новых противомикробных препаратов, находящихся в стадии разработки. Таким образом, инфекции, вызванные лекарственно-устойчивыми бактериями, в настоящее время опережают разработку новых противомикробных препаратов и угрожают снова превратить обычные инфекции в проблему жизни или смерти.
На комменсальные микробы домашнего скота также влияет использование антибиотиков, которые используются в качестве стимуляторов роста и для лечения инфекций. Пищевой перенос затем позволяет резистентным микроорганизмам колонизировать людей. Кроме того, узкие места в открытии и клинических испытаниях новых антибиотиков привели к нехватке новых противомикробных препаратов, находящихся в стадии разработки. Таким образом, инфекции, вызванные лекарственно-устойчивыми бактериями, в настоящее время опережают разработку новых противомикробных препаратов и угрожают снова превратить обычные инфекции в проблему жизни или смерти.
Все большее число исследований показывает, что природа антибиотиков широкого спектра действия и их чрезмерное использование оказывают длительное пагубное воздействие на здоровую микробиоту человека, которая играет важную роль в обмене веществ, устойчивости к патогенам и развитии иммунной системы [2, 3 ]. Например, здоровая микробиота кишечника придает устойчивость к колонизации вторгающимся патогенам и играет жизненно важную роль в приобретении питательных веществ и модуляции иммунной системы [2]. Нарушение структуры сообщества и, следовательно, функции микробиоты, известное как дисбактериоз, связано с множественными иммунологическими и метаболическими заболеваниями [2, 3].
Нарушение структуры сообщества и, следовательно, функции микробиоты, известное как дисбактериоз, связано с множественными иммунологическими и метаболическими заболеваниями [2, 3].
У маленьких детей воздействие антибиотиков может быть особенно вредным, поскольку созревание сообщества кишечной микробиоты имеет решающее значение для здорового развития ребенка, влияя на рост мышечной, жировой и костной ткани и развитие здоровой иммунной системы [3]. ]. У взрослых длительное применение антибиотиков также может привести к снижению микробного разнообразия кишечника и повышению восприимчивости к желудочно-кишечному патогену Clostridium difficile. При C. difficile 9Инфекции 0038 лечат дополнительными антибиотиками, частота повторных инфекций может достигать 65% [4]. Таким образом, хотя антибиотики широкого спектра действия играют решающую роль в спасении жизней и лечении инфекции, их использование может привести к долгосрочным пагубным последствиям и повреждению микробиоты человека.
Прецизионные противомикробные препараты: новые разработки и проблемы
Альтернативой антибиотикам широкого спектра действия являются прецизионные противомикробные препараты. Прецизионные противомикробные препараты функционируют либо путем i) специфического ингибирования критического узла патогенеза, чтобы нарушить поддержание и/или персистенцию патогена в организме хозяина, либо путем ii) специфического уничтожения патогенного организма с минимальными нецелевыми эффектами. Такие стратегии с меньшей вероятностью вызывают резистентность, чем противомикробные препараты широкого спектра действия, поскольку воздействие на ключевые факторы, необходимые для вирулентности конкретных бактерий, ограничивает способы, которыми бактерии могут развивать резистентность при сохранении функции вирулентности. Кроме того, резидентные микроорганизмы с меньшей вероятностью разовьют устойчивость к терапии, направленной против патогенов, поскольку они не используют одни и те же биохимические пути.
Биомедицинские исследования прилагают огромные усилия для разработки прецизионных противомикробных препаратов нового поколения для наиболее распространенных в мире патогенов, особенно для тех заболеваний, возбудители которых обладают высокой резистентностью. Например, индекс лекарственной устойчивости инфекций мочевыводящих путей (ИМП) показывает, что с середины 2000-х годов число инфекций, сталкивающихся с трудностями в лечении, увеличилось из-за быстрого распространения устойчивости среди грамотрицательных микроорганизмов, в том числе Escherichia coli 9.0038, основная причина ИМП [5]. Недавнее исследование Spaulding et al. [6] продемонстрировали, как использование прецизионных противомикробных препаратов может помочь решить эту проблему. Уропатогенная E. coli (UPEC), вызывающая большинство ИМП, бессимптомно обитает в кишечном резервуаре. УПЭК выделяются с фекалиями, могут колонизировать периуретральную область, а затем подниматься по уретре, вызывая ИМП. Пили типа 1 с адгезином FimH облегчают колонизацию UPEC как кишечника, так и мочевого пузыря путем связывания маннозилированных белков, украшающих эпителий кишечника и мочевого пузыря (рис. 1) [6]. Замещенные аналоги маннозы, называемые маннозидами, были разработаны для специфического блокирования способности UPEC колонизировать хозяина путем связывания с E. coli FimH [7]. Оптимальными аналогами являются бифенилманнозиды, которые связывают FimH с сродством на порядки выше (~ 1 000 000×), чем природный рецептор [7]. Сполдинг и др. [6] показали, что бифенилманнозиды не только эффективны при лечении активной инфекции мочевого пузыря, но также способны одновременно снижать колонизацию УПЭК в желудочно-кишечном тракте мышей, оставляя при этом структуру микробного сообщества ненарушенной (рис. 1) [ 6]. Таким образом, эта антибиотико-сберегающая терапия может предотвратить рецидивы ИМП как за счет уменьшения персистенции UPEC в кишечном резервуаре хозяина, так и за счет предотвращения колонизации мочевого пузыря. Кроме того, мутации в fimH , которые придают устойчивость к связыванию маннозидов, вероятно, также нарушат его важные взаимодействия с маннозилированными белками-хозяевами.
1) [6]. Замещенные аналоги маннозы, называемые маннозидами, были разработаны для специфического блокирования способности UPEC колонизировать хозяина путем связывания с E. coli FimH [7]. Оптимальными аналогами являются бифенилманнозиды, которые связывают FimH с сродством на порядки выше (~ 1 000 000×), чем природный рецептор [7]. Сполдинг и др. [6] показали, что бифенилманнозиды не только эффективны при лечении активной инфекции мочевого пузыря, но также способны одновременно снижать колонизацию УПЭК в желудочно-кишечном тракте мышей, оставляя при этом структуру микробного сообщества ненарушенной (рис. 1) [ 6]. Таким образом, эта антибиотико-сберегающая терапия может предотвратить рецидивы ИМП как за счет уменьшения персистенции UPEC в кишечном резервуаре хозяина, так и за счет предотвращения колонизации мочевого пузыря. Кроме того, мутации в fimH , которые придают устойчивость к связыванию маннозидов, вероятно, также нарушат его важные взаимодействия с маннозилированными белками-хозяевами. Таким образом, маннозиды являются многообещающими терапевтическими кандидатами с низким давлением отбора в отношении резистентности.
Таким образом, маннозиды являются многообещающими терапевтическими кандидатами с низким давлением отбора в отношении резистентности.
Антибиотик-сберегающий маннозид одновременно лечит активную инфекцию мочевого пузыря и воздействует на желудочно-кишечный резервуар уропатогенной E. coli . Уропатогенная E. coli (UPEC) связывает маннозилированные белки ( синий ) обнаруживают на эпителии кишечника и мочевого пузыря. 1 В кишечнике UPEC связывается в криптах толстой кишки посредством взаимодействия между адгезином FimH на пилях I типа и маннозой. 2 Маннозиды ( красный ) связывают FimH с большей аффинностью, чем манноза, удаляя колонизирующие UPEC из желудочно-кишечного тракта. 3–5 Инфекционный цикл инфекции мочевыводящих путей включает несколько стадий, включая начальное прикрепление ( 3 ), внутриклеточную пролиферацию ( 4 ), филаментация и отток ( 5 ) и повторный вход. Прикрепление и повторное проникновение требуют, чтобы FimH связывал маннозу ( blue ) на эпителии мочевого пузыря. 6 Маннозиды ( красный ) связывают FimH и предотвращают связывание с клетками мочевого пузыря, способствуя элиминации UPEC из ткани. УПЭК, Уропатогенный Escherichia coli
Прикрепление и повторное проникновение требуют, чтобы FimH связывал маннозу ( blue ) на эпителии мочевого пузыря. 6 Маннозиды ( красный ) связывают FimH и предотвращают связывание с клетками мочевого пузыря, способствуя элиминации UPEC из ткани. УПЭК, Уропатогенный Escherichia coli
Изображение полного размера
Авидоцин-CD также являются примером прецизионного антибиотика, который не нарушает микробиоту кишечника. Кирк и др. [8] продемонстрировали, что класс бактерицидов Avidocin-CD специфически убивает C. difficile путем нацеливания на SlpA, основной компонент S-слоя C. difficile . Можно разработать различные формы авидоцина-CD, которые убивают определенные изоляты C. difficile на основе типа S-слоя [8]. Хотя мутанты с нулевым S-слоем, устойчивые к этому бактерициду, были идентифицированы in vitro, они являются авирулентными, что демонстрирует важность S-слоя в споруляции C. difficile и продукции токсина [8]. Показав, что устойчивость к авидоцину-CD вызывает C. difficile для потери вирулентности, эта работа представляет собой элегантный пример преимуществ разработки бактерицидов, нацеленных на факторы вирулентности.
difficile и продукции токсина [8]. Показав, что устойчивость к авидоцину-CD вызывает C. difficile для потери вирулентности, эта работа представляет собой элегантный пример преимуществ разработки бактерицидов, нацеленных на факторы вирулентности.
Успешные прецизионные терапевтические средства могут также воздействовать на ряд других путей вирулентности, таких как производство токсинов. Небольшие молекулы вирстатина и токстазина В являются противовирулентными ингибиторами экспрессии токсина Vibrio cholerae , и оба они эффективны на животных моделях инфекции V. cholerae [9]. Противовирулентный препарат безлотоксумаб, моноклональное антитело против C. difficile токсин TcdB был одобрен FDA в 2016 году для лечения C. difficile пациентов с высоким риском рецидивирующей инфекции [10]. FDA также одобрило использование терапевтических средств, которые нейтрализуют нейротоксины Clostridium botulinum (BoNT) и защитный антиген Bacillus anthracis , компонент как летального токсина, так и токсина отека [10].
Существует ряд важных соображений, связанных с успешной разработкой и внедрением точной терапии. В дополнение к проблемам традиционных антибиотиков, таким как токсичность, биодоступность и возможность производства, клиническое использование прецизионных противомикробных препаратов потребует быстрой диагностики для выявления пациентов, для которых будет полезна конкретная терапия. Создание эффективного прецизионного противомикробного препарата также требует детального понимания механизмов, управляющих инфекционным циклом патогена. Эти знания помогут разработать индивидуальные лекарства, которые предотвращают вирулентность и/или персистенцию конкретного патогенного организма, воздействуя на пути, отсутствующие в полезной микробиоте, а также в человеке-хозяине. Динамика бактериального сообщества также должна учитываться, если прецизионные противомикробные препараты должны использоваться при полимикробных инфекциях. Эти вопросы потребуют дальнейшего изучения по мере развития области прецизионных противомикробных препаратов.
Сотрудничество между академическими лабораториями и фармацевтическими компаниями будет способствовать решению уникальных задач, связанных с разработкой прецизионных противомикробных препаратов. Такое сотрудничество уже показывает многообещающие результаты в области предоставления прецизионных противомикробных препаратов у постели больного. Например, авидоцины и маннозиды в настоящее время разрабатываются компаниями AvidBiotics (Южный Сан-Франциско, Калифорния) и Fimbrion Therapeutics (Сент-Луис, Миссури) соответственно. Fimbrion Therapeutics сотрудничает с GlaxoSmithKline (Брентфорд, Лондон) для разработки маннозидов в качестве терапевтических средств, сберегающих антибиотики. Ряд других антивирулентных терапий для Staphylococcus aureus и Pseudomonas aeruginosa также проходят клинические испытания [10]. Поскольку будущее терапии инфекционных заболеваний смещается в сторону прецизионных противомикробных препаратов, крайне важно, чтобы крупные фармацевтические компании все активнее участвовали в своих исследованиях и разработках.
Выводы
Рост устойчивости к антибиотикам в сочетании с длившимся десятилетиями затишьем в открытии новых антибиотиков указывает на то, что антибиотики для лечения устойчивых к лекарствам инфекций могут закончиться. Кроме того, мы только начинаем осознавать неразрывную связь между микробиотой человека и здоровьем хозяина и то, как лечение антибиотиками меняет эту динамику. Поэтому становится все более очевидным, что для сохранения здоровья человека необходимо использовать новые терапевтические парадигмы, в том числе использование прецизионных противомикробных препаратов. Прецизионные противомикробные препараты предлагают путь к сохранению терапевтической эффективности за счет специфического удаления целевых патогенов. Отсутствие нецелевых эффектов уменьшит селективное давление на комменсальные микробы, а также предотвратит нарушение ключевых функций, выполняемых микробиотой. Чтобы предотвратить резистентность патогенов к противомикробным препаратам, противомикробные препараты следующего поколения должны быть разработаны для уничтожения или обезвреживания микроорганизмов путем воздействия на факторы, имеющие решающее значение для вирулентности. Успешное использование этих стратегий для E. coli , C. difficile , B. anthracis и другие демонстрируют светлое будущее медицины, поскольку мы вступаем в новую эру целенаправленной разработки противомикробных препаратов.
Успешное использование этих стратегий для E. coli , C. difficile , B. anthracis и другие демонстрируют светлое будущее медицины, поскольку мы вступаем в новую эру целенаправленной разработки противомикробных препаратов.
Сокращения
- УПЭК:
Уропатогенный Escherichia coli
- УТИ:
Инфекции мочевыводящих путей
Ссылки
Laxminarayan R, Duse A, Wattal C, Zaidi AK, Wertheim HF, Sumpradit N, et al. Устойчивость к антибиотикам — необходимость глобальных решений. Ланцет Infect Dis. 2013;13:1057–98.
Артикул пабмед Google Scholar
Lozupone CA, Stombaugh JI, Gordon JI, Jansson JK, Knight R.
 Разнообразие, стабильность и устойчивость микробиоты кишечника человека. Природа. 2012; 489: 220–30.
Разнообразие, стабильность и устойчивость микробиоты кишечника человека. Природа. 2012; 489: 220–30.Артикул КАС пабмед ПабМед Центральный Google Scholar
Лэнгдон А., Крук Н., Дантас Г. Влияние антибиотиков на микробиом на протяжении всего развития и альтернативные подходы к терапевтической модуляции. Геном Мед. 2016;8:39.
Артикул пабмед ПабМед Центральный Google Scholar
Хига Дж.Т., Келли С.П. Новые препараты и стратегии лечения колита Clostridium difficile . J Интенсивная терапия Мед. 2014;29:190–9.
Артикул КАС пабмед Google Scholar
Индекс лекарственной устойчивости. https://resistancemap.cddep.org/DRI.php. По состоянию на 19 ноября 2017 г.
Spaulding CN, Klein RD, Ruer S, Kau AL, Schreiber HL, Cusumano ZT, et al.
 Селективное уничтожение уропатогенной кишечной палочки из кишечника с помощью антагониста FimH. Природа. 2017; 546: 528–32.
Селективное уничтожение уропатогенной кишечной палочки из кишечника с помощью антагониста FimH. Природа. 2017; 546: 528–32.КАС пабмед Google Scholar
Cusumano CK, Pinkner JS, Han Z, Greene SE, Ford BA, Crowley JR, et al. Лечение и профилактика инфекции мочевыводящих путей перорально активными ингибиторами FimH. Sci Transl Med. 2011;3:109ра115.
Артикул пабмед ПабМед Центральный Google Scholar
Кирк Дж.А., Гебхарт Д., Бакли А.М., Лок С., Шолль Д., Дус Г.Р. и др. Новый класс прецизионных противомикробных препаратов переопределяет роль S-слоя Clostridium difficile в вирулентности и жизнеспособности. Sci Transl Med. 2017;9. doi:10.1126/scitranslmed.aah6813.
Антуард Р., ДиРита В.Дж. Химическая биология применительно к изучению бактериальных патогенов. Заразить иммун. 2015; 83: 456–69.

Артикул пабмед ПабМед Центральный Google Scholar
Dickey SW, Cheung GYC, Otto M. Различные лекарства от вредных насекомых: противовирусные стратегии в эпоху устойчивости к антибиотикам. Nat Rev Drug Discov. 2017; 16: 457–71.
Артикул КАС пабмед Google Scholar
Ссылки на скачивание
Финансирование
Эта работа поддерживается грантами NIH: RO1DK051406, R01AI048689и P50DK064540. CNS была поддержана в Медицинской школе Вашингтонского университета по номеру 1F31DK107057.
Информация об авторе
Авторы и организации
Кафедра молекулярной микробиологии, Медицинский факультет Вашингтонского университета, Сент-Луис, Миссури, 63110, США
Александра Э. Пахарик, Генри Л. Шрайбер IV, Кейт Лин Н. Сполдинг , Karen W. Dodson & Scott J. Hultgren
Департамент иммунологии и инфекционных заболеваний, Гарвардский университет T.
 H. Школа общественного здравоохранения Чана, Бостон, Массачусетс, 02115, США
H. Школа общественного здравоохранения Чана, Бостон, Массачусетс, 02115, СШАКейтлин Н. Сполдинг
Центр исследований женских инфекционных заболеваний, Медицинский факультет Вашингтонского университета, Сент-Луис, Миссури, 63110, США
Александра Э. Пахарик, Генри Л. Шрайбер IV, Кейтлин Н. Сполдинг, Karen W. Dodson & Scott J. Hultgren
Авторы
- Alexandra E. Paharik
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Генри Л. Шрайбер IV
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Caitlin N. Spaulding
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Karen W. Dodson
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Scott J.
 Hultgren
HultgrenПросмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
Contributions
AEP отвечала за составление рукописи. CNS и AEP создали фигуру. Все авторы внесли свой вклад в доработку рукописи и утвердили окончательный вариант.
Автор, ответственный за переписку
Переписка с Скотт Дж. Халтгрен.
Декларации этики
Конкурирующие интересы
SJH является изобретателем патента США US8937167 B2, который касается использования антагонистов лиганда FimH на основе маннозида для лечения заболеваний. SJH владеет долей в Fimbrion Therapeutics и может извлечь выгоду, если компания добьется успеха в маркетинге маннозидов.
Примечание издателя
Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Права и разрешения
Открытый доступ Эта статья распространяется в соответствии с условиями международной лицензии Creative Commons Attribution 4. 0 (http://creativecommons.org/licenses/by/4.0/), которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии вы должным образом указываете автора (авторов) и источник, предоставляете ссылку на лицензию Creative Commons и указываете, были ли внесены изменения. Отказ от права Creative Commons на общественное достояние (http://creativecommons.org/publicdomain/zero/1.0/) применяется к данным, представленным в этой статье, если не указано иное.
0 (http://creativecommons.org/licenses/by/4.0/), которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии вы должным образом указываете автора (авторов) и источник, предоставляете ссылку на лицензию Creative Commons и указываете, были ли внесены изменения. Отказ от права Creative Commons на общественное достояние (http://creativecommons.org/publicdomain/zero/1.0/) применяется к данным, представленным в этой статье, если не указано иное.
Перепечатки и разрешения
Об этой статье
Глоссарий — АЛЬЯНС ЗА РАЗУМНОЕ ИСПОЛЬЗОВАНИЕ АНТИБИОТИКОВ
Антибактериальные препараты
(см. Антибактериальные препараты)
Антибиотики
(см. О бактериях и антибиотиках)
Устойчивость к антибиотикам
(см. Сведения об устойчивости к антибиотикам)
Антимикробные препараты
Антимикробные препараты — это широкий термин, используемый для описания любого агента, который препятствует нормальному функционированию микроскопических организмов, включая бактерии, грибы, дрожжи, вирусы и простейшие. Антибиотики, которые воздействуют только на бактерии, являются одним из видов противомикробных препаратов.
Антибиотики, которые воздействуют только на бактерии, являются одним из видов противомикробных препаратов.
Бактерии
(см. О бактериях и антибиотиках)
Биологическое разнообразие (биоразнообразие)
Относится к количеству живых организмов и изменчивости среди них и окружающей их среды.
Антибиотики широкого спектра действия
(см. Антибиотики узкого и широкого спектра действия)
Колонизация
Колонизация происходит, когда новый вид бактерий образует колонию (группу бактерий одного типа) в новое место, например, кишечный тракт человека. Бактерии могут колонизировать хозяина, не вызывая инфекции или заболевания.
Комменсал
Обычно относится к микроорганизму, который живет в тесном контакте с организмом-хозяином (человеком, животным или растением), не вызывая заболевания у хозяина. Комменсальные организмы могут быть полезными для хозяина. Некоторые микроорганизмы могут быть комменсалами для одного вида хозяина, но вызывать заболевание у другого вида.
Некоторые микроорганизмы могут быть комменсалами для одного вида хозяина, но вызывать заболевание у другого вида.
Воздействие на окружающую среду
Изменения экологии и живых организмов, вызванные деятельностью человека или природой.
Экология
Изучение взаимоотношений и взаимодействий между организмами и окружающей средой.
Экосистема
Место с живыми (животные, растения, микроорганизмы и другие организмы) и неживыми (почва, вода, камни) элементами, образующими сложную сеть взаимозависимостей.
Сточные воды
Сточные воды (очищенные или неочищенные), выходящие из водоочистных сооружений, коллекторов или промышленных предприятий; как правило, отходы, сбрасываемые в поверхностные воды.
Кишечные бактерии
Бактерии, живущие в кишечнике человека или животных.
Окружающая среда
Физические элементы, которые формируют окружение.
Гриб
(Множественное число: грибы) Многоклеточный организм с клеточными стенками и ядрами, но без хлорофилла. К грибам относятся многие неродственные или только отдаленно родственные организмы, такие как грибы, дрожжи (например, те, которые используются при приготовлении хлеба или пива) и плесневые грибы (например, те, которые используются при производстве сыра или вызывают гниение продуктов). Грибы могут вызывать многие заболевания растений и животных. Однако они также являются источником ряда полезных антибиотиков (например, пенициллина, происходящего из Penicillium плесень).
Ген
Сегмент молекулы ДНК, несущий инструкции по построению белка; единица наследственности.
Непатентованные антибиотики и антибиотики с торговыми названиями (негенерические)
Имеющиеся в продаже антибиотики могут называться двумя разными названиями. Родовое название — это общепринятая семейная идентификация, предоставленная химиками, например «Амоксициллин». Торговое название дается ему производителем и часто используется врачами и фармацевтами при назначении и отпуске лекарств. Одно из торговых названий амоксициллина — аугментин.
Торговое название дается ему производителем и часто используется врачами и фармацевтами при назначении и отпуске лекарств. Одно из торговых названий амоксициллина — аугментин.
Грамположительные и грамотрицательные бактерии
При окрашивании грамположительных бактерий красителем клеточная стенка удерживает краситель внутри, и бактерии окрашиваются в темно-фиолетовый цвет. Клеточные стенки грамотрицательных бактерий более проницаемы — они не удерживают большую часть красителя, поэтому их клеточные стенки не сильно окрашиваются.
Стимуляторы роста
Класс веществ, обычно антибиотиков, используемых в низких дозах для стимуляции роста сельскохозяйственных животных.
Горизонтальный перенос генов
Обмен генетическим материалом между двумя микроорганизмами; не создается новый микроорганизм.
Хозяин
Многоклеточный организм (например, дерево, собака или человек), колонизированный комменсальными или патогенными микроорганизмами.
Микроорганизмы
Микроскопические или субмикроскопические живые организмы: их невозможно увидеть человеческим глазом. К ним относятся бактерии, некоторые грибы и простейшие. В эту категорию иногда включают вирусы, хотя некоторые ученые не относят вирусы к микроорганизмам, поскольку не считают, что вирусы следует классифицировать как живые организмы.
Множественная лекарственная устойчивость
Способность организма противостоять нескольким различным лекарствам.
Антибиотики узкого спектра действия против антибиотиков широкого спектра действия
Антибиотик может быть классифицирован как «узкий» или «широкий спектр» в зависимости от ряда типов бактерий, на которые он воздействует. Антибиотики узкого спектра действия активны в отношении избранной группы типов бактерий. Антибиотики широкого спектра действия активны в отношении большего количества типов бактерий и, таким образом, могут использоваться для лечения различных инфекционных заболеваний. Антибиотики широкого спектра действия особенно полезны, когда инфекционный агент (бактерии) неизвестен. Примерами антибиотиков узкого спектра действия являются старые пенициллины (penG), макролиды и ванкомицин. Примерами антибиотиков широкого спектра действия являются аминогликозиды, цефалоспорины 2-го и 3-го поколений, хинолоны и некоторые синтетические пенициллины.
Антибиотики широкого спектра действия особенно полезны, когда инфекционный агент (бактерии) неизвестен. Примерами антибиотиков узкого спектра действия являются старые пенициллины (penG), макролиды и ванкомицин. Примерами антибиотиков широкого спектра действия являются аминогликозиды, цефалоспорины 2-го и 3-го поколений, хинолоны и некоторые синтетические пенициллины.
Естественный отбор
Процесс, при котором организмы, лучше приспособленные к окружающей среде, процветают и размножаются, в то время как организмы, менее приспособленные к окружающей среде, не процветают и не размножаются успешно.
Противомикробные средства, не относящиеся к общественному здравоохранению
Средства, которые контролируют или ингибируют бактерии, вызывающие запах.
Внутрибольничные инфекции
Инфекции, приобретаемые в больнице при лечении другого заболевания.
Патоген
Микроорганизм, вирус или другое вещество, вызывающее заболевание у другого организма-хозяина.
Плазмида
Небольшая петля генетического материала, не являющаяся частью хромосом, которая может легко переноситься между бактериями.
Профилактические средства
Лекарства, используемые для предотвращения заболевания до появления каких-либо симптомов заболевания.
Противомикробные средства для общественного здравоохранения
Агенты, предназначенные для борьбы с инфекционными микроорганизмами, которые могут представлять опасность для здоровья человека. Чтобы агент получил статус «противомикробного средства для общественного здравоохранения», производитель должен представить в EPA данные, демонстрирующие, что агент эффективен против конкретных инфекционных микроорганизмов и соответствует стандартам безопасности и токсичности. Агент считается эффективным, если он контролирует указанные микроорганизмы, не обязательно заболевания, вызванные микроорганизмами. Производитель не может утверждать, что средство предотвращает заболевания.
Резервуар устойчивости
Фраза, используемая для описания комменсальных бактерий, устойчивых к противомикробным препаратам. Эти комменсальные бактерии не вызывают заболеваний у своих хозяев; однако в конечном итоге устойчивость может быть передана организму, который вызовет устойчивое к противомикробным препаратам заболевание у другого хозяина.
Резистентность
(см. Об устойчивости к антибиотикам)
Селективное давление
Влияние, оказываемое некоторым фактором (например, антибиотиком) на естественный отбор для продвижения одной группы организмов над другой. В случае устойчивости к антибиотикам антибиотики вызывают избирательное давление, убивая восприимчивые бактерии, позволяя устойчивым к антибиотикам бактериям выживать и размножаться.
Субтерапевтические средства
Лекарства, используемые в дозах, которые слишком малы, чтобы быть эффективными в борьбе с болезнью; антибиотики обычно используются в субтерапевтических дозах для стимуляции роста пищевых животных.
Супербактерия
Некоторые штаммы бактерий стали устойчивыми ко многим антибиотикам, поэтому их иногда называют «супербактериями» или «супермикробами». Примерами супербактерий являются Staphylococcus aureus , устойчивые к метициллину и ванкомицину, Pseudomonas aeruginosa (вызывает многие легочные и ожоговые инфекции), устойчивые к ванкомицину Enterococcus faecalis (VRE) (могут вызывать инфекцию в пищеварительной системе) и полирезистентные Mycobacterium tuberculosis (бактерии, вызывающие туберкулез ). Некоторые из этих штаммов устойчивы ко всем известным антибиотикам — более чем к 100 различным препаратам.
Восприимчивость
Показатель того, насколько хорошо противомикробные препараты действуют на бактерии. Восприимчивые бактерии могут быть уничтожены или ингибированы противомикробными препаратами.
Терапевтические средства
Лекарства, используемые для лечения заболеваний.


