М | Медицинский центр «Сердолик»
Специфическая профилактика (Вакцинация и ревакцинация БЦЖ)
Вакцина БЦЖ была получена французскими учеными Calmette и Guerin в 1919 году из культуры МБТ бычьего типа, утратившей свои вирулентные свойства и сохранившей полностью все иммуногенные свойства, присущие МБТ.
Препараты вакцины БЦЖ и БЦЖ-М представляют собой живые микобактерии вакцинного штамма БЦЖ, лиофильно высушенные 1,5% растворе глютамината натрия, имеют вид белой высушенной массы.
Одна ампула вакцины БЦЖ – содержит 0,1 мг вакцины (20 доз по 0,05 мг). Одна ампула вакцины БЦЖ-М содержит 0,5 мг вакцины, что составляет 20 доз, каждая по 0,025 мг препарата. Это препарат пониженной антигенной нагрузки и используется для щадящей иммунизации.
Живые микобактерии штамма БЦЖ, размножаясь в организме привитого, приводят к развитию длительного специфического иммунитета к туберкулезу. Вакцины БЦЖ и БЦЖ-М используются для активной специфической профилактики туберкулеза.
Вакцинация БЦЖ
- Первичную вакцинацию осуществляют здоровым новорожденным детям на 4-7 день жизни в отдельно отведенной комнате. Вводят вакцину строго внутрикожно, в верхнюю треть левого плеча.
- Дети, не привитые в родильном отделении должны прививаться в детских поликлиниках в течение 2-х месяцев вакциной БЦЖ, без предварительной туберкулинодиагностики. Детям старше 2-х месячного возраста, перед вакцинацией необходимо проводить пробу Манту.
- Вакцинируются дети с отрицательной реакцией на туберкулин.
- Дети, не привитые в родильном отделении по медицинским противопоказаниям, должны прививаться на педиатрическом участке вакциной БЦЖ-М.
- Интервал между пробой Манту и вакцинацией должен быть не менее 3 дней и не более 2-х недель.
- Выписку новорожденного из родильного отделения можно проводить при условии обязательного обследования на туберкулез отца, родственников, проживающих в одной квартире.
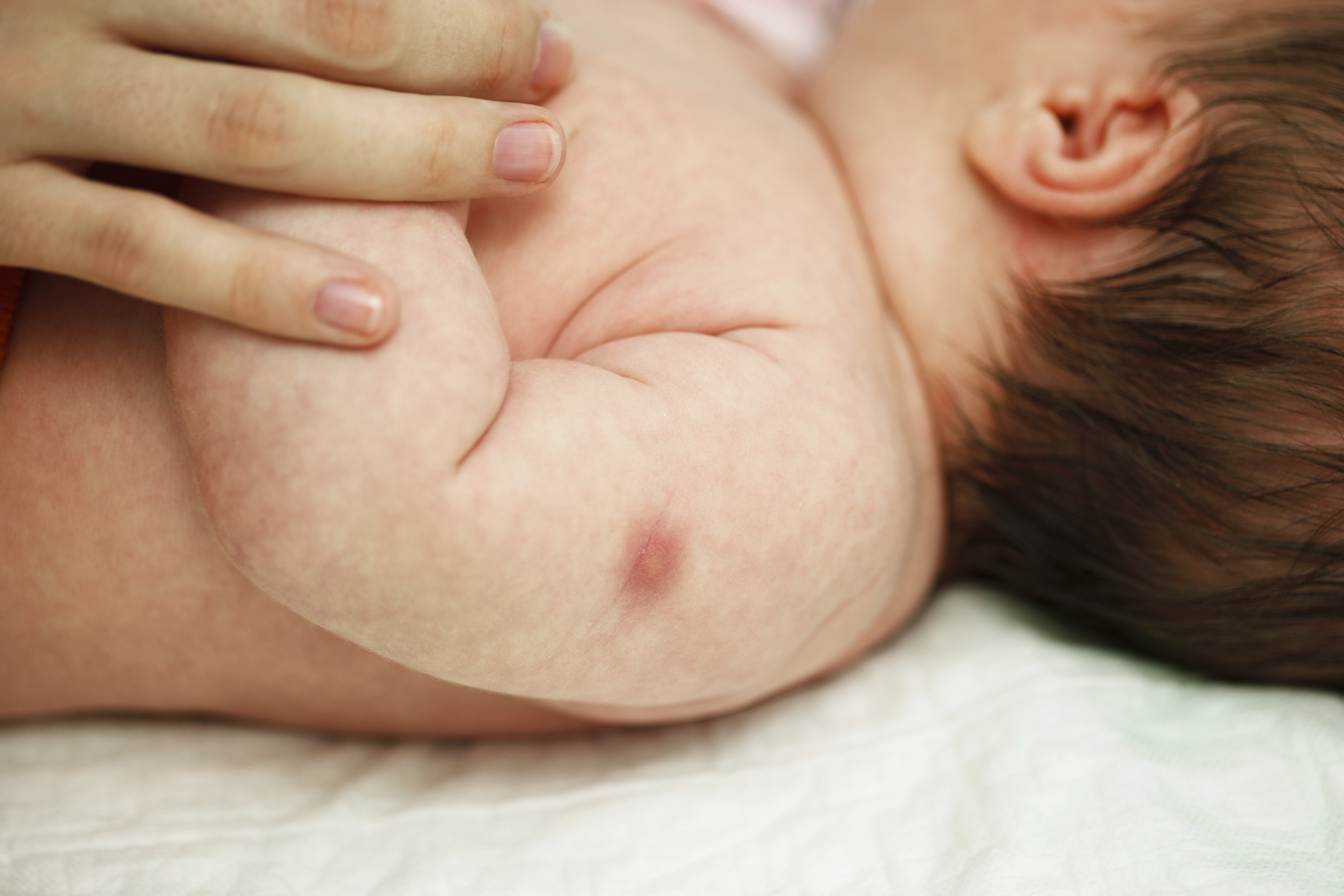
- При отсутствии рубца на прививку БЦЖ (БЦЖ-М) проба Манту ставится один раз в 6 месяцев и при отрицательной реакции на туберкулин дети прививаются в возрасте 2-х лет. При наличии некачественного рубца к году жизни дети повторно прививаются БЦЖ-М в возрасте 2-х лет при отрицательной пробе Манту.
- С целью раннего выявления осложнений после прививки БЦЖ врачам педиатрам необходимо наблюдать прививочную реакцию в 1,3,6,9,12 месяцев.
- Вакцинация (ревакцинация) БЦЖ проводится через 4 недели после других профилактических прививок, а после проведенной вакцинации БЦЖ другие профилактические прививки проводятся не ранее, чем через 2 месяца, то есть после заживления местной прививочной реакции.
При качественно проведенной вакцинации у 90-95% вакцинированных новорожденных к 4 месяцам жизни должен сформироваться рубчик размером от 5 до 10 мм.
Противопоказания к вакцинации новорожденных
Временные:
- Сепсис новорожденных (допустимость прививки через 6 месяцев)
- Внутриутробная инфекция (через 1 месяц после выздоровления)
- Гнойные кожные заболевания (через 2 месяц после выздоровления)
- Острые респираторные заболевания (через 1 месяц после выздоровления)
- Гемолитическая болезнь новорожденных среднетяжелая и тяжелая формы (через 6 месяцев при отсутствии анемии)
- Тяжелые повреждения ЦНС с выраженной неврологической симптоматикой (через 3 месяца после осмотра невропатологом)
- Недоношенные дети 2-4 ст.(при достижении веса).
Постоянный медицинский отвод:
- Врожденные ферментопатии
- Иммунодефицитные состояния
- Генерализованная БЦЖ – инфекция у других детей в семье
- ВИЧ – инфекция у матери.
Ревакцинация БЦЖ
Ревакцинации подлежат здоровые дети и подростки в декретированных возрастах, имеющих отрицательную пробу Манту.

2-я ревакцинация – в возрасте 14-15 лет (учащиеся 9-х классов), а также подросткам средних специальных учебных заведений (ПТУ, техникум) на первом году обучения. В неблагоприятных по эпидемиологии туберкулеза регионах проводится ревакцинация в междекретированых возрастах детям и подросткам, у которых отсутствуют прививочные знаки, через 2 года после вакцинации и 1 год после ревакцинации. В эти же сроки осуществляется ревакцинация детей и подростков, имеющих в декретированных возрастах ременные медицинские отводы от прививки.
Ревакцинация взрослых (18-30 лет) осуществляется в организованных коллективах. Сроки ревакцинации определяются с учетом эпидемиологической ситуации по туберкулезу в соответствующем регионе. Ревакцинация взрослых проводится при отрицательной и сомнительной реакции Манту.
Противопоказания к ревакцинации БЦЖ
Постоянный медицинский отвод:
- Инфицированность МБТ или перенесенный туберкулез
- Положительная или сомнительная реакция Манту
- Осложненные реакции на предыдущее введение вакцины БЦЖ или БЦЖ-М
- Заболевания крови
- Злокачественные новообразования
- Иммунодефицитные состояния. Лечение иммунодепрессантами
- Беременность (все сроки).
Временные:
- Аллергические болезни – кожные и респираторные (в стадии обострения) (допустимость прививки после выздоровления или достижения ремиссии по заключению специалиста)
- Острые заболевания, включая период реконвалесценции, хронические заболевания в стадии обострения или декомпенсации (через 1 месяц после выздоровления, ремиссии).
Новости
13 Апрель 2021 13:17
01-03 апреля 2021г. проходил уже четвертый форум «Онлайн-диагностика 3.0», проводимый самым крупным региональным отделением Российского общества рентгенологов и радиологов (Московское региональное отделение).
Приглашаем Вас принять участие в семинаре «Практикум по торакальной хирургии: организация, техника, риски», который состоится с 21 по 22 апреля 2021 года в он-лайн формате.
24 Март 2021 15:46
С прискорбием сообщаем, что 22 марта 2021 года в Екатеринбурге в возрасте 62 лет скончался наш коллега, доктор медицинских наук, главный научный сотрудник Центра клинических исследований и апробаций, профессор кафедры фтизиатрии и пульмонологии Уральского государственного медицинского университета Игорь Давыдович Медвинский.
3 Февраль 2021 15:25
Европейский Конгресс по клинической микробиологии и инфекционным заболеваниям (ECCMID) состоится в Вене, Австрия, с 9 по 12 июля 2021 года.
3 Февраль 2021 10:05
Ежегодная Всероссийской конференции молодых ученых с международным участием «Современные инновационные технологии в эпидемиологии, диагностике и лечении туберкулеза взрослых и детей» пройдет 24, 25 и 26 марта 2021 года частично в on-line формате и частично в очной форме.
29 Январь 2021 17:05
25 января 2021 года на 59-м году жизни скончался доктор медицинских наук, профессор, заведующий кафедрой фтизиатрии РНИМУ им. Н.И. Пирогова Владимир Анатольевич Стаханов.
Он внес неоценимый вклад в развитие отечественной фтизиатрии. В сферу его научных интересов входили вопросы патогенеза, раннего выявления и излечения туберкулеза в различных возрастных группах, в том числе у больных с сопутствующими заболеваниями, а также проблемы профилактики туберкулеза.
12 Январь 2021 15:48
Согласно рекомендациям президиума ВАК распоряжением Минобрнауки России от 9 декабря 2020 г.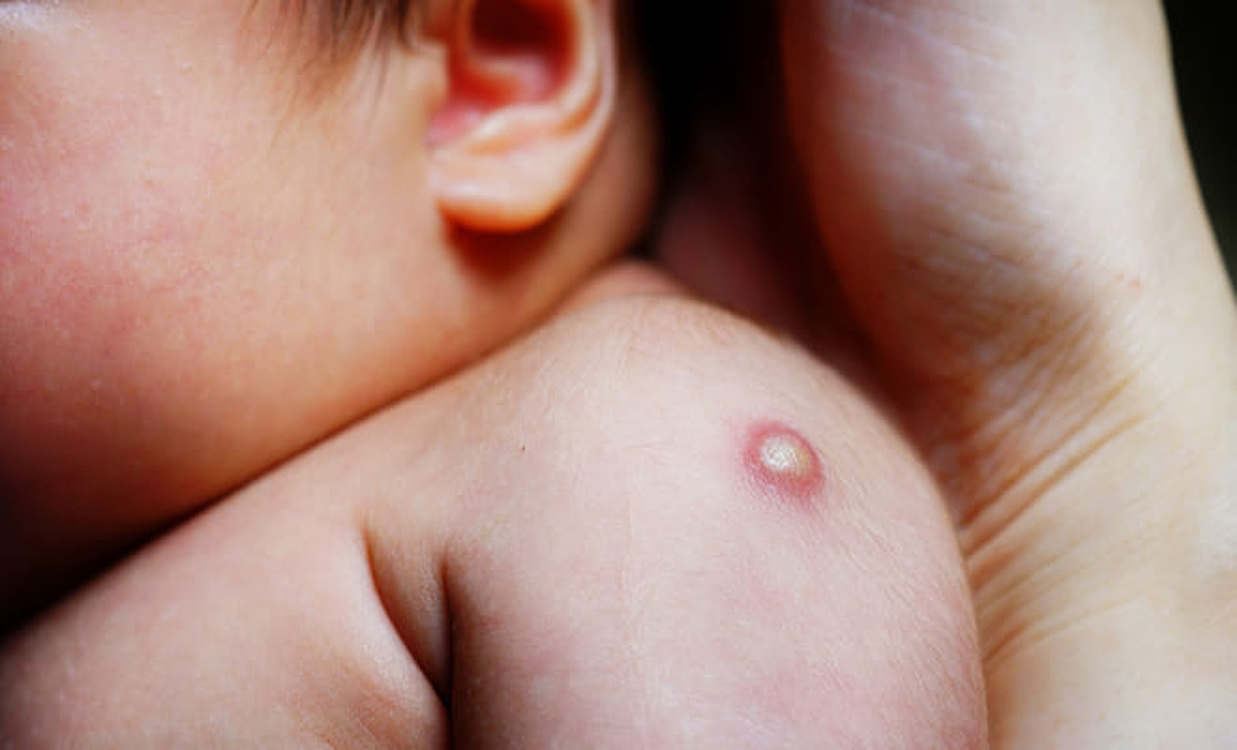 № 427-р издание «Медицинский Альянс (МедАльянс)» дополнительно включено в Перечень по научной специальности и соответствующей ей отрасли науки, по которой присуждаются ученые степени 14.01.17 — Хирургия (медицинские науки).
№ 427-р издание «Медицинский Альянс (МедАльянс)» дополнительно включено в Перечень по научной специальности и соответствующей ей отрасли науки, по которой присуждаются ученые степени 14.01.17 — Хирургия (медицинские науки).
17 Декабрь 2020 17:12
Европейский совет АОSpine продлил до апреля 2024 года Санкт-Петербургскому НИИ фтизиопульмонологии действие сертификата AOSpine-центра, рекомендуемого для стажировок членов AOSpine.
11 Декабрь 2020 09:29
Исследовательский центр Борстель объявляет о начале приёма заявок на участие в недавно учрежденной стипендиальной программе в честь семьи Монтей-Мусиолик, которые — с их пожертвованием — пожелали способствовать трансляционным исследованиям туберкулеза и развитию обучающего исследовательского потенциала.
Прививки от туберкулеза | Государственное бюджетное учреждение здравоохранения «Городская поликлиника №3»
ПОМНИТЕ!
Большое значение имеет и состояние общего иммунитета организма человека. Необходимым условием для повышения сопротивляемости организма туберкулёзной инфекции является полноценное питание, достаточное пребывание на свежем воздухе, закаливающие процедуры, правильный образ жизни, душевное спокойствие. Особое значение имеет борьба с вредными привычками (курение, употребление алкоголя и наркотиков).
Особые профилактические мероприятия требуются в очагах туберкулёзной инфекции. Одними из важнейших методов профилактики туберкулёза являются изоляция здорового человека от больного и назначение лекарственной профилактики всем членам семьи.
Соблюдение всех рекомендаций по профилактике туберкулёза поможет предупредить заболевание и снизить риск заражения окружающих.
АСТРАХАНЬ – 2016
ТУБЕРКУЛЁЗ (чахотка) – это инфекционное заболевание, вызываемое микобактериями туберкулёза, которые часто называют палочкой Коха. Заболевание развивается только в ответ на размножение в организме человека этих микробов. Основным источником заражения туберкулёзом является человек, который более туберкулёзом, также туберкулёзом могут болеть и животные. Из дыхательных путей, особенно во время кашля, отделяется мокрота, содержащая микобактерии туберкулёза. Мелкие капли мокроты могут попадать в дыхательные пути здорового человека, находящегося рядом. Мокрота может оседать на поверхности пола или земли, на предметах и вещах. Инфекция может попасть в организм человека вследствие нарушения правил гигиены или употребления в пищу немытых овощей и фруктов, плохо обработанного мяса и некипяченого молока.
Заболевание развивается только в ответ на размножение в организме человека этих микробов. Основным источником заражения туберкулёзом является человек, который более туберкулёзом, также туберкулёзом могут болеть и животные. Из дыхательных путей, особенно во время кашля, отделяется мокрота, содержащая микобактерии туберкулёза. Мелкие капли мокроты могут попадать в дыхательные пути здорового человека, находящегося рядом. Мокрота может оседать на поверхности пола или земли, на предметах и вещах. Инфекция может попасть в организм человека вследствие нарушения правил гигиены или употребления в пищу немытых овощей и фруктов, плохо обработанного мяса и некипяченого молока.
Основные симптомы, характерные для туберкулёза:
кашель на протяжении 2-3 недель и более;
боль в груди;
снижение или отсутствие аппетита, потеря веса;
наличие крови в мокроте;
повышенная потливость, особенно по ночам;
периодическое повышение температуры до 37-37,5 градусов;
быстрая утомляемость и появление слабости;
увеличение периферических лимфатических узлов.
Для детей и подростков самым основным методом профилактики туберкулёза является противотуберкулёзная вакцинация БЦЖ и диагностическая проба Манту.
Прививка БЦЖ входит в число обязательных в нашей стране и включена в национальный календарь профилактических прививок. Её цель – создание противотуберкулёзного иммунитета (невосприимчивости к туберкулёзу).
Вакцина туберкулёзная (БЦЖ) – это ослабленный вакцинный штамм, который не может вызывать заболевания туберкулёзом, но позволяет вырабатываться иммунитету против него.
Существует вариант вакцины БЦЖ – это вакцина БЦЖ-М, в которой содержится в 2 раза меньше микробных тел, чем в обычной вакцине. Вакциной БЦЖ-М прививают ослабленных и маловесных недоношенных детей, и обычно эту вакцину уже применяют не в роддоме, а в стационаре, куда переведут ребёнка. Также её применяют у детей, которых по каким-либо причинам не привили в роддоме.
Показания к вакцинации, ревакцинации БЦЖ и реакции Манту
Препарат предназначен для активной специфической профилактики туберкулёза.
Первичную вакцинацию осуществляют здоровым доношенным новорождённым детям на 3-7-ой день жизни в родильном доме.
Вакцину БЦЖ вводят строго внутрикожно на границе верхней и средней трети наружной поверхности левого плеча. Введение препарата под кожу недопустимо, т.к. при этом может образоваться холодный абсцесс. На месте внутрикожного введения вакцины БЦЖ развивается специфическая реакция в виде папулы, везикулы или пустулы размером 5-10 мм в диаметре. Место реакции следует предохранять от механического раздражения, особенно во время водных процедур. У 90-95% вакцинированных на месте прививки должен образоваться рубчик до 10 мм в диаметре.
Иммунитет после вакцинации БЦЖ держится 6-7 лет, поэтому всем детям с отрицательной реакцией Манту в 7 лет предлагают повторную вакцинацию БЦЖ.
Ревакцинации (в 6-7 лет) подлежат здоровые дети, имеющие отрицательную реакцию Манту. Реакция считается отрицательной при полном отсутствии инфильтрата, гиперемии или при наличии уколочной реакции (1 мм).
Многолетние наблюдения и исследования показали, что две прививки, сделанные в родильном доме и в 7 лет достаточны для поддержания противотуберкулёзного иммунитета у ребёнка.
К сожалению, некоторые родители, принимая решение об отказе вакцинации от туберкулёза своего ребёнка, лишают его возможности защититься от инфекции. Однако, принимая такое решение, необходимо помнить, от туберкулёза не застрахован никто, особенно ребёнок. В силу возрастных особенностей дети в гораздо большей степени подвержены заболеванию туберкулёзом при первичном инфицировании, чем взрослые.
Именно поэтому, для контроля состояния противотуберкулёзного иммунитета и выявления момента первичного инфицирования детям ежегодно делается туберкулиновая проба Манту.
Взрослым пробу Манту проводят по показаниям.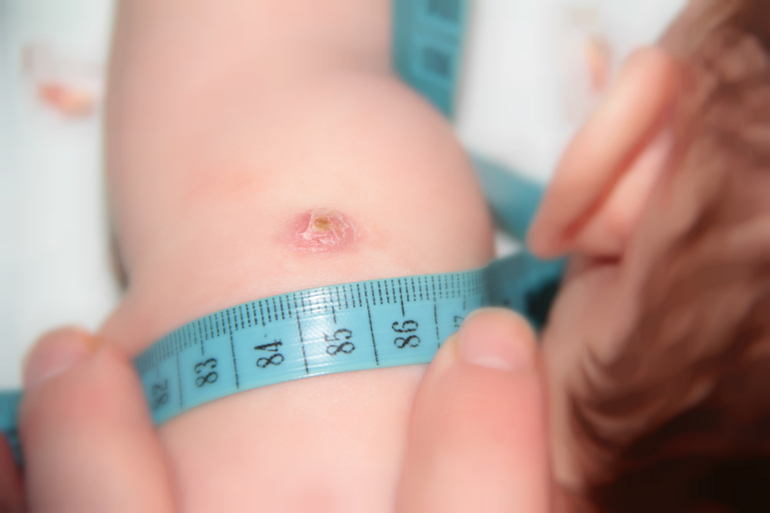 Проба Манту основана на внутрикожном введении малых доз туберкулина, совершенно безвредного для организма, с последующей оценкой аллергической реакцией, возникшей на месте введения. Туберкулин является продуктом жизнедеятельности микобактерий. Следует подчеркнуть, что проба Манту является безвредной.
Проба Манту основана на внутрикожном введении малых доз туберкулина, совершенно безвредного для организма, с последующей оценкой аллергической реакцией, возникшей на месте введения. Туберкулин является продуктом жизнедеятельности микобактерий. Следует подчеркнуть, что проба Манту является безвредной.
Вакцинация от туберкулеза детям в Москве
Не менее трети людей, проживающих на планете, являются носителями микобактерии туберкулеза, однако болезнь развивается только у 5-10% инфицированных. Снизить заболеваемость помогает только вакцинация от туберкулеза детям, поскольку меры по раннему выявлению инфекции не дают должного эффекта для ребенка. При снижении иммунитета, неправильном питании, неудовлетворительной санитарной обстановке спящая бактерия может начать активно размножаться и провоцировать туберкулез, поэтому это заболевание считается социальным.
От заболевания туберкулезом не застрахован никто – прививки рекомендуется делать каждому ребенку независимо от того, в какой социальной обстановке он проживает. БЦЖ не предохраняет от заражения микобактерией, поскольку в современных условиях это невозможно, однако эта вакцина дает два важных результата:
- ослабляет тяжесть течения болезни;
- исключает вероятность менингита и диссеминированных форм туберкулеза, которые практически всегда заканчиваются летальным исходом.
БЦЖ (калька с латинских букв BCG — bacillus Calmette–Guerin) – вакцина против туберкулеза, приготовленная из штамма коровьей туберкулезной палочки, которая утратила вирулентность для человека. В мире приготавливается огромное количество типов вакцин БЦЖ, но в 90% случаев они содержат один из трех штаммов – «Пастеровский», «Глаксо» и Токийский. Их эффективность совершенно одинакова.
Когда и как делают вакцинацию?
В России вакцина БЦЖ применяется ко всем младенцам поголовно из-за неблагоприятной ситуации по туберкулезу (в развитых странах она делается только детям из группы риска). Она производится на 3-7 сутки уже в роддоме. 2/3 детей до 7 лет уже успевают инфицироваться бактерией туберкулеза, БЦЖ помогает не допустить развития тяжелых смертельных форм болезни. Ревакцинация проводится в 7 лет, после чего повторные вакцинации больше не требуются.
Она производится на 3-7 сутки уже в роддоме. 2/3 детей до 7 лет уже успевают инфицироваться бактерией туберкулеза, БЦЖ помогает не допустить развития тяжелых смертельных форм болезни. Ревакцинация проводится в 7 лет, после чего повторные вакцинации больше не требуются.
Для новорожденных примеряется БЦЖ или БЦЖ-м, более щадящий вариант, в котором лишь половина состава составляет микроорганизмы. Он применяется для слабых и недоношенных детей. Препарат вводится внутрикожно в плечо, между верхней и средней третью. Реакция формируется спустя 4-6 недель. На месте введения прививки образуется гнойничок, который покрывается коростой и заживает. После отпадении коросты на всю жизнь остается рубчик, который свидетельствует о поставленной прививке.
Совместно с БЦЖ запрещено вводить какие-либо прививки, это правило касается и периода 4-6 недель после нее. По этой причине младенцу сначала ставят прививку от гепатита В, которая дает реакции сразу (проходят через 3-5 суток). После БЦЖ у ребенка наступает период покоя до 3 месяцев.
Реакция на вакцину и противопоказания
Прививка не должна вызывать болезненных ощущений в первые дни после нее – реакции развиваются через некоторое время после введения. Чаще всего замечаются следующие нормальные и свидетельствующие о правильности усвоения прививки реакции:
- Покраснение – нормальная прививочная реакция, должно находиться в месте инъекции и не распространяться дальше.
- Нагноение и нарывы – нормальная прививочная реакция, прививка должна принять форму гнойничка с корочкой, красноты на данный момент быть не должно (в этом случае следует обратиться к врачу). Если ранка нагнаивается несколько раз, ставится диагноз БЦЖит.
- Место укола опухло – это происходит сразу после введения вакцины и продолжается максимум 2-3 дня. После этого место введения иглы должно стать обычным, не отличимым от других тканей рядом. Нагноение начинается только через 1,5 месяца.
- Зуд – эта реакция является нормальной, однако чесать место прививки не следует.

- Температура – редко появляется сразу после вакцинации, иногда может появиться при образовании гнойничка.
К противопоказаниям для применения вакцины относятся небольшая масса новорожденного, обострение хронических заболеваний, иммунодефицит, наличие ВИЧ у матери, положительная проба Манту, наличие лимфаденита или келоидного рубца после предыдущей вакцины и некоторые другие характеристики.
Прививка БЦЖ новорожденному – противопоказания и последствия
Уже в первые дни жизни крохе предстоит пройти обязательную вакцинацию. А поскольку сегодня родителям предоставлено право соглашаться или отказываться от вакцинации, молодые мамочки хотят узнать, что такое прививка БЦЖ новорожденным, чтобы грамотно взвесить все «за и против».
среда, января 24th, 2018
Присоединяйтесь к Клубу Заботливых Мам NestleBaby®!
Зарегистрируйся сегодня
Получайте полезные советы и принимайте участие в тестировании продукции
БЦЖ прививка – что это и для чего?
БЦЖ прививка – вакцина, предупреждающая туберкулез. Состав вакцины основан на культуре живых и мертвых штаммов бактерий. Простыми словами, это палочка туберкулеза, но в слабой форме, которая не нанесет вреда маленькому организму. Для чего ее нужно делать? Для того, чтобы организм малютки смог выработать иммунитет на туберкулезную палочку и впоследствии не допустить заболевания. Целью такой вакцины является:
- минимизация риска заразиться туберкулезом;
- защита от преобразования скрытой формы заболевания в открытую;
- профилактика от заражения;
- предотвращение развития заболевания и перетекания в тяжелую форму;
- предотвращение летального исхода в случае заражения.
Календарь вакцинации
Прививка от туберкулеза новорожденному проводится впервые 3-4 дня после рождения, еще в роддоме. Далее согласно календарю прививок осуществляется две ревакцинация, в 7 и 14 лет. Если по каким-то причинам, к примеру, ввиду противопоказаний, врач отложил первую вакцинацию, спустя пару месяцев малышу сделают пробу Манту, результаты которой дадут понять, готов ли он на проведение БЦЖ, так же происходит в 7 и 14 лет. Таким способом врачи снижают восприимчивость ребенка к палочке туберкулеза, а также влиянию микробактерий. И если родители вправе отказать в проведении вакцинации при обычных обстоятельствах, то в случае контакта ребенка с зараженными туберкулезом – вакцинирование осуществляется в обязательном порядке.
Если по каким-то причинам, к примеру, ввиду противопоказаний, врач отложил первую вакцинацию, спустя пару месяцев малышу сделают пробу Манту, результаты которой дадут понять, готов ли он на проведение БЦЖ, так же происходит в 7 и 14 лет. Таким способом врачи снижают восприимчивость ребенка к палочке туберкулеза, а также влиянию микробактерий. И если родители вправе отказать в проведении вакцинации при обычных обстоятельствах, то в случае контакта ребенка с зараженными туберкулезом – вакцинирование осуществляется в обязательном порядке.
Прививка БЦЖ новорожденным: особенности вакцинации
Реакция новорожденного на прививку БЦЖ носит отложенный характер и длится на протяжении 2, а то и 4 месяцев. В это время ребенку нельзя давать какие либо препараты или вакцинировать, поскольку организм занят формированием иммунитета и борьбой с инфекцией. Методика вакцинирования заключается во введении препарата внутрикожно, одним или двумя проколами во внешнюю сторону левого плеча.
Реакция малютки проявляется через месяц с момента укола, на месте прививки обязуется гнойничок, который припухает и покрывается корочкой. Такие явления не должны пугать молодых родителей, так как являются нормальной реакцией организма. В течение месяца или двух ранка заживет, а на ее месте останется маленький рубец. Также одной из реакций, которая не должна вызывать опасений, является повышенная температура. Но врачи все же рекомендуют контролировать ее изменения и держать в курсе своего ведущего терапевта.
Возможные последствия прививки БЦЖ
Последствия прививки БЦЖ – первое, что беспокоит любящих родителей. Но ни один врач не даст стопроцентную гарантию на ту или иную реакцию маленького организма. Ведь все организмы и степень восприимчивости индивидуальны, поэтому реакция может быть разнообразной. Поэтому, осознавая значимость БЦЖ, большинство родителей все же идут на риск, а весомым аргументом становится статистика, демонстрирующая минимальный процент деток с неблагоприятными последствиями.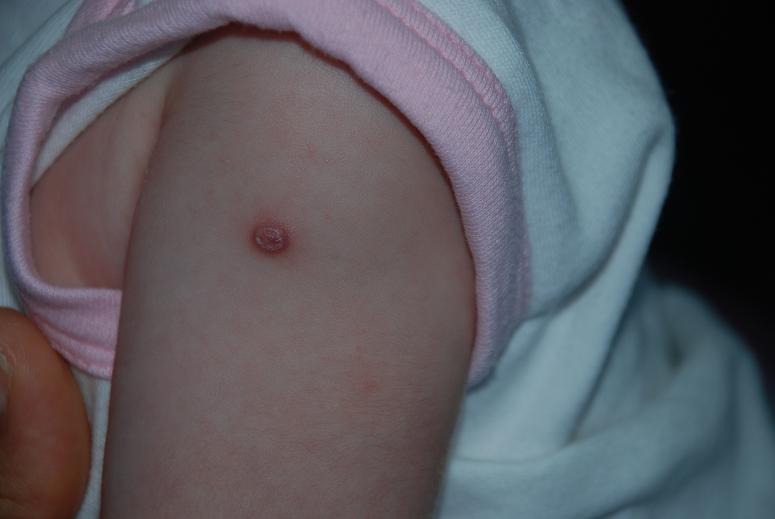
Одним из наиболее частых последствий является то, что иммунитет так и не сформировался. Причиной тому может быть слабая иммунная система либо отсутствие подверженности к микробактериям, что большой плюс, потому что ребенок не восприимчив к туберкулезу. Иногда родители сталкиваются с плохим и медленным заживлением ранки, после чего может образоваться келоидный рубец. Осложнения от прививки БЦЖ могут быть вызваны неправильной методикой вакцинирования или невнимательным отношением врача, который не определил противопоказаний. Поэтому если родитель не доверяет конкретному специалисту, провести прививку можно у частного врача, не вызывающего сомнения.
Противопоказания к прививке
Бывают случаи, когда прививка противопоказана малышам. Виной тому может быть слабый иммунитет или заболевания. Тогда проведение вакцинирования откладывают до семилетнего возраста. Также основанием для противопоказания является:
- низкий вес ребенка – меньше 2,5 кг;
- мама с ВИЧ;
- сложные заболевания;
- контакт с бактериями за несколько дней до вакцинации;
- неблагоприятные последствия после вакцины у кого-то из членов семьи.
В таких случаях можно либо не делать прививку, либо отложить ее до момента полного восстановления малыша. Прививка БЦЖ новорожденным – решение родителей. Помните, что эта вакцина предотвращает туберкулезное поражение, лечение которого бывает крайне сложным, а иногда вообще не дает результатов. Маленький неокрепший организм с несформированным иммунитетом может легко стать носителем палочки в случае отказа от прививки.
Подробнее
Памятка для родителей по вакцинопрофилактике
Предупредить! Защитить! Привить!
Вакционопрофилактика – система мероприятий, осуществляемых в целях предупреждения, ограничения распространения и ликвидации инфекционных болезней путём проведения профилактических прививок.
Одним из важнейших мероприятий, предпринимаемых для сохранения и укрепления здоровья детей, является организация и проведение профилактических прививок.
Защиту организма от возбудителей инфекционных заболеваний осуществляет иммунная система. Она способна защитить ребенка от постоянно окружающих нас микроорганизмов (кишечной палочки, стрептококков и других), но не всегда в силах справиться с возбудителями дифтерии, вирусного гепатита «А», «В», столбняка, коклюша, кори и других инфекционных заболеваний. Прививки, полученные в детстве, в большинстве случаев, создают основу иммунитета против отдельных инфекций на всю жизнь.
Рекомендации перед вакцинацией и после
Перед прививкой ребенка нужно оберегать от контактов с больными. При наличии пищевой аллергии необходимо строго соблюдать диету, не вводить в рацион новые продукты. Такой же тактики нужно придерживаться в течение 5-7 дней после прививки.
После прививки у некоторых детей может наблюдаться постпрививочная реакция, такая как: повышение температуры, покраснение или уплотнение в месте введения вакцины. Это закономерная реакция, которая говорит о начале формирования защиты от инфекции. Как правило, такая реакция носит кратковременный характер (1-3 дня).
При повышении температуры до 380 не требуется никакого лечения, температура выше 380, необходимо использовать жаропонижающие средства, назначение сделает врач-педиатр, в соответствии с возрастом вашего ребенка.
В случае покраснения и уплотнения в месте введения вакцины, необходимо поставить в известность медработника, проводившего прививку. Для детей, у которых наблюдалась постпрививочная реакция, рекомендуются подготовительные мероприятия, которые назначит врач перед следующей прививкой.
Каждый человек имеет право сделать свой выбор – прививаться или нет, но родители должны знать, что отказываясь от прививок, они лишают своих детей прав на здоровье. Кроме того, если в детском учреждении карантин по какой-то инфекции, а у вашего ребёнка отсутствует прививка, то его могут не принять в детский коллектив.
Родители! Отказываясь от прививок, Вы не только лишаете защиты своего ребенка, но и подвергаете опасности других детей, а также способствуете распространению инфекционных заболеваний в обществе.
Важно подчеркнуть, что современная медицина не имеет пока более эффективного средства профилактики инфекционных заболеваний, чем вакцинация.
Календарь профилактических прививок детям
Возраст | Название прививки | Вид вакцинации |
12 часов | вирусный гепатит В (ВГВ) | первая вакцинация |
3-5 суток | туберкулез (БЦЖ) | вакцинация |
1 мес. | ВГВ | вторая вакцинация |
3 мес. | полиомиелит | первая вакцинация |
4 мес. | АКДС, полиомиелит | вторая вакцинация |
5 мес. | АКДС, ВГВ, полиомиелит [или инактивированная полиомиелитная вакцина (ИПВ)] | третья вакцинация |
1 год | корь, краснуха, эпидемический паротит | первая вакцинация |
2 года | полиомиелит | вторая ревакцинация |
6 лет | корь, краснуха, эпидемический паротит дифтерия, столбняк | ревакцинация |
7 лет | полиомиелит туберкулез (БЦЖ) | третья ревакцинация ревакцинация |
13 лет | ВГВ (если ранее не прививался) | трехкратная вакцинация |
14 лет | туберкулез (БЦЖ) | ревакцинация |
Каждый год до 15 лет ребенку проводится туберкулинодиагностика (проба Манту)
Вакцинация защищает здоровье человека на каждом этапе его жизни
Пять причин сделать прививку:
- Предупредить ненужные страдания, связанные с заболеванием.

- Предупредить развитие осложненных форм болезни.
- Предупредить негативное влияние на планы семьи.
- Наличие широкого спектра вакцин с высоким профилем безопасности и профилактической эффективности.
Возможность индивидуализации иммунизации: применение разных схем и методов вакцинации для создания достаточного иммунитета у каждого прививаемого человека
Иммунизация – метод создания искусственного иммунитета у людей и животных.
О значимости вакцины БЦЖ — статьи от специалистов клиники «Мать и дитя»
«В 1921 году во Франции Кальметом впервые была использована вакцина БЦЖ для предупреждения туберкулеза у ребенка 6-ти лет. Дальнейшие наблюдения за этим ребенком в течение 5 лет показали, что туберкулезом он не заболел.В СССР Вакцинация БЦЖ началась с 1926 года, вначале как научное изыскание.
К тридцатым — сороковым годам были закончены клинические наблюдения за вакцинированными БЦЖ детьми и контрольной группой детей, не получивших вакцину. Установили, что заболеваемость туберкулезом среди детей, получивших вакцину, в 7 раз меньше, чем у невакцинированных. Кроме того, если и появлялись случаи возникновения туберкулёза у привитых детей, то формы туберкулеза были не осложненными с благоприятным исходом.
Предполагались различные методы введения вакцины, в том числе и пероральный. В ходе научных работ установлен наиболее оптимальный способ введения вакцины — внутрикожный. К сожалению, длительность хранения вакцины была непродолжительной, что затрудняло её транспортировку в стране.
С 1937 года начались работы по изысканию методов по удлинению сроков хранения вакцины. В 62 году ВОЗ утвердила требования к сухой вакцине. Каждая страна выпускает вакцину БЦЖ с различным содержанием жизнеспособных микобактерий, участвующих в создании иммунитета. В Российской вакцине БЦЖ (НИИ эпидемиологии и микробиологии им. Гамалеи Н.Ф.) содержится 8 млн/мг живых бактерий. В прививочной дозе отечественной вакцины содержится 500-600 тысяч бактерий, способных к росту на питательных средах.
Клинические наблюдения за реакцией организма на вакцинацию БЦЖ подтверждены данными патоморфологов. Основные изменения развиваются в системе лимфатических узлов, ретикуло-эндотелиальном аппарате печени, селезенки и легких. Изменения в организме при введении вакцины начинаются в первые недели после вакцинации и нарастают через 3-4 месяца.
Через 4-6 недель после вакцинации на месте внутрикожного введения вакцины развивается специфическая реакция в виде инфильтрата диаметром 5-8 мм с небольшим узелком в центре. Узелок увеличивается в размерах, превращается в пустулу с казеозным содержимым. Пустула может вскрыться, выделяется капелька густого гноя — казеоза. Над вскрывшейся пустулой формируется геморрагическая корочка, под которой вновь накапливается казеоз. Через 2-3 дня корочка снимается, капелька казеоза удаляется. И так несколько раз. С каждым разом корочка становится меньше в диаметре, постепенно формируется поствакцинальный рубчик. У части детей (около 16% от всех привитых БЦЖ) рубчик не формируется, что обусловлено врожденными особенностями иммунитета. Но это не значит, что ребенок получивший вакцину БЦЖ, у которого в дальнейшем не сформировался поствакцинальный рубчик, не защищен от туберкулеза. Местная прививочная реакция не требует какого-либо вмешательства. У детей с нормальным иммунитетом вакцина БЦЖ не вызывает каких-либо патологий.
В настоящее время помимо вакцины БЦЖ с 1986 года используется вакцина БЦЖ-М для щадящей иммунизации. Эта вакцина отличается от вакцины БЦЖ тем, что в прививочной дозе содержится меньшее количество мертвых микробных тел, что способствует уменьшению неспецифического аллергического воздействия на организм человека.
С 2020 года планируется отмена ревакцинаций БЦЖ и БЦЖ-М в 7 лет и 14 лет. То есть ребенок должен быть привит от туберкулеза единожды, желательно в раннем детском возрасте».
Вакцинация БЦЖ у детей, инфицированных ВИЧ . Этот риск намного выше среди ВИЧ-инфицированных детей, а данные о защитной эффективности БЦЖ у ВИЧ-инфицированных детей отсутствуют. Недавние исследования безопасности вакцины БЦЖ для ВИЧ-инфицированных младенцев привели к изменениям в политике, но их реализация затруднена.Необходимы новые подходы к профилактике туберкулеза среди младенцев и детей, особенно ВИЧ-инфицированных младенцев. В этом документе кратко рассматриваются вопросы безопасности и эффективности БЦЖ у ВИЧ-инфицированных младенцев и обсуждаются другие подходы к профилактике ТБ, включая новые противотуберкулезные вакцины и стратегии вакцинации.
Недавние исследования безопасности вакцины БЦЖ для ВИЧ-инфицированных младенцев привели к изменениям в политике, но их реализация затруднена.Необходимы новые подходы к профилактике туберкулеза среди младенцев и детей, особенно ВИЧ-инфицированных младенцев. В этом документе кратко рассматриваются вопросы безопасности и эффективности БЦЖ у ВИЧ-инфицированных младенцев и обсуждаются другие подходы к профилактике ТБ, включая новые противотуберкулезные вакцины и стратегии вакцинации.
1. Введение
По оценкам, во всем мире ежегодно вводится более 100 миллионов доз вакцины БЦЖ [1]. Однако точный характер защиты от туберкулеза после вакцинации БЦЖ полностью не выяснен.Эффективность и безопасность вакцины в контексте ВИЧ-инфекции являются противоречивыми и являются темой значительных недавних и текущих исследований. Такие исследования имеют большое значение для глобального общественного здравоохранения, поскольку эндемичные по ТБ районы часто совпадают с районами с высокой распространенностью ВИЧ, а коинфекция ВИЧ / ТБ распространена как среди взрослых, так и среди детей. В период с 2004 по 2006 год заболеваемость туберкулезом среди ВИЧ-инфицированных младенцев в Кейптауне, Южная Африка, составляла 1596 случаев на 100 000 по сравнению с 66 на 100 000 среди младенцев, не инфицированных ВИЧ [2].Младенцы и дети раннего возраста, контактирующие с больными туберкулезом взрослых, подвергаются высокому риску развития тяжелых и сложных форм туберкулеза. Диагностические трудности и сложность, связанные с клиническим ведением младенцев и детей с коинфекцией, увеличивают масштабы педиатрической проблемы. Существует острая необходимость в безопасных и эффективных стратегиях профилактики туберкулеза у младенцев и детей, особенно у ВИЧ-инфицированных.
2. Эффективность вакцины БЦЖ
Клиническая эффективность вакцины измеряется в процентах снижения заболеваемости вакцинированных лиц, связанного с вакцинацией.Эффективность представляет собой совокупный результат трех событий: (1) доля вакцины, «принятая», (2) степень защиты вакцины и (3) продолжительность защитного иммунитета [3].
Исследованию эффективности БЦЖ препятствовала невозможность определить надежный клинический или иммунологический параметр, указывающий на защиту от развития туберкулеза после вакцинации БЦЖ. Ни наличие рубца БЦЖ, ни реактивность кожной туберкулиновой пробы не коррелируют с защитой от туберкулеза [4].
В попытке лучше понять иммунитет, индуцированный БЦЖ, исследователи описали природу иммунных ответов после вакцинации БЦЖ и латентной инфекции ТБ. У многих людей вакцинация БЦЖ способна вызывать полифункциональный Т-клеточный ответ, в котором преобладают клетки, способные продуцировать цитокины 1 типа (включая интерферон- (IFN-) гамма, интерлейкин- (IL-) 2 и фактор некроза опухоли (TNF)) [ 5].
Были также попытки определить специфические иммунные дефекты у людей, которые очень восприимчивы к развитию туберкулеза или осложнений после вакцинации живой ослабленной БЦЖ, включая ВИЧ-инфицированных людей и младенцев с первичными иммунодефицитными расстройствами [3].Было показано, что среди ВИЧ-инфицированных младенцев, не получающих антиретровирусную терапию, БЦЖ вызывает гораздо более низкую частоту и качество специфических Т-лимфоцитов CD4, чем у ВИЧ-неинфицированных младенцев, и это сохраняется в течение первого года жизни [6]. Шестинедельные контактировавшие с ВИЧ (рожденные от ВИЧ-инфицированных матерей), но неинфицированные младенцы, получившие БЦЖ при рождении, имели более низкие ответы на IFN-гамма, чем младенцы, не подвергавшиеся воздействию ВИЧ [7]. У детей, получающих антиретровирусную терапию, возможно восстановление антимикобактериального иммунного ответа [8].Лица с генетическими нарушениями пути цитокинов IFN-гамма особенно предрасположены к развитию активного туберкулеза [9].
Крупные рандомизированные клинические испытания предоставили данные об эффективности БЦЖ. Было показано, что у младенцев, не инфицированных ВИЧ, введение разовой дозы вакцины Bacillus Calmette-Guérin (БЦЖ) при рождении или вскоре после рождения обеспечивает примерно 80% защиту от диссеминированных форм туберкулеза (милиарный туберкулез и туберкулезный менингит) в младенчестве [ 10–12]. БЦЖ менее эффективна и вариабельна в профилактике туберкулеза легких у младенцев и взрослых с эффективностью от 0% до 80%, о которой сообщалось в клинических испытаниях в прошлом веке [12].Эти данные свидетельствуют о том, что БЦЖ вряд ли будет эффективна для предотвращения заражения M. tuberculosis , но может предотвратить прогрессирование инфекции в болезнь, особенно диссеминированные формы туберкулеза. Поскольку диссеминированное заболевание чаще встречается среди детей раннего возраста и связано с высокой заболеваемостью и смертностью, вакцинация новорожденных БЦЖ может быть рентабельной в качестве педиатрического вмешательства, но мало влияет на передачу туберкулеза среди взрослых [3]. Факторы, которые, как считается, влияют на вариабельность защиты, включают вариацию штамма БЦЖ, дозу вакцины, возраст пациента на момент вакцинации, статус питания, генетические факторы хозяина, микобактериальные и глистные инфекции окружающей среды и географическое положение [13–15].
БЦЖ менее эффективна и вариабельна в профилактике туберкулеза легких у младенцев и взрослых с эффективностью от 0% до 80%, о которой сообщалось в клинических испытаниях в прошлом веке [12].Эти данные свидетельствуют о том, что БЦЖ вряд ли будет эффективна для предотвращения заражения M. tuberculosis , но может предотвратить прогрессирование инфекции в болезнь, особенно диссеминированные формы туберкулеза. Поскольку диссеминированное заболевание чаще встречается среди детей раннего возраста и связано с высокой заболеваемостью и смертностью, вакцинация новорожденных БЦЖ может быть рентабельной в качестве педиатрического вмешательства, но мало влияет на передачу туберкулеза среди взрослых [3]. Факторы, которые, как считается, влияют на вариабельность защиты, включают вариацию штамма БЦЖ, дозу вакцины, возраст пациента на момент вакцинации, статус питания, генетические факторы хозяина, микобактериальные и глистные инфекции окружающей среды и географическое положение [13–15].
Данные о защитной эффективности БЦЖ среди ВИЧ-инфицированных очень ограничены, поскольку большинство крупных исследований эффективности БЦЖ проводилось до начала пандемии ВИЧ. У ВИЧ-инфицированных взрослых вакцинация БЦЖ не показала статистически значимого эффекта в предотвращении легочного или диссеминированного туберкулеза [16]. Сообщалось о нескольких исследованиях с участием детей. В замбийском ретроспективном исследовании случай-контроль сообщалось об отсутствии защитного эффекта БЦЖ в 116 случаях ТБ и 154 контрольных случаях без ТБ; напротив, 59% защитный эффект (OR 0.41, 95% ДИ 0,18–0,92) вакцинации БЦЖ было обнаружено у ВИЧ-неинфицированных детей [17]. Другое ретроспективное исследование, проведенное в Аргентине, показало, что у ВИЧ-инфицированных детей, вакцинированных БЦЖ, не было значительно более низкой заболеваемости туберкулезом по сравнению с невакцинированными детьми в течение 12-летнего периода наблюдения (Аннотация WeOa0104, третья конференция IAS по патогенезу и лечению ВИЧ, 2005, [ 18]).
Такие ретроспективные эпидемиологические исследования ограничены потенциальной систематической ошибкой из-за нестандартных критериев диагностики туберкулеза, потенциальных практик селективной вакцинации БЦЖ и плохой документации вакцинации БЦЖ или использования рубца БЦЖ для обозначения вакцинации БЦЖ, которая, как сообщается, была реже у ВИЧ-инфицированных по сравнению с ВИЧ-неинфицированными детьми [19].
Перспектива проспективных рандомизированных исследований по оценке безопасности и эффективности вакцинации БЦЖ у ВИЧ-инфицированных и ВИЧ-инфицированных младенцев и детей осложняется описанными факторами: отсутствие клинического или иммунного коррелята защиты, индуцированной БЦЖ, доказательства эффективности против диссеминированных форм туберкулеза у детей, не инфицированных ВИЧ, трудностей с диагностическими критериями заболевания туберкулезом у детей и того факта, что ВИЧ-статус младенцев неизвестен при рождении, то есть при введении вакцины БЦЖ в развивающихся странах.Дополнительной областью неопределенности является влияние раннего начала антиретровирусной терапии (АРТ) у младенцев на иммунитет, вызванный БЦЖ, и потенциальная роль отсроченной вакцинации БЦЖ до наступления срока АРТ или ревакцинации.
3. Безопасность вакцины БЦЖ
Нормальное развитие местной кожной реакции после внутрикожной вакцинации БЦЖ включает развитие эритематозного пятна (через 3 недели после вакцинации), образование папулы (через 6 недель), неглубокую язву ( на 10 недель) и заживление (на 14 недель).
До пандемии ВИЧ БЦЖ имела хорошие показатели безопасности: сообщалось в основном о незначительных реакциях, а серьезные побочные эффекты, как правило, ограничивались младенцами с первичными иммунодефицитными расстройствами, включая тяжелый комбинированный иммунодефицит (ТКИД), хроническую гранулематозную болезнь (ХГБ), синдром ДиДжорджи, IFN дефицит гамма-рецепторов и дефицит ИЛ-12 [19]. По оценкам, местные побочные эффекты у младенцев возникают у <0,04% реципиентов вакцины, а диссеминированное заболевание БЦЖ - у <0. 002% реципиентов вакцины [20, 21].
002% реципиентов вакцины [20, 21].
Более серьезное заболевание БЦЖ было описано у ВИЧ-инфицированных младенцев и даже у взрослого ВИЧ-инфицированного человека через 30 лет после вакцинации [22]. Последующее многоцентровое исследование показало, что риск диссеминированного заболевания БЦЖ у взрослых, инфицированных ВИЧ с ослабленным иммунитетом, которые получили вакцинацию БЦЖ в младенчестве, был очень низким [23]. Однако риск как местной, так и диссеминированной болезни БЦЖ среди ВИЧ-инфицированных младенцев и детей стал серьезной проблемой для общественного здравоохранения.
Два дозорных исследования в Южной Африке, хотя и ретроспективные серии случаев, показали, что среди ВИЧ-инфицированных младенцев с ослабленным иммунитетом, еще не получающих АРТ, распространенность подтвержденной посевом БЦЖ отдаленной или диссеминированной болезни БЦЖ гораздо выше, чем считалось ранее. Первое исследование выявило одно важное объяснение непризнания болезни БЦЖ. Лабораторный посев респираторного секрета (включая образцы промывания желудка) на туберкулез идентифицирует M. tuberculosis complex (который включает M.tuberculosis и M. bovis среди прочих), и дальнейшее видообразование обычно не проводится. В этом исследовании ученые выполнили дальнейшее видообразование комплекса M. tuberculosis в 183 культивируемых изолятах от 49 ВИЧ-инфицированных детей с диагнозом «туберкулез» [24]. Датский штамм M. bovis BCG был изолирован от пяти младенцев, все из которых имели тяжелую иммуносупрессию. В группе из пяти младенцев у четырех был подмышечный лимфаденит, ипсилатеральный по отношению к месту вакцинации БЦЖ, у двух были признаки легочной болезни БЦЖ, и у двух была региональная и легочная болезнь БЦЖ.
Второе исследование представляло собой ретроспективный обзор клинически подтвержденной болезни БЦЖ у детей младше 13 лет, диагностированной в течение трех лет [25]. Среди 25 детей 88% имели местное заболевание, 32% — отдаленное или диссеминированное заболевание, а 20% — оба заболевания. Семнадцать из 25 детей были ВИЧ-инфицированы, а двое имели другие иммунодефициты. Все восемь детей с отдаленным или диссеминированным заболеванием имели тяжелый иммунодефицит (шесть были ВИЧ-инфицированы), а уровень смертности в этой группе составил 75%.
Семнадцать из 25 детей были ВИЧ-инфицированы, а двое имели другие иммунодефициты. Все восемь детей с отдаленным или диссеминированным заболеванием имели тяжелый иммунодефицит (шесть были ВИЧ-инфицированы), а уровень смертности в этой группе составил 75%.
Подходы математического моделирования оценивают риск распространения БЦЖ у ВИЧ-инфицированных младенцев в контексте Южной Африки в пределах от 329 до 417 на 100 000 реципиентов вакцины, при условии 95% охвата вакциной БЦЖ, распространенности ВИЧ среди беременных женщин 12,4–15,4% и уровень вертикальной передачи ВИЧ составляет 5% [26]. Это очень много.
Еще одно важное наблюдение заключается в том, что БЦЖ является относительно частой ассоциацией с воспалительным синдромом восстановления иммунитета (ВСВИ) среди младенцев и детей раннего возраста, начинающих АРТ.IRIS относится к возникновению парадоксального инфекционного или воспалительного состояния у пациента, выздоравливающего после тяжелого иммунодефицита [27]. «Разоблачение» туберкулеза после начала АРТ — одна из самых распространенных форм ВСВИ, описываемых у взрослых, тогда как БЦЖ-ВСВИ, проявляющаяся как «парадоксальная» форма синдрома, отмечалась у 3–14,8% детей, начинающих АРТ на юге страны. Африканские и тайские когорты [28–30]. Обычное клиническое проявление BCG-IRIS — воспалительный ипсилатеральный подмышечный или регионарный лимфаденит с воспалением или образованием абсцесса в месте вакцинации или без него.Более молодой возраст и более высокая исходная вирусная нагрузка ВИЧ были определены как факторы риска развития BCG-IRIS [29]. Хотя подозрение на отдаленное или диссеминированное заболевание, особенно с поражением легких или костей, было описано в контексте BCG-IRIS, неясно, может ли диссеминация происходить на ранней стадии после вакцинации при рождении, но проявляться клинически только после начала АРТ в возрасте нескольких месяцев. .
Следует ли отложить вакцинацию БЦЖ при рождении новорожденным, контактировавшим с ВИЧ, и вообще избегать вакцинации ВИЧ-инфицированных детей?
Как обсуждалось выше, клинические и иммунологические доказательства защитной эффективности вакцинации БЦЖ у ВИЧ-инфицированных младенцев отсутствуют, и существуют серьезные опасения относительно безопасности БЦЖ у ВИЧ-инфицированных младенцев как до, так и после начала АРТ. В 2007 году Глобальный консультативный комитет по безопасности вакцин (GACVS) Всемирной организации здравоохранения (ВОЗ) опубликовал пересмотренные рекомендации, противопоказавшие вакцинацию БЦЖ детям с ВИЧ-инфекцией [31].
В 2007 году Глобальный консультативный комитет по безопасности вакцин (GACVS) Всемирной организации здравоохранения (ВОЗ) опубликовал пересмотренные рекомендации, противопоказавшие вакцинацию БЦЖ детям с ВИЧ-инфекцией [31].
Более актуальным является вопрос о том, следует ли вводить вакцину БЦЖ всем младенцам, в том числе младенцам, рожденным от ВИЧ-инфицированных матерей при рождении, или необходимо отложить вакцинацию БЦЖ для младенцев, контактировавших с ВИЧ, до тех пор, пока ВИЧ-инфекционный статус не будет окончательно установлен. вирусологическое тестирование в возрасте около 6 недель.Увеличение охвата мерами по сокращению передачи ВИЧ от матери к ребенку (включая профилактические антиретровирусные препараты для матери и ребенка или антиретровирусную терапию для матери и безопасное вскармливание младенцев) приводит к тому, что большинство младенцев, рожденных от ВИЧ-инфицированных матерей, в конечном итоге остаются неинфицированными. Ожидается, что этим младенцам принесет пользу вакцинация БЦЖ без риска диссеминированного заболевания БЦЖ, наблюдаемого у ВИЧ-инфицированных младенцев. Отсрочка вакцинации БЦЖ с рождения до 10-недельного возраста может привести к усилению Т-клеточного ответа памяти CD4, включая полифункциональные Т-клетки, экспрессирующие IFN-γ , TNF- α и IL-2, при измерении в возрасте 1 года у ВИЧ. -неинфицированные младенцы [32].Это также может быть применимо к неинфицированным младенцам, контактировавшим с ВИЧ, но необходимы дальнейшие лабораторные и клинические исследования.
Есть опасения, что практика выборочной отсрочки вакцинации может поставить под угрозу преимущества высоких показателей охвата вакциной БЦЖ в результате того, что контактировавшие с ВИЧ, но неинфицированные дети, пропускающие последующую вакцинацию после 6-недельного возраста. Рабочая группа BCG Секции здоровья легких детей Международного союза борьбы с туберкулезом и легочными заболеваниями опубликовала консенсусное заявление о соответствующих критериях, которые должны учитываться программами по ВИЧ / ТБ при введении отсрочки селективной вакцинации БЦЖ [33]. К ним относятся: высокая посещаемость материнского тестирования на ВИЧ в сочетании с эффективными стратегиями профилактики передачи от матери ребенку (ППМР), включая АРТ матери; ранняя вирусологическая диагностика ВИЧ-инфекции у младенцев в сочетании с учреждением АРТ; координация программ ППМР, вакцинации и борьбы с туберкулезом для сведения к минимуму потерь для последующего наблюдения, внедрения альтернативных стратегий профилактики туберкулеза и проведения успешной вакцинации после выборочной невакцинации при рождении. В настоящее время реализация стратегий селективной вакцинации неосуществима в большинстве стран, которые являются высокоэндемичными по ВИЧ и туберкулезу, и всеобщая вакцинация младенцев БЦЖ, вероятно, будет продолжаться в течение некоторого времени.
К ним относятся: высокая посещаемость материнского тестирования на ВИЧ в сочетании с эффективными стратегиями профилактики передачи от матери ребенку (ППМР), включая АРТ матери; ранняя вирусологическая диагностика ВИЧ-инфекции у младенцев в сочетании с учреждением АРТ; координация программ ППМР, вакцинации и борьбы с туберкулезом для сведения к минимуму потерь для последующего наблюдения, внедрения альтернативных стратегий профилактики туберкулеза и проведения успешной вакцинации после выборочной невакцинации при рождении. В настоящее время реализация стратегий селективной вакцинации неосуществима в большинстве стран, которые являются высокоэндемичными по ВИЧ и туберкулезу, и всеобщая вакцинация младенцев БЦЖ, вероятно, будет продолжаться в течение некоторого времени.
4. Другие способы защиты ВИЧ-инфицированных младенцев от туберкулеза
Раннее начало АРТ (особенно в возрасте до 12 недель) у ВИЧ-инфицированных младенцев, независимо от клинических критериев или критериев подсчета CD4, значительно снижает смертность и заболеваемость туберкулезом [34] и может снизить частоту и тяжесть BCG-IRIS, вероятно, в результате сохранения иммунитета (Abstract 600, четырнадцатая конференция по ретровирусам и оппортунистическим инфекциям, 2008 г., [35]).
Рутинная предконтактная профилактика изониазидом для всех ВИЧ-инфицированных младенцев (младше 12 месяцев) в настоящее время не рекомендуется ВОЗ по результатам двойного слепого рандомизированного плацебо-контролируемого исследования с участием 452 младенцев, которые не показали никаких преимуществ (38, Резюме G2-1346a, 48-я международная конференция по противомикробным препаратам и химиотерапии, 2008 г., [36]).Ранее опубликованное исследование показало значительное снижение смертности и заболеваемости туберкулезом среди ВИЧ-инфицированных младенцев и детей, получающих профилактику изониазидом [37]. В последних рекомендациях ВОЗ рекомендуется шесть месяцев профилактической терапии изониазидом (ПЛИ) для ВИЧ-инфицированных детей любого возраста, подвергшихся воздействию инфекционного источника ТБ после исключения заболевания ТБ, и шесть месяцев ПЛИ для ВИЧ-инфицированных детей в возрасте старше 12 месяцев. которые, как известно, не инфицированы туберкулезом [38].
которые, как известно, не инфицированы туберкулезом [38].
Введение вакцины БЦЖ ВИЧ-инфицированным младенцам или детям младшего возраста после начала АРТ и достижения некоторой степени восстановления иммунитета — еще один интересный подход, который еще не изучался подробно.Однако с учетом опасений по поводу безопасности живых вакцин в целом и БЦЖ в частности среди ВИЧ-инфицированных или лиц с иным ослабленным иммунитетом, а также пересмотренной рекомендации ВОЗ избегать применения БЦЖ у младенцев, контактировавших с ВИЧ, маловероятно, что БЦЖ будет проходить проспективную оценку при ВИЧ. -инфицированные младенцы или дети.
Новые вакцины БЦЖ имеют большие перспективы в среднесрочной и долгосрочной перспективе и могут в конечном итоге решить вопросы, связанные с эффективностью и безопасностью, на устойчивой основе.Достижения в области генетической технологии и секвенирования генома M. tuberculosis ( M. tb ) в течение 1990-х годов ускорили разработку новых вакцин-кандидатов против туберкулеза, и пять из них достигли стадии 1-й фазы испытаний на людях. Поскольку ВИЧ-инфицированные лица несут такую большую долю общего бремени ТБ, важной характеристикой идеальной противотуберкулезной вакцины является безопасность, иммуногенность и эффективность в профилактике ТБ у лиц с ВИЧ-инфекцией или СПИДом, включая детей.Живые аттенуированные микобактериальные вакцины, такие как БЦЖ, вероятно, будут вытеснены рекомбинантными векторными вакцинами или субъединичными вакцинами [39].
Новые вакцины необходимо тестировать на разных этапах естественного течения инфекции ТБ и развития болезни. Стратегии вакцинации включают прединфекционную вакцинацию, проводимую при рождении или вскоре после него (как с БЦЖ), или в качестве ревакцинации после БЦЖ во время родов. Этот подход хорошо подходит для сред с тяжелым бременем ТБ, а метод бустинга имеет преимущество в том, что потенциально повышает иммуногенность и эффективность БЦЖ, избегая при этом этической дилеммы полного отказа от БЦЖ. Недостатком метода повторной вакцинации после вакцинации БЦЖ является то, что сохраняются опасения по поводу безопасности применения БЦЖ, особенно у ВИЧ-инфицированных младенцев.
Недостатком метода повторной вакцинации после вакцинации БЦЖ является то, что сохраняются опасения по поводу безопасности применения БЦЖ, особенно у ВИЧ-инфицированных младенцев.
Другой подход — постинфекционная вакцинация после доказательства естественного инфицирования M. tb с целью повышения или повышения иммунитета и предотвращения прогрессирования туберкулеза. Этот подход, при условии, что вакцина безопасна, будет особенно актуален для ВИЧ-инфицированных, в том числе детей раннего возраста с их высокими показателями заражения и заражения ТБ, а также повышенным риском прогрессирования ТБ, включая тяжелые формы внелегочных заболеваний.Две рекомбинантные векторные вакцины (MVA85A и AERAS-402) исследуются для использования в качестве бустерных вакцин у лиц, примированных БЦЖ, и для постинфекционной вакцинации. Это наиболее вероятные вакцины-кандидаты и стратегии вакцинации, вокруг которых можно было бы разработать этически приемлемые клинические испытания среди младенцев и детей, в том числе тех, кто контактировал с ВИЧ или инфицирован ВИЧ [39].
Лишь немногие из ведущих вакцин-кандидатов против туберкулеза до сих пор прошли клинические испытания на ВИЧ-инфицированных детях, однако эти две рекомбинантные векторные вакцины добились значительного прогресса в разработке вакцин.MVA85A состоит из модифицированной коровьей оспы Ankara (MVA), генетически сконструированной для экспрессии M. tb антигена 85A [40]. Вакцины на основе MVA имеют хорошие показатели безопасности после широкого использования в эпоху ликвидации оспы и в исследованиях кандидатных вакцин против ВИЧ [41, 42]. Ожидаются данные по безопасности и иммуногенности MVA85A у взрослых, инфицированных ВИЧ, инфицированных ТБ и ВИЧ-ТБ, а также у здоровых детей и младенцев (Hawkridge A. in Proceedings of Tuberculosis Vaccines for the World Conference, 2006, см. [43]) .Вакцина AERAS-402 использует аденовирус серотипа 35, неспособный к репликации, но модифицированный для экспрессии слитого белка трех антигенов M. tb (85A, 85B и TB10.4). Она была разработана для использования в качестве бустерной вакцины у лиц, получавших вакцину БЦЖ, и вошла в клинические исследования на людях [39].
tb (85A, 85B и TB10.4). Она была разработана для использования в качестве бустерной вакцины у лиц, получавших вакцину БЦЖ, и вошла в клинические исследования на людях [39].
Субъединичная вакцина Mtb72F содержит слитый белок двух иммуногенных белков M. tb , объединенных с адъювантом. Модификация, вакцина M72, оказалась безопасной и иммуногенной для здоровых взрослых добровольцев, хотя более реактогенной для людей, ранее подвергавшихся воздействию M.tb. Клинические испытания продолжаются в Европе и Южной Африке [39].
Проблемы, связанные с разработкой новых противотуберкулезных вакцин, включают ограниченное понимание защитных иммунных ответов против ТБ, трудности в выявлении латентной инфекции и дифференциации инфекции от болезни, трудности с определением клинических конечных точек испытаний и необходимость улучшения эпиднадзора за туберкулезом заболеваемость и смертность в контексте крупных испытаний вакцины 3 фазы, проводившихся в течение многих лет [39].
Другая важная проблема связана с этическими проблемами, связанными с внедрением новой противотуберкулезной вакцины в контексте существующей, хотя и очень несовершенной вакцины (БЦЖ), которая обычно вводится всем новорожденным в эндемичных по ТБ странах. Вероятно, что немногие страны, если вообще какие-либо страны, успешно выполнили рекомендацию ВОЗ избегать вакцинации БЦЖ новорожденных, контактировавших с ВИЧ, до тех пор, пока окончательный ВИЧ-статус не будет установлен в возрасте 6 недель. С этической точки зрения испытания вакцин с участием младенцев и детей, которые исключают вакцинацию БЦЖ в своей структуре, должны учитывать включение альтернативных мер профилактики ТБ, таких как обеспечение профилактической терапии изониазидом и рутинное раннее начало АРТ для ВИЧ-инфицированных младенцев и детей. , поскольку они могут стать стандартными вмешательствами.Поскольку новые противотуберкулезные вакцины, предназначенные для ВИЧ-инфицированных, вряд ли будут живыми аттенуированными вакцинами, ПЛИ вряд ли повлияет на меры иммуногенности вакцины, но может снизить риск развития активной формы туберкулеза у инфицированных ТБ лиц. Однако сохранение или восстановление иммунитета благодаря АРТ может повысить иммуногенность вакцины по сравнению с ВИЧ-инфицированными людьми, не получающими АРТ. Моральный императив включения таких вмешательств в испытания вакцин с участием ВИЧ-инфицированных младенцев и детей должен преобладать над другими соображениями.
Однако сохранение или восстановление иммунитета благодаря АРТ может повысить иммуногенность вакцины по сравнению с ВИЧ-инфицированными людьми, не получающими АРТ. Моральный императив включения таких вмешательств в испытания вакцин с участием ВИЧ-инфицированных младенцев и детей должен преобладать над другими соображениями.
5. Заключение
Вакцинация ВИЧ-инфицированных младенцев БЦЖ имеет неопределенную эффективность и связана со значительными проблемами безопасности у нелеченных младенцев и детей, получающих АРТ. Диагностика и лечение болезни БЦЖ сложны, что приводит к недооценке и неоптимальному уходу в условиях ограниченных ресурсов. Всеобщая иммунизация БЦЖ при рождении связана с высокими показателями охвата, тогда как выборочная отсрочка иммунизации БЦЖ до установления статуса ВИЧ-инфекции у младенцев создает риск значительного снижения охвата вакциной БЦЖ среди значительной доли инфицированных ВИЧ младенцев.Всеобщее раннее начало АРТ у ВИЧ-инфицированных младенцев в настоящее время может быть наиболее эффективным подходом к снижению риска как болезни БЦЖ, так и заболевания туберкулезом в этой группе. Профилактическая терапия изониазидом для младенцев и детей старшего возраста, контактировавших с ТБ, является важной дополнительной стратегией профилактики ТБ, в то время как новые вакцины БЦЖ с лучшими профилями безопасности и эффективности находятся в стадии исследования.
(PDF) Кожная реакция на БЦЖ у здоровых детей с отрицательным результатом Манту
BMC Infectious Diseases 2005, 5:19 http: // www.biomedcentral.com/1471-2334/5/19
Страница 4 из 5
(номер страницы не для цитирования)
определить характер реакции БЦЖ, сравнивая ранее вакцинированные
детей с невакцинированными детьми.
Как уже упоминалось, было проведено очень мало исследований по тесту БЦЖ
у детей, ранее вакцинированных БЦЖ.
Одно из таких исследований проведено PMUdani [7]: Тест БЦЖ при диагнозе
туберкулеза у детей — Indian Pediatric,
(1982), приложение, касающееся «Теста БЦЖ у детей, которые
ранее получали БЦЖ. имеется в наличии.«В этом исследовании он
имеется в наличии.«В этом исследовании он
пришел к трем группам выводов.
Первый
Отрицательный тест БЦЖ: младенец или ребенок могут не получить никакой реакции
из-за вакцинации БЦЖ, и организм ведет себя как
, если не была сделана предварительная иммунизация Предыдущий вакцина BCG vac-
, введенная при рождении, не способствовала иммунному ответу ребенка
Второй
Сильно положительный тест BCG, классическая ускоренная реакция.Эта реакция аналогична реакции, наблюдаемой у пациента
, страдающего туберкулезом.
Третий
Умеренно положительная реакция. При этой реакции у ребенка может появиться уплотнение
от 6 до 9 мм. Он приписал третий тип реакции
из-за предшествующей вакцинации БЦЖ.
В настоящем исследовании большая часть (около 84%) преувеличенных ответов теста
BCG в группе I имела реакцию между 6–8
мм, аналогичную реакции третьего типа, о чем свидетельствует
Удани [7].В исследовании, проведенном Удани [7], не было упомянуто
критериев исключения и исключения из исследования —
, и, вероятно, в исследование были включены все дети, которым ранее была сделана вакцинация
БЦЖ. Как упоминалось ранее, в настоящем исследовании сравниваются результаты теста
БЦЖ у детей, вакцинированных БЦЖ, и детей, вакцинированных БЦЖ, с
детей, не вакцинированных БЦЖ.
Хотя 50 мальчиков и 50 девочек, включенных в данное исследование
, не были отобраны в точности на основе формальных процедур случайной выборки
, вероятность систематической ошибки
невелика.Несмотря на отсутствие критерия включения, за исключением
с массой тела более 80% и исключения любого случая
с любым заболеванием, мы понимаем, что отсутствие
формального случайного распределения является ограничением для исследования.
Однако очень значимые результаты (p-значение <
0,00001) значительно перекрывают ограничение.
Диагностировать туберкулез у детей непросто. Как и у взрослых,
не всегда следует думать о терапевтических испытаниях у детей, так как
лекарства очень токсичны, а побочные эффекты, такие как рит Optic Neu-
, нелегко диагностировать у детей.Итак, Diagnos-
Лечение и лечение туберкулеза у детей — это палка о двух концах.
В наши дни ПЦР и другие новые исследования имеют
, которые стали полезными, но они просто добавляют к старому режиму исследования
и не позволяют полностью прогнозировать болезнь на
самостоятельно. Поэтому для постановки диагноза туберкулеза у детей требуется
больших клинических навыков и правильная интерпретация исследований
.
Нет сомнений в том, что у некоторых детей
может быть трудно решить, является ли тест БЦЖ положительным из-за предшествующей вакцинации
БЦЖ или из-за естественной туберкулезной инфекции.
Избыточный диагноз туберкулеза обычно делается с использованием
преувеличенного ответа на тест БЦЖ в качестве параметра для принятия решения
противотуберкулезная терапия у пациентов, у которых в противном случае
анамнез, клинические особенности, чувствительность туберкулиновой пробы, рентген
грудная клетка и т. д. не полностью указывают на болезнь Коха.
Настоящее исследование показывает, что у нормальных здоровых детей
может быть слегка преувеличенный ответ на тест БЦЖ, т. Е. Индукция рациона до 8 мм из-за предшествующей вакцинации БЦЖ.
Таким образом, пациенты, которые были иммунизированы вакциной БЦЖ при рождении
и дали положительный результат теста БЦЖ, и у которых другие параметры
для диагностики туберкулеза не внушают доверия, возможно, получают ненужные противотуберкулезные препараты
терапия. Положительный тест может иметь значение после сопоставления его
с возрастом ребенка, питанием, размером туберкулиновой пробы
уплотнение, анамнез контакта и симптомами для диагностики
и проведения химиотерапии [1].
Заключение
78% (39 из 50) детей в группе I (предыдущая вакцинация БЦЖ —
) и 18% (9 из 50) детей в группе II (предыдущая вакцинация
БЦЖ не проводилась) преувеличенный ответ BCG
; определяется как уплотнение, большее или равное 6
мм. Статистическая разница (значение p <0,00001) между
Группой I и Группой II была очень значимой. 72% детей
в группе I, которые показали преувеличенный ответ на БЦЖ,
имели уплотнение в диапазоне 6–8 мм.Только 6% детей
показали уплотнение размером 9, 10 или более 10 мм. У 22% из
детей в группе I уплотнение было менее 6 мм. Дети
детей в группе II, показавшие преувеличенный ответ на БЦЖ, имели уплотнение
размером 6 или 7 мм. Различия между показаниями мужчин
и женщин в каждой из двух групп были статистически недостоверными. Показания 1-го и 3-го суток были статистически на
более значимыми по сравнению с показаниями на 7-й и 6-недельный периоды —
раза.Все дети в группе II, показывающей преувеличенный ответ на БЦЖ
, и в группе I, показавшую уплотнение на 10 мм или на
больше, были обследованы с помощью рентгеновского снимка грудной клетки, чтобы исключить туберкулез
. Даже в отсутствие предварительной вакцинации БЦЖ около
нормальных здоровых детей из группы II демонстрировали слегка завышенный ответ БЦЖ на
. Вероятно,
можно объяснить туберкулезной инфекцией, не требующей лечения. У значительного числа (78%) здоровых детей
, прошедших предыдущую вакцинацию БЦЖ, которые были отрицательными по Манту
и получили БЦЖ в качестве «диагностического теста» или как повторную вакцинацию
, показали преувеличенный ответ БЦЖ.Поскольку эти
детей здоровы, преувеличенный ответ БЦЖ в таких
Отсутствует отрицательный эффект вакцинации БЦЖ на психомоторное развитие ребенка: результаты датского исследования Calmette
Аннотация
Цели
Оценить неспецифический эффект вакцинации против Bacillus Calmette-Guérin (БЦЖ) при рождении на психомоторное развитие.
Дизайн
Это предварительно определенный вторичный результат рандомизированного клинического исследования.
Настройка
Родильные отделения и педиатрические отделения трех университетских больниц Дании.
Участников
Дети, рожденные в гестационном возрасте (GA) 32 недели и старше. Все женщины, планирующие рожать в трех местах, были приглашены в период набора. Из 4262 рандомизированных детей 144 были недоношенными (GA <37 недель). Было рандомизировано 2129 детей (71 недоношенный) в группу БЦЖ и 2133 детей (73 недоношенных) в контрольную группу.
Вмешательства
Вакцинация БЦЖ 0,05 мл внутрикожно в верхнюю левую руку в больнице в течение семи дней после рождения. Детям контрольной группы никакого вмешательства не проводилось. Родители не закрывали глаза на выделение.
Основные показатели результатов
Психомоторное развитие измерялось с помощью анкеты по возрасту и этапам (ASQ), заполненной родителями в 12 месяцев. Кроме того, родители недоношенных детей (гестационный возраст <37 недель) заполнили ASQ в 6 и 22 месяца.Оценка развития была доступна для 3453/4262 (81%).
Результаты
Средняя разница в оценке ASQ через 12 месяцев с поправкой на возраст и недоношенность составила -0,7 балла (БЦЖ по сравнению с контролем, доверительный интервал 95%; от -3,7 до 2,4), p = 0,67, что соответствует величине эффекта d Коэна. = -0,015 (от -0,082 до 0,052). Средняя разница в баллах ASQ для недоношенных детей в возрасте 22 месяцев составила -7,8 балла (от -20,6 до 5,0, p = 0,23), d = -0,23 (от -0,62 до 0,15).
Выводы
У доношенных детей исключено отрицательное неспецифическое влияние вакцинации БЦЖ при рождении на психомоторное развитие.
Образец цитирования: Kjærgaard J, Stensballe LG, Birk NM, Nissen TN, Foss KT, Thøstesen LM, et al. (2016) Отсутствие отрицательного влияния вакцинации БЦЖ на психомоторное развитие детей: результаты датского исследования Кальметта — рандомизированного клинического испытания. PLoS ONE 11 (4):
e0154541.
https://doi.org/10.1371/journal.pone.0154541
PLoS ONE 11 (4):
e0154541.
https://doi.org/10.1371/journal.pone.0154541
Редактор: Имти Чунара, Ноттингемский университет, СОЕДИНЕННОЕ КОРОЛЕВСТВО
Поступила: 10 декабря 2015 г .; Одобрена: 29 марта 2016 г .; Опубликовано: 28 апреля 2016 г.
Авторские права: © 2016 Kjærgaard et al.Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Доступность данных: Наши основные данные содержат идентифицирующую информацию о пациентах и, следовательно, подлежат этическим ограничениям на публичное распространение. С разумными запросами от заинтересованных исследователей можно связаться с Йеспером Кьоргаардом ([email protected]) для запроса базовых данных в обезличенном формате.
Финансирование: Датский национальный исследовательский фонд предоставил грант (DNRF108) своему Центру передового опыта — Центру вакцин и витаминов (www.cviva.dk), который выделил часть гранта на проведение Датского исследования Кальметта. . JK получил дополнительное финансирование от Rigshospitalets Forskningsfond, Dagmar Marshall fonden, Else og Mogens Wedell Wedellsborgs fond и Christian Larsen og Dommer Ellen Larsens Fond.Финансирующие организации не играли никакой роли в дизайне исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи.
Конкурирующие интересы: Андреас Андерсен, статистик, связан с Statens Serum Institut (SSI). SSI производит вакцину БЦЖ, использованную в исследовании авторов. Вакцины, использованные в этом исследовании, были куплены по стандартным ценам, и SSI не участвовала в разработке, проведении, анализе или финансировании исследования.
Введение
Вакцина против туберкулеза Bacillus Calmette-Guérin (БЦЖ) является одной из наиболее широко используемых вакцин во всем мире.Ежегодно его получают около 100 миллионов детей. Вакцина обеспечивает некоторую защиту от заражения M . туберкулез и прогрессирование туберкулеза у детей [1]. ВОЗ рекомендует БЦЖ при рождении в странах с высокой распространенностью туберкулеза [2]. Рандомизированное исследование [3] и несколько обсервационных исследований [4–7] показали, что БЦЖ имеет неспецифические положительные эффекты, приводящие к снижению смертности и заболеваемости от инфекций [8] среди вакцинированных БЦЖ детей в странах с низким уровнем доходов.Снижение смертности и заболеваемости от инфекций было больше, чем можно было бы объяснить профилактикой туберкулеза, т.е. неспецифическим эффектом. Кроме того, БЦЖ снижает риск атопических заболеваний [9]. Детская смертность в Дании низкая, но распространены инфекционные и аллергические заболевания [10]. На этой основе было проведено большое рандомизированное исследование — Датское исследование Calmette — с целью изучить, может ли БЦЖ, назначенная при рождении, снизить заболеваемость детей в стране с высоким уровнем доходов [11].
Насколько нам известно, возможные неспецифические эффекты БЦЖ на психомоторное развитие ребенка ранее не изучались.Вакцинация БЦЖ вызывает воспалительные Th2-ответы и Th3-ответы на неродственные патогены у вакцинированных детей [12,13]. БЦЖ также вызывает локализованное воспаление в месте инъекции в течение нескольких месяцев [14]. Воздействие слабого воспаления в раннем возрасте связано с развитием психоневрологических расстройств, таких как когнитивные расстройства, церебральный паралич и расстройства аутистического спектра [15,16]. Это также было связано с повышенной восприимчивостью к повреждению после гипоксически-ишемического инсульта на животных моделях [17] и с изменениями в созревании мозга у недоношенных овец [18].По этой причине мы хотели исследовать влияние вакцины БЦЖ на развитие нервной системы, что особенно актуально для использования БЦЖ для предотвращения некритических заболеваний и, возможно, даже в большей степени для недоношенных детей, которые считаются более восприимчивыми к воспалительным процессам.
Таким образом, вторичным результатом датского исследования Calmette [11] было рассмотрение вопроса о том, может ли БЦЖ при рождении оказывать негативное влияние на развитие ребенка.
Методы
В этом исследовании сообщается о вторичном исходе датского исследования Кальметта, подробно описанном в другом месте [11].Изначально мы планировали изучить развитие только недоношенных детей, но когда мы разработали веб-платформу для родительского отчета о психомоторном развитии детей в возрасте шести месяцев, мы поняли, что сможем оценить всю когорту, используя тот же подход, и мы запросили и получили этическое разрешение сделать это вовремя для отчета за 12 месяцев.
Исследование было одобрено комитетами по этике биомедицинских исследований (J.no. H-3-2010-087), Датским советом по защите данных (J.нет. 2009-41-4141) и Датское агентство по лекарственным средствам (J.no. 2612-4356. EudraCT 2010-021979-85. Протокол 2009-323) и зарегистрированы на сайте www.clinicaltrials.gov (NCT01694108). Исследование проходило под наблюдением отделов надлежащей клинической практики столичного региона и региона Южная Дания. Исследование контролировалось независимой комиссией по мониторингу данных и безопасности, состоящей из трех членов. Все родители дали письменное информированное согласие.
Кратко о методологии исследования
Испытание проводилось в родильных отделениях и педиатрических отделениях трех университетских больниц Дании.В течение семи дней после рождения исследовательский персонал рандомизировал детей для получения БЦЖ (датский штамм SSI 1331) в стандартной дозе 0,05 мл внутрикожно на левое плечо или в контрольную группу без вмешательства. Родители не были скрыты в отношении распределения, поскольку местную воспалительную реакцию после вакцинации БЦЖ невозможно было воспроизвести. Рандомизация стратифицировалась по преждевременным родам (гестационный возраст [GA] <37 недель или ≥ 37 недель), и дети распределялись 1: 1 в переставляемых блоках по 2-4-6 с использованием онлайн-системы.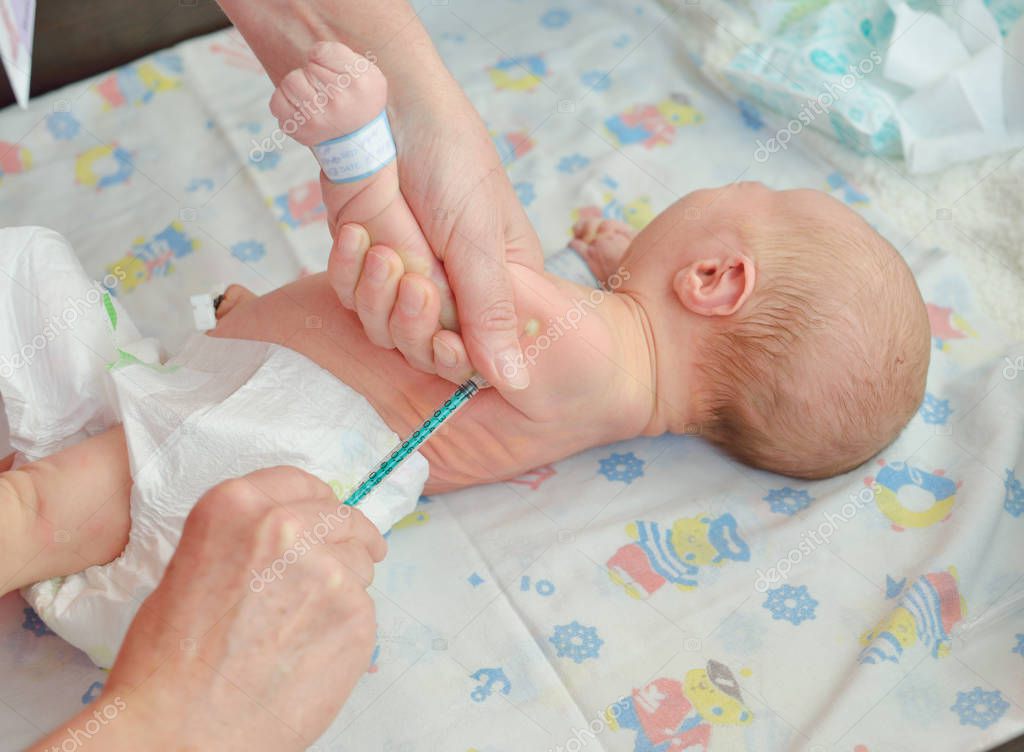 Критерии исключения: GA <32 недель, масса тела при рождении <1000 г, ребенок в критическом состоянии, известный иммунодефицит, отсутствие говорящих по-датски родителей и использование матерью иммуномодулирующих препаратов во время беременности. Последующее наблюдение включало телефонные интервью и клиническое обследование через 3 и 13 месяцев, а также диагнозы при поступлении в больницу, полученные из национальных регистров через 15 месяцев.
Критерии исключения: GA <32 недель, масса тела при рождении <1000 г, ребенок в критическом состоянии, известный иммунодефицит, отсутствие говорящих по-датски родителей и использование матерью иммуномодулирующих препаратов во время беременности. Последующее наблюдение включало телефонные интервью и клиническое обследование через 3 и 13 месяцев, а также диагнозы при поступлении в больницу, полученные из национальных регистров через 15 месяцев.
Продолжение исследования
Опросник по возрасту и стадиям (ASQ) представляет собой серию проверенных анкет, связанных с возрастом от 2 до 60 месяцев, по сообщениям родителей и предназначенных для выявления детей с задержкой в развитии.Каждый вопросник содержит 30 вопросов о повседневной деятельности ребенка в пяти поддоменах (общение, развитие мелкой моторики, развитие крупной моторики, решение проблем, а также личное и социальное развитие) [19]. Родители могут отметить каждый пункт «да», «иногда» или «еще нет». Элемент получает 10 баллов за «да», 5 за «иногда» и 0 за «еще нет», а также оценка для каждого поддомена (от 0 до 60) и общий балл ASQ (от 0 до 300), если все поддомены завершены. ASQ предназначен для выявления детей с задержкой в развитии, т.е.е. те, у кого баллы находятся в левом хвосте распределения. Считается, что дети с оценкой ниже –1,5 стандартного отклонения имеют риск задержки в развитии. Распределение общего балла ASQ усечено вправо при применении к предполагаемой возрастной группе. Мы хотели получить максимальную мощность для обнаружения разницы в средней оценке ASQ и, следовательно, стремились к неуклонному распределению оценок ASQ. Чтобы получить это, мы использовали ASQ, предназначенный для детей в возрасте 8 месяцев для нашей недоношенной популяции в 6 месяцев, ASQ для 14-месячных детей для всей нашей когорты в возрасте 12 месяцев и ASQ для 24-месячных детей для нашей недоношенной популяции. в 22 месяца.При использовании ASQ для непреднамеренной возрастной группы невозможно определить оптимальную оценку ASQ априори .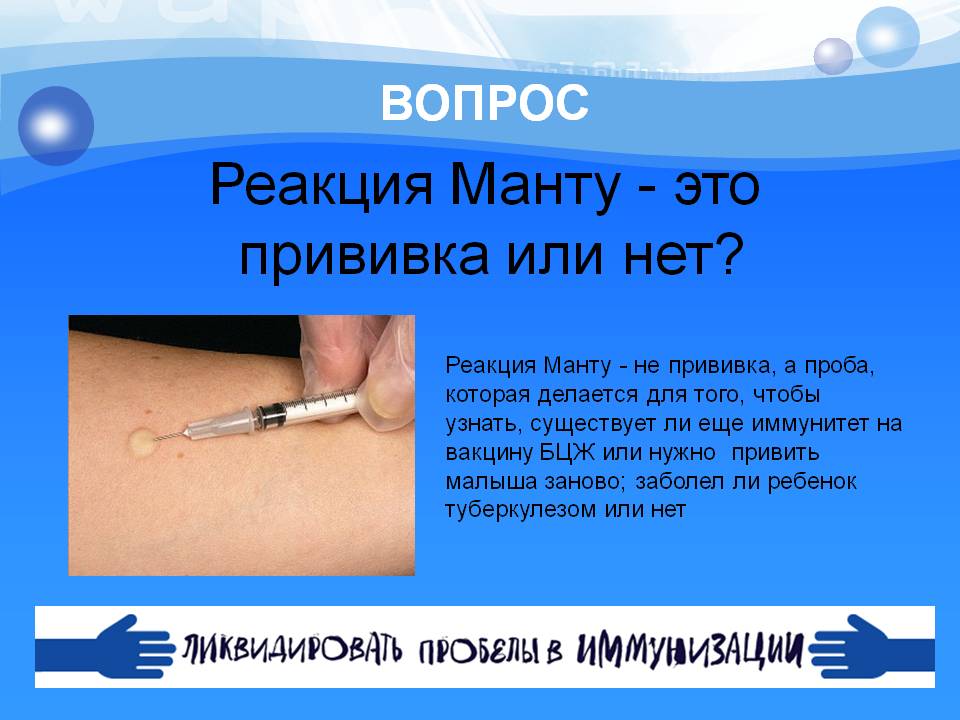
ASQ не публиковался на датском языке. Мы получили разрешение от издателя использовать версию (ASQ 2 nd edition), переведенную для использования в предыдущих исследованиях [20], и адаптировали ее для использования в Интернете.
Мы разослали онлайн-опрос родителям в первый день рождения ребенка, используя автоматически созданное электронное письмо со ссылкой. Мы напомнили родителям, которые не заполнили ASQ при 13-месячном телефонном и клиническом наблюдении.Родители недоношенных детей также получили ASQ, когда ребенку было 6 и 22 месяца. Наблюдение проходило с 8 апреля th 2013 по 21 августа st 2015.
Результаты
Первичным результатом этого исследования была оценка ASQ за один год для всей когорты с использованием полных вопросников. Были запланированы подгрупповые анализы недоношенных и доношенных детей и мальчиков и девочек в течение одного года. Вторичными результатами были баллы ASQ через 6, 12 и 22 месяца у недоношенных детей и баллы поддомена ASQ для всей когорты через 12 месяцев с использованием полных вопросников.Все анализы были запланированы до снятия слепоты с данных, за исключением исследовательского анализа среднего эффекта БЦЖ на недоношенных детей в 6, 12 и 22 месяцев, который был решен post hoc .
Размер выборки, управление данными и статистика
Исходный размер выборки Датского исследования Calmette (4300 детей) был определен таким образом, чтобы выявить 20% -ное сокращение числа госпитализаций до 15 месяцев с мощностью 90% [11]. При таком размере выборки уровень значимости 0.05 и средний балл ASQ 200 со стандартным отклонением (SD) 40, это исследование имеет мощность 98% для обнаружения разницы в 5 баллов (размер эффекта 0,13) в среднем балле ASQ за один год. Мы ожидали, что 5,5% когорты будут недоношенными (GA <37 недель), что дает мощность 50% для обнаружения 10-балльной разницы (величина эффекта 0,25) у недоношенных детей.
При каждом последующем наблюдении мы сгруппировали родителей на респондентов, , если анкета была заполнена, частично ответивших, , если анкета была неполной, и не ответивших, , если анкета отсутствовала.
Непрерывные исходы были проанализированы с использованием множественных регрессионных моделей с поправкой на возраст ребенка при последующем наблюдении и на недоношенность (бинарная переменная, GA ≥ или <37 недель), и представлены необработанные оценки, а также размер эффекта Коэна d ; рассчитывается как бета-коэффициент, деленный на квадратный корень из средней остаточной дисперсии. Первичный анализ представлял собой регрессионную модель с поправкой на недоношенность с использованием только полных случаев. Вторичные результаты сообщаются, если были даны ответы на все вопросы в поддомене ASQ.Анализ чувствительности к первичному результату был проведен с поправкой на переменные, которые могли быть связаны с отсутствующим результатом; т.е. возраст на момент наблюдения, пол ребенка, место исследования, гестационный возраст в днях, год рождения матери, образование матери, многоплодные роды, курение матери во время беременности, старшие братья и сестры. Из-за ошибки системы управления данными недоношенные дети с гестационным возрастом от 32 недель до 33 недель и 3 дней не получали ASQ в 6 месяцев. Этот механизм потери для последующего наблюдения был интерпретирован как случайное отсутствие, поскольку вероятность пропуска не была связана с результатом.Чтобы исследовать это, мы использовали общие / многомерные нормальные линейные модели, оцененные по максимальной вероятности, чтобы изучить связи между показателями BCG и ASQ во времени для недоношенных детей с учетом корреляции измерений у детей. Модель включает переменную последующего наблюдения и взаимосвязь между БЦЖ и последующим наблюдением, что позволяет оценить отдельные эффекты БЦЖ через 6, 12 и 22 месяца. Неструктурированные ковариационные матрицы использовались, чтобы не ограничивать дисперсии и корреляции.Эту модель часто называют многомерной или смешанной моделью. Повторные измерения обозначают MMRM.
Незначительное усечение вправо было обнаружено через 12 месяцев наблюдения (S1 рис.), Но остатки регрессии были нормально распределены, то есть были выполнены предположения первичного регрессионного анализа. Дискретные данные с ненормальным распределением анализировали с использованием критерия Манна-Уитни U . Категориальные исходы анализировали с использованием χ 2 . Уровень значимости составлял 0,05, и все тесты были двусторонними.Все представленные анализы представляют собой анализы намерения лечить.
Дискретные данные с ненормальным распределением анализировали с использованием критерия Манна-Уитни U . Категориальные исходы анализировали с использованием χ 2 . Уровень значимости составлял 0,05, и все тесты были двусторонними.Все представленные анализы представляют собой анализы намерения лечить.
Все анализы были выполнены с использованием STATA 13.1 (StataCorp, Техас, США). Используемый статистический код доступен в S1 Text.
Результаты
В период с октября 2012 г. по ноябрь 2013 г. были приглашены в общей сложности 16 521 беременная женщина. В исследование были включены 4184 матери, 4262 новорожденных ребенка были рандомизированы (рис. 1). Исходные характеристики были равномерно распределены между группами распределения, за исключением недатской этнической принадлежности и курения отцов во время беременности, которые чаще встречались в контрольной группе (Stensballe, 2015).Исходные характеристики, сгруппированные по ответам на контрольные вопросники, представлены в таблице 1.
В группе БЦЖ было 350/2129 (16,4%) частично ответивших и не ответивших на лечение по сравнению с 459/2133 (21,5%) в контрольной группе, p <0,001. Среди частично ответивших и не ответивших было значительно больше женщин с базовым образованием и нетеоретической подготовкой (212/809 [26,2%] против 695/3453 [20,1%]; p <0,001) и больше семей с братьями и сестрами ( 370/807 [два неизвестны] [45.9%] против 1391/3453 [40,3%]; р = 0,004).
Было 46/144 (32,4%) преждевременных пациентов с частичным ответом и без ответа через 6 месяцев, 29/144 (20,1%) через 12 месяцев и 22/144 (15,3%) через 22 месяца.
Средний балл ASQ среди 3453 детей, заполнивших анкету через 12 месяцев, составил 178,2 балла (СО 52,4) в группе БЦЖ по сравнению с 179,9 балла (СО 53,6) в контрольной группе. Всего 22 ребенка набрали максимальный балл 300.
Первичные и вторичные исходы
Средняя разница в оценке ASQ через 12 месяцев с поправкой на возраст и недоношенность составила -0.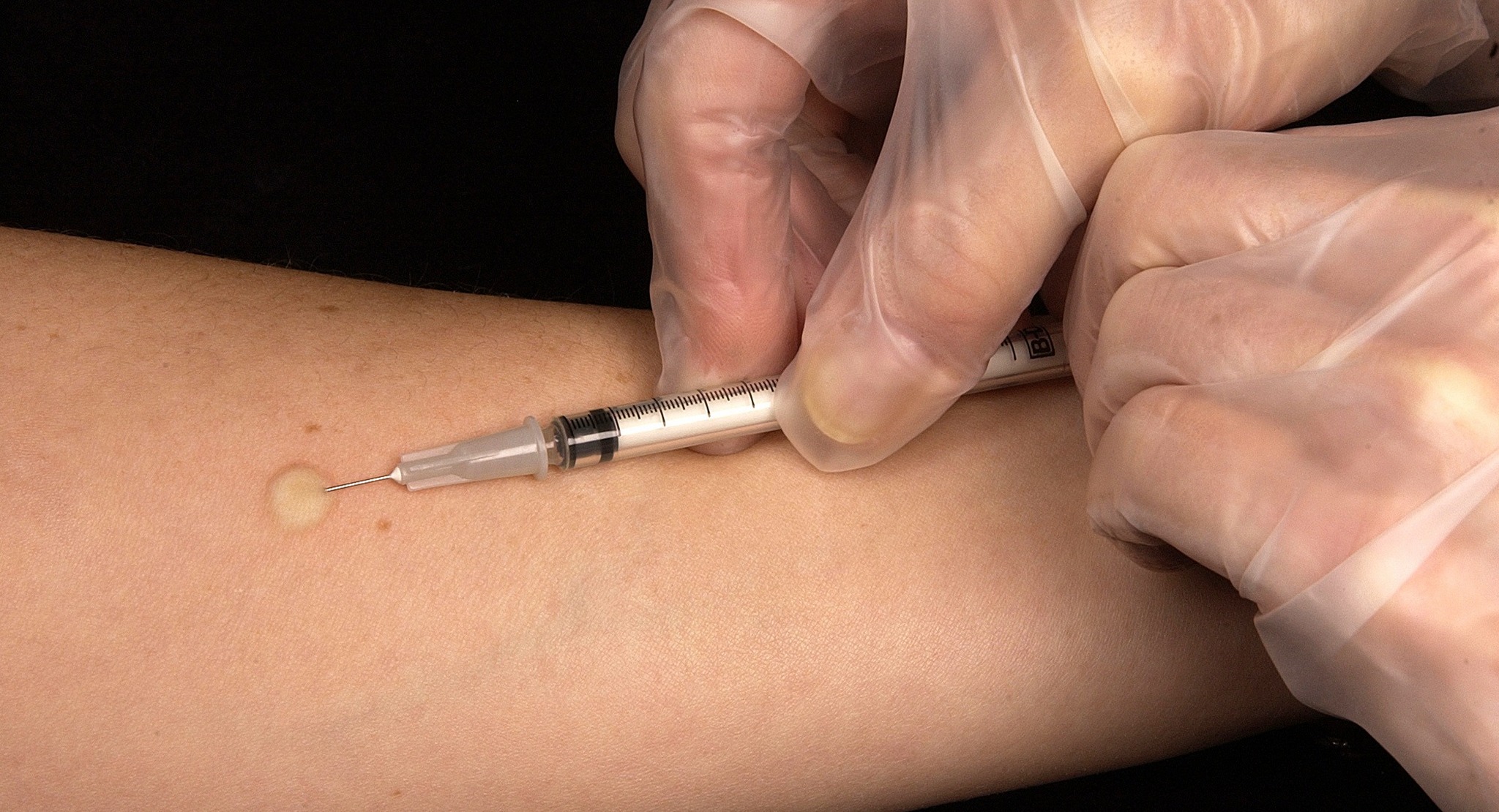 7 баллов (БЦЖ по сравнению с контролем, 95% доверительный интервал [95% ДИ]; от -3,7 до 2,4, p = 0,67), что соответствует величине эффекта d = -0,015 (от -0,082 до 0,052). Статистически значимых различий ни в одном из субдоменов ASQ не было (таблица 2). В 22 месяца эффект БЦЖ у недоношенных детей составил -7,8 балла (-20,6 до 5,0), d = -0,23 (-0,62 до 0,15). Средние различия для недоношенных детей в 6 месяцев и 12 месяцев также были отрицательными, но не статистически значимыми, а эффект БЦЖ не отличался статистически значимо между недоношенными и доношенными детьми в 12 месяцев (Таблица 3).Результаты были практически такими же, как при анализе по протоколу (таблица 4).
7 баллов (БЦЖ по сравнению с контролем, 95% доверительный интервал [95% ДИ]; от -3,7 до 2,4, p = 0,67), что соответствует величине эффекта d = -0,015 (от -0,082 до 0,052). Статистически значимых различий ни в одном из субдоменов ASQ не было (таблица 2). В 22 месяца эффект БЦЖ у недоношенных детей составил -7,8 балла (-20,6 до 5,0), d = -0,23 (-0,62 до 0,15). Средние различия для недоношенных детей в 6 месяцев и 12 месяцев также были отрицательными, но не статистически значимыми, а эффект БЦЖ не отличался статистически значимо между недоношенными и доношенными детьми в 12 месяцев (Таблица 3).Результаты были практически такими же, как при анализе по протоколу (таблица 4).
У недоношенных детей эффект БЦЖ достоверно не отличался через 6, 12 и 22 месяца, p = 0,47. Средний эффект BCG не был значительным при объединении трех оценок; БЦЖ по сравнению с контролем: -6,4 балла (от -15,6 до 2,8), p = 0,17. Не существует последовательной схемы, в которой оценки поддомена влияют на 6, 12 и 22 месяца для недоношенных детей (рис. 2). Поправка на факторы, возможно, связанные с неполучением ответов в анализе чувствительности, не повлияла существенно на оценки (Таблица 5).
Рис. 2. Коробчатые диаграммы поддомена ASQ и общих баллов в 6, 12, 22 месяцев для недоношенных детей.
ASQ: Анкета по возрастам и этапам. Coms: оценка связи. Fms: Оценка мелкой моторики. Gms: Общий балл мотора. Pss: Оценка решения проблем. Psds: оценка личного и социального развития. БЦЖ: вакцина Bacillus Calmette-Guèrin.
https://doi.org/10.1371/journal.pone.0154541.g002
Во всей когорте через один год средний скорректированный по возрасту эффект БЦЖ для мальчиков составил -3.2 балла (от -7,4 до 0,9), d = -0,072 (от -0,16 до 0,020) и 2,0 балла (от -2,4 до 6,4), d = 0,045 (от -0,052 до 0,14) для девочек. Разница в эффекте между мальчиками и девочками не была значимой (р = 0,087 для взаимодействия).
Обсуждение
В настоящем исследовании мы сообщаем о предварительно определенном вторичном анализе рандомизированного клинического исследования, изучающего, влияет ли вакцинация БЦЖ при рождении на психомоторное развитие детей.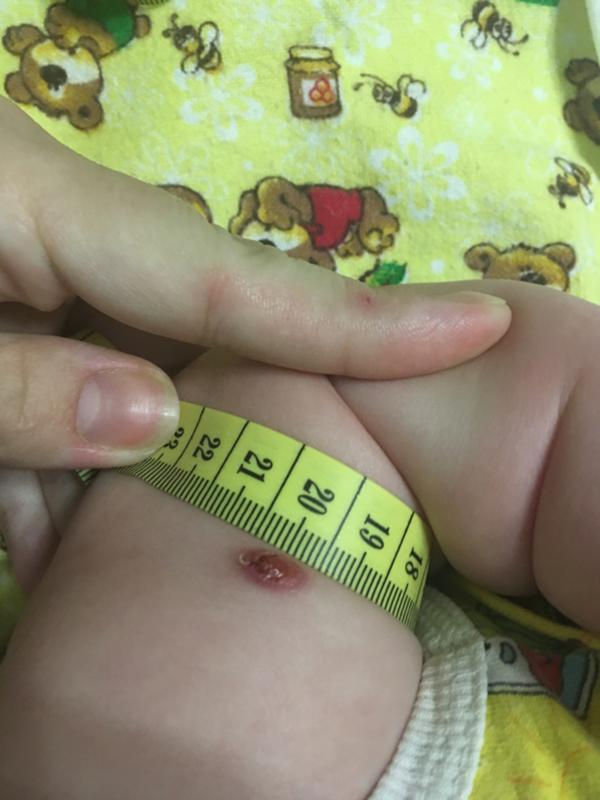 Мы не обнаружили влияния БЦЖ на психомоторное развитие в 12-месячном возрасте.
Мы не обнаружили влияния БЦЖ на психомоторное развитие в 12-месячном возрасте.
Исследование обладает достаточной мощностью, чтобы обнаружить даже небольшую разницу в оценке ASQ среди взрослых детей, и, следовательно, имеет низкий риск не обнаруживать клинически значимый эффект. Для измерения развития мы использовали хорошо известный и широко используемый опросник ASQ, который заполняют родители и который, как было показано, имеет высокую достоверность, чувствительность и специфичность как инструмент для выявления задержки в развитии [21]. Нам удалось получить распределение оценок ASQ с небольшим усечением, так как менее одного процента набрали максимальную оценку для основного результата и, таким образом, получили максимально возможную мощность для обнаружения разницы в средней оценке для респондентов.Кроме того, изучение возможных неспецифических эффектов с использованием рандомизированного дизайна дает низкий риск систематической ошибки. Наше исследование имеет некоторые ограничения, которые могут привести к смещению результатов в сторону нуля; у нас было 14,1% пациентов, не ответивших на первичный результат. Среди не ответивших было больше детей, отнесенных к контрольной группе, был более низкий уровень материнского образования и больше семей со старшими братьями и сестрами. Мы подозревали, что не ответившие люди не вернули анкеты из-за одного или нескольких из этих факторов или из-за более низкой приверженности исследованию, если ребенок был в контрольной группе [22], т.е.е. не по причинам, связанным с исходом, но это не может быть установлено. Мы считаем, что риск дифференциального выбывания невелик, поскольку анализ чувствительности, включающий переменные, которые, как мы ожидали, могли быть связаны с выбыванием, существенно не изменил оценку первичного результата, даже несмотря на то, что анализ чувствительности не может контролировать выбывание, связанное с исходом. . Еще одно важное ограничение — это риск смещения производительности. Поскольку родители не были слепы к распределению, они могли занижать информацию о побочных эффектах, но мы считаем маловероятным, чтобы родители сообщали о развитии своего ребенка по-разному в зависимости от распределения в нашем исследовании, поскольку информационный лист для родителей (текст S2) был сосредоточен на инфекционных и атопических заболеваниях. , я.е. основные результаты датского исследования в Кальметте. Мы набрали только около 60% запланированных недоношенных детей из-за логистики исследования и повышенной обеспокоенности родителей по поводу участия в исследовании в этой группе. Наконец, хорошо известно, что иммунный ответ на микобактериальные антигены заметно различается между разными штаммами БЦЖ [23], и поскольку влияние БЦЖ на развитие ребенка опосредуется иммунологической реакцией на вакцину, результаты этого исследования могут не совпадать. распространяются на другие штаммы.
, я.е. основные результаты датского исследования в Кальметте. Мы набрали только около 60% запланированных недоношенных детей из-за логистики исследования и повышенной обеспокоенности родителей по поводу участия в исследовании в этой группе. Наконец, хорошо известно, что иммунный ответ на микобактериальные антигены заметно различается между разными штаммами БЦЖ [23], и поскольку влияние БЦЖ на развитие ребенка опосредуется иммунологической реакцией на вакцину, результаты этого исследования могут не совпадать. распространяются на другие штаммы.
Изучение потенциально отрицательных эффектов в ходе испытаний допустимо с этической точки зрения только в том случае, если ожидаемые преимущества перевешивают возможные побочные эффекты. Имея ожидаемую пользу в виде сокращения госпитализаций на 20%, мы утверждаем, что уравновешивание, необходимое для этического проведения испытания [24], присутствовало, особенно с учетом того, что имеющиеся данные показывают, что недоношенные дети получают наибольшую пользу от неспецифического воздействия БЦЖ на смертность [3]. Насколько нам известно, это первое исследование по оценке неспецифического воздействия БЦЖ на психомоторное развитие.БЦЖ считается безопасной вакциной, и побочные эффекты, характерные для БЦЖ, хорошо описаны [25–27]. Серьезные побочные эффекты, такие как диссеминированная инфекция БЦЖ или остит БЦЖ, встречаются редко [14], но по мере увеличения знаний об иммунном ответе, вызываемом БЦЖ, а также о сложном взаимодействии между иммунной системой и нервным развитием [28], увеличивается и ряд вероятных неспецифических эффектов, как положительных, так и отрицательных. Было показано, что сенсибилизация даже при небольшой системной инфекционной нагрузке может привести к повышению восприимчивости к повреждению мозга после гипоксически-ишемического инсульта [29], а БЦЖ действительно вызывает воспалительную реакцию в месте инъекции, которая обычно длится 2–4 месяца. [25,27,30], как потенциальный источник системной инфекции. Два недавних обзора пришли к выводу, что существует возможная связь между хроническим воспалением слабой степени в раннем возрасте и риском развития ряда нейропсихиатрических расстройств в подростковом или взрослом возрасте [15,17] и эффектом вакцинации БЦЖ взрослых пациентов с ранний рассеянный склероз проявился только через 18 месяцев, и со временем эффект, казалось, усиливался [31]. Таким образом, наш обнадеживающий результат на одном году жизни не исключает более поздних эффектов — неблагоприятных или полезных.
Два недавних обзора пришли к выводу, что существует возможная связь между хроническим воспалением слабой степени в раннем возрасте и риском развития ряда нейропсихиатрических расстройств в подростковом или взрослом возрасте [15,17] и эффектом вакцинации БЦЖ взрослых пациентов с ранний рассеянный склероз проявился только через 18 месяцев, и со временем эффект, казалось, усиливался [31]. Таким образом, наш обнадеживающий результат на одном году жизни не исключает более поздних эффектов — неблагоприятных или полезных.
Чтобы подтвердить или опровергнуть оценку негативного воздействия, которую мы обнаружили у недоношенных детей, мы предлагаем оценивать исходы нервного развития, предпочтительно с использованием ASQ, в рамках текущих и будущих испытаний БЦЖ для недоношенных детей, даже если данные, возможно, потребуется объединить. между исследованиями, чтобы достичь достаточной мощности.Возможно, особенно в группах населения с низкой распространенностью туберкулеза и низким бременем неонатальных инфекций, т. Е. В условиях, когда неспецифический положительный эффект БЦЖ на смертность, вероятно, будет играть второстепенную роль, и где профилактика туберкулеза не является приоритетной задачей. уровень сообщества. И наоборот, в условиях ограниченных ресурсов, где было продемонстрировано положительное влияние БЦЖ на смертность от всех причин, результаты этого исследования не должны препятствовать вакцинации БЦЖ недоношенных детей, которые, по всей видимости, приносят наибольшую пользу [3].
Заключение
Клинически значимое отрицательное неспецифическое влияние вакцинации БЦЖ при рождении на психомоторное развитие в возрасте 12 месяцев было исключено у доношенных детей. В настоящем исследовании нельзя было сделать четких выводов об эффекте у недоношенных детей (GA <37 недель).
Благодарности
Весь исследовательский персонал во всех трех исследовательских центрах и, в частности, участвующие семьи.
Вклад авторов
Задумал и спроектировал эксперименты: JK LGS GG. Проведены эксперименты: JK NMB TNN GTP LMT KTF. Проанализированы данные: JK GG AA. Предоставленные реагенты / материалы / инструменты анализа: JK NMB TNN GTP LMT KTF. Написал документ: JK NMB TNN GTP LMT KTF LGS GG PEK OP. Руководил сбором данных: LGS GG PEK OP.
Проведены эксперименты: JK NMB TNN GTP LMT KTF. Проанализированы данные: JK GG AA. Предоставленные реагенты / материалы / инструменты анализа: JK NMB TNN GTP LMT KTF. Написал документ: JK NMB TNN GTP LMT KTF LGS GG PEK OP. Руководил сбором данных: LGS GG PEK OP.
Список литературы
- 1. Рой А., Эйзенхут М., Харрис Р.Дж., Родригес Л.К., Шридхар С., Хаберманн С. и др. Эффект вакцинации БЦЖ против инфекции Mycobacterium tuberculosis у детей: систематический обзор и метаанализ.BMJ. 2014; 349: g4643. pmid: 25097193
- 2. КТО. Документ с изложением позиции: Вакцина БЦЖ. Wkly Epidemiol Rec. 2004. 79: 27–48. Доступно: http://www.who.int/wer/2004/en/wer7904.pdf?ua=1 pmid: 14768305
- 3. Aaby P, Roth A, Ravn H, Napirna BM, Rodrigues A, Lisse IM, et al. Рандомизированное испытание вакцинации БЦЖ детям с низкой массой тела при рождении: положительные неспецифические эффекты в неонатальном периоде? J Infect Dis. 2011; 204: 245–52. pmid: 21673035
- 4. Рот А., Густафсон П., Нхага А., Джана К., Поулсен А., Гарли М.-Л. и др.Шрам от вакцинации БЦЖ связан с большей выживаемостью детей в Гвинее-Бисау. Int J Epidemiol. 2005; 34: 540–7. pmid: 15659474
- 5. Рот А., Содеманн М., Йенсен Х., Поульсен А., Густафсон П., Вайз С. и др. Туберкулиновая реакция, рубец БЦЖ и снижение женской смертности. Эпидемиология. 2006; 17: 562–8. pmid: 16878042
- 6. Сторгаард Л., Родригес А., Мартинс С., Нильсен БУ, Равн Х., Бенн С.С. и др. Развитие рубца БЦЖ и последующая заболеваемость и смертность в сельских районах Гвинеи-Бисау.Clin Infect Dis. 2015; civ452.
- 7. Кристенсен И., Оби П., Дженсен Х. Регулярные вакцинации и выживание детей: последующее исследование в Гвинее-Бисау, Западная Африка. BMJ. 2000; 321: 1435–8. pmid: 11110734
- 8.
Стенсбаль Л.Г., Нант Э., Йенсен И.П., Кофоед П.-Э, Поульсен А., Йенсен Х. и др. Острые инфекции нижних дыхательных путей и респираторно-синцитиальный вирус у младенцев в Гвинее-Бисау: положительный эффект вакцинации БЦЖ для девочек, исследование методом случай-контроль.
 Вакцина. 2005; 23: 1251–7. pmid: 15652667
Вакцина. 2005; 23: 1251–7. pmid: 15652667 - 9. Стинхейс Т.Дж., ван Алдерен WMC, Блоксма Н., Нийкамп Ф.П., ван дер Лааг Дж., Ван Ловерен Х. и др. Вакцинация Bacille-Calmette-Guerin и развитие аллергических заболеваний у детей: рандомизированное проспективное простое слепое исследование. Clin Exp Allergy. 2008. 38: 79–85. pmid: 17956585
- 10. Йохансен А., Йесперсен Л., Давидсен М., Мичелсен С., Морген С., Хельвег-Ларсен К. и др. Danske børns sundhed og sygelighed [Интернет].Копенгаген; 2009. Доступно: http://www.si-folkesundhed.dk/upload/web_susy_b%C3%B8rn.pdf
- 11. Thøstesen LM, Nissen TN, Kjærgaard J, Pihl GT, Birk NM, Benn CS и др. Иммунизация Bacillus Calmette-Guérin при рождении и заболеваемость среди детей в Дании: проспективное рандомизированное клиническое испытание. Клинические испытания Contemp. 2015; 42: 213–218. pmid: 25896113
- 12. Ota MOC, Vekemans J, Schlegel-Haueter SE, Fielding K, Sanneh M, Kidd M и др. Влияние Mycobacterium bovis bacillus Calmette-Guérin на антитела и цитокиновые реакции на вакцинацию новорожденных.J Immunol. 2002; 168: 919–925. pmid: 11777990
- 13. Йенсен К.Дж., Ларсен Н., Биринг-Соренсен С., Андерсен А., Эриксен Х. Б., Монтейро И. и др. Гетерологические иммунологические эффекты ранней вакцинации БЦЖ у детей с низкой массой тела при рождении в Гвинее-Бисау: рандомизированное контролируемое исследование. J Infect Dis. 2015; 211: 956–67. pmid: 25210141
- 14. Statens Serum Institut. Информационный бюллетень SSI BCG. В: Информация о продукте [Интернет]. 2015 г. [цитировано 12 августа 2015 г.]. Доступно: http: // www.produktresume.dk/docushare/dsweb/GetRendition/Document-13163/html
- 15.
Hagberg H, Gressens P, Mallard C. Воспаление во время эмбриональной и неонатальной жизни: последствия для неврологических и психоневрологических заболеваний у детей и взрослых. Анналы неврологии. 2012. С. 444–457.
 pmid: 22334391
pmid: 22334391 - 16. Шастри А., Бонифати Д.М., Кишор Ю. Врожденный иммунитет и нейровоспаление. Медиаторы Inflamm. 2013; 2013: 342931. pmid: 23843682
- 17. Hagberg H, Mallard C, Ferriero DM, Vannucci SJ, Levison SW, Vexler ZS и др.Роль воспаления в перинатальной травме головного мозга. Nat Rev Neurol. 2015; 11: 192–208. pmid: 25686754
- 18. Кио М.Дж., Беннет Л., Друри П.П., Бут Л.С., Матхай С., Нейлор А.С. и др. Субклиническое воздействие низких доз эндотоксина ухудшает созревание ЭЭГ у недоношенных плодов овец. Am J Physiol Regul Integr Comp Physiol. 2012; 303: R270–8. pmid: 22696578
- 19. Сквайрс Дж., Поттер Л., Брикер Д. Руководство пользователя ASQ по анкетам для возрастов и стадий: система мониторинга детей, заполняемая родителями.Балтимор, Мэриленд: Пол Х. Брукс; 1999.
- 20. Пломгаард А.М., Хансен Б.М., Грейзен Г. Измерение дефицита развития у детей, родившихся в гестационном возрасте менее 26 недель, с использованием анкеты развития, заполненной родителями. Acta Paediatr. 2006; 95: 1488–94. pmid: 17062482
- 21. Сквайрс Дж., Брикер Д., Поттер Л. Пересмотр созданного родителями инструмента скрининга развития: анкеты по возрастам и стадиям. J Pediatr Psychol. 1997. 22: 313–328. pmid: 9212550
- 22.Petersen S, Zoffmann V, Kjrgaard J, Stensballe LG, Greisen G. Разочарование и приверженность родителей новорожденных, отнесенных к контрольной группе: качественное исследование рандомизированного клинического исследования. Испытания. 2014; 15: 126. pmid: 24731249
- 23. Ритц Н., Ханеком В.А., Робинс-Браун Р., Бриттон В.Дж., Кертис Н. Влияние вакцинного штамма БЦЖ на иммунный ответ и защиту от туберкулеза. FEMS Microbiol Rev.2008; 32: 821–41. pmid: 18616602
- 24.Чау К., Корен Г. Принцип эквипойза в исследованиях педиатрических препаратов. Педиатрические препараты. 2014; 17: 17–21.
- 25.
Trunz BB, Fine P, Dye C.
 Влияние вакцинации БЦЖ на детский туберкулезный менингит и милиарный туберкулез во всем мире: метаанализ и оценка экономической эффективности. Ланцет. 2006; 367: 1173–1180. pmid: 16616560
Влияние вакцинации БЦЖ на детский туберкулезный менингит и милиарный туберкулез во всем мире: метаанализ и оценка экономической эффективности. Ланцет. 2006; 367: 1173–1180. pmid: 16616560 - 26. Colditz GA, Berkey CS, Mosteller F, Brewer TF, Wilson ME, Burdick E, et al. Эффективность вакцинации против бациллы Кальметта-Герена новорожденных и младенцев в профилактике туберкулеза: метаанализ опубликованной литературы.Педиатрия. 1995; 96: 29–35. pmid: 7596718
- 27. Перейра С.М., Дантас О.М., Ксименес Р., Баррето М.Л. Вакцина БЦЖ против туберкулеза: ее защитный эффект и политика вакцинации. Rev Saude Publica. 2007; 41.
- 28. Бильбо SD, Шварц JM. Иммунная система и программирование развития мозга и поведения. Фронт нейроэндокринол. 2012; 33: 267–86. pmid: 22982535
- 29. Czech M, Gressens P, Kaindl AM. Инь и янь микроглии. Dev Neurosci.2011; 33: 199–209. pmid: 21757877
- 30. Grange JM. Осложнения вакцинации против бациллы Кальметта-Герена (БЦЖ) и иммунотерапии и их лечение. Общественное здравоохранение. 1998; 1: 84–88. pmid: 9644119
- 31. Ристори Дж., Романо С., Каннони С., Висконти А., Тинелли Е., Мендоцци Л. и др. Эффекты бациллы Кальметта-Герена после первого демиелинизирующего события в ЦНС. Неврология. 2014; 82: 41–8. pmid: 24306002
Терапевтические препараты для лечения детей, вызванных вакциной БЦЖ
Бацилла Кальметта-Герена (БЦЖ) — широко используемая противотуберкулезная вакцина, полученная из неинфекционного штамма туберкулезной палочки крупного рогатого скота ( Mycobacterium bovis ) и предназначенная в основном детям младшего возраста.Обычно единственной побочной реакцией на вакцину является язва на месте инъекции, которая может оставить небольшой шрам.
Однако очень редко, особенно у детей с ослабленной иммунной системой, вакцина может вызывать более серьезные побочные эффекты. Это могут быть местные инфекции в месте инъекции, которые могут распространяться на лимфатические узлы, вызывая лимфаденопатию и кости, и даже могут оказаться опасными для жизни. Эти побочные реакции на вакцину БЦЖ представляют особый риск для детей, инфицированных вирусом иммунодефицита человека (ВИЧ), при этом состояние известно как воспалительный синдром восстановления иммунитета БЦЖ (BCG-IRIS).
Это могут быть местные инфекции в месте инъекции, которые могут распространяться на лимфатические узлы, вызывая лимфаденопатию и кости, и даже могут оказаться опасными для жизни. Эти побочные реакции на вакцину БЦЖ представляют особый риск для детей, инфицированных вирусом иммунодефицита человека (ВИЧ), при этом состояние известно как воспалительный синдром восстановления иммунитета БЦЖ (BCG-IRIS).
Во многих случаях инфекции проходят без какого-либо вмешательства, но лечение может включать пероральные антибиотики, пункционную аспирацию, дренирование абсцессов и хирургическое удаление инфицированных лимфатических узлов. Этот обзор был проведен, чтобы попытаться определить эффективность этих различных методов лечения.
В обзоре не было обнаружено доказательств какой-либо пользы пероральных антибиотиков для лечения местного или регионального заболевания, вызванного БЦЖ. У пациентов с абсцессообразующей лимфаденопатией единственным вмешательством с доказанной пользой была пункционная аспирация абсцессов с местной инъекцией антибиотика изониазида или без нее.
Основываясь на этих выводах, авторы обзора рекомендуют выжидательный подход с последующими посещениями при незначительных реакциях и лимфаденопатии без абсцессов. При лимфаденопатии, вызывающей абсцесс, которая может вызвать дискомфорт и дискомфорт, рекомендуется пункционная аспирация. Однако этот обзор основан только на пяти исследованиях, все из которых были оценены как имеющие низкое или очень низкое качество доказательств. Как следствие, авторы приходят к выводу, что существует острая необходимость в дополнительных и более качественных исследованиях способов профилактики и лечения заболеваний, вызванных БЦЖ, особенно БЦЖ-ВСВИ.
Долгосрочное наблюдение за остеомиелитом, вызванным вакцинацией бациллами Кальметта-Герена, у иммунокомпетентных детей
ТБ является одной из 10 основных причин смерти и ведущей причиной смерти от инфекционных заболеваний во всем мире. Дети младшего возраста подвергаются более высокому риску развития активного туберкулеза после первичного инфицирования. Вакцина БЦЖ играет важную роль в защите маленьких детей от тяжелого туберкулеза.
Вакцина БЦЖ играет важную роль в защите маленьких детей от тяжелого туберкулеза.
В нашем исследовании были проанализированы четыре ребенка с лабораторно подтвержденным остеомиелитом БЦЖ, получавших лечение в едином специализированном центре на Тайване с января 2001 года по апрель 2019 года.Наиболее частыми симптомами были отек костей и мягких тканей с умеренной болью; только у одного пациента поднялась температура. Всем четырем пациентам были выполнены хирургические вмешательства в диагностических или терапевтических целях и они получали антимикобактериальные препараты в течение не менее 10 месяцев после постановки диагноза. После лечения большинство симптомов улучшилось.
Диагностика остеомиелита БЦЖ обычно не проводится до тех пор, пока болезнь не продвинется далеко вперед из-за незаметных симптомов 8 . Необходимо различать отличительные особенности бактериального остеомиелита и БЦЖ-остеомиелита и остита.У детей с бактериальным остеомиелитом обычно наблюдается резкое повышение температуры и боли в костях 9 . Напротив, пациенты с остеомиелитом БЦЖ часто имеют относительно локализованные симптомы. Из различных симптомов в литературе чаще всего упоминаются местная болезненность, припухлость и анталгическая поза. 10,11,12 . Клинические проявления наших случаев были сопоставимы с таковыми в предыдущих исследованиях. Только у одного ребенка поднялась температура, что является необычным симптомом 12 .Разнообразие симптомов затрудняет диагностику; Следовательно, остеомиелит БЦЖ следует рассматривать как возможность у маленьких детей с любым из вышеупомянутых симптомов.
Трое из четырех наших пациентов были вакцинированы против туберкулеза в течение 1 месяца после рождения; четвертый был вакцинирован в возрасте 6,5 месяцев. Согласно данным активной системы надзора за побочными эффектами, связанными с вакциной БЦЖ, разработанной Тайваньским центром по контролю заболеваний, все пациенты с остеомиелитом или оститом, связанным с вакциной БЦЖ, в период 2003–2012 гг. Были вакцинированы в течение 3 месяцев после рождения 13 .В 2016 году Тайваньская национальная программа медицинского страхования перенесла вакцинацию на 5–8 месяцев после рождения в надежде снизить заболеваемость остеомиелитом или оститом, несмотря на отсутствие прямых доказательств связи между временем вакцинации и началом заболевания. . В соответствии с предыдущими исследованиями 11,12 , возраст начала заболевания в нашем исследовании варьировался от 9 до 20 месяцев. Время от вакцинации до начала вакцинации колебалось от 6,5 до 19 месяцев и составляло в среднем 11 месяцев.9 месяцев, что было аналогично 13,9 месяцам, указанным в предыдущих данных системного обзора.
Традиционно, при обнаружении остеомиелита БЦЖ на простой пленке наблюдаются остеолитические поражения и легкая периостальная реакция. Типичные результаты наблюдались для всех четырех пациентов в нашем исследовании. Однако у пациента 1 была выраженная периостальная реакция, распространяющаяся от дистального к проксимальному отделу большеберцовой кости. Надкостничная реакция определяется агрессивностью, интенсивностью и продолжительностью раздражения надкостницы.Кроме того, у ребенка с более активной надкостницей может наблюдаться более очевидная периостальная реакция на простую пленку 14 .
Не существует стандартной процедуры лечения остеомиелита или остеита, связанного с БЦЖ. Согласно обзору литературы 11 , пациенты, которые прошли диагностические процедуры, только значительно избежали серьезных осложнений; таким образом, операции должны выполняться по возможности минимально. В отличие от аналогичных исследований, в нашем исследовании участвовали четыре пациента, которым была проведена хирургическая обработка раны.У всех были удовлетворительные краткосрочные результаты без остаточных повреждений, как показано на простой пленке.
Однако из трех пациентов с отдаленными результатами у двоих во время наблюдения развились ортопедические осложнения, связанные с остеомиелитом БЦЖ. На одном из них было обнаружено поражение в правой дистальной части локтевой кости с отрицательной локтевой дисперсией 0,6 см на последнем снимке. У него была отрицательная локтевая дисперсия 0,4 см на левом запястье. Во время последнего визита не наблюдалось ни грубой деформации, ни ограничения объема движений, ни очаговой болезненности.Пациенту 3 была проведена не только открытая обработка правого дистального отдела бедренной кости, но и артроскопия с синовэктомией при подозрении на внутрисуставное поражение. Его пораженная конечность однажды показалась на рентгеновском снимке параллельной линией остановки роста по Харрису, а затем через 28 месяцев после операции достигла длины на 0,92 см длиннее другой стороны без нарушения походки. Однако через 4 года после первичной операции расхождение уменьшилось до 0,18 см на орторентгенограмме. О подобном клиническом течении остеомиелита или остита, связанного с БЦЖ, ранее не сообщалось.Мы связали задержку роста и разрастание физиса с процессом выздоровления.
На одном из них было обнаружено поражение в правой дистальной части локтевой кости с отрицательной локтевой дисперсией 0,6 см на последнем снимке. У него была отрицательная локтевая дисперсия 0,4 см на левом запястье. Во время последнего визита не наблюдалось ни грубой деформации, ни ограничения объема движений, ни очаговой болезненности.Пациенту 3 была проведена не только открытая обработка правого дистального отдела бедренной кости, но и артроскопия с синовэктомией при подозрении на внутрисуставное поражение. Его пораженная конечность однажды показалась на рентгеновском снимке параллельной линией остановки роста по Харрису, а затем через 28 месяцев после операции достигла длины на 0,92 см длиннее другой стороны без нарушения походки. Однако через 4 года после первичной операции расхождение уменьшилось до 0,18 см на орторентгенограмме. О подобном клиническом течении остеомиелита или остита, связанного с БЦЖ, ранее не сообщалось.Мы связали задержку роста и разрастание физиса с процессом выздоровления.
Многие исследования описывают осложнения, возникающие в результате остеомиелита у детей. Явные и серьезные последствия, такие как неправильное положение, деформация суставов и несоответствие длины конечностей, уже давно вызывают беспокойство, потому что они в течение всей жизни влияют на функции и внешний вид. Исследования документально подтвердили, что чрезмерный рост является более частым следствием повышенного кровоснабжения, чем подрост.
Однако мы наблюдали подлесок правой верхней локтевой кости у Пациента 2 и разрастание правого дистального отдела бедренной кости у Пациента 3.Мы считали, что этот феномен связан с более высоким соотношением поражений к физикам в дистальном отделе локтевой кости, чем в дистальном отделе бедренной кости, что вызывает относительно большие повреждения физичек. Отношение поражения к физике дистальных отделов локтевой кости и бедра определялось как квадрат диаметра, который составлял 0,225 и 0,052 соответственно, измеренный на их исходной МРТ. Это соотношение казалось рациональным предиктором повреждения физики. Однако у Пациента 4 это соотношение составляло 0,241, но никаких признаков расхождения ног во время последующего наблюдения не наблюдалось.Это открытие предполагает, что другие факторы, такие как возраст, период времени от начала заболевания до вмешательства, и вклад форм могут влиять на нарушение роста; однако для окончательного вывода необходимы дальнейшие исследования. Тем не менее, на наш взгляд, несмотря на влияние других факторов, на дистальный физик локтевой кости приходится только примерно 20% роста, что может объяснить незначительное расхождение, наблюдаемое в нашем случае.
Это соотношение казалось рациональным предиктором повреждения физики. Однако у Пациента 4 это соотношение составляло 0,241, но никаких признаков расхождения ног во время последующего наблюдения не наблюдалось.Это открытие предполагает, что другие факторы, такие как возраст, период времени от начала заболевания до вмешательства, и вклад форм могут влиять на нарушение роста; однако для окончательного вывода необходимы дальнейшие исследования. Тем не менее, на наш взгляд, несмотря на влияние других факторов, на дистальный физик локтевой кости приходится только примерно 20% роста, что может объяснить незначительное расхождение, наблюдаемое в нашем случае.
По нашему опыту, операция кажется вариантом, который не причиняет вреда и может сочетаться с лечением пациентов с поражением физики.Кроме того, мы считаем, что во время операции следует применять минимально инвазивные методы, чтобы не навредить физикам. В нашем исследовании двум пациентам было выполнено мягкое выскабливание и санация раны под интраоперационной рентгеноскопией. В нашем обзоре литературы рентгеноскопия и эндоскопия используются как вспомогательные средства для хирургического лечения остеомиелита эпифизарных или физических поражений 15,16 . Сообщается, что эндоскопическая хирургия под рентгеноскопическим контролем полезна для лечения эпифизарного остеомиелита, вызванного Mycobacterium разновидностей 17 .Практическим решением представляется интраоперационное руководство с помощью рентгеноскопии или эндоскопии для предотвращения повреждения физического тела. Физис сохраняет свою функцию, и процесс ремоделирования продолжается многие годы.
Большинство рецидивов остеомиелита происходит в течение 6 месяцев после первичного хирургического вмешательства, как сообщалось в предыдущих исследованиях 16,18,19 . Наши пациенты наблюдались в амбулаторных условиях, каждые 2–4 недели делали рентгенограммы до тех пор, пока на рентгеновских снимках не наблюдалось сращение кости.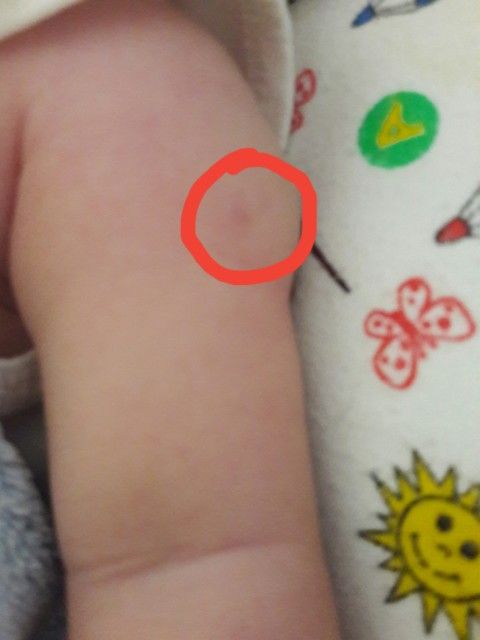 Рентгенографию затем повторяли каждые 1-2 года после операции, если нарушение роста стало проблемой.Недавние телефонные консультации показали отличные результаты у всех четырех пациентов. В этой статье подробно описаны отдаленные результаты у трех из четырех пациентов. В соответствии с результатами предыдущих исследований 10,11,12 их клинические проявления казались многообещающими и благоприятными. Кроме того, мы согласны с тем, что необходим мониторинг серьезных побочных реакций после вакцинации БЦЖ и отдаленных результатов.
Рентгенографию затем повторяли каждые 1-2 года после операции, если нарушение роста стало проблемой.Недавние телефонные консультации показали отличные результаты у всех четырех пациентов. В этой статье подробно описаны отдаленные результаты у трех из четырех пациентов. В соответствии с результатами предыдущих исследований 10,11,12 их клинические проявления казались многообещающими и благоприятными. Кроме того, мы согласны с тем, что необходим мониторинг серьезных побочных реакций после вакцинации БЦЖ и отдаленных результатов.
Хотя соответствующее рандомизированное контрольное исследование не проводилось и не было разработано руководящих принципов лечения остеомиелита или остита БЦЖ, комбинации методов лечения, применяемые во всем мире, имеют схожую основу, включая режим HR.Наш выбор лечения соответствовал предыдущей рекомендации относительно режима HR в течение 6–12 месяцев 11 . За исключением пациента 1, который все еще проходит курс лечения HR, все пациенты в настоящем исследовании завершили 10–12-месячные режимы HR.
Некоторые ограничения этого исследования требуют дальнейшего рассмотрения. Во-первых, редкость остеомиелита БЦЖ и ретроспективный характер этого исследования могли ограничить возможность обобщения наших наблюдений. Несмотря на то, что с 2008 года в нашей национальной справочной микобактериальной лаборатории для детей младше 5 лет с изолированными внелегочными штаммами туберкулеза проводится диагностика БЦЖ, включая молекулярные тесты, случаи заболевания могут быть диагностированы неправильно.Кроме того, небольшое количество дел делает невозможным дальнейший анализ. Во-вторых, за пациентами в этом исследовании не наблюдали до тех пор, пока они не достигли зрелости скелета. Поэтому мы не можем определить, могут ли деформации развиться в будущем. Тем не менее случаи в нашем исследовании были подтверждены молекулярными методами. Мы продемонстрировали тщательные клинические курсы на основе полученных изображений, лечения, краткосрочных и долгосрочных результатов. Это исследование проводилось в едином центре с последовательными принципами лечения.Таким образом, клинические исходы пациентов в сочетании с их представлением могут предоставить дополнительную информацию. Дальнейшие исследования остеомиелита и остита, связанного с БЦЖ, могут помочь нам определить роль хирургического вмешательства, кандидатов на инвазивные процедуры, а также соответствующие схемы и продолжительность лечения.
Это исследование проводилось в едином центре с последовательными принципами лечения.Таким образом, клинические исходы пациентов в сочетании с их представлением могут предоставить дополнительную информацию. Дальнейшие исследования остеомиелита и остита, связанного с БЦЖ, могут помочь нам определить роль хирургического вмешательства, кандидатов на инвазивные процедуры, а также соответствующие схемы и продолжительность лечения.
Таким образом, остеомиелит и остит после вакцинации БЦЖ требуют своевременной диагностики и соответствующего вмешательства для предотвращения дальнейших серьезных осложнений. В случае маленьких детей, у которых наблюдается легкая боль и отек мягких тканей наряду с незначительными лабораторными исследованиями, клиницисты должны быть внимательны к возможности скелетного туберкулеза.Своевременная и надлежащая санация раны может иметь решающее значение для пациентов с поражениями, затрагивающими физику или сустав, чтобы предотвратить необратимые последствия.
реакция экспертов на историю о передозировке вакцины БЦЖ у ребенка в Сканторпе
Ребенку случайно ввели в 10 раз большую дозу противотуберкулезной вакцины БЦЖ — впоследствии он лечился в больнице, но его жизнь не считалась опасной.
Д-р Дэвид Эллиман, консультант по общественному детскому здоровью, Королевский колледж педиатрии и детского здоровья и Детская больница на Грейт-Ормонд-стрит, сказал:
«Способ введения БЦЖ отличается от большинства других вакцин. Обычно вакцины распространяются производителями в виде разовых доз во флаконе или шприце. Однако для БЦЖ каждый флакон содержит эквивалент 10 стандартных доз по 0,1 мл. Ребенок обычно получает половину стандартной дозы, данной ребенку (0.05 мл, а не 0,1 мл), поэтому в каждом флаконе фактически содержится 20 доз для ребенка.
«Вакцина БЦЖ предназначена для лечения туберкулеза, но не содержит самого туберкулеза человека (Mycobacterium tuberculosis). Вакцина содержит родственный микроб, вызывающий туберкулез крупного рогатого скота (Mycobacterium bovis). Это означает, что вакцинированный ребенок технически не болен туберкулезом. Вакцина Bacillus Calmette-Guerin — это живая, но сильно смягченная вакцина, которая была модифицирована, чтобы сделать ее гораздо менее серьезной.
«Когда ребенку вводят вакцину, она вводится непосредственно под кожу i.е. внутрикожно и обычно образует небольшую твердую шишку. Десятикратная доза вызовет шишку в десять раз больше, что обычно является индикатором передозировки, но если инъекция была сделана слишком глубоко, шишка может быть намного меньше. Слишком глубокое введение вакцины может вызвать собственные проблемы, и обычно, если вводится слишком много вакцины или вводится слишком глубоко, можно ожидать развития абсцесса. Они не похожи на нормальные абсцессы, поскольку не краснеют и не болезненны и развиваются медленно.
«Специалист решит, какое лечение необходимо провести при развитии абсцесса. Есть два варианта: проколоть его и / или назначить антибиотики, как при туберкулезе. Их вводят в течение месяцев, а не дней. Очень, очень, очень редко, например, если у ребенка что-то не в порядке с его иммунной системой, может быть более общее распространение, что является более серьезным ».
Служба охраны здоровья семьи — {page_title}
Вакцина с бациллой Кальметта-Герена (БЦЖ)
(Содержание пересмотрено 11/2017)
Туберкулез (ТБ)
Туберкулез вызывается микобактериями.Он распространяется по воздуху и обычно поражает легкие (туберкулез легких). Другие части тела, такие как кости, печень, мозг и почки, также могут быть поражены (внелегочный туберкулез). Туберкулез по-прежнему является серьезным инфекционным заболеванием на местном уровне, поскольку Гонконг является густонаселенным сообществом.
Туберкулез по-прежнему является серьезным инфекционным заболеванием на местном уровне, поскольку Гонконг является густонаселенным сообществом.
Вакцина БЦЖ
A. Зачем делать прививки?
Хотя БЦЖ не обеспечивает 100% защиты от туберкулеза, она помогает локализовать инфекцию в легких и эффективно защищает от серьезных осложнений заболевания.В Гонконге вакцина БЦЖ включена в Гонконгскую программу иммунизации детей.
B. Когда моему ребенку следует сделать прививку?
Всем местным новорожденным следует делать БЦЖ при рождении. Детям в возрасте до 15 лет, проживающим в Гонконге и ранее не получавшим БЦЖ, рекомендуется прямая вакцинация БЦЖ.
C. Следующие лица НЕ должны получать BCG
- получил другие живые вакцины за последние четыре недели (БЦЖ можно вводить после этого интервала)
- при иммуносупрессивной терапии (e.грамм. облучение, лечение цитотоксическими препаратами или системными стероидами)
- иммунодефицит, врожденный или приобретенный (например, ВИЧ-инфекция)
- рак (например, лейкемия, лимфома)
- Болезни кожи тяжелые
- новорожденных от матерей, получавших биологическую терапию во время беременности (проконсультируйтесь со специалистами, поскольку возможна отсрочка вакцинации)
Д.Какие побочные эффекты?
- У некоторых детей может развиться небольшая красная папула или язва в месте инъекции через 2–4 недели после вакцинации. Он постепенно пройдет и заживет через несколько недель, оставив небольшой шрам или вообще не оставив шрама. Иногда у некоторых детей под мышкой могут образовываться шишки из-за увеличения лимфоузлов. Другие побочные реакции очень редки.