как переносится ревакцинация, когда делают прививку
Столбняк, дифтерия и коклюш – это инфекционные патологии, которые тяжело протекают и часто встречаются у детей ввиду несформированности иммунитета. Последняя болезнь переносится легко, но может иметь тяжелые осложнения. Дифтерия и столбняк нередко приводят к смерти.
В целях защиты, в рамках Национального календаря прививок, проводят вакцинацию от этих трех заразных патологий. Для формирования крепкого иммунитета применяют АКДС. Препарат довольно реактогенный и иногда провоцирует побочные реакции.
В интернете нередко можно прочитать отзывы о том, что четвертая прививка АКДС переносится особенно тяжело. Чтобы понять, стоит ли соглашаться на ревакцинацию, рекомендуется рассмотреть сроки проведения иммунопрофилактики и вероятные последствия.
Сроки вакцинации и ревакцинации
АКДС – это инактивированный тип вакцины. Состав представлен дифтерийным, коклюшным и столбнячным токсоидами.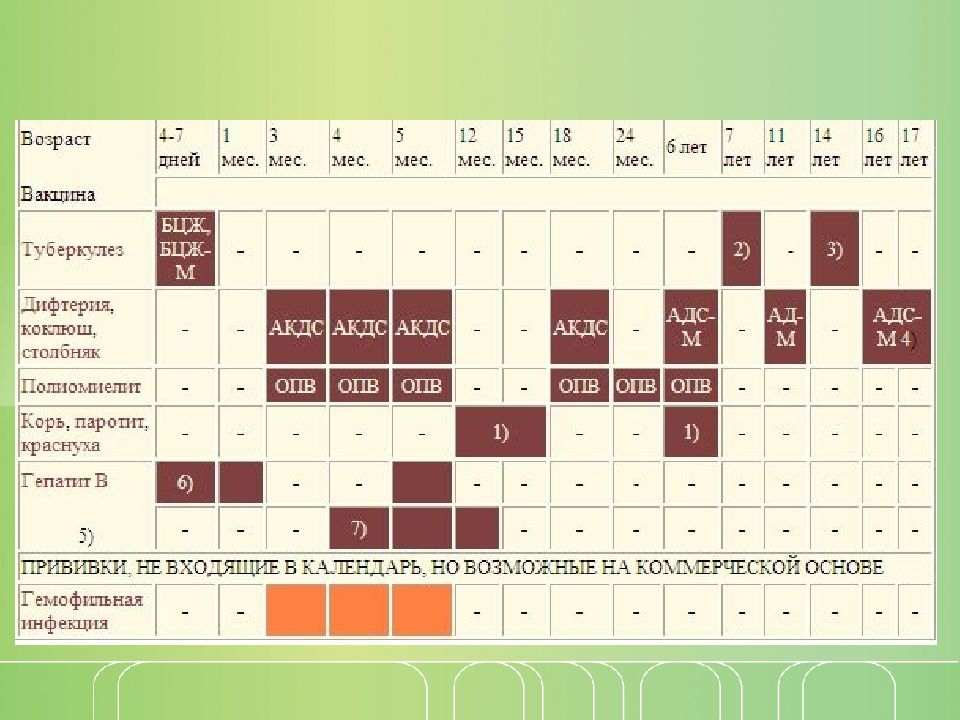
По предложенной Министерством Здравоохранения схеме, вакцинацию проводят тремя дозами. При этом выдерживают промежуток между инъекциями, который составляет не меньше 30-40 дней. Вводят препарат внутримышечно в область бедра.
Вакцина АКДС
Первую прививку по утвержденному графику делают в трехмесячном возрасте. Раньше иммунизировать детей не имеет смысла, поскольку первые 90-93 дня, в крови присутствуют антитела переданные от матери. Затем защитные силы начинают ослабевать, малыш становится подверженным заражению столбняком, коклюшем и дифтерией.
У некоторых лиц имеются временные противопоказания к иммунизации АКДС. В таких случаях прививку переносят на период полного выздоровления. В некоторых странах оптимальным сроком вакцинации считается возраст 2-4 месяца. Уже после первого укола начинают вырабатываться антитела.
Но их недостаточно и концентрация их уменьшается со временем. Для создания стойкого иммунитета препарат используют повторно. Вторую дозу АКДС вводят в 4,5 месяца, спустя 45 дней после первой инъекции. Медики применяют ту же самую дозу и колют препарат также в бедро. Третья прививка делается в полгода.
При необходимости можно перенести АКДС на два месяца вперед. После курса иммунизации, состоящего из трех доз, российским календарем профилактики инфекционных патологий предусмотрена ревакцинация.
Ее делают в 6-7 лет, затем в 14. С 24-летнего возраста против столбняка, дифтерии прививают каждые 10 лет. Препараты с коклюшным компонентом уже не используют. Применяют АДС-М или импортные вакцины.
Для ослабленных лиц схему вакцинации и ревакцинации педиатры подбирают индивидуально. Если АКДС переносится плохо, доктора рекомендуют использовать аналоги Инфанрикс или Пентаксим. В них нет цельноклеточного коклюшного компонента и мертиолята.
Обязательно ли делать 4 АКДС?
Некоторые родители думают, что после трех прививок ребенок становится полностью и надолго защищенным от заражения палочками дифтерии, столбняка и коклюша. В интернете на форумах можно прочитать, что четвертая прививка АКДС может переноситься детским организмом хуже предыдущих.
Ревакцинация АКДС считается обязательной. Но каждый родитель вправе написать отказ, основываясь на положения законодательства.
Доктора приводят такие аргументы в пользу четвертой прививки:- в 6-7 лет ребенок обычно начинает ходить в школу. Там малыш активно контактирует с другими детьми и учителями. Соответственно у него повышается риск заражения инфекционно-вирусными патологиями;
- дифтерия и столбняк – это опасные заболевания.
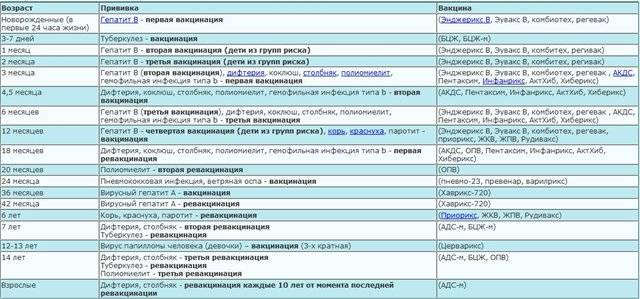 Особенно им подвержены дети в виду слабого иммунитета. От столбнячной палочки до сих пор нет эффективных препаратов. Поэтому риск смертности от этой болезни очень высокий;
Особенно им подвержены дети в виду слабого иммунитета. От столбнячной палочки до сих пор нет эффективных препаратов. Поэтому риск смертности от этой болезни очень высокий; - у 15-20% привитых тремя дозами АКДС детей, уже спустя год не обнаруживается достаточное количество антител в крови. Это связано с индивидуальными особенностями организма. Четвертая вакцинация определить концентрацию антител в 6 лет можно путем сдачи крови на анализ. Как правило, к этому возрасту у большинства детей защитные силы против дифтерии, столбняка и коклюша уже снижены. Поэтому четвертая прививка АКДС показана всем.
Комаровский рекомендует не игнорировать иммунопрофилактику, если у ребенка нет противопоказаний. Доктор отмечает, что последствия инфекционно-вирусных патологий развиваются гораздо чаще и они более опасные, чем побочные реакции на прививку, которые можно быстро устранить медикаментозно.
Во сколько лет ребенку делается четвертая прививка?
Четвертую прививку против заражения палочками дифтерии, столбняка и коклюша делают в 6-7 лет. Интервал между третьей вакцинацией и первой ревакцинацией составляет 5,5-6,5 лет.
Интервал между третьей вакцинацией и первой ревакцинацией составляет 5,5-6,5 лет.
Бывает, что из-за наличия у ребенка временных противопоказаний иммунопрофилактику третьей дозой переносят. В этом случае четвертую прививку делают по установленному графику – в 6-7 лет.
Как переносится 4 АКДС: нормальная реакция и осложнения
По мере взросления вероятность развития побочных эффектов и их выраженность увеличиваются. Также плохую переносимость можно объяснить тем, что у ребенка в крови уже есть определенное количество антител, которые при очередном введении антигенного материала начинают активизироваться, вызывая ряд изменений в самочувствии.
Особенно подвержены побочным реакциям ослабленные, склонные к аллергии лица. Все реакции на АКДС можно поделить на нормальные и патологические. Первые свидетельствуют о правильном формировании иммунитета, а вторые – о развитии осложнений.
После четвертой дозы АКДС могут возникнуть такие изменения в состоянии здоровья:
Эти симптомы носят кратковременный характер: проходят спустя несколько дней.
К осложнениям АКДС относятся такие состояния:
- аллергия в виде отека Квинке, крапивницы, синдрома Стивенса-Джонсона, анафилаксии;
- абсцесс в месте постановки укола;
- токсический шок;
- лихорадка;
- судорожные припадки;
- воспаление головного мозга;
- хромота;
- присоединение сопутствующей инфекции.
Для лучшей переносимости четвертой дозы АКДС, доктора рекомендуют давать несколько дней после укола жаропонижающие и антигистаминные средства.
Также для минимизации риска негативных последствий вакцинации, не следует прививать ребенка при наличии у него таких состояний:- общее недомогание;
- появление тяжелых побочных реакций на предыдущую инъекцию АКДС;
- сниженный иммунитет;
- обострение хронической патологии;
- рак;
- гипертермия;
- сыпь по телу.
Как правило, у большинства детей после четвертой АКДС возникает реакция местного характера и повышается температура.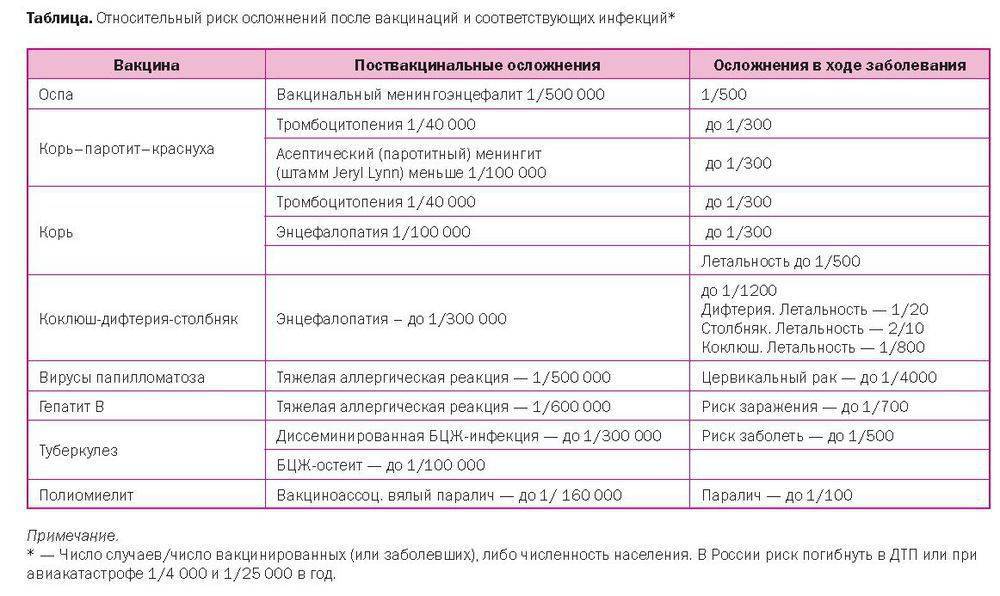 При этом первые три прививки могут не давать никаких изменений в самочувствии в поствакцинальный период.
При этом первые три прививки могут не давать никаких изменений в самочувствии в поствакцинальный период.
Что делать, если пропустили прививку?
Если была пропущена прививка, то рекомендуется возобновить иммунопрофилактику в срок, максимально приближенный к графику вакцинации. Четвертую дозу лучше делать препаратом АДС или АДС-М. Эти средства не содержат цельноклеточный коклюшный компонент, поэтому переносятся детьми лучше.
Если ребенок не переболел коклюшем и родители хотят полностью привить малыша от этой инфекционной патологии, то четвертую дозу АКДС стоит делать спустя полгода после третьей инъекции.
Видео по теме
О вакцинации препаратом АКДС в Школе доктора Комаровского:
Таким образом, для защиты от столбняка, коклюша и дифтерии детей с трехмесячного возраста начинают прививать АКДС.
В этот период малыш начинает ходить в школу, его круг контактов расширяется. Вместе с этим растет и вероятность заражения инфекционно-вирусными патологиями. Поэтому отказываться от четвертой прививки не стоит. Если АКДС переносится плохо и у родителей есть опасения по поводу развития осложнений у ребенка, то педиатр может порекомендовать профилактику импортными вакцинами.
прививка АКДС чуть не моего сделала ребёнка инвалидом — Рамблер/женский
Согласно календарю прививок, первая вакцинация от коклюша, дифтерии и столбняка проводится в 3 месяца. Пока мой сын дорос до этого возраста, я, как и все, успела наслушаться страшилок про АКДС. Например, моя сестра говорила, что эта вакцина замедляет речевое развитие, дети неделями температурят и потом подолгу лечатся у неврологов. Я не понимала, откуда она берет эти мифы: вместо цельноклеточной («живой») АКДС она ставила детям только импортные бесклеточные аналоги, то есть лично с осложнениями не сталкивалась. А в интернете чего только не напишут!
Я не понимала, откуда она берет эти мифы: вместо цельноклеточной («живой») АКДС она ставила детям только импортные бесклеточные аналоги, то есть лично с осложнениями не сталкивалась. А в интернете чего только не напишут!
Зато в пользу АКДС у меня было много аргументов:
Вакцина ставится во всех городских поликлиниках нашей страны. И будь она так страшна, её бы давно сняли с производства.
Она бесплатная и всегда в доступе, в отличие от импортных Инфанрикса и Пентаксима. Например, 1,5 года назад они были в дефиците, и сестра искала их по всей Москве. Потом таскала детей на другой конец города и отдавала за вакцинацию по 5000-6000 р. Правда, в стоимость входил ещё осмотр педиатра – кандидата наук.
Сейчас с этим проще: импортные вакцины можно купить в аптеках по рецепту (1300-1900 р.), а поставить бесплатно в своей поликлинике. Но год назад даже трата 1000 р. показалась бы мне блажью!
«Неживые» вакцины действительно показаны только больным детям: с раком, ВИЧ, серьёзной аллергией. А мой сын был здоров!
А мой сын был здоров!
В общем, я не увидела причин отказываться от бесплатной прививки.
Если нет медотвода, вакцинация против коклюша, дифтерии и столбняка проходит в 3 этапа: в 3, 4,5 и 6 месяцев. У сына не было ни ОРВИ, ни высыпаний, ни неврологических проблем, и мы никак не готовились к прививкам – просто приходили к педиатру и получали направления.
В день первой вакцинации ребёнок был слегка капризным – видимо, из-за лёгкой температуры (37,2). Вторую и третью перенёс чуть хуже – 3 дня температурил (до 38,4), было красное горло, плохо спал. Но я знала, что это варианты нормы, и не волновалась. Такова уж цена иммунитета!
Неготовность к ревакцинации
Когда пришло время ревакцинации (в 1,5 года), педиатр предупредила, что 4-е введение АКДС переносится хуже. Она советовала 3 дня давать сыну антигистаминное и избегать общественных мест.
Но соблюсти рекомендации не вышло: за 5 дней до прививки мы сходили на детский день рождения. Там мой сын попробовал шоколад, и к вечеру его обсыпало. Я собиралась – правда собиралась! – купить капли от аллергии, но к утру сыпь прошла сама, и я не стала пичкать ребёнка лекарствами. А педиатр в день прививки ничего не заметила.
Я собиралась – правда собиралась! – купить капли от аллергии, но к утру сыпь прошла сама, и я не стала пичкать ребёнка лекарствами. А педиатр в день прививки ничего не заметила.
После ревакцинации я не могла нарадоваться: прошли день, два – у сына не было даже температуры. Я решила, что иммунитет выработался ещё в прошлые разы, и расслабилась. Но через трое суток ребёнок разбудил в 5 утра страшным криком! В кроватке блестела огромная лужа рвоты, малыш был потный, красный, а градусник показал 39,1. Врач со «скорой» обнаружил ещё и уплотнение на ножке в месте укола. Но меня успокоили: такая реакция бывает у многих – пройдёт.
Следующие 4 дня показались адом: после жаропонижающих температура падала на 1,5-2 часа и подскакивала снова. Ребенок ничего не ел, иногда его рвало, появился кашель. Место укола я, по совету педиатра, мазала Траумелем, но ножка опухла и стала болеть – сыночек её волочил. В итоге педиатр, уставшая ходить к нам каждый день, дала направление в стационар с подозрением на менингит.
Конечно, никакого менингита у сына не было. В больнице заверили, что это ПВО – поствакцинальные осложнения. Чтобы их избежать, перед прививкой даже здоровым детям даются препараты от аллергии. А ещё запрещено ходить по детским мероприятиям: мы вот наелись там шоколада и добавили иммунитету хлопот, а подцепить еще и ОРВИ…
Про «живые» и «неживые» вакцины врач сказал вот что. Во-первых, без подготовки любая прививка может дать осложнения. А во-вторых, статистика говорит не в пользу «живой» (цельноклеточной) вакцины: после нее в 50-55% случаев возникают реакции, а после импортных лишь в 10% бывают температура выше 38, боль и припухлость на ножке, и в 25% капризность, недомогание и другие изменения.
В больнице сын поправился за неделю: антибиотики сделали свое дело. Но больше всего я боялась, что не пройдет хромота и малыш останется инвалидом. Волочил ногу он целый месяц.
По возможности прививаться бесклеточными вакцинами. Вероятность осложнений меньше, а значит, меньше поводов казнить себя. Есть аллергия или нет – давать ребёнку антигистаминные 3 дня до и 3 дня после вакцинации.Не посещать общественные места и детские мероприятия перед прививкой. Следить за тем, что ест ребёнок перед вакцинацией. Новый (и очень аллергенный!) продукт сын попробовал только по моему недосмотру.Сдать общие анализы крови и мочи. Даже если участковый педиатр не даст направления, платные анализы стоят копейки и помогут выявить, нет ли у ребёнка аллергии и начинающегося ОРВИ. Тогда прививку лучше отложить.
Есть аллергия или нет – давать ребёнку антигистаминные 3 дня до и 3 дня после вакцинации.Не посещать общественные места и детские мероприятия перед прививкой. Следить за тем, что ест ребёнок перед вакцинацией. Новый (и очень аллергенный!) продукт сын попробовал только по моему недосмотру.Сдать общие анализы крови и мочи. Даже если участковый педиатр не даст направления, платные анализы стоят копейки и помогут выявить, нет ли у ребёнка аллергии и начинающегося ОРВИ. Тогда прививку лучше отложить.
Ревакцинация АКДС: как переносится вторая и третья прививка
Прививая своего ребенка АКДС, вы защищаете его от таких болезней, как дифтерия, коклюш и столбняк. Многие родители отказываются прививать своих детей, основываясь на информации о возможных тяжелых последствиях прививок. Так ли страшна на самом деле вакцинация? Кто же больше рискует своим здоровьем – привитый ребенок или тот, чьи родители отказались от вакцинации?
Зачем детям проводят вакцинацию и ревакцинацию АКДС?
АКДС – адсорбированная вакцина против 3-х опаснейших детских инфекционных заболеваний: коклюша, дифтерии и столбняка.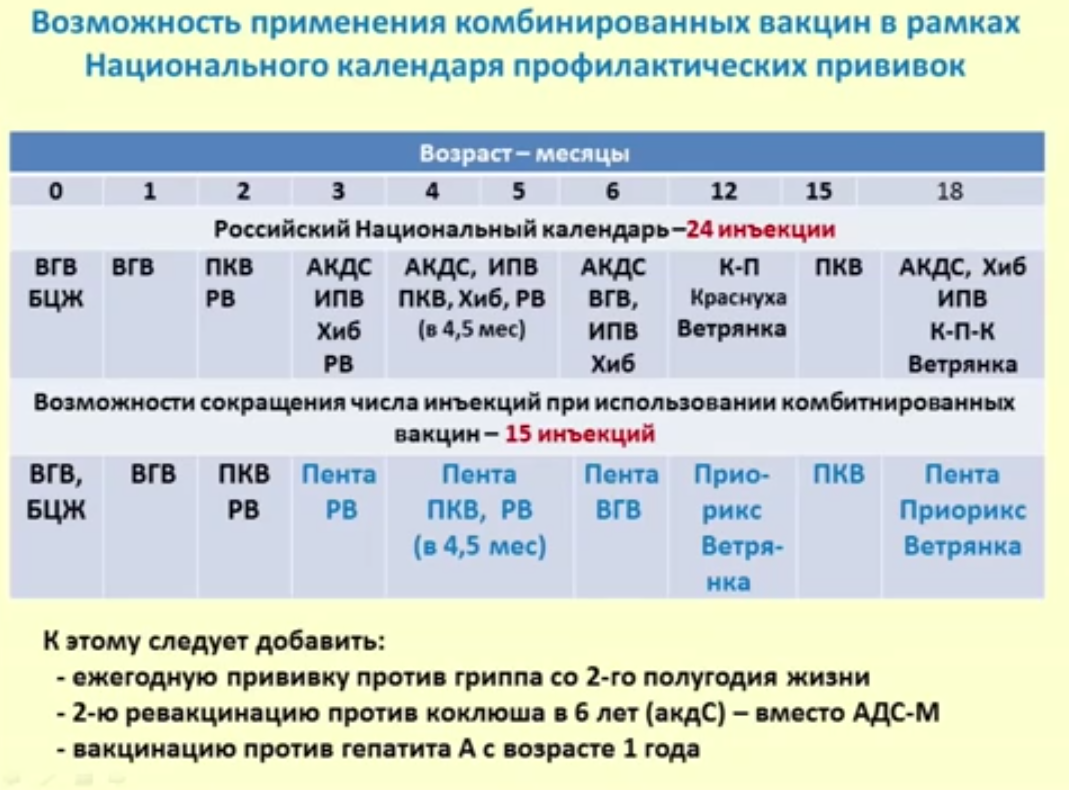 Вакцинация АКДС используется медиками всего мира, чтобы обезопасить детей от тяжелых последствий этих патологий. Именно эти инфекции занимают первые места среди распространенных причин детской смертности.
Вакцинация АКДС используется медиками всего мира, чтобы обезопасить детей от тяжелых последствий этих патологий. Именно эти инфекции занимают первые места среди распространенных причин детской смертности.
Вакцинация АКДС – это введение в организм ребенка убитых или ослабленных клеток возбудителя дифтерии и анатоксинов коклюша и столбняка. После попадания в кровь эти чужеродные агенты создают видимость болезни в легкой форме, а организм ребенка начинает с ними бороться. Происходит формирование стойких защитных сил. Для того чтобы поддерживать иммунитет к конкретному заболеванию на необходимом уровне, периодически проводят ревакцинацию – повторное введение облегченной вакцины.
Многие родители задают себе вопрос, какой иммунитет крепче – искусственный или естественный (если ребенок переболеет этой болезнью). На самом деле ответ очевиден, ведь курс прививок АКДС защитит организм ребенка от болезней на 6-12 лет. Тогда как перенесенные дифтерия и столбняк, во-первых, крайне опасны для жизни, а во-вторых, организм самостоятельно не вырабатывает к ним иммунитет. Переболевший коклюшем ребенок получает защиту на тот же срок, что и при вакцинации. Зачем же рисковать здоровьем?
Переболевший коклюшем ребенок получает защиту на тот же срок, что и при вакцинации. Зачем же рисковать здоровьем?
Какие препараты используют для иммунизации в России:
- АКДС. Отечественное средство в виде суспензии для внутримышечных инъекций. Не реализуется в аптеках, но имеется в наличии в поликлиниках.

- Инфанрикс (рекомендуем прочитать: в чем отличие вакцины Инфанрикс Гекса от Инфанрикс?). Бельгийский препарат, выпускается в ампулах объемом 0,5 мл.
- Пентаксим (см. также: когда требуется ревакцинация Пентаксимом?). Французская вакцина, реализуется в виде шприца с суспензией. К препарату дополнительно добавляется гемофильный компонент со столбнячным анатоксином.
- АДС. Рекомендован для вакцинации в возрасте старше 4-х лет. В нем нет коклюшевого компонента. Он и не нужен – при своевременной вакцинации АКДС иммунитет к коклюшу уже приобретен.
- АДС-М. Вакцина, формирующая стойкий иммунитет к столбняку и дифтерии у детей старше 6 лет.
Также применяют средства, которые защищают ребенка от 4 и более инфекций. Среди них: Инфанрикс ИПВ (защита от столбняка, коклюша, дифтерии и полиомиелита), Инфанрикс Гекса (защита от тех же инфекций, а также от гепатита В, полиомиелита и гемофильной инфекции). Все прививки желательно делать одним и тем же препаратом, но при индивидуальной реакции на состав вакцины врач предложит иной вариант.
Календарь вакцинации и ревакцинации АКДС
Если ребенок родился недоношенным, или есть медицинские противопоказания к иммунизации (недавно перенесенные простудные, инфекционные болезни, повышенная температура тела, обострение хронических заболеваний), то возможна отсрочка прививок.
Комплексное действие препарата достаточно сильное, поэтому если в анамнезе пациента есть аллергические реакции, рекомендуют заменить тяжелую АКДС на упрощенную АДС-М, в которой отсутствует коклюшный компонент, часто вызывающий аллергию.
Вторая и последующие АКДС играют не менее важную роль, чем первая. Благодаря их использованию организм получает наивысшую степень защиты от инфекций. Чем старше ребенок, тем проще он переносит прививку, ведь с возрастом иммунитет становится крепче. Прививки делают поэтапно, начиная с 2 месяцев, последняя прививка АКДС ставится в полуторагодовалом возрасте. Затем в течение всей жизни с определенными интервалами проводится ревакцинация.
Согласно календарю вакцинаций, первичный курс прививок проводится:
- 1-я – в 2-3 месяца;
- 2-я – в 4-5 месяцев;
- 3-я – в 6 месяцев;
- 4-я – в 18 месяцев.
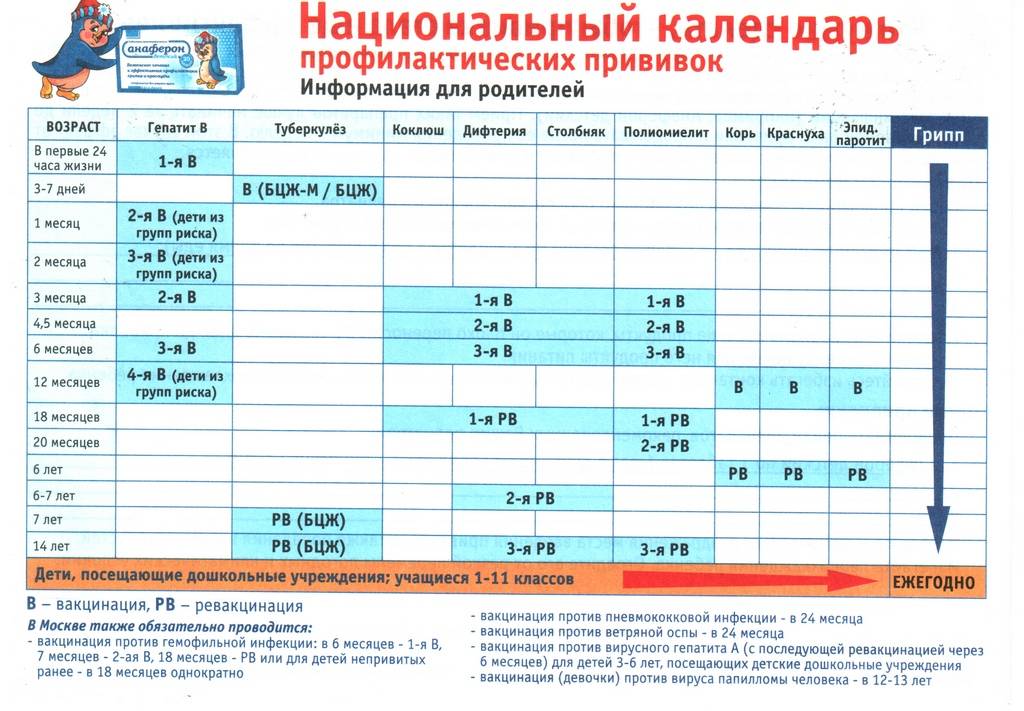
Считается, что в первые несколько месяцев после рождения ребенка защищает врожденный иммунитет. Антитела к этим заболеваниям переходят через пуповинную кровь от матери. Интервал между прививками АКДС может увеличиваться в зависимости от состояния ребенка и его здоровья. Например, если первую прививку сделали малышу в 3 месяца, то вторая по показаниям должна быть не ранее, чем через месяц. То же самое касается третьей и четвертой и последней прививки.
Первая ревакцинация проходит в полтора годаНезависимо от расположения медицинского учреждения все данные о прививках вносятся в карту вакцинаций. Это нужно для того, чтобы в будущем, по мере взросления малыша, было видно, когда и какой вакциной проводилась иммунизация. Это важно как для медицинского статистического контроля, так и для дальнейших иммунизационных мероприятий.
Важное условие – сохранение минимального интервала между прививками (30 дней), и только четвертая вакцинация проводится немного позже. Врачи рекомендуют не делать перерыв между ревакцинациями больше года, это может снизить эффект от иммунизации. Именно эти 4 процедуры введения препарата и являются основной вакцинацией, позволяющей защитить организм ребенка от возникновения дифтерии, коклюша и столбняка. После чего через определенные промежутки времени делают ревакцинацию бесклеточным коклюшным компонентом (АДС):
Именно эти 4 процедуры введения препарата и являются основной вакцинацией, позволяющей защитить организм ребенка от возникновения дифтерии, коклюша и столбняка. После чего через определенные промежутки времени делают ревакцинацию бесклеточным коклюшным компонентом (АДС):
- в 6-7 лет;
- в 14 лет;
- далее – во взрослом возрасте каждые 10 лет.
К сожалению, ревакцинация АКДС во взрослом возрасте в России проходит далеко не всегда по календарю. При нарушении графика ревакцинаций взрослых АКДС ВОЗ рекомендует не начинать прививки сначала, а возобновлять их с того этапа, на котором и произошел «сбой», и делать столько ревакцинаций, сколько необходимо.
Как дети переносят вакцинацию?
Малышей вакцинируют внутримышечно, вводя препарат в массивную бедренную мышцу. Деткам постарше, начиная с 4 лет, прививку делают в мышцы предплечья. Специфика препарата такова, что, попадая в мышцу, он не сразу всасывается в кровь, а постепенно, что стимулирует выработку антител организмом.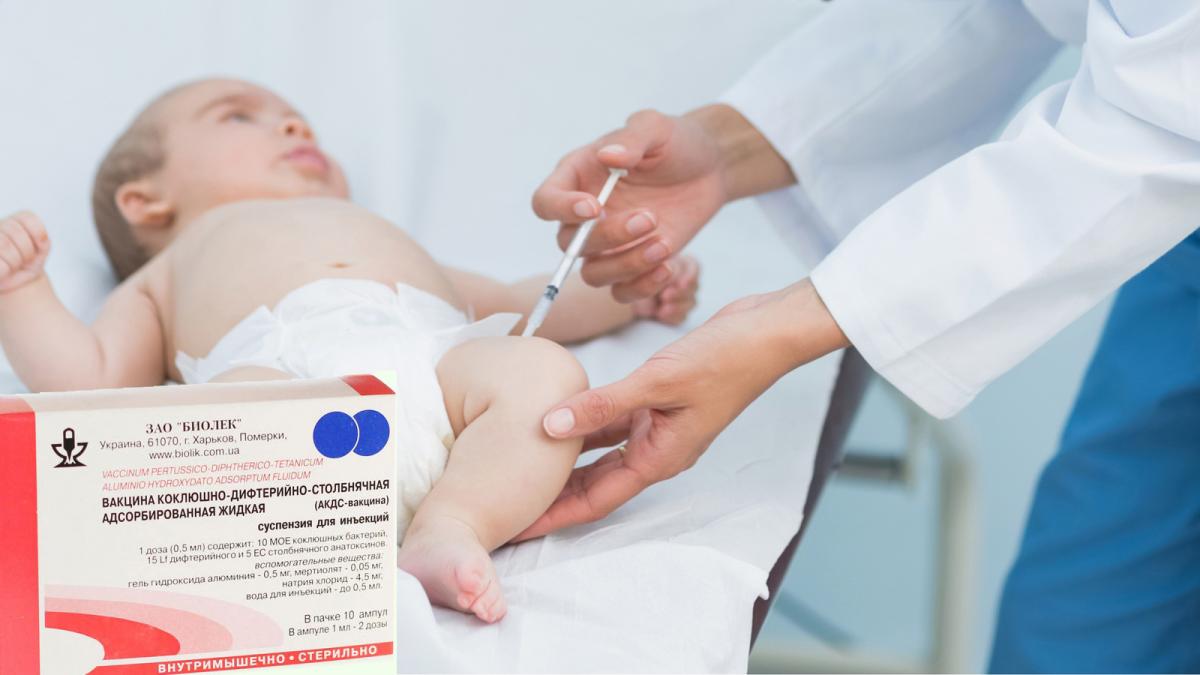 Проведение иммунизации может пройти для ребенка абсолютно незамеченным. Однако иногда родители могут заметить изменения в месте инъекции или в поведении ребенка.
Проведение иммунизации может пройти для ребенка абсолютно незамеченным. Однако иногда родители могут заметить изменения в месте инъекции или в поведении ребенка.
Организм ребенка может отреагировать на прививку легко, но может и «взбунтоваться». Для того чтобы понять, когда организм реагирует на вакцину нормально, а когда инъекция переносится тяжело, следует обратиться за помощью к врачу.
Нормальные побочные реакции
Появление у ребенка некоторых из этих симптомов говорит о нормальной реакции организма на введение вакцины:
- Место укола становится более плотным, возможно покраснение. Для устранения этой реакции можно сделать спиртовой компресс на место инъекции.
- Потеря аппетита, возможны рвота и понос. При диарее рекомендован прием энтеросорбентов (Смекты, Энтеросгеля, активированного угля).
- Небольшое повышение температуры тела. Этот симптом наиболее частый, и может сохраняться до нескольких дней. Жаропонижающие средства облегчат состояние ребенка.

- Кашель. Как правило, проходит без вспомогательного лечения через несколько дней.
- Сыпь. Аллергия уходит после приема антигистаминных средств.
- Ребенок прихрамывает на одну ножку. Это связано с тем, что у детей небольшая мышечная масса, и это затрудняет рассасывание препарата. Для устранения симптома можно помассировать ногу, обернуть теплым полотенцем.
- Смена поведения. Из спокойного и тихого он стал капризным и плаксивым, или наоборот – активный малыш становится вялым, заторможенным и сонным.
Все рассмотренные симптомы – это стандартная реакция на введение чужеродных и враждебных клеток, ведь именно такими и являются элементы вакцины по отношению к организму. Ребенок при появлении реакции на первую прививку скорее всего во время второй, третьей и последующих отреагирует так же. Поэтому родители должны иметь в аптечке заранее приготовленные лекарства для устранения неприятных симптомов. Нужно наблюдать за ребенком и в случае резкого ухудшения состояния обратиться в больницу. Такие проявления могут быть не только нормальной реакцией организма на прививку или ревакцинацию, а признаком отдельного заболевания, проявившегося после вакцинации.
Нужно наблюдать за ребенком и в случае резкого ухудшения состояния обратиться в больницу. Такие проявления могут быть не только нормальной реакцией организма на прививку или ревакцинацию, а признаком отдельного заболевания, проявившегося после вакцинации.
При каких симптомах требуется незамедлительно обращаться к врачу?
Негативные последствия после иммунизации АКДС проявляются в течение первых суток. Если состояние здоровья ребенка ухудшилось спустя несколько дней после процедуры, стоит установить иную причину. При каких симптомах после вакцинации нужно срочно обратиться к врачу во избежание острой реакции:
- резкое повышение температуры тела до 39 градусов;
- в месте введения вакцины появился отек более 5-8 см в окружности;
- ребенок беспрерывно плачет на протяжении нескольких часов.
Возможные осложнения после прививки АКДС
По статистическим данным, серьезные последствия после рассматриваемой прививки или ревакцинации – достаточно редкое явление (они наблюдаются всего у 1-3 детей из 100 тысяч).
Серьезная аллергическая реакция после прививкиЭти осложнения потенциально возможны, и они провоцируют ухудшение общего состояния здоровья малыша:
- серьезную аллергию на один или несколько компонентов вакцины;
- судорожный синдром, возникший без повышения температуры тела;
- неврологические осложнения на фоне высокой температуры тела (коклюшный компонент вакцины АКДС действует на мозговые оболочки) (рекомендуем прочитать: почему возникает температура от АКДС?).
Достаточно редкими осложнениями иммунизации являются патологии почек, печени или заболевания ЦНС. Шанс возникновения тяжелых побочных явлений достаточно мал, но при подозрении на такие осложнения следует срочно обратиться к врачу. В больнице проконтролируют общее состояние ребенка, и при необходимости окажут квалифицированную помощь.
Особенности ухода за ребенком после прививки
Прививка АКДС отличается от всех остальных большим риском возникновения побочных реакций организма, однако отказываться от нее не стоит. После проведения вакцинации и ревакцинации согласно графику у ребенка выработается стойкий иммунитет к коклюшу, дифтерии и столбняку. Малыша стоит подготовить к вакцинации для сведения к минимуму риска возникновения побочных реакций:
- если ребенок склонен к аллергиям (частый диатез, аллергия на пищевые продукты), за несколько суток до процедуры стоит пропить курс антигистаминных препаратов;
- непосредственно в день процедуры нужно дать ребенку сироп или таблетку (малышу до года – поставить свечку) для предупреждения повышения температуры тела.
Перед любой прививкой необходим осмотр педиатра, и показана сдача анализов. Первая прививка требует посещения не только педиатра, но и узких специалистов: невропатолога, отоларинголога, аллерголога. Если у ребенка не выявлено патологий, и никаких противопоказаний к вакцинации нет – ему вводят препарат.
На протяжении 2-3 дней после прививки нужно следовать рекомендациям:
- обеспечить ребенку обильное питье и контролировать температуру в помещении, где находится малыш;
- не купать ребенка в день прививки;
- на протяжении нескольких дней желательно избегать людных мест;
- не стоит вводить новый прикорм до или сразу после прививки;
- несколько дней измерять температуру тела даже без видимых причин для беспокойства, перед сном дать профилактическую дозу жаропонижающего препарата;
- можно дать ребенку противовоспалительное средство – это не принесет вреда, а малыш будет лучше спать.
Выполнение этих рекомендаций поможет малышу спокойно перенести иммунизацию. Каждый родитель решает сам, проводить ли ревакцинацию АКДС своему ребенку. Однако стоит помнить о том, что своевременная иммунизация согласно графику поможет ребенку приобрести иммунитет от заболеваний, опасных для его здоровья и жизни. Один вовремя не привитый ребенок – это потенциальная угроза для огромного количества людей.
Врач-педиатр 2 категории, аллерголог-иммунолог, окончила БГМУ Федерального агентства по здравоохранению и социальному развитию. Подробнее »Поделитесь с друьями!
Вакцинация против дифтерии, столбняка и коклюша (АКДС) и против полиомиелита
В 3 месяца начинается вакцинация против коклюша, дифтерии, столбняка, полиомиелита. В Национальный календарь защита от данных инфекций введена в 1953 году, а против столбняка с 1966. Для вакцинации используются следующие вакцины:
— АКДС – это адсорбированная комбинированная вакцина, которая содержит убитую цельную коклюшную палочку (поэтому она еще называется цельноклеточная), анатоксин (обезвреженный токсин) дифтерийный и анатоксин столбнячный. Это российская вакцина (Микроген) и ее использование практически ликвидировало дифтерию и столбняк и заметно уменьшило число случаев коклюша.
Единственное, что не нравится многим родителям – это подъем температуры в первые сутки – это вариант нормальной реакции на вакцинацию, так как клетки иммунной системы начинают активно работать в ответ на контакт с обломками коклюшной палочки.
Но вакцинопрофилактика постоянно совершенствуется, и в настоящее время выпускаются вакцины бесклеточные (или ацеллюлярные). Данные вакцины содержат только 2 или 3 коклюшных антигена, в их составе нет целой коклюшной палочки (до 3000 коклюшных антигена). Но на сегодня подобные вакцины только зарубежного производства. В России зарегистрировано несколько подобных вакцин:
— первая вакцина, зарегистрированная в России в начале 2000 годов – Инфанрикс (ГлаксоСмитКляйн, Бельгия). Вакцина содержит 3 коклюшных антигена, дифтерийный и столбнячный анатоксины.
— несколько позже зарегистрирована вакцина Инфанрикс гекса (ГлаксоСмитКляйн. Бельгия). В дополнение к составу предыдущей вакцины здесь содержится еще инактивированная вакцина против полиомиелита, гепатита В и вакцина Хиберикс (против гемофильной палочки, которая является причиной осложнений при ОРВИ у детей раннего возраста).
— Пентаксим (Санофи, Франция), зарегистрирована и с успехом применяется в России с 2008 года. В своей комбинации данная вакцина содержит еще и инактивированную (убитую) вакцину против полиомиелита, вакцину против гемофильной палочки.
В редакции основного приказа по вакцинации в рамках Национального календаря N125н от 13.04.2017 есть следующие дополнения – определены дети из группы риска для вакцинации против гемофильной палочки и полного курса вакцинации инактивированной полиомиелитной вакциной:
- С иммунодефицитными состояниями;
- С анатомическими дефектами, приводящими к резко повышенной опасности заболевания гемофильной инфекцией;
- С аномалиями развития кишечника;
- С онкологическими заболеваниями и /или длительно получающим иммуносупрессивную терапию;
- Рожденные от матерей с ВИЧ инфекцией;
- Находящиеся в домах ребенка;
- Недоношенные и маловесные дети.
Вакцинация и ревакцинация детям, относящимся к группам риска, может осуществляться иммунобиологическими лекарственными препаратами для иммунопрофилактики инфекционных болезней, содержащими комбинации вакцин (например, Пентаксим), предназначенных для применения в соответствующие возрастные периоды (редакция приказа МЗ РФ N 175н от 13.04.2017г).
Дети, не входящие в группу риска, могут по желанию родителей привиться бесклеточными препаратами для вакцинации против коклюша, дифтерии и столбняка платно. Информацию в таком случае можно получить у участкового педиатра.
Могут быть и другие варианты вакцинации детей, что зависит от возможностей регионального бюджета.
В 2016 году в России зарегистрирована вакцина Адасель (Санофи, Франция), она также не содержит целую коклюшную палочку, а содержание дифтерийного и столбнячного анатоксинов в составе меньше, чем в других препаратах. Данная вакцина, в основном, предназначена для ревакцинации детей старше 4 лет и взрослых (после 14 лет можно каждые 10 лет), так как иммунитет против коклюша недлительный.
Для детей, кто не привит вовремя и имеет возраст старше 4 лет, по Национальному календарю прививаются только против дифтерии и столбняка (вакцинация АКДС препаратом проводится до 4 лет, препаратом Инфанрикс гекса до 36 мес), но по желанию родителей может быть выполнена вакцинация и препаратами Пентаксим и Инфанрикс, так как они не имеют возрастных ограничений.
Для вакцинации против полиомиелита также существуют изменения в Национальном календаре с 2014 года.
Если раньше для массовой вакцинации с 1958-59 годов использовали живую ослабленную вакцину Сэбина (она содержала 3 вакцинных штамма полиовируса), далее для предупреждения вакциноассоциированного полиомиелита у привитых и у контактных непривитых с 2014 года схема вакцинации изменилась:
-V1 и V2 все дети получают инактивированную вакцину в 3 мес. и в 4,5 мес.,
-V3 в 6 мес. и последующие ревакцинации в 1 г 6 мес., 1 г 8 мес. и в 14 лет получают оральной полиомиелитной вакциной ОПВ, причем с весны 2017 года ОПВ содержит только 2 штамма прививочных вирусов – I и III- БиВак полио (ФНЦИРИП им Чумакова, Россия).
Инактивированные вакцины, зарегистрированные в России:
- Имовакс Полио (Санофи, Франция) – применяется на сегодня в составе комбинированной вакцины Пентаксим,
- Полиорикс (ГлаксоСмитКляйн, Бельгия) – применяется на сегодня в составе комбинированной вакцины Инфанрикс гекса,
- Полимилекс (Нанолек, Россия) – применяется для проведения V1 и V2 против полиомиелита с весны 2017 г.
Дифтерия – это серьезная инфекция, которой болеют и взрослые, и дети. Причина инфекции – дифтерийная палочка, которая передается воздушно-капельным путем, иногда через общие игрушки, предметы быта. Дифтерия поражает нос, глотку, гортань, реже – кожу, глаза. У больного образуются пленки в зеве, которые могут распространиться в нос и гортань и перекрыть дыхание. У детей до года пленки сразу переходят на гортань, голосовые связки, появляется круп (отек гортани). В этих случаях требуются неотложные мероприятия, иначе человек задохнется. Кроме того, дифтерия чревата серьезными осложнениями – поражением сердца, почек, нервной системы. Избежать заболевания можно только при своевременной вакцинации. Вакцинация защищает от токсина, вырабатываемого бактерией дифтерии, который и вызывает все жизнеугрожающие состояния.
Привитые люди не болеют тяжелой опасной формой дифтерии. У них возможно развитие ангины, но жизни это не угрожает.
Столбняк (тетанус) – острая инфекция с поражением нервной системы, вызванное токсином, который выделяет столбнячная палочка, когда попадает в рану из земли. Столбняк протекает крайне тяжело и может развиться в любом возрасте. Токсин поражает нервную систему, при этом возникают мышечные спазмы и судороги. Смертность при столбняке достигает 90%. Иммунитет при вакцинации формируется против токсина, как и при дифтерии.
Коклюш – заболевание с особым поражением дыхательной системы, характеризуется приступообразным «спазматическим» кашлем. Ребенок «заходится» в кашле до рвоты, покраснения лица и появлением мелких кровоизлияний на лице, склерах глаз. Особенно приступы кашля беспокоят ночью и под утро Коклюш опасен осложнениями- воспалением легких, а у маленьких детей – смертью из-за апноэ – остановки дыхания, судорогами и поражением мозга из-за кислородного голодания
Полиомиелит – вызывается тремя типами полиомиелитных вирусов, передаётся с водой и пищей. От полиомиелита, как правило, не умирают, но может остаться паралич или парез, чаще одной ноги, при котором конечность постепенно худеет и укорачивается, а ребенок или тяжело хромает, или совсем не может двигаться без поддержки. Иногда развивается паралич дыхательных мышц и человек не может дышать без помощи специальных аппаратов.
Вакцины АКДС и инактивированная против полиомиелита вводятся внутримышечно в переднебоковую поверхность бедра.
План вакцинации.
Вакцинация АКДС и против полиомиелита начинается в 3 мес. После проведения вакцинации и ревакцинации АКДС (см ниже), согласно календарю прививок, проводятся ревакцинации взрослых каждые 10 лет (вакциной АДС-М).
Вакцинация детей согласно календарю прививок:
|
Возраст |
|
|
Первая вакцинация АКДС и Полимилекс |
3 месяца |
|
Вторая вакцинация АКДС и Полимилекс |
4,5 месяца |
|
Третья вакцинация АКДС и БиВак полио
Ревакцинация 2 Бивак полио
Ревакцинация 2 АДС-м
Ревакцинация 3 АДС-м и БиВак полио
|
6 месяцев
20 месяцев
7 лет
14 лет |
Побочные эффекты.
Вакцина АКДС вызывает умеренные побочные эффекты: небольшая лихорадка в первые сутки; умеренная болезненность, покраснение и припухание в месте инъекции может возникнуть при V 3 или R 1. Повышение температуры тела (как правило, не выше 37,5 С) и легкое недомогание также могут наблюдаться в течение 1-2 дней после прививки, редко (до 4 % может быть подъем t выше 38). При t выше 38,5 необходимо дать в домашних условиях жаропонижающие препараты по рекомендации врача парацетамол или ибупрофен. В случае повторного подъема t или недостаточного ответа на жаропонижающие препараты нужно вызвать педиатра или скорую помощь и объем необходимой терапии назначит врач. Обтирания водкой или спиртом не рекомендуется.
У детей, склонных к аллергическим реакциям, может быть сыпь, поэтому педиатр может назначить противоаллергические препараты до и после вакцинации.
Серьезные осложнения, вызванные АКДС – иммунизацией редки; они происходят меньше чем в одном проценте случаев. Это могут быть судороги на фоне высокой температуры, поэтому детей с возможной реакцией рекомендуется прививать на фоне жаропонижающих средств (парацетамол или ибупрофен).
Для того, чтобы уменьшить число побочных эффектов на цельноклеточную АКДС вакцину, её можно заменить комбинированным аналогом (вакцина Пентаксим, Инфанрикс), в которых цельноклеточный коклюшный компонент (до 3000 антигенов) заменен на бесклеточный вариант (2-3 антигена), который практически не вызывает побочных реакций. Кроме того, комбинированные вакцины значительно снижают инъекционную нагрузку, позволяют уменьшить суммарную дозу дополнительных веществ (стабилизаторы вакцин, консерванты).
После прививки коклюша иммунитет недолгосрочный и спустя 5-7 лет можно заболеть коклюшем. Для ревакцинации в 7 лет, 14 лет и далее ч/з 10 лет можно использовать вакцину Адасель. Единственное, привитые могут заболеть в более стертой форме – в диагнозе может звучать бронхит или пневмония, может не быть характерных приступов спазматического кашля, но для непривитых такой больной является источником инфекции.
Иммунолог объяснил, почему ревакцинация переносится тяжелее первой прививки
Ревакцинация от COVID-19 призвана усилить и продлить иммунный ответ на вирус. При этом реакция организма часто оказывается более сильной, чем при первой прививке. Об этом «Вечерней Москве» рассказал доктор медицинских наук, врач-иммунолог Владислав Жемчугов.
— При первичном знакомстве с микробом в организме формируется некоторое количество различных молекул, а главное, в нем остаются клетки памяти. При вторичном контакте клетки памяти вспоминают и формируют защитную реакцию уже гораздо быстрее. Например, при ревакцинации от столбняка после базовой прививки АКДС для этого достаточно одних суток, — объяснил он.
Специалист подчеркнул, что уберечься от вируса помогают не только антитела, но и другие компоненты. Иногда при большом количестве антител у человека бывает слабая реальная иммунная защита, отметил он.
По словам Жемчугова, при вторичном ответе реакция организма часто оказывается более сильной, чем при первичном. Вот почему в результате ревакцинации стоит ожидать повышения температуры и образования покраснений с большой вероятностью.
— Реакция организма и должна быть сильнее, этого стоит ждать. Говоря конкретно о векторных вакцинах, в которых есть носитель, стоит отметить: возникает иммунный ответ на носитель, то есть на аденовирус. Это один из возбудителей ОРВИ: человек мог болеть раньше, тогда у него уже есть память о носителе. С каждым последующим введением вакцина будет «гаситься» иммунным ответом именно на него, а не на коронавирусный материал, — пояснил Жемчугов.
Выходом из ситуации может стать решение повторно ревакцинироваться препаратом, в котором нет вектора (носителя) аденовируса (например, «КовиВак» или «ЭпиВакКорона»), посоветовал иммунолог.
Утром 1 июля мэр Москвы Сергей Собянин заявил о начале ревакцинации от коронавируса в Москве. Жители столицы смогут пройти ее в павильонах «Здоровая Москва». С 5 июля начнется запись на процедуру в 12 городских поликлиниках.
Поделиться в FBПоделиться в VKПоделиться в TWПоделиться в OKПоделиться в TG
Вакцина коклюшно-дифтерийно-столбнячная адсорбированная жидкая (АКДС-вакцина) — «Так ли страшна отечественная АКДС? Какая из 4-х прививок переносится хуже всего? Расскажу о наших трех прививках в 6, 7,5 и 10 месяцев, а так же о том, какие медикаменты надо иметь под рукой, и как избежать шишки на месте укола.»
Небольшое отступление от темы
В который раз убеждаюсь, что у Фатума специфическое чувство юмора. Перед очередной прививкой в моей жизни всплывали стародавние знакомые, случайные попутчики и совершенно незнакомые люди с воинствующей позицией в отношении прививок.
Они ловили меня в очередях, заговаривали в транспорте и на детских площадках. Разговор плавно подходил к теме вакцинации, и тут начинался жесткий прессинг. Информационный посыл был следующим: сами они, конечно же, детей не прививают, но вот их знакомые привили, и ребенок тут же заболел аутизмом.
По ощущениям в Воронежской области намечалась эпидемия аутизма, ибо количество детей знакомых знакомых с этим постпрививочным недугом всё увеличивалось.
Был и еще один довод в пользу отказа от вакцинации. Якобы, участковые педиатры имеют денежные премии от минздрава с каждого привитого. Глядя не землистое, усталое лицо нашего врача, с трудом верилось, что в ее карманах звенят «прививочные» капиталы.
До кучи я решила глянуть ролик Кураева (православный апологет с левыми взглядами) на тему прививок. Зря я это сделала. Кураев рассказал жуткую историю, как к нему приходила женщина, у которой умерло 2 ребенка. Первый был не привит и умер от болезни, которую давно победили вакцинацией, второго она решила привить и он умер от прививки.
Поняв, что ни сподвижники Божьи, ни интернет, ни знакомые не вносят в мой сумбур никакой конкретики, я с тяжелым сердцем пошла сдаваться (до этого у нас был медотвод из-за плохой НСГ).
Вакцина АКДС наводит ужас не только на впечатлительных мамаш, но и на бывалых педиатров. Ну может, и не ужас, но отношение к ней более трепетное, чем к другим вакцинам. А уж отечественная прививка — отдельная песня. Как сказал в одном интервью доктор Комаровский:
произведенную в России вакцину АКДС надо запретить!
В чем же отличие отечественной вакцины от импортного аналога?
Наша вакцина (АКДС) содержит убитый компонент коклюшной палочки. Именно он виновен в тяжелой переносимости этой прививки и ответственен за побочные эффекты.
В импортной вакцине (АаКДС) не содержится целой клетки возбудителя коклюша, а лишь некоторые ее фрагменты.
В частности, в популярной вакцине «Пентаксим» содержится всего один (из десятков, если не сотен) характерных для возбудителя белков — гемагглютинин, в «Инфанриксе» — всего два, гемагглютинин и пертактин.
Она переносится легче, но тут имеются иные подводные камни (если верить некоторым статьям):
Курс прививок новой безопасной вакциной, возможно, защитит от коклюша, но вряд ли эффективно предотвратит инфицирование, бактерионосительство и распространение палочки.
Считается, что мать, переболевшая в детстве коклюшем или привитая АКДС, передает своему ребенку антитела, которые будут защищать его в первые полгода жизни, когда это заболевание особенно опасно. А вот привитые АаКДС имеют нестойкий иммунитет, который к детородному возрасту утрачивается. Детям таких мам антитела не передаются.
Я не медик и не поручусь за правдивость информации (было бы интересно увидеть комментарии врачей относительно этой инфы), но на мой дилетантский взгляд логика тут есть.
И всё бы ничего, но родители, столкнувшиеся с вакцинацией в России в 2015-2016 годах знают, что импортные Инфарникс и Пентаксим исчезли из поликлиник, аптек и даже из платных центров по причине не пройденной сертификации.
В Воронеже я обзвонила все имеющиеся медицинские центры и посетила огромное количество аптек. Когда разум окончательно меня покинул, я стала прикидывать, можно ли заказать такую вакцину на Али))) Всё было тщетно, и на горизонте маячила лишь отечественная АКДС, интернетная репутация которой была ниже плинтуса.
Итак, если следовать графику, первая вакцина АКДС ставится в 3 ребенкиных месяца, но мы посетили прививочный кабинет в полгода. Рекомендуемый интервал между прививками от 45 до 90 дней.
Накануне дня Х я шерстила интернет, пытаясь узнать, какая же по счету прививка переносится хуже всего. Сразу скажу, не ждите никакой ясности ни от интернета, ни от врачей, ни от меня. Есть 2 противоположные точки зрения: каждая последующая прививка дает более тяжелую реакцию и наоборот. Невролог сказала, что самая страшная — это первая прививка, а педиатр, что четвертая (ревакцинация). Интернет говорит, что с каждой новой прививкой общая реакция организма (температура, слабость) уменьшается, но сильнее проявляется местная реакция (шишка в месте укола).
Мы не попали ни под какую категорию. Мне остается только развести руками и описать наш опыт.
Наш прививочный опыт:
На данный момент нам сделали 3 отечественные АКДС.
Перенесли мы их по-разному.
1. Первую прививку поставили в 6 месяцев, вернее, сразу две прививки: в одну ножку коклюшно-столбнячную, в другую — от полиомиелита. Сам процесс сопровождался ором, минут через 20 дочка задремала.
Первую прививку деть перенес вполне сносно. Повышение температуры было незначительным (37,2-37,4), капризность умеренная. Ширялись мы утром, и уже на следующий день не осталось никаких воспоминаний от похода к врачу, окромя шишечки на месте укола. Шишка была чуть больше горошины, но держалась довольно долго (около месяца). Муж вечерами ее массировал и мял, пребывая в уверенности, что способствует ее рассасыванию))
2. Вторую прививку делали через 45 дней — в 7,5 месяцев. Опять совмещали 2 прививки: от гепатита и АКДС.
Так как, по мнению педиатра, реакция на прививки должна идти по нарастающей, был дан совет поставить жаропонижающую свечу сразу по приходу домой. Сначала мне показалось странным сбивать температуру как бы заранее, но она успокоила, что свеча еще и болеутоляющая, а ребенок безусловно испытывает болезненные ощущения в ножке.
Еще врач посоветовала прикладывать к месту укола ватку, пропитанную магнезией (магния сульфат). Сделали компресс сразу же, как пришли домой, и на ночь (препарат наносится на ватный диск и крепится пластырем). Больше с проблемой шишек мы не сталкивались.
Второй раз ребенок отхватил все прелести общей реакции. Поле дневного сна у человека повысилась температура до 39 градусов. Сироп Эфералган оказался слабеньким и сбивал температуру лишь до 38,5. Свечи нурофен показали лучший результат, но они, собаки, довольно долго раскачиваются. Ситуацию усугубляла 40-градусная летняя жара и отсутствие кондиционера.
Мы набирали прохладную ванночку и вымачивали там детку, пока не спадет жар, а там уж и свечки начинали действовать.
Ночью температура так же держалась
Вообще, ребенкин жар переносится плохо не столько им самим, сколько родителями. Особенно после красочных статей антипрививочников об обязательных судорогах, реанимации и последующей инвалидности. На деле — это обычная, распространенная и даже желательная реакция организма, который борется с введенной заразой и формирует иммунитет.
К вечеру следующего дня состояние резко улучшилось, температура спала, капризы прекратились.
3. Ох, как же я не хотела делать третью прививку, ведь если прогнозы педиатра относительно реакций верны, ничего хорошего ждать не приходилось(( Вместе в АКДС была еще вакцина от полиомиелита. В этот раз не кололи, а капали препарат в рот.
Дома мы так же поставили заранее жаропонижающую свечу и стали ждать, затаив дыхание. Температуру я измеряла каждые полчаса, и если ребенок и был слегка капризен, то только от действий полоумной мамаши, не расстающейся с градусником.
Никаких реакций на вакцину в третий раз не последовало. Температура ни разу не повышалась, шишки не было, капризность особо не повысилась.
В сети встречается инфа что, якобы, каждая прививка отбрасывает развитие ребенка на несколько недель назад, и он забывает, всё чему научился. В нашем же случае дочь в день прививки самостоятельно пошла))) Да и ранее никаких скачков во времени замечено не было.
Кстати, слоняясь по обшарпанным коридорам детской поликлиники, я наткнулась на такой плакат:
Чтоб вы знали, взрослое население так же подлежит вакцинации, но на деле всё не так просто.
Готовясь к материнству (но еще не будучи беременной), я хотела привиться от краснухи, но в поликлинике мне в грубой форме сказали, что уже поздно. Беременеть или прививаться — не уточнили)) Ну да, на плакате указан возраст до 25-ти лет, а мне то уже было 30 на тот момент. Видимо, по мнению наших медиков, пора место на кладбище подыскивать, а не размножаться в столь мудром возрасте.
Зато когда меня покусал клещ, доктора меня любили, жалели и тут же вкатили прививочку от столбняка.
Какие лекарства надо иметь под рукой накануне вакцинации.
Сейчас врачи советуют проводить подготовку антигистаминными препаратами за 3 дня до прививки, и еще 3 дня после.
Обязательно иметь дома набор жаропонижающих свечей. Доктор Комаровский советует запастись двумя формами выпуска: свечи и сироп, и двумя действующими веществами: парацетамол и нурофен.
Имейте в виду, если вы вкатили сиропчик с парацетамолом и он не подействовал, то свечу с этим же веществом ставить нельзя — будет передозировка.
Нам больше всего помогали свечи нурофен, но на всю ночь их всё рано не хватает.
И еще одно.
Ребенок должен быть абсолютно здоров в день вакцинации. Педиатр безусловно проведет осмотр, но она может выявить уже начало болезни. И только мама знает, что утром ребеночек был квелый, что ночью он как-то ворочался, отказался от завтрака, пару раз кхекнул. Мама может заподозрить болезнь еще до начала видимых симптомов.
В этом случае не бойтесь сообщать о подобном врачу. Даже если вас поднимут на смех, даже если будут уговаривать привиться, настаивайте на своем и откладывайте вакцинацию.
У нас третья прививка стояла по плану на сентябрь. Но старшая дочь пошла в школу, начала покашливать и запустила в квартире вирусную карусель. Я сообщила об этом врачу, и она предложила пару недель понаблюдать.
Думаю, из отзыва видно, что ничего страшного в нашей жизни после вакцинации не произошло.
возможные осложнения и побочные эффекты после вакцины
Для начала рассмотрим заболевания, против которых направлена вакцина АКДС. Это даст возможность адекватно оценить необходимость вакцинации и поможет каждому родителю в принятии правильного решения.
Дифтерия
Дифтерия – это бактериальная инфекция, для которой характерны специфические изменения в ротоглотке и выраженный токсический синдром. Дифтерия передается воздушно-капельным путем (от больного или носителя при дыхании), реже контактным (с загрязненных предметов). Заражение наступает примерно на 2-10 день от момента контакта.
Для дифтерии характерны выраженные изменения в ротоглотке. Горло краснеет, затем покрывается плотной фибриновой пленкой, которая тяжело отделяется со слизистых оболочек, и иногда затрудняет дыхание. Дифтерия гортани сопровождается осиплостью и потерей голоса, затруднением дыхания, в некоторых случаях кровотечением.
Дифтерийная палочка – возбудитель инфекции, способна продуцировать токсин. Под его влиянием в организме развивается токсический синдром – отек верхних дыхательных путей, подкожно-жировой клетчатки. При этом у больных выраженно плохое самочувствие: высокая температура, затрудненное дыхание, головные боли. Кроме того, заболевание часто осложняется миокардитами и патологией нервной системы (энцефалит). Для лечения дифтерии применяют антибиотики, а также антитоксическую сыворотку или иммуноглобулин.
Дифтерия сейчас встречается редко. Она не очень «заразна». Но, заболевание это тяжелое, и в допрививочную эпоху именно оно стояло на первых местах, как причина детской смертности.
Коклюш
Коклюш – инфекционное заболевание, передающееся воздушно-капельным путем. Оно проявляется длительным, интенсивным, навязчивым кашлем. Инкубационный период у коклюша длится от 1-й до 2-х недель. После развития заболевания больной может являться источником инфекции до месяца. Кроме того, возможно бессимптомное носительство.
У детей до года инфекция коклюша часто приводит к приступам остановки дыхания. А на этом фоне развиваются осложнения со стороны нервной и сердечно-сосудистой системы. У детей старшего возраста, заболевание начинается с симптомов обычной простуды: повышения температуры, насморка, кашля, покраснения горла. Затем развивается длительный мучительный приступообразный кашель. Приступы иногда сопровождаются рвотой, кровоизлияниями в кожу лица и конъюнктиву, слюно и слезотечением, вздутием вен шеи. Длится такой кашель может до полугода.
Для лечения коклюша используют антибактериальные препараты. Однако, они могут быть эффективны только в начальный период, когда коклюш практически невозможно отличить от других ОРВИ. В период приступообразного кашля антибиотикотерапия не эффективна. Лечение проводится симптоматически и практически не может повлиять на длительность кашля.
Коклюш чрезвычайно заразен. Им заболевают до 95% контактировавших не привитых. Даже сейчас, на фоне всеобщей вакцинации, случаи коклюша нередки. Особенно опасно заболевание у малышей, еще не успевших получить прививку по какой-то причине.
Столбняк
Столбняк – тяжелая бактериальная инфекция с контактным механизмом передачи, для которой характерно поражение нервной системы с развитием судорог и тонического напряжения мышц. Инфекция передается контактным путем. Микроб широко распространён в природе, особенно в сельскохозяйственных районах. Его находят в почве, воде, домашней пыли. Часто он является обитателем кишечника животных, иногда человека. Столбнячная палочка может образовывать споры, которые устойчивы к воздействию высоких и низких температур, растворов антисептиков.
Свои патогенные свойства столбнячная палочка приобретает в отсутствии кислорода (анаэробной среде). Попадая в рану с загрязненных поверхностей, микроб начинает размножаться и выделять токсин. Токсин через кровь попадает в нервную систему. Развивается клиническая картина. От заражения до первых симптомов проходит примерно от 1-й до 3-х недель. Вначале поражаются мышцы лица и головы – происходит резкий спазм мускулатуры. Затем изменения переходят на туловище и конечности, появляются судороги. Мышечные сокращения могут быть настолько интенсивными, что травмируют суставы и связки. Нередки поражения мышц сердца и дыхательных путей.
В современных условиях пациент погибает от столбняка примерно в 20% случаев. Особенно опасна инфекция у детей первого года жизни. Летальность достигает 90-95%. Своевременное лечение позволяет снизить летальность и уменьшит проявления болезни. Однако, даже при его применении выздоровление наступает только после 2-4 месяцев, некоторые последствия остаются необратимые для нервной системы.
Столбняк очень опасная инфекция. До сих пор встретить споры столбнячной палочки в природе не редкость.
Какие бывают прививки от коклюша, дифтерии и столбняка?
- АКДС – в нашей стране применяется наиболее широко писпользуемая вакцина. В нее входит анатоксин (нейтрализованный токсин) столбняка и дифтерии, а также убитые коклюшные бактерии. Помимо основных компонентов в состав вакцины входят адъюванты, антисептики и консерванты, а также основная среда – разбавитель.
- АДС и АДС-М – вакцина без коклюшного компонента. В вакцине АДС-М снижено количество дифтерийного анатоксина. Эти вакцины применяют для ревакцинации у детей после 7-ми лет и у взрослых, когда вакцинация от коклюша уже не показана.
- «Бубо-Кок» – в эту вакцину помимо компонентов АКДС входит часть белка вирусного гепатита В. Это сделано для того, чтобы не делать одновременно малышу два укола, т.к. прививки по календарю делаются вместе.
- «Бубо-М» – вакцина без коклюшного компонента.
- «Пентаксим» – в состав входит столбнячный, дифтерийный и коклюшный анатоксины, частички коклюшного микроба. Дополнительно, для удобства использования в эту вакцину ввели полиомиелит. По календарю прививок графики вакцинации АКДС и полиомиелитом совпадают. В эту вакцину из отдельного флакона можно добавить компонент против гемофильной инфекции. Решение о необходимости его введения принимает врач. Вакцина отличается отсутствием целых коклюшных клеток – это вызывает меньше побочных эффектов.
- «Инфанрикс» – по составу идентичен «Пентаксиму», за исключением полиомиелитного компонента – в нем он отсутствует.
- «Инфанрикс гекса» – помимо компонентов «Инфанрикса» включает инактивированные вирусы полиомиелита и часть белка вируса гепатита В.
- «Адасель» – включает в себя: дифтерийный, столбнячный, коклюшный анатоксины и фрагменты коклюшной бактерии.
Когда делают прививку АКДС?
Согласно национальному календарю прививка АКДС делается в 3 месяца, 4,5 месяца и 6 месяцев. Ревакцинацию делают в 18 месяцев. Вторая ревакцинация в 6-7 лет проводится без коклюшного компонента. Третья – в 14 лет, а затем каждые 10 лет – также без добавления коклюшного компонента.
Как быть, если прививка АКДС не была сделана вовремя?
Если прививки не доделаны, календарь продолжают с теми же промежутками, которые указаны в календаре. Вторую вакцину делают не менее чем, через 1,5 месяца от первой. Третью не менее чем через 1,5 месяца от второй. Ревакцинация не менее, чем через 12 месяцев от последней прививки.
Прививку АКДС делают до 4-х лет. После 4-х делают АаКДС (в этом случае интервал между третьей прививкой и ревакцинацией может быть сокращен до 6 месяцев).
«Инфанрикс гекса», согласно инструкции, делается только до 36 месяцев.
«Инфанрикс» и «Пентаксим» можно делать до 6 лет.
«Адасель» используют только для ревакцинации в 6-7 лет и для прививки взрослым каждые 10 лет.
Дети старше 6 лет прививаются только безкоклюшными вакцинами (АДС, АДС-М, Бубо-М) или вакциной «Адасель». Им делается две прививки с разницей в 1,5 – 2 месяца. Ревакцинация через 9-12 месяцев. И вторая ревакцинация через 2 года.
Какие осложнения могут быть после прививки АКДС?
АКДС одна из наиболее реактогенных прививок в календаре. Стоит ли ее бояться и отказываться от нее?
Действительно, после введения АКДС часто встречаются побочные реакции:
- Повышение температуры тела до 38,5*С встречается примерно в половине случаев после инъекции прививки АКДС. При применении бесклеточных вакцин («Превенар», «Инфанрикс» или «Адасель») встречается примерно в 2-3 раза реже. Реже встречается повышение температуры до 39*С (примерно в 10% случаев). Крайне редко – до 40*С (менее 0,5% всех привитых). Такое повышение температуры проходит через 1-3 дня после прививки самостоятельно и требует только применения жаропонижающего препарата в возрастной дозе для улучшения самочувствия ребенка.
- Раздражительность и продолжительный плач. Тоже довольно частое явление. Для АКДС примерно 40% от всех вакцинаций. Для бесклеточных вакцин этот процент падает примерно до 15%. Проходит самостоятельно за 1-2 дня. Требует только наблюдения и ухода за малышом.
- Местные реакции в виде отека, покраснения и боли в месте инъекции встречаются с разной интенсивностью примерно у половины привитых. В разы реже местные реакции наблюдаются у привитых бесклеточной вакциной. Болезненность в первые дни после прививки можно уменьшит с помощью тех же лекарств, которыми сбивают высокую температуру. В случае, если краснота, отек и болезненность нарастают, а препараты оказываются малоэффективными малыша имеет смысл показать врачу, чтобы не упустить осложнения связанные с инфицированием места введения, либо нарушением техники введения препарата.
- Иногда несколько дней после прививки малыша беспокоит нарушение аппетита и как следствие потеря веса. Это явление временное, не требующее коррекции.
- Рвота встречается примерно у 15 % привитых детей. Никогда не бывает мучительной, многократной и длительной. Не требует лечения. Но вашего лечащего врача о такой реакции стоит оповестить.
- Редко (примерно 0,02% для АКДС и еще ниже для бесклеточных вакцин) у детей после прививки встречаются фебрильные судороги. Такие судороги происходят на высоте подъема температуры. Чаще дети имеют врожденную предрасположенность к развитию таких судорог. Прививка в таких ситуациях служит лишь провоцирующим фактором. В большинстве случаев фебрильные судороги не опасны для малыша, несмотря на то что они очень пугают родителей. Ребенка после судорожного приступа нужно обязательно показать врачу. И предупредить лечащего врача о предыдущих случаях такой побочной реакции.
К тяжелым и редко встречающимся осложнениям после прививки можно отнести:
- Острые аллергические реакции. Сразу после прививки маме с малышом рекомендуют провести около получаса в стенах медицинского учреждения.
- Гипотензивно-гипореспонсивный синдром. Его риск имеется примерно первые 12 часов после прививки. Ребенок резко бледнеет, становится вялый, заторможенный. Это осложнение не требует лечения, проходит само, но при нем необходимо наблюдение врача. Гипотензивно-гипореспонсивный синдром после прививки АКДС ставит вопрос о дальнейшей вакцинации.
Чтобы уменьшить риск тяжелых побочных реакций рекомендуют осмотр перед вакцинацией. Ребенок перед прививкой не должен быть болен острой респираторной инфекцией. Хронические заболевания должны быть в стадии ремиссии. При необходимости лечащий врач может назначить ребенку с хроническим заболеванием лечение на время вакцинации.
Надо сказать, что последующая прививка переносится тяжелее предыдущей. У детей с выраженными реакциями вакцину целесообразно заменить на бесклеточную или не содержащую коклюшный компонент.
Когда прививку АКДС делать нельзя?
- Если у ребенка обострение хронического заболевания прививки откладываются до разрешения лечащего врача.
- Если у ребенка есть аллергическая реакция на компоненты препарата, или была острая аллергическая реакция на предыдущее введение.
- Если у ребенка есть тяжелое прогрессирующее заболевание нервной системы.
С осторожностью делают прививки малышу, если после предыдущего введения у него:
- поднялась температура выше 40,5*С;
- были судороги после предыдущего введения препарата;
- возникновение гипотензивно-гипореспонсивный синдрома после предыдущей вакцины.
Стратегии вакцинации против копандемии Mtb / ВИЧ
Spertini, F. et al. Безопасность иммунизации человека живой аттенуированной вакциной против Mycobacterium tuberculosis: рандомизированное двойное слепое контролируемое исследование фазы I. Ланцет Респир. Med. 3 , 953–962 (2015).
CAS PubMed Статья PubMed Central Google Scholar
Harding, E. Доклад ВОЗ о глобальном прогрессе в области элиминации туберкулеза. Ланцет Респир. Med. 8 , 19 (2020).
PubMed Статья PubMed Central Google Scholar
Краситель, C. Более широкое использование наиболее широко применяемой в мире вакцины: пересмотр вакцинации от бациллы Кальметта-Герена. J. R. Soc. Интерфейс 10 , 20130365 (2013).
PubMed PubMed Central Статья Google Scholar
Блэк, Г. Ф. и др. БЦЖ-индуцированное усиление интерферон-гамма-ответа на микобактериальные антигены и эффективность вакцинации БЦЖ в Малави и Великобритании: два рандомизированных контролируемых исследования. Ланцет 359 , 1393–1401 (2002).
PubMed Статья PubMed Central Google Scholar
Lalor, M. K. et al. Популяционные различия в иммунных ответах на вакцинацию бациллой Кальметта-Герена в младенчестве. J. Infect. Дис. 199 , 795–800 (2009).
CAS PubMed PubMed Central Статья Google Scholar
Lalor, M. K. et al. Вакцинация БЦЖ индуцирует различные профили цитокинов после вакцинации младенцев БЦЖ в Великобритании и Малави. J. Infect. Дис. 204 , 1075–1085 (2011).
CAS PubMed PubMed Central Статья Google Scholar
Zhang, L. et al. Переменная вирулентность и эффективность вакцинных штаммов БЦЖ у мышей и корреляция с полиморфизмом генома. Мол. Ther. 24 , 398–405 (2016).
PubMed PubMed Central Статья CAS Google Scholar
Ким, Б. Дж., Ким, Б. Р., Кук, Ю. Х. и Ким, Б. Дж. Возможности рекомбинантных Mycobacterium paragordonae, экспрессирующих Gag ВИЧ-1, в качестве основной вакцины против инфекции ВИЧ-1. Sci. Отчетность 9 , 15515 (2019).
PubMed PubMed Central Статья CAS Google Scholar
Kilpelainen, A. et al. Рекомбинантная БЦЖ, экспрессирующая первичный HTI и рекомбинантный бустер ChAdOx1, безопасна и вызывает ВИЧ-1-специфические Т-клеточные ответы у мышей BALB / c. Vaccines 7 , https://doi.org/10.3390/vaccines7030078 (2019).
Ким, Б. Дж., Ким, Б.Р., Кук, Ю. Х. и Ким, Б. Дж. Разработка живой рекомбинантной БЦЖ, экспрессирующей Gag вируса иммунодефицита человека типа 1 (ВИЧ-1), с использованием векторной системы pMyong2: потенциальное использование в качестве новой вакцины против ВИЧ-1. Front Immunol. 9 , 643 (2018).
PubMed PubMed Central Статья CAS Google Scholar
Кориот-Шмитц, Б. и др. Резус-иммунные ответы на Gag SIV, экспрессируемые рекомбинантными векторами БЦЖ, не зависят от ранее существовавшего микобактериального иммунитета. Вакцина 33 , 5715–5722 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Сиксмит, Дж. Д. и др. Рекомбинантные векторы бактерий Mycobacterium bovis bacillus Кальметта-Герена являются первичными для сильных клеточных реакций на рвотную реакцию вируса иммунодефицита обезьян у макак-резусов. Clin. Вакцин. Иммунол. 21 , 1385–1395 (2014).
Артикул CAS Google Scholar
Martins, M.A. et al. Вакцинация фрагментами генов Gag, Vif и Nef обеспечивает частичный контроль репликации вируса после заражения слизистой оболочкой SIVmac239. J. Virol. 88 , 7493–7516 (2014).
PubMed PubMed Central Статья CAS Google Scholar
Альдовини А. и Янг Р. А. Гуморальные и клеточно-опосредованные иммунные ответы на живые рекомбинантные вакцины БЦЖ-ВИЧ. Nature 351 , 479–482 (1991).
CAS PubMed Статья PubMed Central Google Scholar
Venkataswamy, M. M. et al. Улучшение Mycobacterium bovis bacillus Calmette-Guerin в качестве вектора доставки вакцины для вирусных антигенов путем включения гликолипидных активаторов NKT-клеток. PLoS ONE 9 , e108383 (2014).
PubMed PubMed Central Статья CAS Google Scholar
Tameris, M. et al. Живая аттенуированная вакцина против Mycobacterium tuberculosis MTBVAC по сравнению с БЦЖ у взрослых и новорожденных: рандомизированное контролируемое двойное слепое исследование с увеличением дозы. Ланцет Респир. Мед 7 , 757–770 (2019).
CAS PubMed Статья PubMed Central Google Scholar
Suliman, S. et al. Ревакцинация взрослых с латентной инфекцией Mycobacterium tuberculosis Bacillus Calmette-Guerin (BCG) вызывает долгоживущие БЦЖ-реактивные ответы NK-клеток. J. Immunol. 197 , 1100–1110 (2016).
CAS PubMed PubMed Central Статья Google Scholar
Nemes, E. et al. Профилактика инфекции M. tuberculosis с помощью вакцины h5: IC31 или ревакцинации БЦЖ. N. Engl. J. Med 379 , 138–149 (2018).
CAS PubMed PubMed Central Статья Google Scholar
Suliman, S. et al. Оптимизация дозы вакцины H56: IC31 для эндемичных по туберкулезу групп населения. Двойное слепое плацебо-контролируемое испытание по выбору дозы. г. J. Respir. Крит. Care Med 199 , 220–231 (2019).
CAS PubMed Статья PubMed Central Google Scholar
Broset, E. et al. Вакцина против ТБ-ВИЧ на основе MTBVAC безопасна, вызывает реакцию Т-лимфоцитов и защищает мышей от Mycobacterium tuberculosis. Мол. Ther. 13 , 253–264 (2019).
CAS Google Scholar
Chege, G.K. et al. Устойчивый иммунитет к ауксотрофной кандидатной вакцине против ВИЧ от Mycobacterium bovis BCG-VLP на нечеловеческой модели приматов. J. Virol. 87 , 5151–5160 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Чеге, Г. К. и др. Схема первичной иммунизации с использованием рекомбинантных вакцин BCG и вирусоподобных частиц Pr55 (gag) на основе подтипа C ВИЧ 1 типа успешно вызывает Gag-специфические ответы у павианов. Vaccine 27 , 4857–4866 (2009).
CAS PubMed Статья Google Scholar
Falk, L.A. et al. Рекомбинантная палочка Кальметта-Герена как потенциальный вектор для профилактических вакцин против ВИЧ 1 типа. AIDS Res Hum. Ретровирусы 6 , 91–98 (2000).
Артикул Google Scholar
Honda, M. et al. Защитные иммунные ответы, индуцированные секрецией химерного растворимого белка из рекомбинантной вакцины-кандидата вектора Mycobacterium bovis bacillus Calmette-Guerin против вируса иммунодефицита человека типа 1 у мелких животных. Proc. Natl Acad. Sci. США 92 , 10693–10697 (1995).
CAS PubMed Статья Google Scholar
Kaushal, D. et al. Вакцинация слизистой оболочки ослабленной Mycobacterium tuberculosis вызывает сильные реакции центральной памяти и защищает от туберкулеза. Nat. Commun. 6 , 8533 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Бригадир Т.W. et al. Непатологическое инфицирование макак ослабленной микобактериальной вакциной не активируется в условиях коинфекции ВИЧ. г. J. Pathol. 187 , 2811–2820 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Darrah, P. A. et al. Профилактика туберкулеза у макак после внутривенной иммунизации БЦЖ. Природа 577 , 95–102 (2020).
CAS PubMed PubMed Central Статья Google Scholar
Картрайт, Э. К. и др. Начало антиретровирусной терапии восстанавливает гомеостаз CD4 + T стволовых клеток памяти у макак, инфицированных вирусом иммунодефицита обезьян. J. Virol. 90 , 6699–6708 (2016).
CAS PubMed PubMed Central Статья Google Scholar
Nowak, P. et al. Разнообразие кишечной микробиоты позволяет прогнозировать иммунный статус при инфекции ВИЧ-1. AIDS 29 , 2409–2418 (2015).
CAS PubMed Статья Google Scholar
Singh, S. K. et al. ВИЧ препятствует представлению антигена Mycobacterium tuberculosis в дендритных клетках человека. г. J. Pathol. 186 , 3083–3093 (2016).
CAS PubMed Статья Google Scholar
Manosuthi, W., Kiertiburanakul, S., Phoorisri, T. & Sungkanuparph, S. Воспалительный синдром восстановления иммунитета при туберкулезе у ВИЧ-инфицированных пациентов, получающих противотуберкулезную и антиретровирусную терапию. J. Infect. 53 , 357–363 (2006).
PubMed Статья Google Scholar
Лаун, С. Д., Майер, Л., Беккер, Л. Г. и Вуд, Р. Бремя туберкулеза в программе антиретровирусного лечения в странах Африки к югу от Сахары: влияние на результаты лечения и последствия для борьбы с туберкулезом. AIDS 20 , 1605–1612 (2006).
PubMed Статья Google Scholar
Уилсон, Дж. У., Нильсен, Д. М. и Маркс, С. М. Туберкулез с множественной лекарственной устойчивостью у пациентов с вирусом иммунодефицита человека. Соображения по поводу управления в условиях высоких ресурсов. Ann. Являюсь. Грудной. Soc. 17 , 16–23 (2020).
PubMed Статья Google Scholar
Ganatra, S.R. et al. Антиретровирусная терапия не снижает реактивацию туберкулеза в модели сочетанной инфекции туберкулеза и ВИЧ. J. Clin. Вкладывать деньги. , https://doi.org/10.1172/jci136502 (2020).
Bucşan, A. N. et al. Механизмы реактивации латентной туберкулезной инфекции вследствие коинфекции SIV. J. Clin. Вкладывать деньги. 129 , 5254–5260 (2019).
PubMed PubMed Central Статья Google Scholar
Nemes, E., Scriba, T. J. и Hatherill, M. Перспективы вакцины для профилактики туберкулеза, связанного с ВИЧ. Curr. Opin. ВИЧ СПИД 13 , 522–527 (2018).
CAS PubMed Статья Google Scholar
Nusbaum, R.J. et al. Туберкулез легких у гуманизированных мышей, инфицированных ВИЧ-1. Sci. Отчет 6 , 21522 (2016).
CAS PubMed PubMed Central Статья Google Scholar
Чакраварти, С. Д. и др. Блокада фактора некроза опухоли при хроническом туберкулезе мышей усиливает гранулематозное воспаление и дезорганизует гранулемы в легких. Заражение. Иммун. 76 , 916–926 (2008).
CAS PubMed PubMed Central Статья Google Scholar
Арриага, А. К., Ороско, Э. Х., Агилар, Л. Д., Рук, Г. А. и Эрнандес Пандо, Р. Иммунологический и патологический сравнительный анализ экспериментальной латентной туберкулезной инфекции и прогрессирующего туберкулеза легких. Clin. Exp. Иммунол. 128 , 229–237 (2002).
CAS PubMed PubMed Central Статья Google Scholar
Датта, Н. К., Иллей, П. Б., Джайн, С. К. и Каракусис, П. С. Характеристика новой модели некротической гранулемы латентной туберкулезной инфекции и реактивации у мышей. г. J. Pathol. 184 , 2045–2055 (2014).
CAS PubMed PubMed Central Статья Google Scholar
Gonzalo-Asensio, J., Marinova, D., Martin, C. & Aguilo, N. MTBVAC: ослабление возбудителя туберкулеза (ТБ) человека на пути к многообещающей вакцине против эпидемии ТБ. Front Immunol. 8 , 1803 (2017).
PubMed PubMed Central Статья CAS Google Scholar
Aguilo, N. et al. Вакцина MTBVAC безопасна, иммуногенна и обеспечивает защитную эффективность против Mycobacterium tuberculosis у новорожденных мышей. Туберкулез (Ред.) 96 , 71–74 (2016).
CAS Статья Google Scholar
Kilpelainen, A. et al. Праймирование рекомбинантной БЦЖ, экспрессирующей новые консервативные мозаичные иммуногены ВИЧ-1, и усиление рекомбинантным ChAdOx1 является безопасным, стабильным и вызывает ВИЧ-1-специфические Т-клеточные ответы у мышей BALB / c. Front Immunol. 10 , 923 (2019).
CAS PubMed PubMed Central Статья Google Scholar
Мюррей, П. Дж., Альдовини, А. и Янг, Р. А. Манипуляция и усиление противомикобактериального иммунитета с использованием штаммов рекомбинантных бацилл Кальметта-Герена, которые секретируют цитокины. Proc. Natl Acad. Sci. США 93 , 934–939 (1996).
CAS PubMed Статья PubMed Central Google Scholar
Grode, L. et al. Повышение эффективности вакцины против туберкулеза рекомбинантной бациллы Mycobacterium bovis с мутантами Кальметта-Герена, секретирующими листериолизин. J. Clin. Вкладывать деньги. 115 , 2472–2479 (2005).
CAS PubMed PubMed Central Статья Google Scholar
Dey, R.J., Dey, B., Singh, A.K., Praharaj, M. & Bishai, W. Bacillus Calmette-Guérin, сверхэкспрессирующая эндогенный стимулятор агониста генов интерферона, обеспечивает усиленную защиту от туберкулеза легких. J. Infect. Дис. 221 , 1048–1056 (2020).
CAS PubMed PubMed Central Google Scholar
Calderon, V. E. et al. Гуманизированная модель туберкулеза на мышах. PLoS ONE 8 , e63331 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Perdomo-Celis, F. et al. Хроническая, острая и реактивированная ВИЧ-инфекция на моделях гуманизированных иммунодефицитных мышей. J. Vis. Exp. 154 , https://doi.org/10.3791/60315 (2019).
Fan, T. J. et al. Создание модели инфекции ВИЧ-1 in vivo у гуманизированных мышей B-NSG. Virol. Грех. 4 , 417–425 (2019).
Google Scholar
Ши, С., Ши, Дж. И Сюй, З. Обзор мышиных моделей латентной туберкулезной инфекции. Сканд. J. Infect. Дис. 43 , 848–856 (2011).
CAS PubMed Статья PubMed Central Google Scholar
Murawski, A. M. et al. Визуализация эволюции реактивации туберкулеза легких у мышей с использованием 18F-FDG PET. J. Nucl. Med. 55 , 1726–1729 (2014).
CAS PubMed PubMed Central Статья Google Scholar
Клинкенберг, Л. Г., Сазерленд, Л.A., Bishai, W. R. & Karakousis, P. C. Метронидазол не обладает активностью против Mycobacterium tuberculosis в латентной модели гипоксической гранулемы in vivo. J. Infect. Дис. 198 , 275–283 (2008).
CAS PubMed PubMed Central Статья Google Scholar
Линч, Р. М., Ямамото, Т. и МакДермотт, А. Б. Исследование и открытие вакцины против ВИЧ на модели нечеловеческих приматов: единая теория профилактики заражения и борьбы с инфекцией ВИП. Curr. Opin. ВИЧ СПИД 8 , 288–294 (2013).
CAS PubMed PubMed Central Google Scholar
Форман, Т. В., Мехра, С., Лакнер, А. А. и Каушал, Д. Трансляционные исследования на нечеловеческой модели туберкулеза приматов. ILAR J. 58 , 151–159 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Каушал, Д., Мехра, С., Дидье, П. Дж. И Лакнер, А. А. Модель туберкулеза приматов, не относящихся к человеку. J. Med Primatol. 41 , 191–201 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Рахман М. А., Роберт-Гурофф М. и Акселератинг, Х. И. В. Разработка вакцины с использованием моделей приматов, не относящихся к человеку. Expert Rev. Vaccines 18 , 61–73 (2019).
PubMed Статья CAS PubMed Central Google Scholar
Laddy, D. J. et al. К разработке вакцины против туберкулеза: рекомендации по дизайну исследования на нечеловеческих приматах. Заражение. Иммун. 86 , https://doi.org/10.1128/iai.00776-17 (2018).
Стапранс, С. И. и Файнберг, М. Б. Роли нечеловеческих приматов в доклинической оценке кандидатных вакцин против СПИДа. Expert Rev. Vaccines 3 , S5 – S32 (2004).
PubMed Статья PubMed Central Google Scholar
Rivera-Hernandez, T. et al. Вклад моделей приматов, не относящихся к человеку, в разработку вакцин для человека. Дискотека. Med. 18 , 313–322 (2014).
Google Scholar
Jensen, K. et al. Рекомбинантный аттенуированный вакцинный штамм Mycobacterium tuberculosis безопасен для детенышей макак, инфицированных вирусом обезьяньего иммунодефицита. Clin. Вакцин. Иммунол. 19 , 1170–1181 (2012).
CAS Статья Google Scholar
Larsen, M.H. et al. Эффективность и безопасность живых аттенуированных персистентных и быстро очищаемых вакцин против Mycobacterium tuberculosis для приматов, кроме человека. Vaccine 27 , 4709–4717 (2009).
CAS PubMed PubMed Central Статья Google Scholar
Jensen, K. et al. Уравновешивание тренированного иммунитета со стойкой иммунной активацией и риском заражения вирусом обезьяньего иммунодефицита у детенышей макак, вакцинированных аттенуированной вакциной Mycobacterium tuberculosis или Mycobacterium bovis BCG. Clin Vaccine Immunol 24 , https://doi.org/10.1128/cvi.00360-16 (2017).
White, A. D. et al. Оценка безопасности и иммуногенности кандидатной противотуберкулезной вакцины MVA85A, доставляемой аэрозолем в легкие макак. Clin. Вакцин. Иммунол. 20 , 663–672 (2013).
CAS Статья Google Scholar
Verreck, F. A. et al. Усиление вакцины BCG MVA.85A и аттенуированная вакцина против M. tuberculosis с дефицитом фосфора демонстрируют защитную эффективность против туберкулеза у макак-резусов. PLoS ONE 4 , e5264 (2009 г.).
PubMed PubMed Central Статья CAS Google Scholar
World Health, вакцина О. БЦЖ: позиционный документ ВОЗ, февраль 2018 г. — Рекомендации. Vaccine 36 , 3408–3410 (2018).
Артикул Google Scholar
Dijkman, K. et al. Профилактика туберкулезной инфекции и заболевания с помощью местной БЦЖ у многократно контактировавших с макаками-резусами. Nat. Med. 25 , 255–262 (2019).
CAS PubMed Статья PubMed Central Google Scholar
Биллесков Р. и др. Тестирование вакцины H56, введенной в 4 различных адъювантах в качестве бустера БЦЖ, на модели туберкулеза на нечеловеческих приматах. PLoS ONE 11 , e0161217 (2016).
PubMed PubMed Central Статья CAS Google Scholar
Lindenstrom, T. et al. Субъединичная вакцинация против туберкулеза обеспечивает долгосрочный защитный иммунитет, характеризующийся многофункциональными Т-клетками памяти CD4. J. Immunol. 182 , 8047–8055 (2009).
CAS PubMed Статья PubMed Central Google Scholar
Aagaard, C. et al. Защита и полифункциональные Т-клетки, индуцированные Ag85B-TB10.4 / IC31 против Mycobacterium tuberculosis, сильно зависят от дозы антигена. PLoS ONE 4 , e5930 (2009 г.).
PubMed PubMed Central Статья CAS Google Scholar
Седер, Р. А., Дарра, П. А. и Родерер, М. Качество Т-клеток в памяти и защите: значение для разработки вакцины. Nat. Rev. Immunol. 8 , 247–258 (2008).
CAS PubMed Статья PubMed Central Google Scholar
Колер Р. Н. и др. Терапевтическая иммунизация против Mycobacterium tuberculosis является эффективным дополнением к лечению антибиотиками. J. Infect. Дис. 207 , 1242–1252 (2013).
CAS PubMed Статья PubMed Central Google Scholar
Bertholet, S. et al. Определенный кандидат против туберкулезной вакцины усиливает БЦЖ и защищает от микобактерий туберкулеза с множественной лекарственной устойчивостью. Sci. Пер. Med. 2 , 53ра74 (2010).
PubMed PubMed Central Статья CAS Google Scholar
Vingert, B. et al. Контроллеры ВИЧ поддерживают популяцию высокоэффективных эффекторных клеток Th2 в отличие от пациентов, получающих лечение в течение длительного времени. J. Virol. 86 , 10661–10674 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Clerici, M. & Shearer, G.M. Переключение Th2–> Th3 является критическим этапом в этиологии ВИЧ-инфекции. Immunol. Сегодня 14 , 107–111 (1993).
CAS PubMed Статья PubMed Central Google Scholar
Hoft, D. F. et al. Безопасность и иммуногенность рекомбинантной вакцины БЦЖ AERAS-422 у здоровых взрослых, не получавших БЦЖ: рандомизированное, активно контролируемое, первое исследование фазы 1 с участием людей. EBioMedicine 7 , 278–286 (2016).
PubMed PubMed Central Статья Google Scholar
Velmurugan, K. et al. Доклиническая разработка кандидатов на замену вакцины БЦЖ. Вакцины 1 , 120–138 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Jambo, K. C. et al. Бронхоальвеолярные CD4 + Т-клеточные ответы на респираторные антигены нарушены у ВИЧ-инфицированных взрослых. Грудь 66 , 375–382 (2011).
PubMed PubMed Central Статья Google Scholar
Kalsdorf, B. et al. Инфекция ВИЧ-1 нарушает ответ бронхоальвеолярных Т-клеток на микобактерии. г. J. Respir. Крит. Care Med. 180 , 1262–1270 (2009).
CAS PubMed PubMed Central Статья Google Scholar
Murray, L. W. et al. Инфекция вируса иммунодефицита человека нарушает Th2 и Th27 Mycobacterium tuberculosis-специфические Т-клеточные ответы. J. Infect. Дис. 217 , 1782–1792 (2018).
CAS PubMed PubMed Central Статья Google Scholar
Amelio, P. et al. ВИЧ-инфекция функционально нарушает специфические для Mycobacterium tuberculosis ответы CD4 и CD8 Т-клеток. J. Virol. 93 , https://doi.org/10.1128/jvi.01728-18 (2019).
Day, C. L. et al. Инфекция ВИЧ-1 связана с истощением и функциональным нарушением Т-лимфоцитов CD4, специфичных для Mycobacterium tuberculosis, у лиц с латентной туберкулезной инфекцией. J. Immunol. 199 , 2069–2080 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Foreman, T. W. et al. CD4 + Т-клеточные независимые механизмы подавляют реактивацию латентного туберкулеза на модели коинфекции ВИЧ на макаках. Proc. Natl Acad. Sci. США 113 , E5636 – E5644 (2016).
CAS PubMed Статья PubMed Central Google Scholar
Форд, Н., Витория, М. и Доэрти, М. Обеспечение антиретровирусной терапии для всех, кто инфицирован ВИЧ: клинические, общественные и программные преимущества лечения всех. J. Int. AIDS Soc. 21 , https://doi.org/10.1002/jia2.25078 (2018).
Джонс, Дж. Л., Хэнсон, Д. Л., Дворкин, М. С. и Декок, К. М. ВИЧ-ассоциированный туберкулез в эпоху высокоактивной антиретровирусной терапии. Спектр ВИЧ-инфицированных взрослых / подростков. Внутр.J. Tuberc. Lung Dis. 4 , 1026–1031 (2000).
CAS PubMed PubMed Central Google Scholar
Golub, J. E. et al. Влияние антиретровирусной терапии и профилактической терапии изониазидом на заболеваемость туберкулезом у ВИЧ-инфицированных пациентов в Рио-де-Жанейро, Бразилия. AIDS 21 , 1441–1448 (2007).
PubMed PubMed Central Статья Google Scholar
Scriba, T. J. et al. Испытание фазы IIa новой противотуберкулезной вакцины MVA85A у взрослых, инфицированных ВИЧ и / или Mycobacterium tuberculosis. г. J. Respir. Крит. Care Med. 185 , 769–778 (2012).
CAS PubMed PubMed Central Статья Google Scholar
Черчъярд, Г. Дж. И др. Безопасность и иммуногенность вакцины против туберкулеза с 35 вектором аденовируса у ВИЧ-инфицированных, вакцинированных БЦЖ взрослых с количеством CD4 (+) Т-клеток> 350 клеток / мм (3). Вакцина 33 , 1890–1896 (2015).
CAS PubMed Статья PubMed Central Google Scholar
Reither, K. et al. Безопасность и иммуногенность h2 / IC31 (R), адъювантной субъединичной вакцины против туберкулеза, у ВИЧ-инфицированных взрослых с количеством CD4 + лимфоцитов более 350 клеток / мм3: фаза II, многоцентровая, двойная слепая, рандомизированная, плацебо-контролируемая пробный. PLoS ONE 9 , e114602 (2014).
PubMed PubMed Central Статья CAS Google Scholar
Thacher, E. G. et al. Безопасность и иммуногенность кандидатной противотуберкулезной вакцины M72 / AS01 у ВИЧ-инфицированных взрослых при комбинированной антиретровирусной терапии: фаза I / II, рандомизированное испытание. AIDS 28 , 1769–1781 (2014).
CAS PubMed Статья PubMed Central Google Scholar
Hopkins, R. et al. Платформа двойной вакцины для новорожденных против ВИЧ-1 и M. tuberculosis. PLoS ONE 6 , e20067 (2011).
CAS PubMed PubMed Central Статья Google Scholar
Im, E.J. et al. Платформа вакцин для профилактики туберкулеза и передачи вируса иммунодефицита человека 1 типа от матери ребенку при грудном вскармливании. J. Virol. 81 , 9408–9418 (2007).
CAS PubMed PubMed Central Статья Google Scholar
Ndiaye, B.P. et al. Безопасность, иммуногенность и эффективность кандидатной противотуберкулезной вакцины MVA85A у здоровых взрослых, инфицированных ВИЧ-1: рандомизированное плацебо-контролируемое исследование фазы 2. Ланцет Респир. Мед 3 , 190–200 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Nemes, E. et al. Безопасность и иммуногенность вакцинации новорожденных MVA85A и селективной отсроченной вакцинации Bacille Calmette-Guerin для младенцев от матерей, инфицированных вирусом иммунодефицита человека: рандомизированное контролируемое исследование фазы 2. Clin. Заразить. Дис. 66 , 554–563 (2018).
CAS PubMed Статья Google Scholar
Manjaly Thomas, Z. R. et al. Альтернативная аэрозольная и системная иммунизация рекомбинантным вирусным вектором против туберкулеза MVA85A: рандомизированное контролируемое исследование фазы I. PLoS Med. 16 , e1002790 (2019).
PubMed PubMed Central Статья CAS Google Scholar
Kumarasamy, N. et al. Рандомизированное контролируемое исследование безопасности и иммуногенности кандидатной противотуберкулезной вакцины M72 / AS01 на ВИЧ-инфицированных взрослых индийцах. Медицина 95 , e2459 (2016).
CAS PubMed PubMed Central Статья Google Scholar
Hoft, D. F. et al. Рекомбинантный аденовирус, экспрессирующий иммунодоминантные антигены ТБ, может значительно усиливать индуцированный БЦЖ иммунитет человека. Вакцина 30 , 2098–2108 (2012).
CAS PubMed Статья PubMed Central Google Scholar
Abel, B. et al. Новая противотуберкулезная вакцина AERAS-402 индуцирует устойчивые и полифункциональные CD4 + и CD8 + Т-клетки у взрослых. г. J. Respir. Крит.Care Med. 181 , 1407–1417 (2010).
CAS PubMed PubMed Central Статья Google Scholar
Penn-Nicholson, A. et al. Безопасность и иммуногенность новой противотуберкулезной вакцины ID93 + GLA-SE у здоровых взрослых, вакцинированных БЦЖ, в Южной Африке: рандомизированное двойное слепое плацебо-контролируемое исследование фазы 1. Ланцет Респир. Med. 6 , 287–298 (2018).
CAS PubMed Статья PubMed Central Google Scholar
Aguilo, N. et al. Реактогенность по отношению к основным антигенам туберкулеза, отсутствующим в БЦЖ, связана с улучшенной защитой от Mycobacterium tuberculosis. Nat. Commun. 8 , 16085 (2017).
PubMed PubMed Central Статья Google Scholar
Covián, C. et al. Перекрестная защита, индуцированная БЦЖ, и развитие тренированного иммунитета: значение для разработки вакцины. Front Immunol. 10 , 2806 (2019).
PubMed PubMed Central Статья CAS Google Scholar
О’Нил, Л. А. Дж. И Нетеа, М. Г. Тренированный иммунитет, вызванный БЦЖ: может ли он обеспечить защиту от COVID-19? Nat. Rev. Immunol. 20 , 335–337 (2020).
PubMed Статья CAS Google Scholar
Aaby, P. et al. Рандомизированное испытание вакцинации БЦЖ детям с низкой массой тела при рождении: положительные неспецифические эффекты в неонатальном периоде? Дж.Заразить. Дис. 204 , 245–252 (2011).
CAS PubMed Статья Google Scholar
Kleinnijenhuis, J. et al. Бацилла Кальметта-Герена индуцирует NOD2-зависимую неспецифическую защиту от повторного заражения посредством эпигенетического репрограммирования моноцитов. Proc. Natl Acad. Sci. США 109 , 17537–17542 (2012).
CAS PubMed Статья Google Scholar
Jensen, K. et al. Вызванные вакциной слизистые оболочки и системные антитела связаны со снижением виремии обезьяньего иммунодефицита у детенышей макак-резус. J. Virol. 90 , 7285–7302 (2016).
CAS PubMed PubMed Central Статья Google Scholar
Профилактика заболеваний, предупреждаемых с помощью вакцин, у детей и подростков с ВИЧ-инфекцией
Профилактика заболеваний, предупреждаемых с помощью вакцин, у детей и подростков с ВИЧ-инфекцией
Вакцины являются чрезвычайно эффективным средством первичной профилактики, и вакцины, защищающие от 16 болезней, рекомендуются для рутинного использования у детей и подростков в Соединенных Штатах.Графики вакцинации детей от рождения до 18 лет ежегодно публикуются Центрами по контролю и профилактике заболеваний. Для получения дополнительной информации см .:
Эти таблицы составлены на основе утвержденных рекомендаций по политике в отношении конкретных вакцин, которые стандартизированы в сотрудничестве с основными организациями, занимающимися разработкой политики в отношении вакцин и поставками вакцин (например, Консультативным комитетом по практике иммунизации [ACIP], Американской академией педиатрии [AAP ], Американской академии семейных врачей [AAFP] и Американского колледжа акушеров и гинекологов [ACOG]) (см. Рекомендации ACIP).
Дети с ВИЧ-инфекцией должны быть защищены от болезней, которые можно предотвратить с помощью вакцин. Большинство вакцин, рекомендованных для рутинного использования, можно безопасно вводить детям, которые контактировали с ВИЧ или заразились ВИЧ. Рекомендуемый график вакцинации для детей в возрасте от 0 до 18 лет, контактировавших с ВИЧ или ВИЧ-положительных, соответствует утвержденному ACIP графику для всех детей с одобренными ACIP дополнениями, специфичными для детей с включенной ВИЧ-инфекцией (см. Рисунок 1).
Все инактивированные вакцины — будь то убитый целый организм или субъединица, рекомбинантные, токсоидные, полисахаридные или конъюгированные с полисахаридным белком — можно безопасно вводить лицам с измененной иммунокомпетентностью.Кроме того, из-за риска повышения тяжести заболевания у детей с ВИЧ-инфекцией специальные вакцины, такие как пневмококковая вакцина и конъюгированная вакцина Haemophilus influenzae типа b, также рекомендуются для детей с ВИЧ старше обычного рекомендуемого возраста для здоровых детей (если они не вводились ранее. в обычно рекомендуемом возрасте в раннем детстве). Также рекомендуются дополнительные вакцины, такие как пневмококковая полисахаридная вакцина для детей в возрасте ≥2 лет после получения пневмококковой конъюгированной вакцины и вакцина MenACWY, которую рекомендуется начинать в возрасте 2 месяцев.Другие вакцины могут быть рекомендованы вне обычного возрастного окна детям с ВИЧ, включая пневмококковую конъюгированную вакцину (PCV13) или вакцину против вируса папилломы человека для мужчин. Живая аттенуированная вакцина против гриппа (LAIV) противопоказана детям с ВИЧ. Ежегодная вакцинация против гриппа в соответствии с возрастом рекомендуется детям с ВИЧ в рамках плановой профилактики гриппа. 1 Эффективность любой вакцины может быть неоптимальной у человека с иммунодефицитным состоянием. 2-4
По сравнению с детьми с иммунодефицитом, дети с ВИЧ подвержены более высокому риску осложнений некоторых заболеваний, от которых доступны только живые вакцины. Основываясь на ограниченных данных по безопасности, иммуногенности и эффективности у детей с ВИЧ, вакцину против ветряной оспы с одним антигеном следует рассматривать для детей и подростков с ВИЧ-инфекцией с процентным содержанием Т-лимфоцитов CD4 (CD4) ≥15%. Соответствующие критериям дети должны получить 2 дозы с интервалом 3 месяца, причем первую дозу вводят как можно скорее после первого дня рождения ребенка.Две дозы вакцины против кори, эпидемического паротита и краснухи (MMR) рекомендуются для всех людей с ВИЧ в возрасте ≥12 месяцев, у которых нет доказательств тяжелой иммуносупрессии в настоящее время. 5
Оральная вакцина против брюшного тифа не следует вводить детям с ВИЧ.
Если рекомендовано, вакцину против желтой лихорадки (ЖЖ) можно вводить детям в возрасте от 9 месяцев до 6 лет с процентным содержанием CD4> 24% от общего количества лимфоцитов или детям в возрасте ≥6 лет с числом CD4 ≥500 на мм 3 .Медицинские работники должны убедиться, что у пациентов нет СПИДа или других клинических проявлений ВИЧ, что является противопоказанием.
Следует соблюдать меры предосторожности при проведении вакцинации против YFV, и введение YFV может быть рассмотрено для людей с ВИЧ в возрасте ≥6 лет с числом CD4 от 200 до 499 / мм 3 или детей в возрасте от 6 месяцев до 6 лет с процентом CD4 15% до 24% от общего числа лимфоцитов. Медицинские работники должны гарантировать, что пациенты не болеют СПИДом или другими клиническими проявлениями ВИЧ, что является противопоказанием.Если требования к международным поездкам, а не повышенный риск заражения YFV, являются единственной причиной для вакцинации кого-либо с мерами предосторожности, это лицо должно быть освобождено от вакцинации и выдано медицинское разрешение на соблюдение санитарных норм.
YFV — Противопоказан всем детям младше 6 месяцев. YFV также противопоказан всем детям со СПИДом, другими клиническими проявлениями ВИЧ и детям с числом CD4 <200 на мм 3 или <15% от общего количества лимфоцитов для детей в возрасте <6 лет.Если человек с тяжелой иммуносупрессией на основе числа CD4 (<200 на мм 3 или <15% всего), СПИД или симптоматический ВИЧ не может избежать поездки в район, где желтая лихорадка носит эндемический характер, следует предоставить медицинский отказ и Особое внимание следует уделять консультированию по мерам защиты от укусов комаров. Люди, которые были ВИЧ-положительными на момент введения начальной дозы YFV, должны получать бустерную дозу каждые 10 лет, если они продолжают путешествовать или живут в районах, которые подвергают их риску заражения вирусом желтой лихорадки.Подробный перечень мер предосторожности и противопоказаний для вакцинации против желтой лихорадки см. В «Желтой книге» и рекомендациях ACIP.
Имеются ограниченные данные по клиническим испытаниям безопасности ротавирусных вакцин у младенцев с ВИЧ-инфекцией, у которых на момент вакцинации клинические симптомы протекали бессимптомно или с умеренными симптомами. 6 Имеющиеся данные не предполагают, что профиль безопасности ротавирусных вакцин у младенцев с клинически бессимптомной или слабо симптоматической ВИЧ-инфекцией отличается от профиля безопасности младенцев, не инфицированных ВИЧ. 7,8 Два других соображения поддерживают ротавирусную вакцинацию младенцев, контактировавших с ВИЧ или инфицированных ВИЧ: во-первых, диагноз перинатальной ВИЧ-инфекции не может быть установлен у младенцев, рожденных от матерей с ВИЧ-инфекцией до достижения самого старшего возраста, в котором проводится серия ротавирусных вакцин. можно вводить; 9 и, во-вторых, вакцинные штаммы ротавируса аттенуированы, что позволяет предположить, что если вакцина вызвана заболеванием, то оно будет умеренным. Перед введением ротавирусной вакцины рекомендуется проконсультироваться с иммунологом или специалистом по инфекционным заболеваниям для младенцев с известной или предполагаемой измененной иммунокомпетентностью, таких как младенцы с ВИЧ-инфекцией с низким процентом или количеством CD4.
Для некоторых вакцин (таких как гепатит А) ответ на вакцинацию может быть выше при восстановлении иммунитета после антиретровирусной терапии (АРТ), 10 или могут быть вариации иммуногенности в зависимости от вирусной нагрузки (например, улучшенный иммунный ответ при более низком уровне ВИЧ вирусная нагрузка), например, с YFV. 11 Для большинства вакцин пациенты с более высоким числом CD4 имеют улучшенный иммунный ответ, что также означает, что ответ (например, на вакцинацию от гриппа, MMR, желтую лихорадку), вероятно, улучшится после начала АРТ. 1,12,11,13 Обеспокоенность по поводу отсутствия защиты от вакцин, вводимых ребенку до начала АРТ, вызвала дебаты о необходимости плановой повторной иммунизации после того, как ребенок будет получать эффективную АРТ. 11,14 На основании низких показателей серопротекции кори у детей с ВИЧ, которые получали вакцину MMR до начала АРТ, а также безопасности и высоких показателей серопротекции кори, связанных с повторной иммунизацией MMR после того, как дети получали АРТ, 15 ACIP дал конкретные рекомендации по плановой повторной иммунизации MMR после начала АРТ. 5 Лица с перинатальной ВИЧ-инфекцией, которые были вакцинированы до начала эффективной АРТ, должны получить две соответствующим образом распределенные дозы вакцины MMR после того, как будет установлена эффективная АРТ, за исключением случаев, когда у них имеется серьезная иммуносупрессия или другие приемлемые текущие доказательства иммунитета к кори. 5 Для некоторых вакцин (например, от гепатита B) ACIP рекомендует провести серологическое исследование после вакцинации, чтобы гарантировать иммунный ответ.
Дети, живущие в семье со взрослым или ребенком с ВИЧ, могут получить вакцину MMR, поскольку вирусы, содержащиеся в этой вакцине, не передаются от человека к человеку.Все члены семьи в возрасте старше 6 месяцев могут получать вакцины от гриппа ежегодно. Иммунизация против ветряной оспы приветствуется для всех домашних контактов детей с ВИЧ-инфекцией, имеющих доказанный иммунитет к ветряной оспе. 15 Передача вируса вакцины против ветряной оспы от иммунизированного иммунокомпетентного человека домашнему контакту происходит редко.
Для получения более подробной информации о рекомендациях, мерах предосторожности и противопоказаниях для использования конкретных вакцин ознакомьтесь с конкретными заявлениями ACIP (доступными в Рекомендациях и руководствах по вакцинам ACIP) (см. Профилактика пневмококковой инфекции и использование 2-х дозовой схемы вакцинации против вируса папилломы человека). 10,12,15,16-27
Список литературы
- Fiore AE, Uyeki TM, Broder K и др. Профилактика гриппа и борьба с ним с помощью вакцин: рекомендации Консультативного комитета по практике иммунизации (ACIP), 2010 г. MMWR Recomm Rep . 2010; 59 (РР-8): 1-62. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/20689501.
- Крогер А.Т., Аткинсон В.Л., Маркузе Е.К., Пикеринг Л.К., Консультативный комитет по центрам практики иммунизации по болезни C, Профилактика.Общие рекомендации по иммунизации: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep . 2006; 55 (RR-15): 1-48. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/17136024.
- Хорстер С., Лаубендер Р.П., Лемейер Л. и др. Влияние антиретровирусной терапии на иммуногенность одновременных вакцинаций против гриппа, пневмококковой инфекции и гепатита А и В у лиц с положительным вирусом иммунодефицита человека. J Заражение. 2010; 61 (6): 484-491. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/20875454.
- Литгоу Д., Коул С. Повторное исследование уровня сероконверсии у лиц, вакцинированных против гепатита В. Biol Res Nurs. 2015; 17 (1): 49-54. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/25504950.
- Центры по контролю и профилактике заболеваний. Профилактика кори, краснухи, синдрома врожденной краснухи и эпидемического паротита, 2013 г .: сводные рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2013; 62 (RR-04): 1-34. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/23760231.
- Стил А.Д., Мадхи С.А., Лоу CE и др. Безопасность, реактогенность и иммуногенность ротавирусной вакцины человека RIX4414 у младенцев с вирусом иммунодефицита человека в Южной Африке. Pediatr Infect Dis J. 2011; 30 (2): 125-130. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/20842070.
- Laserson KF, Nyakundi D, Feikin DR, et al. Безопасность пятивалентной ротавирусной вакцины (PRV), RotaTeq ((R)), в Кении, в том числе среди ВИЧ-инфицированных и контактировавших с ВИЧ младенцев. Вакцина. 2012; 30 Приложение 1: A61-70. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/22520138.
- Левин М.Дж., Линдси Дж.С., Каплан С.С. и др. Безопасность и иммуногенность живой аттенуированной пятивалентной ротавирусной вакцины для контактировавших с ВИЧ младенцев с ВИЧ-инфекцией или без нее в Африке. СПИД. 2017; 31 (1): 49-59. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/27662551
- Центры профилактики болезни C. Достижения в области общественного здравоохранения. Снижение перинатальной передачи ВИЧ-инфекции — США, 1985–2005 гг. MMWR Morb Mortal Wkly Rep. 2006; 55 (21): 592-597. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/16741495.
- Fiore AE, Wasley A, Bell BP. Профилактика гепатита А посредством активной или пассивной иммунизации: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2006; 55 (RR-7): 1-23. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/16708058.
- Staples JE, Gershman M, Fischer M, Центры болезней C, Профилактика.Вакцина против желтой лихорадки: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2010; 59 (RR-7): 1-27. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/20671663.
- Watson JC, Hadler SC, Dykewicz CA, Reef S, Phillips L. Использование вакцины против кори, эпидемического паротита и краснухи и стратегии ликвидации кори, краснухи и синдрома врожденной краснухи и борьба с эпидемическим паротитом: рекомендации Консультативного комитета по иммунизации Практики (ACIP). MMWR Recomm Rep. 1998; 47 (RR-8): 1-57. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/9639369.
- Sutcliffe CG, Moss WJ. Нужно ли ревакцинировать ВИЧ-инфицированных детей, получающих ВААРТ? Lancet Infect Dis. 2010; 10 (9): 630-642. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/20797645.
- Мелвин А.Дж., Мохан К.М. Ответ на иммунизацию вакцинами против кори, столбняка и Haemophilus influenzae типа b у детей, инфицированных вирусом иммунодефицита человека типа 1 и получающих высокоактивную антиретровирусную терапию. Педиатрия. 2003; 111 (6, часть 1): e641-644. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/12777579.
- Марин М., Гурис Д., Чавес С.С. и др. Профилактика ветряной оспы: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep . 2007; 56 (RR-4): 1-40. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/17585291.
- Абзуг М.Дж., Цинь М., Левин М.Дж. и др. Иммуногенность, иммунологическая память и безопасность после ревакцинации против кори у ВИЧ-инфицированных детей, получающих высокоактивную антиретровирусную терапию. J Заразить Dis . 2012; 206 (4): 512-522. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/22693229.
- Cortese MM, Parashar UD, Центры по контролю и профилактике заболеваний. Профилактика ротавирусного гастроэнтерита среди младенцев и детей: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep . 2009; 58 (РР-2): 1-25. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/19194371.
- Конъюгированные вакцины против Haemophilus b для профилактики болезни Haemophilus influenzae типа b среди младенцев и детей в возрасте двух месяцев и старше.Рекомендации консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 1991; 40 (RR-1): 1-7. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/1899280.
- Fiore AE, Shay DK, Broder K и др. Профилактика гриппа и борьба с ним: рекомендации Консультативного комитета по практике иммунизации (ACIP), 2008 г. MMWR Recomm Rep . 2008; 57 (RR-7): 1-60. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/18685555.
- Консультативный комитет по практике иммунизации.Профилактика пневмококковой инфекции у младенцев и детей раннего возраста. Рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2000; 49 (RR-9): 1-35. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/11055835.
- Превоц Д.Р., Берр Р.К., Саттер Р.В., Мерфи ТВ, Консультативный комитет по практике иммунизации. Профилактика полиомиелита в США. Обновленные рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2000; 49 (РР-5): 1-22; викторина CE21-27. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/15580728.
- Mast EE, Margolis HS, Fiore AE и др. Комплексная стратегия иммунизации для ликвидации передачи инфекции вируса гепатита В в Соединенных Штатах: рекомендации Консультативного комитета по практике иммунизации (ACIP), часть 1: иммунизация младенцев, детей и подростков. MMWR Recomm Rep . 2005; 54 (RR-16): 1-31. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/16371945.
- Билуха О.О., Розенштейн Н., Национальный центр инфекционных болезней CDC, Профилактика. Профилактика и борьба с менингококковой инфекцией. Рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 2005; 54 (RR-7): 1-21. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/15917737.
- Центры по контролю и профилактике заболеваний. Примечание для читателей: рекомендация Консультативного комитета по практике иммунизации (ACIP) по применению четырехвалентной менингококковой конъюгированной вакцины (MCV4) у детей в возрасте 2 — 10 лет с повышенным риском инвазивного менингококкового заболевания. MMWR Morb Mortal Wkly Rep . 2007; 56: 1265-1266. Доступно по адресу: http://www.cdc.gov/mmwr/preview/mmwrhtml/mm5648a4.htm.
- Противококлюшная вакцинация: использование бесклеточной коклюшной вакцины среди младенцев и детей раннего возраста. Рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep. 1997; 46 (RR-7): 1-25. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/
80.
- Бродер К.Р., Кортезе М.М., Искандер Дж.К. и др. Профилактика столбняка, дифтерии и коклюша среди подростков: использование столбнячного анатоксина, редуцированного дифтерийного анатоксина и бесклеточных коклюшных вакцин Рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Recomm Rep . 2006; 55 (РР-3): 1-34. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/16557217.
- Центры заболеваний C, Консультативный комитет по профилактике по вопросам иммунизации. Пересмотренные рекомендации Консультативного комитета по практике иммунизации по вакцинации всех лиц в возрасте от 11 до 18 лет конъюгированной менингококковой вакциной. MMWR Morb Mortal Wkly Rep . 2007; 56 (31): 794-795. Доступно по адресу: http://www.ncbi.nlm.nih.gov/pubmed/17694617.
PLOS ONE: вакцинация и иммунизация
Димитриос Каруссис, Хагай Шор, […], Ривка Абулафия-Лапид
Генри Тумвебейз, Элиода Тумвесиги, […], Конни Селум
Сяньфэн Чэн, Сон Ван, […], Джихонг Мэн
Соломон Одафе, Кваси Торпи, […], Отто Чабикули
Вивиана Буффа, Катя Кляйн, Люсия Фишетти, Робин Дж.Shattock
Сильвия Борхерс, Мелани Бремм, […], Ульрике Кёль
Луис Фелипе М. Прота, Людмила Чеботару, […], Уильям Б. Гуджино
Бах Суан Тран, Арто Охинмаа, […], Стэн Хьюстон
Рашель М.Бьюкенен, Шерри Тетланд, Хизер Л. Уилсон
Стивен П. Картер, Марк А. Чемберс, […], Робби А. Макдональд
Торстен Зюсс, Корнелиус Ремшмидт, […], Удо Бухгольц
Саджад Рафик, Маргарет Л. Рассел, […], Марк Леб
Исмаил Себина, Жаклин М.Утес, […], Стивен Коз
Временной интервал ревакцинации 23-валентной пневмококковой полисахаридной вакциной более 5 лет не влияет на иммуногенность и безопасность у пожилых людей в Японии Пневмония, Streptococcus pneumoniae, инфекции, приобретенные сообществом, вакцина Pnu-Imune
Trending Feeds
Метаболический синдром и СД2
Метаболический синдром — комплексное заболевание, характеризующееся кластером метаболических нарушений, включая гипертензию, диабет 2 типа и ожирение.Вот последние исследования метаболического синдрома и сахарного диабета 2 типа.
CRISPR-скрининг в вирусологии
Этот канал посвящен применению системы CRISPR-Cas в высокопроизводительных полногеномных скринингах для выявления генов, влияющих на взаимодействие вируса с хозяином. Вот последнее исследование.
Криогенная электронная микроскопия
Криогенная электронная микроскопия (Cryo-EM) позволяет определять биологические макромолекулы и их сборки с разрешением, близким к атомному.Вот последнее исследование.
Crispr In Malaria
Система CRISPR-Cas позволяет редактировать гены для создания или исправления мутаций. Эта технология изучается для борьбы с малярией путем нацеливания на определенные участки векторной ДНК и редактирования генома в определенных местах. Вот последнее исследование.
РНК и аксональные функции
Этот канал фокусируется на субклеточной регуляции и регуляции трансляции РНК в аксонах и на том, как это влияет на аксональные функции. Ознакомьтесь с последними исследованиями здесь.
CRISPR и анализ отдельных клеток
Система CRISPR-Cas позволяет редактировать гены для создания или исправления мутаций. Этот канал посвящен приложениям CRISPR-Cas, относящимся к анализу отдельных клеток. Вот последнее исследование.
Обонятельная навигация
Этот канал фокусируется на влиянии запаха и восприятия пространства, а также на механизмах, лежащих в основе навигационного поведения животных. Вот последние исследования обонятельной навигации.
Рибопереключатели и рибозимы
Рибозимы — это каталитические РНК, которые взаимодействуют с различными низкомолекулярными субстратами и кофакторами, внутриклеточное изобилие которых определяется рибопереключателями, которые модулируют транскрипцию, стабильность РНК или трансляцию.Вот последнее исследование.
Enzyme Evolution
Этот корм ориентирован на молекулярные модели эволюции ферментов и новые подходы (такие как адаптивная лабораторная эволюция) к метаболической инженерии микроорганизмов. Вот последнее исследование.
Сопутствующие документы
Вакцина
Kenji KawakamiLuwy K Musey
Pediatric Blood & Cancer
Mariane Susande MontalembertDaniel A Scott
Vaccine
10 R AIDS
10 FrenckB Vaccine
10 FrenckB Group
As’ad E BhoratBeate Schmoele-Thoma
Успешная иммунизация и безопасность, подтвержденные в носовой полости
ОСЛО, НОРВЕГИЯ — (Marketwire — 10 мая 2012 г.) — Bionor Pharma (ОСЛО: BIONOR)
Сводка новостей
- Связанные с вакциной иммунные ответы, обнаруженные у пациентов с ВИЧ, которым вводили вакцину Vacc-4x вместе с эндоцином через нос в плацебо-контролируемом исследовании
- В исследовании также задокументирована безопасность при введении через нос
- Дальнейшие анализы продолжаются и будут опубликованы на более позднем этапе.
Bionor Pharma ASA (OSLO: BIONOR), Eurocine Vaccines AB и Университетская больница Осло сегодня объявили, что иммунные ответы, связанные с вакцинацией, задокументированы у пациентов, получавших активную вакцину, в исследовании назальной иммунизации, сочетающем вакцину Bionor Pharma Vacc-4x и адъювант Endocine от Eurocine Vaccines. .Различия, связанные с дозами, в настоящее время оцениваются, и дополнительные данные, включая продукцию антител в секретах слизистой оболочки, будут проанализированы и опубликованы на более позднем этапе.
Кроме того, результаты подтверждают безопасность вакцины при назальном введении. Клинические расходы были покрыты за счет гранта Исследовательского совета Норвегии (RCN) в размере 1,2 миллиона долларов США (6,9 миллиона норвежских крон) в рамках программы GLOBVAC.
Vacc-4x — терапевтическая вакцина против ВИЧ на основе четырех слегка модифицированных пептидов (строительных блоков белков) из консервативных частей вируса ВИЧ.Эндоцин представляет собой адъювант, который, как было показано, усиливает иммунный ответ на антигены вакцины, вводимые через нос.
Исследователи из Университетской больницы Осло изучали эффект назальной доставки Vacc-4x в сочетании с адъювантом Endocine от Eurocine Vaccines по сравнению с эффектом одного Endocine.
«Мы рады сообщить о положительных предварительных результатах исследования, показывающих, что вакцина Vacc-4x для пациентов с ВИЧ может вводиться как через нос, так и путем инъекций», — сказал профессор Даг Квале, доктор медицинских наук.D., главный исследователь Университетской больницы Осло. «Эти результаты являются многообещающими для пациентов с ВИЧ во всем мире, поскольку потенциально могут предоставить новый класс лечения ВИЧ, который будет еще проще осуществить».
«Мы считаем эти данные важными как для вакцины Vacc-4x, так и для других наших вакцин-кандидатов», — сказал Стин Кройер, генеральный директор Bionor Pharma ASA.
«Положительные результаты этого исследования с комбинацией вакцины Vacc-4x и Endocine, вводимой через нос, могут проложить путь для помощи растущему числу пациентов с ВИЧ с неудовлетворенными медицинскими потребностями», — сказал Ханс Арвидссон, генеральный директор Eurocine Vaccines AB.
Об исследовании и результатах
Единственное слепое рандомизированное плацебо-контролируемое исследование иммуногенности включало 24 пациента, все из которых получали традиционные лекарства от ВИЧ (антиретровирусная терапия, АРТ). 18 пациентов получали активную назальную вакцину (как Vacc-4x, так и адъювант Endocine) при любом из трех различных уровней доз Vacc-4x, а 6 пациентов получали только Endocine (контрольная группа). Всем пациентам вводили назальные капли еженедельно в течение четырех недель (один пациент был исключен на 6 неделе без причин, связанных с исследованием).Последний визит в рамках исследования был назначен на 8-ю неделю. В целом, лечение переносилось очень хорошо, хотя некоторые из них в тот же день сообщили о легких и преходящих ощущениях в носу.
Только пациенты, которым вводили активную назальную вакцину (с Vacc-4x), увеличивали свой связанный с вакциной иммунный ответ в течение 8-недельного периода исследования. Этот результат был дополнительно подтвержден кожным тестом (DTH).
Эти результаты подтверждают, что иммунизация ВИЧ-инфицированных путем одновременного назального введения вакцины Vacc-4x и адъюванта Endocine безопасна и способна усилить иммунный ответ, связанный с вакциной.
О вакцине против ВИЧ Vacc-4x
Vacc-4x — терапевтическая вакцина против ВИЧ, основанная на четырех, слегка модифицированных пептидных последовательностях из консервативных (стабильных) частей вируса ВИЧ, которые не изменяются даже при мутации вируса (меняется). Выбранные пептиды были модифицированы для повышения иммуногенности вакцины. Продукт имеет широкую патентную защиту.
О компании Eurocine Vaccines
Eurocine Vaccines — это публичная компания, занимающаяся клинической стадией разработки назальных вакцин, отвечающих важным медицинским потребностям.Вакцины разрабатываются до подтверждения концепции (клиническая фаза I / II) и передаются партнерам по лицензии для дальнейшей разработки и коммерциализации. Запатентованные компанией технологии адъювантных вакцин, которые являются ключевым элементом назальных вакцин, также предлагаются партнерам по лицензированию для разработки по различным показаниям.
Более подробную информацию о Eurocine Vaccines, ее исследованиях и продуктах можно найти на сайте www.eurocine-vaccines.com
О Bionor Pharma ASA
Bionor Pharma — это биофармацевтическая компания, зарегистрированная в Осло, Норвегия.Инвестиции компании в разработку терапевтических вакцин превышают 70 миллионов долларов США. Вакцины Bionor основаны на запатентованной технологической платформе, разработанной после более чем двух десятилетий исследований пептидов. Вакцины предназначены для безопасной активации иммунной системы каждого человека для борьбы с вирусными заболеваниями.
Ведущий исследовательский продукт Компании, терапевтическая вакцина против ВИЧ Vacc-4x, в завершенной фазе IIb многонационального (США, Германия, Великобритания, Испания и Италия) плацебо-контролируемого двойного слепого исследования продемонстрировал статистически значимое снижение вирусной нагрузки. .
ИсследователиBionor считают, что снижение вирусной нагрузки на 64% у пациентов, получавших вакцину Vacc-4x в исследовании фазы IIb, является долговременным вирусным контролем в результате новой способности иммунной системы пациента убивать вирус-продуцирующие клетки, в отличие от снижение вируса, достигаемое ежедневной традиционной медициной (антиретровирусная терапия, АРТ). Исследования показывают, что лечение АРТ переводит вирус-продуцирующие клетки в состояние покоя, из которого они могут «проснуться» даже более чем через десять лет и снова начать продуцировать вирус в течение нескольких недель, если пациенты прекратят АРТ.Поскольку известно, что большинство пациентов, получающих АРТ, прекращают принимать ее по разным причинам (высокая стоимость, ограниченный доступ, развитие резистентности и серьезные побочные эффекты), Bionor считает, что Vacc-4x может быть жизненно важным вариантом лечения, который может стабилизировать состояние пациентов, даже если они перестают принимать АРТ.
Планируется, что вторая терапевтическая вакцинаBionor от ВИЧ, Vacc-C5 будет готова к первому клиническому испытанию на людях во 2 квартале 2012 года. Она разработана для индукции антител к ВИЧ, которые могут снизить иммунную гиперактивацию, связанную с ВИЧ-инфекцией.
После испытаний Vacc-C5 фазы I / II, Bionor намеревается объединить Vacc-4x с Vacc-C5, которые могут лечь в основу как терапевтической, так и профилактической вакцины.
По данным организации ООН ЮНЭЙДС, в 2010 году 34 миллиона человек жили с ВИЧ. Ежегодно инфицируются примерно три миллиона новых людей. Продажи фармацевтических препаратов для лечения ВИЧ составляют 10,6 млрд долларов США (63 млрд норвежских крон) в год, а стоимость лечения на одного пациента составляет прибл. 15 000 долларов США (90 000 норвежских крон) в год.
Лишь один из шести ВИЧ-инфицированных в мире сегодня получает лечение.
Пути выхода на рынок вакцин против ВИЧ
Исследователи Bionor изучат различные независимые пути выхода на рынок вакцин-кандидатов против ВИЧ Vacc-4x и Vacc-C5, в ходе дальнейших клинических исследований, начиная с этого года:
1. Ревакцинация Vacc-4x у пациентов, участвовавших в исследовании фазы IIb, целью которого является дальнейшее снижение вирусной нагрузки за счет уничтожения клеток, продуцирующих вирус, в периоды, когда пациенты не получают АРТ.
2. Vacc-4x в сочетании с Revlimid® (леналидомид) у пациентов с ослабленной иммунной системой, состояние которой не улучшается, несмотря на хорошо контролируемую вирусную нагрузку при лечении АРТ.
3. Фаза I / II клинических испытаний Vacc-C5, чтобы подтвердить, увеличивает ли Vacc-C5 антитела к ВИЧ, а затем Vacc-C5 в комбинации с Vacc-4x с целью искоренения ВИЧ и, таким образом, революционизирует лечение ВИЧ.
Вакцины от других вирусных заболеваний
Инновационная технологическая платформа компании также хорошо подходит для разработки вакцин от других вирусных заболеваний, таких как грипп, HCV (гепатит C), HPV (вирус папилломы человека) и CMV (цитомегаловирус).
Планируется, что во второй половине 2012 г. будут завершены все доклинические испытания вакцин против гриппа (универсальная вакцина против гриппа) и вакцины против гепатита С (вакцина против гепатита С), включая токсикологические испытания, что позволит подготовить их к клиническим исследованиям на людях.
Более подробная информация о Bionor Pharma, ее исследованиях и продуктах доступна на сайте www.bionorpharma.com.
Эта информация является предметом требований по раскрытию информации в соотв. согласно §5-12 vphl
(Норвежский закон о торговле ценными бумагами).Vacc-4x — это исследуемый препарат, который не был одобрен для продажи каким-либо регулирующим органом .
Bionor Pharma ASA
Осло:
+47 23 01 09 60
Лаборатории Bionor Pharma:
+47 35 90 85 00
Стин Кройер
Генеральный директор
Видар Вендел-Хансен
CMO
Убитая цельная вакцина против ВИЧ; использует хорошо отработанную стратегию для противовирусных вакцин | Исследования и терапия СПИДа
Чой Э., Михальски С.Дж., Чу С.Х. и др.Первая фаза I клинического испытания убитой цельной вакцины против ВИЧ-1 на людях: демонстрация ее безопасности и усиление реакции антител против ВИЧ. Ретровирология. 2016; 13:82. DOI: 10.1186 / s12977-016-0317-2.
Артикул PubMed PubMed Central Google Scholar
Барре-Синусси Ф., Черманн Дж. К., Рей Ф. и др. Выделение Т-лимфотропного ретровируса от пациента с риском синдрома приобретенного иммунодефицита (СПИД). Наука.1983; 220: 868–71.
CAS Статья PubMed Google Scholar
Проверить E. Новости природы: вернуться к «плану А». Природа. 2003; 423: 912–4.
CAS Статья PubMed Google Scholar
План вакцины против СПИДа. В: Задача области, дорожная карта для прогресса. Нью-Йорк: Международная инициатива по вакцине против СПИДа — IAVI; 2008 г. https: //www.iavi.орг.
Mascola JR. Современная эра разработки вакцины против ВИЧ-1. Наука. 2015; 349: 139–40.
CAS Статья PubMed Google Scholar
Секалы р-п. Неудачное исследование вакцины Merck против ВИЧ: шаг назад или отправная точка для разработки вакцины в будущем? J Exp Med. 2008; 205: 7–12.
CAS Статья PubMed PubMed Central Google Scholar
Haynes BF, Gilbert PB, McElrath J, et al. Иммунно-коррелятный анализ испытания эффективности вакцины против ВИЧ-1. N Engl J Med. 2012; 366: 1275–86.
CAS Статья PubMed PubMed Central Google Scholar
Khowsroy K, Dhitavat J, Sabmee Y, et al. Ожидание добровольцев относительно эффективности вакцины в ходе испытания фазы III первичной бустерной вакцины против ВИЧ во время неслепого исследования. AIDS Res Hum Retrovir. 2014; 30: 1041–5.
Артикул PubMed PubMed Central Google Scholar
Плоткин С.А. Испытание тайской вакцины против ВИЧ RV144. Hum Vaccine. 2010; 6: 159.
Google Scholar
Ваккари М., Пунам П., Франкини Г. Испытание вакцины против ВИЧ фазы III в Таиланде: шаг к защитной вакцине от ВИЧ. Экспертные ревакцины. 2010; 9: 997–1005.
CAS Статья PubMed Google Scholar
Вейлетт М., Коуту М., Ричард Дж. И др.CD4-связанная конформация gp120 ВИЧ-1 предпочтительно является мишенью антител-зависимых антител, опосредующих клеточную цитотоксичность, в сыворотках от ВИЧ-1-инфицированных индивидуумов. J Virol. 2015; 89: 545–51.
Артикул PubMed Google Scholar
Динг С., Вейлетт М., Куту М. и др. Высококонсервативный остаток внутреннего домена gp120 ВИЧ-1 важен для антителозависимых реакций клеточной цитотоксичности, опосредованных антителами против кластера А.J Virol. 2016; 90: 2127–34.
CAS Статья PubMed Central Google Scholar
Hammer SM, et al. Испытание эффективности профилактической вакцины против ВИЧ-1 ДНК / rAd5. N Engl J Med. 2013; 369: 2083–92.
CAS Статья PubMed PubMed Central Google Scholar
Wyatt R, Kwong PD, Desjardins E, et al. Антигенная структура гликопротеина оболочки gp120 ВИЧ.Природа. 1998. 393: 705–11.
CAS Статья PubMed Google Scholar
Alsalmi W., Mahalingam M, Hamlin NAC, et al. Новый подход к получению тримеров оболочки ВИЧ-1: как расщепление, так и правильное гликозилирование необходимы для создания аутентичных тримеров. J Biol Chem. 2015; 290: 19780–95.
CAS Статья PubMed PubMed Central Google Scholar
Miller NZ. Вакцина против полиомиелита; критическая оценка его загадочной истории, эффективности и долгосрочных последствий для здоровья. Med Veritas. 2004. 1 (2): 239–51.
Артикул Google Scholar
Брайт Р.А., Картер Д.М., Данилюк С. и др. Частицы, подобные вирусу гриппа, вызывают более широкий иммунный ответ, чем вирус гриппа, инактивированный цельным вирионом, или рекомбинантный гемагглютинин. Вакцина. 2007. 25: 3871–8.
CAS Статья PubMed Google Scholar
Калбертсон К.Г., Пек Ф. Б. младший, Пауэлл Х. М.. Вакцина против бешенства утиных эмбрионов; исследование вакцины с фиксированным вирусом, выращенной в утиных яйцах с зародышем и убитой бета-пропиолактоном (BPL). J Am Med Assoc. 1956; 162: 1373–6.
CAS Статья PubMed Google Scholar
Hilleman MR. Вакцина против гепатита и гепатита А: немного истории. J Hepatol. 1993; 18 (Дополнение 2): S5–10.
Артикул PubMed Google Scholar
Orchestra Therapeutics прекращает программу разработки вакцины против ВИЧ. 2007. http://www.biospace.com/News/orchestra-therapeutics-discontinues-its-hiv/63327.
Шеппард Х.В., Дорман Б.П. Пришло время систематически взглянуть на инактивированные вакцины против ВИЧ. СПИД. 2015; 29: 125–7.
Артикул PubMed Google Scholar
Rios A, Poteet EC, Siwak EB, et al. Инактивация ВИЧ: время для второго взгляда. СПИД.2015; 29: 129–31.
Артикул PubMed Google Scholar
Кирхгоф Ф., Гриноу Т.С., Бреттлер Д.Б. и др. Краткий отчет: отсутствие интактных последовательностей nef у длительного выжившего с непрогрессирующей инфекцией ВИЧ-1. N Engl J Med. 1995; 332: 228–32.
CAS Статья PubMed Google Scholar
Родос Д.И., Эштон Л., Соломон А. и др. Характеристика трех штаммов nef-дефектного вируса иммунодефицита человека типа 1, ассоциированных с длительным непрогрессированием.J Virol. 2000; 74: 10581–8.
CAS Статья PubMed PubMed Central Google Scholar
Кестлер Х.В. III, Ринглир Д.Д., Мори К. и др. Важность гена nef для поддержания высокой вирусной нагрузки и развития СПИДа. Клетка. 1991; 65: 651–62.
CAS Статья PubMed Google Scholar
Джеймисон Б.Д., Памг С., Альдрованди Г.М. и др.Необходимость nef вируса иммунодефицита человека типа 1 для репликации in vitro и патогенности. J Virol. 1994; 68: 3478–85.
CAS PubMed PubMed Central Google Scholar
Li Y, Luo L, Thomas DY, Kang CY. Контроль экспрессии, гликозилирования и секреции gp120 ВИЧ-1 с помощью гомологичных и гетерологичных сигнальных последовательностей. Вирусология. 1994; 204: 266–78.
CAS Статья PubMed Google Scholar
Li Y, Luo L, Thomas DY, Kang CY. Сигнальная последовательность белка Env ВИЧ-1 замедляет его расщепление и подавляет укладку гликопротеина. Вирусология. 2000. 272: 417–28.
CAS Статья PubMed Google Scholar
Россио Дж. Л., Эссер М. Т., Сурьянараяна К. и др. Инактивация вируса иммунодефицита человека 1-го типа с сохранением конформационной и функциональной целостности поверхностных белков вириона. J Virol.1998. 72: 7992–8001.
CAS PubMed PubMed Central Google Scholar
Rutebemberwa A, Bess JW Jr, Brown B, et al. Оценка инактивированного альдритиолом-2 препарата ВИЧ типа 1 подтипов A, B и D в качестве реагентов для мониторинга Т-клеточных ответов. AIDS Res Hum Retrovir. 2007; 23: 532–42.
CAS Статья PubMed Google Scholar
Хендерсон Э., Тюдор Дж., Ян Дж.Инактивация вируса иммунодефицита человека типа 1 (ВИЧ-1) ультрафиолетовым и X-излучением. Radiat Res. 1992; 131: 169–76.
CAS Статья PubMed Google Scholar
Fiebig EW, Wright DJ, Rawal BD, et al. Динамика ВИЧ-виремии и сероконверсии антител у доноров плазмы: значение для диагностики и определения стадии первичной ВИЧ-инфекции. СПИД. 2003; 17: 1871–189.
Артикул PubMed Google Scholar
Сандерс Р.В., Ван Гилс М.Дж., Деркинг Р. и др. Нейтрализующие антитела к ВИЧ-1, индуцированные нативными триммерами оболочки. Наука. 2015; 349: 154.
CAS Статья Google Scholar
Jardine JG, Ota T, Sok D, et al. Примирование широко нейтрализующего ответа антител на ВИЧ-1 с использованием иммуногена, нацеленного на зародышевую линию. Наука. 2015; 349: 156–61.
CAS Статья PubMed PubMed Central Google Scholar
Grobler J, Gray CM, Rademeyer C, et al. Заболеваемость двойной инфекцией ВИЧ-1 и ее связь с повышенным заданным значением вирусной нагрузки в когорте женщин секс-бизнеса, инфицированных ВИЧ-1 подтипа С. J Infect Dis. 2004; 190: 1355–9.
Артикул PubMed Google Scholar
Altfeld M, Allen TM, Yu XG, et al. Суперинфекция ВИЧ-1, несмотря на широкие Т-клеточные ответы CD8 + , содержащие репликацию первичного вируса. Природа.2002; 420: 434–9.
CAS Статья PubMed Google Scholar
