Саркома легкого — причины, симптомы, кто лечит
Саркома легкого — причины, симптомы, кто лечитЧто необходимо сделать для диагностики и лечения саркомы легкого? Для решения данной проблемы пациенту первым шагом необходимо записаться на прием к торакальному хирургу. После первичного осмотра врач может назначить дополнительные исследования:
- Консультация у онколога
- рентген легких
- КТ легких с контрастом
- МРТ легких
- Бронхоскопия
- Лабораторные анализы
- Биопсия.
Саркома — это группа редких злокачественных новообразований, которые развиваются из тканей стенок сосудов, мышечной и фиброзной ткани, оболочек периферических нервов. Этот вид рака встречается редко. Саркомы мягких тканей могут развиваться в любых тканях, которые поддерживают, соединяют, окружают и защищают органы тела.
Виды сарком легких
По своему происхождению саркома легких делится на первичную (растущую из собственных тканей легкого) и вторичную — саркома, которая метастазировала из других тканей. Высокодифференцированные саркомы легких различаются в зависимости от источника бластоматозного процесса:
- ангиосаркома
- фибросаркома
- лимфосаркома
- нейросаркома
- хондросаркома
- липосаркома
- гемангиоперицитома.
Недифференцированные саркомы легких делятся на:
- веретеноклеточные
- круглоклеточные
- полиморфно-клеточные.

Причины саркомы легких
Причины возникновения саркомы легких неизвестны. Существуют определенные факторы, которые могут повлиять на вероятность развития новообразования. Это так называемые факторы риска. Наличие факторов риска не означает, что обязательно разовьется саркома, и у пациентов без факторов риска она все равно может развиться. К группе риска по возникновению саркомы легких относятся:
- курильщики со стажем боле 5 лет
- онкопациенты с историей онкологических заболеваний дыхательных органов и других форм сарком.
- работники, контактирующие с производственными канцерогенами (асбестом, анилиновыми красителями, пестицидами
- злоупотребление загаром или солярием.
Симптомы саркомы легкого
Симптомы саркомы легкого аналогичны проявлениям рака легкого, но отличаются более агрессивным проявлением. Признаки включают:
- кашель с кровью
- отдышка
- боль в груди.
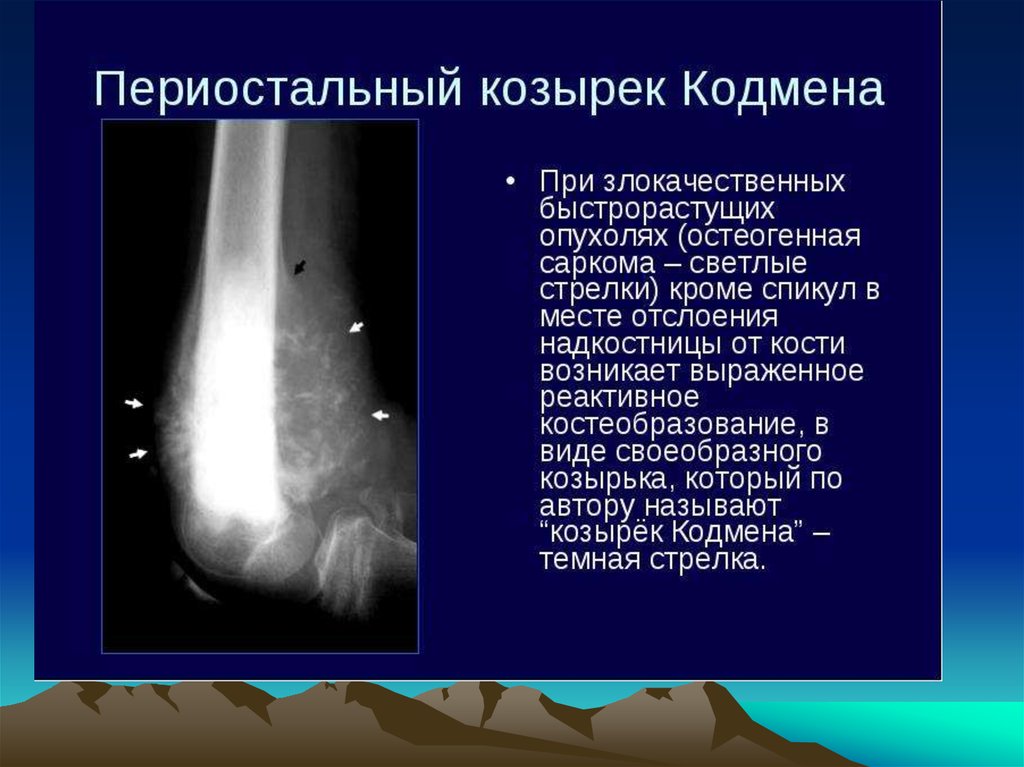
Как врач ставит диагноз легочная саркома
Для диагностики саркомы легких онколог или торакальный хирург назначит некоторые из следующих исследований:
- рентгенография легких
- КТ легких с контрастом
- МРТ легких
- Бронхоскопия
- Биопсия.
Лучшие врачи Санкт-Петербурга
Арамян Давид Суренович
Рейтинг: 4.9 / 5
Записаться
Богушевич Ирина Геннадьевна
Рейтинг: 4.8 / 5
Записаться
Борисов Сергей Владимирович
Рейтинг: 4.7 / 5
Записаться
Васильев Яков Васильевич
Рейтинг: 4.5 / 5
Записаться
Власьева Ольга Валерьевна
Рейтинг: 4.6 / 5
Записаться
Гриневич Владимир Станиславович
Рейтинг: 4.
Записаться
Поделиться:
Научные источники:
- Тришкин В.А., Барчук А.С., Столяров В.И., Тришкина Е.А., Семенов И.И., Волков О.Н. Лечение легочных метастазов у больных саркомами мягких тканей. // Вопросы онкологии, 1997, — № 2, — с. 154-157.
- Габуния Р.И., Колесникова Е.К. Компьютерная томография в клинической диагностике. М., — Медицина, — 1995, — с. 53 — 131.
- Тюрин И.Е. Компьютерная томография при метастатическом поражении легких. // Вестник рентгенологии и радиологии. 1998, — № 2, — с. 38 — 50.
- Рыбакова Н.И. Рентгенодиагностика метастатических опухолей легких (по материалам Института экспериментальной и клинической онкологии АМН СССР) // дис. докт. Москва, — 1964, с. 314.
- Трущенко С.Г. Возможности магнитно-резонансной томографии в диагностике позвоночно-спинномозговой травмы: Дисс. . канд. мед. наук С.Г.Трущенко. Спб, 1996. — 179 с.
Полезная информация
Гамартома легкого
Что необходимо сделать для диагностики и лечения гамартомы легкого? Для решения данной проблемы пациенту первым шагом необходимо записаться на прием к пульмонологу. После первичного осмотра врач может назначить дополнительные исследования:
КТ органов грудной клетки
МРТ легких
Биопсия с гистологией.
После первичного осмотра врач может назначить дополнительные исследования:
КТ органов грудной клетки
МРТ легких
Биопсия с гистологией.
читать далее +
КТ легких
КТ легких проводят в рамках МСКТ органов грудной клетки, которые включают в себя легкие, бронхи, часть трахеи, лимфоузлы, вилочковую железу, ключицы, ребра. В качестве показаний к проведению мультиспиральной компьютерной томографии выступает: необходимость установления очага воспалительных процессов в легких и бронхах; повреждение сосудистой системы грудной клетки; бронхиальная астма и туберкулез;
читать далее +
МРТ легких и бронхов
МРТ легких — один из диагностических инструментов в арсенале врачей в борьбе за здоровые легкие. К сожалению, заболевания органов дыхания находятся на лидирующих позициях среди наиболее распространенных болезней человека. Статистика неутешительна, процент больных с легочными заболеваниями растет с каждым годом, и успех лечения во многом зависит от своевременной и правильной постановки диагноза. Метод магнитно-резонансной томографии
К сожалению, заболевания органов дыхания находятся на лидирующих позициях среди наиболее распространенных болезней человека. Статистика неутешительна, процент больных с легочными заболеваниями растет с каждым годом, и успех лечения во многом зависит от своевременной и правильной постановки диагноза. Метод магнитно-резонансной томографии
читать далее +
Введите имя*
Ваш e-mail*
Текст отзыва*
Название медицинского учреждения*
Модель оборудования*
Режим работы*
Контактный телефон*
Район*
Адрес*
Метро*
Виды диагностики*
МРТ
КТ
УЗИ
Прайс-лист* Прикрепите файл с прайс листом
Я даю согласие на обработку моих персональных данных
Саркома легких: что это такое? Симптомы и лечение, прогнозы при саркоме легкого
Саркома — это злокачественное новообразование, произрастающее из недифференцированных (незрелых) клеток соединительной ткани. Главное отличие от раковых опухолей заключается в том, что последние возникают из эпителиальных клеток, которые выстилают внутренние органы, кожу и слизистые оболочки, а саркома — из соединительнотканных. Все виды рака имеют привязку к конкретному органу, в то время, как саркома может произрастать в любом месте, где есть соединительная ткань, т. е. в любом месте организма. В том числе и в легких.
Главное отличие от раковых опухолей заключается в том, что последние возникают из эпителиальных клеток, которые выстилают внутренние органы, кожу и слизистые оболочки, а саркома — из соединительнотканных. Все виды рака имеют привязку к конкретному органу, в то время, как саркома может произрастать в любом месте, где есть соединительная ткань, т. е. в любом месте организма. В том числе и в легких.
Саркома легких — это очень редкая опухоль. Она развивается менее чем в 1% всех случаев злокачественных процессов в легких. По некоторым данным на 1 случай саркомы приходится до 250 случаев рака легкого.
Классификация и стадии
- Саркома легких низкой степени злокачественности. Она образуется из более зрелых (дифференцированных) клеток. Они не склонны к быстрому делению, как другие виды сарком, поэтому прогрессирование происходит относительно медленно. Сама опухоль преимущественно состоит из стромы, в которой имеются вкрапления злокачественных клеток.
 Их количество относительно общей массы невелико.
Их количество относительно общей массы невелико. - Саркома со средней степенью злокачественности образуется из клеток низкой степени дифференцировки. В структуре опухоли злокачественные элементы уже имеют преобладающее значение. Помимо этого, имеется хорошее кровоснабжение благодаря разветвленной сосудистой сети. Это способствует раннему метастазированию.
- Саркома легких высокой степени злокачественности образуется из недифференцированных клеток, которые настолько незрелые, что их еще нельзя отнести к какому-либо виду ткани. Они с равной долей вероятности могут стать любой клеткой соединительной ткани. Недифференцированные опухоли легких крайне агрессивны. Они стремительно растут и очень быстро метастазируют, образуя множественные метастатические очаги.
Легкое — это орган, имеющий сложное строение, состоящее из альвеол, бронхиол и бронхов, кровеносных и лимфатических сосудов и других элементов. Все данные структуры имеют клетки соединительной ткани, из которой могут образовываться разные виды высокодифференцированных сарком. Поэтому саркома легкого — это сборное понятие, включающее в себя несколько видов новообразований легких (ангиосаркомы, фибросаркомы и др).
Поэтому саркома легкого — это сборное понятие, включающее в себя несколько видов новообразований легких (ангиосаркомы, фибросаркомы и др).
Недифференцированные саркомы разделяют в зависимости от морфологических особенностей клеток:
- Веретеноклеточные.
- Круглоклеточные.
- Полиморфноклеточные.
Причины возникновения
Причины возникновения саркомы легких неизвестны. Тем не менее, ученые склонны считать, что здесь не обходится без факторов риска, актуальных для рака легких:
- Высокое содержание канцерогенов во вдыхаемом воздухе — курение, в том числе пассивное, проживание в экологически неблагополучных районах, работа на вредных производствах.
- Наследственная предрасположенность — многие саркомы развиваются в детском возрасте. Тем не менее, стоит отметить, что убедительных научных данных, указывающих на связь саркомы легких с наследственностью, на сегодняшний день нет.
- Воздействие высоких доз ионизирующего излучения, в том числе получение лучевой терапии в анамнезе.

- Ультрафиолетовое облучение — злоупотребление загаром, как естественным, так и искусственным.
- Вторичная саркома легкого может развиться в результате метастазирования опухоли из другого органа.
Определение стадии саркомы легкого основано на размерах опухоли и наличии метастазов:
- 1 стадия — опухоль легких имеет размер, не превышающий 3 см. Метастазов нет.
- 2 стадии — размеры опухоли не превышают 6 см в наибольшем измерении, имеются единичные метастазы в регионарные лимфатические узлы, расположенные перибронхиально или в корне легкого.
- 3 стадия — размеры опухолевого инфильтрата превышают 6 см, имеются метастазы в лимфатические узлы средостения или плевру.
- 4 стадия — опухоль может быть любого размера, но имеются отдаленные метастазы, в том числе поражающие другие органы.
Симптомы саркомы легкого
Симптомы саркомы аналогичны симптомам рака легкого, с той разницей, что прогрессируют гораздо быстрее. Проявление болезни будет зависеть от локализации опухоли и стадии заболевания.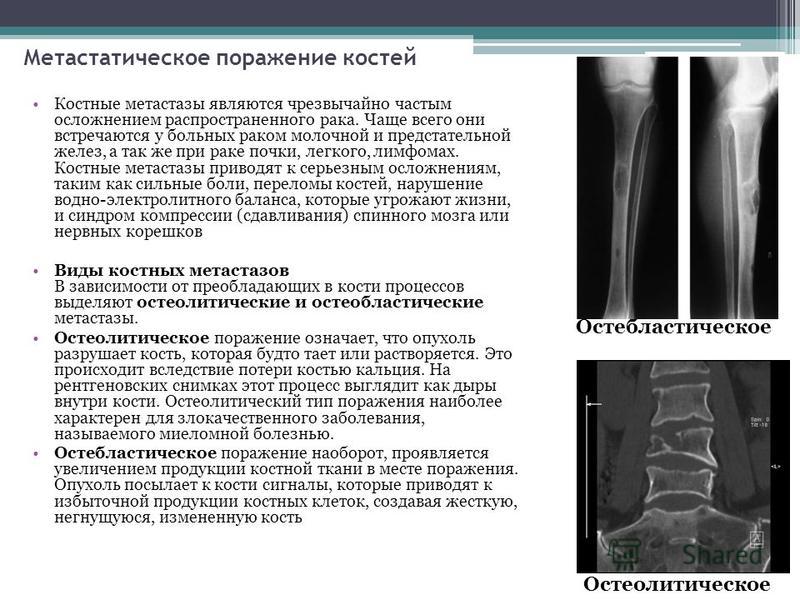
Если саркома растет внутри бронха, она может приводить к его закупорке с развитием сухого надсадного кашля. После обтурации (перекрытия) бронха появляется мокрота слизистого или слизисто-гнойного характера. При распаде опухоли или повреждении кровеносных сосудов может возникнуть кровохарканье или легочное кровотечение. Также присутствует одышка и боли в груди.
Из вторичных проявлений присутствует повышение температуры тела, слабость и отсутствие аппетита. Если саркома проросла за пределы легкого, появляются другие признаки:
- При поражении пищевода — нарушение глотания, дисфагия.
- Сдавление венозных стволов — синдром верхней полой вены. Отек, цианоз и расширение вен в верхней половине тела.
- Если опухоль легких проросла в плевру, развиваются геморрагический плеврит, при поражении оболочек сердца — геморрагический перикардит.
Диагностика
Ключевое значение для обнаружения саркомы легких играет рентгенологическое исследование, в частности компьютерная томография.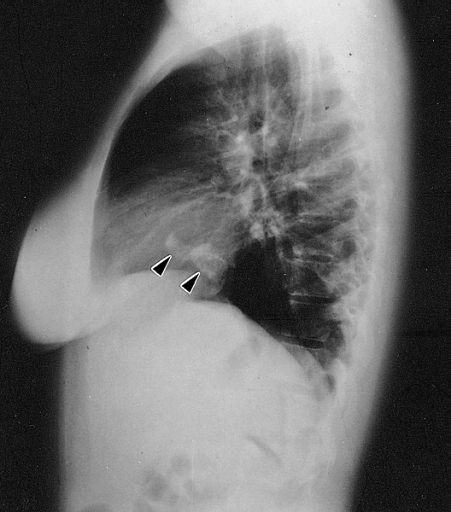 На снимках обнаруживают тень с нечеткими контурами. При проведении контрольного снимка в динамике эта тень увеличивается в размерах. Если саркома растер в просвет бронха, ее можно обнаружить на бронхоскопии.
На снимках обнаруживают тень с нечеткими контурами. При проведении контрольного снимка в динамике эта тень увеличивается в размерах. Если саркома растер в просвет бронха, ее можно обнаружить на бронхоскопии.
Окончательная постановка диагноза возможна только после гистологического исследования. С этой целью проводят эндоскопическую биопсию, тонкоигольную трансторакальную биопсию под контролем КТ. В ряде случаев гистологическое исследование возможно только после оперативного удаления саркомы. Также помочь с диагнозом может цитологическое исследование экссудата при плеврите.
Лечение
Способ лечения саркомы легкого у конкретного пациента определяется локализацией опухоли, ее гистологическим типом и стадией. Как правило, требуется комплексный подход, включающий в себя хирургическую операцию, химио- и/или лучевую терапию.
Химиотерапия
Чаще всего, лечение саркомы легких начинается с курса интенсивной полихимиотерапии. Она может длиться несколько недель. Цель этого курса — уменьшить размер опухоли легких и по возможности уничтожить метастазы, в том числе микрометастазы, которые еще не видны на снимках. Это позволяет провести операцию максимально щадяще и в то же время радикально, удалив всю опухоль.
Это позволяет провести операцию максимально щадяще и в то же время радикально, удалив всю опухоль.
Чтобы лечение было максимально эффективным, назначается комбинация из нескольких препаратов, которые подбираются с учетом морфологических и цитогенетических особенностей саркомы. Затем проводится операция или лучевая терапия.
После этого опять назначается полихимиотерапия. Ее интенсивность будет зависеть от изначального объема опухоли и ее первичного ответа на первую химиотерапию. Если прогноз хороший, проводят несколько блоков цитостатической химиотерапии. При неблагоприятном прогнозе (агрессивная опухоль, распространенная стадия) рассматривается вариант высокодозной полихимиотерапии с поддерживающей трансплантацией гемопоэтических стволовых клеток.
Хирургическое лечение саркомы
Хирургическое лечение саркомы легкого предполагает следующие типы операций:
- Лобэктомия — удаление доли легкого.
- Пульмонэктомия — удаление всего легкого.
Обязательно проводится иссечение регионарных лимфатических узлов. Если радикальное удаление невозможно, проводят паллиативные операции, направленные на устранение тягостных симптомов и улучшение качества жизни пациентов.
Если радикальное удаление невозможно, проводят паллиативные операции, направленные на устранение тягостных симптомов и улучшение качества жизни пациентов.
Если саркома легкого носит вторичный характер и является метастазом опухоли, локализованной в другом органе, могут быть проведены одномоментные операции с удалением всех патологических очагов. Это помогает существенно увеличить продолжительность жизни больных, а в ряде случаев добиться радикальности лечения.
Лучевая терапия
Лучевая терапия применяется в качестве комплексного лечения высокозлокачественных сарком легких или при невозможности проведения хирургических операций, в том числе, в рамках паллиативного лечения. Могут использоваться гамматерапия, электронотерапия, брахитерапия и селективная внутренняя радиотерапия, когда радиоизотопы вводят в кровеносные сосуды, питающие опухоль.
Иммунотерапия
На иммунотерапию сарком возлагаются большие надежды. Суть данного лечения заключается в том, чтобы сделать злокачественные клетки «заметными» для иммунной системы организма, дабы она смогла их уничтожить. Главная сложность заключается в том, что видов сарком очень много, и разработать единое лекарство не представляется возможным. Какие-то виды опухоли могут реагировать на один метод иммунотерапии, у других же он будет неэффективен. Наиболее известным препаратом для лечения сарком легких является Оларатумаб, который был одобрен к использованию в 2016 году, но исследование его эффективности продолжается.
Главная сложность заключается в том, что видов сарком очень много, и разработать единое лекарство не представляется возможным. Какие-то виды опухоли могут реагировать на один метод иммунотерапии, у других же он будет неэффективен. Наиболее известным препаратом для лечения сарком легких является Оларатумаб, который был одобрен к использованию в 2016 году, но исследование его эффективности продолжается.
Послеоперационное восстановление
Операции на легком являются серьезным хирургическим вмешательством. Первое время после резекции или удаления легкого организм приспосабливается к новым условиям дыхания. Для того, чтобы помочь ему, первое время пациент использует кислородную маску. Также необходимо выполнять специальные дыхательные упражнения и своевременно отхаркивать мокроту. Проведению этих процедур может препятствовать выраженный болевой синдром, поэтому, чтобы его купировать, пациенту предлагают обезболивание, вплоть до эпидуральной анестезии. Постепенно оставшаяся ткань легкого возьмёт на себя всю нагрузку и процесс дыхания наладится. Сроки восстановления будут зависеть от исходного состояния пациента.
Сроки восстановления будут зависеть от исходного состояния пациента.
Амбулаторное наблюдение
После окончания курса лечения, за больным устанавливается амбулаторное наблюдение. В первые 2–3 года он должен посещать врача раз в 4 месяца, на 4–5 год — раз в 6 месяцев и далее ежегодно. Для своевременного обнаружения рецидива врач назначит специальное обследование:
- Рентген органов грудной клетки.
- УЗИ.
- КТ и/или МРТ.
Кратность прохождения данных исследований определяется врачом индивидуально.
При возникновении рецидива саркомы и ее дальнейшем прогрессировании, развиваются тяжелые осложнения, которые могут привести к смерти больного:
- Распад опухоли с кровотечением.
- Инфекционные осложнения на фоне снижения иммунитета из-за химиотерапии и действия опухоли. Как правило, возникают упорные, неподдающиеся лечению пневмонии и плевриты.
- Ателектазы — спадение доли легкого.
- Тяжелое истощение (кахексия).
- Помимо этого, наблюдаются осложнения со стороны органов, пораженных метастазами.

Прогноз выживаемости
Прогноз при саркоме легкого зависит от морфологических характеристик опухоли и стадии распространенности процесса. При благоприятных условиях (1–2 стадия высокодифференцированной саркомы) пятилетняя выживаемость пациентов составляет приблизительно 50%. При 3–4 стадии или высокозлокачественном типе саркомы, пятилетняя выживаемость не превышает 20%.
Запись на консультацию круглосуточно
+7 (495) 668-82-28
Чрезвычайно редкая первичная саркома легкого с метастазами в брюшную и тонкую кишку: клинический случай | Всемирный журнал хирургической онкологии
- Отчет о клиническом случае
- Открытый доступ
- Опубликовано:
- Саня Плештина 1 ,
- Никша Либреняк 2 ,
- Анте Марушич 3 ,
- Ловорка Бателя Вулетич 4 ,
- Зоран Яневски 5 и
- …
- Марко Якопович 6 90 015
Всемирный журнал хирургической онкологии том 17 , Номер статьи: 147 (2019) Процитировать эту статью
4557 доступов
5 Цитаты
Сведения о показателях
Abstract
История вопроса
Первичная саркома легкого — очень редкая злокачественная опухоль, составляющая менее 0,5% всех опухолей легких и представляющая трудности в диагностике и лечении. Мы описываем случай пациента с диагнозом первичной недифференцированной плеоморфной саркомы легкого, у которого развились последующие метастазы в брюшину и тонкий кишечник, что свидетельствует о весьма необычном проявлении заболевания.
Мы описываем случай пациента с диагнозом первичной недифференцированной плеоморфной саркомы легкого, у которого развились последующие метастазы в брюшину и тонкий кишечник, что свидетельствует о весьма необычном проявлении заболевания.
Описание клинического случая
57-летний мужчина поступил с обширной частично некротической опухолью в левой верхней доле (ВЛЛ) легкого, которая вовлекла бронх ВНЛ и распространилась на висцеральную плевру. Признаков узловой или висцеральной диссеминации не было. После первоначального обращения пациент был госпитализирован в пульмонологическое отделение больницы для дальнейшего обследования. Наиболее вероятным диагнозом на основании биоптата была низкодифференцированная саркома. Выполнена левосторонняя пневмонэктомия с диссекцией медиастинальных лимфатических узлов. Заключительный патоморфологический диагноз (ПГД): недифференцированная плеоморфная саркома (НПС). Через три месяца после операции на легких была проведена повторная компьютерная томография, которая показала 60-мм обструктивное метастатическое внутрибрюшное поражение с инфильтрацией тонкой кишки и отдельными отложениями на брюшине. К сожалению, потребовалась срочная операция, так как у больного появились признаки острого живота вследствие перфорации кишечника. Только через 2 месяца пациент скончался дома.
К сожалению, потребовалась срочная операция, так как у больного появились признаки острого живота вследствие перфорации кишечника. Только через 2 месяца пациент скончался дома.
Выводы
Варианты лечения УПС основаны на алгоритмах, используемых при лечении поражений конечностей с хорошо известной ролью хирургии. Тем не менее, роль периоперационной химиотерапии остается сомнительной, и нет убедительных данных, основанных на доказательствах, из-за редкости заболевания. Тонкая кишка является неожиданным местом метастазирования, но имеет большое клиническое значение.
Предыстория
Недифференцированная плеоморфная саркома (UPS) — редкая опухоль, составляющая менее 0,2% всех опухолей легких [1,2,3] и, следовательно, представляет собой проблему диагностики и лечения. Это образование называлось злокачественной фиброзной гистиоцитомой до 2012 года, когда Всемирная организация здравоохранения реклассифицировала его как недифференцированную плеоморфную саркому. Саркома мягких тканей обычно поражает конечности или брюшную полость и таз, хотя может возникать в любом месте тела [4]. О метастазах в легкие от внелегочных первичных сарком сообщалось чаще, чем о первичных легочных саркомах. Со времени первого сообщения о первичной легочной ЗФГ 40 лет назад в литературе, доступной на английском языке, было зарегистрировано примерно 50 дополнительных случаев [3, 5]. В этой статье мы представляем случай пациента с первичной недифференцированной плеоморфной саркомой легкого с последующими кишечными и перитонеальными метастазами, что является довольно необычным проявлением заболевания.
Саркома мягких тканей обычно поражает конечности или брюшную полость и таз, хотя может возникать в любом месте тела [4]. О метастазах в легкие от внелегочных первичных сарком сообщалось чаще, чем о первичных легочных саркомах. Со времени первого сообщения о первичной легочной ЗФГ 40 лет назад в литературе, доступной на английском языке, было зарегистрировано примерно 50 дополнительных случаев [3, 5]. В этой статье мы представляем случай пациента с первичной недифференцированной плеоморфной саркомой легкого с последующими кишечными и перитонеальными метастазами, что является довольно необычным проявлением заболевания.
Описание случая
57-летний мужчина был госпитализирован в отделение легочной онкологии Центра университетской больницы Загреба в ноябре 2017 года с кашлем и кровохарканьем. Он выкуривал 27 пачек в год, злоупотреблял алкоголем в анамнезе, у него не было никаких признаков новообразований мягких тканей в настоящем или прошлом или радиационного облучения в анамнезе. Его оценка по Карновски составила 80. Последующее физикальное обследование выявило снижение поступления воздуха в левое легкое. Общий анализ крови и биохимические показатели были в пределах нормы. Первоначальная рентгенограмма грудной клетки показала обширное уплотнение в левом легком, предполагающее возможное злокачественное новообразование; Рекомендовано КТ грудной клетки и брюшной полости. КТ показала обширную частично некротическую опухоль в левой верхней доле (LUL), простирающуюся от левого ворота с инфильтрацией бронха LUL до висцеральной плевры, размером 74 мм в наибольшем диаметре (рис. 1).
Его оценка по Карновски составила 80. Последующее физикальное обследование выявило снижение поступления воздуха в левое легкое. Общий анализ крови и биохимические показатели были в пределах нормы. Первоначальная рентгенограмма грудной клетки показала обширное уплотнение в левом легком, предполагающее возможное злокачественное новообразование; Рекомендовано КТ грудной клетки и брюшной полости. КТ показала обширную частично некротическую опухоль в левой верхней доле (LUL), простирающуюся от левого ворота с инфильтрацией бронха LUL до висцеральной плевры, размером 74 мм в наибольшем диаметре (рис. 1).
Обширная частично некротическая опухоль в LUL легкого
Изображение в натуральную величину
При поступлении признаков узловой или висцеральной диссеминации не было. Выполнено бронхоскопическое исследование с биопсией и взят образец из бронха LUL. Гистопатологический анализ показал почти полностью некротизированную опухоль с долей менее 10% жизнеспособных плеоморфных опухолевых клеток, экспрессирующих виментин и CD99, и фокальный положительный десмин. Отсутствовала экспрессия AE1/AE3, p40, TTF-1, напсина А, эпителиального мембранного антигена (ЕМА), CK7 и S100. Наиболее вероятным диагнозом была низкодифференцированная саркома.
Отсутствовала экспрессия AE1/AE3, p40, TTF-1, напсина А, эпителиального мембранного антигена (ЕМА), CK7 и S100. Наиболее вероятным диагнозом была низкодифференцированная саркома.
Для окончательной стадии была проведена ПЭТ/КТ, которая не показала экстраторакального распространения заболевания. Междисциплинарная комиссия по опухолям сочла, что операция на легких была лучшей альтернативой лечению, и через несколько недель была выполнена левосторонняя пневмонэктомия с диссекцией медиастинальных лимфатических узлов. Окончательный патогистологический анализ показал размер опухоли 100 × 85 × 71 мм, более 80% которой были некротическими. Плеоморфные опухолевые клетки показали тот же иммуногистохимический профиль, что и в биоптате. Синовиальная саркома-ассоциированная транслокация была отрицательной. Все хирургические края и рассеченные медиастинальные лимфатические узлы были свободны от опухолей. На основании этого был поставлен окончательный диагноз недифференцированная плеоморфная саркома (3 степень) (рис. 2).
2).
Иммуногистохимия и микроскопия УПС
Изображение в натуральную величину
Пациент хорошо восстановился после операции, последующее наблюдение было запланировано. При первом последующем посещении через 7 недель после операции на легких у пациента не было злокачественного заболевания по данным физического осмотра и рентгенографии грудной клетки. Через три месяца после операции на легких была проведена контрольная компьютерная томография, которая показала 60-мм метастатическое интраабдоминальное поражение с явным поражением тонкой кишки, а также отдельные злокачественные новообразования в брюшине. Сканирование также показало легкое восходящее расширение тонкой кишки, свидетельствующее о частичной непроходимости (рис. 3).
Рис. 3Сравнительная КТ брюшной полости в ноябре 2017 г. и апреле 2018 г. с впервые развившимися внутрибрюшными метастазами и дилатацией тонкой кишки
Изображение в натуральную величину
Таким образом, была запланирована абдоминальная операция. Однако уже через пару дней пациент поступил в отделение неотложной помощи с клиническими признаками острого живота вследствие перфорации кишечника. Выполнена срочная абдоминальная операция с резекцией перфорированного сегмента подвздошной кишки, инфильтрированного опухолью. Затем накладывают монополярную илеостому. Гистопатологический анализ подтвердил метастазирование недифференцированной саркомы (рис. 4).
Однако уже через пару дней пациент поступил в отделение неотложной помощи с клиническими признаками острого живота вследствие перфорации кишечника. Выполнена срочная абдоминальная операция с резекцией перфорированного сегмента подвздошной кишки, инфильтрированного опухолью. Затем накладывают монополярную илеостому. Гистопатологический анализ подтвердил метастазирование недифференцированной саркомы (рис. 4).
Гистологические препараты поражения легкого и тонкой кишки
Изображение в натуральную величину
Пациент был выписан из больницы через 9 дней с оценкой по шкале Карновского 40; таким образом, была показана наилучшая поддерживающая терапия. Больной умер дома через 2 мес.
Обсуждение
Первичные легочные саркомы встречаются крайне редко и составляют от 0,1 до 0,5% всех случаев легочных новообразований. Наиболее распространенные саркомы включают лейомиосаркому, злокачественную фиброзную гистиоцитому и синовиальную саркому [6, 7]. Симптомы и рентгенологические проявления аналогичны таковым при более распространенных карциномах легких. Рентгенологические признаки сарком вариабельны, не специфичны для поражения и недостаточны для того, чтобы предложить специфический диагноз [8]. Клиническая картина заболевания больше зависит от локализации опухоли, чем от гистопатологических особенностей [9].]. После исключения злокачественного новообразования эпителия наиболее важной дифференциальной диагностикой первичной легочной саркомы является метастатическое распространение внелегочной саркомы. Другие дифференциальные диагнозы включают плеоморфную карциному легкого, легочную саркоматоидную карциному и злокачественную меланому. Поэтому необходим подробный анамнез и соответствующее диагностическое обследование для уточнения первичного легочного происхождения опухоли. Поскольку пациенты с диагнозом саркома легких встречаются довольно редко, трудно определить надежный протокол ведения таких пациентов [2].
Симптомы и рентгенологические проявления аналогичны таковым при более распространенных карциномах легких. Рентгенологические признаки сарком вариабельны, не специфичны для поражения и недостаточны для того, чтобы предложить специфический диагноз [8]. Клиническая картина заболевания больше зависит от локализации опухоли, чем от гистопатологических особенностей [9].]. После исключения злокачественного новообразования эпителия наиболее важной дифференциальной диагностикой первичной легочной саркомы является метастатическое распространение внелегочной саркомы. Другие дифференциальные диагнозы включают плеоморфную карциному легкого, легочную саркоматоидную карциному и злокачественную меланому. Поэтому необходим подробный анамнез и соответствующее диагностическое обследование для уточнения первичного легочного происхождения опухоли. Поскольку пациенты с диагнозом саркома легких встречаются довольно редко, трудно определить надежный протокол ведения таких пациентов [2].
Иммуногистохимия играет важную роль в точной диагностике и классификации типа саркомы. Он часто бывает положительным на кератин, актин, десмин, EMA, CD99 и CD34, но положительные окрашивания обычно не помогают в диагностике, поэтому УПС является диагнозом исключения [10]. В нашем случае не было признаков эпителиальной дифференцировки. Белок S-100, который может быть положительным при злокачественной опухоли оболочки периферического нерва и меланоме, был отрицательным. Синовиальная саркома характеризуется тучными клетками внутри опухоли, но в данном случае их не обнаружено. Характерная транслокация для синовиальной саркомы была отрицательной. Микроскопическое описание, характерное для УПС, имелось и в опухолевой ткани нашего больного: сториформный рисунок, неправильные пучки, переменная клеточность, плеоморфные и причудливые опухолевые клетки с пенистой цитоплазмой и выраженной атипией; на фоне воспаленной коллагеновой стромы выявлялись многоядерные гигантские клетки, а также многочисленные митотические фигуры, в том числе атипичные формы. Степень опухоли определяли в соответствии с системными критериями FNCLCC.
Он часто бывает положительным на кератин, актин, десмин, EMA, CD99 и CD34, но положительные окрашивания обычно не помогают в диагностике, поэтому УПС является диагнозом исключения [10]. В нашем случае не было признаков эпителиальной дифференцировки. Белок S-100, который может быть положительным при злокачественной опухоли оболочки периферического нерва и меланоме, был отрицательным. Синовиальная саркома характеризуется тучными клетками внутри опухоли, но в данном случае их не обнаружено. Характерная транслокация для синовиальной саркомы была отрицательной. Микроскопическое описание, характерное для УПС, имелось и в опухолевой ткани нашего больного: сториформный рисунок, неправильные пучки, переменная клеточность, плеоморфные и причудливые опухолевые клетки с пенистой цитоплазмой и выраженной атипией; на фоне воспаленной коллагеновой стромы выявлялись многоядерные гигантские клетки, а также многочисленные митотические фигуры, в том числе атипичные формы. Степень опухоли определяли в соответствии с системными критериями FNCLCC.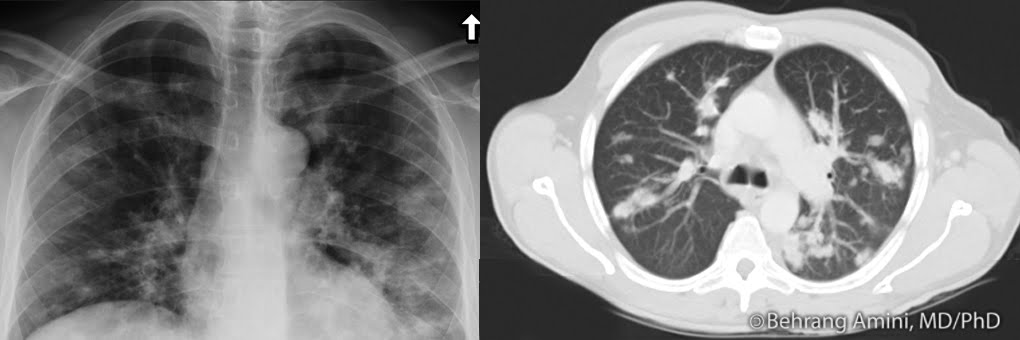
Варианты лечения основаны на алгоритмах, используемых при лечении поражений конечностей, с общепризнанной ролью широкой хирургической резекции, направленной на освобождение от опухоли краев, в качестве основного терапевтического метода. Некоторые авторы обнаружили, что полнота резекции коррелировала со значительным увеличением выживаемости, но не с размером и степенью опухоли [11]. Радикальная резекция признана единственным методом лечения, который может обеспечить излечение или пролонгацию жизни, если опухоль кажется операбельной [2, 12, 13]. С другой стороны, роль периоперационной химиотерапии до сих пор остается спорной [13, 14]. По последним данным, периоперационная химиотерапия не улучшает общую выживаемость. Единственным независимым фактором, связанным с лучшей выживаемостью, является лечебная резекция с микроскопически отрицательным краем [15]. Имеются данные о более высокой частоте поражения лимфоузлов при первичных саркомах легких, чем при саркомах мягких тканей конечностей. Поэтому у пациентов с первичной саркомой легкого прогноз значительно хуже [16]. Принимая во внимание эти доказательства, мы решили не лечить пациента неоадъювантной химиотерапией. После предварительной радикальной операции с обширной медиастинальной лимфаденэктомией, которая показала четкие края и отсутствие поражения лимфоузлов, мы также решили не проводить адъювантную химиотерапию. Было рекомендовано тщательное наблюдение из-за относительно высокой частоты рецидивов.
Поэтому у пациентов с первичной саркомой легкого прогноз значительно хуже [16]. Принимая во внимание эти доказательства, мы решили не лечить пациента неоадъювантной химиотерапией. После предварительной радикальной операции с обширной медиастинальной лимфаденэктомией, которая показала четкие края и отсутствие поражения лимфоузлов, мы также решили не проводить адъювантную химиотерапию. Было рекомендовано тщательное наблюдение из-за относительно высокой частоты рецидивов.
Роль адъювантной лучевой терапии до сих пор остается неоднозначной. Она может обеспечить приемлемый локальный контроль над некоторыми саркомами мягких тканей после хирургической резекции [17], но также имеются опубликованные данные не в пользу адъювантной лучевой терапии [2]. Таким образом, нет убедительных доказательных данных о том, что лучевая терапия является неотъемлемой частью адъювантного лечения первичной саркомы легкого.
Эти новообразования имеют агрессивное клиническое течение с высокой вероятностью рецидива и метастазирования. На поздних стадиях в качестве паллиативного подхода может использоваться комбинация химиотерапии или лучевой терапии, хотя опухоль кажется нечувствительной как к химиотерапии, так и к лучевой терапии [3]. Общая медиана выживаемости составляет от 24 до 48 месяцев согласно ретроспективным обзорам пациентов с первичной саркомой легких с различными гистологическими типами (mOS 17 месяцев для сарком 3 степени) [9]., 12]. Однако, несмотря на агрессивное поведение саркомы легких, есть несколько сообщений о пациентах с длительной выживаемостью.
На поздних стадиях в качестве паллиативного подхода может использоваться комбинация химиотерапии или лучевой терапии, хотя опухоль кажется нечувствительной как к химиотерапии, так и к лучевой терапии [3]. Общая медиана выживаемости составляет от 24 до 48 месяцев согласно ретроспективным обзорам пациентов с первичной саркомой легких с различными гистологическими типами (mOS 17 месяцев для сарком 3 степени) [9]., 12]. Однако, несмотря на агрессивное поведение саркомы легких, есть несколько сообщений о пациентах с длительной выживаемостью.
В течение короткого периода наблюдения у нашего пациента развилась неожиданная перитонеальная диссеминация, о которой, насколько нам известно, еще не сообщалось как о месте метастатического распространения первичной легочной саркомы. В литературе описан один случай метастазирования в сердце недифференцированной плеоморфной саркомы легкого с симптоматической правожелудочковой сердечной недостаточностью [18] и лечения хирургической резекцией.
Признаками высокого риска в нашем случае были низкодифференцированная гистология и размер опухоли; таким образом, несмотря на радикальную операцию с полной резекцией, четкими краями и отсутствием поражения узлов, пациент скончался менее чем через год после постановки диагноза.
Заключение
Первичная недифференцированная плеоморфная саркома легкого остается крайне редкой злокачественной опухолью без стандартизированного лечения и с плохим прогнозом. Оптимальная стратегия лечения еще не выяснена из-за ограниченности имеющихся данных, хотя полное хирургическое иссечение остается предпочтительным вариантом лечения. Необходимы дальнейшие исследования и сбор данных из клинической практики для улучшения результатов, оптимизации лечения и определения последующего подхода к этому агрессивному злокачественному новообразованию.
Наличие данных и материалов
Данные можно получить у соответствующего автора по обоснованному запросу.
Сокращения
- CT:
Компьютерная томография
- EMA:
Антиген эпителиальной мембраны
- FNCLCC:
Национальная федерация центров борьбы с раком
- ЛУЛ:
Левая верхняя доля
- MFH:
Злокачественная фиброзная гистиоцитома
- ПЭТ/КТ:
Позитронно-эмиссионная томография/компьютерная томография
- тел.
 :
: Патогистологический диагноз
- ИБП:
Недифференцированная плеоморфная саркома
Ссылки
Манкин Х.Дж., Хорничек Ф.Дж. Диагностика, классификация и лечение сарком мягких тканей. Контроль рака. 2005; 12:5–21.
Артикул Google Scholar
Джошгун Т., Тезел Ю., Акыл М., Колбаш И., Шен А., Тезел Ч. Первичная злокачественная фиброзная гистиоцитома легких. Терк Торак Дж. 18 апреля 2017 г. (2): 54–56.
Артикул Google Scholar
Li X, Liu R, Shi T, et al. Первичная злокачественная фиброзная гистиоцитома легких: клинический случай и обзор литературы. Дж. Торак Дис. 2017 авг; 9 (8): E702–8.
Артикул Google Scholar
- «>
Goldblum JR, Weiss SW, Enzinger FM, редакторы. Опухоли мягких тканей Энцингера и Вейса. 6-е изд. Филадельфия: Эльзевир Сондерс; 2014.
Патель Д.П., Ганди Ю.С., Соммерс К.Е., Мангар Д., Кампореси Э.М. Первичная злокачественная фиброзная гистиоцитома легких. Представитель дела Пульмонол. 2015;2015:381276.
ПабМед ПабМед Центральный Google Scholar
Кил С.Б., Бача Э., Марк Э.Дж. и др. Первичная легочная саркома: клинико-патологическое исследование 26 случаев. Мод Патол. 1999; 12:1124–31.
КАС пабмед Google Scholar
Ву Дж. М., Монтгомери Э. Классификация и патология. Surg Clin North Am. 2008;88:483–520 Вернуться к процитированному тексту №. 2.
Артикул Google Scholar
Чакир О., Топал У.
 , Байрам А.С., Толунай С. Саркомы: редкие первичные злокачественные опухоли грудной клетки. Диагн Интерв Радиол. 2005;11(1):23–7.
, Байрам А.С., Толунай С. Саркомы: редкие первичные злокачественные опухоли грудной клетки. Диагн Интерв Радиол. 2005;11(1):23–7.ПабМед Google Scholar
Этьен-Мастроянни Б., Фальчеро Л., Шалабрейс Л., Луара Р., Раншер Д., Суке П.Дж. и др. Первичные саркомы легкого: клинико-патологическое исследование 12 случаев. Рак легких. 2002; 38: 283–9..
Артикул Google Scholar
Голдблюм младший. Подход к плеоморфным саркомам: можем ли мы подклассифицировать и имеет ли это значение? Мод Патол. 2014;27(S1). https://doi.org/10.1038/modpathol.2013.174.
Артикул Google Scholar
Bacha EA, Wright CD, Grillo HC, Wain JC, Moncure A, Keel SB, Donahue DM, Mathisen DJ. Хирургическое лечение первичных сарком легких. Eur J Cardiothorac Surg. 1999;15(4):456–60.
Артикул КАС Google Scholar
Janssen JP1, Mulder JJ, Wagenaar SS, Elbers HR, van den Bosch JM. Первичная саркома легкого: клиническое исследование с длительным наблюдением. Энн Торак Серг. 1994;58(4):1151–5.
Артикул КАС Google Scholar
Halyard MY, Camoriano JK, Culligan JA, Weiland LH, Allen MS, Pluth JR, Pairolero PC. Злокачественная фиброзная гистиоцитома легкого. Отчет о четырех случаях и обзор литературы. Рак. 1996 15 декабря; 78 (12): 2492–7.
Артикул КАС Google Scholar
Уайлдер Ф., Д’Анджело С., Краго А.М. Опухоли мягких тканей туловища: лечение локального заболевания молочной железы, грудной клетки и брюшной стенки. Дж. Хирург Онкол. 2015;111:546e552.
Артикул Google Scholar
- «>
Ю П.Ю., Бил Э.В., Хьюз Т.М., Суарес-Келли Л.П., Шелби Р.Д., Этан К.Г., Ховард Дж.Х. Периоперационная химиотерапия не связана с улучшением выживаемости при саркоме ствола высокой степени злокачественности. J Surg Res. 2018; 231: 248–56. https://doi.org/10.1016/j.jss.2018.05.030.
Артикул пабмед Google Scholar
Spraker M, Bair E, Bair R, Connell P, Mahmood U, Koshy M. Анализ характеристик пациентов и клинических исходов при первичной саркоме легких. Дж. Торак Онкол. 2013;8(2):147–51.
Артикул Google Scholar
Zagars GK, Mullen JR, Pollack A. Злокачественная фиброзная гистиоцитома: исход и прогностические факторы после органосохраняющей операции и лучевой терапии. Int J Radiat Oncol Biol Phys. 1996 15 марта; 34 (5): 983–94.
Артикул КАС Google Scholar
- «>
Xu G, Shi X, Shao G. Необычный случай метастазирования легочной недифференцированной плеоморфной саркомы в правый желудочек: клинический случай. J Med Case Rep. 2013; 7:165.
Артикул Google Scholar
Ссылки на скачивание
Благодарности
Неприменимо.
Финансирование
Не применимо.
Информация об авторе
Авторы и организации
Кафедра респираторных заболеваний, UHC Zagreb, Медицинский факультет Университета Риеки, Jordanovac 104, 10000, Zagreb, Croatia
Sanja Pleština 90 045
Отделение онкологии, UHC Zagreb , Kišpatićeva 12, 10000, Zagreb, Croatia
Nikša Librenjak
Отделение радиологии, UHC Zagreb, Kišpatićeva 12, 10000, Zagreb, Croatia
Ante Marusic
Кафедра патологии, UHC Zagreb, Медицинский факультет Загребского университета, Kišpatićeva 12, 10000, Загреб, Хорватия
Lovorka Batelja Vuletić
9000 4Хирургическое отделение UHC Zagreb, Jordanovac 104, 10000 , Загреб, Хорватия
Зоран Яневски
Кафедра респираторных заболеваний, UHC Загреб, Медицинский факультет Загребского университета, Йордановац 104, 10000, Загреб, Хорватия
Марко Якопович
Авторы
- Саня Плештина
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Nikša Librenjak
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Ante Marusić
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Академия
- Lovorka Batelja Vuletić
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Zoran Janevski
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Marko Jakopović
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Академия
Пожертвования
С. П. принимала активное участие в написании рукописи, ее составлении, поиске литературы и лечении пациента. NL проанализировала и интерпретировала данные пациентов и приняла участие в поиске литературы. ZJ лечил пациента и участвовал в написании рукописи. AM участвовал в диагностике и принятии решений о лечении, а также помогал в написании и рентгенологических снимках. ЛБВ провел гистологическое исследование опухолей и предоставил картины опухолевой патологии. MJ принимал участие в принятии решений о лечении и написании. Все авторы прочитали и одобрили окончательный вариант рукописи.
П. принимала активное участие в написании рукописи, ее составлении, поиске литературы и лечении пациента. NL проанализировала и интерпретировала данные пациентов и приняла участие в поиске литературы. ZJ лечил пациента и участвовал в написании рукописи. AM участвовал в диагностике и принятии решений о лечении, а также помогал в написании и рентгенологических снимках. ЛБВ провел гистологическое исследование опухолей и предоставил картины опухолевой патологии. MJ принимал участие в принятии решений о лечении и написании. Все авторы прочитали и одобрили окончательный вариант рукописи.
Авторы переписки
Переписка с Саня Плештина или Никша Либреняк.
Декларация этики
Одобрение этики и согласие на участие
Неприменимо.
Согласие на публикацию
Было получено письменное информированное согласие на публикацию данного клинического случая и прилагаемых изображений от родственника пациента. Копия письменного согласия доступна для ознакомления главному редактору этого журнала.
Конкурирующие интересы
Авторы заявляют, что у них нет конкурирующих интересов.
Дополнительная информация
Примечание издателя
Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Права и разрешения
Открытый доступ Эта статья распространяется на условиях международной лицензии Creative Commons Attribution 4.0 (http://creativecommons.org/licenses/by/4.0/), которая разрешает неограниченное использование, распространение, и воспроизведение на любом носителе, при условии, что вы укажете автора(ов) оригинала и источник, предоставите ссылку на лицензию Creative Commons и укажете, были ли внесены изменения. Отказ от права Creative Commons на общественное достояние (http://creativecommons.org/publicdomain/zero/1.0/) применяется к данным, представленным в этой статье, если не указано иное.
Перепечатки и разрешения
Об этой статье
Первичная саркома легкого – прогностическое значение клинико-патологических характеристик 26 случаев
Научная статьяКлинические исследования
ХОСЕ ДЮРАН-МОРЕНО, СТЕФАНИЯ КОККА ЛИ, ВАСИЛЕЙОС РАМФИДИС, МАРИЯ САЛОМИДУ, АНТОНИЯ ДИГКЛИЯ, АННА КУМАРИАНУ, ПЕРИКЛИС ТОМОС, НЕКТАРИОС КУФОПУЛОС, ИОАННИС ВАМВАКАРИС, ЭЛЕНИ ПСИХОГИУ и КОНСТАНТИНОС СИРИГОС
Противораковые исследования, март 2020 г. , 40 (3) 1697-1703; DOI. 0061
, 40 (3) 1697-1703; DOI. 0061
Предпосылки/Цель: Первичные саркомы легких (PSL ) представляют собой редкое, в значительной степени неизвестное существо. Здесь мы представляем ретроспективное исследование 26 пациентов с диагнозом ПСЛ. Пациенты и методы. В течение 10 лет были собраны и проанализированы истории болезни пациентов из 5 центров. Результаты: средний возраст на момент постановки диагноза составил 61,9 года.6 лет (диапазон = 31-75 лет). У восьми пациентов (33,33%) была инвазия медиастинального узла (MNI). Из 17 больных (70,83%) с локализованным заболеванием 11 (64,70%) оперированы. Частота рецидивов составила 72,72%. Медиана безрецидивного периода составила 15 месяцев. Медиана общей выживаемости (ОВ) пациентов с метастазами составила 4 месяца и 10 месяцев для всей популяции. Только операция повлияла на выживаемость. Заключение: Прогноз ПСЛ мрачный. Высокая доля пациентов с МНИ при постановке диагноза может служить показанием для хирургической оценки средостения и поднимает вопрос о том, следует ли лечить пациентов с локорегионарным ПСЛ более агрессивным подходом.
- Саркома легкого
- эпидемиология
- прогностические факторы
- выживаемость
Первичные саркомы легкого (ПСЛ) составляют гетерогенную группу редких злокачественных опухолей, на долю которых приходится менее 0 0,5% злокачественных опухолей легких (1). Они возникают из мезенхимальной ткани сосудов бронхиальной стенки или легочной стромы (2) и обычно присутствуют у людей среднего и пожилого возраста. Патофизиологические механизмы и молекулярные пути, лежащие в основе ПСЛ, в значительной степени неизвестны. В одном исследовании сообщается о связи с курением, загрязнением окружающей среды, промышленными токсинами и хроническим бронхитом (3). Наиболее распространенными описанными гистологическими подтипами являются синовиальная саркома, эпителиоидная гемангиоэндотелиома, лейомиосаркома и злокачественная опухоль оболочки периферического нерва (4), за которыми следуют недифференцированная плеоморфная саркома, липосаркома и рабдомиосаркома (5-7).
Диагностика ПСЛ всегда затруднена из-за отсутствия клинического подозрения, поскольку первичные карциномы легких встречаются в 700 раз чаще, чем саркомы (8). Симптомы неспецифичны, и основная диагностическая дилемма заключается в том, является ли опухоль первичной или метастатической, поскольку саркомы очень часто распространяются на легкие. В большинстве случаев морфологии с тщательно подобранной иммуногистохимической панелью и молекулярным тестированием будет достаточно для дифференциации ПСЛ от их гистологических имитаторов (саркоматоидная карцинома легкого, лимфома и доброкачественные мезенхимальные опухоли).
В этом исследовании мы ретроспективно проанализировали клинико-патологические особенности 25 случаев ПСЛ, диагностированных и леченных в пяти различных центрах лечения саркомы.
Таблица I.
Характеристики пациентов и начальное лечение.
Пациенты и методы
Отбор пациентов. Были ретроспективно проанализированы записи всех пациентов в возрасте 16 лет и старше с гистологическим диагнозом первичной саркомы легкого в пяти участвующих учреждениях в период с июня 2008 г. по декабрь 2018 г. Мы включили только случаи, в которых первичное расположение, отличное от легкого, было исключено с помощью визуализирующих исследований [компьютерная томография (КТ) головного мозга, грудной клетки и брюшной полости]. Методы этого исследования соответствуют действующим законам Греции и Общему регламенту ЕС по защите данных (GDPR).
по декабрь 2018 г. Мы включили только случаи, в которых первичное расположение, отличное от легкого, было исключено с помощью визуализирующих исследований [компьютерная томография (КТ) головного мозга, грудной клетки и брюшной полости]. Методы этого исследования соответствуют действующим законам Греции и Общему регламенту ЕС по защите данных (GDPR).
Сбор данных. Мы собрали клинические данные всех пациентов, включая анамнез, физикальное обследование, гематологические и биохимические анализы и визуализирующие исследования [КТ грудной клетки и КТ или магнитно-резонансную томографию (МРТ) брюшной полости и головного мозга].
Все системные методы лечения были зарегистрированы в псевдоанонимизированной базе данных, включая схему химиотерапии, другое системное лечение и количество циклов. Кроме того, мы восстановили данные о патологии, хирургическом вмешательстве, включая статус хирургического края, лучевую терапию, места метастазирования и клинические результаты. Реакция опухоли была восстановлена из рентгенологических отчетов КТ или МРТ на основе критериев RECIST версии 1. 1 (9).).
1 (9).).
Статистический анализ. Для оценки характеристик пациентов была проведена описательная статистика. Для анализа выживаемости использовали анализ Каплана-Мейера и таблицы выживаемости. Общая выживаемость (ОВ) определялась как временной интервал между датой постановки диагноза ПСЛ и датой смерти или датой последнего наблюдения. Для пациентов с заболеванием, ограниченным грудной клеткой на момент поступления, которым была проведена хирургическая резекция их первичной опухоли, безрецидивный интервал (DFI) рассчитывался от даты операции до первой известной даты рецидива. Пациенты, которые были еще живы, подвергались цензуре на дату их последнего известного последующего визита. Для сравнения групп применялся логарифмический ранговый критерий. Анализ проводили с помощью SPSS v.24 (IBM Corp., Армонк, Нью-Йорк, США).
Результаты
Клиническая картина. Всего было выявлено 25 случаев из файлов отделений патологии, торакальной хирургии или медицинской онкологии каждого учреждения. Клинические особенности и начальное лечение перечислены в таблице I. Средний возраст на момент постановки диагноза (AD) составлял 61,96 ± 12,26 года (диапазон = 31-75 лет). Асимметрия и эксцесс по возрасту при распределении диагноза составляют -1,187 и 0,651 соответственно. Большинство пациентов были мужчинами, соотношение полов = 18:7. Из 17 пациентов с болезнью, ограниченной легкими при первоначальном обращении, размер первичной опухоли был ≤5 см в 9 случаях.пациентов (52,9%) и >5 см у 8 пациентов (47,1%). Метастатическое заболевание распространилось на легкие (12), брюшину (1), кости (4), плевру (4) и лимфатические узлы (1). Стадирование опухоли при постановке диагноза было пересмотрено, и пациенты были повторно оценены в соответствии с 8-й версией системы Американского объединенного комитета по раку (AJCC) для рака легких (10).
Клинические особенности и начальное лечение перечислены в таблице I. Средний возраст на момент постановки диагноза (AD) составлял 61,96 ± 12,26 года (диапазон = 31-75 лет). Асимметрия и эксцесс по возрасту при распределении диагноза составляют -1,187 и 0,651 соответственно. Большинство пациентов были мужчинами, соотношение полов = 18:7. Из 17 пациентов с болезнью, ограниченной легкими при первоначальном обращении, размер первичной опухоли был ≤5 см в 9 случаях.пациентов (52,9%) и >5 см у 8 пациентов (47,1%). Метастатическое заболевание распространилось на легкие (12), брюшину (1), кости (4), плевру (4) и лимфатические узлы (1). Стадирование опухоли при постановке диагноза было пересмотрено, и пациенты были повторно оценены в соответствии с 8-й версией системы Американского объединенного комитета по раку (AJCC) для рака легких (10).
Образцы опухолей и гистологические подтипы. Диагностические образцы ткани были получены путем хирургической резекции у 11 пациентов и с помощью биопсии бронхов или биопсии под контролем КТ из легочного поражения у остальных. Гистологическими подтипами были синовиальная саркома (40%), недифференцированная плеоморфная саркома (40%), эпителиальная саркома (4%), ангиосаркома (4%), фибросаркома (4%), воспалительная фибробластная опухоль (4%) и саркома с дефицитом SMARCA4. 4%).
Гистологическими подтипами были синовиальная саркома (40%), недифференцированная плеоморфная саркома (40%), эпителиальная саркома (4%), ангиосаркома (4%), фибросаркома (4%), воспалительная фибробластная опухоль (4%) и саркома с дефицитом SMARCA4. 4%).
Лечение и исход. Из 17 пациентов (68 %) с локализованным заболеванием 11 (70,6 %) подверглись хирургическому вмешательству, а у 6 пациентов было распространенное заболевание, не поддающееся хирургическому лечению. Хирургическое удаление первичной опухоли было квалифицировано как R0 (отрицательные края) в 9 случаях и R2 (макроскопическая резидуальная опухоль) в одном случае. Два пациента с олигометастатическим заболеванием (ограниченным легкими) были оперированы; R0 в одном случае и R1 в другом. У пациента с резекцией R2 было выявлено прогрессирование заболевания при первой послеоперационной оценке, и он был исключен из анализа рецидивов. При медиане наблюдения 12 месяцев (диапазон = 1-56 месяцев) частота рецидивов составила 72,72% (8/11). Медиана безрецидивного интервала (DFI) составила 15 месяцев (95% ДИ = 11,257-18,743), как показано на рисунке 1А.
Медиана безрецидивного интервала (DFI) составила 15 месяцев (95% ДИ = 11,257-18,743), как показано на рисунке 1А.
Актуарная канцер-специфическая выживаемость за 3 года составила 42%, а медиана общей выживаемости (ОВ) — 15 месяцев (95% ДИ = 11,056–18,944).
Три пациента получили адъювантную химиотерапию. Один больной получил неоадъювантную химиотерапию без последующего хирургического лечения в связи с прогрессированием заболевания. Все остальные больные с рецидивом получали системную терапию. Из четырех пациентов без рецидива один умер от хирургических осложнений через 2 месяца после операции и второй пациент умер от причин, не связанных с раком, через 8 месяцев после операции.
Данные анализа выживаемости для всей популяции и по стадиям со средним периодом наблюдения 10 (диапазон = 1-56 месяцев) были доступны для 24 пациентов и обобщены в Таблице II.
Обсуждение
Саркомы мягких тканей (СМТ) представляют собой злокачественные новообразования мезенхимального происхождения, которые могут возникать в любой части тела. ПСЛ встречаются крайне редко, поскольку на их долю приходится менее 0,5% всех опухолей легких (11). Из-за их редкости данные по диагностике и лечению ограничены сообщениями о случаях и сериями случаев (1-4, 8, 12-20). Поэтому никаких конкретных руководящих принципов управления не установлено.
ПСЛ встречаются крайне редко, поскольку на их долю приходится менее 0,5% всех опухолей легких (11). Из-за их редкости данные по диагностике и лечению ограничены сообщениями о случаях и сериями случаев (1-4, 8, 12-20). Поэтому никаких конкретных руководящих принципов управления не установлено.
Неоднократно сообщалось, что возраст н.э. колеблется от 18 до 85 лет со средним значением от 45 до 63 лет в соответствии с различными сериями (2, 3, 15, 20). Средний возраст AD в нашей серии составил 62 года (диапазон = 31-75 лет), и у большинства пациентов
были мужчинами с соотношением полов 2,57:1. Это значительно отличается от соотношений, о которых сообщалось в более ранних сериях. До сих пор неоднократно сообщалось о соотношении полов, которое указывало на слабую тенденцию к мужскому полу до 1,8 (4). Анализ наборов баз данных SEER показал, что соотношение полов составляет 1,25:1, в то время как другие более мелкие серии (включая самую последнюю Голоту и др. в 2018 году) (2) обнаружена тенденция к женскому полу.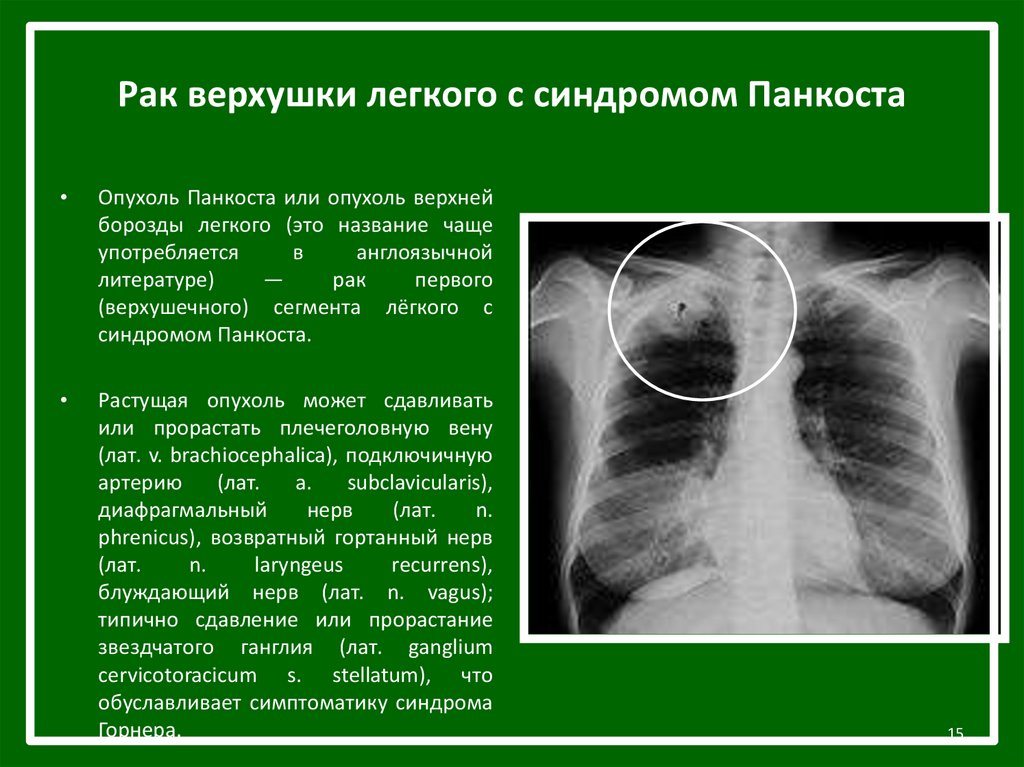
Рис. 1.
Кривые общей выживаемости (ОВ) и безрецидивной выживаемости (ВБВ). A. Кривая выживаемости для безрецидивного интервала (DFI) пациентов с удаленным локализованным заболеванием. Медиана DFI: 15 месяцев (95% ДИ = 11,257–18,743). B. Кривая выживания для общей выживаемости всей популяции. Медиана ОС: 10 месяцев (95% ДИ = 7,608-12,392).
Гистопатологическая характеристика сарком развивалась в течение последних десятилетий, и классификация опухолей мягких тканей и костей Всемирной организации здравоохранения (ВОЗ) постоянно обновляется (21). Эта эволюция может объяснить пресловутое несоответствие в различных частотах гистотипов между сериями. Лейомиосаркомы и миофибробластические опухоли являются наиболее частыми гистотипами (16% и 15% соответственно), тогда как синовиальная саркома (12%) является третьим наиболее распространенным подтипом (18). Однако в более ранних исследованиях было обнаружено, что синовиальная саркома встречается гораздо реже, и только Keel и др. (14) обнаружили более высокую частоту синовиальной саркомы 23% (6 случаев из 26). Неожиданно в нашем наборе данных не было обнаружено лейомиосарком, тогда как синовиальная саркома и недифференцированная плеоморфная саркома были наиболее частыми типами (40% каждый).
(14) обнаружили более высокую частоту синовиальной саркомы 23% (6 случаев из 26). Неожиданно в нашем наборе данных не было обнаружено лейомиосарком, тогда как синовиальная саркома и недифференцированная плеоморфная саркома были наиболее частыми типами (40% каждый).
Поскольку STS метастазируют в легкие, более ранние исследования систематически исключали из анализа пациентов с метастазами. Наша серия включает восемь пациентов с метастатическим заболеванием (стадия IV) на момент постановки диагноза. Стадия IV была описана как единственное первичное поражение легкого с метастазами по крайней мере в один орган, кроме самого легкого. У шести пациентов с местно- или локорегионарно распространенным заболеванием, не поддающимся хирургическому удалению, наблюдалось метастатическое прогрессирование с метастазами в легкие (6), метастазы в головной мозг (2) и метастазы в плевру (1), в то время как у семи пациентов с удаленным заболеванием возник рецидив в легком (7). , плевра (1) и медиастинальные лимфатические узлы (1). У всех пациентов с рецидивом заболевания были обнаружены метастазы в легких, что указывает на то, что PLS сохраняет легочный тропизм метастазирования, как и STS других локализаций. Однако такие локализации, как головной мозг, медиастинальные лимфатические узлы и плевра, указывают на метастатические бронхогенные карциномы, а не на саркомы, что позволяет предположить, что саркомы могут приобретать сходный характер диссеминации в зависимости от их первичной локализации.
У всех пациентов с рецидивом заболевания были обнаружены метастазы в легких, что указывает на то, что PLS сохраняет легочный тропизм метастазирования, как и STS других локализаций. Однако такие локализации, как головной мозг, медиастинальные лимфатические узлы и плевра, указывают на метастатические бронхогенные карциномы, а не на саркомы, что позволяет предположить, что саркомы могут приобретать сходный характер диссеминации в зависимости от их первичной локализации.
Вовлечение лимфатических узлов при СТС традиционно описывалось с низкой частотой. В недавней большой серии исследований, посвященных этому вопросу, сообщалось о частоте 1,1% лимфоузлов от СТС конечностей, а также о 3,1% от внутригрудных СТС, хотя никакой дифференциации «внутригрудных сарком» (т.е. медиастинальных, сердечных, легочных или плевральная саркома) (20). И наоборот, в предыдущих исследованиях ПСЛ сообщалось о высоких показателях MNI от 16% (18) до 25% (15). В нашей серии восемь пациентов (33,33%) имели MNI, что представляет собой самый высокий показатель.
Сообщалось о снижении 5-летней выживаемости на 25% у пациентов с поражением лимфоузлов ( p <0,0001) (18). Пациенты с MNI в нашем исследовании имели более низкую ОВ по сравнению с пациентами без MNI, хотя разница не была статистически значимой (таблица II). Точнее, не было статистически значимых различий в ОВ между пациентами со II, III и IV стадиями рака легкого, в соответствии с данные, представленные Golota et al. (2) (рис. 2). Этот факт указывает на то, что, даже если ПСЛ может распространяться как рак легкого, стадирование пациентов, как при раке легкого, может не давать прогностической информации. Тем не менее, из-за высокой частоты MNI средостение должно быть хирургически оценено у всех пациентов, оперированных по поводу ПСЛ, независимо от гистотипа.
Таблица II.
Общая выживаемость.
Размер опухоли считается прогностическим фактором, оказывающим наибольшее влияние на выживаемость (12, 13, 18). В нашей серии, несмотря на тенденцию к увеличению ОВ у больных с опухолями <5 см, статистически значимых различий обнаружено не было. Поскольку наша серия включала пациентов с метастатическим и нерезектабельным заболеванием, анализ также проводился только для пациентов (10) с полностью удаленным заболеванием. Небольшой размер выборки и неравномерный вес групп (только у одного пациента с размером опухоли >5 см была выполнена полная резекция) не позволили сделать выводы. Однако Regnard и Porte с 24 (15) и 18 (16) пациентами соответственно не обнаружили статистически значимых различий в ОВ между пациентами с опухолями больше или меньше 5 см. Эти противоречивые данные позволяют предположить, что размер, вероятно, не является столь надежным прогностическим фактором, как при STS конечностей.
Поскольку наша серия включала пациентов с метастатическим и нерезектабельным заболеванием, анализ также проводился только для пациентов (10) с полностью удаленным заболеванием. Небольшой размер выборки и неравномерный вес групп (только у одного пациента с размером опухоли >5 см была выполнена полная резекция) не позволили сделать выводы. Однако Regnard и Porte с 24 (15) и 18 (16) пациентами соответственно не обнаружили статистически значимых различий в ОВ между пациентами с опухолями больше или меньше 5 см. Эти противоречивые данные позволяют предположить, что размер, вероятно, не является столь надежным прогностическим фактором, как при STS конечностей.
Тринадцать пациентов в нашем исследовании подверглись хирургической резекции, в том числе 11 пациентов с локализованным заболеванием и два пациента с метастатическим заболеванием. Полная хирургическая резекция была указана как один из наиболее важных прогностических факторов в нескольких сериях исследований (2, 3, 13, 16-18). В нашем исследовании хирургическое вмешательство было в значительной степени связано с выживаемостью (рис. 3), хотя этот результат может быть поставлен под угрозу включением в этот анализ пациентов с метастатическим заболеванием. После стереотаксической лучевой терапии (SBRT)
эффективен при лечении метастазов от СТС (22), возникает вопрос, может ли эта стратегия также быть применима для ПСЛ и должна быть исследована в проспективных сериях.
3), хотя этот результат может быть поставлен под угрозу включением в этот анализ пациентов с метастатическим заболеванием. После стереотаксической лучевой терапии (SBRT)
эффективен при лечении метастазов от СТС (22), возникает вопрос, может ли эта стратегия также быть применима для ПСЛ и должна быть исследована в проспективных сериях.
Рисунок 2.
Оценки выживаемости по Каплану-Мейеру для определения стадии рака легкого. Медиана ОВ для стадии II: 12 месяцев (95% ДИ = 0,00–42,897). Медиана ОВ для стадии III: 8 месяцев (95% ДИ = 4,399-11,601). Медиана ОВ для стадии IV: 11 месяцев (95% ДИ = 5,868-16,132). р=0,052.
О неоадъювантной химиотерапии сообщалось только у двух пациентов из-за размера опухоли со значительной усадкой опухоли с последующей полной резекцией (16). В нашем исследовании одному пациенту была проведена индукционная химиотерапия без ответа, поэтому от операции отказались. Ни один из пациентов с MNI не лечился неоадъювантной химиотерапией. Как указано Spraker и др. , даже если MNI при ПСЛ не следует рассматривать как бронхогенные карциномы, лучшие хирургические результаты и местный контроль все же могут быть достигнуты с помощью неоадъювантной химиотерапии или химиолучевой терапии (18).
Как указано Spraker и др. , даже если MNI при ПСЛ не следует рассматривать как бронхогенные карциномы, лучшие хирургические результаты и местный контроль все же могут быть достигнуты с помощью неоадъювантной химиотерапии или химиолучевой терапии (18).
Адъювантная химиотерапия на основе антрациклинов (AC) применялась у трех пациентов без явного улучшения ОВ. Опять же, неравномерное распределение групп (3 с AC против 9 без AC) не позволяет сделать какой-либо вывод. Более ранние серии не изучали эффект адъювантной химиотерапии из-за той же проблемы (17).
Медиана ОВ для всей популяции нашей серии составила 10 месяцев (рис. 1В), что заметно отличается от
сообщалось в более ранних исследованиях. Это может быть связано с более высоким процентом пациентов с метастатическим и нерезектабельным заболеванием в нашей группе, поскольку предыдущие серии включали исключительно пациентов с опухолями, ограниченными легкими и в большинстве случаев резецированными. Однако при отдельном анализе у пациентов, перенесших хирургическую резекцию, средняя выживаемость составляет 15 месяцев, что примерно на 10 месяцев меньше, чем сообщалось ранее. Как Голота и др. сообщили (2), что мужской пол может неблагоприятно повлиять на выживаемость при ПСЛ, что также показано в нашей серии. Более ранние исследования показали, что размер и стадия карциномы легкого могут быть важными прогностическими факторами. Следует отметить, что популяция нашего исследования имеет равномерное распределение как по размеру >5 см и <5 см (47% и 53% соответственно), так и по МНВ (47% с вовлечением и 53% без вовлечения). Маловероятно, что размер опухоли влияет на выживаемость в нашей серии из-за других сопутствующих прогностических факторов, таких как метастазирование. Хотя также сообщалось, что MNI статистически влияет на ОВ, наше исследование не указывает на то, что это плохой прогностический фактор.
Как Голота и др. сообщили (2), что мужской пол может неблагоприятно повлиять на выживаемость при ПСЛ, что также показано в нашей серии. Более ранние исследования показали, что размер и стадия карциномы легкого могут быть важными прогностическими факторами. Следует отметить, что популяция нашего исследования имеет равномерное распределение как по размеру >5 см и <5 см (47% и 53% соответственно), так и по МНВ (47% с вовлечением и 53% без вовлечения). Маловероятно, что размер опухоли влияет на выживаемость в нашей серии из-за других сопутствующих прогностических факторов, таких как метастазирование. Хотя также сообщалось, что MNI статистически влияет на ОВ, наше исследование не указывает на то, что это плохой прогностический фактор.
Рисунок 3.
Оценка выживаемости по Каплану-Мейеру после операции. Медиана ОВ для пациентов, не подвергшихся хирургическому вмешательству: 8 месяцев (95% ДИ = 2,605-13,395). Медиана ОВ для пациентов, перенесших операцию: 12 месяцев (95% ДИ = 6,967–17,033). р=0,012.
р=0,012.
Из-за ретроспективного дизайна наше исследование было ограничено отсутствием доступных данных. Важные незарегистрированные переменные, такие как продление хирургического вмешательства или лучевой терапии, возможно, могли внести путаницу в анализ. Гистопатологический диагноз не мог быть пересмотрен центральным патологом из-за проблем с логистикой, и это является серьезным ограничением, поскольку даты постановки диагноза варьируются от 2008 до 2018 г., тогда как классификация ВОЗ была изменена в 2013 г. (21). Еще одним ограничением является небольшой размер выборки, что делает невозможным получение надежных выводов из анализа подгрупп. Поскольку большинство ограничений повторяются во всех опубликованных сериях, можно было бы ожидать, что проспективный анализ этих новообразований мог бы более надежно ответить на важные вопросы, такие как прогностическое значение поражения лимфатических узлов и размера опухоли или роль адъювантной химиотерапии.
Заключение
Данные пациентов с диагнозом PLS значительно отличаются от ранее опубликованных серий. Гистологическое распределение изменено с преобладанием синовиальной саркомы и недифференцированной плеоморфной саркомы. Ранее задокументированные прогностические факторы не могли быть подтверждены в нашем исследовании. Высокая доля пациентов с МНИ на момент постановки диагноза может служить показанием для хирургической оценки средостения во всех случаях и ставит вопрос о том, следует ли лечить пациентов с локорегионарным ПСЛ более агрессивным подходом, как при бронхогенном раке.
Гистологическое распределение изменено с преобладанием синовиальной саркомы и недифференцированной плеоморфной саркомы. Ранее задокументированные прогностические факторы не могли быть подтверждены в нашем исследовании. Высокая доля пациентов с МНИ на момент постановки диагноза может служить показанием для хирургической оценки средостения во всех случаях и ставит вопрос о том, следует ли лечить пациентов с локорегионарным ПСЛ более агрессивным подходом, как при бронхогенном раке.
Сноски
↵* Эти авторы внесли равный вклад в эту работу.
Вклад авторов
Хосе Дюран Морено, Стефания Коккали и Мария Саломиду придумали концепцию исследования. Хосе Дюран Морено и Стефания Коккали выполнили поиск литературы, анализ и подбор данных, а также подготовили исходную статью. Хосе Дюран Морено, Стефания Коккали, Мария Саломиду, Василиос Рамфидис, Антония Дигклиа, Анна Кумариану, Периклис Томос и Константинос Сиригос: Предоставление ресурсов.
 Нектариос Куфопулос, Иоаннис Вамвакарис, Элени Психогиу: Проведен гистологический диагноз. Все авторы выполняли рецензирование и редактирование, а Константинос Сиригос контролировал всю работу.
Нектариос Куфопулос, Иоаннис Вамвакарис, Элени Психогиу: Проведен гистологический диагноз. Все авторы выполняли рецензирование и редактирование, а Константинос Сиригос контролировал всю работу.Конфликт интересов
Авторы сообщают об отсутствии конфликта интересов, связанного с данным исследованием.
- Получено 4 февраля 2020 г.
- Доработка получена 11 февраля 2020 г.
- Принято 13 февраля 2020 г. 332
- ↵
- Бенедикт Этьен-Мастроянни LF,
- Шалабрейс Лара,
- Луара Робер,
- Раншер Доминик,
- Souquet Pierre-Jean,
- Cordier Jean-Francois
: Первичные саркомы легких. Клинико-патологическое исследование 12 случаев.
 Lung Cancer 38: 7, 2002. PMID: 12445750. DOI: 10.1016/s0169-5002(02)00303-3
Lung Cancer 38: 7, 2002. PMID: 12445750. DOI: 10.1016/s0169-5002(02)00303-3 - ↵
- Голота Дж.,
- Осовецка К.,
- Орловски Т.
: Первичная саркома легких — отдаленные результаты лечения и прогноз стические факторы. Кардиочир Торакохирургия Пол 15(3): 162-169, 2018. PMID: 30310394. DOI: 10.5114/kitp.2018.78440
- ↵
- Gebauer C
: Первичные легочные саркомы: этиология, клиническая оценка и прогноз в сравнении с легочными карциномами – обзор 41 случая и 394 других литературных случаев. Jpn J Surg 12(2): 148-159, 1982. PMID: 7050480. DOI: 10.1007/bf02469384.
- ↵
- Attanoos RL,
- Appleton MA,
- Gibbs AR
: Первичные саркомы легких: клинико-патологическое и иммуногистохимическое исследование 14 случаев.
 Histopathology 29(1): 29-36, 1996. PMID: 8818691. DOI: 10.1046/j.1365-2559.1996.d01-481.x
Histopathology 29(1): 29-36, 1996. PMID: 8818691. DOI: 10.1046/j.1365-2559.1996.d01-481.x - ↵
- Noh HW,
- Park KJ,
- Sun JS,
- Won JH,
- Kwack KS, 900 05 Choi H,
- Lee KB,
- Park JH
- ↵
- Son C,
- Choi PJ,
- Roh MS
: Первичная миксоидная липосаркома легких с транслокацией t(1 2;16)(q13;p11) у молодой пациентки: краткий случай отчет. Korean J Pathol 46(4): 392-394, 2012. PMID: 23110035. DOI: 10.4132/KoreanJPathol.2012.46.4.392
- ↵
- Джи Г.
 Ю.,
Ю., - Mao H
: Первичная рабдомиосаркома легких у взрослых: отчет о клиническом случае и обзор литературы. J Zhejiang Univ Sci B 14(9): 859-865, 2013. PMID: 24009208. DOI: 10.1631/jzus.B1200248
- Джи Г.
- ↵
- Cameron EW
: Первичная саркома легкого. Thorax 30(5): 516-520, 1975. PMID: 1198390. DOI: 10.1136/thx.30.5.516
- ↵
- Шварц Л.Х.,
- Seymour L,
- Litiere S,
- Ford R,
- Gwyther S,
- Mandrekar S,
- Shankar L,
- Bogaerts J, 9 0005 Чен А,
- Дэнси Дж,
- Хейс В,
- Hodi FS,
- Hoekstra OS,
- Huang EP,
- Lin N,
- Liu Y,
- Therasse P,
- Wolchok JD, 900 05 de Vries E
- ↵
- Amin MB,
- Edge S,
- Greene F,
- Byrd DR,
- Brookland RK, 9000 5 Washington MK,
- Gershenwald JE,
- Compton CC,
- Hess KR,
- Салливан, округ Колумбия,
- Джессуп Дж.М.,
- Бриерли Дж.Д.,
- Гаспар Л.Е.,
- Шилски Р.Л.,
- Balch CM,
- Winchester DP,
- Asare EA,
- Madera M,
- Gress DM,
- Meyer LR
- ↵
- Travis WD,
- Brambilla E,
- Burke AP,
- Marx A,
- Nicholson AG 90 317
: Классификация ВОЗ опухолей легких, плевры, вилочковой железы и сердца.
 Издание четвертое, 4 изд. МАИР, 2015.
Издание четвертое, 4 изд. МАИР, 2015. - ↵
- Nascimento AG,
- Unni KK,
- Bernatz PE
: Саркомы легких. Mayo Clin Proc 57(6): 355-359, 1982. PMID: 6952059.
- ↵
- Janssen JP,
- Mulder JJ,
- Wagenaar SS,
- Elbers HR,
- van den Bosch JM 9 0004
: Первичная саркома легкого: клиническое исследование с длительным наблюдением -вверх. Энн Торак Хирург 58(4): 1151-1155, 1994. PMID: 7944769. DOI: 10.1016/0003-4975(94)
- -6
- ↵
- Keel SB,
- Bacha E,
- Mark EJ,
- Nielsen GP,
- Rosenberg AE 9031 7
: Первичная саркома легких: клинико-патологическое исследование 26 случаев. Mod Pathol 12(12): 1124-1131, 1999. PMID: 10619264.
- ↵
- Regnard JF,
- Icard P,
- Guibert L,
- de Montpreville VT,
- Magdeleinat P,
- Levasseur P
: Прогностические факторы и результаты после хирургического лечения первичных сарком легких.
 Ann Thorac Surg 68(1): 227-231, 1999. PMID: 10421146. DOI: 10.1016/s0003-4975(99)00398-7
Ann Thorac Surg 68(1): 227-231, 1999. PMID: 10421146. DOI: 10.1016/s0003-4975(99)00398-7 - ↵
- Porte HL,
- Metois DG,
- Leroy X,
- Conti M,
- Gosselin B, 90 005 Вюрц А
- ↵
- Магне Н,
- Порсин Б,
- Пивот Х,
- Чикнаворян Х,
- Марси П.Ю.,
- Foa C,
- Otto J,
- Schneider M,
- Thyss A
: Первичные саркомы легких: Длительное выживание, полученное с помощью итеративной полной хирургии. Рак легких 31(2-3): 241-245, 2001. PMID: 11165403. DOI: 10.1016/s0169-5002(00)00167-7
- ↵
- Spraker MB,
- Bair E,
- Bair R,
- Connell PP,
- Mahmood U, 90 005 Koshy M
- Унал ОУ,
- Озтоп I,
- Ясар Н,
- Уракчи З,
- Озатли Т,
- Бозкурт О, 9 0004
- Севинц А,
- Гунайдин Ю,
- Япар Таскойлу Б,
- Arpaci E,
- Ulas A,
- Kodaz H,
- Tonyali O,
- Avci N,
- Aksoy A,
- Yilmaz AU 9031 7
Клинико-патологические характеристики, результаты лечения и прогностические факторы первичного грудного саркома мягких тканей: многоцентровое исследование анатолийского общества медицинской онкологии (asmo). Рак грудной клетки 6(1): 85-90, 2015. PMID: 26273340. DOI: 10.1111/1759-7714.12150
- ↵
- Keung EZ,
- Chiang YJ,
- Voss RK,
- Cormier JN,
- Torres KE,
- Hunt KK,
- Feig BW,
- Roland CL
: Определение Частота и клиническое значение метастазирования в лимфатические узлы при саркоме мягких тканей.
: Первичный злокачественная фиброзная гистиоцитома легких имитирует аневризму легочной артерии с частичным тромбозом: различные рентгенологические оценки. Eur Radiol 18(8): 1653-1657, 2008. PMID: 18351344. DOI: 10.1007/s00330-008-0922-0
: Recist 1.1 — стандартизация и болезни -специфические адаптации: взгляды рабочей группы recist. Eur J Cancer 62: 138-145, 2016. PMID: 27237360. DOI: 10.1016/j.ejca.2016.03.082
Eur J Cancer 62: 138-145, 2016. PMID: 27237360. DOI: 10.1016/j.ejca.2016.03.082
(ред. .): Руководство по стадированию рака AJCC, 8-е изд. Издательство Springer International, 2017.
: Хирургическое лечение первичной саркомы легкого. Eur J Cardiothorac Surg 18(2): 136-142, 2000. PMID: 10925220. DOI: 10.1016/s1010-7940(00)00465-6
: Анализ характеристик пациентов и клинических исходов при первичном легочном саркома. J Thorac Oncol 8(2): 147-151, 2013. PMID: 23263688. DOI: 10.1097/JTO.0b013e318277401f
J Thorac Oncol 8(2): 147-151, 2013. PMID: 23263688. DOI: 10.1097/JTO.0b013e318277401f
