Карта сайта
|
|
Карта сайта
|
|
Рекомендации по лечению астмы: целенаправленные обновления на 2020 г.

КУРТИС С. ЭЛВАРД, доктор медицинских наук, магистр здравоохранения, FAAFP, Sentara Medical Group, Шарлоттсвилль, Вирджиния, и Университет Содружества Вирджинии, Ричмонд, Вирджиния
Целевые обновления 2020 г. к рекомендациям по лечению астмы представляют собой первый пересмотр рекомендаций Национальной программы обучения и профилактики астмы более чем за 10 лет. 1 Отчет отличается от рекомендаций Глобальной инициативы по борьбе с астмой (GINA) из-за большого количества рассматриваемых вопросов и характера обзора фактических данных. 2
В то время как рекомендации GINA представляют собой постоянную серию пересмотров по широкому кругу тем, связанных с астмой, Целевые обновления 2020 г. нацелены на шесть ключевых областей лечения астмы, к которым был проявлен большой интерес и имеется достаточно доказательств, чтобы повлиять на лечение пациентов. Кроме того, он использовал систематические обзоры Агентства медицинских исследований и качества и строгую методологию GRADE для оценки дизайна исследования и актуальности текущих доказательств. 3 Другие сильные стороны включают внимание к перспективе первичного звена и участие представителей первичного звена в руководящих ролях в группе.
нацелены на шесть ключевых областей лечения астмы, к которым был проявлен большой интерес и имеется достаточно доказательств, чтобы повлиять на лечение пациентов. Кроме того, он использовал систематические обзоры Агентства медицинских исследований и качества и строгую методологию GRADE для оценки дизайна исследования и актуальности текущих доказательств. 3 Другие сильные стороны включают внимание к перспективе первичного звена и участие представителей первичного звена в руководящих ролях в группе.
Ингаляционные кортикостероиды
ИНТЕРМИТИРУЮЩАЯ АСТМА
GINA рекомендует лечить пациентов с легкой интермиттирующей астмой по мере необходимости ингаляционными кортикостероидами (ИГКС) с бета-агонистами короткого действия 4 1 года для детей от 6 до 900 возраст и потребность в ИКС/формотероле у взрослых. 4 Однако панель Focused Updates не затронула эту тему и перенесла свою предыдущую рекомендацию по использованию SABA по мере необходимости. Группа выявила ограничения в литературе, описывающей риски альбутерола, но предпочла подчеркнуть важность обучения пациентов использованию SABA вместо того, чтобы препятствовать его использованию. Переключение спасательной терапии с КДБА на ИКС/формотерол при интермиттирующей астме также повлечет за собой значительные дополнительные расходы.
Группа выявила ограничения в литературе, описывающей риски альбутерола, но предпочла подчеркнуть важность обучения пациентов использованию SABA вместо того, чтобы препятствовать его использованию. Переключение спасательной терапии с КДБА на ИКС/формотерол при интермиттирующей астме также повлечет за собой значительные дополнительные расходы.
ПЕРСИСТЕНТНАЯ АСТМА
Для пациентов с легкой персистирующей астмой Focused Updates рекомендует один из следующих вариантов: ежедневный прием низких доз ИГКС с БАКД по мере необходимости или ИГКС с БАКД по мере необходимости (используемые один за другим) при обострении астмы.
При персистирующей астме легкой и средней степени тяжести предпочтительна однократная поддерживающая и облегчающая терапия (SMART). Такой подход снижает потенциальные побочные эффекты хронического использования стероидов, снижает количество посещений отделений неотложной помощи и госпитализаций, а также упрощает схемы лечения пациентов. 1
Для пациентов от четырех лет и старше с персистирующей астмой средней и тяжелой степени предпочтительнее использовать SMART с ИКС/формотеролом ежедневно и по мере необходимости. Для пациентов в возрасте 12 лет и старше с персистирующей астмой средней и тяжелой степени условно предпочтительнее использовать один ингалятор ICS/формотерола (т. е. SMART) ежедневно и по мере необходимости. 5 GINA рекомендует ежедневный прием умеренных доз ИКС или ИКС/бета-агониста длительного действия 2 агониста (ДДБА) с ИКС/формотеролом по мере необходимости в качестве эквивалентных вариантов; тем не менее, группа Focused Updates сочла, что данные о ежедневном приеме ИКС/формотерола и по мере необходимости (SMART) являются более убедительными.
Для пациентов в возрасте 12 лет и старше с персистирующей астмой средней и тяжелой степени условно предпочтительнее использовать один ингалятор ICS/формотерола (т. е. SMART) ежедневно и по мере необходимости. 5 GINA рекомендует ежедневный прием умеренных доз ИКС или ИКС/бета-агониста длительного действия 2 агониста (ДДБА) с ИКС/формотеролом по мере необходимости в качестве эквивалентных вариантов; тем не менее, группа Focused Updates сочла, что данные о ежедневном приеме ИКС/формотерола и по мере необходимости (SMART) являются более убедительными.
SMART содержит несколько предостережений. Будесонид/формотерол не одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США для использования в качестве средства быстрого облегчения. Наиболее изученным устройством был сухой порошок Симбикорт Турбохалер; однако в Соединенных Штатах доступно только дозирующее устройство. Исследования показывают, что салметерол (ДДБА в Advair) менее эффективен и не рекомендуется в качестве альтернативы формотеролу. По состоянию на 30 сентября 2021 г. исследования по применению вилантерола (ДДБА в Breo Ellipta) или мометазона/формотерола (Dulera) по мере необходимости не публиковались.
По состоянию на 30 сентября 2021 г. исследования по применению вилантерола (ДДБА в Breo Ellipta) или мометазона/формотерола (Dulera) по мере необходимости не публиковались.
ОСТРЫЕ ОБОСТРЕНИЯ АСТМЫ
Применение ИГКС при острой астме без сопутствующего приема пероральных стероидов ранее не одобрялось. Тем не менее, для пациентов в возрасте от рождения до четырех лет с рецидивирующими хрипами, вызванными только инфекциями дыхательных путей, и отсутствием хрипов между инфекциями, «Фокусированные обновления» теперь условно рекомендуют короткий курс ICS в дебюте инфекции верхних дыхательных путей с ингаляционным SABA. по мере необходимости. 5 Эта стратегия снижает использование системных стероидов и снижает количество посещений отделений неотложной помощи и госпитализаций.
Целевые обновления и рекомендации GINA не предназначены для пациентов, которые чувствуют себя хорошо большую часть года, но имеют обострения, требующие вмешательства в определенных ситуациях или сезонах. SMART может быть полезным подходом для этих пациентов и снижает общее использование стероидов по сравнению с круглогодичным лечением ICS/LABA. Выбор использования SMART или традиционного перорального приема стероидов зависит от того, насколько точно пациенты могут воспринимать симптомы и успешно применять многократные дозы ICS/формотерола ежедневно. Стоимость также является фактором.
SMART может быть полезным подходом для этих пациентов и снижает общее использование стероидов по сравнению с круглогодичным лечением ICS/LABA. Выбор использования SMART или традиционного перорального приема стероидов зависит от того, насколько точно пациенты могут воспринимать симптомы и успешно применять многократные дозы ICS/формотерола ежедневно. Стоимость также является фактором.
Смягчение воздействия аллергена
Для пациентов с астмой, подвергающихся воздействию определенных веществ в помещении и имеющих аллергию, условно рекомендуется использовать несколько стратегий для снижения воздействия аллергена.
Иммунотерапия
Иммунотерапия условно рекомендуется в качестве дополнительного лечения для пациентов с аллергической астмой легкой и средней степени тяжести, у которых продемонстрирована аллергическая сенсибилизация и признаки ухудшения симптомов астмы после воздействия. Однако, в отличие от GINA, обзор доказательств группы не поддерживает использование сублингвальной иммунотерапии для лечения аллергической астмы.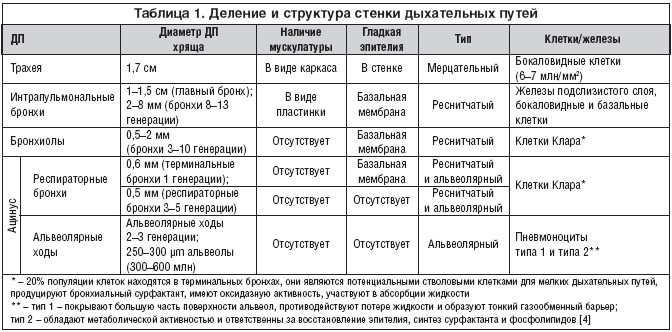
Фракционная экскреция оксида азота
Полезность измерений фракционной экскреции оксида азота (FeNO) для руководства лечением астмы в учреждениях первичной медико-санитарной помощи крайне ограничена. В литературе не поддерживается использование FeNO для диагностики или прогнозирования развития астмы у пациентов в возрасте от рождения до четырех лет.
Бронхотермопластика
Рекомендация Focused Updates по бронхотермопластике отличается от GINA. Доказательства, найденные группой, свидетельствуют о том, что большинству пациентов 18 лет и старше с неконтролируемой астмой не следует выполнять бронхотермопластику из-за ее ограниченной пользы, умеренного риска и неопределенных долгосрочных результатов.
Мускариновые агенты длительного действия
У пациентов в возрасте 12 лет и старше с астмой, не контролируемой только ИКС, рекомендуется добавление ДДБА вместо мускаринового агента длительного действия к ИКС, за исключением случаев, когда терапия ДДБА непереносима. Если контроль неадекватен с помощью ICS/LABA, то рекомендуется добавление мускаринового агента длительного действия.
Если контроль неадекватен с помощью ICS/LABA, то рекомендуется добавление мускаринового агента длительного действия.
Ограничения целевых обновлений 2020 г.
Группа экспертов сосредоточила свое внимание на астме. Рекомендации по иммунотерапии относятся только к их роли в лечении астмы, а не к другим элементам лечения аллергии. Обновления не касаются биологических препаратов, потому что на момент выбора тем доказательства в отношении биологических препаратов были ограничены. Стоимость лечения была признана, но это не позволяло решить сложный характер оплаты медицинских услуг и страхового покрытия. В обновлениях было отмечено потенциальное влияние на различия в рекомендуемых тестах и методах лечения в каждой тематической области.
Эти целенаправленные обновления являются важным ресурсом для навигации по постоянно усложняющимся вариантам лечения астмы. Группа экспертов приглашает семейных врачей высказать свое мнение по этим рекомендациям и другим областям, в которых сохраняются важные клинические вопросы (электронная почта: nhlbiinfo@nhlbi. nih.gov).
nih.gov).
Руководство GINA по лечению астмы у взрослых от 2019 г.
Фарм. 901:00 2020;45(7/8):18-24.
ВЫДЕРЖКА: Установление контроля над симптомами астмы с помощью фармакологических и немедикаментозных вмешательств улучшает качество жизни и предотвращает обострения у пациентов с астмой. Руководящие принципы Глобальной инициативы по борьбе с астмой 2019 г. содержат рекомендации по лечению астмы, разделенные на пять этапов, которые коррелируют с тяжестью заболевания. Варианты лечения включают ингаляционные кортикостероиды (ИКС), бета- 2 агонистов длительного действия, бета-9 короткого действия0023 2 Агонисты (SABA), антагонисты лейкотриеновых рецепторов и пероральные кортикостероиды. Недавние данные показывают неблагоприятные исходы для БАК, используемых отдельно для лечения симптомов легкой астмы по мере необходимости. Изменения в рекомендациях включают использование низких доз ICS с формотеролом для лечения по мере необходимости у взрослых с легкой астмой или для использования всякий раз, когда будет использоваться SABA. Соответствующие эффективные схемы лечения в сочетании с консультированием по правильной технике ингаляции помогут пациентам достичь целей лечения астмы.
Соответствующие эффективные схемы лечения в сочетании с консультированием по правильной технике ингаляции помогут пациентам достичь целей лечения астмы.
Астма, хроническое воспалительное заболевание дыхательных путей, характеризующееся гиперреактивностью дыхательных путей, может проявляться такими симптомами, как свистящее дыхание, одышка, стеснение в груди и кашель. 1 Эти симптомы могут меняться с течением времени и по интенсивности, что делает важным эффективное лечение астмы. Триггеры симптомов могут включать физические упражнения, вирусные респираторные инфекции и факторы окружающей среды, такие как курение. Симптомы, которые не лечатся, могут привести к обострению. обострение 90–100 — это острый эпизод, при котором симптомы резко ухудшаются, а функция легких постепенно снижается. Любое обострение требует обсуждения текущего режима лечения астмы пациента из-за рисков госпитализации, обращений за неотложной помощью и смерти, связанной с астмой.
Руководящие принципы Глобальной инициативы по борьбе с астмой (GINA) 2019 г. не рекомендуют использовать бета-агонист короткого действия 2 (SABA) отдельно для лечения легкой астмы; вместо этого они рекомендуют использовать низкие дозы ингаляционных кортикостероидов (ICS)-формотерол по мере необходимости и для поддерживающей терапии. 2 У пациентов с тяжелой или трудно поддающейся лечению астмой в качестве дополнения к ингаляционной терапии могут быть рассмотрены другие варианты, такие как антагонисты лейкотриеновых рецепторов (АЛР), тиотропий, биопрепараты, азитромицин и пероральные кортикостероиды (ОКС). ).
не рекомендуют использовать бета-агонист короткого действия 2 (SABA) отдельно для лечения легкой астмы; вместо этого они рекомендуют использовать низкие дозы ингаляционных кортикостероидов (ICS)-формотерол по мере необходимости и для поддерживающей терапии. 2 У пациентов с тяжелой или трудно поддающейся лечению астмой в качестве дополнения к ингаляционной терапии могут быть рассмотрены другие варианты, такие как антагонисты лейкотриеновых рецепторов (АЛР), тиотропий, биопрепараты, азитромицин и пероральные кортикостероиды (ОКС). ).
Астма контроль обозначает степень, в которой признаки астмы могут наблюдаться у пациента или уменьшаться или устраняться в результате лечения. 2 Необходимо пересмотреть контроль над астмой в течение предыдущих 4 недель. Пациенту следует задать следующие вопросы: «Были ли у Вас за предыдущие 4 недели: 1) дневные симптомы астмы чаще двух раз в неделю? 2) были ли ночные пробуждения из-за астмы? 3) использовать средство для облегчения симптомов астмы более двух раз в неделю? 4) какие-либо ограничения активности из-за астмы?» Если пациент отвечает «Нет» на все четыре вопроса, его или ее астма хорошо контролируется.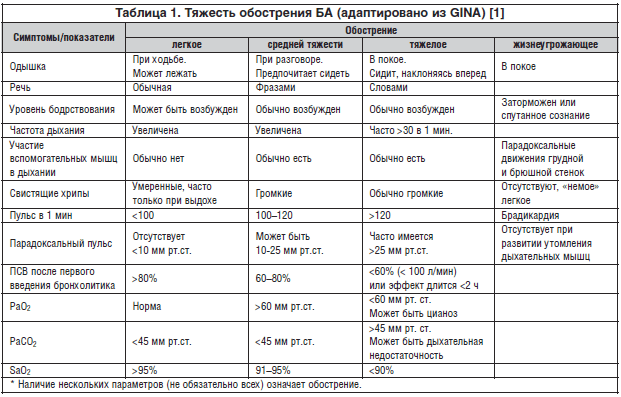 Если пациент отвечает «да» на один или два вопроса, астма частично контролируется, но если ответ «да» на три-четыре вопроса, астма плохо контролируется. 2 Факторы риска, которые могут вызвать обострение, включают неконтролируемую астму, курение, воздействие аллергенов, загрязнение воздуха, сопутствующие заболевания, такие как ожирение, и активное употребление КДБА.
Если пациент отвечает «да» на один или два вопроса, астма частично контролируется, но если ответ «да» на три-четыре вопроса, астма плохо контролируется. 2 Факторы риска, которые могут вызвать обострение, включают неконтролируемую астму, курение, воздействие аллергенов, загрязнение воздуха, сопутствующие заболевания, такие как ожирение, и активное употребление КДБА.
Еще одним важным шагом является оценка соблюдения пациентом режима лечения ингаляционными препаратами. Существует множество причин, по которым пациент может не соблюдать режим приема лекарств от астмы, в том числе трудности с использованием ингаляторов, стоимость лекарств, забывчивость, непонимание предписанных указаний и ощущение, что лекарства не нужны. 2
Цели терапии астмы включают достижение контроля над симптомами для поддержания нормального уровня активности, предотвращение стойкого ограничения воздушного потока и уменьшение побочных эффектов лекарств, описанных в ТАБЛИЦА 1 . Фармакологические и немедикаментозные вмешательства снижают риск будущих обострений, ведущих к госпитализации или смерти от астмы. 2
Фармакологические и немедикаментозные вмешательства снижают риск будущих обострений, ведущих к госпитализации или смерти от астмы. 2
Нефармакологические вмешательства для всех пациентов с астмой включают дыхательные упражнения, повышенную физическую активность, включение здорового питания и предотвращение воздействия дыма и других веществ. 2 Практика йоги и методы дыхания, такие как методы Бутейко и Папворта, изменяют модели дыхания, чтобы уменьшить гипервентиляцию, тем самым способствуя добровольному сокращению использования облегчающих и улучшая симптомы астмы. 3 У пациентов с ожирением потеря веса в сочетании с аэробными и силовыми упражнениями два раза в неделю более эффективна для контроля симптомов, чем только физическая активность. 2 Консультирование по правильной технике использования ингаляторов поможет пациентам достичь целей лечения астмы.
Фармакологическое лечение В схемы лечения астмы вносятся коррективы посредством цикла лечения астмы, основанного на контроле, показанного на РИСУНОК 1.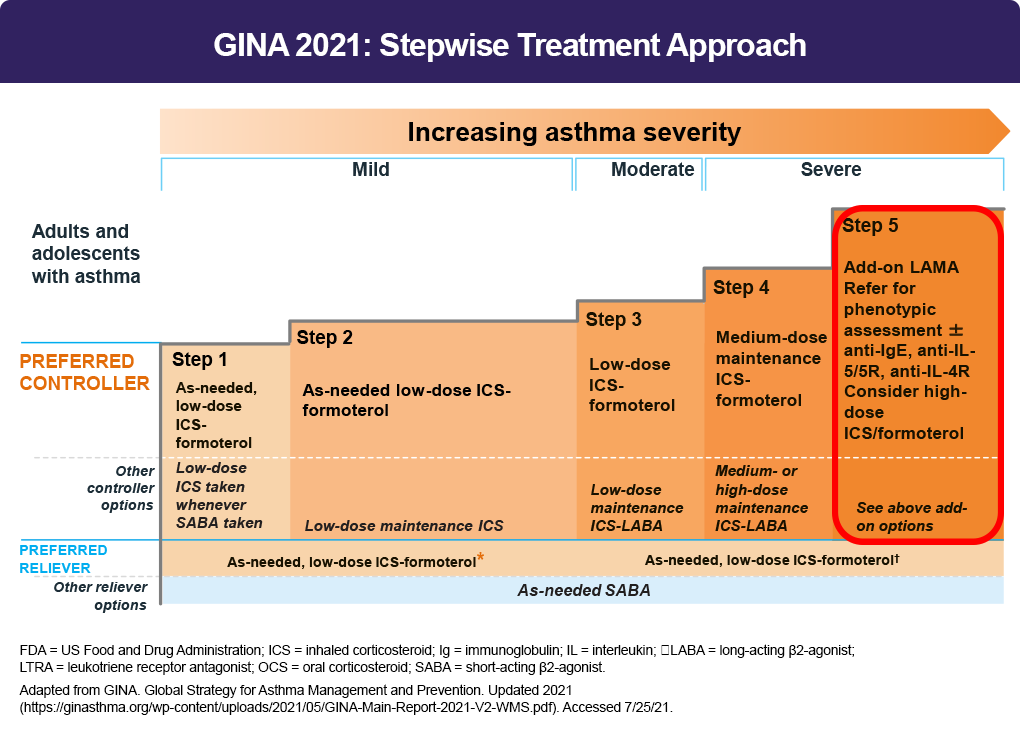 2
2
GINA рекомендует следующие этапы лечения астмы 2 :
• Этап 1: Этот этап рекомендуется для пациентов с легкой астмой, у которых симптомы проявляются реже двух раз в месяц и отсутствует риск обострений.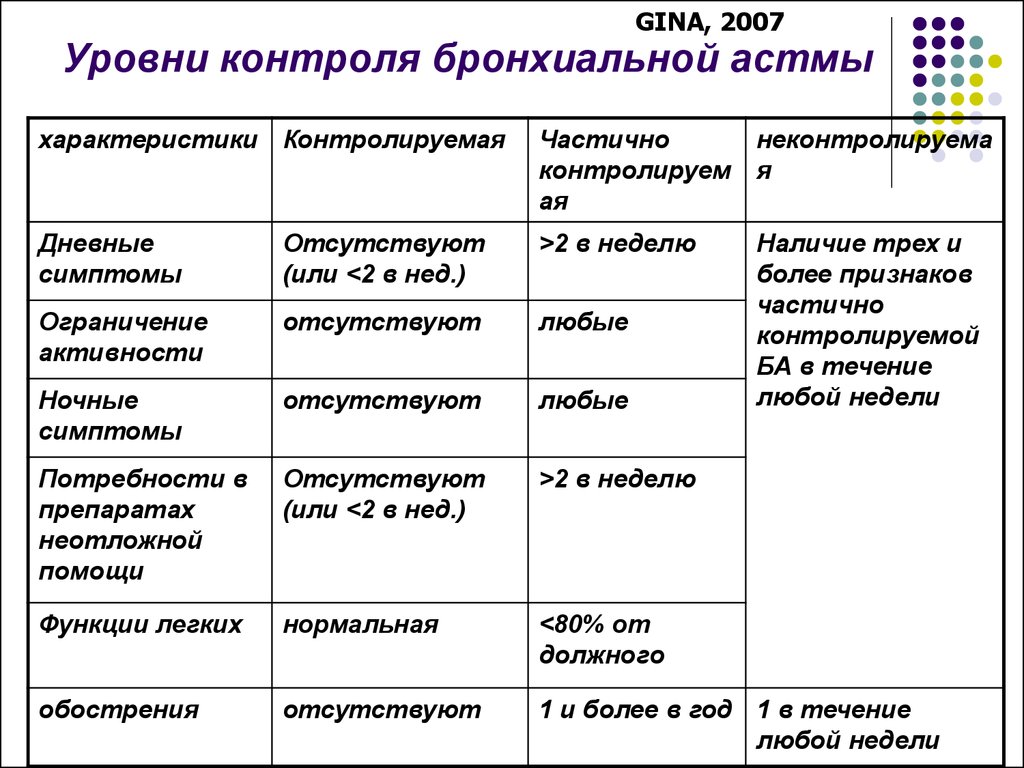 Как упоминалось ранее, на основе новых данных руководство GINA 2019 года больше не рекомендует использовать только КДБА для лечения астмы.
Как упоминалось ранее, на основе новых данных руководство GINA 2019 года больше не рекомендует использовать только КДБА для лечения астмы.
• Этап 2. Предпочтительная схема контроля — низкие дозы ICS-формотерола по мере необходимости или ежедневные низкие дозы ICS плюс по мере необходимости SABA. Схема ИГКС-формотерол позволяет избежать необходимости в ежедневном приеме ИГКС, обеспечивая такие же преимущества в отношении бронхоспазма, вызванного физической нагрузкой, как и ежедневный ИГКС с КДБА по мере необходимости.
• Этап 3: Предпочтительные контролирующие методы лечения включают низкие дозы ИГКС – бета-агониста длительного действия 2 (ДДБА) плюс по мере необходимости БАКД или низкие дозы ИГКС-формотерола как для поддерживающей терапии, так и для облегчения симптомов.
• Этап 4. Предпочтительным контролирующим лечением являются низкие дозы ICS-формотерола в качестве поддерживающей терапии и облегчения симптомов или средние дозы ICS-ДДБА в качестве поддерживающей терапии плюс КДБА по мере необходимости.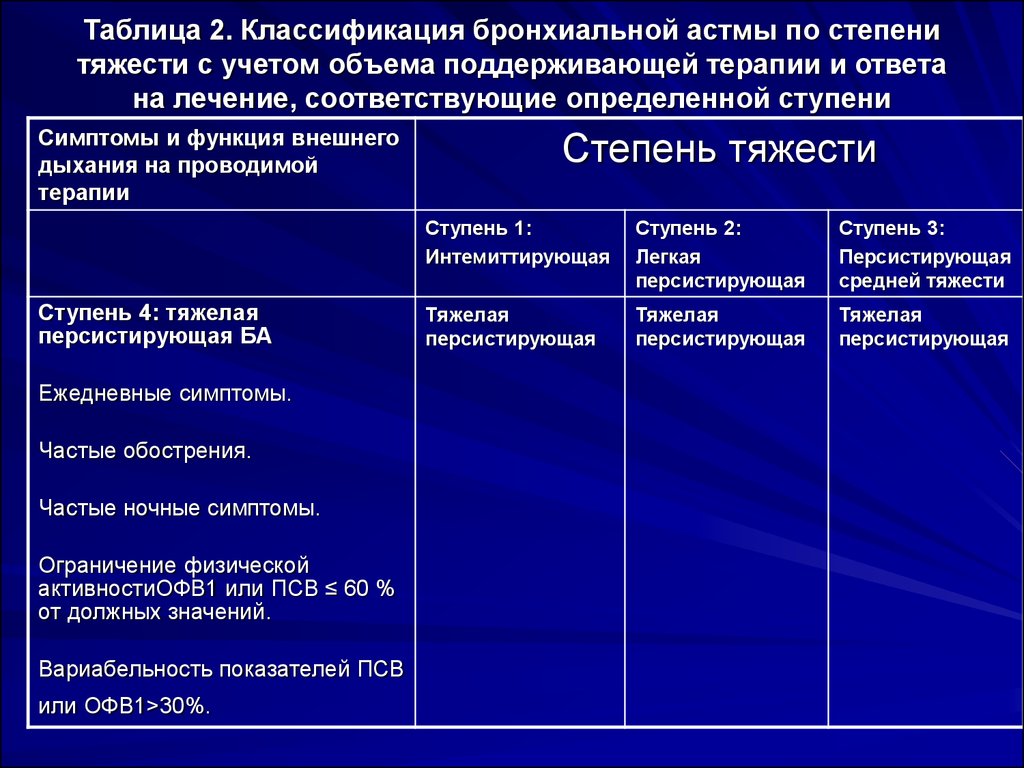 Обратите внимание, что ИКС-формотерол не следует комбинировать с ИКС-ДДБА, содержащим другой ДДБА.
Обратите внимание, что ИКС-формотерол не следует комбинировать с ИКС-ДДБА, содержащим другой ДДБА.
• Этап 5: постоянные обострения или ухудшение симптомов, несмотря на соблюдение режима лечения и правильную технику ингаляции. Считается, что эти пациенты имеют тяжелую или трудно поддающуюся лечению астму и должны быть направлены к пульмонологу.
Прохождение вышеописанных стадий уместно, если у пациентов постоянно наблюдается плохой контроль над симптомами или обострения, несмотря на лечение низкими дозами ИГКС в течение 2–3 месяцев. Понижение целесообразно, когда у пациента наблюдается хороший контроль симптомов и стабильная функция легких в течение как минимум 3 месяцев. Варианты перехода на более низкий уровень зависят от того, какое лекарство принимает пациент и на каком этапе он находится, но для большинства пациентов результат будет хуже, если полностью отменить ИГКС или ДДБА. 2 Дозировка ИКС указана в ТАБЛИЦА 2.
Симптомы можно оценить с помощью таких инструментов, как Анкета контроля астмы, Тест контроля астмы и Три вопроса Королевского колледжа врачей. 2 Эти анкеты позволяют связать балл с симптомами и задают пациентам вопросы о частоте и типах симптомов, таких как ночные пробуждения и ограничения в повседневной активности.
2 Эти анкеты позволяют связать балл с симптомами и задают пациентам вопросы о частоте и типах симптомов, таких как ночные пробуждения и ограничения в повседневной активности.
Термин обострение астмы относится к острому ухудшению функции легких и симптомам, выходящим за рамки того, что обычно испытывает пациент. Предпочтительной облегчающей терапией во время обострения являются низкие дозы ICS-формотерола, которые могут быть увеличены по мере необходимости при ухудшении симптомов. Использование ИКС-ДДБА (беклометазона или будесонида и формотерол) в качестве как облегчающего, так и контролирующего препарата улучшает контроль симптомов и снижает количество госпитализаций и использование ГКС по сравнению с такой же или более высокой дозой контролирующего препарата плюс по мере необходимости КДБА. 4
Короткий курс ОКС является вариантом лечения во время обострения, когда пациент не реагирует на повышенную дозу облегчающего и контролирующего средства через 2–3 дня, если в анамнезе были внезапные тяжелые обострения или у него быстро ухудшается функция легких. (пиковая скорость выдоха или объем форсированного выдоха за 1 секунду <60% от личного лучшего или прогнозируемого значения). 4
(пиковая скорость выдоха или объем форсированного выдоха за 1 секунду <60% от личного лучшего или прогнозируемого значения). 4
См. ТАБЛИЦА 1 для сводки побочных эффектов различных лекарств от астмы. 5-16
Тяжелая или трудно поддающаяся лечению астма относится к неконтролируемой астме на этапах лечения 4 и 5, несмотря на адекватную приверженность лечению и лечение сопутствующих факторов. После первоначальной оценки пациентов в возрасте 12 лет и старше с неадекватно контролируемой астмой, принимающих средние дозы ИГКС в сочетании с ДДБА и/или третьим контролирующим средством, таким как LTRA или теофиллин замедленного высвобождения, переводят на исследование высокоэффективных препаратов. дозы ICS в течение 3-6 месяцев. В дополнение к увеличению ICS, может быть рассмотрено испытание дополнительных небиологических препаратов, таких как тиотропий, модификатор лейкотриенов или OCS. Для взрослых пациентов с персистирующими симптомами астмы, несмотря на умеренные или высокие дозы ИГКС и ДДБА, 2019 г.Рекомендации GINA рекомендуют азитромицин в качестве дополнения. 17
Для взрослых пациентов с персистирующими симптомами астмы, несмотря на умеренные или высокие дозы ИГКС и ДДБА, 2019 г.Рекомендации GINA рекомендуют азитромицин в качестве дополнения. 17
Если небиологические препараты, такие как ДДБА, тиотропий и модификаторы лейкотриенов, не справляются с симптомами астмы у пациента, в зависимости от цены и ресурсов пациента можно рассмотреть возможность применения биологических препаратов. Терапия антииммуноглобулинами Е, такими как омализумаб, может быть рассмотрена у пациентов с аллергической астмой. В случае, если биопрепараты не подходят для пациента, можно рассмотреть применение ОКС в дозе 7,5 мг или менее в день, эквивалентной преднизолону. Тем не менее, OCS связаны со значительными побочными эффектами, такими как остеопороз, ожирение, диабет, катаракта, гипертензия и угнетение функции надпочечников, и поэтому их следует рассматривать в качестве последней линии. 17
В двойном слепом исследовании, проведенном О’Бирном и его коллегами, изучались преимущества использования ICS плюс SABA по сравнению с традиционным лечением. 18 В общей сложности 3849 пациентов в возрасте 12 лет и старше с легкой астмой были рандомизированы в группы тербуталина (плацебо два раза в день плюс тербуталин 0,5 мг перорально), будесонид-формотерол (плацебо два раза в день плюс будесонид-формотерол 200 мкг/6 мкг). prn) или поддерживающая терапия будесонидом (дважды в день 200 мкг будесонида плюс тербуталин prn). Основная цель состояла в том, чтобы определить, превосходит ли будесонид-формотерол по мере необходимости по мере необходимости тербуталин для контроля симптомов. Этот результат был измерен с помощью данных, полученных из электронного дневника симптомов.
18 В общей сложности 3849 пациентов в возрасте 12 лет и старше с легкой астмой были рандомизированы в группы тербуталина (плацебо два раза в день плюс тербуталин 0,5 мг перорально), будесонид-формотерол (плацебо два раза в день плюс будесонид-формотерол 200 мкг/6 мкг). prn) или поддерживающая терапия будесонидом (дважды в день 200 мкг будесонида плюс тербуталин prn). Основная цель состояла в том, чтобы определить, превосходит ли будесонид-формотерол по мере необходимости по мере необходимости тербуталин для контроля симптомов. Этот результат был измерен с помощью данных, полученных из электронного дневника симптомов.
Будесонид-формотерол в дозе по мере необходимости лучше контролировал симптомы астмы по сравнению с тербуталином по мере необходимости у пациентов с легкой астмой. У пациентов, принимавших будесонид-формотерол, наблюдался хороший контроль астмы в течение 34,4% недель по сравнению с 31,1% недель в группе тербуталина ( P = 0,046). Тербуталин ассоциировался с самой высокой годовой частотой тяжелых обострений (0,20) по сравнению с комбинацией будесонид-формотерол (0,07) и поддерживающей терапией будесонидом (0,09).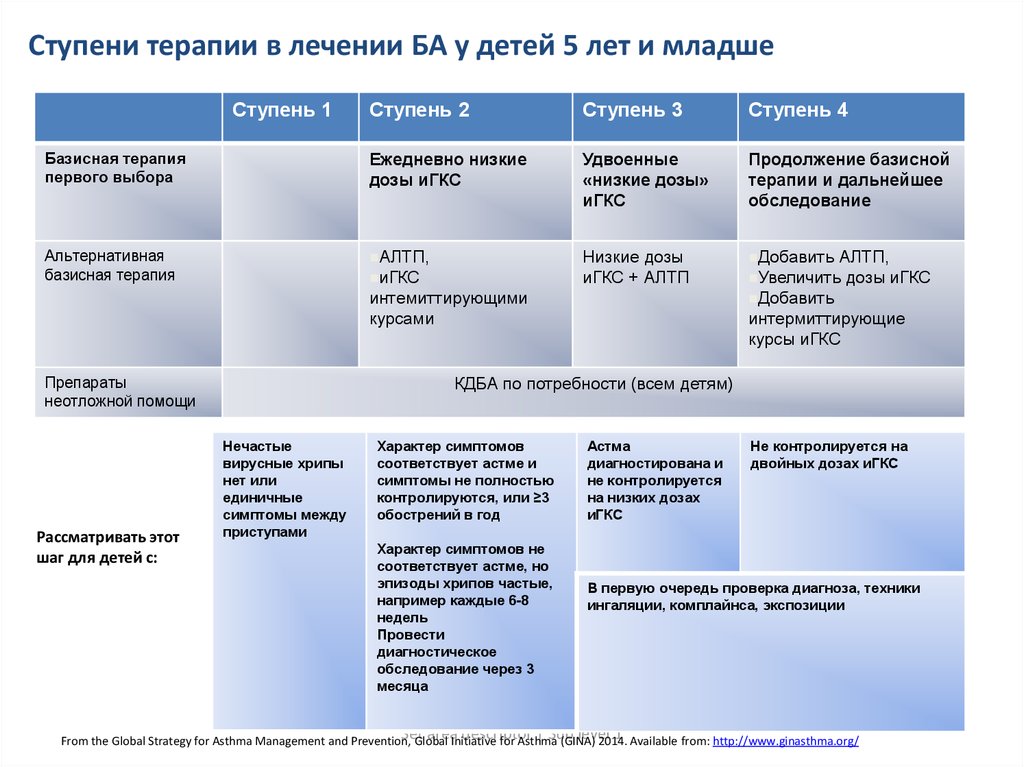 Преимущество комбинации будесонид-формотерол заключалось в том, что воздействие кортикостероидов было снижено из-за снижения дозы будесонида в этой группе на 17% по сравнению с группой поддерживающей терапии будесонидом (57 мкг против 340 мкг соответственно). 18
Преимущество комбинации будесонид-формотерол заключалось в том, что воздействие кортикостероидов было снижено из-за снижения дозы будесонида в этой группе на 17% по сравнению с группой поддерживающей терапии будесонидом (57 мкг против 340 мкг соответственно). 18
Бейтман и его коллеги исследовали эффективность ингаляционного глюкокортикоидного компонента с быстродействующим средством для облегчения легкой астмы. 5 В это 52-недельное двойное слепое многоцентровое исследование было включено 4215 пациентов с легкой астмой в возрасте 12 лет и старше, которым было назначено лечение регулярными ингаляционными глюкокортикоидами. Участники были разделены на две группы, чтобы оценить, была ли более эффективной терапия будесонидом-формотеролом по мере необходимости или поддерживающей терапией будесонидом два раза в день в отношении годовой частоты тяжелых обострений. Группа будесонида-формотерола не уступала группе поддерживающей терапии будесонидом в отношении тяжелых обострений. Кроме того, средняя суточная дозированная доза ингаляционного глюкокортикоида была ниже в группе будесонида и формотерола (66 мкг), чем в группе будесонида и поддерживающей терапии (267 мкг). Время до первого обострения было одинаковым между группами; однако была разница в 0,11 ЕД в пользу группы поддерживающей терапии будесонидом, у которой были более низкие баллы по Опроснику контроля астмы-5 (ACQ-5) по сравнению с группой, получавшей будесонид-формотерол. Минимальная клинически значимая разница в баллах ACQ-5 составляет 0,5 ед. Кроме того, между двумя группами не было различий в нежелательных явлениях, прекращении лечения, связанном с астмой, или уровне смертности. Это исследование и исследование О’Бирна поддерживают текущую рекомендацию GINA от 2019 г. против использования только SABA и вместо него следует использовать ICS-формотерол.
Кроме того, средняя суточная дозированная доза ингаляционного глюкокортикоида была ниже в группе будесонида и формотерола (66 мкг), чем в группе будесонида и поддерживающей терапии (267 мкг). Время до первого обострения было одинаковым между группами; однако была разница в 0,11 ЕД в пользу группы поддерживающей терапии будесонидом, у которой были более низкие баллы по Опроснику контроля астмы-5 (ACQ-5) по сравнению с группой, получавшей будесонид-формотерол. Минимальная клинически значимая разница в баллах ACQ-5 составляет 0,5 ед. Кроме того, между двумя группами не было различий в нежелательных явлениях, прекращении лечения, связанном с астмой, или уровне смертности. Это исследование и исследование О’Бирна поддерживают текущую рекомендацию GINA от 2019 г. против использования только SABA и вместо него следует использовать ICS-формотерол.
В исследовании, проведенном Гибсоном и его коллегами, изучалась эффективность и безопасность перорального азитромицина в качестве дополнительной терапии у пациентов с неконтролируемой персистирующей астмой, которые также принимали средние или высокие дозы ИГКС в сочетании с ДДБА. 17 В этом рандомизированном двойном слепом плацебо-контролируемом исследовании с параллельными группами 420 пациентов были случайным образом распределены в одну из двух групп лечения (азитромицин 500 мг или плацебо три раза в неделю в течение 48 недель). Первичные конечные точки эффективности включали общую частоту обострений астмы (тяжелых и умеренных) и общее качество жизни, связанное с астмой, за период исследования.
17 В этом рандомизированном двойном слепом плацебо-контролируемом исследовании с параллельными группами 420 пациентов были случайным образом распределены в одну из двух групп лечения (азитромицин 500 мг или плацебо три раза в неделю в течение 48 недель). Первичные конечные точки эффективности включали общую частоту обострений астмы (тяжелых и умеренных) и общее качество жизни, связанное с астмой, за период исследования.
В исследовании Gibson было обнаружено, что азитромицин снижает частоту обострений астмы; У 44% пациентов, принимавших азитромицин, было хотя бы одно обострение, по сравнению с 61% пациентов, получавших плацебо ( P <0,0001). Кроме того, применение азитромицина значительно улучшало качество жизни, связанное с астмой, что выражалось в улучшении всех категорий оценочной шкалы (т. е. активности, симптомов, эмоций и окружающей среды) качества жизни, связанного с астмой. Единственным другим заметным различием между исследуемыми группами была частота диареи, которая была значительно выше у пациентов, получавших азитромицин (34% против 19%). % пациентов, получавших плацебо). Для мониторинга безопасности ЭКГ выполняли при скрининге, через 6 недель лечения и в конце лечения. Удлинение интервала QTc более 480 мс привело к выбыванию из исследования двух пациентов (по одному из каждой группы). 17
% пациентов, получавших плацебо). Для мониторинга безопасности ЭКГ выполняли при скрининге, через 6 недель лечения и в конце лечения. Удлинение интервала QTc более 480 мс привело к выбыванию из исследования двух пациентов (по одному из каждой группы). 17
Руководство 2019 г. включает пять важных изменений, касающихся лечения астмы у взрослых. Первым изменением является переход от лечения, состоящего только из SABA, к лечению, содержащему ICS, для лечения симптомов легкой астмы по мере необходимости. 4 Вторым изменением является использование дополнительных низких доз азитромицина три раза в неделю для длительного лечения пациентов с симптоматической астмой, несмотря на лечение умеренными или высокими дозами ICS-LABA; однако следует учитывать потенциальные побочные эффекты. 17
Третьим изменением является рекомендация по дупилумабу, моноклональному антителу к альфа-рецептору интерлейкина-4, в качестве дополнительного варианта лечения для пациентов в возрасте 12 лет и старше с тяжелой астмой 2 типа или астмой, зависимой от OCS. 19 Исследование Wenzel et al. показало, что дупилумаб улучшает функцию легких и снижает частоту тяжелых обострений у пациентов с неконтролируемой персистирующей астмой. 20
19 Исследование Wenzel et al. показало, что дупилумаб улучшает функцию легких и снижает частоту тяжелых обострений у пациентов с неконтролируемой персистирующей астмой. 20
Четвертое изменение заключается в включении лечения высокими дозами ICS-LABA только на шаге 5, тогда как ранее это было включено в шаг 4 с умеренными дозами ICS-LABA; это связано с рекомендацией назначать высокие дозы ИГКС только на несколько месяцев с учетом возможных нежелательных явлений. 17 Пятым изменением является переключение поддерживающей OCS с «предпочтительного» варианта лечения на «другой вариант контролера» на шаге 5, исходя из высокого риска неблагоприятных исходов. 19
На основании новых данных обновленные рекомендации GINA 2019 г. не рекомендуют использовать только ингаляторы SABA для лечения легкой астмы; вместо этого для поддерживающей и поддерживающей терапии рекомендуются низкие дозы ICS-формотерола. Для пациентов с тяжелой или трудно поддающейся лечению астмой в качестве дополнения к ингаляционной терапии могут быть рассмотрены другие варианты, включая LTRA, тиотропий, биопрепараты, азитромицин и OCS. Чтобы обеспечить лучшую приверженность лечению, схемы терапии астмы должны быть индивидуальными для каждого пациента, с пошаговым подходом к поиску схемы, которая контролирует симптомы астмы у пациента, удерживая пациента на минимально возможной дозе, а также должна быть экономически эффективной.
Чтобы обеспечить лучшую приверженность лечению, схемы терапии астмы должны быть индивидуальными для каждого пациента, с пошаговым подходом к поиску схемы, которая контролирует симптомы астмы у пациента, удерживая пациента на минимально возможной дозе, а также должна быть экономически эффективной.
1. Американский фонд астмы и аллергии. Астма. www.aafa.org/астма-симптомы. По состоянию на 8 апреля 2020 г.
2. Глобальная инициатива по борьбе с астмой. Глобальная стратегия лечения и профилактики астмы, 2019 г. www.ginasthma.org. По состоянию на 8 апреля 2020 г.
3. Сантино Т.А., Чавес Г.С., Фрейтас Д.А. и соавт. Дыхательная гимнастика для взрослых с астмой. Cochrane Database Syst Rev. 2020;3(3):CD001277.
4. O’Byrne PM, FitzGerald JM, Bateman ED, et al. Ингаляции комбинированного будесонида-формотерола по мере необходимости при легкой форме астмы. N Английский J Med . 2018;378(20):1865-1876.
5. Бейтман Э.Д., Реддел Х. К., О’Бирн П.М. и соавт. Будесонид-формотерол по мере необходимости по сравнению с поддерживающей терапией будесонидом при легкой форме астмы. N Английский J Med . 2018;378(20):1877-1887.
К., О’Бирн П.М. и соавт. Будесонид-формотерол по мере необходимости по сравнению с поддерживающей терапией будесонидом при легкой форме астмы. N Английский J Med . 2018;378(20):1877-1887.
6. Инструкции по применению Симбикорта (будесонид-формотерол). Уилмингтон, Делавэр: AstraZeneca Pharmaceuticals LP; Январь 2017 г.
7. Рид CE. Бронхиальная астма у пожилых: диагностика и лечение. J Allergy Clin Immunol . 2010;126(4):681-687.
8. Вкладыш в упаковку ProAir HFA (альбутерол). Фрейзер, Пенсильвания: Teva Respiratory, LLC; февраль 2019.
9. Листок-вкладыш Flovent HFA (флутиказон). Research Triangle Park, Северная Каролина: GlaxoSmithKline; Январь 2019 г.
10. Инструкции по применению Сингуляра (монтелукаста). Станция Уайтхаус, Нью-Джерси: Merck & Co, Inc; Апрель 2020 г.
11. Waljee AK, Rogers MA, Lin P, et al. Краткосрочное использование пероральных кортикостероидов и связанный с этим вред среди взрослых в Соединенных Штатах: когортное исследование населения. БМЖ . 2017;357:j1415.
БМЖ . 2017;357:j1415.
12. Foster JM, McDonald VM, M Guo, Reddel HK. «Я проиграл во всех аспектах своей жизни»: скрытое бремя тяжелой астмы. Евр Респир J . 2017;50(3):1700765.
13. Вкладыш в упаковку Rayos (преднизолон). Дирфилд, Иллинойс: Horizon Pharma, Inc; 2012.
14. Спирива ХандиХалер (тиотропий) вкладыш. Риджфилд, Коннектикут: Boehringer Ingelheim Pharmaceuticals, Inc; Февраль 2018 г.
15. Инструкции по применению Спирива Респимат (тиотропий). Риджфилд, Коннектикут: Boehringer Ingelheim Pharmaceuticals, Inc; Март 2019 г.
16. Ксолар (омализумаб) листок-вкладыш. Южный Сан-Франциско, Калифорния: Genentech, Inc.; May 2019.
17. Gibson PG, Yang IA, Upham JW, et al. Влияние азитромицина на обострения астмы и качество жизни у взрослых с персистирующей неконтролируемой астмой (AMAZES): рандомизированное двойное слепое плацебо-контролируемое исследование. Ланцет . 2017;390(10095):659-668.
18. O’Byrne PM, Barnes PJ, Rodriguez-Roisin R, et al.

 Г. Чучалина
Г. Чучалина