Туберкулез — заразное заболевание
Туберкулез — заразное заболевание
Туберкулез (чахотка) — тяжелое заболевание, характеризуется образованием воспалительных изменений в органах, чаще всего в легких, могут поражаться кости, суставы, глаза и др. Чаще болеют люди с ослабленным иммунитетом.
Факторы, способствующие заболеванию туберкулезом (снижению иммунитета):
Возбудитель туберкулеза — микобактерии (палочки Коха, открыты в 1882 году немецким врачом Р. Кохом), имеют высокую устойчивость к факторам внешней среды: при кипячении погибают через 5 минут, при температуре 600 С — выживают 20 минут, в уличной пыли сохраняются до 10 дней, в воде до 5 месяцев. Вещества, содержащие активный хлор, вызывают гибель микобактерий в течение 3-5 часов. Микобактерии сохраняют свою жизнеспособность в условиях высокой влажности, на различных предметах, а также в продуктах, особенно молочных.
Источник инфекции — человек, крупный рогатый скот, который также болеет туберкулезом.
Профилактика:
Пути передачи:
При чихании и кашле прикрывайте рот.
Не плюйте — микобактерии очень живучии.
Старайтесь лишний раз не браться за поручни.
Проводите больше времени на свежем воздухе.
Признаки, требующие обращения к врачу:
Длительное время туберкулез может протекать незаметно для больного и скрываться под маской ОРЗ, бронхита, воспаления легких и т. д.
Своевременно выявленный туберкулез при рано начатом лечении излечивается!
Раннее выявление туберкулеза:
У детей реакция Манту, у взрослых — флюорография.
Вакцинация детей вакциной БЦЖ проводится в родильном доме и ревакцинация — в 7 и 14 лет, взрослых — до 30 лет по медицинским показаниям.
При появлении положительной пробы или увеличение ее размера на 6 мм. и больше, по сравнению с предыдущей пробой, необходимо обследоваться в противотуберкулезном диспансере.
Флюорография грудной клетки проводится ежегодно, что позволяет, кроме туберкулеза, своевременно выявить другую патологию легких, сердца, онкологические и профессиональные заболевания. Если в вашем окружении есть больной туберкулезом, обследоваться нужно 2 раза в год в противотуберкулезном диспансере. Детям и подросткам необходимо пройти химиопрофилактику (лечение противотуберкулезными средствами). Отказ от профилактического обследования и рекомендаций врача может провести к трудноизлечимым формам туберкулеза.
Кто должен чаще осматриваться на туберкулез?
Существует несколько уязвимых групп граждан и профессиональных категорий специалистов, которые в силу различных причин должны чаще обследоваться на туберкулез.
2 раза в год должны обследоваться:
1 раз в год должны проходить обязательный медицинский осмотр на туберкулез:
Кроме того, в индивидуальном (внеочередном) порядке осматриваются:
Как следует лечиться от туберкулеза.
Туберкулез излечим, но только при прохождении полного курса лечения специальными противотуберкулезными препаратами.
Курс лечения длится не менее 6 месяцев, при тяжелой форме — до 9 месяцев. Как только больной начинается лечиться, вероятность того, что он заразит окружающих, значительно уменьшается.
Бактерии туберкулеза очень живучи и могут длительное время сохраняться в организме, поэтому, даже если их перестали обнаруживать в мокроте, а самочувствие больного значительно улучшилось, болезнь еще не излечима.
Если больной прерывает лечение, туберкулез вспыхивает вновь, но с большей силой. При этом бактерии могут приобрести устойчивость к противотуберкулезным препаратам, развивается лекарственно-устойчивый туберкулез, полностью излечить который трудно, а иногда — невозможно.
Как вести себя в очаге в очаге туберкулезной инфекции
Необходима изоляция больного с туберкулезом:
— На период бактериовыделения больному необходимо находиться в противотуберкулезном учреждении
— В последующем максимально изолировать больного, путем выделения ему отдельной комнаты, или части, отделив ширмой кровать, вешалку.
— Ограничить количество предметов повседневного использование больным, оставив лишь вещи, которые легко поддаются чистке, мойке и обеззараживанию.
— Кровать больного должна располагаться на расстоянии не менее 0,5 метров от стены и не меньше чем на 1,5 метров от кроватей других членов семьи.
— Квартиру, где находится больной туберкулезом, необходимо ежедневно убирать при открытых окнах, увлажняя тряпку для уборки мыльно-содовым раствором или дезраствором.
— При обращении с детьми больной туберкулезом не должен брать их на руки, целовать, совместно спать.
— Больной не должен плевать на пол, на землю, в раковину, носовой платок.
Кратность обследования лиц контактных с больным туберкулезом:
Профилактическое лечение лиц, контактных с больным туберкулезом.
Целью химиопрофилактики является предупреждение развития заболевания у лиц из групп риска. Различают:
первичная химиопрофилактика — предупреждение заболевания у неифицированных людей с отрицательной реакцией на туберкулин;
вторичная химиопрофилактика — предупреждение развития туберкулеза у неинфицированных людей.
Химиопрофилактику проводят в течение 3-6 мес. противотуберкулезными препаратами. Перед назначением химиопрофилактики все лица из групп риска проходят клинико-рентгенологическое обследование в противотуберкулезном отделении для исключения активных проявлений туберкулеза.
До проведения и ежемесячно при профилактическом лечении назначают общие клинические анализы крови и мочи.
Здоровый образ жизни – путь к долголетию!
Профилактика туберкулеза среди лиц с повышенным риском возникновения заболевания — Официальный сайт государственного бюджетного учреждения здравоохранения «Областная туберкулезная больница №3»
К лицам с повышенным риском заболеть туберкулезом относятся здоровые лица, у которых имеются рентгенологические признаки излеченного туберкулеза в виде плотных очаговых изменений с четкими контурами и тяжистого фиброза на ограниченной площади. Иногда их называют остаточными туберкулезными изменениями (ОТИ), Лиц с ОТИ делят на две подгруппы: А — переведенные в VII группу диспансерного учета из III группы в связи с выздоровлением в результате ранее проведенного лечения; Б — лица, у которых выявлены ОТИ в виде фиброзно-очаговых и цирротических изменений, множественные кальцинаты. Как правило, этих лиц выявляют при массовых профилактических осмотрах населения и, если при дополнительном обследовании признаков активности туберкулезного процесса не обнаруживают, берут на учет в группу VIIB.
Как правило, этих лиц выявляют при массовых профилактических осмотрах населения и, если при дополнительном обследовании признаков активности туберкулезного процесса не обнаруживают, берут на учет в группу VIIB.
Следует подчеркнуть, что в VII группе выделяют лиц, у которых, кроме остаточных изменений, имеются сопутствующие заболевания (сахарный диабет, язвенная болезнь желудка и двенадцатиперстной кишки, неспецифические заболевания легких и др.). У этого контингента особенно высок риск развития туберкулеза.
В соответствии с «Методическими указаниями по группировке контингентов противотуберкулезных диспансерных учреждений», утвержденными Минздравом СССР 5.03,1988 г., лица, состоящие на диспансерном учете по VII группе, при наличии больших остаточных изменений должны находиться под наблюдением в течение всей жизни. Они подлежат обследованию в противотуберкулезном диспансере не реже 1 раза в год, а при наличии хронических заболеваний внутренних органов, в первую очередь хронических неспецифических заболеваний легких, частота посещений диспансера определяется медицинскими показаниями и необходимостью проведения лечебно-оздоровительных мероприятий.
Под диспансерным наблюдением находятся также лица, выздоравливающие от туберкулеза, так как у них имеется риск обострения и рецидива заболеваний (II и IV группы диспансерного учета). Лица, у которых выявлены туберкулезные изменения в легких или внутригрудных лимфатических узлах, наблюдаются по группе диспансерного учета 0, в этот период им проводят «пробное» лечение химиопрепаратами.
В связи с тем что лиц, у которых при флюорографии выявлены малые остаточные изменения после излеченного туберкулеза, на учет в противотуберкулезный диспансер не ставят, документация на них хранится во флюоротеке поликлиники в отдельной группе «рентгеноположительных». К малым остаточным изменениям относятся единичные (не более 5) компоненты первичного комплекса
(очаг Гона и кальцинированные лимфатические узлы) размером не более 1 см, единичные плотные, четко очерченные очаги размером не более 1 см, ограниченный фиброз в пределах одного сегмента легкого, запаянные синусы и междолевые шварты.
Дополнительными факторами риска у лиц, у которых имеются остаточные изменения после излеченного туберкулеза, являются алкоголизм, наркомания, а также социальные факторы, обусловливающие их социальную ущербность, низкий доход, не обеспечивающий прожиточный минимум, бродяжничество и другие формы миграции, плохие жилищные условия и т. д. Указанная группа также должна быть охвачена профилактическими мероприятиями (периодические медицинские обследования, в случае необходимости химиопрофилактика). В последние годы к группам риска принято относить также лиц, у которых имеются ближайшие родственники, которые переболели или больны туберкулезом. В данном случае риск связан не только с возможным контактом, но и с генетическими факторами и наследственной предрасположенностью к туберкулезу, существование которой доказано В. П.
Диспансерное наблюдение за контингентами противотуберкулезных диспансеров и группами риска, не состоящими на диспансерном учете, включает:
1) получение точных сведений о лицах, относящихся к группам риска: адрес, место работы, состояние здоровья, вредные привычки, экологические, профессиональные и социальные факторы, оказывающие неблагоприятное влияние на состояние здоровья;
2) проведение периодических медицинских обследований, включающих необходимые рентгенологические, лабораторные и другие исследования. При наличии у этих лиц кашля с выделением мокроты, особенно у больных острыми и хроническими заболеваниями легких, обязательно проводят исследование мокроты на наличие микобактерий туберкулеза и посев мокроты на питательные среды;
3) осуществление оздоровительных мероприятий и рациональное трудоустройство, при наличии показаний проведение в период отпуска санаторного и санаторно-климатического лечения, периодическое оздоровление в дневных и ночных санаториях;
4) лечение острых и хронических заболеваний внутренних органов;
5) проведение специфической (превентивной) химиопрофилактики тубазидом в дозе 0,45—0,6 г в сутки либо двумя химиопрепаратами — комбинацией тубазида и этамбутола или пиразинамида, или ПАСК. Длительность курса химиопрофилактики 3—6 мес, можно провести два курса по 3 мес.
Длительность курса химиопрофилактики 3—6 мес, можно провести два курса по 3 мес.
Комментарий: Врожденные лимфоидные клетки группы 3 опосредуют ранний защитный иммунитет против туберкулеза. Во всем мире два миллиарда человек инфицированы
Mtb , при этом ежегодно умирает 1,7 миллиона человек (1). Одним из наиболее важных факторов, ведущих к глобальной эпидемии туберкулеза, является отсутствие адекватных и безопасных вакцин. Хотя в настоящее время единственная лицензированная противотуберкулезная вакцина, бацилла Кальметта-Герена (БЦЖ), может предотвратить
Врожденный иммунитет против туберкулеза играет очень важную роль в борьбе с ранней инфекцией
 7, 8). Кроме того, В-клетки в 9Легкие, инфицированные 0003 Mtb
7, 8). Кроме того, В-клетки в 9Легкие, инфицированные 0003 Mtb Недавно было сообщено о новаторском исследовании врожденных лимфоидных клеток группы 3 (ILC3) в Природа (10). Арден и др. (10) впервые выявили, что ILC3 опосредуют раннюю защитную роль в иммунитете к инфекции Mtb в легких посредством образования IL-17 и IL-22 в хемокиновом лиганде 13 с мотивом C-X-C (CXCL13) – хемокиновом рецепторе 5 с мотивом C-X-C. (CXCR5)-зависимым образом с образованием индуцируемых структур лимфоидной ткани, ассоциированной с бронхами (iBALT), что обеспечивает новое понимание механистического процесса взаимодействия между туберкулезной инфекцией и врожденными иммунными клетками (рис.
Рисунок 1 . Регуляторная роль ILC3 при раннем туберкулезе легких. ILC3 перемещаются из крови в легкие и рекрутируют иммунные клетки через IL-17 и IL-22 для формирования структур iBALT зависимым от CXCL13-CXCR5 образом, оказывая ранний защитный эффект от инфекции
Признанные только в последнее десятилетие, ILC в настоящее время классифицируются как врожденные лимфоидные клетки группы 1 (ILC1), естественные клетки-киллеры (NK), врожденные лимфоидные клетки группы 2 (ILC2), ILC3, лимфоидно-тканевые индукторы (LTi) клетки и регуляторные врожденные лимфоидные клетки (ILCregs) на основе их развития, фенотипа и функции (11–13). ILC1 в основном продуцируют цитокин Th2-типа IFN-γ. ILC2 секретируют цитокины Th3-типа, такие как интерлейкин (IL)-4, IL-5, IL-9.и Ил-13. ILC3, в том числе рецептор-отрицательные по естественной цитотоксичности (NCR — ) и NCR + ILC3, в основном продуцируют IL-17 и IL-22, подобно клеткам Th27 и Th32.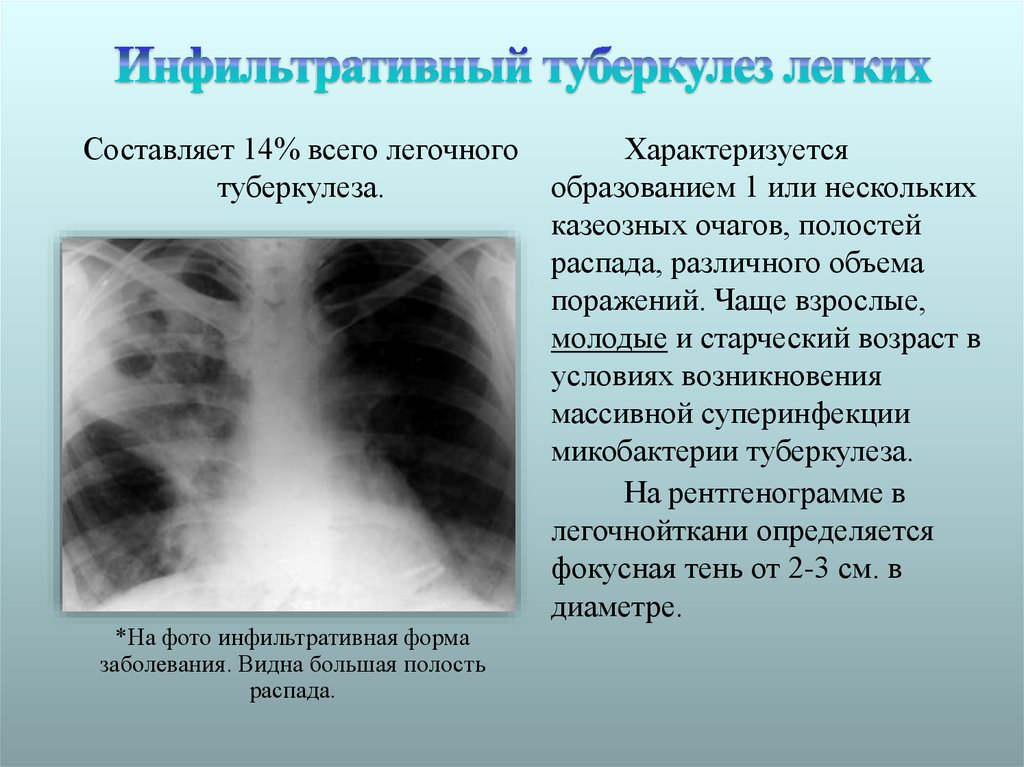 NK-клетки функционально представляют собой аналог CD8 + цитотоксических Т-клеток. Наконец, ILCregs высвобождают как IL-10, так и TGF-β, отражая функции Treg (11, 14, 15). Хорошо известно, что ILC3 существуют в основном в слизистой оболочке кишечника, эпителиальной ткани и коже, которые, как считается, участвуют в восстановлении тканей и гомеостазе слизистой оболочки, тогда как ILC2 в основном расположены в легких, коже, жировой ткани и периферических лимфатических тканях, которые позволяют этим тканям и органам защищаться от заражения гельминтами и инвазии аллергенов.
NK-клетки функционально представляют собой аналог CD8 + цитотоксических Т-клеток. Наконец, ILCregs высвобождают как IL-10, так и TGF-β, отражая функции Treg (11, 14, 15). Хорошо известно, что ILC3 существуют в основном в слизистой оболочке кишечника, эпителиальной ткани и коже, которые, как считается, участвуют в восстановлении тканей и гомеостазе слизистой оболочки, тогда как ILC2 в основном расположены в легких, коже, жировой ткани и периферических лимфатических тканях, которые позволяют этим тканям и органам защищаться от заражения гельминтами и инвазии аллергенов.
Участие ILC3 в респираторных заболеваниях на сегодняшний день менее четко определено. Воодушевляюще, Ardain et al. выводы о том, что ILC3, но не ILC2, могут защищать легочную ткань от ранней инфекции Mtb , заставляют нас вновь признать новые действия ILC3 в легких. Важно отметить, что они могут инициировать не только быстрый неспецифический ответ на внеклеточные микробы, но также и защиту от внутриклеточного специфического патогена Mtb , который считается важным регулятором тканевого гомеостаза и воспалительной реакции (12). В этом исследовании исследователи заметили, что популяция ILC, включая ILC3, была сильно истощена в Mtb — инфицированных пациентов по сравнению со здоровыми людьми. Интересно, что количество ILC1 и ILC3, но не ILC2, восстанавливалось после лечения, что указывает на то, что бактериемия Mtb может модулировать накопление ILC. Используя человеческие и мышиные модели инфекции Mtb , они обнаружили, что накопление ILC3 синхронизируется с увеличением количества альвеолярных макрофагов в легких, чтобы усилить контроль над Mtb . Авторы также проследили локализацию ILCs на нескольких животных моделях и обнаружили, что у мышей с интактной иммунной системой ILC3s мигрируют из крови в легкие, направляясь к инфицированной легочной ткани, и продуцируют молекулы-мессенджеры IL-17 и IL-22. Эти цитокины являются критическими индукторами CXCL13 для рекрутирования иммунных клеток для формирования структур гранулемы, связанных с iBALT, зависимым от CXCL13-CXCR5 образом (рис.
В этом исследовании исследователи заметили, что популяция ILC, включая ILC3, была сильно истощена в Mtb — инфицированных пациентов по сравнению со здоровыми людьми. Интересно, что количество ILC1 и ILC3, но не ILC2, восстанавливалось после лечения, что указывает на то, что бактериемия Mtb может модулировать накопление ILC. Используя человеческие и мышиные модели инфекции Mtb , они обнаружили, что накопление ILC3 синхронизируется с увеличением количества альвеолярных макрофагов в легких, чтобы усилить контроль над Mtb . Авторы также проследили локализацию ILCs на нескольких животных моделях и обнаружили, что у мышей с интактной иммунной системой ILC3s мигрируют из крови в легкие, направляясь к инфицированной легочной ткани, и продуцируют молекулы-мессенджеры IL-17 и IL-22. Эти цитокины являются критическими индукторами CXCL13 для рекрутирования иммунных клеток для формирования структур гранулемы, связанных с iBALT, зависимым от CXCL13-CXCR5 образом (рис. 1). Кроме того, ILC3 также способны ингибировать Mtb рост в виде фаголизосомного слияния (16).
1). Кроме того, ILC3 также способны ингибировать Mtb рост в виде фаголизосомного слияния (16).
CXCL13, один из членов семейства СХС-хемокинов, обычно экспрессируется стромальными клетками, фолликулярными дендритными клетками (ФДК) и CD11c + ДК во время инфекции Mtb (17). Фактически, все больше данных подтверждает, что ось CXCL13-CXCR5 связана с формированием iBALT (17, 18). iBALT состоит главным образом из отдельных областей В-клеток, содержащих ФДК, областей Т-клеток, содержащих ДК, высокоэндотелиальных венул (ВЭВ), специализированных стромальных клеток, а также лимфатических сосудов (18, 19).). В соответствии с этими отчетами Ardain et al. обнаружили, что уровень CXCL13 был повышен у мышей, инфицированных Mtb , и у больных туберкулезом. Кроме того, экспрессия CXCR5, рецептора CXCL13, на поверхности ILC3 также повышалась, что позволяет предположить, что ось CXCL13-CXCR5 может участвовать в регуляции инфекции Mtb с помощью ILC3 (10). Кроме того, ILC3 кажутся очень гетерогенными. Фенотипические характеристики NCR — ILC3 включают Lin — , CCR6 + , NKP44 — (у людей), CD25 + , CD117 + , CD127 + и CD161 + , но NCR + ilc3S 3S44444444444444444444444444444444444. , который полностью отличается от NCR — ILC3 (8). Таким образом, заслуживает дальнейшего изучения регулирующая роль каждой субпопуляции ILC3 при туберкулезной инфекции. Примечательно, что в легких мышей с иммунодефицитом без функциональных ILC количество макрофагов было снижено при плохом иммунном контроле туберкулеза, что демонстрирует, что макрофаги могут опосредовать, в частности, активацию ILC3 через IL-1β.
Кроме того, ILC3 кажутся очень гетерогенными. Фенотипические характеристики NCR — ILC3 включают Lin — , CCR6 + , NKP44 — (у людей), CD25 + , CD117 + , CD127 + и CD161 + , но NCR + ilc3S 3S44444444444444444444444444444444444. , который полностью отличается от NCR — ILC3 (8). Таким образом, заслуживает дальнейшего изучения регулирующая роль каждой субпопуляции ILC3 при туберкулезной инфекции. Примечательно, что в легких мышей с иммунодефицитом без функциональных ILC количество макрофагов было снижено при плохом иммунном контроле туберкулеза, что демонстрирует, что макрофаги могут опосредовать, в частности, активацию ILC3 через IL-1β.
С другой стороны, кишечные CD103 + CD11b + DC инструктируют специфический для легких транспорт циркулирующих IL-22 + ILC3 посредством повышения экспрессии CCR4 рецептора самонаведения в легких на IL-22 + ILC3.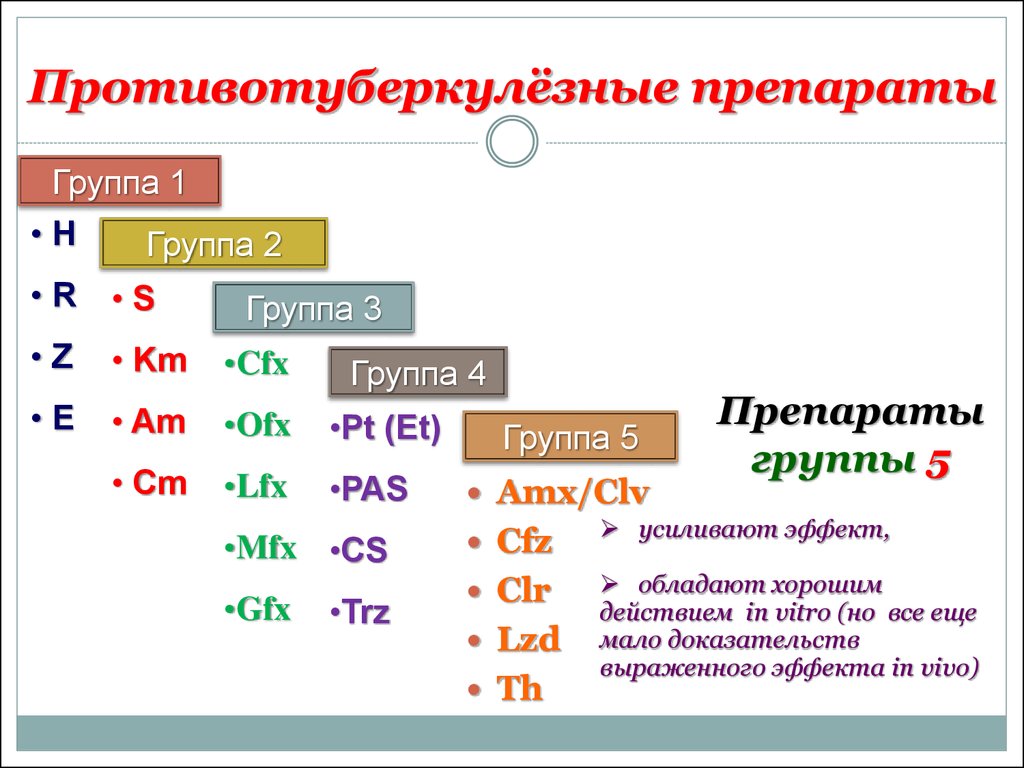 CCR4 рекрутируется хемокинами CCL17 или CCL20, генерируемыми клетками легочного эпителия (20). Ly6C low CD11b + активированных моноцитов увеличивает частоту IL-17 + ILC3s в легких K . пневмония- инфицировали мышей через , продуцирующих TNF-α, который заметно повышал уровень CCL20 в эпителиальных клетках легких (21). Хорошо известно, что ILC3 NCR + в основном экспрессируют IL-22, но ILC3 NCR — преимущественно продуцируют IL-17 (12). Следовательно, заслуживает изучения то, как NCR — ILC3 попадают в легкие, и функционируют ли легочные CD103 + CD11b + DC при селективной миграции NCR + ILC3 в легкие.
CCR4 рекрутируется хемокинами CCL17 или CCL20, генерируемыми клетками легочного эпителия (20). Ly6C low CD11b + активированных моноцитов увеличивает частоту IL-17 + ILC3s в легких K . пневмония- инфицировали мышей через , продуцирующих TNF-α, который заметно повышал уровень CCL20 в эпителиальных клетках легких (21). Хорошо известно, что ILC3 NCR + в основном экспрессируют IL-22, но ILC3 NCR — преимущественно продуцируют IL-17 (12). Следовательно, заслуживает изучения то, как NCR — ILC3 попадают в легкие, и функционируют ли легочные CD103 + CD11b + DC при селективной миграции NCR + ILC3 в легкие.
Прежде всего, ILC3 играют ключевую и ранее недооцененную роль в иммунитете против легочного ТБ. Они в основном опосредуют раннюю защиту организма от туберкулезной инфекции через ось IL-17/IL-22 в зависимости от CXCL13-CXCR5 с образованием iBALT, который устраняет разрыв между врожденными иммунными клетками и адаптивными иммунными реакциями и способствует нашему пониманию патогенеза. ТБ. Во время инфекции Mtb стромальные клетки, FDC и B-клетки экспрессируют CXCL13 в iBALT, посредством чего циркулирующие CXCR5-экспрессирующие ILC3 привлекаются в легкие, чтобы опосредовать защитный иммунитет от Мбт (18). Прорывное открытие не только открывает двери для исследований ILC в отношении их регулирования туберкулезной инфекции, но также прокладывает путь к разработке потенциальной схемы лечения туберкулеза или особенно лекарственно-устойчивого туберкулеза. Мы разумно делаем вывод, что этот ранний защитный эффект ILC3 проявляется при кишечной инфекции Mtb . Однако вопрос о том, как воздействовать на ILC3 или их секретируемые функциональные молекулы, которые помогают организму сопротивляться вторжению Mtb , требует дальнейшего изучения. Кроме того, вакцинация БЦЖ у животных неожиданно инициирует быстрое сильное рекрутирование ILC3, которые вызывают защитный иммунный ответ на Mtb в легких через интраназальный путь введения, что позволяет предположить, что существуют ILC3, подобные памяти легких (22).
ТБ. Во время инфекции Mtb стромальные клетки, FDC и B-клетки экспрессируют CXCL13 в iBALT, посредством чего циркулирующие CXCR5-экспрессирующие ILC3 привлекаются в легкие, чтобы опосредовать защитный иммунитет от Мбт (18). Прорывное открытие не только открывает двери для исследований ILC в отношении их регулирования туберкулезной инфекции, но также прокладывает путь к разработке потенциальной схемы лечения туберкулеза или особенно лекарственно-устойчивого туберкулеза. Мы разумно делаем вывод, что этот ранний защитный эффект ILC3 проявляется при кишечной инфекции Mtb . Однако вопрос о том, как воздействовать на ILC3 или их секретируемые функциональные молекулы, которые помогают организму сопротивляться вторжению Mtb , требует дальнейшего изучения. Кроме того, вакцинация БЦЖ у животных неожиданно инициирует быстрое сильное рекрутирование ILC3, которые вызывают защитный иммунный ответ на Mtb в легких через интраназальный путь введения, что позволяет предположить, что существуют ILC3, подобные памяти легких (22). Следовательно, ILC3 играют важную роль в защитном иммунитете против туберкулеза, которую мы в настоящее время не признаем. Мы представляем, что подобные памяти ILC3 могут быть разработаны в качестве потенциальных вакцин в будущем.
Следовательно, ILC3 играют важную роль в защитном иммунитете против туберкулеза, которую мы в настоящее время не признаем. Мы представляем, что подобные памяти ILC3 могут быть разработаны в качестве потенциальных вакцин в будущем.
Вклад автора
FX задумал этот комментарий. БЖ и ФО составили его. КД отвечал за критическое прочтение. FX и RX пересмотрели и доработали рукопись. Все авторы прочитали и одобрили окончательный вариант рукописи.
Финансирование
Эта работа была поддержана Национальным фондом естественных наук Китая (номер гранта 81172824) и крупным проектом синергетических инноваций городской научно-технической программы Гуанчжоу (номер гранта 201604020146) для FX.
Конфликт интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Каталожные номера
1. Darrah PA, Zeppa JJ, Maiello P, Hackney JA, Wadsworth MHN, Hughes TK, et al. Профилактика туберкулеза у макак после внутривенной иммунизации БЦЖ. Природа. (2020) 577: 95–102. doi: 10.1038/s41586-019-1817-8
Профилактика туберкулеза у макак после внутривенной иммунизации БЦЖ. Природа. (2020) 577: 95–102. doi: 10.1038/s41586-019-1817-8
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
2. Гупта Н., Кумар Р., Агравал Б. Новые игроки в иммунитете к туберкулезу: микробиом хозяина, эпителий легких и врожденные иммунные клетки. Фронт Иммунол. (2018) 9:709. дои: 10.3389/fimmu.2018.00709
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
3. Abubakar I, Pimpin L, Ariti C, Beynon R, Mangtani P, Sterne JA, et al. Систематический обзор и метаанализ современных данных о продолжительности защиты бациллой Кальметта-Герена от вакцинации против туберкулеза. Оценка медицинских технологий. (2013) 17:1–372. doi: 10.3310/hta17370
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
4. Хантер Р., Актер Дж. Патогенез вторичного туберкулеза. Изменения в разработке вакцин. Туберкулез (Эдинб). (2019) 116S:S114–17. doi: 10.1016/j.tube.2019.04.018
(2019) 116S:S114–17. doi: 10.1016/j.tube.2019.04.018
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
5. Dheda K, Limberis JD, Pietersen E, Phelan J, Esmail A, Lesosky M, et al. Исходы, заразность и динамика передачи больных туберкулезом с широкой лекарственной устойчивостью и выписанных на дому больных программно неизлечимым туберкулезом: проспективное когортное исследование. Ланцет Resp Med. (2017) 5: 269–81. doi: 10.1016/S2213-2600(16)30433-7
Реферат PubMed | Полный текст перекрестной ссылки | Google Scholar
6. Эрнст Д.Д. Механизмы уклонения от иммунитета M.tuberculosis как проблемы при разработке противотуберкулезной вакцины. Микроб-хозяин клетки. (2018) 24:34–42. doi: 10.1016/j.chom.2018.06.004
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
7. Этна М.П., Джакомини Э., Севера М., Кочча Э.М. Про- и противовоспалительные цитокины при туберкулезе: палка о двух концах в патогенезе туберкулеза. Семин Иммунол. (2014) 26:543–51. doi: 10.1016/j.smim.2014.09.011
Семин Иммунол. (2014) 26:543–51. doi: 10.1016/j.smim.2014.09.011
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
8. Simmons JD, Stein CM, Seshadri C, Campo M, Alter G, Fortune S, et al. Иммунологические механизмы устойчивости человека к персистентной инфекции Mycobacterium tuberculosis . Nat Rev Immunol. (2018) 18: 575–89. doi: 10.1038/s41577-018-0025-3
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
9. Дятлов А.В., Апт А.С., Линге И.А. В-лимфоциты в антимикобактериальном иммунном ответе: патогенез или защита? Туберкулез. (2019) 114:1–8. doi: 10.1016/j.tube.2018.10.011
Полный текст CrossRef | Google Scholar
10. Ardain A, Domingo-Gonzalez R, Das S, Kazer SW, Howard NC, Singh A, et al. Врожденные лимфоидные клетки группы 3 опосредуют ранний защитный иммунитет против туберкулеза. Природа. (2019) 570: 528–32. doi: 10.1038/s41586-019-1276-2
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
11. Zeng B, Shi S, Liu J, Xing F. Commentary: регуляторные врожденные лимфоидные клетки контролируют врожденное воспаление кишечника. Фронт Иммунол. (2018) 9:1522. doi: 10.3389/fimmu.2018.01522
Zeng B, Shi S, Liu J, Xing F. Commentary: регуляторные врожденные лимфоидные клетки контролируют врожденное воспаление кишечника. Фронт Иммунол. (2018) 9:1522. doi: 10.3389/fimmu.2018.01522
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
12. Zeng BN, Shi SN, Ashworth G, Dong CJ, Liu J, Xing FY. ILC3 действует как палка о двух концах при воспалительных заболеваниях кишечника. Дис. клеточной смерти. (2019) 10:315. doi: 10.1038/s41419-019-1540-2
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
13. Vivier E, Artis D, Colonna M, Diefenbach A, Di Santo JP, Eberl G, et al. Врожденные лимфоидные клетки: 10 лет спустя. Сотовый. (2018) 174:1054–66. doi: 10.1016/j.cell.2018.07.017
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
14. Колонна М. Врожденные лимфоидные клетки: разнообразие, пластичность и уникальные функции в иммунитете. Иммунитет. (2018) 48:1104–17. doi: 10.1016/j.immuni.2018.05.013
doi: 10.1016/j.immuni.2018.05.013
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
15. Zook EC, Kee BL. Развитие врожденных лимфоидных клеток. Нат Иммунол. (2016) 17:775–82. doi: 10.1038/ni.3481
Реферат PubMed | Полный текст перекрестной ссылки | Google Scholar
16. Ardain A, Porterfield JZ, Kloverpris HN, Leslie A. ILC типа 3 при заболеваниях легких. Фронт Иммунол. (2019) 10:92. doi: 10.3389/fimmu.2019.00092
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
17. Слайт С.Р., Рангель-Морено Дж., Гопал Р., Лин И., Фаллерт Джунеко Б.А., Мехра С. и другие. Т-хелперные клетки CXCR5(+) опосредуют защитный иммунитет против туберкулеза. Дж Клин Инвест. (2013) 123:712–26. дои: 10.1172/JCI65728
Реферат PubMed | Полный текст перекрестной ссылки | Google Scholar
18. Хванг Дж. Ю., Рэндалл Т. Д., Сильва-Санчес А. Индуцибельная лимфоидная ткань, связанная с бронхами: укрощение воспаления в легких. Фронт Иммунол. (2016) 7:258. doi: 10.3389/fimmu.2016.00258
Фронт Иммунол. (2016) 7:258. doi: 10.3389/fimmu.2016.00258
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
19. Hirahara K, Shinoda K, Morimoto Y, Kiuchi M, Aoki A, Kumagai J, et al. Иммунное клеточно-эпителиальное/мезенхимальное взаимодействие, способствующее возникновению патологии, связанной с аллергическим воспалением дыхательных путей. Фронт Иммунол. (2019) 10:570. doi: 10.3389/fimmu.2019.00570
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
20. Gray J, Oehrle K, Worthen G, Alenghat T, Whitsett J, Deshmukh H. Кишечные комменсальные бактерии опосредуют иммунитет слизистой оболочки легких и способствуют устойчивости новорожденных мышей к инфекции. Sci Transl Med. (2017) 9:eaaf9412. doi: 10.1126/scitranslmed.aaf9412
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
21. Xiong H, Keith JW, Samilo DW, Carter RA, Leiner IM, Pamer EG. Врожденные перекрестные помехи лимфоцитов/моноцитов Ly6C(hi) способствуют элиминации klebsiella pneumoniae. Сотовый. (2016) 165: 679–89. doi: 10.1016/j.cell.2016.03.017
Сотовый. (2016) 165: 679–89. doi: 10.1016/j.cell.2016.03.017
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
22. Хорено-Парра Дж.А., Вайнштейн Л.И., Юнис Э.Дж., Зунига Дж., Эрнандес-Пандо Р. Нестандартное мышление: реакции врожденной и В-клеток памяти как новые защитные механизмы против туберкулеза. Фронт Иммунол. (2020) 11:226. doi: 10.3389/fimmu.2020.00226
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Туберкулез
Туберкулез- All topics »
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- Ресурсы »
- Бюллетени
- Факты в картинках
- Мультимедиа
- Публикации
- Вопросы и Ответы
- Инструменты и наборы инструментов
- Популярный »
- Загрязнение воздуха
- Коронавирусная болезнь (COVID-19)
- Гепатит
- оспа обезьян
- Все страны »
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- В
- Ш
- X
- Y
- Z
- Регионы »
- Африка
- Америка
- Юго-Восточная Азия
- Европа
- Восточное Средиземноморье
- Западная часть Тихого океана
- ВОЗ в странах »
- Статистика
- Стратегии сотрудничества
- Украина ЧП
- все новости »
- Выпуски новостей
- Заявления
- Кампании
- Комментарии
- События
- Тематические истории
- Выступления
- Прожекторы
- Информационные бюллетени
- Библиотека фотографий
- Список рассылки СМИ
- Заголовки »
- Сосредоточиться на »
- Афганистан кризис
- COVID-19 пандемия
- Кризис в Северной Эфиопии
- Сирийский кризис
- Украина ЧП
- Вспышка оспы обезьян
- Кризис Большого Африканского Рога
- Последний »
- Новости о вспышках болезней
- Советы путешественникам
- Отчеты о ситуации
- Еженедельный эпидемиологический отчет
- ВОЗ в чрезвычайных ситуациях »
- Наблюдение
- Исследовать
- Финансирование
- Партнеры
- Операции
- Независимый контрольно-консультативный комитет
- Призыв ВОЗ о чрезвычайной ситуации в области здравоохранения 2023 г.
- Данные ВОЗ »
- Глобальные оценки здоровья
- ЦУР в области здравоохранения
- База данных о смертности
- Сборы данных
- Панели инструментов »
- Информационная панель COVID-19
- Приборная панель «Три миллиарда»
- Монитор неравенства в отношении здоровья
- Основные моменты »
- Глобальная обсерватория здравоохранения
- СЧЕТ
- Инсайты и визуализации
- Инструменты сбора данных
- Отчеты »
- Мировая статистика здравоохранения 2022 г.
- избыточная смертность от COVID
- DDI В ФОКУСЕ: 2022 г.
- О ком »
- Люди
- Команды
- Состав
- Партнерство и сотрудничество
- Сотрудничающие центры
- Сети, комитеты и консультативные группы
- Трансформация
- Наша работа »
- Общая программа работы
- Академия ВОЗ
- Деятельность
- Инициативы
- Финансирование »
- Инвестиционный кейс
- Фонд ВОЗ
- Подотчетность »
- Аудит
- Программный бюджет
- Финансовые отчеты
- Портал программного бюджета
- Отчет о результатах
- Управление »
- Всемирная ассамблея здравоохранения
- Исполнительный совет
- Выборы Генерального директора
- Веб-сайт руководящих органов
- Портал государств-членов
- Главная/
- Отдел новостей/
- Информационные бюллетени/
- Деталь/
- Туберкулез
Ключевые факты
- Всего в 2021 году от туберкулеза умерло 1,6 миллиона человек (в том числе 187 000 человек с ВИЧ).
 Во всем мире туберкулез занимает 13-е место среди основных причин смерти и второе место среди причин смерти от инфекционных заболеваний после COVID-19.(выше ВИЧ/СПИД).
Во всем мире туберкулез занимает 13-е место среди основных причин смерти и второе место среди причин смерти от инфекционных заболеваний после COVID-19.(выше ВИЧ/СПИД). - По оценкам, в 2021 году во всем мире туберкулезом заболело 10,6 миллиона человек. Шесть миллионов мужчин, 3,4 миллиона женщин и 1,2 миллиона детей. Туберкулез присутствует во всех странах и во всех возрастных группах. Но туберкулез излечим и предотвратим.
- В 2021 году во всем мире туберкулезом заболело 1,2 миллиона детей. Медицинские работники часто упускают из виду детский и подростковый туберкулез, и его трудно диагностировать и лечить.
- В 2021 г. на 30 стран с высоким бременем ТБ приходилось 87% новых случаев ТБ
- Туберкулез с множественной лекарственной устойчивостью (МЛУ-ТБ) остается кризисом общественного здравоохранения и угрозой безопасности здравоохранения. В 2020 году только каждый третий человек с лекарственно-устойчивым туберкулезом обращался за лечением.
- Во всем мире заболеваемость туберкулезом снижается примерно на 2% в год, а в период с 2015 по 2020 год совокупное снижение составило 11%.
 Это было более чем на полпути к рубежу Стратегии по ликвидации туберкулеза, предусматривающему снижение заболеваемости на 20 % в период с 2015 по 2020 год .
Это было более чем на полпути к рубежу Стратегии по ликвидации туберкулеза, предусматривающему снижение заболеваемости на 20 % в период с 2015 по 2020 год . - По оценкам, в период с 2000 по 2020 год благодаря диагностике и лечению туберкулеза было спасено 66 миллионов жизней9.0297
- Согласно последнему национальному исследованию расходов на лечение больных туберкулезом, во всем мире почти каждое второе домохозяйство, пораженное туберкулезом, сталкивается с расходами, превышающими 20% от дохода их домохозяйства. К 2020 году мир не достиг рубежа в 0% больных туберкулезом и их домохозяйств, столкнувшихся с катастрофическими расходами в результате заболевания туберкулезом.
- К 2022 г. ежегодно требуется 13 млрд долл. США на профилактику, диагностику, лечение и уход для достижения глобальной цели, согласованной на совещании высокого уровня ООН по туберкулезу в 2018 г.
- Финансирование в странах с низким и средним уровнем дохода (СНСД), на которые приходится 98% зарегистрированных случаев ТБ, далеко не соответствует потребностям.
 Расходы в 2020 году составили 5,3 млрд долларов США, что меньше половины (41%) глобального целевого показателя.
Расходы в 2020 году составили 5,3 млрд долларов США, что меньше половины (41%) глобального целевого показателя. - В период с 2019 по 2020 год расходы сократились на 8,7% (с 5,8 млрд долларов США до 5,3 млрд долларов США), при этом финансирование противотуберкулезной помощи в 2020 году вернулось к уровню 2016 года.
- Прекращение эпидемии туберкулеза к 2030 г. входит в число задач в области здравоохранения Целей устойчивого развития Организации Объединенных Наций (ЦУР).
Туберкулез (ТБ) вызывается бактериями (Mycobacterium tuberculosis), которые чаще всего поражают легкие. Туберкулез излечим и предотвратим.
Туберкулез передается от человека к человеку воздушно-капельным путем. Когда люди с туберкулезом легких кашляют, чихают или плюются, они выбрасывают микробы туберкулеза в воздух. Чтобы заразиться, человеку нужно вдохнуть лишь несколько из этих микробов.
По оценкам, около четверти населения земного шара инфицированы бактериями туберкулеза, но у большинства людей заболевание туберкулезом не развивается, а у некоторых инфекция исчезает. Те, кто инфицирован, но (еще) не болен этой болезнью, не могут ее передавать.
Те, кто инфицирован, но (еще) не болен этой болезнью, не могут ее передавать.
У людей, инфицированных бактериями ТБ, риск заболеть ТБ в течение жизни составляет 5–10%. Люди с ослабленной иммунной системой, такие как люди, живущие с ВИЧ, недоеданием или диабетом, или люди, употребляющие табак, имеют более высокий риск заболеть.
Когда у человека развивается активная форма туберкулеза, симптомы (такие как кашель, лихорадка, ночная потливость или потеря веса) могут быть легкими в течение многих месяцев. Это может привести к задержке обращения за медицинской помощью и передаче бактерий другим людям. Люди с активной формой туберкулеза могут заразить от 5 до 15 человек при тесном контакте в течение года. Без надлежащего лечения в среднем 45% ВИЧ-отрицательных людей с ТБ и почти все ВИЧ-положительные люди с ТБ умрут.
Кто подвергается наибольшему риску?
Туберкулез в основном поражает взрослых в наиболее продуктивном возрасте. Однако все возрастные группы находятся в группе риска. Более 80% случаев и смертей приходится на страны с низким и средним уровнем дохода.
Более 80% случаев и смертей приходится на страны с низким и средним уровнем дохода.
Люди, инфицированные ВИЧ, в 16 раз более склонны к развитию активной формы туберкулеза (см. раздел «ТБ и ВИЧ» ниже). Риск активного туберкулеза также выше у лиц, страдающих другими состояниями, нарушающими иммунную систему. Люди с недоеданием в 3 раза больше подвержены риску. В 2021 году во всем мире было зарегистрировано 2,2 миллиона новых случаев туберкулеза, которые были связаны с недоеданием.
Расстройство, связанное с употреблением алкоголя, и курение табака повышают риск заболевания туберкулезом. В 2021 г. 0,74 миллиона новых случаев туберкулеза во всем мире были связаны с расстройствами, связанными с употреблением алкоголя, а 0,69 миллиона — с курением.
Глобальное воздействие туберкулеза
Туберкулез встречается во всех частях мира. В 2021 г. наибольшее число новых случаев ТБ было зарегистрировано в Регионе ВОЗ для Юго-Восточной Азии (46% новых случаев), затем следует Африканский регион ВОЗ (23% новых случаев) и Западно-Тихоокеанский регион ВОЗ (18%).
В 2020 г. 87% новых случаев ТБ произошло в 30 странах с высоким бременем ТБ. На восемь стран приходилось более двух третей общемирового объема: Индия, Индонезия, Китай, Филиппины, Пакистан, Нигерия, Бангладеш и Демократическая Республика Конго.
Симптомы и диагностика
Общими симптомами активного туберкулеза легких являются кашель с мокротой и кровью, боли в груди, слабость, потеря веса, лихорадка и ночная потливость. ВОЗ рекомендует использовать быстрые молекулярные диагностические тесты в качестве начального диагностического теста для всех лиц с признаками и симптомами ТБ, поскольку они обладают высокой диагностической точностью и приведут к значительному улучшению раннего выявления ТБ и лекарственно-устойчивого ТБ. Экспресс-тесты, рекомендованные ВОЗ, — это анализы Xpert MTB/RIF Ultra и Truenat.
Диагностика ТБ с множественной лекарственной устойчивостью и других устойчивых форм ТБ (см. раздел «ТБ с множественной лекарственной устойчивостью» ниже), а также ВИЧ-ассоциированного ТБ может быть сложной и дорогостоящей задачей.
Туберкулез особенно трудно диагностировать у детей.
Лечение
Туберкулез — излечимое и излечимое заболевание. Лекарственно-чувствительный ТБ лечится стандартным 4-месячным или 6-месячным курсом из 4 противомикробных препаратов, которые предоставляются пациенту при поддержке медицинского работника или обученного помощника по лечению. Без такой поддержки соблюдение режима лечения затруднено.
С 2000 года благодаря диагностике и лечению туберкулеза было спасено около 74 миллионов жизней.
ТБ и ВИЧ
Люди, живущие с ВИЧ, в 16 (интервал неопределенности: 14–18) раз чаще заболевают туберкулезом, чем люди без ВИЧ.
ВИЧ и туберкулез представляют собой смертельную комбинацию, в которой каждый из них ускоряет развитие другого. В 2021 году около 187 000 человек умерли от ВИЧ-ассоциированного туберкулеза. Доля зарегистрированных больных ТБ, у которых был документально подтвержден результат теста на ВИЧ в 2021 г., составила всего 76% по сравнению с 73% в 2020 г. Африканский регион ВОЗ имеет самое высокое бремя ВИЧ-ассоциированного ТБ В целом в 2021 г. только 46% ТБ пациенты, о которых известно, что они живут с ВИЧ, получали АРТ.
Африканский регион ВОЗ имеет самое высокое бремя ВИЧ-ассоциированного ТБ В целом в 2021 г. только 46% ТБ пациенты, о которых известно, что они живут с ВИЧ, получали АРТ.
ВОЗ рекомендует 12-компонентный подход к совместной деятельности по борьбе с ТБ-ВИЧ, включая действия по профилактике и лечению инфекций и заболеваний, для снижения смертности.
Туберкулез с множественной лекарственной устойчивостью
Противотуберкулезные препараты использовались в течение десятилетий, и штаммы, устойчивые к одному или нескольким лекарствам, были зарегистрированы в каждой обследованной стране. Лекарственная устойчивость возникает, когда противотуберкулезные препараты используются ненадлежащим образом, из-за неправильного назначения медицинских работников, некачественных лекарств и преждевременного прекращения лечения пациентами.
Туберкулез с множественной лекарственной устойчивостью (МЛУ-ТБ) — это форма туберкулеза, вызываемая бактериями, которые не реагируют на изониазид и рифампицин, два наиболее эффективных противотуберкулезных препарата первого ряда. МЛУ-ТБ поддается лечению и излечим с помощью препаратов второго ряда. Однако варианты лечения второй линии ограничены и требуют обширной химиотерапии (от 9 месяцев до 20 месяцев лечения) дорогими и токсичными лекарствами.
МЛУ-ТБ поддается лечению и излечим с помощью препаратов второго ряда. Однако варианты лечения второй линии ограничены и требуют обширной химиотерапии (от 9 месяцев до 20 месяцев лечения) дорогими и токсичными лекарствами.
В некоторых случаях может развиться более обширная лекарственная устойчивость. Туберкулез, вызванный бактериями, которые не реагируют на наиболее эффективные противотуберкулезные препараты второго ряда, может оставить пациентов с ограниченными возможностями лечения.
МЛУ-ТБ остается кризисом общественного здравоохранения и угрозой безопасности здравоохранения.
В соответствии с рекомендациями ВОЗ для выявления МЛУ/РУ-ТБ требуется бактериологическое подтверждение ТБ и тестирование на лекарственную устойчивость с использованием экспресс-тестов, культуральных методов или технологий секвенирования.
Для лечения МЛУ/РУ-ТБ требуется курс препаратов второго ряда в течение как минимум 9 месяцев и до 20 месяцев, сопровождаемый консультированием и мониторингом нежелательных явлений. ВОЗ рекомендует расширить доступ к полностью пероральным схемам лечения.
ВОЗ рекомендует расширить доступ к полностью пероральным схемам лечения.
Только примерно каждый третий человек с лекарственно-устойчивым ТБ получил доступ к лечению в 2020 г.
Во всем мире в 2019 г. показатель успешного лечения больных МЛУ/РУ-ТБ составил 60%. В 2020 г. ВОЗ рекомендовала новый более короткий (9–11 месяцев) и полностью пероральный режим для пациентов с МДБ-ТБ. Результаты исследований показали, что пациентам легче завершить курс по сравнению с более длительными режимами, которые длятся до 20 месяцев. Перед началом лечения по этой схеме следует исключить резистентность к фторхинолонам.
К концу 2021 года 92 страны начали использовать более короткие схемы лечения МЛУ-ТБ, а 109 стран начали использовать бедаквилин, чтобы повысить эффективность лечения МЛУ-ТБ.
Катастрофические затраты
Цель Стратегии ВОЗ по ликвидации ТБ «Ни один больной ТБ и члены их домохозяйств не несут катастрофических расходов в результате заболевания ТБ», отслеживаемый странами и ВОЗ с момента принятия Стратегии WHA67. 1 по ликвидации ТБ в 2015 г., показывает, что мир не достиг рубежа в 0% к 2020 г.
1 по ликвидации ТБ в 2015 г., показывает, что мир не достиг рубежа в 0% к 2020 г.
Согласно результатам 27 национальных обследований расходов, с которыми сталкиваются больные ТБ и их домохозяйства, процент катастрофических расходов* колебался от 13% до 92%, а среднее значение, взвешенное по количеству зарегистрированных случаев в каждой стране, составило 48%.
*общие расходы > 20% годового дохода домохозяйства
Инвестиции в профилактику, диагностику и лечение ТБ и исследования
13 миллиардов долларов США ежегодно необходимы для профилактики, диагностики, лечения и ухода за ТБ для достижения глобальных целей, согласованных в ООН совещание высокого уровня по туберкулезу.
- Глобальные расходы на основные противотуберкулезные услуги сократились с 6,0 млрд долларов США в 2019 г. до 5,4 млрд долларов США в 2021 г., что составляет менее половины глобального целевого показателя.
- Из 5,4 млрд долларов США, потраченных на лечение и услуги по лечению туберкулеза в 2021 г.
 , 79% поступило из внутренних источников, при этом на страны БРИКС (Бразилия, Российская Федерация, Индия, Китай и Южная Африка) пришлось 2,7 млрд долларов США (64% от общей суммы внутреннее финансирование).
, 79% поступило из внутренних источников, при этом на страны БРИКС (Бразилия, Российская Федерация, Индия, Китай и Южная Африка) пришлось 2,7 млрд долларов США (64% от общей суммы внутреннее финансирование).
В странах с низким и средним уровнем дохода международное донорское финансирование по-прежнему имеет решающее значение. Основным источником является Глобальный фонд для борьбы со СПИДом, туберкулезом и малярией (Глобальный фонд).
- Правительство Соединенных Штатов (США) является крупнейшим спонсором Глобального фонда, а также крупнейшим двусторонним донором; в целом на него приходится около 50% финансирования борьбы с туберкулезом международными донорами.
- На исследования и разработки, по данным Группы действий по лечению, в 2020 году было доступно только 0,9 млрд долларов США из 2 млрд долларов США, необходимых в год для ускорения разработки новых инструментов. Для ускорения разработки новых инструментов требуется как минимум дополнительно 1,1 млрд долларов США в год.

Глобальные обязательства и ответные меры ВОЗ
26 сентября 2018 г. Организация Объединенных Наций (ООН) провела свое первое совещание высокого уровня по ТБ, на котором обсуждалось состояние эпидемии ТБ и способы прекращения уровне глав государств и правительств. Она последовала за первой глобальной министерской конференцией по туберкулезу, организованной ВОЗ и правительством России в ноябре 2017 г. Результатом стала политическая декларация, согласованная всеми государствами-членами ООН, в которой были подтверждены существующие обязательства в отношении ЦУР и Стратегии ВОЗ по ликвидации туберкулеза, а также новые добавлены.
Задача 3.3 ЦУР включает прекращение эпидемии ТБ к 2030 г. Стратегия «Положить конец ТБ» определяет этапы (на 2020 и 2025 гг.) и задачи (на 2030 и 2035 гг.) по сокращению случаев заболевания ТБ и смертности от него. Задачи на 2030 г. – снижение смертности от ТБ на 90% и заболеваемости ТБ на 80% (новых случаев на 100 000 населения в год) по сравнению с уровнями 2015 г. Целевые ориентиры на 2020 г. – снижение на 35% смертности от туберкулеза и снижения заболеваемости туберкулезом на 20%. Стратегия также включает достижение к 2020 г. цели, согласно которой больные туберкулезом и члены их домохозяйств не понесут катастрофических расходов в результате заболевания туберкулезом.
Целевые ориентиры на 2020 г. – снижение на 35% смертности от туберкулеза и снижения заболеваемости туберкулезом на 20%. Стратегия также включает достижение к 2020 г. цели, согласно которой больные туберкулезом и члены их домохозяйств не понесут катастрофических расходов в результате заболевания туберкулезом.
Политическая декларация встречи высокого уровня ООН включала четыре новые глобальные цели:
- вылечить 40 миллионов человек от туберкулеза за пятилетний период 2018–2022 гг.;
- охват не менее 30 миллионов человек профилактическим лечением латентной формы туберкулеза за 5-летний период 2018–2022 гг.;
- ежегодно мобилизовывать не менее 13 миллиардов долларов США для всеобщего доступа к диагностике, лечению и уходу за больными ТБ к 2022 г.;
- ежегодно мобилизовывать не менее 2 миллиардов долларов США на исследования в области ТБ.
Как указано в политической декларации:
- В 2019 г. ВОЗ завершила разработку и опубликовала Многосекторальную систему подотчетности по туберкулезу (MAF-TB).
 отчет и обзор прогресса с привлечением руководства высокого уровня, всех соответствующих секторов, гражданского общества и других заинтересованных сторон.
отчет и обзор прогресса с привлечением руководства высокого уровня, всех соответствующих секторов, гражданского общества и других заинтересованных сторон. - В 2020 году при поддержке ВОЗ был разработан и выпущен доклад Генерального секретаря ООН Генеральной Ассамблее о ходе работы.
- Примеры руководства высокого уровня по многосекторальной подотчетности включают инициативы президента или главы государства по ликвидации туберкулеза и формализованные механизмы вовлечения и подотчетности заинтересованных сторон в Индии, Индонезии, Пакистане, Филиппинах и Вьетнаме, а также национальные кампании по стимулированию таких как «Гонка за ликвидацию туберкулеза».
ВОЗ тесно сотрудничает со странами, партнерами и гражданским обществом в расширении масштабов противотуберкулезных мероприятий. ВОЗ выполняет шесть основных функций для содействия достижению целей политической декларации совещания высокого уровня ООН, ЦУР, Стратегии по ликвидации туберкулеза и стратегических приоритетов ВОЗ:
- Обеспечение глобального лидерства в борьбе с ТБ посредством разработки стратегии, политического и многосекторального взаимодействия, усиления контроля и подотчетности, адвокации и партнерства, в том числе с гражданским обществом;
- Формирование программы исследований и инноваций в области ТБ и стимулирование создания, перевода и распространения знаний;
- Установление норм и стандартов по профилактике и лечению ТБ, а также поощрение и содействие их внедрению;
- Разработка и продвижение этических и научно обоснованных вариантов политики профилактики и лечения ТБ;
- Обеспечение предоставления специализированной технической поддержки государствам-членам и партнерам совместно с региональными и страновыми бюро ВОЗ, стимулирование изменений и наращивание устойчивого потенциала;
- Мониторинг и отчетность о состоянии эпидемии ТБ и прогрессе в финансировании и осуществлении ответных мер на глобальном, региональном и страновом уровнях.