Характеристика лейкоцитарных индексов у новорожденных
Общая характеристика лейкоцитов
Определение 1
Лейкоциты – это группа клеток крови, неоднородных по функциям и внешнему виду, отличительными признаками которых является наличие ядра и отсутствие самостоятельной окраски.
Замечание 1
Главной функцией лейкоцитов является удаление продуктов разрушения тканей и защита организма от различных патогенов.
В зависимости от наличия в цитоплазме клетки специфических гранул все лейкоциты подразделяются на две группы: гранулоциты (базофилы, нейтрофилы (сегментоядерные, палочкоядерные), эозинофилы) и агранулоциты (лимфоциты, мононуклеарные фагоциты (моноциты, дендритные клетки, тканевые макрофаги)).
Характеристика различных видов лейкоцитов:
- Нейтрофилы. Ядра молодых форм имеют вид палочки, затем по мере созревания нейтрофилов их ядро разделяется на 3-4 сегмента, которые соединены тонкими хроматиновыми нитями. Основная функция нейтрофилов — защита организма от инфекционно-токсических агентов, которая осуществляется путем фагоцитоза и переваривания микробных и различных других патологических для организма клеток, а также за счет выработки целого ряда ферментов, обладающих бактерицидным действием.
- Эозинофилы. Ядро этих клеток чаще всего состоит из двух сегментов. У эозинофилов также имеется фагоцитарная активность, однако она выражена значительно меньше, чем у нейтрофилов, поэтому фагоцитоз нельзя считать основной их функцией. Главная же роль эозинофилов заключается в метаболизме гистамина, который они активно адсорбируют на своей поверхности в местах его максимального скопления. Затем с помощью фермента гистаминазы эозинофилы инактивируют гистамин, а также переносят его к органам выделения – кишечнику и легким. Такой функцией эозинофилов объясняется возрастание их количества при глистных инвазиях, аллергических реакциях и аутоиммунных заболеваниях.

- Базофилы. В цитоплазме этих клеток присутствуют крупные гранулы, содержащие большое количество гистамина, гепарина и гиалуроновой кислоты, синтез которых и является главной функцией базофилов. При связывании антигенов на поверхности базофилов, они выделяют из гранул гистамин, вызывающий такие проявления аллергических реакций, как покраснение кожи, расширение сосудов, зудящую сыпь. Гепарин поддерживает жидкое состояние крови.
- Лимфоциты. Эти клетки обеспечивают специфический иммунный ответ при различных инфекционных заболеваниях за счет выработки специфических белков – иммуноглобулинов (антител). Также они принимают активное участие в разрушении токсических веществ, которые образуются в самом организме.
- Моноциты. Это самые крупные элементы периферической крови, функция которых заключается в неспецифической защите организма за счет наибольшей фагоцитарной активности среди всех лейкоцитов.
Особенности лейкоцитарных показателей крови у новорожденных
Замечание 2
При отсутствии патологических процессов количество различных видов лейкоцитов в крови должно находиться примерно в одном процентном соотношении.
Нормы этих показателей для новорожденных детей отличаются от таковых для взрослых людей и детей других возрастных групп в силу еще не сформировавшейся до конца иммунной системы. Наиболее значимые отличия в лейкоцитарной формуле новорожденных связаны с содержанием лимфоцитов и нейтрофилов, в то время как остальные показатели «белых» клеток крови не имеют существенных отличий от показателей взрослых людей.
Особенности лейкоцитарных показателей крови у новорожденных:
- В течение первой недели жизни ребенка различные формы нейтрофилов составляют примерно 60-65% всех лейкоцитов крови, а на долю лимфоцитов приходится 30-35%.
- Затем постепенно количество нейтрофилов сокращается, а количество лимфоцитов, наоборот, увеличивается, и к началу второй недели жизни (обычно на четвертый день) их соотношение становится примерно равным (около 45%).
 Этот этап получил название «первого физиологического перекреста» лейкоцитарной формулы.
Этот этап получил название «первого физиологического перекреста» лейкоцитарной формулы. - Далее на 10-14 дне жизни новорожденного в его крови отмечается уже физиологический лимфоцитоз – на долю лимфоцитов приходится около 55-60% всех лейкоцитов. Другой характерной особенностью этого периода является увеличение количества моноцитов до 10%. Лимфоцитоз у детей вплоть до 4-5- летнего возраста представляет собой физиологический компенсаторный механизм, обусловленный становлением иммунной системы в результате выраженной стимуляции неокрепшего детского организма антигенами.
- Движение показателей лейкоцитарной формулы ребенка к значениям взрослого человека начинается в 4-5лет, когда происходит «второй физиологический перекрест» лейкоцитарной формулы.
- Картина лейкограммы взрослого человека устанавливается ближе к 10 годам (доля сегментоядерных нейтрофилов — 47-72%, лимфоцитов- 19-37%, моноцитов — 6-8%, эозинофилов — 0,5-5%, базофилов — 0-1%).
Лейкоцитарные индексы у новорожденных
Однако абсолютных значений тех или иных показателей лейкоцитов иногда может быть недостаточно для объективной оценки состояния крови в связи с индивидуальными особенностями организма, поэтому было предложено рассчитывать ряд индексов лейкоцитарной формулы, определение которых также имеет большое значение при подозрении на внутриутробное инфицирование.
Наиболее распространенные лейкоцитарные индексы и их значения у доношенных здоровых детей в первые сутки жизни:
- Нейтрофильный индекс (НИ). Для его расчета сумму всех молодых форм нейтрофилов (палочкоядерных, юных, миелоцитов) делят на общее количество нейтрофилов. Полученное значение в норме не должно превышать 0,21 (0, 17 -0,21).
- Лейкоцитарный индекс (ЛИ). Для его расчета количество лимфоцитов делят на число сегментоядерных нейтрофилов. Полученное значение в норме составляет от 0,5 до 0,96 и отражает соотношение гуморального (лимфоциты) и клеточного (нейтрофилы) звеньев иммунитета.

- Лимфоцитарно-гранулоцитарный индекс (ИЛГ). Для его расчета количество лимфоцитов умножают на 10 и полученное значение делят на сумму всех гранулоцитов (сегментоядерных и палочкоядерных нейтрофилов, миелоцитов, метамиелоцитов, миелоцитов, базофилов и эозинофилов). Нормальными значениями этого показателя являются цифры от 3, 85 до 5,09. ИЛГ играет большую роль в дифференциальной диагностике инфекционной интоксикации и аутоинтоксикации.
- Индекс сдвига лейкоцитов (ИСЛ). Для его расчета сумму всех гранулоцитов (сегментоядерных и палочкоядерных нейтрофилов, миелоцитов, метамиелоцитов, миелоцитов, базофилов и эозинофилов) делят на сумму моноцитов и лимфоцитов. Нормальные значения этого показателя: от 2,41 до 3,57. Его повышение отмечается при активных воспалительных процессах и нарушениях иммунологической реактивности.
|
Особенности гемограммы развивающегося организма Кровь эмбриона Первые клетки – мегалобласты I и II генерации, первичные эритроциты (мегалоциты). К 3 мес эмбрионального развития количество эритробластов составляет до 8% всех элементов красной крови. Количество лейкоцитов – около 1х109/л (75% относится к бластам, остальные – к гранулоцитам). Лимфоциты появляются с 4–5 мес, моноциты – с 5-го. С 3–4 мес количество ретикулоцитов составляет 705‰, с 4–5 мес – 501‰, с 5–7 мес – 271‰. Кровь недоношенных детей Количество Нb – 155–217 г/л, эритроцитов – (7,2– 4,45)х1012/л. При исследовании мазков крови отмечается эритробластоз, ретикулоцитоз, повышенное количество полихроматофилов. Отмечается анизоцитоз и умеренный пойкилоцитоз. Количество лейкоцитов – (3,6–36)х10 Кровь новорожденных Содержание Нb –167–240 г/л, количество эритроцитов – (4,5–7,5)х1012/л. Выражен анизоцитоз, диаметр эритроцитов 3,25–10,25 мкм. Выражены явления полихромазии, количество ретикулоцитов 8–42‰. Количество лейкоцитов (10–30)х109/л, со стороны нейтрофилов сдвиг влево до миелоцитов. Число лимфоцитов при рождении составляет 16–34%, к концу новорожденности 50–60%. Отмечается анизоцитоз кровяных пластинок, наличие гигантских форм. Содержание Нb в первые месяцы снижается, к 5–6 мес – 116–133 г/л, количество эритроцитов (6–3)х1012/л. Анизоцитоз и полихромазия выражены слабее. Содержание ретикулоцитов 2–21‰. Количество лейкоцитов (6,2–22)х109/л. Со стороны нейтрофилов имеется умеренный сдвиг влево, помимо малых и средних лимфоцитов обнаруживаются и большие. Характерен лимфоцитоз и умеренный моноцитоз, обнаруживаются плазматические клетки лимфоидного и лимфобластического типа. Количество тромбоцитов (230–250)х109/л, анизоцитоз кровяных пластинок выражен слабее. Кровь детей старше года Содержание Нb постепенно нарастает, достигая к 5–8 годам 126 – 150 г/л, к 8–15 годам – 133–153 г/л. Количество эритроцитов увеличивается до уровня взрослого человека. Количество ретикулоцитов 2–6‰, общее количество лейкоцитов снижается до (8–7)х10
Таблица 1.2.1. Показатели гемограммы у новорожденных (И. Н. Усов)
Таблица 1.
Таблица 1.
Таблица 1.
Таблица 1.
Примечание.
Таблица 1.2.6. Показатели белой крови здоровых детей (Е. Д. Гольдберг, Р. М. Тарлова)
Примечание.
Таблица 1.2.7. Показатели системы гемостаза у здоровых детей 3-14 лет (М. С. Игнатова, Ю. В. Вельтищев)
Таблица 1.
Таблица 1.
Таблица 1.
Таблица 1.
Таблица 1.2.12. Объем циркулирующей крови у здоровых детей, мл/кг (Г. А. Баиров)
Таблица 1.
|
||||||||||||||||
Лейкоцитарная формула (с микроскопией мазка крови при выявлении патологических изменений)
Лейкоцитарная формула – процентное соотношение различных форм лейкоцитов в сыворотке крови и подсчет их числа в единице объема. 9/л (10 в ст. 9/л).
9/л (10 в ст. 9/л).
Какой биоматериал можно использовать для исследования?
Венозную, капиллярную кровь.
Как правильно подготовиться к исследованию?
- Исключить из рациона алкоголь за сутки перед сдачей крови.
- Не принимать пищу за 2-3 часа до исследования (можно пить чистую негазированную воду).
- Исключить физическое и эмоциональное перенапряжение и не курить за 30 минут до исследования.
Общая информация об исследовании
Лейкоциты, как и другие клетки крови, образуются в костном мозге. Основная их функция – борьба с инфекцией, а также ответ на повреждение тканей.
В отличие от эритроцитов, популяция которых является однородной, лейкоциты делятся на 5 типов, отличающихся по внешнему виду и выполняемым функциям: нейтрофилы, лимфоциты, моноциты, эозинофилы, базофилы.
Лейкоциты образуются из стволовых клеток костного мозга. Они живут недолго, поэтому происходит их постоянное обновление. Продукция лейкоцитов в костном мозге возрастает в ответ на любое повреждение тканей, это часть нормального воспалительного ответа. Разные типы лейкоцитов имеют несколько разные функции, однако они способны к координированным взаимодействиям путем «общения» с использованием определенных веществ – цитокинов.
Долгое время лейкоцитарную формулу высчитывали вручную, однако современные анализаторы позволяют гораздо точнее проводить исследование в автоматическом режиме (врач смотрит 100-200 клеток, анализатор – несколько тысяч). Если анализатором определяются атипичные формы клеток либо выявляются значительные отклонения от референсных значений, то лейкоцитарная формула дополняется микроскопическим исследованием мазка крови, который позволяет диагностировать некоторые заболевания, такие как, например, инфекционный мононуклеоз, определить степень тяжести инфекционного процесса, описать тип выявленных атипичных клеток при лейкозе.
Нейтрофилы – наиболее многочисленные из лейкоцитов – первыми начинают бороться с инфекцией и первыми появляются в месте повреждения тканей.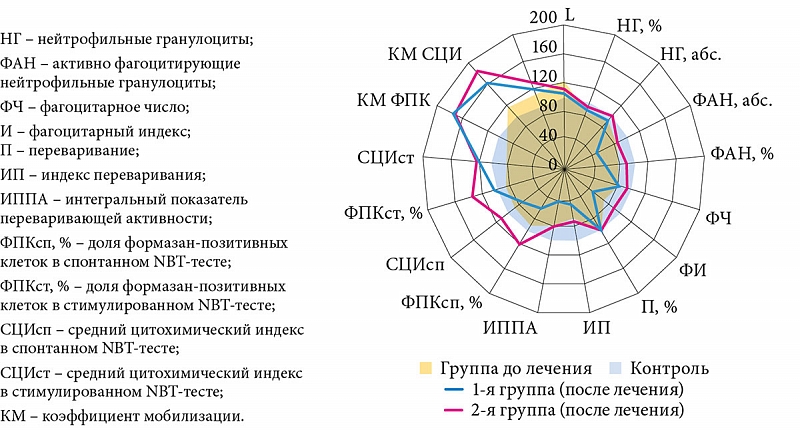 Нейтрофилы имеют ядро, разделенное на несколько сегментов, поэтому их еще называют сегментоядерными нейтрофилами или полиморфноядерными лейкоцитами. Эти названия, однако, относятся только к зрелым нейтрофилам. Созревающие формы (юные, палочкоядерные) содержат цельное ядро.
Нейтрофилы имеют ядро, разделенное на несколько сегментов, поэтому их еще называют сегментоядерными нейтрофилами или полиморфноядерными лейкоцитами. Эти названия, однако, относятся только к зрелым нейтрофилам. Созревающие формы (юные, палочкоядерные) содержат цельное ядро.
В очаге инфекции нейтрофилы окружают бактерии и ликвидируют их путем фагоцитоза.
Лимфоциты – одно из важнейших звеньев иммунной системы, они имеют большое значение в уничтожении вирусов и борьбе с хронической инфекцией. Существует два вида лимфоцитов – Т и В (в лейкоцитарной формуле подсчета видов лейкоцитов по отдельности нет). B-лимфоциты вырабатывают антитела – специальные белки, которые связываются с чужеродными белками (антигенами), находящимися на поверхности вирусов, бактерий, грибов, простейших. Окруженные антителами клетки, содержащие антигены, доступны для нейтрофилов и моноцитов, которые убивают их. Т-лимфоциты способны разрушать зараженные клетки и препятствовать распространению инфекции. Также они распознают и уничтожают раковые клетки.
Моноцитов в организме не очень много, однако они осуществляют крайне важную функцию. После непродолжительной циркуляции в кровяном русле (20-40 часов) они перемещаются в ткани, где превращаются в макрофаги. Макрофаги способны уничтожать клетки, так же как нейтрофилы, и держать на своей поверхности чужеродные белки, на которые реагируют лимфоциты. Они играют роль в поддержании воспаления при некоторых хронических воспалительных заболеваниях, таких как ревматоидный артрит.
Эозинофилов в крови содержится небольшое количество, они тоже способны к фагоцитозу, однако в основном играют другую роль – борются с паразитами, а также принимают активное участие в аллергических реакциях.
Базофилов в крови также немного. Они перемещаются в ткани, где превращаются в тучные клетки. Когда они активируются, из них выделяется гистамин, обусловливающий симптомы аллергии (зуд, жжение, покраснение).
Для чего используется исследование?
- Для оценки способности организма противостоять инфекции.

- Для определения степени выраженности аллергии, а также наличия в организме паразитов.
- Для выявления неблагоприятного воздействия некоторых лекарственных препаратов.
- Для оценки иммунного ответа на вирусные инфекции.
- Для дифференциальной диагностики лейкозов и для оценки эффективности их лечения.
- Для контроля за воздействием на организм химиотерапии.
Когда назначается исследование?
- Совместно с общим анализом крови при плановых медицинских осмотрах, подготовке к хирургическому вмешательству.
- При инфекционном заболевании (или подозрении на него).
- Если есть подозрение на воспаление, аллергическое заболевание или заражение паразитами.
- При назначении некоторых лекарственных препаратов.
- При лейкозах.
- При контроле за различными заболеваниями.
Что означают результаты?
Лейкоцитарная формула обычно интерпретируется в зависимости от общего количества лейкоцитов. Если оно отклоняется от нормы, то ориентирование на процентное соотношение клеток в лейкоцитарной формуле может приводить к ошибочным заключениям. В этих ситуациях оценка производится на основании абсолютного количества каждого вида клеток (в литре – 1012/л – или микролитре – 109/л). Увеличение или уменьшение количества какой-либо популяции клеток обозначается как «нейтрофилез» и «нейтропения», «лимфоцитоз» и «лимфопения», «моноцитоз» и «моноцитопения» и т. д.
Референсные значения
Лейкоциты
|
Возраст |
Референсные значения |
|
Меньше 1 года |
6 — 17,5 *10^9/л |
|
1-2 года |
6 — 17 *10^9/л |
|
2-4 года |
5,5 — 15,5 *10^9/л |
|
4-6 лет |
5 — 14,5 *10^9/л |
|
6-10 лет |
4,5 — 13,5 *10^9/л |
|
10-16 лет |
4,5 — 13 *10^9/л |
|
Больше 16 лет |
4 — 10 *10^9/л |
Нейтрофилы
|
Возраст |
Референсные значения |
|
Меньше 1 года |
1,5 — 8,5 *10^9/л |
|
1-2 года |
1,5 — 8,5 *10^9/л |
|
2-4 года |
1,5 — 8,5 *10^9/л |
|
4-6 лет |
1,5 — 8 *10^9/л |
|
6-8 лет |
1,5 — 8 *10^9/л |
|
8-10 лет |
1,8 — 8 *10^9/л |
|
10-16 лет |
1,8 — 8 *10^9/л |
|
Больше 16 лет |
1,8 — 7,7 *10^9/л |
Нейтрофилы, %
|
Возраст |
Референсные значения |
|
Меньше 1 года |
16 — 45 % |
|
1-2 года |
28 — 48 % |
|
2-4 года |
32 — 55 % |
|
4-6 лет |
32 — 58 % |
|
6-8 лет |
38 — 60 % |
|
8-10 лет |
41 — 60 % |
|
10-16 лет |
43 — 60 % |
|
Больше 16 лет |
47 — 72 % |
Чаще всего уровень нейтрофилов повышен при острых бактериальных и грибковых инфекциях.9/л
Лимфоциты, %
|
Возраст |
Референсные значения |
|
Меньше 1 года |
45 — 75 % |
|
1-2 года |
37 — 60 % |
|
2-4 года |
33 — 55 % |
|
4-6 лет |
33 — 50 % |
|
6-8 лет |
30 — 50 % |
|
8-10 лет |
30 — 46 % |
|
10-16 лет |
30 — 45 % |
|
Больше 16 лет |
19 — 37 % |
Причины повышенного уровня лимфоцитов:
- инфекционный мононуклеоз и другие вирусные инфекции (цитомегаловирус, краснуха, ветряная оспа, токсоплазмоз),
- некоторые бактериальные инфекции (туберкулез, коклюш),
- онкологические заболевания костного мозга (хронический лимфолейкоз) и лимфоузлов (неходжкинская лимфома).9/л.
Базофилы, %: 0 — 1,2 %.
Увеличение содержания базофилов встречается редко: при онкологических заболеваниях костного мозга и лимфоузлов, истинной полицитемии, аллергических заболеваниях.
Уменьшаться количество базофилов может при острой фазе инфекции, гипертиреозе, длительной терапии кортикостероидами (преднизолоном).
Скачать пример результатаТакже рекомендуется
Кто назначает исследование?
Врач общей практики, терапевт, педиатр, хирург, инфекционист, гематолог, гинеколог, уролог.
Клинико-лабораторные проявления врожденных инфекционно-воспалительных заболеваний у детей с экстремально низкой и очень низкой массой тела при рождении
Цель исследования. Изучить особенности клинико-лабораторных проявлений врожденных инфекций у детей с экстремально низкой (ЭНМТ) и очень низкой массой тела (ОНМТ) при рождении.ФГБУ Научный центр акушерства, гинекологии и перинатологии им. академика В.И. Кулакова Минздрава России, Москва
Материал и методы. В проспективное исследование были включены 129 новорожденных с ЭНМТ и ОНМТ, у 51 из которых была выявлена врожденная инфекция; 52 ребенка составили группу высокого риска реализации врожденной инфекции, у 26 новорожденных была исключена врожденная инфекция. Исследовали клинический анализ крови на 1-е и 3-и сутки жизни, биохимический анализ крови, гемостазиограмму – на 3-и сутки жизни; кислотно-основное состояние (КОС) и лактатемия капиллярной крови оценивались каждые 6–8 часов, С-реактивный белок (СРБ) и прокальцитонин (ПКТ) – на 3-и сутки жизни. Нейросонография, ультразвуковое исследование органов брюшной полости, ЭХО-кардиография, рентгенография органов грудной клетки выполнялись в 1-е сутки жизни, в зависимости от тяжести состояния – повторно на 3-и сутки жизни.
Результаты исследования. Характерным проявлением врожденных инфекционно-воспалительных заболеваний у детей с ЭНМТ и ОНМТ в первые 72 часа жизни является полиорганная недостаточность с развитием преимущественно дыхательной, почечной недостаточности, гемодинамических нарушений, сопровождающаяся выраженными метаболическими нарушениями (гипергликемией и стойкими нарушениями КОС). Воспалительные изменения клинического анализа крови не имеют достаточной чувствительности и специфичности для верификации диагноза врожденной инфекции у детей с ЭНМТ и ОНМТ в первые 72 часа жизни. Исключение составляет нейтрофильный индекс, измеренный в первые сутки жизни, который обладает умеренной специфичностью, однако имеет низкую чувствительность.
Заключение. Изолированное повышение одного из биохимических маркеров системного воспаления (СРБ или ПКТ) при отсутствии других клинико-лабораторных признаков не может использоваться в качестве достоверного признака диагностики врожденной инфекции у детей с ЭНМТ и ОНМТ, по крайней мере, в первые 72 часа жизни.полиорганная недостаточность
клинический анализ крови
С-реактивный белок
прокальцитонин
глубоконедоношенные новорожденные
1. Самсыгина Г.А. О предрасполагающих факторах и факторах риска развития неонатального сепсиса и о современных подходах его лечения. Педиатрия. Журнал имени Г.Н. Сперанского. 2012; 91(3): 32-7.
Милая Ольга Владимировна, аспирант отделения реанимации и интенсивной терапии новорожденных ФГБУ НЦАГиП им. академика В.И. Кулакова Минздрава России. Адрес: 117997, Россия, Москва, ул. Академика Опарина, д. 4. Телефон: 8 (495) 438-22-77. E-mail: [email protected]
2. Шабалов Н.П. Общебиологическая проблема: закономерности и последствия перинатального инфицирования. Педиатрия. Журнал имени Г.Н. Сперанского. 2012; 91(3): 26-31.
3. Голубцова Ю.М., Дегтярев Д.Н. Современные подходы к профилактике, диагностике и лечению раннего неонатального сепсиса. Неонатология. 2014; 2: 15-25.
4. Антонов А.Г., Байбарина Е.Н. Внутриутробная пневмония (Критерии диагностики и стандарты лечения). Методические рекомендации. М.; 1997: 3-6.
5. Ионов О.В., Мостовой А.В., Овсянников Д.Ю. Дыхательные расстройства у новорожденных. В кн.: Володин Н.Н., ред. Неонатология. Национальное руководство. Краткое издание. М.: ГЕОТАР-Медиа; 2013: 204-10.
6. Самсыгина Г.А., Шабалов Н.П., Дегтярева М.В. Сепсис. В кн.: Володин Н.Н., ред. Неонатология. Национальное руководство. Краткое издание. М.: ГЕОТАР-Медиа; 2013: 766-70.
7. Report on the expert meeting on neonatal and paediatric sepsis. 8 June 2010, EMA London.
8. Janota J., Stranák Z., Statecá B., Dohnalová A., Šípek A., Šimák J. Characterization of multiple organ dysfunction syndrome in very low birthweight infants: a new sequential scoring system. Shock. 2001; 15(5): 348-52.
9. Wójkowska-Mach J., Borszewska-Kornacka M., Domańska J., Gadzinowski J., Gulczyńska E., Helwich E. et al. Early-onset infections of very-low-birth-weight infants in Polish neonatal intensive care units. Pediatr. Infect. Dis. J. 2012; 31(7): 691-5.
10. Cetinkaya M., Köksal N., Özkan H. A new scoring system for evaluation of multiple organ dysfunction syndrome in premature infants. Am. J. Crit. Care. 2012; 21(5): 328-37.
11. Shah B.A., Padbury J.F. Neonatal sepsis: an old problem with new insights. Virulence. 2014; 5(1): 170-8.
12. Decaro M.H., Vain N.E. Hyperglycaemia in preterm neonates: what to know, what to do. Early Hum. Dev. 2011; 87(Suppl.1): S19-22.
13. Makkar M., Gupta C., Pathak R., Garg S., Mahajan N.C. Performance evaluation of hematologic scoring system in early diagnosis of neonatal sepsis. J. Clin. Neonatol. 2013; 2(1): 25-9.
14. Arif S.A., Ehsan A., Arif M., Hussain J., Bano R. Early diagnosis of neonatal sepsis through haematological and biochemical markers. Gomal J. Med. Sci. 2013; 11(2): 178.
15. Jiang Z., Ye G.Y. 1:4 matched case-control study on influential factor of early onset neonatal sepsis. Eur. Rev. Med. Pharmacol. Sci. 2013; 17(18): 2460-6.
16. Hofer N., Zacharias E., Müller W., Resch B. An update on the use of C-reactive protein in early-onset neonatal sepsis: current insights and new tasks. Neonatology. 2012; 102(1): 25-36.
17. Remington J.S., Klein J.O., eds. Infectious diseases of the fetus and newborn infant. 3rd ed. Philadelphia: Saunders; 1990.
Ионов Олег Вадимович, к.м.н., руководитель отделения реанимации и интенсивной терапии новорожденных ФГБУ НЦАГиП им. академика В.И. Кулакова Минздрава России. Адрес: 117997, Россия, Москва, ул. Академика Опарина, д. 4. Телефон: 8 (495) 438-22-77. E-mail: [email protected]
Дегтярева Анна Владимировна, д.м.н., руководитель научно-консультативного педиатрического отделения ФГБУ НЦАГиП им. академика В.И. Кулакова Минздрава России. Адрес: 117997, Россия, Москва, ул. Академика Опарина, д. 4. Телефон: 8 (495) 438-26-00. E-mail: [email protected]
Левадная Анна Викторовна, к.м.н., научный сотрудник отделения клинической фармакологии ФГБУ НЦАГиП им. академика В.И. Кулакова Минздрава России. Адрес: 117997, Россия, Москва, ул. Академика Опарина, д. 4. Телефон: 8 (495) 438-26-00. E-mail: [email protected]
Дегтярев Дмитрий Николаевич, д.м.н., профессор, заместитель директора по научной работе ФГБУ НЦАГиП им. академика В.И. Кулакова Минздрава России. Адрес: 117997, Россия, Москва, ул. Академика Опарина, д. 4. Телефон: 8 (495) 438-23-88. E-mail: [email protected]Лейкоцитарная формула крови. Показатели, норма и расшифровка результатов анализа
Дифференцированный подсчет лейкоцитов (лейкоцитарная формула) может назначаться при плановых обследованиях, диагностике заболеваний, а также для контроля проводимой терапии.Стоимость услуги…
Фагоцитарная активность лейкоцитов напрямую влияет на уровень сопротивления организма чужеродной микрофлоре.Узнать больше…
Изменение содержания лейкоцитов в крови может быть следствием целого ряда факторов, а также свидетельствовать о наличии заболевания.Подробнее об обследовании…
Некоторые лаборатории могут предложить бесплатную консультацию специалиста по оказываемым услугам.Записаться…
Для того чтобы результаты анализов были максимально достоверным, необходимо правильно подготовиться к их сдаче.Как подготовиться?
Сэкономьте на медицинских услугах, став участником специальной дисконтной программы.Узнать больше…
Контроль качества клинических лабораторных исследований, осуществляемый по международным стандартам, – весомый аргумент при выборе лаборатории.Подробнее…
Лейкоциты играют важнейшую роль в организме — они обеспечивают защиту от различных вредных микроорганизмов, поглощая и обезвреживая чужеродные частицы. Поэтому, наблюдая за поведением этих клеток, можно обнаружить любой воспалительный процесс. Для комплексной диагностики состояния лейкоцитов в крови существует специальный анализ — лейкоцитарная формула (лейкоформула). Давайте разберемся, насколько полезным может быть это исследование.
Показатели лейкоформулы: норма содержания
Лейкоцитарная формула представляет собой соотношение нескольких видов лейкоцитов. Часто исследование назначают вместе с общим анализом крови. Нейтрофилы, базофилы, эозинофилы, моноциты, лимфоциты — эти белые кровяные тельца и являются объектом наблюдения. Рассмотрим подробнее каждую из составляющих анализа.
Нейтрофилы служат для обеспечения безопасности организма. Они способны распознавать вредоносные бактерии, захватывая и уничтожая их. Наличие базофилов в крови обусловливает появление различных аллергических реакций — эти клетки не позволяют вредным ядам и токсинам распространяться по всей кровеносной системе. Эозинофилы защищают нас от всевозможных паразитов, обеспечивая противопаразитарный иммунитет. Функции моноцитов совпадают с функциями нейтрофилов с тем лишь отличием, что фагоцитарная способность первых частиц выше, к тому же они не только устраняют вредные микроорганизмы, но и поглощают погибшие лейкоциты, очищая кровь, тем самым давая тканям возможность регенерировать. Лимфоциты способны распознавать и запоминать различные антигены, обеспечивая противовирусный и противоопухолевый иммунитет.
Общее количество лейкоцитов в крови у здорового человека приведено в таблице:
Возраст
Концентрация лейкоцитов
тыс./мкл (103 клеток/мкл)1 день — 12 месяцев
6,0 — 17,5
12 месяцев — 2 года
6,0 — 17,0
2 — 4 года
5,5 — 15,5
4 года — 6 лет
5,0 — 14,5
6 — 10 лет
4,50 — 13,5
10 — 16 лет
4,50 — 13,0
16 и более лет
4,50 — 11,0
Помимо общей лейкоцитарной формулы существуют так называемые лейкоцитарные индексы — исследование соотношений разных типов белых кровяных телец в крови. Одним из наиболее распространенных является лейкоцитарный индекс интоксикации, он служит для определения тяжести воспалительного процесса. Помимо него существуют индексы аллергизации, иммунореактивности и другие.
Для того чтобы выяснить соотношение белых кровяных телец в крови, врач назначает специальный анализ, результатом которого и является лейкоформула.
Как проводится анализ крови на определение лейкоцитарной формулы
Использование лейкоцитарной формулы для однозначной диагностики заболеваний довольно затруднительно, ведь соотношение частиц при различных патологических процессах в организме часто схоже. Полученные данные обычно применяют для отслеживания динамики заболевания и уровня эффективности лечения.
Подготовка к забору крови на анализ не слишком сложная — пациенту достаточно отказаться от приема пищи не менее чем за 4 часа до процедуры, а накануне лучше избегать серьезных физических и эмоциональных нагрузок.
Материалом для определения лейкоцитарной формулы служит венозная кровь. Перед процедурой лаборант специальным ремешком пережимает предплечье пациента, а потом вводит в вену в локтевом сгибе тонкую иглу, по которой кровь попадет непосредственно в пробирку. Конечно, нельзя назвать этот процесс совершенно безболезненным, но обычно он вызывает лишь слабые или умеренные болевые ощущения. Каплю полученной крови переносят на стеклянную пластинку, чтобы с помощью микроскопа определить количество и соотношение лейкоцитов. Если клиника оснащена современным оборудованием, то подсчет частиц ведет специальный аппарат — анализатор, а необходимость человеческого вмешательства возникает лишь в том случае, если результат показал сильные отклонения от нормы или наличие аномальных частиц.
Скорость получения результата анализа зависит от учреждения, в котором проводят исследование, но чаще всего это занимает не более нескольких дней. Оценку полученных значений проводит лечащий врач.
Расшифровка анализа с лейкоцитарной формулой
Существует несколько критериев, по которым специалист оценивает состояние крови и соотношение лейкоцитов.
Сдвиг лейкоцитарной формулы влево и вправоИсследование нейтрофилов в мазке крови имеет особое значение. Врач делает вывод о наличии или скорости развития патологии, исходя не только из их количества. Не последнюю роль играет «возраст» клеток, в частности, преобладание «молодых» форм нейтрофилов над «зрелыми» или наоборот. Сдвигом результат анализа называется потому, что запись формулы крови подчинена определенному порядку — сначала идет учет молодых форм нейтрофилов, а затем более зрелых клеток в порядке возрастания. Таким образом, при возникновении дисбаланса показатели «сдвигаются» в ту или иную сторону.
Увеличение количества «молодых» нейтрофилов означает сдвиг лейкоцитарной формулы влево и может означать наличие различных патологических процессов в организме. Он указывает на воспаление, некротические процессы в тканях, инфекционные заболевания, отравление пищей или газом, а также проявляется при приеме различных медикаментов. Но сдвиг лейкоформулы влево не обязательно свидетельствует о патологии — временный дисбаланс клеток может возникать после тяжелых физических нагрузок и довольно быстро приходит в норму.
Обратная ситуация, то есть сдвиг лейкоцитарной формулы вправо, означает преобладание зрелых нейтрофилов над молодыми. Такое распределение белых кровяных телец свидетельствует о лучевой болезни, недостатке витамина B12, а также о болезнях печени и почек. Сдвиг вправо характерен для пациентов, в недавнем времени перенесших переливание крови.
Повышение показателейУвеличение числа нейтрофилов в крови может быть признаком множества заболеваний, а также различных специфических состояний пациента. Этот эффект можно наблюдать при возникновении инфекционных болезней, в том числе и грибковых (например, кандидоз), ревматизме, повышении уровня глюкозы в крови при диабете, наличии раковых опухолей любой локализации, отравлениях свинцом или ртутью. Также большое количество нейтрофилов в крови наблюдается после тяжелых эмоциональных, физических, болевых нагрузок, а также под влиянием экстремально низких или высоких температур.
Превышение нормы лимфоцитов служит свидетельством наличия инфекционного заболевания, патологий крови, отравления свинцом или мышьяком, а также может быть последствием приема некоторых лекарственных препаратов.
После перенесенного инфекционного заболевания в крови пациента повышен уровень моноцитов. Также такое состояние крови характерно для людей с аутоиммунными заболеваниями, злокачественными опухолями и при отравлении тетрахлорэтаном и фосфором.
Интересный факт
Перед тем как погибнуть, лейкоциты способны передавать специфический сигнал об опасности находящимся рядом клеткам. К такому выводу пришли ученые из Австралии, проанализировавшие поведение клеток с помощью специального устройства, способного делать несколько сотен снимков в секунду.Повышенный уровень эозинофилов наблюдается при аллергии на антибиотики, лекарства от туберкулеза и судорожных состояний, паразитарной инвазии, некоторых патологиях кожи и легких, остром течении инфекционного заболевания.
Грипп, ветряная оспа, туберкулез — эти заболевания способны вызвать повышение в крови количества базофилов. Помимо этого концентрация белых кровяных телец данного типа возрастает при аллергических реакциях, язвенном колите, в результате гиперчувствительности к каким-либо пищевым продуктам, а также может указывать на наличие раковых опухолей в организме.
Понижение показателейЕсли концентрация нейтрофилов в крови существенно снижена, то врач может диагностировать одно из инфекционных заболеваний (брюшной тиф, туберкулез), повышенную чувствительность к медикаментам (антибиотики, антигистаминные и противовоспалительные препараты), анемию и анафилактический шок.
Лимфоциты в лейкоцитарной формуле имеют сниженные показатели при иммунодефицитных состояниях, острых воспалительных процессах в организме, почечной недостаточности и системной красной волчанке. Кроме этого, увеличение количества частиц свойственно людям, подвергшимся влиянию рентгенологического излучения.
Не менее серьезными причинами бывает вызвано снижение количества моноцитов в анализе крови. К причинам относятся онкогематологические заболевания, пиогенные инфекции и апластическая анемия. К тому же эффект в виде уменьшения количества моноцитов вызывает прием некоторых лекарственных препаратов и состояние сильного шока.
Самое начало воспаления можно диагностировать, если уровень эозинофилов значительно понижен. Также это случается при тяжелом протекании гнойной инфекции и при отравлении тяжелыми металлами.
Беременность, сильный стресс и период овуляции могут быть естественными причинами уменьшения количества базофилов в крови. Среди патологических причин присутствуют инфекционные заболевания и синдром Кушинга.
Лейкоцитарная формула помогает врачу диагностировать и отслеживать уровень эффективности лечения при аллергических реакциях, воспалениях, различных болезнях крови и других патологиях. Имея такие преимущества, как высокая точность, объективность и воспроизводимость, анализ по праву может считаться одним из самых показательных методов исследования крови. Провести процедуру в домашних условиях невозможно, поэтому для определения соотношения разных видов лейкоцитов в крови, следует обратиться в медицинское учреждение.
Динамика лейкоцитарных индексов у новорожденных телят
DOI: 10.24411/9999-007А-2020-10006
УДК 619:615.035Турков Владимир Георгиевич, ФГБОУ ВО Ивановская ГСХА, доктор ветеринарных наук, профессор, [email protected]
Клетикова Людмила Владимировна, ФГБОУ ВО Ивановская ГСХА, доктор биологических наук, профессор, [email protected]
Якименко Нина Николаевна, ФГБОУ ВО Ивановская ГСХА, кандидат ветеринарных наук, доцент, [email protected]
Маннова Мария Сергеевна, ФГБОУ ВО Ивановская ГСХА, кандидат биологических наук, доцент, [email protected]
Шишкина Наталья Петровна, ФГБОУ ВО Ивановская ГСХА, студентка 5 курса, [email protected].Исследование выполнено за счет средств федерального бюджета по заказу Минсельхоза России в 2020 году
Аннотация. В статье рассмотрено изменение общего количества лейкоцитов и соотношения их отдельных видов в период новорожденности у телят на фоне применения полиметилсилоксана полигидрата. Для оценки уровня интоксикации и адаптационного потенциала телят применены расчетные лейкоцитарные индексы крови. Полиметилсилоксана полигидрат эффективен для преодоления критического периода развития новорожденных телят.
Ключевые слова: телята, лейкоциты, лейкограмма, лейкоцитарные индексы, полиметилсилоксана полигидрат
Введение. Неонатальная и ранняя постнатальная патология телят наносит значительный экономический ущерб [6]. Для оценки состояния новорожденных телят применяют не только клинические методы, но и лабораторные исследования, и интегральные расчетные индексы крови. Лейкоцитарные индексы весьма точно указывают на уровень интоксикации, коррелируют с динамикой патологического процесса, позволяют оценить адаптационный потенциал и уровень стресса новорожденных животных [1, 3, 4, 7]. В настоящее время предложено порядка 20 интегральных показателей, которые условно можно разделить на 3 группы – индексы интоксикации, индексы неспецифической реактивности и индексы активности воспаления.
Цель настоящего исследования – анализ вариабельности отдельных видов лейкоцитов у телят в период новорожденности в условиях сельскохозяйственного производства.
Условия и методика исследования. Научная работа выполнена в 2020 г на кафедре акушерства, хирургии и незаразных болезней животных Ивановской ГСХА. В исследовании участвовало 48 клинически здоровых телят, полученных от коров костромской породы 3-4 летнего возраста. Содержание животных осуществлялось по стандартной технологии, принятой в хозяйстве.
Телятам, согласно плану ветеринарных мероприятий, в течение первых суток жизни ввели сыворотку против пастереллеза, сальмонеллеза, эшерихиоза, парагриппа-3 и инфекционного ринотрахеита крупного рогатого скота в соответствии с наставлением по применению. Для проведения эксперимента телят распределили по 12 голов в 4 группы, где первая служила контролем, 2-4 опытные. Контрольная группа получала основной рацион (молозиво и молочные продукты), 2, 3 и 4 группы, кроме основного рациона (ОР), спустя 2 часа после последнего кормления получали взвесь полиметилсилоксана полигидрата соответственно в дозе 0,1 г/кг, 0,3 г/кг и 0,5 г/кг живой массы.
Согласно схеме эксперимента, объектом послужили телята 1-15-суточного возраста, предметом – периферическая кровь. Взятие крови осуществляли у новорожденных телят и в утренние часы (до кормления) у 5-и 15-суточных телят из яремной вены.
Для достижения цели исследования определили концентрацию лейкоцитов с помощью автоматического гематологического анализатора BCE-90Vet, выполнили подсчет отдельных видов лейкоцитов на мазках, окрашенных по Романовскому-Гимзе. В соответствии с классификацией лейкоцитарных индексов [2] оценили изменение отдельных из них у телят контрольной и опытных групп при рождении, в 5- и 15-суточном возрасте.
Результаты и их обсуждение. В крови новорожденных телят содержание лейкоцитов составило (15,86±0,14)?109/л, с преобладанием сегментоядерных нейтрофилов, процентная концентрация которых достигла 60, превысив концентрацию лимфоцитов в 2 раза. На основе полученных данных можно отметить, что у новорожденных телят нейтрофильный тип крови.
У 5-суточных телят контрольной группы на фоне введения сыворотки содержание лейкоцитов увеличилось, где процентная концентрация сегментоядерных нейтрофилов составила 41,2, а лимфоцитов 49,4. В этот период наблюдается физиологический перекрест между содержанием нейтрофилов и лимфоцитов. Перекрест лейкоцитарной формулы возникает из-за того, что у телят происходит становление иммунитета. При достижении телятами 15-суточного возраста содержание лейкоцитов составило 13,80?109/л, сегментоядерных нейтрофилов 36,8%, лимфоцитов 54,8% (р?0,05), что еще раз подтверждает изменение скорости образования разных форм клеток. У 2 группы телят к 5 суткам содержание лейкоцитов снизилось на 18,7%, достигнув к 15-суточному возрасту 7,82?109/л, при этом процентная концентрация лимфоцитов увеличилась в 2,3 раза. В 3 группе на 5 сутки жизни телят содержание лейкоцитов снизилось на 17,2%, к 15 суткам их количество составило 7,84?109/л, процентное содержание лимфоцитов увеличилось в 2 раза. В 4 группе на 5 сутки исследования содержание лейкоцитов в крови снизилось на 27,2% по сравнению с первоначальным показателем, в 15-суточном возрасте составило 7,12?109/л, процент лимфоцитов увеличился в 2,2 раза (р?0,05).
Экспериментальными и клиническими исследованиями установлено, что определение клеточного состава крови по морфологическим признакам позволяет не только определять, но и прогнозировать состояние систем специфического и неспецифического иммунитета и организма в целом [5].
Наиболее информативными индексами интоксикации (ИИ) являются ЛИИр (индекс интоксикации Б.А. Рейса), РОН (реактивный ответ нейтрофилов Т.Ш. Хабирова) и ЯИ (ядерный индекс Г.Д. Даштаянца), они позволяют оценить иммунологический статус.
У новорожденных телят наиболее высокий индекс ЛИИр, который с возрастом снижается. Так в контрольной группе у 5- и 15-суточных телят ЛИИр снизился в 2,46 раза и в 3,03 раза. Пероральное введение взвеси полиметилсилоксана полигидрата телятам 2 группы способствовало снижению ЛИИр у 5- и 15-суточных телят в 5,69 раз; 3 группы – в 3,31 и 3,37 раза, 4 группы – в 3,64 и 3,87 раза соответственно. Фактически ЛИИр отражает в количественном выражении сдвиг лейкоцитарной формулы в сторону отдельных видов лейкоцитов, подтверждая физиологический лейкоцитарный перекрест.
РОН, как и ЛИИр наиболее высокий у новорожденных теля. В контрольной группе уже на 5 сутки он снизился в 3,89 раза, и оставался на низком уровне у телят 15-сточного возраста. Во 2 опытной группе у 5- и 15- суточных телят РОН снизился на 18,28 и 33,64 раза, в 3 опытной – в 7,93 и 9,04 раза, в 4 опытной – в 3,45 и 14,5 раза соответственно.
ЯИ – показывает соотношение суммы моноцитов и палочкоядерных нейтрофилов к содержанию сегментоядерных нейтрофилов в крови. У 5-суточных телят 1 группы индекс увеличился в 1,37 раза и не изменился при достижении 15-суточного возраста. У 5-суточных телят 2 группы индекс снизился в 1,33 раза и к 15-суткам достиг первоначального показателя. У телят 3 группы к 5-суточному возрасту ЯИ снизился в 2,29 раза, к 15-суточному повысился, однако был ниже, чем первоначальный показатель. В 4 группе отмечено снижение индекса в 5-суточном возрасте в 2,29 раза и отсутствие дальнейших изменений.
Анализ группы ИИ показал, что применение полиметилсилоксана полигидрата способствует существенному снижению интоксикации у телят опытных групп.
Вторая группа анализируемых лейкоцитарных индексов – группа, отражающая реактивность организма, то есть способность организма дифференцировано отвечать на действие раздражителей. От реактивности зависит способность новорожденного приспосабливаться к меняющимся условиям среды обитания, поддерживать гомеостаз.
Рассматриваемые индексы – ИГ (индекс адаптации Л.Х Гаркави) и ИСНМ (индекс соотношения нейтрофилов и моноцитов) у новорожденных телят составили соответственно 0,51 и 13,58.
Индекс Гаркави представляет отношение процента лимфоцитов к проценту сегментоядерных нейтрофилов, и, как правило, с увеличением процента лимфоцитов повышается. У 5-суточных телят 1 группы ИГ повысился в 2,35 раза, 15-суточных – в 2,92 раза. У телят 2 группы 5- и 15-суточного возраста ИГ увеличился в 6,16 и 6,31 раза, у телят 3 группы – в 3,49 и 3,51 раза, 4 группы – в 3,94 и 4,16 раза соответственно. Повышение ИГ можно трактовать как фактор активной ответной реакции организма («переактивация») [8].
ИСНМ позволяет судить о соотношении компонентов микрофагально-макрофагальной системы защиты. У новорожденных телят индекс составил 13,58. В 1 группе телят в 5- и 15-суточном отмечено снижение индекса в 2,5 и 2,6 раза. Во 2 опытной группе у телят 5- и 15-суточного возраста отмечено незначительное снижение ИСНМ (в 1,02 и 1,23 раза). У телят 3 опытной и 4 опытной групп наблюдали повышение данного индекса, в частности у 5- и 15-суточных телят 3 группы в 1,57 и 1,41 раза, 4 группы – в 1,75 и 2,96 раза соответственно, что, свидетельствует о повышении защитных механизмов.
ЛГИ – лимфоцитарно-гранулоцитарный индекс, предложенный И.С. Шевченко, относят к группе индексов, отвечающих за воспаление. У новорожденных телят концентрация лимфоцитов меньше, чем суммарное содержание гранулоцитов, что было установлено при анализе лейкограммы, поэтому у них ЛГИ не высокий – 0,48. У 5-суточных телят контрольной группы индекс увеличился в 2,39 раза, у 15-суточных – в 3,02 раза (р?0,05).
У телят, получивших взвесь полиметилсилоксана полигидрата в дозе 0,1 г/кг ответная реакция организма была выше: у 5-суточных телят ЛГИ повысился в 6,1 раза, у 15-суточных – в 5,83 раза. У 5- и 15-суточных телят, получивших взвесь препарата в дозе 0,3 г/кг живой массы, индекс увеличились в 3,6 и 3,52 раза, а у получивших взвесь в дозе 0,5 г/кг – в 4,0 и 4,17 раза соответственно.
Таблица – Динамика лейкоцитарных индексов у телят контрольной и опытных групп, n=12
Показатель
Индексы интоксикации
Индексы неспецифической реактивности
Индекс воспаления
ЛИИр
РОН
ЯИ
ИГ
ИСНМ
ЛГИ
Новорожденные
1,82
8,41
0,16
0,51
13,58
0,48
1 группа
5 суток
0,74
2,16
0,22
1,2
5,4
1,15
15 суток
0,60
2,37
0,22
1,49
5,22
1,45
2 группа
5 суток
0,32
0,46
0,12
3,14
13,30
2,93
15 суток
0,32
0,25
0,16
3,22
11,06
2,80
3 группа
5 суток
0,55
1,06
0,07
1,78
21,36
1,73
15 суток
0,54
0,93
0,12
1,79
19.20
1,69
4 группа
5 суток
0,50
2,44
0,07
2,01
23,86
1,93
15 суток
0,47
0,58
0,07
2,12
40.24
2.00
Заключение. Концентрация лейкоцитов в периферической крови у новорожденных телят и их процентное соотношение является лабильным показателем и зависит от скорости лейкопоэза.
Сравнив полученные данные контрольной и опытных групп, можем отметить, что на фоне применения взвеси полиметилсилоксана полигидрата в течение 15 дней у телят 2, 3 и 4 групп индексы интоксикации были значительно ниже, индексы реактивности и уровень клеточной защиты выше по сравнению с контрольной группой.
Таким образом, использование интегральных показателей лейкоцитарной формулы крови при проведении клинических исследований позволяет повысить информативность традиционных диагностических тестов и прогнозировать течение процесса адаптации.
Полиметилсилоксана полигидрат можем рекомендовать телятам в период новорожденности для преодоления критического периода развития. Для уменьшения риска срыва адаптационного процесса в первые пять дней жизни телят целесообразно использовать взвесь полиметилсилоксана полигидрата в дозе 0,3-0,5 г/кг, в более позднем – взвесь препарата в дозе 0,1-0,3 г/кг живой массы.
Список литературы:
1. Абрамович М., Плоскирева А. Оценка гематологических показателей при проведении клинических исследований в педиатрической практике // Врач. 2013. №11. С.72-75
2. Волков В.П., Росман С.В. Неспецифическая резистентность организма больных шизофренией при развитии нейролептической кардиомиопатии //Universum: Медицина и фармакология : электрон. научн. журн. 2014. № 11 (12). URL: http://7universum.com/ru/med/ archive/item/1722.
3. Дерхо М.А., Самойлова Е.С. Интегральные индексы интоксикации как критерий оценки уровня эндогенной интоксикации при бабезиозе // Учёные записки Казанской государственной академии ветеринарной медицины им. Н.Э. Баумана. 2011. Т. 207. С. 170-177.
4. Жуков А.П., Шарафутдинова Е.Б., Датский А.П. Информативность лейкоцитарных индексов в лабораторном скрининге лёгочной патологии у телят // Известия Оренбургского государственного аграрного университета. 2016. № 3 (59). С. 101-104.
5. Кавцевич Н.Н. Морфологические и цитохимические особенности клеток крови морских млекопитающих в связи с адаптацией к среде обитания: автореф. дис.…док. биол. наук. – Петрозаводск, 2011. – 38 с.
6. Клетикова Л.В., Мартынов А.Н., Шишкина Н.П. Физиологический статус новорожденных телят голштинской породы// Вестник КрасГАУ. 2019. №8. С. 68-75.
7. Шишкина Н.П., Клетикова Л.В., Мартынов А.Н. Интегральные показатели крови в оценке степени реактивности и устойчивости новорожденных телят // Наука. Исследования. Практика: сборник избранных статей по материалам Международной научной конференции (Санкт-Петербург, 2019). – СПб.: ГНИИ «Нацразвитие», 2019. – С.19-23.
8. Фролов О.К. Практикум з імунології «Методологія імунної системи ссавців»: навчально-методичний посібник для студентів вищих навчальних закладів / О.К. Фролов, В.В. Копійка, Є.Р. Федотов. – Запоріжжя: Copy Art, 2012. – 152 с.Добавлено: Пресс-службой портала Создание модели оценки и совершенствования качества помощи при сепсисе у новорожденных
На правах рукописи
СОКОЛОВСКАЯ Юлия Валерьевна
СОЗДАНИЕ МОДЕЛИ ОЦЕНКИ И СОВЕРШЕНСТВОВАНИЯ КАЧЕСТВА ПОМОЩИ ПРИ СЕПСИСЕ У НОВОРОЖДЕННЫХ (ПЕРИНАТАЛЬНЫЙ АУДИТ)
14.00.09 — Педиатрия
АВТОРЕФЕРАТ диссертации на соискание ученой степени кандидата медицинских наук
Москва — 2005
Работа выполнена в отделении реанимации и интенсивной терапии новорожденных и выхаживания маловесных детей ГУ Научный центр акушерства, гинекологии и перинатологии РАМН.
Научные руководители:
доктор медицинских наук
доктор медицинских наук, профессор
Байбарина Е.Н. Фролова О.Г.
Официальные оппоненты:
доктор медицинских наук доктор медицинских наук, профессор
Рюмина ИЛ. Пономарева Л.П.
Ведущая организация — ГУ Научный центр здоровья детей РАМН
Диссертационного совета К001.053.01 при ГУ Научный центр акушерства, гинекологии и перинатологии РАМН (117997, г. Москва, ул. Академика Опарина, д.4)
С диссертацией можно ознакомиться в библиотеке ГУ Научный центр акушерства, гинекологии и перинатологии РАМН.
Автореферат разослан «_»_2005г.
Ученый секретарь диссертационного совета
доктор медицинских наук Калинина Е.А.
Защита состоится «_»
2005г. в_часов на заседании
СПИСОК СОКРАЩЕНИЙ
• ДВС — синдром диссеминированного внутрисосудистого
свертывания
• ДС — диагностическая специфичность
• ДЧ — диагностическая чувствительность
• ИВЛ — искусственная вентиляция легких
• НИ — нейтрофильный индекс
• ПОН — полиорганная недостаточность
• ГОСТ — прокальцитонин
• СВО — системный воспалительный ответ
• СРБ — С-реактивный белок
• ЦНС — центральная нервная система
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы: Важнейшей задачей современного здравоохранения является повышение качества медицинской помощи. При этом важна не только разработка высокотехнологичных стандартов лечения, но и выявление того, как они применяются в практике и какие барьеры существуют для их внедрения.
В целях комплексной оценки действительной терапевтической эффективности, экономической оправданности и доступности существующих диагностических или лечебных мероприятий в клинической практике используется т.н. медицинский аудит [Bugalho А, Bergstrom S., 1993, Dunn P.M., 1996, Swain S., 1994].
В зависимости от поставленных задач применяют разные виды медицинского аудита, однако, наиболее распространен локальный аудит (проводящийся в медицинском учреждении или определенной территории) по какой-либо четко очерченной проблеме.
При проведении этого вида аудита группа экспертов, анализируя медицинскую документацию, выявляет соответствие пациента критериям включения, то есть верифицирует диагноз, а затем сравнивает проведенное лечение с существующими стандартами [Mcllwaine G.,1996], Это дает возможность выработки обоснованных рекомендаций по улучшению качества медицинской помощи.
В нашем исследовании в качестве модели проведения аудита выбран сепсис новорожденных, поскольку эта проблема остается одной из наиболее актуальных в современной педиатрии.
Актуальность изучения сепсиса новорожденных определяется не только высокой летальностью при этой патологии, доходящей, по данным отделыщх,авторов до 90% [Kaplan S.L.,1998, Todd J.K., 1997], но и
появлением новых данных, касающихся патогенеза сепсиса, что привело к необходимости введения новой терминологии и пересмотру существующих классификаций.
Все большее распространение в терапевтической и хирургической практике приобретает новый подход к диагностике сепсиса, позволяющий объективизировать верификацию этого заболевания. Указанный подход изложен в классификации, принятой в начале 90-х на Согласительной конференции обществ пульмонологов и реаниматологов США [Bone R.C., Balk R.A., Cerra F.B.,1991, Bone R.C., 1992], в которой рекомендованы для практического применения следующие определения и понятия: сепсис-синдром, синдром системной воспалительной реакции, сепсис, тяжелый сепсис, септический шок.
В системе диагностики сепсиса у взрослых к настоящему времени произошли качественные изменения: теперь сепсис верифицируется на основе четких показателей, из процесса диагностики практически исключен элемент субъективизма.
Для новорожденных эти принципиально новые диагностические подходы еще не разработаны. Дискуссионными на сегодня являются само определение сепсиса, критерии постановки диагноза и выявления синдрома системного воспалительного ответа организма (СВО) [Володин КН., 2003].
В отечественной и зарубежной литературе упоминания о проведении перинатального аудита при сепсисе новорожденных нам не встретилось, в то же время его проведение позволило бы выявить резервы снижения летальности при этой патологии [Bugalho A., Bergstrom S., 1993; Swain S., 1994].
Для проведения аудита по сепсису у новорожденных необходимо иметь его четкие диагностические критерии, позволяющие включать в аудит только детей с объективно верифицированным заболеванием, необходимы также критерии качества лечения.
К настоящему времени, указанные обязательные условия еще не разработаны, так же как не создана и модель проведения аудита по какой-либо патологии, что и послужило побудительным мотивом для проведения данной работы.
Цель исследования
Разработка модели перинатального аудита при сепсисе у новорожденных.
Задачи исследования
1. На основании вычисления диагностической чувствительности и диагностической специфичности клинико-лабораторных тестов определить оптимальные критерии для выявления синдрома системного воспалительного ответа при сепсисе у новорожденных. Создать систему критериев для объективизации диагноза «сепсис» у новорожденного.
2. Разработать шкалу для количественной оценки степени выраженности полиорганной недостаточности.
3. Провести ретроспективный анализ качества диагностики и лечения сепсиса у новорожденных.
4. Представить модель оценки и совершенствования качества помощи при сепсисе у новорожденных.
Научная новизна:
Впервые с позиций доказательной медицины разработаны критерии объективной диагностики сепсиса у новорожденных на основе наличия инфекционного очага, полиорганной недостаточности и вычисления диагностической чувствительности, а также диагностической специфичности комплексов признаков системного воспалительного ответа.
Впервые разработана модель перинатального аудита, применение которой позволило выявить, что лечение сепсиса проводится наименее качественно у детей с неверно выставленным диагнозом, а также при сочетании сепсиса с тяжелыми врожденными пороками развития и структурной патологией ЦНС.
Впервые показано, что использование критериев минимального достаточного объема медикаментозной помощи позволяет снизить летальность при сепсисе новорожденных в 3,4 раза.
Практическая значимость:
Разработанные критерии диагностики сепсиса новорожденных позволяют объективизировать верификацию диагноза, а также получать более достоверные данные для сравнения частоты этого заболевания, оценки эффективности комплексного лечения в различных регионах и, таким образом, наметить пути снижения летальности в группах новорожденных с сепсисом.
Использование разработанных критериев объективной диагностики и качества медикаментозного лечения позволяет существенно повысить эффективность лечения сепсиса у новорожденных.
Показано, что применение шкалы определения степени тяжести состояния новорожденных (ШОТ) позволяет количественно оценить выраженность полиорганной недостаточности, а определение уровня прокальцитонина — подтвердить наличие системного воспалительного ответа при сепсисе.
Создание модели оценки и совершенствования качества помощи при сепсисе может послужить методологической основой для проведения перинатального аудита при других заболеваниях.
Положения, выносимые на защиту:
1. Использование современных методов клинической эпидемиологии и доказательной медицины позволяет разработать объективные критерии установления диагноза и достаточности медикаментозного лечения. Диагноз «сепсис» у новорожденного верифицируется при наличии инфекционного очага, полиорганной недостаточности и системного воспалительного ответа. Последний документируется при выявлении двух признаков системного воспалительного ответа если один из них является гематологическим, либо не менее трех любых признаков СВО.
2. Экспертный анализ карт новорожденных с исходным диагнозом «сепсис» позволил выявить гипердиагностику в 5,1%, а при первичном диагнозе «пневмония» в 16% случаев выявлен «сепсис». Ложноположительное выявление СВО при пневмонии составило 6,8%, а ложноотрицательное его отсутствие при сепсисе — 8,5%.
3. Проведение аудита в группе новорожденных с сепсисом показало, что наиболее часто недостаточное лечение выявляется в группах больных с неверно выставленным диагнозом, а также при сочетании сепсиса с другими тяжелыми заболеваниями (пороки развития, структурная патология ЦНС). Проведение медикаментозного лечения в соответствии с критериями достаточности снижает летальность в 3,4 раза.
Внедрение результатов в практику
Результаты проведенных исследований и основные рекомендации внедрены в клиническую практику отделения реанимации и интенсивной терапии новорожденных и выхаживания маловесных детей ГУ Научный центр акушерства, гинекологии и перинатологии РАМН и используются в лекциях и семинарах для практических врачей.
Апробация диссертационного материала
Материалы диссертации доложены на республиканской научно-практической конференции «Инфекции плода и новорожденного. Современные технологии в диагностике и лечении» (Казань, 2005), IV съезде РАСПМ (Москва 2002), на межотделенческой конференции и апрбационной комиссии ГУ НЦАГиП РАМН.
Публикации результатов исследования. По теме диссертации опубликовано 5 печатных работ.
Структура и объем диссертации. Диссертация состоит из введения, 4-х глав, в которых содержатся: обзор литературы, объем и методы
исследования, результаты исследований, обсуждение полученных результатов, выводы, практические рекомендации, список литературы. Работа изложена на 175 страницах машинописного текста, содержит 37 таблиц, 19 рисунков. Библиография включает 162 литературных источника, в том числе 70 отечественных и 92 зарубежных авторов.
Содержание работы
Объем и методы исследования
Работа проведена в рамках нескольких «пилотных» родовспомогательных учреждений Москвы (3 учреждения), Архангельска, Омска, Смоленска, Уфы. Проанализировано 275 карт новорожденных, страдавших сепсисом (группа 1) и пневмонией (группа 2) и 90 историй развития родов у женщин за период с 1980 по 2005 год. Характеристики новорожденных каждой группы представлены в таблице 1.
80% детей с сепсисом, и 67 % детей с пневмонией родились у матерей с многочисленными факторами риска. Наиболее частой патологией у матерей новорожденных группы 1 была угроза прерывания беременности, кольпит, хр. пиелонефрит с обострением во время беременности, хориоамнионит, у матерей новорожденных группы 2 -угроза прерывания, истмико-цервикальная недостаточность, развитие острого респираторного заболевания во время беременности и обострение хронических инфекционных заболеваний.
Таблица 1.
Характеристика пациентов
группы Гестационный Масса тела Оценка Оценка дети
возраст при Апгар на Апгар на
рождении, г 1 мин на 5 ИВЛ
мин <%)
1 группа 34,9+0,34 2425+72 5,1+0,33 6,5+0,21 37
2 группа 33,3+0,46 1934+78 4,2+0,25 5,9+0,19 67,7
В группе 1 врожденный сепсис отмечен у 56% новорожденных. У 44% детей (родившихся преимущественно недоношенными, длительно находящимися на лечении с применением инвазивных методов) развился сепсис новорожденного.
В группе 2 у 49% детей развилась внутриутробная, а у 51% детей неонатальная пневмония (на фоне частичных ателектазов и болезни гиалиновых мембран).
Среди сопутствующих заболеваний в обеих группах чаще встречалась патология центральной нервной системы (у 65% группы 1 и 54% группы 2), у 25% детей в каждой группе имелись внутрижелудочковые кровоизлияния. ДВС синдром отмечен у 18,3% детей группы 1 и у 24% детей группы 2. Нарушение функции почек развилось у 10,8% детей группы 1 и у 16% детей группы 2, что в 89,4% и 70,5% случаев соответственно привело к возникновению острой почечной недостаточности.
Заболевание закончилось летальным исходом у 70 новорожденных с пневмонией и 100 — с сепсисом.
Данные о патологоанатомическом диагнозе имелись в картах 97 новорожденных из группы 1 (у 3-х вскрытия не проводилось), и 69 детей, из группы 2 (у одного ребенка вскрытия не проводилось).
Для разработки диагностических критериев сепсиса новорожденных из общего числа карт были отобраны карты детей, умерших от сепсиса, и от пневмонии, при наличии патологоанатомического подтверждения (рисунок 1).
■к.
Умершие ■1 Умершие
и пат/ан- пат/ан-
сепсис пнеемония
П-10Т п=вв
к. J
| Разработка критериев сепсиса
Рис. 1. Дизайн исследования — 1 этап.
На втором этапе во всей группе детей (275 карт) в соответствии с разработанными критериями диагностики проведена верификация диагноза и отбор группы новорожденных для проведения аудита (рисунок 2).
Рис. 2. Дизайн исследования — 2 этап.
Создание системы критериев постановки диагноза «сепсис» у новорожденных проводилось на основе определения сепсиса, консенсусно принятого рабочей группой по сепсису Российской Ассоциации Специалистов Перинатальной Медицины (РАСПМ) [Володин Н.Н., 2003]:
СЕПСИС — бактериальное инфекционное заболевание с ациклическим течением, наличием очага гнойного воспаления и/или бактериемии, системной воспалительной реакции организма и полиорганной недостаточности.
Разработка диагностических критериев сепсиса проводилась на основании трех составляющих данного определения, а именно наличия:
1. очага гнойного воспаления и/или бактериемии
2. признаков полиорганной недостаточности
3. признаков системной воспалительной реакции организма.
О наличии очага гнойного воспаления судили по выявлению воспалительных процессов различной локализации (пневмония, омфалит, менингит, перитонит, конъюнктивит).
Наличие полиорганной недостаточности оценивали на основании признаков, разработанных экспертами РАСПМ [Володин H.H., 2003].
Кроме того, состояние новорожденных, обследованных проспективно, оценивали на основании шкалы CRIB (Clinical Risk Index for Baby — индекс клинического риска для младенцев) [Cocburn F., Cooke R.W.J., 1993] и шкалы NEOMOD [Janota J, Stranak Z, 2001] и разработанной шкалы оценки степени тяжести состояния новорожденного (ШОТ).
О наличии СВО судили по следующим лабораторным признакам: повышение/снижение температуры тела, лейкоцитоз/лейкопения, нейтрофилез/нейтропения, сдвиг лейкоцитарной формулы влево, повышение нейтрофильного индекса (НИ), С-реактивного белка (СРБ), прокальцитонина (ПКТ), появление токсической зернистости нейтрофилов, лабораторных признаков синдрома гиперкатаболизма (повышение мочевины плазмы, гипергликемия, ацидоз)[Шабалов Н.П., 1999г].
Основным методологическим приемом исследования явилось определение диагностической чувствительности (ДЧ) и диагностической специфичности (ДС) одного или различных сочетаний признаков [Флетчер Р., Флетчер С.. Вагнер Э., 1998].
Обработка полученных результатов проводилась с использованием персонального компьютера и программы STATISTTCA 6.0.
Результаты исследования и их обсуждение
Первым обязательным условием проведения аудита является наличие разработанных диагностических критериев сепсиса у новорожденных. Для этого из общего числа карт (N=275) были отобраны карты детей с патологоанатомически подтвержденным диагнозом «сепсис» (всего -107), и «пневмония» (всего — 59). Именно эти карты с «золотым стандартом» подтверждения диагноза были включены в первый этап исследования.
Хотя бы один гнойно-воспалительный очаг присутствовал у 100% больных с сепсисом и пневмонией. Среднее число гнойно-воспалительных очагов в группе сепсиса составило 2,8±0,12, в группе пневмонии -1,4±0,09. Чаще всего, в качестве воспалительного очага в обеих группах встречалась пневмония.
Положительная гемокультура отмечена также в обеих группах. Посев крови в первые два дня заболевания был положительным у 17 (73,9%) из 23 детей с сепсисом, которым проводилось исследование. Из больных с пневмонией исследование крови на выявление возбудителя заболевания проводилось у 16 (27,1%) детей, рост бактерий получен в половине исследований. В спектре возбудителей преобладала грамположительная флора.
Таким образом, наличие гнойно-воспалительного очага и/или бактериемии встречалось и при сепсисе и при пневмонии. Указанные признаки не позволяли дифференцировать эти заболевания.
С целью углубленного анализа признаков ПОН дети с сепсисом и с пневмонией были оценены по шкалам: CRIB — индекс клинического риска для младенцев и шкале NEOMOD, которая служит для оценки состояния недоношенных новорожденных. При этом показатели были выше в ipyirae
детей, страдавших пневмонией, что, по нашему мнению, отражает недостаточно углубленную оценку тяжести ПОН по этим шкалам. В связи с этим нами была разработана более подробная шкала оценки тяжести состояния (ШОТ), в которую были включены данные о степени нарушения функции по каждой из систем органов с учетом гестационного возраста пациента, а также применения современных высокотехнологичных методов лечения с возможностью оценки изменения состояния ребенка в динамике. И действительно, при использовании шкалы ШОТ оценка у детей с сепсисом (29,1±6,7) была статистически достоверно выше, чем у детей с пневмонией (22,0±0,98).
Признаки ПОН минимум по трем системам отмечались у всех исследуемых, в среднем по 5,5±0,1 систем органов в группе умерших от сепсиса, и 4,7±0,11 в группе умерших от тяжелой пневмонии.
Таким образом, одно только наличие признаков ПОН не может быть само по себе диагностическим критерием сепсиса. Эти данные также свидетельствуют о том, что классификация сепсиса по Bone неприемлема для новорожденных.
Итак, при наличии одного гнойно-воспалительного очага и полиорганной недостаточности диагностика сепсиса может основываться лишь на выявлении системного воспалительного ответа. В дальнейшем над поиском критериев его выявления работа была продолжена.
Анализ признаков системного воспалительного ответа у исследуемых детей показал, что в группе детей с сепсисом чаще всего выявлялись: тромбоцитопения и другие признаки синдрома диссеминированного внутрисосудистого свертывания (ДВС-синдрома) — у 47,7%, токсическая зернистость нейтрофилов — у 41,4%, выраженный лейкоцитоз — у 36%, повышение уровня мочевины — у 29,7% и сдвиг
формулы крови влево — у 27,9% детей, появление белка острой фазы — С-реактивного белка у 75% обследованных детей. Нейтрофилез (13,5%) и повышение нейтрофильного индекса (НИ >_0,2 — у 15,9%, НИ > 0,4 — у 11,7%) определялись со значительно меньшей частотой.
В группе детей с тяжелой пневмонией чаще выявлялись: гипогликемия — у 22%, повышение уровня мочевины — у 18,6%, тромбоцитопения и другие признаки ДВС-синдрома — у 13,5%. Гипотермии, нейтропении, повышения нейтрофильного индекса более 0,4 у больных пневмонией отмечено не было.
Таким образом, ни один признак СВО не встречался у всех больных с сепсисом, поэтому было решено подойти к поиску наиболее надежного диагностического теста используя методологию определения диагностической чувствительности и диагностической специфичности различных признаков и их групп. Компромисс между ДЧ и ДС выражали, как это принято в современной клинической эпидемиологии, характеристической кривой (рисунок 3).
В начале было выявлено, — если принять, что СВО имеется при наличии хотя бы одного любого лабораторного признака (Kl), то диагностическая чувствительность составляет 100%, (то есть у всех новорожденных с сепсисом имеется хотя бы один признак СВО), но и диагностическая специфичность составляет всего 35,6% (т.е. у 64,4% больных тяжелой пневмонией обнаруживается такой признак). Показатели диагностической чувствительности и специфичности по одному признаку СВО нас не удовлетворили. Далее мы проанализировали ДЧ ДС одновременного наличия двух любых лабораторных признаков СВО (К2). При этом диагностическая чувствительность составила 94,3%, а частота ложноположительных результатов при пневмонии составила 25,4%.
При индивидуальном анализе карт мы отметили неравнозначность признаков СВО, так наиболее часто при сепсисе отмечались изменения в клиническом анализе крови. Поэтому было решено диагностировать СВО при наличии одного гематологического признака плюс не менее одного другого, либо при наличии не менее, чем трех разных клинико-лабораторных признаков СВО (К2-3). Такой подход продемонстрировал диагностическую чувствительность 91,5% (8,5% ложноотрицательных результатов при сепсисе) и 6,8% ложноположительных результатов при пневмонии, что являлось вполне удовлетворительным показателем.
Повышение количества признаков при констатации СВО до четырех (К4) снизило диагностическую чувствительность до 38,3%, резко повысив при этом специфичность до 98,3%.
Поскольку оптимальное соотношение между ДЧ и ДС находится на «плече» характеристической кривой, искомым нами признан тест, где СВО документируется у больного при выявлении двух или трех его лабораторных признаков.
9 детям проводили определение уровня прокальцитонина (ПКТ). У детей с сепсисом его концентрация превышала 10 нг/мл. У детей с пневмонией значения не превышали 2нг/мл, что подтвердило правильность группировки больных в соответствии с разработанными нами критериями.
‘»
К2
К1
94 91,5
Истинно-положительные
¡Км
г
результаты при сепсисе (%)
6,8 25,4 64
Ложноположительные результаты при пневмонии (%)
Рис. 3. Характеристическая кривая тестов выявления СВО. Ю-при наличии одного любого признака, К2 — при наличии двух любых лабораторных признаков, К2-3 — при наличии двух-трех лабораторных признаков, К4 — при наличии четырех любых лабораторных признаков.
Таким образом, на основании полученных нами данных, критериями постановки диагноза сепсис новорожденного мы предлагаем одновременное наличие:
— гнойно-воспалительного очага/очагов и/ или бактериемии
— Признаков ПОН
— Признаков СВО
Предложенные диагностические критерии мы использовали как критерии включения новорожденных в программу аудита по сепсису.
Для того, чтобы аудит носил абсолютно объективный характер, нам следовало выработать критерии качественного (оптимального) и некачественного (субоптимального) лечения.
Располагая лишь заполненными картами, а не полными историями болезни, мы могли разработать только модель проведения аудита, поскольку многие вопросы качественности проведенного лечения будут недоступны для нашего анализа. Поэтому, мы поставили перед собой задачу определить объем минимального достаточного медикаментозного лечения сепсиса, обоснованный с позиций доказательной медицины.
По сведениям, полученным нами из базы данных Кохрановского сообщества, основой медикаментозного лечения сепсиса (категория доказательности А) является рациональная антибактериальная терапия и применение внутривенных иммуноглобулинов [Cochrane Database Syst Rev., 2002].
Анализ качества лечения проведен в группе (145 детей) с диагнозом, верифицированным в соответствии с разработанными критериями (рис.2). Лечение в случаях с летальным исходом признано неоптимальным у 87% детей, а среди выживших — у 35,9% детей. Полученные результаты свидетельствовали о недостаточном качестве лечения при сепсисе у 68,2% всех исследованных детей.
Далее, в исследуемой группе мы выделили группу умерших от сепсиса в сочетании с другими тяжелыми заболеваниями (пороки развития, структурная патология ЦНС).
Наиболее часто субоптимальное лечение было выявлено именно в этой подгруппе детей — в 62,5% случаев и в группах больных с неверно выставленным диагнозом — в 78,9%.
Ретроспективный экспертный анализ качества лечения показал, что летальность при нерациональной антибактериальной терапии и отсутствии заместительной иммунотерапии составила 100%, при рациональной антибиотикотерапии без иммунглобулина — 55,5%, в то
время как при комбинированной антибиотикотерапии в сочетании с применением внутривенных иммуноглобулинов она не превышала 29,2%. Проведение медикаментозного лечения в соответствии с критериями достаточности может снизить летальность в 3,4 раза (рисунок 4).
Таким образом, анализ карт детей с сепсисом выявил существенно высокий процент некачественного лечения, что на первый взгляд можно легко объяснить недостаточными материальными ресурсами. Однако, проведение перинатального аудита помогло выявить и другие важные причины не полного использования терапевтических возможностей: это неверная диагностика, которая зачастую является следствием недостаточного обследования детей группы риска, и наличие у ребенка кроме сепсиса иной тяжелой патологии.
нерациональная антибактериальная
терапия без иммунотерапии
Рациональная антибиотикотерапия без иммунотерапии
Рациональная антибиотикотерапия и иммунотерапия
летальность
| ] летальность > {55,51
Снижение в 3/4 раза
летальность
Рис. 4. Летальность при разных видах лечения.
Другими словами, дети, считающиеся некурабельными, вследствие тяжелых врожденных пороков развития и органических поражений центральной нервной системы при возникновении у них септического процесса не получили достаточного объема лечения, становясь потенциальным источником вспышки гнойно-септических инфекций в родовспомогательных или детских учреждениях.
Поскольку перинатальный аудит является постоянно действующим процессом улучшения качества медицинской помощи, то после внедрения указанных рекомендаций следует провести новую «спираль аудита» на новом уровне. Для этого потребуется разработка новых карт с обеспечением адекватных сведений по исследуемой патологии или проблеме данным и сбор информации.
Для объективного анализа карт необходимо выработать критерии включения в исследование и критерии качественности медицинской помощи, а затем, на основе проведенного аудита разработать соответствующие рекомендации.
Указанная модель перинатального аудита применима к любому заболеванию и, являясь действенным инструментом повышения качества медицинской помощи должна широко использоваться в современной медицине.
Выводы
1. Перинатальный аудит является современным инструментом повышения качества медицинской помощи. Модель его проведения заключается в разработке объективных критериев верификации диагноза и оценки оптимальности’ лечения, анализе данных о лечебном процессе, проводящемся в реальных условиях, и в выработке на этой основе концепции совершенствования медицинской помощи матерям и детям.
2. Объективными критериями верификации диагноза «сепсис» у новорожденных являются наличие инфекционного очага, полиорганной недостаточности и системного воспалительного ответа. На основе применения методик доказательной медицины установлено, что наличие последнего может быть документировано при выявлении двух лабораторных признаков системного воспалительного ответа если один из них является гематологическим, либо трех любых его признаков. Ложноположительное выявление системного воспалительного ответа при пневмонии отмечено в 6,8%, а ложноотрицательное при сепсисе — в 8,5% случаев.
3. Использование шкалы определения тяжести состояния новорожденных (ШОТ) дает возможность количественно оценить выраженность полиорганной недостаточности, а определение уровня прокальцитонина — подтвердить наличие системного воспалительного ответа при сепсисе.
4. В результате проведения аудита выявлено, что в 16% случаев сепсис распознан не был и проходил под диагнозом пневмонии. Гипердиагностика сепсиса выявлялась в 3 раза реже — в 5,1% случаев.
5. С позиций доказательной медицины основой медикаментозного лечения при сепсисе (категория А) является рациональная антибиотикотерапия в сочетании с применением внутривенных иммуноглобулинов. Ретроспективный экспертный анализ качества лечения показал, что проведение медикаментозного лечения в соответствии с указанными критериями снижает летальность в 3,4 раза.
6. Наиболее часто недостаточное лечение выявлено в группах больных с неверно выставленным диагнозом — 78,9%, а также при сочетании сепсиса с другими тяжелыми заболеваниями (пороки развития, структурная патология ЦНС) — в 62,5%.
7. Для совершенствования качества помощи новорожденным при сепсисе необходимо внедрение стандарта обследования новорожденных с высоким риском развития септического процесса (дети матерей с обострением хронических воспалительных процессов и хориоамнионитом) и проведение регулярного внутреннего аудита для решения вопроса о качестве рутинно оказываемой помощи и постоянного ее совершенствования на новом уровне знаний.
Практические рекомендации
1. С целью объективизации диагностики сепсиса новорожденных рекомендуется использовать следующие критерии: наличие гнойно-воспалительного очага (очагов) и/или бактериемии, полиорганной недостаточности (не менее 3 систем), признаков системного воспалительного ответа (два признака, при условии, что один из группы гемограммы, либо не менее, чем один признак из трех разных групп).
2. При наличии у новорожденного подтвержденного по критериям сепсиса в план лечебных мероприятий помимо поддержания основных жизненно важных функций организма рекомендуется включить: стартовую эмпирическую комбинированную антибиотикотерапию с использованием препаратов широкого спектра действия, а, затем антибактериальную терапию по чувствительности высеваемой флоры в сочетании с внутривенным применением иммуноглобулинов.
3. Для повышения точности определения степени выраженности полиорганной недостаточности у новорожденных при сепсисе рекомендуется использовать шкалу оценки степени тяжести состояния новорожденного и определение уровня прокальцитонина.
4. У детей, с подозрением на септический процесс в план лабораторного обследования с целью выявления возбудителя и установления наличия признаков системного воспалительного ответа необходимо включить: клинический анализ крови с количеством тромбоцитов, биохимический анализ крови с обязательным определением уровня мочевины и глюкозы, микробиологическое исследование крови.
5. Основные этапы проведения перинатального аудита у новорожденных должны включать разработку объективных критериев диагностики, обоснование минимального достаточного объема медикаментозного лечения, основанного на доказательных принципах, анализ качества помощи и выработку обоснованной концепции путей совершенствования помощи.
СПИСОК ОПУБЛИКОВАННЫХ РАБОТ.
1. Байбарина E.H., Соколовская Ю.В. Диагностические критерии сепсиса у новорожденных // материалы IV Российского форума «Мать и Дитя»: / — М, ч.2Д002г.- с 487-488.
2. Байбарина E.H., Соколовская Ю.В. Доказательная медицина в неонатологии // тез. форума «Репродукция человека 2003»: / -М, 2003г.- с.23.
3. Володин H.H., Антонов А.Г., Байбарина E.H., Дегтярев Д.Н., Соколовская Ю.В. Сепсис новорожденных и доказательная медицинская практика-новый подход к повышению качества медицинской помощи// Журнал Педиатрия. — 2003 .-№5. — с. 56-59.
4. Байбарина E.H., Сорокина З.Х. Трудные вопросы диагностики и терапии вирусно-бакгериальных инфекций у новорожденных.// Медико-фармацевтический вестник Татарстана. — 2005.-№4.
5. Соколовская Ю.В. Создание модели оценки и совершенствования качества помощи при сепсисе у новорожденных // материалы V съезда РАСПМ./ — М., 2005г.
Напечатано с готового оригинал-макета
Издательство ООО «МАКС Пресс» Лицензия ИД N 00510 or01.12.99 г. Подписано к печати 16.05.2005 г. Формат 60×90 1/16. Усл.печ.л.1,5. Тираж 100 экз. Заказ 321. Тел. 939-3890. Тел./факс 939-3891. 119992, ГСП-2, Москва, Ленинские горы, МГУ им. М.В. Ломоносова, 2-й учебный корпус, 627 к.
»11247
РНБ Русский фонд
2006-4 5936
Роль индекса дельта нейтрофилов в определении этиологии неонатального сепсиса
Цели
Для демонстрации количества незрелых гранулоцитов (IG) и значений дельта-нейтрофильного индекса (DNI) (новый потенциальный прогностический маркер неонатального сепсиса) для новорожденных.
Методы
Это проспективное контролируемое клиническое исследование включало 208 пациентов (77 в исследуемой группе и 131 в контрольной группе), которые были доставлены в период с января 2016 года по январь 2018 года в отделение интенсивной терапии новорожденных Университета Хаджеттепе в Анкаре, Турция.В этом исследовании мы оценили значение DNI в диагностике неонатального сепсиса, сравнив значения DNI у новорожденных с положительным посевом сепсиса со здоровыми новорожденными.
Результаты
В нашем исследовании средний межквартильный размах (IQR = 25–75%) DNI составлял 0,1% (0,0–0,3%) в контрольной группе и 1,5% (1,0–2,45%) в группе сепсиса (p <0,05). В нашем анализе кривой ROC пороговое значение для DNI в качестве маркера сепсиса составляло 0,65%, со специфичностью 96,2% и чувствительностью 97,4%. Пациенты с грамотрицательными изолятами имели значительно более высокие показатели DNI и IG по сравнению с пациентами с грамположительными бактериями (p <0.05).
Выводы
Наши результаты показали, что количество DNI является важным диагностическим биомаркером неонатального сепсиса. Они также могут быть полезны при определении этиологии сепсиса (различение грамположительных и грамотрицательных агентов).
Введение
Неонатальный сепсис является одной из основных причин смертности и заболеваемости новорожденных [1], [2], а частота подтвержденного сепсиса в развивающихся странах составляет 16 случаев на 1000 живорождений [3].Из-за риска смерти важно диагностировать сепсис на ранней стадии и начать соответствующее лечение. Золотым стандартом диагностики сепсиса является выделение микроорганизмов из посевов крови [4]. Однако из-за физиологических особенностей новорожденных и ограничений лабораторных методов посевы крови требуют 48–72 часов для обнаружения роста бактерий, и они могут даже давать ложноотрицательные результаты. Таким образом, биомаркеры можно использовать для получения быстрых результатов, подтверждающих диагноз сепсиса, при этом постоянно разрабатываются новые биомаркеры [5].Наиболее часто используемые биомаркеры — это уровень С-реактивного белка (CRP), уровень прокальцитонина, общее количество лейкоцитов и отношение незрелых нейтрофилов к общему (I / T) [6], [7]. Однако до сих пор не существует идеального лабораторного теста с высокой чувствительностью и специфичностью; поэтому продолжаются исследования по выявлению недорогих и более легко измеряемых лабораторных биомаркеров. В недавних клинических исследованиях было предложено, что соотношение незрелых гранулоцитов (IG), автоматически полученное с помощью приборов для полного анализа крови (дельта-нейтрофильный индекс, DNI), можно использовать в качестве нового биомаркера сепсиса.
В этом исследовании мы изучили использование DNI в диагностике неонатального сепсиса, сравнив значения DNI здоровых новорожденных (без сепсиса) и новорожденных с сепсисом, подтвержденным посевом крови. Кроме того, мы стремились найти пороговое значение DNI для использования в диагностике сепсиса.
Материалы и методы
Это проспективное обсервационное клиническое исследование проводилось с января 2016 г. по январь 2018 г. в отделении интенсивной терапии новорожденных Университета Хаджеттепе в Анкаре, Турция.До проведения исследования было получено одобрение Комитета по этике клинических исследований Университета Хаджеттепе (GO-17 / 824-29).
Пациенты
В исследуемую популяцию вошли пациенты, находящиеся под наблюдением в отделении интенсивной терапии новорожденных, у которых был диагностирован сепсис на основании роста бактерий в посеве крови. В исследование были включены новорожденные с хотя бы одной из четырех групп (клинические, гемодиманические, тканевая перфузия и воспалительные переменные), перечисленные в таблице 1, и чьи результаты не были идентифицированы с каким-либо другим заболеванием, кроме сепсиса [8], [9] .
Таблица 1:Критерии диагностики сепсиса (изменено из [8]).
Клинические параметры Нестабильность температуры (лихорадка> 38,0 ° C, гипотермия <36,0 ° C) ЧСС> SD выше нормы для возраста (≥180 уд / мин, ≤100 уд / мин) Частота дыхания> 60 вдохов / мин плюс хрюканье / спад или десатурация Вялость / изменение психического статуса Непереносимость глюкозы (глюкоза в плазме> 10 ммоль / л) Непереносимость кормления Гемодинамические переменные Артериальная гипотензия (артериальное давление на 2 SD ниже нормы для гестационного возраста) Переменные тканевой перфузии Заполнение капилляров> 3 с Лактат в плазме> 3 ммоль / л Воспалительные переменные Лейкоцитоз (количество лейкоцитов> 15000 / мм 3 ) Лейкопения (количество лейкоцитов <4000 / мм 3 ) Незрелые нейтрофилы (ленточные формы)> 10% Незрелые: общее соотношение нейтрофилов> 0.2 Тромбоцитопения (<100000 / мм 3 ) CRP> 0,8 мг / дл Прокальцитонин> 2,0 нг / мл Контрольную группу составили пациенты, госпитализированные в отделение интенсивной терапии новорожденных без подозрений или диагнозов сепсиса и у которых по какой-либо причине был запрошен общий анализ крови. Для этого исследования отдельный забор крови не проводился.В контрольной группе не было никаких признаков сепсиса (таблица 1) и применения антибиотиков до взятия пробы и трех дней спустя. Пациенты контрольной группы, отобранные из отделения интенсивной терапии, были аналогичны исследуемой группе по полу, гестационному возрасту и массе тела при рождении.
Первоначально в исследование был включен 281 пациент: 103 в исследовательскую группу и 178 в контрольную группу. Однако 73 пациента с неполными формами согласия и неполными лабораторными результатами были исключены.Таким образом, исследование было завершено с участием 208 пациентов: 77 в основной группе и 131 в контрольной группе. Схема пациента показана на Рисунке 1.
Рисунок 1:
Блок-схема исследуемой и контрольной группы.
Если пациенты с микроорганизмами, выделенными в культурах крови, но клинически несовместимы с сепсисом, результаты посева крови оценивались как контаминация, и эти пациенты не включались в исследование.
Биохимический анализ
Забор крови
Полный анализ крови, мазок периферической крови, уровень СРБ, уровень прокальцитонина и посев крови были получены непосредственно перед началом лечения антибиотиками у пациентов с подозрением на сепсис.
Для общего анализа крови образцы крови помещали в пробирки, содержащие этилендиаминтетрауксусную кислоту (K2-EDTA), и отправляли в лабораторию в течение 1 часа. Подсчет периферических клеток, дифференциал, подсчет IG и мазок крови выполнялись с помощью Unicel DxH 800 (Beckman Coulter, Inc., Бреа, Калифорния, США) автоматический счетчик клеток. IG каждого пациента был получен из системы [10]. Для мазка крови использовали краситель Райта.
Отношение нейтрофиловI / T, а также количество незрелых и общих нейтрофилов определяли микроскопическим исследованием при 100-кратном увеличении [11].
Для определения сывороточного СРБ и прокальцитонина были помещены в пробирки ST и доставлены в лабораторию через 1 час. Уровни прокальцитонина в сыворотке измеряли методом гомогенного иммуноанализа, методом TRACE (Time Resolved Amplified Cryptate Emission, Kryptor; Brahms, Германия) с высоким пределом обнаружения (0 нг / мл) и линейным диапазоном 0.02–100 нг / мл. Уровни СРБ в сыворотке измеряли методом скоростной нефелометрии (Beckman Coulter Inc., Калифорния, США) с линейностью 5–300 мг / дл.
В исследуемой группе значения DNI не проверялись после антибактериальной терапии.
Unicel DxH 800
Unicel DxH 800 использует электрический импеданс, радиочастотную проводимость, а также объем, проводимость и многоугловое рассеяние света для подсчета и различения субпопуляций лейкоцитов [10]. Процент DNI каждого пациента был получен с помощью Unicel DxH 800.После этого автоматически рассчитывается количество ИГ лейкоцитов x DNI в процентах.
Статистический анализ
Статистический анализ этого исследования был проведен с использованием IBM SPSS Statistics для Windows версии 22 (IBM Corp., Армонк, Нью-Йорк, США). Переменные с нормальным распределением оценивались с использованием независимого выборочного критерия t , а переменные с ненормальным распределением оценивались с использованием непараметрического критерия Манна-Уитни U . Категориальные переменные анализировались с использованием точного критерия Фишера и критерия хи-квадрат Пирсона.Значения p <0,05 считались статистически значимыми. Подсчитанные переменные были выражены как среднее (± стандартное отклонение), а измеренные значения были выражены как медиана (минимум – максимум, 25–75 процентиль).
Результаты
Демографические и неонатальные характеристики 77 пациентов в исследуемой группе и 131 пациента в контрольной группе показаны в таблице 2.
Таблица 2:Демографические особенности пациентов, включенных в исследование.
Учебная группа n = 77 Контрольная группа n = 131 p-значение Пол, n (%) (женский / мужской) 39/38 (50,6 / 49,4) 71/60 (54,2 / 45,8) 0,621 Срок беременности (неделя) a 34.3 ± 5,4 34,8 ± 3,5 0,953 Вес при рождении (гр) b 2480 (1 110–3 235) 2 310 (1 700–3 160) 0,568 Оценка по шкале Апгар на 5-й минуте b 8 (7–9) 10 (10–10) <0,001 Форма поставки, n (%) (НСВД / ЦС) 22/55 (28.6 / 71,4) 3/128 (2,3 / 97,7) <0,001 Реанимация, n (%) 28 (36,4) 9 (6,9) <0,001 Вспомогательные репродуктивные технологии, n (%) 9 (11,7) 8 (6,1) 0,247 RDS, п (%) 24 (31,2) 20 (15,3) 0.011 ИГБ, п (%) 21 (27,3) 27 (20,6) 0,271 NEC, n (%) 15 (19,5) 10 (7,6) 0,021 КПК, п (%) 15 (19,5) 5 (3,8) 0,001 BPD, n (%) 19 (24,7) 11 (8.4) 0,003 ICH, п (%) 7 (9,1) 4 (3,1) 0,104 Возраст на момент диагностики сепсиса (дни) b 15 (7–33) Возраст на момент взятия крови (дни) б 15 (7–33) 9 (5–18) <0,001 Продолжительность госпитализации (сутки) б 28 (15–72) 11 (5–20) <0.001 Не было статистических различий между исследуемой и контрольной группами по полу (p = 0,621), неделям беременности (p = 0,953), массе тела при рождении (p = 0,568), использованию методов вспомогательного оплодотворения (p = 0,247), непрямая гипербилирубинемия (p = 0,271) или частота внутричерепных кровоизлияний (p = 0,104). Однако 5-минутные баллы по шкале Апгар в исследуемой группе были значительно ниже, чем в контрольной группе (p <0,001). Более того, в исследуемой группе показатели реанимации были значительно выше (p <0.001), респираторный дистресс-синдром (p = 0,011), некротический энтероколит (p = 0,021), открытый артериальный проток (p = 0,001), бронхолегочная дисплазия (p = 0,003), смертность (p = 0,003), день забора крови (p < 0,001) и более длительное пребывание в больнице (p <0,001). Кесарево сечение было значительно чаще в контрольной группе, чем в исследовательской (p <0,001).
Полный анализ крови и острофазовые реактивы пациентов приведены в таблице 3.
Таблица 3:Общий анализ крови и реактивы острой фазы пациентов.
Учебная группа n = 77 Контрольная группа n = 131 p-значение Гемоглобин a (г / дл) 13,0 ± 2,9 14,8 ± 1,7 <0,001 Гематокрит a (%) 39,1 ± 8,7 46.3 ± 5,3 <0,001 Количество тромбоцитов b (клеток / мкл) 1,74,000 (88,500–3,07,500) 2,40,000 (1,97,000–2,76,000) 0,003 Количество лейкоцитов b (клеток / мкл) 11 900 (7 150–18 350) 10 200 (8 600–13 000) 0,150 ANC b (клеток / мкл) 7 200 (3 700–11 500) 5 400 (3 900–7 300) 0.015 Отношение I / T b 0,2 (0,18–0,25) 0,06 (0–0,11) <0,001 DNI b (%) 1,5 (1,0–2,5) 0,1 (0–0,3) <0,001 Количество IG b (клеток / мкл) 196 (88–355) 13 (0–35) <0,001 CRP b (мг / дл) 3.02 (1,23–10,5) Прокальцитонин b (нг / мл) 5,63 (1,05–16,53) NLR b 2,86 (1,38–6,45) 1,55 (1,04–2,00) <0,001 Показатели гемоглобина и гематокрита были значительно ниже в основной группе, чем в контрольной (p <0.001 для обоих), и не было статистически значимой разницы между группами в отношении количества лейкоцитов (p = 0,150). В исследуемой группе было значительно более низкое среднее количество тромбоцитов по сравнению с контрольной группой (p = 0,003). Однако в исследуемой группе были статистически более высокие значения абсолютного количества нейтрофилов (ANC) (p = 0,015), отношения нейтрофилов I / T (p <0,001), процента DNI (p <0,001), количества IG (p <0,001), и отношение нейтрофилов к лимфоцитам (NLR) (p <0,001).Значения CRP и прокальцитонина нельзя было сравнивать, потому что они не были оценены в контрольной группе.
В нашем исследовании средний межквартильный размах (IQR = 25–75%) DNI составлял 0,1% (0,0–0,3%) в контрольной группе и 1,5% (1,0–2,45%) в группе сепсиса (p <0,05). Мы определили пороговые значения DNI в соответствии с контрольной и исследовательской группами, используя анализ кривой рабочих характеристик приемника (ROC) (рисунок 2). В нашем исследовании пороговое значение DNI 0,65% имело специфичность 96,2% и 97.Чувствительность 4% как биомаркер сепсиса.
Рисунок 2:
Кривая рабочих характеристик приемника для определения дельта-нейтрофильного индекса как диагностического маркера неонатального сепсиса.
Микроорганизмы, выделенные в культурах крови 77 пациентов исследуемой группы, и их характеристики окрашивания по Граму показаны в таблице 4.
Таблица 4:Микроорганизмы, выделенные в культурах крови.
грамположительные бактерии n = 51 п (%) Грамотрицательные бактерии n = 24 п (%) Эпидермальный стафилококк 15 (19,5) Klebsiella pneumoniae 15 (19,5) Стафилококк головного мозга 11 (14.2) Serratia marcenses 3 (3,9) Золотистый стафилококк 6 (7,8) Enterobacter cloacae 3 (3,9) Гемолитический стафилококк 4 (5,2) Acinetobacter baumannii 1 (1,3) Staphylococcus hominis 3 (3.9) Sphingomonas paucimobilis 1 (1,3) Paenibacillus spp. 3 (3,9) Pseudomonas spp. 1 (1,3) Enterococcus faecium 3 (3,9) Streptococcus agalactiae 2 (2,6) Bacillus licheniformis 2 (2.6) Streptococcus mitis / oralis 1 (1,3) Streptococcus parasanguinis 1 (1,3) Посев крови выявил грамположительные бактерии у 51 пациента и грамотрицательные бактерии у 24 пациентов исследуемой группы. Грибы были выделены в двух посевах крови пациентов (2.6%).
В таблице 5 показано сравнение биомаркеров сепсиса у пациентов с грамположительными и грамотрицательными бактериальными изолятами в культурах крови. Пациенты с сепсисом, посев крови которых выявил Candida spp., Не были включены в статистику из-за их небольшого количества.
Таблица 5:Сравнение биомаркеров сепсиса у пациентов с грамположительными и грамотрицательными бактериальными изолятами в культурах крови.
Грамположительные, n = 51 Грамотрицательные, n = 24 p-значение Количество тромбоцитов (клеток / мкл) 2,11,000 (1,32,000–3,37,000) 1,23,000 (26,250–1,78,250) <0.001 Количество лейкоцитов (клеток / мкл) 12 000 (7 900–18 400) 10 350 (5 625–14 750) 0,175 ANC (клеток / мкл) 7 700 (3 600–12 000) 5 800 (3 900–12 125) 0,069 Отношение I / T 0,2 (0,17–0,22) 0,24 (0,2–0,3) <0,001 DNI (%) 1.2 (1.0–1.8) 2,7 (1,7–3,7) <0,001 Количество IG (клеток / мкл) 175 (87–301) 318 (108–431) <0,001 CRP (мг / дл) 2,31 (1,09–8,04) 4,30 (1,29–14,55) 0,103 Прокальцитонин (нг / мл) 5,09 (0,75–16,53) 8,0 (1.97–35.32) 0,068 NLR 2,33 (1,27–7,19) 3,48 (1,76–6,35) <0,001 Пациенты с грамотрицательными бактериями в культурах крови имели значительно более высокое соотношение нейтрофилов I / T, процент DNI, количество IG и значение NLR по сравнению с пациентами с грамположительными изолятами (p <0,001 для всех). Существенных различий между группами по количеству лейкоцитов не было (p = 0.175), ANC (p = 0,069), уровень CRP (p = 0,103) или уровень прокальцитонина (p = 0,068).
Обсуждение
Сепсис — основная причина смертности и заболеваемости, которая часто встречается в отделениях интенсивной терапии новорожденных [2]. Хотя положительный посев крови остается золотым стандартом диагностики, изолировать возбудитель у новорожденных сложно по разным причинам и требует времени [4]. Следовательно, необходимы биомаркеры сепсиса с высокой диагностической чувствительностью и специфичностью.
Одним из наиболее часто используемых параметров в отделениях для новорожденных является соотношение нейтрофилов I / T, более высокое соотношение нейтрофилов I / T указывает на присутствие большего количества IG (миелоцитов, промиелоцитов и метамиелоцитов) в периферическом кровообращении.Отношение нейтрофилов I / T более 0,2 считается показателем сепсиса [11]; тем не менее, этот параметр может иметь вариабельность, зависящую от наблюдателя, поскольку он основан на оценке наблюдателем клеток крови в периферическом мазке [7]. Это привело к недавней разработке автоматизированных гематологических анализаторов, способных подсчитывать ИГ [12]. Появляется все больше данных, демонстрирующих взаимосвязь между автоматическим подсчетом IG и инфекцией [13], [14], [15]. Nahm et al. [14] не сообщили о статистической разнице между количеством незрелых нейтрофилов, подсчитанным автоматическим гематологическим анализатором, и количеством, вычисленным гематологом на основе ручного подсчета 200 клеток в периферическом мазке.Поэтому мы запланировали настоящее исследование для определения чувствительности и специфичности DNI, автоматически рассчитываемого гематологическим анализатором во время общего анализа крови при диагностике сепсиса. В нашем исследовании медиана ([IQR] = 25–75%) отношения нейтрофилов I / T составляла 0,2 (0,18–0,25) в исследуемой группе, что было значительно выше, чем в контрольной группе [0,06 (0–0,11). ] (р <0,001). Подобно нашим выводам, Zaki et al. [16] сообщили о более высоком соотношении нейтрофилов I / T в инфицированной группе, чем 0.12 ± 0,12 - контрольная группа (0,30 ± 0,17 против 0,12 ± 0,12).
Cimenti et al. [7] определили пороговое значение DNI как 1,3%, сравнивая значения DNI у 21 новорожденного с сепсисом и 112 новорожденных контрольной группы. Ли и др. [17] сравнили значения DNI 24 новорожденных с сепсисом и 48 детей без сепсиса и обнаружили статистически значимые различия. Среднее значение DNI на момент постановки диагноза составляло 6,5 ± 2,4% у умерших пациентов с сепсисом, 3,7 ± 1,8% у выживших пациентов с сепсисом и 1,1 ± 0,7% в контрольной группе здоровых людей.Elik et al. [18] обнаружили, что пороговый уровень DNI составлял 4,6 при 85% чувствительности и 80% специфичности в исследовании, в котором они изучали случаи как доказанного, так и клинически неонатального сепсиса. В нашем исследовании в исследование были включены только случаи с доказанным сепсисом. В нашем исследовании медиана (IQR = 25–75%) DNI составила 0,1% (0,0–0,3%) в контрольной группе и 1,5% (1,0–2,45%) в группе сепсиса (p <0,001). В нашем анализе кривой ROC пороговое значение для DNI в качестве маркера сепсиса составляло 0,65%, со специфичностью 96,2% и 97.Чувствительность 4%. Согласно многим предыдущим исследованиям, новорожденных больше. Senthilnayagam et al. [19] сообщили, что исследование 200 пациентов с 29 новорожденными, 0,5% для IG может быть использовано для обнаружения бактериемии с чувствительностью 86,3% и чувствительностью 92,2%. Фернандес и Хамагучи [20] обнаружили, что оптимальное время для определения количества незрелых гранулоцитов было в пределах 60 минут после взятия крови, когда значение IG у здоровых взрослых было ниже 0,52%. В других исследованиях недостаточно данных о сроках анализа образцов крови.В нашем исследовании образцы крови, взятые во время диагностики сепсиса, анализировались в течение 60 минут. В исследовании с участием более 2400 образцов, разработанном для определения референтного диапазона соотношения незрелых гранулоцитов в зависимости от возраста, верхний предел для IG как у детей до 10 лет, так и у младенцев был предложен на уровне 0,3% [21]. Существует потребность в дополнительных проспективных клинических исследованиях с участием большего числа случаев сепсиса и здоровых людей из разных возрастных групп.
Мы определили, что среднее количество IG, рассчитанное с использованием значения DNI, было выше в группе сепсиса, чем в контрольной группе в настоящем исследовании (196 vs.13 мкл соответственно) (p <0,001). Cimenti et al. [7] сообщили о пороговом значении 240 / мкл для подсчета IG в своем исследовании.
В нашем исследовании медиана (IQR = 25–75%) NLR составила 2,86 (1,38–6,45) в группе сепсиса и 1,55 (1,04–2,00) в контрольной группе. Алкан Оздемир и др. [22] сообщили о 73% чувствительности и 78% специфичности с использованием порогового значения NLR 1,77, а Omran et al. [23] рассчитал пороговое значение 2,7. В нашем исследовании медиана NLR в группе сепсиса была выше пороговых значений, указанных в других исследованиях, и была статистически значимо выше, чем в контрольной группе (p <0.001).
В этом исследовании наиболее частыми возбудителями, выделенными в культурах крови больных сепсисом, были Klebsiella pneumonia (15 пациентов) и Staphylococcus epidermidis (15 пациентов). Грамположительные микроорганизмы были выделены у 51 пациента (66,2%), а грамотрицательные микроорганизмы — у 24 пациентов (31,2%). Пациенты с грамотрицательными изолятами имели значительно более высокие показатели DNI и IG по сравнению с пациентами с грамположительными агентами (p <0,001 для обоих).Мы связали это открытие с тем, что грамотрицательные бактерии вызывают более серьезную реакцию на инфекцию. Подобно результатам нашего исследования, в исследовании Celik et al. [18], новорожденные с грамотрицательным сепсисом имели более высокие значения DNI, чем грамположительные.
Chacha et al. [24] сообщили о более высоких значениях CRP у пациентов с грамотрицательными изолятами. Однако в нашем исследовании не было статистических различий между грамположительными и грамотрицательными группами с точки зрения количества лейкоцитов, АНК, уровня СРБ или уровней прокальцитонина.Lai et al. [25] проанализировали 1010 значений CRP у новорожденных с диагнозом сепсис и обнаружили, что у пациентов с более низким уровнем CRP было меньше грамотрицательных изолятов. В другом исследовании Fendler et al. [26], включая 78 новорожденных с грамотрицательными и грамположительными изолятами, уровни прокальцитонина были выше в группе с грамотрицательными препаратами. Мы объяснили отсутствие существенной разницы в нашем исследовании меньшим числом пациентов.
Поскольку в наше исследование были включены только новорожденные, не было сделано никаких обобщений или прогнозов относительно значения DNI в диагностике сепсиса в других детских возрастных группах.
Наши результаты показали, что количество DNI и IG являются важными диагностическими биомаркерами неонатального сепсиса, и они также могут быть полезны при определении этиологии сепсиса (различая грамположительные и грамотрицательные агенты). Как параметр, который может быть автоматически рассчитан гематологическими анализаторами вместе с полным анализом крови, DNI выделяется как доступный биомаркер, который легко получить без дополнительного забора крови, что делает его более удобным и выгодным, чем другие лабораторные тесты, такие как маркеры воспаления. .Наше исследование показывает, что даже в случаях, когда нет возможности анализировать CRP, Procalcitonin, IL-6, значения DNI, полученные автоматически, можно использовать в качестве лабораторных маркеров для диагностики сепсиса новорожденных.
Существенное участие в разработке концепции и дизайна исследования принимали все авторы.
Ссылки
1. Лоун, Дж. Э., Кузенс, С., Зупан, Дж., Руководящая группа по выживанию новорожденных «Ланцет». 4 миллиона неонатальных смертей: когда? Где? Почему?. Lancet 2005; 365: 891–900.https://doi.org/10.1016/s0140-6736(05)71048-5. Искать в Google Scholar
2. Hedegaard, SS, Wisborg, K, Hvas, AM. Диагностическая ценность биомаркеров неонатального сепсиса — систематический обзор. Infect Dis (Лондон) 2015; 47: 117–24. https://doi.org/10.3109/00365548.2014.971053. Искать в Google Scholar
3. Thaver, D, Zaidi, AK. Бремя неонатальных инфекций в развивающихся странах: обзор данных исследований на уровне сообществ. Pediatr Infect Dis J 2009; 28.S3–9. https://doi.org/10.1097/inf.0b013e3181958780. Искать в Google Scholar
4. Connell, TG, Rele, M, Cowley, D, Buttery, JP, Curtis, N. Насколько надежен отрицательный результат посева крови? Объем крови, сданной на посев в повседневной практике детской больницы. Педиатрия 2007; 119: 891–6. https://doi.org/10.1542/peds.2006-0440. Искать в Google Scholar
5. Тевабе, Т., Мохаммед, С., Тилахун, Й, Мелаку, Б., Фента, М., Дагнау, Т. и др. Клинические исходы и факторы риска неонатального сепсиса среди новорожденных в специализированной больнице Felege Hiwot, Бахир-Дар, региональный штат Амхара, Северо-Западная Эфиопия, 2016 г .: обзор ретроспективной карты. BMC Res Notes 2017; 10: 265. https://doi.org/10.1186/s13104-017-2573-1. Поиск в Google Scholar
6. Чаухан, Н., Тивари, С., Джайн, У. Потенциальные биомаркеры для эффективного скрининга инфекций неонатального сепсиса: обзор. Microb Pathog 2017; 107: 234–42. https://doi.org/10.1016/j.micpath.2017.03.042. Поиск в Google Scholar
7. Cimenti, C, Erwa, W, Müller, W, Resch, B. Роль подсчета незрелых гранулоцитов и информации о незрелом миелоиде в диагностике неонатального сепсиса. Clin Chem Lab Med 2012; 50: 1429–32. https://doi.org/10.1515/cclm-2011-0656. Искать в Google Scholar
8. Haque, KN. Определения инфекции кровотока у новорожденного. Pediatr Crit Care Med 2005; 6: S45–9. https://doi.org/10.1097/01.pcc.0000161946.73305.0a. Искать в Google Scholar
9. elik, HT, Portakal, O, Yiğit, Ş, Hasçelik, G, Korkmaz, A, Yurdakök, M. Эффективность новых параметров лейкоцитов по сравнению с С-реактивным белком, прокальцитонином и интерлейкином-6 в сыворотке в диагностике неонатального сепсиса. Pediatr Int 2016; 58: 119–25. https://doi.org/10.1111/ped.12754. Искать в Google Scholar
10. Ward, PC. CBC на рубеже тысячелетий: обзор. Clin Chem 2000; 46: 1215–20. https://doi.org/10.1093/clinchem/46.8.1215. Искать в Google Scholar
11. Edwards, MS. Клинические особенности, оценка и диагностика сепсиса у доношенных и поздних недоношенных детей ; 2017. Доступно по адресу: www.uptodate.com. Искать в Google Scholar
12.Нигро, К.Г., О’Риордан, Массачусетс, Моллой, Э.Дж., Уолш, М.С., Сандхаус, Л.М. Производительность автоматизированного подсчета незрелых гранулоцитов как предиктора неонатального сепсиса. Am J Clin Pathol 2005; 123: 618–24. https://doi.org/10.1309/73h7k7ubw816pbjj. Искать в Google Scholar
13. Ансари-Лари, М.А., Киклер, Т.С., Боровиц, М.Дж. Измерение незрелых гранулоцитов с помощью Sysmex XE-2100: связь с инфекцией и сепсисом. Am J Clin Pathol 2003; 120: 795–9. https://doi.org/10.1309/lt30bv9ujjv9cfhq.Поиск в Google Scholar
14. Nahm, CH, Choi, JW, Lee, J. Дельта-индекс нейтрофилов в автоматизированном подсчете незрелых гранулоцитов для оценки тяжести заболевания пациентов с сепсисом. Ann Clin Lab Sci 2008; 38: 241–6. Искать в Google Scholar
15. Виланд, Э.Л., Сандхаус, Л.М., Георгиевская, З., Хойен, С.М., О’Риордан, М.А., Нок, М.Л. Автоматизированные нормы незрелых гранулоцитов у взрослых и детей не подходят для оценки раннего сепсиса у новорожденных. Acta Paediatr 2014; 103: 494–7.https://doi.org/10.1111/apa.12563. Поиск в Google Scholar
16. Заки Мел, С., Эль-Сайед, Х. Оценка микробиологических и гематологических параметров и E-селектина как ранних предикторов исхода неонатального сепсиса. Arch Pathol Lab Med 2009; 133: 1291–6. https://doi.org/10.1043/1543-2165-133.8.1291. Поиск в Google Scholar
17. Ли, С.М., Ын, Х.С., Намгунг, Р., Парк, М.С., Парк, К.И., Ли, К. Полезность индекса дельта-нейтрофилов для оценки неонатального сепсиса. Acta Paediatr 2013; 102: e13–6.https://doi.org/10.1111/apa.12052. Искать в Google Scholar
18. Челик, И.Х., Арифоглу, И., Арслан, З., Аксу, Г., Бас, А.Ю., Демирель, Н. Значение индекса дельта нейтрофилов в диагностике неонатального сепсиса, последующем наблюдении и прогнозировании смертности. Early Hum Dev 2019; 131: 6–9. https://doi.org/10.1016/j.earlhumdev.2019.02.003. Искать в Google Scholar
19. Сентильнаягам, Б., Кумар, Т., Сукумаран, Дж., Джея, М., Рао, КР. Автоматическое измерение незрелых гранулоцитов: рабочие характеристики и применение в повседневной клинической практике. Patholog Res Int 2012; 2012: 1–6. https://doi.org/10.1155/2012/483670. Искать в Google Scholar
20. Фернандес, Б., Хамагучи, Ю. Автоматизированный подсчет незрелых гранулоцитов. Am J Clin Pathol 2007; 128: 454–63. https://doi.org/10.1309/tvgkd5tvb7w9hhc7. Искать в Google Scholar
21. Roehrl, MH, Lantz, D, Sylvester, C, Wang, JY. Зависимые от возраста эталонные диапазоны для автоматической оценки незрелых гранулоцитов и клинической значимости в амбулаторных условиях. Arch Pathol Lab Med 2011; 135: 471–7. https://doi.org/10.1043/2010-0258-OA.1. Поиск в Google Scholar
22. Алкан Оздемир, С., Арун Озер, Э, Ильхан, О, Суткуоглу, С. Может ли соотношение нейтрофилов и лимфоцитов предсказать поздний сепсис у недоношенных детей? J Clin Lab Anal 2018; 32: e22338. https://doi.org/10.1002/jcla.22338. Искать в Google Scholar
23. Omran, A, Maaroof, A, Saleh, MH, Abdelwahab, A. С-реактивный белок слюны, средний объем тромбоцитов и соотношение нейтрофильных лимфоцитов как диагностические маркеры неонатального сепсиса. J Pediatr 2018; 94: 82–7. https://doi.org/10.1016/j.jpedp.2017.07.004. Искать в Google Scholar
24. Чача, Ф., Мирамбо, М.М., Муши, М.Ф., Каянг, Н., Зюхнер, А., Киденья, Б.Р. и др. Полезность качественного анализа C-реактивного белка и количества лейкоцитов в диагностике неонатальной сепсиса в Медицинском центре Бугандо, Танзания. BMC Pediatr 2014; 14: 248. https://doi.org/10.1186/1471-2431-14-248. Искать в Google Scholar
25. Лай, М.Ю., Цай, М.Х., Ли, С.В., Чан, М.С., Лиен, Р., Фу, Р.Х. и др.Характеристики новорожденных с подтвержденной посевом инфекций кровотока с низким уровнем С-реактивного белка (≥10 мг / л). BMC Infect Dis 2015; 15: 320. https://doi.org/10.1186/s12879-015-1069-7. Искать в Google Scholar
26. Fendler, WM, Piotrowski, AJ. Прокальцитонин в ранней диагностике внутрибольничного сепсиса у недоношенных новорожденных. J Paediatr Child Health 2008; 44: 114–8. https://doi.org/10.1111/j.1440-1754.2007.01230.x. Искать в Google Scholar
Поступила: 27.01.2020
Принято: 2020-04-20
Опубликовано в сети: 17.08.2020
© 2021 Melek Büyükeren et al., опубликовано De Gruyter, Берлин / Бостон
Значение индекса дельта-нейтрофилов в диагностике неонатального сепсиса, последующем наблюдении и прогнозировании смертности
Основные моменты
- •
Полный подсчет клеток крови и периферический мазок являются основой диагностики неонатального сепсиса
- •
- индекс нейтрофилов (DNI) показывает дифференцировку лейкоцитов без дополнительной потребности в крови
- •
DNI полезен для диагностики, дифференциации этиологии, последующего лечения и прогнозирования смертности при неонатальном сепсисе
Резюме
Справочная информация
Полный анализ крови (ОАК) и мазок периферической крови были наиболее часто назначаемыми тестами для диагностики неонатального сепсиса.Дельта-нейтрофильный индекс (DNI) показывает дифференцировку лейкоцитов и рассчитывается при выполнении общего анализа крови.
Цели
Мы стремились оценить значение DNI при неонатальном сепсисе.
Дизайн исследования
DNI был измерен с помощью приборов Siemens Advia 2120 и 2120i. DNI рассчитывали как (количество нейтрофилов и эозинофилов в канале миелопероксидазы) — (количество полиморфноядерных лейкоцитов в канале дольчатости ядра).
Результаты
В исследуемую популяцию вошли 141 и 87 новорожденных с сепсисом (110 подтвержденных, 31 клиническая) и контрольная группы.Демографические признаки были похожи между группами. Группа с доказанным сепсисом имела более низкий вес при рождении и более высокую частоту развития сепсиса с поздним началом, чем в группе клинического сепсиса и контрольной группе. Медиана DNI (16,3 против 1,4) и CRP (6,8 против 0,03 мг / дл) были значительно выше в группе сепсиса. В группе с доказанным сепсисом уровень DNI был значительно выше, чем в группе с клиническим сепсисом (20,8 против 9,1). Пороговый уровень DNI составил 4,6 при чувствительности 85% и специфичности 80%. Пороговый уровень CRP составлял 0,58 мг / дл с чувствительностью 81% и специфичностью 82%.Комбинация DNI и CRP дала 98% чувствительность и 76% специфичность. Летальность в группе сепсиса составила 39%. Средний уровень DNI у пациентов со смертностью был значительно выше (30,1 против 9,6). Пороговый уровень DNI для прогнозирования смертности составил 16,1 с чувствительностью 75% и специфичностью 65%. Последующие уровни DNI значительно снизились через 6–10 дней до нормального уровня (с 16,3 до 4,2).
Выводы
DNI оказался полезным для диагностики, последующего наблюдения и прогнозирования смертности при неонатальном сепсисе без дополнительной крови для общего анализа крови.
Ключевые слова
Индекс дельта нейтрофилов
Диагностика неонатального сепсиса
Дифференциация этиологии
Эффективность лечения
Прогноз смертности
Рекомендуемые статьиЦитирующие статьи (0)
Полный текстB.V.
Рекомендуемые статьи
Ссылки на статьи
Можем ли мы полагаться на сдвиг нейтрофилов влево для диагностики неонатального сепсиса? Необходимость переоценки
Реферат
Предпосылки
Неонатальный сепсис вызывает значительную заболеваемость и смертность среди пораженных новорожденных.Золотым стандартом диагностики является посев крови. Однако его полезность ограничена многими факторами. Быстрый диагностический тест с высокой чувствительностью и специфичностью необходим для быстрой идентификации неонатального сепсиса, не подвергая здоровых новорожденных лечению антибиотиками. Точность подсчета незрелых нейтрофилов для диагностики неонатального сепсиса, является спорной.
Цель
Это быстрое, простое и легкодоступное исследование было направлено на переоценку полезности сдвига нейтрофилов влево для диагностики неонатального сепсиса и оценку его прогностической ценности в отражении результатов для пациентов.
Методы
Это проспективное поперечное исследование включало 285 новорожденных, поступивших в отделение интенсивной терапии новорожденных Каирского университета. Были собраны демографические, клинические и лабораторные данные, включая полные картины крови с ручным дифференцированием и результаты посева крови. Диагностическая точность сдвига нейтрофилов влево была достигнута путем применения множественной логистической регрессии и кривой рабочих характеристик приемника [ROC].
Результаты
Среди исследуемой группы 61.У 4% был определенный сепсис, а у 12,3% — вероятный сепсис. Среднее отношение незрелых нейтрофилов к общему количеству нейтрофилов (отношение I / T) составляло 0,25, IQR 0,21, диапазон 0,03–0,8. Отношение I / T ≥0,2 присутствовало у 65,6% пациентов и имело значительно повышенные шансы инфицирования, чувствительность (82,4%), специфичность (81,3%), положительную прогностическую ценность (92,5%) и отрицательную прогностическую ценность (62,2%). Построив график сдвига нейтрофилов влево относительно посева крови, общего количества лейкоцитов (WBC) и количества тромбоцитов на кривой ROC и вычислив площади под кривой (AUC), он оказался хорошим диагностическим тестом (AUC: 0.861), в то время как общее количество лейкоцитов (AUC: 0,515) и количество тромбоцитов (AUC: 0,366) имело низкую диагностическую точность.
Заключение
Сдвиг нейтрофилов влево — это быстрый, простой и легкодоступный тест, который имеет разумную положительную прогностическую ценность и специфичность, что указывает на его полезность в ранней диагностике неонатального сепсиса, а также в снижении риска заражения новорожденных без сепсиса. антимикробная терапия.
Ключевые слова
Сдвиг влево
Незрелые нейтрофилы
Неонатальный сепсис
Повязки
Соотношение I / T
Рекомендуемые статьи Цитирующие статьи (0)
Просмотреть аннотацию© 2018 The Egyptian Pediatric Association Gazette.Издательские услуги, предоставляемые Elsevier B.V.
Рекомендуемые статьи
Ссылки на статьи
Могут ли реакции нейтрофилов у младенцев с очень низкой массой тела при рождении предсказать микроорганизмы, ответственные за поздний бактериальный или грибковый сепсис?
Большое внимание было сосредоточено на подсчете нейтрофилов и различных индексах нейтрофилов, особенно нейтропении и соотношении I: T с использованием референсных диапазонов для нейтрофилов, предложенных Manroe et al. 8 при выявлении новорожденных с ранним сепсисом.Некоторые исследователи отметили недостаточную чувствительность и низкую прогностическую ценность любого из этих параметров при раннем сепсисе. 9, 10, 11 Эти параметры не изучались широко у недоношенных новорожденных с очень низкой массой тела и поздним началом сепсиса, а также не проводились специфические для организма нейтрофильные реакции. Кроме того, новые референсные диапазоны с поправкой на массу тела при рождении, рекомендованные Mouzinho et al. 6 не исследовались при позднем сепсисе.
В настоящем исследовании мы показали, что реакция нейтрофилов на грамотрицательный бактериальный сепсис у детей с очень низкой массой тела количественно отличается по сравнению с инфекцией, вызванной грамположительными бактериями или грибами.И грамположительный бактериальный, и грибковый сепсис оказывали сходный эффект на нейтрофильные реакции в дополнение к крайне редким случаям нейтропении (ANC <1100 / мм 3 ), присутствующей только в трех из 113 эпизодов (2,6%) грамположительных бактериальных инфекций. сепсис, и ни один из них — грибковый сепсис. Редкая встречаемость нейтропении в этом исследовании противоречит результатам Funke et al. , 12 , которые также использовали контрольные диапазоны с поправкой на массу тела при рождении для изучения нейтропении у младенцев с сепсисом.Это исследование, однако, включало как недоношенных VLBW, так и доношенных новорожденных с сепсисом, большинство из которых были ранними и не были подтверждены посевом. Даже используя эталонные диапазоны, предложенные Manroe et al. 8 для зрелых младенцев, Fanaroff et al. 13 также сообщил о нейтропении только 8% случаев (ANC <1500 / мм 3 ) у младенцев с поздним началом сепсиса. В их большом многоцентровом исследовании более двух третей случаев были вызваны грамотрицательными микроорганизмами.Аналогичные наблюдения были сделаны Engle et al. , 5 , которые отметили, что «поздняя инфекция коагулазонегативными стафилококками редко была связана с нейтропенией, тогда как от 15 до 20% эпизодов поздней грамотрицательной инфекции проявлялись или развивали нейтропению». Это редкое явление. Возникновение нейтропении при позднем сепсисе контрастирует с обычным возникновением нейтропении, связанной с «истощением костного мозга, а также сниженной способностью к ускоренному производству нейтрофилов» у недоношенных детей с ранним сепсисом. 14
Причина этой разницы в частоте возникновения нейтропении при сепсисе с ранним и поздним началом неизвестна, равно как и более высокая частота нейтропении в связи с поздним началом грамотрицательной бактериальной инфекции по сравнению с грамположительными бактериальными инфекциями. или грибковые инфекции хорошо изучены. Это может быть связано с вирулентностью инфицирующего организма или с различными уровнями GCSF, поскольку было отмечено, что средний уровень GCSF на организм варьирует для разных организмов у младенцев с сепсисом. 15
Частота нейтропении могла быть выше при серийных измерениях общего анализа крови, особенно у младенцев, у которых была задержка начала соответствующей антибактериальной терапии. Однако, в отличие от длительной тромбоцитопении, наблюдаемой при сепсисе, нейтропения, вызванная сепсисом, обычно сохраняется менее 24 часов. 12 Анализируя исходный общий анализ крови, полученный одновременно с культурой крови, кажется маловероятным, что многие случаи нейтропении были пропущены.
Во многих исследованиях сообщается о сложности определения того, какие изоляты посева крови отражают истинные инфекции, а какие являются контаминантами, особенно в отношении коагулазонегативного стафилококка .Мы полагаем, что у младенцев в этом исследовании были определенные инфекции, поскольку диагноз сепсиса в текущем исследовании был основан на наличии обоих клинических признаков синдрома сепсиса в дополнение к положительным единичным бактериальным или грибковым изолятам из одного места посева крови. Ранее мы показали, что посев крови из одного очага должен быть достаточным для документирования сепсиса у младенцев с симптомами и является биологически правдоподобным, поскольку у маленьких детей наблюдается бактериемия с большим количеством колоний, бактериальный клиренс медленнее, а бактериемия более продолжительная у новорожденных с сепсисом. чем у пожилых пациентов.
, 18 , и что все антибиотики имеют хорошее проникновение в спинномозговую жидкость и одинаково эффективны для лечения менингита, который обычно ассоциируется с грамотрицательным сепсисом.В действительности, когда выбираются эмпирические антибиотики для лечения сепсиса с поздним началом, следует особенно беспокоиться о фульминантном грамотрицательном сепсисе с поздним началом, при котором младенцы умирают до того, как будут выявлены патогены и чувствительность к антибиотикам, часто менее чем за 48 часов от начала заболевания. болезнь. 18 При изменении паттернов микроорганизмов (например, коагулазонегативных Staphylococcus и Candida ), вызывающих большинство случаев позднего сепсиса в отделениях интенсивной терапии интенсивной терапии, нейтропения у детей с ОНМТ с большей вероятностью будет вызвана другими причинами, такими как доброкачественные поздние — начавшаяся нейтропения, как описано Omar et al. 19 , а не сепсис. В то время как единичное обнаружение нейтропении у стабильного недоношенного ребенка может не служить основанием для оценки сепсиса или агрессивного лечения, нейтропения у больного ребенка может быть зловещей и может служить ранним предупреждением о грамотрицательном бактериальном сепсисе, если не доказано иное.Необходимы дальнейшие проспективные и более масштабные исследования, чтобы лучше понять основу наблюдаемых эффектов различных организмов на количество и индексы нейтрофилов, а также для оценки того, предсказывают ли специфические реакции нейтрофилов у детей с ОНМТ организмов, ответственных за поздний бактериальный или грибковый сепсис .В частности, необходимо изучить взаимодействия между нейтрофилами, инфекционными организмами и GCSF у детей с очень низкой массой тела, страдающих сепсисом.
Прогностическое значение индекса дельта нейтрофилов при остановке сердца у детей
В настоящем исследовании мы продемонстрировали, что DNI может быть важным независимым предиктором 30-дневной смертности и неврологических исходов у детей в раннем постреанимационном периоде. Конкретно, значение DNI выше 3,3% через 24 часа после СА значительно предсказывало 30-дневную смертность (HR: 11.8; P <0,001) и неврологические исходы (OR: 8,04; P = 0,003) в этой исследуемой группе педиатрических пациентов.
В нашем исследовании значение DNI было значительно выше у выживших, чем у выживших, с момента сразу после CA до более позднего времени. После СА пациенты испытали «синдром после остановки сердца», который имитирует физиологические изменения, соответствующие наблюдениям за тяжелым сепсисом 1,25 . Ишемия-реперфузия после СА стимулирует врожденный иммунитет, а последующее высвобождение цитокинов опосредует стерильные системные воспалительные реакции и полиорганную дисфункцию 16,25 .Ранее Yune и др. . сообщили, что значения DNI более 8,4% сразу после поступления в отделение неотложной помощи (HR: 3,22) и более 12,9% через 24 часа после поступления в ED (HR: 3,29) были связаны с 30-дневной смертностью у взрослых с ВГОК. пациенты 20 .
DNI и ишемия-реперфузия после остановки сердца
DNI показывает отношение незрелых гранулоцитов в крови к общему количеству нейтрофилов. DNI рассчитывается с использованием автоматического анализатора клеток крови 26 с двумя отдельными каналами, миелопероксидазными (MPO) каналами и каналами ядерной долей 17 .Вычитая долю зрелых полиморфно-ядерных лейкоцитов из суммы MPO-реактивных клеток, можно оценить долю незрелых гранулоцитов, таких как метамиелоциты, миелоциты и промиелоциты 17 .
Высокий DNI указывает на увеличение циркулирующих незрелых гранулоцитов, и это происходит при различных острых состояниях, таких как острые гематологические злокачественные новообразования, кровотечение и сепсис 18 . Предыдущие исследования также описали DNI как полезный маркер для диагностики сепсиса и септического шока, прогнозирования положительного посева крови и диссеминированного внутрисосудистого свертывания 17,18,28 .Подобно DNI, повышенное соотношение незрелых / общих гранулоцитов (IG%), называемое сдвигом влево 27 , является еще одним показателем увеличения незрелых гранулоцитов. Sauneuf и др. . сообщили, что более высокое соотношение незрелых / общих гранулоцитов при поступлении в ОИТ независимо предсказывало смерть или плохие неврологические исходы (CPC 3-5) в большой проспективной когорте пациентов после OHCA 29 .
Синдром после остановки сердца является второй сложной фазой после CA 1,25 .Системная ишемия / реперфузия — один из ключевых компонентов этого статуса 30 . Системная ишемия / реперфузия вызывает воспаление всего тела, подобное SIRS 1,31 . Сообщалось об увеличении циркулирующих незрелых гранулоцитов в ранний пост-CA период 20,29 , и предполагается, что это связано с различными механизмами, такими как ишемия костного мозга 32 , паралич нейтрофилов 33 , эндотоксемия 34 , и компенсаторный ответ за счет истощения зрелых нейтрофилов в костном мозге 35 .
В этом исследовании мы использовали автоматический анализатор клеток крови (ADVIA 2120) для определения DNI, который преодолевает ограничение ручного подсчета, которое сильно коррелирует с ручным подсчетом незрелых гранулоцитов 17,20 . Юн и др. . использовали тот же анализатор ADVIA 2120 и продемонстрировали, что DNI были связаны с 30-дневной смертностью у взрослых OHCA (пороговое значение 12,9% через 24 часа после поступления в ED) 20 .
В то время как большинство опубликованных исследований использовали ADVIA для измерения DNI для оценки доли незрелых гранулоцитов 36 , большинство из них было сосредоточено на сепсисе или инфекционных заболеваниях.Поскольку мы смогли найти только одно исследование, в котором оценивалась клиническая ценность DNI как диагностического или прогностического маркера после CA 20 , следует провести дополнительные исследования того, как DNI пропорционально отражает ишемический инсульт после CA, с использованием больших когорт.
В отличие от DNI, наши результаты показали, что количество лейкоцитов (WBC) и абсолютное количество нейтрофилов (ANC) в 0 час было ниже у умерших пациентов по сравнению с выжившими. В предыдущем исследовании также сообщалось, что первоначальные анализы крови во время реанимации выявили значительно более низкий уровень лейкоцитов в группе с устойчивым ROSC у взрослых пациентов с ВГОК 37 .В другом ретроспективном одноцентровом исследовании взрослых пациентов с IHCA и OHCA, которым проводилось целенаправленное регулирование температуры по поводу синдрома после остановки сердца в течение 6 часов после CA, количество лейкоцитов и медиана ANC также были значительно ниже у умерших, чем у выживших 38 .
Ишемия / реперфузия после КА активирует иммунологический процесс, что приводит к повышению уровня цитокинов, растворимых рецепторов и эндотоксинов; и эти изменения связаны с клинически плохими исходами 1,25 .При сепсисе избыточное производство оксида азота (NO), хемокинов и цитокинов снижает хемотаксис и адгезионные взаимодействия между нейтрофилами и эндотелием. Алвес-Филхо и др. . предполагают, что нейтрофильный паралич характеризуется неспособностью нейтрофилов мигрировать в очаг инфекции и несоответствующей секвестрацией нейтрофилов в отдаленных органах 39 . При синдроме после остановки сердца, как и при SIRS 1 , после CA 25,33 наблюдались повышенные уровни P- и E-селектина, растворимая молекула адгезии сосудистых клеток-1 и растворимая межклеточная молекула-1.Хотя механизмы, лежащие в основе снижения лейкоцитов и АНК в отличие от незрелых гранулоцитов во время раннего периода реанимации, неясны, нейтрофильный паралич при синдроме после остановки сердца может быть возможным объяснением; тяжелая ишемия может вызвать большую степень взаимодействия между молекулами адгезии и активированными нейтрофилами с последующим более низким уровнем циркулирующих нейтрофилов 20 .
Таким образом, ишемия / реперфузия всего тела после СА приводит к состоянию, аналогичному сепсис-подобному синдрому.Он также повышает цитокины, присутствие эндотоксина в плазме, активацию путей коагуляции и ингибирование путей антикоагулянта 1,30,40 . Однако педиатрические исследования, оценивающие иммунно-воспалительный ответ, который представляет статус системной ишемии / реперфузии после СА, ограничены по сравнению с исследованиями на взрослых 41 . Таким образом, данные, экстраполированные из исследований взрослых, в настоящее время используются для понимания и лечения педиатрического синдрома после остановки сердца 30,42 .
В нашем исследовании пациенты, которые имели более высокие значения, чем пороговое значение для DNI в каждый момент времени, показали значительно более короткое время выживания на кривых Каплана-Мейера. Sol и др. . сообщили, что DNI на момент поступления в педиатрическое отделение интенсивной терапии (ICU) было связано с серьезностью заболевания и смертностью, при этом пороговое значение для прогнозирования смертности составляло 4,95% 43 . Пороговое значение DNI через 24 часа для прогнозирования 30-дневной смертности в нашем исследовании было аналогично результатам для вышеупомянутых педиатрических пациентов ICU.
Тем не менее, пороговое значение через 24 часа в нашем исследовании было намного ниже, чем у взрослых пациентов с ВГОК (3,3% против 12,9%). Это несоответствие может быть связано с различиями между включенными пациентами. Нашими субъектами были в основном педиатрические пациенты с CA (IHCA) в стационаре. По сравнению с OHCA пациенты с IHCA, как правило, имеют более низкий риск ишемического повреждения из-за раннего распознавания CA и назначения высококачественной CPR 44,45 . Следовательно, более низкое пороговое значение DNI в нашем исследовании может отражать более низкую степень ишемического инсульта.Однако исследований о взаимосвязи между степенью ишемии и DNI у педиатрических пациентов не проводилось. Следовательно, необходимы дальнейшие исследования, чтобы продемонстрировать, как воспалительный ответ отражается на DNI и чем он отличается у взрослых и детей в статусе после остановки сердца.
До сих пор DNI был в первую очередь известен как полезный диагностический и прогностический биомаркер у пациентов с бактериемией и сепсисом. Park и др. . сообщил, что значение DNI больше 6.5% было полезным лабораторным маркером для дифференциации тяжелого сепсиса и септического шока у взрослых пациентов в отделении интенсивной терапии 18 . Следовательно, значения DNI у пациентов, у которых CA этиология предположительно является сепсисом, могут быть высокими до ареста, а также влиять на связь между уровнем DNI и исходами. Тем не менее, в нашем исследовании среднее значение DNI не отличалось между группами, ассоциированными с сепсисом, и группами другой этиологии в каждый момент времени (дополнительная таблица S10).
Кроме того, дыхательная недостаточность вызывалась другими инфекционными заболеваниями (например,грамм. пневмония) может влиять на циркулирующие лейкоциты; однако DNI обычно повышается при более тяжелых инфекциях, таких как сепсис или тяжелый системный воспалительный статус 18,46 . Например, предыдущие исследования показали, что DNI может быть полезен для различения различных инфекционных состояний, таких как APN от нижних ИМП (пороговое значение> 1,3%) 47 , туберкулез легких от внебольничной пневмонии (CAP) (вырезать пороговое значение, ≤1,0%) 48 , и ВБП низкой степени злокачественности от инфекции верхних дыхательных путей (пороговое значение> 1.7%) 49 . Однако их пороговые значения были намного ниже, чем для сепсиса (пороговое значение> 6,5%) 18 , бактериемии (пороговое значение 4,4%) 46 или прогностическое пороговое значение для взрослых OHCA (пороговое значение> 8,4%) 20 с нашим результатом (пороговое значение 3,3%).
Кроме того, CRP в 0 час может быть повышен из-за тяжелой инфекции, но он также может быть повышен в дни после реанимации CA 50,51 , отражая системную воспалительную реакцию.Предыдущие исследования показали, что уровень ПКТ и СРБ повышается после СА у взрослых, но ни уровень ПКТ, ни уровень СРБ не были связаны с инфекцией 52,53,54,55 .
В настоящем исследовании большинство случаев респираторной этиологии было связано с обструкцией дыхательных путей (68,9%, например, смещение / обструкция Т-образной трубки, ларингоспазм, бронхиальная астма). Следовательно, более высокий уровень СРБ в 0 часов у пациентов, умерших в течение 30 дней, может быть вызван не инфекционной причиной, а, скорее, их тяжелой системной воспалительной реакцией.
Основные заболевания
Другим фактором, который может влиять на циркулирующие незрелые гранулоциты, были гематологические злокачественные новообразования. В нашем исследовании большинство пациентов с гематологическими злокачественными новообразованиями прошли как минимум более трех химиотерапевтических процедур и / или трансплантацию гемопоэтических стволовых клеток. Кроме того, значение DNI до CA (отбор образцов в течение 48 часов до CA) было в основном 0. Таким образом, мы предположили, что DNI можно использовать для оценки тяжести ишемического инсульта, отражая системный воспалительный статус, возникающий в результате ишемической реперфузии в посткардиальный период. статус ареста.К сожалению, количество образцов, взятых в течение 48 часов до CA, было настолько маленьким, что мы не смогли провести анализ подгруппы.
Другие прогностические факторы
Наряду со значением DNI, более длительная продолжительность СЛР и более высокое содержание натрия в 0 час также показали значительную связь со смертностью в нашей модели многомерной логистической регрессии. Было показано, что более длительная компрессия связана со снижением выживаемости как у детей с IHCA, так и у пациентов с OHCA 4,8 .В нашем исследовании продолжительность СЛР также была значительно короче у выживших. Кроме того, при однофакторном анализе СЛР продолжительностью более 30 минут была значимо связана с 30-дневной смертностью.
Макино и др. . обнаружили, что 105 взрослых пациентов с ВГОК, поступивших в отделение неотложной помощи, не имели разницы в уровне натрия по сравнению с контрольными пациентами 56 . Отдельно Shin и др. . 57 сообщил, что среди исходных лабораторных параметров крови, присутствующих во время СЛР взрослых пациентов с ВГОК, уровень натрия не показал значительной разницы между группами выживания и невыживанием.Для сравнения, в нашем исследовании более высокий уровень натрия был связан со смертностью после педиатрической СА.
Фактически, уровень натрия может иметь отношение к введенному SB. Введение SB считается вариантом лечения тяжелого метаболического ацидоза при СА. Использование SB во время CA также связано с повышенной смертностью 8 , но остается спорным в отношении педиатрических пациентов 58 . В нашем исследовании уровень натрия был значительно выше в 0 час 24 часа в группе смерти.Однако общее введенное количество SB существенно не отличалось в 0 час, но было значительно выше через 24 часа и 48 часов в группе смерти. Только введение SB в течение 30 дней после CA было значимо связано с 30-дневной смертностью в однофакторном анализе Кокса.
До сих пор, насколько нам известно, не было специального исследования, в котором изучалась бы связь между уровнем натрия и прогнозом после СА. Следовательно, необходимы будущие исследования, чтобы определить и подтвердить взаимосвязь между уровнем натрия в сыворотке и результатами после СА.
Значение DNI и неврологические исходы
В нашем исследовании DNI был значительно выше в случаях плохого неврологического исхода в каждый момент времени. Связь между DNI и неврологическим исходом при различных состояниях, включая ранний постреанимационный статус, изучалась редко, хотя одно одноцентровое ретроспективное исследование OHCA у взрослых показало, что значения DNI более 8,4% при поступлении в отделение неотложной помощи (HR: 2,718; ). P <0,001) и более 10,5% через 24 часа после поступления в ED (HR: 1.709; P = 0,02) были связаны с плохими неврологическими исходами для выживших после OHCA 20 .
Пороговый уровень DNI был почти таким же, как и в нашем исследовании на очень ранней стадии (8,4% против 8,1%) после CA; однако через 24 часа после CA он все еще был выше нашего результата (10,5% против 3,3%). Как упоминалось выше, эти результаты могут быть связаны не только с различиями между включенными пациентами (OHCA и IHCA), но также с нейрональной уязвимостью детей к гипоксически-ишемическому инсульту 59 .У детей повышен церебральный кровоток и более высокие метаболические потребности по сравнению со взрослыми, и они подвергаются созреванию нейронов и синаптогенезу во время инсульта 42 . Следовательно, более низкий DNI, который может отражать более низкую степень воспалительного статуса (ишемию) в раннем статусе ROSC, может привести к худшим неврологическим исходам у детей. Однако это явление требует дальнейшего изучения.
Получены противоречивые результаты относительно корреляции между pH и неврологическими исходами при CA.В недавнем когортном исследовании педиатрических пациентов с IHCA, пациенты с плохими неврологическими исходами показали более низкие уровни pH в соответствии со шкалой PCPC 14 . Точно так же в нашем исследовании более низкий уровень pH в 0 часов был независимо связан с краткосрочными плохими неврологическими исходами. Однако другой отчет с участием педиатрических пациентов с ВГОК показал, что уровень pH не был связан с неврологическим восстановлением на основе баллов по шкале адаптивного поведения Вайнленда, второе издание (VABS-II) 60 . Протоколы исследования, такие как дизайн когорты, методы оценки результатов и место CA, могут способствовать или учитывать эти различия.
DNI можно определить с помощью CBC без дополнительных затрат или времени. Более того, DNI может выполняться независимо и независимо от клинических условий. Следовательно, DNI может быть быстрым и недорогим методом оценки прогноза у детей после CA, особенно в контексте ограниченных ресурсов. Однако сочетание других прогностических параметров может улучшить прогноз исходов, поэтому клиницисты должны учитывать множество факторов при прогнозировании исходов у младенцев и детей после CA 2,6,14,60,61 .
Гематологический профиль сепсиса у новорожденных: нейтрофильный CD64 как диагностический маркер
Реферат
ЦЕЛЬ. Цель состояла в том, чтобы определить полезность CD64 нейтрофилов в качестве диагностического маркера сепсиса у новорожденных.
МЕТОДЫ. Было проведено проспективное исследование, в котором последовательно участвовали младенцы с подозрением на сепсис. Был проведен полный анализ крови с дифференцировкой, посев крови и измерение индекса CD64, и индексы нейтрофилов CD64 были коррелированы с диагнозами подтвержденного и подозреваемого сепсиса.
РЕЗУЛЬТАТЫ. Было проведено 293 эпизода оценки сепсиса у 163 младенцев. Младенцы с эпизодами сепсиса (подтвержденными или подозреваемыми; n = 40) имели больший гестационный возраст (34,7 ± 0,9 недели) по сравнению с детьми ( n = 123) без сепсиса (32,6 ± 0,5 недели), но имели аналогичный вес при рождении (2325 ± 200 против 1969 ± 94 г) и оценка по шкале Апгар на 1 и 5 минуте. Разницы в продолжительности госпитализации для двух групп не было. Как и ожидалось, гематологические профили эпизодов сепсиса ( n = 128) характеризовались более высоким количеством лейкоцитов, абсолютным количеством нейтрофилов, абсолютным количеством полос и соотношением незрелых / общих нейтрофилов, но более низким количеством тромбоцитов.Эпизоды сепсиса имели более высокие показатели CD64 нейтрофилов (5,61 ± 0,85 против 2,63 ± 0,20). Для всех эпизодов сепсиса индекс CD64 имел площадь под кривой при анализе рабочих характеристик приемника 0,74; при пороговом значении 2,30 индекс CD64 в сочетании с абсолютным числом нейтрофилов имел наивысшую отрицательную прогностическую ценность (93%) для исключения сепсиса и 95% чувствительности для диагностики сепсиса. Для эпизодов сепсиса с положительной культурой индекс CD64 имел самую высокую площадь под кривой (0.852) всех гематологических переменных с чувствительностью 80% и специфичностью 79%, с пороговым значением 4,02.
ВЫВОДЫ. CD64 нейтрофилов — высокочувствительный маркер неонатального сепсиса. Требуются проспективные исследования, включающие CD64 в систему оценки сепсиса.
Подозрение на сепсис у новорожденного
Джонатан М. Кляйн, MD
Статус экспертной оценки: внутренняя экспертная проверкаИз-за различных факторов новорожденные, как недоношенные, так и доношенные, очень восприимчивы к сепсису в период новорожденности.В отличие от младенцев старшего возраста, детей и взрослых признаки сепсиса у новорожденных расплывчаты и неспецифичны. Самыми ранними признаками могут быть апноэ, респираторная недостаточность или плохое питание. Другие признаки и симптомы включают летаргию, нестабильность температуры, гипербилирубинемию, брадикардию, судороги и ацидоз.
При подозрении на сепсис необходимо провести обследование на сепсис, чтобы включить общий анализ крови с дифференцировкой, посев крови и спинномозговую жидкость для анализа и посева. Антибиотики следует начинать сразу после завершения обследования.Посев мочи может быть исключен из обследований на сепсис при рождении, но его следует включить в последующие обследования на сепсис. Если есть другие обстоятельства, указывающие на происхождение сепсиса, следует получить дополнительные подходящие культуры, например, из трахеальной жидкости или из области целлюлита.
Младенцы с сепсисом часто имеют повышенное абсолютное количество полосок и / или пониженное абсолютное количество нейтрофилов или повышенное соотношение I: T (см. Общее количество гранулоцитов, стр.106, и контрольные значения индексов лейкоцитов, стр.107). Однако нормальное количество лейкоцитов у младенца с признаками сепсиса (см. I) не исключает инфекции, и поэтому антибиотики следует начинать в ожидании результатов посева.
Схема антибиотикотерапии при обследовании на сепсис, проводимом при рождении или поступившем у новорожденного в возрасте до 30 дней, включает ампициллин и гентамицин.
Если ребенок находился в яслях и подозревается сепсис, в схему лечения следует включать ванкомицин и гентамицин. Пиперациллин также следует рассмотреть, если есть предположение о возможной грамотрицательной инфекции, например.g., при окраске по Граму трахеального аспирата или при наличии псевдомонад в детской.
Лечение ацикловиром должно быть рассмотрено, если возможно инфицирование ВПГ, до получения результатов обследования на ВПГ. Это исследование должно включать поверхностные культуры на ВПГ, тесты функции печени и ЦСЖ для подсчета клеток и ПЦР ВПГ.Когда было проведено обследование на сепсис, младенца следует повторно обследовать через 72 часа. Можно рассмотреть возможность прекращения приема антибиотиков, если клиническое течение не указывает на инфекцию, а посевы отрицательные.
Если посев крови положительный, лечить 10 дней. Получите повторный посев крови через 24-48 часов терапии, чтобы обеспечить эффективную терапию.
Если посев спинномозговой жидкости положительный, проводите лечение в течение 14-21 дней.У младенцев с положительными культурами антимикробная терапия корректируется в соответствии с чувствительностью. Уровни антибиотиков в сыворотке крови должны соблюдаться в соответствии с рекомендациями на странице XX.
Если получены C-реактивные белки (CRP), начальный CRP <1 не является определенным подтверждением отсутствия инфекции.


 2.2. Возрастные особенности осмотической резистентности эритроцитов у детей, %
2.2. Возрастные особенности осмотической резистентности эритроцитов у детей, %  2.3. Гематокритная величина и эритроцитометрические показатели у здоровых детей различного возраста (А. Ф. Тур, Н. П. Шабалов, И. Тодоров)
2.3. Гематокритная величина и эритроцитометрические показатели у здоровых детей различного возраста (А. Ф. Тур, Н. П. Шабалов, И. Тодоров)  2.4. Нормальный состав периферической крови детей разного возраста (Е. Н. Мосягина и соавт.)
2.4. Нормальный состав периферической крови детей разного возраста (Е. Н. Мосягина и соавт.)  число, х109/л
число, х109/л 2.5. Показатели красной крови, СОЭ и содержание тромбоцитов в крови здоровых детей (Е. Д. Гольдберг, Р. М. Тарлова)
2.5. Показатели красной крови, СОЭ и содержание тромбоцитов в крови здоровых детей (Е. Д. Гольдберг, Р. М. Тарлова)  * В строке «а» — величины М±m, в строке «б» — пределы колебаний М±m
* В строке «а» — величины М±m, в строке «б» — пределы колебаний М±m * В строке «а» — относительные величины содержания форменных элементов, % (М±m), в строке «б» — абсолютные величины (сегментоядерные нейтрофилы и лимфоциты, тыс.) в системе СИ -107л (М±m).
* В строке «а» — относительные величины содержания форменных элементов, % (М±m), в строке «б» — абсолютные величины (сегментоядерные нейтрофилы и лимфоциты, тыс.) в системе СИ -107л (М±m). 2.8. Факторы свертывания крови у новорожденных и сроки их возрастания до уровня взрослых (В. А. Мазурин, И. М. Воронцов)
2.8. Факторы свертывания крови у новорожденных и сроки их возрастания до уровня взрослых (В. А. Мазурин, И. М. Воронцов) 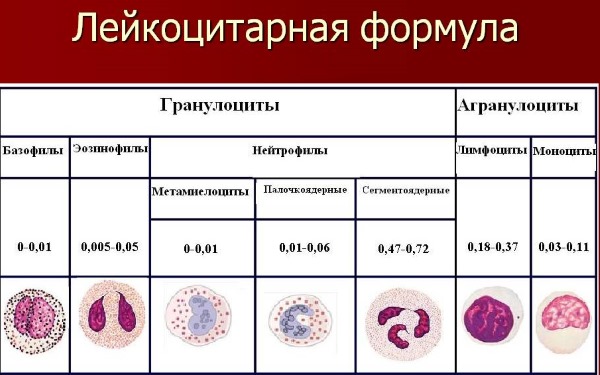 2.9. Основные показатели нормальной коагулограммы у детей (Е. П. Иванов)
2.9. Основные показатели нормальной коагулограммы у детей (Е. П. Иванов)  2.10. Коагулограмма здоровых детей
2.10. Коагулограмма здоровых детей  2.11. Минутный объем крови (МОК) у детей, мл
2.11. Минутный объем крови (МОК) у детей, мл  2.13. Буферная система крови здоровых детей
2.13. Буферная система крови здоровых детей