Гидроторакс | Клиника «Оберіг»
Гидроторакс – это скопление жидкости между плевральными листками – в плевральной полости. Плевральные листки покрывают легкие и выстилают внутреннюю поверхность грудной клетки. В норме между ними содержится всего несколько миллилитров жидкости, которая выполняет функцию смазки.
Если легкие воспаляются, между плевральными листками скапливается экссудат. Это жидкость, которая выделяется из мелких кровеносных сосудов. В плевральной полости может появиться также транссудат. Он накапливается вследствие нарушения крово- и лимфообращения.
В отличие от экссудата, образование транссудата не связано с воспалительными процессами. Экссудат характерен для другого заболевания – плеврита. В этой статье мы рассмотрим накопление транссудата.
Причины гидроторакса легких могут быть различными. Это сердечная недостаточность, заболевания почек, цирроз печени и портальная гипертензия, тромбоэмболия легочной артерии и др.
Гидроторакс также сопровождает онкологические заболевания.
СИМПТОМЫ И ПРИЗНАКИ ГИДРОТОРАКСА
Симптомы гидроторакса вызываются сдавливанием легких скопившейся жидкостью. Пациентов беспокоит чувство тяжести, давления в груди, сухой кашель, одышка. Если в плевральной полости накапливается большое количество транссудата, затрудняется отток крови из шейных вен. Тогда становится заметным их набухание.
Классификация гидроторакса основывается на объеме и расположении жидкости. Выделяют малый и большой, правосторонний и левосторонний, тотальный и осумкованный гидроторакс. В большинстве случаев гидроторакс охватывает обе плевральные полости, а при метастатическом его характере чаще наблюдается одностороннее поражение.
ДИАГНОСТИКА ГИДРОТОРАКСА
Проводится рентгенологическое обследование органов грудной клетки, которое позволяет выявить наличие жидкости в плевральной полости. При подозрении на опухолевый гидроторакс показана компьютерная томография для выявления метастазов в органах грудной клетки.
При подозрении на опухолевый гидроторакс показана компьютерная томография для выявления метастазов в органах грудной клетки.
Окончательный диагноз при гидротораксе можно поставить только после лабораторного исследования жидкости в плевральной полости. Для ее забора проводится плевральная пункция. Жидкость отсасывается через небольшой прокол в грудной клетке. Лабораторный анализ показывает, является он экссудатом или транссудатом.
Тем не менее, в ряде случаев путем лабораторного анализа жидкости не удается установить причину развития гидроторакса, и для окончательной установки диагноза может быть рекомендована видеоторакоскопия. Этот эндоскопический метод позволяет осмотреть плевральную полость и произвести биопсию подозрительного участка.
ЛЕЧЕНИЕ ГИДРОТОРАКСА
Небольшой гидроторакс не требует специального лечения. Жидкость рассасывается самостоятельно при успешной терапии основного заболевания.
При значительном накоплении транссудата плевральная пункция используется в качестве не только диагностического, но и лечебного метода.
Лечение гидроторакса легких с помощью плевроцентеза улучшает состояние пациента, уменьшает одышку и неприятные ощущения. Но поскольку гидроторакс – вторичное заболевание, последующее лечение должно быть направлено на причину его развития.
При персистирующем гидротораксе, в особенности – метастатического характера, может быть выполнен видеоторакоскопический плевродез. Хирург под контролем эндовидеокамеры вводит в плевральную полость различные агенты, чаще химические (тальковый плевродез). Процедура вызывает спаечный процесс между листками плевры, который препятствует дальнейшему накоплению жидкости.
В Торакопульмонологическом центре Универсальной клиники «Оберіг» имеется все необходимое для диагностики и лечения гидроторакса. Плевральная пункция, а также видеоторакоскопия, осуществляется с помощью современного высокотехнологичного оборудования.
В Универсальной клинике «Оберіг» работает собственный патогистологический центр, в котором проводится исследование плевральной жидкости. Точная диагностика причины гидроторакса – основа правильной стратегии лечения пациента.
Запишитесь на прием к специалистам Торакопульмонологического центра, позвонив по телефону:
(044) 521 30 03
Гидроторакс — лечение в санаториях Пятигорска, цены на 2021 год
Я, субъект персональных данных, в соответствии с Федеральным законом от 27 июля 2006 года № 152 «О персональных данных» предоставляю владельцу сайта «Санатории Пятигорска» данные которого указаны в разделе сайта Контакты (далее — Оператор), расположенному по адресу Пятигорск. ул. Воровского 20, согласие на обработку персональных данных, указанных мной в форме веб-чата и/или в форме заказа обратного звонка на сайте sanatorii-pyatigorska.ru в сети «Интернет», владельцем которого является Оператор.
- Состав предоставляемых мной персональных данных является следующим: ФИО, адрес электронной почты и номер телефона.

- Целями обработки моих персональных данных являются: обеспечение обмена короткими текстовыми сообщениями в режиме онлайн-диалога и обеспечение функционирования обратного звонка.
- Согласие предоставляется на совершение следующих действий (операций) с указанными в настоящем согласии персональными данными: сбор, систематизацию, накопление, хранение, уточнение (обновление, изменение), использование, передачу (предоставление, доступ), блокирование, удаление, уничтожение, осуществляемых как с использованием средств автоматизации (автоматизированная обработка), так и без использования таких средств (неавтоматизированная обработка).
- Я понимаю и соглашаюсь с тем, что предоставление Оператору какой-либо информации о себе, не являющейся контактной и не относящейся к целям настоящего согласия, а равно предоставление информации, относящейся к государственной, банковской и/или коммерческой тайне, информации о расовой и/или национальной принадлежности, политических взглядах, религиозных или философских убеждениях, состоянии здоровья, интимной жизни запрещено.
- В случае принятия мной решения о предоставлении Оператору какой-либо информации (каких-либо данных), я обязуюсь предоставлять исключительно достоверную и актуальную информацию и не вправе вводить Оператора в заблуждение в отношении своей личности, сообщать ложную или недостоверную информацию о себе.
- Я понимаю и соглашаюсь с тем, что Оператор не проверяет достоверность персональных данных, предоставляемых мной, и не имеет возможности оценивать мою дееспособность и исходит из того, что я предоставляю достоверные персональные данные и поддерживаю такие данные в актуальном состоянии.
- Согласие действует по достижении целей обработки или в случае утраты необходимости в достижении этих целей, если иное не предусмотрено федеральным законом.
- Согласие может быть отозвано мною в любое время на основании моего письменного заявления.
Гидроторакс симптомы и лечение — Евромедклиник
Гидроторакс – это скопление жидкости (транссудата) в околосердечной, плевральной или брюшной полости.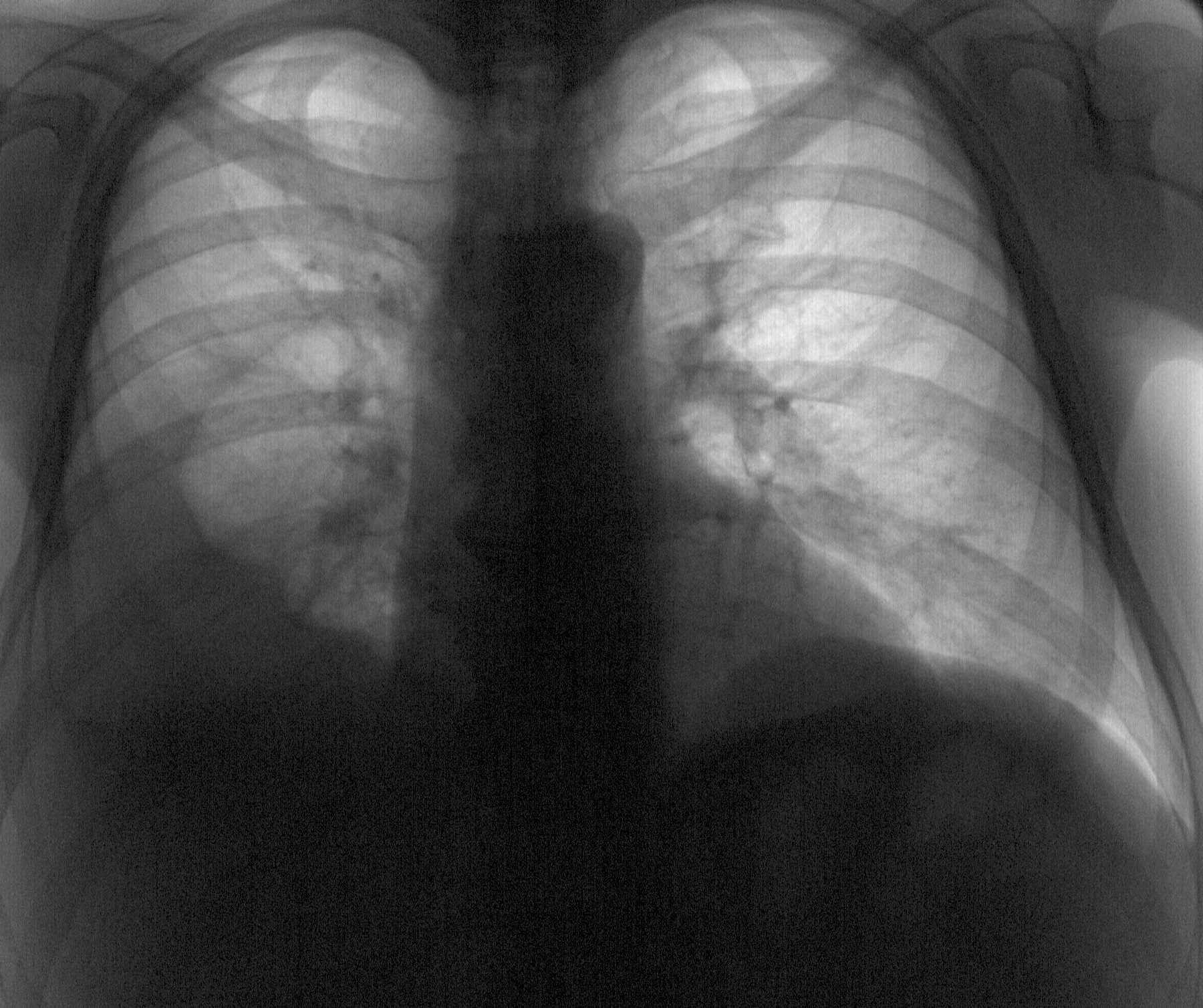 Причина такого состояния — это, как правило, сердечная недостаточность застойного типа, которая имеет самое разное происхождение. Сдавливающий перикардит, пороки сердца, различные поражения сердечной мышцы – все это вызывает застой и приводит, в результате, к скоплению транссудата. Также причиной гидроторакса могут стать заболевания, которые характеризуются значительной гипоптеинемией – некоторые поражения почек, заболевания печени. Ощущения больного при застое жидкости зависят от ее количества: немного транссудата практические не ощущается и не влияет на течение основного заболевания, а значительный объем жидкости в плевральной полости провоцирует расстройства кровообращения и дыхания.
Причина такого состояния — это, как правило, сердечная недостаточность застойного типа, которая имеет самое разное происхождение. Сдавливающий перикардит, пороки сердца, различные поражения сердечной мышцы – все это вызывает застой и приводит, в результате, к скоплению транссудата. Также причиной гидроторакса могут стать заболевания, которые характеризуются значительной гипоптеинемией – некоторые поражения почек, заболевания печени. Ощущения больного при застое жидкости зависят от ее количества: немного транссудата практические не ощущается и не влияет на течение основного заболевания, а значительный объем жидкости в плевральной полости провоцирует расстройства кровообращения и дыхания.
Симптомы гидроторакса
Симптомы гидроторакса – одышка, чувство тяжести в той половине груди, где скапливается жидкость (или в обеих половинах, если гидроторакс двусторонний). Больной старается занять положение, при котором верхняя часть туловища приподнята и наклонена в ту сторону, где накапливается транссудат.
Лечение гидроторакса
Лечение гидроторакса зависит от объема транссудата. Небольшое количество жидкости чаще всего резорбируется самостоятельно при излечении основного заболевания. Грамотные специалисты, принимающие пациентов в нашей клинике, объективно оценят необходимость аспирации жидкости и правильно осуществят ее. Мы приложим все усилия к тому, чтобы тщательно пролечить основное заболевание и предупредить повторное скопление жидкости.
Консультация и прием врача
Более подробную информацию Вы можете узнать по телефонам указанным на сайте или обратиться в наш Медицинский Центр. Мы работаем Без Выходных с 8.00 до 22.00 по адресу: г.Москва ВАО (Восточный Администривный Округ) Сиреневый Бульвар 32А
Гидроторакс.
 Клиническая картина и диагностика гидроторакса!
Клиническая картина и диагностика гидроторакса!1.Что такое гидроторакс
В отличие от экссудата, содержащего в своём составе значительное количество белков (до 30%) и ферментов, транссудат является более водянистой жидкостью. Он чаще всего прозрачен, почти не содержит свойственных плазме ферментов, а белка в нём обнаруживается не более 3%.
Накопление жидкости в плевральной полости в подавляющем большинстве случаев развивается как осложнением других заболеваний. Гидроторакс неясной этиологии – редкое явление, относимое, скорее, к погрешностям диагностики.
Хотя гидроторакс локализуется в лёгких, он чаще всего имеет симптоматику сердечнососудистых нарушений. Проблемы с дыханием самим больным ощущаются реже. Накопление жидкости происходит постепенно. На протяжении значительного периода жидкость пропотевает через сосудистые стенки капиллярной сети и наполняет плевральную полость.
Обязательно для ознакомления!
Помощь в госпитализации и лечении!
2.Причины гидроторакса
Этиопатогенетической причиной гидроторакса чаще всего выступает хроническая сердечнососудистая недостаточность, для которой характерны застойные явления в тканях и органах всего организма. К примеру, перикардит и серьёзные пороки сердца в большинстве случаев сопровождаются нарушениями, связанными с задержкой жидкости и капиллярной недостаточностью.
Одной из распространённых причин также являются заболевания почек. Нарушения в чашечно-лоханочном аппарате мочевыделительной системы приводят к гиперпротеинемии. Развивающаяся почечная недостаточность приводит к двустороннему гидротораксу при амилоидозе и на фоне нефротического синдрома.
Правосторонний гидроторакс характерен при циррозе печени. У 10 пациентов их ста, имеющих этот диагноз, жидкость из брюшины проникает в правую часть плевральной полости лёгких вследствие изменений, затрагивающих ткани диафрагмы в области печени.
Опухолевые заболевания органов средостения в ряде случаев также сопровождаются накоплением транссудата в лёгких.
Посетите нашу страницу
Пульмонология
3.
 Клиническая картина и диагностика гидроторакса
Клиническая картина и диагностика гидротораксаГидроторакс часто сочетается с признаками накопления жидкости в подкожно-жировой клетчатке и других полостях тела (перикардиальной, брюшной).
Транссудат в объёме 100-150 мл при малом гидротораксе не имеет выраженной клинической картины. Компрессия органов грудной клетки начинает проявляться лишь при большом скоплении лимфы в плевральной полости. Дебют этого состояния обычно не острый – симптоматика усугубляется постепенно.
Прогрессирующее течение гидроторакса характеризуется следующими нарастающими симптомами:
- одышка;
- тяжесть в области диафрагмы;
- неудовлетворённость вдохом и другие проявления затруднённого дыхания.
В дифференциальной диагностике гидроторакса важно исключить пневмоторакс, признаками которого является выраженный болевой синдром и проявления воспалительного характера (повышение температуры, общее недомогание, слабость).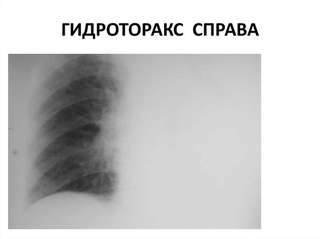
Визуальный осмотр может выявить акроцианоз кожных покровов (синюшность кожи) со стороны скопления транссудата. Больной, как правило, стремится принять вынужденную полусидячую позу. Осмотр проводится путём пальпации, перкуссии границ сердца и лёгочного звука. Также прибегают к их аускультации (анализу звуков сердечной деятельности и дыхания).
Для уточнения диагноза могут быть назначены следующие диагностические мероприятия:
- компьютерная томография;
- рентгеноскопия;
- ультразвуковая диагностика;
- плевральная пункция с целью последующего микробиологического и цитологического исследования.
Также показан общий и биохимический анализ крови и проведение пробы Ривальта, которая при наличии гидроторакса даёт отрицательный результат.
О нашей клинике
м. Чистые пруды
Страница Мединтерком!
4.
 Лечение гидроторакса
Лечение гидротораксаЛечение гидроторакса, исходя из того, что данная патология не является самостоятельной нозологической единицей, заключается в устранении первопричин, спровоцировавших скопление жидкости.
Если этиопатогенетически гидроторакс связан с сердечнососудистой недостаточностью, комплексная терапия включает не только препараты, поддерживающие работу сердца, но и сочетается с мерами, направленными на коррекцию образа жизни больного. Рекомендуется внести изменения в режим труда и отдыха, сон, диету, физическую активность. Для вывода жидкости необходимо ограничить приём поваренной соли. Из лекарственных препаратов могут быть назначены:
- гликозиды;
- ингибиторы фосфодиэстеразы;
- диуретики;
- ингибиторы АПФ;
- периферические вазодилататоры.
При связи гидроторакса с почечной недостаточностью отёчно-нефрофитовый синдром требует постельного режима, полного исключения соли в питании, контроля диуреза.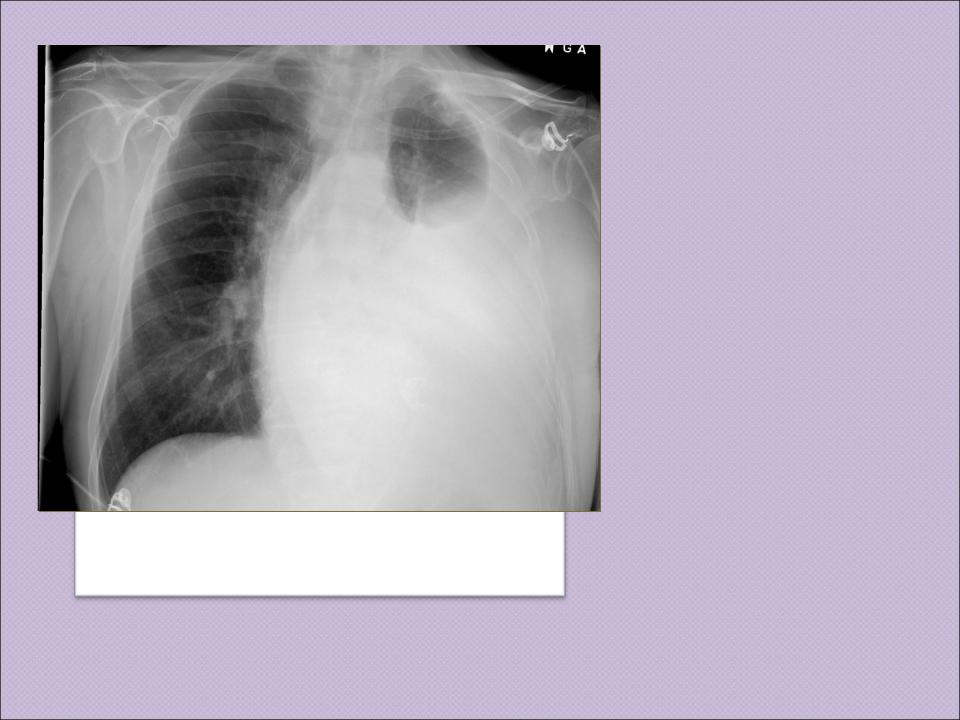 Лечебная тактика опирается на результаты диагностики – препараты назначаются в зависимости от первопричин и динамики заболевания почек.
Лечебная тактика опирается на результаты диагностики – препараты назначаются в зависимости от первопричин и динамики заболевания почек.
Оперативная помощь может потребоваться при неэффективности консервативного лечения, а также в случаях развития острых дыхательных расстройств и сердечнососудистой недостаточности.
Гидроторакс — Медицинская энциклопедия
I
Гидроторакс (hydrothorax; греч. hydōr вода + thōrax грудь: синоним грудная водянка)
скопление жидкости невоспалительного происхождения (транссудата) в плевральных полостях. Может возникать при сердечной недостаточности, сопровождающейся застоем крови в малом круге кровообращения; заболеваниях почек, особенно с формированием нефротического синдрома; циррозах печени; асците различного генеза; синдроме нарушенного всасывания; алиментарной дистрофии; перитонеальном диализе; при опухолях средостения.
Основным механизмом накопления жидкости в плевральных полостях при сердечной недостаточности является повышение гидростатического давления в большом и малом кругах кровообращения. Формирование Г. при болезнях почек, синдроме нарушенного всасывания, алиментарной дистрофии обусловлено снижением онкотического давления плазмы крови в результате гипоальбуминемии. Развитие Г. при асците и перитонеальном диализе связано с непосредственным поступлением жидкости из брюшной полости в плевральную через поры в диафрагме в результате повышения внутрибрюшного давления. При циррозах печени Г. может быть обусловлен как гипоальбуминемией, так и проникновением асцитической жидкости из брюшной полости в плевральную. Г. при опухолях средостения возникает вследствие местного нарушения оттока крови и лимфы.
Формирование Г. при болезнях почек, синдроме нарушенного всасывания, алиментарной дистрофии обусловлено снижением онкотического давления плазмы крови в результате гипоальбуминемии. Развитие Г. при асците и перитонеальном диализе связано с непосредственным поступлением жидкости из брюшной полости в плевральную через поры в диафрагме в результате повышения внутрибрюшного давления. При циррозах печени Г. может быть обусловлен как гипоальбуминемией, так и проникновением асцитической жидкости из брюшной полости в плевральную. Г. при опухолях средостения возникает вследствие местного нарушения оттока крови и лимфы.
Клиническая картина Г. определяется объемом жидкости в плевральных полостях и симптомами заболевания, послужившего его причиной. В большинстве случаев Г. бывает двусторонним. Объем плеврального выпота может быть незначительным или массивным, достигая нескольких литров. Значительное накопление жидкости в плевральных полостях сопровождается появлением симптомов дыхательной недостаточности (Дыхательная недостаточность) — одышки, цианоза.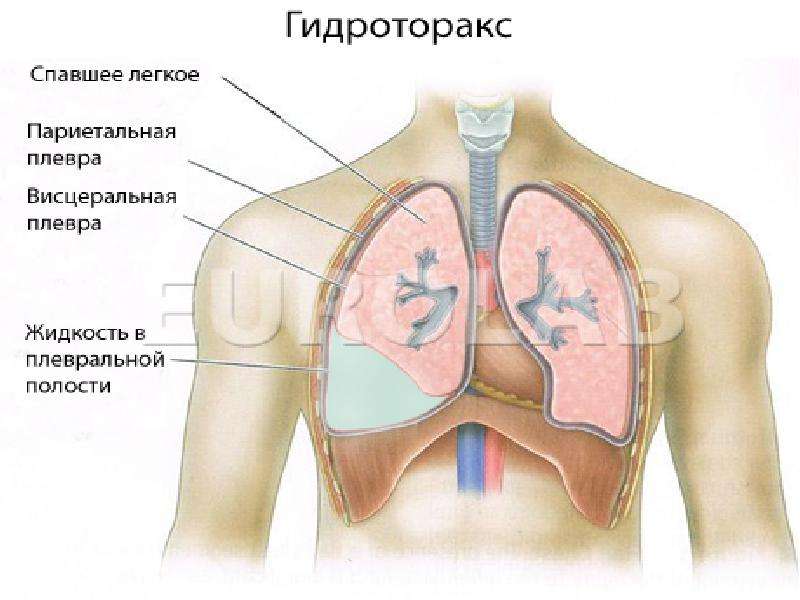 Лихорадка, боли в грудной клетке не характерны. Г. нередко сочетается с периферическими отеками, анасаркой (распространенным отеком подкожной клетчатки), гидроперикардом. У больных обычно выявляются тяжелые болезни сердца, почек, печени и другие патологические состояния, послужившие причиной развития гидроторакса.
Лихорадка, боли в грудной клетке не характерны. Г. нередко сочетается с периферическими отеками, анасаркой (распространенным отеком подкожной клетчатки), гидроперикардом. У больных обычно выявляются тяжелые болезни сердца, почек, печени и другие патологические состояния, послужившие причиной развития гидроторакса.
При физикальном исследовании над зоной накопления жидкости удается выявить ослабление или отсутствие голосового дрожания; приглушенный или тупой перкуторный звук с косой верхней границей; отсутствие дыхательных шумов. Важным диагностическим признаком плеврального выпота является смещение перкуторной границы тупости при изменении положения больного.
Рентгенологическое исследование позволяет обнаружить гомогенную тень жидкости с верхней границей, смещающейся при наклоне тела. Обязательным условием правильного распознавания плеврального выпота является рентгенологическое исследование в латеропозиции. С помощью ультразвукового метода можно выявить даже небольшое количество жидкости в плевральной полости и выбрать место для плевральной пункции.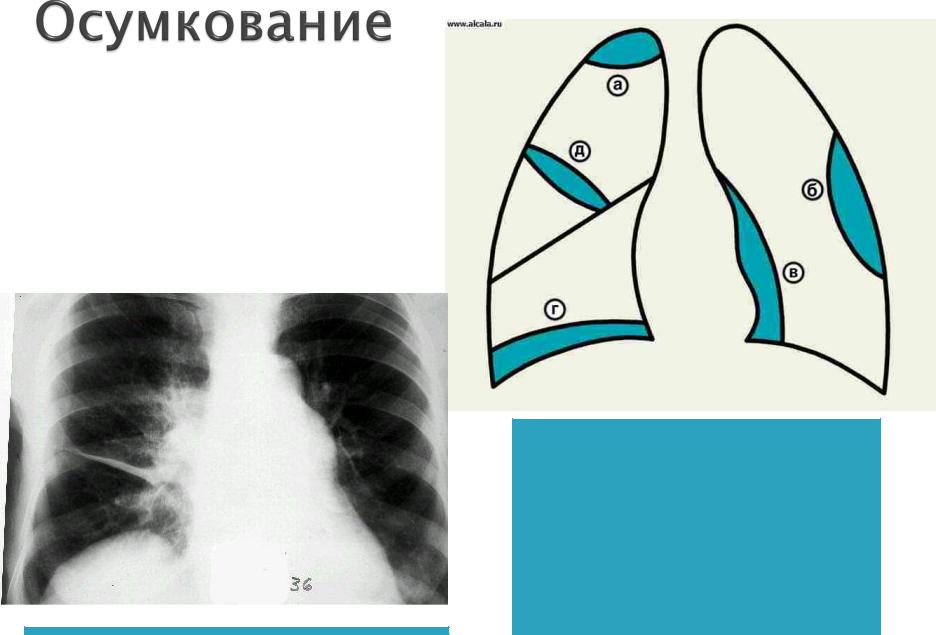 Плевральная пункция позволяет уточнить характер плеврального выпота и провести дифференциальный диагноз с плевритом, Гемотораксом, хилотораксом (см. Грудной проток). Транссудат в отличие от экссудата, накапливающегося в плевральной полости при плеврите, представляет собой прозрачную жидкость соломенно-желтого цвета, иногда геморрагического характера, не имеющую запаха, с щелочной реакцией. Количество белка в нем не превышает 30 г/л, удельный вес обычно колеблется от 1,006 до 1,012. Содержание фибриногена скудное. После центрифугирования при микроскопии осадка обнаруживают клетки эндотелия (мезотелия), небольшое количество лейкоцитов — менее 1000 в 1 мкл. При гемотораксе во время плевральной пункции получают кровь, при хилотораксе — лимфу.
Плевральная пункция позволяет уточнить характер плеврального выпота и провести дифференциальный диагноз с плевритом, Гемотораксом, хилотораксом (см. Грудной проток). Транссудат в отличие от экссудата, накапливающегося в плевральной полости при плеврите, представляет собой прозрачную жидкость соломенно-желтого цвета, иногда геморрагического характера, не имеющую запаха, с щелочной реакцией. Количество белка в нем не превышает 30 г/л, удельный вес обычно колеблется от 1,006 до 1,012. Содержание фибриногена скудное. После центрифугирования при микроскопии осадка обнаруживают клетки эндотелия (мезотелия), небольшое количество лейкоцитов — менее 1000 в 1 мкл. При гемотораксе во время плевральной пункции получают кровь, при хилотораксе — лимфу.
Лечение направлено на устранение причины гидроторакса. При массивном Г., сопровождающемся дыхательной недостаточностью, показано медленное удаление содержимого плевральной полости во время плевральной пункции.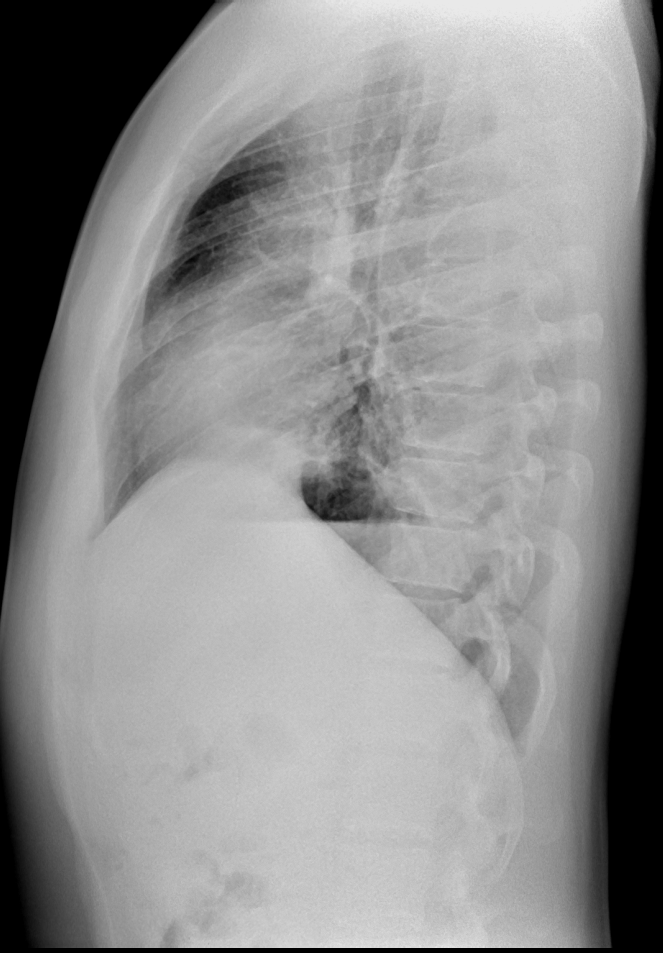
Библиогр.: лайт Р.У. Болезни плевры, пер. с англ., с. 111, М., 1986; Справочник по пульмонологии, под. ред. Н.В. Путова и др., с. 61, Л., 1987.
II
Гидроторакс (hydrothorax; гидро- (Гидр-) + греч. thōrax грудь, грудная клетка; син. водянка грудная)
скопление транссудата в плевральной полости.
Источник: Медицинская энциклопедия на Gufo.me
Значения в других словарях
- гидроторакс — Гидр/о/то́ракс/. Морфемно-орфографический словарь
- гидроторакс —
гидроторакс м. Скопление жидкости в полости плевры, возникающее при легочных и сердечных заболеваниях.
 Толковый словарь Ефремовой
Толковый словарь Ефремовой - гидроторакс — ГИДРОТОРАКС (Hydrothorax), грудная водянка, скопление транссудата между листками плевры в грудной полости. Г. — явление вторичное, возникающее при мн. болезнях, чаще при хронич. Ветеринарный энциклопедический словарь
- гидроторакс — орф. гидроторакс, -а Орфографический словарь Лопатина
- гидроторакс — См. гидра Толковый словарь Даля
- Гидроторакс —
(от Гидро.
 .. и греч. thorax — грудь) скопление выпота (Транссудата) в плевральной полости, возникающее при различных сердечных и почечных заболеваниях. Г. проявляется ослабленным дыханием, одышкой, редко — болью. Лечение — устранение основного заболевания.
Большая советская энциклопедия
.. и греч. thorax — грудь) скопление выпота (Транссудата) в плевральной полости, возникающее при различных сердечных и почечных заболеваниях. Г. проявляется ослабленным дыханием, одышкой, редко — болью. Лечение — устранение основного заболевания.
Большая советская энциклопедия - гидроторакс — Гидроторакс, гидротораксы, гидроторакса, гидротораксов, гидротораксу, гидротораксам, гидроторакс, гидротораксы, гидротораксом, гидротораксами, гидротораксе, гидротораксах Грамматический словарь Зализняка
- гидроторакс — сущ., кол-во синонимов: 2 болезнь 995 водянка 41 Словарь синонимов русского языка
SARS-CoV-2-ассоциированная пневмония
Фото носит иллюстративный характер. Из открытых источников
Из открытых источников
Манифестация болезни
Пациент В., мужчина, 52 года, без сопутствующей патологии. Заболел остро: недомогание, озноб, повышение температуры до 38,5 °С, покашливание. В течение трех дней лихорадка до 38,5 °С, беспокоили сухой болезненный кашель, миалгии, артралгии. В связи с отсутствием улучшения самочувствия обратился к терапевту. Выполнены общеклинический анализ крови, биохимический анализ крови, рентгенография органов грудной клетки, ЭКГ. По результатам обследования выставлен диагноз: внебольничная пневмония в нижней доле справа, ДН0-1, среднетяжелое течение. Рекомендованы антибиотики (амоксициллин/клавуланат 1 000 мг каждые 12 ч внутрь, кларитромицин 500 мг каждые 12 ч внутрь), назначены муколитическая терапия, НПВС.
В последующие дни продолжал лихорадить до фебрильных значений, отмечал некоторое уменьшение сухого кашля. Через 2 дня после обращения в поликлинику в связи с сохранением температуры и кашля на фоне проводимого лечения вызвал скорую медицинскую помощь.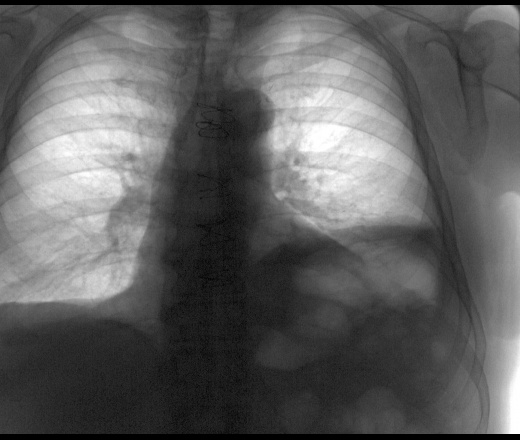 Бригадой СМП собран детальный эпидемиологический анамнез пациента, в том числе информация о выездах за пределы страны в течение последнего месяца. Выяснилось, что за неделю до начала заболевания пациент в течение 5 дней находился в Германии. В связи с подозрением на SARS-CoV-2- ассоциированную пневмонию доставлен в Городскую клиническую инфекционную больницу Минска. Госпитализирован в боксированное инфекционное отделение.
Бригадой СМП собран детальный эпидемиологический анамнез пациента, в том числе информация о выездах за пределы страны в течение последнего месяца. Выяснилось, что за неделю до начала заболевания пациент в течение 5 дней находился в Германии. В связи с подозрением на SARS-CoV-2- ассоциированную пневмонию доставлен в Городскую клиническую инфекционную больницу Минска. Госпитализирован в боксированное инфекционное отделение.
Госпитализация
При поступлении в ГКИБ предъявлял жалобы на повышение температуры до 39,5 °С, общую слабость, потливость, сухой кашель. Общее состояние средней тяжести. Температура при осмотре 38,5 °С. Ориентирован всесторонне, на вопросы отвечает по существу, команды выполняет. Менингеальных знаков, очаговой неврологической симптоматики, координаторных нарушений нет. Кожные покровы бледно-розовые, без сыпи. Зев гиперемирован, налетов на миндалинах нет. В легких дыхание везикулярное, ослаблено в нижних отделах с обеих сторон, ниже угла лопатки справа — фокус мелкопузырчатых хрипов, ЧД 20 в минуту, SpO2 96–97 % без вспомогательной респираторной поддержки кислородом.
Ритм сердца правильный, тоны ясные, ЧСС 60 в минуту. Язык сухой, обложен на спинке грязно-серым налетом. Печень, селезенка не увеличены. Живот пальпаторно мягкий, безболезненный, доступен для глубокой пальпации во всех отделах.
Перитонеальные симптомы отрицательные. Стул один раз в сутки, оформленный, без патологических примесей.
Мочеиспуcкание свободное, безболезненное. Диурез, со слов, достаточный.
На следующий день появилась речевая одышка до 22–24 в минуту, сатурация кислорода периферической крови снизилась до 92–94 % при дыхании атмосферным воздухом.
Пациент переведен в ОРИТ для обеспечения вспомогательной респираторной поддержки кислородом.
Пребывание в отделении интенсивной терапии и реанимации CоViD-19 подтвержден методом ПЦР респираторных смывов из носо- и ротоглотки на РНК SARS-CoV-2. Выставлен диагноз: внебольничная двусторонняя первично-вирусная полисегментарная пневмония, вызванная SARS-CoV-2, тяжелое течение, ДН 1.
Клиническая динамика: в последующие 7 дней от начала госпитализации у пациента сохранялась лихорадка
до 38,0–39,5 °С, малопродуктивный кашель с небольшим количеством трудно отделяемой мокроты, слабость, головокружение при попытке быстро изменить положение тела на вертикальное.
При объективном осмотре дыхание в легких везикулярное, с мелкопузырчатыми хрипами в нижних отделах с обеих сторон, частота дыхания 18–20 в минуту, до 22 в минуту при речевой нагрузке, SpO2
92– 94 % без вспомогательной респираторной поддержки, до 98–99 % при респираторной поддержке интраназальным кислородом с потоком 3,0–5,0 л/минуту. Постепенно лихорадочно-интоксикационный синдром, явления дыхательной недостаточности разрешились, и пациент после 12 дней пребывания в ОРИТ переведен в боксированное инфекционное отделение.
Рентгенологические данные
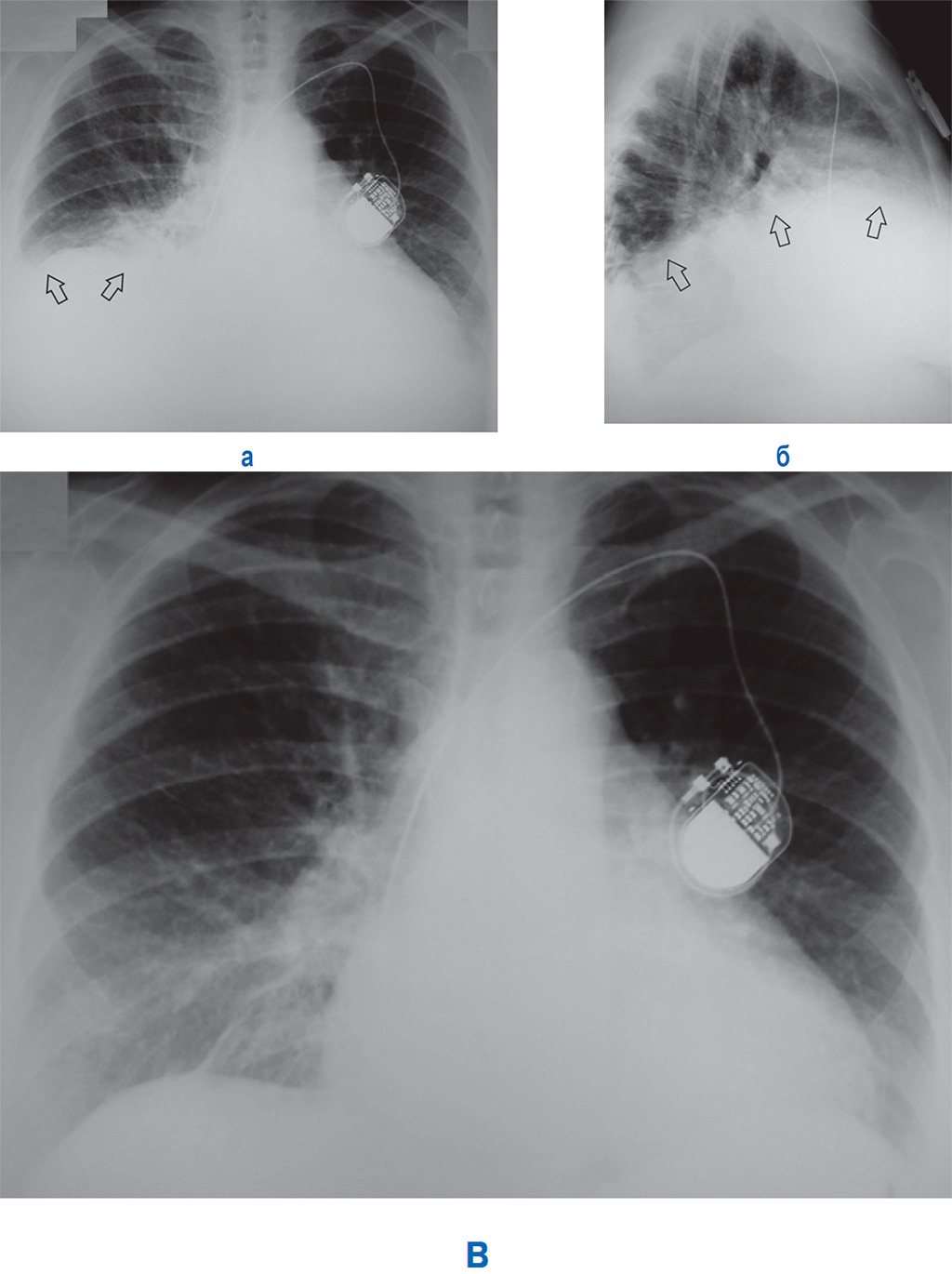
Р-графия ОГК от 10.03.2020. Легкие расправлены. В проекции средней, нижней долей правого легкого определяется массивная инфильтрация по типу матового стекла. В среднем легочном поле левого легкого локально обогащен легочной рисунок. Правый корень расширен. Купола диафрагмы четкие, ровные. Синусы свободны. Средостение не расширено, не смещено. Заключение: Р-картина правосторонней полисегментарной пневмонии (интерстициальная?) с отрицательной динамикой от 07.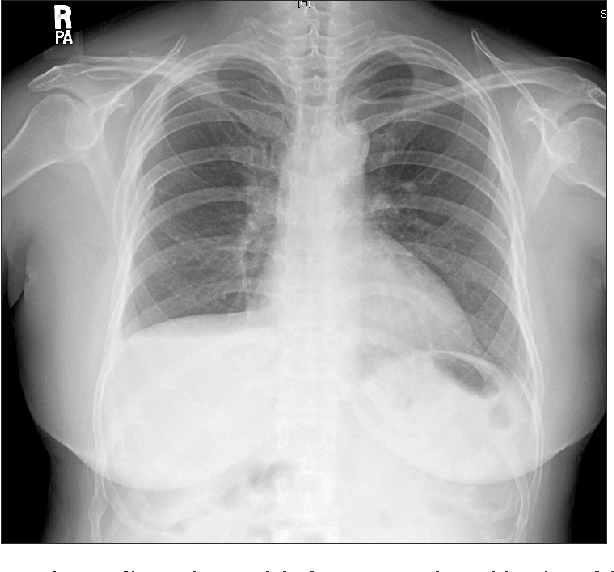 03.2020. Левосторонняя нижнедолевая пневмония?
03.2020. Левосторонняя нижнедолевая пневмония?
Р-графия ОГК от 12.03.2020. Легкие расправлены. Определяется выраженная отрицательная динамика изменений в обоих легких. Инфильтрация увеличилась в размерах, в правом легком определяется субтотально, в левом — в среднем легочном поле, а также в латеральных отделах. Корни расширены, неструктурны. Купола диафрагмы четкие, ровные. Синусы свободны. Средостение не расширено, не смещено. Тень ЦВК определяется в проекции устья верхней полой вены. Заключение: Р-картина двусторонней пневмонии. Респираторный дистресс-синдром?
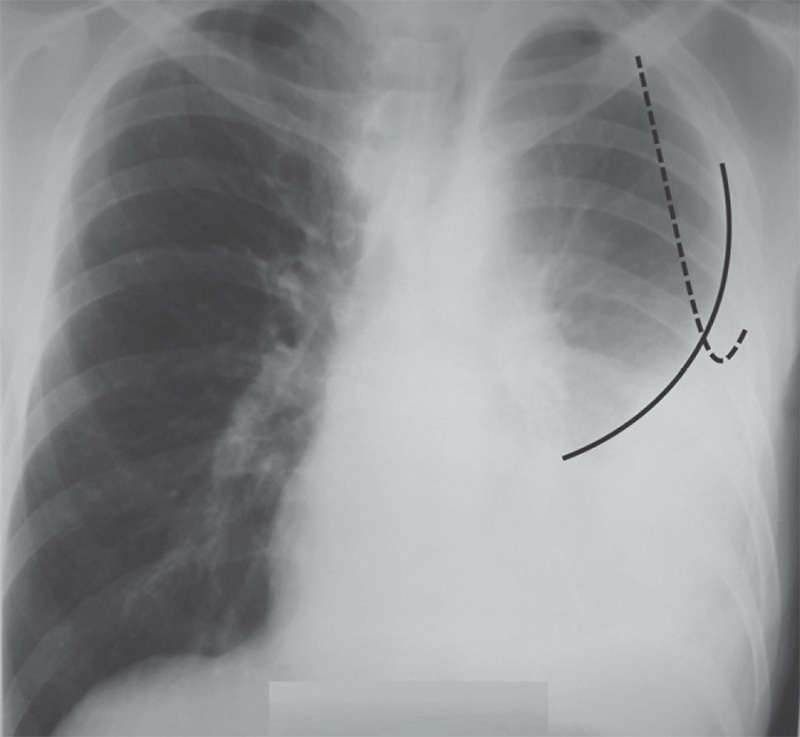
Р-графия ОГК от 18.03.2020. Легкие расправлены. Сохраняется инфильтрация в обоих легких без существенной динамики в правом легком, с отрицательной динамикой в левом легком. Корни расширены. Купола диафрагмы четкие, ровные.
Синусы свободны. Средостение не расширено, не смещено. Заключение: Р-картина двусторонней пневмонии с положительной динамикой от 12.03.2020.
Р-графия ОГК от 23.03.2020. Легкие расправлены. Пневматизация легких повысилась, инфильтрация уменьшилась в размерах и интенсивности (более выражена положительная динамика в правом легком). Корни не расширены. Купола диафрагмы четкие, ровные. Синусы свободны. Средостение не расширено, не смещено. Заключение: Р-картина двусторонней пневмонии с положительной динамикой от 18.03.2020.
КТ ОГК от 18.03.2020. По всем легочным полям на фоне усиления рисунка определяются сливные участки интерстициальной инфильтрации с утолщением внутридольковых и междольковых перегородок, с неровными нечеткими контурами. Бронхи 1–3-го порядка проходимы. Трахея без особенностей. Лимфоузлы не увеличены. Плевральные полости: жидкость по дорсальным поверхностям с обеих сторон до 10 мм. Жидкость в полости перикарда до 4,5 мм.
Заключение: КТ-картина двустороннего интерстициального воспалительного процесса в легких. Двусторонний малый гидроторакс, гидроперикард.
Терапия
В течение 7 дней в реанимационном отделении пациент получал потенциально эффективное в отношении SARS-CoV-2 лекарственное средство гидроксихлорохин 400 мг/сут перорально, антибактериальную терапию: эртапенем 1,0 г каждые 24 ч внутривенно капельно + левофлоксацин 750 мг каждые 24 ч внутривенно капельно, муколитики, жаропонижающие, инфузионную терапию кристаллоидными растворами.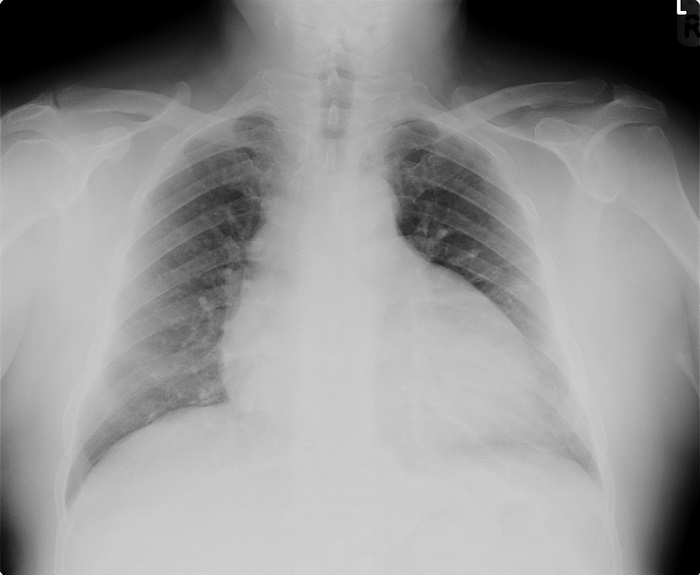
Повторный тест ПЦР респираторных смывов из рото- и носоглотки на РНК SARS-CoV-2 на 10-й день госпитализации оставался положительным. На 16-й день результат ПЦР стал отрицательным, однако на 21-й и 24-й дни вновь положительным. Учитывая существующие критерии выписки лиц с подтвержденной CоViD-19 инфекцией, пациент был выписан из стационара только на 30-й день госпитализации после получения двух отрицательных результатов ПЦР на РНК SARS-CoV-2 на 28-й и 29-й дни, взятых с интервалом в 24 часа, и клиническим выздоровлением.
Общие выводы
Описанный нами клинический случай является вполне типичным для CoViD-19, если проанализировать многочисленные опубликованные данные, и заставляет сделать ряд выводов.
- Учитывая распространение инфекции CоViD-19 в мире в период заболевания пациента, крайне важно было уточнить эпидемиологический анамнез (выезд в регионы с высокой распространенностью коронавирусной инфекции, контакт с лицами, прибывшими из других стран, и т.
 д.) при наличии респираторной симптоматики. Это не было сделано при первом контакте врача-терапевта с пациентом, что послужило причиной его отсроченной госпитализации и, соответственно, расширило перечень контактных с ним лиц. В настоящее время, учитывая локальную трансмиссию CоViD-19 на территории Беларуси, любая респираторная инфекция, особенно с развитием интерстициальной пневмонии, двусторонней полисегментарной пневмонии, пневмонии, требующей госпитализации в реанимационные отделения, должна рассматриваться как вероятная инфекция CoViD-19 с соответствующим лабораторным обследованием пациентов.
д.) при наличии респираторной симптоматики. Это не было сделано при первом контакте врача-терапевта с пациентом, что послужило причиной его отсроченной госпитализации и, соответственно, расширило перечень контактных с ним лиц. В настоящее время, учитывая локальную трансмиссию CоViD-19 на территории Беларуси, любая респираторная инфекция, особенно с развитием интерстициальной пневмонии, двусторонней полисегментарной пневмонии, пневмонии, требующей госпитализации в реанимационные отделения, должна рассматриваться как вероятная инфекция CoViD-19 с соответствующим лабораторным обследованием пациентов. - Следует обратить внимание на быстрое развитие отрицательной динамики с нарастанием дыхательной недостаточности, несмотря на кажущееся одностороннее поражение легких по данным рентгенограммы органов грудной клетки на момент госпитализации пациента и объективных аускультативных данных. При CoViD-19-ассоциированной пневмонии превалирует поражение интерстиция легких, которое плохо визуализируется на рентгенограмме, соответственно, клинически может быть картина выраженной дыхательной недостаточности при минимальных патологических отклонениях на снимке.
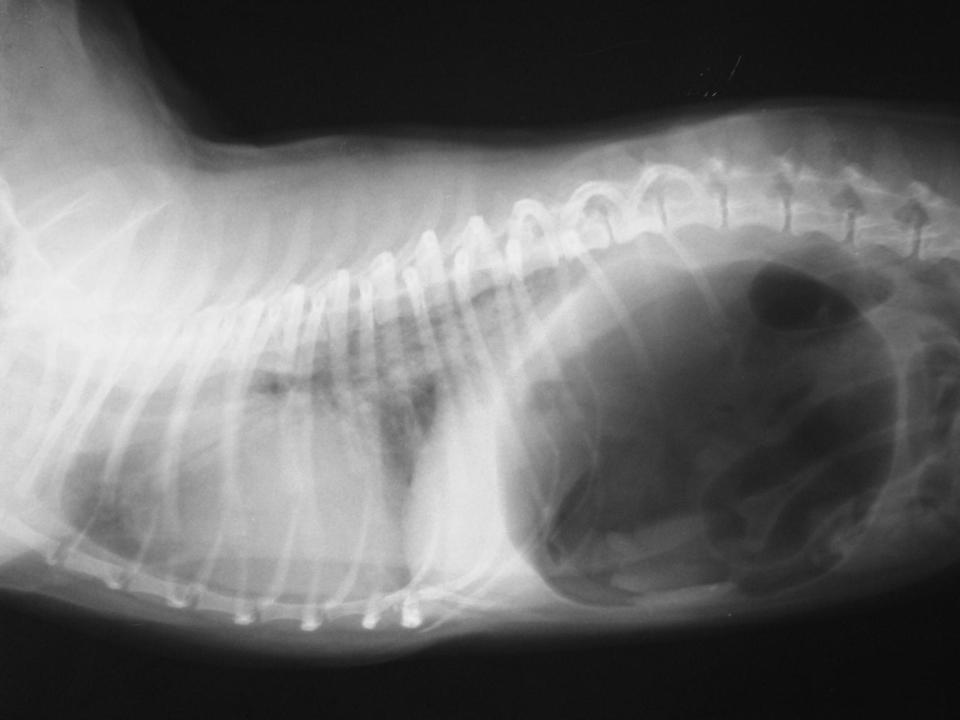 Гораздо более информативным методом диагностики является компьютерная томография органов грудной клетки. Она полноценно визуализирует вирусный воспалительный процесс в легких, однако не всегда доступна в некоторых учреждениях здравоохранения, в том числе ГКИБ (для выполнения данного исследования пациент после стабилизации состояния с соблюдением мер инфекционной безопасности транспортировался в другой стационар). Известно, что отклонения при КТ органов грудной клетки выявляется практически у 100 % пациентов, у 98 % в виде двустороннего поражения (Huang C. et al., 2020). У пациентов в критическом состоянии типичны билатеральные мультилобальные и субсегментарные зоны консолидации легочной ткани, у менее тяжелых — изменения легочной ткани по типу матового стекла и субсегментарные зоны консолидации. Хорошей альтернативой КТ для ранней диагностики инфекции служит УЗИ легких.
Гораздо более информативным методом диагностики является компьютерная томография органов грудной клетки. Она полноценно визуализирует вирусный воспалительный процесс в легких, однако не всегда доступна в некоторых учреждениях здравоохранения, в том числе ГКИБ (для выполнения данного исследования пациент после стабилизации состояния с соблюдением мер инфекционной безопасности транспортировался в другой стационар). Известно, что отклонения при КТ органов грудной клетки выявляется практически у 100 % пациентов, у 98 % в виде двустороннего поражения (Huang C. et al., 2020). У пациентов в критическом состоянии типичны билатеральные мультилобальные и субсегментарные зоны консолидации легочной ткани, у менее тяжелых — изменения легочной ткани по типу матового стекла и субсегментарные зоны консолидации. Хорошей альтернативой КТ для ранней диагностики инфекции служит УЗИ легких. - У большинства пациентов с CoViD-19 клинически характерно сочетание лихорадки до фебрильных значений, проявлений интоксикационного синдрома (слабость, миалгии, головная боль), сухого кашля и одышки.
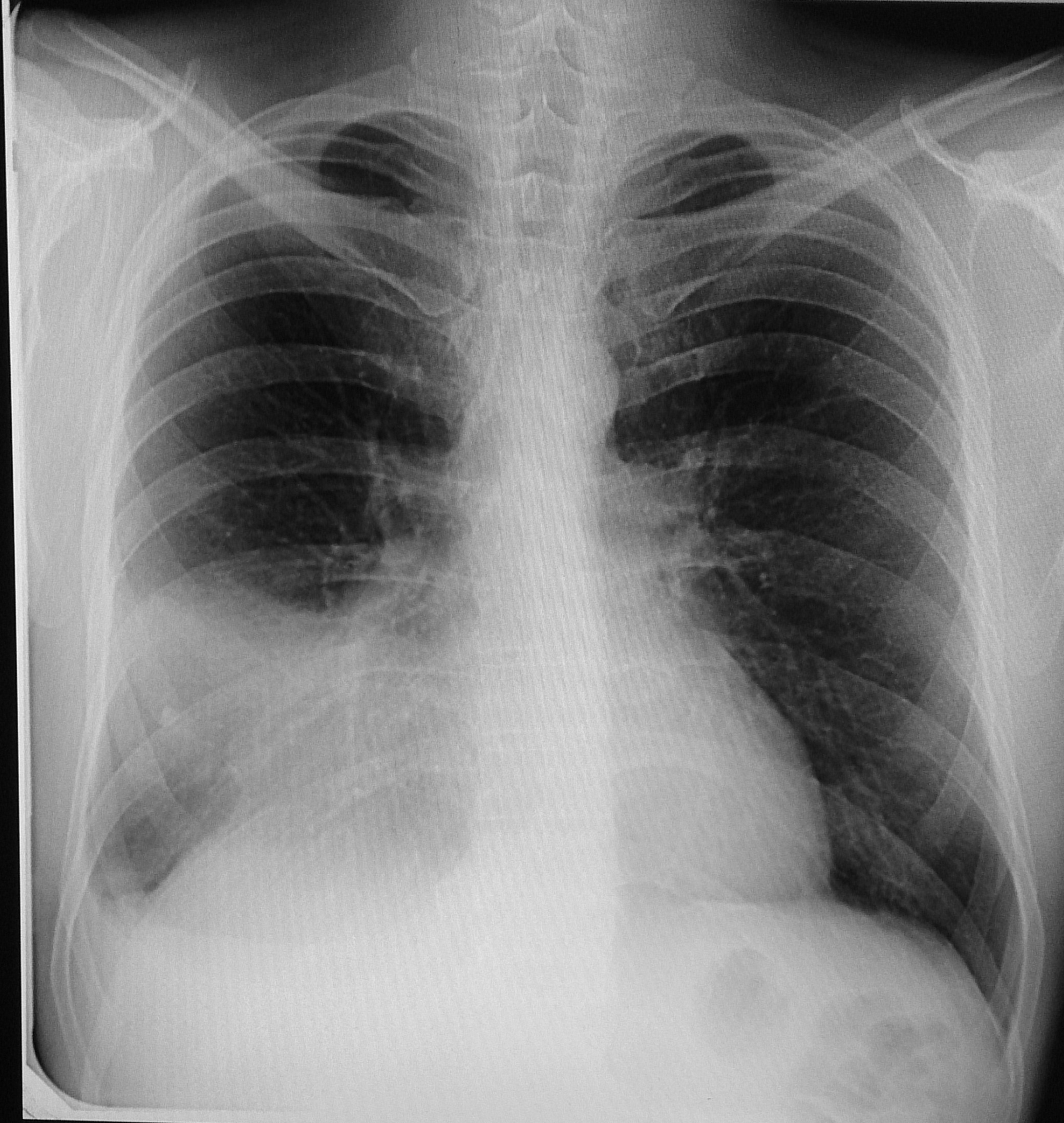 В описании 41 случая CoViD-19 из КНР лихорадка отмечалась у 98 %, кашель у 76 %, миалгии у 44 %, одышка у 55 % пациентов (Huang C. et al., 2020). Все вышеуказанные симптомы имелись и у нашего пациента. Однако впоследствии было показано, что лихорадка и другие проявления CoViD-19 могут встречаться в меньшем проценте случаев. Так, согласно мета-анализу 10 исследований, лихорадка отмечалась в 89,1 % (95 %, ДИ 81,8–94,5 %) подтвержденных случаев коронавирусной инфекции, кашель — только в 72,2 % (95 %, ДИ 65,7–78,2 %) (Sun P. et al., 2020). Учитывая, что у части пациентов инфицирование возбудителем может вовсе не сопровождаться клиническими проявлениями или они будут стертыми, следует сохранять настороженность при осмотре пациентов с отягощенным эпидемиологическим анамнезом и даже минимальной респираторной симптоматикой.
В описании 41 случая CoViD-19 из КНР лихорадка отмечалась у 98 %, кашель у 76 %, миалгии у 44 %, одышка у 55 % пациентов (Huang C. et al., 2020). Все вышеуказанные симптомы имелись и у нашего пациента. Однако впоследствии было показано, что лихорадка и другие проявления CoViD-19 могут встречаться в меньшем проценте случаев. Так, согласно мета-анализу 10 исследований, лихорадка отмечалась в 89,1 % (95 %, ДИ 81,8–94,5 %) подтвержденных случаев коронавирусной инфекции, кашель — только в 72,2 % (95 %, ДИ 65,7–78,2 %) (Sun P. et al., 2020). Учитывая, что у части пациентов инфицирование возбудителем может вовсе не сопровождаться клиническими проявлениями или они будут стертыми, следует сохранять настороженность при осмотре пациентов с отягощенным эпидемиологическим анамнезом и даже минимальной респираторной симптоматикой. - Описан ряд лабораторных отклонений в общеклиническом и биохимическом анализе крови при CoViD-19: лейкопения и лимфопения, тромбоцитопения, повышение уровня трансаминаз, лактатдегидрогеназы, креатинфосфокиназы, D-димеров, повышение С-реактивного белка при нормальных значениях прокальцитонина.
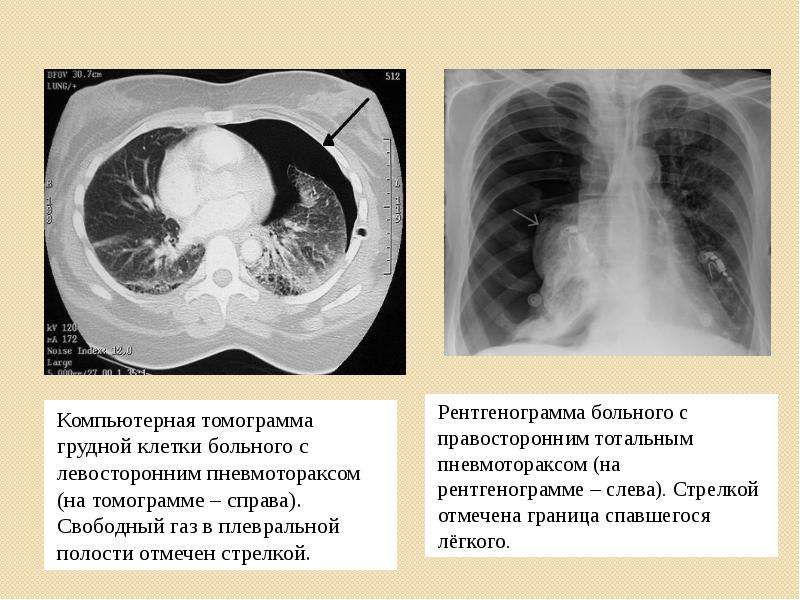 У нашего пациента имелся нормальный и повышенный уровень лейкоцитов при явной лимфопении (4–11 %) в первую неделю заболевания, нормальный уровень тромбоцитов, выраженное повышение уровней креатинфосфокиназы и лактатдегидрогеназы, высокие значения С-реактивного белка при стойко нормальном уровне прокальцитонина. Прокальцитонин является высокоспецифичным маркером бактериальной инфекции и может быть использован для дифференциации между первично-вирусной и вирусно-бактериальной, вторично-бактериальной пневмониями, а также для ранней диагностики бактериальных инфекций, связанных с оказанием медицинской помощи. Стойко сохраняющаяся лимфопения и высокий/ нарастающий уровень D-димеров могут являться прогностически неблагоприятными маркерами CoViD-19 и должны настораживать клинициста в плане более агрессивной тактики ведения пациентов.
У нашего пациента имелся нормальный и повышенный уровень лейкоцитов при явной лимфопении (4–11 %) в первую неделю заболевания, нормальный уровень тромбоцитов, выраженное повышение уровней креатинфосфокиназы и лактатдегидрогеназы, высокие значения С-реактивного белка при стойко нормальном уровне прокальцитонина. Прокальцитонин является высокоспецифичным маркером бактериальной инфекции и может быть использован для дифференциации между первично-вирусной и вирусно-бактериальной, вторично-бактериальной пневмониями, а также для ранней диагностики бактериальных инфекций, связанных с оказанием медицинской помощи. Стойко сохраняющаяся лимфопения и высокий/ нарастающий уровень D-димеров могут являться прогностически неблагоприятными маркерами CoViD-19 и должны настораживать клинициста в плане более агрессивной тактики ведения пациентов. - Несмотря на отрицательную динамику по данным рентгенографии органов грудной клетки в первую неделю заболевания, пациент оставался относительно стабильным, не требовал увеличения респираторной поддержки, не имел существенных отклонений в кислотно-щелочном анализе крови, клинически постепенно демонстрировал улучшение состояния.
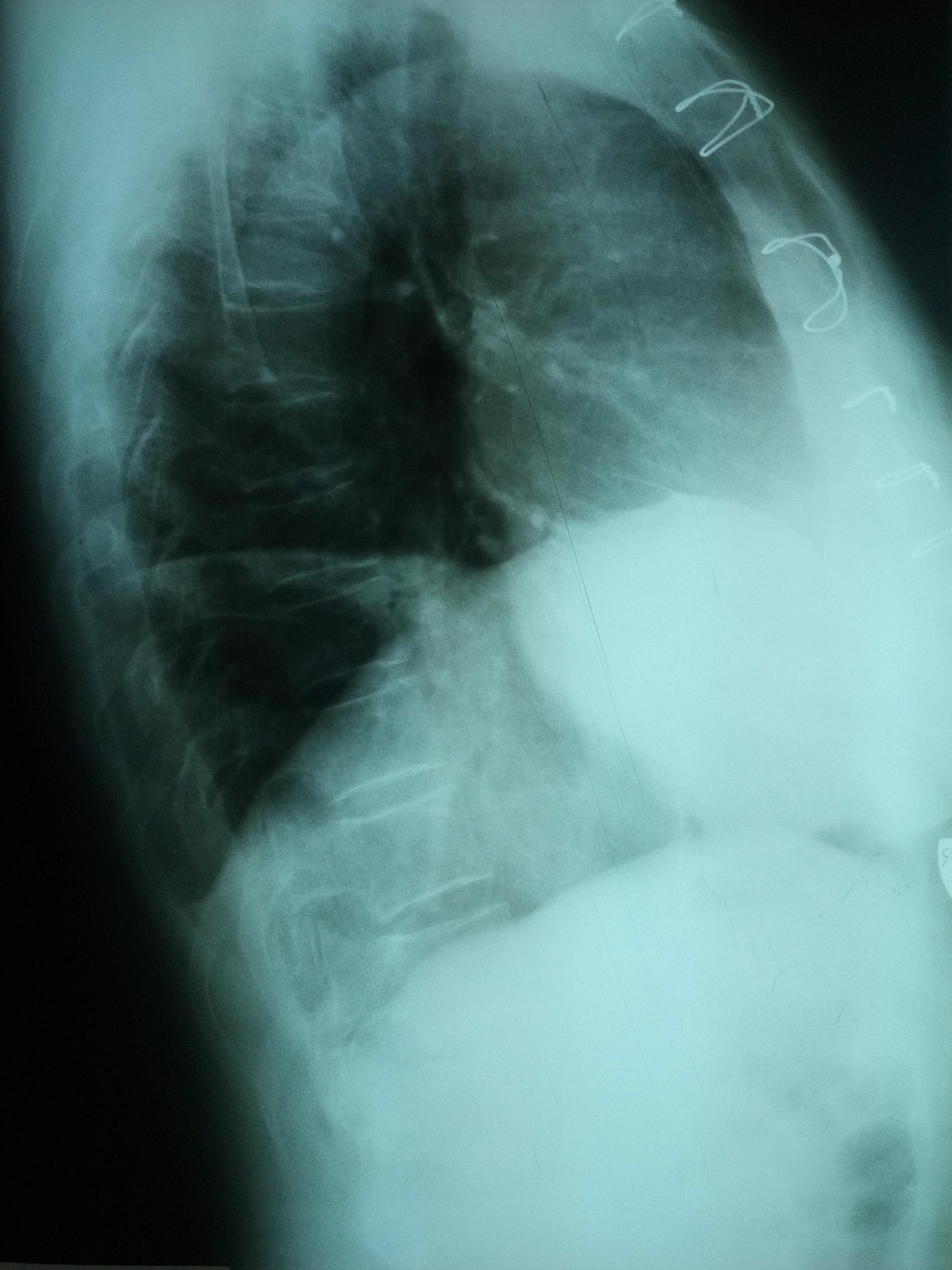 Следовательно, возможен диссонанс между визуализируемыми патологическими отклонениями на рентгенограммах и клиническими проявлениями заболевания. Данный случай в очередной раз показывает первичность клиники над параклиническими методами исследования. В настоящий момент в арсенале авторов уже до двух десятков примеров явного диссонанса между выраженными изменениями на рентгенограммах и минимальными клиническими проявлениями у пациентов с верифицированной CoViD-19 инфекцией.
Следовательно, возможен диссонанс между визуализируемыми патологическими отклонениями на рентгенограммах и клиническими проявлениями заболевания. Данный случай в очередной раз показывает первичность клиники над параклиническими методами исследования. В настоящий момент в арсенале авторов уже до двух десятков примеров явного диссонанса между выраженными изменениями на рентгенограммах и минимальными клиническими проявлениями у пациентов с верифицированной CoViD-19 инфекцией. - Исследование методом ПЦР респираторных смывов на РНК SARS-CoV-2 продемонстрировало отрицательный результат на 16-й день госпитализации, однако на 21-й и 24-й дни результат тестов вновь стал положительным. Данный сценарий может быть достаточно распространенным в клинической практике и уже описан коллегами из других стран. Так, у 4 медицинских работников с подтвержденным CoViD-19, у которых на момент выздоровления отмечалось 2 отрицательных результата ПЦР с интервалом забора материала не менее 24 ч, впоследствии через 5–13 дней повторные результаты ПЦР были вновь положительными (Lan et al.
 , 2020). Пациенты не имели каких-либо признаков заболевания и патологических отклонений по данным КТ ОГК. При этом ни один из членов семьи, контактировавших с ними после реконвалесценции, не развил инфекцию. Возможно, это связано с длительной персистенцией генетического материала нежизнеспособного возбудителя в респираторном эпителии. Также описаны случаи длительной детекции РНК SARS-CoV-2 в мокроте (вплоть до 39 дней от момента заболевания) даже при неопределяемой РНК возбудителя в ротоглоточных смывах (Chen et al., 2020). Возможную контагиозность пациентов с длительно детектируемой РНК вируса в респираторных образцах, а также надежные критерии выписки реконвалесцентов еще предстоит определить.
, 2020). Пациенты не имели каких-либо признаков заболевания и патологических отклонений по данным КТ ОГК. При этом ни один из членов семьи, контактировавших с ними после реконвалесценции, не развил инфекцию. Возможно, это связано с длительной персистенцией генетического материала нежизнеспособного возбудителя в респираторном эпителии. Также описаны случаи длительной детекции РНК SARS-CoV-2 в мокроте (вплоть до 39 дней от момента заболевания) даже при неопределяемой РНК возбудителя в ротоглоточных смывах (Chen et al., 2020). Возможную контагиозность пациентов с длительно детектируемой РНК вируса в респираторных образцах, а также надежные критерии выписки реконвалесцентов еще предстоит определить. - Пациенту назначено лекарственное средство гидроксихлорохин, потенциально обладающее противовирусной активностью в отношении SARS-CoV-2. На настоящий момент инициировано несколько клинических исследований, которые в будущем позволят оценить эффективность ряда препаратов при CoViD-19, а также определить оптимальный режим их дозирования.
 Первые эксперименты in vitro и исследования на малых выборках пациентов демонстрируют вирусологическую и клиническую эффективность хлорохина и гидроксихлорохина, особенно при их раннем назначении (Wang M. et al., 2020, Gautret P. et al., 2020).
Первые эксперименты in vitro и исследования на малых выборках пациентов демонстрируют вирусологическую и клиническую эффективность хлорохина и гидроксихлорохина, особенно при их раннем назначении (Wang M. et al., 2020, Gautret P. et al., 2020).
Гидроксихлорохин, являющийся аналогом хлорохина, обладает более высокой активностью в отношении SARS-CoV-2, лучшим профилем безопасности, меньшим числом лекарственных взаимодействий и может быть использован в более высоких дозах, в том числе при длительных курсах терапии (Marmor et al., 2016, Yao et al., 2020). Исследовательская группа D. Raoult во Франции провела оценку применения гидроксихлорохина и комбинации гидроксихлорохина и азитромицина для лечения пациентов с подтвержденной CoViD-19 инфекцией (Gautret et al., 2020). 70 % пациентов, получивших гидроксихлорохин, продемонстрировали вирусологическое излечение по сравнению с 12,5 % пациентов контрольной группы на 6-й день лечения (р = 0,001). При сопоставлении комбинации гидроксихлорохина с азитромицином и монотерапии гидроксихлорохином 100 % пациентов в группе комбинированной терапии достигли вирусологического излечения по сравнению с 57,1 % в группе монотерапии (р<0,001). Результаты данного исследования внедрены в настоящее время в клиническую практику лечения CoViD-19 в Беларуси. И аминохинолины, и азитромицин способны удлинять интервал QT, увеличивая риск потенциально фатальных желудочковых аритмий. Кроме того, при длительном применении аминохинолинов возможно развитие ретинопатии и кардиомиопатии. Соответственно, при использовании хлорохина и гидроксихлорохина, особенно в комбинации с азитромицином, следует тщательно мониторировать ЭКГ и отменять данные лекарственные средства при появлении признаков кардиотоксичности.
Результаты данного исследования внедрены в настоящее время в клиническую практику лечения CoViD-19 в Беларуси. И аминохинолины, и азитромицин способны удлинять интервал QT, увеличивая риск потенциально фатальных желудочковых аритмий. Кроме того, при длительном применении аминохинолинов возможно развитие ретинопатии и кардиомиопатии. Соответственно, при использовании хлорохина и гидроксихлорохина, особенно в комбинации с азитромицином, следует тщательно мониторировать ЭКГ и отменять данные лекарственные средства при появлении признаков кардиотоксичности.
Никита Соловей, доцент кафедры инфекционных болезней БГМУ, кандидат мед. наук;
Александр Дедков, заведующий отделением интенсивной терапии и реанимации ГКИБ Минска;
Елена Блатун, заведующая отделением воздушно-капельных инфекций «Боковой изолятор» ГКИБ Минска;
Юрий Горбич, заведующий кафедрой инфекционных болезней и детских инфекций БелМАПО, кандидат мед. наук, доцент;
наук, доцент;
Игорь Карпов, заведующий кафедрой инфекционных болезней БГМУ, доктор мед. наук, профессор.
Медицинский вестник, 22 апреля 2020
Поделитесь
Вопрос-ответ
Вопрос от: Сергей
19 Января 2021
Здравствуйте. Подскажите пожалуйста, проводится ли специалистами вашего лечебного учреждения внутрибрюшинная химиотерапия?
Отвечает Данов Александр Николаевич, врач-онколог
Здравствуйте, Сергей! Нет, такое лечение не проводится, рекомендуется обращаться в федеральные медицинские центры (Москва, Санкт-Петербург).
Вопрос от: Евгения
18 Января 2021
Здравствуйте! У моего папы опухоль головного мозга (лимфома) В Москве сделали СТБ головного мозга и все необходимые обследования. Сами жители Томской области,с. Парабель,направление по месту жительства взяли. Скажите пожалуйста к какому доктору нам обращаться,помогут ли папе. Операцию на данном этапе делать нельзя,так сказал нейрохирург из НИХЦ им. Пирогова.
Операцию на данном этапе делать нельзя,так сказал нейрохирург из НИХЦ им. Пирогова.
Отвечает Данов Александр Николаевич, врач-онколог
Здравствуйте, Евгения! Вам необходимо обратиться к гематологу Томской областной клинической больницы, контакт-центр: 8(382-2) 63-00-63Вопрос от: КривошеинаЕлена
16 Января 2021
В интернете видела информацию о том, что можно отправить фото родинок для получения консультации дерматолога-онколога в диспансере. Но войдя на сайт ничего подобного не нашла. Есть еще такая услуга? У мамы есть родинки на спине, которые мне очень не нравятся, но уговорить ее показаться врачу не могу.
Отвечает Петлин Глеб Фёдорович, врач-онколог
Добрый день, Елена! Да, Вы можете отправить фото «подозрительных» родинок на ресурс «ОНКОДОЗОР: проверь родинку».Вопрос от: Юлия
13 Января 2021
Здравствуйте! Сыну, 11 лет, необходимо удалить родинку на спине, проводите ли вы такие процедуры детям? Есть показания к удалению, были на приеме у дерматолога в другой клинике.
Отвечает Петлин Глеб Фёдорович, врач-онколог
Добрый день! Вам нужно взять направление в Томский областной онкологический диспансер к онкологу-дерматологу. Его можно получить в поликлинике по месту прикрепления.
Вопрос от: Татьяна
12 Января 2021
Моей дочери 25 лет,поставили диагноз 25.12.2020 рак правой почки 4ст(т4н1м1).Канцероматоз.Асцит.Малый двусторонний гидроторакс.Инвазия опухоли в нижнюю полую вену.Тромбоз опухоли в нижнюю полую вену с полной окклюзией просвета до уровня атриокавального устья.Можно помочь?
Отвечает Данов Александр Николаевич, врач-онколог
Здравствуйте, Татьяна! Мало информации, для полноценной консультации необходимо предоставить пакет документов на телемедицинскую консультацию через отдел по работе с иногородними пациентами, если вы не жители Томской области.
Плевральный выпот: симптомы, причины, лечение
Что такое плевральный выпот?
Плевральный выпот, иногда также называемый «водой в легких», представляет собой скопление избыточной жидкости между слоями плевры вне легких. Плевра — это тонкие мембраны, выстилающие легкие и внутреннюю часть грудной полости, смазывая и облегчая дыхание. В норме в плевре присутствует небольшое количество жидкости.
Плевра — это тонкие мембраны, выстилающие легкие и внутреннюю часть грудной полости, смазывая и облегчая дыхание. В норме в плевре присутствует небольшое количество жидкости.
Насколько серьезен плевральный выпот?
Серьезность состояния зависит от основной причины плеврального выпота, нарушения дыхания и возможности эффективного лечения.Причины плеврального выпота, которые можно эффективно лечить или контролировать, включают инфекцию, вызванную вирусом, пневмонию или сердечную недостаточность. Необходимо учитывать два фактора: лечение связанных с ними механических проблем, а также лечение основной причины плеврального выпота.
Каковы симптомы плеврального выпота?
У некоторых пациентов с плевральным выпотом симптомы отсутствуют, и это состояние обнаруживается на рентгеновском снимке грудной клетки, выполненном по другой причине.У пациента могут быть несвязанные симптомы из-за заболевания или состояния, вызвавшего выпот. Симптомы плеврального выпота включают:
- Боль в груди
- Сухой непродуктивный кашель
- Одышка (одышка или затрудненное, затрудненное дыхание)
- Ортопноэ (невозможность легко дышать, если человек не сидит прямо или не стоит прямо)
Что вызывает плевральный выпот?
По данным Национального института рака, плевральные выпоты очень распространены: ежегодно в США диагностируется около 100 000 случаев.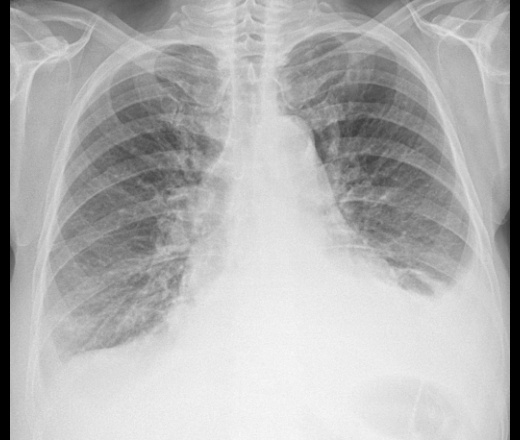
В зависимости от причины избыток жидкости может быть бедным белком (транссудативный) или богатым белком (экссудативный). Эти две категории помогают врачам определить причину плеврального выпота.
Наиболее частые причины транссудативного (водянистого) плеврального выпота включают:
Экссудативный (богатая белком жидкость) плевральный выпот чаще всего вызывается следующими причинами:
Другие менее частые причины плеврального выпота включают:
- Туберкулез
- Аутоиммунное заболевание
- Кровотечение (при травме грудной клетки)
- Хилоторакс (травма)
- Редкие инфекции органов грудной клетки и брюшной полости
- Асбестовый плевральный выпот (вследствие воздействия асбеста)
- Синдром Мейга (из-за доброкачественной опухоли яичника)
- Синдром гиперстимуляции яичников
Некоторые лекарства, абдоминальная хирургия и лучевая терапия также могут вызывать плевральный выпот. Плевральный выпот может возникать при нескольких типах рака, включая рак легких, рак груди и лимфому. В некоторых случаях сама жидкость может быть злокачественной (раковой) или может быть прямым результатом химиотерапии.
Плевральный выпот может возникать при нескольких типах рака, включая рак легких, рак груди и лимфому. В некоторых случаях сама жидкость может быть злокачественной (раковой) или может быть прямым результатом химиотерапии.
Последний раз проверял медицинский работник Cleveland Clinic 18.12.2018.
Ссылки
- «Плевральный выпот.»Энциклопедия рака Гейла. Группа Гейл, Инк., 2002. Answers.com .
- «Злокачественный плевральный выпот». Национальный институт рака. По состоянию на 26 октября 2006 г.
- «Плевральный выпот». Медицинская энциклопедия MedLine Plus. Доступ 26 октября 2006 г.
- Colice G L, Curtis A, Deslauriers J, Heffner J, Light R, Littenberg B, Sahn S, Weinstein R.
 A, Yusen R. D. «Медицинское и хирургическое лечение парапневмонических выпотев: руководство, основанное на фактах». Сундук , 2000; 118; 1158-1171.
A, Yusen R. D. «Медицинское и хирургическое лечение парапневмонических выпотев: руководство, основанное на фактах». Сундук , 2000; 118; 1158-1171. - Rubins J. «Плевральный выпот». 2005. eMedicine. Доступ 26 октября 2006 г.
- Interact CardioVasc Thorac Surg 2006; 5: 307-310. doi: 10.1510 / icvts.2005.118018 © 2006 Европейская ассоциация кардио-торакальной хирургии
Получите полезную, полезную и актуальную информацию о здоровье и благополучии
е Новости Клиника Кливленда — некоммерческий академический медицинский центр.Реклама на нашем сайте помогает поддерживать нашу миссию. Мы не поддерживаем продукты или услуги, не принадлежащие Cleveland Clinic. Политика
Политика
Плевральный выпот — причины, симптомы, типы и лечение
Плевральный выпот — это необычное количество жидкости вокруг легкого. Многие медицинские условия могут привести к этому, поэтому, даже если ваш плевральный выпот, возможно, придется удалить, ваш врач, скорее всего, нацелит лечение на то, что вызвало его.
Плевра — это тонкая мембрана, выстилающая поверхность легких и внутреннюю часть грудной клетки. Когда у вас плевральный выпот, жидкость накапливается в пространстве между слоями плевры.
Обычно только чайные ложки водянистой жидкости находятся в плевральной полости, что позволяет вашим легким плавно двигаться в грудной полости, когда вы дышите.
Причины
Плевральный выпот может быть вызван множеством факторов. Вот некоторые из наиболее распространенных:
Утечка из других органов.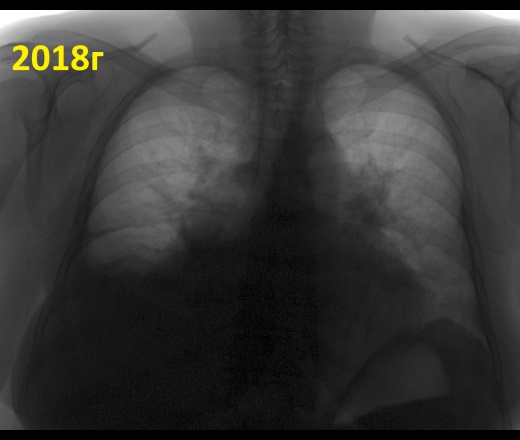 Это обычно происходит, если у вас застойная сердечная недостаточность, когда ваше сердце не перекачивает кровь к вашему телу должным образом. Но это также может быть связано с заболеванием печени или почек, когда жидкость накапливается в вашем теле и просачивается в плевральную полость.
Это обычно происходит, если у вас застойная сердечная недостаточность, когда ваше сердце не перекачивает кровь к вашему телу должным образом. Но это также может быть связано с заболеванием печени или почек, когда жидкость накапливается в вашем теле и просачивается в плевральную полость.
Продолжение
Рак. Обычно проблемой является рак легких, но другие виды рака, распространившиеся на легкие или плевру, также могут вызывать ее.
Инфекции. Некоторые заболевания, которые приводят к плевральному выпоту, — это пневмония или туберкулез.
Аутоиммунные состояния. Волчанка или ревматоидный артрит — это некоторые заболевания, которые могут его вызывать.
Тромбоэмболия легочной артерии. Это закупорка артерии в одном из легких, которая может привести к плевральному выпоту.
Признаки
У вас их может не быть. Вероятность появления симптомов выше при плевральном выпоте среднего или большого размера, а также при воспалении.
Если у вас есть симптомы, они могут включать:
- Одышка
- Боль в груди, особенно при глубоком вдохе (это называется плевритом или плевритной болью.)
- Лихорадка
- Кашель
Диагноз
Ваш врач расскажет вам о ваших симптомах и проведет медицинский осмотр. Они постучат вам по груди и послушают с помощью стетоскопа.
Чтобы подтвердить наличие плеврального выпота, вам необходимо пройти визуализацию, например:
Рентген грудной клетки. Плевральный выпот на рентгеновских снимках выглядит белым, а воздушное пространство — черным. Если вероятен плевральный выпот, вы можете сделать больше рентгеновских снимков, лежа на боку.Они могут показать, свободно ли течет жидкость в плевральной полости.
Продолжение
Компьютерная томография (КТ). Сканер компьютерной томографии быстро принимает множество рентгеновских снимков, а компьютер создает изображения всей грудной клетки — внутри и снаружи. КТ показывает больше деталей, чем рентген грудной клетки.
КТ показывает больше деталей, чем рентген грудной клетки.
УЗИ. Датчик на груди создает изображения внутренней части вашего тела, которые отображаются на видеоэкране. Ваш врач может использовать ультразвук, чтобы определить местонахождение жидкости и взять образец для анализа.
Кроме того, ваш врач может назначить процедуру, называемую торакоцентез. Для проверки возьмут немного жидкости. Для этого они вводят иглу и трубку, называемую катетером, между ребрами в плевральную полость.
Типы
Вы можете слышать, как ваш врач использует термины «транссудативный» и «экссудативный» для описания двух основных типов плевральных выпотов.
Транссудативный. Эта жидкость из плеврального выпота похожа на жидкость, которая обычно содержится в плевральной полости.Он образуется из жидкости, протекающей через нормальную плевру. Этот тип редко нужно сливать, если он не очень большой. Застойная сердечная недостаточность — наиболее частая причина этого типа.
Экссудативный. Он образуется из лишней жидкости, белка, крови, воспалительных клеток или иногда бактерий, которые проникают через поврежденные кровеносные сосуды в плевру. Возможно, вам потребуется его дренировать, в зависимости от его размера и степени воспаления. Причины этого типа включают пневмонию и рак легких.
Лечение
Вашему врачу может потребоваться лечение только того заболевания, которое вызвало плевральный выпот. Например, вы получите антибиотики от пневмонии или диуретики от сердечной недостаточности.
Большие инфицированные или воспаленные плевральные выпоты часто необходимо дренировать, чтобы улучшить самочувствие и предотвратить появление новых проблем.
Процедуры лечения плеврального выпота включают:
Торакоцентез. Если выпот большой, врач может выпить больше жидкости, чем необходимо для анализа, просто для облегчения симптомов.
Трубчатая торакостомия (грудная трубка). Врач делает небольшой разрез в грудной стенке и вводит пластиковую трубку в плевральную полость на несколько дней.
Врач делает небольшой разрез в грудной стенке и вводит пластиковую трубку в плевральную полость на несколько дней.
Плевральный дренаж. Если ваши плевральные выпоты продолжают возвращаться, ваш врач может ввести катетер длительного действия через вашу кожу в плевральную полость. После этого вы сможете удалить плевральный выпот в домашних условиях. Ваш врач скажет вам, как и когда это делать.
Продолжение
Pleurodesis .Ваш врач вводит раздражающее вещество (например, тальк или доксициклин) через дренажную трубку в плевральную полость. Вещество вызывает воспаление плевры и грудной клетки, которые затем плотно связываются друг с другом по мере заживления. Во многих случаях плевродез может предотвратить повторение плеврального выпота.
Декортикация плевры. Хирурги могут оперировать плевральную полость, удаляя потенциально опасные воспаления и нездоровые ткани. Для этого ваш хирург может сделать небольшие разрезы (торакоскопия) или большие (торакотомия).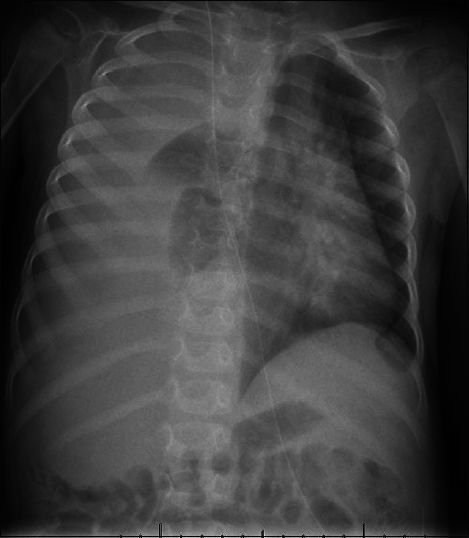
Плевральный выпот: причины, диагностика и лечение
Плевральный выпот — это скопление жидкости в пространстве между легкими и грудной полостью. Это может быть результатом пневмонии и многих других заболеваний. Это также может быть опасно для жизни.
Плевральный выпот, или «вода в легких», может напоминать респираторную инфекцию. Иногда причина может быть респираторной, но есть и другие возможные причины. Медицинскому работнику необходимо будет диагностировать первопричину, чтобы назначить соответствующее лечение.
Симптомы плеврального выпота могут включать кашель, боль в груди и затрудненное дыхание.
В этой статье будет рассмотрено, что происходит при плевральном выпоте, почему он возникает, и некоторые варианты решения этой проблемы.
Плевральный выпот у человека означает скопление жидкости в пространстве между легкими и грудной полостью или плевральной полостью. И легкие, и грудная полость имеют слизистую оболочку, состоящую из плевры, которая представляет собой тонкую мембрану.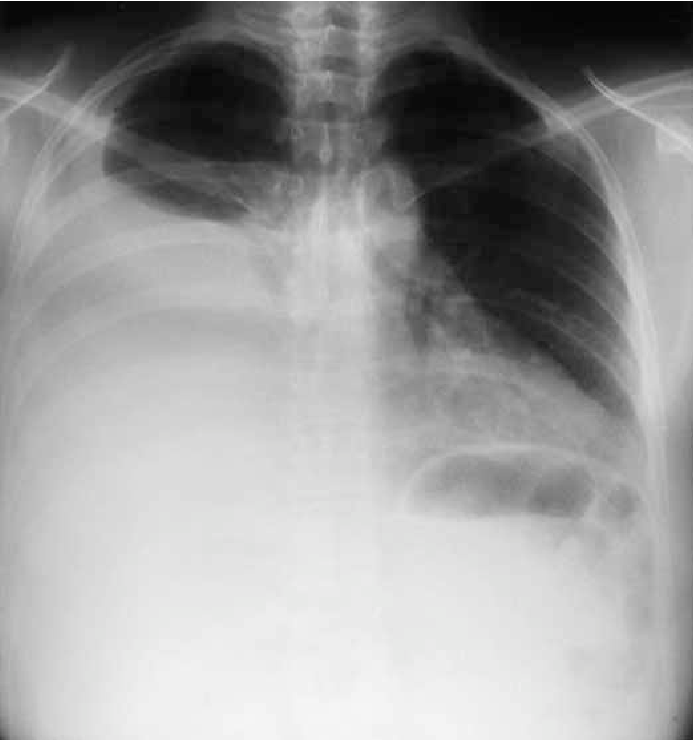
В здоровых легких эти мембраны обеспечивают наличие небольшого количества жидкости между легкими и грудной клеткой.Это предотвращает трение, поскольку легкие расширяются и сжимаются во время дыхания.
Однако у человека с плевральным выпотом в плевральной полости слишком много жидкости.
Любому, у кого может быть плевральный выпот, требуется немедленная медицинская помощь, поскольку без лечения это может быть опасно для жизни.
Плевральный выпот всегда является результатом другого заболевания. Это может быть вызвано многими условиями. Вот некоторые из наиболее частых причин:
Некоторые медицинские процедуры также могут вызвать плевральный выпот.Примеры:
- операция на открытом сердце или другая операция на грудной клетке
- определенные лекарства, включая метотрексат, амиодарон и фенитоин
- лучевая терапия
- гиперстимуляция яичников
Некоторые люди не испытывают никаких симптомов плеврального выпота .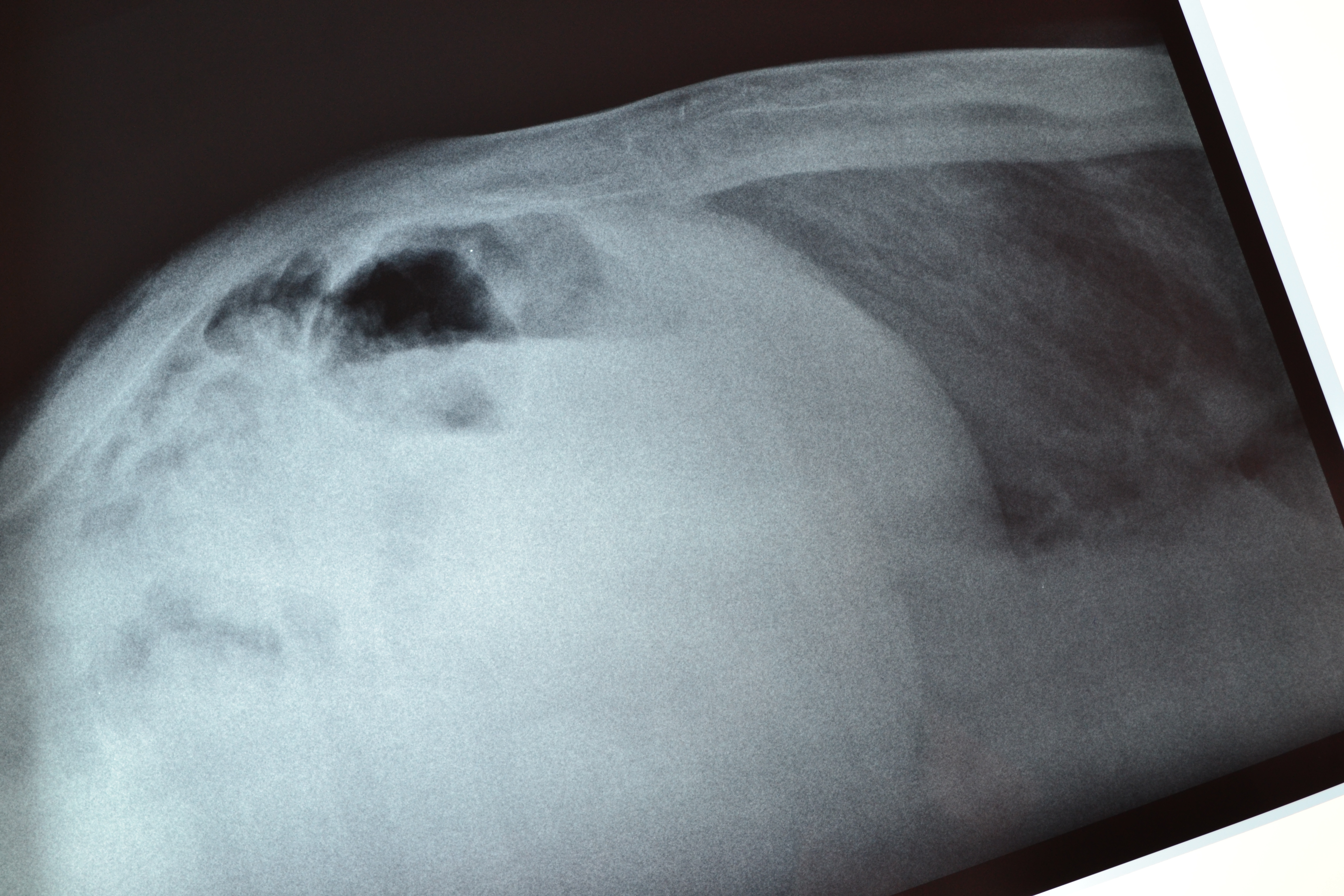 Если симптомы все же возникают, они обычно начинают появляться по мере того, как жидкость заполняет грудную полость.
Если симптомы все же возникают, они обычно начинают появляться по мере того, как жидкость заполняет грудную полость.
Некоторые возможные симптомы включают:
- сухой или непродуктивный кашель
- затрудненное дыхание, особенно в положении лежа
- лихорадка и симптомы гриппа
- боль в груди
- острая, сильная боль при глубоком вдохе
Постоянная икота также может быть признаком плеврального выпота.
Некоторые люди узнают, что у них плевральный выпот, только когда проходят тест на другое заболевание.
Также важно отметить, что симптомы плеврального выпота могут напоминать симптомы других заболеваний легких. Человеку требуется срочная медицинская помощь, если он испытывает какие-либо из этих симптомов.
Ниже представлена трехмерная модель плеврального выпота. Он полностью интерактивен.
Изучите модель с помощью коврика для мыши или сенсорного экрана, чтобы узнать больше об этом состоянии.
Диагностировать плевральный выпот может быть сложно, поскольку симптомы могут частично совпадать с симптомами многих других заболеваний.
Чтобы поставить диагноз, медицинский работник:
- спросит человека об его симптомах
- спросит его об их общем состоянии здоровья и истории болезни
- проведет физическое обследование
- предложит тесты визуализации, такие как X- лучевая, ультразвуковая или компьютерная томография
Медицинскому работнику также необходимо определить, является ли выпот транссудатом или экссудатом.В следующих разделах эти типы рассматриваются более подробно.
Выпот транссудата
Выпот транссудата обычно возникает, когда другое состояние вызывает дисбаланс давления в кровеносных сосудах. В результате жидкость просачивается обратно в грудную клетку. Жидкость в выпоте, вероятно, будет состоять из соединений из плазмы крови.
Выпот экссудата
Выпот экссудата обычно возникает в результате:
- воспалительных состояний
- инфекции
- рака
- травматического повреждения
- закупорки кровеносных или лимфатических сосудов в этой области
Медицинский работник может взять образец жидкость из плевральной полости путем введения иглы между ребрами.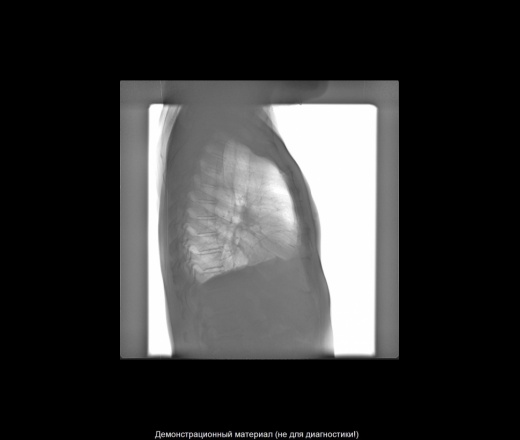
Эти образцы могут помочь обнаружить признаки инфекции, уровень белка и раковые клетки. Они также могут помочь определить, есть ли у человека осложненный или неосложненный плевральный выпот.
При осложненном плевральном выпоте в жидкости будут присутствовать признаки воспаления или инфекции. Человеку может потребоваться немедленное лечение, чтобы предотвратить потенциально серьезные осложнения.
При неосложненном выпоте в жидкости не будет признаков инфекции или воспаления.Неосложненный выпот может протекать легче и с меньшей вероятностью приведет к необратимому повреждению легких.
Некоторые другие тесты могут помочь определить причину выпота. К ним относятся:
- функциональные тесты почек
- функциональные тесты печени
- биопсия легких
- бронхоскопия
- ультразвуковое исследование сердца для оценки сердечной недостаточности
Эти тесты помогают медицинскому работнику сузить причину плеврального выпота и обеспечить соответствующее лечение.
Лечение будет зависеть от основной причины. Помимо лечения основного заболевания, медицинскому работнику может потребоваться слить жидкость из груди.
Слив из грудной клетки
Для дренирования грудной клетки медицинский работник вставляет трубку в плевральную полость и позволяет жидкости покинуть тело.
Они будут использовать местные анестетики, чтобы заглушить боль в месте проникновения иглы в тело. Когда действие анестетиков прекратится, эта область может болеть.
Им также может потребоваться повторить процесс, если жидкость продолжает собираться в плевральной полости.
Существует небольшой риск осложнений, связанных с дренированием грудной клетки. К ним относятся:
- инфекция
- кровотечение
- коллапс легкого
- жидкость, попадающая в легкие
Однако эти осложнения возникают редко.
Другие методы лечения
В некоторых случаях могут потребоваться другие методы лечения.
При плевродезе, например, хирург закрывает зазор между плеврой легкого и грудной полостью, чтобы предотвратить скопление жидкости между ними.
В более тяжелых случаях хирург может направить жидкость из грудной полости в брюшную полость. В некоторых случаях они могут также удалить часть плевральной оболочки.
Плевральный выпот — признак основного заболевания. И основное заболевание, и сам плевральный выпот могут быть опасными для жизни.
Перспектива и время, необходимое для выздоровления, будут зависеть от причины излияния, общего состояния здоровья человека и тяжести его симптомов.
Человеку, возможно, придется провести время в больнице, где он может пройти обследования и наблюдение.Лечение часто может устранить плевральный выпот, хотя не всегда возможно вылечить его первопричину.
Жидкость в грудной клетке (плевральный выпот)
Что такое плевральный выпот?
Плевральный выпот, также называемый водой в легких, — это чрезмерное скопление жидкости в пространстве между легкими и грудной полостью.
Тонкие оболочки, называемые плеврой, покрывают внешнюю часть легких и внутреннюю часть грудной полости.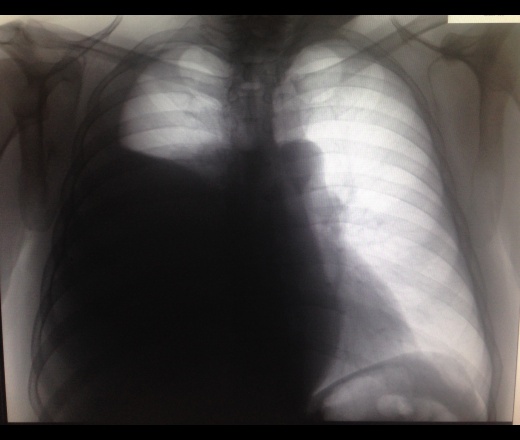 Внутри этой подкладки всегда есть небольшое количество жидкости, которая помогает смазывать легкие, поскольку они расширяются в груди во время дыхания.
Внутри этой подкладки всегда есть небольшое количество жидкости, которая помогает смазывать легкие, поскольку они расширяются в груди во время дыхания.
Некоторые заболевания могут вызвать плевральный выпот.
По данным Американского торакального общества, плевральные выпоты являются обычным явлением, ежегодно в США диагностируется около 1 миллиона случаев. Это серьезное заболевание, связанное с повышенным риском смерти. В одном исследовании 15 процентов госпитализированных людей с диагнозом плевральный выпот умерли в течение 30 дней.
Плевра выделяет слишком много жидкости, когда она раздражена, воспалена или инфицирована. Эта жидкость накапливается в грудной полости за пределами легких, вызывая так называемый плевральный выпот.
Определенные виды рака могут вызывать плевральный выпот, наиболее распространенными являются рак легких у мужчин и рак груди у женщин.
Другие причины плеврального выпота включают:
Есть несколько типов плевральных выпотов, каждый из которых имеет разные причины и варианты лечения.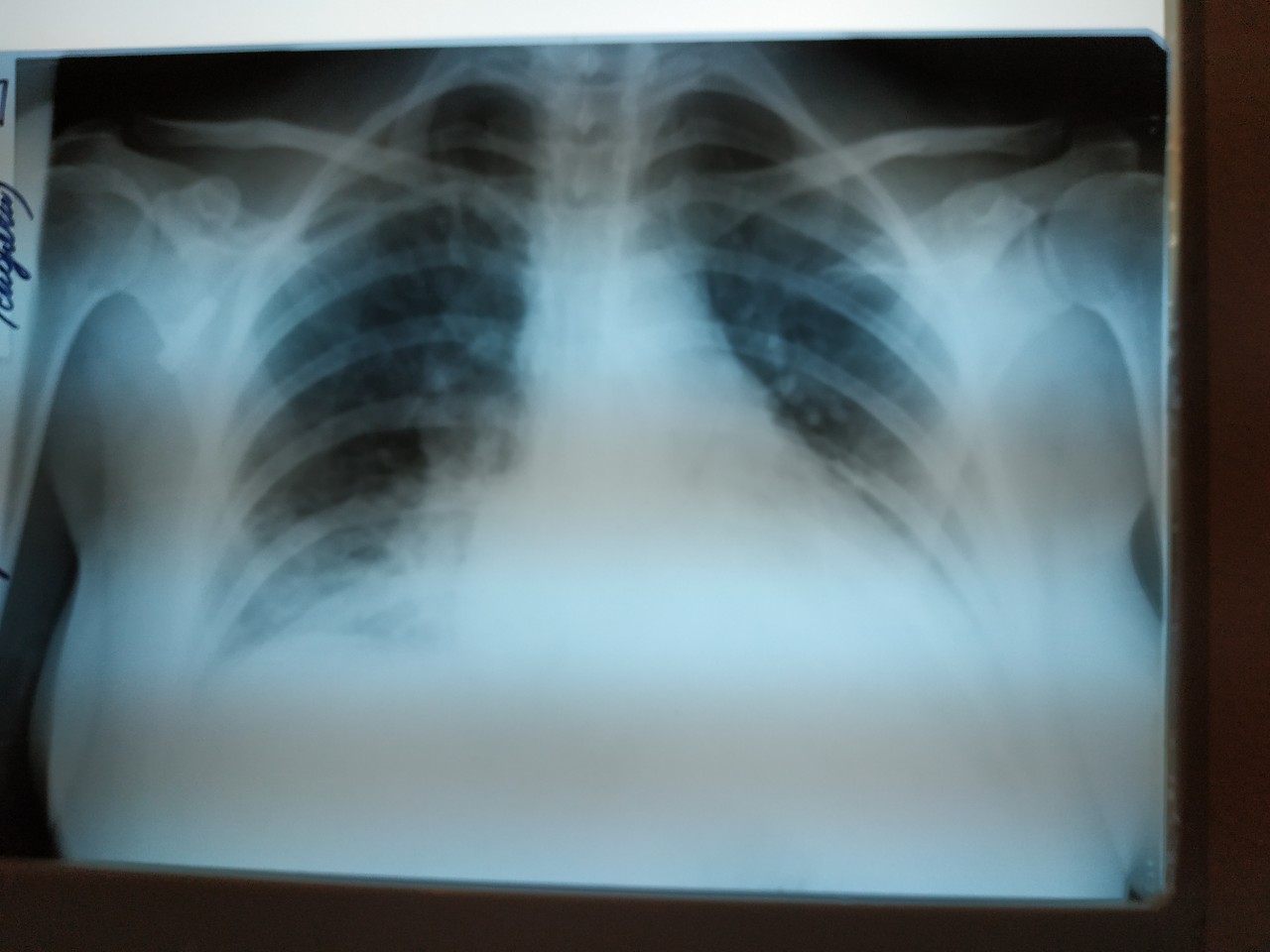 Первая классификация плевральных выпотов бывает транссудативной или экссудативной.
Первая классификация плевральных выпотов бывает транссудативной или экссудативной.
Транссудативный плевральный выпот
Этот тип вызывается утечкой жидкости в плевральную полость в результате либо низкого количества белка в крови, либо повышенного давления в кровеносных сосудах.Наиболее частая причина — застойная сердечная недостаточность.
Экссудативный выпот
Этот тип вызван:
- блокировкой лимфы или кровеносных сосудов
- воспалением
- опухолью
- повреждением легкого
Общие состояния, которые могут привести к этому типу плевральной инфузии, включают легочную эмболию, пневмонию, и грибковые инфекции.
Осложненные и неосложненные плевральные выпоты
Есть также сложные и неосложненные плевральные выпоты.Неосложненные плевральные выпоты содержат жидкость без признаков инфекции или воспаления. У них гораздо меньше шансов вызвать постоянные проблемы с легкими.
Однако осложненные плевральные выпоты содержат жидкость со значительной инфекцией или воспалением.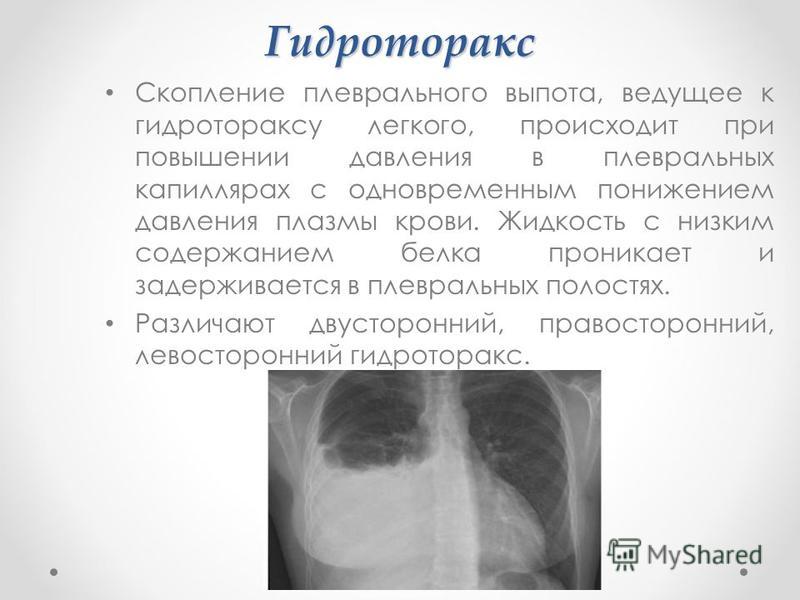 Они требуют немедленного лечения, которое часто включает дренирование грудной клетки.
Они требуют немедленного лечения, которое часто включает дренирование грудной клетки.
У некоторых людей плевральный выпот не проявляется. Эти люди обычно узнают о своем заболевании на рентгеновском снимке грудной клетки или при физическом обследовании по другой причине.
Общие симптомы плеврального выпота включают:
Немедленно обратитесь к врачу, если у вас есть симптомы плеврального выпота.
Ваш врач проведет медицинский осмотр и послушает ваши легкие с помощью стетоскопа. Они также могут заказать рентген грудной клетки, чтобы диагностировать плевральный выпот. Другие возможные тесты включают:
При анализе плевральной жидкости ваш врач удалит жидкость из области плевральной мембраны, введя иглу в грудную полость и всасывая жидкость шприцем.Процедура называется плевроцентез. Это также обычная процедура для слива лишней жидкости из грудной полости. Затем жидкость будет проверена для определения причины.
Ваш врач может также выбрать биопсию плевры, которая включает взятие образца ткани плевры.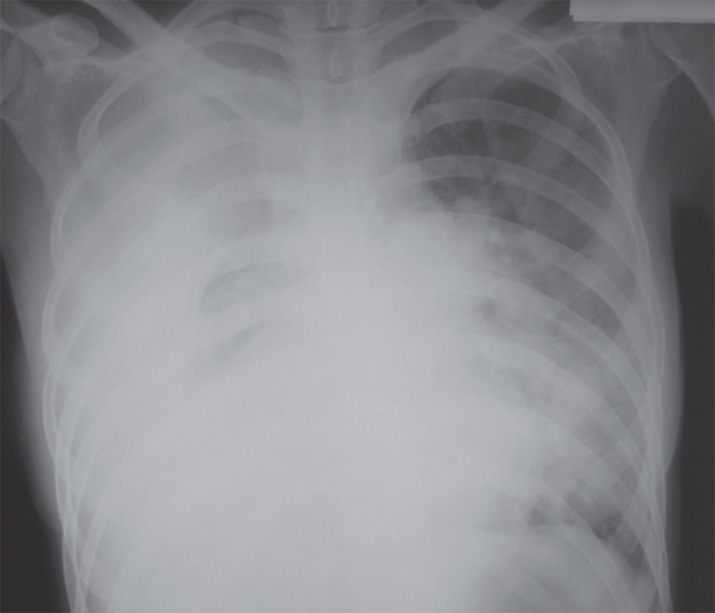 Это можно сделать, введя небольшую иглу снаружи грудной клетки в грудную полость.
Это можно сделать, введя небольшую иглу снаружи грудной клетки в грудную полость.
Если они обнаруживают, что у вас плевральный выпот, но не могут определить, какой тип, ваш врач может назначить торакоскопию.Это хирургическая процедура, которая позволяет врачу заглянуть внутрь грудной клетки с помощью оптоволоконной камеры.
Для этой процедуры ваш врач сделает несколько небольших разрезов в области груди, пока вы находитесь под общей анестезией. Затем они вставляют камеру через один разрез, а хирургический инструмент — через другой, чтобы извлечь небольшое количество жидкости или ткани для анализа.
Основная причина состояния и тяжесть выпота будут определять лечение.
Дренаж жидкости
Обычно лечение включает в себя дренирование жидкости из грудной полости с помощью иглы или небольшой трубки, вставленной в грудную клетку.
Перед процедурой вам сделают местную анестезию, что сделает процедуру более комфортной. Вы можете почувствовать боль или дискомфорт в месте разреза после того, как действие анестетика закончится. Большинство врачей пропишут лекарства, чтобы облегчить боль.
Большинство врачей пропишут лекарства, чтобы облегчить боль.
Эта обработка может потребоваться более одного раза, если жидкость снова накапливается.
Другие методы лечения могут потребоваться для предотвращения скопления жидкости, если причиной плеврального выпота является рак.
Плевродез
Плевродез — это лечение, при котором возникает легкое воспаление между легким и плеврой грудной полости. После извлечения лишней жидкости из грудной полости врач вводит в эту область лекарство. Препарат часто представляет собой смесь талька. Это лекарство заставляет два слоя плевры слипаться, что предотвращает накопление жидкости между ними в будущем.
Хирургия
В более серьезных случаях врач хирургическим путем вставляет шунт или небольшую трубку в грудную полость. Это помогает перенаправить жидкость из груди в брюшную полость, где ее легче удалить. Это может быть вариант для тех, кто не отвечает на другие виды лечения. Плеврэктомия, при которой часть плевральной оболочки удаляется хирургическим путем, также может быть вариантом в определенных случаях.
В некоторых случаях плевральный выпот можно лечить с помощью лекарств и другой поддерживающей терапии.Большинство людей выздоравливают в течение нескольких дней или недель. Незначительные осложнения от более инвазивных методов лечения могут включать легкую боль и дискомфорт, которые часто проходят со временем. В некоторых случаях плевральный выпот может иметь более серьезные осложнения в зависимости от тяжести состояния, причины и применяемого лечения.
К серьезным осложнениям могут относиться:
- отек легких или жидкость в легких, которые могут возникнуть в результате слишком быстрого дренирования жидкости во время плевроцентеза
- частичное коллапс легкого
- инфекция или кровотечение
Эти осложнения, хотя и серьезные, встречаются очень редко. .Ваш врач поможет определить наиболее эффективный вариант лечения и обсудит преимущества и риски каждой процедуры.
Плевральный выпот может быть результатом распространения раковых клеток на плевру. Они также могут быть результатом того, что раковые клетки блокируют поток нормальной жидкости в плевре. Жидкость также может накапливаться в результате определенных методов лечения рака, таких как лучевая терапия или химиотерапия.
Они также могут быть результатом того, что раковые клетки блокируют поток нормальной жидкости в плевре. Жидкость также может накапливаться в результате определенных методов лечения рака, таких как лучевая терапия или химиотерапия.
Некоторые виды рака с большей вероятностью вызывают плевральный выпот, чем другие, в том числе:
Признаки и симптомы часто включают:
- одышка
- кашель
- боль в груди
- потеря веса
Плевродез часто используется в качестве лечение злокачественных плевральных выпотов, вызванных раком.Ваш врач может назначить антибиотики, если у вас есть инфекция или вы подвержены ей. Стероиды или другие противовоспалительные препараты могут уменьшить боль и воспаление.
В дополнение к лечению плеврального выпота ваш врач лечит вызвавший его рак. Плевральный выпот обычно является результатом метастатического рака.
Люди, проходящие курс лечения от рака, также могут иметь ослабленную иммунную систему, что делает их более склонными к инфекциям или другим осложнениям.
Плевральный выпот может быть серьезным и опасным для жизни. Большинству из них требуется госпитализация, а некоторым — операция. Время, необходимое для восстановления после плеврального выпота, зависит от причины, размера и тяжести выпота, а также от вашего общего состояния здоровья.
Вы начнете выздоровление в больнице, где вам будут предоставлены необходимые лекарства и помощь, которые помогут вам начать выздоровление. Многие люди сообщают о чувстве усталости и слабости в первую неделю после выписки из больницы.В среднем вы увидите, что места разрезов после операции заживают в течение двух-четырех недель. Когда вы вернетесь домой, вам потребуется постоянный уход и наблюдение.
Плевральный выпот | Michigan Medicine
Обзор темы
Плевральный выпот (скажем «PLER-uhl eh-FYOO-zhun») — это скопление жидкости в пространстве между тканями, выстилающими легкие, и грудной стенкой (плевральная полость). Из-за скопления жидкости легкие могут быть не в состоянии полностью расшириться, и вам будет трудно дышать. Легкое или его часть может разрушиться.
Легкое или его часть может разрушиться.
Как диагностируется плевральный выпот?
Плевральный выпот обычно диагностируется при физическом осмотре и визуализирующих исследованиях, таких как рентген или компьютерная томография. Врач также послушает воздушный поток в ваших легких.
Анализы крови или анализы, выполненные на образце жидкости, взятой вокруг легких, могут использоваться, чтобы помочь выяснить, что вызвало накопление жидкости.
Каковы симптомы?
Симптомы плеврального выпота могут включать:
- Проблемы с дыханием.
- Одышка.
- Боль в груди.
- Лихорадка.
- Кашель.
Незначительный плевральный выпот может не вызывать никаких симптомов.
Что вызывает плевральный выпот?
Плевральный выпот имеет много причин. К ним относятся сердечная недостаточность, пневмония и другие инфекции, рак, тромбоэмболия легочной артерии, заболевания печени и воспаление тканей вокруг легких.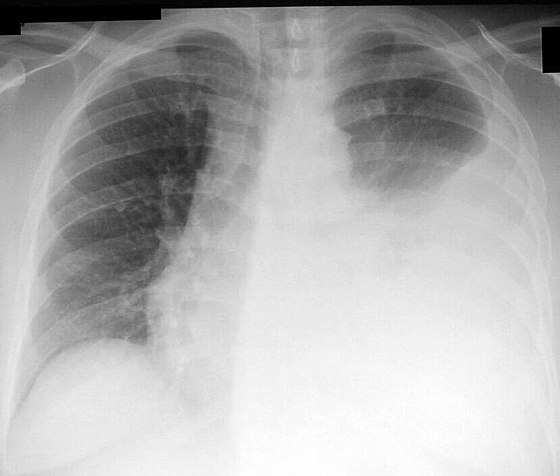
Как лечится?
Незначительный плевральный выпот часто проходит сам по себе без лечения.
В других случаях врачу может потребоваться лечение состояния, которое вызывает плевральный выпот. Например, вам могут назначить антибиотики для лечения пневмонии. Или вы можете получить другие лекарства для лечения сердечной недостаточности.
Плевральный выпот также можно лечить путем удаления жидкости из плевральной полости. Это может помочь облегчить симптомы, такие как одышка и боль в груди. Это также может помочь легким более полно расшириться.
Жидкость можно удалить, введя иглу в плевральную полость.Это лечение называется торакоцентез. Небольшой образец жидкости может быть взят и отправлен в лабораторию, чтобы выяснить, что вызывает скопление жидкости.
Если плевральный выпот серьезный или не проходит, в грудную клетку можно ввести небольшую катетерную трубку или большую трубку. Это позволяет жидкости вытекать из пространства, окружающего легкие.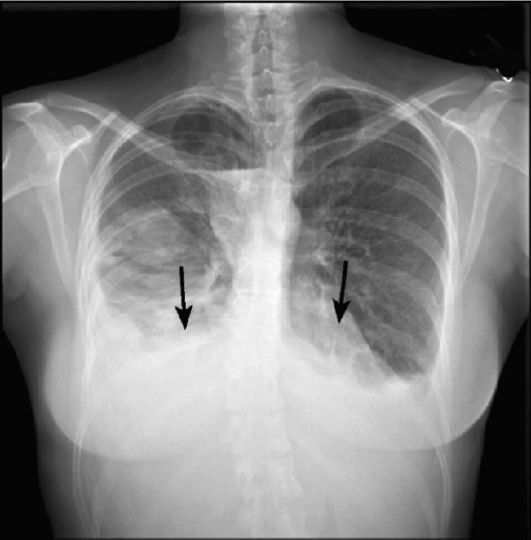 Трубка остается в грудной клетке до тех пор, пока жидкость не будет слита или пока врач не удалит ее. Большинство людей остаются в больнице, пока установлена плевральная дренажная трубка.
Трубка остается в грудной клетке до тех пор, пока жидкость не будет слита или пока врач не удалит ее. Большинство людей остаются в больнице, пока установлена плевральная дренажная трубка.
При некоторых заболеваниях, например, при раке легких, со временем может накапливаться жидкость.В этих случаях трубку можно вводить в грудную клетку столько, сколько нужно человеку. Его можно использовать для слива жидкости каждый раз, когда она накапливается. Большинство людей могут пойти домой с этим типом плевральной дренажной трубки и самостоятельно слить жидкость.
Некоторые люди могут пройти курс лечения, называемый плевродезом, чтобы удалить жидкость, а затем ввести лекарство в грудную полость. Это помогает предотвратить повторное скопление слишком большого количества жидкости.
Лечение доброкачественных неинфекционных плевральных выпотов
Введение
За последнее десятилетие в лечении злокачественных плевральных выпотов был достигнут значительный прогресс, при этом ряд рандомизированных контролируемых исследований теперь используются в практике [1–3].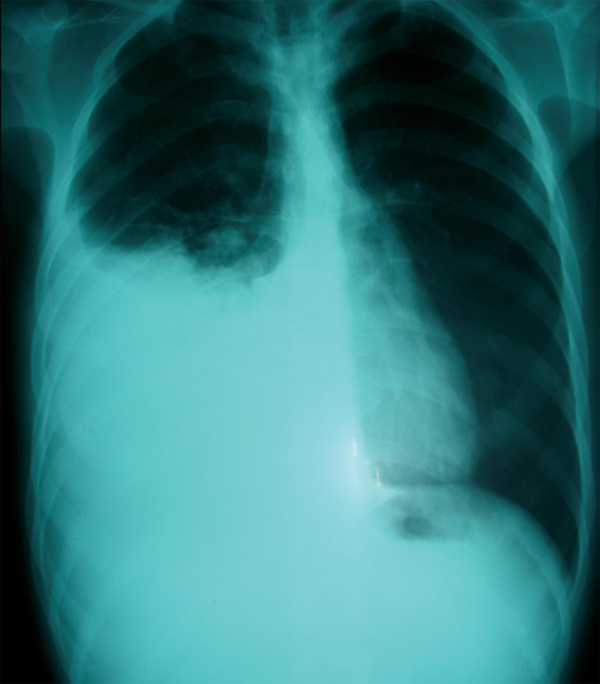 Этот прогресс, напротив, не был отражен в незлокачественных заболеваниях плевры, доказательная база которых по-прежнему сформирована в основном из обсервационных исследований. В результате при лечении доброкачественных плевральных выпотов часто используются методы, разработанные и проверенные при злокачественных заболеваниях. Точно так же, хотя международные рекомендации, разработанные Британским торакальным обществом и Американским торакальным обществом, доступны для злокачественных плевральных выпотов [4, 5], таких эквивалентных рекомендаций для доброкачественных плевральных заболеваний не существует.
Этот прогресс, напротив, не был отражен в незлокачественных заболеваниях плевры, доказательная база которых по-прежнему сформирована в основном из обсервационных исследований. В результате при лечении доброкачественных плевральных выпотов часто используются методы, разработанные и проверенные при злокачественных заболеваниях. Точно так же, хотя международные рекомендации, разработанные Британским торакальным обществом и Американским торакальным обществом, доступны для злокачественных плевральных выпотов [4, 5], таких эквивалентных рекомендаций для доброкачественных плевральных заболеваний не существует.
Потенциальные причины незлокачественного плеврального выпота многочисленны, часто встречаются редко и в некоторых случаях плохо изучены. Это отсутствие четкой классификации и определения может частично объяснить отсутствие высококачественных доказательств и установленных руководств. Поскольку у пораженных пациентов часто наблюдаются сопутствующие заболевания, а их плевральный выпот может быть проявлением болезненного процесса, управляемого специалистами, не относящимися к респираторным заболеваниям, тесные междисциплинарные связи особенно важны в этой группе пациентов для обеспечения скоординированных и оптимизированных путей оказания помощи.
Цель данной статьи — обрисовать бремя и спектр доброкачественных плевральных выпотов и обобщить доказательную базу для стратегий лечения.
Эпидемиология
Незлокачественные плевральные выпоты являются обычным явлением, а спектр заболеваний широк. В частности, плевральный выпот, связанный с сердечной недостаточностью, часто наблюдается у взрослых пациентов, госпитализированных в больницу, и пациентов, находящихся в отделениях интенсивной терапии. Многие из этих выпотов могут быть субклиническими и исчезать параллельно с лечением основного заболевания.Однако существует значительное бремя симптоматических заболеваний, требующих специального лечения.
Неопубликованные данные аудита из Бристоля (Великобритания) 327 пациентов с доброкачественными выпотами, направленных в третичную плевральную службу для дальнейшего исследования в течение 5-летнего периода, показаны в таблице 1. Эти данные демонстрируют распределение возможных этиологий после вызванных выпотом. по злокачественному новообразованию или травме были исключены.
по злокачественному новообразованию или травме были исключены.
Пропорции причин незлокачественных плевральных выпотов
Оценка плеврального выпота
Оценка плеврального выпота основывается на тщательном анамнезе и обследовании, но часто требует визуализации и анализа плевральной жидкости, чтобы сузить дифференциальный диагноз .
Наиболее частым симптомом плеврального выпота является одышка. Степень одышки может быть непропорциональна размеру выпота и зависеть от сопутствующих заболеваний сердца и легких. Одышка может быть результатом уменьшения нормального движения диафрагмы в дополнение к уменьшению дыхательного объема, напрямую связанного с массовым влиянием жидкости в грудной полости [6].
Скорость появления симптомов (чаще всего одышка) часто помогает определить возможную первопричину, хотя сопутствующая радиология может дать объективную оценку этого.В таблице 2 подробно описаны общие особенности истории болезни пациента, которые могут иметь значение.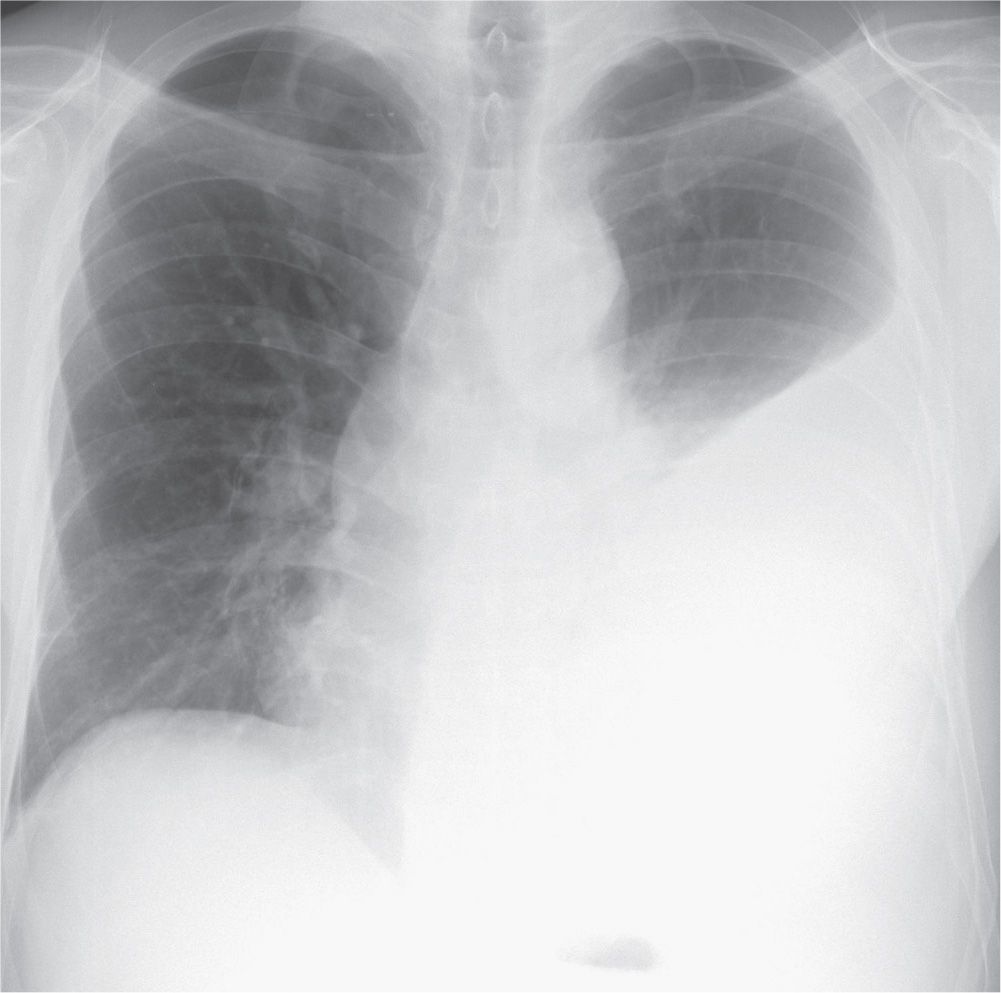
Анамнез, анализы плевральной жидкости и другие исследования, использованные для оценки доброкачественных плевральных выпотов
Анализ плевральной жидкости
Кроме того, анализ плевральной жидкости часто дает важную информацию при оценке доброкачественного плеврального выпота. чтобы помочь установить, требуются ли дальнейшие исследования на злокачественность. В таблице 2 подробно описаны компоненты стандартного тестирования плевральной жидкости и крови, а также более целенаправленных анализов, которые могут быть показаны в конкретных случаях подозрения на доброкачественные выпоты.
Факторы, обуславливающие использование расширенных тестов, могут возникать из-за внешнего вида жидкости или факторов пациента, специфичных для конкретного случая. Например, жидкость молочного цвета увеличивает вероятность хилоторакса и должна быть оценена с запросом уровней триглицеридов и холестерина, а также наличия или отсутствия хиломикронов. Оставление жидкости на скамейке в течение 30 минут также может помочь отличить эмпиему от хилоторакса, поскольку при эмпиеме образуется прозрачный супернатант, тогда как хилезный выпот остается равномерно мутным.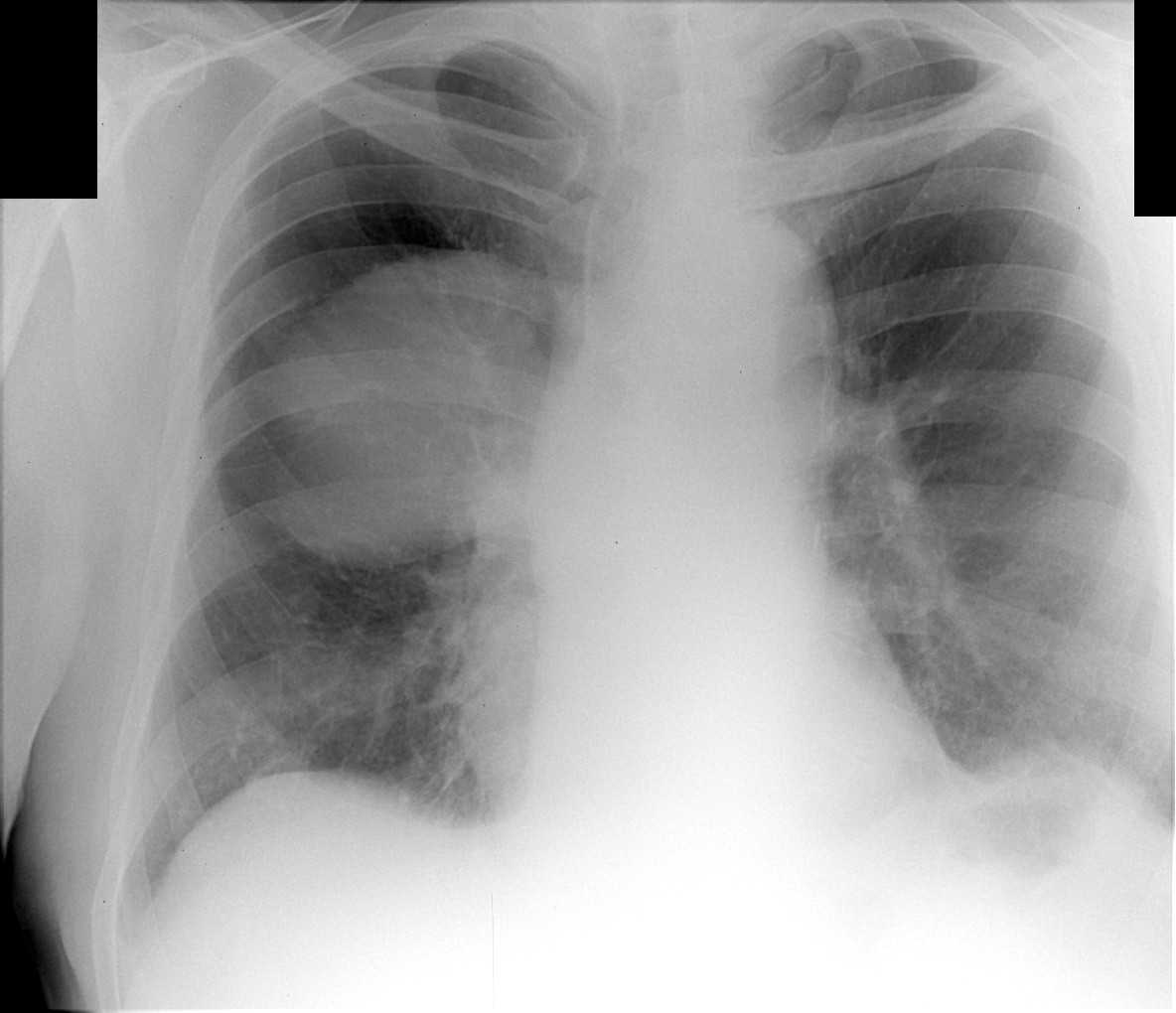
Хотя критерии Света не являются полностью специфичными или чувствительными для идентификации злокачественного новообразования, выпот, классифицируемый как транссудат по этим критериям, сильно указывает на доброкачественную причину и, в частности, повышает вероятность выпота из-за сердечной недостаточности. , почечная недостаточность или печеночный гидроторакс [8]. Однако следует отметить, что около 5% злокачественных плевральных выпотов изначально классифицируются как транссудаты согласно критериям Лайт [9].
На инфекцию плевры обычно указывает низкий pH или низкий уровень глюкозы, значения которых коррелированы [10].Однако эти характеристики жидкости также могут наблюдаться при выпотах, вызванных ревматоидным артритом, злокачественными новообразованиями и перфорацией пищевода [11].
Дифференциальный подсчет клеток тестируется не во всех лабораториях, но дает полезную информацию. В плевральных выпотах обычно преобладают лимфоциты, хотя наличие значительного количества нейтрофилов и эозинофилов может помочь сузить возможные диагнозы.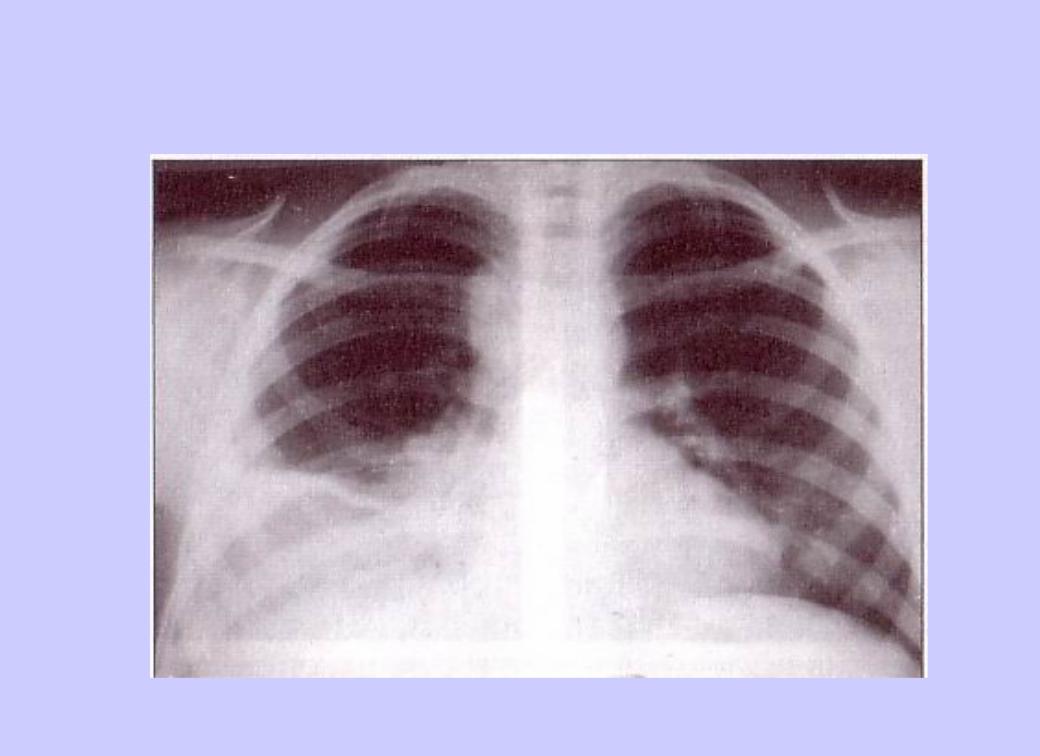 Обычно хронические плевральные выпоты преимущественно заняты лимфоцитами, а из-за более острых процессов — нейтрофилами.Присутствие эозинофилов часто связано с воздухом или кровью в плевральной полости, но остаются другие диагностические возможности [12].
Обычно хронические плевральные выпоты преимущественно заняты лимфоцитами, а из-за более острых процессов — нейтрофилами.Присутствие эозинофилов часто связано с воздухом или кровью в плевральной полости, но остаются другие диагностические возможности [12].
Стандартный биохимический анализ крови при плевральном выпоте, вероятно, будет состоять из полного анализа крови, мочевины и электролитов, функции печени, анализов коагуляции и С-реактивного белка. В определенных случаях могут быть показаны более специфические тесты, включая N-концевой натрийуретический пептид мозга (NT-proBNP), и анализы, такие как ревматоидный фактор, аутоиммунный профиль и цитоплазматические антитела против нейтрофилов.
Во многих случаях доброкачественных выпотов диагноз может быть ясен после первоначальной оценки и исследования плевральной жидкости, хотя у значительного числа пациентов могут потребоваться более подробные исследования.
Визуализация
Рентгенограммы грудной клетки и ультразвуковое исследование грудной клетки играют ключевую роль в оценке и лечении плеврального выпота [13]. Плевральные проявления, видимые на компьютерной томографии (КТ) у пациентов с доброкачественными заболеваниями, могут быть более тонкими, чем у пациентов со злокачественными новообразованиями.Однако при количественной оценке и характеристике плевральных выпотов и утолщения плевры КТ является бесценным инструментом. Ценность использования внутривенного контраста в поздней венозной фазе была продемонстрирована для характеристики утолщения плевры и выявления злокачественного заболевания плевры [14]. Было показано, что аспирация или дренирование плевральной жидкости перед компьютерной томографией существенно не улучшает диагностические характеристики при оценке патологии плевры [15].
Плевральные проявления, видимые на компьютерной томографии (КТ) у пациентов с доброкачественными заболеваниями, могут быть более тонкими, чем у пациентов со злокачественными новообразованиями.Однако при количественной оценке и характеристике плевральных выпотов и утолщения плевры КТ является бесценным инструментом. Ценность использования внутривенного контраста в поздней венозной фазе была продемонстрирована для характеристики утолщения плевры и выявления злокачественного заболевания плевры [14]. Было показано, что аспирация или дренирование плевральной жидкости перед компьютерной томографией существенно не улучшает диагностические характеристики при оценке патологии плевры [15].
Магнитно-резонансная томография (МРТ) в настоящее время не играет рутинной роли в оценке заболевания плевры, но обеспечивает высококачественную визуализацию инвазии грудной клетки при злокачественном заболевании, что отражается в ее использовании при злокачественной мезотелиоме.Это может быть полезно для более молодых пациентов и пациентов, у которых есть подозрения на аномалии мягких тканей грудной клетки.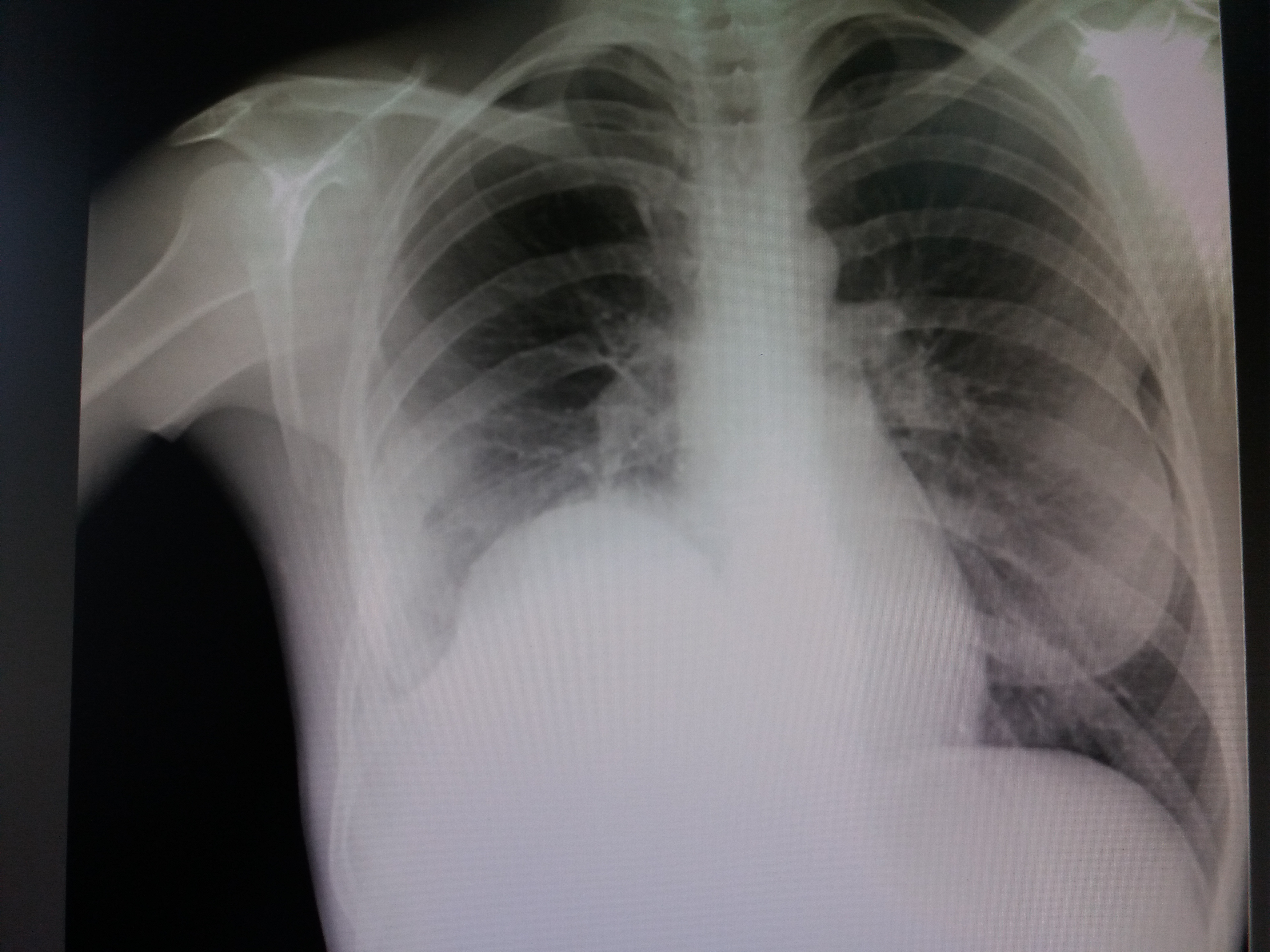 Было продемонстрировано, что МРТ помогает охарактеризовать плевральный выпот как транссудат, простой или сложный экссудат [16]. МРТ и лимфосцинтиграммы могут быть очень полезны для демонстрации места утечки из лимфатической системы в случаях хилоторакса [17].
Было продемонстрировано, что МРТ помогает охарактеризовать плевральный выпот как транссудат, простой или сложный экссудат [16]. МРТ и лимфосцинтиграммы могут быть очень полезны для демонстрации места утечки из лимфатической системы в случаях хилоторакса [17].
Диагностика ткани
Биопсия плевры может быть проведена как закрытая процедура в случае чрескожной биопсии под радиологическим контролем или под прямым визуальным контролем в случае торакоскопии.Было показано, что чувствительность биопсии под контролем КТ при установлении злокачественности плевры превосходит биопсию Абрамса (87% против 47%) [18], хотя в регионах с высокой распространенностью туберкулеза биопсия Абрамса может все еще иметь роль в связи с большей чувствительностью, которую они проявляют при диагностике туберкулеза (82%) [19].
Торакоскопические процедуры могут варьироваться от однопортовой процедуры, проводимой под местной анестезией и седацией, до многопортовой торакоскопической хирургии с видеосвязью (VATS) под общим наркозом.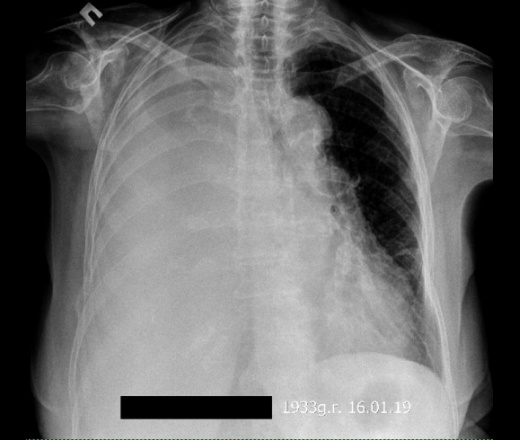 Вопрос о том, какую из этих процедур следует провести, может зависеть от местной доступности и факторов пациента, которые могут указывать на предпочтение более или менее инвазивного подхода.
Вопрос о том, какую из этих процедур следует провести, может зависеть от местной доступности и факторов пациента, которые могут указывать на предпочтение более или менее инвазивного подхода.
Основанием для выполнения биопсии обычно является конкретное исключение злокачественных новообразований, хотя они также могут быть полезны при установлении некоторых незлокачественных заболеваний. Гистопатологические особенности многих незлокачественных выпотов обычно неспецифичны, и изолированная биопсия вряд ли окончательно установит этиологию.Однако существуют заметные исключения, такие как туберкулез, который можно без сомнения установить, если микобактерии будут идентифицированы при биопсии плевры.
Патология выпота
Плевральный выпот вызывается широким спектром процессов, ряд из которых обсуждается ниже. На рисунке 1 показаны множественные состояния и системы органов, потенциально вовлеченные в развитие доброкачественного выпота, а также их характерная классификация по критериям Лайта.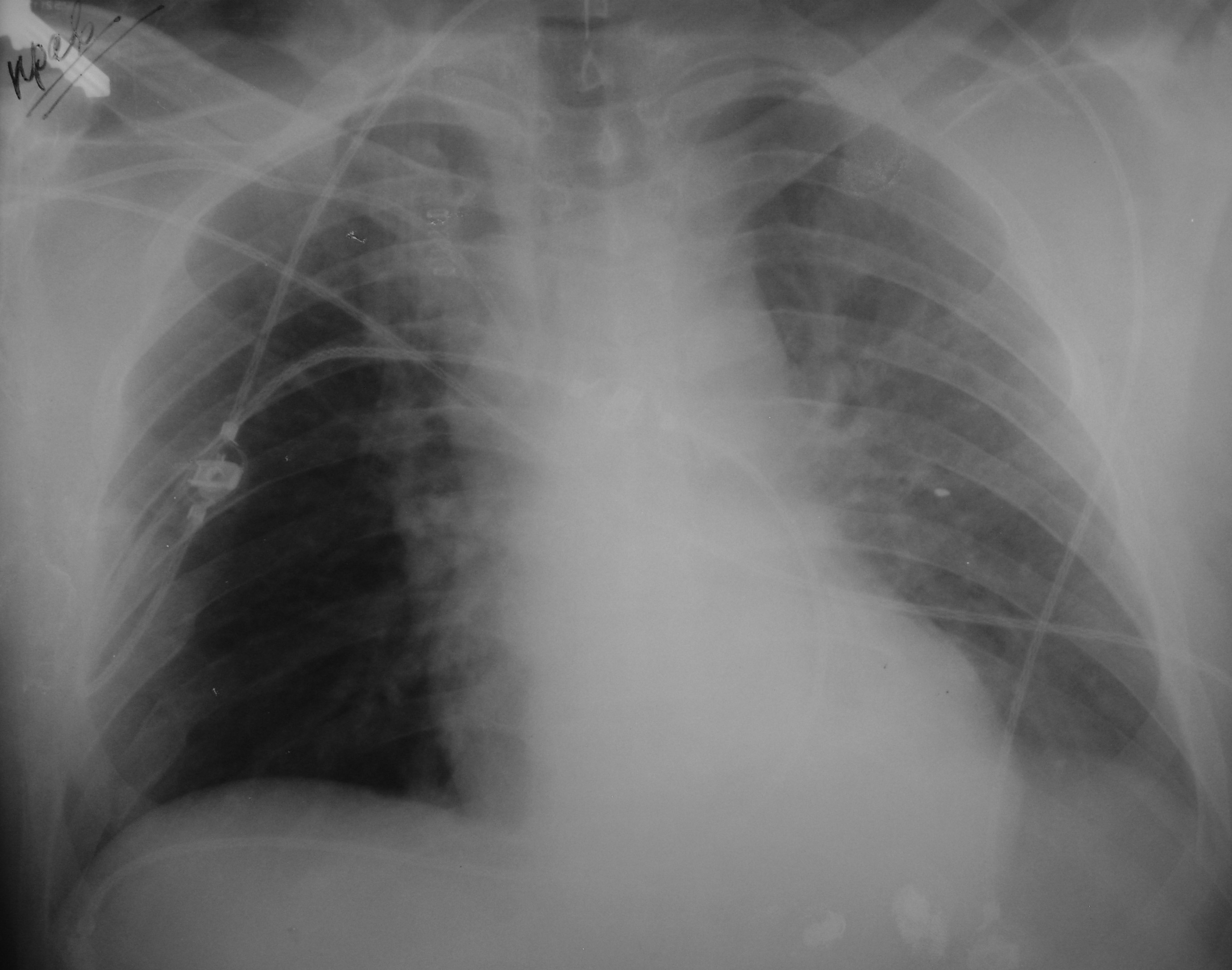
Схематическая диаграмма, иллюстрирующая ряд мультисистемных патологий, ведущих к доброкачественным выпотам, классифицированных по их склонности вызывать экссудаты или транссудаты.
Плевральный выпот развивается из-за увеличения продукции или уменьшения реабсорбции плевральной жидкости или обоих процессов в унисон.
Сердечный
Сердечная недостаточность приводит к образованию плеврального выпота из-за повышения легочного капиллярного давления и, как следствие, утечки в плевральную полость. Это возникает в результате ряда сердечных патологий, включая дисфункцию левого желудочка, которая может быть диастолической или систолической, дисфункцией клапана или констриктивным перикардитом.Распространенность клинически выявленной сердечной недостаточности составляет ~ 3–20 случаев на 1000 населения и заметно увеличивается с возрастом [20]. Из тех пациентов с декомпенсированной сердечной недостаточностью, которым требуется лечение диуретиками, у 87% наблюдается плевральный выпот на КТ [21].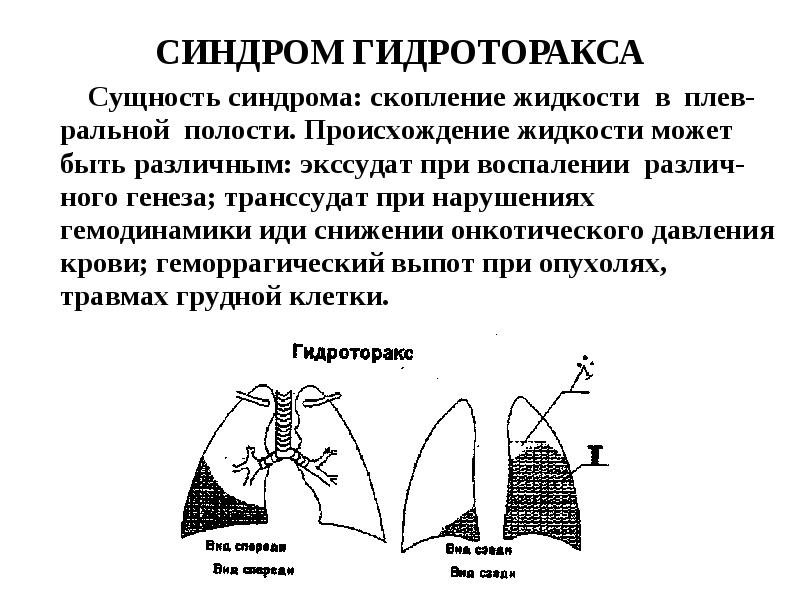 У пациентов с неосложненной сердечной недостаточностью с плевральным выпотом в 73% случаев наблюдается двусторонний выпот [22]. Большая часть этих плевральных выпотов улучшится при оптимизированном лечении сердечной недостаточности. Проспективное исследование 60 пациентов показало, что у 89% пациентов с первоначальным ответом на лечение диуретиками больше не было плеврального выпота через 2 недели наблюдения [21].Лечение обычно включает прием лекарств, таких как диуретики, ингибирование ангиотензинпревращающего фермента, β-блокада или процедуры, такие как ресинхронизация сердца или вмешательство для лечения дисфункции клапана. В последние десятилетия были достигнуты значительные успехи в лечении сердечной недостаточности, что привело к переходу от пациентов с острым декомпенсированным заболеванием к более стабильному и хроническому течению.
У пациентов с неосложненной сердечной недостаточностью с плевральным выпотом в 73% случаев наблюдается двусторонний выпот [22]. Большая часть этих плевральных выпотов улучшится при оптимизированном лечении сердечной недостаточности. Проспективное исследование 60 пациентов показало, что у 89% пациентов с первоначальным ответом на лечение диуретиками больше не было плеврального выпота через 2 недели наблюдения [21].Лечение обычно включает прием лекарств, таких как диуретики, ингибирование ангиотензинпревращающего фермента, β-блокада или процедуры, такие как ресинхронизация сердца или вмешательство для лечения дисфункции клапана. В последние десятилетия были достигнуты значительные успехи в лечении сердечной недостаточности, что привело к переходу от пациентов с острым декомпенсированным заболеванием к более стабильному и хроническому течению.
Хотя плевральный выпот чаще ассоциируется с левосторонней недостаточностью, он также возникает при правосторонней сердечной недостаточности.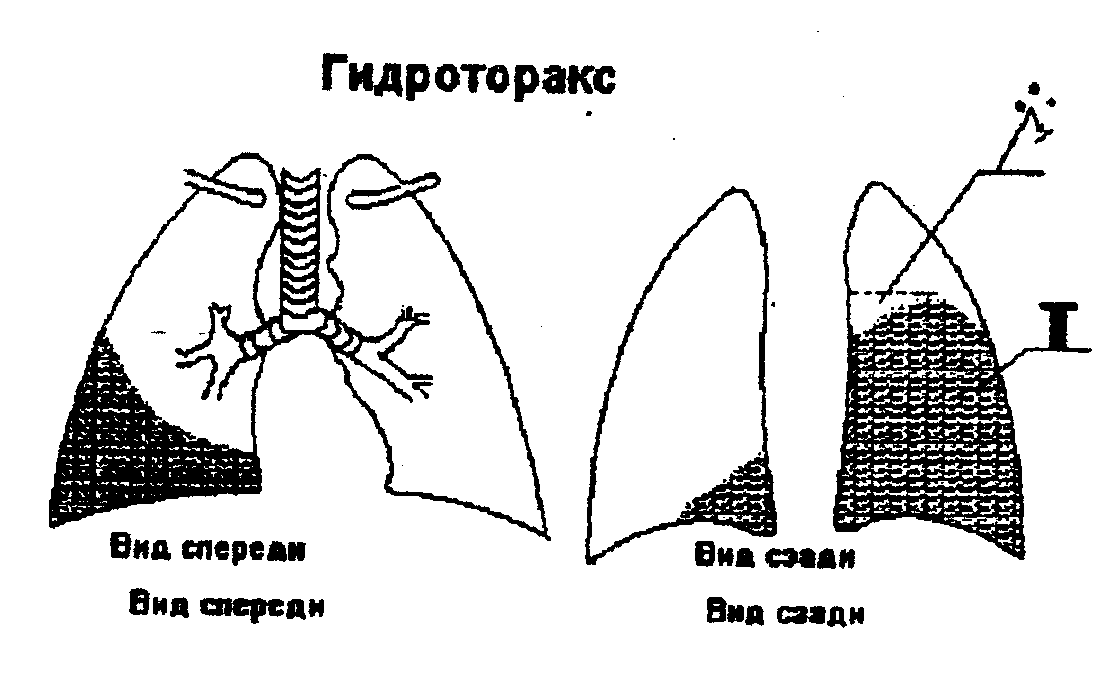 Хотя чаще всего это небольшие выпоты, около 13% пациентов с идиопатической или семейной гипертензией легочной артерии имеют плевральные выпоты, связанные с правосторонней сердечной недостаточностью [23]. Считается, что процесс накопления жидкости происходит из-за процессов, включая снижение реабсорбции плевральной жидкости, повышение гидростатического давления в бронхиальных венах или расширение легочных артерий, препятствующих лимфатическому потоку. Эти выпоты чаще всего бывают правосторонними (58%) или двусторонними (26%) и обычно являются транссудатами [23].Сообщается, что пациенты с сердечным выпотом, получавшие диуретики, имеют повышенный уровень белка в плевральной жидкости по сравнению с его уровнем в крови, в результате чего выпот классифицируется как экссудат по критериям Лайт [24]. У пациентов с экссудативным выпотом с подозрением на сердечную причину корреляция с эхокардиографией или измерением NT-proBNP может быть полезна для выяснения этиологии; Следует проявлять осторожность, чтобы исключить другие соответствующие потенциальные причины, такие как злокачественные новообразования или легочная эмболия.
Хотя чаще всего это небольшие выпоты, около 13% пациентов с идиопатической или семейной гипертензией легочной артерии имеют плевральные выпоты, связанные с правосторонней сердечной недостаточностью [23]. Считается, что процесс накопления жидкости происходит из-за процессов, включая снижение реабсорбции плевральной жидкости, повышение гидростатического давления в бронхиальных венах или расширение легочных артерий, препятствующих лимфатическому потоку. Эти выпоты чаще всего бывают правосторонними (58%) или двусторонними (26%) и обычно являются транссудатами [23].Сообщается, что пациенты с сердечным выпотом, получавшие диуретики, имеют повышенный уровень белка в плевральной жидкости по сравнению с его уровнем в крови, в результате чего выпот классифицируется как экссудат по критериям Лайт [24]. У пациентов с экссудативным выпотом с подозрением на сердечную причину корреляция с эхокардиографией или измерением NT-proBNP может быть полезна для выяснения этиологии; Следует проявлять осторожность, чтобы исключить другие соответствующие потенциальные причины, такие как злокачественные новообразования или легочная эмболия.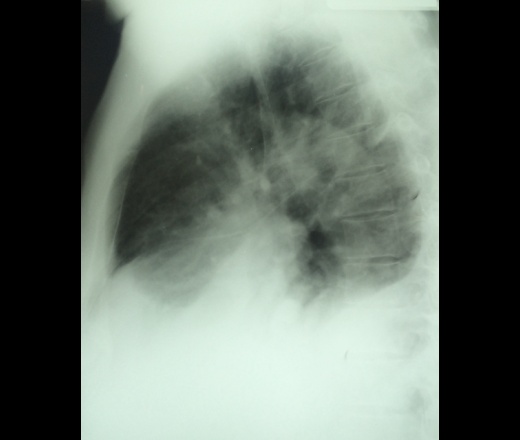
Прямое лечение плеврального выпота из-за сердечной недостаточности может затрудняться наличием двустороннего выпота. Однако, несмотря на то, что изолированные правосторонние или левосторонние выпоты встречаются редко, двусторонние выпоты часто имеют больший лево- или правосторонний компонент [22]. Принимая во внимание одышку, связанную с самой сердечной недостаточностью, пациенты могут получить значительную пользу от дренажа изотопа, который сохраняется, несмотря на оптимизированное лечение сердечной недостаточности.
Плевральный выпот присутствует почти у всех пациентов сразу после аортокоронарного шунтирования и со временем уменьшается, при этом большинство ранних выпотов остаются небольшими и не являются причиной значимых симптомов [25, 26].Плевральный выпот после аортокоронарного шунтирования можно разделить на ранние или поздние излияния, которые считаются отдельными процессами, при этом ранние излияния с большей вероятностью будут геморрагическими, с преобладанием эозинофилов и связанными с высоким уровнем ЛДГ, а более поздние — с большей вероятностью негеморрагический и характеризуется преобладанием лимфоцитов, воспалительным процессом [27].
Из этих пациентов со стойким плевральным выпотом после аортокоронарного шунтирования многим требуется только один торакоцентез, а более длительное лечение требуется редко [28].Плевральные выпоты также возникают как проявление посткардиального повреждения (или синдрома Дресслера) [29].
Печеночный
Печеночный гидроторакс присутствует примерно у 5% пациентов с циррозом печени и асцитом [30]. Печеночные гидротораксы чаще всего правосторонние, хотя они могут быть двусторонними или присутствовать исключительно слева [31]. Считается, что эта тенденция в сторону правой стороны связана с предрасположенностью к дефектам диафрагмы, поражающим правое полушарие [32]. При наличии такого дефекта отрицательное внутригрудное давление приводит к перетоку жидкости из брюшной полости в грудную клетку.
Хотя гидроторакс печени встречается реже, он также возникает при отсутствии клинически очевидного асцита [31]. Однако даже у этих пациентов был продемонстрирован односторонний поток радиоактивно меченного коллоида через диафрагму, что позволяет предположить, что у этих пациентов поток через диафрагму соответствует скорости образования асцита [33].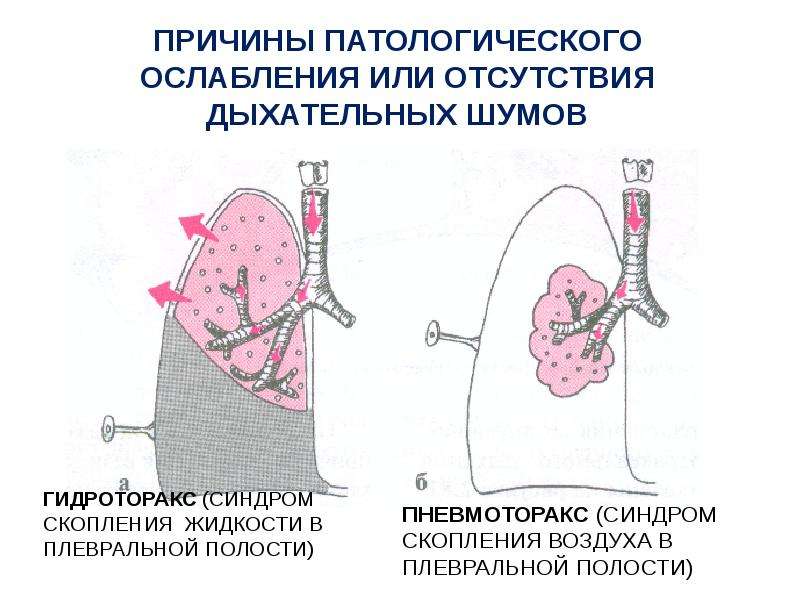
Наличие гидроторакса печени при циррозе печени связано с особенно плохим прогнозом. В исследовании 77 пациентов с гидротораксом печени только 33 (43%) выжили в течение 1 года после постановки диагноза [31].
Гидроторакс печени лечится с помощью ограничения соли и диуретической терапии, а лечение асцита может привести к увеличению количества жидкости над диафрагмой. Используется хирургическое лечение диафрагмы, хотя чаще, при наличии персистирующей жидкости, может потребоваться трансъямгулярный внутрипеченочный портосистемный шунт или трансплантация печени. Если эти процедуры неэффективны, недоступны или противопоказаны, может потребоваться прямое удаление плевральной жидкости. Кроме того, некоторые центры используют постоянные плевральные катетеры в качестве моста к более окончательному лечению, например, к трансплантации печени.
Потеря жидкости и белка является проблемой, которая особенно актуальна для пациентов с плевральными выпотами из-за печеночного гидроторакса, и привела к практике внутривенного введения раствора человеческого альбумина, который используется у пациентов с циррозом печени, требующих парацентеза. Хотя четких указаний или доказательств не существует, гепатологи часто рекомендуют использовать раствор человеческого альбумина для пациентов с гидротораксом печени, у которых обычно большой объем жидкости, отводимой через через постоянный плевральный катетер, может быть особой проблемой [34].
Хотя четких указаний или доказательств не существует, гепатологи часто рекомендуют использовать раствор человеческого альбумина для пациентов с гидротораксом печени, у которых обычно большой объем жидкости, отводимой через через постоянный плевральный катетер, может быть особой проблемой [34].
Почечная
В ретроспективном обзоре когорты из 257 пациентов, получавших длительный гемодиализ по поводу почечной недостаточности, у 52 (20%) пациентов в анамнезе был плевральный выпот [35]. Эти плевральные выпоты чаще всего были вызваны гиперволемией (62%) и обычно связаны с двусторонними транссудативными выпотами. Остальные были связаны с сердечной недостаточностью, уремией или инфекцией. Наблюдательное исследование 430 пациентов с хронической болезнью почек (стадии 3-5) показало, что частота плевральных выпотов составляет 6.7%, что существенно ниже, чем у пациентов с более тяжелым заболеванием, требующим заместительной почечной терапии [36].
Плевральный выпот, связанный с почечной недостаточностью, обычно бывает двусторонним и классифицируется как транссудат по критериям Лайта. Среди пациентов, у которых на длительном гемодиализе развивается экссудативный плевральный выпот, наиболее частой причиной является уремический плеврит, который может быть односторонним и двусторонним и развивается у ~ 4% пациентов, находящихся на длительном диализе. Уремический плеврит обычно связан с выпотом, окрашенным кровью, а биопсия указывает на фибринозный плеврит [35].
Среди пациентов, у которых на длительном гемодиализе развивается экссудативный плевральный выпот, наиболее частой причиной является уремический плеврит, который может быть односторонним и двусторонним и развивается у ~ 4% пациентов, находящихся на длительном диализе. Уремический плеврит обычно связан с выпотом, окрашенным кровью, а биопсия указывает на фибринозный плеврит [35].
Пациенты, получающие длительную заместительную почечную терапию, вероятно, будут более уязвимы к плевральной инфекции, учитывая потенциальную степень иммунодефицита, наблюдаемую у этих пациентов. Поэтому необходимость тщательно исключить возможность инфицирования плевры является важным фактором для этой группы пациентов.
Перитонеальный диализ представляет собой альтернативный процесс, посредством которого может накапливаться плевральный выпот у пациентов с почечной недостаточностью [37]. Сообщается, что это осложнение влияет на 1.6% пациентов, получающих хронический амбулаторный перитонеальный диализ, могут иметь показания по снижению адекватности перитонеального диализа.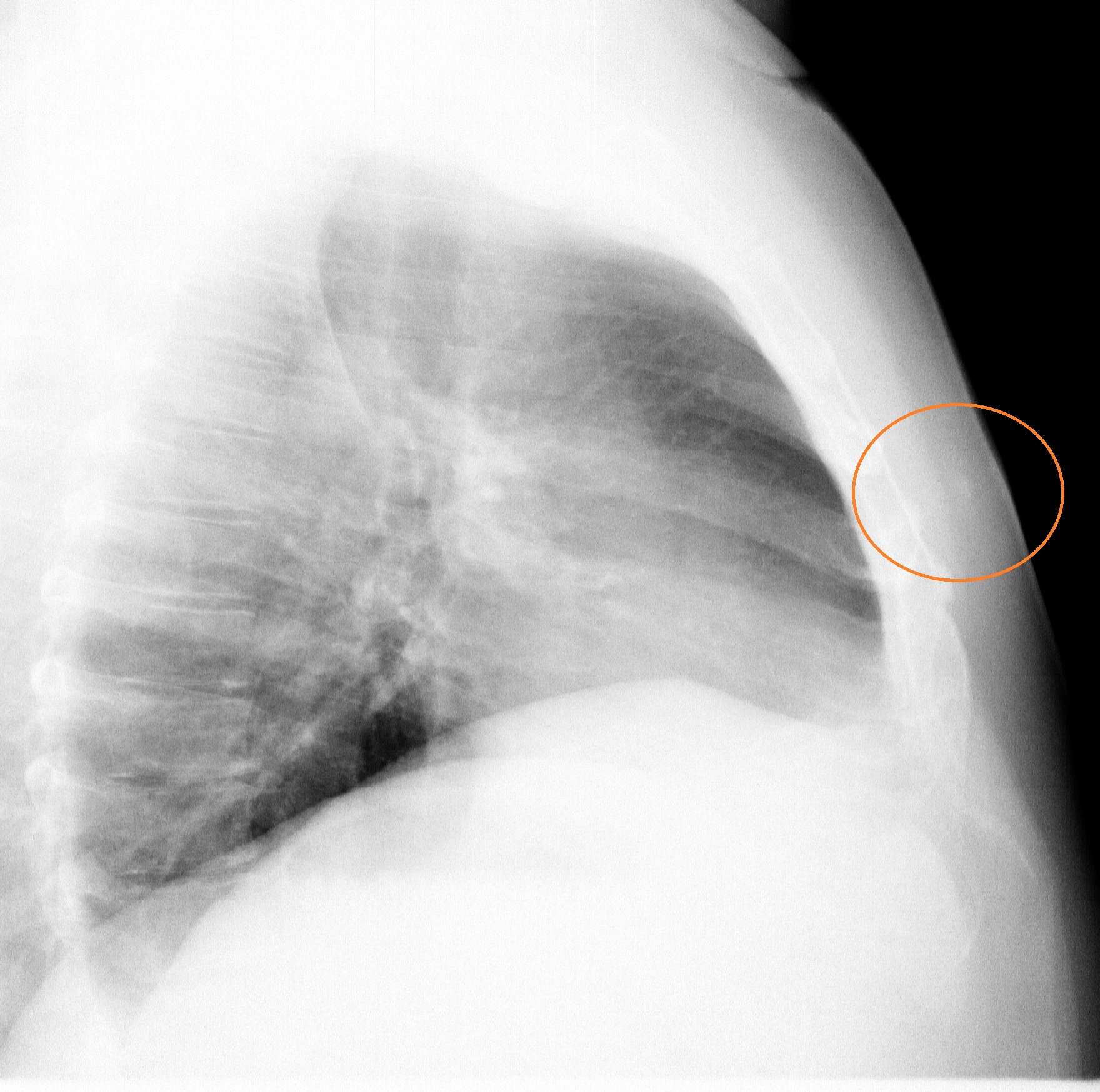 Развитие плеврального выпота может произойти примерно во время начала перитонеального диализа или намного позже; 50% выпотов возникают в течение 30 дней после начала перитонеального диализа [38]. Биохимия плевральной жидкости в таких случаях будет характерно представлять компоненты перитонеального диализата, обычно с очень низким содержанием белка и лактатдегидрогеназы.Подобно плевральной жидкости, которая накапливается при циррозе печени из-за диафрагмального транзита асцита, гораздо более распространены правосторонние плевральные выпоты из-за перитонеального диализа. Рекомендуемые варианты лечения плевральных выпотов, вызванных перитонеальным диализом, включают консервативные меры, такие как временный переход на гемодиализ, использование более частых и меньших объемов обмена, химический плевродез или хирургический ВАТС [39].
Развитие плеврального выпота может произойти примерно во время начала перитонеального диализа или намного позже; 50% выпотов возникают в течение 30 дней после начала перитонеального диализа [38]. Биохимия плевральной жидкости в таких случаях будет характерно представлять компоненты перитонеального диализата, обычно с очень низким содержанием белка и лактатдегидрогеназы.Подобно плевральной жидкости, которая накапливается при циррозе печени из-за диафрагмального транзита асцита, гораздо более распространены правосторонние плевральные выпоты из-за перитонеального диализа. Рекомендуемые варианты лечения плевральных выпотов, вызванных перитонеальным диализом, включают консервативные меры, такие как временный переход на гемодиализ, использование более частых и меньших объемов обмена, химический плевродез или хирургический ВАТС [39].
Другие причины
Широкий спектр менее распространенных патологий может вызывать плевральный выпот, диагностика которого может быть значительно менее простой, чем при сердечной, печеночной или почечной недостаточности, лежащая в основе недостаточности органов которой, вероятно, будет распознана до развития плеврального выпота.
Доброкачественный асбестовый плевральный выпот — это диагноз исключения, при котором возможность мезотелиомы требует тщательного рассмотрения, как и у всех пациентов, подвергшихся воздействию асбеста и заболеванию плевры в анамнезе. Доброкачественный асбестовый плевральный выпот обычно односторонний и характеризуется экссудативным выпотом, который обычно возникает в течение 15 лет после воздействия асбеста, но может возникнуть намного позже [40]. Вытекание может протекать бессимптомно или быть связано с одышкой и болью в груди, и примерно в одной трети случаев в жидкости присутствует высокий уровень эозинофилов [41].Биопсия плевры необходима для исключения злокачественного новообразования, а радиологическое наблюдение в течение 2-летнего периода с КТ грудной клетки рекомендуется в связи с необходимостью установить, есть ли прогрессирующая патология и утолщение плевры. Доброкачественный асбестовый плевральный выпот часто сопровождается преходящим выпотом, длительное лечение которого может не потребоваться.
Примерно 50% пациентов с синдромом желтого ногтя имеют плевральный выпот наряду с лимфатическим отеком, хроническими респираторными проявлениями и аномалиями самих ногтей [42].Анализ плевральной жидкости обычно выявляет лимфоцитарный выпот, хотя у некоторых пациентов может развиться хилоторакс. Биопсия может выявить хронический фиброзный плеврит [42].
Тромбоэмболия легочной артерии
Плевральный выпот — частая находка у 30% пациентов с тромбоэмболией легочной артерии и, как полагают, вызван самой ишемией или выбросом цитокинов [43]. Однако эти выпоты обычно присутствуют не более 1 месяца [44], а 90% составляют менее одной трети гемиторакса [45].Степень одышки, непропорциональная размеру плеврального выпота и плевритной боли в груди, может быть признаком выпота, связанного с тромбоэмболией легочной артерии.
Хотя плевральные выпоты обычно присутствуют на той же стороне, что и легкое, пораженное тромбоэмболией легочной артерии, они могут быть односторонними, несмотря на двустороннюю эмболию, или двусторонними, если легочная эмболия односторонняя.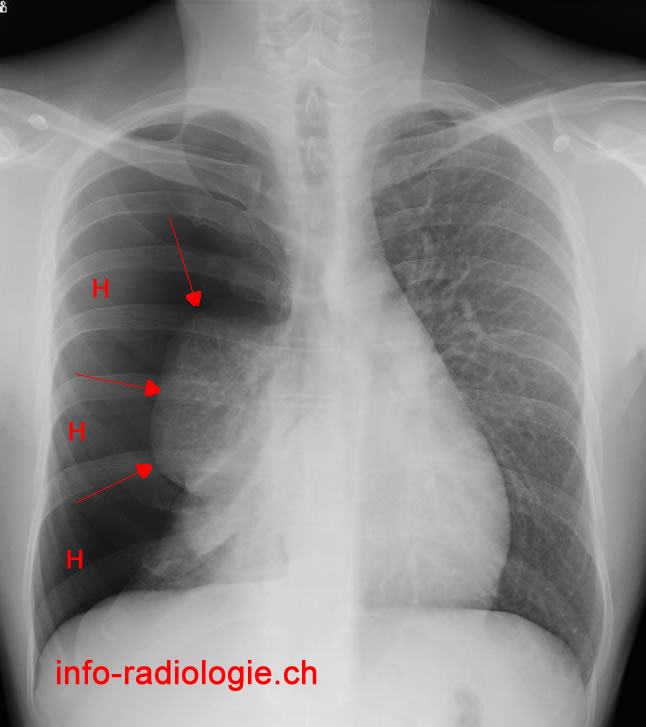 Удивительно, но выпот также присутствует односторонне и контралатерально по отношению к эмболии на ∼7.5% пациентов с излияниями вследствие тромбоэмболии легочной артерии [45].
Удивительно, но выпот также присутствует односторонне и контралатерально по отношению к эмболии на ∼7.5% пациентов с излияниями вследствие тромбоэмболии легочной артерии [45].
Более ранние исследования с методологическими ограничениями показали, что плевральный выпот из-за тромбоэмболии легочной артерии может быть транссудатом; однако более поздние исследования показали, что все выпоты, связанные с тромбоэмболией легочной артерии, являются экссудатами в соответствии с критериями Лайта [45]. Кроме того, плевральная жидкость обычно окрашена кровью и преобладает нейтрофилы [45]. Поскольку эти излияния обычно очень малы, более крупный излияние может потребовать оценки сопутствующей причины.
Панкреатит
Повышенный уровень амилазы плевральной жидкости, на который указывает уровень амилазы плевральной жидкости, превышающий сывороточный уровень амилазы, или уровень амилазы плевральной жидкости, превышающий верхний предел нормы сывороточного значения, свидетельствует об остром или хроническом панкреатите. Разрыв псевдокисты поджелудочной железы и образование свища могут привести к прямому сообщению с грудной полостью и скоплению плевральной жидкости.
Разрыв псевдокисты поджелудочной железы и образование свища могут привести к прямому сообщению с грудной полостью и скоплению плевральной жидкости.
Повышенное содержание амилазы в плевральной жидкости также наблюдается при выпотах из-за разрыва пищевода и, возможно, также при злокачественных плевральных выпотах.В сложных случаях изоферментный анализ может позволить провести различие между амилазой слюны и панкреатической амилазой.
Самовоспалительный
Ревматоидный артрит связан с различными легочными и плевральными проявлениями. Высокий титр ревматоидного фактора является прогностическим признаком плеврального выпота наряду с другими внесуставными особенностями. Ревматоидное заболевание плевры чаще встречается у мужчин [46]. Хотя плевральный выпот описан у 3-5% пациентов с ревматоидным артритом, гораздо чаще обнаруживаются отклонения на рентгенограммах грудной клетки [47].Плевральные выпоты, связанные с ревматоидным артритом, обычно безболезненны, характеризуются как экссудаты, имеют низкие pH и низкий уровень глюкозы, и поэтому их можно спутать с инфекцией плевры.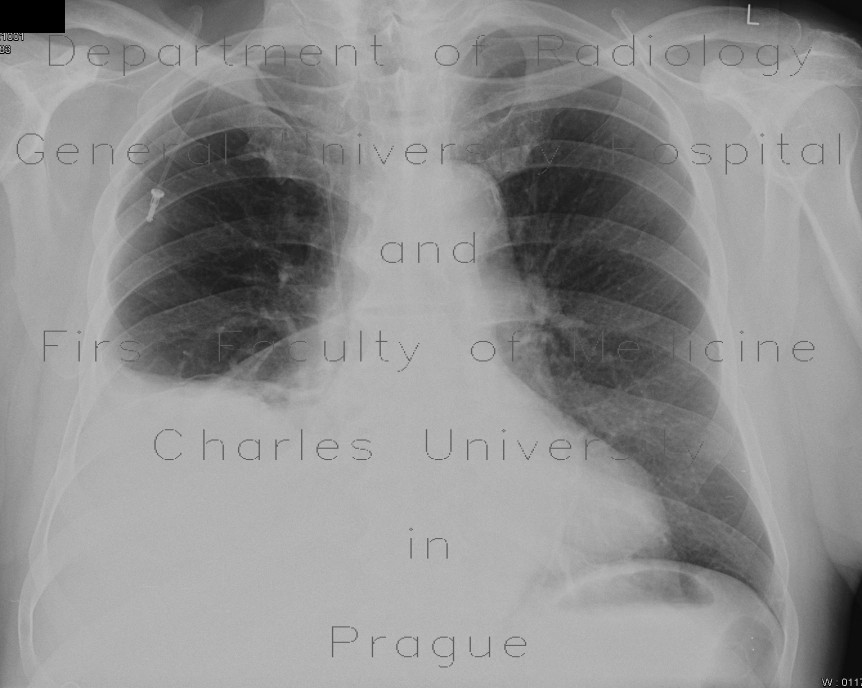
У пациентов с ревматоидным артритом с плевральным выпотом возможность лекарств, вызывающих выпот, должна рассматриваться как ряд антиревматоидных терапий, включая метотрексат, сульфасалазин и D -пеницилламин.
Системная красная волчанка может вызывать плевральный выпот непосредственно через волчаночный плеврит или через вторичный процесс, такой как почечная недостаточность, сердечная недостаточность или тромбоэмболия легочной артерии [47].Плевральные выпоты, вызванные волчанкой, обычно имеют более высокий уровень глюкозы по сравнению с теми, которые связаны с ревматоидным артритом, и могут вызывать значительную боль в груди как часть синдрома серозита. Высокие титры антиядерных антител чувствительны, но не специфичны для волчаночного выпота; высокие титры антинуклеарных антител также могут наблюдаться при злокачественных плевральных выпотах [48]. Однако клетки красной волчанки считаются очень специфичными.
Заболевания соединительной ткани, такие как системный склероз, смешанное заболевание соединительной ткани, гранулематоз с полиангиитом, анкилозирующий спондилит и болезнь Стилла, также могут иметь признаки поражения плевры.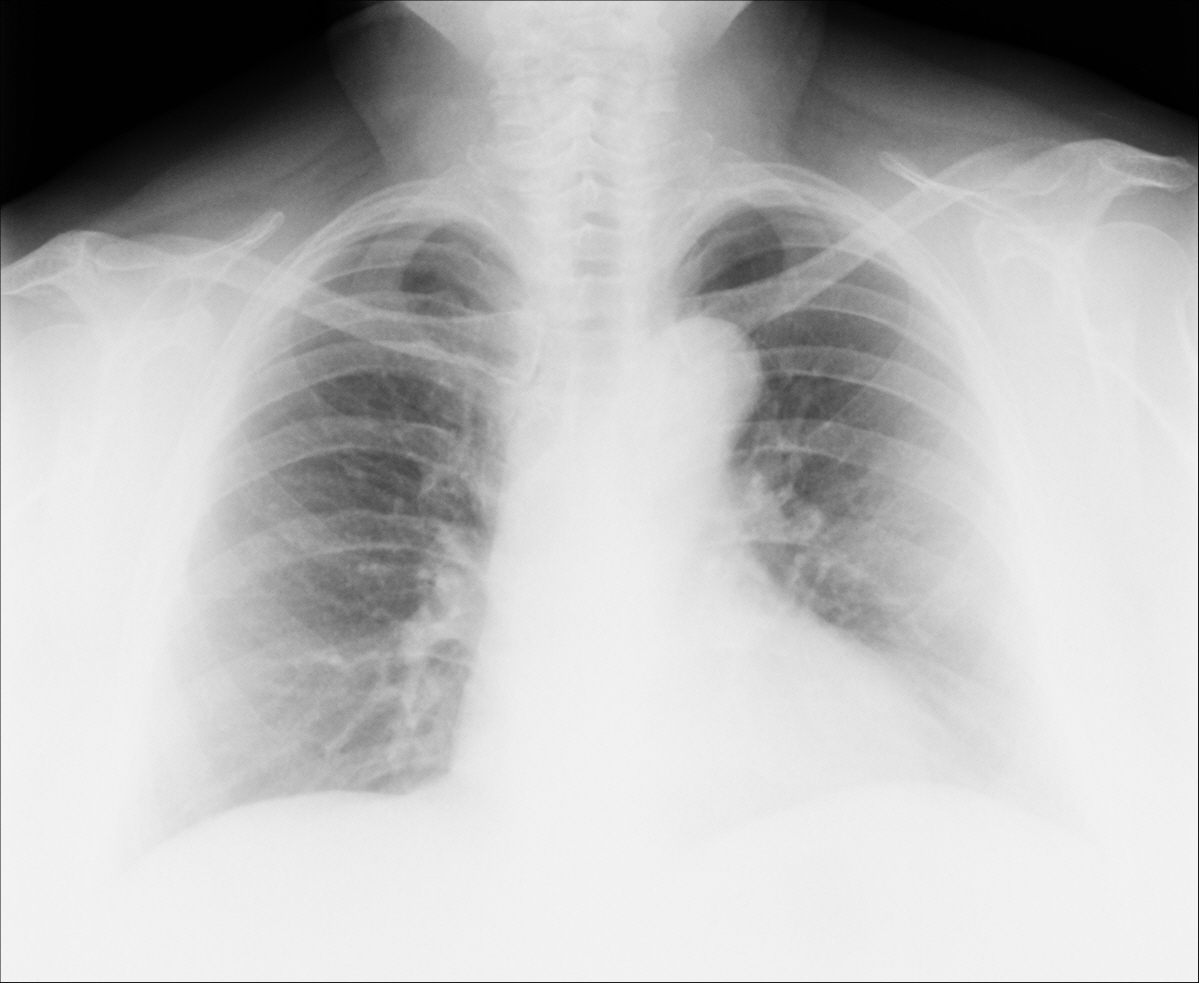 Семейная средиземноморская лихорадка может вызвать воспаление плевры, связанное с односторонней плевритной болью в груди и плевральными выпотами, которые обычно бывают небольшими и непродолжительными.
Семейная средиземноморская лихорадка может вызвать воспаление плевры, связанное с односторонней плевритной болью в груди и плевральными выпотами, которые обычно бывают небольшими и непродолжительными.
Хилоторакс
Хилоторакс может возникнуть в результате разрыва грудного протока на его пути от цистерны хили вверх по заднему средостению до левой подключичной вены. Прекращение оттока хилуса приводит к накоплению жидкости в грудной полости. Поскольку грудной проток пересекает среднюю линию, хилоторакс может присутствовать как в гемитораксе, так и с обеих сторон.
Примерно половина хилотораксов возникает в результате травм. Из остальных 38% вызваны злокачественными новообразованиями, чаще всего лимфомой или лейкемией. Незлокачественные причины включают врожденные лимфатические нарушения, такие как болезнь Горама или Милроя, или такие состояния, как лимфангиома, лимфангиолейомиоматоз, синдром желтого ногтя или волчанка, или могут быть вторичными по отношению к хилезному асциту, чаще всего осложнению цирроза печени [49].
Хилоторакс представляет собой патологический механизм, отличный от механизмов, характерных для большинства других доброкачественных выпотов, и требует особого рассмотрения.Диагноз хилоторакса часто ставится на основании типичного внешнего вида жидкости и легко устанавливается на основании биохимии плевральной жидкости или наличия хиломикронов, но в некоторых случаях внешний вид может быть ошибочно принят за гнойный выпот из-за инфекции. При тщательном соблюдении диеты с пониженным содержанием жиров она может уменьшить выделение хилуса и привести к самопроизвольному закрытию дефекта грудного протока. В случае неудачи может потребоваться хирургическая перевязка или чрескожная эмболизация, чтобы напрямую заблокировать утечку хилуса.Лимфосцинтиграфия может помочь определить место утечки (рис. 2).
РИСУНОК 2 Визуализация лимфосцинтиграммы и ОФЭКТ-КТ (однофотонная эмиссионная компьютерная томография в сочетании со встроенной компьютерной томографией с низкой дозой) у пациента с хилотораксом.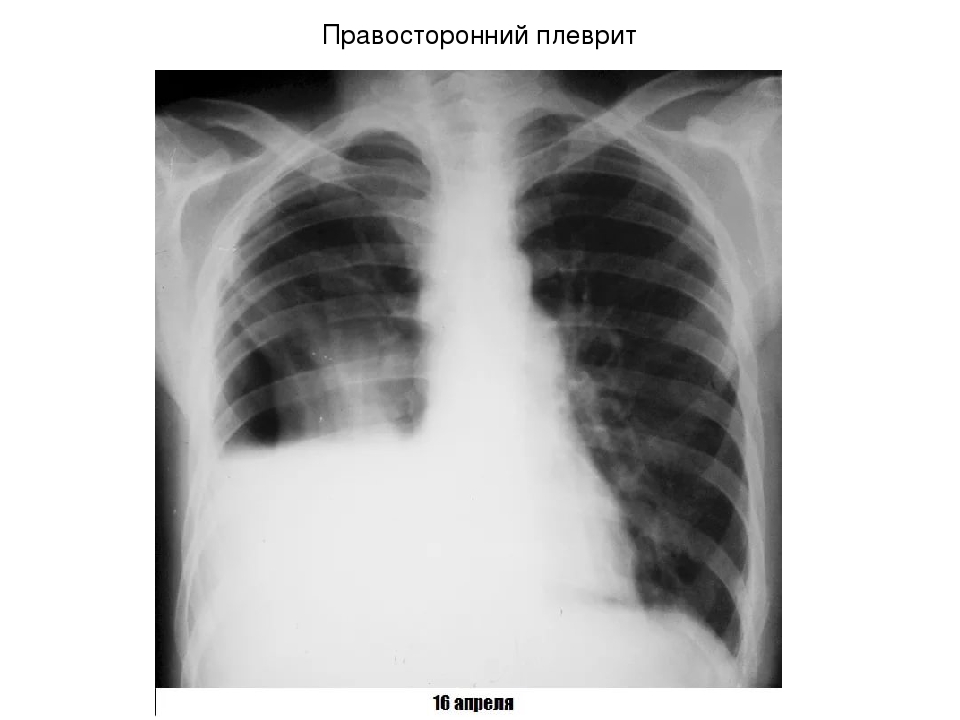 У 74-летнего мужчины с неходжкинской лимфомой после ранее проведенного талькового плевродеза был рецидив правостороннего плеврального выпота. Был вставлен межреберный катетер и дренировано> 3,5 л молочной жидкости с уровнем триглицеридов 17 ммоль · л -1 , что подтверждает хилоторакс.Отток хилуса уменьшился, но продолжался, несмотря на полное питание родителей. Компьютерная томография брюшной полости также показала сливающееся лимфоматозное образование вокруг аорты и нижней полой вены с асцитом и лимфаденопатией. Лимфосцинтиграфия была проведена для определения точки утечки хилуса. Меченый Tc99 человеческий сывороточный альбумин-DTPA инъецировали в межпальцевое перепончатое пространство первой педали с двух сторон, и серийную ОФЭКТ-КТ всего тела выполняли с интервалами от 90 мин до 6,5 ч после введения индикатора.Этот случай иллюстрирует важность лимфангиосцинтиграфии Tc99, поскольку она выявила место утечки хилуса в брюшной полости для правого хилоторакса (вместо утечки в грудной части грудного протока) и изменила тактику ведения пациента.
У 74-летнего мужчины с неходжкинской лимфомой после ранее проведенного талькового плевродеза был рецидив правостороннего плеврального выпота. Был вставлен межреберный катетер и дренировано> 3,5 л молочной жидкости с уровнем триглицеридов 17 ммоль · л -1 , что подтверждает хилоторакс.Отток хилуса уменьшился, но продолжался, несмотря на полное питание родителей. Компьютерная томография брюшной полости также показала сливающееся лимфоматозное образование вокруг аорты и нижней полой вены с асцитом и лимфаденопатией. Лимфосцинтиграфия была проведена для определения точки утечки хилуса. Меченый Tc99 человеческий сывороточный альбумин-DTPA инъецировали в межпальцевое перепончатое пространство первой педали с двух сторон, и серийную ОФЭКТ-КТ всего тела выполняли с интервалами от 90 мин до 6,5 ч после введения индикатора.Этот случай иллюстрирует важность лимфангиосцинтиграфии Tc99, поскольку она выявила место утечки хилуса в брюшной полости для правого хилоторакса (вместо утечки в грудной части грудного протока) и изменила тактику ведения пациента. Пациент был направлен на лучевую терапию по поводу опухоли живота. а) Лимфосцинтиграмма, показывающая место утечки хилуса в брюшной полости через 2 часа после инъекции. б) ОФЭКТ-КТ с низкой дозой показала скопление индикатора под диафрагмой, что подтвердило утечку хилуса из брюшного источника в брюшную полость.c) Последующая лимфосцинтиграмма показала поглощение индикатора над правой плевральной полостью, подтверждая, что утечка хилуса из брюшной полости мигрировала трансдиафрагмально, вызывая правый хилоторакс через 6,5 ч после инъекции. (Изображения любезно предоставлены А. Йогендраном, Университет Западной Австралии, Перт, Австралия).
Пациент был направлен на лучевую терапию по поводу опухоли живота. а) Лимфосцинтиграмма, показывающая место утечки хилуса в брюшной полости через 2 часа после инъекции. б) ОФЭКТ-КТ с низкой дозой показала скопление индикатора под диафрагмой, что подтвердило утечку хилуса из брюшного источника в брюшную полость.c) Последующая лимфосцинтиграмма показала поглощение индикатора над правой плевральной полостью, подтверждая, что утечка хилуса из брюшной полости мигрировала трансдиафрагмально, вызывая правый хилоторакс через 6,5 ч после инъекции. (Изображения любезно предоставлены А. Йогендраном, Университет Западной Австралии, Перт, Австралия).
Выпоты холестерина (или псевдохилезные выпоты) могут иметь вид, похожий на молочный, как истинный хилезный выпот, но их можно отличить после измерения уровней триглицеридов и холестерина.Двумя наиболее частыми причинами излияния холестерина являются туберкулез и ревматоидное заболевание плевры; Гельминтозы и случаи вторичных злокачественных новообразований встречаются реже [50].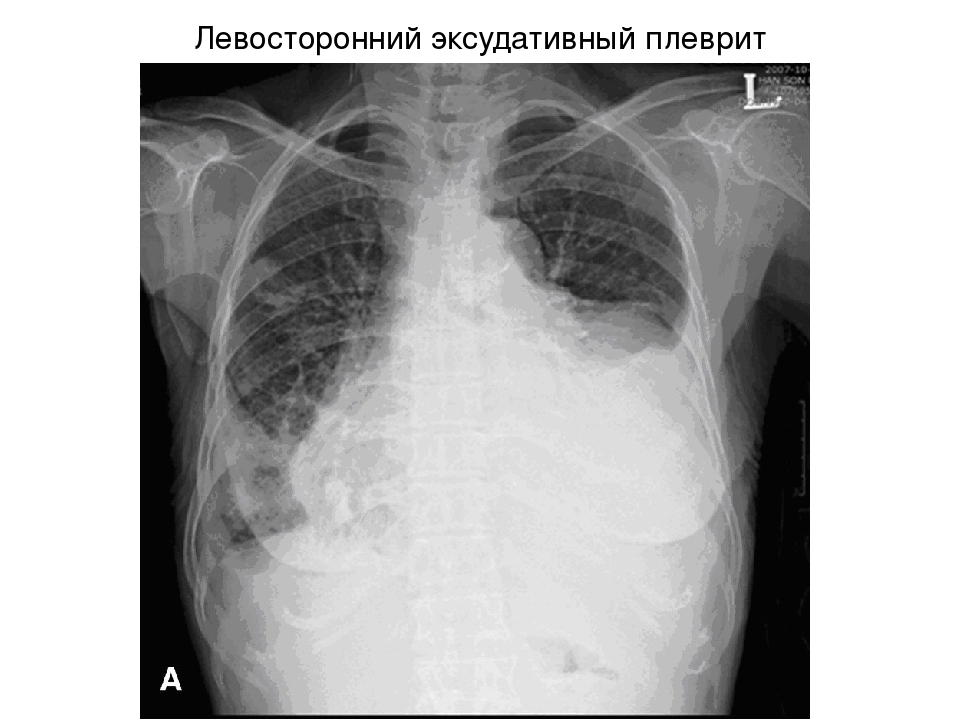
Захваченное легкое
Захватывающее легкое (нерасширяемое) может вызвать плевральный выпот из-за развития более сильного отрицательного плеврального давления, вызванного утолщением висцеральной плевры, препятствующим расширению легкого [51]. Это отрицательное давление способствует перемещению из плевральных капилляров в плевральную полость.Часто развитие застойного легкого является следствием патологического процесса, уже приводящего к плевральному выпоту, после которого утолщение висцеральной плевры способствует сохранению выпота [52]. Этот процесс может происходить в контексте давнишнего излияния любой причины. Однако в качестве возможных причин описаны перенесенная в анамнезе инфекция плевры, торакальная хирургия, ревматоидное заболевание плевры, облучение грудной клетки или гемоторакс [52].
Ятрогенный
Плевральный выпот, вызванный лекарствами, встречается редко, хотя потенциально может быть задействован широкий спектр лекарств.Сообщается, что более 70 лекарственных препаратов вызывают плевральный выпот, среди них сердечно-сосудистые препараты и препараты эрголина, а также химиотерапевтические препараты [53].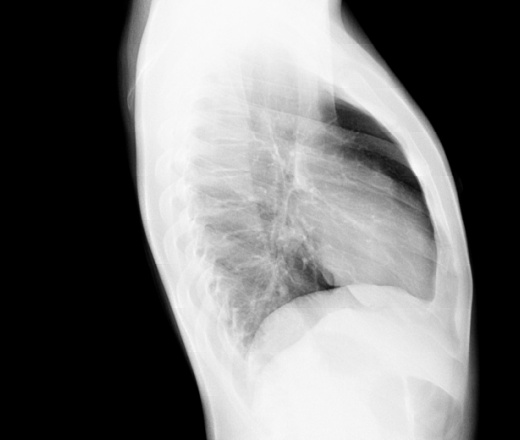 Более часто ассоциированные препараты включают метотрексат, амиодарон и нитрофурантоин [13]. Механизмы включают гиперчувствительность, прямую токсичность, продукцию свободных радикалов и химическое воспаление [54]. Ряд лекарств может вызвать излияние при волчаночном плеврите. Эозинофилия плевральной жидкости может предупредить врача о возможности лекарственного выпота, хотя это открытие не является ни чувствительным, ни специфическим.Помимо лекарств, ятрогенные плевральные выпоты могут возникать как осложнение терапевтических вмешательств, таких как лучевая терапия.
Более часто ассоциированные препараты включают метотрексат, амиодарон и нитрофурантоин [13]. Механизмы включают гиперчувствительность, прямую токсичность, продукцию свободных радикалов и химическое воспаление [54]. Ряд лекарств может вызвать излияние при волчаночном плеврите. Эозинофилия плевральной жидкости может предупредить врача о возможности лекарственного выпота, хотя это открытие не является ни чувствительным, ни специфическим.Помимо лекарств, ятрогенные плевральные выпоты могут возникать как осложнение терапевтических вмешательств, таких как лучевая терапия.
Плевральная жидкость в некоторых случаях может быть экзогенной жидкостью, которая накапливается в плевральной полости в результате транзита жидкости из другой полости тела, например, при перитонеальном диализе, или ятрогенных последствий неправильного размещения центральных венозных катетеров, перфорации пищевода или в случае спинальной или урологической хирургии — скопление спинномозговой жидкости или мочи, соответственно, в плевральной полости. Управление этими процессами здесь не обсуждается.
Управление этими процессами здесь не обсуждается.
Лечение доброкачественных плевральных выпотов
Лечение незлокачественных плевральных выпотов в основном направлено на облегчение симптомов. Накопление плеврального выпота может значительно увеличить уровень одышки у пациента со значительным уже существующим бременем симптомов сопутствующих состояний. Незлокачественные выпоты сами по себе не представляют значительного риска смертности, но являются причиной значительных заболеваний, адекватное лечение которых зависит от выявления основного заболевания.
Лечение основной этиологии
Решающее значение имеет лечение основной причины скопления плеврального выпота. Такое лечение может ослабить или привести к полному исчезновению выпота. Кроме того, во многих случаях такое лечение может облегчить симптомы или улучшить прогноз независимо от плеврального выпота.
В этой статье не рассматривается прямое лечение всех потенциальных патологий, которые приводят к плевральным выпотам; поэтому здесь основное внимание будет уделено непосредственному лечению самого выпота. У значительного числа пациентов может потребоваться прямое вмешательство либо для удаления плевральной жидкости, либо для предотвращения ее накопления.
У значительного числа пациентов может потребоваться прямое вмешательство либо для удаления плевральной жидкости, либо для предотвращения ее накопления.
Целенаправленное ведение плевральной жидкости
Аспирация плевральной жидкости может потребоваться до окончательного установления этиологии, а у других пациентов — после подтверждения диагноза. У небольшого числа пациентов, несмотря на все усилия, может оказаться невозможным поставить четкий диагноз, а у других может оказаться, что лечение, направленное на устранение симптомов, может быть прагматическим подходом, предпочтительным по сравнению с текущими и потенциально более инвазивными исследованиями, особенно у пациентов с неблагоприятным прогнозом.Интересно отметить, что удаление плевральной жидкости, по-видимому, приводит к уменьшению одышки, не отраженному напрямую степенью улучшения газообмена [55].
Варианты лечения, используемые для пациентов с доброкачественными плевральными выпотами, тесно связаны с теми, которые используются для пациентов со злокачественными заболеваниями, у которых доказательная база для спектра доступных методов лечения часто более сильна.
При некоторых незлокачественных плевральных выпотах может потребоваться только наблюдение.Небольшие и бессимптомные плевральные выпоты, возникающие вскоре после кардиохирургической операции, могут, например, разрешиться спонтанно, и любой доброкачественный выпот, достигающий устойчивого состояния, не вызывая симптомов, не требует вмешательства.
Терапевтическая аспирация
Терапевтическая аспирация играет важную роль в лечении любого плеврального выпота. Во время получения образца плевральной жидкости для диагностических целей значительный объем может быть удален для терапевтических целей.Это должно улучшить симптомы пациента в течение периода, в котором может проводиться диагностическая оценка, позволяет оценить скорость накопления жидкости, предоставляет доказательства степени симптоматического улучшения, которое может быть достигнуто за счет удаления жидкости, и проясняет, есть ли какие-либо доказательства. захваченного легкого, которые могут направить дальнейшее лечение.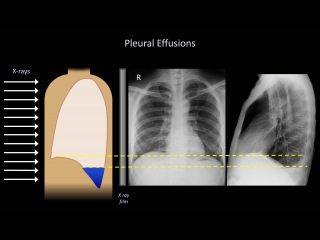
Для некоторых пациентов терапевтическая аспирация может представлять собой законный терапевтический вариант в долгосрочной перспективе. В зависимости от скорости повторного накопления жидкости терапевтические устремления могут потребоваться только с частотой, приемлемой как для врачей, так и для пациентов.Обратной стороной этого подхода является то, что симптомы могут постепенно ухудшаться по мере накопления жидкости. Поскольку эту стратегию можно применять амбулаторно и с использованием неспециализированного оборудования, она требует небольших финансовых затрат, превышающих затраты времени пациента и врача. Однако следует учитывать совокупный риск кровотечения и заноса инфекции во время повторных процедур. Хотя риск развития застойного легкого у пациентов, которым требуются повторные терапевтические аспирации, не определен, возможность утолщения висцеральной плевры со временем, поскольку она постоянно находится в плевральной жидкости, является потенциальным недостатком этого подхода.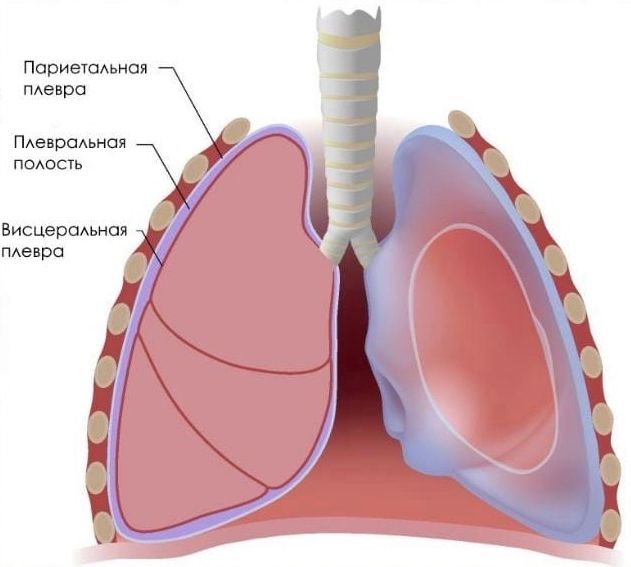
При злокачественных плевральных выпотах рекомендуется максимальный объем аспирации 1,5 л [4]. Хотя риск повторного расширения отека легких невелик, следует проявлять осторожность при рассмотрении аспираций большего объема, а механизм, вызывающий повторное расширение отека, также применяется при доброкачественных выпотах. Некоторые авторитетные источники рекомендуют использовать манометрию в качестве ориентира для определения необходимого объема для удаления [56]. При отсутствии манометрии подходящей стратегией может быть аспирация только 1.5 л за один раз, хотя, если пациент не испытывает таких симптомов, как кашель или боль в груди, может быть разумным осторожно аспирировать больше, чем этот объем, в каждом конкретном случае.
Постоянные плевральные катетеры
Катетер PleurX (CareFusion, Вернон-Хиллз, Иллинойс, США) был одобрен Управлением по контролю за продуктами и лекарствами США в 1997 году для лечения злокачественных плевральных выпотов [57]. С 2001 года лицензия была расширена и теперь распространяется на доброкачественные плевральные выпоты [58].
Использование постоянного плеврального катетера при злокачественных плевральных выпотах. В настоящее время появляется все больше данных, подтверждающих безопасное использование постоянных плевральных катетеров при злокачественном заболевании плевры, что позволяет проводить амбулаторное лечение. Использование постоянных плевральных катетеров при злокачественных новообразованиях считается рентабельным по сравнению с тальковым плевродезом (который требует госпитализации), хотя это зависит от ожидаемого прогноза [59, 60].
Использование постоянных плевральных катетеров при доброкачественных выпотах не так хорошо подтверждается доступными доказательствами, и отсутствие знаний о постоянных плевральных катетерах среди многопрофильной бригады, занимающейся лечением этих пациентов, может способствовать тому, что их использование не так широко .Являются ли постоянные плевральные катетеры экономически эффективными при незлокачественных заболеваниях, еще не установлено, и не стоит вопрос о том, какие пациенты с доброкачественными выпотами могут получить наибольшую пользу.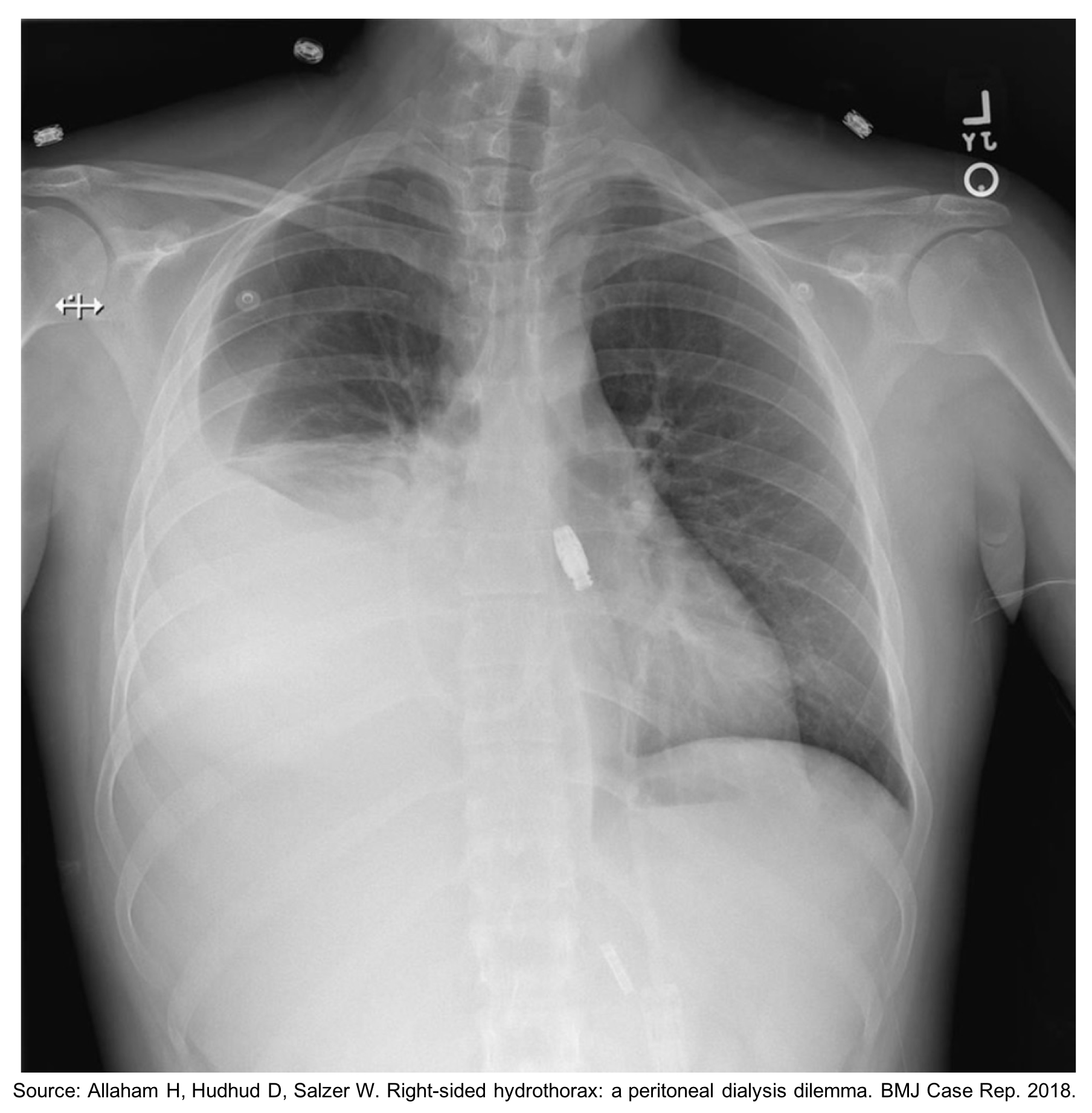
Существует ряд наблюдательных исследований, в которых сообщается об использовании постоянных плевральных катетеров при незлокачественных заболеваниях, при этом большинство исследований включает в себя ряд групп пациентов, а не отдельные группы заболеваний. Частота осложнений, связанных с использованием постоянных плевральных катетеров при доброкачественных выпотах, кажется сходной с таковой у пациентов со злокачественными заболеваниями [34, 61].Обзор доступной литературы, включающей 377 пациентов, включенных в обсервационные исследования, состоял из разнообразного набора случаев, при этом наибольший вклад внесли пациенты с застойной сердечной недостаточностью (40%), гидротораксом печени (17%) или идиопатическим плевритом (15%). Наиболее частыми осложнениями были эмпиема или инфекция дренажного узла, которые наблюдались у 5,2% и 2,9% соответственно [61].
Плевродез может возникать у пациентов, получавших постоянный плевральный катетер, без особой цели (рис. 3).Часто описываемый как «спонтанный» плевродез, этот процесс происходит примерно у одной трети пациентов с доброкачественными выпотами, которым вводили постоянный плевральный катетер.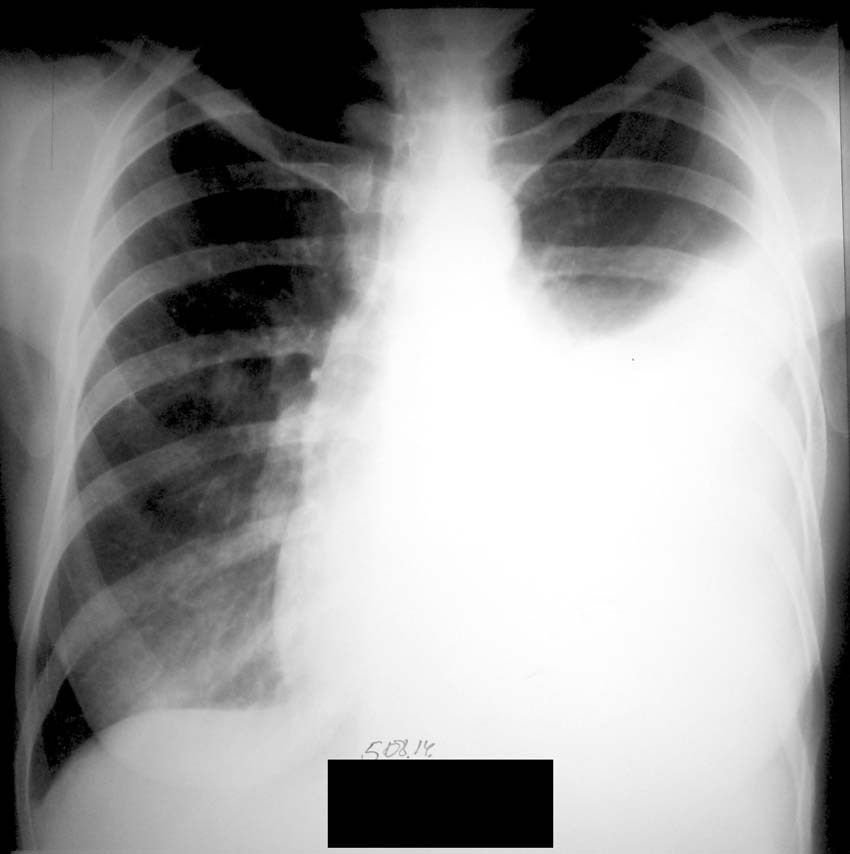 Частота плевродеза варьируется и зависит от причины. Частота спонтанного плевродеза особенно низка при гидротораксе печени [34].
Частота плевродеза варьируется и зависит от причины. Частота спонтанного плевродеза особенно низка при гидротораксе печени [34].
Рентгенограммы грудной клетки пациента с транссудативным плевральным выпотом из-за подтвержденного биопсией системного амилоидоза, вызывающего нефротический синдром.а) При поступлении с правосторонним плевральным выпотом. б) Рецидив плеврального выпота после попытки талькового плевродеза, который был выполнен из-за частой потребности в плевральной аспирации. в) через 6 месяцев после установки постоянного плеврального катетера. На этом этапе уменьшение объема дренированной жидкости указывает на «спонтанный» плевродез и позволяет удалить дренаж.
Использование постоянных плевральных катетеров при доброкачественных выпотах является предметом рандомизированного контролируемого исследования (REDUCE) в Великобритании, набор участников в который продолжается (www.isrctn.co.uk ISRCTN66354436). В этом исследовании участвуют пациенты с симптоматическими плевральными выпотами с сердечной недостаточностью или печеночной недостаточностью, которые сохраняются, несмотря на то, что оптимизированное лечение рандомизировано либо на лечение постоянным плевральным катетером, либо на терапевтическую аспирацию плевры, если это необходимо. По завершении это исследование должно предоставить надежные данные о рисках, преимуществах и экономической эффективности постоянных плевральных катетеров в этой популяции.
По завершении это исследование должно предоставить надежные данные о рисках, преимуществах и экономической эффективности постоянных плевральных катетеров в этой популяции.
Плевродез
Плевродез — давно зарекомендовавший себя, безопасный и эффективный метод, проверенный у пациентов со злокачественным выпотом.Как и в случае с другими методами, существует меньше доказательств, подтверждающих его использование при доброкачественных выпотах. При доброкачественных выпотах использовался широкий спектр плевродезных агентов, хотя лучше всего описан тальк. Тальк может быть доставлен через грудной дренаж (в виде суспензии) или при торакоскопии (в виде пудры).
Существуют исторические опасения в отношении талька, содержащего следы асбеста, и сообщения об остром респираторном дистресс-синдроме, связанном с использованием талька без градации, который может быть уместен у пациентов с доброкачественными заболеваниями.Однако использование современного французского талька позволяет снизить эти риски [62]. Было показано, что плевродез с использованием неклассифицированного талька с мелкими частицами (<10 мкМ) связан со значительно более высокими уровнями системного воспаления и худшим газообменом, чем градуированный тальк, в котором эти мелкие частицы удаляются [63].
Было показано, что плевродез с использованием неклассифицированного талька с мелкими частицами (<10 мкМ) связан со значительно более высокими уровнями системного воспаления и худшим газообменом, чем градуированный тальк, в котором эти мелкие частицы удаляются [63].
Большое ретроспективное исследование 611 пациентов, которое оценивало успех талькового плевродеза через дренаж грудной клетки , сообщило об успешности 77% у 68 пациентов с доброкачественными заболеваниями.Это исследование, однако, исключило пациентов, перенесших более одной попытки плевродеза, и конкретная этиология среди включенных в него доброкачественных выпотов не ясна [64]. Глейзер и др. . [65] сообщили о 75% успешности талькового плевродеза при 16 незлокачественных выпотах различной этиологии. О аналогичном уровне успеха в 80% сообщили Sudduth et al . [66] с использованием ряда плевродезирующих средств в 25 выпотах с доброкачественными заболеваниями.
Имеются данные из небольшой серии случаев, свидетельствующие о том, что использование талькового плевродеза у пациентов с гидротораксом печени сопряжено со значительным риском; летальность после процедуры составляет 45 лет. 5% [67]. Неясно, в какой степени этот результат может быть объяснен крайне коморбидной популяцией пациентов.
У пациентов с гидротораксом печени, перенесших обливание тальком при торакоскопии, в небольшой серии из 21 процедуры у 18 пациентов показатель успеха составил только 47,6% [68]. Как и в случае с пациентами с гидротораксом печени, получавших плевродез с тальком через дренажную трубку , наблюдались высокие показатели смертности (38,9% смертность в течение 3 месяцев наблюдения), а также значительная заболеваемость и длительное пребывание в стационаре.
Плеврально-перитонеальное и плевровенозное шунты
Плевро-перитонеальное или плевровенозное шунтирование плевральной жидкости из плевральной полости является концептуально привлекательной идеей. В серии случаев 12 пациентов с доброкачественными выпотами, которым вводили шунт из плевральной полости в подключичную или яремную вену, были получены обнадеживающие результаты. Используемые устройства состояли из Denver Shunt с внешним ручным насосом, и все устройства оставались запатентованными, за исключением одного пациента, у которого через 4 недели произошла окклюзия шунта [69].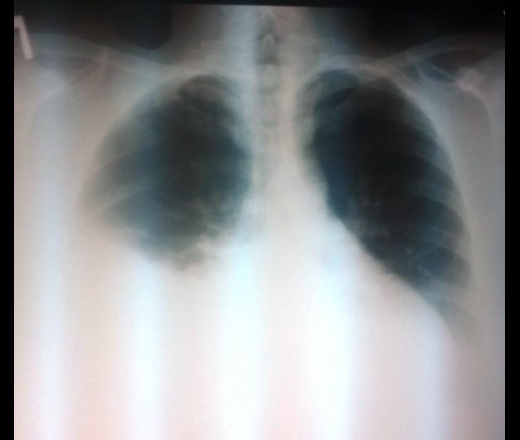 В этом исследовании не сообщалось о воздушной эмболии, хотя этот механизм может привести к пневмотораксу или пневмотораксу ex vacuo , что станет опасным для жизни осложнением. Плевровенозное шунтирование уменьшит потерю белка и объема, связанную с внешним дренажом жидкости, к которому пациенты с гидротораксом печени могут быть особенно чувствительны.
В этом исследовании не сообщалось о воздушной эмболии, хотя этот механизм может привести к пневмотораксу или пневмотораксу ex vacuo , что станет опасным для жизни осложнением. Плевровенозное шунтирование уменьшит потерю белка и объема, связанную с внешним дренажом жидкости, к которому пациенты с гидротораксом печени могут быть особенно чувствительны.
Плевро-перитонеальные устройства успешно использовались с доказательством эффективного облегчения симптомов как при злокачественных, так и при доброкачественных плевральных выпотах, хотя они обычно противопоказаны пациентам с асцитом [70–72].Ввиду разницы давлений между плевральным и брюшным пространством для достижения потока необходим насос, а используемые устройства включают однонаправленный клапан.
Хирургические методы
Дряхлость и сопутствующие заболевания некоторых пациентов с доброкачественным плевральным выпотом могут выступать в качестве сдерживающего фактора против некоторых более инвазивных методов, но хирургическая плеврэктомия может быть подходящим вариантом для некоторых пациентов с постоянным выпотом, если менее инвазивные методы позволяют были предприняты и потерпели неудачу или противопоказаны иным образом.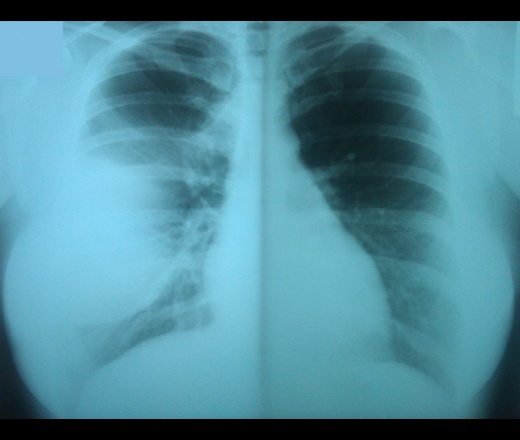
Исследование одностороннего плеврального выпота у взрослых: Руководство Британского торакального общества по заболеваниям плевры, 2010 г. дисфункция и лекарства.1
Плевральный выпот возникает в результате повышенного образования жидкости и / или снижения резорбции жидкости. Точная патофизиология накопления жидкости варьируется в зависимости от основной этиологии.Поскольку дифференциальный диагноз одностороннего плеврального выпота обширен, необходим систематический подход к исследованию. Цель состоит в том, чтобы быстро установить диагноз, сведя к минимуму ненужные инвазивные исследования и облегчая лечение, избегая необходимости повторных терапевтических попыток, когда это возможно.
Со времени выпуска руководства 2003 г. было опубликовано несколько клинически значимых исследований, в которых были опубликованы новые рекомендации по визуализации плевральных процедур с очевидными преимуществами для комфорта и безопасности пациента, оптимальным отбором и обработкой пробы плевральной жидкости и особой ценностью торакоскопической биопсии плевры. Это руководство также включает обзор недавних данных об использовании новых биомаркеров, включая N-концевой натрийуретический пептид мозга (NT-proBNP), мезотелин и суррогатные маркеры туберкулезного плеврита.
Это руководство также включает обзор недавних данных об использовании новых биомаркеров, включая N-концевой натрийуретический пептид мозга (NT-proBNP), мезотелин и суррогатные маркеры туберкулезного плеврита.
Клиническая оценка и история болезни
Аспирацию не следует выполнять при двусторонних выпотах в клинических условиях, явно указывающих на наличие транссудата, за исключением случаев, когда имеются атипичные признаки или они не реагируют на терапию. (✓)
Во время клинической оценки необходимо собрать точный анамнез препарата.(✓)
Анамнез и физикальное обследование пациента с плевральным выпотом могут помочь клиницисту определить, является ли выпот транссудатом или экссудатом. Это важное различие сужает дифференциальный диагноз и направляет дальнейшее исследование.
Сама по себе клиническая оценка часто позволяет выявить транссудативный выпот. Следовательно, в соответствующих клинических условиях, таких как левожелудочковая недостаточность с подтверждающим рентгеновским снимком грудной клетки, такие выпоты не нужно отбирать, если нет атипичных признаков или они не поддаются лечению.
Примерно 75% пациентов с тромбоэмболией легочной артерии и плевральным выпотом в анамнезе страдали плевритной болью. Эти выпоты обычно занимают менее одной трети гемиторакса, а одышка часто непропорциональна размеру выпота.2 3 Поскольку тесты плевральной жидкости бесполезны при диагностике тромбоэмболии легочной артерии, требуется высокий индекс подозрения. чтобы не пропустить диагноз.
История наркотиков пациента также важна. Сообщается, что некоторые лекарства, хотя и редко, вызывают экссудативный плевральный выпот (вставка 1).Полезные ресурсы для получения более подробной информации включают Британский национальный формуляр и веб-сайт http://www.pneumotox.com/.
Вставка 1 Обычно назначаемые препараты, вызывающие плевральный выпот (более 100 случаев зарегистрировано во всем мире)
Метотрексат
Амиодарон
Фенитоин
Нитрофурантоин
Прикроватный ультразвуковой контроль значительно увеличивает вероятность успешной аспирации плевральной жидкости и снижает риск прокола органа. (B)
Ультразвук обнаруживает перегородки плевральной жидкости с большей чувствительностью, чем КТ. (C)
Диагностический образец плевральной жидкости следует аспирировать с помощью иглы с тонким отверстием (21G) и шприца на 50 мл. (✓)
Прикроватный ультразвуковой контроль повышает вероятность успеха и снижает количество осложнений (включая пневмоторакс) и поэтому рекомендуется для диагностических целей.(B)
Плевральную жидкость всегда следует отправлять на протеин, лактатдегидрогеназу, окраску по Граму, цитологию и микробиологический посев. (C)
Критерии Лайта должны использоваться для различения экссудата плевральной жидкости и транссудата ( вставка 2). (B)
Чтобы применить критерии Лайта, необходимо измерить общий белок и лактатдегидрогеназу (ЛДГ) как в крови, так и в плевральной жидкости.(B)
Плевральная жидкость является экссудатом, если выполняется один или несколько из следующих критериев:
Белок плевральной жидкости, деленный на белок сыворотки> 0,5
Лактатдегидрогеназа (ЛДГ) плевральной жидкости, деленная на ЛДГ сыворотки, составляет> 0,6
ЛДГ плевральной жидкости> 2/3 верхних пределов лабораторных нормальных значений ЛДГ в сыворотке.
Левожелудочковая недостаточность
Цирроз печени
1650004 Гипоальбуминемия
Гипоальбуминемия
04
Гипотироидизм
Нефротический синдром
Митральный стеноз
- Парагнитный выпот
Туберкулез
0 β-блокаторы
Источник: http: //www.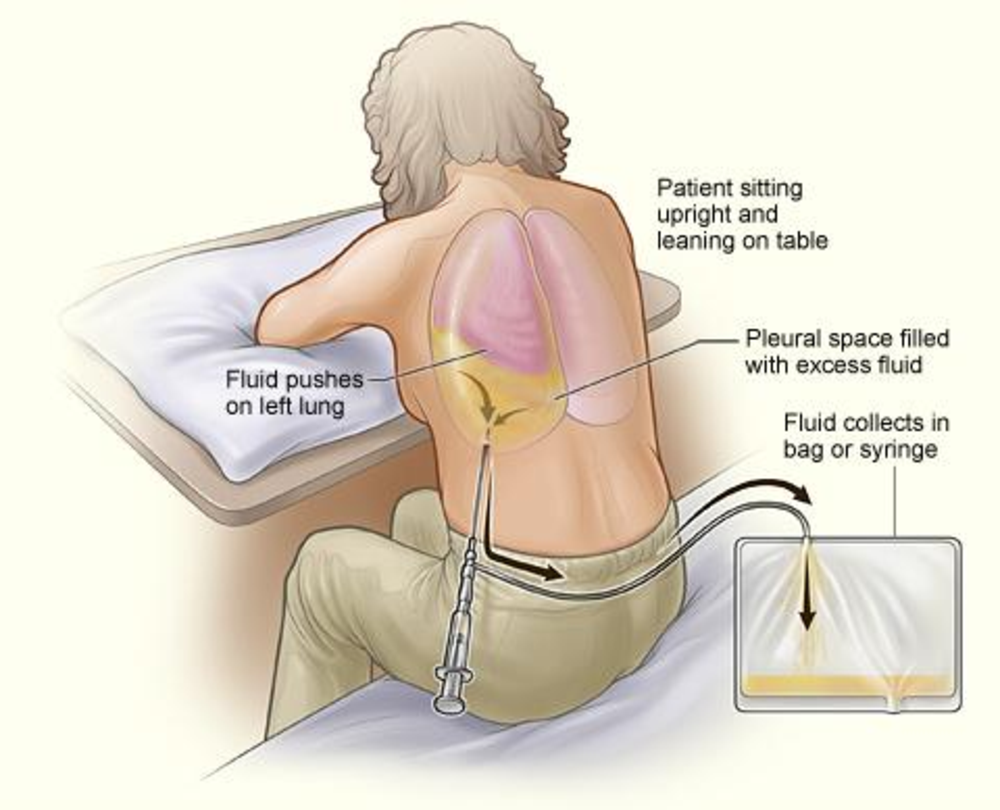 pneumotox.com (2009)
pneumotox.com (2009)
Должен быть задокументирован профессиональный анамнез, включая подробности известного или предполагаемого воздействия асбеста и потенциального вторичного воздействия через родителей или супругов. Алгоритм исследования одностороннего плеврального выпота показан на рисунке 1.
Рисунок 1Диагностический алгоритм исследования одностороннего плеврального выпота.
Первичная диагностическая визуализация
Обычная рентгенография
Обычно характерны простые рентгенографические признаки плеврального выпота.Задне-передний (PA) рентген грудной клетки не соответствует норме при наличии около 200 мл плевральной жидкости. Однако только 50 мл плевральной жидкости может вызвать заметное притупление заднего реберно-диафрагмального угла на латеральном рентгеновском снимке грудной клетки.4
В условиях интенсивной терапии большинство рентгеновских снимков грудной клетки выполняется в виде передних исследований в положении лежа на спине, в результате чего остается свободная плевральная жидкость. кзади в зависимой части грудной клетки. Следовательно, выпоты видны как увеличение непрозрачности гемиторакса с сохранением сосудистых теней на рентгенограмме в положении лежа на спине.Другие признаки включают потерю резкого силуэта ипсилатеральной гемидиафрагмы и просачивание жидкости вниз в косые или горизонтальные трещины, что приводит к явному утолщению трещин. Объем плевральной жидкости обычно недооценивается на рентгенограмме грудной клетки в положении лежа на спине, и «нормальный» внешний вид не исключает наличия выпота.5
Подлегочный выпот возникает, когда плевральная жидкость накапливается между диафрагмальной поверхностью легкого и диафрагмой. Они часто являются транссудатами, их трудно диагностировать на пленке PA и может потребоваться ультразвуковое сканирование.Пленка PA часто показывает латеральный выступ явно приподнятой гемидиафрагмы, которая имеет крутой боковой наклон с постепенным медиальным наклоном (см. Рисунок 2). Боковой рентгеновский снимок может иметь плоский вид задней части гемидиафрагмы с крутым наклоном вниз у большой трещины.6
Рисунок 2Рентген грудной клетки показывает умеренный плевральный выпот слева и сублегочный выпот справа (a ). Обратите внимание на боковой выступ правого полушария. Воспроизведено с разрешения профессора Дэвида Милна из Оклендского университета.
Ультразвук
Ультразвуковой контроль повышает вероятность успешной аспирации плевры. Несколько исследований показали, что жидкость может быть успешно получена с помощью ультразвука у 88% пациентов после неудачной клинической и простой попытки рентгенологического исследования грудной клетки.7–9
Ультразвуковой контроль снижает частоту ятрогенного пневмоторакса после плевроцентеза, и несколько исследований показали, что этот эффект не зависит от размера выпота.10 11 Это преимущество, по-видимому, теряется, когда используется метод «X отмечает точку». использовались, предположительно из-за различий в расположении пациентов при УЗИ и процедуре.12
Клиническая оценка с обзором рентгеновского снимка грудной клетки сравнивалась с УЗИ при планировании места диагностической аспирации в проспективном исследовании, включающем 255 клинических оценок 67 пациентов .4 Чувствительность и специфичность клинической оценки по сравнению с золотым стандартом ультразвука составила 76,6% и 60,3% соответственно. Ультразвук увеличил количество точных участков на 26%; 15% клинически определенных участков могли привести к пункции печени, селезенки или легкого, и, хотя возрастал риск при небольших или локализованных излияниях, 60% возможных проколов органов происходили в радиологически больших или умеренных излияниях.
Ультразвук превосходит простую рентгенографию в диагностике и количественной оценке плеврального выпота и отличает плевральную жидкость от утолщения с высокой специфичностью, особенно при использовании цветного допплера.13–16 Это особенно полезно при диагностике небольших выпотов или у лежачих пациентов (например, находящихся на ИВЛ и находящихся в критическом состоянии) из-за низкой чувствительности простой рентгенографии в этих ситуациях.
Диагностическая роль ультразвукового исследования грудной клетки в раннем исследовании плеврального выпота выходит за рамки выявления и безопасной аспирации жидкости.
Ультразвук обнаруживает перегородки в плевральной жидкости с большей чувствительностью, чем компьютерная томография.17 Вид перегородок может наблюдаться при злокачественных выпотах или плевральной инфекции и встречается с одинаковой частотой при обоих диагнозах.18
Ультразвук положительно идентифицирует экссудативный выпот, когда плевральная жидкость сложная, разделенная или эхогенная, хотя простые (анэхогенные) выпоты могут быть экссудатами или транссудатами. 19
Ультразвуковые признаки могут отличить злокачественный от доброкачественного выпота. Qureshi и др. продемонстрировали 95% специфичность для злокачественного диагноза, 95% для париетального утолщения плевры> 1 см, 100% для висцерального утолщения плевры, 95% для утолщения диафрагмы> 7 мм и 100% для диафрагмальных узелков, как визуализировано при ультразвуковом исследовании. .20 Общая чувствительность ультразвука для дифференциации злокачественных опухолей от доброкачественных выпотов составила 79% (95% ДИ 61–91%), а специфичность 100% (95% ДИ 82–100%), при этом специфичность по сравнению с КТ-сканированием ( 89%).
Плевральная аспирация
Это основной способ оценки плевральной жидкости, результаты которого используются для дальнейшего исследования.
УЗИ плевры следует использовать у постели больного для безопасного выбора места аспирации плевры. Ультразвук увеличивает шансы на успешную аспирацию и сводит к минимуму необходимость в повторных попытках.21 Прямая аспирация под контролем УЗИ или ультразвуковое исследование у постели больного непосредственно перед процедурой предпочтительнее, чем метод «X отмечает точку». Боковой участок является предпочтительным при условии, что здесь на УЗИ будет продемонстрировано адекватное количество жидкости, поскольку риск травмы межреберных сосудов увеличивается при большем количестве задних или медиальных проколов (см. Рисунок 3).
Рисунок 3Компьютерная томография (A) до и (B) через 2 дня после аспирации плевры с несоответствующим медиальным доступом и пункцией межреберной артерии с последующим гемотораксом, требующим хирургического вмешательства.Обратите внимание на активное кровотечение, указанное стрелкой.
Согласие пациента и другие технические детали плевральной аспирации описаны в руководстве по плевральным процедурам. В таблице 1 приведены инструкции по сбору образцов для конкретных тестов плевральной жидкости.
Зеленая игла (21G) и шприц на 50 мл подходят для диагностической аспирации плевры. Если есть диагностическое подозрение на плевральную инфекцию и необходимо измерить pH плевральной жидкости, аспирированную жидкость следует немедленно набрать в шприц с гепаринизированным газом крови, который затем следует закрыть в ожидании анализа, чтобы избежать контакта жидкости с воздухом.Оставшийся образец следует разделить между емкостями для образцов для микробиологического (5 мл), биохимического (2–5 мл) и цитологического (оставшийся образец, который должен быть 20–40 мл) анализа. Для всех проб плевральной жидкости необходимо провести микроскопическое исследование осадка плевральной жидкости, окрашенного по Граму. Если есть подозрение на инфекцию, часть плевральной жидкости следует отправить во флаконы для посева крови, что повысит диагностическую точность, особенно для анаэробных организмов22.
Имеются противоречивые данные относительно оптимального объема плевральной жидкости для диагностики злокачественных новообразований; Чувствительность зависит от клеточности образца и технологии обработки, а также от представленного объема.23 24 Разумно послать как можно больший объем из пробы 50–60 мл, полученной после диагностической аспирации, поскольку для других тестов требуются только небольшие объемы. При комнатной температуре образец для цитологического исследования следует отправить в лабораторию как можно быстрее, но, если ожидается задержка, образец можно хранить в холодильнике при 4 ° C на срок до 14 дней без ухудшения диагностической ценности злокачественных новообразований (таблица 1) .25
Таблица 1Анализы плевральной жидкости и руководство по сбору проб
Внешний вид
В Таблице 2 кратко описывается появление плевральных выпотов, вызванных определенными причинами.Жидкость может казаться серозной, с оттенком крови, откровенно кровянистой или гнойной. Центрифугирование мутной или молочной плевральной жидкости позволит различить эмпиему и липидный выпот. Если супернатант прозрачный, мутная жидкость возникла из-за клеточного мусора и вероятна эмпиема, а если она все еще мутная, вероятен хилоторакс или псевдохилоторакс26. .
Таблица 2Диагностически полезные характеристики плевральной жидкости
Грубая кровянистая плевральная жидкость обычно возникает из-за злокачественных новообразований, эмболии легочной артерии с инфарктом, травмы, доброкачественных асбестовых плевральных выпотов или синдрома пост-сердечной травмы.27 28
Гемоторакс можно отличить от других кровянистых выделений, измерив гематокрит плевральной жидкости. Гематокрит плевральной жидкости> 50% гематокрита периферической крови пациента указывает на гемоторакс.29
Дифференциация экссудата плевральной жидкости и транссудата
Вставка 2 Критерии Лайта
Разделение плевральных выпотов на транссудаты и экссудаты — важный ранний шаг в сужении дифференциальной диагностики и направлении последующих исследований и лечения (см. Вставки 3 и 4).
Вставка 3 Причины плевральных транссудатов
Очень частые причины
Менее распространенные причины
Редкие причины
Вставка 4 Причины плеврального экссудата
Общие причины
Менее распространенные причины
Легочная эмболия
Ревматоидный артрит и другой аутоиммунный плеврит
Доброкачественный выпот асбеста
- 9 0004 Панкреатит
Постинфаркт миокарда
Посткоронарный шунтирующий шунт
Редкие причины
Классически белок плевральной жидкости> 30 г / л указывает на экссудат и <30 г / л транссудат.Эта классификация не точна, если уровень сывороточного белка не соответствует норме или когда белок плевральной жидкости близок к 30 г / л, и, поскольку это очень часто, всегда рекомендуется применение критериев Лайта.30
Значительное количество других биохимических маркеров были сопоставлены с критериями Лайта, но последний, с диагностической точностью 93–96%, остается надежным методом.31 32 Эта дискриминационная точность вряд ли будет превзойдена в качестве «золотого стандарта» для сравнения в клинической диагностике, которая сама по себе несет частота ошибок.
При застойной сердечной недостаточности терапия диуретиками увеличивает концентрацию белка, лактатдегидрогеназы (ЛДГ) и липидов в плевральной жидкости, и в этом контексте признано, что критерии Лайта ошибочно классифицируют значительную часть выпотов как экссудаты. 33 34
Хотя было предложено использование непрерывных отношений правдоподобия, а не дихотомического разделения транссудатов и экссудатов, в частности, для преодоления потери точности критериев Лайта, когда уровни плеврального белка и ЛДГ близки к пороговым значениям, вероятно, в этом громоздком виде мало пользы. статистический метод, выходящий за рамки тщательной интерпретации результатов испытаний в свете клинической оценки.35
N-концевой натрийуретический пептид мозга (NT-proBNP)
NT-proBNP является чувствительным маркером как систолической, так и диастолической сердечной недостаточности. Уровни в крови и плевральной жидкости тесно коррелируют, и в нескольких сериях было показано, что их измерение эффективно в различении транссудатов, связанных с застойной сердечной недостаточностью, от других транссудативных или экссудативных причин.36–39 Однако пороговое значение этих исследований: варьировала в широких пределах от 600 до 4000 пг / мл (наиболее часто использовалось 1500 пг / мл), и из большинства исследований исключались пациенты с более чем одной возможной этиологией выпота.Было показано, что NT-proBNP правильно диагностирует застойную сердечную недостаточность как причину большинства излишеств, которые были ошибочно классифицированы как экссудаты по критериям Лайта. Таким образом, использование этого теста позволяет избежать повторных инвазивных исследований у пациентов с сильным клиническим подозрением на сердечную недостаточность. 40–42. Поскольку результаты с плевральной жидкостью и кровью сопоставимы, достаточно применить тест только к крови (см. на сайте BTS www.brit-thoracic.org.uk).
Доказательства использования измерения BNP (также известного как C-концевой BNP, активный пептид, от которого отщепляется NT-proBNP) на сегодняшний день относительно немного.
Дифференциальный подсчет клеток плевральной жидкости
Пропорции клеток плевральной жидкости помогают сузить дифференциальный диагноз, но ни один из них не является специфическим для заболевания. (C)
Любой длительный плевральный выпот имеет тенденцию заселяться лимфоцитами. Злокачественные новообразования плевры, сердечная недостаточность и туберкулез являются частыми специфическими причинами излияния с преобладанием лимфоцитов. (C)
Если дифференциальное количество клеток плевральной жидкости показывает преобладающий лимфоцитоз (> 50% клеток составляют лимфоциты), наиболее вероятными диагнозами во всем мире являются злокачественные новообразования и туберкулез (ТБ).43 Сердечная недостаточность также является частой причиной лимфоцитарного выпота. Очень высокая пропорция лимфоцитов (> 80%) чаще всего встречается при туберкулезе, лимфоме, хроническом ревматоидном плеврите, саркоидозе и поздних выпотах после коронарного шунтирования (АКШ) (см. Вставку 5) .44
Вставка 5 Причины лимфоцитарных плевральных выпотов (т.е. лимфоциты составляют> 50% ядерных клеток)
Плевральные выпоты с преобладанием нейтрофилов связаны с острыми процессами. Они возникают при парапневмонических выпотах, тромбоэмболии легочной артерии, остром туберкулезе и доброкачественных асбестовых плевральных выпотах.28 45
Плевральные выпоты, в которых ≥10% клеток являются эозинофилами, определяются как эозинофильные.46 Наиболее частой причиной эозинофилии плевральной жидкости является воздух или кровь в плевральном пространстве.47 Плевральная эозинофилия является относительно неспецифической находкой, поскольку она может возникать при парапневмонических выпотах, медикаментозном плеврите, доброкачественных асбестовых плевральных выпотах, синдроме Чарджа-Стросса, лимфоме, инфаркте легкого и паразитарных заболеваниях48. 49 Злокачественные новообразования также являются частой причиной; злокачественный диагноз был поставлен в 37% из 60 эозинофильных выпотов в одной серии.46
pH
При негнойных выпотах при подозрении на плевральную инфекцию следует измерять pH плевральной жидкости при условии соблюдения соответствующей техники сбора и наличия анализатора газов крови. (B)
Включение воздуха или местного анестетика в образцы может значительно изменить результаты pH, и этого следует избегать. (B)
При парапневмоническом выпоте pH <7,2 указывает на необходимость дренирования через трубку.(B)
Ацидоз плевральной жидкости (pH <7,30) возникает при злокачественных выпотах, осложненной плевральной инфекции, заболеваниях соединительной ткани (особенно ревматоидном артрите), туберкулезных плевральных выпотах и разрыве пищевода, и, по отдельности, он не делает различий между эти причины.50
Ацидоз плевральной жидкости отражает увеличение выработки молочной кислоты и углекислого газа из-за локального повышения метаболической активности, а также снижение потока ионов водорода через аномальные плевральные мембраны.Повышенное потребление глюкозы без замены в тех же условиях означает, что плевральная жидкость часто имеет как низкий pH, так и низкую концентрацию глюкозы.51
При злокачественных плевральных выпотах низкий pH был связан с более короткой выживаемостью, более обширным заболеванием и меньшими шансами на успех. плевродез.52 Метаанализ с участием 417 пациентов со злокачественными плевральными выпотами показал, что pH плевры <7,28 был связан со средней выживаемостью 2,5 месяца и 3-месячной выживаемостью 38.9% (95% ДИ от 31,1% до 46,8%) по сравнению со средней выживаемостью 4,3 месяца и 3-месячной выживаемостью 61,6% (95% ДИ от 55,7% до 67,4%), если pH был> 7,28,53
В клинических условиях На практике наиболее важным показателем pH плевральной жидкости является принятие решения о лечении плевральной инфекции с помощью дренажной трубки. Метаанализ исследований, изучающих pH плевры и необходимость дренирования плевральной трубки или хирургического вмешательства у пациентов с парапневмоническим выпотом, показал, что pH <7,2 является наиболее специфическим дискриминатором осложненной плевральной инфекции.54 Это подробно описано в руководстве по инфекциям плевры.
Было показано, что при локализованных парапневмонических выпотах рН жидкости значительно варьируется между локулами, так что при рН> 7,2 у пациента с другими клиническими показателями осложненной плевральной инфекции следует с осторожностью рассматривать.55
Техника сбора и анализа может иметь клинически значимое влияние на результаты pH плевральной жидкости. Проспективное исследование показало, что контакт жидкости с воздухом в шприце увеличивает измеренный pH плевральной жидкости на ≥0.05 в 71% проб и включение 0,2 мл местного анестетика привело к снижению pH в среднем на 0,15 (95% ДИ от 0,13 до 0,18) .56 Плевральную жидкость следует собирать и транспортировать без воздействия атмосферного воздуха, а местный анестетик следует избегать для диагностики стремления, при которых pH будет использоваться для руководства. PH плевры существенно не изменится, если обработка отложена на час при комнатной температуре. Следует использовать газоанализатор артериальной крови.57 В повседневной клинической практике часто бывает трудно соблюдать эти требования по сбору, и, если они не могут быть выполнены, общая клиническая оценка может быть предпочтительнее, чем полагаться на субоптимальный результат pH плевральной жидкости.
Глюкоза
При отсутствии патологии плевры глюкоза свободно диффундирует через плевральную мембрану, а концентрация глюкозы в плевральной жидкости эквивалентна концентрации глюкозы в крови.1
Низкий уровень глюкозы в плевральной жидкости (<3,4 ммоль / л) может быть обнаружен в осложненный парапневмонический выпот, эмпиема, ревматоидный плеврит и плевральный выпот, связанный с туберкулезом, злокачественными новообразованиями и разрывом пищевода.1 Наиболее частыми причинами очень низкого уровня глюкозы в плевральной жидкости (<1,6 ммоль / л) являются ревматоидный артрит и эмпиема.58 59
Хотя уровень глюкозы обычно низкий при плевральной инфекции и коррелирует со значениями pH плевральной жидкости, для дренирования плевральной жидкости это значительно менее точный индикатор, чем pH. 54
При измерении глюкозы в плевральной жидкости образец следует отправить в трубка с фторидоксалатом.
Амилаза
Регулярные измерения амилазы плевральной жидкости или ее изоферментов не требуются. Однако он может быть полезен при подозрении на разрыв пищевода или излияния, связанные с заболеваниями поджелудочной железы.(C)
Уровни амилазы в плевральной жидкости повышаются, если они превышают верхний предел нормы для сыворотки или соотношение плевральная жидкость / сыворотка> 1,0.60 Это указывает на острый панкреатит, псевдокиста поджелудочной железы, разрыв пищевода. , прерванная внематочная беременность или злокачественное новообразование плевры (особенно аденокарцинома) .61 62 Приблизительно в 10% злокачественных выпотов повышен уровень амилазы плевральной жидкости 63, хотя оценка амилазы плевры, вероятно, не играет никакой роли в рутинном исследовании злокачественных выпотов.64
Анализ изоферментов может быть полезен, но во многих лабораториях он недоступен. Повышение уровня амилазы в слюне предполагает разрыв пищевода или злокачественное новообразование.61 62 Плевральный выпот, связанный с заболеванием поджелудочной железы, обычно содержит панкреатическую амилазу.61 Частота плеврального выпота при остром панкреатите превышает 50%. Пациенты с острым панкреатитом и плевральным выпотом, как правило, имеют более тяжелое заболевание и более высокую вероятность последующего развития псевдокисты, чем пациенты без выпота.65 Если разрыв пищевода рассматривается как дифференциальный диагноз, показано срочное более конкретное исследование с помощью контрастной рентгенографии или эндоскопии.
Имеется немного данных относительно измерения липазы плевральной жидкости, хотя в отчетах о случаях плеврального выпота, вторичного по отношению к панкреатиту, описано ее повышение наряду с амилазой.66
Цитология
Злокачественные выпоты могут быть диагностированы с помощью цитологии плевральной жидкости примерно 60% случаев. (B)
Результат от отправки более двух образцов (взятых в разных случаях) очень низок, и этого следует избегать.(B)
Иммуноцитохимия должна использоваться для различения типов злокачественных клеток и может иметь очень важное значение при проведении онкологической терапии. (C)
При подозрении на злокачественное новообразование цитологическое исследование плевральной жидкости является быстрым и минимально инвазивным способом постановки диагноза. В сериях, посвященных диагностике злокачественных новообразований плевральной цитологии, сообщается о средней чувствительности около 60% (диапазон 40–87%) 67–70 Результаты отправки более двух образцов плевральной жидкости, взятых в разных случаях, являются низкими.Одно исследование показало, что выход составляет 65% от первого образца, еще 27% от второго и только 5% от третьего70. Диагностическая ценность злокачественных опухолей зависит от подготовки образца, опыта цитолога и типа опухоли. Уровень диагностики аденокарциномы выше, чем для мезотелиомы, плоскоклеточного рака, лимфомы и саркомы.
Swiderek et al обнаружили, что отправка пробы плевральной жидкости объемом 60 мл дает значительно лучшую чувствительность для диагностики злокачественных новообразований, чем 10 мл, но предыдущие исследования показали, что отправка объемов> 50 мл не улучшила диагностический результат.23 24 Доказательства отправки больших объемов плевральной жидкости недостаточно убедительны, чтобы оправдать повышенный риск осложнений, связанных с использованием венфлона и трехходового крана для начальной диагностической аспирации. На цитологию следует отправить как можно больше жидкости из доступного диагностического образца (вероятно, 20-40 мл), и, если первоначальный результат отрицательный, но есть подозрение на злокачественное новообразование, следует отправить образец большего объема после второй аспирации. считается. Если первоначальная аспирация является одновременно лечебной и диагностической, необходимо отправить ≥60 мл на цитологическое исследование.
Плевральную жидкость следует отправлять в простом контейнере, который позволяет клеточной части отделяться с образованием фибринозного «сгустка», который может окутывать злокачественные клетки. Затем они могут пройти гистологическое исследование и будут зарегистрированы с помощью цитологического исследования жидкости. Некоторые отделы, однако, предпочитают использовать бутыли, содержащие цитрат натрия, чтобы клетки оставались в свободной суспензии. Не следует использовать никакие другие антикоагулянты или консерванты, так как они могут нарушить клеточную приверженность предметным стеклам и иммуноцитохимический анализ.
Выявление злокачественных новообразований увеличивается, если из образцов плевральной жидкости готовят как клеточные блоки (которые формируются путем центрифугирования образца и извлечения твердой клеточной части), так и мазки.71
В таблице 3 представлена интерпретация обычных отчетов цитологического исследования плевральной жидкости. в клинической практике.
После морфологического подтверждения злокачественности следует использовать иммуноцитохимию для дифференциации различных типов злокачественных клеток. Это может быть выполнено на цитологическом образце, клеточном блоке или сгустке.72 Существует особенно обширное морфологическое совпадение между злокачественной мезотелиомой и метастатическими клетками аденокарциномы, и иммуноцитохимия может помочь в их дифференцировке. Однако, когда это возможно, следует получить плевральную ткань для подтверждения диагноза злокачественной мезотелиомы.
Если при морфологическом исследовании подозревается лимфома, в идеале образец следует отправить на проточную цитометрию для дальнейшего типирования, но можно использовать иммуноцитохимический анализ, если он недоступен (таблица 3).73
Таблица 3Отчетность результатов цитологического исследования плевральной жидкости
Онкомаркеры
На уровне отсечения, который обеспечивает 100% специфичность для диагностики злокачественных новообразований, панель опухолевых маркеров плевральной жидкости, включая CEA, CA-125, CA 15 -3 и CYFRA достигают комбинированной чувствительности только 54%, так что отрицательный результат не может использоваться для поддержки консервативного подхода к мониторингу и исследованию.74
Мезотелин, однако, показал более многообещающие диагностические возможности. характеристики (см. таблицу доказательств B, доступную на веб-сайте BTS по адресу www.brit-thoracic.org.uk).
Мезотелин
Мезотелин — это гликопротеиновый онкомаркер, который присутствует в более высоких средних концентрациях в крови и плевральной жидкости пациентов со злокачественной мезотелиомой, чем у пациентов с другими причинами плеврального выпота.75 76 Исследования, изучающие уровни мезотелина в сыворотке и / или плевральная жидкость продемонстрировала чувствительность 48–84% и специфичность 70–100% для диагностики мезотелиомы.75–80 Прогностическая ценность отрицательного результата теста ограничена ложноотрицательными результатами при саркоматоидной мезотелиоме.79 Положительные результаты были также получены при бронхогенной аденокарциноме, метастатической карциноме поджелудочной железы, лимфоме и карциноме яичников.76 78 81
Положительный уровень мезотелина в сыворотке или плевральной жидкости с большой вероятностью указывает на злокачественность плевры и может быть использован для ускорения тканевой диагностики, но отрицательный результат нельзя считать обнадеживающим. Было показано, что мезотелин плевральной жидкости имеет дополнительную ценность помимо цитологии плевральной жидкости при диагностике мезотелиомы и может использоваться из-за его положительной прогностической ценности для уточнения неопределенных результатов цитологии.80 Хотя мезотелин имеет более высокую диагностическую точность, чем другие опухолевые маркеры, его реальная клиническая полезность при исследовании недиагностированного плеврального выпота, особенно в сочетании с рутинной клинической и радиологической оценкой, требует дальнейшего изучения, прежде чем его использование может быть рекомендовано на регулярной основе.
Дальнейшая диагностическая визуализация
Компьютерная томография (КТ)
КТ-сканирование плеврального выпота должно выполняться с контрастированием плевры и до полного дренирования плевральной жидкости.(C)
Компьютерная томография должна выполняться при исследовании всех недиагностированных экссудативных плевральных выпотов и может быть полезна для отличия злокачественного от доброкачественного утолщения плевры. (C)
Компьютерная томография должна быть запрошена при осложненной плевральной инфекции, когда первоначальный дренаж через трубку оказался неудачным и необходимо рассмотреть возможность хирургического вмешательства. (C)
При исследовании плеврального выпота перед полным дренированием жидкости необходимо выполнить КТ грудной клетки с контрастным усилением, так как аномалии плевры будут лучше визуализированы.82 Свободно текущая плевральная жидкость выглядит как серповидное помутнение в наиболее зависимой части грудной клетки. Подвешенные пузырьки воздуха в жидкости предполагают наличие перегородок (рисунок 4), но КТ не различает внутренние характеристики плевральной жидкости с той же чувствительностью, что и ультразвук.17
Рисунок 4КТ-сканирование левой эмпиемы с усилением плевры (а) и взвешенным воздухом пузыри (б).
КТ особенно полезен при диагностике эмпиемы, когда плевра интенсивно увеличивается вокруг жидкости, которая обычно образует линзовидное помутнение (рис. 4).83 84 КТ также отличает эмпиемы от абсцессов легких.
Есть функции КТ грудной клетки с контрастированием, которые могут помочь отличить доброкачественные заболевания от злокачественных (рис. 5). В исследовании 74 пациентов, 39 из которых имели злокачественное заболевание, Leung et al показали, что злокачественному заболеванию способствует узловое утолщение плевры, утолщение плевры средостения, пристеночное утолщение плевры> 1 см и периферическое утолщение плевры. Эти особенности имели специфичность 94%, 94%, 88% и 100%, соответственно, и чувствительность 51%, 36%, 56% и 41%.85 Точность критериев Leung et al для обнаружения злокачественного новообразования плевры была подтверждена в нескольких проспективных исследованиях 82. 86 Дифференцировать мезотелиому плевры от метастатического злокачественного новообразования плевры очень сложно, так как эти состояния имеют много общих черт КТ.
Рисунок 5Злокачественный плевральный выпот справа с увеличивающимся узловым утолщением плевры (а), распространяющимся на средостение (б).
Магнитно-резонансная томография (МРТ)
МРТ точно различает доброкачественные и злокачественные плевральные выпоты по разнице в интенсивности сигнала на Т2-взвешенных изображениях.87 В некоторых исследованиях было показано, что различие морфологических признаков злокачественных новообразований плевры с помощью МРТ равно КТ, а оценка поражения диафрагмы и грудной стенки лучше. в это время, но может использоваться для точной оценки заболевания плевры у пациентов, которым противопоказан контраст. МРТ с динамическим контрастированием показала многообещающие результаты в мониторинге реакции мезотелиомы плевры на химиотерапию.89
ПЭТ-КТ-визуализация
Хотя было показано, что поглощение 18-фтордезоксиглюкозы (ФДГ) больше при злокачественных плевральных выпотах, ценность ПЭТ-КТ-визуализации в различении доброкачественных и злокачественных заболеваний ограничивается ложными положительными результатами с воспалением плевры, включая плевральную инфекцию и последующий плевродез талька.90–92 ПЭТ-КТ в настоящее время не играет роли в рутинном исследовании плевральных выпотов, но, как и в случае с динамической МРТ с контрастированием, появляются новые данные, указывающие на потенциальную роль в мониторинге реакции на лечение мезотелиомы плевры.93–95
Инвазивные исследования
Чрескожная биопсия плевры
При исследовании недиагностированного выпота, при котором подозревается злокачественное новообразование и на КТ с контрастным усилением показаны узловые участки плевры, для чрескожной биопсии плевры используется режущая игла с визуальным контролем. метод выбора. (A)
Игольная биопсия по Абрамсу полезна только с диагностической точки зрения в областях с высокой заболеваемостью туберкулезом, хотя было показано, что режущие иглы для торакоскопии и визуализации имеют более высокую диагностическую ценность.(C)
Обзор результатов биопсии плевры по Абрамсу на основании 2893 обследований показал, что частота диагностики злокачественных новообразований составляет только 57 %.96 Выход по сравнению с одним только цитологическим исследованием плевральной жидкости увеличивается только на 7–27% для злокачественных новообразований.68 69 Осложнения биопсии плевры по Абрамсу включают боль в месте (1-15%), пневмоторакс (3-15%), вазовагальную реакцию (1-5%), гемоторакс (<2%), локальную гематому (<1%), преходящую лихорадку ( <1%) и очень редко смерть в результате кровотечения.
КТ грудной клетки с контрастным усилением пациента с плевральным выпотом часто выявляет очаговую область аномальной плевры.Биопсия с помощью режущей иглы под визуальным контролем позволяет провести биопсию этой фокальной области аномалии. Он имеет более высокий результат, чем слепая биопсия плевры при диагностике злокачественных новообразований. Этот метод особенно полезен для пациентов, которые не подходят для торакоскопии.
Злокачественные отложения плевры, как правило, преобладают вблизи средней линии и диафрагмы, которые лучше всего избегать при выполнении биопсии Абрамса. Тем не менее, эти анатомические области можно безопасно биопсировать под рентгенологическим исследованием.В недавнем проспективном исследовании 33 пациентам с плевральным выпотом и утолщением плевры, продемонстрированным на КТ с контрастным усилением, была проведена чрескожная биопсия плевры под визуальным контролем. Правильный гистологический диагноз был поставлен у 21 из 24 (чувствительность 88%, специфичность 100%), включая 13 из 14 пациентов с мезотелиомой (чувствительность 93%) .97 В более крупном ретроспективном обзоре биопсии плевры под визуальным контролем в одном отделении, выполненной одним рентгенологом , 18 из 21 случая мезотелиомы были правильно идентифицированы (чувствительность 86%, специфичность 100%).98
Было показано, что биопсия с помощью режущей иглы под визуальным контролем превосходит биопсию с иглой Абрамса по диагностической эффективности злокачественных заболеваний. В рандомизированном контролируемом исследовании 50 последовательных пациентов с подозрением на злокачественный плевральный выпот с отрицательным цитологическим исследованием, биопсия Абрамса правильно диагностировала злокачественное новообразование у 8/17 (чувствительность 47%, специфичность 100%, отрицательная прогностическая ценность 44%, положительная прогностическая ценность 100%) и КТ — биопсия под контролем правильно диагностировала злокачественное новообразование у 13/15 (чувствительность 87%, специфичность 100%, отрицательная прогностическая ценность 80%, положительная прогностическая ценность 100%).99
В проспективном исследовании, сравнивающем торакоскопию под местной анестезией с биопсией Абрамса в области с высокой распространенностью ТБ, было обнаружено, что торакоскопия 100 имеет комбинированную чувствительность посева / гистологии 100% по сравнению с 79% для биопсии плевры Абрамса. Таким образом, торакоскопия с местной анестезией является методом с наивысшим уровнем диагностики туберкулезного плеврита на основании опубликованных данных. Однако, поскольку слепая биопсия плевры имеет достаточно высокую чувствительность и, вероятно, будет более рентабельной в качестве первоначальной диагностической процедуры, она часто будет процедурой первого выбора в районах с ограниченными ресурсами с высокой заболеваемостью туберкулезом.Слепая биопсия плевры не может быть оправдана для диагностики ТБ, когда заболеваемость недостаточно высока для поддержания опыта оператора (см. Таблицу доказательств C, доступную на веб-сайте BTS по адресу www.brit-thoracic.org.uk).
Торакоскопия
У пациентов с симптоматическим экссудативным плевральным выпотом, когда диагностическая аспирация плевры отрицательна или неубедительна, торакоскопия предлагается в качестве следующего исследования выбора, поскольку процедура будет относительно несложной и будет показан плевродез.
Торакоскопия с местной анестезией
Торакоскопия с местной анестезией может выполняться врачами или хирургами и является безопасной и хорошо переносимой процедурой. Серьезные осложнения (например, эмпиема, кровотечение и пневмония) встречаются только у 2,3% (95% ДИ от 1,9% до 2,8%), а смерть редко — 0,40% (95% ДИ от 0,2% до 0,7%). Он имеет диагностическую чувствительность при злокачественном заболевании плевры 92,6% (95% ДИ от 91,0% до 93,9%) 101–121. Он также имеет более высокую диагностическую ценность, чем слепая биопсия плевры при туберкулезном плеврите.В конце процедуры можно вводить тальк, который обеспечивает успешный плевродез в 80–90% случаев (более подробную информацию см. В руководстве BTS по торакоскопии.
Видео-торакоскопическая хирургия (VATS)
Выполняется торакальными хирургами и требует общей анестезии. Следовательно, она не подходит для слабых людей и людей с другими тяжелыми сопутствующими заболеваниями. Эта процедура сообщает о столь же высоких показателях диагностической чувствительности около 95% для злокачественных новообразований, а также является относительно безопасной с низким уровнем осложнений.В одной серии из 566 обследований наиболее частым побочным эффектом была подкожная эмфизема с сердечной аритмией и воздушной эмболией, которые наблюдались у <1% и не приводили к летальному исходу.122
Одним из преимуществ VATS перед торакоскопией с местной анестезией является то, что хирург может продолжить к другим торакальным хирургическим вариантам, если это необходимо, во время процедуры. В частности, можно сделать вывод о том, заблокировано ли легкое или свободно расширяется. При синдроме защемленного легкого плевродез, вероятно, будет менее эффективным, поэтому во время VATS можно установить постоянный плевральный катетер (см. Руководство BTS по торакоскопии.
Бронхоскопия
Обычная диагностическая бронхоскопия не должна выполняться при недиагностированном плевральном выпоте. (C)
Бронхоскопию следует рассмотреть, если есть кровохарканье или клинические или рентгенологические признаки, указывающие на обструкцию бронхов. (C)
Бронхоскопия играет ограниченную роль в исследовании пациентов с недиагностированным плевральным выпотом, поскольку ее диагностическая ценность очень низкая.123–126 Его следует использовать для пациентов, радиология которых предполагает наличие массы или потери объема, или когда в анамнезе есть кровохарканье, возможная аспирация инородного тела или застрявшее легкое с подозрением на проксимальное образование легкого.
Если бронхоскопия считается необходимой, ее следует выполнить после дренажа плевры, чтобы провести адекватное обследование без сдавления внешних дыхательных путей плевральной жидкостью.
Особые условия и тесты
Туберкулезный плеврит
После взятия биопсии плевры ее следует отправить как на гистологическое исследование, так и на посев для повышения диагностической чувствительности на ТБ.(B)
Торакоскопическая биопсия плевры — это тест, который с наибольшей вероятностью даст положительные результаты посева микобактерий (и, следовательно, чувствительность к лекарствам). (B)
Суррогатные маркеры плеврального туберкулеза являются полезными тестами для «исключения» в странах с низкой заболеваемостью. Аденозиндезаминаза наиболее тщательно проверена на сегодняшний день. (B)
Туберкулезный плеврит — это реакция гиперчувствительности IV типа к микобактериальному белку, и микобактериальная нагрузка в плевральной жидкости обычно невысока.Таким образом, микроскопия плевральной жидкости на кислотоустойчивые бациллы имеет чувствительность <5%, а посев плевральной жидкости - 10–20% .127 Было показано, что торакоскопическая биопсия плевры имеет чувствительность> 70% для посева плевральной ткани и общей диагностической чувствительности приближается к 100%, когда данные о казеозных гранулемах при гистологическом исследовании плевральной биопсии сочетаются с посевом. 100
Суррогатные маркеры плеврального туберкулеза
Туберкулезный плеврит является излечимой причиной лимфоцитарного плеврального выпота.Желательно исключить диагноз у пациентов с лимфоцитарным выпотом, избегая несоответствующей и склонной к побочным эффектам эмпирической противотуберкулезной терапии. У пациентов, которые не подходят для инвазивных исследований, могут быть полезны плевральная жидкость или биомаркеры инфекции крови. Аденозиндезаминаза (АДА) — это фермент, присутствующий в лимфоцитах, и его уровень в плевральной жидкости значительно повышается при большинстве туберкулезных плевральных выпотов. Метаанализ 63 исследований по диагностическому использованию ADA подтвердил чувствительность 92%, специфичность 90% и отношение правдоподобия положительного и отрицательного результата 9.0 и 0,10 соответственно.128 Повышенные уровни ADA также можно увидеть при эмпиеме, ревматоидном плеврите и, иногда, при злокачественных новообразованиях. Ограничение использования ADA лимфоцитарными излияниями или измерение изофермента ADA-2 может значительно снизить количество ложноположительных результатов.129 ADA очень дешевый и быстрый в исполнении и остается стабильным при хранении при 4 ° C до 28 дней130. у пациентов с ВИЧ или пациентов с ослабленным иммунитетом (например, при трансплантации почки). В странах с низкой распространенностью туберкулеза ADA является полезным тестом для исключения.
Было также показано, что нестимулированные уровни интерферона γ в плевральной жидкости имеют такую же диагностическую точность, что и ADA, в метаанализе.131 Однако первый метод более дорог. Были изучены тесты высвобождения интерферона γ (IGRA). При применении к крови в областях с низкой заболеваемостью туберкулезом сообщалось о чувствительности до 90%, но специфичность ограничена неспособностью тестов отличить латентный туберкулез от активного.132 В небольших исследованиях IGRA применяли к плевральной жидкости с демонстрацией превосходная чувствительность (96.4%), хотя коммерческие тесты еще не прошли валидацию для других жидкостей, кроме крови.133 Хотя ожидаются дальнейшие исследования, общие диагностические характеристики, простота использования и стоимость вряд ли будут конкурировать с ADA.134
В хорошо обеспеченных ресурсами системах здравоохранения В таких условиях наибольшие шансы на получение культуры микобактерий и чувствительность следует проверять с помощью торакоскопической биопсии плевры. Однако обширный обзор 7549 случаев туберкулезного плеврита, проведенный Центром по контролю за заболеваниями, показал, что характеристики лекарственной устойчивости плеврального туберкулеза в США в целом отражают таковые для легочного туберкулеза в том же регионе.135 Если микобактериальная культура и чувствительность не достигнуты, режим лечения должен отражать местные образцы устойчивости.
Заболевания соединительной ткани
Ревматоидный артрит и системная красная волчанка (СКВ) являются наиболее частыми заболеваниями соединительной ткани, поражающими плевру. Плевральный выпот возникает при заболевании соединительной ткани из-за первичного аутоиммунного плеврита или вторичного почечной, сердечной, тромбоэмболической болезни или лекарственной терапии.
Плевральные выпоты, связанные с ревматоидным артритом
Поражение плевры встречается у 5% пациентов с ревматоидным артритом.136 Плевральные выпоты, связанные с ревматоидным артритом, чаще встречаются у мужчин, хотя само заболевание чаще встречается у женщин.137 Хронические ревматоидные выпоты являются наиболее частой причиной псевдохилезных (холестериновых) выпотов в странах с низкой заболеваемостью туберкулезом, но они могут также иметь серозный или геморрагический вид.138. 139 Измерение триглицеридов и холестерина в молочных выпотах подтвердит диагноз псевдохилезной картины, а при ревматоидном артрите это делает маловероятными другие причины выпота.Ревматоидный артрит вряд ли станет причиной хронического выпота, если уровень глюкозы в жидкости> 1,6 ммоль / л, что служит полезным скрининговым тестом58. 80% ревматоидных плевральных выпотов имеют соотношение глюкозы в плевральной жидкости к сыворотке < 0,5 и pH <7,30. 140 Однако при остром ревматоидном плеврите уровень глюкозы и pH может быть нормальным.141 Дополнительную помощь может оказать измерение C4-комплемента в плевральной жидкости с уровнями <0,04 г / л во всех случаях ревматоидного плеврального болезни и только у 2 из 118 контрольных групп, о которых сообщалось в одном исследовании.141 Ревматоидный фактор может быть измерен в плевральной жидкости и часто имеет титр> 1: 320. 142 Однако он может присутствовать в выпотах другой этиологии и часто отражает значение в сыворотке крови, что незначительно диагностически. 141
Системная красная волчанка (СКВ) )
Плеврит является первым проявлением СКВ у 5–10% пациентов, но является ранним признаком у 25–30% и обычно сопровождается мультисистемным поражением. Плевральный выпот часто бывает небольшим и у 50% пациентов двусторонний.143
Ни один тест не позволяет однозначно отличить плеврит СКВ от других причин экссудативного выпота. Биохимические особенности не являются различимыми или непротиворечивыми.144 145 Повышенное содержание антинуклеарных антител (ANA) в плевральной жидкости и повышенное соотношение ANA плевральной жидкости к сыворотке свидетельствует о плеврите с СКВ, но иногда это повышение также наблюдается при злокачественных выпотах.146 Измерения Porcel et al. Титры АНА плевральной жидкости у 266 пациентов с плевральным выпотом установленной причины, в том числе у 15 пациентов с СКВ.Они продемонстрировали чувствительность 100% (95% ДИ от 97% до 100%) и специфичность 94% (95% ДИ от 91% до 97%) для теста плевральной жидкости, но, в соответствии с предыдущими отчетами, результаты были идентичными, когда Тестирование сыворотки.147 Нет никакой дополнительной ценности в измерении ANA плевральной жидкости помимо сывороточного теста.
Плевральный выпот вследствие тромбоэмболии легочной артерии
Плевральный выпот, обнаруживаемый на рентгенограмме грудной клетки, встречается у 23–48% пациентов с тромбоэмболией легочной артерии.148 Выпоты небольшие (менее одной трети гемиторакса) почти в 90% случаев. случаев, хотя также распознаются умеренные и массивные излияния.3 Они могут быть ипсилатеральными, контралатеральными или двусторонними относительно эмбола, обнаруженного рентгенологически.2 3
Недавние серии исследований с применением критериев Лайта показали, что плевральные выпоты, связанные с тромбоэмболией легочной артерии, всегда являются экссудатами.3 149 Характеристики жидкости, однако, неспецифичны. и бесполезны при постановке диагноза, который следует проводить радиологически, учитывая высокий индекс клинического подозрения или в контексте излияния, которое остается недиагностированным после стандартных базовых исследований.
Хилоторакс и псевдохилоторакс
Если плевральная жидкость имеет молочный оттенок, следует рассмотреть возможность хилоторакса и псевдохилоторакса. Иногда эмпиема бывает настолько мутной, что ее можно спутать с хилусом. Их можно отличить лабораторным центрифугированием, при котором в эмпиеме остается прозрачный супернатант, а хилезный выпот остается молочного цвета. Следует отметить, что у голодных пациентов хилус может не выглядеть молочным.
Истинный хилезный выпот (хилоторакс) возникает в результате разрушения грудного протока или его притоков, так что хилез присутствует в плевральной полости.
Травмы, особенно после торакальной хирургии, вероятно, вызывают около 50% медицинских причин, включая злокачественные новообразования (особенно лимфому), туберкулез и лимфатические пороки, составляющие большую часть оставшейся половины (вставка 6). псевдохилоторакс
Хилоторакс
Травма: торакальная хирургия (особенно при поражении заднего средостения, например, эзофагэктомия), травмы грудной клетки
Новообразование: лимфома или метастатическая карцинома
, цирроз, обструкция центральных вен, хилоацитИдиопатический (около 10%)
Псевдохилоторакс
Туберкулез
Ревматоидный эффузивный артрит
Диагностика другого его
Хилоторакс следует отличать от псевдохилоторакса или «холестеринового плеврита», который возникает в результате накопления кристаллов холестерина. Ревматоидный плеврит и туберкулезный плеврит являются наиболее частыми причинами псевдохилезного выпота.138. 151 Псевдохилоторакс обычно возникает в результате хронического (часто многолетнего) плеврального выпота, и плевра обычно заметно утолщена.152 Существуют исключения, и клиницистам рекомендуется не отказываться от диагноза при отсутствии хронического заболевания и утолщенной плевры.153
Хилоторакс и псевдохилоторакс можно отличить с помощью липидного анализа жидкости. Демонстрация хиломикронов подтверждает хилоторакс, тогда как наличие кристаллов холестерина диагностирует псевдохилоторакс. Истинный хилоторакс обычно имеет высокий уровень триглицеридов, обычно> 1,24 ммоль / л (110 мг / дл), и его обычно можно исключить, если уровень триглицеридов <0.56 ммоль / л (50 мг / дл). При псевдохилотораксе уровень холестерина> 5,18 ммоль / л (200 мг / дл) или наличие кристаллов холестерина являются диагностическими независимо от уровней триглицеридов (см. Таблицу 4) .152–154
Таблица 4Значения липидов плевральной жидкости при псевдохилотораксе и цилотораксе
Хилоторакс может быть результатом трансдиафрагмальной миграции хилезного асцита, который может быть вторичным по отношению к циррозу печени. В этих случаях плевральный выпот часто бывает транссудатом.
Доброкачественный асбестовый плевральный выпот
Доброкачественный асбестовый плевральный выпот обычно диагностируется в первые два десятилетия после воздействия асбеста.Распространенность зависит от дозы и имеет более короткий латентный период по сравнению с другими заболеваниями, связанными с асбестом.155 Выпот обычно небольшой и бессимптомный, часто с геморрагической плевральной жидкостью.156, 157 Существует склонность к исчезновению выпота в течение 6 месяцев. оставляя после себя остаточное диффузное утолщение плевры.156, 157 Поскольку окончательных тестов нет, диагноз может быть установлен с уверенностью только после длительного периода наблюдения, и следует рассмотреть возможность ранней торакоскопии с биопсией плевры у любого пациента с плевральным выпотом. и история воздействия асбеста, особенно при наличии боли в груди.В таблице 5 приведены клинические характеристики и характеристики плевральной жидкости других важных причин односторонних плевральных выпотов.