инструкция к применениюю лекарственного средства
Торговое названиеВалидол®
Международное непатентованное название
Нет
Лекарственная форма
Таблетки сублингвальные, 0,06 г
Состав
Одна таблетка содержит
активное вещество — раствор ментола в ментиловом эфире кислоты изовалериановой (натуральный ментол- экстракт мяты- 4,9 %) 0,06 г;
вспомогательные вещества: сахар измельченный (пудра), кальция стеарат.
Описание
Таблетки плоскоцилиндрической формы с фаской и риской, белого или желтовато-белого цвета, с характерным запахом ментола. На поверхности таблеток допускаются серые вкрапления и налет порошка сахарной пудры.
Фармакотерапевтическая группа
Прочие комбинированные препараты для лечения заболеваний сердца.
Код АТХ С01Е Х
Фармакологические свойства
Фармакокинетика
При сублингвальном применении Валидол® абсорбируется со слизистой оболочки полости рта. Терапевтический эффект наступает приблизительно через 5 минут.
После всасывания биотрансформируется в печени и выделяется с мочой в виде глюкуронидов.
Фармакодинамика
Препарат проявляет успокаивающее действие на центральную нервную систему, а также оказывает умеренное рефлекторное сосудорасширяющее (коронаролитическое) влияние путем рефлекторного раздражения чувствительных нервных («холодовых») рецепторов слизистой оболочки полости рта. Стимуляция рецепторов сопровождается индукцией высвобождения эндорфинов, энкефалинов, динорфинов и других пептидов, гистамина, кининов, которые играют важную роль в уменьшении болевой чувствительности, нормализации проницаемости сосудов и регуляции других важных механизмов функционирования сердечно-сосудистой и нервной систем.
Показания к применению
– приступы стенокардии легкой степени тяжести
– морская и воздушная болезни
– истерия
– невроз
– головная боль, связанная с приемом нитратов
Способ применения и дозы
Таблетки держать во рту (под языком) до полного рассасывания.
Разовая доза для взрослых составляет 1-2 таблетки; суточная – 2-4 таблетки.
При необходимости суточную дозу можно увеличить. Максимальная суточная доза – 600 мг.
Длительность лечения – до 7 дней.
Побочные действия
При продолжительном применении изредка могут наблюдаться легкая тошнота, дискомфорт в животе, слезотечение, головокружение, кратковременная артериальная гипотензия, сонливость, которые быстро проходят самостоятельно.
Возможно развитие аллергических реакций, в том числе отёка Квинке, крапивницы, сыпи, зуда.
Противопоказания
– повышенная чувствительность к компонентам препарата
– выраженная артериальная гипотензия
– острый инфаркт миокарда
– детский возраст до 18 лет
Лекарственные взаимодействия
Валидол® усиливает седативный эффект психотропных средств, опиоидных аналгетиков, алкоголя и средств для наркоза при их одновременном применении.
Возможно потенцирование действия антигипертензивных препаратов при их одновременном применении с Валидолом®.
Валидол® уменьшает выраженность головной боли, обусловленной приемом нитратов.
Особые указания
В случаях, когда боль в области сердца не проходит после приема препарата, необходимо обязательно обратиться к врачу для исключения острого коронарного синдрома.
Препарат содержит сахар, что следует учитывать пациентам с сахарным диабетом.
Применение в педиатрии
Опыта применения препарата для лечения детей нет.
Применение в период беременности или лактации
Применение препарата в период беременности или кормления грудью возможно, если, по мнению врача, ожидаемый положительный эффект для матери превышает потенциальный риск для плода/ребенка.
Особенности влияния препарата на способность управлять транспортным средством или потенциально опасными механизмами
Необходима осторожность в первые часы после приёма препарата при управлении транспортными средствами или работе, которая требует повышенного внимания, из-за возможных побочных эффектов (головокружение и сонливость).
Передозировка
Симптомы: головная боль, тошнота, возбуждение, нарушение деятельности сердца, падение артериального давления, угнетение центральной нервной системы, реакции гиперчувствительности к компонентам препарата (ангионевротический отек, крапивница, зуд, сыпь).
Лечение: отмена препарата и симптоматическая терапия.
Форма выпуска и упаковка
По 10 таблеток в контурную ячейковую упаковку из пленки полимерной бесцветной и фольги алюминиевой печатной лакированной.
По 1 контурной упаковке вместе с инструкцией по медицинскому применению помещают в пачку из картона.
По 10 таблеток в контурной ячейковой упаковке из пленки поливинилхлоридной бесцветной и фольги алюминиевой печатной лакированной без вложения в пачку.
Допускается по согласованию с потребителем групповая упаковка по 200 или 300 контурных ячейковых упаковок вместе с соответствующим количеством инструкций по медицинскому применению на государственном и русском языках в ящик из гофрокартона.
Условия храненияХранить в оригинальной упаковке при температуре не выше 15 °С.
Хранить в недоступном для детей месте!
Срок хранения
2 года
Не использовать по истечении срока годности.
Условия отпуска из аптек
Без рецепта
Производитель
ПАО «Фармак», Украина, 04080, г. Киев, ул. Фрунзе, 74.
Держатель регистрационного удостоверения
ПАО «Фармак», Украина
Наименование, адрес и контактные данные организации на территории Республики Казахстан, принимающей претензии от потребителей по качеству лекарственных средств и ответственной за пострегистрационное наблюдение за безопасностью лекарственного средства
Представительство ПАО «Фармак» в Республике Казахстан
Республика Казахстан, 050012, г. Алматы, ул. Аманагельды 59 «А» Бизнес центр «Шартас», 9 этаж.
Тел +7 (727) 267-64-63, факс +7 (727) 267-63-73, электронный адрес: [email protected]
Мультивитаминный комплекс с глицином и витамином D3
O`vie Мультивитаминный комплекс рекомендован взрослым в качестве дополнительного источника витаминов C, Е, D3, В1, В2, В3 (ниацина), В5 (пантотеновой кислоты), В6, В9 (фолиевой кислоты), В12, биотина, источника глицина.
Данный комплекс способствует повышению концентрации внимания, улучшению работоспособность, повышению иммунитета. Глицин и витамин D3, входящие в состав комплекса, усиливают действие друг друга: помогают пережить стрессовые ситуации и конфликты без потерь для нервной системы, повышая настроение, улучшая память и внимание, а также нормализуют сон.
Состав: лимонная кислота (антиокислитель), гидрокарбонат натрия (регулятор кислотности), глицин, сорбит (подсластитель), витаминный премикс (L-аскорбиновая кислота, мальтодекстрин, DL-альфа-токоферола ацетат, никотиномид, D-пантотенат кальция, D-биотин, цианокобаламин, рибофлавин-5-фосфат натрия, фолиевая кислота, пиридоксина гидрохлорид, тиамина мононитрат), ароматизатор апельсин (мальтодекстрин, вкусоароматические субстанции, носитель гуммиарабик), ароматизатор лимон (мальтодекстрин, ароматический экстракт, носитель гуммиарабик), сахарин натрия (подсластитель), краситель бета-каротин (мальтодекстрин, носитель гуммиарабик, сахароза, среднецепочечные триглицериды, антиокислитель аскорбат натрия, краситель бета-каротин, носитель диоксид кремния, антиокислитель смесь токоферолов), холекальциферол.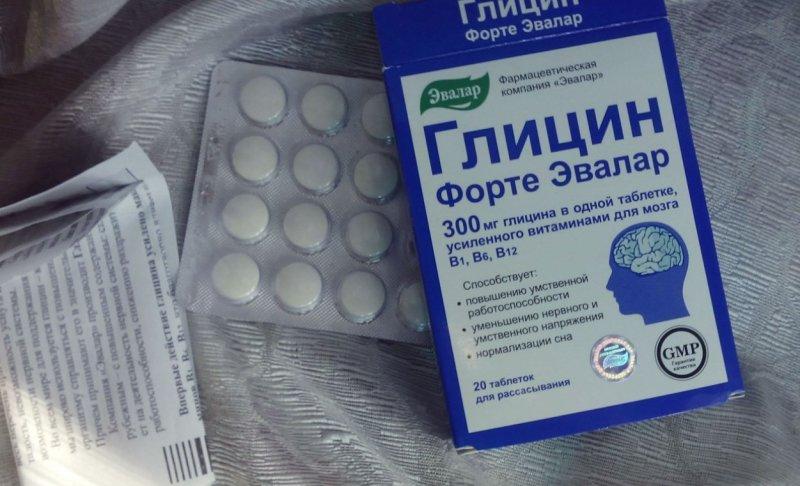
! Содержит подсластитель (сорбит). При чрезмерном употреблении может оказывать слабительное действие.
Активные ингредиенты в 1 таблетке:
|
Компонент |
Количество |
% от рекомендуемой |
|
пантотеновая кислота |
6 мг |
100% |
|
фолиевая кислота |
0,2 мг |
100% |
|
биотин |
0,05 мг |
100% |
|
ниацин |
16 мг |
89% |
|
витамин C |
80 мг |
133*% |
|
витамин E |
12 мг |
120*% |
|
витамин В6 |
1,4 мг |
70% |
|
витамин В2 |
1,4 мг |
88% |
|
витамин В1 |
1,1 мг |
79% |
|
витамин D3 |
0,01 мг |
200*% |
|
витамин В12 |
0,0025 мг |
250*% |
|
глицин |
600 мг |
17% |
* не превышает верхний допустимый уровень потребления.
Рекомендации по применению: взрослым принимать по 1 таблетке 1 раз в день во время приема пищи, растворив в стакане воды (200 мл). Продолжительность приема: 20 дней. При необходимости прием можно повторить. Перед применением рекомендуется проконсультироваться с врачом.
Противопоказания: индивидуальная непереносимость компонентов БАД, беременность, кормление грудью, склонность к расстройству функции кишечника.
Форма выпуска: 20 шипучих таблеток.
Условия хранения: хранить в защищенном от прямых солнечных лучей, недоступном для детей месте, при температуре не выше 25°С.
Страна-изготовитель: Венгрия.
! БАД. Не является лекарственным средством.
Гипоглицинемия и задержка психомоторного развития у ребенка с пигментной ксеродермой
Сохранить цитату в файл
Формат: Резюме (текст)PubMedPMIDAbstract (текст)CSV
Добавить в коллекции
- Создать новую коллекцию
- Добавить в существующую коллекцию
Назовите свою коллекцию:
Имя должно содержать менее 100 символов
Выберите коллекцию:
Не удалось загрузить вашу коллекцию из-за ошибки
Повторите попытку
Добавить в мою библиографию
- Моя библиография
Не удалось загрузить делегатов из-за ошибки
Повторите попытку
Ваш сохраненный поиск
Название сохраненного поиска:
Условия поиска:
Тестовые условия поиска
Электронная почта: (изменить)
Который день? Первое воскресеньеПервый понедельникПервый вторникПервая средаПервый четвергПервая пятницаПервая субботаПервый деньПервый рабочий день
Который день? ВоскресеньеПонедельникВторникСредаЧетвергПятницаСуббота
Формат отчета: РезюмеРезюме (текст)АбстрактАбстракт (текст)PubMed
Отправить максимум:
1 шт. 5 шт. 10 шт. 20 шт. 50 шт. 100 шт. 200 шт.
5 шт. 10 шт. 20 шт. 50 шт. 100 шт. 200 шт.
Отправить, даже если нет новых результатов
Необязательный текст в электронном письме:
Создайте файл для внешнего программного обеспечения для управления цитированием
Полнотекстовые ссылки
Уайли
Полнотекстовые ссылки
Отчеты о делах
. 1999 декабрь; 22 (8): 915-24.
дои: 10.1023/а:1005691424004.
Э. Дж. Квакенбуш 1
принадлежность
- 1 Отделение генетики, Детская больница, Бостон, Массачусетс 02115, США.

- PMID: 10604143
- DOI: 10.1023/а:1005691424004
Отчеты о клинических случаях
. 1999 декабрь; 22 (8): 915-24.
дои: 10.1023/а:1005691424004.
Авторы
Э. Дж. Квакенбуш 1 , К. Х. Кремер, В. А. Гал, В. Ширх, Д. А. Уайтман, К. Левин, Х. Л. Леви
принадлежность
- 1 Отделение генетики, Детская больница, Бостон, Массачусетс 02115, США.

- PMID: 10604143
- DOI: 10.1023/а:1005691424004
Абстрактный
Глицин — заменимая аминокислота, которая служит как тормозным, так и возбуждающим нейротрансмиттером. Гиперглицинемия возникает при некетотической гиперглицинемии, первичном дефекте пути расщепления глицина и как вторичный признак некоторых врожденных нарушений метаболизма органических кислот. Однако никогда не сообщалось о особенно низких уровнях глицина. Здесь мы сообщаем о ребенке с пигментной ксеродермой (XP) группы комплементации C, характеризующейся мутацией донора сплайсинга в гене XPC, множественными раками кожи и специфической и стойкой гипоглицинемией. У него когнитивная задержка, отсутствие речи, аутистические черты, гиперактивность и гипотония, все это не объясняется диагнозом ХР группы С, не неврологической формой заболевания. Лечение пероральным глицином улучшило его гиперактивность. Специфическая гипоглицинемия может указывать на нарушение обмена веществ, вызывающее неврологическую дисфункцию. Неясно, связано ли это с XP или совпадает с ним.
Лечение пероральным глицином улучшило его гиперактивность. Специфическая гипоглицинемия может указывать на нарушение обмена веществ, вызывающее неврологическую дисфункцию. Неясно, связано ли это с XP или совпадает с ним.
Похожие статьи
Неврологические симптомы и естественное течение пигментной ксеродермы.
Анттинен А., Коулу Л., Никоскелайнен Э., Портин Р., Курки Т., Эркиньюнтти М., Ясперс Н.Г., Раамс А., Грин М.Х., Леманн А.Р., Винг Дж.Ф., Арлетт С.Ф., Марттила Р.Дж. Анттинен А. и соавт. Мозг. 2008 г., август; 131 (часть 8): 1979-89. doi: 10.1093/мозг/awn126. Epub 2008 21 июня. Мозг. 2008. PMID: 18567921
Мутационный спектр пигментной ксеродермы группы А у пациентов из Египта.
Амр К.
 , Мессауд О., Эль-Дарути М., Абдельхак С., Эль-Камах Г.
Амр К. и др.
Ген. 2014 янв. 1; 533 (1): 52-6. doi: 10.1016/j.gene.2013.09.125. Epub 2013 14 октября.
Ген. 2014.
PMID: 24135642
, Мессауд О., Эль-Дарути М., Абдельхак С., Эль-Камах Г.
Амр К. и др.
Ген. 2014 янв. 1; 533 (1): 52-6. doi: 10.1016/j.gene.2013.09.125. Epub 2013 14 октября.
Ген. 2014.
PMID: 24135642Снижение уровней мРНК гена репарации ДНК XPC у клинически здоровых родителей пациентов с пигментной ксеродермой.
Хан С.Г., О К.С., Шахлави Т., Уэда Т., Буш Д.Б., Инуи Х., Эммерт С., Имото К., Муниз-Медина В., Бейкер К.С., ДиДжиованна Дж.Дж., Шмидт Д., Хадави А., Метин А., Гозукара Э., Слор Х., Сарасин А., Кремер К.Х. Хан С.Г. и соавт. Канцерогенез. 2006 янв; 27(1):84-94. doi: 10.1093/carcin/bgi204. Epub 2005 4 августа. Канцерогенез. 2006. PMID: 16081512
Распространенная мутация с эффектом основателя у пигментной ксеродермы группы C из Северной Африки.

Суфир Н., Гед С., Бурийон А., Аустерлиц Ф., Шемин С., Старый А., Армьер Дж., Фам Д., Хадир К., Рум Дж., Хадж-Рабиа С., Буаджар Б., Тайеб А., де Верней Х., Бенчики Х., Грандшан Б, Сарасин А. Суфир Н. и др. Джей Инвест Дерматол. 2010 июнь; 130 (6): 1537-42. doi: 10.1038/jid.2009.409. Epub 2010 7 января. Джей Инвест Дерматол. 2010. PMID: 20054342
Пигментная ксеродерма, трихотиодистрофия и синдром Коккейна: сложная взаимосвязь генотип-фенотип.
Кремер К.Х., Патронас Н.Дж., Шиффманн Р., Брукс Б.П., Тамура Д., ДиДжиованна Дж.Дж. Кремер К.Х. и соавт. Неврология. 2007 г., 14 апреля; 145(4):1388-96. doi: 10.1016/j.neuroscience.2006.12.020. Epub 2007 1 февраля. Неврология. 2007. PMID: 17276014 Бесплатная статья ЧВК. Обзор.
Посмотреть все похожие статьи
Цитируется
Дефицит гуанидиноуксусной кислоты: новое явление в клинической медицине?
Остойич С.
 М., Ратгебер Л., Олах А., Бетлехем Дж., Акс П.
Остойич С.М. и соавт.
Int J Med Sci. 2020 12 сентября; 17 (16): 2544-2550. doi: 10.7150/ijms.47757. Электронная коллекция 2020.
Int J Med Sci. 2020.
PMID: 33029096
Бесплатная статья ЧВК.
Обзор.
М., Ратгебер Л., Олах А., Бетлехем Дж., Акс П.
Остойич С.М. и соавт.
Int J Med Sci. 2020 12 сентября; 17 (16): 2544-2550. doi: 10.7150/ijms.47757. Электронная коллекция 2020.
Int J Med Sci. 2020.
PMID: 33029096
Бесплатная статья ЧВК.
Обзор.Роль аминокислот в нейротрансмиссии и флуоресцентные инструменты для их обнаружения.
Далангин Р., Ким А., Кэмпбелл Р.Э. Далангин Р. и соавт. Int J Mol Sci. 2020 авг 27;21(17):6197. doi: 10.3390/ijms21176197. Int J Mol Sci. 2020. PMID: 32867295 Бесплатная статья ЧВК. Обзор.
XPC: Идем туда, где раньше не было ни одного датчика повреждения ДНК.
Немцов Л., Любин А., Чжан Л., Гонг Ф. Немцов Л.
 и соавт.
Восстановление ДНК (Amst). 2015 дек;36:19-27. doi: 10.1016/j.dnarep.2015.09.004. Epub 2015 9 сентября.
Восстановление ДНК (Amst). 2015.
PMID: 26422135
Бесплатная статья ЧВК.
Обзор.
и соавт.
Восстановление ДНК (Amst). 2015 дек;36:19-27. doi: 10.1016/j.dnarep.2015.09.004. Epub 2015 9 сентября.
Восстановление ДНК (Amst). 2015.
PMID: 26422135
Бесплатная статья ЧВК.
Обзор.Ограничение питательных веществ в раннем возрасте ухудшает метаболический профиль крови и головного мозга и нейроповедение, предрасполагая к болезни Альцгеймера с возрастом.
Томи М., Чжао И., Тамотаран С., Шин Б.К., Деваскар С.У. Томи М. и др. Мозг Res. 2013 7 февраля; 1495: 61-75. doi: 10.1016/j.brainres.2012.11.050. Epub 2012 7 декабря. Мозг Res. 2013. PMID: 23228723 Бесплатная статья ЧВК.
Рак и неврологическая дегенерация при пигментной ксеродерме: долгосрочное наблюдение характеризует роль репарации ДНК.

Брэдфорд П.Т., Гольдштейн А.М., Тамура Д., Хан С.Г., Уэда Т., Бойл Дж., О К.С., Имото К., Инуи Х., Мориваки С., Эммерт С., Пайк К.М., Разиуддин А., Плона Т.М., ДиДжиованна Дж.Дж., Такер М.А., Кремер К.Х. Брэдфорд П.Т. и др. J Med Genet. 2011 март; 48(3):168-76. doi: 10.1136/jmg.2010.083022. Epub 2010 19 ноября. J Med Genet. 2011. PMID: 21097776 Бесплатная статья ЧВК.
Просмотреть все статьи «Цитируется по»
Рекомендации
- Клин Хим. 1996 март; 42(3):349-55 — пабмед
- Анальная хим. 1975 июль; 47 (8): 1313-21 — пабмед
- Джей Инвест Дерматол.
 1998 ноябрь; 111 (5): 791-6
—
пабмед
1998 ноябрь; 111 (5): 791-6
—
пабмед
- Джей Инвест Дерматол.
- Анальная биохимия. 15 ноября 1997 г .; 253 (2): 201–9. — пабмед
- Арка Дерматол. 1987 г., февраль; 123 (2): 241–50. — пабмед
Типы публикаций
термины MeSH
вещества
Грантовая поддержка
- Z01 BC004517-31/Внутренний NIH HHS/США
Полнотекстовые ссылки
Уайли
Укажите
Формат: ААД АПА МДА НЛМ
Отправить по номеру
Богатая пролином/глицином область белка адгезии биопленки Aap образует удлиненный стебель, который сопротивляется уплотнению
. 2017 20 января; 429 (2): 261-279.
2017 20 января; 429 (2): 261-279.
doi: 10.1016/j.jmb.2016.11.017. Epub 2016 25 ноября.
Александр Яравский 1 , Лэнс Р Английский 2 , Стивен Т. Уиттен 2 , Эндрю Б. Герр 3
Принадлежности
- 1 Программа магистратуры по молекулярной генетике, биохимии и микробиологии, Медицинский колледж Университета Цинциннати, Цинциннати, Огайо, 45267, США; Отделение иммунобиологии и Центр системной иммунологии, Медицинский центр детской больницы Цинциннати, Цинциннати, Огайо, 45229, США.
- 2 Кафедра химии и биохимии Техасского государственного университета, Сан-Маркос, Техас 78666, США.

- 3 Отделение иммунобиологии и Центр системной иммунологии, Медицинский центр детской больницы Цинциннати, Цинциннати, Огайо 45229, США; Отделение инфекционных заболеваний, Медицинский центр детской больницы Цинциннати, Цинциннати, Огайо, 45229, США. Электронный адрес: [email protected].
- PMID: 278
- PMCID: PMC5363081
- DOI: 10.1016/j.jmb.2016.11.017
Бесплатная статья ЧВК
Александр Э. Яравски и соавт.
Дж Мол Биол. .
Бесплатная статья ЧВК
. 2017 20 января; 429 (2): 261-279.
doi: 10.1016/j.jmb.2016.11.017. Epub 2016 25 ноября.
Авторы
Александр Яравский 1 , Лэнс Р Английский 2 , Стивен Т. Уиттен 2 , Эндрю Б. Герр 3
Принадлежности
- 1 Программа магистратуры по молекулярной генетике, биохимии и микробиологии, Медицинский колледж Университета Цинциннати, Цинциннати, Огайо, 45267, США; Отделение иммунобиологии и Центр системной иммунологии, Медицинский центр детской больницы Цинциннати, Цинциннати, Огайо, 45229, США.

- 2 Кафедра химии и биохимии Техасского государственного университета, Сан-Маркос, Техас 78666, США.
- 3 Отделение иммунобиологии и Центр системной иммунологии, Медицинский центр детской больницы Цинциннати, Цинциннати, Огайо 45229, США; Отделение инфекционных заболеваний, Медицинский центр детской больницы Цинциннати, Цинциннати, Огайо, 45229, США. Электронный адрес: [email protected].
- PMID: 278
- PMCID: PMC5363081
- DOI: 10.1016/j.jmb.2016.11.017
Абстрактный
Staphylococcus epidermidis является одним из основных видов бактерий, ответственных за инфекции, связанные с оказанием медицинской помощи. Наиболее важным фактором вирулентности S. epidermidis является его способность образовывать биопленку, которая придает бактериям высокую устойчивость к иммунным реакциям хозяина и действию антибиотиков. Межклеточная адгезия внутри биопленки опосредуется белком, ассоциированным с накоплением (Aap), белком, закрепленным на клеточной стенке, который самособирается зависимым от цинка образом. С-концевая часть Аар содержит богатую пролином/глицином область (PGR) длиной 135 аминокислот, которая еще не охарактеризована. Область содержит набор из 18 почти идентичных повторов AEPGKP. Анализ PGR с использованием биофизических методов показал, что эта область представляет собой сильно вытянутый, внутренне неупорядоченный полипептид с необычно высокой склонностью к спирали полипролина II типа. В отличие от многих внутренне неупорядоченных полипептидов, наблюдалась минимальная температурная зависимость глобального конформационного состояния PGR в растворе, измеренная с помощью аналитического ультрацентрифугирования и динамического светорассеяния.
Наиболее важным фактором вирулентности S. epidermidis является его способность образовывать биопленку, которая придает бактериям высокую устойчивость к иммунным реакциям хозяина и действию антибиотиков. Межклеточная адгезия внутри биопленки опосредуется белком, ассоциированным с накоплением (Aap), белком, закрепленным на клеточной стенке, который самособирается зависимым от цинка образом. С-концевая часть Аар содержит богатую пролином/глицином область (PGR) длиной 135 аминокислот, которая еще не охарактеризована. Область содержит набор из 18 почти идентичных повторов AEPGKP. Анализ PGR с использованием биофизических методов показал, что эта область представляет собой сильно вытянутый, внутренне неупорядоченный полипептид с необычно высокой склонностью к спирали полипролина II типа. В отличие от многих внутренне неупорядоченных полипептидов, наблюдалась минимальная температурная зависимость глобального конформационного состояния PGR в растворе, измеренная с помощью аналитического ультрацентрифугирования и динамического светорассеяния. Кроме того, PGR был устойчив к конформационному коллапсу или образованию α-спирали при добавлении осмолита N-оксида триметиламина или сорастворителя 2,2,2-трифторэтанола. В совокупности эти результаты свидетельствуют о том, что PGR функционирует как упругий удлиненный стебель, который проецирует остальную часть Aap наружу от стенки бактериальной клетки, способствуя межклеточной адгезии между клетками в биопленке. Эта работа проливает свет на области низкой сложности, которые часто обнаруживаются вблизи точки прикрепления белков, закрепленных на клеточной стенке бактерий.
Кроме того, PGR был устойчив к конформационному коллапсу или образованию α-спирали при добавлении осмолита N-оксида триметиламина или сорастворителя 2,2,2-трифторэтанола. В совокупности эти результаты свидетельствуют о том, что PGR функционирует как упругий удлиненный стебель, который проецирует остальную часть Aap наружу от стенки бактериальной клетки, способствуя межклеточной адгезии между клетками в биопленке. Эта работа проливает свет на области низкой сложности, которые часто обнаруживаются вблизи точки прикрепления белков, закрепленных на клеточной стенке бактерий.
Ключевые слова: эпидермальный стафилококк; аналитическое ультрацентрифугирование; заякоренный белок клеточной стенки; круговой дихроизм; внутренне неупорядоченный белок.
Copyright © 2016 Elsevier Ltd. Все права защищены.
Цифры
Рисунок 1. PGR показывает аберрантную подвижность и…
PGR показывает аберрантную подвижность и…
Рисунок 1. PGR демонстрирует аберрантную подвижность и существует в виде удлиненного мономера в растворе
(а)…
Рисунок 1. PGR демонстрирует аберрантную подвижность и существует в виде удлиненного мономера в растворе. (a) Схема Aap, прикрепленного к пептидогликановому слою клеточной стенки S. epidermidis с помощью мотива LPXTG Sortase A, с примерными границами доменов, показанными в относительном масштабе. (b) Аминокислотная последовательность PGR, фланкированная концом супердомена B-повтора (EYGPT) и мотивом LPXTG ( подчеркнуто ) — обратите внимание на повторяющиеся гекстады AEPGKP. Аминокислоты пронумерованы так, как они появляются в Aap из S. epidermidis RP62A. Положительно заряженные остатки в PGR окрашены в синий цвет , а отрицательно заряженные остатки окрашены в красный цвет .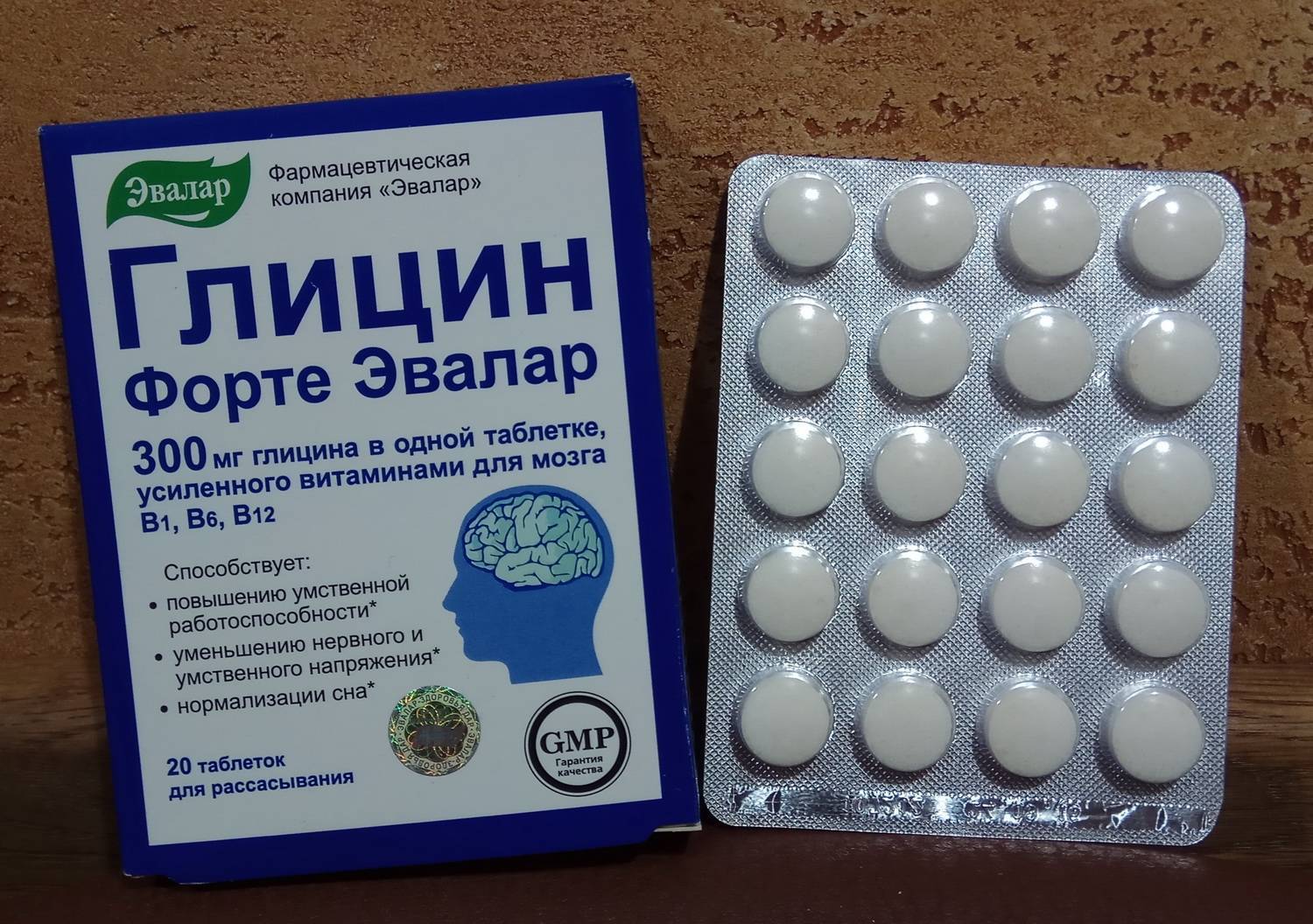 На панели (c) показана аберрантная подвижность PGR с помощью окрашенного серебром SDS-PAGE. Fusion относится к гибридному белку His-MBP-PGR. +TEV через 6 часов после добавления протеазы TEV для отщепления метки His-MBP от PGR. PGR представляет собой посточистку ANX. В то время как слитый белок His-MBP-PGR мигрирует, как и ожидалось, расщепленный PGR (13,2 кДа) мигрирует более чем в 10 раз медленнее, чем ожидалось. (d) Скорость седиментации Данные поглощения AUC ( маркеров ) и модель наилучшего соответствия ( линий ) на верхней панели . Остаточная ошибка на нижней панели , демонстрирующая хорошее соответствие данным. На панели (е) показан анализ распределения c(s) PGR при различных концентрациях (75 мкМ = 1 мг/мл), что указывает на то, что PGR не собирается самосборкой. Коэффициент трения колебался от 2,1 до 2,3, что указывает на сильно удлиненный вид. Расчетная молекулярная масса была близка к мономерной PGR, что позволяет предположить, что PGR существует в виде сильно вытянутого мономера в нативных условиях во всем протестированном диапазоне концентраций.
На панели (c) показана аберрантная подвижность PGR с помощью окрашенного серебром SDS-PAGE. Fusion относится к гибридному белку His-MBP-PGR. +TEV через 6 часов после добавления протеазы TEV для отщепления метки His-MBP от PGR. PGR представляет собой посточистку ANX. В то время как слитый белок His-MBP-PGR мигрирует, как и ожидалось, расщепленный PGR (13,2 кДа) мигрирует более чем в 10 раз медленнее, чем ожидалось. (d) Скорость седиментации Данные поглощения AUC ( маркеров ) и модель наилучшего соответствия ( линий ) на верхней панели . Остаточная ошибка на нижней панели , демонстрирующая хорошее соответствие данным. На панели (е) показан анализ распределения c(s) PGR при различных концентрациях (75 мкМ = 1 мг/мл), что указывает на то, что PGR не собирается самосборкой. Коэффициент трения колебался от 2,1 до 2,3, что указывает на сильно удлиненный вид. Расчетная молекулярная масса была близка к мономерной PGR, что позволяет предположить, что PGR существует в виде сильно вытянутого мономера в нативных условиях во всем протестированном диапазоне концентраций. Стандартизованные коэффициенты седиментации ( s 20, w ) отображаются как s при 20°C и в воде. Для определения стандартизованного коэффициента седиментации при бесконечном разбавлении ( с 0 20, w ) была проведена линейная регрессия путем экстраполяции с 20, с (к нулю концентрации), вставка), что дает значение 1,06 S. Значения, использованные в экстраполяции, показаны в белых кружках , тогда как значение 300 мкМ (4 мг/мл) показано как закрашенный кружок опущен. Подробные результаты можно найти в таблице S1.
Стандартизованные коэффициенты седиментации ( s 20, w ) отображаются как s при 20°C и в воде. Для определения стандартизованного коэффициента седиментации при бесконечном разбавлении ( с 0 20, w ) была проведена линейная регрессия путем экстраполяции с 20, с (к нулю концентрации), вставка), что дает значение 1,06 S. Значения, использованные в экстраполяции, показаны в белых кружках , тогда как значение 300 мкМ (4 мг/мл) показано как закрашенный кружок опущен. Подробные результаты можно найти в таблице S1.
Рисунок 2. Эксклюзионная хроматография (SEC) подтверждает…
Рис. 2. Эксклюзионная хроматография (ЭХ) подтверждает расширенную конформацию в растворе
Панель (а)…
Рисунок 2. Эксклюзионная хроматография (SEC) подтверждает расширенную конформацию в растворе. Панель
Эксклюзионная хроматография (SEC) подтверждает расширенную конформацию в растворе. Панель (a) представляет собой репрезентативный набор данных экспериментов SEC с использованием смолы G-100. Свернутые стандарты белков отображаются в виде пустых кружков , а их линейная регрессия представлена пунктирной линией . R h свернутых белков оценивали как полумаксимальное расстояние C α -C α , полученное из рентгеноструктурного анализа структур бычьего сывороточного альбумина (BSA – PDB ID: 4F5S) [128]. , куриный альбумин (Alb – PDB ID: 1OVA) [129], карбоангидраза (CA – PDB ID: 1V9I) [130] и миоглобин лошади (Myo – PDB ID: 2O58) [131]. Измеренное методом SEC значение K D PGR ( синий кружок ) наносили на линейную регрессию белковых стандартов с получением R h 37,21 Å (обозначено пунктирными линиями ) , или в среднем 37,06 Å в 4 независимых экспериментах (2 с использованием смолы G-75, 2 с использованием смолы G-100), в каждом из которых было 3–9 повторов обучающих белков и 2–3 повтора PGR или PGR-Tyr.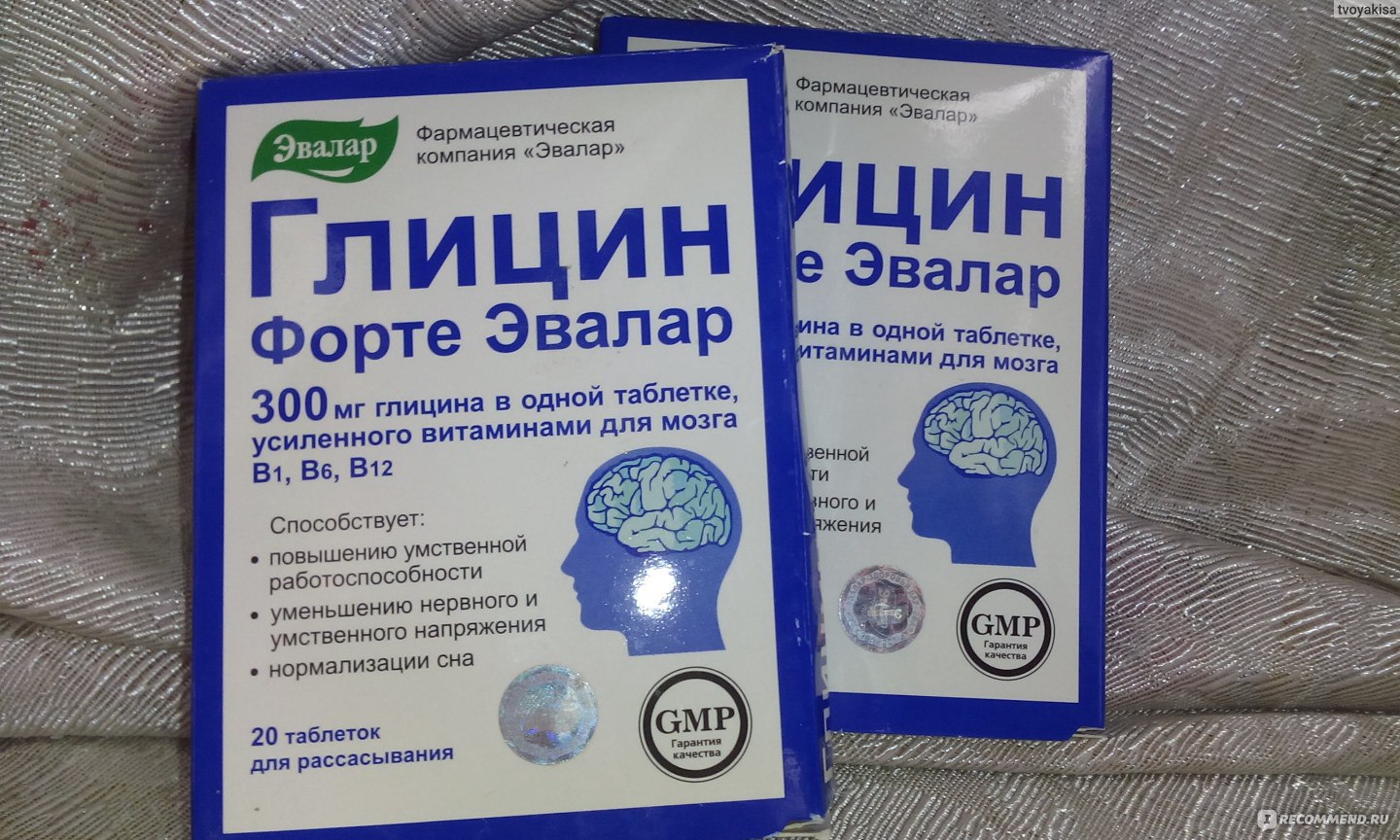 Добавление Tyr к С-концу PGR, по-видимому, не оказывает существенного влияния на R h , но позволял проводить измерения при 1 мг/мл, а не при 3-4 мг/мл, необходимых для PGR. На панели (b) исследуется линейная зависимость между K D и log MW для стандартов свернутого белка. Очевидно, что PGR отклоняется от этой тенденции. PGR имеет 90 398 K 90 426 D 90 429 90 399, что можно ожидать для свернутого белка 50,9 кДа (log 90 398 MW 90 399 = 4,71), как показано 90 398 пунктирными линиями 90 399, начинающимися с PGR 9.0398 К Д и заканчивая бревном МВт . На панели (c) показано соотношение между log R h в Å и log N , где N представляет собой количество остатков. Свернутые белки [51, 53] ( пустых кружков, пунктирная линейная регрессия ) отклоняются иначе, чем IDP [42] ( закрашенных кружков, сплошная линейная регрессия ). Тенденции PGR с IDP и несвернутыми белками. Также для справки показан IDP p53 (1-93).
Добавление Tyr к С-концу PGR, по-видимому, не оказывает существенного влияния на R h , но позволял проводить измерения при 1 мг/мл, а не при 3-4 мг/мл, необходимых для PGR. На панели (b) исследуется линейная зависимость между K D и log MW для стандартов свернутого белка. Очевидно, что PGR отклоняется от этой тенденции. PGR имеет 90 398 K 90 426 D 90 429 90 399, что можно ожидать для свернутого белка 50,9 кДа (log 90 398 MW 90 399 = 4,71), как показано 90 398 пунктирными линиями 90 399, начинающимися с PGR 9.0398 К Д и заканчивая бревном МВт . На панели (c) показано соотношение между log R h в Å и log N , где N представляет собой количество остатков. Свернутые белки [51, 53] ( пустых кружков, пунктирная линейная регрессия ) отклоняются иначе, чем IDP [42] ( закрашенных кружков, сплошная линейная регрессия ). Тенденции PGR с IDP и несвернутыми белками. Также для справки показан IDP p53 (1-93).
Рисунок 3. PGR содержит полипролин типа II…
Рисунок 3. PGR содержит спираль полипролина II типа
На панели (a) показаны спектры КД…
Рисунок 3. PGR содержит спираль полипролина II типа. На панели (а) показаны спектры КД PGR от 5°C в пурпурном до 95°C в красном , собранные с шагом 10°C. Эти спектры напоминают спектры пептидов, содержащих PPII, показывая, что PPII переходит в неупорядоченный клубок при повышении температуры. Средняя эллиптичность остатка, [θ] (градусы см 2 дмоль -1 остаток -1 ), в тысячах нанесен на график зависимости от длины волны. На вставке показана температурная зависимость минимума при 200 нм. На панели (b) показан разностный график спектра при каждой температуре, вычтенной из спектра при 95°C. На вставке показана температурная зависимость локального максимума при 222 нм, связанная с содержанием PPII.
На вставке показана температурная зависимость локального максимума при 222 нм, связанная с содержанием PPII.
Рисунок 4. PGR показывает слабую температурную зависимость…
Рис. 4. PGR демонстрирует слабую температурную зависимость R h
На панели (a) показаны рассчитанные c(s)…
Рис. 4. PGR демонстрирует слабую температурную зависимость R h Панель (а) показывает рассчитанное распределение c(s) PGR с небольшим изменением коэффициента седиментации при 25 мкМ между 4°C ( фиолетовая линия ), 20°С ( зеленый ) и 37°С ( красный ). На панели (b) показано c( s , f/f 0 ) двумерное распределение PGR по размеру и форме при 4°C ( слева ), 20°C ( в середине ) и 37 ° C ( справа ) при 25 мкМ, что указывает на один вид в каждом случае. Обратите внимание, что коэффициенты седиментации на этой панели представляют собой кажущиеся ( с*) значения, которые сходятся к 1,0-1,1 после поправки на влияние температуры на вязкость и плотность буфера. Панель (c) отображает DLS, измеренное R h для PGR в синих кружках. Измерения проводились с шагом 10°C между 5°C и 45°C. Столбики погрешностей показывают ± стандартное отклонение для измерений DLS. Открытый квадрат обозначает R h , измеренный SEC (37,06 Å при 22°C). Красный треугольник вдоль оси y ( R h ) показывает предсказанное R h значение 38,50 Å из степенной зависимости масштабирования. Черные треугольники показывают молярную эллиптичность остатка при 222 нм при каждой температуре, соответствующую содержанию PPII. Данные CD предполагают небольшое температурно-зависимое снижение содержания PPII, но это не приводит к R h столько, сколько можно было бы ожидать на основании предыдущих наблюдений в литературе [51, 52].
Обратите внимание, что коэффициенты седиментации на этой панели представляют собой кажущиеся ( с*) значения, которые сходятся к 1,0-1,1 после поправки на влияние температуры на вязкость и плотность буфера. Панель (c) отображает DLS, измеренное R h для PGR в синих кружках. Измерения проводились с шагом 10°C между 5°C и 45°C. Столбики погрешностей показывают ± стандартное отклонение для измерений DLS. Открытый квадрат обозначает R h , измеренный SEC (37,06 Å при 22°C). Красный треугольник вдоль оси y ( R h ) показывает предсказанное R h значение 38,50 Å из степенной зависимости масштабирования. Черные треугольники показывают молярную эллиптичность остатка при 222 нм при каждой температуре, соответствующую содержанию PPII. Данные CD предполагают небольшое температурно-зависимое снижение содержания PPII, но это не приводит к R h столько, сколько можно было бы ожидать на основании предыдущих наблюдений в литературе [51, 52]. Например, температурная зависимость R h p53(1-93) показана серыми кружками , которые также отражают собственную молярную эллиптичность остатка при 221 нм, локальный максимум PPII, наблюдаемый для p53 ( перерисовано из [51]). Линейные соответствия данных DLS для PGR и p53 (1-93) показаны сплошными линиями. Наклон (м) линии для подбора PGR (m = -0,015) менее крутой, чем у подбора для p53(1-93) (m = -0,076), что указывает на более слабую температурную зависимость R h по сравнению с p53(1-93).
Например, температурная зависимость R h p53(1-93) показана серыми кружками , которые также отражают собственную молярную эллиптичность остатка при 221 нм, локальный максимум PPII, наблюдаемый для p53 ( перерисовано из [51]). Линейные соответствия данных DLS для PGR и p53 (1-93) показаны сплошными линиями. Наклон (м) линии для подбора PGR (m = -0,015) менее крутой, чем у подбора для p53(1-93) (m = -0,076), что указывает на более слабую температурную зависимость R h по сравнению с p53(1-93).
Рисунок 5. Локальная конформация PGR…
Рисунок 5. Локальная конформация PGR показывает устойчивость к химическим возмущающим факторам
(а) спектры КД…
Рисунок 5. Локальная конформация PGR демонстрирует устойчивость к химическим воздействиям.
(а) Спектры КД, показывающие индукцию PGR PPII при 0 М, 2 М, 4 М, 6 М мочевине ( темная заливка до светлая заливка ; спектры 0 М и 2 М накладываются друг на друга при 37°C). (b) Спектры КД PGR в 0 М, 2 М, 4 М, 6 М GdnHCl ( темное заполнение от до светлое заполнение ; спектры 0 М и 2 М перекрываются, а 4 М и 6 М перекрываются при 4 ° C ), показывая более слабую индукцию PPII, чем с мочевиной. (c) КД-спектры PGR в 0 М ( темная заливка ) или 3 М ( светлая заливка ) ТМАО без изменений, что указывает на высокую устойчивость к этому осмолиту. D , КД спектры PGR в 0%, 15%, 45% или 75% TFE ( темная заливка до светлая заливка ; спектры 0% и 15% TFE накладываются друг на друга) при 4°C ( фиолетовых кругов) ), 20°C ( зеленых квадратов ) или 37°C ( красных треугольников ). Неожиданно никаких существенных изменений в спектрах от 0 до 15% ТФЭ не наблюдалось. Данные по мочевине, GdnHCl и ТМАО показаны только в диапазоне 210–240 нм из-за высокого уровня шума ниже 208 нм.
Рисунок 6. Кулоновские эффекты не играют…
Рисунок 6. Кулоновские эффекты не играют роли в локальных или глобальных конформациях
…
Рисунок 6. Кулоновские эффекты не играют роли в локальных или глобальных конформациях. Спектры КД в (а) не показывают различий в 30 мМ, 100 мМ, 300 мМ или 1 М NaF ( темная заливка 9от 0399 до светлая заливка ) при 4°C ( фиолетовых кружков ), 20°C ( зеленых квадратов ) или 37°C ( красных треугольников ). На (b) спектры КД PGR при pH 2 ( светлая заливка ) имеют несколько менее отрицательный минимум около 200 нм при всех температурах, но спектры при pH 7,4 ( средняя заливка ) или pH 12 ( темная заливка ) не показывают различий.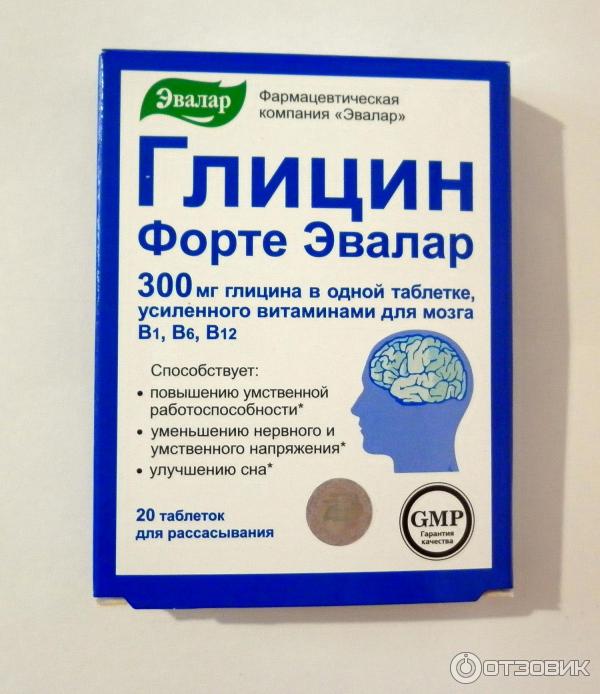 Вместе (a) и (b) указывают на то, что взаимодействия зарядов не влияют на локальное содержание PPII. Панель (с) показывает c(s) распределения из экспериментов по скорости седиментации AUC при 30 мМ, 100 мМ, 300 мМ или 1 М ( сплошные, короткие пунктирные, длинные пунктирные и пунктирные линии ) NaCl при 4°C ( фиолетовые линии ), 20°C ( зеленый ) или 37°C ( красный ), выявляя лишь небольшое изменение s 20, w при 20°C и 37°C при 1 М NaCl . Эти данные показывают, что кулоновские эффекты мало влияют на глобальные конформации, доступные для PGR. (г), c(s) распределения из экспериментов скорости седиментации AUC на апо-PGR ( черная линия ) или PGR в присутствии 2 мМ CaCl 2 ( фиолетовый ), 2 мМ MgCl 2 ( зеленый ) или 2 мМ ZnCl 2 ( красный ) при 20°C, не показывая изменений общей конформации из-за взаимодействий с двухвалентными катионами.
Вместе (a) и (b) указывают на то, что взаимодействия зарядов не влияют на локальное содержание PPII. Панель (с) показывает c(s) распределения из экспериментов по скорости седиментации AUC при 30 мМ, 100 мМ, 300 мМ или 1 М ( сплошные, короткие пунктирные, длинные пунктирные и пунктирные линии ) NaCl при 4°C ( фиолетовые линии ), 20°C ( зеленый ) или 37°C ( красный ), выявляя лишь небольшое изменение s 20, w при 20°C и 37°C при 1 М NaCl . Эти данные показывают, что кулоновские эффекты мало влияют на глобальные конформации, доступные для PGR. (г), c(s) распределения из экспериментов скорости седиментации AUC на апо-PGR ( черная линия ) или PGR в присутствии 2 мМ CaCl 2 ( фиолетовый ), 2 мМ MgCl 2 ( зеленый ) или 2 мМ ZnCl 2 ( красный ) при 20°C, не показывая изменений общей конформации из-за взаимодействий с двухвалентными катионами.
Рисунок 7. Модель ААП на…
Модель ААП на…
Рис. 7. Модель Аар на поверхности S. epidermidis
Стенка грамположительной клетки…
Рис. 7. Модель Аар на поверхности S. epidermidis .Стенка грамположительных клеток S. epidermidis содержит слой пептидогликана. Сортаза А ковалентно связывает мотив LPXTG Аар с липидом II по направлению к внешней стороне пептидогликанового слоя. Область, богатая P/G, образует удлиненный стебель с высокой склонностью к спирали полипролина II типа и высокой устойчивостью к уплотнению. Эта область выталкивает супердомен В-повтора наружу и от поверхности клетки, где он может лучше взаимодействовать с супердоменом В-повтора соседних 9 клеток.0398 клеток S. epidermidis в присутствии ионов Zn 2+ и способствуют образованию биопленок.
См. это изображение и информацию об авторских правах в PMC
это изображение и информацию об авторских правах в PMC
Похожие статьи
Функциональные последствия изменчивости последовательности B-повторов в белке стафилококковой биопленки Aap: расшифровка кода сборки.
Шелтон С.Л., Конради Д.Г., Герр А.Б. Шелтон С.Л. и соавт. Biochem J. 1 февраля 2017 г.; 474(3):427-443. DOI: 10.1042/BCJ20160675. Epub 2016 21 ноября. Биохим Дж. 2017. PMID: 27872164 Бесплатная статья ЧВК.
Белок адгезии биопленки Aap из Staphylococcus epidermidis образует цинкзависимые амилоидные волокна.
Яравски А.Е., Джонс С.Л., Шук П., Герр А.Б. Яравский А.Е. и соавт. Дж. Биол. Хим. 3 апреля 2020 г.; 295(14):4411-4427. doi: 10.1074/jbc.
 RA119.010874. Epub 2020 26 февраля.
Дж. Биол. Хим. 2020.
PMID: 32102851
Бесплатная статья ЧВК.
RA119.010874. Epub 2020 26 февраля.
Дж. Биол. Хим. 2020.
PMID: 32102851
Бесплатная статья ЧВК.За межклеточную адгезию в стафилококковых биопленках отвечает цинкзависимый модуль адгезии.
Conrady DG, Brescia CC, Horii K, Weiss AA, Hassett DJ, Herr AB. Конради Д.Г. и соавт. Proc Natl Acad Sci U S A. 2008 Dec 9;105(49):19456-61. doi: 10.1073/pnas.0807717105. Epub 2008 1 декабря. Proc Natl Acad Sci U S A. 2008. PMID: 136 Бесплатная статья ЧВК.
Матрицы биопленок на белковой основе у стафилококков.
Speziale P, Pietrocola G, Foster TJ, Geoghegan JA. Специале П. и др. Front Cell Infect Microbiol. 2014 10 декабря; 4:171. doi: 10.3389/fcimb.2014.00171.
 Электронная коллекция 2014.
Front Cell Infect Microbiol. 2014.
PMID: 25540773
Бесплатная статья ЧВК.
Обзор.
Электронная коллекция 2014.
Front Cell Infect Microbiol. 2014.
PMID: 25540773
Бесплатная статья ЧВК.
Обзор.Структурные основы формирования биопленок Staphylococcus epidermidis: механизмы и молекулярные взаимодействия.
Бюттнер Х., Мак Д., Роде Х. Бюттнер Х. и др. Front Cell Infect Microbiol. 2015 17 фев; 5:14. doi: 10.3389/fcimb.2015.00014. Электронная коллекция 2015. Front Cell Infect Microbiol. 2015. PMID: 25741476 Бесплатная статья ЧВК. Обзор.
Посмотреть все похожие статьи
Цитируется
Экспрессия, очистка и характеристика р53-связывающего домена белка 6, связывающего ретинобластому (RBBP6).
Рассел Б.Л., Нтваса М.
 Рассел Б.Л. и соавт.
ПЛОС Один. 2023 10 февраля; 18 (2): e0277478. doi: 10.1371/journal.pone.0277478. Электронная коллекция 2023.
ПЛОС Один. 2023.
PMID: 36763571
Бесплатная статья ЧВК.
Рассел Б.Л. и соавт.
ПЛОС Один. 2023 10 февраля; 18 (2): e0277478. doi: 10.1371/journal.pone.0277478. Электронная коллекция 2023.
ПЛОС Один. 2023.
PMID: 36763571
Бесплатная статья ЧВК.Механистические основы межвидовой конкуренции стафилококков за колонизацию кожи.
Maciag JJ, Chantraine C, Mills KB, Yadav R, Yarawsky AE, Chaton CT, Vinod D, Fitzkee NC, Mathelié-Guinlet M, Dufrêne YF, Fey PD, Horswill AR, Herr AB. Масиаг Дж. Дж. и др. bioRxiv. 2023 27 января: 2023.01.26.525635. дои: 10.1101/2023.01.26.525635. Препринт. bioRxiv. 2023. PMID: 36747832 Бесплатная статья ЧВК.
Антибактериальная и антибиопленочная активность дисаспидина ВВ в отношении Staphylococcus epidermidis .

Лан С., Чен С., Инь С., Се С., Ван С., Дэн Р., Шэнь З. Лан С. и др. Фронт микробиол. 2023 19 января; 14:999449. doi: 10.3389/fmicb.2023.999449. Электронная коллекция 2023. Фронт микробиол. 2023. PMID: 36744091 Бесплатная статья ЧВК.
Конвергентное поведение расширенных областей стебля стафилококковых поверхностных белков с широко расходящимися образцами последовательностей.
Yarawsky AE, Ori AL, English LR, Whitten ST, Herr AB. Яравский А.Е. и соавт. bioRxiv. 2023 7 января: 2023.01.06.523059. дои: 10.1101/2023.01.06.523059. Препринт. bioRxiv. 2023. PMID: 36711672 Бесплатная статья ЧВК.
Структурные исследования растворов преамилоидных олигомерных состояний белка биопленки Аар.

