Сохраните у себя Поиск аналогов Описание активных компонентов препарата Линекс® (Linex®) Приведенная научная информация является обобщающей и не может быть использована для принятия решения о возможности применения конкретного лекарственного препарата. Дата обновления: 2020. Владелец регистрационного удостоверения:Произведено:LEK d.d. (Словения) Код ATX: A07FA51 (Микроорганизмы, продуцирующие молочную кислоту, в комбинации с другими препаратами) Лекарственная форма
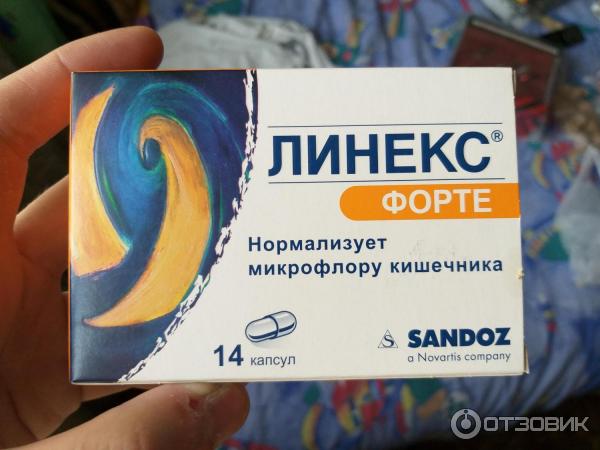
Форма выпуска, упаковка и состав препарата Линекс®Капсулы непрозрачные, с белым корпусом и крышечкой; содержимое — порошок белого цвета, без запаха. (в 1 г активного ингредиента Лебенин®, порошка содержится: Lactobacillus acidophilus (species L.gasseri) — 300 мг, Bifidobacterium infantis — 300 мг, Enterococcus faecium — 300 мг, лактоза — 50 мг, крахмал картофельный — 50 мг) Вспомогательные вещества: магния стеарат — 8.4 мг. Состав оболочки капсулы: метилгидроксибензоат — 0.19 мг, пропилгидроксибензоат — 0.08 мг, титана диоксид (Е171) — 0.98 мг, желатин — до 63 мг. 8 шт. — блистеры из мягкой алюминиевой/жесткой алюминиевой фольги (Al/Al) (2) — пачки картонные. Клинико-фармакологическая группа: Препарат, регулирующий равновесие кишечной микрофлоры (пробиотик) Фармако-терапевтическая группа: МИБП-эубиотик Сохраните у себя Если вы хотите разместить ссылку на описание этого препарата — используйте данный код Линекс®. |
инструкция по применению, доставка на дом
Характеристики
| Зарегистрировано как | |
| Количество в упаковке | 14 шт |
| Минимальный возраст от. | 0 лет |
| Минимальная допустимая температура хранения, °С | 5 °C |
| Максимальная допустимая температура хранения, °С | 25 °C |
| Срок годности | |
| Форма выпуска | Капсулы |
| Порядок отпуска | Без рецепта |
| Действующее вещество | Лактобактерии ацидофильные (Lactobacillus acidophilus) |
| Сфера применения | Гастроэнтерология |
Описание
Линекс® Форте помогает нормализовать микрофлору кишечника. Пробиотики полезны для здоровья взрослых и детей. Состав и состояние кишечной микрофлоры в самом раннем возрасте может повлиять на будущее здоровье человека в течение всей его жизни. Пробиотические продукты под маркой Линекс® помогают восстанавливать и поддерживать баланс кишечной микрофлоры у взрослых и детей.
Линекс® Форте помогает защищать и восстанавливать микрофлору кишечника, помогая предотвращать и облегчать диарею, вздутие живота и другие расстройства пищеварения.
Линекс® Форте содержит два типа живых молочнокислых бактерий, подверженных особой обработке (лиофилизации)1:
— лактобактерии Lactobacillus acidophilus (LA-5)*
— бифидобактерии Bifidobacterium animalis subsp. lactis (BB-12)*
Каждая капсула Линекс® Форте содержит не менее 2 миллиардов колониеобразующих единиц (KОЕ) 1 Линекс® Форте производится в форме капсул, состоящих из полисахаридной матрицы, которая защищает полезные бактерии от воздействия пищеварительных соков и доставляет их в кишечник2. Линекс® Форте не содержит лактозы, глютена, желатина.
Пробиотики полезны для здоровья взрослых и детей. Состав и состояние кишечной микрофлоры в самом раннем возрасте может повлиять на будущее здоровье человека в течение всей его жизни. Пробиотические продукты под маркой Линекс® помогают восстанавливать и поддерживать баланс кишечной микрофлоры у взрослых и детей.
Линекс® Форте помогает защищать и восстанавливать микрофлору кишечника, помогая предотвращать и облегчать диарею, вздутие живота и другие расстройства пищеварения.
Линекс® Форте содержит два типа живых молочнокислых бактерий, подверженных особой обработке (лиофилизации)1:
— лактобактерии Lactobacillus acidophilus (LA-5)*
— бифидобактерии Bifidobacterium animalis subsp. lactis (BB-12)*
Каждая капсула Линекс® Форте содержит не менее 2 миллиардов колониеобразующих единиц (KОЕ) 1 Линекс® Форте производится в форме капсул, состоящих из полисахаридной матрицы, которая защищает полезные бактерии от воздействия пищеварительных соков и доставляет их в кишечник2. Линекс® Форте не содержит лактозы, глютена, желатина.
Действующие вещества
Бифидобактерии + Лактобактерии
Форма выпуска
Капсулы
Состав
1 капсула содержит:
Активный ингредиент: порошок Пробио-тек АБ Бленд 64 (Probio-tec® АВ Blend 64) – 60,000 мг (порошок содержит: Lactobacillus acidophilus (CHR.
Фармакологический эффект
Фармакодинамика
Линекс® Форте нормализует микрофлору кишечника.
Одна капсула препарата Линекс® Форте содержит молочнокислые бактерии (Lactobacillus acidophilus (CHR. HANSEN LA-5®) и Bifidobacterium animalis subsp. lactis (CHR. HANSEN BB-12®)), каждая капсула содержит 2 x 109 колониеобразующих единиц живых лиофилизированных молочнокислых бактерий. Живые молочнокислые бактерии являются нормальной составляющей естественной микрофлоры кишечника.
Основные функции молочнокислых бактерий:
• защитная: синтез веществ с антибактериальной активностью,
• ферментопродуцирующая: гидролиз клетчатки, белков, жиров, крахмала, деконъюгация желчных кислот,
• синтетическая: синтез витаминов группы В, С, К, аминокислот, органических кислот и т.д.
Молочнокислые бактерии CHR. HANSEN LA-5® и CHR. HANSEN BB-12® ингибируют рост патогенных бактерий посредством:
• снижения pH в кишечнике (результат способности CHR. HANSEN LA-5® синтезировать молочную кислоту и CHR. HANSEN BB-12® синтезировать уксусную и янтарную кислоты в дополнение к молочной кислоте),
• выработки метаболитов, которые обладают токсическим действием в отношении патогенных бактерий (образование Н2О2),
• образования противомикробных веществ, бактериоцинов (CHR.
lactis (CHR. HANSEN BB-12®)), каждая капсула содержит 2 x 109 колониеобразующих единиц живых лиофилизированных молочнокислых бактерий. Живые молочнокислые бактерии являются нормальной составляющей естественной микрофлоры кишечника.
Основные функции молочнокислых бактерий:
• защитная: синтез веществ с антибактериальной активностью,
• ферментопродуцирующая: гидролиз клетчатки, белков, жиров, крахмала, деконъюгация желчных кислот,
• синтетическая: синтез витаминов группы В, С, К, аминокислот, органических кислот и т.д.
Молочнокислые бактерии CHR. HANSEN LA-5® и CHR. HANSEN BB-12® ингибируют рост патогенных бактерий посредством:
• снижения pH в кишечнике (результат способности CHR. HANSEN LA-5® синтезировать молочную кислоту и CHR. HANSEN BB-12® синтезировать уксусную и янтарную кислоты в дополнение к молочной кислоте),
• выработки метаболитов, которые обладают токсическим действием в отношении патогенных бактерий (образование Н2О2),
• образования противомикробных веществ, бактериоцинов (CHR.
Фармакокинетика
Молочнокислые бактерии, такие как CHR. HANSEN LA-5® и CHR. HANSEN BB-12®, действуют непосредственно в желудочно-кишечном тракте, при приеме внутрь препарат не подвергается системному всасыванию. Стандартные фармакокинетические исследования, таким образом, не применимы. Устойчивость CHR. HANSEN LA-5® и CHR. HANSEN BB-12® к воздействию желудочного сока и желчи позволяет штаммам в большом количестве выживать при прохождении через желудок и 12-перстную кишку. Оба штамма прикрепляются к слизистой кишечника. Подобно другим микроорганизмам, они постепенно выводятся из желудочно-кишечного тракта перистальтикой и дефекацией.
HANSEN LA-5® и CHR. HANSEN BB-12®, действуют непосредственно в желудочно-кишечном тракте, при приеме внутрь препарат не подвергается системному всасыванию. Стандартные фармакокинетические исследования, таким образом, не применимы. Устойчивость CHR. HANSEN LA-5® и CHR. HANSEN BB-12® к воздействию желудочного сока и желчи позволяет штаммам в большом количестве выживать при прохождении через желудок и 12-перстную кишку. Оба штамма прикрепляются к слизистой кишечника. Подобно другим микроорганизмам, они постепенно выводятся из желудочно-кишечного тракта перистальтикой и дефекацией.
Показания
• Лечение и профилактика дисбактериоза кишечника. Дисбактериоз кишечника проявляется следующими симптомами: диарея (понос), диспепсия (нарушение
пищеварения), запоры, метеоризм (вздутие живота), тошнота, отрыжка, рвота, боли в животе, возможны аллергические кожные реакции.
• Облегчение запоров у взрослых и детей старше 12 лет.
• Дополнение к стандартной эрадикационной терапии Helicobacter pylori у взрослых и детей старше 12 лет. • В комплексной терапии и для профилактики диареи, метеоризма и других нарушений пищеварения, вызванных:
— вирусными и бактериальными инфекциями желудочно-кишечного тракта (например, ротавирусные инфекции, диарея путешественника),
— терапией антибиотиками широкого спектра действия и другими противомикробными препаратами,
— лучевой терапией органов брюшной полости и малого таза.
• В комплексной терапии и для профилактики диареи, метеоризма и других нарушений пищеварения, вызванных:
— вирусными и бактериальными инфекциями желудочно-кишечного тракта (например, ротавирусные инфекции, диарея путешественника),
— терапией антибиотиками широкого спектра действия и другими противомикробными препаратами,
— лучевой терапией органов брюшной полости и малого таза.
Противопоказания
• гиперчувствительность к компонентам препарата, • наследственная непереносимость фруктозы, дефицит сахаразы, изомальтазы или глюкозо-галактозная мальабсорбция.
Меры предосторожности
С осторожностью при сахарном диабете (в состав входят простые сахара), недостаточность иммунной системы (например, ВИЧ-инфекция). Диарею у детей младше 6 лет необходимо лечить под наблюдением врача.
Применение при беременности и кормлении грудью
Сообщений о нежелательных явлениях при применении препарата Линекс® Форте во время беременности и в период грудного вскармливания не поступало. В случае возникновения острой диареи у женщин во время беременности и в период грудного вскармливания следует соблюдать меры предосторожности во избежание развития дефицита жидкости и электролитов в организме и других нежелательных явлений, независимо от приема препарата Линекс® Форте, потому что острая диарея может стать угрозой здоровью плода и беременной женщины. Лечение диареи у беременных и кормящих грудью женщин должно проводиться под наблюдением врача.
В случае возникновения острой диареи у женщин во время беременности и в период грудного вскармливания следует соблюдать меры предосторожности во избежание развития дефицита жидкости и электролитов в организме и других нежелательных явлений, независимо от приема препарата Линекс® Форте, потому что острая диарея может стать угрозой здоровью плода и беременной женщины. Лечение диареи у беременных и кормящих грудью женщин должно проводиться под наблюдением врача.
Способ применения и дозы
Капсулы Линекс® Форте предпочтительно принимать во время или после еды, запивая небольшим количеством жидкости.
Лечение и профилактика дисбактериоза, в комплексной терапии и для профилактики диареи, метеоризма и других нарушений пищеварения, вызванных вирусными и бактериальными инфекциями желудочно-кишечного тракта, терапией антибиотиками широкого спектра действия и другими противомикробными препаратами, лучевой терапией органов брюшной полости и малого таза:
Взрослые и подростки старше 12 лет: по 1 капсуле 1-3 раза в день (в зависимости от тяжести симптомов). Дети от 2 до 12 лет: по 1 капсуле 1-2 раза в день (в зависимости от тяжести симптомов).
Новорожденные и дети до 2-х лет: по 1 капсуле 1 раз в день.
Диарею у детей младше 6 лет необходимо лечить под наблюдением врача.
Прием препарата Линекс® Форте у детей в возрасте до 1 года не рекомендуется. Для данной возрастной группы рекомендуется выбирать более удобные для приема формы выпуска.
Длительность лечения зависит от причины развития дисбактериоза и индивидуальных особенностей организма.
Дополнение к стандартной эрадикационной терапии Helicobacter pylori и для облегчения запоров: взрослые и подростки старше 12 лет: по 1 капсуле 3 раза в день.
При назначении Линекс® Форте детям и пациентам, которые не могут проглотить целую капсулу, ее необходимо вскрыть, содержимое высыпать в ложку и смешать с небольшим количеством жидкости.
Препарат Линекс® Форте можно принимать до исчезновения симптомов.
Не следует превышать рекомендованные ежедневные дозы препарата.
Дети от 2 до 12 лет: по 1 капсуле 1-2 раза в день (в зависимости от тяжести симптомов).
Новорожденные и дети до 2-х лет: по 1 капсуле 1 раз в день.
Диарею у детей младше 6 лет необходимо лечить под наблюдением врача.
Прием препарата Линекс® Форте у детей в возрасте до 1 года не рекомендуется. Для данной возрастной группы рекомендуется выбирать более удобные для приема формы выпуска.
Длительность лечения зависит от причины развития дисбактериоза и индивидуальных особенностей организма.
Дополнение к стандартной эрадикационной терапии Helicobacter pylori и для облегчения запоров: взрослые и подростки старше 12 лет: по 1 капсуле 3 раза в день.
При назначении Линекс® Форте детям и пациентам, которые не могут проглотить целую капсулу, ее необходимо вскрыть, содержимое высыпать в ложку и смешать с небольшим количеством жидкости.
Препарат Линекс® Форте можно принимать до исчезновения симптомов.
Не следует превышать рекомендованные ежедневные дозы препарата.
Побочные действия
Препарат хорошо переносится. Сообщений о нежелательных эффектах нет, однако могут отмечаться реакции гиперчувствительности.
Сообщений о нежелательных эффектах нет, однако могут отмечаться реакции гиперчувствительности.
Передозировка
Данных о симптомах передозировки нет.
Взаимодействие с другими препаратами
Нежелательного взаимодействия с другими лекарственными средствами не отмечено. При одновременном применении с антибиотиками рекомендуется принимать препарат Линекс® Форте не ранее, чем через 3 часа после приема антибиотиков.
Особые указания
Не следует запивать Линекс® Форте горячими напитками и принимать одновременно с алкоголем.
Необходимо проконсультироваться с лечащим врачом перед приемом препарата, если у Вас:
температура тела выше 38°С,
следы крови или слизи в стуле,
диарея длится более двух дней и сопровождается острыми болями в животе, обезвоживанием и потерей веса,
хронические заболевания (например, сахарный диабет, сердечно-сосудистые заболевания) или иммуно-дефицитные состояния (например, ВИЧ-инфекция).
При лечении диареи необходимо возмещение потерянной жидкости и электролитов. При наличии запоров рекомендуется соблюдать сбалансированную диету, обеспечивающую поступление достаточного количества клетчатки и жидкости, соблюдать режим физической активности и стараться опорожнять кишечник в одно и то же время каждый день. Если запор длится более семи дней, необходимо проконсультироваться с врачом.
Прием препарата Линекс® Форте у детей в возрасте до 1 года не рекомендуется. Для данной возрастной группы рекомендуется выбирать более удобные для приема формы выпуска.
При наличии запоров рекомендуется соблюдать сбалансированную диету, обеспечивающую поступление достаточного количества клетчатки и жидкости, соблюдать режим физической активности и стараться опорожнять кишечник в одно и то же время каждый день. Если запор длится более семи дней, необходимо проконсультироваться с врачом.
Прием препарата Линекс® Форте у детей в возрасте до 1 года не рекомендуется. Для данной возрастной группы рекомендуется выбирать более удобные для приема формы выпуска.
Условия хранения
Хранить при температуре не выше 25°С. Хранить в недоступном для детей месте.
LINE-X Truck Bedliner Часто задаваемые вопросы | Старые блоги | LINE-X Truck Bedliner Часто задаваемые вопросы | Старые блоги | Line-X Мир! | LINE-X of Virginia Beach
Пожалуйста, ознакомьтесь с часто задаваемыми вопросами о чехлах для грузовых автомобилей Line-X. Если вы хотите записаться на прием, пожалуйста, используйте форму «Запросить цену» на этом сайте или позвоните нам по телефону 757-490-8848.
Что такое процесс LINE-X?
Сколько времени занимает этот процесс?
Есть ли гарантия на товар?
В чем разница между надрельсовым и подрельсовым?
Можете ли вы снять с моих заводских рельсовых заглушек и распылить «через рельс»?
Подойдут ли мои аксессуары?
Закупорит ли LINE-X сливные отверстия?
Исчезнет ли LINE-X со временем?
Можно ли удалить LINE-X?
Требуется ли какое-либо техническое обслуживание моего нового постельного белья LINE-X?
Почему спрей LINE-X для покрытия кузова грузовика, а не конкуренты?
Материал высокого давления лучше материала низкого давления?
Спрей LINE-X при нанесении горячий или холодный?
Выдерживает ли спрей LINE-X для покрытия кузова грузовика экстремальные температуры?
Каковы преимущества продукта для спрея LINE-X на материале постельного белья?
Можно ли использовать LINE-X в качестве грунтовки?
Какие другие области применения продукта LINE-X?
Является ли LINE-X экологически безопасным?
1.
 Начнем с очистки кузова грузовика от мусора. Все оборудование из вашего грузовика удалено, чтобы в будущем у вас был полный доступ к платформе грузовика.
Начнем с очистки кузова грузовика от мусора. Все оборудование из вашего грузовика удалено, чтобы в будущем у вас был полный доступ к платформе грузовика.Мы используем бумагу, малярную ленту и специальную малярную ленту с проволокой, чтобы создать четкие четкие линии на краях вашего грузовика.
3. После того, как ваш грузовик будет полностью защищен, кузов грузовика шлифуется, чтобы создать травленую поверхность, и протирается обезжиривающим средством, чтобы удалить все остатки с поверхности.
4. Затем с помощью эксклюзивной техники наносится LINE-X, обеспечивающий равномерную текстурированную отделку для великолепного внешнего вида и предотвращения скольжения.
5. После завершения процесса с грузовика снимается маска, а оборудование переустанавливается и затягивается в соответствии со спецификациями производителя.
6. Гарантийный ярлык LINE-X приклеен к кузову грузовика, а наклейка LINE-X прикреплена для гордости владельца.
7.
 Пожизненная гарантия LINE-X для вашего грузовика внесена в базу данных, и процесс завершен.
Пожизненная гарантия LINE-X для вашего грузовика внесена в базу данных, и процесс завершен.Весь процесс можно выполнить всего за один день.
Наш сертифицированный техник подготовит ваш грузовик и нанесет на него напыляемое покрытие кузова LINE-X, которое высыхает за 3–5 секунд. Как правило, на изготовление большинства обычных постельных принадлежностей уходит от 2 до 3 человеко-часов. Нанесение цветных лайнеров и LINE-X PREMIUM может занять дополнительный час.
На него распространяется гарантия на отслаивание, вздутие, отслаивание, вздутие или другие проблемы с качеством изготовления, и любой из обширной сети из 500 дилеров компании по всей стране может обработать запрос на ремонт.
Во-первых, разница между верхним и нижним рельсом принципиальна.
Над рельсом — это когда продукт LINE-X перемещается по рельсу на любую линию, указанную заказчиком. Под рельсом — когда изделие LINE-X останавливается под краем рельса.
Нет. Как только вы снимете заводские заглушки с рельсов, заглушки будут уничтожены. И то, что осталось, — это ряд дыр в рельсах, которые трудно починить или закрыть.
Да!
Крышки кроватей, чехлы для грузовых автомобилей, каркасы кемперов, ящики для инструментов, служебные ящики и крепежные приспособления идеально подходят друг другу, потому что изделия LINE-X повторяют все контуры вашего грузовика и обычно не мешают установке аксессуаров.
№
Благодаря быстрому высыханию продукта line-x ваши сливные отверстия не засорятся и не будут заполнены. Если у вас есть отверстия от аксессуаров или сцепных устройств, которые вы хотели бы скрыть, мы можем легко закрыть их и сделать практически невидимыми.
К сожалению, все обшивки кроватей выцветают с той же скоростью, что и шины и неокрашенная отделка кузова.
LINE-X может со временем потерять свой блеск, но обычно не становится меловым или серым. Если вы хотите сохранить глянцевый вид вашего нового постельного белья, мы рекомендуем вам обновить его, включив в него LINE-X Premium, наше УФ-покрытие, которое действует как солнцезащитный крем для вашего LINE-X.
LINE-X — это полиуретановое покрытие, которое навсегда приклеивается к вашему грузовику.
Удаление этого покрытия очень сложно и не рекомендуется.
Лучший способ сохранить внешний вид вашего постельного белья LINE-X — использовать мойку высокого давления.
Для удаления стойких загрязнений и копоти мы рекомендуем использовать безопасное чистящее средство, такое как Simple Green, или средство для чистки цитрусовых со щеткой для шин, чтобы очистить подкладку.
LINE-X — единственная компания, которая разрабатывает и контролирует производство собственного материала, что придает ему самую высокую прочность на растяжение в отрасли.
Материал рассчитан на укладку за 3-5 секунд, что гарантирует стабильное и равномерное распределение материала без наплывов и провисаний.
Кроме того, в LINE-X используется высокотемпературная система высокого давления, что позволяет получить прочную заводскую отделку. Это единственная крупная компания, занимающаяся напылением покрытий для грузовых автомобилей, которая предлагает общенациональную ограниченную пожизненную гарантию, действующую в более чем 500 франшизах LINE-X.
Не обязательно. Как и во всем, есть компромиссы.
Более мягкий материал низкого давления обеспечивает немного лучшее сцепление, а более твердый материал высокого давления гораздо более устойчив к физическим повреждениям. Эта разница особенно важна в жаркую погоду, когда температура поверхности черного постельного белья может достигать 160°F на солнце. При этих температурах материал низкого давления размягчается, теряя до 50% своей прочности.
Распылительное оборудование Line-X имеет нагреватели с электронным управлением, которые нагревают материал до заданной температуры, обычно 140F.
Снижает вязкость продукта, придавая подкладке тонкую текстурированную поверхность.
Обивка кузова грузовиков LINE-X рассчитана на использование при температурах от минусовых холодов на Аляске до 250F жары в Аризоне.
Если требуется более высокая температура (до 350F), LINE-X предлагает продукт коммерческого класса в качестве опции.
Прочность и прочность
Устойчивость к большинству распространенных химикатов
Контур точной формы кузова грузовика
Устойчивость к царапинам и вмятинам
Амортизирующие свойства, гасящие звук
Привлекательная заводская отделкаПовышает стоимость нового или подержанного грузовика при перепродаже
Нет, однако его можно применять в проектах по восстановлению вне кузова, когда автомобиль полностью раздет.

LINE-X можно наносить практически на любую надлежащим образом подготовленную поверхность, требующую прочного защитного покрытия.
Например, это приложение идеально подходит для джипов, фургонов, грузовых автомобилей, полуприцепов и т. д.
LINE-X не использует ЛОС или ХФУ.
Кроме того, LINE-X одобрен и сертифицирован для использования в системах приготовления пищи и питьевого водоснабжения.
Использование пробиотиков для коррекции дисбактериоза нормальной микробиоты после болезни или разрушительных событий: систематический обзор
1. Katan MB. Почему Европейское управление по безопасности пищевых продуктов было прав, когда отклоняло утверждения о пользе пробиотиков. Польза микробов 2012;3:85–9 [PubMed] [Google Scholar]
2. Донован С.М., Шнееман Б., Гибсон Г.Р. и соавт. Установление и оценка заявлений о полезности пробиотиков. Amer Soc Nutr Adv Nutri 2012;3:723–5 [бесплатная статья PMC] [PubMed] [Google Scholar]
3. Европейское управление по безопасности пищевых продуктов (EFSA). Руководство по научным требованиям к заявлениям о пользе для здоровья, связанным с кишечником и иммунной функцией. ЕФСА J
2011;9:1984 [Google Scholar]
Европейское управление по безопасности пищевых продуктов (EFSA). Руководство по научным требованиям к заявлениям о пользе для здоровья, связанным с кишечником и иммунной функцией. ЕФСА J
2011;9:1984 [Google Scholar]
4. Binnendijk KH, Rijkers GT. Что такое польза для здоровья? Оценка мнения EFSA о пользе для здоровья пробиотиков. Польза микробов 2013;4:223–30 [PubMed] [Google Scholar]
5. McFarland LV. Систематический обзор и метаанализ Saccharomyces boulardii у взрослых пациентов. Мир J Гастроэнтерол 2010;16:2202–22 [бесплатная статья PMC] [PubMed] [Google Scholar]
6. Buts JP, Stilmant C, Bernasconi P, et al. Характеристика альфа, альфа-трегалазы, высвобождаемой в просвете кишечника пробиотиком Saccharomyces boulardii . Scand J Гастроэнтерол 2008;43:1489–96 [PubMed] [Google Scholar]
7. McFarland LV. Антибиотикоассоциированная диарея: эпидемиология, тенденции и лечение. Будущая микробиология 2008;3:563–78 [PubMed] [Google Scholar]
8. Dethlefsen L, Huse S, Sogin ML, et al.
Проникающие эффекты антибиотика на микробиоту кишечника человека, выявленные с помощью глубокого секвенирования 16S рРНК. ПЛОС Биол
2008;6:e280. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Dethlefsen L, Huse S, Sogin ML, et al.
Проникающие эффекты антибиотика на микробиоту кишечника человека, выявленные с помощью глубокого секвенирования 16S рРНК. ПЛОС Биол
2008;6:e280. [Бесплатная статья PMC] [PubMed] [Google Scholar]
9. Макфарланд Л.В. Нормальная флора: разнообразие и функции. Microb Ecol Health Dis 2000;12:193–207 [Google Scholar]
10. Sanders ME. Влияние пробиотиков на колонизирующую микробиоту кишечника. J Clin Гастероэнтерол 2011;45:S115–19 [PubMed] [Google Scholar]
11. Янг В.Б., Шмидт Т.М. Антибиотикоассоциированная диарея, сопровождающаяся масштабными изменениями состава фекальной микробиоты. Джей Клин Микробиол 2004;42:1203–6 [бесплатная статья PMC] [PubMed] [Google Scholar]
12. Nylund L, Satokari R, Nikkilä J, et al. Микроматричный анализ выявляет выраженную аберрантность кишечной микробиоты у младенцев с экземой по сравнению со здоровыми детьми из группы риска атопического заболевания. БМС Микробиол 2013;13:12. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Prince T, McBain AJ, O’Neill CA. Lactobacillus reuteri защищает эпидермальные кератиноциты от гибели клеток, вызванной Staphylococcus aureus , путем конкурентного исключения. Appl Environ Microbiol
2012;78:5119–26 [Бесплатная статья PMC] [PubMed] [Google Scholar]
Prince T, McBain AJ, O’Neill CA. Lactobacillus reuteri защищает эпидермальные кератиноциты от гибели клеток, вызванной Staphylococcus aureus , путем конкурентного исключения. Appl Environ Microbiol
2012;78:5119–26 [Бесплатная статья PMC] [PubMed] [Google Scholar]
14. Vitali B, Cruciani F, Baldassarre ME, et al. Пищевые добавки с пробиотиками на поздних сроках беременности: влияние на вагинальную микробиоту и секрецию цитокинов. БМС Микробиол 2012;12:236. [Бесплатная статья PMC] [PubMed] [Google Scholar]
15. Nugent RP, Krohn MA, Hillier SL. Надежность диагностики бактериального вагиноза повышается с помощью стандартизированного метода интерпретации окраски по Граму. Джей Клин Микробиол 1991; 29: 297–301 [бесплатная статья PMC] [PubMed] [Google Scholar]
16. Ciprandi G, Vizzaccaro A, Cirillo I, et al. Bacillus clausii проявляет иммуномодулирующую активность у субъектов с аллергией: экспериментальное исследование. Евр Энн Аллергия Клин Иммунол 2005;37:129–34 [PubMed] [Google Scholar]
17. Marseglia GL, Tosca M, Cirillo I, et al.
Эффективность спор Bacillus clausii в профилактике рецидивирующих респираторных инфекций у детей: экспериментальное исследование. Ther Clin Risk Manag
2007; 3:13–17 [бесплатная статья PMC] [PubMed] [Google Scholar]
Marseglia GL, Tosca M, Cirillo I, et al.
Эффективность спор Bacillus clausii в профилактике рецидивирующих респираторных инфекций у детей: экспериментальное исследование. Ther Clin Risk Manag
2007; 3:13–17 [бесплатная статья PMC] [PubMed] [Google Scholar]
18. Iniesta M, Herrera D, Montero E, et al. Пробиотические эффекты перорально вводимых таблеток Lactobacillus reuteri-, содержащих таблетки, на поддесневую и слюнную микробиоту у пациентов с гингивитом. Рандомизированное клиническое исследование. Дж. Клин Пародонтолог 2012;39:736–44 [PubMed] [Google Scholar]
19. Shah MP, Gujjari SK, Chandrasekhar VS. Оценка влияния пробиотика (инерсана) в отдельности, комбинации пробиотика с доксициклином и только доксициклина на агрессивный пародонтит — клинико-микробиологическое исследование. J Clin Diagn Res 2013;7:595–600 [бесплатная статья PMC] [PubMed] [Google Scholar]
20. Teughels W, Durukan A, Ozcelik O, et al.
Клинические и микробиологические эффекты пробиотиков Lactobacillus reuteri при лечении хронического периодонтита: рандомизированное плацебо-контролируемое исследование. Дж. Клин Пародонтолог
2013;40:1025–35 [бесплатная статья PMC] [PubMed] [Google Scholar]
Дж. Клин Пародонтолог
2013;40:1025–35 [бесплатная статья PMC] [PubMed] [Google Scholar]
21. Kleessen B, Bezirtzoglou E, Matto J. Культуральные знания о биоразнообразии, развитии и стабильности микрофлоры желудочно-кишечного тракта человека. Micro Ecol Health Dis 2000; 12:53–63 [Google Scholar]
22. Шмайссер С., Стил Х., Штрейт В.Р. Метагеномика, биотехнология с некультивируемыми микробами. Appl Microbiol Биотехнология 2007;75:955–62 [PubMed] [Google Scholar]
23. Preidis GA, Versalovic J. Ориентация на микробиом человека с помощью антибиотиков, пробиотиков и пребиотиков: гастроэнтерология вступает в эру метагеномики. Гастроэнтерол 2009;136:2015–31 [бесплатная статья PMC] [PubMed] [Google Scholar]
24. Aagaard K, Petrosino J, Keitel W, et al. Стратегия проекта микробиома человека для всестороннего отбора проб микробиома человека и того, почему это важно. ФАСЭБ Ж 2013;27:1012–22 [бесплатная статья PMC] [PubMed] [Google Scholar]
25. Хандельсман Дж. Метагеномика: применение геномики к некультивируемым микроорганизмам. Микро Мол Биол Ред.
2004;68:669–85 [бесплатная статья PMC] [PubMed] [Google Scholar]
Метагеномика: применение геномики к некультивируемым микроорганизмам. Микро Мол Биол Ред.
2004;68:669–85 [бесплатная статья PMC] [PubMed] [Google Scholar]
26. Gill SR, Pop M, Deboy RT, et al. Метагеномный анализ микробиома дистального отдела кишечника человека. Наука 2006;312:1355–9 [бесплатная статья PMC] [PubMed] [Google Scholar]
27. Frank DN, Pace NR. Микробиология желудочно-кишечного тракта вступает в эру метагеномики. Карр Опин Гастроэнтерол 2008; 24:4–10 [PubMed] [Google Scholar]
28. Swidsinski A, Loening-Baucke V, Kirsch S, et al. Функциональная биоструктура кишечной микробиоты (центральная зона брожения, зона зародышевого запаса и отделяющий слой слизи) у здоровых людей и пациентов с диареей, получавших Saccharomyces boulardii ]. Гастроэнтерол Клин Биол 2010;34(Suppl 1):S79–92 [PubMed] [Google Scholar]
29. Sanders ME, Guarner F, Guerrant R, et al.
Обновленная информация об использовании и исследовании пробиотиков в области здоровья и болезней. кишки
2013; 62: 787–96 [Бесплатная статья PMC] [PubMed] [Google Scholar]
кишки
2013; 62: 787–96 [Бесплатная статья PMC] [PubMed] [Google Scholar]
30. Moher D, Liberati A, Tetzlaff J, et al. Предпочтительные элементы отчетности для систематических обзоров и метаанализов: заявление PRISMA. БМЖ 2009;339:332–6 [Google Scholar]
31. Franks AH, Harmsen HJ, Raangs GC, et al. Вариации бактериальных популяций в фекалиях человека, измеренные с помощью флуоресцентной гибридизации in situ с олигонуклеотидными зондами, нацеленными на 16S рРНК. Appl Environ Microbiol 1998; 64:3336–45 [бесплатная статья PMC] [PubMed] [Google Scholar]
32. Вада М., Нагата С., Сайто М. и др. Влияние энтерального введения Bifidobacterium breve на пациентов, проходящих химиотерапию по поводу злокачественных новообразований у детей. Поддержка лечения рака 2010;18:751–9 [PubMed] [Google Scholar]
33. Odamaki T, Xiao JZ, Iwabuchi N, et al.
Влияние приема Bifidobacterium longum BB536 на фекальную микробиоту у лиц с поллинозом японского кедра в сезон пыльцы. Джей Мед Микробиол
2007; 56 (Pt 10): 1301–8 [PubMed] [Google Scholar]
Джей Мед Микробиол
2007; 56 (Pt 10): 1301–8 [PubMed] [Google Scholar]
34. Секи Х., Шиохара М., Мацумура Т. и др. Профилактика антибиотикоассоциированной диареи у детей с помощью Clostridium butyricum MIYAIRI. Педиатр Интерн. 2003;45:86–90 [PubMed] [Google Scholar]
35. Mustafa RA, Santesso N, Brozek J, et al. Подход GRADE воспроизводим при оценке качества доказательств синтеза количественных доказательств. Дж. Клин Эпидемиол 2013;66:736–42 [PubMed] [Google Scholar]
36. McFarland LV. Метаанализ пробиотиков для профилактики антибиотикоассоциированной диареи и лечения Clostridium difficile болезнь. Am J Гастроэнтерол 2006;101:812–22 [PubMed] [Google Scholar]
37. McFarland LV, Goh S. Профилактика антибиотикоассоциированной диареи и инфекций Clostridium difficile у детей с помощью пробиотиков: метаанализ. мир J мета анал 2013;1:102–20 [Google Scholar]
38. Goldenberg JZ, Ma SS, Saxton JD, et al.
Пробиотики для профилактики Clostridium difficile -ассоциированной диареи у взрослых и детей. Системная версия базы данных Cochrane
2013;5:CD006095. [PubMed] [Google Scholar]
Системная версия базы данных Cochrane
2013;5:CD006095. [PubMed] [Google Scholar]
39. Shen J, Zuo Z, Mao A. Влияние пробиотиков на индукцию ремиссии и поддерживающую терапию язвенного колита, болезни Крона и поухита: метаанализ рандомизированных контролируемых исследований. Воспаление кишечника Dis 2014;20:21–35 [PubMed] [Google Scholar]
40. McFarland LV, Dublin S. Метаанализ пробиотиков для лечения синдрома раздраженного кишечника. Мир J Гастроэнтерол 2008;14:2650–61 [бесплатная статья PMC] [PubMed] [Google Scholar]
41. Макфарланд Л.В. Метаанализ пробиотиков для профилактики диареи путешественников. Travel Med Infect Dis 2007; 5:97–105 [PubMed] [Google Scholar]
42. Huang H, Song L, Zhao W. Эффекты пробиотиков для лечения бактериального вагиноза у взрослых женщин: метаанализ рандомизированных контролируемых исследований. Arch Gynecol Obstet 2014;289:1225–34 [PubMed] [Google Scholar]
43. McFarland LV, Elmer GW, McFarland M.
Мета-анализ пробиотиков для профилактики и лечения острой диареи у детей . Internl J Пробиотики Пребиотики
2006;1:63–76 [Google Scholar]
Internl J Пробиотики Пребиотики
2006;1:63–76 [Google Scholar]
44. Dinleyici EC, Eren M, Ozen M, et al. Эффективность и безопасность Saccharomyces boulardii при острой инфекционной диарее. Экспертное мнение Биол Тер 2012;12:395–410 [PubMed] [Google Scholar]
45. Szajewska H, Ruszczyński M, Kolaček S. Мета-анализ показывает ограниченные доказательства использования Lactobacillus acidophilus LB для лечения острого гастроэнтерита у детей. Акта Педиатр 2014;103:249–55 [PubMed] [Google Scholar]
46. Alvaro E, Andrieux C, Rochet V, et al. Состав и метаболизм кишечной микробиоты у потребителей и непотребителей йогурта. Бр Дж Нутр 2007;97:126–33 [PubMed] [Google Scholar]
47. Зубадалашвили Н.Г., Махвиладзе М.А., Диасамидзе М.Т. Сравнительное исследование Линекса и Лакто-Г в лечении взрослых больных дисбактериозом. Русский. Медицинские Новости Грузии 2009;170:38–42 [PubMed] [Google Scholar]
48. Klein SM, Elmer GW, McFarland LV, et al. Восстановление и устранение биотерапевтического агента, Saccharomyces boulardii у здоровых добровольцев. Фарм Рез
1993;10:1615–19 [PubMed] [Google Scholar]
Восстановление и устранение биотерапевтического агента, Saccharomyces boulardii у здоровых добровольцев. Фарм Рез
1993;10:1615–19 [PubMed] [Google Scholar]
49. Rochet V, Rigottier-Gois L, Ledaire A, et al. Выживание Bifidobacterium animalis DN-173 010 в фекальной микробиоте после введения в лиофилизированной форме или ферментированном продукте — рандомизированное исследование у здоровых взрослых. Дж Мол Микробиол Биотехнолог 2008;14:128–36 [PubMed] [Google Scholar]
50. Engelbrektson AL, Korzenik JR, Sanders ME, et al. Анализ влияния лечения на микробную экологию кишечника человека. FEMS Microbiol Ecol 2006;57:239–50 [PubMed] [Google Scholar]
51. Zoppi G, Cinquetti M, Benini A, et al. Модуляция кишечной экосистемы пробиотиками и лактулозой у детей на фоне лечения цефтриаксоном. Curr Ther Res 2001;62:418–35 [Google Scholar]
52. Orrrhage K, Brismar B, Nord CE.
Влияние добавок Bifidobacterium longum и Lactobacillus acidophilus на кишечную микробиоту при введении клиндамицина. Microb Ecol Health Dis
1994; 7:17–25 [Google Scholar]
Microb Ecol Health Dis
1994; 7:17–25 [Google Scholar]
53. Ларсен Н., Вогенсен Ф.К., Гёбель Р. и соавт. Преобладающие роды фекальной микробиоты у детей с атопическим дерматитом не изменяются при приеме пробиотических бактерий Lactobacillus acidophilus NCFM и Bifidobacterium animalis subsp. лактис Би-07. FEMS Microbiol Ecol 2011;75:482–96 [PubMed] [Google Scholar]
54. Lidbeck A, Edlund C, Gustafsson JA, et al. Влияние Lactobacillus acidophilus на нормальную микрофлору кишечника после введения двух противомикробных препаратов. Инфекционное заболевание 1988;16:329–36 [PubMed] [Google Scholar]
55. Black F, Einarsson K, Lidbeck A, et al. Влияние молочнокислых бактерий на микрофлору кишечника человека при лечении ампициллином. Scand J Infect Dis 1991;23:247–54 [PubMed] [Google Scholar]
56. Jernberg C, Sullivan A, Edlund C, et al.
Мониторинг антибиотикоиндуцированных изменений микрофлоры кишечника человека и выявление пробиотических штаммов с использованием полиморфизма длин терминальных рестрикционных фрагментов. Appl Environ Microbiol
2005; 71: 501–6 [бесплатная статья PMC] [PubMed] [Google Scholar]
Appl Environ Microbiol
2005; 71: 501–6 [бесплатная статья PMC] [PubMed] [Google Scholar]
57. Madden JA, Plummer SF, Tang J, et al. Влияние пробиотиков на предотвращение нарушения кишечной микрофлоры после антибактериальной терапии: двойное слепое плацебо-контролируемое пилотное исследование. Инт Иммунофармакол 2005;5:1091–7 [PubMed] [Google Scholar]
58. Plummer SF, Garaiova I, Sarvotham T, et al. Влияние пробиотиков на состав кишечной микробиоты после антибактериальной терапии. Антимикробные агенты Int J 2005;26:69–74 [PubMed] [Google Scholar]
59. ван дер Аа Л.Б., Хейманс Х.С., ван Алдерен В.М. и др. Влияние новой синбиотической смеси на атопический дерматит у младенцев: рандомизированное контролируемое исследование. Клин Эксперт Аллергия 2010;40:795–804 [PubMed] [Google Scholar]
60. Lata J, Novotný I, Príbramská V, et al.
Влияние пробиотиков на кишечную флору, уровень эндотоксина и шкалу Чайлд-Пью у пациентов с циррозом печени: результаты двойного слепого рандомизированного исследования. Eur J Гастроэнтерол Гепатол
2007;19:1111–13 [PubMed] [Google Scholar]
Eur J Гастроэнтерол Гепатол
2007;19:1111–13 [PubMed] [Google Scholar]
61. Петрицевич Л., Витт А. Роль Lactobacillus casei rhamnosus Lcr35 в восстановлении нормальной микрофлоры влагалища после антибиотикотерапии бактериального вагиноза. БЖОГ 2008;115:1369–74 [PubMed] [Google Scholar]
62. Nobaek S, Johansson ML, Molin G, et al. Изменение кишечной микрофлоры связано с уменьшением вздутия живота и болей у больных с синдромом раздраженного кишечника. Am J Гастроэнтерол 2000;95:1231–8 [PubMed] [Google Scholar]
63. Klarin B, Johansson ML, Molin G, et al. Адгезия пробиотической бактерии Lactobacillus plantarum 299v на слизистую оболочку кишечника у пациентов в критическом состоянии: рандомизированное открытое исследование. Критический уход 2005;9:R285–93 [бесплатная статья PMC] [PubMed] [Google Scholar]
64. Klarin B, Molin G, Jeppsson B, et al.
Использование пробиотика Lactobacillus plantarum 299 для уменьшения количества патогенных бактерий в ротоглотке интубированных пациентов: рандомизированное контролируемое открытое пилотное исследование. Критический уход
2008;12:R136. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Критический уход
2008;12:R136. [Бесплатная статья PMC] [PubMed] [Google Scholar]
65. Girard-Pipau F, Pompei A, Schneider S, et al. Кишечная микрофлора, короткоцепочечные и клеточные жирные кислоты, влияние пробиотика S. boulardii . Микроб Экология Здоровье Dis 2002;14:220–7 [Google Scholar]
66. Swidsinski A, Loening-Baucke V, Verstraelen H, et al. Биоструктура фекальной микробиоты у здоровых лиц и больных хронической идиопатической диареей. Гастроэнтерология 2008;135:568–79 [PubMed] [Google Scholar]
67. Reid G, Beuerman D, Heinemann C, et al. Доза пробиотика Lactobacillus необходима для восстановления и поддержания нормальной микрофлоры влагалища. ФЭМС Иммунол Мед Микробиол 2001; 32:37–41 [PubMed] [Google Scholar]
68. Reid G, Charbonneau D, Erb J, et al.
Пероральное использование Lactobacillus rhamnosus GR-1 и L. fermentum RC-14 значительно изменяет вагинальную флору: рандомизированное плацебо-контролируемое исследование с участием 64 здоровых женщин. ФЭМС Иммунол Мед Микробиол
2003;35:131–4 [PubMed] [Google Scholar]
ФЭМС Иммунол Мед Микробиол
2003;35:131–4 [PubMed] [Google Scholar]
69. Кирпич И.А., Соловьева Н.В., Лейхтер С.Н., и соавт. Пробиотики восстанавливают флору кишечника и улучшают ферменты печени при повреждении печени, вызванном алкоголем: пилотное исследование. Алкоголь 2008; 42: 675–82 [бесплатная статья PMC] [PubMed] [Google Scholar]
70. Hummelen R, Changalucha J, Butamanya NL, et al. Lactobacillus rhamnosus GR-1 и L. reuteri RC-14 для профилактики или лечения бактериального вагиноза у женщин с ВИЧ. Int J Gynaecol Obstet 2010;111:245–8 [PubMed] [Google Scholar]
71. Uchida K, Takahashi T, Inoue M, et al. Иммунонутриентные эффекты при терапии синбиотиками у детей с синдромом короткой кишки. Педиатр Сург Инт 2007;23:243–8 [PubMed] [Google Scholar]
72. Mastromarino P, Macchia S, Meggiorini L, et al.
Эффективность вагинальных таблеток, содержащих Lactobacillus, при лечении симптоматического бактериального вагиноза. Клин микробиол инфекция
2009 г. ;15:67–74 [PubMed] [Google Scholar]
;15:67–74 [PubMed] [Google Scholar]
73. Roessler A, Forssten SD, Glei M, et al. Влияние пробиотиков на фекальную микробиоту и генотоксическую активность фекальной воды у пациентов с атопическим дерматитом: рандомизированное плацебо-контролируемое исследование. Клин Нутр 2012;31:22–9 [PubMed] [Google Scholar]
74. Kajander K, Hatakka K, Poussa T, et al. Пробиотическая смесь облегчает симптомы у пациентов с синдромом раздраженного кишечника: контролируемое 6 месячное вмешательство. Алимент Фармакол Тер 2005; 22: 387–9.4 [PubMed] [Google Scholar]
75. Lyra A, Krogius-Kurikka L, Nikkilä J, et al. Влияние многовидовой пробиотической добавки на количество кишечных микробных филотипов, связанных с синдромом раздраженного кишечника. БМК Гастроэнтерол 2010;10:110. [Бесплатная статья PMC] [PubMed] [Google Scholar]
76. Wong VW, Tse CH, Lam TT, et al.
Молекулярная характеристика фекальной микробиоты у пациентов с неалкогольным стеатогепатитом — продольное исследование.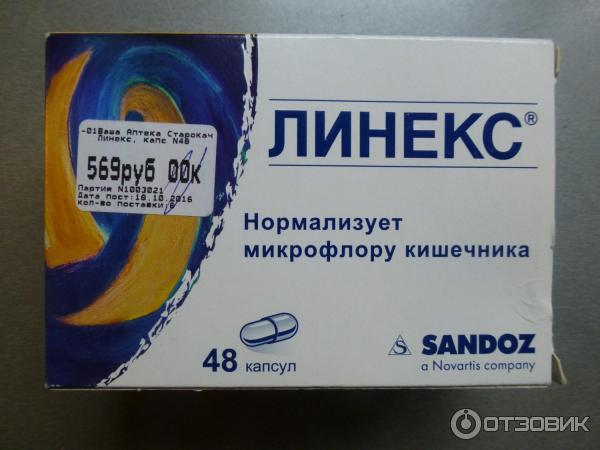 ПЛОС ОДИН
2013;8:e62885. [Бесплатная статья PMC] [PubMed] [Google Scholar]
ПЛОС ОДИН
2013;8:e62885. [Бесплатная статья PMC] [PubMed] [Google Scholar]
77. Вентури А., Джионкетти П., Риццелло Ф. и др. Влияние на состав фекальной флоры нового пробиотического препарата: предварительные данные по поддерживающей терапии больных язвенным колитом. Алимент Фармакол Тер 1999;13:1103–8 [PubMed] [Google Scholar]
78. Brigidi P, Vitali B, Swennen E, et al. Влияние введения пробиотиков на состав и ферментативную активность фекальной микробиоты человека у пациентов с синдромом раздраженного кишечника или функциональной диареей. Рез микробиол 2001; 152:735–41 [PubMed] [Google Scholar]
79. Kuhbacher T, Ott SJ, Helwig U, et al. Бактериальная и грибковая микробиота в связи с пробиотикотерапией (VSL#3) при поухите. кишки 2006;55:833–41 [бесплатная статья PMC] [PubMed] [Google Scholar]
80. Ng SC, Lam ERC, Lam TTY, et al. Влияние пробиотических бактерий на микробиоту кишечника при синдроме раздраженного кишечника. J Гастроэнтерол Гепатол 2013;28:1624–31 [PubMed] [Google Scholar]
81. Oswari H, Prayitno L, Dwipoerwantoro PG, et al.
Сравнение состава микробиоты стула, концентраций альфа-1-антитрипсина и кальпротектина в стуле и заболеваемости диареей у индонезийских младенцев, которых кормили грудным молоком или смесью с пробиотиками/пребиотиками. J Педиатр Детское здоровье
2013;49:1032–9 [PubMed] [Google Scholar]
Oswari H, Prayitno L, Dwipoerwantoro PG, et al.
Сравнение состава микробиоты стула, концентраций альфа-1-антитрипсина и кальпротектина в стуле и заболеваемости диареей у индонезийских младенцев, которых кормили грудным молоком или смесью с пробиотиками/пребиотиками. J Педиатр Детское здоровье
2013;49:1032–9 [PubMed] [Google Scholar]
82. Langhendries JP, Detry J, Van Hees J, et al. Влияние ферментированной детской смеси, содержащей жизнеспособные бифидобактерии, на состав фекальной флоры и рН здоровых доношенных детей. J Ped Гастроэнтерол Нутр 1995;21:177–81 [PubMed] [Google Scholar]
83. Benno Y, Mitsuoka T. Влияние Bifidobacterium longum на фекальную микрофлору человека. Микробиол Иммунол 1992;36:683–94 [PubMed] [Google Scholar]
84. Fujiwara S, Seto Y, Kimura A, et al.
Кишечный транзит перорально вводимого стрептомицин-рифампицин-резистентного варианта Bifidobacterium longum SBT2928: его долговременное выживание и влияние на кишечную микрофлору и метаболизм. J Appl микробиол
2001;90:43–52 [PubMed] [Google Scholar]
J Appl микробиол
2001;90:43–52 [PubMed] [Google Scholar]
85. Harmsen HJ, Raangs GC, Franks AH, et al. Влияние пребиотика инулина и пробиотика Bifidobacterium longum на фекальную микрофлору здоровых добровольцев, измеренное с помощью FISH и DGGE. Micro Ecol Health Dis 2002;14:211–19 [Google Scholar]
86. Guerin-Danan C, Chabanet C, Pedone C, et al. Молоко сквашенное йогуртовыми культурами и Lactobacillus casei по сравнению с йогуртом и желированным молоком: влияние на микрофлору кишечника у здоровых детей грудного возраста. Ам Джей Клин Нутри 1998;67:111–17 [PubMed] [Google Scholar]
87. Rochet V, Rigottier-Gois L, Sutren M, et al. Влияние перорально введенного Lactobacillus casei DN-114 001 на состав или активность доминирующей фекальной микробиоты у здоровых людей. Бр Дж Нутр 2006;95:421–9 [PubMed] [Google Scholar]
88. Rochet V, Rigottier-Gois L, Levenez F, et al.
Модуляция Lactobacillus casei в образцах подвздошной кишки и кала здоровых добровольцев после употребления ферментированного молока, содержащего Lactobacillus casei DN-114 001. Can J Microbiol
2008;54:660–7 [PubMed] [Google Scholar]
Can J Microbiol
2008;54:660–7 [PubMed] [Google Scholar]
89. Brunser O, Gotteland M, Cruchet S, et al. Влияние молочной смеси с пребиотиками на микробиоту кишечника детей раннего возраста после антибиотикотерапии. Педиатр Рез 2006;59:451–6 [PubMed] [Google Scholar]
90. Goossens D, Jonkers D, Russel M, et al. Эффект Lactobacillus plantarum 299v на бактериальный состав и метаболическую активность в фекалиях здоровых добровольцев: плацебо-контролируемое исследование начала и продолжительности эффектов. Алимент Фармакол Тер 2003;18:495–505 [PubMed] [Google Scholar]
91. Goossens D, Jonkers D, Russel M, et al. Выживаемость пробиотика L. plantarum 299v и его влияние на фекальную бактериальную флору с ингибированием желудочного сока и без него. Копать печень 2005; 37:44–50 [PubMed] [Google Scholar]
92. Goossens DA, Jonkers DM, Russel MG, et al.
Влияние пробиотического напитка с Lactobacillus plantarum 299v на бактериальный состав фекалий и биоптатов слизистой прямой и восходящей ободочной кишки. Алимент Фармакол Тер
2006;23:255–63 [PubMed] [Google Scholar]
Алимент Фармакол Тер
2006;23:255–63 [PubMed] [Google Scholar]
93. Berggren A, Soderberg L, Onning G, et al. Функция кишечника, микрофлора и потребление питательных веществ у детей после введения ферментированного овсяного продукта, содержащего Lactobacillus plantarum ДСМ 9843(299v). Microb Ecol Health Dis 2003;15:160–8 [Google Scholar]
94. Karlsson C, Ahrné S, Molin G, et al. Пробиотическая терапия мужчин с начальным атеросклерозом инициирует увеличение бактериального разнообразия в толстой кишке: рандомизированное контролируемое исследование. Атеросклероз 2010;208:228–33 [PubMed] [Google Scholar]
95. Gueimonde M, Sakata S, Kalliomäki M, et al. Влияние потребления матерями лактобактерий GG на перенос и формирование фекальной бифидобактериальной микробиоты у новорожденных. J Педиатр Гастроэнтерол Нутр 2006; 42:166–70 [PubMed] [Google Scholar]
96. Sierra S, Lara-Villoslada F, Sempere L, et al.
Кишечные и иммунологические эффекты ежедневного перорального введения Lactobacillus salivarius CECT5713 здоровым взрослым. Анаэроб
2010;16:195–200 [PubMed] [Google Scholar]
Анаэроб
2010;16:195–200 [PubMed] [Google Scholar]
97. Vanhoutte T, De Preter V, De Brandt E, et al. Молекулярный мониторинг фекальной микробиоты здоровых людей во время введения лактулозы и Saccharomyces boulardii . Appl Environ Microbiol 2006;72:5990–7 [бесплатная статья PMC] [PubMed] [Google Scholar]
98. Zhong Y, Huang CY, He T, et al. [Влияние пробиотиков и йогурта на микрофлору толстой кишки у лиц с непереносимостью лактозы]. Вэй Шэн Янь Цзю 2006;35:587–91 [PubMed] [Google Scholar]
99. He T, Priebe MG, Zhong Y, et al. Влияние добавок йогурта и бифидобактерий на микробиоту толстой кишки у субъектов с непереносимостью лактозы. J Appl микробиол 2008;104:595–604 [PubMed] [Google Scholar]
100. Yang YJ, Sheu BS. Йогурты, содержащие пробиотики, подавляют Helicobacter pylori нагружают и изменяют иммунный ответ и микробиоту кишечника у детей, инфицированных Helicobacter pylori . Хеликобактер 2012;17:297–304 [PubMed] [Google Scholar]
101. Mah KW, Chin VI, Wong WS, et al.
Влияние молочной смеси, содержащей пробиотики, на фекальную микробиоту азиатских младенцев, подверженных риску атопических заболеваний. Педиатр Рез
2007;62:674–9 [PubMed] [Google Scholar]
Mah KW, Chin VI, Wong WS, et al.
Влияние молочной смеси, содержащей пробиотики, на фекальную микробиоту азиатских младенцев, подверженных риску атопических заболеваний. Педиатр Рез
2007;62:674–9 [PubMed] [Google Scholar]
102. Rafter J, Bennett M, Caderni G, et al. Диетические синбиотики снижают факторы риска рака у пациентов с полипэктомией и раком толстой кишки. Am J Clin Nutr 2007; 85: 488–96 [PubMed] [Google Scholar]
103. Kubota A, He F, Kawase M, et al. Штаммы Lactobacillus стабилизируют микробиоту кишечника у больных поллинозом японского кедра. Микробиол Иммунол 2009; 53:198–205 [PubMed] [Google Scholar]
104. Morelli L, Zonenschain D, Callegari ML, et al. Оценка нового синбиотического препарата у здоровых добровольцев: выживаемость, персистенция пробиотических штаммов и его влияние на аборигенную флору. Нутр Дж 2003; 2:11. [Бесплатная статья PMC] [PubMed] [Google Scholar]
105. Салливан А., Норд К.Э., Эвенгард Б.
Влияние добавки с продуцирующими молочную кислоту бактериями на усталость и физическую активность у пациентов с синдромом хронической усталости. Нутр Дж
2009;8:1–6 [бесплатная статья PMC] [PubMed] [Google Scholar]
Нутр Дж
2009;8:1–6 [бесплатная статья PMC] [PubMed] [Google Scholar]
106. McNulty NP, Yatsunenko T, Hsiao A, et al. Влияние консорциума ферментированных молочных штаммов на микробиом кишечника гнотобиотических мышей и монозиготных близнецов. Sci Transl Med 2011;3:106ra106 [бесплатная статья PMC] [PubMed] [Google Scholar]
107. Guarner F, Khan AG, Garisch J, et al.; Всемирная гастроэнтерологическая организация. Глобальные рекомендации Всемирной гастроэнтерологической организации: пробиотики и пребиотики, октябрь 2011 г. J Clin Gastroenterol 2012;46:468–81 [PubMed] [Google Scholar]
108. Министерство здравоохранения и социальных служб США, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов, Центр безопасности пищевых продуктов и прикладного питания. Диетические добавки Руководящие документы и нормативная информация. 2008. http://www.fda/gov/food/guidanceregulation/guidancedocumentsregulatoryinformation/dietarysupplements/default.htm (по состоянию на 29май 2014 г.

 08.11
08.11
 Описание препарата в справочнике Видаль.
Описание препарата в справочнике Видаль.