Streptococcus pyogenes, ДНК [реал-тайм ПЦР]
Исследование для выявления возбудителя стрептококковой инфекции (Streptococcus pyogenes), в ходе которого с помощью метода полимеразной цепной реакции в реальном времени определяется генетический материал (ДНК) стрептококка в образце биоматериала.
Синонимы русские
Пиогенный стрептококк, бета-гемолитический стрептококк группы А, БГСА, β-гемолитический стрептококк группы А, β-ГСА [полимеразная цепная реакция в реальном времени, ПЦР в реальном времени].
Синонимы английские
S. pyogenes, Group A streptococcus, GAS, β-hemolytic streptococcus group A, β-hemolytic streptococcus group A.
Метод исследования
Полимеразная цепная реакция в режиме реального времени.
Какой биоматериал можно использовать для исследования?
Мазок из зева (ротоглотки), мазок из носоглотки, соскоб урогенитальный.
Общая информация об исследовании
S.
Традиционно для подтверждения диагноза «стрептококковая инфекция» применяют бактериологический посев биоматериала на специальные среды. В качестве биоматериала может выступать отделяемое миндалин или носоглотки (при подозрении на острый фарингит), мокрота (при пневмонии). Как правило, результат может быть получен лишь через несколько суток, что связано с промедлением в постановке точного диагноза и назначении специфического лечения. Однако выявлено, что своевременная диагностика и специфическое лечение не только уменьшают продолжительность болезни и интенсивность симптомов, но также снижают риск развития таких осложнений, как паратонзиллярный абсцесс, средний отит, острая ревматическая лихорадка и постстрептококковый гломерулонефрит (при остром фарингите), стрептококковый сепсис (при пневмонии), деструкция сустава и инвалидизация (при септическом артрите).
В реакции РТ-ПЦР применяются специфические праймеры к фрагменту ДНК S. pyogenes. Такая особенность позволяет выявлять только пиогенный стрептококк, а не родственные ему другие стрептококки – представители нормальной микрофлоры зева (Streptococcus mutans, Streptococcus viridians). По специфичности РТ-ПЦР не уступает бактериологическому посеву и значительно превосходит другие методы идентификации возбудителя (например, экспресс-тест для определения антигена).
Достаточно часто биоматериал на исследование берется уже на фоне лечения заболевания. В результате чувствительность методов диагностики снижается и вероятность получить ложноотрицательный результат выше. В такой ситуации метод РТ-ПЦР обладает некоторым преимуществом перед другими видами диагностики. Это объясняется тем, что для идентификации возбудителя в реакции используется генетический материал возбудителя – как геномная ДНК живого микроорганизма, так и фрагменты ДНК бактерии, подвергшейся лизису. При этом становится возможным выявление не только живых, активно размножающихся микроорганизмов, но и убитых в результате лечения бактерий. В отличие от РТ-ПЦР, обязательным условием для осуществления других методов диагностики (иммуноферментного анализа или бактериологического посева) является наличие живых микроорганизмов. Поэтому, если биоматериал сдается уже на фоне лечения, метод РТ-ПЦР следует предпочесть другим методам диагностики.
Высокая чувствительность РТ-ПЦР позволяет использовать этот метод при диагностике осложнений острого фарингита: острой ревматической лихорадки и постстрептококкового гломерулонефрита.
Выявление S. pyogenes в так называемых стерильных средах – это всегда патологический признак. С другой стороны, обнаружение этого микроорганизма в нестерильных средах (мокрота, отделяемое носоглотки) не всегда указывает на наличие заболевания. Выявлено, что около 12-20 % детей школьного возраста и 2,4-3,7 % взрослых людей являются бессимптомными носителями S. pyogenes. В таких случаях трактовку положительного результата исследования следует расценивать с учетом бактериальной нагрузки и в сочетании с некоторыми другими клиническими и лабораторными признаками. Как правило, бессимптомное носительство характеризуется меньшим количеством бактерий по сравнению с активной инфекцией. Поэтому обнаружение высокой бактериальной нагрузки S. pyogenes в мазке из зева у пациента с лихорадкой, болью в горле и болезненным регионарным лимфаденитом подтверждает диагноз «острый стрептококковый фарингит». И, наоборот, обнаружение низкой бактериальной нагрузки этого микроорганизма в мазке из зева при отсутствии жалоб и клинической картины следует расценить как бессимптомное носительство. РТ-ПЦР – это полуколичественный метод, позволяющий косвенно оценить бактериальную нагрузку. Поэтому он оказывается особенно полезным при обследовании «здоровых носителей» стрептококка.
Выявлено, что около 12-20 % детей школьного возраста и 2,4-3,7 % взрослых людей являются бессимптомными носителями S. pyogenes. В таких случаях трактовку положительного результата исследования следует расценивать с учетом бактериальной нагрузки и в сочетании с некоторыми другими клиническими и лабораторными признаками. Как правило, бессимптомное носительство характеризуется меньшим количеством бактерий по сравнению с активной инфекцией. Поэтому обнаружение высокой бактериальной нагрузки S. pyogenes в мазке из зева у пациента с лихорадкой, болью в горле и болезненным регионарным лимфаденитом подтверждает диагноз «острый стрептококковый фарингит». И, наоборот, обнаружение низкой бактериальной нагрузки этого микроорганизма в мазке из зева при отсутствии жалоб и клинической картины следует расценить как бессимптомное носительство. РТ-ПЦР – это полуколичественный метод, позволяющий косвенно оценить бактериальную нагрузку. Поэтому он оказывается особенно полезным при обследовании «здоровых носителей» стрептококка.
Для чего используется исследование?
Для диагностики:
- острого фарингита;
- острой ревматической лихорадки и постстрептококкового фарингита у пациентов с указанием на перенесенный эпизод острого фарингита в анамнезе или без него;
- бессимптомного носительства S. pyogenes у пациента с частыми рецидивами фарингита;
- бессимптомного носительства S. pyogenes у членов семьи пациента с частыми рецидивами стрептококкового фарингита;
- внебольничной пневмонии;
- септического артрита.
Когда назначается исследование?
- При симптомах острого фарингита: боль при глотании, отек и эритема слизистой зева, гнойное отделяемое с поверхности миндалин, болезненный регионарный лимфаденит;
- при симптомах острой ревматической лихорадки: мигрирующий полиартрит или артралгия, чувство перебоев в работе сердца, боль в области сердца, немотивированная слабость, кольцевидная эритема и подкожные узелки, а также неврологическая симптоматика в виде хореического гиперкинеза;
- при симптомах постстрептококкового гломерулонефрита: отек (периорбитальной области или генерализованный), макрогематурия, немотивированная слабость, протеинурия менее 3,5 г/сут.
 , артериальная гипертензия;
, артериальная гипертензия; - при обследовании пациента с рецидивирующим фарингитом;
- при обследовании членов семьи пациента с рецидивирующим фарингитом;
- при обследовании членов семьи пациента с частыми рецидивами острого стрептококкового фарингита;
- при наличии такого фактора риска S. pyogenes (ассоциированной пневмонии), как вирус гриппа h2N1;
- при симптомах внебольничной пневмонии: внезапное начало болезни, лихорадка, одышка, боль в грудной клетке, кашель с отхождением гнойной мокроты;
- при наличии факторов риска септического артрита: младенческий и старческий возраст, иммуносупрессивная терапия, соматические заболевания, гемодиализ;
- при симптомах септического артрита: боли в суставе в покое и при движении, эритема кожных покровов над областью сустава, нарушение подвижности в суставе, повышение температуры тела и немотивированная слабость.
Что означают результаты?
Референсные значения: отрицательно.
Причины положительного результата
В отделяемом носоглотки и миндалин:
- острый фарингит;
- острая ревматическая лихорадка;
- постстрептококковый гломерулонефрит.
В мокроте:
- пневмония;
- острый бронхит, бронхит курильщика.
Что может влиять на результат?
- Применение антибактериальных препаратов пенициллинового ряда (амоксиклав, ампициллин), цефалоспоринов (цефиксим, цефтибутен) и макролидов (азитромицин, кларитромицин) до взятия материала на анализ может привести к получению отрицательного результата.
Важные замечания
- Около 12-20 % детей школьного возраста и 2,4-3,7 % взрослых людей являются бессимптомными носителями S. pyogenes.
- Результат исследования следует оценивать вместе с некоторыми другими лабораторными анализами.
Также рекомендуется
- Общий анализ крови (без лейкоцитарной формулы и СОЭ)
- Общий анализ мокроты
- Антистрептолизин О
- С-реактивный белок, количественно (высокочувствительный метод)
- Streptococcus pneumoniae, ДНК [реал-тайм ПЦР]
Кто назначает исследование?
Врач общей практики, ЛОР, инфекционист, пульмонолог, эпидемиолог, травматолог.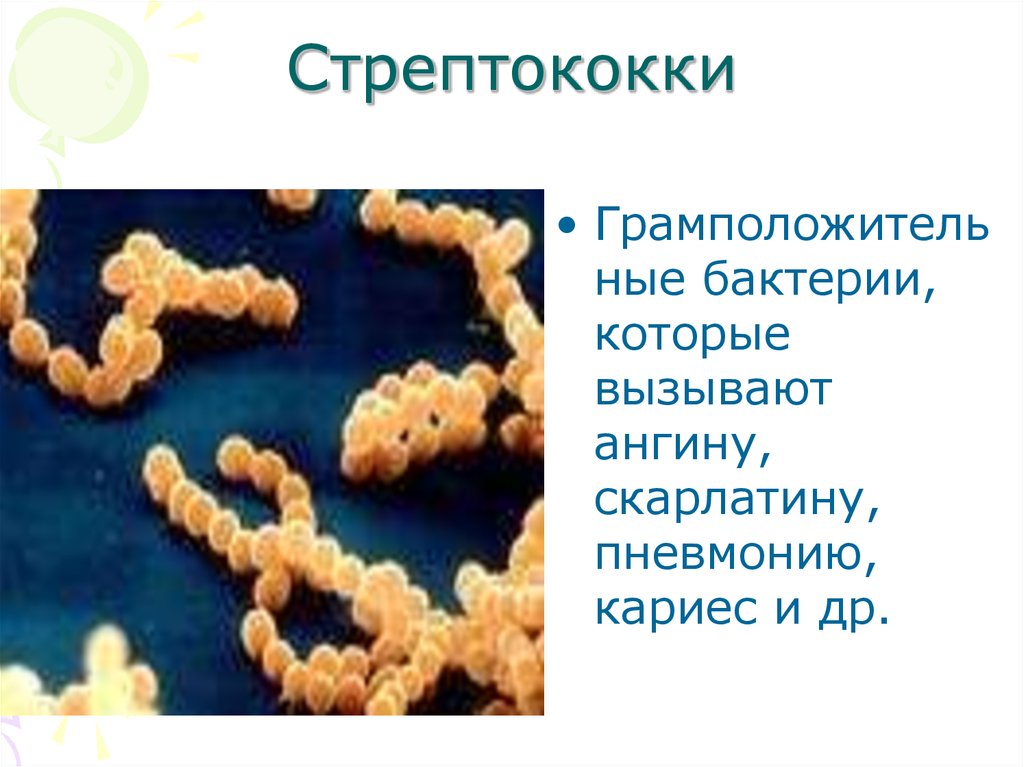
Литература
- Lee JH, Uhl JR, Cockerill FR 3rd, Weaver AL, Orvidas LJ. Real-time PCR vs standard culture detection of group A beta-hemolytic streptococci at various anatomic sites in tonsillectomy patients. Arch Otolaryngol Head Neck Surg. 2008 Nov;134(11):1177-81.
- Uhl JR et al. Comparison of LightCycler PCR, rapid antigen immunoassay, and culture for detection of group Astreptococci from throat swabs. J Clin Microbiol. 2003 Jan;41(1):242-9.
- Chiappini E, Regoli M, Bonsignori F, Sollai S, Parretti A, Galli L, de Martino M. Analysis of different recommendations from international guidelines for the management of acute pharyngitis in adults and children. Clin Ther. 2011 Jan;33(1):48-58.
- Hill HR. Group A streptococcal carrier versus acute infection: the continuing dilemma. Clin Infect Dis. 2010 Feb 15;50(4):491-2.
- García-Arias M, Balsa A, Mola EM. Best Pract Res Clin Rheumatol. Septic arthritis. 2011 Jun;25(3):407-21.
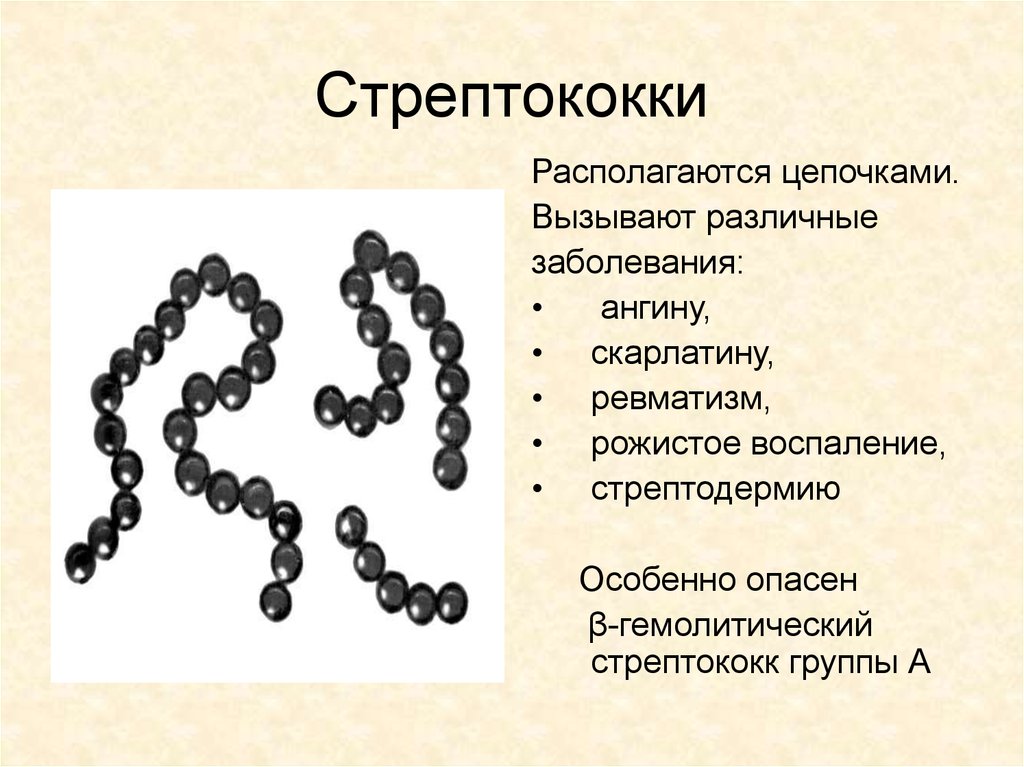
Поделиться Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей. Автор: Трубачева Е.С., врач – клинический фармаколог Микробиологические аспекты S.pyogenes является грамположительным кокком, собранным в цепочки. 100% штаммов чувствительны к пенициллинам, при этом Резистентность к макролидам в Европе – от 2 до 32%, в США – 7%. У нас в связи с великой любовью к этой группе, особенно среди педиатров, скорее всего, как в Европе. То есть о макролидах в этой ситуации надо забыть, к тому же тем же азитромицином не получится создать необходимую экспозицию в связи с ограничениями по срокам применения. Клинические аспекты При всем вышеперечисленном БГСА – зверь страшный, и основная проблема в том, что страх к нему мы почти потеряли. Лирическое отступление on. Именно этот зверь был постоянной причиной хирургических инфекций и родильной горячки (послеродового сепсиса) в доантибиотиковую эру. А женщины, как вы помните, умирали от нее, как мухи, пока Земмельвейс не заставил врачей мыть руки (за что закончил в психушке), но они их хотя бы на руках таскать перестали. Потому напомним, что S.pyogenes может вызывать следующие заболевания:
Практические вопросы диагностики: Микробиологическая диагностика S. Но самым быстрым тестом для точной диагностики на месте является стрептатест, который в течение пяти минут дает ответ о вероятности наличия БГСА у больного с острым фарингитом. Аспекты медикаментозного лечения
Говоря «аминопенициллины», мы имеем в виду амоксициллин и его защищенные формы. Ампициллин в таблетках не в состоянии создать достаточной подавляющей концентрации, так как его биодоступность в районе 40%, и дозировать придется на шесть приемов достаточно приличную горсть таблеток, которую никто не даст назначить, и уж тем более не станет пить. В отличие от 2-3 приемов в день амоксициллина. Если ангина произошла впервые в жизни – лечим 10 дней. Если имеем дело с постоянными рецидивами – 14 дней, так как зверь может уйти во внутриклеточное состояние, оттуда руля процессом, и, чтобы до него добраться, доза должна быть выше средней, а курс лечения соответствующим. Когда БГСА может уйти внутрь клетки? На тех самых пресловутых 5-7 днях, когда налеты с миндалин только сошли, температура только-только нормализовалась, а антибиотик взяли и отменили. И хорошо, если после подобного произойдет только рецидивирование фарингита, а не начнутся такие осложнения, как ревматизм, гломерулонефриты и далее по списку.
При непереносимости пенициллинов помним о клиндамицине как об их адекватной замене.
Альтернативой в режиме монотерапии могут служить:
Почему максимально важно соблюдать как дозировку, так и кратность введения читаем тут – /vracham/antibiotikoterapiya/polozheniya (часть 1 и часть 2). В заключение хочется снова воскликнуть – пожалуйста, помните о пиогенном стрептококке и о правильной длительности его лечения. ← Предыдущая статья Следующая статья → Поделиться Вас может заинтересовать
|
Streptococcus Pyogenes — StatPearls — NCBI Bookshelf
Программа непрерывного образования
Streptococcus pyogenes — это основной специфический для человека бактериальный патоген, вызывающий широкий спектр проявлений, начиная от легких локализованных инфекций и заканчивая опасными для жизни инвазивными инфекциями. Неэффективное лечение инфекций, вызванных S. pyogenes, может привести к постинфекционным последствиям острой ревматической лихорадки и постстрептококкового гломерулонефрита. Кроме того, он вызывает инвазивные инфекции, такие как некротизирующий фасциит и синдром токсического шока, что связано с высокой заболеваемостью и смертностью. В этом мероприятии описывается бактерия Streptococcus pyogenes (S. pyogenes), а также рассматриваются эпидемиология, клинические проявления инфекций, вызванных S. pyogenes, оценка и лечение клинических инфекций, вызванных S. pyogenes.
Неэффективное лечение инфекций, вызванных S. pyogenes, может привести к постинфекционным последствиям острой ревматической лихорадки и постстрептококкового гломерулонефрита. Кроме того, он вызывает инвазивные инфекции, такие как некротизирующий фасциит и синдром токсического шока, что связано с высокой заболеваемостью и смертностью. В этом мероприятии описывается бактерия Streptococcus pyogenes (S. pyogenes), а также рассматриваются эпидемиология, клинические проявления инфекций, вызванных S. pyogenes, оценка и лечение клинических инфекций, вызванных S. pyogenes.
Цели:
Определите этиологию S. pyogenes.
Опишите соответствующий анамнез, медицинский осмотр и оценку стрептококкового фарингита.
Ознакомьтесь с вариантами лечения стрептококкового фарингита.
Опишите стратегии межпрофессиональной бригады по улучшению координации помощи и коммуникации для улучшения исходов тяжелых инвазивных инфекций, вызванных S.
 pyogenes.
pyogenes.
Получите доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Streptococcus pyogenes является основным специфическим для человека бактериальным патогеном, вызывающим широкий спектр проявлений, начиная от легких локализованных инфекций и заканчивая опасными для жизни инвазивными инфекциями.[1] Неэффективное лечение инфекции S. pyogenes может привести к постинфекционным последствиям острой ревматической лихорадки и постстрептококковому гломерулонефриту. Кроме того, он вызывает инвазивные инфекции, такие как некротизирующий фасциит и синдром токсического шока, что связано с высокой заболеваемостью и смертностью.
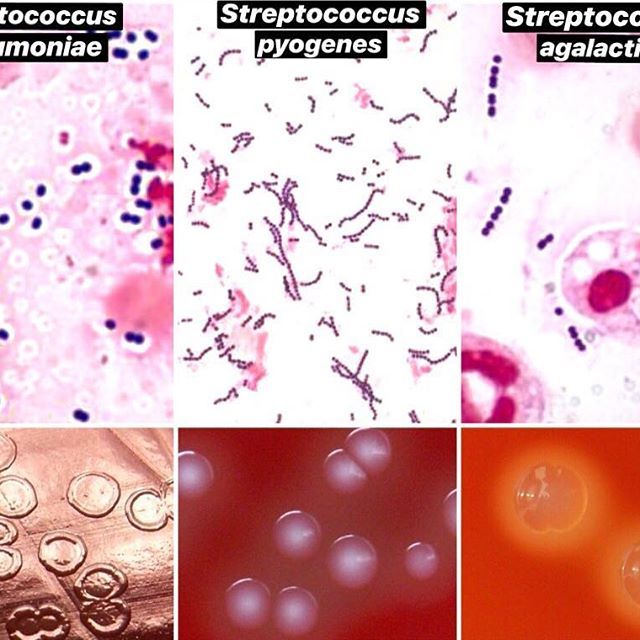
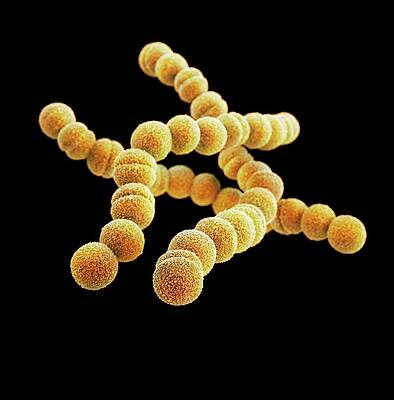
Стрептококки представляют собой грамположительные, каталазоотрицательные и коагулазоотрицательные кокки, которые встречаются парами или цепочками. По типу гемолиза на кровяном агаре их делят на три группы: бета-гемолитические (полный лизис эритроцитов), гемолитические (зеленый гемолиз) и гамма-гемолитические (отсутствие гемолиза). Бета-гемолитические стрептококки характеризуются как стрептококки группы А ( Streptococcus pyogenes ) и стрептококки группы В ( Streptococcus agalactiae ).
Бета-гемолитические стрептококки характеризуются как стрептококки группы А ( Streptococcus pyogenes ) и стрептококки группы В ( Streptococcus agalactiae ).
Этиология
S. pyogenes – грамположительный, каталазоотрицательный, оксидазоотрицательный, β-гемолитический стрептококк. Это факультативный анаэроб, который лучше всего растет при содержании углекислого газа от 5 до 10% и образует точечные колонии на чашках с кровяным агаром. Система серологической группировки Лансфилда используется для дифференциации стрептококков группы А (GAS) от других стрептококков. Антиген типа А S. pyogenes представляет собой полисахарид, состоящий из N-ацетилглюкозамина, присоединенного к основной цепи полимера рамнозы.[2] Белок М является основным поверхностным белком, присутствующим на S. pyogenes клеточная стенка и штаммы GAS дополнительно подразделяются на разные серотипы на основе антигенных характеристик белка М. На основе белка М было идентифицировано более 80 различных серотипов [2]. В зависимости от постинфекционных последствий S. pyogenes подразделяются на два класса: класс I и класс II. Штаммы класса I вызывают ревматическую лихорадку, а штаммы класса II вызывают острый гломерулонефрит.[3]
В зависимости от постинфекционных последствий S. pyogenes подразделяются на два класса: класс I и класс II. Штаммы класса I вызывают ревматическую лихорадку, а штаммы класса II вызывают острый гломерулонефрит.[3]
S. pyogenes обычно колонизирует глотку, задний проход и слизистую оболочку половых органов. Инфекции, вызванные S. pyogenes очень заразны. Передача может происходить воздушно-капельным путем, при контакте рук с выделениями из носа или с предметами или поверхностями, зараженными бактериями, при контакте кожи с зараженными поражениями или зараженными источниками пищи. Штаммы GAS могут попадать на кожу через ссадины и кожные повреждения, что может привести к рожистому воспалению или целлюлиту.[2] GAS может вызывать инфекцию мышц и фасций, что приводит к миозиту и некротизирующему фасциту, обычно после легкой травмы, и может привести к синдрому токсического шока. S. pyogenes может вызывать инфекцию слизистой оболочки влагалища и матки, вызывая септицемию. [2] Поражения кожи были идентифицированы как наиболее распространенный предрасполагающий фактор для тяжелых инфекций S. pyogenes .[4] Многолюдные места, такие как военные лагеря, дома престарелых и школы, вызывают легкую передачу организма и приводят к эпидемиям стрептококковой инфекции группы А.
[2] Поражения кожи были идентифицированы как наиболее распространенный предрасполагающий фактор для тяжелых инфекций S. pyogenes .[4] Многолюдные места, такие как военные лагеря, дома престарелых и школы, вызывают легкую передачу организма и приводят к эпидемиям стрептококковой инфекции группы А.
Эпидемиология
Частота инфекций, вызванных S. pyogenes , различается в разных частях мира в зависимости от клинических проявлений инфекций. СГС всегда ассоциировался с серьезными заболеваниями, приводящими к высокой заболеваемости и смертности. Инфекции GAS снизились к середине 20 века. Однако к концу 1980 возобновились тяжелые инфекции, вызванные стрептококком группы А (GAS).[5] За последние два десятилетия увеличилось количество негнойных и гнойных осложнений инфекции S. pyogenes . Это увеличение бремени болезни может быть связано с множеством факторов, включая изменение вирулентности и устойчивости к антибиотикам. Инфекции GAS и их осложнения различаются между слаборазвитыми и хорошо развитыми странами. В слаборазвитых странах высоки распространенность ревматической болезни сердца (РБС) и частота летальных исходов, связанных с РБС. И наоборот, в хорошо развитых странах высока частота летальных исходов из-за инвазивной ГАС-инфекции.
В слаборазвитых странах высоки распространенность ревматической болезни сердца (РБС) и частота летальных исходов, связанных с РБС. И наоборот, в хорошо развитых странах высока частота летальных исходов из-за инвазивной ГАС-инфекции.
Глобальное бремя тяжелых инфекций, вызванных S. pyogenes , составляет 18,1 миллиона случаев, при этом ежегодно регистрируется 1,78 миллиона новых случаев. Распространенность РБС во всем мире составляет не менее 15,6 млн случаев, при этом ежегодно регистрируется 282 000 новых случаев. Приблизительно 233 000 смертей в год связаны с RHD. Каждый год регистрируется примерно 663 000 новых случаев инвазивного СГБ, из них 163 000 летальных исходов в год.[8] 616 миллионов случаев инфекции ангины во всем мире в год можно отнести к S. pyogenes ; также 111 миллионов случаев кожной инфекции у детей из развивающихся стран. [1]. В Соединенных Штатах от 15% до 30% случаев фарингита у детей и от 5% до 20% случаев фарингита в год у взрослых вызваны S. pyogenes. Более того, наблюдается всплеск случаев ОРЛ у детей из семей среднего класса в США.[9]
pyogenes. Более того, наблюдается всплеск случаев ОРЛ у детей из семей среднего класса в США.[9]
Инфекция горла чаще встречается в районах с умеренным климатом, и заболеваемость увеличивается в конце зимы и ранней весной. Импетиго чаще встречается у детей, проживающих во влажном климате. Также было замечено, что тяжесть инвазивных кожных инфекций, вызванных GAS, возрастала с января по апрель и коррелирует с восприимчивостью хозяина к заражению серьезной инфекцией.
Токсикокинетика
За клинические проявления S. pyogenes ответственны многочисленные факторы вирулентности. Бактериальная капсула, состоящая из гиалуроновой кислоты, обеспечивает защиту от фагоцитоза. Белок М, липотейхоевая кислота и белок F отвечают за прикрепление бактерий к клеткам-хозяевам. Белок М также отвечает за ингибирование опсонизации путем связывания с регуляторами комплемента и фибриногеном. Белок M является наиболее важным фактором вирулентности для S. pyogenes , поскольку эксперименты показали, что мутанты М не могут выжить в человеческой крови, содержащей фагоциты. [11] S. pyogenes также продуцирует экзотоксины, такие как пирогенный (эритрогенный) токсин, который вызывает сыпь при скарлатине и синдром токсического шока. Другие вирулентные факторы включают стрептокиназу, стрептодорназу, гиалуронидазу и стрептолизины, которые способствуют проникновению в ткани.
[11] S. pyogenes также продуцирует экзотоксины, такие как пирогенный (эритрогенный) токсин, который вызывает сыпь при скарлатине и синдром токсического шока. Другие вирулентные факторы включают стрептокиназу, стрептодорназу, гиалуронидазу и стрептолизины, которые способствуют проникновению в ткани.
Анамнез и физикальное исследование
Анамнез и физикальные данные будут различаться в зависимости от типа приобретенной инфекции; тем не менее, для постановки точного клинического диагноза 9 требуется точный анамнез и надлежащая клиническая оценка.0033 Инфекция S. pyogenes .
Боль в горле обычно является серьезной жалобой при стрептококковом фарингите. Наиболее распространенные клинические признаки стрептококкового фарингита включают внезапное начало лихорадки, недомогание, фарингеальный экссудат, болезненную шейную лимфаденопатию и увеличение миндалин.[12]
У детей импетиго является одной из наиболее распространенных кожных инфекций. S. pyogenes вызывают небуллезное импетиго. Обычно вокруг рта или носа появляется зудящая красноватая сыпь, которая позже превращается в заполненный жидкостью пузырь. Волдыри легко лопаются и покрываются коркой медового цвета. Высыпания обычно хорошо локализованы и поражают открытые участки тела: лицо и нижние конечности. Системных проявлений импетиго обычно не бывает.
Обычно вокруг рта или носа появляется зудящая красноватая сыпь, которая позже превращается в заполненный жидкостью пузырь. Волдыри легко лопаются и покрываются коркой медового цвета. Высыпания обычно хорошо локализованы и поражают открытые участки тела: лицо и нижние конечности. Системных проявлений импетиго обычно не бывает.
У больного скарлатиной обычно отмечаются лихорадка высокой степени, боль в горле, клубничный язык и бледная, папулезная несливающаяся сыпь. Сыпь обычно длится от 7 до 10 недель, после чего следует шелушение. Шелушение можно наблюдать только на ладонях и подошвах.[13]
Инвазивные инфекции мягких тканей, вызванные S. pyogenes , в основном проявляются шоком и полиорганной недостаточностью.
Некротизирующий фасциит, вызванный стрептококком группы А ( S. pyogenes ) представляет собой глубокую инфекцию подкожной клетчатки, вызывающую быстрое разрушение фасций и жира. Люди с системным или местным иммунодефицитом подвержены повышенному риску развития некротизирующего фасциита. Другие факторы риска включают хирургические процедуры, ожоги, тупую травму, небольшие порезы и роды. Локализованная боль, некроз инфицированного поражения кожи, отек, покраснение, отек, учащение пульса и лихорадка являются типичными проявлениями некротизирующего фасциита. В далеко зашедшей стадии заболевания может наблюдаться картина септического шока.[14]
Другие факторы риска включают хирургические процедуры, ожоги, тупую травму, небольшие порезы и роды. Локализованная боль, некроз инфицированного поражения кожи, отек, покраснение, отек, учащение пульса и лихорадка являются типичными проявлениями некротизирующего фасциита. В далеко зашедшей стадии заболевания может наблюдаться картина септического шока.[14]
Оценка
Streptococcus pyogenes , также известный как стрептококк группы А (GAS), является основной причиной фарингита у детей и подростков. Клиницистам следует использовать клинические и эпидемиологические данные для определения вероятности ГАС-фарингита. Американское общество инфекционных заболеваний (IDSA) рекомендует использовать экспресс-тест на обнаружение антигена (RADT) в качестве меры первой линии, чтобы помочь клиницистам в диагностике ГАС-фарингита. Рекомендуется проводить посев из зева у детей с отрицательными результатами RADT, чтобы предотвратить развитие осложнений.[15] Комбинированный подход с использованием утвержденных клинических критериев, таких как модифицированная шкала Centor или шкала FeverPAIN вместе с RADT, является эффективной стратегией снижения стоимости ненужных анализов и неоправданного назначения антибиотиков.
Золотым стандартом для выявления GAS является посев из горла; однако это нерентабельно и может отсрочить лечение.[16] Тест на активность пирролидинилариламидазы (PYR) используется для того, чтобы отличить S. pyogenes от других бета-гемолитических стрептококков, а также тесты на наличие фермента пирролидиниламинопептидазы.
Титры антистрептолизина О (АСО) и анти-ДНКазы В (АДБ) указывают на перенесенную стрептококковую инфекцию и могут быть использованы для диагностики постстрептококковых осложнений.
Лечение/управление
Препаратом выбора для лечения бактериального фарингита является пероральный пенициллин в течение 10 дней или в/м бензатин пенициллин. Это лечение экономически выгодно и имеет узкий спектр действия.
У пациентов с аллергией на пенициллин можно использовать макролиды и цефалоспорины первого поколения.[17][18] Однако некоторые штаммы S. pyogenes выработали устойчивость к макролидам, и макролиды используются в качестве третьей линии лечения стрептококковой инфекции горла.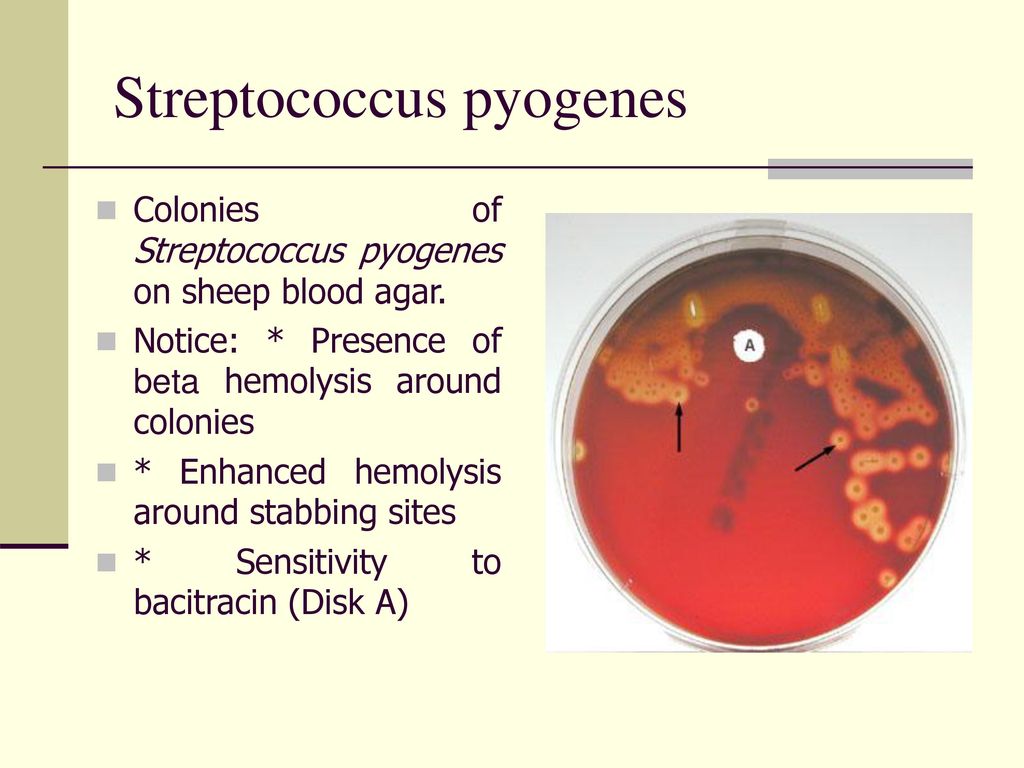 [19]]
[19]]
Тяжелые инвазивные инфекции S. pyogenes можно лечить ванкомицином или клиндамицином.[20] В случае инфекции мягких тканей кожи, вызванной S. pyogenes , рекомендуется внутривенная антибиотикотерапия и операция по удалению некротических тканей.
Дифференциальный диагноз
Стрептококковый фарингит следует дифференцировать от инфекций горла, вызванных вирусом парагриппа, риновирусом, вирусом Коксаки, аденовирусом и т. д.), Mycoplasma species, Corynebacterium diphtheria и вирус Эпштейна-Барр.
Скарлатину можно спутать с корью и краснухой. Однако отсутствие симптомов инфекции верхних дыхательных путей и сливной сыпи при кори может помочь дифференцировать эти заболевания.
Импетиго, вызванное S. pyogenes , необходимо дифференцировать от инфекции импетиго, вызванной золотистым стафилококком. S. pyogenes вызывает небуллезное импетиго, тогда как S. aureus приводит к буллезному импетиго.
Прогноз
Согласно отчету Всемирной организации здравоохранения (ВОЗ) СГЯ занимает девятое место среди инфекционных заболеваний по этиологии смертности человека.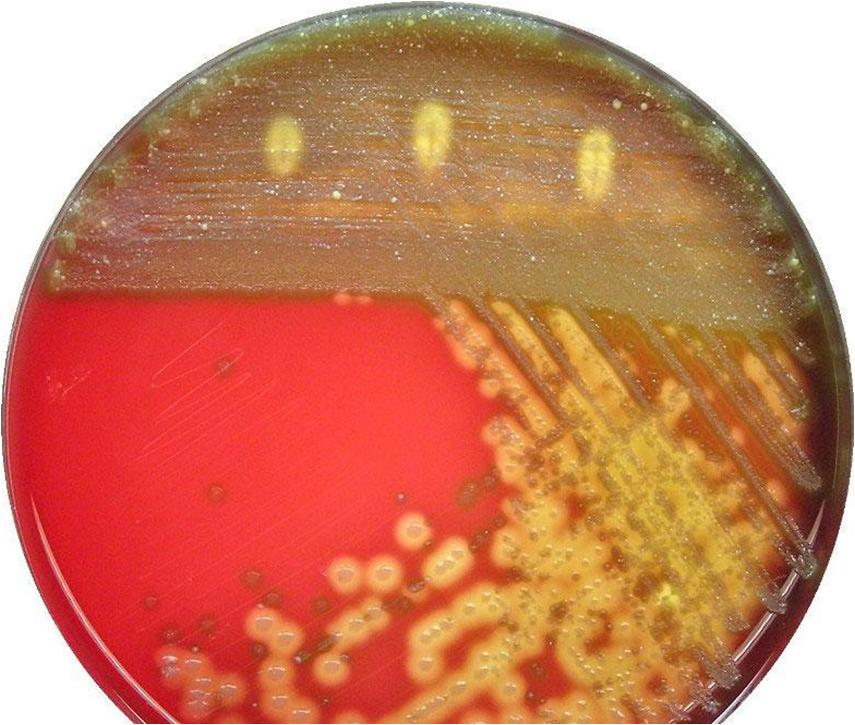 Большинство смертей происходит из-за инвазивных инфекций и RHD, особенно в странах третьего мира.[8] Тяжелые инфекции GAS высоки в богатых странах, от 14% до 19%.[21] Стрептококковый фарингит обычно проходит через 7–10 дней. Однако несоблюдение режима лечения может привести к постинфекционным осложнениям.
Большинство смертей происходит из-за инвазивных инфекций и RHD, особенно в странах третьего мира.[8] Тяжелые инфекции GAS высоки в богатых странах, от 14% до 19%.[21] Стрептококковый фарингит обычно проходит через 7–10 дней. Однако несоблюдение режима лечения может привести к постинфекционным осложнениям.
Осложнения
Осложнения инфекций S. pyogenes можно разделить на гнойные и негнойные осложнения.
Нагноительные осложнения включают перитонзиллярный абсцесс, перитонзиллярный целлюлит, заглоточный абсцесс, средний отит и синусит, увулит, шейный лимфаденит, менингит и абсцесс головного мозга, артрит, эндокардит, остеомиелит и абсцесс печени.
Негнойные осложнения – ревматическая лихорадка, постстрептококковый гломерулонефрит, PANDAS (детские аутоиммунные нервно-психические расстройства, связанные со стрептококковыми инфекциями), хорея Сиденгама и другие аутоиммунные двигательные расстройства.[19]]
Сдерживание и обучение пациентов
Пациенты должны быть проинформированы о важности завершения курса антибиотиков. Им следует посоветовать обратиться к врачу и соблюдать личную гигиену. Мытье рук может значительно снизить вероятность заражения кожными инфекциями, вызванными S. pyogenes .
Им следует посоветовать обратиться к врачу и соблюдать личную гигиену. Мытье рук может значительно снизить вероятность заражения кожными инфекциями, вызванными S. pyogenes .
Pearls and Other Issues
Неэффективное лечение инфекции кожи или глотки, вызванной стрептококком группы А, приводит к острой ревматической лихорадке. Профилактика повторных эпизодов ОРЛ и развития возможных тяжелых исходов ревмокардита требуют вторичной профилактики пенициллином. Вторичная профилактика является наиболее эффективным методом снижения заболеваемости ОРЛ и РБС. Тем не менее первичная профилактика набирает популярность во всем мире. Первичная профилактика включает быстрое лечение стрептококковой инфекции горла или кожи с помощью однократной инъекции бензатинпенициллина или пенициллина перорально в течение 10 дней после подтверждения Инфекция S. pyogenes . Своевременное лечение антибиотиками не только снижает бремя ОРЛ, но также снижает частоту гнойных осложнений, таких как средний отит.
Улучшение результатов работы бригады здравоохранения
Хотя поставщик общих медицинских услуг почти всегда занимается лечением пациентов со стрептококковой инфекцией, уходом за пациентами с тяжелым стрептококковым заболеванием, важно консультироваться с межпрофессиональной командой специалистов, в состав которой входят общий хирург, пластический хирург, рентгенолог, инфекционист и медсестры, прошедшие специальную подготовку.
Некротизирующий фасциит представляет собой опасное для жизни состояние, и из-за сложности этого заболевания требуется коллективный подход. Поскольку некротический фасциит требует неотложной хирургической помощи, необходимо, чтобы пациент был госпитализирован в хирургическое отделение интенсивной терапии, где медицинский персонал имеет навыки проведения санации и, при необходимости, реконструктивной хирургии. Требуется неотложная хирургическая консультация для исследования и удаления некротических тканей. Кроме того, хирургическое исследование определяет этиологию и степень некроза.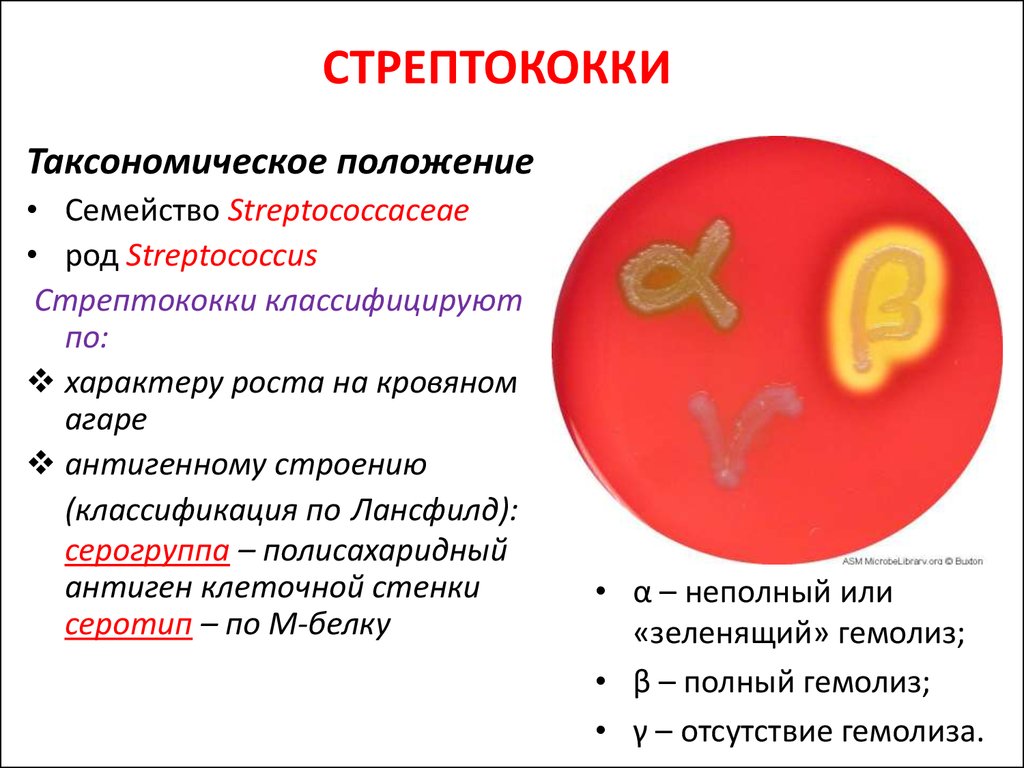 КТ и МРТ могут быть полезны для обнаружения первичных очагов инфекции. Гемодинамическая стабильность должна быть сохранена.
КТ и МРТ могут быть полезны для обнаружения первичных очагов инфекции. Гемодинамическая стабильность должна быть сохранена.
У пациентов с синдромом токсического шока важно контролировать сердечный выброс. Из-за высокой частоты острого респираторного дистресс-синдрома (55%) у пациентов с тяжелой стрептококковой инфекцией мягких тканей необходима интубация и искусственная вентиляция легких. Более чем у 50% пациентов с тяжелыми инфекциями мягких тканей может развиться острая почечная недостаточность; следовательно, может потребоваться диализ.
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Прокомментируйте эту статью.
Рисунок
Микрофотография, Streptococcus pyogenes, бактерии, Образец гноя, Окраска по Паппенгейму, Ревматическая лихорадка, Патология. Предоставлено Центрами по контролю и профилактике заболеваний (CDC)
Ссылки
- 1.
Ibrahim J, Eisen JA, Jospin G, Coil DA, Khazen G, Tokajian S.
 Анализ генома Streptococcus pyogenes, связанного с фарингитом и Кожные инфекции. ПЛОС Один. 2016;11(12):e0168177. [Бесплатная статья PMC: PMC5158041] [PubMed: 27977735]
Анализ генома Streptococcus pyogenes, связанного с фарингитом и Кожные инфекции. ПЛОС Один. 2016;11(12):e0168177. [Бесплатная статья PMC: PMC5158041] [PubMed: 27977735]- 2.
Каннингем М.В. Патогенез стрептококковых инфекций группы А. Clin Microbiol Rev. 2000 Jul; 13(3):470-511. [Бесплатная статья PMC: PMC88944] [PubMed: 10885988]
- 3.
Ferretti JJ, McShan WM, Ajdic D, Savic DJ, Savic G, Lyon K, Primeaux C, Sezate S, Suvorov AN, Kenton S, Lai HS, Lin SP, Qian Y, Jia HG, Najar FZ, Ren Q, Zhu H, Song L, White J, Yuan X, Clifton SW, Roe BA, McLaughlin R. Полная последовательность генома штамма M1 Streptococcus pyogenes. Proc Natl Acad Sci U S A. 2001 Apr 10;98(8):4658-63. [Бесплатная статья PMC: PMC31890] [PubMed: 11296296]
- 4.
Lamagni TL, Darenberg J, Luca-Harari B, Siljander T, Efstratiou A, Henriques-Normark B, Vuopio-Varkila J, Bouvet A, Крети Р., Экелунд К., Колиу М., Рейнерт Р.Р., Стати А., Стракова Л.
 , Унгуряну В., Шален С., Исследовательская группа Strep-EURO. Джасир А. Эпидемиология тяжелого пиогенного стрептококка в Европе. Дж. Клин Микробиол. 2008 июль; 46 (7): 2359-67. [Бесплатная статья PMC: PMC2446932] [PubMed: 18463210]
, Унгуряну В., Шален С., Исследовательская группа Strep-EURO. Джасир А. Эпидемиология тяжелого пиогенного стрептококка в Европе. Дж. Клин Микробиол. 2008 июль; 46 (7): 2359-67. [Бесплатная статья PMC: PMC2446932] [PubMed: 18463210]- 5.
Стивенс Д.Л. Инвазивные стрептококковые инфекции группы А. Клин Инфекция Дис. 1992 янв.; 14(1):2-11. [PubMed: 1571429]
- 6.
Martin JM, Green M, Barbadora KA, Wald ER. Устойчивые к эритромицину стрептококки группы А у школьников в Питтсбурге. N Engl J Med. 2002 г., 18 апреля; 346(16):1200-6. [PubMed: 11961148]
- 7.
Куинн А., Уорд К., Фишетти В.А., Хемрик М., Каннингем М.В. Иммунологическая взаимосвязь между эпитопом класса I стрептококкового М-белка и миозином. Заразить иммун. 1998 сентября; 66 (9): 4418-24. [Статья бесплатно PMC: PMC108534] [PubMed: 9712796]
- 8.
Carapetis JR, Steer AC, Mulholland EK, Weber M. Глобальное бремя стрептококковых заболеваний группы А.
 Ланцет Infect Dis. 2005 ноябрь; 5 (11): 685-94. [PubMed: 16253886]
Ланцет Infect Dis. 2005 ноябрь; 5 (11): 685-94. [PubMed: 16253886]- 9.
Veasy LG, Wiedmeier SE, Orsmond GS, Ruttenberg HD, Boucek MM, Roth SJ, Tait VF, Thompson JA, Daly JA, Kaplan EL. Рецидив острой ревматической лихорадки в межгорной зоне США. N Engl J Med. 1987 19 февраля; 316 (8): 421-7. [PubMed: 3807984]
- 10.
Olafsdottir LB, Erlendsdóttir H, Melo-Cristino J, Weinberger DM, Ramirez M, Kristinsson KG, Gottfredsson M. Инвазивные инфекции, вызванные Streptococcus pyogenes, и клинические характеристики тяжести течения: сезонные изменения , Исландия, 1975–2012 гг. Euro Surveill. 2014 01 мая;19(17):5-14. [PubMed: 24821122]
- 11.
MAXTED WR. Непрямой бактерицидный тест как средство выявления антител к М-антигену Streptococcus pyogenes. Br J Exp патол. 1956 августа; 37(4):415-22. [Бесплатная статья PMC: PMC2082572] [PubMed: 13364152]
- 12.
Эбелл М.Х., Смит М.А., Барри Х.К., Айвз К.
 , Кэри М. Рациональное клиническое обследование. У этого пациента ангина? ДЖАМА. 2000 г., 13 декабря; 284(22):2912-8. [PubMed: 11147989]
, Кэри М. Рациональное клиническое обследование. У этого пациента ангина? ДЖАМА. 2000 г., 13 декабря; 284(22):2912-8. [PubMed: 11147989]- 13.
Basetti S, Hodgson J, Rawson TM, Majeed A. Скарлатина: руководство для врачей общей практики. Лондон J Prim Care (Абингдон). 2017 сен;9(5):77-79. [Бесплатная статья PMC: PMC5649319] [PubMed: 29081840]
- 14.
Misiakos EP, Bagias G, Patapis P, Sotiropoulos D, Kanavidis P, Machairas A. Современные концепции лечения некротизирующего фасциита. Передний сург. 2014;1:36. [Бесплатная статья PMC: PMC4286984] [PubMed: 25593960]
- 15.
Stewart EH, Davis B, Clemans-Taylor BL, Littenberg B, Estrada CA, Centor RM. Экспресс-тест на стрептококк группы А для диагностики фарингита: систематический обзор и метаанализ. ПЛОС Один. 2014;9(11):e111727. [Бесплатная статья PMC: PMC4219770] [PubMed: 25369170]
- 16.
Fox JW, Marcon MJ, Bonsu BK. Диагностика стрептококкового фарингита путем обнаружения Streptococcus pyogenes в образцах из задней части глотки по сравнению с образцами из ротовой полости.
 Дж. Клин Микробиол. 2006 г., июль; 44 (7): 2593-4. [Бесплатная статья PMC: PMC1489465] [PubMed: 16825390]
Дж. Клин Микробиол. 2006 г., июль; 44 (7): 2593-4. [Бесплатная статья PMC: PMC1489465] [PubMed: 16825390]- 17.
Чобы Б.А. Диагностика и лечение стрептококкового фарингита. Ам семейный врач. 2009 01 марта; 79 (5): 383-90. [PubMed: 19275067]
- 18.
Ким С. Оптимальная диагностика и лечение стрептококкового фарингита группы А. Заразить Чематер. 2015 сен; 47 (3): 202-4. [Бесплатная статья PMC: PMC4607776] [PubMed: 26483997]
- 19.
Аль-Хамад AM. Стрептококковое горло. Терапевтические возможности и устойчивость к макролидам. Saudi Med J. 2015 Sep; 36 (9): 1128-9. [Бесплатная статья PMC: PMC4613642] [PubMed: 26318475]
- 20.
Икебе Т., Хирасава К., Судзуки Р., Исобе Дж., Танака Д., Кацукава С., Кавахара Р., Томита М., Огата К., Эндох М., Окуно Р., Ватанабэ Х. Исследование чувствительности Streptococcus pyogenes к противомикробным препаратам, выделенных в Японии от пациентов с тяжелыми инвазивными стрептококковыми инфекциями группы А.
 Противомикробные агенты Chemother. 2005 фев; 49(2): 788-90. [Бесплатная статья PMC: PMC547282] [PubMed: 15673769]
Противомикробные агенты Chemother. 2005 фев; 49(2): 788-90. [Бесплатная статья PMC: PMC547282] [PubMed: 15673769]- 21.
Лепутр А., Долой А., Биде П., Леблон А., Перрошо А., Бинген Э., Триё-Куо П., Буве А., Пояр С., Леви -Брюль Д., микробиологи сети Epibac. Эпидемиология инвазивных инфекций Streptococcus pyogenes во Франции в 2007 г. J Clin Microbiol. 2011 Декабрь; 49 (12): 4094-100. [Бесплатная статья PMC: PMC3232948] [PubMed: 21976764]
Streptococcus Pyogenes — StatPearls — NCBI Bookshelf
Непрерывное обучение
Streptococcus pyogenes является основным специфическим для человека бактериальным патогеном, который вызывает широкий спектр проявлений, начиная от легких локализованных инфекций и заканчивая опасными для жизни инвазивными инфекциями. Неэффективное лечение инфекций, вызванных S. pyogenes, может привести к постинфекционным последствиям острой ревматической лихорадки и постстрептококкового гломерулонефрита. Кроме того, он вызывает инвазивные инфекции, такие как некротизирующий фасциит и синдром токсического шока, что связано с высокой заболеваемостью и смертностью. В этом мероприятии описывается бактерия Streptococcus pyogenes (S. pyogenes), а также рассматриваются эпидемиология, клинические проявления инфекций, вызванных S. pyogenes, оценка и лечение клинических инфекций, вызванных S. pyogenes.
В этом мероприятии описывается бактерия Streptococcus pyogenes (S. pyogenes), а также рассматриваются эпидемиология, клинические проявления инфекций, вызванных S. pyogenes, оценка и лечение клинических инфекций, вызванных S. pyogenes.
Цели:
Определите этиологию S. pyogenes.
Опишите соответствующий анамнез, медицинский осмотр и оценку стрептококкового фарингита.
Ознакомьтесь с вариантами лечения стрептококкового фарингита.
Опишите стратегии межпрофессиональной бригады по улучшению координации помощи и коммуникации для улучшения исходов тяжелых инвазивных инфекций, вызванных S. pyogenes.
Получите доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Streptococcus pyogenes является основным специфическим для человека бактериальным патогеном, вызывающим широкий спектр проявлений, начиная от легких локализованных инфекций и заканчивая опасными для жизни инвазивными инфекциями.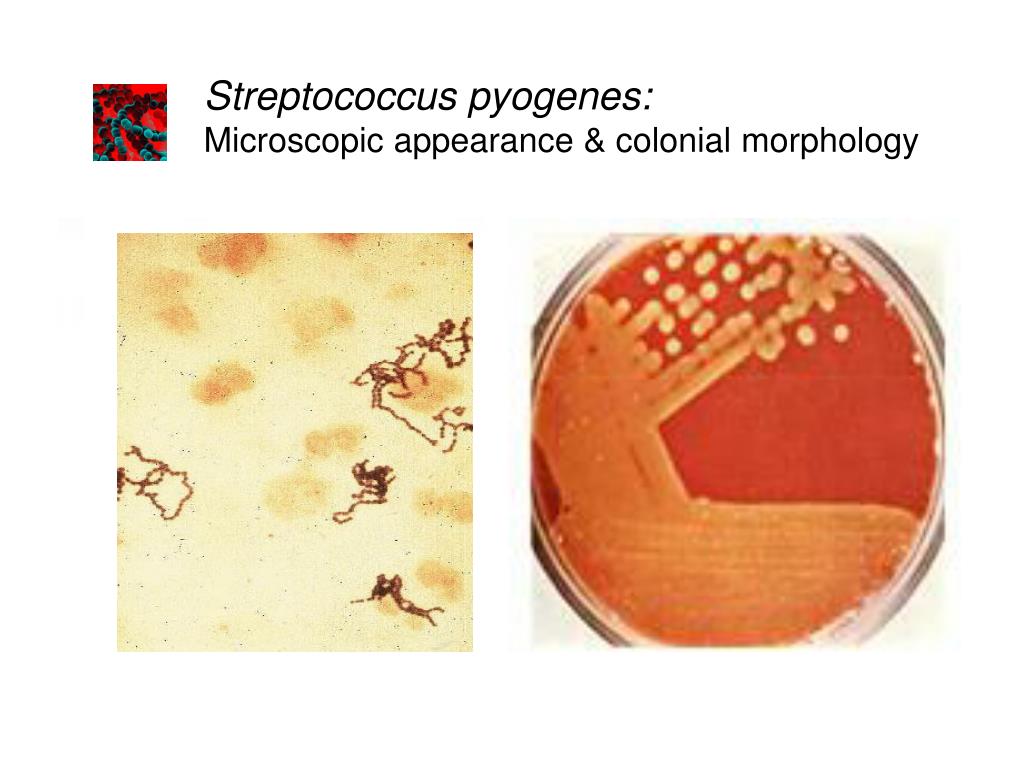 [1] Неэффективное лечение инфекции S. pyogenes может привести к постинфекционным последствиям острой ревматической лихорадки и постстрептококковому гломерулонефриту. Кроме того, он вызывает инвазивные инфекции, такие как некротизирующий фасциит и синдром токсического шока, что связано с высокой заболеваемостью и смертностью.
[1] Неэффективное лечение инфекции S. pyogenes может привести к постинфекционным последствиям острой ревматической лихорадки и постстрептококковому гломерулонефриту. Кроме того, он вызывает инвазивные инфекции, такие как некротизирующий фасциит и синдром токсического шока, что связано с высокой заболеваемостью и смертностью.
Стрептококки представляют собой грамположительные, каталазоотрицательные и коагулазоотрицательные кокки, которые встречаются парами или цепочками. По типу гемолиза на кровяном агаре их делят на три группы: бета-гемолитические (полный лизис эритроцитов), гемолитические (зеленый гемолиз) и гамма-гемолитические (отсутствие гемолиза). Бета-гемолитические стрептококки характеризуются как стрептококки группы А ( Streptococcus pyogenes ) и стрептококки группы В ( Streptococcus agalactiae ).
Этиология
S. pyogenes – грамположительный, каталазоотрицательный, оксидазоотрицательный, β-гемолитический стрептококк. Это факультативный анаэроб, который лучше всего растет при содержании углекислого газа от 5 до 10% и образует точечные колонии на чашках с кровяным агаром.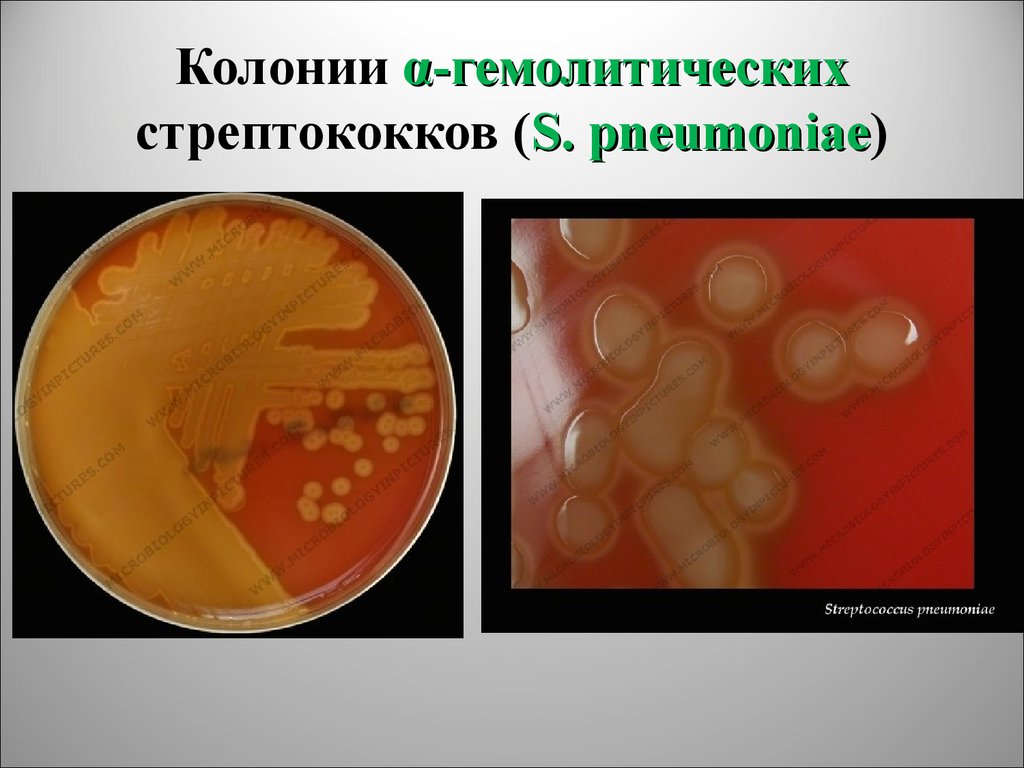 Система серологической группировки Лансфилда используется для дифференциации стрептококков группы А (GAS) от других стрептококков. Антиген типа А S. pyogenes представляет собой полисахарид, состоящий из N-ацетилглюкозамина, присоединенного к основной цепи полимера рамнозы.[2] Белок М является основным поверхностным белком, присутствующим на S. pyogenes клеточная стенка и штаммы GAS дополнительно подразделяются на разные серотипы на основе антигенных характеристик белка М. На основе белка М было идентифицировано более 80 различных серотипов [2]. В зависимости от постинфекционных последствий S. pyogenes подразделяются на два класса: класс I и класс II. Штаммы класса I вызывают ревматическую лихорадку, а штаммы класса II вызывают острый гломерулонефрит.[3]
Система серологической группировки Лансфилда используется для дифференциации стрептококков группы А (GAS) от других стрептококков. Антиген типа А S. pyogenes представляет собой полисахарид, состоящий из N-ацетилглюкозамина, присоединенного к основной цепи полимера рамнозы.[2] Белок М является основным поверхностным белком, присутствующим на S. pyogenes клеточная стенка и штаммы GAS дополнительно подразделяются на разные серотипы на основе антигенных характеристик белка М. На основе белка М было идентифицировано более 80 различных серотипов [2]. В зависимости от постинфекционных последствий S. pyogenes подразделяются на два класса: класс I и класс II. Штаммы класса I вызывают ревматическую лихорадку, а штаммы класса II вызывают острый гломерулонефрит.[3]
S. pyogenes обычно колонизирует глотку, задний проход и слизистую оболочку половых органов. Инфекции, вызванные S. pyogenes очень заразны. Передача может происходить воздушно-капельным путем, при контакте рук с выделениями из носа или с предметами или поверхностями, зараженными бактериями, при контакте кожи с зараженными поражениями или зараженными источниками пищи. Штаммы GAS могут попадать на кожу через ссадины и кожные повреждения, что может привести к рожистому воспалению или целлюлиту.[2] GAS может вызывать инфекцию мышц и фасций, что приводит к миозиту и некротизирующему фасциту, обычно после легкой травмы, и может привести к синдрому токсического шока. S. pyogenes может вызывать инфекцию слизистой оболочки влагалища и матки, вызывая септицемию.[2] Поражения кожи были идентифицированы как наиболее распространенный предрасполагающий фактор для тяжелых инфекций S. pyogenes .[4] Многолюдные места, такие как военные лагеря, дома престарелых и школы, вызывают легкую передачу организма и приводят к эпидемиям стрептококковой инфекции группы А.
Штаммы GAS могут попадать на кожу через ссадины и кожные повреждения, что может привести к рожистому воспалению или целлюлиту.[2] GAS может вызывать инфекцию мышц и фасций, что приводит к миозиту и некротизирующему фасциту, обычно после легкой травмы, и может привести к синдрому токсического шока. S. pyogenes может вызывать инфекцию слизистой оболочки влагалища и матки, вызывая септицемию.[2] Поражения кожи были идентифицированы как наиболее распространенный предрасполагающий фактор для тяжелых инфекций S. pyogenes .[4] Многолюдные места, такие как военные лагеря, дома престарелых и школы, вызывают легкую передачу организма и приводят к эпидемиям стрептококковой инфекции группы А.
Эпидемиология
Частота инфекций, вызванных S. pyogenes , различается в разных частях мира в зависимости от клинических проявлений инфекций. СГС всегда ассоциировался с серьезными заболеваниями, приводящими к высокой заболеваемости и смертности. Инфекции GAS снизились к середине 20 века. Однако к концу 1980 возобновились тяжелые инфекции, вызванные стрептококком группы А (GAS).[5] За последние два десятилетия увеличилось количество негнойных и гнойных осложнений инфекции S. pyogenes . Это увеличение бремени болезни может быть связано с множеством факторов, включая изменение вирулентности и устойчивости к антибиотикам. Инфекции GAS и их осложнения различаются между слаборазвитыми и хорошо развитыми странами. В слаборазвитых странах высоки распространенность ревматической болезни сердца (РБС) и частота летальных исходов, связанных с РБС. И наоборот, в хорошо развитых странах высока частота летальных исходов из-за инвазивной ГАС-инфекции.
Однако к концу 1980 возобновились тяжелые инфекции, вызванные стрептококком группы А (GAS).[5] За последние два десятилетия увеличилось количество негнойных и гнойных осложнений инфекции S. pyogenes . Это увеличение бремени болезни может быть связано с множеством факторов, включая изменение вирулентности и устойчивости к антибиотикам. Инфекции GAS и их осложнения различаются между слаборазвитыми и хорошо развитыми странами. В слаборазвитых странах высоки распространенность ревматической болезни сердца (РБС) и частота летальных исходов, связанных с РБС. И наоборот, в хорошо развитых странах высока частота летальных исходов из-за инвазивной ГАС-инфекции.
Глобальное бремя тяжелых инфекций, вызванных S. pyogenes , составляет 18,1 миллиона случаев, при этом ежегодно регистрируется 1,78 миллиона новых случаев. Распространенность РБС во всем мире составляет не менее 15,6 млн случаев, при этом ежегодно регистрируется 282 000 новых случаев. Приблизительно 233 000 смертей в год связаны с RHD. Каждый год регистрируется примерно 663 000 новых случаев инвазивного СГБ, из них 163 000 летальных исходов в год.[8] 616 миллионов случаев инфекции ангины во всем мире в год можно отнести к S. pyogenes ; также 111 миллионов случаев кожной инфекции у детей из развивающихся стран. [1]. В Соединенных Штатах от 15% до 30% случаев фарингита у детей и от 5% до 20% случаев фарингита в год у взрослых вызваны S. pyogenes. Более того, наблюдается всплеск случаев ОРЛ у детей из семей среднего класса в США.[9]
Каждый год регистрируется примерно 663 000 новых случаев инвазивного СГБ, из них 163 000 летальных исходов в год.[8] 616 миллионов случаев инфекции ангины во всем мире в год можно отнести к S. pyogenes ; также 111 миллионов случаев кожной инфекции у детей из развивающихся стран. [1]. В Соединенных Штатах от 15% до 30% случаев фарингита у детей и от 5% до 20% случаев фарингита в год у взрослых вызваны S. pyogenes. Более того, наблюдается всплеск случаев ОРЛ у детей из семей среднего класса в США.[9]
Инфекция горла чаще встречается в районах с умеренным климатом, и заболеваемость увеличивается в конце зимы и ранней весной. Импетиго чаще встречается у детей, проживающих во влажном климате. Также было замечено, что тяжесть инвазивных кожных инфекций, вызванных GAS, возрастала с января по апрель и коррелирует с восприимчивостью хозяина к заражению серьезной инфекцией.
Токсикокинетика
За клинические проявления S. pyogenes ответственны многочисленные факторы вирулентности. Бактериальная капсула, состоящая из гиалуроновой кислоты, обеспечивает защиту от фагоцитоза. Белок М, липотейхоевая кислота и белок F отвечают за прикрепление бактерий к клеткам-хозяевам. Белок М также отвечает за ингибирование опсонизации путем связывания с регуляторами комплемента и фибриногеном. Белок M является наиболее важным фактором вирулентности для S. pyogenes , поскольку эксперименты показали, что мутанты М не могут выжить в человеческой крови, содержащей фагоциты.[11] S. pyogenes также продуцирует экзотоксины, такие как пирогенный (эритрогенный) токсин, который вызывает сыпь при скарлатине и синдром токсического шока. Другие вирулентные факторы включают стрептокиназу, стрептодорназу, гиалуронидазу и стрептолизины, которые способствуют проникновению в ткани.
Бактериальная капсула, состоящая из гиалуроновой кислоты, обеспечивает защиту от фагоцитоза. Белок М, липотейхоевая кислота и белок F отвечают за прикрепление бактерий к клеткам-хозяевам. Белок М также отвечает за ингибирование опсонизации путем связывания с регуляторами комплемента и фибриногеном. Белок M является наиболее важным фактором вирулентности для S. pyogenes , поскольку эксперименты показали, что мутанты М не могут выжить в человеческой крови, содержащей фагоциты.[11] S. pyogenes также продуцирует экзотоксины, такие как пирогенный (эритрогенный) токсин, который вызывает сыпь при скарлатине и синдром токсического шока. Другие вирулентные факторы включают стрептокиназу, стрептодорназу, гиалуронидазу и стрептолизины, которые способствуют проникновению в ткани.
Анамнез и физикальное исследование
Анамнез и физикальные данные будут различаться в зависимости от типа приобретенной инфекции; тем не менее, для постановки точного клинического диагноза 9 требуется точный анамнез и надлежащая клиническая оценка. 0033 Инфекция S. pyogenes .
0033 Инфекция S. pyogenes .
Боль в горле обычно является серьезной жалобой при стрептококковом фарингите. Наиболее распространенные клинические признаки стрептококкового фарингита включают внезапное начало лихорадки, недомогание, фарингеальный экссудат, болезненную шейную лимфаденопатию и увеличение миндалин.[12]
У детей импетиго является одной из наиболее распространенных кожных инфекций. S. pyogenes вызывают небуллезное импетиго. Обычно вокруг рта или носа появляется зудящая красноватая сыпь, которая позже превращается в заполненный жидкостью пузырь. Волдыри легко лопаются и покрываются коркой медового цвета. Высыпания обычно хорошо локализованы и поражают открытые участки тела: лицо и нижние конечности. Системных проявлений импетиго обычно не бывает.
У больного скарлатиной обычно отмечаются лихорадка высокой степени, боль в горле, клубничный язык и бледная, папулезная несливающаяся сыпь. Сыпь обычно длится от 7 до 10 недель, после чего следует шелушение. Шелушение можно наблюдать только на ладонях и подошвах.[13]
Шелушение можно наблюдать только на ладонях и подошвах.[13]
Инвазивные инфекции мягких тканей, вызванные S. pyogenes , в основном проявляются шоком и полиорганной недостаточностью.
Некротизирующий фасциит, вызванный стрептококком группы А ( S. pyogenes ) представляет собой глубокую инфекцию подкожной клетчатки, вызывающую быстрое разрушение фасций и жира. Люди с системным или местным иммунодефицитом подвержены повышенному риску развития некротизирующего фасциита. Другие факторы риска включают хирургические процедуры, ожоги, тупую травму, небольшие порезы и роды. Локализованная боль, некроз инфицированного поражения кожи, отек, покраснение, отек, учащение пульса и лихорадка являются типичными проявлениями некротизирующего фасциита. В далеко зашедшей стадии заболевания может наблюдаться картина септического шока.[14]
Оценка
Streptococcus pyogenes , также известный как стрептококк группы А (GAS), является основной причиной фарингита у детей и подростков. Клиницистам следует использовать клинические и эпидемиологические данные для определения вероятности ГАС-фарингита. Американское общество инфекционных заболеваний (IDSA) рекомендует использовать экспресс-тест на обнаружение антигена (RADT) в качестве меры первой линии, чтобы помочь клиницистам в диагностике ГАС-фарингита. Рекомендуется проводить посев из зева у детей с отрицательными результатами RADT, чтобы предотвратить развитие осложнений.[15] Комбинированный подход с использованием утвержденных клинических критериев, таких как модифицированная шкала Centor или шкала FeverPAIN вместе с RADT, является эффективной стратегией снижения стоимости ненужных анализов и неоправданного назначения антибиотиков.
Клиницистам следует использовать клинические и эпидемиологические данные для определения вероятности ГАС-фарингита. Американское общество инфекционных заболеваний (IDSA) рекомендует использовать экспресс-тест на обнаружение антигена (RADT) в качестве меры первой линии, чтобы помочь клиницистам в диагностике ГАС-фарингита. Рекомендуется проводить посев из зева у детей с отрицательными результатами RADT, чтобы предотвратить развитие осложнений.[15] Комбинированный подход с использованием утвержденных клинических критериев, таких как модифицированная шкала Centor или шкала FeverPAIN вместе с RADT, является эффективной стратегией снижения стоимости ненужных анализов и неоправданного назначения антибиотиков.
Золотым стандартом для выявления GAS является посев из горла; однако это нерентабельно и может отсрочить лечение.[16] Тест на активность пирролидинилариламидазы (PYR) используется для того, чтобы отличить S. pyogenes от других бета-гемолитических стрептококков, а также тесты на наличие фермента пирролидиниламинопептидазы.
Титры антистрептолизина О (АСО) и анти-ДНКазы В (АДБ) указывают на перенесенную стрептококковую инфекцию и могут быть использованы для диагностики постстрептококковых осложнений.
Лечение/управление
Препаратом выбора для лечения бактериального фарингита является пероральный пенициллин в течение 10 дней или в/м бензатин пенициллин. Это лечение экономически выгодно и имеет узкий спектр действия.
У пациентов с аллергией на пенициллин можно использовать макролиды и цефалоспорины первого поколения.[17][18] Однако некоторые штаммы S. pyogenes выработали устойчивость к макролидам, и макролиды используются в качестве третьей линии лечения стрептококковой инфекции горла.[19]]
Тяжелые инвазивные инфекции S. pyogenes можно лечить ванкомицином или клиндамицином.[20] В случае инфекции мягких тканей кожи, вызванной S. pyogenes , рекомендуется внутривенная антибиотикотерапия и операция по удалению некротических тканей.
Дифференциальный диагноз
Стрептококковый фарингит следует дифференцировать от инфекций горла, вызванных вирусом парагриппа, риновирусом, вирусом Коксаки, аденовирусом и т. д.), Mycoplasma species, Corynebacterium diphtheria и вирус Эпштейна-Барр.
д.), Mycoplasma species, Corynebacterium diphtheria и вирус Эпштейна-Барр.
Скарлатину можно спутать с корью и краснухой. Однако отсутствие симптомов инфекции верхних дыхательных путей и сливной сыпи при кори может помочь дифференцировать эти заболевания.
Импетиго, вызванное S. pyogenes , необходимо дифференцировать от инфекции импетиго, вызванной золотистым стафилококком. S. pyogenes вызывает небуллезное импетиго, тогда как S. aureus приводит к буллезному импетиго.
Прогноз
Согласно отчету Всемирной организации здравоохранения (ВОЗ) СГЯ занимает девятое место среди инфекционных заболеваний по этиологии смертности человека. Большинство смертей происходит из-за инвазивных инфекций и RHD, особенно в странах третьего мира.[8] Тяжелые инфекции GAS высоки в богатых странах, от 14% до 19%.[21] Стрептококковый фарингит обычно проходит через 7–10 дней. Однако несоблюдение режима лечения может привести к постинфекционным осложнениям.
Осложнения
Осложнения инфекций S. pyogenes можно разделить на гнойные и негнойные осложнения.
Нагноительные осложнения включают перитонзиллярный абсцесс, перитонзиллярный целлюлит, заглоточный абсцесс, средний отит и синусит, увулит, шейный лимфаденит, менингит и абсцесс головного мозга, артрит, эндокардит, остеомиелит и абсцесс печени.
Негнойные осложнения – ревматическая лихорадка, постстрептококковый гломерулонефрит, PANDAS (детские аутоиммунные нервно-психические расстройства, связанные со стрептококковыми инфекциями), хорея Сиденгама и другие аутоиммунные двигательные расстройства.[19]]
Сдерживание и обучение пациентов
Пациенты должны быть проинформированы о важности завершения курса антибиотиков. Им следует посоветовать обратиться к врачу и соблюдать личную гигиену. Мытье рук может значительно снизить вероятность заражения кожными инфекциями, вызванными S. pyogenes .
Pearls and Other Issues
Неэффективное лечение инфекции кожи или глотки, вызванной стрептококком группы А, приводит к острой ревматической лихорадке. Профилактика повторных эпизодов ОРЛ и развития возможных тяжелых исходов ревмокардита требуют вторичной профилактики пенициллином. Вторичная профилактика является наиболее эффективным методом снижения заболеваемости ОРЛ и РБС. Тем не менее первичная профилактика набирает популярность во всем мире. Первичная профилактика включает быстрое лечение стрептококковой инфекции горла или кожи с помощью однократной инъекции бензатинпенициллина или пенициллина перорально в течение 10 дней после подтверждения Инфекция S. pyogenes . Своевременное лечение антибиотиками не только снижает бремя ОРЛ, но также снижает частоту гнойных осложнений, таких как средний отит.
Профилактика повторных эпизодов ОРЛ и развития возможных тяжелых исходов ревмокардита требуют вторичной профилактики пенициллином. Вторичная профилактика является наиболее эффективным методом снижения заболеваемости ОРЛ и РБС. Тем не менее первичная профилактика набирает популярность во всем мире. Первичная профилактика включает быстрое лечение стрептококковой инфекции горла или кожи с помощью однократной инъекции бензатинпенициллина или пенициллина перорально в течение 10 дней после подтверждения Инфекция S. pyogenes . Своевременное лечение антибиотиками не только снижает бремя ОРЛ, но также снижает частоту гнойных осложнений, таких как средний отит.
Улучшение результатов работы бригады здравоохранения
Хотя поставщик общих медицинских услуг почти всегда занимается лечением пациентов со стрептококковой инфекцией, уходом за пациентами с тяжелым стрептококковым заболеванием, важно консультироваться с межпрофессиональной командой специалистов, в состав которой входят общий хирург, пластический хирург, рентгенолог, инфекционист и медсестры, прошедшие специальную подготовку.
Некротизирующий фасциит представляет собой опасное для жизни состояние, и из-за сложности этого заболевания требуется коллективный подход. Поскольку некротический фасциит требует неотложной хирургической помощи, необходимо, чтобы пациент был госпитализирован в хирургическое отделение интенсивной терапии, где медицинский персонал имеет навыки проведения санации и, при необходимости, реконструктивной хирургии. Требуется неотложная хирургическая консультация для исследования и удаления некротических тканей. Кроме того, хирургическое исследование определяет этиологию и степень некроза. КТ и МРТ могут быть полезны для обнаружения первичных очагов инфекции. Гемодинамическая стабильность должна быть сохранена.
У пациентов с синдромом токсического шока важно контролировать сердечный выброс. Из-за высокой частоты острого респираторного дистресс-синдрома (55%) у пациентов с тяжелой стрептококковой инфекцией мягких тканей необходима интубация и искусственная вентиляция легких. Более чем у 50% пациентов с тяжелыми инфекциями мягких тканей может развиться острая почечная недостаточность; следовательно, может потребоваться диализ.
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Прокомментируйте эту статью.
Рисунок
Микрофотография, Streptococcus pyogenes, бактерии, Образец гноя, Окраска по Паппенгейму, Ревматическая лихорадка, Патология. Предоставлено Центрами по контролю и профилактике заболеваний (CDC)
Ссылки
- 1.
Ibrahim J, Eisen JA, Jospin G, Coil DA, Khazen G, Tokajian S. Анализ генома Streptococcus pyogenes, связанного с фарингитом и Кожные инфекции. ПЛОС Один. 2016;11(12):e0168177. [Бесплатная статья PMC: PMC5158041] [PubMed: 27977735]
- 2.
Каннингем М.В. Патогенез стрептококковых инфекций группы А. Clin Microbiol Rev. 2000 Jul; 13(3):470-511. [Бесплатная статья PMC: PMC88944] [PubMed: 10885988]
- 3.
Ferretti JJ, McShan WM, Ajdic D, Savic DJ, Savic G, Lyon K, Primeaux C, Sezate S, Suvorov AN, Kenton S, Lai HS, Lin SP, Qian Y, Jia HG, Najar FZ, Ren Q, Zhu H, Song L, White J, Yuan X, Clifton SW, Roe BA, McLaughlin R.
 Полная последовательность генома штамма M1 Streptococcus pyogenes. Proc Natl Acad Sci U S A. 2001 Apr 10;98(8):4658-63. [Бесплатная статья PMC: PMC31890] [PubMed: 11296296]
Полная последовательность генома штамма M1 Streptococcus pyogenes. Proc Natl Acad Sci U S A. 2001 Apr 10;98(8):4658-63. [Бесплатная статья PMC: PMC31890] [PubMed: 11296296]- 4.
Lamagni TL, Darenberg J, Luca-Harari B, Siljander T, Efstratiou A, Henriques-Normark B, Vuopio-Varkila J, Bouvet A, Крети Р., Экелунд К., Колиу М., Рейнерт Р.Р., Стати А., Стракова Л., Унгуряну В., Шален С., Исследовательская группа Strep-EURO. Джасир А. Эпидемиология тяжелого пиогенного стрептококка в Европе. Дж. Клин Микробиол. 2008 июль; 46 (7): 2359-67. [Бесплатная статья PMC: PMC2446932] [PubMed: 18463210]
- 5.
Стивенс Д.Л. Инвазивные стрептококковые инфекции группы А. Клин Инфекция Дис. 1992 янв.; 14(1):2-11. [PubMed: 1571429]
- 6.
Martin JM, Green M, Barbadora KA, Wald ER. Устойчивые к эритромицину стрептококки группы А у школьников в Питтсбурге. N Engl J Med. 2002 г., 18 апреля; 346(16):1200-6. [PubMed: 11961148]
- 7.

Куинн А., Уорд К., Фишетти В.А., Хемрик М., Каннингем М.В. Иммунологическая взаимосвязь между эпитопом класса I стрептококкового М-белка и миозином. Заразить иммун. 1998 сентября; 66 (9): 4418-24. [Статья бесплатно PMC: PMC108534] [PubMed: 9712796]
- 8.
Carapetis JR, Steer AC, Mulholland EK, Weber M. Глобальное бремя стрептококковых заболеваний группы А. Ланцет Infect Dis. 2005 ноябрь; 5 (11): 685-94. [PubMed: 16253886]
- 9.
Veasy LG, Wiedmeier SE, Orsmond GS, Ruttenberg HD, Boucek MM, Roth SJ, Tait VF, Thompson JA, Daly JA, Kaplan EL. Рецидив острой ревматической лихорадки в межгорной зоне США. N Engl J Med. 1987 19 февраля; 316 (8): 421-7. [PubMed: 3807984]
- 10.
Olafsdottir LB, Erlendsdóttir H, Melo-Cristino J, Weinberger DM, Ramirez M, Kristinsson KG, Gottfredsson M. Инвазивные инфекции, вызванные Streptococcus pyogenes, и клинические характеристики тяжести течения: сезонные изменения , Исландия, 1975–2012 гг.
 Euro Surveill. 2014 01 мая;19(17):5-14. [PubMed: 24821122]
Euro Surveill. 2014 01 мая;19(17):5-14. [PubMed: 24821122]- 11.
MAXTED WR. Непрямой бактерицидный тест как средство выявления антител к М-антигену Streptococcus pyogenes. Br J Exp патол. 1956 августа; 37(4):415-22. [Бесплатная статья PMC: PMC2082572] [PubMed: 13364152]
- 12.
Эбелл М.Х., Смит М.А., Барри Х.К., Айвз К., Кэри М. Рациональное клиническое обследование. У этого пациента ангина? ДЖАМА. 2000 г., 13 декабря; 284(22):2912-8. [PubMed: 11147989]
- 13.
Basetti S, Hodgson J, Rawson TM, Majeed A. Скарлатина: руководство для врачей общей практики. Лондон J Prim Care (Абингдон). 2017 сен;9(5):77-79. [Бесплатная статья PMC: PMC5649319] [PubMed: 29081840]
- 14.
Misiakos EP, Bagias G, Patapis P, Sotiropoulos D, Kanavidis P, Machairas A. Современные концепции лечения некротизирующего фасциита. Передний сург. 2014;1:36. [Бесплатная статья PMC: PMC4286984] [PubMed: 25593960]
- 15.

Stewart EH, Davis B, Clemans-Taylor BL, Littenberg B, Estrada CA, Centor RM. Экспресс-тест на стрептококк группы А для диагностики фарингита: систематический обзор и метаанализ. ПЛОС Один. 2014;9(11):e111727. [Бесплатная статья PMC: PMC4219770] [PubMed: 25369170]
- 16.
Fox JW, Marcon MJ, Bonsu BK. Диагностика стрептококкового фарингита путем обнаружения Streptococcus pyogenes в образцах из задней части глотки по сравнению с образцами из ротовой полости. Дж. Клин Микробиол. 2006 г., июль; 44 (7): 2593-4. [Бесплатная статья PMC: PMC1489465] [PubMed: 16825390]
- 17.
Чобы Б.А. Диагностика и лечение стрептококкового фарингита. Ам семейный врач. 2009 01 марта; 79 (5): 383-90. [PubMed: 19275067]
- 18.
Ким С. Оптимальная диагностика и лечение стрептококкового фарингита группы А. Заразить Чематер. 2015 сен; 47 (3): 202-4. [Бесплатная статья PMC: PMC4607776] [PubMed: 26483997]
- 19.
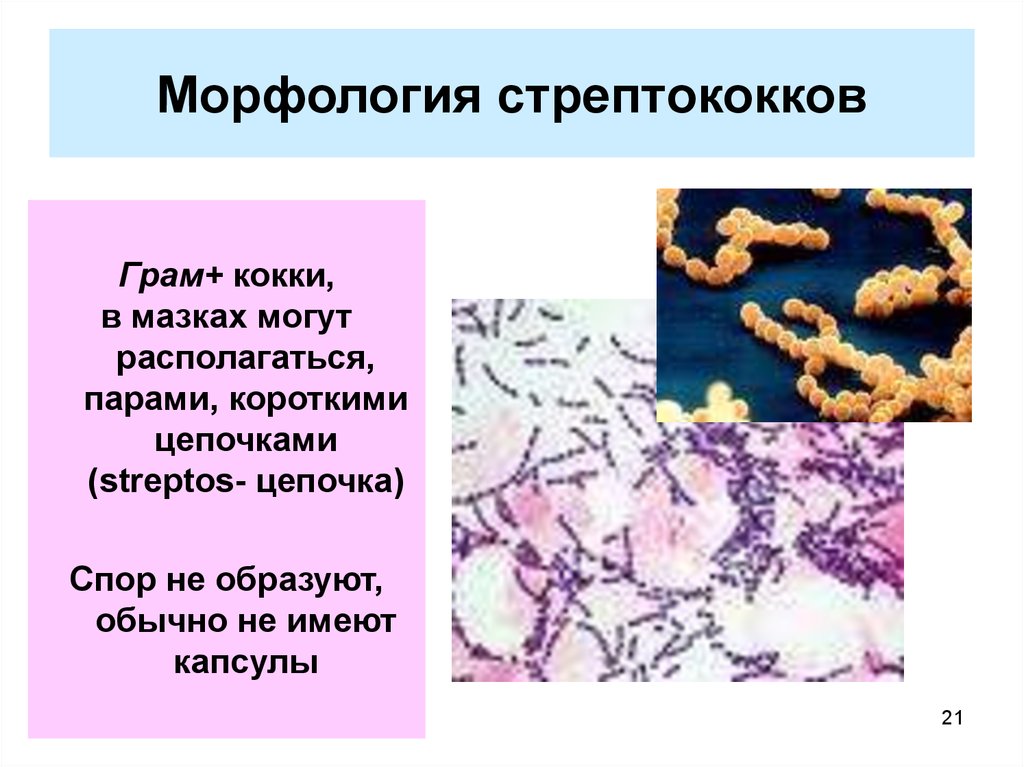

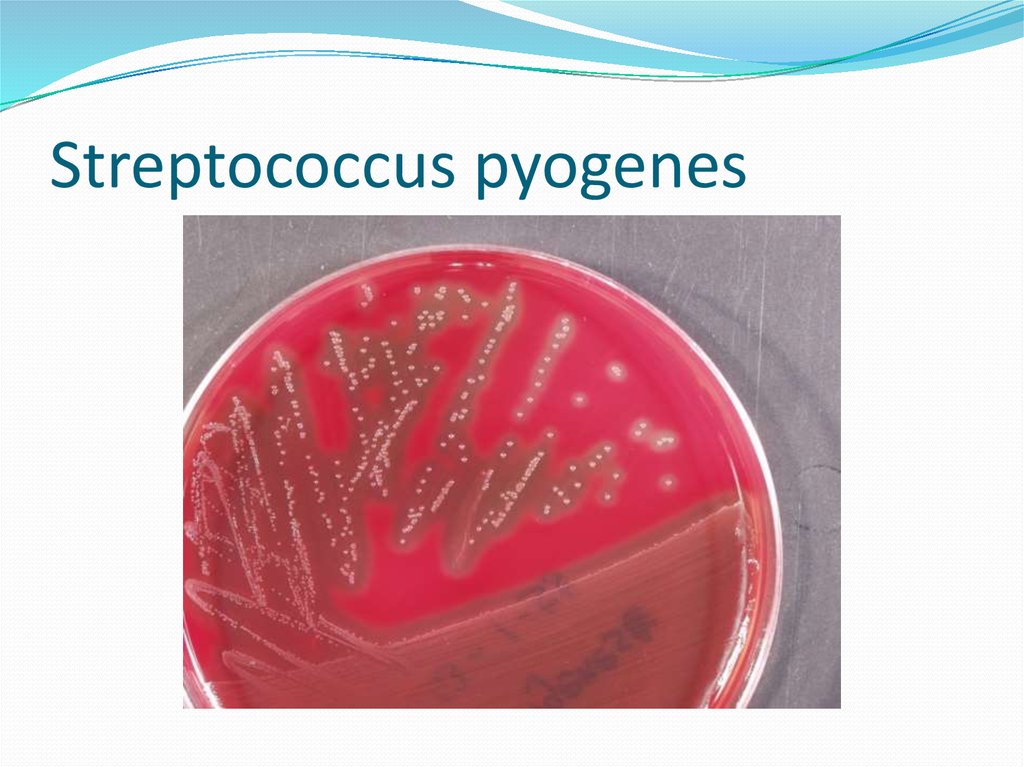 В норме колонизирует глотку у 3% взрослых и 15-20% детей школьного возраста. Так что без клинической картины острого фарингита не надо хвататься за антибиотики, как собственно и что-то сеять вне обострений.
В норме колонизирует глотку у 3% взрослых и 15-20% детей школьного возраста. Так что без клинической картины острого фарингита не надо хвататься за антибиотики, как собственно и что-то сеять вне обострений. Но даже сейчас, не дай бог, хирургу со стрептококковой ангиной подойти к операционному столу, и к концу первых суток стрептококк организует очень больную и страшно воняющую проблему в конкретной послеоперационной ране. Лирическое отступление off.
Но даже сейчас, не дай бог, хирургу со стрептококковой ангиной подойти к операционному столу, и к концу первых суток стрептококк организует очень больную и страшно воняющую проблему в конкретной послеоперационной ране. Лирическое отступление off.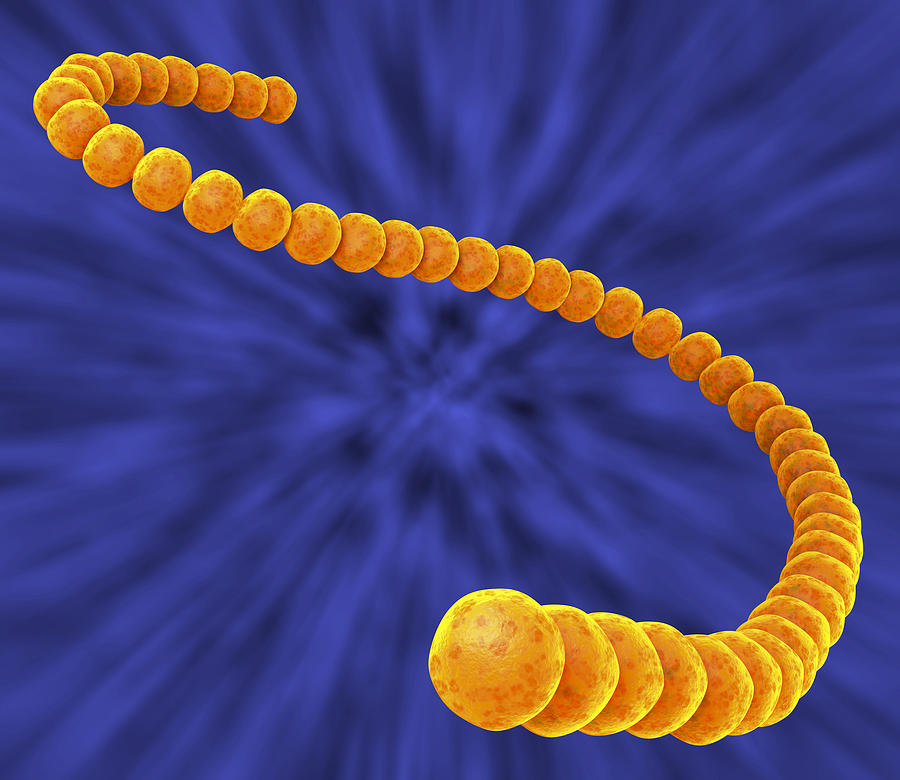 pyogenes не представляет никакого труда, здесь в прямом смысле достаточно покрасить мазок по Граму. Все упирается в организационные аспекты – пока мазок доберется до лаборатории, пока покрасят. Пока ответят, пациент успеет много раз осложнится, если это стрептококк, или выздороветь, если это был фарингит и вызвавший его вирус (все-таки до 60% фарингитов вызваны вирусами, а не бактериальной флорой). Не хотелось бы останавливаться подробно на каждом перечисленном заболевании, но не упомянуть о диагностике острого фарингита, которая чаще всего и запускает множество вторичных осложнений, мы не можем. Для облегчения диагностики острого существуют несколько диагностических шкал. Автору более всего симпатична шкала Мак-Айзека в виду максимальной простоты ее использования.
pyogenes не представляет никакого труда, здесь в прямом смысле достаточно покрасить мазок по Граму. Все упирается в организационные аспекты – пока мазок доберется до лаборатории, пока покрасят. Пока ответят, пациент успеет много раз осложнится, если это стрептококк, или выздороветь, если это был фарингит и вызвавший его вирус (все-таки до 60% фарингитов вызваны вирусами, а не бактериальной флорой). Не хотелось бы останавливаться подробно на каждом перечисленном заболевании, но не упомянуть о диагностике острого фарингита, которая чаще всего и запускает множество вторичных осложнений, мы не можем. Для облегчения диагностики острого существуют несколько диагностических шкал. Автору более всего симпатична шкала Мак-Айзека в виду максимальной простоты ее использования.

 Если совсем все бедно, можно пенициллин – 12 млн в сутки. Но если вы провели правильную периоперационную антибиотикопрофилактику, учли все риски и не забыли про свой личный стрептококк в горле, то риск ранней раневой минимален, а если профилактика продленная на 72 часа, то она и раскрутиться не успеет.
Если совсем все бедно, можно пенициллин – 12 млн в сутки. Но если вы провели правильную периоперационную антибиотикопрофилактику, учли все риски и не забыли про свой личный стрептококк в горле, то риск ранней раневой минимален, а если профилактика продленная на 72 часа, то она и раскрутиться не успеет.