Лейкотриены — Википедия (с комментариями)
Материал из Википедии — свободной энциклопедии
Лейкотрие́ны — группа липидных высокоактивных веществ, образующаяся в организме из арахидоновой кислоты, содержащей 20-членную углеродную цепь. Подкласс лейкотриенов, вместе с простаноидами, входит в класс эйкозаноидов. Один из основных эффектов лейкотриенов — бронхоспазм — лежит в основе патогенеза бронхиальной астмы.
История
В 1938 году Киллвэй и Фелдберг, при исследовании воздействия яда кобры на лёгкие морских свинок, случайно обнаружили в лёгочном перфузате неизвестное ранее вещество, обладающее бронхоконстрикторным действием. Бронхоспазм, развивавшийся под воздействием этого неизвестного вещества, отличался от вызванной гистамином бронхоспастической реакции медленным развитием и большей продолжительностью. В связи с этим учёные назвали это вещество медленнореагирующей субстанцией анафилаксии (сокращенно МРСА, англ. slow reacting substance).
В 1960 году Броклхёрст выделил МРСА из лёгочной ткани больного бронхиальной астмой после проведения ингаляционной провокации с аллергеном. Этим исследованием он подтвердил, что МРСА обладает выраженным бронхоконстрикторным действием и является важным медиатором в развитии аллергического воспаления у больных БА.
В конце 1970-х годов была расшифрована структура молекулы МРСА. В исследованиях Бенгта Самуэльсона и его сотрудников было показано, что МРСА представляет собой неоднородную химическую структуру, относящуюся к семейству липидных медиаторов. Впервые эти медиаторы были выделены из лейкоцитов и характеризовались наличием конъюгированной триеновой структуры. В связи с этим выделенные вещества были названы «лейкотриенами» (ЛТ).
В настоящее время идентифицированы ЛТА
Синтез
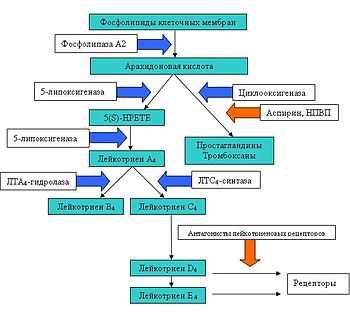 Как было сказано выше, лейкотриены образуются из арахидоновой кислоты, которая, в свою очередь, отщепляется от фосфолипидов цитоплазматической мембраны, с помощью фермента фосфолипаза A2.
Как было сказано выше, лейкотриены образуются из арахидоновой кислоты, которая, в свою очередь, отщепляется от фосфолипидов цитоплазматической мембраны, с помощью фермента фосфолипаза A2.
Далее арахидоновая кислота может трансформироваться двумя путями: под влиянием ЦОГ она превращается в простаноиды, а под влиянием липоксигеназной ферментной системы в лейкотриены.
Липоксигеназная ферментная система относится к растворимым цитозольным ферментам, они обнаружены в цитоплазме альвеолярных макрофагах, тромбоцитах, тучных клетках и лейкоцитах. Наиболее важным среди ферментов этой системы является 5-липоксигеназа (5-ЛОГ). Активация перечисленных клеток приводит к перемещению 5-ЛОГ к мембране ядерного аппарата и связыванию со специфическим белком — 5-ЛОГ-активирующим протеином (5-ЛОГ-АП). 5-ЛОГ-АП является кофактором при взаимодействии арахидоновой кислоты и 5-ЛОГ. Таким образом, арахидоновая кислота под воздействием комплекса 5-ЛОГ + 5-ЛОГ-АП превращается в нестабильное соединение 5-гидроксипероксиэйкозатетраеновую кислоту (5-HPETE), из которой в свою очередь образуется ЛТА
Далее ЛТА4 может превращаться двумя путями: либо при участии цитозольного фермента ЛТА4-гидролазы в ЛТВ4, либо под воздействием ЛТС4-синтетазы с образованием цисЛТС4. ЛТС4 выходит во внеклеточное пространство и далее с помощью g-глутамилтрансептидазы превращается в ЛТD4, который затем под влиянием дипептидазы образует ЛТЕ4. ЛТЕ4 является субстратом для образования ЛТF
Химическое строение
Лейкотриены являются производными арахидоновой кислоты. Последняя является полиненасыщенной кислотой, содержащей 20 атомов углерода, из которых 1-й входит в состав карбоксильной группы (-COOH). Молекула арахидоновой кислоты также содержит 4 двойные связи: первая расположена между 5 и 6 атомом углерода (счет их ведется от -COOH), вторая — между 8 и 9, третья — между 11 и 12, четвёртая — между 14 и 15.
Известно 6 типов лейкотриенов — А, В, С, D, Е и F. Их объединяет — с точки зрения химического строения — наличие карбоксильной группы, общее число атомов углерода в основной цепочке (20) и наличие 4 двойных связей (поэтому после написания названия лейкотриена, указывают индекс 4). Тем не менее, каждая молекула лейкотриенов имеет свои особенности:
- ЛТА4 — его 4 двойные связи расположены следующим образом: первая — между 7 и 8 атомом углерода, вторая — между 9 и 10, третья — между 11 и 12, четвёртая — между 14 и 15. Кроме того, к 5 и 6 атомам углерода присоединяется одна эпоксидная группа.
- ЛТВ4 — его 4 двойные связи расположены иначе: первая — между 6 и 7 атомом углерода, вторая — между 8 и 9, третья — между 10 и 11, четвёртая — между 14 и 15. Кроме того, к 5 и 13 атомам углерода присоединяются гидроксильные группы.
- ЛТС4 — также отличается расположением 4 двойных связей: первая — между 7 и 8 атомом углерода, вторая — между 9 и 10, третья — между 11 и 12, четвёртая — между 13 и 14. Кроме того, к 5-му атому углерода присоединяются гидроксильная группа, а к шестому глутатион, через сульфидную группу цистеина.
- ЛТD4 — очень похож на лейкотриен С4, но он образуется при отщеплении от глутатиона одной аминокислоты — глутамата. Поэтому его боковая пептидная цепочка именуется цистеинилглицином.
- ЛТE4 — образутся из ЛТD4, после того как его пептидная цепь лишается ещё одной аминокислоты — глицина.
- ЛТF4 — очень похож на лейкотриен С4, но он образуется при отщеплении от глутатиона глицина. Поэтому его боковая пептидная цепочка именуется γ-глутамилцистеином).[1]
Таким образом, по химическому строению, можно выделить две группы лейкотриенов:
- 1 группа — «пептидные (цистеиновые) лейкотриены», к ним относят ЛТС4, ЛТD4, ЛТЕ4, ЛТF4.
- 2 группа — лейкотриены, без пептидов: ЛТА4, ЛТВ4.
Роль в организме
Лейкотриеновые рецепторы
Выделяют три основных типа рецепторов лейкотриенов.[2] Причём два из них модулируются «пептидными лейкотриенами»:
- «Пептидные лейкотриены» модулируют специфические рецепторы, сопряженные с G-белком. Их обозначают CysLT-R. В настоящее время выделяют 2 типа CysLT. Взаимодействие лейкотриенов с рецепторами 1 типа (CysLT1) определяет спектр их основных эффектов (бронхоспазм). Связывание ЛТ с рецепторами 2 типа (CysLT2) изменяет тонус и проницаемость сосудов.
- Лейкотриен B4 модулирует другой тип рецепторов — BLT1- и BLT2-рецепторы (другое название LTB4-рецепторы).
Основные эффекты
- ЛТB4 — опосредует хемотаксис, экссудацию плазмы, сокращение паренхимы лёгких, участие в иммунных ответах.
- ЛТC4, ЛТD4, ЛТE4 являются основными компонентами МРСА, поэтому в первую очередь эта группа лейкотриенов относится к мощным бронхоконстрикторам. Также эти лейкотриены способны повышать тонус гладких мышц ЖКТ, опосредовать экссудацию плазмы и сокращение паренхимы лёгких.
Роль в патологии
- Лейкотриены вызывают очень неприятный аспириновый бронхоспазм, возникающий при приёме неселективных НПВС: аспирин и др.[3] Аспириновый бронхоспазм порождается следующим образом: ЦОГ, которую ингибируют НПВС, катализирует реакцию превращения арахидоновой кислоты в циклический эндопероксид ПГ h3. Это ведёт к тому, что синтез ПГ резко уменьшается, а на этом фоне преобладающими станут лейкотриены. Однако, активность фосфолипазы A2 остаётся неизменной, соответственно арахидоновой кислоты отщепляется от фосфолипидов цитоплазматической мембраны столько же, сколько и в норме. Если в физиологических условиях арахидоновая кислота равномерно распределялась, поступая на синтез и ПГ и ЛТ, то при ингибировании ЦОГ, она целиком и полностью будет поступать на синтез лейкотриенов. Таким образом, при использовании неселективных НПВС, в тканях человека будет не просто вакатное (лат.
Возможности фармакологической коррекции эффектов
- В настоящее время разработаны и успешно используются антагонисты CysL-R1: монтелукаст, зафирлукаст и пранлукаст (последний не зарегистрирован в РФ). Препараты могут использоваться в виде монотерапии у больных лёгкой персистирующей бронхиальной астмой. У больных со среднетяжёлым и тяжёлым течением заболевания антагонисты CysLT-R1 используют в качестве дополнительной терапии в комбинации с ингаляционными глюкокортикоидами (ИГКС) с целью уменьшения дозы ИГКС и достижения полного контроля астмы. Отмечено также их положительное влияние на течение аспириновой БА у больных с непереносимостью нестероидных противовоспалительных препаратов.
- Созданы ингибиторы биосинтеза лейкотриенов, подавляющие активность фермента 5-ЛОГ: зилеутон. Установлено, что этот препарат оказывает бронхорасширяющее действие (его начало в течение 2-х часов, продолжительность — 5 часов после приема) и предупреждает развитие бронхоспазма, вызываемого аспирином и холодным воздухом.
- В экспериментах созданы блокаторы 5-ЛОГ-активирующего протеина и рецепторов ЛТB4.
Таким образом, можно выделить 4 точки приложения препаратов:
- Прямые ингибиторы 5-ЛОГ (зилеутон, Z-D2138, АВТ-761),
- Ингибиторы 5-ЛОГ-АП предупреждающие связывание этого мембраносвязанного белка с арахидоновой кислотой (МК-0591, МК-886, BAYxl005 и др.),
- Антагонисты CysLT-R (зафирлукаст, монтелукаст, пранлукаст и др.),
- Антагонисты рецепторов лейкотриенов В4 (U-75, 302).[4]
Напишите отзыв о статье «Лейкотриены»
Примечания
- ↑ [www.xumuk.ru/encyklopedia/2295.html ЛЕЙКОТРИЕНЫ — Химическая энциклопедия].
- ↑ Голубев Л. А., Бабак С. Л., Григорьянц Г. А. [medi.ru/doc/6810110.htm Антагонисты леикотриеновых рецепторов в лечении бронхиальной астмы] // Южно-Российский медицинский журнал. — 2001. — № 1-2.
- ↑ Княжеская Н. П. [rmj.ru/articles_1639.htm Аспириновая бронхиальная астма и антагонисты лейкотриенов] // РМЖ. — 2000. — Т. 8, № 12.
- ↑ [meduniver.com/Medical/pulmonologia/234.html Антилейкотриеновые препараты. Зилеутон].
Ссылки
- [www.consilium-medicum.com/article/15676 consilium-medicum.com]
- [chemport.ru/chemical_encyclopedia_article_1918.html chemport.ru]
- [www.xumuk.ru/encyklopedia/2295.html xumuk.ru]
Отрывок, характеризующий Лейкотриены
– Да, зайду.Ростов долго стоял у угла, издалека глядя на пирующих. В уме его происходила мучительная работа, которую он никак не мог довести до конца. В душе поднимались страшные сомнения. То ему вспоминался Денисов с своим изменившимся выражением, с своей покорностью и весь госпиталь с этими оторванными руками и ногами, с этой грязью и болезнями. Ему так живо казалось, что он теперь чувствует этот больничный запах мертвого тела, что он оглядывался, чтобы понять, откуда мог происходить этот запах. То ему вспоминался этот самодовольный Бонапарте с своей белой ручкой, который был теперь император, которого любит и уважает император Александр. Для чего же оторванные руки, ноги, убитые люди? То вспоминался ему награжденный Лазарев и Денисов, наказанный и непрощенный. Он заставал себя на таких странных мыслях, что пугался их.
Запах еды преображенцев и голод вызвали его из этого состояния: надо было поесть что нибудь, прежде чем уехать. Он пошел к гостинице, которую видел утром. В гостинице он застал так много народу, офицеров, так же как и он приехавших в статских платьях, что он насилу добился обеда. Два офицера одной с ним дивизии присоединились к нему. Разговор естественно зашел о мире. Офицеры, товарищи Ростова, как и большая часть армии, были недовольны миром, заключенным после Фридланда. Говорили, что еще бы подержаться, Наполеон бы пропал, что у него в войсках ни сухарей, ни зарядов уж не было. Николай молча ел и преимущественно пил. Он выпил один две бутылки вина. Внутренняя поднявшаяся в нем работа, не разрешаясь, всё также томила его. Он боялся предаваться своим мыслям и не мог отстать от них. Вдруг на слова одного из офицеров, что обидно смотреть на французов, Ростов начал кричать с горячностью, ничем не оправданною, и потому очень удивившею офицеров.
– И как вы можете судить, что было бы лучше! – закричал он с лицом, вдруг налившимся кровью. – Как вы можете судить о поступках государя, какое мы имеем право рассуждать?! Мы не можем понять ни цели, ни поступков государя!
– Да я ни слова не говорил о государе, – оправдывался офицер, не могший иначе как тем, что Ростов пьян, объяснить себе его вспыльчивости.
Но Ростов не слушал.
– Мы не чиновники дипломатические, а мы солдаты и больше ничего, – продолжал он. – Умирать велят нам – так умирать. А коли наказывают, так значит – виноват; не нам судить. Угодно государю императору признать Бонапарте императором и заключить с ним союз – значит так надо. А то, коли бы мы стали обо всем судить да рассуждать, так этак ничего святого не останется. Этак мы скажем, что ни Бога нет, ничего нет, – ударяя по столу кричал Николай, весьма некстати, по понятиям своих собеседников, но весьма последовательно по ходу своих мыслей.
– Наше дело исполнять свой долг, рубиться и не думать, вот и всё, – заключил он.
– И пить, – сказал один из офицеров, не желавший ссориться.
– Да, и пить, – подхватил Николай. – Эй ты! Еще бутылку! – крикнул он.
В 1808 году император Александр ездил в Эрфурт для нового свидания с императором Наполеоном, и в высшем Петербургском обществе много говорили о величии этого торжественного свидания.
В 1809 году близость двух властелинов мира, как называли Наполеона и Александра, дошла до того, что, когда Наполеон объявил в этом году войну Австрии, то русский корпус выступил за границу для содействия своему прежнему врагу Бонапарте против прежнего союзника, австрийского императора; до того, что в высшем свете говорили о возможности брака между Наполеоном и одной из сестер императора Александра. Но, кроме внешних политических соображений, в это время внимание русского общества с особенной живостью обращено было на внутренние преобразования, которые были производимы в это время во всех частях государственного управления.
Жизнь между тем, настоящая жизнь людей с своими существенными интересами здоровья, болезни, труда, отдыха, с своими интересами мысли, науки, поэзии, музыки, любви, дружбы, ненависти, страстей, шла как и всегда независимо и вне политической близости или вражды с Наполеоном Бонапарте, и вне всех возможных преобразований.
Князь Андрей безвыездно прожил два года в деревне. Все те предприятия по именьям, которые затеял у себя Пьер и не довел ни до какого результата, беспрестанно переходя от одного дела к другому, все эти предприятия, без выказыванья их кому бы то ни было и без заметного труда, были исполнены князем Андреем.
Он имел в высшей степени ту недостававшую Пьеру практическую цепкость, которая без размахов и усилий с его стороны давала движение делу.
Одно именье его в триста душ крестьян было перечислено в вольные хлебопашцы (это был один из первых примеров в России), в других барщина заменена оброком. В Богучарово была выписана на его счет ученая бабка для помощи родильницам, и священник за жалованье обучал детей крестьянских и дворовых грамоте.
Одну половину времени князь Андрей проводил в Лысых Горах с отцом и сыном, который был еще у нянек; другую половину времени в богучаровской обители, как называл отец его деревню. Несмотря на выказанное им Пьеру равнодушие ко всем внешним событиям мира, он усердно следил за ними, получал много книг, и к удивлению своему замечал, когда к нему или к отцу его приезжали люди свежие из Петербурга, из самого водоворота жизни, что эти люди, в знании всего совершающегося во внешней и внутренней политике, далеко отстали от него, сидящего безвыездно в деревне.
Кроме занятий по именьям, кроме общих занятий чтением самых разнообразных книг, князь Андрей занимался в это время критическим разбором наших двух последних несчастных кампаний и составлением проекта об изменении наших военных уставов и постановлений.
Весною 1809 года, князь Андрей поехал в рязанские именья своего сына, которого он был опекуном.
Пригреваемый весенним солнцем, он сидел в коляске, поглядывая на первую траву, первые листья березы и первые клубы белых весенних облаков, разбегавшихся по яркой синеве неба. Он ни о чем не думал, а весело и бессмысленно смотрел по сторонам.
Проехали перевоз, на котором он год тому назад говорил с Пьером. Проехали грязную деревню, гумны, зеленя, спуск, с оставшимся снегом у моста, подъём по размытой глине, полосы жнивья и зеленеющего кое где кустарника и въехали в березовый лес по обеим сторонам дороги. В лесу было почти жарко, ветру не слышно было. Береза вся обсеянная зелеными клейкими листьями, не шевелилась и из под прошлогодних листьев, поднимая их, вылезала зеленея первая трава и лиловые цветы. Рассыпанные кое где по березнику мелкие ели своей грубой вечной зеленью неприятно напоминали о зиме. Лошади зафыркали, въехав в лес и виднее запотели.
Лакей Петр что то сказал кучеру, кучер утвердительно ответил. Но видно Петру мало было сочувствования кучера: он повернулся на козлах к барину.
– Ваше сиятельство, лёгко как! – сказал он, почтительно улыбаясь.
– Что!
– Лёгко, ваше сиятельство.
«Что он говорит?» подумал князь Андрей. «Да, об весне верно, подумал он, оглядываясь по сторонам. И то зелено всё уже… как скоро! И береза, и черемуха, и ольха уж начинает… А дуб и не заметно. Да, вот он, дуб».
На краю дороги стоял дуб. Вероятно в десять раз старше берез, составлявших лес, он был в десять раз толще и в два раза выше каждой березы. Это был огромный в два обхвата дуб с обломанными, давно видно, суками и с обломанной корой, заросшей старыми болячками. С огромными своими неуклюжими, несимметрично растопыренными, корявыми руками и пальцами, он старым, сердитым и презрительным уродом стоял между улыбающимися березами. Только он один не хотел подчиняться обаянию весны и не хотел видеть ни весны, ни солнца.
«Весна, и любовь, и счастие!» – как будто говорил этот дуб, – «и как не надоест вам всё один и тот же глупый и бессмысленный обман. Всё одно и то же, и всё обман! Нет ни весны, ни солнца, ни счастия. Вон смотрите, сидят задавленные мертвые ели, всегда одинакие, и вон и я растопырил свои обломанные, ободранные пальцы, где ни выросли они – из спины, из боков; как выросли – так и стою, и не верю вашим надеждам и обманам».
Князь Андрей несколько раз оглянулся на этот дуб, проезжая по лесу, как будто он чего то ждал от него. Цветы и трава были и под дубом, но он всё так же, хмурясь, неподвижно, уродливо и упорно, стоял посреди их.
«Да, он прав, тысячу раз прав этот дуб, думал князь Андрей, пускай другие, молодые, вновь поддаются на этот обман, а мы знаем жизнь, – наша жизнь кончена!» Целый новый ряд мыслей безнадежных, но грустно приятных в связи с этим дубом, возник в душе князя Андрея. Во время этого путешествия он как будто вновь обдумал всю свою жизнь, и пришел к тому же прежнему успокоительному и безнадежному заключению, что ему начинать ничего было не надо, что он должен доживать свою жизнь, не делая зла, не тревожась и ничего не желая.
По опекунским делам рязанского именья, князю Андрею надо было видеться с уездным предводителем. Предводителем был граф Илья Андреич Ростов, и князь Андрей в середине мая поехал к нему.
Был уже жаркий период весны. Лес уже весь оделся, была пыль и было так жарко, что проезжая мимо воды, хотелось купаться.
Князь Андрей, невеселый и озабоченный соображениями о том, что и что ему нужно о делах спросить у предводителя, подъезжал по аллее сада к отрадненскому дому Ростовых. Вправо из за деревьев он услыхал женский, веселый крик, и увидал бегущую на перерез его коляски толпу девушек. Впереди других ближе, подбегала к коляске черноволосая, очень тоненькая, странно тоненькая, черноглазая девушка в желтом ситцевом платье, повязанная белым носовым платком, из под которого выбивались пряди расчесавшихся волос. Девушка что то кричала, но узнав чужого, не взглянув на него, со смехом побежала назад.
Князю Андрею вдруг стало от чего то больно. День был так хорош, солнце так ярко, кругом всё так весело; а эта тоненькая и хорошенькая девушка не знала и не хотела знать про его существование и была довольна, и счастлива какой то своей отдельной, – верно глупой – но веселой и счастливой жизнию. «Чему она так рада? о чем она думает! Не об уставе военном, не об устройстве рязанских оброчных. О чем она думает? И чем она счастлива?» невольно с любопытством спрашивал себя князь Андрей.
Граф Илья Андреич в 1809 м году жил в Отрадном всё так же как и прежде, то есть принимая почти всю губернию, с охотами, театрами, обедами и музыкантами. Он, как всякому новому гостю, был рад князю Андрею, и почти насильно оставил его ночевать.
В продолжение скучного дня, во время которого князя Андрея занимали старшие хозяева и почетнейшие из гостей, которыми по случаю приближающихся именин был полон дом старого графа, Болконский несколько раз взглядывая на Наташу чему то смеявшуюся и веселившуюся между другой молодой половиной общества, всё спрашивал себя: «о чем она думает? Чему она так рада!».
wiki-org.ru
Лейкотриены — Википедия
Лейкотрие́ны — органические соединения, группа липидных высокоактивных веществ, образующаяся в организме из арахидоновой кислоты, содержащей 20-членную углеродную цепь. Подкласс лейкотриенов, вместе с простаноидами, входит в класс эйкозаноидов. Один из основных эффектов лейкотриенов — бронхоспазм — лежит в основе патогенеза бронхиальной астмы.
История
В 1938 году Киллвэй и Фелдберг, при исследовании воздействия яда кобры на лёгкие морских свинок, случайно обнаружили в лёгочном перфузате неизвестное ранее вещество, обладающее бронхоконстрикторным действием. Бронхоспазм, развивавшийся под воздействием этого неизвестного вещества, отличался от вызванной гистамином бронхоспастической реакции медленным развитием и большей продолжительностью. В связи с этим учёные назвали это вещество медленнореагирующей субстанцией анафилаксии (сокращенно МРСА, англ. slow reacting substance).
В 1960 году Броклхёрст выделил МРСА из лёгочной ткани больного бронхиальной астмой после проведения ингаляционной провокации с аллергеном. Этим исследованием он подтвердил, что МРСА обладает выраженным бронхоконстрикторным действием и является важным медиатором в развитии аллергического воспаления у больных БА.
В конце 1970-х годов была расшифрована структура молекулы МРСА. В исследованиях Бенгта Самуэльсона и его сотрудников было показано, что МРСА представляет собой неоднородную химическую структуру, относящуюся к семейству липидных медиаторов. Впервые эти медиаторы были выделены из лейкоцитов и характеризовались наличием конъюгированной триеновой структуры. В связи с этим выделенные вещества были названы «лейкотриенами» (ЛТ).
В настоящее время идентифицированы ЛТА4, ЛТВ4, ЛТС4, ЛТD4, ЛТE4, ЛТF4. Среди них выделяют 2 подгруппы лейкотриенов: к первой относят ЛТC4, ЛТD4, ЛТE4 и ЛТF4, они содержат в боковой цепи пептидные остатки, ко второй относят ЛТВ4, имеющий другое строение.
Синтез
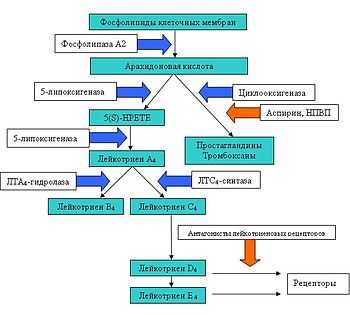 Метаболизм арахидоновой кислоты. Синие стрелки — участие фермента, красные стрелки — блокирование
Метаболизм арахидоновой кислоты. Синие стрелки — участие фермента, красные стрелки — блокированиеКак было сказано выше, лейкотриены образуются из арахидоновой кислоты, которая, в свою очередь, отщепляется от фосфолипидов цитоплазматической мембраны, с помощью фермента фосфолипаза A2.
Далее арахидоновая кислота может трансформироваться двумя путями: под влиянием ЦОГ она превращается в простаноиды, а под влиянием липоксигеназной ферментной системы в лейкотриены.
Липоксигеназная ферментная система относится к растворимым цитозольным ферментам, они обнаружены в цитоплазме альвеолярных макрофагах, тромбоцитах, тучных клетках и лейкоцитах. Наиболее важным среди ферментов этой системы является 5-липоксигеназа (5-ЛОГ). Активация перечисленных клеток приводит к перемещению 5-ЛОГ к мембране ядерного аппарата и связыванию со специфическим белком — 5-ЛОГ-активирующим протеином (5-ЛОГ-АП). 5-ЛОГ-АП является кофактором при взаимодействии арахидоновой кислоты и 5-ЛОГ. Таким образом, арахидоновая кислота под воздействием комплекса 5-ЛОГ + 5-ЛОГ-АП превращается в нестабильное соединение 5-гидропероксиэйкозатетраеновую кислоту (5-HPETE), из которой в свою очередь образуется ЛТА4. Обе эти реакции катализируются активированной 5-ЛОГ, расположенной на перинуклеарной мембране.
Далее ЛТА4 может превращаться двумя путями: либо при участии цитозольного фермента ЛТА4-гидролазы в ЛТВ4, либо под воздействием ЛТС4-синтетазы с образованием цисЛТС4. ЛТС4 выходит во внеклеточное пространство и далее с помощью g-глутамилтрансептидазы превращается в ЛТD4, который затем под влиянием дипептидазы образует ЛТЕ4. ЛТЕ4 является субстратом для образования ЛТF4.
Химическое строение
Лейкотриены являются производными арахидоновой кислоты. Последняя является полиненасыщенной кислотой, содержащей 20 атомов углерода, из которых 1-й входит в состав карбоксильной группы (-COOH). Молекула арахидоновой кислоты также содержит 4 двойные связи: первая расположена между 5 и 6 атомом углерода (счет их ведется от -COOH), вторая — между 8 и 9, третья — между 11 и 12, четвёртая — между 14 и 15.
Известно 6 типов лейкотриенов — А, В, С, D, Е и F. Их объединяет — с точки зрения химического строения — наличие карбоксильной группы, общее число атомов углерода в основной цепочке (20) и наличие 4 двойных связей (поэтому после написания названия лейкотриена, указывают индекс 4). Тем не менее, каждая молекула лейкотриенов имеет свои особенности:
- ЛТА4 — его 4 двойные связи расположены следующим образом: первая — между 7 и 8 атомом углерода, вторая — между 9 и 10, третья — между 11 и 12, четвёртая — между 14 и 15. Кроме того, к 5 и 6 атомам углерода присоединяется одна эпоксидная группа.
- ЛТВ4 — его 4 двойные связи расположены иначе: первая — между 6 и 7 атомом углерода, вторая — между 8 и 9, третья — между 10 и 11, четвёртая — между 14 и 15. Кроме того, к 5 и 13 атомам углерода присоединяются гидроксильные группы.
- ЛТС4 — также отличается расположением 4 двойных связей: первая — между 7 и 8 атомом углерода, вторая — между 9 и 10, третья — между 11 и 12, четвёртая — между 13 и 14. Кроме того, к 5-му атому углерода присоединяются гидроксильная группа, а к шестому глутатион, через сульфидную группу цистеина.
- ЛТD4 — очень похож на лейкотриен С4, но он образуется при отщеплении от глутатиона одной аминокислоты — глутамата. Поэтому его боковая пептидная цепочка именуется цистеинилглицином.
- ЛТE4 — образутся из ЛТD4, после того как его пептидная цепь лишается ещё одной аминокислоты — глицина.
- ЛТF4 — очень похож на лейкотриен С4, но он образуется при отщеплении от глутатиона глицина. Поэтому его боковая пептидная цепочка именуется γ-глутамилцистеином).[1]
Таким образом, по химическому строению, можно выделить две группы лейкотриенов:
- 1 группа — «пептидные (цистеиновые) лейкотриены», к ним относят ЛТС4, ЛТD4, ЛТЕ4, ЛТF4.
- 2 группа — лейкотриены, без пептидов: ЛТА4, ЛТВ4.
Роль в организме
Лейкотриеновые рецепторы
Выделяют три основных типа рецепторов лейкотриенов.[2] Причём два из них модулируются «пептидными лейкотриенами»:
- «Пептидные лейкотриены» модулируют специфические рецепторы, сопряженные с G-белком. Их обозначают CysLT-R. В настоящее время выделяют 2 типа CysLT. Взаимодействие лейкотриенов с рецепторами 1 типа (CysLT1) определяет спектр их основных эффектов (бронхоспазм). Связывание ЛТ с рецепторами 2 типа (CysLT2) изменяет тонус и проницаемость сосудов.
- Лейкотриен B4 модулирует другой тип рецепторов — BLT1- и BLT2-рецепторы (другое название LTB4-рецепторы).
Основные эффекты
- ЛТB4 — опосредует хемотаксис, экссудацию плазмы, сокращение паренхимы лёгких, участие в иммунных ответах.
- ЛТC4, ЛТD4, ЛТE4 являются основными компонентами МРСА, поэтому в первую очередь эта группа лейкотриенов относится к мощным бронхоконстрикторам. Также эти лейкотриены способны повышать тонус гладких мышц ЖКТ, опосредовать экссудацию плазмы и сокращение паренхимы лёгких.
Роль в патологии
- Лейкотриены участвуют в патогенезе бронхиальной астмы. Вместе с гистамином лейкотриены относятся к медиаторам ранней фазы аллергической реакции немедленного типа. В результате действия гистамина возникает мгновенный и кратковременный бронхоспазм, лейкотриены же вызывают отсроченный и более длительный бронхоспазм.
- Лейкотриены вызывают очень неприятный аспириновый бронхоспазм, возникающий при приёме неселективных НПВС: аспирин и др.[3] Аспириновый бронхоспазм порождается следующим образом: ЦОГ, которую ингибируют НПВС, катализирует реакцию превращения арахидоновой кислоты в циклический эндопероксид ПГ h3. Это ведёт к тому, что синтез ПГ резко уменьшается, а на этом фоне преобладающими станут лейкотриены. Однако, активность фосфолипазы A2 остаётся неизменной, соответственно арахидоновой кислоты отщепляется от фосфолипидов цитоплазматической мембраны столько же, сколько и в норме. Если в физиологических условиях арахидоновая кислота равномерно распределялась, поступая на синтез и ПГ и ЛТ, то при ингибировании ЦОГ, она целиком и полностью будет поступать на синтез лейкотриенов. Таким образом, при использовании неселективных НПВС, в тканях человека будет не просто вакатное (лат. vacuus — пустой) преобладание ЛТ, но они будут синтезироваться интенсивнее, чем в норме. ЛТC4, ЛТD4, ЛТE4 входят в комплекс МРСА, которая порождает бронхоспазм.
Возможности фармакологической коррекции эффектов
- В настоящее время разработаны и успешно используются антагонисты CysL-R1: монтелукаст, зафирлукаст и пранлукаст (последний не зарегистрирован в РФ). Препараты могут использоваться в виде монотерапии у больных лёгкой персистирующей бронхиальной астмой. У больных со среднетяжёлым и тяжёлым течением заболевания антагонисты CysLT-R1 используют в качестве дополнительной терапии в комбинации с ингаляционными глюкокортикоидами (ИГКС) с целью уменьшения дозы ИГКС и достижения полного контроля астмы. Отмечено также их положительное влияние на течение аспириновой БА у больных с непереносимостью нестероидных противовоспалительных препаратов.
- Созданы ингибиторы биосинтеза лейкотриенов, подавляющие активность фермента 5-ЛОГ: зилеутон. Установлено, что этот препарат оказывает бронхорасширяющее действие (его начало в течение 2-х часов, продолжительность — 5 часов после приема) и предупреждает развитие бронхоспазма, вызываемого аспирином и холодным воздухом.
- В экспериментах созданы блокаторы 5-ЛОГ-активирующего протеина и рецепторов ЛТB4.
Таким образом, можно выделить 4 точки приложения препаратов:
- Прямые ингибиторы 5-ЛОГ (зилеутон, Z-D2138, АВТ-761),
- Ингибиторы 5-ЛОГ-АП предупреждающие связывание этого мембраносвязанного белка с арахидоновой кислотой (МК-0591, МК-886, BAYxl005 и др.),
- Антагонисты CysLT-R (зафирлукаст, монтелукаст, пранлукаст и др.),
- Антагонисты рецепторов лейкотриенов В4 (U-75, 302).[4]
Примечания
Ссылки
wikipedia.green
|
|
ЛЕЙКОТРИЕНЫ (LT), производные полиеновых к-т, содержащие в молекуле три сопряженные двойные связи, а также (наряду с др. заместителями) гидроксигруппу в положении 5 или эпоксигруппу в положении 5,6; выполняют ф-ции прир. биорегуляторов.
Известно 6 типов лейкотриенов — А, В, С, D, Е и F (см. ф-лы I-III, Glu — остаток глутаминовой к-ты, Gly — глицина).
Внутри каждого типа различают три серии лейкотриенов, отличающиеся числом двойных связей (обозначают цифрами 3,4, 5 или 6 в ниж. индексе — в зависимости от числа двойных связей). Большинство лейкотриенов — нестабильные соед., и, как правило, их можно охарактеризовать только в виде производных. Так, для метилового эфира LTA4 т. пл. 28-32 °С, [a]D20 -27° (гексан). Все лейкотриены имеют характерный УФ спектр с тремя максимумами поглощения, напр. для спектра LTB4 в метаноле lмакс 260 (e 3,8.104), 270,5 (e 5,0.104) и 281 нм (e 3,9.104), для LTC4lмакс 270 (e 3,2.104), 280 (с 4,0.104) и 290 нм (e 3,1.104) В организме животных обнаружены структурные изомеры лейкотриенов — т. наз. липотриeны (см., напр., ф-лу IV). В отличие от лейкотриенов они содержат гидроксигруппу в положении 15 или эпоксигруппу в положении 14, 15. Принципиально новый класс метаболитов эйкозаполиеновых к-т, родственных лейкотриенам, — липоксины, имеющие в молекуле 4 сопряженные двойные связи и 3 гидроксигруппы (V-VI). Серосодержащиe (пептидные) лейкотриены (LTC4 и др.) образуются в разл. нормальных и трансформированных клетках млекопитающих (лейкоцитах, моноцитах, макрофагах, в базофилах крыс, больных лейкемией и др.). Более широко распространены лейкотриены типов А и В. Они найдены не только у животных, но и в нек-рых растениях, напр. картофеле. Лейкотриены не накапливаются в тканях, а синтезируются в ответ на определенные стимулы. Они участвуют в воспалит. р-циях и являются медиаторами анафилаксии (аллергической р-ции немедленного типа, развивающейся в ответ на присутствие аллергена). Для пептидных лейкотриенов более характерно миотропное действие (сокращение гладкой мускулатуры желудочно-кишечного тракта, бронхов, паренхимы легких, кровеносных сосудов). LTB4 проявляет выраженное лейкотропное действие — вызывает агрегацию, хемотаксис (направленное движение) и хемокинезис (повышение подвижности) лейкоцитов — и является активным ионофором для Са2+. Установлено, что в ряде случаев физиол. действие лейкотриенов опосредовано их взаимодействием со специфич. рецепторами. Липоксины стимулируют хемотаксис лейкоцитов и агрегацию тромбоцитов. Биосинтез лейкотриенов, липотриенов и липоксинов осуществляется через промежут. реакционноспособные гидропероксиды (соотв. через 5- или 15-гидропероксиэйкозаполиеновые и 5,15-дигидропероксиэйкозаполиеновые к-ты), к-рые образуются в результате окисления эйкозаполиеновых к-т при участии 5- или (и) 15-лилооксигеназ. Моногидропероксиэйкозаполиеновые к-ты далее превращаются в нестабильный эпоксид типа А, из к-рого образуются лейкотриены др. типов. Осн. путь катаболизма лейкотриенов — их w-окисление с образованием 20-гидрокси- и 20-нор-19-карбоксипроизводных. В лаб. условиях лейкотриены получают из полиеновых к-т с использованием ферментативных р-ций или синтезируют с помощью р-ции Виттига, осуществляя конденсацию углеводородного и карбоксилсодержащего фрагментов. Для количеств. определения лейкотриенов обычно используют высокоэффективную жидкостную хроматографию и радиоиммунный анализ (используются меченные радиоактивными атомами антигены). Вследствие важной роли лейкотриенов в патогенезе таких заболеваний, как бронхиальная астма, проводится интенсивный поиск лек. ср-в, блокирующих биосинтез лейкотриенов или их рецепторов. === Исп. литература для статьи «ЛЕЙКОТРИЕНЫ»: Будницкая Е, В., «Успехи биологической химии», 1985, т. 26, с. 269-77; Евстигнеева Р. П.. Мягкова Г. И.. «Успехи химии». 1986. т. 55. в. 5. с. 843-78; Современные направления в органическом синтезе, пер. с англ., М.. 1986, с. 12-28; Leukotrienes and other lipoxygenase products, ed. by P. Samuelsson, R. Paoletti, N. Y.. 1982; Schewc Т., Rapoport S. M., Kuhn H., в сб.: Advances in enzymology and related areas of molecular biology, v. 58. 1986, p. 191-272; Kuhn H. [a. o.], «Europ. J. Biochem.». 1987, v. 169, № 3, p. 593-601. В. В. Безуглов. В. 3. Ланкин. Страница «ЛЕЙКОТРИЕНЫ» подготовлена по материалам химической энциклопедии. |

|
www.xumuk.ru
Лейкотриены — Википедия. Что такое Лейкотриены
Лейкотрие́ны — органические соединения, группа липидных высокоактивных веществ, образующаяся в организме из арахидоновой кислоты, содержащей 20-членную углеродную цепь. Подкласс лейкотриенов, вместе с простаноидами, входит в класс эйкозаноидов. Один из основных эффектов лейкотриенов — бронхоспазм — лежит в основе патогенеза бронхиальной астмы.
История
В 1938 году Киллвэй и Фелдберг, при исследовании воздействия яда кобры на лёгкие морских свинок, случайно обнаружили в лёгочном перфузате неизвестное ранее вещество, обладающее бронхоконстрикторным действием. Бронхоспазм, развивавшийся под воздействием этого неизвестного вещества, отличался от вызванной гистамином бронхоспастической реакции медленным развитием и большей продолжительностью. В связи с этим учёные назвали это вещество медленнореагирующей субстанцией анафилаксии (сокращенно МРСА, англ. slow reacting substance).
В 1960 году Броклхёрст выделил МРСА из лёгочной ткани больного бронхиальной астмой после проведения ингаляционной провокации с аллергеном. Этим исследованием он подтвердил, что МРСА обладает выраженным бронхоконстрикторным действием и является важным медиатором в развитии аллергического воспаления у больных БА.
В конце 1970-х годов была расшифрована структура молекулы МРСА. В исследованиях Бенгта Самуэльсона и его сотрудников было показано, что МРСА представляет собой неоднородную химическую структуру, относящуюся к семейству липидных медиаторов. Впервые эти медиаторы были выделены из лейкоцитов и характеризовались наличием конъюгированной триеновой структуры. В связи с этим выделенные вещества были названы «лейкотриенами» (ЛТ).
В настоящее время идентифицированы ЛТА4, ЛТВ4, ЛТС4, ЛТD4, ЛТE4, ЛТF4. Среди них выделяют 2 подгруппы лейкотриенов: к первой относят ЛТC4, ЛТD4, ЛТE4 и ЛТF4, они содержат в боковой цепи пептидные остатки, ко второй относят ЛТВ4, имеющий другое строение.
Синтез
 Метаболизм арахидоновой кислоты. Синие стрелки — участие фермента, красные стрелки — блокирование
Метаболизм арахидоновой кислоты. Синие стрелки — участие фермента, красные стрелки — блокированиеКак было сказано выше, лейкотриены образуются из арахидоновой кислоты, которая, в свою очередь, отщепляется от фосфолипидов цитоплазматической мембраны, с помощью фермента фосфолипаза A2.
Далее арахидоновая кислота может трансформироваться двумя путями: под влиянием ЦОГ она превращается в простаноиды, а под влиянием липоксигеназной ферментной системы в лейкотриены.
Липоксигеназная ферментная система относится к растворимым цитозольным ферментам, они обнаружены в цитоплазме альвеолярных макрофагах, тромбоцитах, тучных клетках и лейкоцитах. Наиболее важным среди ферментов этой системы является 5-липоксигеназа (5-ЛОГ). Активация перечисленных клеток приводит к перемещению 5-ЛОГ к мембране ядерного аппарата и связыванию со специфическим белком — 5-ЛОГ-активирующим протеином (5-ЛОГ-АП). 5-ЛОГ-АП является кофактором при взаимодействии арахидоновой кислоты и 5-ЛОГ. Таким образом, арахидоновая кислота под воздействием комплекса 5-ЛОГ + 5-ЛОГ-АП превращается в нестабильное соединение 5-гидропероксиэйкозатетраеновую кислоту (5-HPETE), из которой в свою очередь образуется ЛТА4. Обе эти реакции катализируются активированной 5-ЛОГ, расположенной на перинуклеарной мембране.
Далее ЛТА4 может превращаться двумя путями: либо при участии цитозольного фермента ЛТА4-гидролазы в ЛТВ4, либо под воздействием ЛТС4-синтетазы с образованием цисЛТС4. ЛТС4 выходит во внеклеточное пространство и далее с помощью g-глутамилтрансептидазы превращается в ЛТD4, который затем под влиянием дипептидазы образует ЛТЕ4. ЛТЕ4 является субстратом для образования ЛТF4.
Химическое строение
Лейкотриены являются производными арахидоновой кислоты. Последняя является полиненасыщенной кислотой, содержащей 20 атомов углерода, из которых 1-й входит в состав карбоксильной группы (-COOH). Молекула арахидоновой кислоты также содержит 4 двойные связи: первая расположена между 5 и 6 атомом углерода (счет их ведется от -COOH), вторая — между 8 и 9, третья — между 11 и 12, четвёртая — между 14 и 15.
Известно 6 типов лейкотриенов — А, В, С, D, Е и F. Их объединяет — с точки зрения химического строения — наличие карбоксильной группы, общее число атомов углерода в основной цепочке (20) и наличие 4 двойных связей (поэтому после написания названия лейкотриена, указывают индекс 4). Тем не менее, каждая молекула лейкотриенов имеет свои особенности:
- ЛТА4 — его 4 двойные связи расположены следующим образом: первая — между 7 и 8 атомом углерода, вторая — между 9 и 10, третья — между 11 и 12, четвёртая — между 14 и 15. Кроме того, к 5 и 6 атомам углерода присоединяется одна эпоксидная группа.
- ЛТВ4 — его 4 двойные связи расположены иначе: первая — между 6 и 7 атомом углерода, вторая — между 8 и 9, третья — между 10 и 11, четвёртая — между 14 и 15. Кроме того, к 5 и 13 атомам углерода присоединяются гидроксильные группы.
- ЛТС4 — также отличается расположением 4 двойных связей: первая — между 7 и 8 атомом углерода, вторая — между 9 и 10, третья — между 11 и 12, четвёртая — между 13 и 14. Кроме того, к 5-му атому углерода присоединяются гидроксильная группа, а к шестому глутатион, через сульфидную группу цистеина.
- ЛТD4 — очень похож на лейкотриен С4, но он образуется при отщеплении от глутатиона одной аминокислоты — глутамата. Поэтому его боковая пептидная цепочка именуется цистеинилглицином.
- ЛТE4 — образутся из ЛТD4, после того как его пептидная цепь лишается ещё одной аминокислоты — глицина.
- ЛТF4 — очень похож на лейкотриен С4, но он образуется при отщеплении от глутатиона глицина. Поэтому его боковая пептидная цепочка именуется γ-глутамилцистеином).[1]
Таким образом, по химическому строению, можно выделить две группы лейкотриенов:
- 1 группа — «пептидные (цистеиновые) лейкотриены», к ним относят ЛТС4, ЛТD4, ЛТЕ4, ЛТF4.
- 2 группа — лейкотриены, без пептидов: ЛТА4, ЛТВ4.
Роль в организме
Лейкотриеновые рецепторы
Выделяют три основных типа рецепторов лейкотриенов.[2] Причём два из них модулируются «пептидными лейкотриенами»:
- «Пептидные лейкотриены» модулируют специфические рецепторы, сопряженные с G-белком. Их обозначают CysLT-R. В настоящее время выделяют 2 типа CysLT. Взаимодействие лейкотриенов с рецепторами 1 типа (CysLT1) определяет спектр их основных эффектов (бронхоспазм). Связывание ЛТ с рецепторами 2 типа (CysLT2) изменяет тонус и проницаемость сосудов.
- Лейкотриен B4 модулирует другой тип рецепторов — BLT1- и BLT2-рецепторы (другое название LTB4-рецепторы).
Основные эффекты
- ЛТB4 — опосредует хемотаксис, экссудацию плазмы, сокращение паренхимы лёгких, участие в иммунных ответах.
- ЛТC4, ЛТD4, ЛТE4 являются основными компонентами МРСА, поэтому в первую очередь эта группа лейкотриенов относится к мощным бронхоконстрикторам. Также эти лейкотриены способны повышать тонус гладких мышц ЖКТ, опосредовать экссудацию плазмы и сокращение паренхимы лёгких.
Роль в патологии
- Лейкотриены участвуют в патогенезе бронхиальной астмы. Вместе с гистамином лейкотриены относятся к медиаторам ранней фазы аллергической реакции немедленного типа. В результате действия гистамина возникает мгновенный и кратковременный бронхоспазм, лейкотриены же вызывают отсроченный и более длительный бронхоспазм.
- Лейкотриены вызывают очень неприятный аспириновый бронхоспазм, возникающий при приёме неселективных НПВС: аспирин и др.[3] Аспириновый бронхоспазм порождается следующим образом: ЦОГ, которую ингибируют НПВС, катализирует реакцию превращения арахидоновой кислоты в циклический эндопероксид ПГ h3. Это ведёт к тому, что синтез ПГ резко уменьшается, а на этом фоне преобладающими станут лейкотриены. Однако, активность фосфолипазы A2 остаётся неизменной, соответственно арахидоновой кислоты отщепляется от фосфолипидов цитоплазматической мембраны столько же, сколько и в норме. Если в физиологических условиях арахидоновая кислота равномерно распределялась, поступая на синтез и ПГ и ЛТ, то при ингибировании ЦОГ, она целиком и полностью будет поступать на синтез лейкотриенов. Таким образом, при использовании неселективных НПВС, в тканях человека будет не просто вакатное (лат. vacuus — пустой) преобладание ЛТ, но они будут синтезироваться интенсивнее, чем в норме. ЛТC4, ЛТD4, ЛТE4 входят в комплекс МРСА, которая порождает бронхоспазм.
Возможности фармакологической коррекции эффектов
- В настоящее время разработаны и успешно используются антагонисты CysL-R1: монтелукаст, зафирлукаст и пранлукаст (последний не зарегистрирован в РФ). Препараты могут использоваться в виде монотерапии у больных лёгкой персистирующей бронхиальной астмой. У больных со среднетяжёлым и тяжёлым течением заболевания антагонисты CysLT-R1 используют в качестве дополнительной терапии в комбинации с ингаляционными глюкокортикоидами (ИГКС) с целью уменьшения дозы ИГКС и достижения полного контроля астмы. Отмечено также их положительное влияние на течение аспириновой БА у больных с непереносимостью нестероидных противовоспалительных препаратов.
- Созданы ингибиторы биосинтеза лейкотриенов, подавляющие активность фермента 5-ЛОГ: зилеутон. Установлено, что этот препарат оказывает бронхорасширяющее действие (его начало в течение 2-х часов, продолжительность — 5 часов после приема) и предупреждает развитие бронхоспазма, вызываемого аспирином и холодным воздухом.
- В экспериментах созданы блокаторы 5-ЛОГ-активирующего протеина и рецепторов ЛТB4.
Таким образом, можно выделить 4 точки приложения препаратов:
- Прямые ингибиторы 5-ЛОГ (зилеутон, Z-D2138, АВТ-761),
- Ингибиторы 5-ЛОГ-АП предупреждающие связывание этого мембраносвязанного белка с арахидоновой кислотой (МК-0591, МК-886, BAYxl005 и др.),
- Антагонисты CysLT-R (зафирлукаст, монтелукаст, пранлукаст и др.),
- Антагонисты рецепторов лейкотриенов В4 (U-75, 302).[4]
Примечания
Ссылки
wiki.sc
Лейкотриен Википедия
Лейкотрие́ны — органические соединения, группа липидных высокоактивных веществ, образующаяся в организме из арахидоновой кислоты, содержащей 20-членную углеродную цепь. Подкласс лейкотриенов, вместе с простаноидами, входит в класс эйкозаноидов. Один из основных эффектов лейкотриенов — бронхоспазм — лежит в основе патогенеза бронхиальной астмы.
История
В 1938 году Киллвэй и Фелдберг, при исследовании воздействия яда кобры на лёгкие морских свинок, случайно обнаружили в лёгочном перфузате неизвестное ранее вещество, обладающее бронхоконстрикторным действием. Бронхоспазм, развивавшийся под воздействием этого неизвестного вещества, отличался от вызванной гистамином бронхоспастической реакции медленным развитием и большей продолжительностью. В связи с этим учёные назвали это вещество медленнореагирующей субстанцией анафилаксии (сокращенно МРСА, англ. slow reacting substance).
В 1960 году Броклхёрст выделил МРСА из лёгочной ткани больного бронхиальной астмой после проведения ингаляционной провокации с аллергеном. Этим исследованием он подтвердил, что МРСА обладает выраженным бронхоконстрикторным действием и является важным медиатором в развитии аллергического воспаления у больных БА.
В конце 1970-х годов была расшифрована структура молекулы МРСА. В исследованиях Бенгта Самуэльсона и его сотрудников было показано, что МРСА представляет собой неоднородную химическую структуру, относящуюся к семейству липидных медиаторов. Впервые эти медиаторы были выделены из лейкоцитов и характеризовались наличием конъюгированной триеновой структуры. В связи с этим выделенные вещества были названы «лейкотриенами» (ЛТ).
В настоящее время идентифицированы ЛТА4, ЛТВ4, ЛТС4, ЛТD4, ЛТE4, ЛТF4. Среди них выделяют 2 подгруппы лейкотриенов: к первой относят ЛТC4, ЛТD4, ЛТE4 и ЛТF4, они содержат в боковой цепи пептидные остатки, ко второй относят ЛТВ4, имеющий другое строение.
Синтез
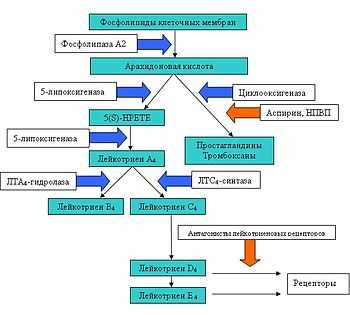 Метаболизм арахидоновой кислоты. Синие стрелки — участие фермента, красные стрелки — блокирование
Метаболизм арахидоновой кислоты. Синие стрелки — участие фермента, красные стрелки — блокированиеКак было сказано выше, лейкотриены образуются из арахидоновой кислоты, которая, в свою очередь, отщепляется от фосфолипидов цитоплазматической мембраны, с помощью фермента фосфолипаза A2.
Далее арахидоновая кислота может трансформироваться двумя путями: под влиянием ЦОГ она превращается в простаноиды, а под влиянием липоксигеназной ферментной системы в лейкотриены.
Липоксигеназная ферментная система относится к растворимым цитозольным ферментам, они обнаружены в цитоплазме альвеолярных макрофагах, тромбоцитах, тучных клетках и лейкоцитах. Наиболее важным среди ферментов этой системы является 5-липоксигеназа (5-ЛОГ). Активация перечисленных клеток приводит к перемещению 5-ЛОГ к мембране ядерного аппарата и связыванию со специфическим белком — 5-ЛОГ-активирующим протеином (5-ЛОГ-АП). 5-ЛОГ-АП является кофактором при взаимодействии арахидоновой кислоты и 5-ЛОГ. Таким образом, арахидоновая кислота под воздействием комплекса 5-ЛОГ + 5-ЛОГ-АП превращается в нестабильное соединение 5-гидропероксиэйкозатетраеновую кислоту (5-HPETE), из которой в свою очередь образуется ЛТА4. Обе эти реакции катализируются активированной 5-ЛОГ, расположенной на перинуклеарной мембране.
Далее ЛТА4 может превращаться двумя путями: либо при участии цитозольного фермента ЛТА4-гидролазы в ЛТВ4, либо под воздействием ЛТС4-синтетазы с образованием цисЛТС4. ЛТС4 выходит во внеклеточное пространство и далее с помощью g-глутамилтрансептидазы превращается в ЛТD4, который затем под влиянием дипептидазы образует ЛТЕ4. ЛТЕ4 является субстратом для образования ЛТF4.
Химическое строение
Лейкотриены являются производными арахидоновой кислоты. Последняя является полиненасыщенной кислотой, содержащей 20 атомов углерода, из которых 1-й входит в состав карбоксильной группы (-COOH). Молекула арахидоновой кислоты также содержит 4 двойные связи: первая расположена между 5 и 6 атомом углерода (счет их ведется от -COOH), вторая — между 8 и 9, третья — между 11 и 12, четвёртая — между 14 и 15.
Известно 6 типов лейкотриенов — А, В, С, D, Е и F. Их объединяет — с точки зрения химического строения — наличие карбоксильной группы, общее число атомов углерода в основной цепочке (20) и наличие 4 двойных связей (поэтому после написания названия лейкотриена, указывают индекс 4). Тем не менее, каждая молекула лейкотриенов имеет свои особенности:
- ЛТА4 — его 4 двойные связи расположены следующим образом: первая — между 7 и 8 атомом углерода, вторая — между 9 и 10, третья — между 11 и 12, четвёртая — между 14 и 15. Кроме того, к 5 и 6 атомам углерода присоединяется одна эпоксидная группа.
- ЛТВ4 — его 4 двойные связи расположены иначе: первая — между 6 и 7 атомом углерода, вторая — между 8 и 9, третья — между 10 и 11, четвёртая — между 14 и 15. Кроме того, к 5 и 13 атомам углерода присоединяются гидроксильные группы.
- ЛТС4 — также отличается расположением 4 двойных связей: первая — между 7 и 8 атомом углерода, вторая — между 9 и 10, третья — между 11 и 12, четвёртая — между 13 и 14. Кроме того, к 5-му атому углерода присоединяются гидроксильная группа, а к шестому глутатион, через сульфидную группу цистеина.
- ЛТD4 — очень похож на лейкотриен С4, но он образуется при отщеплении от глутатиона одной аминокислоты — глутамата. Поэтому его боковая пептидная цепочка именуется цистеинилглицином.
- ЛТE4 — образутся из ЛТD4, после того как его пептидная цепь лишается ещё одной аминокислоты — глицина.
- ЛТF4 — очень похож на лейкотриен С4, но он образуется при отщеплении от глутатиона глицина. Поэтому его боковая пептидная цепочка именуется γ-глутамилцистеином).[1]
Таким образом, по химическому строению, можно выделить две группы лейкотриенов:
- 1 группа — «пептидные (цистеиновые) лейкотриены», к ним относят ЛТС4, ЛТD4, ЛТЕ4, ЛТF4.
- 2 группа — лейкотриены, без пептидов: ЛТА4, ЛТВ4.
Роль в организме
Лейкотриеновые рецепторы
Выделяют три основных типа рецепторов лейкотриенов.[2] Причём два из них модулируются «пептидными лейкотриенами»:
- «Пептидные лейкотриены» модулируют специфические рецепторы, сопряженные с G-белком. Их обозначают CysLT-R. В настоящее время выделяют 2 типа CysLT. Взаимодействие лейкотриенов с рецепторами 1 типа (CysLT1) определяет спектр их основных эффектов (бронхоспазм). Связывание ЛТ с рецепторами 2 типа (CysLT2) изменяет тонус и проницаемость сосудов.
- Лейкотриен B4 модулирует другой тип рецепторов — BLT1- и BLT2-рецепторы (другое название LTB4-рецепторы).
Основные эффекты
- ЛТB4 — опосредует хемотаксис, экссудацию плазмы, сокращение паренхимы лёгких, участие в иммунных ответах.
- ЛТC4, ЛТD4, ЛТE4 являются основными компонентами МРСА, поэтому в первую очередь эта группа лейкотриенов относится к мощным бронхоконстрикторам. Также эти лейкотриены способны повышать тонус гладких мышц ЖКТ, опосредовать экссудацию плазмы и сокращение паренхимы лёгких.
Роль в патологии
- Лейкотриены участвуют в патогенезе бронхиальной астмы. Вместе с гистамином лейкотриены относятся к медиаторам ранней фазы аллергической реакции немедленного типа. В результате действия гистамина возникает мгновенный и кратковременный бронхоспазм, лейкотриены же вызывают отсроченный и более длительный бронхоспазм.
- Лейкотриены вызывают очень неприятный аспириновый бронхоспазм, возникающий при приёме неселективных НПВС: аспирин и др.[3] Аспириновый бронхоспазм порождается следующим образом: ЦОГ, которую ингибируют НПВС, катализирует реакцию превращения арахидоновой кислоты в циклический эндопероксид ПГ h3. Это ведёт к тому, что синтез ПГ резко уменьшается, а на этом фоне преобладающими станут лейкотриены. Однако, активность фосфолипазы A2 остаётся неизменной, соответственно арахидоновой кислоты отщепляется от фосфолипидов цитоплазматической мембраны столько же, сколько и в норме. Если в физиологических условиях арахидоновая кислота равномерно распределялась, поступая на синтез и ПГ и ЛТ, то при ингибировании ЦОГ, она целиком и полностью будет поступать на синтез лейкотриенов. Таким образом, при использовании неселективных НПВС, в тканях человека будет не просто вакатное (лат. vacuus — пустой) преобладание ЛТ, но они будут синтезироваться интенсивнее, чем в норме. ЛТC4, ЛТD4, ЛТE4 входят в комплекс МРСА, которая порождает бронхоспазм.
Возможности фармакологической коррекции эффектов
- В настоящее время разработаны и успешно используются антагонисты CysL-R1: монтелукаст, зафирлукаст и пранлукаст (последний не зарегистрирован в РФ). Препараты могут использоваться в виде монотерапии у больных лёгкой персистирующей бронхиальной астмой. У больных со среднетяжёлым и тяжёлым течением заболевания антагонисты CysLT-R1 используют в качестве дополнительной терапии в комбинации с ингаляционными глюкокортикоидами (ИГКС) с целью уменьшения дозы ИГКС и достижения полного контроля астмы. Отмечено также их положительное влияние на течение аспириновой БА у больных с непереносимостью нестероидных противовоспалительных препаратов.
- Созданы ингибиторы биосинтеза лейкотриенов, подавляющие активность фермента 5-ЛОГ: зилеутон. Установлено, что этот препарат оказывает бронхорасширяющее действие (его начало в течение 2-х часов, продолжительность — 5 часов после приема) и предупреждает развитие бронхоспазма, вызываемого аспирином и холодным воздухом.
- В экспериментах созданы блокаторы 5-ЛОГ-активирующего протеина и рецепторов ЛТB4.
Таким образом, можно выделить 4 точки приложения препаратов:
- Прямые ингибиторы 5-ЛОГ (зилеутон, Z-D2138, АВТ-761),
- Ингибиторы 5-ЛОГ-АП предупреждающие связывание этого мембраносвязанного белка с арахидоновой кислотой (МК-0591, МК-886, BAYxl005 и др.),
- Антагонисты CysLT-R (зафирлукаст, монтелукаст, пранлукаст и др.),
- Антагонисты рецепторов лейкотриенов В4 (U-75, 302).[4]
Примечания
Ссылки
wikiredia.ru
Лейкотриены — WiKi
История
В 1938 году Киллвэй и Фелдберг, при исследовании воздействия яда кобры на лёгкие морских свинок, случайно обнаружили в лёгочном перфузате неизвестное ранее вещество, обладающее бронхоконстрикторным действием. Бронхоспазм, развивавшийся под воздействием этого неизвестного вещества, отличался от вызванной гистамином бронхоспастической реакции медленным развитием и большей продолжительностью. В связи с этим учёные назвали это вещество медленнореагирующей субстанцией анафилаксии (сокращенно МРСА, англ. slow reacting substance).
В 1960 году Броклхёрст выделил МРСА из лёгочной ткани больного бронхиальной астмой после проведения ингаляционной провокации с аллергеном. Этим исследованием он подтвердил, что МРСА обладает выраженным бронхоконстрикторным действием и является важным медиатором в развитии аллергического воспаления у больных БА.
В конце 1970-х годов была расшифрована структура молекулы МРСА. В исследованиях Бенгта Самуэльсона и его сотрудников было показано, что МРСА представляет собой неоднородную химическую структуру, относящуюся к семейству липидных медиаторов. Впервые эти медиаторы были выделены из лейкоцитов и характеризовались наличием конъюгированной триеновой структуры. В связи с этим выделенные вещества были названы «лейкотриенами» (ЛТ).
В настоящее время идентифицированы ЛТА4, ЛТВ4, ЛТС4, ЛТD4, ЛТE4, ЛТF4. Среди них выделяют 2 подгруппы лейкотриенов: к первой относят ЛТC4, ЛТD4, ЛТE4 и ЛТF4, они содержат в боковой цепи пептидные остатки, ко второй относят ЛТВ4, имеющий другое строение.
Синтез
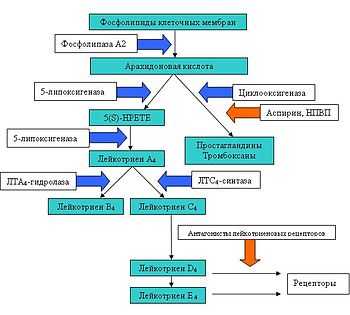 Метаболизм арахидоновой кислоты. Синие стрелки — участие фермента, красные стрелки — блокирование
Метаболизм арахидоновой кислоты. Синие стрелки — участие фермента, красные стрелки — блокированиеКак было сказано выше, лейкотриены образуются из арахидоновой кислоты, которая, в свою очередь, отщепляется от фосфолипидов цитоплазматической мембраны, с помощью фермента фосфолипаза A2.
Далее арахидоновая кислота может трансформироваться двумя путями: под влиянием ЦОГ она превращается в простаноиды, а под влиянием липоксигеназной ферментной системы в лейкотриены.
Липоксигеназная ферментная система относится к растворимым цитозольным ферментам, они обнаружены в цитоплазме альвеолярных макрофагах, тромбоцитах, тучных клетках и лейкоцитах. Наиболее важным среди ферментов этой системы является 5-липоксигеназа (5-ЛОГ). Активация перечисленных клеток приводит к перемещению 5-ЛОГ к мембране ядерного аппарата и связыванию со специфическим белком — 5-ЛОГ-активирующим протеином (5-ЛОГ-АП). 5-ЛОГ-АП является кофактором при взаимодействии арахидоновой кислоты и 5-ЛОГ. Таким образом, арахидоновая кислота под воздействием комплекса 5-ЛОГ + 5-ЛОГ-АП превращается в нестабильное соединение 5-гидропероксиэйкозатетраеновую кислоту (5-HPETE), из которой в свою очередь образуется ЛТА4. Обе эти реакции катализируются активированной 5-ЛОГ, расположенной на перинуклеарной мембране.
Далее ЛТА4 может превращаться двумя путями: либо при участии цитозольного фермента ЛТА4-гидролазы в ЛТВ4, либо под воздействием ЛТС4-синтетазы с образованием цисЛТС4. ЛТС4 выходит во внеклеточное пространство и далее с помощью g-глутамилтрансептидазы превращается в ЛТD4, который затем под влиянием дипептидазы образует ЛТЕ4. ЛТЕ4 является субстратом для образования ЛТF4.
Химическое строение
Лейкотриены являются производными арахидоновой кислоты. Последняя является полиненасыщенной кислотой, содержащей 20 атомов углерода, из которых 1-й входит в состав карбоксильной группы (-COOH). Молекула арахидоновой кислоты также содержит 4 двойные связи: первая расположена между 5 и 6 атомом углерода (счет их ведется от -COOH), вторая — между 8 и 9, третья — между 11 и 12, четвёртая — между 14 и 15.
Известно 6 типов лейкотриенов — А, В, С, D, Е и F. Их объединяет — с точки зрения химического строения — наличие карбоксильной группы, общее число атомов углерода в основной цепочке (20) и наличие 4 двойных связей (поэтому после написания названия лейкотриена, указывают индекс 4). Тем не менее, каждая молекула лейкотриенов имеет свои особенности:
- ЛТА4 — его 4 двойные связи расположены следующим образом: первая — между 7 и 8 атомом углерода, вторая — между 9 и 10, третья — между 11 и 12, четвёртая — между 14 и 15. Кроме того, к 5 и 6 атомам углерода присоединяется одна эпоксидная группа.
- ЛТВ4 — его 4 двойные связи расположены иначе: первая — между 6 и 7 атомом углерода, вторая — между 8 и 9, третья — между 10 и 11, четвёртая — между 14 и 15. Кроме того, к 5 и 13 атомам углерода присоединяются гидроксильные группы.
- ЛТС4 — также отличается расположением 4 двойных связей: первая — между 7 и 8 атомом углерода, вторая — между 9 и 10, третья — между 11 и 12, четвёртая — между 13 и 14. Кроме того, к 5-му атому углерода присоединяются гидроксильная группа, а к шестому глутатион, через сульфидную группу цистеина.
- ЛТD4 — очень похож на лейкотриен С4, но он образуется при отщеплении от глутатиона одной аминокислоты — глутамата. Поэтому его боковая пептидная цепочка именуется цистеинилглицином.
- ЛТE4 — образутся из ЛТD4, после того как его пептидная цепь лишается ещё одной аминокислоты — глицина.
- ЛТF4 — очень похож на лейкотриен С4, но он образуется при отщеплении от глутатиона глицина. Поэтому его боковая пептидная цепочка именуется γ-глутамилцистеином).[1]
Таким образом, по химическому строению, можно выделить две группы лейкотриенов:
- 1 группа — «пептидные (цистеиновые) лейкотриены», к ним относят ЛТС4, ЛТD4, ЛТЕ4, ЛТF4.
- 2 группа — лейкотриены, без пептидов: ЛТА4, ЛТВ4.
Роль в организме
Лейкотриеновые рецепторы
Выделяют три основных типа рецепторов лейкотриенов.[2] Причём два из них модулируются «пептидными лейкотриенами»:
- «Пептидные лейкотриены» модулируют специфические рецепторы, сопряженные с G-белком. Их обозначают CysLT-R. В настоящее время выделяют 2 типа CysLT. Взаимодействие лейкотриенов с рецепторами 1 типа (CysLT1) определяет спектр их основных эффектов (бронхоспазм). Связывание ЛТ с рецепторами 2 типа (CysLT2) изменяет тонус и проницаемость сосудов.
- Лейкотриен B4 модулирует другой тип рецепторов — BLT1- и BLT2-рецепторы (другое название LTB4-рецепторы).
Основные эффекты
- ЛТB4 — опосредует хемотаксис, экссудацию плазмы, сокращение паренхимы лёгких, участие в иммунных ответах.
- ЛТC4, ЛТD4, ЛТE4 являются основными компонентами МРСА, поэтому в первую очередь эта группа лейкотриенов относится к мощным бронхоконстрикторам. Также эти лейкотриены способны повышать тонус гладких мышц ЖКТ, опосредовать экссудацию плазмы и сокращение паренхимы лёгких.
Роль в патологии
- Лейкотриены участвуют в патогенезе бронхиальной астмы. Вместе с гистамином лейкотриены относятся к медиаторам ранней фазы аллергической реакции немедленного типа. В результате действия гистамина возникает мгновенный и кратковременный бронхоспазм, лейкотриены же вызывают отсроченный и более длительный бронхоспазм.
- Лейкотриены вызывают очень неприятный аспириновый бронхоспазм, возникающий при приёме неселективных НПВС: аспирин и др.[3] Аспириновый бронхоспазм порождается следующим образом: ЦОГ, которую ингибируют НПВС, катализирует реакцию превращения арахидоновой кислоты в циклический эндопероксид ПГ h3. Это ведёт к тому, что синтез ПГ резко уменьшается, а на этом фоне преобладающими станут лейкотриены. Однако, активность фосфолипазы A2 остаётся неизменной, соответственно арахидоновой кислоты отщепляется от фосфолипидов цитоплазматической мембраны столько же, сколько и в норме. Если в физиологических условиях арахидоновая кислота равномерно распределялась, поступая на синтез и ПГ и ЛТ, то при ингибировании ЦОГ, она целиком и полностью будет поступать на синтез лейкотриенов. Таким образом, при использовании неселективных НПВС, в тканях человека будет не просто вакатное (лат. vacuus — пустой) преобладание ЛТ, но они будут синтезироваться интенсивнее, чем в норме. ЛТC4, ЛТD4, ЛТE4 входят в комплекс МРСА, которая порождает бронхоспазм.
Возможности фармакологической коррекции эффектов
- В настоящее время разработаны и успешно используются антагонисты CysL-R1: монтелукаст, зафирлукаст и пранлукаст (последний не зарегистрирован в РФ). Препараты могут использоваться в виде монотерапии у больных лёгкой персистирующей бронхиальной астмой. У больных со среднетяжёлым и тяжёлым течением заболевания антагонисты CysLT-R1 используют в качестве дополнительной терапии в комбинации с ингаляционными глюкокортикоидами (ИГКС) с целью уменьшения дозы ИГКС и достижения полного контроля астмы. Отмечено также их положительное влияние на течение аспириновой БА у больных с непереносимостью нестероидных противовоспалительных препаратов.
- Созданы ингибиторы биосинтеза лейкотриенов, подавляющие активность фермента 5-ЛОГ: зилеутон. Установлено, что этот препарат оказывает бронхорасширяющее действие (его начало в течение 2-х часов, продолжительность — 5 часов после приема) и предупреждает развитие бронхоспазма, вызываемого аспирином и холодным воздухом.
- В экспериментах созданы блокаторы 5-ЛОГ-активирующего протеина и рецепторов ЛТB4.
Таким образом, можно выделить 4 точки приложения препаратов:
- Прямые ингибиторы 5-ЛОГ (зилеутон, Z-D2138, АВТ-761),
- Ингибиторы 5-ЛОГ-АП предупреждающие связывание этого мембраносвязанного белка с арахидоновой кислотой (МК-0591, МК-886, BAYxl005 и др.),
- Антагонисты CysLT-R (зафирлукаст, монтелукаст, пранлукаст и др.),
- Антагонисты рецепторов лейкотриенов В4 (U-75, 302).[4]
Примечания
Ссылки
ru-wiki.org
Лейкотриены
Для лейкоцитов характерен липооксигеназный путь метаболизма арахидоновой кислоты. Он приводит к образованию лейкотриенов, которые вызывают характерные для развития воспаления процессы. Поэтому лейкотриены называют медиаторами воспаления.
Они вызывают хемотаксис лейкоцитов, повышают проницаемость стенок сосудов и экссудацию плазмы, а также стимулируют сокращение гладких мышц бронхов, кровеносных сосудов и ЖКТ.
Оксид азота
В 1980 г. Американский ученый Роберт Фурхготт обнаружил, что эндотелий сосудов выделяет вещество, расслабляющее гладкую мускулатуру. Позже оказалось, что оно по своей химической природе является оксидом азота (NO), который в клетках образуется из аргинина в концентрациях достаточных для передачи сигналов на соседние структуры.
Гормональная функция оксида азота наиболее изучена в кровеносных сосудах. Здесь показано, что при отсутствии оксида азота ацетилхолин, брадикинин, гистамин, серотонин и многие другие БАВ не могут вызвать расширение сосудов. Эти вазодилятаторы стимулируют выработку эндотелием NO, но не оказывают прямого влияния на гладкие мышцы. Одна часть образовавшегося оксида азота быстро диффундирует в кровь и влияет на агрегацию тромбоцитов, а другая — подходит к гладкомышечным клеткам и вызывает местное расширение кровеносных сосудов.
Частная физиология эндокринной системы гормональная регуляция полового цикла у самок
Половые циклы проявляются периодически возникающими морфологическими и функциональными изменениями в организме половозрелой самки. При этом, наиболее типичные реакции наблюдаются в ее репродуктивных органах и поведении.
В первой половине цикла (фолликулярная фаза) в яичниках развиваются первичные фолликулы, а затем происходит овуляция (яйцеклетка выходит из наиболее активного вторичного фолликула). Оставшаяся после этого часть фолликула превращается в желтое тело (лютеиновая фаза цикла), а готовая к оплодотворению яйцеклетка перемещается в сторону матки. Физиологической причиной временного прерывания половых циклов в репродуктивном возрасте является наступление беременности. В регуляции перечисленных процессов активно участвуют гонадотропные гормоны гипофиза (ЛГ и ФСГ). От них зависит активность развития фолликулов и секреция стероидов в яичнике на всех стадиях полового цикла.
В фолликулярной фазе цикла ФСГ стимулирует развитие нескольких первичных фолликулов яичника и секрецию ими (в присутствии небольших концентраций ЛГ) эстрогенов и прогестинов (прогестерона и его производных). По мере созревания фолликулов, в крови растет концентрация эстрадиола, что тормозит образование ФСГ, но увеличивает чувствительность к нему наиболее зрелого фолликула. Остальные вторичные фолликулы после этого подвергаются атрезии, что делает концентрацию эстрадиола в крови минимальной и вызывает секрецию гипофизом такого количества гонадотропинов, которое стимулирует овуляцию.
Оставшаяся после овуляции часть фолликула превращается в желтое тело (начинается лютеиновая фаза цикла) и под действием ЛГ секретирует прогестерон. Наибольшая концентрация его в крови наблюдается при оплодотворении яйцеклетки. Поэтому своевременное обнаружение высокого уровня прогестерона в плазме позволяет исключить повторное (бесполезное или даже вредное) осеменение животных в ранние сроки наступившей беременности.
Если оплодотворение не произошло, секреция прогестерона уменьшается и происходит дальнейшее снижение уровня эстрадиола в крови, что стимулирует секрецию ФСГ и ЛГ и начинается новый половой цикл.
Таким образом, созревание фолликула и его овуляция регулируются обоими гонадотропинами аденогипофиза, а функция желтого тела находится преимущественно под влиянием одного ЛГ.
В фолликулярной фазе полового цикла эстрогены способствуют восстановлению отторгнутого слоя эндометрия, а в лютеиновой фазе — уже под влиянием прогестинов, эндометрий вырабатывает секрет, необходимый для имплантации оплодотворенной яйцеклетки (в этот период под влиянием прогестерона повышается температура тела).
Вторичный фолликул содержит пептидные гормоны, регулирующие созревание яйцеклетки, овуляцию и секреторную активность желтого тела. К ним относятся активины и ингибины. Эти вещества оказывают аутокринное и паракринное влияние на клетки самого фолликула (например, регулируют секрецию БАВ клетками граафова пузырька), а также оказывают эндокринное влияние на другие ткани (например, регулируют выделение ФСГ клетками аденогипофиза).
studfile.net
