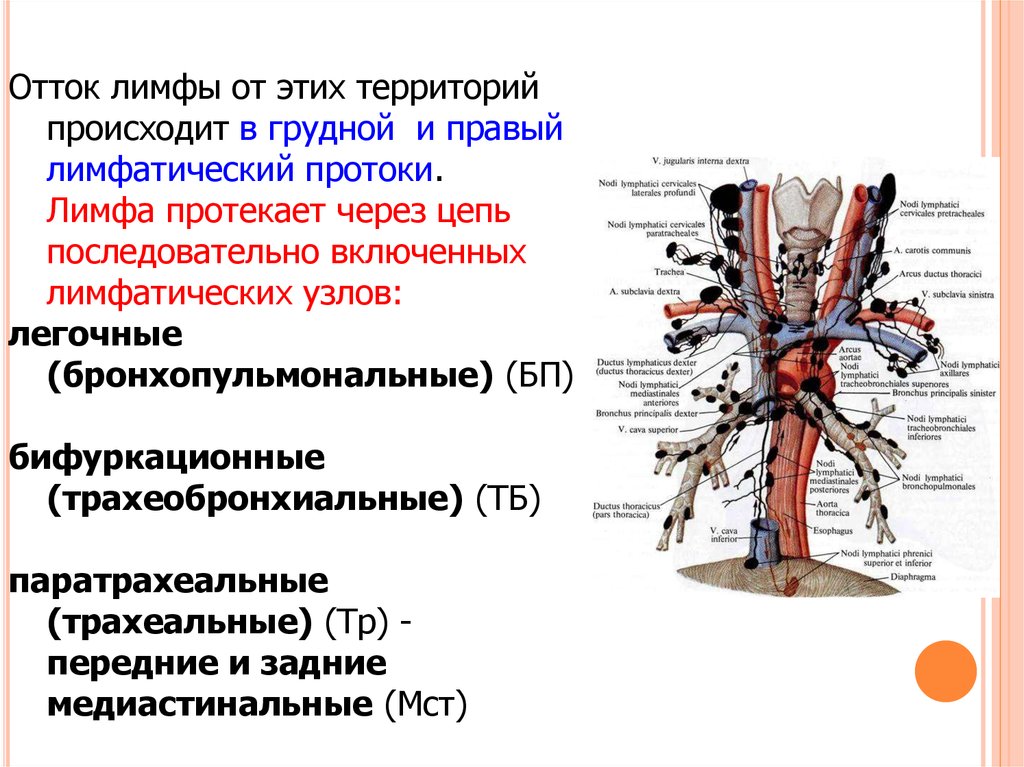
Неспецифические воспалительные заболевания дыхательных путей
Диагноз «неспецифическое воспалительное заболевание» встречается довольно часто, можно сказать: «на слуху». Что же кроется под этим обозначением? Какие заболевания входят в группу НПВЗ?
Бронхит
наиболее часто встречаемый воспалительный процесс в бронхах с острым или хроническим течением.
Причинами развития бронхита могут вирусная или бактериальная инфекция, хронический воспалительный процесс верхних дыхательных путей (носоглотка, гортань, трахея, ППН), загрязненный воздух (пыль, сажа, химические вещества).
В основе заболевания лежит нарушение дренажной функции бронхов, изменение количеств секрета в них, нарушение эвакуации и перистальтики, заполнения бронхов слизью.
Клинически проявляется кашлем с большим количеством мокроты разного, в зависимости от этиологии, характера, повышением температуры тела, отдышкой, интоксикацией.
Диагностика: на рентгенограммах высокого качества можно определить расширение бронхов, утолщение их стенок, Y-образные расширенные разветвления, на СКТ-сканах можно выявить наполненные и обтурированные слизью бронхи, и, как следствие, ателектаз долек.
Бронхиальная астма
это хроническое рецидивирующее аллергическое заболевание, которое характеризуется периодическими возникновениями отдышки, вызванной спазмом бронхов, гиперсекрецией и отеком слизистой оболочки.
По этиологии принято считать «виноватыми» бактериальные аллергены окружающей среды, пыль, холод, запахи, инфекционно-аллергические агенты (микроорганизмы и продукты их жизнедеятельности).
Клинически бронхиальная астма проявляется приступами отдышки, которые могут продолжаться до 3-7 суток: вздох короткий, сильный и глубокий, выдох – медленный судорожный, сопровождается свистящими хрипами. Лицо у больного одутловатое, бледное. Во время приступа отходит большое количество вязкой мокроты.
Лицо у больного одутловатое, бледное. Во время приступа отходит большое количество вязкой мокроты.
Диагностика: на рентген-снимках можно диагностировать эмфизему, зазубренность контура диафрагмы, низкое стояние куполов диафрагмы. При хроническом течении формируются устойчивые изменения в виде бочковидной деформации грудной клетки, фиброзной деформация легочного рисунка, распространенной эмфиземы легких, расширения артериальных сосудов в области корней легких. При помощи спиральной компьютерной томографии (СКТ) можно отчетливо дифференцировать утолщенные стенки бронхов, расширенные просветы бронхиального дерева, различные виды эмфиземы легких, изменение сосудистого рисунка, с преобладанием и усилением в прикорневых отделах, ослаблением в кортикальных.
Фиброзирующие альвеолиты
К этой группе относятся различные нозологические формы, которые возникают вследствие проникновения в организм повреждающих агентов, вызывающих идиопатические, аллергические или токсические альвеолиты. Данная группа заболеваний распространена среди работников сельского хозяйства, в текстильной, швейной, химической и фармацевтической промышленности.
Данная группа заболеваний распространена среди работников сельского хозяйства, в текстильной, швейной, химической и фармацевтической промышленности.
Заболевания характеризуются тремя взаимосвязанными процессами: отек, воспаление, фиброз.
Клинически у больных отмечается развитие отдышки кашель, повышение температуры тела, боль в грудной клетке, постепенная потеря веса. Течение может быть острым (6мес-2 года) и хроническим (6-8 лет) с периодическими рецидивами.
Диагностика: на рентген снимках отмечается усиление и сетчатая деформация легочного рисунка, нечеткая очерченность сосудов и бронхов, местами определяются участки вздутия и коллапса легких, далее присоединяются грубые фиброзные изменения легких и плевры, которая визуализируется в виде перибронхиальной, периваскулярной фиброзной тяжистости, множественные пузыревидные вздутия в кортикальных отделах легких (сотовое легкое). На ранних стадиях при помощи спиральной компьютерной томографии (СКТ) можно определить степень и протяженность фиброзно-кистозных дегенеративных изменений легочной паренхимы и мелкие очаги в периферических отделах легких.
Пневмония
принадлежит к наиболее распространенным заболеваниям легких. Патологический процесс локализуется в бронхах, бронхиолах, альвеолярной паренхиме, соединительной ткани. Различают первичную и вторичную пневмонию. Чаще всего причиной развития первичной пневмонии является бактериальная инфекция. Патологическими агентами может быть пневмококк, стафилококк, палочка Фридлендера, синегнойная и кишечная палочки, прочее. На ряду с бактериальной пневмонией также существует и опасность возникновения вирусной пневмонии (гриппозная, аденовирусная, орнитозная), рикетсиозной пневмонии, паразитарной, грибковой и других видов. Вторичная пневмония развивается в следствие имеющихся инфекционных заболеваний (коклюш, корь, тиф, сифилис) или при наличие гнойных очагов (фурункул, абсцесс, остеомиелит).
Клинически пневмония чаще всего возникает неожиданно, на фоне повышения температуры тела до 39 градусов, сопровождается головной болью, болью в груди, которая усиливается во время дыхания, кашля.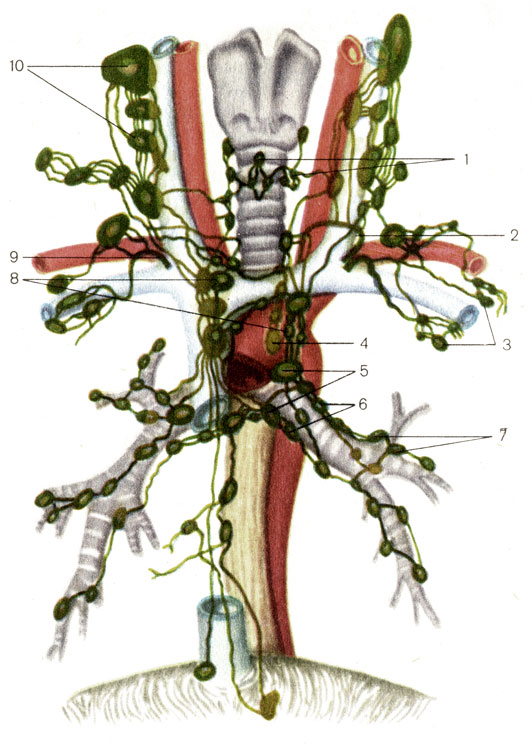
Диагностика: на рентген-снимке определяется частичная локализованная или разлитая (зависит от формы пневмонии) тень, возможны варианты с наличием множественных диссеминированных очагов. При помощи спиральной компьютерной томографии (СКТ) можно точно выявить и локализовать даже мелкие, «невидимые» при рентген-исследовании очаги, определить состояние плевры, наличие жидкости в плевральной полости, СКТ позволяет детально оценить прилегающие отделы неизмененной легочной паренхимы, состояние бронхов, лимфоузлов средостения и прочее.
Как мы видим, различных заболеваний, этиологических факторов и нюансов внешних проявлений масса, относительно общее одно – диагностика. Чаще всего пациенты с жалобами на патологию органов дыхания направляются на рентген диагностику или СКТ, так как при помощи совокупности этих методов можно действительно наиболее детально и точно распознать болезнь даже на ранних стадиях, провести дифференциальную диагностику и назначить необходимое лечение.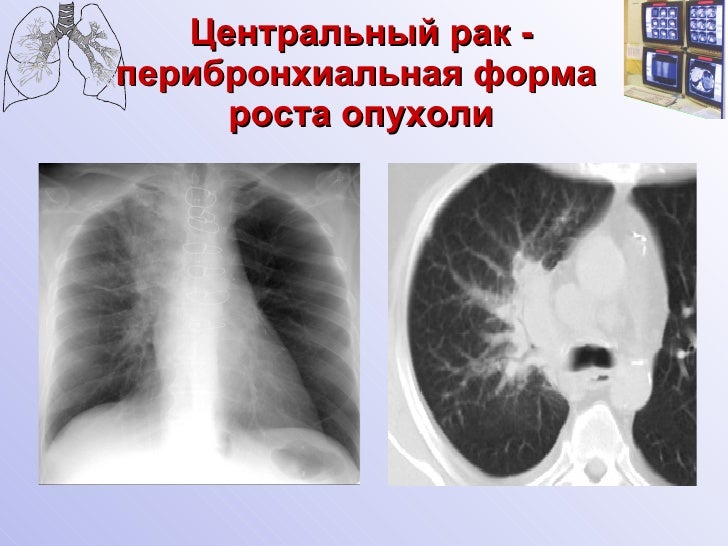
Высококачественная цифровая рентгенография и спиральная компьютерная томография в АЦМД.
Статью подготовили специалисты отделения лучевой диагностики АЦМД-МЕДОКС
Стадирование ТNМ и пересмотренная Международная система стадирования
Первичная опухоль (Т)
• Tx — недостаточно данных для оценки первичной опухоли, или диагноз ставится на основании злокачественных клеток, выявляемых в мокроте или смывах из бронхиального дерева, но опухоль не визуализируется методами рентгенодиагностики или бронхоскопии.
• Tis — карцинома in situ.
• T1 — опухоль размерами 3 см или менее в наибольшем измерении, окруженная легочной тканью или висцеральной плеврой и не прорастающая проксимальнее долевого бронха по данным бронхоскопии (т.е. опухоль не прорастает в главный бронх). (Замечание. Редкие поверхностно-распространяющиеся опухоли любого размера с инвазией в пределах бронхиальной стенки, даже при распространении на главный бронх, также классифицируется как Т1.
 )
)• T2 — опухоль, характеризующаяся следующими признаками:
- размеры опухоли более 3 см в наибольшем измерении;
- вовлечение главного бронха и расположение опухоли на 2 см и более дистальнее карины;
- инвазия висцеральной плевры;
- опухоль, вызывающая ателектаз или обструктивную пневмонию с распространением на корень легкого, но без вовлечения всего легкого.
• T3 — опухоль любого размера с прямой инвазией любой из следующих структур: грудной стенки (включая опухоли верхней борозды), диафрагмы, медиастинальной плевры, париетальной оболочки перикарда; или опухоль главного бронха, расположенная менее чем в 2 см от карины, но без вовлечения ее; или опухоль, вызывающая ателектаз или обструктивную пневмонию всего легкого.
 (Замечание. В большинстве случаев плевральный выпот обусловлен злокачественной опухолью; однако у некоторых пациентов при неоднократных цитологических исследованиях плеврального экссудата опухолевые элементы не выявляются. В этих случаях плевральная жидкость не носит геморрагический характер и не является экссудатом. У таких больных возможно выполнение видеоторакоскопии с биопсией плевры. Если данные обследования не позволяют связать возникновение плеврита с опухолью, наличие плеврального выпота не является элементом стадирования и первичная опухоль должна классифицироваться как T1, T2 или T3.)
(Замечание. В большинстве случаев плевральный выпот обусловлен злокачественной опухолью; однако у некоторых пациентов при неоднократных цитологических исследованиях плеврального экссудата опухолевые элементы не выявляются. В этих случаях плевральная жидкость не носит геморрагический характер и не является экссудатом. У таких больных возможно выполнение видеоторакоскопии с биопсией плевры. Если данные обследования не позволяют связать возникновение плеврита с опухолью, наличие плеврального выпота не является элементом стадирования и первичная опухоль должна классифицироваться как T1, T2 или T3.)Регионарные лимфоузлы (N)
- Nx — недостаточно данных для оценки состояния регионарных лимфоузлов.
- N0 Р регионарные лимфоузлы не поражены метастазами.
- N1 — метастазы в ипсилатеральные перибронхиальные и/или ипсилатеральные лимфоузлы корня легкого и внутрилегочные узлы, в том числе и при прямом распространении первичной опухоли
- N2 Р метастазы в ипсилатеральные медиастинальные и/или бифуркационные лимфоузлы.
- N3 Р метастазы в контралатеральные медиастинальные, контралатеральные корневые, ипсилатеральные или контралатеральные лимфоузлы лестничной мышцы или надключичные лимфоузлы.
Отдаленные метастазы (M)
- MX — недостаточно данных для оценки отдаленных метастазов.
- M0 — отдаленные метастазы отсутствуют.
- M1 — отдаленные метастазы. (Замечание. Наличие опухолевого узла в ипсилатеральной или контралатеральной доле, отличной от локализации первичного очага, классифицируется как M1.)
Локализация метастазов обозначается следующим образом: BRA — головной мозг, LYM — лимфоузлы, OTH — другие, PLE — плевра, EYE — глаз, MAR — костный мозг, OVR — яичник, PUL — легкое, HEP — печень, OSS — костная ткань, PER — брюшина, SKI — кожа.
Группировка по стадиям по системе AJCC
Оккультная (скрытая) карцинома
• TxN0M0
Стадия 0
• TisN0M0
Стадия IA
• T1N0M0
Стадия IB
• T2N0M0
Стадия IIA
• T1N1M0
Стадия IIB
• T2N1M0
• T3N0M0
Стадия IIIA
• T1N2M0
• T2N2M0
• T3N1M0
• T3N2M0
Стадия IIIB
• Любая T, N3, M0
• T4, любая N, M0
Стадия IV
• Любая T, любая N, M1
Пересмотренная Международная система стадирования РЛ
Пересмотренная Международная система стадирования РЛ, основанная на информации, полученной из клинической базы данных, включающей более 5000 пациентов, была принята в 1997 г.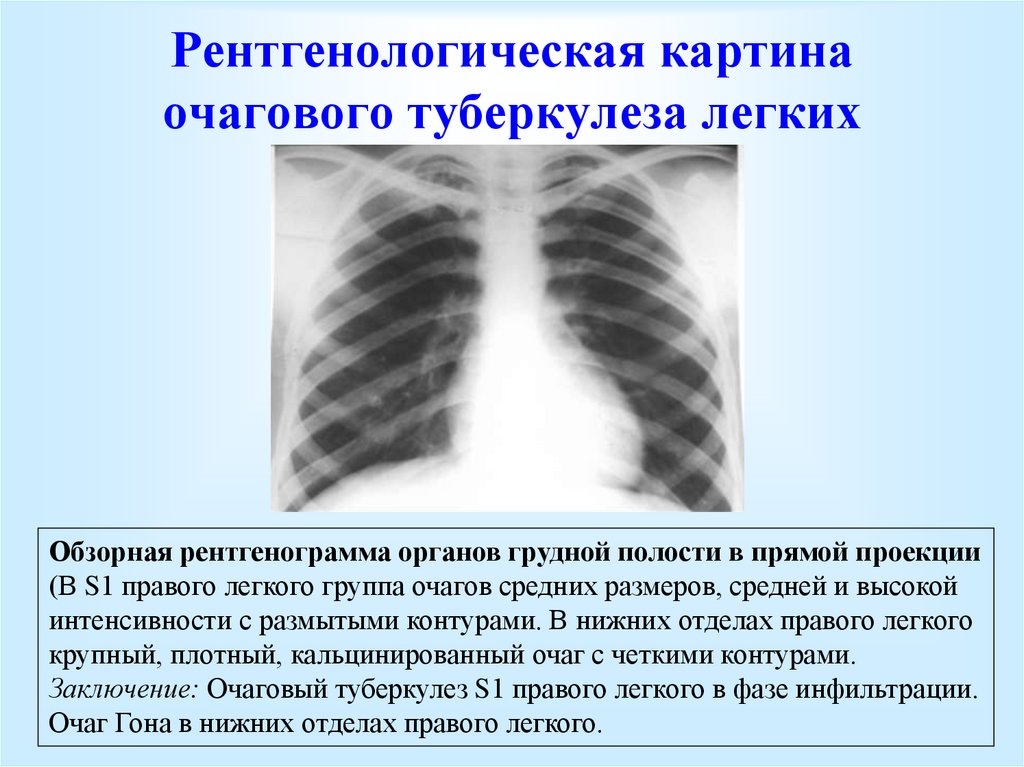 Американским объединенным комитетом по изучению рака (American Joint Committee on Cancer — AJCC) и Международной организацией по борьбе против рака (Union Internationale Contre le Cancer). Пересмотренный вариант системы классификации позволил повысить прогностическую ценность стадирования пациентов; однако корреляция между стадией и прогнозом была оценена до внедрения в клиническую практику ПЭТ. Первая стадия подразделяется на две категории в зависимости от размеров опухоли: IA (Т1N0М0) и IB (Т2N0М0). Вторая стадия заболевания подразделяется на две категории в зависимости от размера опухоли и статуса лимфоузлов: IIA (Т1N1М0) и IIB (Т2N1М0). Опухоль с параметрами Т3N0 была переведена из стадии IIIA в соответствии с версией 1986 г. в стадию IIB согласно современной классификации. Такое изменение обусловлено лучшим прогнозом в этой группе пациентов: у большинства больных с инвазией опухоли в париетальную плевру или грудную стенку при локализации в верхней борозде или на висцеральной плевре (Т3), но без поражения регионарных лимфоузлов, возможно выполнение хирургического вмешательства, иногда в комбинации с лучевым или химиолучевым лечением.
Американским объединенным комитетом по изучению рака (American Joint Committee on Cancer — AJCC) и Международной организацией по борьбе против рака (Union Internationale Contre le Cancer). Пересмотренный вариант системы классификации позволил повысить прогностическую ценность стадирования пациентов; однако корреляция между стадией и прогнозом была оценена до внедрения в клиническую практику ПЭТ. Первая стадия подразделяется на две категории в зависимости от размеров опухоли: IA (Т1N0М0) и IB (Т2N0М0). Вторая стадия заболевания подразделяется на две категории в зависимости от размера опухоли и статуса лимфоузлов: IIA (Т1N1М0) и IIB (Т2N1М0). Опухоль с параметрами Т3N0 была переведена из стадии IIIA в соответствии с версией 1986 г. в стадию IIB согласно современной классификации. Такое изменение обусловлено лучшим прогнозом в этой группе пациентов: у большинства больных с инвазией опухоли в париетальную плевру или грудную стенку при локализации в верхней борозде или на висцеральной плевре (Т3), но без поражения регионарных лимфоузлов, возможно выполнение хирургического вмешательства, иногда в комбинации с лучевым или химиолучевым лечением. Результаты лечения идентичны таковым у пациентов с II стадии НМРЛ после хирургического лечения. Другое изменение уточняет классификацию при множественных опухолевых узлах. Сателлитные опухолевые узлы (которые не являются лимфоузлами) с локализацией в той же доле, что и первичная опухоль, должны быть классифицированы как Т4. Внутрилегочный ипсилатеральный метастаз в долю, отличную от доли с первичной локализацией опухоли, должен расцениваться как М1 (IV стадия). AJCC использует систему классификации по ТNМ.
Результаты лечения идентичны таковым у пациентов с II стадии НМРЛ после хирургического лечения. Другое изменение уточняет классификацию при множественных опухолевых узлах. Сателлитные опухолевые узлы (которые не являются лимфоузлами) с локализацией в той же доле, что и первичная опухоль, должны быть классифицированы как Т4. Внутрилегочный ипсилатеральный метастаз в долю, отличную от доли с первичной локализацией опухоли, должен расцениваться как М1 (IV стадия). AJCC использует систему классификации по ТNМ.
Источники:
Mountain C.F. Revisions in the International System for Staging Lung Cancer. Chest 1997;111(6):1710—7.
Lung. In: American Joint Committee on Cancer. AJCC Cancer Staging Manual. 6th ed. NY, Springer; 2002. p. 167—81.
Смотрите также:
- Гистологическая классификация
- Диагностика и предоперационное стадирование
- Оккультный, или скрытый, НМРЛ
- Информации о лечении по данным Национального Противоракового Института США
↑ Наверх
Анатомия, грудная клетка, лимфатические узлы средостения — StatPearls
Введение
Медиастинальный отдел содержит несколько важных органов и сосудов и служит центральным узлом для лимфатического дренажа.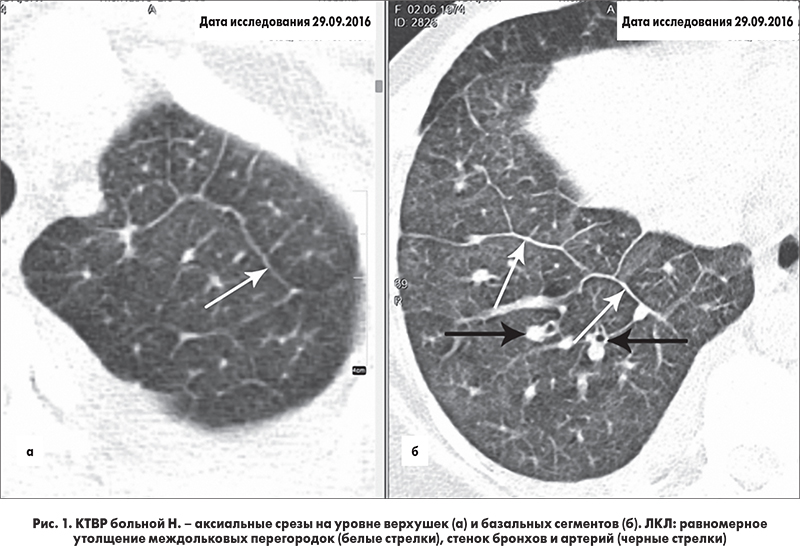 Средостение классически подразделяется на три функциональных отдела: переднее (преваскулярное), среднее (висцеральное) и заднее (паравертебральное) средостение. Эти подразделения используются для описания локализации поражений, тем самым помогая облегчить дифференциальную диагностику и общение между поставщиками. Лимфатические узлы (ЛУ) присутствуют во всех трех функциональных отделах средостения, хотя большая часть лимфатической ткани находится в переднем и среднем отделах, а этиология лимфатической патологии варьируется в зависимости от подразделения. Разделение средостения помогает сузить круг длинных дифференциальных диагнозов, которые могут быть обнаружены в грудной клетке (включая, помимо прочего, такие инфекции, как туберкулез, узловое распространение рака легких, саркоидоз, лимфому, силикоз и асбестоз). В отличие от функциональных подразделений, локализация внутригрудных ЛУ традиционно разделяется на 14 станций в соответствии с их отношением к ориентирам, обнаруженным во время медиастиноскопии и торакотомии по поводу рака легкого.
Средостение классически подразделяется на три функциональных отдела: переднее (преваскулярное), среднее (висцеральное) и заднее (паравертебральное) средостение. Эти подразделения используются для описания локализации поражений, тем самым помогая облегчить дифференциальную диагностику и общение между поставщиками. Лимфатические узлы (ЛУ) присутствуют во всех трех функциональных отделах средостения, хотя большая часть лимфатической ткани находится в переднем и среднем отделах, а этиология лимфатической патологии варьируется в зависимости от подразделения. Разделение средостения помогает сузить круг длинных дифференциальных диагнозов, которые могут быть обнаружены в грудной клетке (включая, помимо прочего, такие инфекции, как туберкулез, узловое распространение рака легких, саркоидоз, лимфому, силикоз и асбестоз). В отличие от функциональных подразделений, локализация внутригрудных ЛУ традиционно разделяется на 14 станций в соответствии с их отношением к ориентирам, обнаруженным во время медиастиноскопии и торакотомии по поводу рака легкого.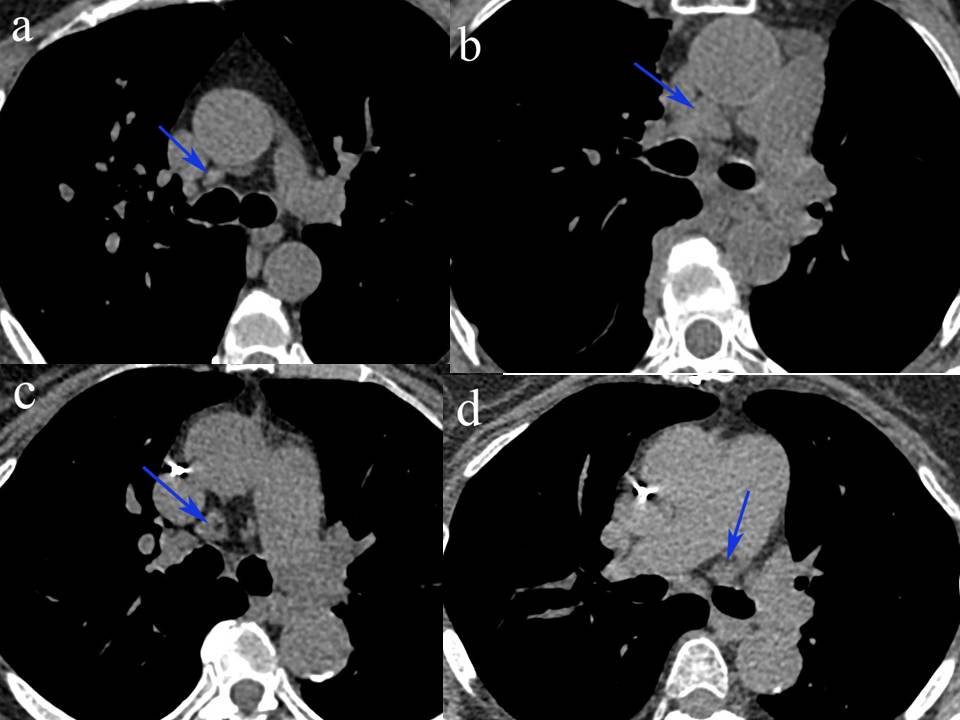 Станции 1–9соответствуют медиастинальным узловым группам, а станции 10–14 представляют прикорневые и другие более периферические экстрамедиастинальные узловые группы.
Станции 1–9соответствуют медиастинальным узловым группам, а станции 10–14 представляют прикорневые и другие более периферические экстрамедиастинальные узловые группы.
Самой актуальной картой внутригрудных лимфатических узлов является карта Международной ассоциации по изучению рака легких (IASLC). Атлас IASLC заменяет все предыдущие схемы и устраняет расхождения между более старыми популярными системами, такими как классификация лимфатических узлов Наруке и модифицированная версия карты лимфатических узлов Американского торакального общества Маунтин-Дреслер.
Структура и функция
Сеть лимфатических сосудов и лимфатических узлов простирается по всему телу, чтобы поддерживать надлежащее функционирование его иммунной системы, а также абсорбцию пищевых жиров и гомеостаз жидкости. В отличие от артерий и вен, лимфатические сосуды представляют собой сосуды со слепыми концами, которые транспортируют интерстициальную жидкость, иммунные клетки и макромолекулы, вместе называемые лимфой, через лимфатические узлы и обратно в грудную клетку для возврата в кровоснабжение через подключичные вены.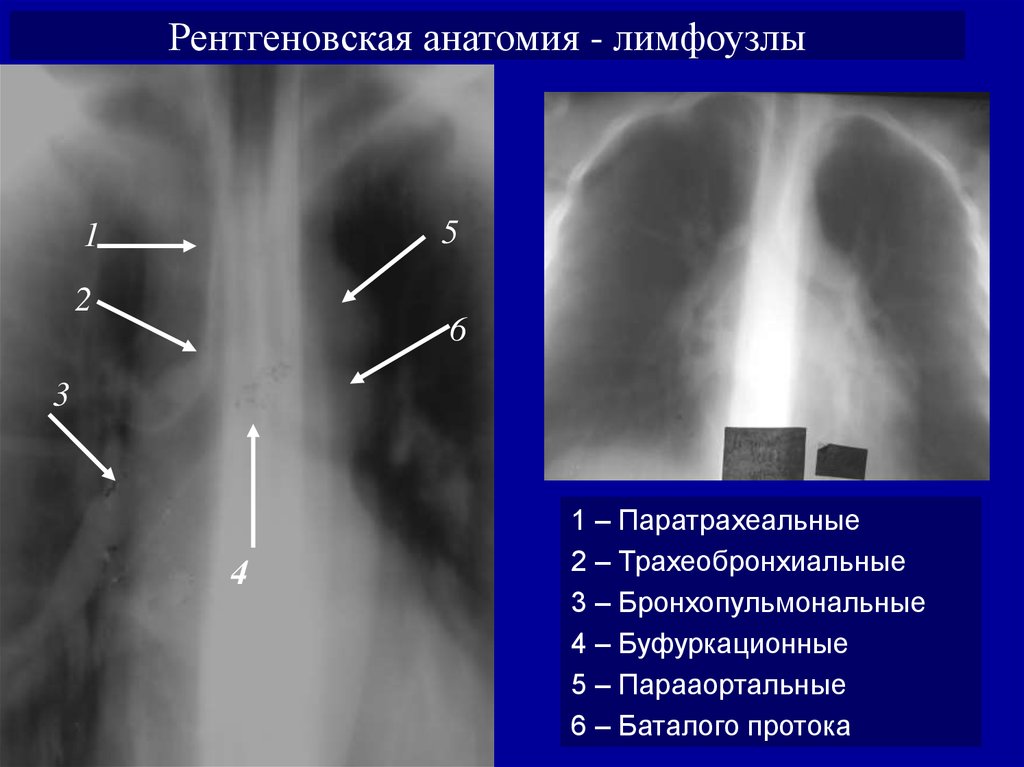 Лимфа возникает, когда плазма крови просачивается из капилляров в интерстициальное пространство. Наряду с нормальными макромолекулами и лимфоцитами в плазме также просачиваются мертвые клетки и материалы, которые могут быть вредными для организма, такие как бактерии, вирусы и опухолевые клетки, которые, в свою очередь, попадают в лимфу. Жидкость и клетки транспортируются обратно в грудную клетку по лимфатическим сосудам. Попутно узлы, подобные тем, что находятся в средостении, берут пробы лимфы, отфильтровывая потенциальные угрозы и нежелательные клеточные остатки, прежде чем они снова попадут в кровоток. Макрофаги в лимфатических узлах фагоцитируют эти нежелательные вещества, а затем расщепляют их для переработки организмом. Т-лимфоциты берут образцы антигенов от патогенов и взаимодействуют с В-клетками, чтобы инициировать клональную экспансию для производства антител. При активации иммунных клеток LN растут как клетки внутри деления. Быстрый рост может вызывать боль, а медленная митотическая активность (часто наблюдаемая при раке) приводит к безболезненной лимфаденопатии.
Лимфа возникает, когда плазма крови просачивается из капилляров в интерстициальное пространство. Наряду с нормальными макромолекулами и лимфоцитами в плазме также просачиваются мертвые клетки и материалы, которые могут быть вредными для организма, такие как бактерии, вирусы и опухолевые клетки, которые, в свою очередь, попадают в лимфу. Жидкость и клетки транспортируются обратно в грудную клетку по лимфатическим сосудам. Попутно узлы, подобные тем, что находятся в средостении, берут пробы лимфы, отфильтровывая потенциальные угрозы и нежелательные клеточные остатки, прежде чем они снова попадут в кровоток. Макрофаги в лимфатических узлах фагоцитируют эти нежелательные вещества, а затем расщепляют их для переработки организмом. Т-лимфоциты берут образцы антигенов от патогенов и взаимодействуют с В-клетками, чтобы инициировать клональную экспансию для производства антител. При активации иммунных клеток LN растут как клетки внутри деления. Быстрый рост может вызывать боль, а медленная митотическая активность (часто наблюдаемая при раке) приводит к безболезненной лимфаденопатии. [5][6]
[5][6]
Эмбриология
Развитие лимфатической системы начинается в конце пятой недели эмбриогенеза, примерно через 2 недели после развития сердечно-сосудистой системы. Хотя это все еще несколько спорно, наиболее распространенная теория состоит в том, что лимфатическая система начинается как каналы, формирующиеся из дивертикулов вне венозного эндотелия. В течение 6-9 недель очаговое расширение каналов приводит к образованию шести первичных лимфатических мешков. Далее из мешочков вдоль крупных вен вырастают лимфатические сосуды. Примерно на 12 неделе внутриутробного развития большая часть лимфатических мешочков трансформируется в группы лимфатических узлов, в то время как вдоль лимфатических сосудов формируются дополнительные лимфатические узлы, в то время как небольшая часть мешочков продолжает вносить вклад в формирование цистерны хили и грудного протока. .[7]
Кровоснабжение и лимфатическая система
Организация медиастинальных лимфатических узлов основана на их отношении к хирургическим ориентирам: магистральным сосудам, трахее/бронхам и плевре.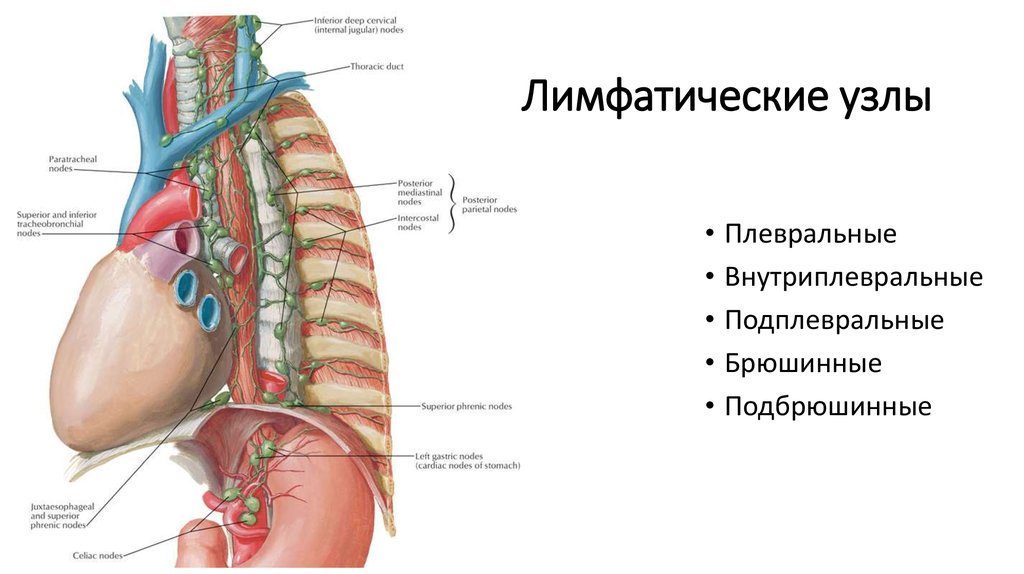 На КТ, предпочтительном радиологическом методе визуализации лимфатических узлов, нормальные медиастинальные узлы представляют собой почковидные структуры мягких тканей с жировыми воротами. Нормальные лимфатические узлы в средостении обычно имеют размеры менее 10 мм по короткой оси. Здоровые лимфатические узлы могут быть больше из-за реактивной гиперплазии при острой инфекции или хронических заболеваниях легких, таких как эмфизема или легочный фиброз; однако увеличенные лимфатические узлы вызывают наибольшее беспокойство при патологическом процессе, таком как лимфома, злокачественные метастазы или саркоидоз.
На КТ, предпочтительном радиологическом методе визуализации лимфатических узлов, нормальные медиастинальные узлы представляют собой почковидные структуры мягких тканей с жировыми воротами. Нормальные лимфатические узлы в средостении обычно имеют размеры менее 10 мм по короткой оси. Здоровые лимфатические узлы могут быть больше из-за реактивной гиперплазии при острой инфекции или хронических заболеваниях легких, таких как эмфизема или легочный фиброз; однако увеличенные лимфатические узлы вызывают наибольшее беспокойство при патологическом процессе, таком как лимфома, злокачественные метастазы или саркоидоз.
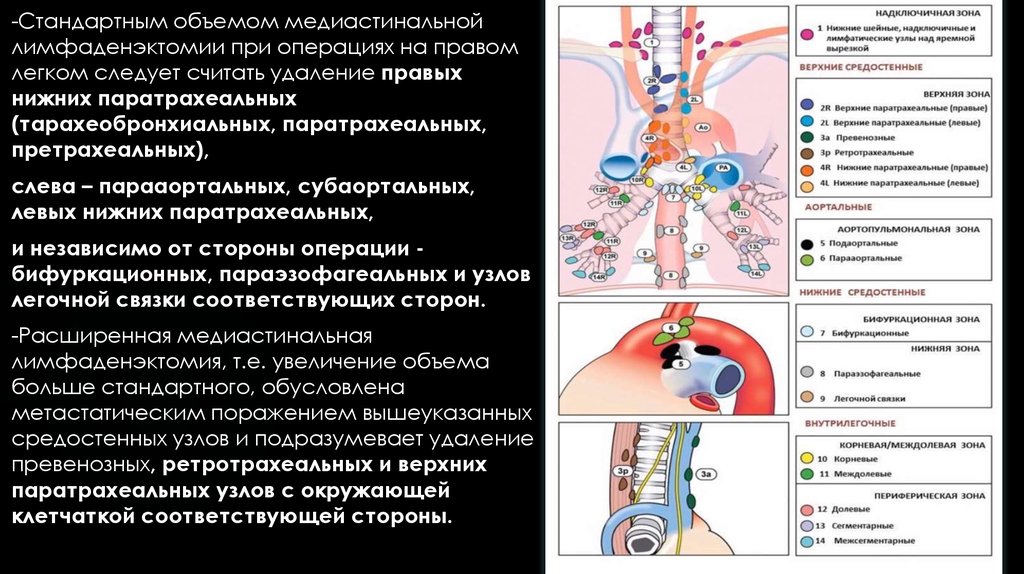
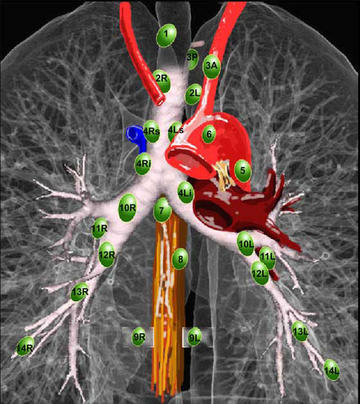
Как уже упоминалось, в соответствии с рекомендациями по стадированию рака легких внутригрудные лимфатические узлы разделены на 14 участков, которые сгруппированы в 7 зон. Станции 1–9 расположены в медиастинальном плевральном рефлексе, а станции 10–14 расположены дистальнее медиастинального плеврального рефлекса и внутри висцеральной плевры. Станции 1, 2, 4 и 10-14 дополнительно имеют обозначения R и L для правого и левого, а станция 3 имеет обозначения A и P для передней и задней части.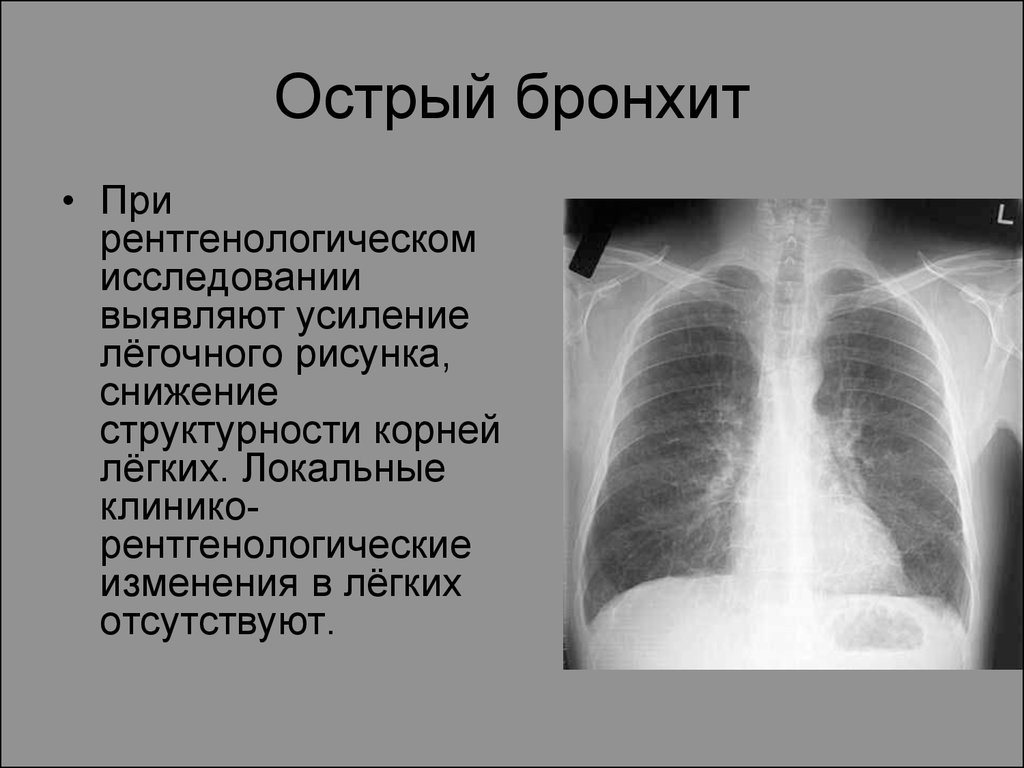 Внутригрудные часто рассматриваются в сочетании с медиастинальными лимфатическими узлами, но для полноты картины в этой статье будут кратко рассмотрены внемедиастинальные лимфатические узлы (станции 10-14).
Внутригрудные часто рассматриваются в сочетании с медиастинальными лимфатическими узлами, но для полноты картины в этой статье будут кратко рассмотрены внемедиастинальные лимфатические узлы (станции 10-14).
Зоны и станции лимфатических узлов
Надключичная зона
Станция 1 (надключичная): Станция 1 включает самую краниальную станцию медиастинальных узлов. Он включает лимфатические узлы в вырезке грудины, надключичной и нижней шейной областях (таким образом, они перекрываются с некоторыми картами шейных лимфатических узлов, используемыми при раке головы и шеи). Перстневидный хрящ служит верхней границей участка 1. Станция 1 простирается книзу до верхнего края рукоятки и вершин ключиц. Средняя линия трахеи используется для обозначения лимфатических узлов 1R и 1L.
Верхняя зона (верхние средостенные ЛУ)
Станция 2 (верхняя паратрахеальная): Зона 2 ЛУ вокруг трахеи и, в отличие от станции 1, левая боковая стенка трахеи вместо средней линии используется в качестве границы для различения 2R и 2L.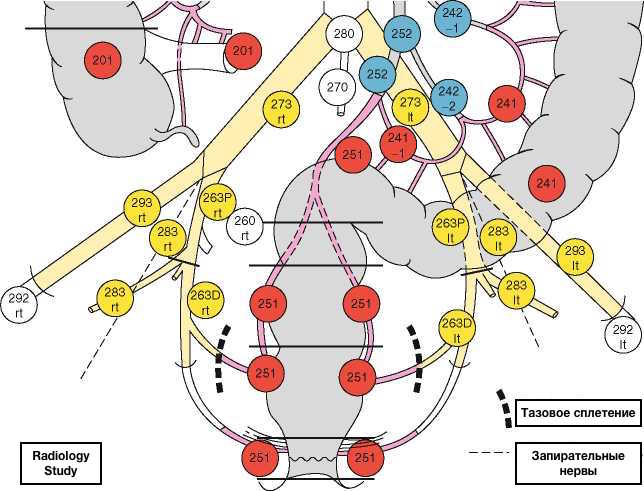 Верхней границей станции 2 является вершина ипсилатеральных легких и плевральных полостей, а по средней линии — верхняя граница рукоятки. Нижняя граница участка 2 справа (2R) находится там, где нижний край левой плечеголовной вены пересекает трахею, а нижняя граница участка 2 слева (2L) является верхней границей дуги аорты.
Верхней границей станции 2 является вершина ипсилатеральных легких и плевральных полостей, а по средней линии — верхняя граница рукоятки. Нижняя граница участка 2 справа (2R) находится там, где нижний край левой плечеголовной вены пересекает трахею, а нижняя граница участка 2 слева (2L) является верхней границей дуги аорты.
Станция 3 (преваскулярная и ретротрахеальная): все преваскулярные лимфатические узлы (3А) расположены за грудиной и кпереди от верхней полой вены и левой сонной артерии. Верхняя граница является вершиной груди (как и станция 2), но простирается дальше каудально до уровня киля. Ретротрахеальные ЛУ (3P), как следует из их названия, расположены в области кзади от трахеи и также простираются от верхушки грудной клетки до киля.
Станция 4 (нижняя паратрахеальная): Нижние паратрахеальные узлы расположены вдоль дистального отдела трахеи, сверху граничащей со станцией 2 и доходят до уровня киля. Они лежат кзади от сосудистой сети аорты, и, как и на станции 2, левая боковая стенка трахеи вместо средней линии используется в качестве границы для дифференциации между 4R и 4L.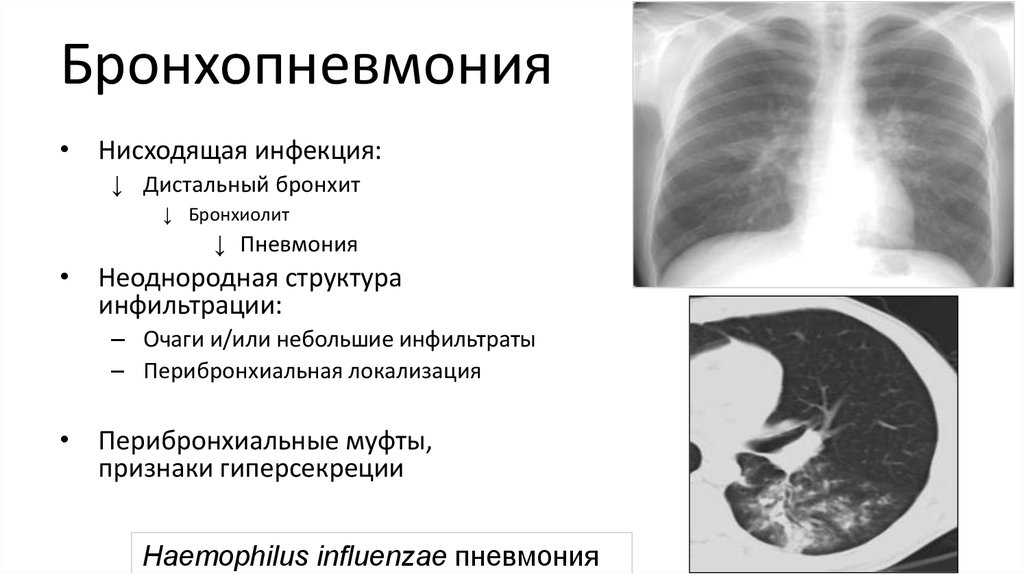
Аортопульмональная зона
Станция 5 (субаротическая): Эти лимфатические узлы, также известные как аортопульмональные (AP) оконные ЛУ, расположены латеральнее артериальной связки, остатка артериального протока. Нижний край дуги аорты служит верхней границей участка 5, а верхний край левой легочной артерии ограничивает нижнее расширение.
Станция 6 (парааортальная): Парааортальные ЛУ лежат на передней и латеральной стороне восходящей аорты и дуги аорты, спереди и/или над субаортальными (переднезаднее окно) ЛУ. Диафрагмальный нерв можно использовать в качестве ориентира для идентификации лимфатических узлов, которые классифицируются как парааортальные.
Субкаринальная зона
Станция 7 (субкаринальные): субкаринальные узлы лежат непосредственно под килем и между главными стволовыми бронхами. Чтобы отличить их от параэзофагеальных ЛУ, которые находятся более каудально, дистальная часть промежуточного бронха и начало левого нижнедолевого бронха используются для разграничения правого и левого нижних расширений станции 7.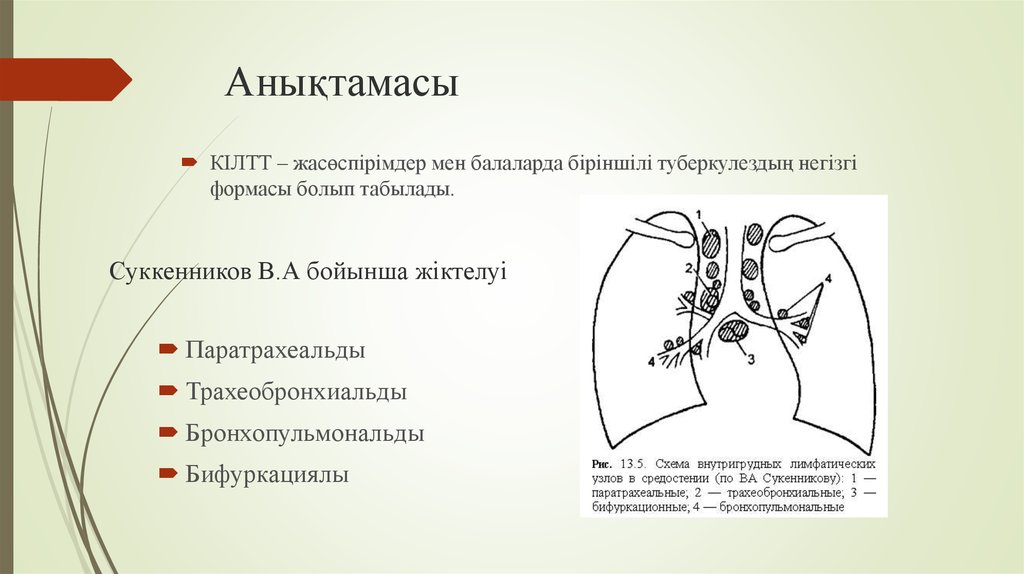 У большинства пациентов это приводит к нижний край, скошенный от горизонтали, учитывая, что окончание промежуточного бронха обычно находится ниже начала левого нижнедолевого бронха).
У большинства пациентов это приводит к нижний край, скошенный от горизонтали, учитывая, что окончание промежуточного бронха обычно находится ниже начала левого нижнедолевого бронха).
Нижняя зона (нижние средостенные ЛУ)
Станция 8 (параэзофагеальная): Параэзофагеальные лимфатические узлы — это медиастинальные лимфатические узлы, расположенные ниже субкаринальных лимфатических узлов, а также в передней или латеральной части пищевода, вплоть до пищеводного отверстия диафрагмы.
Станция 9 (Легочная связка): Узлы легочной связки связаны с легочными связками. Эти «связки» не являются связками, но представляют собой медиастинальные париетально-плевральные рефлексы, которые встречаются ниже правого и левого легочных корней (9).Р и 9Л).
Прикорневая зона + междолевая и периферическая зоны (внемедиастинальные ЛУ)
Все эти лимфатические узлы находятся за пределами плеврального отражения средостения, но в пределах легочной висцеральной плевры.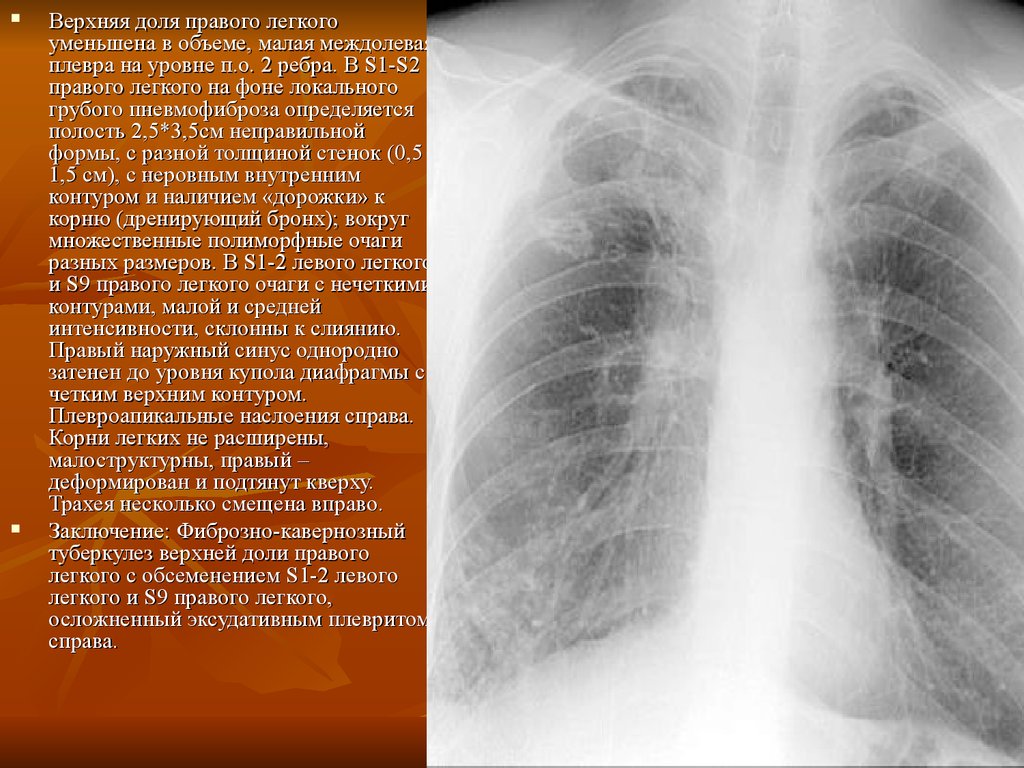
Станция 10 (Hilar): Эти ЛУ расположены вдоль правого и левого главных бронхов до их бифуркации и обозначаются 10R и 10L соответственно.
Участок 11 (междолевой): Участок 11 состоит из ЛУ, расположенных между долевыми бронхами, сразу за бифуркацией каждого главного бронха.
Участки 12-14 (периферические): они также известны как долевые, сегментарные и субсегментарные лимфатические узлы, в зависимости от того, расположены ли они вдоль долевых, сегментарных или субсегментарных бронхов. Эти ЛУ редко видны, и их трудно точно классифицировать при визуализации; поэтому многие используют широкий термин периферийных LN для станций 12-14.
Следует отметить, что, хотя приведенная выше система классификации является наиболее широко используемой схемой картирования и часто применяется при описании медиастинальных лимфатических узлов, не связанных с раком легкого, в некоторых случаях, например, для определения стадии рака пищевода, подходят и другие карты для конкретных заболеваний.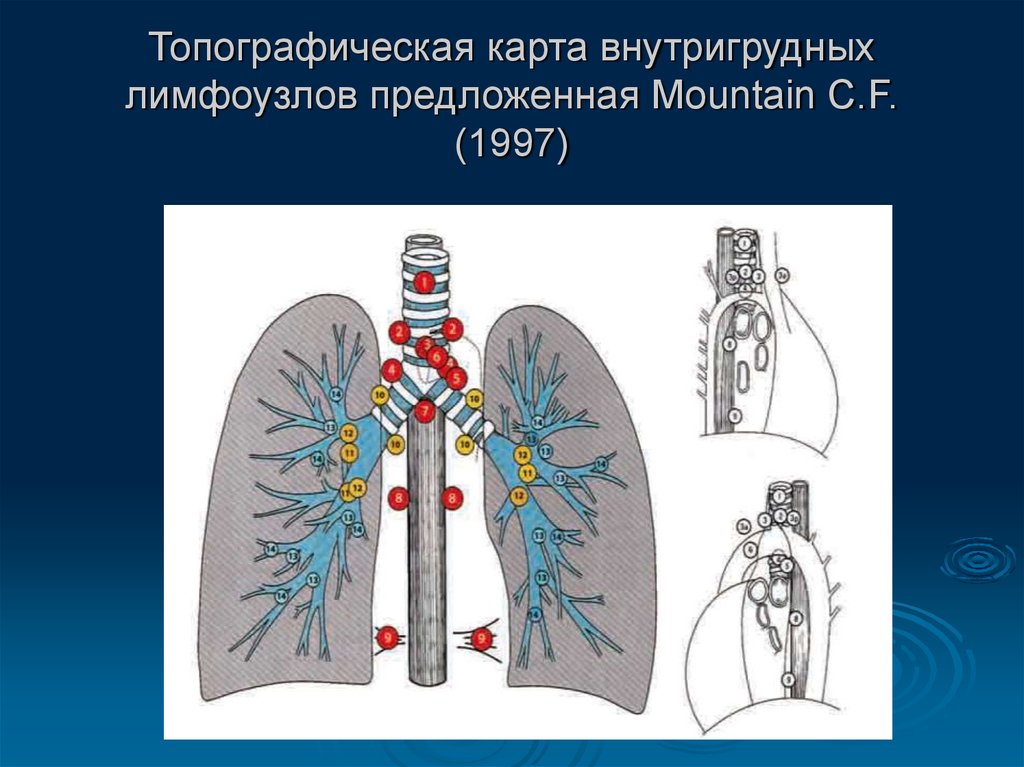 [1] [8] [9]][10]
[1] [8] [9]][10]
Помимо медиастинальных лимфатических узлов, грудной проток является важным компонентом внутригрудной лимфатической системы. Это самый крупный лимфатический сосуд в грудной клетке, начинающийся в верхней части цистерны хилиса на уровне L2 позвонка. Оттуда он проходит краниально между задним краем аорты и передним краем позвоночника примерно до области Th5 позвонка, где он впадает в венозную систему около места слияния левой подключичной и внутренней яремной вен. Приблизительно 75% лимфатической жидкости организма оттекает через грудной проток в венозную систему, что составляет лимфоидный отток от всего тела, за исключением правой руки и правой стороны головы (узлы которых впадают в место соединения правой подключичная и внутренняя яремная вены).[11][12][13]
Физиологические варианты
Отпочкование лимфатических сосудов от вен может быть очень непостоянным у разных людей, и, таким образом, узловые цепочки демонстрируют широко распространенную изменчивость. Примечательно, что наиболее часто идентифицируемый ход грудного протока присутствует только у 40–60% пациентов. Общие проявления включают грудные протоки и соответствующие цистерны хили, которые находятся слева анатомически и впадают в левый венозный угол; грудные протоки и соответствующие им цистерны хили, находящиеся справа анатомически и впадающие в правый венозный угол; плексиформное представление; проксимальные и дистальные парциальные удвоения грудного протока; и несуществующие цистерны хили.[13]
Примечательно, что наиболее часто идентифицируемый ход грудного протока присутствует только у 40–60% пациентов. Общие проявления включают грудные протоки и соответствующие цистерны хили, которые находятся слева анатомически и впадают в левый венозный угол; грудные протоки и соответствующие им цистерны хили, находящиеся справа анатомически и впадающие в правый венозный угол; плексиформное представление; проксимальные и дистальные парциальные удвоения грудного протока; и несуществующие цистерны хили.[13]
Хирургические рекомендации
Забор медиастинальных лимфатических узлов имеет решающее значение для первоначальной диагностики и определения стадии рака легких и пищевода, а также лимфомы. Кроме того, это необходимо для выявления первичных или рецидивирующих метастазов в лимфатических узлах при экстраторакальных злокачественных новообразованиях. Это можно сделать с помощью различных методов, используемых различными специалистами, причем метод обычно определяется локализацией узлового заболевания.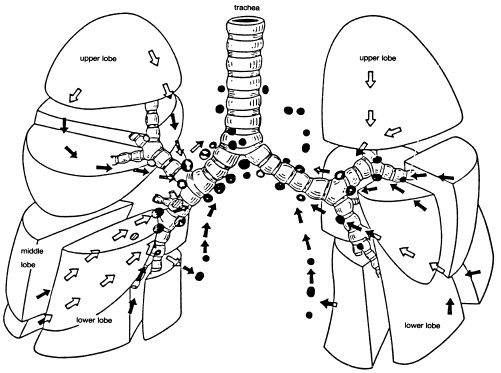 Кардиоторакальные хирурги могут использовать медиастиноскопию для отбора образцов на участках 1, 2П/Л, 3, 4П/Л и 7. Расширенная медиастиноскопия или видеоторакотомия (VATS) могут расширить их диапазон, включив биопсию участков 5 и 6. Гастроэнтерологи может использовать УЗИ пищевода (EUS), которое позволяет провести тонкоигольную аспирацию (FNA) станций медиастинальных лимфатических узлов 2L, 4L, 7, 8 и 9. Пульмонологи могут использовать трансбронхиальную пункционную аспирацию (TBNA), а также эндобронхиальное ультразвуковое исследование (EBUS) FNA, которое позволяет брать образцы тканей из билатеральной станции 10–12 LN (внутренняя и периферическая зоны) в дополнение к 3P, позиции 7 и билатеральной станции. 2 и 4 ЛН. Точно так же эти методы могут быть использованы для диагностики других заболеваний, которые могут поражать медиастинальные лимфатические узлы, таких как саркоидоз, болезнь Кастлемана или туберкулез.
Кардиоторакальные хирурги могут использовать медиастиноскопию для отбора образцов на участках 1, 2П/Л, 3, 4П/Л и 7. Расширенная медиастиноскопия или видеоторакотомия (VATS) могут расширить их диапазон, включив биопсию участков 5 и 6. Гастроэнтерологи может использовать УЗИ пищевода (EUS), которое позволяет провести тонкоигольную аспирацию (FNA) станций медиастинальных лимфатических узлов 2L, 4L, 7, 8 и 9. Пульмонологи могут использовать трансбронхиальную пункционную аспирацию (TBNA), а также эндобронхиальное ультразвуковое исследование (EBUS) FNA, которое позволяет брать образцы тканей из билатеральной станции 10–12 LN (внутренняя и периферическая зоны) в дополнение к 3P, позиции 7 и билатеральной станции. 2 и 4 ЛН. Точно так же эти методы могут быть использованы для диагностики других заболеваний, которые могут поражать медиастинальные лимфатические узлы, таких как саркоидоз, болезнь Кастлемана или туберкулез.
Помимо определения стадии рака, медиастинальные лимфатические нарушения могут иметь и другие хирургические последствия.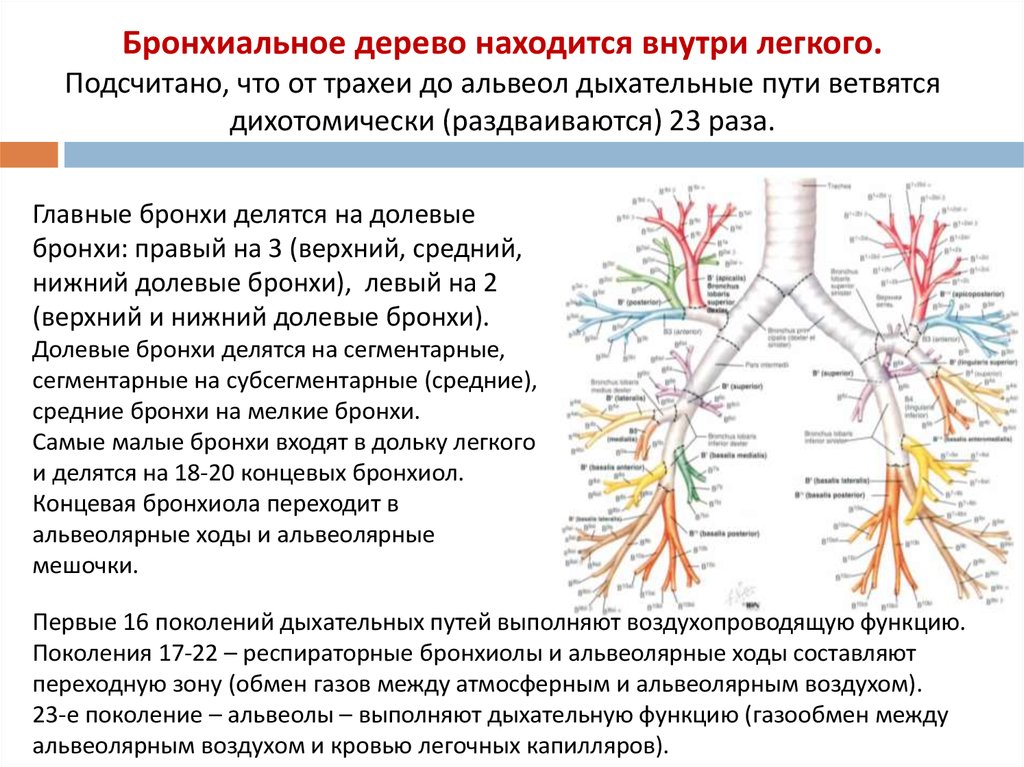 Хилезные плевральные выпоты могут возникать при повреждении внутригрудной лимфатической ткани либо в результате инфекции/воспаления, либо в результате травмы/хирургического вмешательства и утечки лимфы в плевральные полости. Реже хилоперикард может возникнуть, если оскорбительное событие приводит к фистулезному соединению между лимфатическими сосудами и перикардом. Если после развития хилоторакса показана эмболизация лимфатической системы, магнитно-резонансная дуктография имеет наилучшую визуализацию для руководства хирургическим вмешательством, но в качестве альтернативы можно использовать компьютерную томографию, лимфосцинтиграфию и лимфангиографию.[13][14][15][16] [17]
Хилезные плевральные выпоты могут возникать при повреждении внутригрудной лимфатической ткани либо в результате инфекции/воспаления, либо в результате травмы/хирургического вмешательства и утечки лимфы в плевральные полости. Реже хилоперикард может возникнуть, если оскорбительное событие приводит к фистулезному соединению между лимфатическими сосудами и перикардом. Если после развития хилоторакса показана эмболизация лимфатической системы, магнитно-резонансная дуктография имеет наилучшую визуализацию для руководства хирургическим вмешательством, но в качестве альтернативы можно использовать компьютерную томографию, лимфосцинтиграфию и лимфангиографию.[13][14][15][16] [17]
Клиническое значение
При первичных внутригрудных опухолях очень важно точно определить станцию, из которой берутся лимфатические узлы, поскольку информация о том, в какие лимфатические узлы распространилась опухоль, важна для хирургического стадирования пациента. региональное заболевание. В случае рака легкого опухолевое поражение лимфатических узлов на ипсилатеральном участке 10–14, все из которых являются экстраплевральными, считается болезнью N1, в то время как медиастинальные лимфатические узлы на участках 2–9которые ипсилатеральны по отношению к злокачественному новообразованию (включая субкаринальные ЛУ для любой стороны заболевания), считаются заболеванием N2. Контралатеральные медиастинальные или прикорневые лимфатические узлы, а также лимфатические узлы станции 1, в которых присутствуют опухолевые клетки, считаются заболеванием N3. Напротив, при раке пищевода N стадия заболевания определяется количеством регионарных ЛУ, пораженных опухолью, при этом N1 соответствует 1-2 положительным (+) ЛУ, N2 используется для 3-6 + ЛУ, а N3 обозначает случаи с >=7 +LN. Кроме того, не все узловые станции, используемые IASLC для рака легких, считаются региональными ЛУ для определения стадии рака пищевода, а некоторые станции называются по-разному, например, обозначение верхних, средних и нижних параэзофагеальных станций ЛУ.
Контралатеральные медиастинальные или прикорневые лимфатические узлы, а также лимфатические узлы станции 1, в которых присутствуют опухолевые клетки, считаются заболеванием N3. Напротив, при раке пищевода N стадия заболевания определяется количеством регионарных ЛУ, пораженных опухолью, при этом N1 соответствует 1-2 положительным (+) ЛУ, N2 используется для 3-6 + ЛУ, а N3 обозначает случаи с >=7 +LN. Кроме того, не все узловые станции, используемые IASLC для рака легких, считаются региональными ЛУ для определения стадии рака пищевода, а некоторые станции называются по-разному, например, обозначение верхних, средних и нижних параэзофагеальных станций ЛУ.
В дополнение к метастазам, злокачественные медиастинальные лимфатические узлы могут быть вызваны лимфомами, группой раковых заболеваний, возникающих из лейкоцитов. Эта группа заболеваний является наиболее частой причиной узловой патологии переднего отдела, но также является частой причиной лимфаденопатии в среднем отделе.
Аденопатия средостения может быть вызвана неопухолевыми новообразованиями.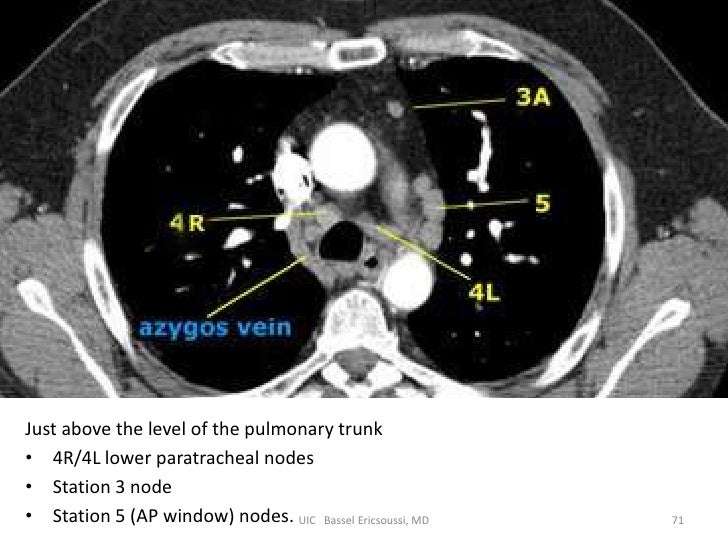 Первичные острые или хронические инфекционно-воспалительные процессы возникают во всех отделах средостения и могут сопровождаться увеличением лимфатических узлов. Точно так же легочные и системные инфекции, такие как пневмония и вирус иммунодефицита человека, могут привести к патологическому увеличению медиастинальных лимфатических узлов. Если медиастинальные лимфатические узлы обызвествлены, это помогает сузить дифференциальный диагноз до таких состояний, как гранулематозные заболевания (гистоплазмоз, туберкулез), силикоз, саркоидоз и пролеченная лимфома. Когда лимфатические сосуды средостения повреждаются, возникающий в результате хилоторакс может нарушать нормальную иммунологическую, пищевую и дыхательную функции.
Первичные острые или хронические инфекционно-воспалительные процессы возникают во всех отделах средостения и могут сопровождаться увеличением лимфатических узлов. Точно так же легочные и системные инфекции, такие как пневмония и вирус иммунодефицита человека, могут привести к патологическому увеличению медиастинальных лимфатических узлов. Если медиастинальные лимфатические узлы обызвествлены, это помогает сузить дифференциальный диагноз до таких состояний, как гранулематозные заболевания (гистоплазмоз, туберкулез), силикоз, саркоидоз и пролеченная лимфома. Когда лимфатические сосуды средостения повреждаются, возникающий в результате хилоторакс может нарушать нормальную иммунологическую, пищевую и дыхательную функции.
Увеличенные медиастинальные лимфатические узлы могут быть обнаружены случайно, а рекомендации по наблюдению и оценке можно найти в Journal of the American College of Радиология . Например, узлы могут вызывать особое беспокойство, если они большие, асимметричные или демонстрируют авидность ФДГ на ПЭТ/КТ. Узлы размером более 15 мм могут потребовать особого внимания, особенно если нет известного объяснения, например, саркоидоза в анамнезе. Руководящие принципы Американского колледжа радиологии также признают ценность категоризации лимфатических узлов по вышеупомянутым подразделениям, выявления аномальных контуров лимфатических узлов и того, являются ли образования солидными или кистозными.[3][8][12][13][18].
Узлы размером более 15 мм могут потребовать особого внимания, особенно если нет известного объяснения, например, саркоидоза в анамнезе. Руководящие принципы Американского колледжа радиологии также признают ценность категоризации лимфатических узлов по вышеупомянутым подразделениям, выявления аномальных контуров лимфатических узлов и того, являются ли образования солидными или кистозными.[3][8][12][13][18].
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Рисунок
Медиастинальные лимфатические узлы. Изображение предоставлено S Bhimji MD
Рисунок
Станции медиастинальных лимфатических узлов. Предоставлено Александрой Лапор
Ссылки
- 1.
Mountain CF, Dresler CM. Классификация регионарных лимфатических узлов для определения стадии рака легкого. Грудь. 1997 июня; 111 (6): 1718-23. [PubMed: 9187199]
- 2.
Craun JB, Banks KP, Clemenshaw MN, Moren RW. Саркоидноподобная реакция неоплазии, вызывающая гиперметаболическую грудную лимфаденопатию в условиях экстраторакальной злокачественности: отчет о двух случаях и обзор дифференциально-диагностических соображений. J Nucl Med Technol. 2012 декабрь; 40 (4): 231-5. [PubMed: 23015478]
- 3.
Картер Б.В., Томияма Н., Бхора Ф.Ю., Росадо де Кристенсон М.Л., Накадзима Дж., Буазель П.М., Деттербек Ф.К., Маром Э.М. Современное определение отделов средостения. Дж. Торак Онкол. 2014 Сентябрь; 9(9 Приложение 2): S97-101. [PubMed: 25396318]
- 4.
Rusch VW, Asamura H, Watanabe H, Giroux DJ, Rami-Porta R, Goldstrow P., члены организационного комитета IASLC. Проект IASLC по стадированию рака легких: предложение по новой международной карте лимфатических узлов в предстоящем седьмом издании классификации TNM для рака легких. Дж. Торак Онкол. 2009 май; 4(5):568-77. [PubMed: 19357537]
- 5.
Аспелунд А., Робчук М.Р., Караман С., Макинен Т., Алитало К. Лимфатическая система в сердечно-сосудистой медицине. Цирк рез. 2016 05 февраля; 118 (3): 515-30. [В паблике: 26846644]
- 6.
Чхве И., Ли С., Хонг Ю.К. Новая эра лимфатической системы: она больше не является вторичной по отношению к кровеносной системе. Колд Спринг Харб Перспект Мед. 2012 апр;2(4):a006445. [Бесплатная статья PMC: PMC3312397] [PubMed: 22474611]
- 7.
Хсу MC, Иткин М. Лимфатическая анатомия. Tech Vasc Interv Radiol. 2016 дек.; 19(4):247-254. [PubMed: 27993319]
- 8.
Ugalde PA, Pereira ST, Araujo C, Irion KL. Корреляционная анатомия средостения. Клиника торакальной хирургии. 2011 май; 21(2):251-72, ix. [В паблике: 21477775]
- 9.
Ляо С., фон дер Вейд П.Ю. Лимфатическая система: активный путь иммунной защиты. Semin Cell Dev Biol. 2015 фев; 38:83-9. [Бесплатная статья PMC: PMC4397130] [PubMed: 25534659]
- 10.

Walker CM, Chung JH, Abbott GF, Little BP, El-Sherief AH, Shepard JA, Lanuti M. Стадирование медиастинальных лимфатических узлов: от неинвазивного к хирургическому. AJR Am J Рентгенол. 2012 июль; 199(1):W54-64. [PubMed: 22733932]
- 11.
Эль-Шериф А.Х., Лау К.Т., Ву К.К., Дрейк Р.Л., Эбботт Г.Ф., Райс Т.В. Карта лимфатических узлов Международной ассоциации по изучению рака легких (IASLC): рентгенологический обзор с иллюстрацией КТ. Рентгенография. 2014 Окт;34(6):1680-91. [PubMed: 25310423]
- 12.
Райс Т.В., Ишваран Х., Фергюсон М.К., Блэкстоун Э.Х., Голдстроу П. Рак пищевода и пищеводно-желудочного соединения: Восьмое издание. Дж. Торак Онкол. 2017 янв; 12(1):36-42. [Бесплатная статья PMC: PMC5591443] [PubMed: 27810391]
- 13.
Johnson OW, Chick JF, Chauhan NR, Fairchild AH, Fan CM, Stecker MS, Killoran TP, Suzuki-Han A. Грудной проток: клиническое значение, анатомические вариации, визуализация и эмболизация .
 Евро Радиол. 2016 авг; 26 (8): 2482-93. [PubMed: 26628065]
Евро Радиол. 2016 авг; 26 (8): 2482-93. [PubMed: 26628065]- 14.
Теран, доктор медицины, Брок М.В. Стадирование метастазов рака легкого в лимфатические узлы средостения. Дж. Торак Дис. 2014 март; 6(3):230-6. [Бесплатная статья PMC: PMC3949187] [PubMed: 24624287]
- 15.
Колелла С., Вильманн П., Конге Л., Клементсен П.Ф. Эндоскопическое ультразвуковое исследование в диагностике и стадировании рака легкого. Эндоск УЗИ. 2014 окт; 3(4):205-12. [PMC бесплатная статья: PMC4247527] [PubMed: 25485267]
- 16.
Szlubowski A, Herth FJ, Soja J, Kołodziej M, Figura J, Cmiel A, Obrochta A, Pankowski J. Эндобронхиальная аспирационная игла под ультразвуковым контролем при рестадировании немелкоклеточного рака легкого, подтвержденном трансцервикальной двусторонней расширенной медиастинальной лимфаденэктомией — проспективное исследование. Eur J Cardiothorac Surg. 2010 май; 37(5):1180-4. [ПубМед: 20022759]
- 17.
Аткинсон С, Бэнкс К. Визуализация идиопатического хилоперикарда с помощью лимфосцинтиграфии 99mTc-SC и ОФЭКТ/КТ. Клин Нукл Мед. 2015 ноябрь;40(11):e508-10. [PubMed: 26284770]
- 18.
Munden RF, Carter BW, Chiles C, MacMahon H, Black WC, Ko JP, McAdams HP, Rossi SE, Leung AN, Boiselle PM, Kent MS, Brown K, Dyer Д.С., Хартман Т.Е., Гудман Э.М., Найдич Д.П., Казеруни Э.А., Берланд Л.Л., Пандхарипанде П.В. Управление случайными находками на КТ грудной клетки: медиастинальные и сердечно-сосудистые находки. Белая книга Комитета по случайным находкам ACR. J Am Coll Radiol. 2018 авг; 15 (8): 1087-1096. [PubMed: 29941240]
Анатомия, грудная клетка, лимфатические узлы средостения — StatPearls
Введение
Медиастинальный отдел содержит множество важных органов и сосудов и служит центральным узлом для лимфооттока. Средостение классически подразделяется на три функциональных отдела: переднее (преваскулярное), среднее (висцеральное) и заднее (паравертебральное) средостение. Эти подразделения используются для описания локализации поражений, тем самым помогая облегчить дифференциальную диагностику и общение между поставщиками. Лимфатические узлы (ЛУ) присутствуют во всех трех функциональных отделах средостения, хотя большая часть лимфатической ткани находится в переднем и среднем отделах, а этиология лимфатической патологии варьируется в зависимости от подразделения. Разделение средостения помогает сузить круг длинных дифференциальных диагнозов, которые могут быть обнаружены в грудной клетке (включая, помимо прочего, такие инфекции, как туберкулез, узловое распространение рака легких, саркоидоз, лимфому, силикоз и асбестоз). В отличие от функциональных подразделений, локализация внутригрудных ЛУ традиционно разделяется на 14 станций в соответствии с их отношением к ориентирам, обнаруженным во время медиастиноскопии и торакотомии по поводу рака легкого. Станции 1–9соответствуют медиастинальным узловым группам, а станции 10–14 представляют прикорневые и другие более периферические экстрамедиастинальные узловые группы.
Эти подразделения используются для описания локализации поражений, тем самым помогая облегчить дифференциальную диагностику и общение между поставщиками. Лимфатические узлы (ЛУ) присутствуют во всех трех функциональных отделах средостения, хотя большая часть лимфатической ткани находится в переднем и среднем отделах, а этиология лимфатической патологии варьируется в зависимости от подразделения. Разделение средостения помогает сузить круг длинных дифференциальных диагнозов, которые могут быть обнаружены в грудной клетке (включая, помимо прочего, такие инфекции, как туберкулез, узловое распространение рака легких, саркоидоз, лимфому, силикоз и асбестоз). В отличие от функциональных подразделений, локализация внутригрудных ЛУ традиционно разделяется на 14 станций в соответствии с их отношением к ориентирам, обнаруженным во время медиастиноскопии и торакотомии по поводу рака легкого. Станции 1–9соответствуют медиастинальным узловым группам, а станции 10–14 представляют прикорневые и другие более периферические экстрамедиастинальные узловые группы.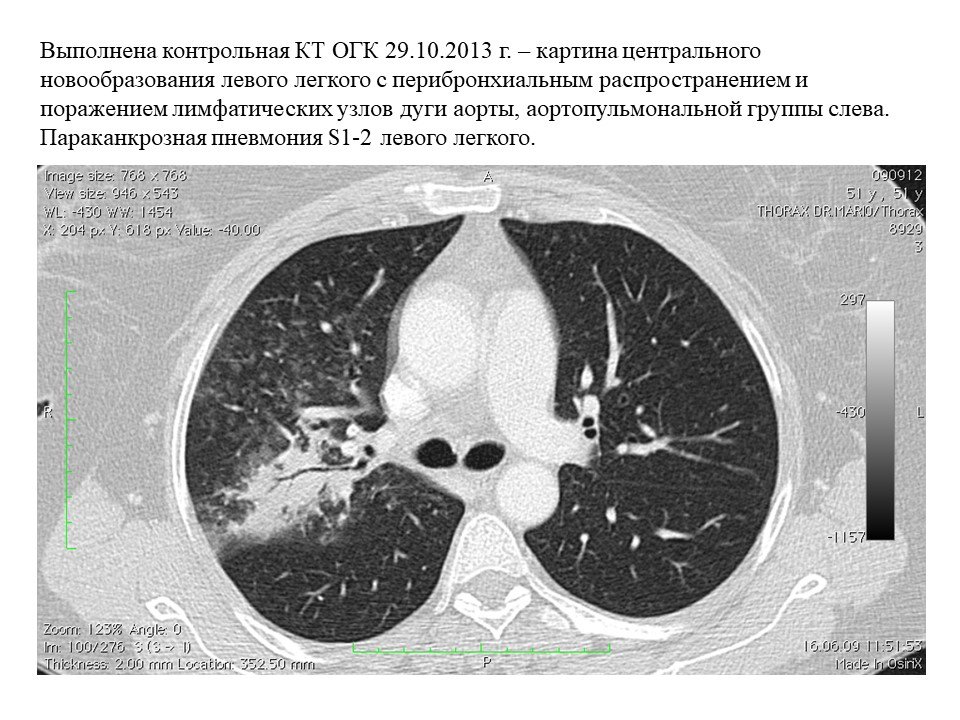
Самой актуальной картой внутригрудных лимфатических узлов является карта Международной ассоциации по изучению рака легких (IASLC). Атлас IASLC заменяет все предыдущие схемы и устраняет расхождения между более старыми популярными системами, такими как классификация лимфатических узлов Наруке и модифицированная версия карты лимфатических узлов Американского торакального общества Маунтин-Дреслер.
Структура и функция
Сеть лимфатических сосудов и лимфатических узлов простирается по всему телу, чтобы поддерживать надлежащее функционирование его иммунной системы, а также абсорбцию пищевых жиров и гомеостаз жидкости. В отличие от артерий и вен, лимфатические сосуды представляют собой сосуды со слепыми концами, которые транспортируют интерстициальную жидкость, иммунные клетки и макромолекулы, вместе называемые лимфой, через лимфатические узлы и обратно в грудную клетку для возврата в кровоснабжение через подключичные вены. Лимфа возникает, когда плазма крови просачивается из капилляров в интерстициальное пространство. Наряду с нормальными макромолекулами и лимфоцитами в плазме также просачиваются мертвые клетки и материалы, которые могут быть вредными для организма, такие как бактерии, вирусы и опухолевые клетки, которые, в свою очередь, попадают в лимфу. Жидкость и клетки транспортируются обратно в грудную клетку по лимфатическим сосудам. Попутно узлы, подобные тем, что находятся в средостении, берут пробы лимфы, отфильтровывая потенциальные угрозы и нежелательные клеточные остатки, прежде чем они снова попадут в кровоток. Макрофаги в лимфатических узлах фагоцитируют эти нежелательные вещества, а затем расщепляют их для переработки организмом. Т-лимфоциты берут образцы антигенов от патогенов и взаимодействуют с В-клетками, чтобы инициировать клональную экспансию для производства антител. При активации иммунных клеток LN растут как клетки внутри деления. Быстрый рост может вызывать боль, а медленная митотическая активность (часто наблюдаемая при раке) приводит к безболезненной лимфаденопатии.[5][6]
Наряду с нормальными макромолекулами и лимфоцитами в плазме также просачиваются мертвые клетки и материалы, которые могут быть вредными для организма, такие как бактерии, вирусы и опухолевые клетки, которые, в свою очередь, попадают в лимфу. Жидкость и клетки транспортируются обратно в грудную клетку по лимфатическим сосудам. Попутно узлы, подобные тем, что находятся в средостении, берут пробы лимфы, отфильтровывая потенциальные угрозы и нежелательные клеточные остатки, прежде чем они снова попадут в кровоток. Макрофаги в лимфатических узлах фагоцитируют эти нежелательные вещества, а затем расщепляют их для переработки организмом. Т-лимфоциты берут образцы антигенов от патогенов и взаимодействуют с В-клетками, чтобы инициировать клональную экспансию для производства антител. При активации иммунных клеток LN растут как клетки внутри деления. Быстрый рост может вызывать боль, а медленная митотическая активность (часто наблюдаемая при раке) приводит к безболезненной лимфаденопатии.[5][6]
Эмбриология
Развитие лимфатической системы начинается в конце пятой недели эмбриогенеза, примерно через 2 недели после развития сердечно-сосудистой системы. Хотя это все еще несколько спорно, наиболее распространенная теория состоит в том, что лимфатическая система начинается как каналы, формирующиеся из дивертикулов вне венозного эндотелия. В течение 6-9 недель очаговое расширение каналов приводит к образованию шести первичных лимфатических мешков. Далее из мешочков вдоль крупных вен вырастают лимфатические сосуды. Примерно на 12 неделе внутриутробного развития большая часть лимфатических мешочков трансформируется в группы лимфатических узлов, в то время как вдоль лимфатических сосудов формируются дополнительные лимфатические узлы, в то время как небольшая часть мешочков продолжает вносить вклад в формирование цистерны хили и грудного протока. .[7]
Хотя это все еще несколько спорно, наиболее распространенная теория состоит в том, что лимфатическая система начинается как каналы, формирующиеся из дивертикулов вне венозного эндотелия. В течение 6-9 недель очаговое расширение каналов приводит к образованию шести первичных лимфатических мешков. Далее из мешочков вдоль крупных вен вырастают лимфатические сосуды. Примерно на 12 неделе внутриутробного развития большая часть лимфатических мешочков трансформируется в группы лимфатических узлов, в то время как вдоль лимфатических сосудов формируются дополнительные лимфатические узлы, в то время как небольшая часть мешочков продолжает вносить вклад в формирование цистерны хили и грудного протока. .[7]
Кровоснабжение и лимфатическая система
Организация медиастинальных лимфатических узлов основана на их отношении к хирургическим ориентирам: магистральным сосудам, трахее/бронхам и плевре. На КТ, предпочтительном радиологическом методе визуализации лимфатических узлов, нормальные медиастинальные узлы представляют собой почковидные структуры мягких тканей с жировыми воротами. Нормальные лимфатические узлы в средостении обычно имеют размеры менее 10 мм по короткой оси. Здоровые лимфатические узлы могут быть больше из-за реактивной гиперплазии при острой инфекции или хронических заболеваниях легких, таких как эмфизема или легочный фиброз; однако увеличенные лимфатические узлы вызывают наибольшее беспокойство при патологическом процессе, таком как лимфома, злокачественные метастазы или саркоидоз.
Нормальные лимфатические узлы в средостении обычно имеют размеры менее 10 мм по короткой оси. Здоровые лимфатические узлы могут быть больше из-за реактивной гиперплазии при острой инфекции или хронических заболеваниях легких, таких как эмфизема или легочный фиброз; однако увеличенные лимфатические узлы вызывают наибольшее беспокойство при патологическом процессе, таком как лимфома, злокачественные метастазы или саркоидоз.
Как уже упоминалось, в соответствии с рекомендациями по стадированию рака легких внутригрудные лимфатические узлы разделены на 14 участков, которые сгруппированы в 7 зон. Станции 1–9 расположены в медиастинальном плевральном рефлексе, а станции 10–14 расположены дистальнее медиастинального плеврального рефлекса и внутри висцеральной плевры. Станции 1, 2, 4 и 10-14 дополнительно имеют обозначения R и L для правого и левого, а станция 3 имеет обозначения A и P для передней и задней части. Внутригрудные часто рассматриваются в сочетании с медиастинальными лимфатическими узлами, но для полноты картины в этой статье будут кратко рассмотрены внемедиастинальные лимфатические узлы (станции 10-14).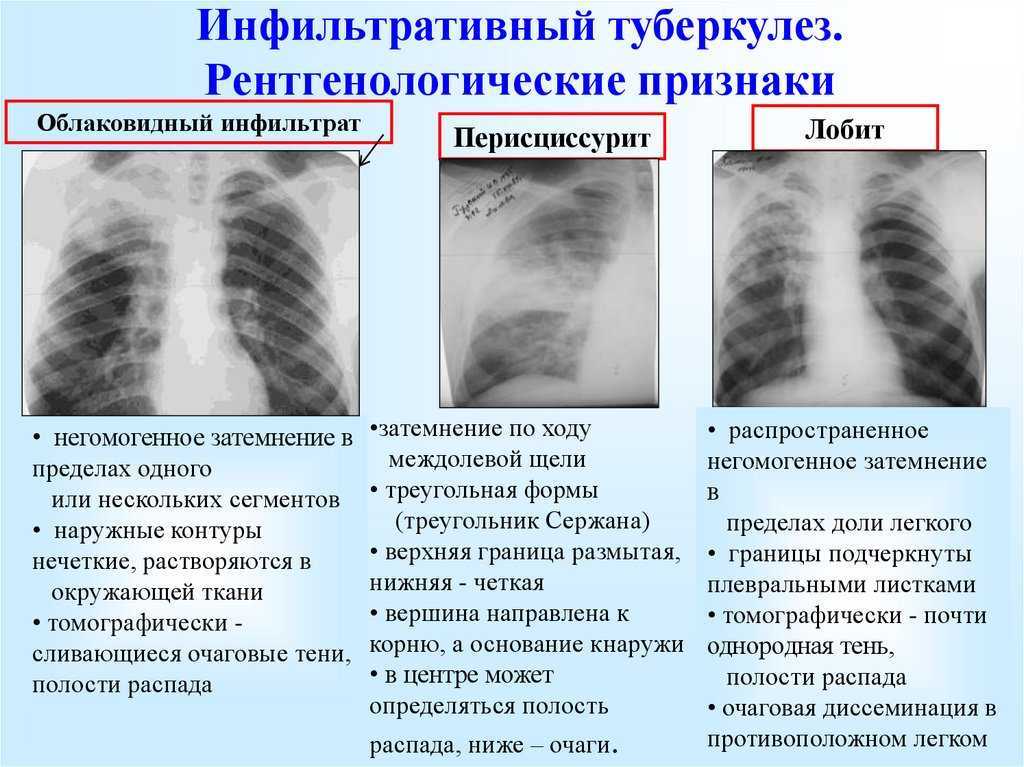
Зоны и станции лимфатических узлов
Надключичная зона
Станция 1 (надключичная): Станция 1 включает самую краниальную станцию медиастинальных узлов. Он включает лимфатические узлы в вырезке грудины, надключичной и нижней шейной областях (таким образом, они перекрываются с некоторыми картами шейных лимфатических узлов, используемыми при раке головы и шеи). Перстневидный хрящ служит верхней границей участка 1. Станция 1 простирается книзу до верхнего края рукоятки и вершин ключиц. Средняя линия трахеи используется для обозначения лимфатических узлов 1R и 1L.
Верхняя зона (верхние средостенные ЛУ)
Станция 2 (верхняя паратрахеальная): Зона 2 ЛУ вокруг трахеи и, в отличие от станции 1, левая боковая стенка трахеи вместо средней линии используется в качестве границы для различения 2R и 2L. Верхней границей станции 2 является вершина ипсилатеральных легких и плевральных полостей, а по средней линии — верхняя граница рукоятки.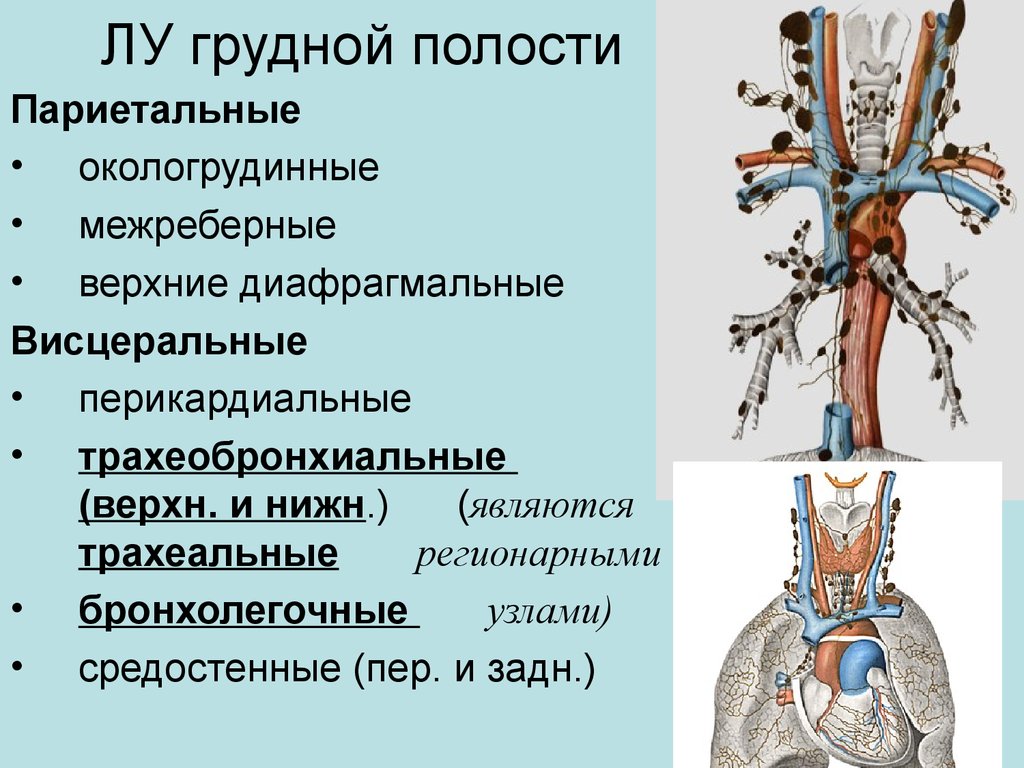 Нижняя граница участка 2 справа (2R) находится там, где нижний край левой плечеголовной вены пересекает трахею, а нижняя граница участка 2 слева (2L) является верхней границей дуги аорты.
Нижняя граница участка 2 справа (2R) находится там, где нижний край левой плечеголовной вены пересекает трахею, а нижняя граница участка 2 слева (2L) является верхней границей дуги аорты.
Станция 3 (преваскулярная и ретротрахеальная): все преваскулярные лимфатические узлы (3А) расположены за грудиной и кпереди от верхней полой вены и левой сонной артерии. Верхняя граница является вершиной груди (как и станция 2), но простирается дальше каудально до уровня киля. Ретротрахеальные ЛУ (3P), как следует из их названия, расположены в области кзади от трахеи и также простираются от верхушки грудной клетки до киля.
Станция 4 (нижняя паратрахеальная): Нижние паратрахеальные узлы расположены вдоль дистального отдела трахеи, сверху граничащей со станцией 2 и доходят до уровня киля. Они лежат кзади от сосудистой сети аорты, и, как и на станции 2, левая боковая стенка трахеи вместо средней линии используется в качестве границы для дифференциации между 4R и 4L.
Аортопульмональная зона
Станция 5 (субаротическая): Эти лимфатические узлы, также известные как аортопульмональные (AP) оконные ЛУ, расположены латеральнее артериальной связки, остатка артериального протока. Нижний край дуги аорты служит верхней границей участка 5, а верхний край левой легочной артерии ограничивает нижнее расширение.
Нижний край дуги аорты служит верхней границей участка 5, а верхний край левой легочной артерии ограничивает нижнее расширение.
Станция 6 (парааортальная): Парааортальные ЛУ лежат на передней и латеральной стороне восходящей аорты и дуги аорты, спереди и/или над субаортальными (переднезаднее окно) ЛУ. Диафрагмальный нерв можно использовать в качестве ориентира для идентификации лимфатических узлов, которые классифицируются как парааортальные.
Субкаринальная зона
Станция 7 (субкаринальные): субкаринальные узлы лежат непосредственно под килем и между главными стволовыми бронхами. Чтобы отличить их от параэзофагеальных ЛУ, которые находятся более каудально, дистальная часть промежуточного бронха и начало левого нижнедолевого бронха используются для разграничения правого и левого нижних расширений станции 7. У большинства пациентов это приводит к нижний край, скошенный от горизонтали, учитывая, что окончание промежуточного бронха обычно находится ниже начала левого нижнедолевого бронха).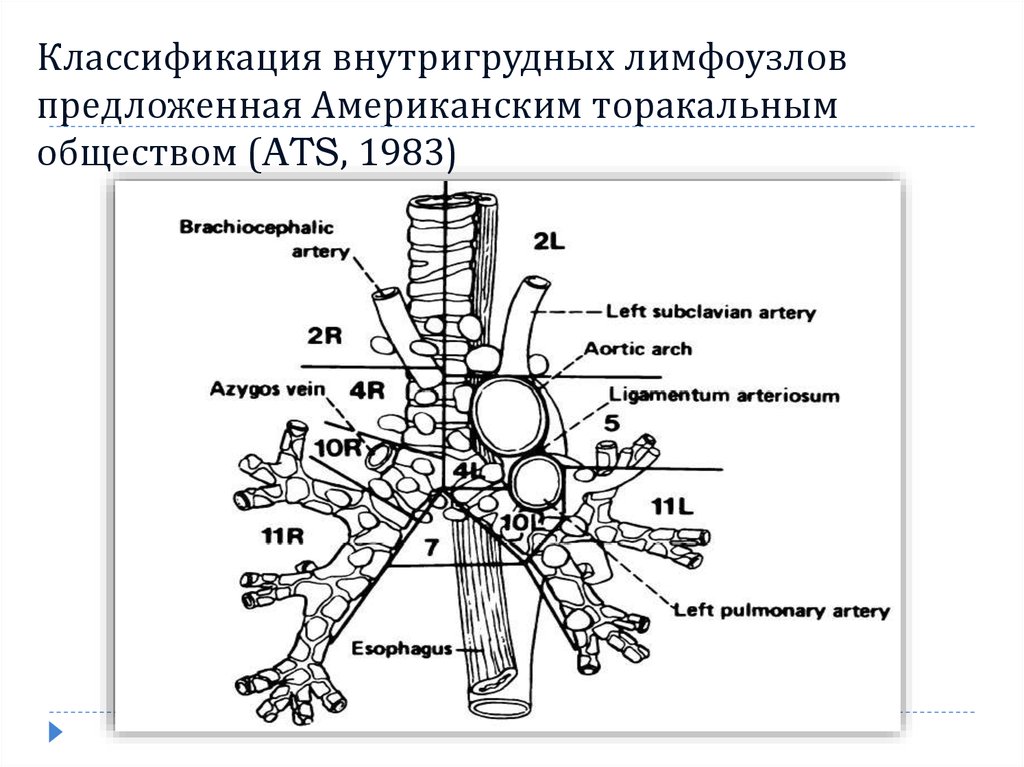
Нижняя зона (нижние средостенные ЛУ)
Станция 8 (параэзофагеальная): Параэзофагеальные лимфатические узлы — это медиастинальные лимфатические узлы, расположенные ниже субкаринальных лимфатических узлов, а также в передней или латеральной части пищевода, вплоть до пищеводного отверстия диафрагмы.
Станция 9 (Легочная связка): Узлы легочной связки связаны с легочными связками. Эти «связки» не являются связками, но представляют собой медиастинальные париетально-плевральные рефлексы, которые встречаются ниже правого и левого легочных корней (9).Р и 9Л).
Прикорневая зона + междолевая и периферическая зоны (внемедиастинальные ЛУ)
Все эти лимфатические узлы находятся за пределами плеврального отражения средостения, но в пределах легочной висцеральной плевры.
Станция 10 (Hilar): Эти ЛУ расположены вдоль правого и левого главных бронхов до их бифуркации и обозначаются 10R и 10L соответственно.
Участок 11 (междолевой): Участок 11 состоит из ЛУ, расположенных между долевыми бронхами, сразу за бифуркацией каждого главного бронха.
Участки 12-14 (периферические): они также известны как долевые, сегментарные и субсегментарные лимфатические узлы, в зависимости от того, расположены ли они вдоль долевых, сегментарных или субсегментарных бронхов. Эти ЛУ редко видны, и их трудно точно классифицировать при визуализации; поэтому многие используют широкий термин периферийных LN для станций 12-14.
Следует отметить, что, хотя приведенная выше система классификации является наиболее широко используемой схемой картирования и часто применяется при описании медиастинальных лимфатических узлов, не связанных с раком легкого, в некоторых случаях, например, для определения стадии рака пищевода, подходят и другие карты для конкретных заболеваний. [1] [8] [9]][10]
Помимо медиастинальных лимфатических узлов, грудной проток является важным компонентом внутригрудной лимфатической системы. Это самый крупный лимфатический сосуд в грудной клетке, начинающийся в верхней части цистерны хилиса на уровне L2 позвонка.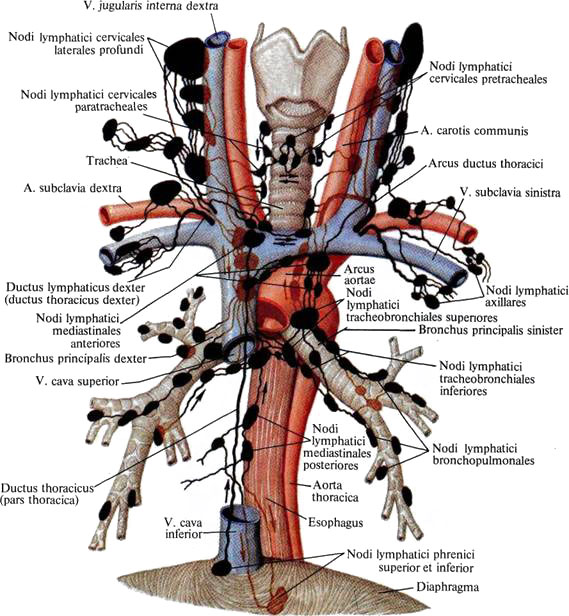 Оттуда он проходит краниально между задним краем аорты и передним краем позвоночника примерно до области Th5 позвонка, где он впадает в венозную систему около места слияния левой подключичной и внутренней яремной вен. Приблизительно 75% лимфатической жидкости организма оттекает через грудной проток в венозную систему, что составляет лимфоидный отток от всего тела, за исключением правой руки и правой стороны головы (узлы которых впадают в место соединения правой подключичная и внутренняя яремная вены).[11][12][13]
Оттуда он проходит краниально между задним краем аорты и передним краем позвоночника примерно до области Th5 позвонка, где он впадает в венозную систему около места слияния левой подключичной и внутренней яремной вен. Приблизительно 75% лимфатической жидкости организма оттекает через грудной проток в венозную систему, что составляет лимфоидный отток от всего тела, за исключением правой руки и правой стороны головы (узлы которых впадают в место соединения правой подключичная и внутренняя яремная вены).[11][12][13]
Физиологические варианты
Отпочкование лимфатических сосудов от вен может быть очень непостоянным у разных людей, и, таким образом, узловые цепочки демонстрируют широко распространенную изменчивость. Примечательно, что наиболее часто идентифицируемый ход грудного протока присутствует только у 40–60% пациентов. Общие проявления включают грудные протоки и соответствующие цистерны хили, которые находятся слева анатомически и впадают в левый венозный угол; грудные протоки и соответствующие им цистерны хили, находящиеся справа анатомически и впадающие в правый венозный угол; плексиформное представление; проксимальные и дистальные парциальные удвоения грудного протока; и несуществующие цистерны хили. [13]
[13]
Хирургические рекомендации
Забор медиастинальных лимфатических узлов имеет решающее значение для первоначальной диагностики и определения стадии рака легких и пищевода, а также лимфомы. Кроме того, это необходимо для выявления первичных или рецидивирующих метастазов в лимфатических узлах при экстраторакальных злокачественных новообразованиях. Это можно сделать с помощью различных методов, используемых различными специалистами, причем метод обычно определяется локализацией узлового заболевания. Кардиоторакальные хирурги могут использовать медиастиноскопию для отбора образцов на участках 1, 2П/Л, 3, 4П/Л и 7. Расширенная медиастиноскопия или видеоторакотомия (VATS) могут расширить их диапазон, включив биопсию участков 5 и 6. Гастроэнтерологи может использовать УЗИ пищевода (EUS), которое позволяет провести тонкоигольную аспирацию (FNA) станций медиастинальных лимфатических узлов 2L, 4L, 7, 8 и 9. Пульмонологи могут использовать трансбронхиальную пункционную аспирацию (TBNA), а также эндобронхиальное ультразвуковое исследование (EBUS) FNA, которое позволяет брать образцы тканей из билатеральной станции 10–12 LN (внутренняя и периферическая зоны) в дополнение к 3P, позиции 7 и билатеральной станции. 2 и 4 ЛН. Точно так же эти методы могут быть использованы для диагностики других заболеваний, которые могут поражать медиастинальные лимфатические узлы, таких как саркоидоз, болезнь Кастлемана или туберкулез.
2 и 4 ЛН. Точно так же эти методы могут быть использованы для диагностики других заболеваний, которые могут поражать медиастинальные лимфатические узлы, таких как саркоидоз, болезнь Кастлемана или туберкулез.
Помимо определения стадии рака, медиастинальные лимфатические нарушения могут иметь и другие хирургические последствия. Хилезные плевральные выпоты могут возникать при повреждении внутригрудной лимфатической ткани либо в результате инфекции/воспаления, либо в результате травмы/хирургического вмешательства и утечки лимфы в плевральные полости. Реже хилоперикард может возникнуть, если оскорбительное событие приводит к фистулезному соединению между лимфатическими сосудами и перикардом. Если после развития хилоторакса показана эмболизация лимфатической системы, магнитно-резонансная дуктография имеет наилучшую визуализацию для руководства хирургическим вмешательством, но в качестве альтернативы можно использовать компьютерную томографию, лимфосцинтиграфию и лимфангиографию.[13][14][15][16] [17]
Клиническое значение
При первичных внутригрудных опухолях очень важно точно определить станцию, из которой берутся лимфатические узлы, поскольку информация о том, в какие лимфатические узлы распространилась опухоль, важна для хирургического стадирования пациента. региональное заболевание. В случае рака легкого опухолевое поражение лимфатических узлов на ипсилатеральном участке 10–14, все из которых являются экстраплевральными, считается болезнью N1, в то время как медиастинальные лимфатические узлы на участках 2–9которые ипсилатеральны по отношению к злокачественному новообразованию (включая субкаринальные ЛУ для любой стороны заболевания), считаются заболеванием N2. Контралатеральные медиастинальные или прикорневые лимфатические узлы, а также лимфатические узлы станции 1, в которых присутствуют опухолевые клетки, считаются заболеванием N3. Напротив, при раке пищевода N стадия заболевания определяется количеством регионарных ЛУ, пораженных опухолью, при этом N1 соответствует 1-2 положительным (+) ЛУ, N2 используется для 3-6 + ЛУ, а N3 обозначает случаи с >=7 +LN. Кроме того, не все узловые станции, используемые IASLC для рака легких, считаются региональными ЛУ для определения стадии рака пищевода, а некоторые станции называются по-разному, например, обозначение верхних, средних и нижних параэзофагеальных станций ЛУ.
региональное заболевание. В случае рака легкого опухолевое поражение лимфатических узлов на ипсилатеральном участке 10–14, все из которых являются экстраплевральными, считается болезнью N1, в то время как медиастинальные лимфатические узлы на участках 2–9которые ипсилатеральны по отношению к злокачественному новообразованию (включая субкаринальные ЛУ для любой стороны заболевания), считаются заболеванием N2. Контралатеральные медиастинальные или прикорневые лимфатические узлы, а также лимфатические узлы станции 1, в которых присутствуют опухолевые клетки, считаются заболеванием N3. Напротив, при раке пищевода N стадия заболевания определяется количеством регионарных ЛУ, пораженных опухолью, при этом N1 соответствует 1-2 положительным (+) ЛУ, N2 используется для 3-6 + ЛУ, а N3 обозначает случаи с >=7 +LN. Кроме того, не все узловые станции, используемые IASLC для рака легких, считаются региональными ЛУ для определения стадии рака пищевода, а некоторые станции называются по-разному, например, обозначение верхних, средних и нижних параэзофагеальных станций ЛУ.
В дополнение к метастазам, злокачественные медиастинальные лимфатические узлы могут быть вызваны лимфомами, группой раковых заболеваний, возникающих из лейкоцитов. Эта группа заболеваний является наиболее частой причиной узловой патологии переднего отдела, но также является частой причиной лимфаденопатии в среднем отделе.
Аденопатия средостения может быть вызвана неопухолевыми новообразованиями. Первичные острые или хронические инфекционно-воспалительные процессы возникают во всех отделах средостения и могут сопровождаться увеличением лимфатических узлов. Точно так же легочные и системные инфекции, такие как пневмония и вирус иммунодефицита человека, могут привести к патологическому увеличению медиастинальных лимфатических узлов. Если медиастинальные лимфатические узлы обызвествлены, это помогает сузить дифференциальный диагноз до таких состояний, как гранулематозные заболевания (гистоплазмоз, туберкулез), силикоз, саркоидоз и пролеченная лимфома. Когда лимфатические сосуды средостения повреждаются, возникающий в результате хилоторакс может нарушать нормальную иммунологическую, пищевую и дыхательную функции.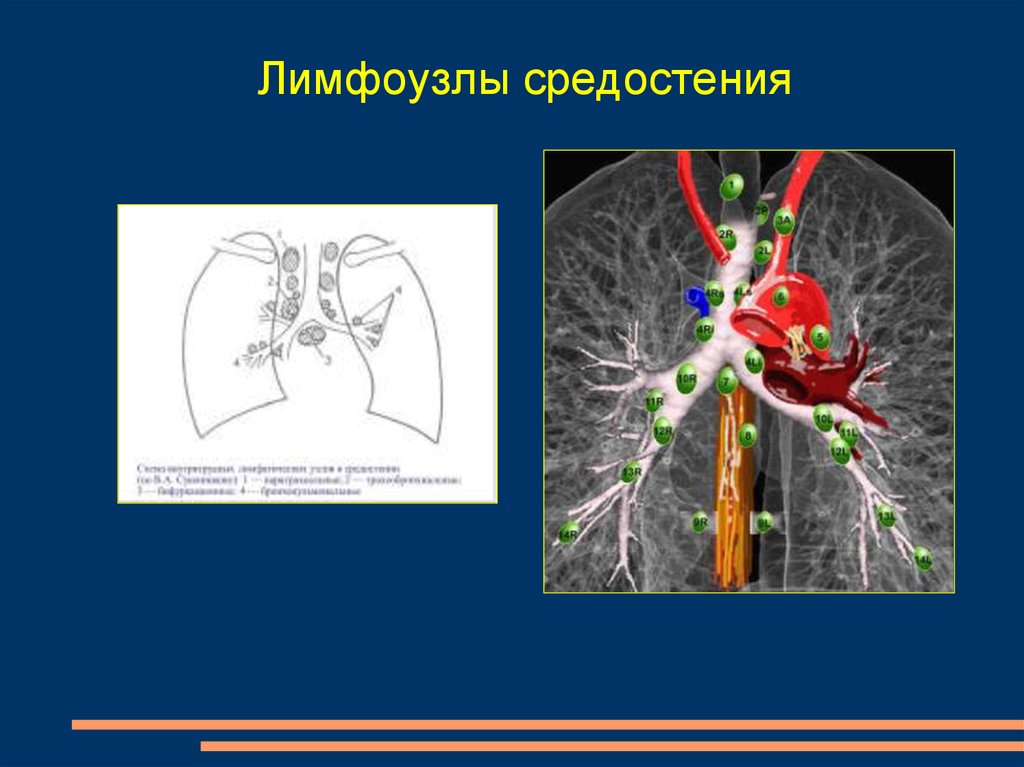
Увеличенные медиастинальные лимфатические узлы могут быть обнаружены случайно, а рекомендации по наблюдению и оценке можно найти в Journal of the American College of Радиология . Например, узлы могут вызывать особое беспокойство, если они большие, асимметричные или демонстрируют авидность ФДГ на ПЭТ/КТ. Узлы размером более 15 мм могут потребовать особого внимания, особенно если нет известного объяснения, например, саркоидоза в анамнезе. Руководящие принципы Американского колледжа радиологии также признают ценность категоризации лимфатических узлов по вышеупомянутым подразделениям, выявления аномальных контуров лимфатических узлов и того, являются ли образования солидными или кистозными.[3][8][12][13][18].
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Рисунок
Медиастинальные лимфатические узлы. Изображение предоставлено S Bhimji MD
Рисунок
Станции медиастинальных лимфатических узлов.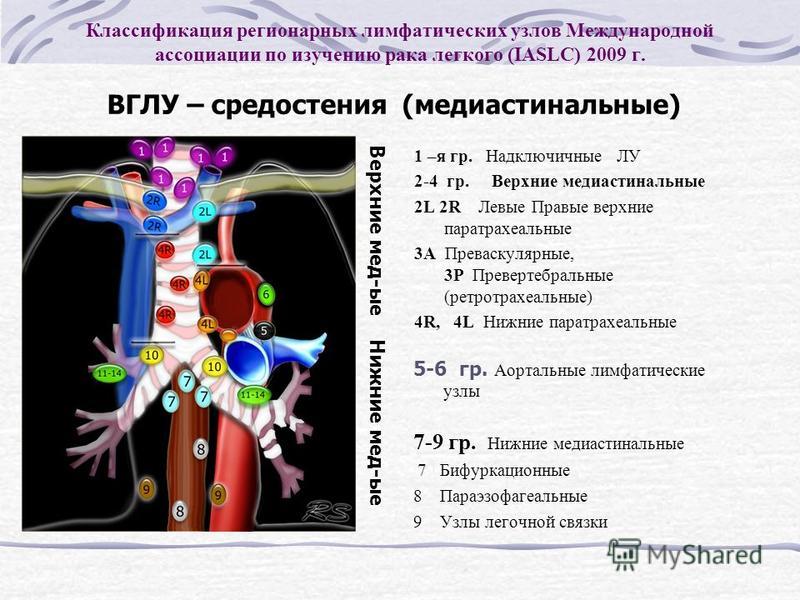 Предоставлено Александрой Лапор
Предоставлено Александрой Лапор
Ссылки
- 1.
Mountain CF, Dresler CM. Классификация регионарных лимфатических узлов для определения стадии рака легкого. Грудь. 1997 июня; 111 (6): 1718-23. [PubMed: 9187199]
- 2.
Craun JB, Banks KP, Clemenshaw MN, Moren RW. Саркоидноподобная реакция неоплазии, вызывающая гиперметаболическую грудную лимфаденопатию в условиях экстраторакальной злокачественности: отчет о двух случаях и обзор дифференциально-диагностических соображений. J Nucl Med Technol. 2012 декабрь; 40 (4): 231-5. [PubMed: 23015478]
- 3.
Картер Б.В., Томияма Н., Бхора Ф.Ю., Росадо де Кристенсон М.Л., Накадзима Дж., Буазель П.М., Деттербек Ф.К., Маром Э.М. Современное определение отделов средостения. Дж. Торак Онкол. 2014 Сентябрь; 9(9 Приложение 2): S97-101. [PubMed: 25396318]
- 4.
Rusch VW, Asamura H, Watanabe H, Giroux DJ, Rami-Porta R, Goldstrow P., члены организационного комитета IASLC.
 Проект IASLC по стадированию рака легких: предложение по новой международной карте лимфатических узлов в предстоящем седьмом издании классификации TNM для рака легких. Дж. Торак Онкол. 2009 май; 4(5):568-77. [PubMed: 19357537]
Проект IASLC по стадированию рака легких: предложение по новой международной карте лимфатических узлов в предстоящем седьмом издании классификации TNM для рака легких. Дж. Торак Онкол. 2009 май; 4(5):568-77. [PubMed: 19357537]- 5.
Аспелунд А., Робчук М.Р., Караман С., Макинен Т., Алитало К. Лимфатическая система в сердечно-сосудистой медицине. Цирк Рез. 2016 05 февраля; 118 (3): 515-30. [В паблике: 26846644]
- 6.
Чхве И., Ли С., Хонг Ю.К. Новая эра лимфатической системы: она больше не является вторичной по отношению к кровеносной системе. Колд Спринг Харб Перспект Мед. 2012 апр;2(4):a006445. [Бесплатная статья PMC: PMC3312397] [PubMed: 22474611]
- 7.
Хсу MC, Иткин М. Лимфатическая анатомия. Tech Vasc Interv Radiol. 2016 дек.; 19(4):247-254. [PubMed: 27993319]
- 8.
Ugalde PA, Pereira ST, Araujo C, Irion KL. Корреляционная анатомия средостения. Клиника торакальной хирургии.
 2011 май; 21(2):251-72, ix. [В паблике: 21477775]
2011 май; 21(2):251-72, ix. [В паблике: 21477775]- 9.
Ляо С., фон дер Вейд П.Ю. Лимфатическая система: активный путь иммунной защиты. Semin Cell Dev Biol. 2015 фев; 38:83-9. [Бесплатная статья PMC: PMC4397130] [PubMed: 25534659]
- 10.
Walker CM, Chung JH, Abbott GF, Little BP, El-Sherief AH, Shepard JA, Lanuti M. Стадирование медиастинальных лимфатических узлов: от неинвазивного к хирургическому. AJR Am J Рентгенол. 2012 июль; 199(1):W54-64. [PubMed: 22733932]
- 11.
Эль-Шериф А.Х., Лау К.Т., Ву К.К., Дрейк Р.Л., Эбботт Г.Ф., Райс Т.В. Карта лимфатических узлов Международной ассоциации по изучению рака легких (IASLC): рентгенологический обзор с иллюстрацией КТ. Рентгенография. 2014 Окт;34(6):1680-91. [PubMed: 25310423]
- 12.
Райс Т.В., Ишваран Х., Фергюсон М.К., Блэкстоун Э.Х., Голдстроу П. Рак пищевода и пищеводно-желудочного соединения: Восьмое издание. Дж. Торак Онкол.
 2017 янв; 12(1):36-42. [Бесплатная статья PMC: PMC5591443] [PubMed: 27810391]
2017 янв; 12(1):36-42. [Бесплатная статья PMC: PMC5591443] [PubMed: 27810391]- 13.
Johnson OW, Chick JF, Chauhan NR, Fairchild AH, Fan CM, Stecker MS, Killoran TP, Suzuki-Han A. Грудной проток: клиническое значение, анатомические вариации, визуализация и эмболизация . Евро Радиол. 2016 авг; 26 (8): 2482-93. [PubMed: 26628065]
- 14.
Теран, доктор медицины, Брок М.В. Стадирование метастазов рака легкого в лимфатические узлы средостения. Дж. Торак Дис. 2014 март; 6(3):230-6. [Бесплатная статья PMC: PMC3949187] [PubMed: 24624287]
- 15.
Колелла С., Вильманн П., Конге Л., Клементсен П.Ф. Эндоскопическое ультразвуковое исследование в диагностике и стадировании рака легкого. Эндоск УЗИ. 2014 окт; 3(4):205-12. [PMC бесплатная статья: PMC4247527] [PubMed: 25485267]
- 16.
Szlubowski A, Herth FJ, Soja J, Kołodziej M, Figura J, Cmiel A, Obrochta A, Pankowski J. Эндобронхиальная аспирационная игла под ультразвуковым контролем при рестадировании немелкоклеточного рака легкого, подтвержденном трансцервикальной двусторонней расширенной медиастинальной лимфаденэктомией — проспективное исследование.