Клебсиелла у детей — симптомы болезни, профилактика и лечение Клебсиеллы у детей, причины заболевания и его диагностика на EUROLAB
Клебсиеллы являются грамотрицательными неподвижными капсульными палочками. Их размер 0,3—1,5×0,6—6 мкм. Располагаются по одиночке, парами или группируясь короткими цепочками. На питательных средах при температуре 35—37 ˚С наблюдается рост клебсиелл, которые формируют слизистые блестящие колонии, похожие на купола.
Обработка бактерицидным мылом зачастую не убивает возбудителя клебсиеллезной инфекции. То же касается и дезинфицирующих средств.
Болезнь у человека возбуждают три вида клебсиелл: К. pneumoniae, К. rhino-scleromatis и К. ozaenae.
Некоторые штаммы К. pneumoniae производят довольно сильный энтеротоксин, который вызывает в разных органах и системах тяжелые морфологические изменения. Данный энтеротоксин приводит к диссеминированному внутрисосудистому свертыванию.
В то же время в области первичных очагов быстро образуются иммунные комплексы, которые оказывают на ткани патогенное влияние.
Клебсиелла у детей бывает таких видов:
- клебиеллезная пневмония;
- клебсиеллезная кишечная инфекция;
- клебсиеллезный сепсис и пр.
Это деление по локализации патологического процесса.
Клебсиеллезная пневмония известна также как пневмония Фридлендера. По симптоматике они похожа на пневмонии другой бактериальной природы – на пневмококковую, например. Болезнь имеет острое начало, температура тела достигает примерно 39 °С, но может быть и выше. Ребенка знобит, появляется кашель (упорный, с отделением кровянисто-слизистой вязкой мокроты).
Аускультация показывает ослабление дыхания над воспалительными очагами и влажные хрипы. С помощью рентгена выявляют мелкоочаговые, крупноочаговые, захватывающие несколько сегментов, а также долевые пневмонии. Течение болезни в основном тяжелое. Клебсиеллезная пневмония в большинстве случаев сочетается с другими инфекциями – например, респираторно-вирусными.
Течение болезни в основном тяжелое. Клебсиеллезная пневмония в большинстве случаев сочетается с другими инфекциями – например, респираторно-вирусными.
При клебсиеллезной пневмонии патологический процесс переходит на альвеолы, наблюдается экссудация с геморрагическим компонентом. Пневмония имеет склонность к абсцедированию; есть случаи, при которых развивается гангрена легкого.
Клебсиеллезная кишечная инфекция по симптоматике и течению сходна с гастроэнтероколитом, энтероколитом, гастроэнтеритом и энтеритом. Начало заболевания характеризуется повышением температуры до уровня 37—39 °С, рвотой или повторными срыгиваниями (у младенцев), жидким стулом. Стул имеет обильный, водянистый характер, оттенок желто-зеленый, в испражнениях наблюдаются непереваренные частицы пищи. У 10—12% больных детей в испражнениях бывает кровяная примесь.
От детей могут поступать жалобы на боли в животе, которые имеют приступообразный характер. У младенцев и дошкольников родители наблюдают приступы беспокойства, которые усиливаются при пальпации живота.
На протяжении 2-12 дней держится высокая температура (в среднем от 3 жо 5 суток). В первые 2-3 суток болезни у ребенка случается рвота 2-8 раз на протяжении дня и ночи. Далее рвота либо прекращается либо случается довольно редко. От 3 до 10 суток длится диарея. Частота стула зависит от каждого конкретного случая. Иногда стул случается около 20 раз.
Тяжелые формы заболевания происходят с развитием токсикоза с эксикозом на протяжении 3-6 дней. У половины заболевших детей наблюдается выраженность обезвоживания II степени. Рвота почти во всех случаях повторяется, случается от 3 до 7 раз за день и ночь.
Фиксируют такие симптомы:
- заторможенность
- вялость
- резкое снижение аппетита.
Изменений паренхиматозных органов нет, нейротоксикоза нет. В периферической крови – умеренный лейкоцитоз, в половине случаев бывает нейтрофилез и в трети случаев фиксируют повышенную СОЭ (до 15—20 мм/ч). Кишечная инфекция вызывается множеством штаммов клебсиелл.
Особенности заболевания у новорожденных и детей 1-го года жизни.
Кишечная инфекция у грудничков имеет острое начало, бурно развивается кишечный синдром, гемодинамические и метоболические нарушения. Дети отказываются сосать грудь, родители замечают их вялость и срыгивания. Стул у младенцев в данном случае происходит от 8 до 20 раз в сутки. Испражнения жидкой консистенции, водянистые, желто-зеленого оттенка, есть примесь мутной слизи. У некоторых заболевших малышей кишечные расстройства проявляются недолгосрочным учащением и разжижением стула.
Большинство новорожденных, заболевших клебсиеллезом, находятся в тяжелом состоянии. За первые несколько суток болезни они теряют значительный процент массы тела (100-500 г) из-за токсикоза с дегидратацией. Кожа приобретает серовато-бледный оттенок, возникает выраженный периоральный и периорбитальный цианоз, а также адинамия, гипорефлексия, заторможенность.
Энтероколит может быть некротизирующим, из-за этого в стуле появляется кровь и возникают осложнения – перфорация кишечника. Из-за присоединения пневмонии случается дыхательная недостаточность. Когда кишечная инфекция сочетается с пневмонией, на первый план среди симптомов выходит нейротоксикоз. У детей проявляются такие симптомы клебсиеллеза:
- судороги
- гипертермия
- гемодинамические расстройства
- ацидоз
- умеренно выраженные симптомы энтерита или энтероколита.
Могут случаться такие осложнения:
- токсический гепатит
- энцефалитические реакции
- токсико-инфекционный миокардит
- гнойный менингит
- геморрагический синдром.
В периферической крови у новорожденных и грудничков наблюдаются лейкоцитоз и гиперлейкоцитоз (35 х 109/л) с появлением миелоцитов до 3—7%, а также умеренная анемия.
У новорожденных клебсиеллы могут размножаться в первую очередь на коже головы в месте прикрепления электродов для мониторного наблюдения, на участках повреждения акушерскими щипцами и в области гематомы. Развивается инфильтративно-некротический процесс вплоть до развития флегмоны и абсцессов.
Развивается инфильтративно-некротический процесс вплоть до развития флегмоны и абсцессов.
Клебсиеллезный сепсис часто поражает костную и суставную ткани. Симптоматически это проявляется как припухлость припухлостью в области воспаления ткани или сустава, ограниченное движение пораженной конечности, резкое беспокойство малыша при пеленании. Температура тела в норме. Обычно патологический процесс локализуется в области бедренной, плечевой и болыпеберцовой костей.
Если Вами ранее были выполнены какие-либо исследования, обязательно возьмите их результаты на консультацию к врачу. Если исследования выполнены не были, мы сделаем все необходимое в нашей клинике или у наших коллег в других клиниках.
У Вас ? Необходимо очень тщательно подходить к состоянию Вашего здоровья в целом. Люди уделяют недостаточно внимания симптомам заболеваний и не осознают, что эти болезни могут быть жизненно опасными. Есть много болезней, которые по началу никак не проявляют себя в нашем организме, но в итоге оказывается, что, к сожалению, их уже лечить слишком поздно.
Если Вы хотите задать вопрос врачу – воспользуйтесь разделом онлайн консультации, возможно Вы найдете там ответы на свои вопросы и прочитаете советы по уходу за собой. Если Вас интересуют отзывы о клиниках и врачах – попробуйте найти нужную Вам информацию в разделе Вся медицина. Также зарегистрируйтесь на медицинском портале
Чем опасна клебсиелла для грудничка: симптомы и лечение инфекции
23 ноября 2018 14:00Клебсиелла относится к условно-патогенным бактериям и именно ее зачастую считают «виновницей» развития дисбактериоза у малышей.
В наши дни все чаще у грудничков встречаются инфекционные заболевания, вызываемые патогенными микроорганизмами. Одними из них являются палочки Фридлендера, провоцирующие появление клебсиеллы. Несмотря на то, что эти палочки считаются достаточно безобидными и могут находиться повсюду, стремительное увеличение их количества имеет самые неожиданные последствия. В чем же причины их размножения клебсиеллы, какие симптомы можно наблюдать при данном заболевании и есть ли необходимость в его лечении, рассмотрим подробнее в данной статье.
Практически каждый родитель боится в результатах анализов на дисбактериоз увидеть это страшное слово – «клебсиелла». Однако данную бактерию можно встретить практически у всех, так как она является одной из множества бактерий, живущих в организме человека, никак себя не проявляя. Но такое «затишье» длится лишь до тех пор, пока в организме сохраняется оптимальная микрофлора. Если же количество «хороших» бактерий по каким-то причинам резко уменьшается, то патогенные бактерии, к которым относится клебсиелла, становится опасными.
Однако данную бактерию можно встретить практически у всех, так как она является одной из множества бактерий, живущих в организме человека, никак себя не проявляя. Но такое «затишье» длится лишь до тех пор, пока в организме сохраняется оптимальная микрофлора. Если же количество «хороших» бактерий по каким-то причинам резко уменьшается, то патогенные бактерии, к которым относится клебсиелла, становится опасными.
Активизироваться клебсиелла начинает не спонтанно. На это ее могут спровоцировать несколько причин:
- Ослабление иммунитета
- Несоблюдение гигиенических условий
- Неочищенная вода и продукты питания
- Контакт с носителем инфекции
Важно помнить, что в основном патогенные микроорганизмы проникают в ткани новорожденного через мать в процессе родов или после них. Но так же существуют и другие штаммы, проникающие в организм крохи через пыль, еду, воду и шерсть животных.
Интересно, что по данным исследований ВОЗ, клебсиелла является потенциальным кандидатом на роль супербактерий, то есть бактерий, устойчивых к антибиотикам. А это значит, что они представляют собой угрозу для существования людей как вида в целом.
А это значит, что они представляют собой угрозу для существования людей как вида в целом.
Для формирования супербактерий достаточно двух причин
Не до конца вылеченные инфекции. Зачастую после начала приема антибиотиков, пациенту становится значительно легче и он преждевременно прекращает прием назначенных медикаментов или же врач просчитывается с назначаемым курсом лечения, что так же может повлиять на развитие супербактерий.
Читайте такжеНасморк у грудного ребенка: причины появления и правильное лечениеИспользование антибиотиков в большом количестве. Организм человека со многими инфекциями, включая и кишечные сбои, способен справиться самостоятельно. А злоупотребление антибиотиками крайне негативно сказывается на организме человека, так как применение таких сильных медикаментов приводит к тому, что бактерии адаптируются к ним, а значит, перестают на них реагировать.
Так как клебсиелла считается одной из самых распространенных больничных инфекций, она автоматически становится очень опасной, так как в больницах систематически применяются антибиотики.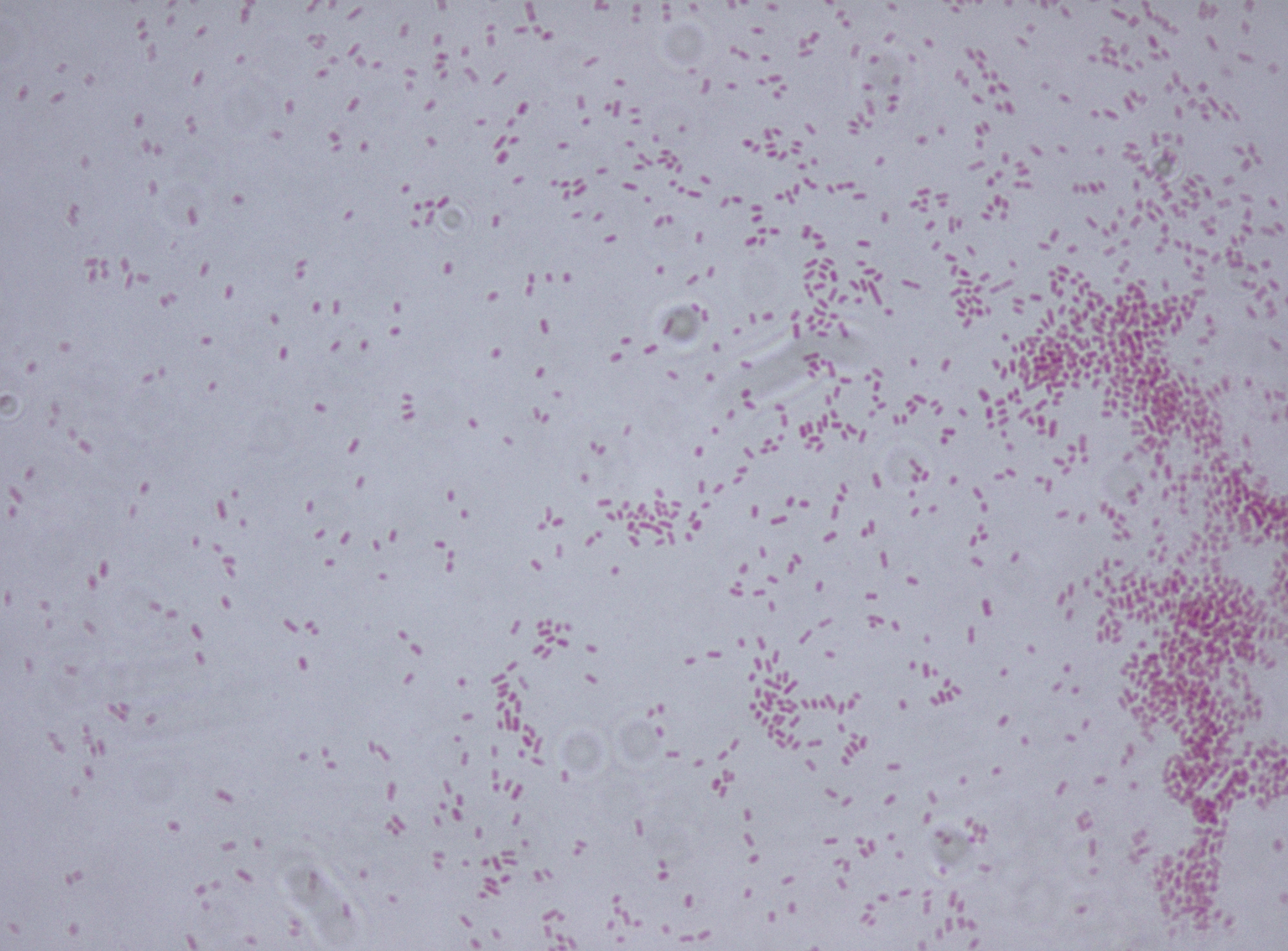 Это чревато тем, что в любой больнице может сформироваться очень устойчивый штамм, а пациенты этой клиники автоматически станут носителями данной супербактерии.
Это чревато тем, что в любой больнице может сформироваться очень устойчивый штамм, а пациенты этой клиники автоматически станут носителями данной супербактерии.
Чаще всего клебсиелла поражает кишечник новорожденного и больше этому подвержены ослабленные и недоношенные малыши. У грудничков клебсиеллез практически всегда протекает достаточно в тяжелой форме. Опасность данного заболевания состоит в том, что ее симптоматику очень легко перепутать с другими воспалительными процессами желудочно-кишечного тракта, такими как:
- повышение температуры тела до 37-39 градусов
- частое срыгивание или рвота, иногда это достигает 6-8 раз в сутки
- очень частый и обильный жидкий стул до 20 раз в сутки
- может присутствовать примесь крови в кале новорожденного
- присутствует сероватый оттенок кожных покровов младенца
- болезненность в области живота, вследствие чего малыш становится капризным
- присутствует вялость и заторможенность
- отсутствует аппетит
Инфекции, вызванные клебсиеллой, длятся дольше остальных кишечных инфекций, чем и отличаются от других подобных заболеваний. В связи с сильным обезвоживанием организма грудничка возникает угроза его жизни! Именно поэтому не стоит заниматься самолечением и при любой кишечной инфекции необходимо своевременно проконсультироваться с лечащим врачом.
В связи с сильным обезвоживанием организма грудничка возникает угроза его жизни! Именно поэтому не стоит заниматься самолечением и при любой кишечной инфекции необходимо своевременно проконсультироваться с лечащим врачом.
Клебсиеллу возможно обнаружить лишь с помощью лабораторных исследований. Для этого у пациента берут часть каловых или рвотных масс, мазки из носа, анализ крови, в котором могут произойти некоторые изменения.
Анализ кала на дисбактериоз может быть непоказательным, поэтому в странах с хорошо развитой медициной данный анализ считается бесполезным и не применяется в таких случаях.
Причины, при которых необходимо лечить клебсиеллез:
- превышенное количество бактерии в кале
- угнетенное самочувствие ребенка
Если же у ребенка наблюдается хороший аппетит, и он не теряет вес, а набирает его по норме, то лечить клебсиеллез нет необходимости.
В чем заключается лечение клебсиеллеза?
Применение лечения с помощью антибиотиков при таком заболевании как клебсиеллез применяется крайне редко, только лишь в тяжелых случаях. Основная методика лечения при более легкой форме заболевания заключается в гидратации, то есть в восполнении жидкости в организме. Зачастую родители не могут справиться с данной проблемой, поэтому им предлагается госпитализация в клинику.
Существует несколько рекомендаций для профилактики клебсиеллеза:
- кормить ребенка необходимо только тогда, когда он голоден, так как печень играет немаловажную роль в поддержании иммунной системы человека, а значит, она не должна быть перегружена
- в рацион маленького ребенка или его мамы (при грудном вскармливании) обязательно должно входить большое количество овощей, фруктов, зелени и круп
- использовать антибиотики в самых крайних случаях, только тогда, когда без них действительно невозможно обойтись.

Симптомы клебсиеллы | Пробиотики Нормофлорины – лечение дисбактериоза
Назад к списку18.06.2012
Загрузка…В летний период становятся актуальны заболевания вызванные инфекционными агентами.
Особенно активны микроорганизмы семейства энтеробактерий – грамотрицательные, палочкообразные, с жгутиками для передвижения и прикрепления, факультативные анаэробы: кишечная палочка, сальмонелла, клебсиелла и др. Так, клебсиелла – klebsiella, может существовать в почве, воде, месяцами оставаясь жизнеспособной, сохраняется на пище и пыли.
Клебсиеллы могут попасть в организм через желудочно-кишечный тракт, с плохо вымытых рук, овощей и фруктов, с водой, с почвой.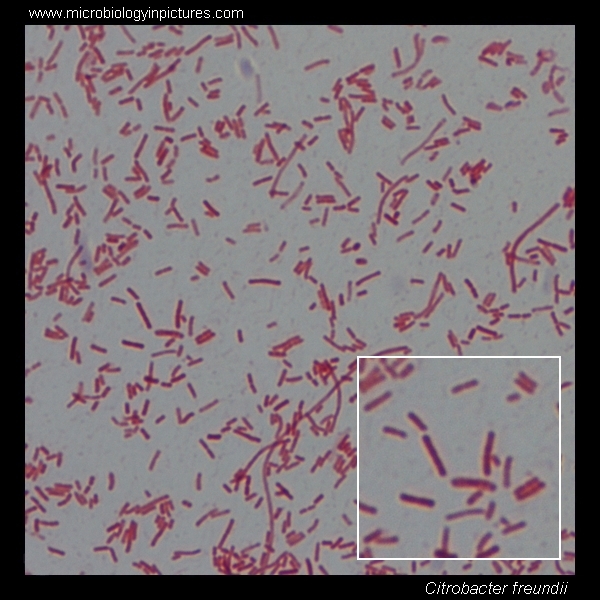 Однако, этот микроорганизм входит в группу условно-патогенной микрофлоры и определяется у абсолютно здоровых детей и взрослых, считается одним из элементов нормальной флоры кишечника.
Однако, этот микроорганизм входит в группу условно-патогенной микрофлоры и определяется у абсолютно здоровых детей и взрослых, считается одним из элементов нормальной флоры кишечника.
При этом, клебсиелла является одной из самых распространённых внутрибольничных инфекций, т.к. она устойчива к действию факторов окружающей среды, высоким температурам. Хотя, за несколько минут она гибнет от дезинфектантов, а при очень высоких температурах через 1-1,5 часа. При несоблюдении надлежащих правил гигиены, санитарных норм в помещениях, встречаются случаи заражения новорожденных клебсиеллой в роддомах. Малыш постоянно плачет и не может заснуть, его беспокоят колики и частый понос. А причина – клебсиелла – бактерия, устойчивая к губительному действию внешней среды, покрытая плотной капсулой.
Факторы развития клебсиеллеза
Клебсиеллы относятся к одному семейству с бактериями рода Serratia и Enterobacter. Этими возбудителями, особенно Serratia, обладающий наибольшей лекарственной устойчивостью, обусловливаются вспышки инфекции в стационарах, в связи с загрязнением ряда медикаментозных средств, лекарственных растворов, применяемых в терапии органов дыхания. Их трудно, но можно дифференцировать только с помощью специальных проб. Klebsiella Enterobacter и Serratia, вызывающие внутрибольничную пневмонию, инфекцию мочевого тракта, бактериемию, обладают различной чувствительностью к противомикробным препаратам.
Этими возбудителями, особенно Serratia, обладающий наибольшей лекарственной устойчивостью, обусловливаются вспышки инфекции в стационарах, в связи с загрязнением ряда медикаментозных средств, лекарственных растворов, применяемых в терапии органов дыхания. Их трудно, но можно дифференцировать только с помощью специальных проб. Klebsiella Enterobacter и Serratia, вызывающие внутрибольничную пневмонию, инфекцию мочевого тракта, бактериемию, обладают различной чувствительностью к противомикробным препаратам.
Позитивное окрашивание. Клетка K. pneumaniae. Ув. x6000
Если защита организма человека по какой то причине ослаблена: снижен общий иммунитет, часто грипп, ОРВИ, применение антибиотиков, употребление загрязненных, некачественных продуктов, сахарный диабет, алкоголизм и др., клебсиелла начинает активно размножаться, выделять токсины, вызывая эндотоксимию и воспалительные процессы в разных органах. Развиваются такие заболевания, как воспаление легких, воспалительные заболевания мочевыводящих путей, менингит, конъюнктивит, кишечные инфекции, сепсис и достаточно редкие болезни – озена (зловонный насморк), риносклерома.
Наиболее часто клебсиелла вызывает пневмонию и поражение кишечника. У взрослых людей чаще встречается пневмония, вызванная палочкой Фридлендера. В связи с особенностью иммунитета новорожденных и недостаточностью у них нормальной микрофлоры на коже, в дыхательных путях и особенно в кишечнике – клебсиелла – Klebsiella oxytoca – чаще вызывает поражения желудочно-кишечного тракта – толстого кишечника.
Симптомы клебсиеллы (клебсиеллёза) в ЖКТ у грудничков
Симптомы клебсиеллы у малышей схожи с симптомами дисбактериоза: вздутие, метеоризм, колики, срыгивание. Но чаще проявляются – жидким стулом со слизью, кровью и резким запахом, повышением температуры, лихорадкой, болями в животе и сильным обезвоживанием организма. В зависимости от того, какой иммунитет у малыша, течение заболевания может протекать как в лёгкой форме, так и грозить тяжелыми инфекционными осложнениями. Если клебсиелла в организме быстро размножается, выделяет токсины, нарастает интоксикация, обезвоживание, то заболевание может проявиться в течение нескольких часов и потребует срочной госпитализации ребенка.
Поэтому, при любом расстройстве стула, необходимо обратиться к врачу, сдать кал ребёнка на анализ, пройти обследование, чтобы точно выявить, какие именно бактерии вызвали изменение состояния ребёнка. Большую роль в восстановлении иммунитета и нормальной микрофлоры у новорожденного играет грудное вскармливание. При высокой обсеменённости клебсиеллой и тяжёлой форме заболевания, лечении ребенка в больнице, назначают сложную терапию с применением антибиотиков. Если заболевание грудничка протекает в лёгкой форме, то для коррекции микрофлоры кишечника назначают пробиотики. Синбиотики – Нормофлорины Л и Б – обладают активным противовоспалительным, антисептическим и питательным действием, что важно при клебсиеллёзной инфекции. Ребенок может чувствовать себя нормально, а при обследовании находят в анализах повышение количества клебсиелл. Тогда препараты с лакто- и бифидобактериями назначают для вытеснения излишнего количества клебсиеллы, повышения иммунитета, улучшения собственной полезной микрофлоры.
Симптомы клебсиеллы в других органах и системах
Если клебсиеллы попадают в мочевыделительную систему, то они способны вызывать уретрит, пиелонефрит, со стойким рецидивирующим течением, плохо поддающимся терапии и часто измененной чувствительностью к антибиотикам. В редких случаях клебсиеллёза, возможно такое осложнение, как – озена – зловонный насморк, с поражением слизистой носа, образованием гнойных, болезненных, кровоточащих корок.
Симптомы и признаки инфекций мочевыводящих путей, желчного пузыря и в брюшной полости, вызываемых клебсиеллами, не отличаются от симптоматики, обусловленной кишечной палочкой. Развиваются они чаще у больных сахарным диабетом и у пациентов, получающих антимикробные препараты, к которым устойчив возбудитель заболевания. Клебсиелла является также важным этиологическим фактором септического шока.
Клебсиелла известна как фактор развития легочных заболеваний, однако, среди причин, вызывающих бактериальную пневмонию, имеет около 1% всех случаев. Встречается преимущественно у мужчин в возрасте старше 40 лет, с хроническими бронхолегочными заболеваниями, больных сахарным диабетом и лиц с алкоголизмом. У пожилых людей, грамотрицательные бактерии заселяют ротоглотку и могут распространиться по дыхательному тракту, вызывая пневмонию или гнойный бронхит.
Клинические симптомы клебсиеллёзной пневмонии сходны с проявлениями при пневмококковой пневмонии, но чаще характеризуются более тяжелым течением: внезапным началом, ознобов, стойким повышением температуры тела, продуктивным кашлем, иногда с прожилками крови и резким запахом, с сильными плевральными болями, появлением одышки. Больные часто находятся в прострации и бредовом состоянии, за счет интоксикации. Чаще всего очаг воспаления располагается в правой верхней доле легкого, но может быстро прогрессировать, если лечение не проводится и распространиться с одной доли на другую. Появляются цианоз и одышка, могут возникнуть желтуха, рвота, диарея. Выявляется, при обследовании, образование плеврального выпота, уплотнение легочной ткани, или некротизирующая пневмония, с быстрой кавернизацией. На фоне интоксикации определяется снижение количества лейкоцитов в периферической крови, а не повышение, как при воспалении. Гораздо чаще наблюдаются абсцессы и эмпиемы легких. Это объясняется способностью клебсиелл вызывать деструкцию ткани. Не всегда выявляются характерные признаки при рентгеновском обследовании: уменьшение объема легкого, его уплотнение, эмфизематозные изменения. При медленном прогрессировании инфекционного воспалительного процесса может развиться хронический некротизирующий пневмонит, напоминающий туберкулез, с продуктивным кашлем, слабостью, выраженной анемией.
Лечение клебсиеллезов
Лечение заболеваний, вызванных клебсиеллой, зависит от локализации и выраженности патологического процесса. Антибиотики назначают в тяжелых случаях по чувствительности, при легком течении или только обнаружении в анализах повышения клебсиелл – не применяют. Обязательно используют разнообразные препараты, восстанавливающие кишечную микрофлору.
Клебсиелла пневмония
Как правило, антимикробную терапию рекомендуют начинать еще до получения результатов посева и определения лекарственной чувствительности к антибиотикам. В этом случае биокомплексы Нормофлорины, содержащие продукты жизнедеятельности живых лакто- и бифидобактерий с активным антисептическим, противовоспалительным действием, оказывают лечебный эффект при клебсиеллёзах, что доказано научными исследованиями и многолетней практикой, как у новорожденных, беременных, кормящих, так и взрослых и пожилых.
Клебсиелла у детей: симптомы, терапия и последствия
Детская иммунная система слабая, и организм часто подвергается негативному воздействию патогенных бактерий. Выявить их и назначить адекватное лечение позволяют лабораторные анализы. Наиболее распространенными бактериями, выявляемыми у маленьких пациентов, являются различные виды кокков. Иногда анализ выявляет у детей клебсиеллу. Что это за бактерия и чем она опасна для ребенка, попробуем разобраться.
Что такое клебсиелла?
Клебсиеллы (Klebsiella) – условно-патогенные прокариотические микроорганизмы. Они входят в одно большое семейство таких энтеробактерий, как кишечная палочка, сальмонеллы и прочие. Бактерии являются грамотрицательными одиночными капсульными палочками. Имеют форму неправильного овала размером 0,3-1,25 мкм.
Клебсиеллы разлагают практически все углеводы, растут в среде с цианистым калием. Они сохраняют жизнеспособность после обработки бактерицидным мылом и препаратами дезинфектантами. Из-за устойчивости ко многим антибактериальным препаратам данные энтеробактерии причислены к наиболее опасным. Они погибают при нагревании в течение часа до температуры 65 градусов. Чувствительны к действию растворов хлорамина, фенола.
Микроорганизмы имеют широкое распространение. Встречаются в кале человека, кожном покрове, слизистых дыхательных путей. Их можно обнаружить в почве, воде, растительных продуктах.
У взрослых и у детей бактерия клебсиелла вызывает пневмонию, риносклерому, озену, поражение мочеполовых органов, кишечные инфекции. Патогены нередко выделяют в составе микрофлоры новорожденных сразу после рождения. Заражение грудничков может привести к формированию тяжелых поражений легочной ткани, кишечных инфекций, токсикосептических состояний со смертельным исходом.
Классификация
Род капсульных палочек Клебсиелла подразделяют на биохимические виды. Классифицируют бактерии на три основных и несколько дополнительных видов. К основным относятся:
- Клебсиелла пневмонии или палочка Фридлендера. Мелкая коккобацилла, не образующая спор. Может располагаться одиночно, попарно или образовывать целые колонии (на агаризованных питательных средах). Поражает в основном слизистые нижних дыхательных путей, является одним из основных возбудителей пневмонии. Также становится причиной инфекций мочевыводящих путей, гнойных воспалений паренхимы печени, селезенки. Встречается при смешанных инфекциях. При кишечных инфекциях у детей стафилококк и клебсиелла обнаруживаются чаще всего. Но наиболее часто возбудитель вызывает бронхиты и бронхиопневмонии.
- Клебсиелла озены (палочка Абеля-Левенберга). Вызывает заболевания верхних дыхательных путей. Воспаление сопровождается сухими клейкими выделениями, издающими зловонный запах, атрофией слизистой и скелета носа. Наиболее часто озена диагностируется в возрасте 8-16 лет. Патологический процесс может распространяться на гортань, трахею. Часто приводит к потере обоняния.
- Клебсиелла риносклерома (палочка Фриша-Волковича). Поражает слизистые оболочки дыхательных путей. В носу и гортани возникают плотные белые узелки с вязкой мокротой. В бронхах появляются инфильтраты, которые позже рубцуются.
- Клебсиелла окситока. Поражает суставы, глаза, оболочки головного мозга, органов мочеполовой системы. Палочки вызывают септикопиемию и становятся причиной заражения крови.
У маленьких пациентов чаще всего выявляется палочка Фридлендера. А вот клебсиелла окситока у детей обнаруживается нечасто.
Как патоген попадает в организм ребенка
Патогенные палочки считают возбудителем внутрибольничных инфекций. Патоген может попасть с рук зараженного персонала, плохо обработанных катетеров. Внебольничных условиях клебсиелла обнаруживается на поверхности овощей, замороженной рыбы, в молочных продуктах. Энтеробактерии выживают и даже размножаются в холодильнике.
Причина появления клебсиеллы в кале у ребенка не всегда инфекционное заболевание. Энтеробактерии могут длительное время находится в организме ребенка, не вызывая патологических изменений. Активизироваться возбудитель может в результате длительного применения антибиотиков, плохого питания, проблем с пищеварением.
Но все же чаще клебсиелла у детей появляется вследствие следующих действий:
- употребление зараженной, некипяченой воды;
- ребенок ест сырые, часто недостаточно хорошо промытые фрукты и овощи;
- несоблюдение ребенком простых правил гигиены: не моет руки после посещения туалета, перед едой, после прогулок;
- ненадлежащая гигиена матери: плохо моет грудь до и после кормления, недостаточно хорошо обрабатывает свои руки;
- близкий контакт с больным человеком: клебсиелла передается воздушно-капельным путем, во время чихания, при кашле;
- использование предметов больного человека: маленькие дети тащат в рот игрушки, которыми играл больной ребенок.
Несмотря на то что капсульные бактерии отличаются высокой живучестью, для их активного роста необходимы определенные условия. В группу риска входят:
- дети грудного возраста;
- рожденные раньше установленного срока;
- имеющие генетические или врожденные пороки развития;
- дети из асоциальных семей: мать страдает алкоголизмом или наркоманией, плохо следит за ребенком;
- ВИЧ-инфицированные;
- часто болеющие и проходящие лечение в условиях стационара.
У некоторых детей благоприятной средой для размножения клебсиеллы становиться наличие аллергии.
Клиническая картина
После попадание капсульной бактерии в организм, наступает инкубационный период. Его продолжительность зависит от типа патогена, состояния иммунитета и ряда других индивидуальных особенностей. Срок от момента проникновения в организм до появления первых симптомов может составлять от нескольких часов до нескольких суток.
В период активного развития клебсиеллы симптомы у ребенка немного отличаются и зависят от локализации энтеробактерии. Если патоген поразил дыхательные пути, то клиническая картина будет следующей:
- резкое повышение температуры;
- лихорадочное состояние, озноб;
- затруднение носового дыхания, появление слизистых выделений со зловонным запахом;
- покраснение, отек гортани;
- появляется кашель сначала дневной сухой, затем мокрый больше в ночное время;
- ребенок не высыпается, плачет и капризничает;
- нарушение частоты и глубины дыхания.
При поражении ЖКТ клебсиеллой у детей наблюдаются следующие клинические проявления:
- сначала приступообразные, затем интенсивные боли в животе;
- усиливается газообразование;
- тошнота, не всегда сопровождающаяся рвотой;
- ребенок отказывается от еды, даже от любимых продуктов;
- нарушается стул: становится жидким, частым, в кале появляется видимая глазу слизь, прожилки крови;
- из-за частого стула раздражается анальное отверстия, возникает гиперемия, иногда мелкая сыпь;
- повышение температуры наблюдается у ослабленных детей или при длительном неоказании медицинской помощи.
Клебсиелла в зеве у ребенка
Микрофлора рта включает огромное число разных микроорганизмов. Бактерии попадают не только с продуктами, но и при вдыхании, разговоре. В норме клебсиелла у ребенка в 3 года или в любом другом возрасте должна отсутствовать. Наличие энтеробактерии говорит о том, что в организме идет воспалительный процесс.
Чаще всего в зеве выявляют у ребенка клебсиеллу пневмонию, окситоку, озену, ринослерому. Бактерии вызывают тяжелые заболевания дыхательных путей. По статистике 35,7% из них имеют летальный исход. Разные виды клебсиеллы вызывают определенные заболевания.
- Клебсиелла риносклерома является возбудителем склеромы. Это воспалительный процесс, затрагивающий стенки дыхательных путей с образованием соединительнотканных узелков (гранулемы). Опасность заболевания в том, что оно начинает развиваться спустя 2-3 года после попадания в организм палочки Фриша-Волковича. Симптомы такие же, как и при простудном заболевании. Родители начинают самостоятельно лечить ребенка, чем усложняют ситуацию.
- Клебсиелла озена вызывает одноименное виду заболевание. Оно характеризуется атрофическим процессом структур носа (слизистая, хрящи и прочие). Озена встречается не часто 1-3% от всех заболеваний носа. Чаще всего болеют девочки в возрасте 7-8 лет. Патология может вызвать осложнения: гайморит, сфеноидит, конъюнктивит, кератит, хронический средний отит.
- Клебсиелла пневмония несмотря на свое название воспаление легочной ткани вызывает у 2-4 % всех больных легочными патологиями. Но заболевание очень опасное, особенно если возникает у ребенка. Основные причины развития у детей клебсиеллы pneumoniae – слишком слабый иммунитет и частые патологии респираторного тракта. Фридлендеровская пневмония часто вызывает легочные и внелегочные осложнения: экссудативный плеврит, абсцессы, сепсис.
Клебсиелла в кале
Клебсиелла пневмония, окситока и другие – представители нормальной флоры кишечника при условии, если их численность менее 10⁴. При более высоком содержании капсульная бактерия вызывает гастроэнтерологические заболевания.
У ребенка клебсиелла в кал попадает из кишечника. В пищеварительном органе энтеробактерия вырабатывает энтеротоксины. Это полипептидные бактерии нарушающие способность всасывать питательные вещества из просвета кишки. Такое патологическое состояние значительно увеличивает риск нарушения баланса флоры кишечника и развития других болезнетворных организмов. Основной признак наличия в кишечнике энтеротоксина – жидкий водянистый стул у ребенка.
Помимо энтеротоксина, клебсиелла вырабатывает мембранотоксин. Они увеличивают проницательность оболочки клетки для ионов водорода, калия, натрия. Это приводит к разрушению клеток и нарушению рН крови.
Дисбактериоз у детей чаще всего развивается из-за того, что в кишечнике «хозяйничает» клебсиелла пневмония. В кале у ребенка при сдаче анализов могут присутствовать и другие патогенные бактерии. Обычно это связано с тем, что капсульная энтеробактерия сильно ослабляет иммунитет, что способствует присоединению вторичных инфекций. Дети начинают часто болеть простудными, вирусными заболеваниями. Слабый организм – наилучшая питательная среда для клебсиеллы.
Клебсиелла у новорожденных
Наилучший благоприятный фон для развития клебсиеллы – слабый организм. Поэтому чаще всего бактерия поражает маленьких детей, у которых только начинает формироваться иммунитет.
Дети, рожденные раньше срока, больше других подвержены инфекционным заболеваниям. Опасность в том патологический процесс у слабых детей прогрессирует ускоренными темпами. Заражение обычно происходит сразу после выписки. Стерильность стационара резко сменяется на обычные условия, организму сложно противостоять такому количеству микробов. У недоношенных детей клебсиелла может одновременно вызывать кишечные расстройства и пневмонию.
Но клебсиелла нередко встречается и у детей, которые родились в срок. Симптомы поражения капсульной бактерией, такие же, как и при кишечных расстройствах:
- Малыш начинает часто испражняться, при этом стул с каждым разом становится более жидким.
- Меняется цвет кала, он становится желто-зеленого оттенка. Наблюдаются слизь, фрагменты непереваренной пищи (если малыш уже на прикорме), прожилки крови. Появляется специфический кислый запах.
- Обильные срыгивания «фонтаном». Такой симптом должен насторожить родителей, он возникает только при поражении кишечника патогенными микробами.
- Вздутие живота. При достраивании малыш начинает плакать, постоянно капризничает.
- При возникновении клебсиеллы у ребенка в год нередко наблюдается повышение температуры. Это свидетельство того, что уже есть иммунитет и организм пытается бороться с патогеном.
Как проводится диагностика
При симптоматике, похожей на развитие респираторных заболеваний или патологий ЖКХ, необходимо сразу показать ребенка педиатру. Самолечение, особенно грудных детей, может привести к фатальным последствиям.
Врач в первую очередь проводит анамнез. По симптомам можно понять, какую именно систему поражает энтеробактерия. После физикального осмотра доктор назначает различные лабораторные анализы:
- Посев на питательные среды. В кале у ребенка клебсиеллу на пневмонию выявляют с помощью анализа на дисбактериоз. Тест также показывает наличие резистентности к тем или иным антибактериальным препаратам. Результаты являются основой для определения антибиотика, с помощью которого будет осуществляться терапия.
- Окрашивание по Граму. Метод позволяет классифицировать бактерии в зависимости от строения и клеточной стенки на грамположительные и грамотрицательные. Способ позволяет дифференцировать стафилококк пневмококк от клебсиеллы пневмонии.
- Серологические методы позволяют определить тип возбудителя и наличие к нему антител. Исследуемый биоматериал – кровь из вены. У совсем маленьких детей подобное исследование проводят редко.
- Копрограмма. С помощью метода диагностируют заболевание, особенности инфекционного процесса. Анализ назначают в любом возрасте.
При подтверждении наличия в организме у детей клебсиеллы лечение назначается с учетом типа бактерии, возраста ребенка. Антибактериальная терапия проводиться под строгим контролем педиатра. В некоторых случаях ее проводят стационарно.
Клебсиелла у ребенка: чем лечить?
Терапевтическая тактика зависит от возраста пациента, особенностей протекания и стадии заболевания. В большинстве случаев лечение проводится амбулаторно, исключение – груднички с врожденными патологиями или очень слабым иммунитетом.
Лечение проводится с помощью антибактериальных препаратов. Но грудным детям использовать антибиотики нежелательно, поскольку они имеют большое число побочных эффектов. их заменяют на бактериофаги. Особенности терапии клебсиеллы бактериофагами:
- препарат принимают трижды в день перед едой (за 20-30 минут), если ребенок на грудном вскармливании можно пить лекарство перед кормлением;
- максимальная разовая доза для детей от рождения до полугода составляет 5 мл;
- 6-12 месяцев – 10 миллилитров;
- от года до трех – 15 мл;
- от трех до семи – 20 мл;
- для детей старше семи лет разовая доза рассчитывается в зависимости от веса.
Клебсиеллу у ребенка в 2 года и старше лечат при помощи безопасных антибактериальных препаратов. Наиболее эффективными являются цефалоспорины («Цефазолин», «Цефалексин») и фторхинолоны («Ципрофлоксацин»). Также могут назначать пенициллины («Амоксиклав»), но они считаются менее действенными.
Для восстановления и укрепления естественной микрофлоры показаны пробиотики: «Бифиформ», «Бифидумбактерин», «Линекс для детей», «Аципол», «Пробифор» и прочие. Пробиотики пьют во время антибактериальной терапии и еще две недели после ее окончания.
Проводится патогенетическое лечение:
- НПВС (жаропонижающие): «Парацетамол», «Нурофен»;
- иммуномодуляторы: «Кипферон», «Генферон Лайт»;
- антигистаминные препараты: «Зодак», «Зиртек».
Симптоматическое лечение:
- при рвоте назначают «Мотилиум» в суспензии, детям с 12 лет можно в таблетках;
- при диареи принимают «Стопдиар», «5-НОК», «Энтерофурил»;
- при обезвоживании ребенку дают регуляторы водно-электролитного баланса «Регидрон», «Гидровит».
Последствия
При своевременном и адекватном лечении клебсиеллы у детей прогноз благоприятный. При позднем обращении или отсутствии терапии инфекция быстро распространяется и вызывает сепсис – опасное состояние, в особенности для ребенка. Помимо системной воспалительной реакции, могут быть и другие тяжелые последствия:
- Одно из часто встречающихся осложнений капсульной бактерии в кишечнике – хроническая диспепсия. Заболевание сопровождается тошнотой, рвотой, постоянными болями в эпигастрии, кровотечениями в разных отделах кишечника.
- У новорожденных детей при неадекватной терапии клебсиеллы может развиться геморрагический диатез. Для заболевания характерны рвота с кровью, дегтеобразный стул, внутренние кровоизлияния.
- Менингит и отек мозга.
- Острая легочная недостаточность.
Даже после грамотно проведенной терапии сильно ослабляются защитные функции организма. маленькие дети часто подвергаются повторному заражению. Опасность заключается в том, что патоген широко распространен и имеет высокую резистентность. Во избежание рецидива необходимо тщательно следить за гигиеной, мыть овощи и фрукты, а лучше подвергать термической обработке. В первое время оградить ребенка от большого скопления людей, контакта с носителями инфекций, передающихся воздушно-капельным путем.
На сегодняшний день вакцин против клебсиеллезов не разработано. Основная мера профилактики – соблюдение правил гигиены и укрепление иммунитета ребенка.
лечение, симптомы, норма, чего боится
Клебсиелла у грудничка в кале – это не всегда признак заболевания. Данные микроорганизмы относятся к условно-патогенным, и в небольшим количестве могут присутствовать в кишечнике ребенка постоянно.
Что такое клебсиелла
При определенных условиях происходит активизация микроорганизмов, увеличивается их количество и развивается воспалительная реакция с появлением соответствующей симптоматики. Одновременно клебсиеллы появляются в кале. В этом случае требуется диагностика дисбактериоза, а также соответствующая терапия.
Один из симптомов появления клебсиеллы в организме — дисбактериозВыделяется несколько видов микроорганизмов. При попадании в ткани они вызывают развитие воспалительных процессов в различных органах. В детском возрасте клебсиелла приводит к возникновению следующих болезней:
- менингит;
- пневмония;
- острый средний отит;
- синуситы;
- пиелонефрит;
- гнойные процессы в мягких тканях различной локализации.
При выраженном снижении иммунитета клебсиеллы провоцируют развитие сепсиса. Состояние сопровождается появлением и размножением микроорганизмов в крови с последующим распространением по всему организму.
Почему активизируется инфекция
Клебсиелла у грудничка в кале появляется из-за увеличения количества микроорганизмов в кишечнике. Обычно это происходит при воздействии определенных факторов:
- нарушение метаболизма на фоне сахарного диабета;
- врожденный иммунодефицит;
- снижение иммунитета;
- хронические заболевания, способствующие истощению организма младенца;
- длительное применение антибиотиков, приводящее к угнетению нормальной микрофлоры и активизации условно-болезнетворных микроорганизмов;
- искусственное вскармливание.
Также увеличение количества бактерий в кишечнике может происходить при употреблении пищи немытыми руками, при контакте с животными.
Важно следить за чистотой в доме. Младенец в процессе познания окружающего мира норовит попробовать различные предметы на вкус. Из-за недостаточной гигиены повышается риск развития кишечных инфекций, включая сальмонеллез и шигеллез. Грудничок может легко заразиться гельминтами, что тоже провоцирует рост количества клебсиелл.
Симптомы, которые указывают на наличие клебсиеллы в организме
На возможную активизацию клебсиеллы указывают такие симптомы:
- вздутие живота;
- частое отхождение газов;
- систематическое срыгивание;
- субфебрильная температура;
- колики, вызывающие выраженное беспокойство ребенка;
- частый жидкий стул;
- появление в кале прожилок крови, слизи, гноя;
- ухудшение аппетита;
- нарушение сна;
- гнилостный запах стула.
На фоне функциональных нарушений пищеварительной системы страдают другие органы. Ребенок становится вялым, капризным, плохо ест и спит. Кожные покровы бледные, часто имеют сероватый оттенок. Отмечается недостаточная прибавка веса.
Диагностика
Выявление клебсиелл в кале проводится при помощи бактериологического исследования. Это лабораторный анализ, который подразумевает посев кала или мазка со слизистой оболочки прямой кишки на специальные питательные среды.
Исследование дает возможность установить:
- факт наличия клебсиеллы у грудничка в кале;
- количество микроорганизмов в единице объема исследуемого биологического материала;
- вид и штамм бактерий — у ребенка в кале обычно появляется клебсиелла окситока;
- устойчивость выделенных микроорганизмов к антибиотикам.
Бактериологический посев – это информативное и ценное исследование. Определение устойчивости к антибиотикам дает возможность оценить, чего боится бактерия, а также подобрать наиболее эффективный препарат для лечения. Это очень важно в современных условиях, так как большое количество штаммов клебсиелл обладает устойчивостью к различным антибиотикам.
Для выяснения причины появления микроорганизмов в кале младенца назначаются различные методики исследований:
- клинический анализ крови и мочи;
- анализ на определение концентрации глюкозы;
- иммунологические и аллергические пробы;
- выявление антител к различным возбудителям инфекционных заболеваний;
- при необходимости, исследование мочи, мокроты, крови на наличие возбудителя;
- УЗИ внутренних органов.
На основании всех данных объективного обследования врач определяет дальнейшую лечебно-профилактическую тактику. Норма клебсиелл в 1 г кала не должна превышать 105 клеток. При эпизодическом увеличении количества назначается медицинское наблюдение с периодическим бактериологическим посевом кала.
Последствия и осложнения
Систематическое повышение количества клебсиелл в кале ребенка провоцирует развитие осложнений:
- нарушение пищеварения с недостаточным усваиванием питательных веществ и витаминов;
- отставание ребенка в развитии;
- повышение риска развития воспалений в различных органах и тканях;
- снижение активности иммунитета, провоцирующее присоединение других инфекций, включая кандидоз;
- развитие острой кишечной инфекции.
В большинстве случаев у детей с диагностированными пневмонией, менингитом, пиелонефритом, синуситами, которые были вызваны клебсиеллами, отмечалось увеличение количества бактерий в кишечнике.
Лечение
Проведение терапевтических мероприятий требуется, когда количество клебсиелл в кале ребенка превышает норму. Лечение заключается в следующем:
- уменьшение количества клебсиелл;
- профилактика инфекционно-воспалительных процессов различной локализации;
- восстановление нормальной микрофлоры кишечника;
- улучшение работы пищеварительной системы и других органов.
Терапевтические мероприятия проводятся в 2 этапа:
- Снижение количества клебсиелл с помощью антибактериальных средств: антибиотики назначаются только врачом по строгим показаниям. Обычно предварительно проводится определение чувствительности выделенных микроорганизмов к антибиотику. Как правило, используются средства с широким спектром действия, к которым относятся полусинтетические пенициллины и цефалоспорины.
- Восстановление нормальной микрофлоры – назначение пробиотиков. Одновременно рекомендуется увеличить количество кисломолочных продуктов в рационе.
Назначаются мероприятия, направленные на снижение факторов, спровоцировавших увеличение количества клебсиелл в кишечнике.
Лечение дисбактериоза должен назначать только врач. Попытки самостоятельно восстановить микрофлору кишечника приводят к усугублению состояния и развитию негативных последствий.
Также интересно почитать: открытое овальное окно в сердце у детей
симптомы наличия в кишечнике у ребенка, новорожденных, лечение бактериофагом бактерии клебсиеллы окситока
Клебсиеллезная инфекция у ребенка — состояние, которое требует адекватной реакции родителей и врачей. Что делать, если у малыша обнаружены клебсиеллы и как лечить инфекцию, вы узнаете из этой статьи.
Что это такое
Клебсиелла — бактерия, которая сама по себе болезнетворной не считается. Это условно-патогенный организм, который может вызывать заболевание лишь при определенных условиях. Названа бактерия в честь своего «отца» -первооткрывателя немецкого патологоанатома Эдвина Клебса. Эта бактерия относится к семейству энтеробактерий и по этому признаку имеет некое родство с кишечной и чумной палочками, с сальмонеллой. В 2017 году клебсиеллу причислили к разряду довольно опасных бактерий, но только за то, что она показывает удивительную стойкость к существующим сегодня антибиотикам. К новым противомикробным препаратам бактерия показывает быструю резистентность.
Клебсиелла — грамотрицательная палочка, имеющая капсулу, которая неплохо защищает ее от воздействия окружающей среды. Чаще всего микроб встречается в каловых массах людей, на кожных покровах и слизистых оболочках органов дыхания, а также может передаваться с почвой, водой и продуктами питания — в основном с фруктами и овощами, если их плохо помыть.
Клебсиелла относится к анаэробным микроорганизмам, ее размножение обычно происходит в бескислородной среде. При кипячении бактерия гибнет, но в условиях привычного нам воздуха не теряет своей активности и потенциальной опасности.
Палочка может быть в организме любого человека незамеченной до тех пор, пока его иммунитет в состоянии сдерживать ее активность. Однако стоит иммунной защите ослабнуть, и бактерия начинает активно размножаться. У грудничков и новорожденных иммунитет недостаточно крепкий сам по себе. Конечно, кроху в некоторой степени защищает врожденный материнский иммунитет, но только до полугода и не от всех болезней. Поэтому риск заразиться клебсиеллой у малышей первого года жизни очень велик.
Бактерия в основном поражает кишечник ребенка. Но вот токсины, которые она выделяет в процессе своего размножения и жизнедеятельности, могут оказать негативное воздействие на любые органы и системы малыша, ведь они у новорожденных очень уязвимы. Пока науке известно восемь разновидностей этого микроорганизма. У них довольно длинные и сложные латинские названия. Отличие между видами заключается в наборе антигенов. Чаще всего в детском возрасте обнаруживают два вида — клесиелла пневмонии (Klebsiella pneumoniae) становится причиной пневмонии, а окситока клебсиелла (Klebsiella oxytoca) — малоприятные желудочно-кишечные проявления с диареей и болями в животе.
Эти и другие виды бактерии способны стать причиной таких заболеваний, как конъюнктивит, менингит, сепсис и даже вызвать риносклерому, при которой тяжело поражается слизистая оболочка дыхательных путей. По своему «поведению» клебсиелла очень близка к золотистому стафилококку, который тоже может очень долгое время существовать в организме зараженного человека незаметно и вполне мирно. Однако под воздействием неблагоприятных (для человека) и очень благоприятных (для бактерии) факторов, начинается рост и размножение.
Заболевание «клебсиеллез» как таковое в международной классификации болезней отсутствует, но МКБ -10 предусматривает определенные позиции для недугов, вызываемых бактерией, например, для бактериальной пневмонии.
Причины
Патологические причины, которые способствуют активности клебсиеллы, довольно разнообразны, но все они в большинстве своем сводятся к снижению иммунитета. А потому дети, которые появились на свет ослабленными и болезненными, недоношенные дети, малыши, унаследовавшие ВИЧ-инфекцию, находятся в группе риска по заражению клебсиеллой.
У грудничков и новорожденных спровоцировать иммунный спад может и перевод с грудного вскармливания на искусственные молочные смеси, поскольку большую часть антител организм крохи получается с молоком матери. Вторая, не менее распространенная, причина развития в организме клебсиеллы заключается в нарушении санитарного режима и правил гигиены. Бактерия может попасть в организм ребенка с водой, если ее не кипятят, с плохо вымытыми овощами и фруктами, и даже с рук взрослых, которые ухаживают за младенцем.
Если ко всему прочему иммунитет слаб, то в кишечнике или на слизистых оболочках органов дыхания ребенка начинается болезнетворный процесс.
Клебсиелла живет не только в человеческом организме, но и у домашних животных. Иногда заражение становится возможным и от контакта младенца с питомцем. Заражение может произойти и в условиях больницы, иногда прямо в роддоме.
Такие больничные бактерии отличаются повышенной устойчивостью к антибиотикам и болезни, которые они вызывают, с большим трудом поддаются терапии.
Нередко у ребенка диагностируется совместное присутствие в организме и стафилококка, и клебсиеллы. Эти два микроба могут действовать в тандеме, стафилококк нарушает микрофлору в кишечнике, что создает более благоприятные условия для существования и размножения клебсиеллы.
Симптомы и признаки
Если в анализе кала у малыша обнаружены клебсиеллы, то этот факт нельзя считать основанием для начала лечения. Скорее, это доказательство того, что у малыша есть эти бактерии, но иммунитет с ними справляется, что само по себе болезнью считать нельзя. О развитии клебсиеллеза можно говорить только тогда, когда у ребенка имеются симптомы.
Признаки не являются специфическими, характерными только для этой патологии, а потому распознать их бывает достаточно сложно:
- Нарушения стула. Кал становится жидким, содержит фрагменты непереваренной пищи, может быть пенистым, иногда с примесями крови. Цвет каловых масс становится желтовато-зеленым, имеет выраженный гнилостный запах.
- Абдоминальные боли. У ребенка вздут живот, он становится беспокойным из-за болевых ощущений в животике, может наблюдаться повышенное газообразование.
- Срыгивания. Понятно, что любое срыгивание не стоит считать признаком бактериальной инфекции. Срыгивание обильное, «фонтаном», превышающее объем столовой ложки, обязательно должно насторожить родителей, поскольку может говорить о наличии клебсиеллы.
- Расстройство пищеварения. У ребенка с клебсиеллезом может наблюдаться рвота. Он отказывается от пищи, страдает аппетит.
- Лихорадка. В острой стадии инфекции может подняться температура до 38,5-39,0 градусов.
При поражении клебсиеллой органов дыхания, симптомы также имеют острый характер. Повышается температура (до 39,0 градусов), появляется сильный кашель, может выделяться мокрота с прожилками крови и неприятным запахом, ребенок становится вялым и сонливым, капризничает и отказывается от пищи. Все эти симптомы могут быть признаками массы других заболеваний, тем важнее обратиться к врачу своевременно. На деле же родители достаточно часто принимают проявления бактериального заражения за дисбактериоз, и самовольно, без ведома доктора, начинают давать ребенку пребиотики и пробиотики. Без должного лечения инфекция развивается дальше, и состояние ребенка значительно ухудшается.
Учитывая, что микроб очень устойчив к антибиотикам, лечение обязательно должно проходить под наблюдением врача, который может назначить правильный антимикробный терапевтический курс.
Диагностика
Увидеть бактерию в домашних условиях и отличить заболевание, которое она вызвала, от других недугов не представляется возможным. Установить факт клебсиеллеза можно только на основании лабораторных исследований. Наиболее часто микроб обнаруживается в каловых массах. Однако врачи этим не ограничиваются и проводят исследование мочи, крови и мокроты малыша на клебсиеллу.
В моче микроб обнаруживается нечасто, только в том случае, если у крохи развивается пиелонефрит, вызванный клебсиеллой. Во всех остальных случаях попадание микроба в анализ мочи считают случайностью. Как уже говорилось, бактерия может присутствовать и в анализах совершенно здорового малыша. Но в этом случае ее содержание не превысит 10 в 5 степени (105 микробов на 1 грамм кала). Если у малыша нашли 10 в 8 степени на 1 грамм клебсиелл в кале, это основание для начала лечения кишечной инфекции, вызванной бактерией.
10 в 6 степени на грамм, обнаруженные в мокроте – основание для подозрения на бактериальную пневмонию и назначения соответствующего лечения. 10 в 7 степени — тоже патологическая концентрация, которая потребует лечения.
Дополнительно могут быть проведены аналогические бакпосевы на стафилококк, ведь он часто сопровождает клебсиеллу. Нечасто, но бывает, что маму просят сдать грудное молоко на наличие бактерии.
Лечение
Не стоит думать, что бактериальная инфекция в обязательном порядке требует применения антибиотиков. Это логично, но не обязательно. Легкие степени клебсиеллезной инфекции лечатся без противомикробных средств. Ребенку назначают пробиотики, которые помогут восстановить баланс микрофлоры кишечника, бактериофаги. Именно бактериофаги — специально созданные вирусы, обладающие способностью уничтожать бактерии, считаются основным методом терапии. Лечение бактериофагом может быть довольно продолжительным — до 3 недель.
Дополнительно, в зависимости от симптомов, назначают жаропонижающие средства «Парацетамол», «Нурофен», а также средства для пероральной регидратации, если у малыша наблюдается длительный понос или частая рвота («Смекта», «Регидрон»). Для более эффективной очистки кишечника могут быть использованы так называемые кишечные антисептики – «Фуразолидон» и ему подобные препараты.
Не все малыши хорошо переносят эти лекарства, у многих он вызывают тошноту и головные боли. А потому при появлении таких симптомов во время лечения обязательно нужно рассказать педиатру, чтобы он подобрал иной способ помочь малышу.
Легкие степени инфекции разрешено лечить в домашних условиях, но с ведома и согласия педиатра. Поскольку груднички — народ малопредсказуемый и ухудшение состояния у них может случиться в любой момент. Если инфекция имеет выраженное протекание, доктор может посоветовать госпитализацию и будет совершенно прав. Отказываться от курса лечения в больнице не стоит, хотя бы из соображений безопасности для грудничка. Чтобы выбрать антибиотик, который будет действовать на конкретную бактерию, обнаруженную у ребенка, в условиях стационара проводят исследование на предмет подверженности бактерии влиянию антибактериальных препаратов.
Для этого в лабораторных условиях клебсиеллу «атакуют» разными противомикробными средствами, и тот препарат, который нанесет ей максимальный урон, будет выбран в качестве основного для лечения конкретного ребенка. Антибиотики дают совместно и иммуномодуляторами, чтобы повысить способность иммунитета малыша к сопротивлению.
Весь этот процесс занимает от 7 суток до 21 дня, он обязательно должен протекать под постоянным врачебным наблюдением, поскольку есть риск инфицированию других органов.
Лечащий врач будет следить за резистентностью микроба-возбудителя и при необходимости заменит один антибиотик на другой.
Для лечения детей в возрасте до 1 года обычно используют антибиотики, которые относятся к семейству пенициллинов или цефалоспоринов. Их воздействие на организм в целом довольно щадящее, что по достоинству оценили врачи-педиатры. Лечение пневмонии, вызванной клебсиеллой, чаще всего проходит в условиях стационара по схеме, которая очень похожа на терапию кишечных недугов, вызванных этим микробом. Одновременно с лечением доктор обязательно рекомендует кормящей маме изменить свой рацион, устранить из него сложные углеводы.
Ребенок, который питается смесями, должен дополнительно получать витамины, в некоторых ситуациях педиатр советует сменить один вид смеси на другой.
В последнее время в лечении клебсиеллы большинство современных докторов стараются избежать применения антибиотиков, поскольку считают, что вред от этой бактерии несколько преувеличен, и иммунитет ребенка при правильном питании и создании благоприятных внешних условий сможет справиться с инфекцией самостоятельно. Естественно, это касается только тех разновидностей бактерии, которые вызывают кишечную симптоматику. В терапии пневмонии, вызванной клебсиеллой, подход остался прежним.
Возможные опасности и последствия
Как лечить и лечить ли бактерию клебсиеллу вообще, должен решать исключительно врач. Прогноз и длительность лечения во многом зависят от того, насколько быстро родители заметили «неладное» и обратились к специалисту. Именно поэтому важно не заниматься лечением поноса и рвоты у младенца народными средствами, а при появлении таких признаков сразу звонить в поликлинику и вызывать врача.
При обильной рвоте, сильной диарее на фоне высокой температуры повышается риск обезвоживания у грудничка, причем процесс этот будет стремительным. А потому важно сразу вызвать «Скорую помощь».
Бояться инфекционного стационара, в котором, по искреннему убеждению многих родителей, «ребенок подхватит еще пару десятков вирусов и бактерий», не надо.
Теоретически клебсиелла в запущенной и агрессивной форме может вызвать не только диарею, но и пагубно сказаться на состоянии суставов, вызвать гайморит и менингит, а также очень опасное осложнение — бактериальный системный сепсис. И хоть вероятность наступления таких последствий для среднестатистического малыша не так уж велика, рисковать жизнью ребенка не стоит.
Профилактика
От клебсиеллы довольно трудно уберечься, поскольку она окружает нас повсюду, и даже собственные родители могут передать этот микроорганизм своему ребенку. Именно поэтому наибольший упор в профилактике стоит сделать не на стерильную чистоту всего, что окружает кроху, а на укрепление его иммунитета.Для этого ребенок должен достаточно времени проводить на свежем воздухе, в его питании должно быть достаточно витаминов и микроэлементов, необходимых для нормальной работы всего организма.
Не стоит пичкать ребенка таблетками и сиропами при первых признаках любого заболевания, ведь вирусы и бактерии «тренируют» иммунитет, который формирует антитела к разным возбудителям болезней. В попытках укрепить иммунитет малыша некоторые родители доходят до медикаментов — иммуностимуляторов и иммуномодуляторов. Не стоит применять такие средства в профилактических целях, поскольку они могут привести к тому, что собственный иммунитет ребенка начнет «лениться».
Исключение составляют случаи клинически подтвержденного иммунодефицита, когда такие препараты выступают, по сути, способом терапии.
Сопутствующая профилактика клебсиеллеза заключается в соблюдении правил и норм гигиены. Взрослые могут даже не догадываться о том, что являются носителями бактерии, а потому важно каждый раз после туалета мыть руки с мылом, прежде чем подойти к ребенку. Самому малышу тоже нужно мыть ручки, если он общался с домашними животными или вернулся с прогулки на улице. Воздушно-капельным путем передается только одна разновидность клебсиеллы, которая вызывает пневмонию. Защититься от нее довольно сложно, но радует тот факт, что такое бактериальное воспаление легких встречается у детей и взрослых нечасто.
Снизить заболеваемость могут и родители зараженного ребенка. После выявления в анализах патологического содержания бактерии, они должны ограничить общение малыша с ровесниками, другими детьми в семье, пресечь совместное пользование игрушками, постельными принадлежностями и посудой до полного излечения малыша.
Подробнее о профилактике и лечении микробных и бактериальных заболеваний вы узнаете из следующего видео.
Бактериофаг клебсиелл поливалентный очищенный инструкция по применению: показания, противопоказания, побочное действие – описание Klebsiella polyvalent bacteriophage purified р-р д/приема внутрь, местн. и наружн. прим. 20 мл: фл. 4 шт. (36442)
Препарат используют для приема внутрь (через рот), в виде клизм, аппликаций, орошений, введения в полости ран, вагины, матки, носа, пазух носа, а также в дренированные полости: абсцессов, брюшную, плевральную, мочевого пузыря, почечной лоханки.
Внутрь препарат принимают натощак за 0,5-1 час до приема пищи.
Рекомендуемые дозировки препарата
| Возраст пациента | Доза на 1 прием при различных способах введения препарата | |
| внутрь (мл) | в клизме (мл) | |
| 0-6 мес | 5 | 10 |
| 6-12 мес | 10 | 20 |
| от 1 года до 3 лет | 15 | 20-30 |
| от 3 до 8 лет | 20 | 30-40 |
| от 8 лет и старше | 20-30 | 40-50 |
Лечение гнойно-воспалительных заболеваний с локализованными поражениями должно проводиться одновременно как местно, так и приемом препарата внутрь.
В случае обработки полости гнойного очага химическими антисептиками перед применением бактериофага она должна быть промыта стерильным 0,9 % раствором натрия хлорида.
При лечении озены и склеромы препарат используют для промывания полости носа и слизистой оболочки верхних дыхательных путей, для введения в полости пазух носа (по клиническим показаниям), а также при поражении глотки, гортани, трахеи в виде ингаляций (без подогрева и использования ультразвука). Доза препарата для обработки слизистых носа и верхних дыхательных путей 10-20 мл. После промывания слизистых в полость носа по очереди в каждый носовой ход вводят турунды, смоченные препаратом, и оставляют на 1 час. Процедуру повторяют 2-3 раза в день в течение 20-40 дней. Поскольку озена и склерома являются хроническими заболеваниями, с целью профилактики обострений рекомендуется 1 раз в год проводить 20-40 дневные курсы лечения по вышеприведенной схеме.
При лечении ангин, фарингитов, ларингитов препарат используют для полосканий полости рта и глотки 3 раза в день по 10-20 мл, курс лечения 7-10 дней.
При лечении бронхитов, пневмоний препарат принимают внутрь 3 раза в день по 10-20 мл, а также применяют в виде аэрозолей и ингаляций (без подогрева и использования ультразвука), курс лечения 15-20 дней.
При лечении отитов препарат используют для.промывания и введения в полость среднего уха по 2-5 мл 1-3 раза в день. Курс лечения 7-15 дней.
При лечении воспалений пазух носа препарат используют для промывания полости носа, носоглотки и пазух носа в дозе 5-10 мл и введения в пазухи 2-3 мл. Процедуру повторяют ежедневно однократно в течение 7-10 дней. Кроме того, препарат вводят в полость носа в виде турунд, смоченных бактериофагом, по очереди и в каждый носовой ход и оставляют в течение 0,5-1 часа. Процедуру повторяют 3 раза в день, курс лечения 7-15 дней.
При лечении стоматитов и хронических пародонтитов препарат используют в виде полосканий полости рта 3-4 раза в день в дозе 10-20 мл, а также введением в пародонтальные карманы турунд, пропитанных бактериофагом клебсиелл, на 5-10 мин, курс лечения 7-10 дней.
При конъюнктивитах и кератоконъюнктивитах препарат применяют по 2-3 капли 4-5 раз в день, курс лечения 5-7 дней; при гнойной язве роговицы — по 4-5 капель в день в течение 7-10 дней; при гнойных иридоциклитах — по 6-8 капель каждые 3 часа в сочетании с приемом внутрь в терапевтических дозировках в течение 7-10 дней.
При абсцессах после вскрытия и удаления гнойного содержимого препарат вводят в количестве меньшем, чем объем удаленного гноя ежедневно однократно, курс лечения 7-10 дней.
При перитонитах и плевритах препарат вводят в дренированные полости брюшную и плевральную через дренажные трубки ежедневно однократно 20-70 мл, курс лечения 10-15 дней.
При остеомиелитах препарат вводят в полость раны через турунды, дренажи в количестве 10-30 мл ежедневно однократно, курс лечения 15-20 дней.
При лечении нагноений ран препарат применяют в виде орошения, аппликаций, повязок, введения в дренаж в дозе 5-50 мл в зависимости от очага поражения не менее одного раза в день, курс лечения 10-15 дней.
При лечении гнойно-воспалительных гинекологических заболеваний (нагноений ран, эндометритов, вульвитов, бартолинитов, кольпитов, сальпингоофоритов) препарат используют для орошений, аппликаций, вводят в полости ран, вагины, матки по 5-20 мл один раз в день в течение 7-10 дней.
При циститах, пиелонефритах, уретритах препарат принимают внутрь в терапевтической дозе 3 раза в день за 1 час до еды в течение 10-20 дней. В том случае, если полость мочевого пузыря или почечной лоханки дренированы, препарат вводят через цистостому, или нефростому 1-3 раза в день по 20-50 мл в мочевой пузырь и 5-7 мл в почечную лоханку, курс лечения 7-15 дней.
При гастоэнтероколитах, панкреатитах, холециститах, а также дисбактериозах кишечника бактериофаг принимают внутрь в возрастных дозировках 3 раза в день за 1 час до еды в течение 7-15 дней (по клиническим показаниям). При неукротимой рвоте препарат применяют в виде высоких клизм 2-3 раза в день по 20-40 мл. При дисбактериозе кишечника препарат может применяться с препаратами нормофлоры.
Для профилактики внутрибольничных хирургических инфекций препарат используют для обработки послеоперационных и свежеинфицированных ран в дозе 5-50 мл в зависимости от очага поражения ежедневно однократно в течение 5-7 дней.
Применение препарата у детей до 1 года (включая недоношенных детей).
При гастоэнтероколите, пневмонии и сепсисе новорожденных препарат применяют, через рот 2-3 раза в сутки по 3-5 мл за 30 минут до кормления. В случаях неукротимой рвоты препарат применяют в виде высоких клизм (через газоотводную трубку или катетер) ежедневно однократно в дозе 5-10 мл. Возможно сочетание ректального (в виде высоких клизм) и перорального применения препарата: курс лечения 7-15 дней (по клиническим показаниям). При рецидивирующем течении заболевания возможно повторное проведение курсов лечения.
С целью профилактики возникновения внутрибольничной инфекции у новорожденных детей бактериофаг применяют по эпидемическим показаниям внутрь по 3-5 мл 3 раза в день за 30 минут до кормления в течение всего срока пребывания в
стационаре.
При лечении омфалитов, пиодермии, инфицированных ран бактериофаг применяют в виде аппликаций по-5-10 мл 2-3 раза в день (марлевую салфетку смачивают бактериофагом и накладывают на пупошгую ранку или пораженный участок кожи) в течение 7-15 дней.
Применение препарата не исключает использование других антибактериальных и противовоспалительных препаратов.
Причины, лечение, диагностика и симптомы
Klebsiella pneumoniae — это тип бактерий, которые могут вызывать ряд инфекций. Обычно они развиваются в больничных условиях.
В пищеварительном тракте людей содержится K. pneumoniae . Когда бактерии распространяются на другие части тела, они могут вызывать различные инфекции, в том числе:
- инфекции мочевыводящих путей
- инфекции кожи и ран
- абсцессы печени
- пневмония
- инфекции крови
- менингит
Продолжайте читать, чтобы узнать больше о причинах, симптомах и лечении K.pneumoniae инфекций.
Поделиться на Pinterest Klebsiella pneumoniae может вызывать такие инфекции, как пневмония, менингит и абсцесс печени.Существует много типов бактерий K. pneumoniae . У некоторых есть капсулы, окружающие их клетки, а у других их нет.
В настоящее время исследователи идентифицировали 77 типов капсул. Бактерии Klebsiella без капсул менее заразны, чем бактерии с капсулами.
Люди являются основными переносчиками K.pneumoniae в окружающей среде, но у большинства людей инфекция не разовьется. Люди с ослабленной иммунной системой из-за приема лекарств или заболеваний имеют более высокий риск.
Исследователи сообщают, что некоторые группы населения являются носителями этого типа бактерий, в том числе люди китайской национальности и люди с алкогольным расстройством.
В некоторых популяциях болезнь с большей вероятностью вызывает определенные инфекции. K. pneumoniae — наиболее частая причина внутрибольничной пневмонии, например, в США.
Между тем, в западных регионах Klebsiella редко вызывает менингит. Однако на Тайване инфекция K. pneumoniae является основной причиной, на которую приходится около 25–40% случаев бактериального менингита у взрослых.
У некоторых людей развивается менингит K. pneumoniae из абсцессов печени. Бактерии из абсцесса могут перемещаться из печени в центральную нервную систему.
Кроме того, катетеры и инструменты в медицинских процедурах могут передавать К.pneumoniae в мочевыводящие пути, кровоток и раны.
Различные типы инфекции, вызванной K. pneumoniae , могут вызывать разные симптомы, которые могут напоминать симптомы других бактериальных инфекций.
Если врач замечает, что бактериальная инфекция сохраняется после первоначального лечения, он может назначить анализы для выявления конкретных бактерий, вызывающих ее. Результаты помогают им выбрать наиболее подходящее лечение антибиотиками.
Любой, кто подозревает, что у него инфекция мочевыводящих путей, пневмония, менингит или целлюлит — все это может быть результатом K.pneumoniae — следует немедленно обратиться к врачу.
В таблице ниже перечислены общие симптомы этих состояний.
Врачи лечат инфекций K. pneumoniae с помощью антибиотиков. Когда инфекция связана с больницей, врачи используют класс антибиотиков, называемых карбапенемами, до тех пор, пока не будут получены результаты теста на чувствительность.
Если врач подозревает, что у бактерий развилась устойчивость к антибиотикам, он может назначить тесты, чтобы определить, насколько чувствительны бактерии к определенным антибиотикам, прежде чем выбрать наиболее эффективный вариант.
Для врачей может быть сложно лечить инфекций K. pneumoniae , потому что все меньше антибиотиков оказывается эффективным. Например, совсем недавно у некоторых K. pneumoniae развилась устойчивость к карбапенемам.
Врач может назначить комбинацию антибиотиков. В одном исследовании наблюдались более низкие показатели смертности у людей с бактериемией от K. pneumoniae , которые получали комбинацию антибиотиков колистина, меропенема и тигециклина.
Когда у человека развивается пневмония от K. pneumoniae , врачи обычно рекомендуют двухнедельное лечение цефалоспорином третьего или четвертого поколения, фторхинолоном или одним из этих антибиотиков в сочетании с аминогликозидами.
Людям с аллергией на пенициллин требуется курс азтреонама или хинолона.
Врачи обычно диагностируют инфекцию Klebsiella , исследуя либо образец инфицированной ткани, либо образец:
Иногда врачи назначают медицинские визуализационные тесты, в том числе:
- УЗИ
- Рентген
- КТ
Один раз врач подтвердит диагноз, он может провести тесты на чувствительность, чтобы определить, какой антибиотик наиболее эффективно лечит инфекцию.
Всем, кто подозревает, что у них инфекция K. pneumoniae , следует немедленно обратиться за медицинской помощью.
Если какая-либо инфекция не исчезнет после ухода на дому или начального курса антибиотиков, важно обратиться за медицинской помощью. Врач может попросить провести дополнительное обследование, чтобы проверить чувствительность бактерий к антибиотикам.
K. pneumoniae инфекция заразна. Человек должен контактировать с бактериями, которые не распространяются по воздуху.
В больницах K. pneumoniae может передаваться от человека к человеку. Люди также могут контактировать с бактериями из-за воздействия окружающей среды, хотя это происходит реже.
Человек может контактировать с этим типом бактерий через:
- вентиляторы или дыхательные аппараты
- внутривенные катетеры
- мочевые катетеры
- открытые раны
Здоровые члены семьи людей с K.pneumoniae имеют низкий риск заражения инфекцией.
Однако необходимо соблюдать все гигиенические меры предосторожности. Гигиена рук остается лучшей защитой от инфекции K. pneumoniae .
Когда врачи быстро идентифицируют K. pneumoniae в образцах и сразу же прописывают соответствующие антибиотики, прогноз улучшается. Однако задержки с диагностикой и тестированием — обычное явление, и это может привести к менее благоприятному прогнозу.
Прогноз для людей с пневмонией от К.pneumoniae часто бывает плохой. Даже когда врачи выбирают соответствующую антибактериальную терапию, смертность составляет 30–50%.
Люди с другими заболеваниями, такими как диабет, пожилые люди и люди с ослабленной иммунной системой, имеют самый высокий риск смерти.
У людей с пневмонией, вызванной этими бактериями, инфекция может ухудшать функцию легких в долгосрочной перспективе, возможно, на месяцы.
K. pneumoniae обычно развиваются в больницах.Самый высокий риск имеют люди с ослабленной иммунной системой и хроническими заболеваниями.
K. pneumoniae выработала устойчивость ко многим антибиотикам, и врачам может быть сложно лечить инфекцию K. pneumoniae . Однако проверка чувствительности бактерий в образцах крови или тканей может помочь им определить наиболее эффективный курс лечения.
Люди, инфицированные K. pneumoniae , могут передавать бактерии другим людям. Соблюдение всех гигиенических мер предосторожности, особенно мытье рук, — лучший способ предотвратить появление K.pneumoniae инфекций от распространения.
Klebsiella oxytoca: лечение, симптомы и осложнения
Klebsiella oxytoca — это разновидность бактерий. У человека есть несколько естественных бактерий Klebsiella в кишечнике, рту и носу.
Хотя Klebsiella oxytoca (KO) остается в кишечнике человека, он считается здоровым и нормальным. Однако, если он выходит из кишечного тракта, он может вызвать серьезные инфекции.
Большинство инфекций KO происходит в медицинских учреждениях, таких как больницы, дома престарелых и отделения интенсивной терапии (ОИТ).
В этой статье мы рассмотрим причины и симптомы инфекций КО, а также способы их лечения.
Симптомы КО инфекции варьируются от человека к человеку и зависят от места заражения.
КО может вызывать различные типы инфекций, некоторые из которых имеют серьезные побочные эффекты, включая пневмонию. Он также может вызывать инфекции мочевыводящих путей (ИМП).
Общие симптомы КО-инфекции включают:
- лихорадку
- озноб
- озноб, ломоту в теле и другие симптомы гриппа
- затрудненное дыхание или поверхностное дыхание
- слизистый кашель
Менее распространенные симптомы КО-инфекции включают:
- выделения из раны
- сильное воспаление вокруг раны
- боль при мочеиспускании (от ИМП)
- боль внизу живота
- рвота
КО-инфекции могут возникают, когда тип бактерий Klebsiella присутствует вне кишечника.Инфекция обычно возникает в медицинских учреждениях, таких как:
- домов престарелых
- больниц
- отделений интенсивной терапии (ОИТ)
К другим факторам риска развития инфекции относятся:
- использование антибиотиков в течение длительного периода
- с использованием определенных медицинских устройств, таких как вентилятор
- с внутривенным катетером
- с постоянными катетерными трубками (для сбора мочи)
- с диабетом
- с алкогольной зависимостью
Люди, находящиеся в хорошем состоянии здоровья до инфекция должна вылечиться быстро и без каких-либо осложнений.
Однако люди с серьезными заболеваниями или чья иммунная система уже ослаблена, могут с трудом выздоравливать.
Людям с дополнительными инфекциями, такими как инфекция кровотока, также может быть труднее устранить инфекцию KO.
Для одновременного лечения обеих инфекций человеку потребуется повышенная доза антибиотиков, которая может вызвать побочные эффекты.
Долговременные осложнения инфекций КО встречаются редко. Однако у людей с легочной инфекцией может развиться повреждение легких, если они не получат быстрое лечение от инфекции.
В редких случаях инфекция КО может быть опасной для жизни, если у человека развивается сепсис. Сепсис — это реакция организма на инфекцию, которая начинает наносить вред его органам и тканям.
Катетеры — частые места инфицирования КО-инфекции. Катетеры часто используются в больницах, чтобы помочь людям, которые не могут ходить в туалет.
Наличие катетера увеличивает риск заражения ИМП. Симптомы ИМП:
- боль и спазмы внизу живота
- боль при мочеиспускании
- частые позывы к мочеиспусканию
- кровь в моче
- лихорадка
- озноб
- боль в спине
диагноз, врач возьмет образец крови, мочи или слизи или их комбинации.
Эти образцы будут отправлены в лабораторию и исследованы под микроскопом, чтобы определить, присутствует ли KO.
Если у человека развивается легочная инфекция или пневмония, ему может потребоваться рентген или компьютерная томография. Эти тесты могут помочь определить серьезность инфекции, а также курс лечения.
Врачи могут провести дополнительные тесты, чтобы выяснить, где бактерии попали в организм. Врачи делают это, потому что определение точки входа помогает им обнаружить другие симптомы инфекции и предотвратить распространение инфекции.
Раны, катетеры и аппараты искусственной вентиляции лёгких — это обычные точки входа в больницу.
Лекарства
Врач обычно назначает антибиотики для лечения инфекции КО. Однако некоторые штаммы устойчивы к наиболее распространенным антибиотикам. В этом случае можно использовать специализированные лабораторные тесты, чтобы найти альтернативные антибиотики для лечения инфекции.
Люди должны принимать антибиотики в соответствии с указаниями врача и проходить полный курс, даже если симптомы исчезли заранее.Невыполнение этого требования увеличивает риск повторного заражения или не устранение первоначальной инфекции.
Регулярное и тщательное мытье рук — лучший способ предотвратить распространение микробов и, следовательно, снизить вероятность заражения.
Если человеку требуется лечение в больнице от инфекции КО, он должен попросить посетителей носить халаты и перчатки, обеспечить использование всеми медицинскими работниками антибактериального геля на руках при входе в палату и как можно чаще мыть руки.
Инфекции КО необходимо лечить антибиотиками. Однако при некоторых осложнениях КО-инфекций можно избавиться с помощью естественных методов лечения.
Некоторые ИМП с легкими симптомами могут поддаваться естественному лечению и домашним средствам. Человек с ИМП может попробовать:
- принимать ацетаминофен
- положить грелку на живот, спину или между бедер
- отдыхать
- пить много жидкости
- избегать секса, если он чувствует себя некомфортно
Другие домашние средства включают йогурт и клюквенный сок, но нет никаких научных доказательств их эффективности.
Много отдыхайте, избегайте алкоголя и курения, а также придерживайтесь здоровой диеты, чтобы уменьшить симптомы гриппа.
Люди могут заразить друг друга при физическом контакте или зараженной окружающей среде. КО не может распространяться по воздуху.
Риск заражения здорового человека низкий. Однако люди с более слабой иммунной системой более уязвимы для инфекции КО.
Госпитализация также увеличивает риск развития КО-инфекции у человека, особенно если у него открытая рана, используется вентилятор или внутривенный катетер.
Лечение КО-инфекции обычно несложно. Однако эффективность лечения и прогноз некоторых осложнений зависят от места заражения и общего состояния здоровья человека.
Если инфекция КО не является лекарственно устойчивой, ее можно эффективно лечить курсом антибиотиков. Большинство людей выздоравливают через 2–4 недели.
Если инфекция устойчива к лекарствам, необходимы дальнейшие тесты, чтобы найти лекарство, которое может уничтожить бактерии.Люди с более слабой иммунной системой также могут выздоравливать дольше и труднее.
Хорошие гигиенические практики, такие как регулярное мытье рук и держание подальше от больных, помогут ускорить выздоровление и, в первую очередь, снизят вероятность заражения.
Принятие лекарств в соответствии с инструкциями и уверенность в том, что они прошли весь курс лечения, также увеличивают шансы человека на полное выздоровление.
ИМП у детей ясельного возраста: причины, симптомы и лечение
Обзор
Что такое инфекция мочевыводящих путей (ИМП) у детей раннего возраста?
ИМП — это инфекция мочевыводящих путей вашего ребенка, которая включает его почки, мочеточники, соединяющие их с мочевым пузырем, и уретру, через которую моча выходит из организма.Бактерии (микробы) попадают в их мочевыводящие пути через кожу вокруг прямой кишки и гениталий или через кровоток из любой части их тела (что встречается гораздо реже).
Поскольку инфекция у ребенка может быть не очевидна, особенно если он еще слишком мал, чтобы озвучить свои симптомы, ИМП у детей иногда остаются незамеченными. Инфекции мочевыводящих путей необходимо лечить немедленно, чтобы предотвратить распространение инфекции и повреждение почек.
Какие типы инфекций мочевыводящих путей у детей ясельного возраста?
ИМП подразделяются на две категории:
- Нижние ИМП: Инфекция мочевого пузыря.
- Верхние ИМП: Инфекция почек (одной или обеих).
Что такое мочевыводящие пути?
Мочевыводящие пути избавляются от лишней жидкости и шлаков. Почки, мочеточники, мочевой пузырь и уретра — это органы, из которых состоит тракт. Почки фильтруют кровь и вырабатывают мочу, моча проходит через мочеточники в мочевой пузырь, в котором хранится моча, а затем моча проходит через уретру и выходит из организма.
Насколько распространены ИМП у детей раннего возраста?
Инфекции мочевыводящих путей у детей — обычное явление.До семи лет одна из 12 девочек и один из 50 мальчиков заболеет ИМП.
В чем разница между инфекцией мочевыводящих путей и инфекцией мочевого пузыря у детей ясельного возраста?
Инфекция мочевого пузыря остается в мочевом пузыре, тогда как ИМП может инфицировать всю мочевую систему. Многие симптомы похожи, но ребенок, скорее всего, будет выглядеть хуже, если у него инфекция выше мочевого пузыря.
Кто болеет ИМП? Какие дети и малыши подвержены риску?
ИМП чаще всего встречаются у детей с ослабленным иммунитетом (дети со слабой иммунной системой) и у детей, которые длительное время принимали антибиотики по другим причинам.Если вашему ребенку недавно была сделана трансплантация органа, он также более уязвим для инфекции мочевыводящих путей. Дети также могут родиться с аномалиями мочевыводящих путей, которые повышают вероятность заражения инфекцией.
Взрослые также уязвимы к инфекциям мочевыводящих путей.
Заразны ли ИМП?
Нет. Инфекции мочевыводящих путей не передаются ни вам, ни кому-либо еще.
Может ли ИМП вызвать жар у моего ребенка?
Да. Повышенная температура — это симптом ИМП.Лихорадка не является обязательной для диагностики ИМП и чаще встречается при инфекциях вне мочевого пузыря.
Может ли ИМП вызвать у моего ребенка боли в спине?
Да. ИМП может вызвать боль в спине или боку у ребенка. Боль, как правило, локализуется ниже ребер и усиливается, когда что-то ударяет ребенка по спине, а затем когда он находится в состоянии покоя.
Может ли ИМП вызвать диарею у детей ясельного возраста?
Да. У детей с ИМП иногда может развиться диарея.
Если я дам своему ребенку клюквенный сок, поможет ли это его ИМП?
Слух о том, что клюквенный сок может помочь вылечить ИМП, имеет научные доказательства.Однако данные показывают, что в первую очередь он помогает женщинам с повторными ИМП, а не детям. Питьевая жидкость поможет избавиться от ИМП, поэтому большое количество воды или других напитков может быть очень полезным.
Симптомы и причины
Что вызывает инфекцию мочевыводящих путей (ИМП) у детей раннего возраста?
Нормальная моча стерильна (нет бактерий или других инфекционных организмов) и содержит жидкости, соли и продукты жизнедеятельности.Инфекция возникает, когда микроорганизмы цепляются за отверстие уретры (полая трубка, по которой моча из мочевого пузыря выходит за пределы тела) и начинает размножаться. Большинство инфекций возникает из-за бактерий Escherichia coli (E. coli), которые обычно живут в пищеварительном тракте.
Различные бактерии могут вызывать инфекцию мочевыводящих путей. К семи наиболее распространенным бактериям относятся следующие:
- Escherichia coli (E. coli), обнаруживается примерно в 85% случаев ИМП у детей.
- Klebsiella.
- Proteus.
- Энтеробактер.
- Citrobacter.
- Staphylococcus saprophyticus.
- Энтерококк.
Эти организмы обитают в кишечнике, репродуктивной системе вашего ребенка или на его коже.
Каковы признаки и симптомы ИМП у детей ясельного возраста? Каковы признаки и симптомы ИМП у детей старшего возраста?
Ниже приведены наиболее распространенные признаки и симптомы ИМП. Однако каждый ребенок может испытывать это по-разному.Признаки и симптомы у младенцев могут включать:
- Лихорадка.
- Боль или чувство распирания в животе.
- Моча с сильным зловонным запахом.
- Плохой рост. Неспособность развиваться.
- Снижение веса или неспособность набрать вес.
- Раздражительность.
- Рвота и диарея.
- Плохое кормление.
- Истощение.
- Желтуха.
Признаки и симптомы у детей старшего возраста могут включать:
- Частые, срочные позывы к мочеиспусканию (необходимость «пойти»).Несмотря на то, что ваш ребенок чувствует позывы, часто выходит лишь небольшое количество мочи.
- Мокрость днем и / или ночью (после того, как вы полностью приучили себя к горшку).
- Болезненное или затрудненное мочеиспускание (дизурия).
- Дискомфорт над лобковой костью.
- Моча с неприятным запахом.
- Кровь в моче.
- Тошнота и / или рвота.
- Лихорадка, озноб.
- Боль в спине или боку (ниже ребер).
- Усталость.
Что ухудшает ИМП у детей ясельного возраста?
Поставить диагноз сложнее, потому что симптомы менее специфичны, а слишком долгое ожидание лечения может привести к инфекции почек.
Является ли ИМП у малыша признаком проблем с мочевым пузырем или почками?
Не обязательно. У большинства детей с ИМП нет других проблем с мочевыводящими путями.
Диагностика и тесты
Как диагностируется инфекция мочевыводящих путей? Как медицинские работники проверяют наличие ИМП у детей ясельного возраста?
После собеседования с вами об истории болезни вашего ребенка и проведения медицинского осмотра поставщик медицинских услуг может назначить следующие тесты:
- Анализы мочи, такие как лейкоцитарная эстераза и посев мочи на наличие бактерий или лейкоцитов.
- Анализы крови на наличие инфекции или функции почек.
- УЗИ или КТ почек и мочевого пузыря.
- Цистоуретрограмма мочеиспускания (VCUG), которая оценивает мочевой пузырь и уретру для выявления пузырно-мочеточникового рефлюкса (когда моча возвращается к почкам, а не выходит через уретру).
Какие вопросы может задать врач моего малыша для диагностики ИМП?
- Какие симптомы у вашего ребенка?
- Как давно у вашего ребенка были эти симптомы?
- У вашего ребенка в анамнезе были урологические проблемы?
- Были ли в семье проблемы с урологией?
- Какие лекарства принимает ваш ребенок?
Ведение и лечение
Как лечить ИМП у детей?
Для лечения инфекции мочевыводящих путей необходимы антибиотики, которые можно вводить внутривенно (через иглу в вены вашего ребенка) или перорально (они проглатывают таблетки или жидкость).Их лечащий врач может также прописать лекарства от лихорадки и / или боли. Общие антибиотики включают:
- Амоксициллин / клавуланат (Аугментин®).
- Цефиксим (Супракс®).
- Цефподоксим.
- Цефпрозил (Cefzil®).
- Цефалексин (Кефлекс®).
- Триметоприм / сульфаметоксазол (Бактрим®, Септра®).
Кто будет лечить ИМП у моего ребенка? Следует ли моему ребенку обратиться к специалисту?
Лечащий врач вашего ребенка, скорее всего, сможет вылечить вашего ребенка от ИМП.Если возникнут какие-либо осложнения, вас могут направить к урологу или нефрологу (поставщикам медицинских услуг, специализирующимся на мочевыводящих путях).
Как скоро после лечения моему ребенку станет лучше? Сколько времени нужно, чтобы оправиться от инфекции мочевыводящих путей?
Они могут почувствовать себя лучше через день или два, а инфекция должна исчезнуть примерно через неделю.
Профилактика
Могу ли я предотвратить инфекцию мочевых путей у моего ребенка?
Делайте все возможное, чтобы участки кожи мочевыводящих путей вашего ребенка были очень чистыми, и приучайте их делать то же самое.Это особенно важно для девочек. Научите их протирать спереди назад, чтобы не загрязнить уретру и анальное отверстие.
Перспективы / Прогноз
Каковы перспективы для детей с инфекциями мочевыводящих путей?
Это временная инфекция с небольшим риском осложнений.При лечении ИМП у вашего ребенка должны длиться не более недели. Однако они могут снова заразиться инфекцией, даже если у них нормальные мочевыводящие пути.
Есть ли какие-либо долгосрочные осложнения ИМП у детей ясельного возраста?
Около 3% детей, заболевших инфекцией мочевыводящих путей, в будущем могут иметь проблемы с почками, включая рубцы. Осложнения рубцевания почек включают:
- Гипертония.
- Хроническая почечная (почечная) недостаточность.
- Токсикоз при беременности.
Жить с
Когда моему ребенку может потребоваться госпитализация по поводу ИМП?
Вашему ребенку может потребоваться госпитализация по следующим причинам:
- Если это младенец или ребенок.
- Если у них высокая температура.
- Если у них болит спина.
- Если они обезвожены (признаки обезвоживания — отсутствие мочеиспускания, сухость во рту и отсутствие слез во время плача).
- Если он или она не может переносить пероральные антибиотики.
- Когда есть опасения, что инфекция распространилась в их кровоток.
Когда мне следует связаться с лечащим врачом моего ребенка?
Инфекции мочевыводящих путей требуют немедленного лечения. Позвоните поставщику медицинских услуг, если ваш ребенок:
- Показывает уменьшение количества пищи или воды.
- Не переносит домашние лекарства.
- Рвота.
- Повышается температура или боль.
- Становится более раздражительным или малоподвижным.
- Имеет какие-либо признаки или симптомы, которые вас беспокоят.
Быстрое лечение ИМП у вашего ребенка снижает риск проблем с почками и риск распространения инфекции.
Записка из клиники Кливленда
Хотя инфекция мочевыводящих путей не является опасным для жизни состоянием, она может привести к госпитализации или осложнениям, которые могут повлиять на качество жизни вашего ребенка.Обязательно покажите их врачу, как только у них появятся симптомы. Всегда следите за тем, чтобы ваш ребенок принимал все прописанные им лекарства. Даже если они кажутся лучше, вы все равно должны попросить их принять лекарство до завершения лечения.
Klebsiella — обзор | Темы ScienceDirect
Клинические проявления
Klebsiella spp . являются важными условно-патогенными микроорганизмами у детей, вызывающими широкий спектр инфекций, включая ИБС, связанные со здоровьем и общиной; инфекции центральной нервной системы (ЦНС), дыхательных путей, мочевыводящих путей, опорно-двигательного аппарата и брюшной полости; глубокие абсцессы и послеоперационные, травматические и ожоговые инфекции.Примерно 75% BSI связаны со здравоохранением. 16–24 Вспышки в неонатальных отделениях вызывают серьезную озабоченность. 25 Инфекции новорожденных включают BSI, менингит, абсцесс мозга, конъюнктивит, абсцесс печени, эндокардит, пневмонию, некротический фасциит, артрит, остеомиелит, инфекцию мочевыводящих путей (UTI) и некротический энтероколит (NEC). 26–32 Клинические проявления инфекции не отличаются от таковых у других грамотрицательных бацилл. Хотя Escherichia coli является наиболее частой причиной ИМП, Klebsiella и Proteus spp . также являются распространенными микроорганизмами Enterobacteriaceae, связанными с ИМП. 33
Грамотрицательные организмы составляют более 50% ИМТ у детей. Во время 6-летнего проспективного исследования грамотрицательных ИБС в педиатрическом медицинском центре третичного уровня в Израиле наиболее часто выявляемым патогеном было K. pneumoniae , составлявшее 26% (109 из 419) изолятов. 19 В обзоре 57 случаев ИМТ у детей, вызванного K. pneumoniae , 67% были моложе 12 месяцев, и у большинства было по крайней мере одно основное заболевание, включая аномалии желудочно-кишечного тракта у 56%, центральный венозный катетер. у 35%, нейтропения у 25% и патология мочевыводящих путей у 16%. 34
Проект по надзору и контролю за патогенами эпидемиологической важности, основанный в Университете Содружества Вирджинии в Ричмонде, предоставил важные данные для выявления преобладающих патогенов, ответственных за связанные со здравоохранением ИБТ у детей. 35 Хотя грамположительные организмы, особенно коагулазонегативные Staphylococcus spp., Составляли более 50% изолятов, Candida spp . приходилось 9.3% и Klebsiella spp . На , Enterobacter spp. И Escherichia coli приходилось 5,8%, 5% и 5% изолятов соответственно.
Другие условия, связанные с Klebsiella spp. BSI в детстве включает недоношенность, предшествующее воздействие антибиотиков, предшествующий ротавирусный гастроэнтерит, процедуру Касаи при атрезии желчных путей, злокачественные новообразования, послеоперационный статус, ожоги, множественные травмы, синдром приобретенного иммунодефицита, нарушения гранулоцитов, гомозиготную серповидно-клеточную анемию, трансплантацию твердых органов, послеоперационный период после спленэктомии, системной красной волчанки и дефицита β1 цепи рецептора интерлейкина-12. 19,35–41 Загрязненные растворы для внутривенного введения также были идентифицированы как источник Klebsiella spp. BSI. 42
Общий коэффициент смертности Klebsiella spp. BSI составляет примерно 11%, а уровень смертности от BSI, связанного со здравоохранением, составляет 14,5%. 19,35 Повышенный уровень смертности в значительной степени связан с острым лейкозом, нейтропенией, инфекциями, связанными со здоровьем (HAI), и предшествующей терапией кортикостероидами.
Цитотоксин-продуцирующие штаммы K.oxytoca были причастны к антибиотико-ассоциированному геморрагическому колиту. 14,43,44 Клиническим проявлениям боли в животе и кровавой диареи обычно предшествует лечение антибиотиками с β-лактамным агентом. Колит обычно сегментарный и локализуется преимущественно в правой толстой кишке. Прекращение применения противомикробного агента и поддерживающая терапия обычно приводят к клиническому разрешению. Энтеротоксигенные и энтероагрегантные штаммы K. pneumoniae также были вовлечены в качестве причин детского гастроэнтерита. 45
Raoultella spp. о них непостоянно сообщалось как о колонизирующих бактериях желудочно-кишечного тракта госпитализированных новорожденных и как возбудителях ИБС и пневмонии у взрослых. 46,47 R. planticola был выделен из мочи взрослых особей; раны, включая внутрибрюшной абсцесс, связанный с панкреатитом; и зараженные смеси для младенцев. 48–50 R. ornithinolytica был выделен из крови новорожденного с висцеральной гетеротаксией, функциональной аспленией и сложным врожденным пороком сердца с НЭК; от одного взрослого с гигантской кистой почек; а от другого — с синдромом, похожим на кишечную лихорадку. 51–53
R. ornithinolytica и R. planticola , по-видимому, вызывает отравление скомброидной (гистаминовой) рыбой. 8 Это состояние возникает после приема внутрь неправильно хранимой (> 20 ° C) скомброидной рыбы (например, тунца, махи-махи, скумбрии, скумбрии, сардины) и возникает в результате расщепления высоких концентраций гистидина на гистамин под действием бактериального гистидиндекарбоксилаза. 51,53 Инкубационный период может составлять от 1 минуты до 3 часов. Клинические проявления могут включать заметное покраснение кожи (особенно лица, верхней части туловища и рук), головную боль, головокружение, спазмы в животе, рвоту, диарею, жжение во рту, крапивницу, генерализованный зуд и (редко) гипотензию и бронхоспазм.
Клинико-патологические данные у детей, умерших в результате инфекции кровотока Klebsiella pneumoniae
Основные моменты
- •
Klebsiella pneumoniae Инфекции кровотока являются основной клинической проблемой у госпитализированных детей
- •
14 907 исследования в области результатов аутопсии
- •
Наша статья привносит другое измерение в понимание Enterobacteriaceae инфекций у детей
- •
Раннее обнаружение образования биопленок в образцах тканей может указывать на неоптимальные ответ на антибиотики
- •
Необходимы дополнительные исследования для понимания молекулярных механизмов образования биопленок, связанных с Klebsiella pneumoniae
Реферат
Предпосылки
Klebsiella pneumoniae 9 0006 инфекция кровотока (KPBSI) тесно связана с госпитализацией и может привести к значительной заболеваемости и смертности.Данных, описывающих результаты вскрытия KPBSI у детей, очень мало.
Методы
Мы провели ретроспективный обзор клинико-патологических данных у детей, умерших во время курса KPBSI в детской больнице в Кейптауне, Южная Африка.
Результаты
Пятнадцать госпитализированных детей, которые умерли и прошли вскрытие, были включены в этот анализ. Их средний возраст (межквартильный диапазон, IQR) составлял 4 (1-22) месяца, 2 (20%) были ВИЧ-инфицированными и 10 (67%) имели умеренно или сильно пониженный вес.Среднее время до смерти с момента получения положительного результата посева крови составляло 1 день (IQR 0–5). Заметными результатами аутопсии были полиорганная недостаточность, вызванная сепсисом, во многих случаях, включая инволюцию тимуса, эрозии пищевода, кровоизлияние в надпочечники, острый некроз канальцев и деструкцию паренхимы легких. Другие гистологические находки включали диссеминированную внутрисосудистую коагулопатию, некротизирующее воспаление во многих органах; и у четырех из пяти детей образование биопленок.
Заключение
KPBSI может вызывать обширную некротическую ткань.
Ключевые слова
Klebsiella pneumoniae Инфекция кровотока
Дети
Африка
Вскрытие / вскрытие
Рекомендуемые статьиЦитирующие статьи (0)
© 2019 Авторы. Опубликовано Elsevier Ltd от имени Британской ассоциации инфекций.
Рекомендуемые статьи
Ссылки на статьи
Инфекции мочевыводящих путей у детей: обзор диагностики и лечения
Предпосылки
Распространенность и эпидемиология
Инфекция мочевыводящих путей (ИМП) — одна из наиболее распространенных бактериальных инфекций у детей.Среди младенцев с лихорадкой, нездоровых детей общей практики и детей старшего возраста с симптомами мочеиспускания 6–8% будут иметь ИМП.1 2 Распространенность варьируется с возрастом, достигая пика у младенцев, детей ясельного возраста и подростков старшего возраста. ИМП чаще встречается у девочек и необрезанных младенцев мужского пола, 1 это понятно, учитывая концентрацию бактериальной флоры кожи под подгузником в младенчестве, более короткое женское уретральное расстояние и площадь поверхности крайней плоти у необрезанных мужчин. В первые годы жизни приучение к туалету может привести к удерживанию по воле и застою мочевого пузыря, что способствует развитию ИМП.3 Распространенность снова достигает пика у девочек-подростков, когда сексуальная активность разрушает бактерии около отверстия уретры.1
Состояния, нарушающие отток мочи, повышают восприимчивость к ИМП. При мочеиспускании бактерии выводятся из мочевыделительной системы.3 Нарушение оттока мочи приводит к застою мочи, что дает бактериям увеличенный резервуар и больше времени для развития инфекции. Причины нарушения мочеиспускания могут быть структурными (урогенитальные аномалии) или функциональными (нейрогенный мочевой пузырь, запор и сдерживание поведения).Измененная иммунная функция может увеличить риск необычных вирусных и грибковых причин ИМП.
Более 30% детей с ИМП будут иметь рецидивирующие ИМП. 4 Общие факторы риска рецидива включают пузырно-мочеточниковый рефлюкс (ПМР) и дисфункцию мочевого пузыря – кишечника. 4 Дети старшего возраста (например, с задержкой в развитии) также чаще рецидивируют ИМП.
Являясь такой распространенной инфекцией, ИМП вносит значительную экономическую нагрузку на систему здравоохранения. Использование основанного на фактических данных управления может привести к значительной экономии средств.5
Этиология
Большинство детских ИМП вызываются грамотрицательными колиформными бактериями, возникающими из фекальной флоры, колонизирующей промежность, которые проникают и поднимаются по мочевым путям. 3 Escherichia c oli ( E.coli ) наиболее распространенный уропатоген, вызывающий примерно 80% ИМП у детей.6 Уропатогенные штаммы E. coli обладают особыми свойствами, такими как фимбрии, прикрепляющиеся к поверхности уроэпителиальных клеток, что позволяет им преодолевать защитные силы хозяина (рис. .3 Другие распространенные уропатогены включают виды Klebsiella , Proteus , Enterobacter и Enterococcus . 6 7
Рисунок 1E scherichia coli с фимбриями. Изображение любезно предоставлено Dennis Kunkel Microscopy, Science Photo Library.
ИМП верхних и нижних трактов
ИМП можно анатомически разделить на инфекции верхних и нижних трактов.8 ИМП верхних трактов включает инфекцию и воспаление в почках (пиелонефрит) и мочеточниках (рис. 2).Обычно это приводит к боли в животе и болезненности поясницы с такими системными признаками, как лихорадка, анорексия, рвота, летаргия и недомогание. ИМП нижних трактов включает инфекцию мочевого пузыря (цистит) и уретры с локализованными симптомами, такими как боль внизу живота или надлобка, дизурия, учащенное мочеиспускание и позывы. У детей старшего возраста могут появиться признаки и симптомы, указывающие на место заражения. У более молодых пациентов эти классические признаки часто отсутствуют, и различие между верхними и нижними ИМП менее очевидно.
Рисунок 2Мочеполовая система: ИМП верхних и нижних трактов. Изображение любезно предоставлено доктором Джонатаном Кауфманом. ИМП, инфекция мочевыводящих путей.
Заболеваемость
Острые ИМП охватывают весь спектр тяжести от легкой дизурии у здорового ребенка до опасного для жизни уросепсиса. Хотя серьезные инфекции встречаются реже, они могут возникать и возникают, особенно у новорожденных.9 После плановой иммунизации против Haemophilus influenzae типа B и Streptococcus pneumoniae ИМП стали более частой причиной скрытых и серьезных бактериальных инфекций у младенцев.8
Кратковременное заболевание может быть вызвано инфекцией почечной системы. Сюда входят системные особенности, включая плохое пероральное потребление и обезвоживание, а также редкие местные осложнения, включая образование перинефрального абсцесса. Кратковременная заболеваемость также возникает в результате распространения гематогенных уропатогенов. Бактаремические ИМП лучше всего изучены у младенцев, так как в этой популяции, скорее всего, будут собирать посев крови во время лихорадочных заболеваний. Приблизительно у 5% детей младше 12 месяцев с ИМП выявляется бактериемия 10, в зависимости от условий исследования.Затем бактериемия может привести к уросепсису. Менингит также может возникать при гематогенном распространении в спинномозговую жидкость (CSF). Риск сосуществования менингита и ИМП составляет 1% в неонатальном периоде 11, что указывает на низкий порог для выполнения люмбальной пункции в этой возрастной группе. После 1 месяца риск меньше.11 Типичные эмпирические антибиотики ИМП имеют плохое проникновение в спинномозговую жидкость и недостаточную продолжительность лечения бактериального менингита.
Долгосрочная заболеваемость возникает после повреждения почек и рубцевания от ИМП верхних мочевых путей.Около 15% детей с первой инфекцией мочевыводящих путей, которым проведено последующее сканирование, будут иметь признаки рубцевания почек.12 Это рубцевание будет иметь клиническое значение, если оно приведет к почечной дисфункции, гипертонии и хронической болезни почек (ХБП). Историческое мышление предполагало, что эти последствия были обычным явлением, что привело к агрессивным рекомендациям по визуализации для выявления детей с риском ХБП. Последние данные показывают, что риски намного ниже. Систематический обзор 1576 случаев 2011 г. не выявил случаев, когда ИМП у детей были основной причиной последующей ХБП.13 Из следующих 366 пациентов с местной ХБП в том же исследовании 13 (3%) имели в анамнезе ИМП в детстве, но у всех были почечные аномалии, очевидные на УЗИ почек, и рецидив ИМП, возможно, был причиной ХБП только в одном случае (0,3%). %) .13 Таким образом, при отсутствии структурных аномалий почек или рецидива ИМП риск ХБП минимален. Споры о значении рубцевания почки после ИМП продолжаются.
Диагноз
Клинические признаки ИМП у детей в высшей степени неспецифичны, особенно у детей младшего возраста.Диагностика может быть сложной задачей, но ее важно учитывать, особенно для младенцев с лихорадкой без внимания.
История болезни
Довербальные дети младшего возраста не могут сообщать о таких симптомах, как дизурия или боль в животе. Родители часто замечают неспецифические признаки, такие как вялость, раздражительность, плохое питание и рвота. Они совпадают со многими распространенными и доброкачественными вирусными инфекциями, а также с серьезными бактериальными инфекциями. Часто присутствует лихорадка, может быть единственным присутствующим признаком, или у ребенка может быть лихорадка.У детей, носящих подгузники, моча с неприятным запахом или обесцвечиванием может скрываться. Дети старшего возраста могут сообщать о местных симптомах, таких как дизурия или боль в боку.
Осмотр
Дети с ИМП могут казаться очень здоровыми или очень нездоровыми. Можно определить лихорадку, болезненность живота и обезвоживание. Локализующие признаки чаще встречаются у детей старшего возраста. Поскольку клинический диагноз недостоверен, для дальнейшей оценки требуется образец мочи.
Сбор образцов мочи: дети с континента
Дети с континента могут отказаться от мочеиспускания по запросу, чтобы сдать образец мочи из среднего потока (MSU) в стерильную емкость для сбора.Первая моча вымывает кожную флору из устья уретры перед забором пробы из середины потока мочи. Очистка водой с мылом перед MSU еще больше снижает загрязнение14.
Сбор образцов мочи: дети в недоношенном возрасте
Дети младшего возраста в западном обществе, как правило, не достигают удержания мочи до 2–3 лет, поэтому для детей с недоношенным заболеванием необходимы другие методы сбора. Неинвазивные методы включают ожидание спонтанного мочеиспускания, затем условный сбор с помощью подгузника, мешка или «чистый улов» струи мочи.Эти методы кажутся удобными и практичными. Однако прокладки и пакеты имеют высокий уровень загрязнения до 50–60% 2 15, что можно понять, учитывая их тесный контакт с кожей под областью под подгузник. Образцы из подушечек и мешков могут быть полезны для скрининга с помощью щупов, но они ненадежны для посева. Сбор ватных шариков особо не рекомендуется.16 Чистый улов имеет самый низкий уровень загрязнения среди всех неинвазивных методов — около 25% 17, но попытки могут быть длительными или безуспешными. Простые методы стимуляции мочеиспускания, такие как техника Quick-Wee, могут повысить скорость и успех чистого улова.18 19
Инвазивные методы извлекают мочу непосредственно из мочевого пузыря с помощью уретральной катетеризации или надлобковой пункционной аспирации (SPA). Эти методы эффективны, но для их выполнения требуются опыт и оборудование, они болезненны и доставляют беспокойство ребенку. Загрязнение из катетера и СПА невелико, на уровне 10% и 1% соответственно 17, поэтому эти методы более надежны для посева и диагностики.
Оптимальный метод сбора остается спорным (таблица 1). У каждого метода есть свои преимущества и ограничения, а в руководствах есть свои рекомендации.20 В Великобритании, где врачи общей практики оказывают первичную помощь, руководящие принципы рекомендуют чистый улов или другие неинвазивные методы, если чистый улов невозможен, и катетер или SPA только в том случае, если неинвазивные методы невозможны или нецелесообразны. там, где педиатры часто оказывают первичную помощь, руководящие принципы рекомендуют обратное, что для подтверждения ИМП требуется катетер или СПА, хотя для скрининга можно использовать удобные методы, такие как мешки для мочи.21 Большинство международных руководств рекомендуют катетер или СПА в качестве золотого стандарта, включая чистый улов в качестве приемлемого метода сбора и, в частности, не рекомендуется использовать образцы из пакетов для посева.22–24 Двухэтапный процесс с использованием начального скрининга мешков и катетерного подтверждения положительных результатов скрининга может снизить частоту инвазивных процедур.25
Таблица 1Методы сбора мочи у недоношенных детей
Кто нуждается в обследовании на ИМП
Клинический диагноз ИМП является ненадежным, поэтому многим детям с лихорадкой или симптомами ИМП требуется анализ мочи для исключения или постановки диагноза. Перед началом приема антибиотиков следует собирать образцы мочи, но не следует откладывать терапию у ребенка с сепсисом.
Детям с локализованными признаками или подозрением на ИМП требуется анализ мочи для подтверждения диагноза. 16
Детям с лихорадкой без внимания, особенно новорожденным и младенцам, необходим образец мочи для оценки потенциальной ИМП. Вне младенческого возраста, и если ребенок не болен, может быть разумным подождать 24 часа для сбора, чтобы увидеть, появится ли альтернативный очаг заболевания.16
Детям с альтернативным очагом болезни обычно не требуется анализ мочи.16 Исключения составляют младенцы с сепсисом, дети с предрасполагающими состояниями (например, почечными аномалиями), дети с риском осложнений (например, единственная почка) и лихорадочное заболевание, не протекающее по ожидаемому клиническому течению.
Скрининг — индикаторная полоска и микроскопия
Индикаторные полоски мочи — это быстрый и недорогой прикроватный скрининг. Полоски с химическим реагентом меняют цвет в присутствии лейкоцитарной эстеразы (фермента, присутствующего в лейкоцитах) и нитритов, которые могут возникать при ИМП. 26 Лейкоциты обычно появляются в моче в ответ на ИМП. Однако стерильная пиурия может возникать и при других инфекциях. Виды Enterococcus , Klebsiella и Pseudomonas также реже вызывают пиурию, чем E.coli у детей с симптоматическими ИМП.27 Большинство уропатогенов превращают пищевые нитраты в нитриты мочи. Однако не все, в том числе Enterococcus и Klebsiella видов26. Мерные полоски также менее надежны для младенцев младшего возраста, у которых частое мочеиспускание вымывает субстраты из мочевого пузыря26.
Ни лейкоциты, ни нитриты не являются полностью чувствительными или специфичными для ИМП. , но они являются полезным скрининговым тестом, особенно когда используются в комбинации. Если ИМП считается маловероятным, индикаторные полоски имеют хорошую прогностическую ценность для отрицательного результата, чтобы исключить диагноз.28 При наличии подозрительных симптомов и наличия лейкоцитов или нитритов показаны эмпирические антибиотики в ожидании посева. 16
Микроскопия мочи также позволяет выявлять лейкоциты и бактерии, расширяя возможности скрининга тест-полосками.
Диагноз: посев
Лабораторный посев — золотой стандарт диагностики ИМП. Моча стерильна; следовательно, присутствие бактерий в достаточном количестве с одновременным доказательством активной инфекции указывает на ИМП. Моча добавляется в питательную среду, по которой определяется чувствительность к бактериям и антибиотикам.Посев занимает около 24 часов, после чего можно проверить предполагаемый диагноз. Все основные руководства по ИМП рекомендуют, чтобы для диагностики ИМП необходим посев. 16 21
Сколько бактерий необходимо для диагностики ИМП у детей? Пороговые значения различаются в зависимости от рекомендаций и методов сбора.24 29 Обычно цитируемый порог в 100 000 КОЕ / мл одного организма основан на основополагающем исследовании взрослых женщин, проведенном Kass30 в 1956 году. Применяется ли этот порог к детям? Американские руководящие принципы предлагают порог 50 000 КОЕ / мл с одновременной пиурией для образцов SPA и катетера.21 Более свежие данные свидетельствуют о том, что даже более низкий порог в 10 000 КОЕ / мл может немного повысить чувствительность без снижения диагностической специфичности.29 Многие руководства предполагают, что любой рост на SPA является ненормальным, 24 поскольку SPA имеет незначительное загрязнение.
Бессимптомная бактериурия (БАС) — это присутствие бактерий в моче без активной инфекции. Распространенность БАС в детстве оценивается в 1,4–1,9 %.31 32 Рост бактерий без признаков активной инфекции (например, пиурии) не указывает на ИМП.
В действительности эти диагностические пороги не являются бинарными.16 Низкое количество колоний в культуре может указывать на раннюю инфекцию, контаминацию или ASB. Пиурия может иногда отсутствовать на ранних стадиях инфицирования или иммунодефицита. Результаты скрининга и посева всегда следует рассматривать в клиническом контексте.
Загрязнение
Загрязнение делает воду мутной при оценке ИМП. Если предположить, что ИМП вызывает один уропатоген, то наличие нескольких организмов предполагает заражение образца. Случайная флора колонизирует перигенитальную кожу и может попасть в образец мочи при мочеиспускании.Пропущенный диагноз может произойти, если истинный уропатоген скрыт в смеси, или ошибочный диагноз, если в культуре доминирует один контаминант. Загрязнение можно свести к минимуму, очистив перигенитальную кожу перед взятием образца14 и избегая прикосновения к сосуду с образцом или поднося сосуд к коже ребенка.
Что на горизонте?
Текущие тесты на ИМП не обладают абсолютной чувствительностью или специфичностью. Биомаркеры в моче, такие как интерлейкин 6 и липокалин, связанный с желатиназой нейтрофилов, были предложены для дифференциации активной инфекции и ASB.ПЦР в реальном времени была предложена для идентификации распространенных уропатогенов, таких как E . coli .28 Необходимы дальнейшие исследования, чтобы понять клиническую полезность этих новых тестов.
Первичное ведение
Общее
Детям с ИМП требуются целевые антибиотики и поддерживающая терапия. Большинство детей с ИМП можно лечить дома с помощью пероральных жидкостей и антибиотиков. Небольшому проценту пациентов потребуется госпитализация для внутривенной терапии, в том числе очень маленьких и очень нездоровых детей, детей со значительными аномалиями почек и детей, не отвечающих на пероральную терапию.
Антибиотикотерапия
При выборе эмпирических антибиотиков необходимо руководствоваться местными правилами, поскольку местная чувствительность к противомикробным препаратам значительно различается (таблица 2). Пригодность исходного агента должна быть проверена после получения результатов посева.
Таблица 2Последние данные, противоречия и новые данные
Пероральные антибиотики эффективны при подавляющем большинстве детских ИМП. Предыдущие Кокрановские обзоры предполагают, что короткие 2–4-дневные курсы столь же эффективны, как и более длительные 7–14-дневные курсы при неосложненном цистите 33, в то время как терапия однократной дозой менее эффективна.34 Американские руководящие принципы рекомендуют продолжительность лечения 7–14 дней как для цистита, так и для пиелонефрита, 21 канадские рекомендации рекомендуют 7–10 дней, 35 в то время как в рекомендациях Национального института здоровья и клинического совершенства (NICE) рекомендуется 7–10 дней для пиелонефрита и менее 3 Дневной курс для детей старше 3 месяцев с циститом.16 Испанские руководящие принципы отражают рекомендации NICE, хотя для детей в возрасте старше 6 лет с неосложненным циститом рекомендуется однократная терапия.36
Детям младшего и более старшего возраста может потребоваться начальная внутривенная терапия.Многие руководящие принципы и центры рекомендуют госпитализацию, внутривенное введение антибиотиков и рассмотрение септического исследования для младенцев <3 месяцев16. Стремитесь перейти на пероральную терапию через 48 часов, если есть клиническое улучшение.
Устойчивость к антибиотикам
Устойчивые к антибиотикам ИМП становятся все более распространенными во всем мире, 6 37 увеличивают заболеваемость и удваивают расходы на здравоохранение.38 Обычный механизм заключается в приобретении улучшенных свойств фермента бета-лактамазы. Некоторые грамотрицательные уропатогены могут инактивировать антибиотики бета-лактамного кольца, такие как пенициллин и цефалоспорины раннего поколения с присущими им ферментами бета-лактамаз.Однако некоторые из них приобрели дополнительную способность к множественной лекарственной устойчивости в результате эволюции этих ферментов, включая способность гидролизовать и инактивировать цефалоспорины расширенного спектра и карбапенемные антибиотики.39 Такие организмы известны как организмы бета-лактамаз расширенного спектра (БЛРС). Предшествующая антибактериальная терапия и госпитализация являются факторами риска носительства БЛРС, что затем способствует носительству в обществе и передаче резистентности. Частота резистентных ИМП особенно высока в странах с ограниченными ресурсами 37, где устойчивость к обычным пероральным антибиотикам, таким как ампициллин и котримоксазол, может достигать 97–100%.40
Визуализация
Исторически в руководствах рекомендовалось агрессивное последующее наблюдение с помощью визуализации для выявления почечных рубцов и осложнений ИМП. В настоящее время известно, что у большинства детей с риском осложнений есть структурные аномалии, идентифицируемые на УЗИ, или рецидивирующие ИМП. Поэтому во многих недавних рекомендациях предлагается меньше или вовсе не визуализация после первой неосложненной ИМП у детей старшего возраста и менее агрессивная визуализация после рецидива ИМП (таблица 3) .24
Таблица 3Сводка рекомендаций по визуализации из избранных международных руководств для маленьких детей с ИМП
УЗИ
Ультразвук неинвазивен, относительно недорого и подходит для исследования первой линии, когда показано изображение.Ультразвук может выявить анатомические аномалии и гидронефроз или гидроуретер, предполагающие обструкцию или ПМР. Американские и канадские руководящие принципы рекомендуют УЗИ для всех детей в возрасте до 2 лет с первой ИМП, 21 35 Руководства Европейской ассоциации урологов рекомендуют УЗИ для всех детей с первой лихорадкой ИМП 23, в то время как NICE рекомендует УЗИ только для младенцев <6 месяцев с первой ИМП, если только не инфекция. нетипична или не поддается лечению.16 Подход NICE отражает точку зрения, что рутинная визуализация после всех первых ИМП не рентабельна; однако визуализация у детей младшего возраста и в других отобранных случаях с большей вероятностью обнаружит клинически значимые результаты.41 Ультразвук не может исключить все случаи ПМР, но должен выявить наиболее тяжелые и клинически значимые случаи.
Сканирование димеркаптоянтарной кислоты (DMSA)
Сканирование DMSA представляет собой сканирование поглощения ядерных изотопов. Снижение захвата почками может отражать либо острую дисфункцию (пиелонефрит), либо долгосрочное повреждение (рубцевание), в зависимости от времени проведения теста.9 Это редко требуется остро, но может помочь в долгосрочном лечении. DMSA может быть показан, если ИМП нетипична, рецидивирует или если первоначальное ультразвуковое исследование значительно отклоняется от нормы.
Цистоуретрограмма мочеиспускания (VCUG)
VCUG использует рентгеноскопию (рентген в реальном времени) для определения курса контраста, вводимого при катетеризации мочевого пузыря. Можно определить наполнение мочевого пузыря, опорожнение и рефлюкс мочеточника. Хотя VCUG является золотым стандартом для выявления и количественной оценки VUR, процедура сопряжена с радиационной нагрузкой и является инвазивной.
Отсутствует консенсус относительно того, кого именно и как изображать. Стоимость, инвазивность и радиационная нагрузка должны быть сбалансированы с вероятностью выявления аномалии, которая может изменить лечение ребенка.Хотя большинству детей с неосложненной ИМП вне младенческого возраста не требуется визуализация, некоторые дети подвержены риску долгосрочных осложнений после ИМП. Таким образом, целевые стратегии визуализации и наблюдения за детьми с выбранными показаниями остаются актуальными.
Архивы медицины | инсайт медицинское издательство
Импакт-фактор журнала: 1,0 *; ICV: 84,60
Архив медицины (ISSN: 1989-5216) предназначен для публикации научных статей, обзоров и кратких сообщений в области медицинских исследований.Это международный журнал открытого доступа с контролируемым качеством, рецензируемый и рецензируемый. Архивы медицины публикуют отчеты об исследованиях и статьи о различных исследовательских процессах, таких как протоколы исследований, пилотные исследования и предварительные протоколы.
Журнал является новым, привлекательным, открытым и рецензируемым медицинским периодическим изданием, призванным служить платформой как для ветеранов, так и для исследователей амперметров с их новаторскими работами, если они технически правильны и научно мотивированы. Тематические области включают исследования в области иммунологии, анестезии, сердечно-сосудистой медицины, комплементарной медицины, стоматологии и оральной медицины, патологии, фармакологии и терапии, дерматологии, респираторной медицины, ревматологии, лекарств и лекарств, уха, носа и горла / отоларингологии, неотложной медицины, инфекционные болезни, неврология, питание и обмен веществ, акушерство и гинекология, эндокринология, гастроэнтерология, генетика, гериатрическая медицина, гематология, онкология, офтальмология, педиатрия, психиатрия, радиология, почечная медицина, фармакогнозия, сексуальное здоровье, урология, эпидемиология, этнические исследования, здоровье политика, гигиена труда, медицинское образование, юридическая и судебная медицина, экологическая медицина и общественное здравоохранение, разработка и тестирование лекарств на безопасность, законодательство о лекарственных средствах и безопасность.
Отправьте рукопись в виде приложения к электронному письму в редакцию по адресу [электронная почта защищена] (или) через Интернет https://www.imedpub.com/submissions/archives-medicine.html
Медицинская визуализация
Медицинская визуализация — это метод и процесс создания визуальных представлений частей тела, тканей или органов для использования в клинической диагностике; включает рентгеновские методы, магнитно-резонансную томографию, однофотонную и позитронно-эмиссионную томографию и ультразвук.Медицинская визуализация, особенно рентгеновское обследование и ультразвуковое исследование, имеет решающее значение в любом медицинском учреждении и на всех уровнях здравоохранения.
Связанные журналы медицинской визуализации
Международный журнал клинической и медицинской визуализации, Клиническая и медицинская биохимия: открытый доступ, визуализация и интервенционная радиология, методы медицинской диагностики, BMC Medical Imaging, журнал медицинской визуализации, Открытый журнал медицинской визуализации, Международный журнал медицинских изображений, медицинской визуализации и радиологии , Journal of Medical Imaging and Radiation Sciences
Emergency Medicine
Экстренная медицина — это медицинская специальность и медицинская практика, занимающаяся диагностикой и лечением непредвиденных заболеваний или травм, требующих немедленной медицинской помощи.Роль врача неотложной помощи заключается в оценке; лечить, принимать или выписывать любого пациента, который обращается за медицинской помощью, в любое время дня и ночи.
Родственные журналы по неотложной медицинской помощи
Доказательная медицина и практика, Журнал неотложной медицины, Журнал неотложной медицины, Американский журнал неотложной медицины, Европейский журнал неотложной медицины, Американский журнал неотложной медицины, Академическая неотложная медицина и Международный журнал неотложной медицины.
Лаборатория медицины
Лабораторная медицина также называется клинической патологией. В лабораторной медицине патологоанатомы проводят анализы образцов пациентов (обычно крови или мочи) в нескольких различных областях.
Родственные журналы лабораторной медицины
Анналы клинических и лабораторных исследований, La Prensa Medica, метаболизм лекарств и токсикология, фармацевтика и исследования доставки лекарств, лекарственная интоксикация и детоксикация: новые подходы, журнал лабораторной и клинической медицины, африканский журнал лабораторной медицины, журналы патологии и лабораторной медицины, Международный журнал патологии и лабораторной медицины, Архив патологии и лабораторной медицины, Архив «Корейского журнала лабораторной медицины», Журнал медицинской лаборатории и диагностики, клинической химии и лабораторной медицины
Внутренняя медицина
Медицинская специальность, занимающаяся диагностикой и лечением взрослых.Внутренняя медицина охватывает широкий спектр состояний, влияющих на внутренние органы тела — сердце, легкие, печень и желудочно-кишечный тракт, почки и мочевыводящие пути, головной мозг, позвоночник, нервы, мышцы и суставы.
Родственные журналы по внутренним болезням
Внутренняя медицина: открытый доступ, Международный журнал совместных исследований в области внутренней медицины и общественного здравоохранения, Общая медицина: открытый доступ, Медицинская и хирургическая патология, Журнал внутренней медицины, Журнал внутренней медицины, Европейский журнал внутренней медицины, Журнал общей внутренней медицины, Открытый журнал внутренней медицины, Каспийский журнал внутренней медицины, Египетский журнал внутренней медицины, Корейский журнал внутренней медицины, Американский журнал внутренней медицины, Европейский журнал отчетов о случаях внутренней медицины
Психосоматическая медицина
Психосоматическая медицина — это междисциплинарная область медицины, изучающая взаимосвязь социальных, психологических и поведенческих факторов с телесными процессами и качеством жизни людей и животных.Психосоматическая медицина дает возможность «удержать» большую часть вашей медицинской и хирургической подготовки и эффективно использовать ее.
Родственные журналы по психосоматической медицине
Судебная психология, Психотерапия и психологические расстройства, Аномальная и поведенческая психология, Прикладная и реабилитационная психология: открытый доступ, Психосоматическая медицина, Журнал психосоматических исследований, Журнал психосоматической медицины, Международный колледж психосоматической медицины, Академия психосоматической медицины, Корейский журнал психосоматической медицины, Журнал психологии и исследований мозга и Acta Psychopathologica.
Кардиология
Кардиология — это отрасль медицины, изучающая сердце и его болезни. Сфера деятельности включает медицинскую диагностику и лечение врожденных пороков сердца, ишемической болезни сердца, сердечной недостаточности.
Родственные журналы по кардиологии
Клиническая и экспериментальная кардиология, сердечно-сосудистая патология: открытый доступ, идеи детской кардиологии, Международный журнал сердечно-сосудистых исследований, Американский журнал кардиологии, журнал интервенционной кардиологии, Международный журнал кардиологии, кардиологии и сердечно-сосудистой медицины, журнал кардиологии, Британский журнал кардиологии , Европейский журнал профилактической кардиологии, Греческий журнал кардиологии, клинической кардиологии, Кардиологический журнал
Неврология
Неврология — это медицинская специальность, занимающаяся диагностикой и лечением заболеваний нервной системы, в том числе головного и спинного мозга и нервов.Научное изучение нервной системы, особенно в отношении ее структуры, функций и аномалий.
Связанные журналы неврологии
Понимание нейрохирургии, неврологии и нейрофизиологии, нейропсихиатрии, детской неврологии и медицины, журнала неврологии, нейрохирургии и психиатрии, журнала когнитивной нейропсихологии, журнала неврологических наук и журнала неврологии Неврологические науки, Европейский журнал неврологии, Анналы Индийской академии неврологии, Журнал сравнительной неврологии, Журнал детской неврологии, Канадский журнал неврологических наук, Открытый журнал неврологии
Общая медицина
Медицинская специальность, занимающаяся диагностикой и лечением взрослых.Общая медицина охватывает широкий спектр состояний, поражающих внутренние органы тела — сердце, легкие, печень и желудочно-кишечный тракт, почки и мочевыводящие пути, головной мозг, позвоночник, нервы, мышцы и суставы.
Родственные журналы по общей медицине
Общая медицина: открытый доступ, Внутренняя медицина: открытый доступ, Международный журнал совместных исследований в области внутренней медицины и общественного здравоохранения, Медицинская и хирургическая патология, Отчеты по общей хирургии, Международный журнал общей медицины, Журнал общей внутренней медицины, Европейский журнал общей медицины , Открытый журнал общей и внутренней медицины, Открытая медицина.
Медицина легких и реанимации
Pulmonary and Critical Care Medicine (PCCM) стремится оказывать помощь тяжелобольным пациентам и пациентам с заболеваниями легких. Pulmonary and Critical Care Medicine обладает клиническими и исследовательскими знаниями по широкому кругу заболеваний, включая астму, ХОБЛ, интенсивную терапию, муковисцидоз, интерстициальную болезнь легких, рак легких.
Связанные журналы по легочной и реанимации
Легочная и респираторная медицина, Хроническая обструктивная болезнь легких: открытый доступ, Качество первичной медико-санитарной помощи, Первичная медико-санитарная помощь: открытый доступ, Американский журнал респираторной и интенсивной терапии, Европейский респираторный журнал, The Lancet Respiratory Medicine, European Respiratory Review, Респираторные исследования, респирология , BMC Pulmonary Medicine, Current Opinion in Pulmonary Medicine, Current Opinion in Pulmonary Medicine, Детская пульмонология, Легочная фармакология и терапия
Токсикология и терапия
Токсикология — это научное исследование побочных эффектов, которые возникают у живых организмов из-за химических веществ, а терапия — это отрасль, которая занимается конкретно лечением болезней, а также искусством и наукой исцеления.
Связанные журналы токсикологии и терапии
Медицинская токсикология и клиническая судебная медицина, метаболизм лекарств и токсикология, судебная токсикология и фармакология, экологическая и аналитическая токсикология, Азиатский журнал фармакологии и токсикологии, легочная фармакология и терапия, BMC Pharmacology and Toxicology кафедры фармакологии и клинической токсикологии, Международный журнал фармакологии и токсикологии, Farmacologia Y Toxicologia, Therapeutics, Pharmacology and Clinical Toxicology
Педиатрия
Педиатрия — это отрасль медицины, которая занимается здоровьем младенцев, детей и подростков и их возможностью полностью раскрыть свой потенциал во взрослом возрасте.Он касается развития, ухода и болезней детей.
Родственные журналы по педиатрии
Интервенционная педиатрия, педиатрия и терапия, неотложная педиатрическая помощь и медицина: открытый доступ, клиническая педиатрическая дерматология, журнал педиатрии, журнал педиатрии, итальянский журнал педиатрии, индийский журнал педиатрии, индийская педиатрия, педиатрическая помощь, международная педиатрия, журнал Journal of Педиатрическое здравоохранение, Журнал педиатрического ухода, Журнал педиатрических инфекционных заболеваний, Клиническая педиатрия, Журнал тропической педиатрии
Аллергические заболевания
Аллергия возникает, когда иммунная система реагирует на безвредные вещества в окружающей среде.
